Organická chemie pro biochemiky I část 11
Organická chemie pro biochemiky I část 11 Organická chemie pro biochemiky I část 11
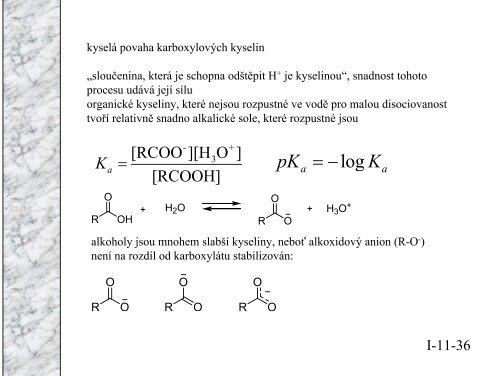
kyselá povaha karboxylových kyselin„sloučenina, která je schopna odštěpit H + je kyselinou“, snadnost tohotoprocesu udává její síluorganické kyseliny, které nejsou rozpustné ve vodě pro malou disociovanosttvoří relativně snadno alkalické sole, které rozpustné jsouKa=ROOH- +[RCOO ][H3O ][RCOOH]H 2 OROpKOa= −logKH 3 O +alkoholy jsou mnohem slabší kyseliny, neboť alkoxidový anion (R-O - )není na rozdíl od karboxylátu stabilizován:aOOOROROROI-11-36
srovnání síly kyselintrifluoroctováfluoroctováchloroctovábromoctovájodoctovámravenčíhydroxyoctováakrylováoctovápropionováF 3 CCOOHFCH 2 COOHClCH 2 COOHBrCH 2 COOHICH 2 COOHHCOOHHOCH 2 COOHPhCOOHCH 2 =CHCOOHCH 3 COOHCH 3 CH 2 COOH0,232,592,582,683,123,753,834,194,254,754,87silnější kyselinaethanolCH 3 CH 2 OH(16)slabá kyselinake zvýšení síly karboxylových kyselin přispívá odtažení elektronů zrezonujícícho karboxylátu jak na alifatickém tak aromatickém zbytkuOOOROROROI-11-37
- Page 1 and 2: Organická chemie pro biochemiky I
- Page 3 and 4: Druhy karbonylových sloučenin (dv
- Page 5 and 6: Polarizovanostδ-Oδ+můžeme vyjá
- Page 7 and 8: formaldehyd, methanal, HCHOštiplav
- Page 9 and 10: Obenzalhehydkapalina s vůní hořk
- Page 11 and 12: příprava aldehydůprimární alko
- Page 13 and 14: karbonylsrovnání s jinými uskupe
- Page 15 and 16: δ-Oδ+ONupříkladem nukleofilní
- Page 17 and 18: významnou nukleofilní reakcí kar
- Page 19 and 20: významnou nukleofilní reakcí kar
- Page 21 and 22: eakce aminů s karbonylovými slou
- Page 23 and 24: δ-Oδ+YYONureakce karbonylu s nukl
- Page 25 and 26: další veledůležitou reakcí kar
- Page 27 and 28: příkladem vstupu nukleofilního
- Page 29 and 30: příklady nukleofilní adice na ko
- Page 31 and 32: karboxylové kyselinyI-11-31
- Page 33 and 34: poznámka na okraj, často se pleto
- Page 35: kyselina mravenčí H-COOHpáchnouc
- Page 39 and 40: příprava karboxylových kyselinhy
- Page 41 and 42: Druhy derivátů karboxylových kys
- Page 43 and 44: eaktivita derivátů karboxylových
- Page 45 and 46: OH 2 OOhydrolýza acyl halogenidů
- Page 47 and 48: esteryshrnutí metod na přípravur
- Page 49 and 50: ROOR'OHRR'OOOHROOH 3 O +ROOHrozdíl
- Page 51 and 52: R BrNaCNR C Npříprava a reakce ni
- Page 53 and 54: polyamidy a polyesteryH 2 NNH 2nClO
- Page 55 and 56: hydroxykyselinyani hydroxyskupina n
- Page 57 and 58: deriváty anorganických kyselin v
- Page 59 and 60: syntheticky jsou zřejmě nejdůle
kyselá povaha karboxylových kyselin„sloučenina, která je schopna odštěpit H + je kyselinou“, snadnost tohoto<strong>pro</strong>cesu udává její síluorganické kyseliny, které nejsou rozpustné ve vodě <strong>pro</strong> malou disociovanosttvoří relativně snadno alkalické sole, které rozpustné jsouKa=ROOH- +[RCOO ][H3O ][RCOOH]H 2 OROpKOa= −logKH 3 O +alkoholy jsou mnohem slabší kyseliny, neboť alkoxidový anion (R-O - )není na rozdíl od karboxylátu stabilizován:aOOOROROROI-<strong>11</strong>-36