VOX PEDIATRIAERh inkompatibilita - stále aktuální problémMUDr. Alice MockováNeonatologické oddělení FN PlzeňSouhrnRh inkompatibilita je imunologický konflikt, vznikající na základě tvorby mateřských protilátek u Rh negativníchžen proti erytrocytárnímu antigenu Rh pozitivních plodů.V současné době je pro klinické projevy tohoto onemocnění upřednostňován název hemolytická nemocplodu a novorozence (HON), protože moderní prenatální diagnostika umožňuje odhalit příznaky nemocimnohem dříve. V posledních desetiletích se podařilo vypracovat a zdokonalit nejen prenatální diagnostiku,ale i systém prevence a léčby onemocnění. Důsledkem těchto opatření bylo snížení závažných foremtéto choroby a omezení počtu perinatálních úmrtí.■ PatofyziologieRh pozitivní jedinec má v membráně erytrocytůRh antigenní komplex, který je tvořen molekuloulipoproteinu o molekulové hmotnosti 30 000 Daltonů.Rh komplex tvoří antigeny C, Cw,c, D, d, E, ea nedědičná poziční varianta Du. Rh komplex mázáklad na třech velmi blízko sebe ležících lokusechgenů na krátkém raménku chromozomu 1,přičemž na lokusu 1 je alela C a c, na lokusu 2 jealela D a d a na lokusu 3 je alela E a e. Tato existujícíkombinace alel je od sebe neoddělitelně děděnaa je také důvodem, proč hovoříme o Rh komplexu.V současné době je upřednostňována CDEnomenklatura zavedená Fisherem, která popisuje8 různých genových kombinací : cde, Cde, cDe,cdE, CDe, cDE, Cde, CDE. Nomenklatura, kterouprosazoval Wiener (který v roce 1940 spolus Landsteinerem Rh systém objevil), se dnes používáméně.Přítomnost D antigenu podmiňuje Rh pozitivitukrve a výskyt D antigenu závisí na etnické příslušnosti.V Evropě se udává až 85% pozitivních jedinců.Výskyt D antigenu bývá ve velké části provázenpřítomností e antigenu a C antigenu. U D - pozitivníhojedince není na základě fenotypu jasné, zdaje jedná o homozygota (DD) nebo heterozygota.I když není zcela jasná funkce povrchovýchproteinů v membráně erytrocytu, je známo, že přiabsenci všech Rh antigenů vzniká více či méně vyvinutáhemolytická anemie.Nejsilnějším antigenem z hlediska imunizace jeantigen D. Po proniknutí tohoto antigenu do organismumatky dochází k jeho destrukci prostřednictvímmakrofágů. Současně se rozbíhá tzv. primárníimunitní odpověď, při které jsou zpočátkuprodukovány protilátky IgM a později IgG. PouzeIgG jsou schopny přejít placentární bariéru a dostatse tak do organismu plodu. Poněvadž je jejichhladina v tomto případě velmi nízká, nezpůsobízávažnější hemolytickou reakci u plodu.Udává se, že intenzita primární imunitní odpovědije závislá na množství Rh pozitivních buněk,které přestoupily placentární bariéru (např. 1 mlRh pozitivní krve způsobí imunizaci v 15% těhotenství,250 ml Rh pozitivní krve imunizuje jižv 70% těhotenství).Jestliže se mateřský organismus setká opětse stejným antigenem, je sekundární imunitníodpověď velmi rychlá a dochází k prudkému navýšeníprotilátek IgG, které se vyznačují ještě zvýšenouafinitou k antigenu. Agresivní IgG protilátkypřestupují placentární bariéru, pokrývají fetálníerytrocyty a tyto jsou poté destruovány lysozomálnímienzymy makrofágů a natural killer lymfocytů,při této reakci není potřeba aktivace komplementu.Důležitý je fakt, že výše titru protilátky neodpovídástupni hemolýzy, takže i při nízkých titrechprotilátek 1:16 může být plod významně ohrožen.Na základě hemolytické reakce dochází u ploduk rozvoji anemie, která stimuluje fetální erytropoézuv játrech, slezině a kostní dřeni a vzácněi v kůži. Extramedulární erytropoéza v játrech můžemít za následek destrukci jaterního parenchymus následně vzniklou dysfunkcí, portální hypertenzía hypoproteinemií, která je spojenas rozvojem ascitu a hydropsu. Při závažném průběhumůže dojít na základě těžké anémie provázenouhypoxií a acidozou k úmrtí plodu.Mateřský organismus může být imunizován několikazpůsoby. Nejčastější možností je fetomaternálnítransport antigenu. Až u 75% graviditdochází ke spontánnímu fetomaternálnímu krvácení,většinou se jedná o velmi malé objemy krve(0,1ml), které však mohou být dostatečné proimunizaci. Pokud je fetomaternální transfuze spojenas traumatem placenty (spontánní nebo arteficiálnípotrat, tupé úrazy břicha, abrupce placenty,mimoděložní gravidita, porod, císařský řez,zevní obraty plodu aj.), riziko imunizace se zvyšuje.Totéž platí i pro všechny diagnostické či terapeuticképrenatální výkony (př. amniocentéza,kordocentéza), při kterých může být integrita placentynarušena.Méně častou příčinou imunizace je podáníinkompatibilní transfuze krve matce nebo přenoskrve injekčními stříkačkami u narkomanek.Pokud nacházíme zvýšené titry protilátek u primigravid,je nutné pátrat i po méně obvyklých důvodechimunizace. Mezi ně patří maternofetálnítransport antigenu, známý také pod názvemgrandmother syndrom (syndrom babičky).Těhotná Rh- negativní primigravida mohla býtimunizována peripartálně svojí Rh - pozitivní matkou,došlo k vytvoření paměťové reakce a k tvorběprotilátek při těhotenství s Rh - pozitivním plodem.I když je Rh faktor přítomen pouze v membráněerytrocytů a trofoblastu, imunizace Rh - negativníženy může nastat i při podání Rh - pozitivního allogenníhokostního štěpu a při opakovaném podáníRh - pozitivních trombocytů. Příčinou zde bývánedostatečná purifikace zmíněných preparátů.■ Prenatální managementu Rh - negativní těhotnéDle doporučení České gynekologicko-porodnickéspolečnosti má být první screening přítomnostiprotilátek proveden u všech těhotných mezi10. -12. týdnem. I ženy laboratorně označené zaRh-pozitivní mohou díky některým atypiím tvořitanti - D protilátky. U Rh- negativních žen jsou přinegativitě prvního odběru indikována ještě 2 dalšívyšetření: ve 20.-24. týdnu ave 32. týdnu těhotenství.Při zjištěné pozitivitě titru protilátek jsou vyšetřeníopakovaná ve 2-3 týdenních intervalech, zahraniční jsou považovány titry 1:16.U rodičů s anamnézou těžké formy Rh-imunizaceplodu v předchozí graviditě a současným vysokýmtitrem protilátek je indikováno vyšetření ge-20VOX PEDIATRIAE - květen/2006 - č.5 - ročník 6
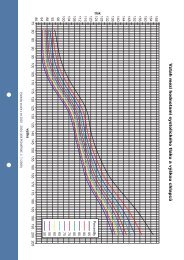
VOX PEDIATRIAEnotypu obou rodičů. Pokud je otec heterozygot Rh- pozitivní, lze stanovit Rh status plodu již na konciI. trimestru odebráním vzorku choriové tkáně(časná biopsie choria) nebo vyšetřením amniocytůz plodové vody, získané amniocentézou. Vzorekfetální krve k vyšetření Rh a event. krevníhoobrazu lze odebrat při přímé punkcí pupečníku(kordocentézou) od 18. týdne gravidity. Dřívehojně používaná metoda měření koncentrace bilirubinoidův plodové vodě, která byla získanáamniocentézou, je dnes považována za doplňkovou.Nejnovější postupy v typizaci fetálního Rhumožňují izolaci samotné fetální DNA z mateřskéhoséra.V současné době je kladen důraz na neinvazivnísledování stupně ohrožení plodu pomocí ultrazvukovédiagnostiky. Pátrá se po hepatosplenomegaliia ascitu v dutině břišní, po výpotkuv dutině pleurální či perikardiální, po edému podkožíplodu a placenty. Dopplerometrické měřeníprůtoků v ACA (a. cerebri media) na vrcholu systolybylo uznáno jako vhodná screeningová metodapro detekci anémie plodu. Zvýšený srdečnívýdej plodu a snižující se viskozita krve přispívajíke zvýšení průtokové rychlosti u plodu s anémii,toto měření je možno provádět od 18. týdne gravidity.V případě zvyšujícího se titru mateřských protilátek,hladině bilirubinoidů ve III. etáži (event. na80 % II. etáže) či přítomnosti USG známek fetálníanémie, je indikována kordocentéza. Z odebranéhokrevního vzorku plodu je stanoven krevní obraz,přímý Coombsův test, ineralogram a ABRHladina HCT pod 0,30 nebo progresivně klesajícíje indikací pro podání intrauterinní transfuze(IUT). Při IUT se používá ozářená a leukocytárnímfiltrem filtrovaná O rh negativní erymasa s hematokritem0,75-0,85, nejvhodnějším místem proaplikaci je oblast úpon pupečníku na placentu.Počet IUT u plodu během těhotenství závisí narychlosti hemolýzy a stupni hydropsu (je známo,že hydropické plody hůře tolerují i adekvátnímnožství transfundované krve, proto je u nichvhodnější IUT opakovat v kratším časovém intervaluse sníženým objemem krve). Cílem IUT jeprodloužení gravidity do doby, kdy není plodohrožen prematuritou, většinou IUT není prováděnapo 35. týdnu gestace. Jako každý invazivníprenatální výkon může být podání IUT provázenokomplikacemi, ke kterým řadíme trombózu umbilikálníchcév s následnou embolizací do oběhuplodu či akutní tamponádu pupečníku při paravazálníaplikaci. Průměr perinatálního přežití novorozencůpo IUT je v literatuře udáván mezi 85-90%, u hydropických plodů je tato hodnotao 15% nižší.Mezi méně časté používané terapeutické metodypatří plazmaferéza, která eliminuje cirkulujícíprotilátky z oběhu matky a podání vysoce dávkovanéhoimunoglobulinu intravenózně matce(dávky až 2g/kg), kterým lze zablokovat Fc receptorna fetálních erytrocytech.■ Prevence imunizace- aplikace anti D globulinuPodáním specifického IgG matce můžemeovlivnit imunitní odpověď Rh negativní ženy na Rhpozitivní antigen. Před aplikací musí být splněnyzákladní podmínky - hladina anti D protilátek nenídetekovatelná, žena je buď těhotná (aplikaceje indikována po amniocentéze v II. a III. trimestru)nebo je optimálně do 72 hodin po předpokládanémprůniku antigenu (způsobeném např.porodem, potratem, intrauterinním úmrtím plodu,operací mimoděložního těhotenství).Poněkud opomíjenou indikací k podání profylaxejsou tupé úrazy břicha u těhotné, zejménapři dopravních nehodách. V indikovaných případechlze aplikaci anti D provést až do 14 dnů poexpozici antigenu.Po porodu se podává obvykle dávka 250 mganti D globulinu intramuskulárně, po císařskýchřezech je indikována dávka dvojnásobná.■ Postnatální managementimunizovaného novorozence s HONProjevy hemolytické nemoci u novorozencejsou závislé na rozsahu proběhlé hemolýzy, jejížstupeň koreluje s účinností a množstvím přestoupenýchanti D protilátek. Hemolytický proces dosáhnevrcholu při porodu, protože poté už do novorozencežádné mateřské protilátky nepronikajíaty, které byly přítomny, se v průběhu následujícíchměsíců odbourávají.Mezi klinické projevy nemoci u novorozencepatří žloutenka (ikterus), bledost, hepatosplenomegaliea v těžších případech hydrops.Ikterus bývá přítomen již v době porodu nebose rozvíjí v průběhu prvních 24 hodin po něm,rychle narůstá především nekonjugovaný bilirubin.Tento bilirubin byl až do porodu byl odstraňovánmatčiným organismem, eliminační funkci plnínezralý jaterní parenchym novorozence jen částečně.Elevaci konjugovaného bilirubinu můžemevysvětlit současně přítomnou poruchou hepatocytů.Bledost je vyvolána anémií, většinou vzniklouna základě hemolýzy, avšak i opakované podáníadultního Hb ve formě intrauterinních transfúzízpůsobí supresi erytropoézy.Hepatosplenomegalie je projevem extramedulárníhematopoézy a bývá spojena s portálníhypertenzí.Zvýšení tlaku v portálním řečišti je jednímz faktorů, přispívajících ke vzniku hydropsu, kterýse projevuje přítomností tekutiny v dutině břišnínovorozence (ascites), pleurálními či perikardiálnímiefuzemi a povšechným prosáknutím podkoží.Po zhodnocení klinického stavu musí být provedenalaboratorní vyšetření. Z pupečníkové krvese stanovuje krevní skupina dítěte, přímý Coombsůvtest a hodnota bilirubinu.Pozitivita přímého Coombsova testu svědčío již vzniklé vazbě IgG protilátek na erytrocyty(matka má pozitivní nepřímý Coombsův test,který slouží k průkazu volně cirkulujících protilátekv séru). Hladina bilirubinu v pupečníkové krvinad 80 umol/l je indikací k provedení výměnnétransfúze.Z krevního vzorku novorozence se dále vyšetřujekrevní obraz, glykemie, celková bílkovina, kalciuma mineralogram. V krevním obrazu bývá nalézánrůzný stupeň anemie, při lehké až středníanémii je stimulována intramedulární erytropoéza,která se projeví zvýšením počtu retikulocytů v periferníkrvi. Přítomnost erytroblastů je důsledkemstimulace extramedulární erytropoézy při těžkéanémii. V bílé krevní řadě je přítomna leukopenie(po intrauterinních transfuzích je však typický nálezneutrofilie na základě zvýšení GM-CS faktoru),nalézáme současně trombopenii.Terapeutický postup u senzibilizovaného novorozencese určen klinickým stavem, hodnotamikrevního obrazu a bilirubinu.Zhruba v 50% případech se jedná o mírnouformu hemolytické nemoci. Novorozenci nejsouanemičtí a mají pouze hyperbilirubinemii, kterábývá korigovatelná fototerapií. Vlivem fototerapieje nekonjugovaný bilirubin (který je rozpustný v tucích)konvertován na fotoizoméry (např. strukturálníizomér lumirubin) rozpustné ve vodě. K poklesubilirubinu dochází při vylučování těchtorozpadových produktů ledvinami.Hemolýzu erytrocytů může ovlivnit také podáníintravenozních imunoglobulinů (IVIG) v dávce0,5 g / kg. IVIG způsobují pravděpodobně blokáduFc receptoru buněk retikuloendotelovéhosystému a znemožňují tak jejich vazbu se senzibilizovanýmierytrocyty, tím je zablokována další hemolýza.Střední forma hemolytické nemoci se vyskytujev cca 25% případech. Je charakterizovánazvýšeným pupečníkovým bilirubinem, mírnou anémiía rychlým vzestupem bilirubinu v prvních 24hodinách po porodu. Není-li tento vzestup ovlivnitelnýfototerapií, bývá jedinou terapeutickou možnostívýměnná transfuze (VT). Její zahájení se řídípodle indikačního grafu dle Poláčka a Hodra.Při výměnné transfuzi je odstraněn cirkulující bilirubina senzibilizované erytrocyty novorozence.Protože většina bilirubinu je v extravaskulárnímprostoru, bývá během výměnné transfuze odstraněnopouze zhruba 25% celkového bilirubinuVOX PEDIATRIAE - květen/2006 - č.5 - ročník 621