potencial elektrode - Student Info
potencial elektrode - Student Info
potencial elektrode - Student Info
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
ELEKTROKEMIJA<br />
EKTROKEMIJA<br />
5. 11. 2007
ELEKTROKEMIJSKI ČLEN<br />
10.11.2007 2
TERMODINAMSKI OPIS<br />
Gibbsova prosta energija<br />
∆ S =∆ Sokolice<br />
+∆S<br />
−∆H<br />
∆ S = +∆S<br />
T<br />
−T∆ S =∆H −T∆S<br />
sistema<br />
sistema<br />
sistema<br />
G = ∆H −T∆S<br />
0<br />
G = G + RTln<br />
K<br />
0<br />
G =−RTln<br />
K<br />
0 0<br />
To je merilo za spontanost reakcije.<br />
G<br />
= −zFE<br />
10.11.2007 3
TERMODINAMSKI OPIS<br />
Nernstova enačba<br />
0<br />
G G RTln<br />
K<br />
= +<br />
0<br />
zFE zFE RT K<br />
− =− +<br />
RT<br />
zF<br />
ln<br />
0<br />
E E K<br />
= −<br />
ln<br />
Opisuje termodinamsko napetost polčlena v<br />
nestandardnih pogojih.<br />
10.11.2007 4
POTENCIAL<br />
• Napetost je razlika med <strong>potencial</strong>oma<br />
polčlenov in meri spontanost reakcije.<br />
• Ko reakcija teče v spontano smer, galvanski<br />
člen nudi napetost <strong>potencial</strong>ne razlike.<br />
• Da bi reakcija tekla v nasprotno smer, moramo<br />
elektrolitskemu členu dovesti višjo negativno<br />
napetost.<br />
U = E − E<br />
katode<br />
anode<br />
10.11.2007 5
MERJENJE POTENCIALA<br />
• Elektrodni <strong>potencial</strong> polčlena je definiran kot<br />
napetost člena, v katerem je anoda SHE,<br />
katoda pa merjena elektroda.<br />
• Standardni elektrodni <strong>potencial</strong> opisuje<br />
standardne pogoje (T = 25 °C, a = 1).<br />
10.11.2007 6
MERJENJE POTENCIALA<br />
Standard za določanje<br />
<strong>potencial</strong>a je<br />
standardna vodikova<br />
elektroda (SHE).<br />
0<br />
SHE<br />
E =<br />
0,00 V<br />
10.11.2007 7
POTENCIAL VODIKA<br />
Potencial<br />
vodika je 0 pri<br />
tlaku 1 atm in<br />
pH 0. Za ostale<br />
pogoje ga<br />
izračunamo iz<br />
Nernstove<br />
enačbe.<br />
E [V]<br />
0 RT<br />
E = E − ln K =<br />
zF<br />
RT pH2<br />
= 0− ln =<br />
+<br />
2<br />
zF ⎡<br />
⎣HO<br />
⎤<br />
3 ⎦<br />
=−4,31⋅10 Tln p −1,98⋅10 T pH<br />
−5 −4<br />
H<br />
pH<br />
10.11.2007 8<br />
2<br />
Potencial vodika pri 25 °C<br />
1 ppm<br />
0,40<br />
0,20<br />
20%<br />
100 %<br />
0,00<br />
-0,20 0 2 4 6 8 10 12 14<br />
-0,40<br />
-0,60<br />
-0,80<br />
-1,00<br />
1%
NAPETOSTNA VRSTA<br />
10.11.2007 9
10.11.2007 10
VPLIV TOKA<br />
• Če skozi elektrokemijski člen teče tok, se<br />
njegova napetost razlikuje od mirovne:<br />
E = Emirovna<br />
− IR<br />
• Napetost galvanskega člena se zniža, napetost<br />
elektroliznega člena pa moramo zvišati, ker<br />
ima člen notranjo upornost.<br />
10.11.2007 11
VPLIV TOKA<br />
10.11.2007 12
PRENAPETOST<br />
Prenapetostna efekta:<br />
• koncentracijska polarizacija (η c ) in<br />
• kinetična polarizacija (η a ).<br />
( η η ) ( η η )<br />
E = E + + − E − + − IR<br />
katode c a katode anode c a<br />
anode<br />
Tudi zaradi njiju je napetost galvanskega člena<br />
nižja od pričakovane, izločilna napetost<br />
elektrolitskega člena pa višja.<br />
10.11.2007 13
ELEKTROGRAVIMETRIJA<br />
Z elektrolizo izločimo kovino, ki jo posušimo<br />
in tehtamo.<br />
Depozit ne sme biti gobast, spužvast ali imeti<br />
primesi.<br />
To dosežemo z nizko gostoto toka, rahlim<br />
mešanjem raztopine, kompleksiranjem<br />
kovinskih kationov, ustrezno temperaturo itd.<br />
10.11.2007 14
POTENCIAL ELEKTRODE<br />
Elektrogravimetrično analizo lahko izvajamo<br />
na dva načina:<br />
• z nadzorom <strong>potencial</strong>a (potenciostatično),<br />
• brez nadzora <strong>potencial</strong>a.<br />
10.11.2007 15
POTENCIOSTATIČNA<br />
ANALIZA<br />
S pomočjo referenčne <strong>elektrode</strong> vzdržujemo<br />
<strong>potencial</strong> <strong>elektrode</strong> z analitom konstanten.<br />
Sklenemo dvoje vezij - elektrolitsko in<br />
referenčno.<br />
Omogoča ločitev vzorcev, ki imajo zelo<br />
podoben <strong>potencial</strong>.<br />
10.11.2007 16
POTENCIOSTATIČNA<br />
ANALIZA<br />
10.11.2007 17
BREZ NADZORA<br />
• Priprava je enostavna.<br />
• Dovedena napetost je<br />
konstantna.<br />
Spreminjajo se<br />
prenapetost, tok in<br />
<strong>potencial</strong>.<br />
• Ima omejitve.<br />
POTENCIALA<br />
10.11.2007 18
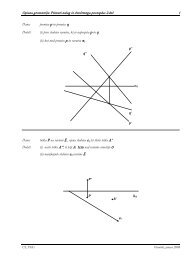
VAJA<br />
• Raztopi 0,3 - 0,5 g vzorca v 15 mL 50 %<br />
HNO 3 , dodaj 10 mL 20 % H 2 SO 4 in segrevaj<br />
do pojava belih par.<br />
•Razredči z dvakratnim volumnom vroče vode,<br />
nevtraliziraj z NH 3 do pojava modre barve<br />
aminkompleksa, dodaj nekaj kapljic H 2 SO 4 .<br />
•Razredči na 250 ml v bučki.<br />
10.11.2007 19
VAJA - REDOKS TITRACIJA<br />
• Odpipetiraj dva alikvota 50 mL, dodaj 2 mL<br />
85 % H 3 PO 4 in 4 g KI.<br />
•Izločeni jod titriraj z 0,1 M tiosulfatom do<br />
svetlo rumene barve. Dodaj 1 mL škrobovice<br />
(raztopina pomodri) in titriraj do razbarvanja.<br />
10.11.2007 20
VAJA - ELEKTROLIZA<br />
•V čašo odpipetiraj 50 mL alikvot raztopine iz<br />
bučke.<br />
• Vanjo potopi čisti elektrodi, vklopi mešanje in<br />
priklopi mrežasto Pt kot katodo. Elektroliziraj<br />
60 min s tokom 0,4 A in 20 min z 0,1 A.<br />
• Dvigni elektrodi iz raztopine, speri z vodo in<br />
odklopi napetost.<br />
• Katodo speri z etanolom, posuši in tehtaj. Nato<br />
jo očisti s HNO 3 , posuši in ponovno stehtaj.<br />
• Razlika je baker.<br />
10.11.2007 21
LITERATURA<br />
• Skoog, Douglas A. et. al. (2004).<br />
Fundamentals of analytical chemistry.<br />
Belmont: Brooks/Cole-Thomson Learning.<br />
• Pihlar, Boris. (2007). Osnove analizne kemije,<br />
2. del. Ljubljana: FKKT.<br />
• Gorenc, D. et. al. (2005). Vaje iz analizne<br />
kemije, kvantitativni del. Ljubljana: FKKT.<br />
10.11.2007 22