Instruktion för läkemedelshantering (pdf) - Västerbottens läns landsting
Instruktion för läkemedelshantering (pdf) - Västerbottens läns landsting Instruktion för läkemedelshantering (pdf) - Västerbottens läns landsting
FÖRVARING, MÄRKNING, LAGRINGS- OCH ANVÄNDNINGSTIDER FÖR LÄKEMEDEL8.2 Lagrings- och användningstider för läkemedelMax lagrings- och användningstidLagringstid iobruten förp.Lagringstid ibruten förp.AnvändningstidTIDtillverkningtillredning/iordningsställandeförsta dos tas utoch ges till patientsista dos har tagitsoch erhållits av patientutgångsdatumSterila läkemedelFör varje läkemedel anges ett utgångsdatum dvs. ettdatum, efter vilket läkemedlet ej skall användas. Tidenmellan tillverkning och utgångsdatum utgör den maximalalagrings- och användningstiden för ett läkemedel.Vid tillredning/iordningställande av ett sterilt läkemedel- såsom upplösning, tillsatser, applicering avinfusionsaggregat - föreligger risk för kontamination.Riskens storlek är beroende av en rad faktorer somlokalens hygieniska standard, utrustning, arbetsteknikoch antal punktioner. Sålunda är kontaminationsriskenstörre om tillredning/iordningställande skett undermindre goda hygieniska förhållanden än om tillredningsker i LAF-bänk/"sterilbänk" i renhetsklassat rummed validerade metoder och av personal med erforderligkompetens (enligt gällande GMP).Tiden mellan tillredning/iordningställande och uttagav första dos benämns här lagringstid i bruten förpackning.Förvaring efter tillredning/-iordningställandeskall om möjligt ske i kylskåp om inte annat anges iproduktinformationen för den enskilda produkten.Vid användning föreligger också en risk för kontamination,som även den är beroende av olika faktorersåsom teknik för uttagande av doser, antal punktioneroch administrationssätt. Fler patienter utsätts för dennasmittorisk om samma förpackning av läkemedletanvänds till fler än en patient.Med användningstid avses den tid från det att förpackningenbryts tills dess att den sista dosen tagits ut ochpatienten erhållit läkemedlet. Även om läkemedletär konserverat 1 föreligger kontaminationsrisk, då ettkonserveringsmedels effekt på olika kontaminerandeagens kan variera. Mot bakgrund härav måste lagrings-och användningstiderna begränsas. Tidpunktför brytande skall anges på förpackningen.De lagrings- och användningstider som anges av tillverkarnaskall i första hand följas. Dessa tider grundaspå tillverkarens dokumentation i enlighet med bl.a.det av EU utgivna dokumentet Note for Guidance onMaximum Shelf-Life for Sterile Products for HumanUse After First Opening or Following Reconstitution”(CPMP/QWP/159/96).De nedan angivna lagrings- och användningstidernadvs. tiden från tillredning/iordningställande av ettsterilt läkemedel intill dess sista dos tagits ur förpackningenoch/eller patienten har erhållit läkemedlet,gäller när annat inte anges av tillverkaren. Om aktuellterapi kräver längre infusionstid än 12 timmar skall riskernamed en förlängning ur hygienisk mikrobiologisksynvinkel bedömas eller belysas med tillväxtstudier.Sterila beredningar där en eventuell kontaminationmedför särskilt stora risker skall endast användas tillen patient.Ampuller och uppdragna sprutorLäkemedel i förpackningar såsom ampuller är avseddaför engångsbruk, vilket innebär att uttag endast skallgöras vid ett tillfälle. Sådana förpackningar skall ejåterförslutas.1Med konserverat läkemedel avses i detta avsnitt läkemedel som uppfyller krav enligt Ph Eur, 5.1.3. Efficacy of antimicrobial preservation38
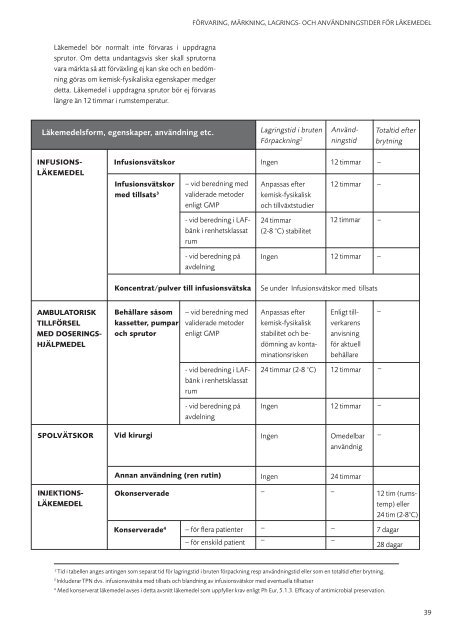
FÖRVARING, MÄRKNING, LAGRINGS- OCH ANVÄNDNINGSTIDER FÖR LÄKEMEDELLäkemedel bör normalt inte förvaras i uppdragnasprutor. Om detta undantagsvis sker skall sprutornavara märkta så att förväxling ej kan ske och en bedömninggöras om kemisk-fysikaliska egenskaper medgerdetta. Läkemedel i uppdragna sprutor bör ej förvaraslängre än 12 timmar i rumstemperatur.Läkemedelsform, egenskaper, användning etc.Lagringstid i brutenFörpackning 2AnvändningstidTotaltid efterbrytningINFUSIONS‐LÄKEMEDELInfusionsvätskorIngen 12 timmar –Infusionsvätskormed tillsats 3– vid beredning medvaliderade metoderenligt GMPAnpassas efterkemisk-fysikaliskoch tillväxtstudier12 timmar –- vid beredning i LAFbänki renhetsklassatrum- vid beredning påavdelning24 timmar(2-8 °C) stabilitetIngen12 timmar –12 timmar –Koncentrat/pulver till infusionsvätskaSe under Infusionsvätskor med tillsatsAMBULATORISKTILLFÖRSELMED DOSERINGS‐HJÄLPMEDELBehållare såsomkassetter, pumparoch sprutor– vid beredning medvaliderade metoderenligt GMPAnpassas efterkemisk-fysikaliskstabilitet och bedömningav kontaminationsriskenEnligt tillverkarensanvisningför aktuellbehållare–- vid beredning i LAFbänki renhetsklassatrum24 timmar (2-8 °C)12 timmar–- vid beredning påavdelningIngen12 timmar–SPOLVÄTSKORVid kirurgi IngenOmedelbar –användnigAnnan användning (ren rutin)Ingen24 timmarINJEKTIONS-LÄKEMEDELOkonserverade––12 tim (rumstemp)eller24 tim (2-8°C)Konserverade 4– för flera patienter– för enskild patient––––7 dagar28 dagar2Tid i tabellen anges antingen som separat tid för lagringstid i bruten förpackning resp användningstid eller som en totaltid efter brytning.3Inkluderar TPN dvs. infusionsvätska med tillsats och blandning av infusionsvätskor med eventuella tillsatser4Med konserverat läkemedel avses i detta avsnitt läkemedel som uppfyller krav enligt Ph Eur, 5.1.3. Efficacy of antimicrobial preservation.39
- Page 1: 2008
- Page 4 and 5: Innehåll1. ANSVAR.................
- Page 6 and 7: 8.1 Förvaring och märkning.......
- Page 8 and 9: ANSVAREnligt SOSFS 2005:12 ska ledn
- Page 10 and 11: ANSVAR• ska rapportera till närm
- Page 12 and 13: ORDINATION AV LÄKEMEDEL2. ORDINATI
- Page 14 and 15: ORDINATION AV LÄKEMEDELDe generell
- Page 16 and 17: ORDINATION AV LÄKEMEDELI god tid f
- Page 18 and 19: IORDNINGSTÄLLANDE AV LÄKEMEDELlä
- Page 20 and 21: IORDNINGSTÄLLANDE AV LÄKEMEDELOBS
- Page 22 and 23: ADMINISTRERING/ÖVERLÄMNANDE AV L
- Page 24 and 25: ADMINISTRERING/ÖVERLÄMNANDE AV L
- Page 26 and 27: REKVISITION AV LÄKEMEDEL5.4 Licens
- Page 28 and 29: REKVISITION AV LÄKEMEDELLäkemedle
- Page 30 and 31: FÖRVARING AV LÄKEMEDELspecialinri
- Page 32 and 33: FÖRVARING AV LÄKEMEDEL6.6 Medel f
- Page 34 and 35: NARKOTIKA7. NARKOTIKAVerksamhetsche
- Page 36 and 37: NARKOTIKA7.10 Inventering och kontr
- Page 40 and 41: FÖRVARING, MÄRKNING, LAGRINGS- OC
- Page 42 and 43: CYTOSTATIKA OCH ANDRA LÄKEMEDEL ME
- Page 44 and 45: BIVERKNINGAR, ÖVERKÄNSLIGHET, ÖV
- Page 46 and 47: KVALITETSSÄKRING11. KVALITETSSÄKR
- Page 48 and 49: HANTERINGSANVISNINGAR FÖR OLIKA BE
- Page 50 and 51: HANTERINGSANVISNINGAR FÖR OLIKA BE
- Page 52 and 53: APO-DOS13. APO-DOSDosrecept utgör
- Page 54 and 55: APO-DOSring mellan sjukhusvård, ö
- Page 56 and 57: BILAGA ISändlista förslagInstrukt
- Page 58 and 59: BILAGA IIILokal instruktion för l
- Page 60 and 61: BILAGA IVExempelAnsvar för läkeme
- Page 62: INDEXakuta läkemedel, 27,28,59alle
FÖRVARING, MÄRKNING, LAGRINGS- OCH ANVÄNDNINGSTIDER FÖR LÄKEMEDELLäkemedel bör normalt inte förvaras i uppdragnasprutor. Om detta undantagsvis sker skall sprutornavara märkta så att förväxling ej kan ske och en bedömninggöras om kemisk-fysikaliska egenskaper medgerdetta. Läkemedel i uppdragna sprutor bör ej förvaraslängre än 12 timmar i rumstemperatur.Läkemedelsform, egenskaper, användning etc.Lagringstid i brutenFörpackning 2AnvändningstidTotaltid efterbrytningINFUSIONS‐LÄKEMEDELInfusionsvätskorIngen 12 timmar –Infusionsvätskormed tillsats 3– vid beredning medvaliderade metoderenligt GMPAnpassas efterkemisk-fysikaliskoch tillväxtstudier12 timmar –- vid beredning i LAFbänki renhetsklassatrum- vid beredning påavdelning24 timmar(2-8 °C) stabilitetIngen12 timmar –12 timmar –Koncentrat/pulver till infusionsvätskaSe under Infusionsvätskor med tillsatsAMBULATORISKTILLFÖRSELMED DOSERINGS‐HJÄLPMEDELBehållare såsomkassetter, pumparoch sprutor– vid beredning medvaliderade metoderenligt GMPAnpassas efterkemisk-fysikaliskstabilitet och bedömningav kontaminationsriskenEnligt tillverkarensanvisningför aktuellbehållare–- vid beredning i LAFbänki renhetsklassatrum24 timmar (2-8 °C)12 timmar–- vid beredning påavdelningIngen12 timmar–SPOLVÄTSKORVid kirurgi IngenOmedelbar –användnigAnnan användning (ren rutin)Ingen24 timmarINJEKTIONS-LÄKEMEDELOkonserverade––12 tim (rumstemp)eller24 tim (2-8°C)Konserverade 4– för flera patienter– för enskild patient––––7 dagar28 dagar2Tid i tabellen anges antingen som separat tid för lagringstid i bruten förpackning resp användningstid eller som en totaltid efter brytning.3Inkluderar TPN dvs. infusionsvätska med tillsats och blandning av infusionsvätskor med eventuella tillsatser4Med konserverat läkemedel avses i detta avsnitt läkemedel som uppfyller krav enligt Ph Eur, 5.1.3. Efficacy of antimicrobial preservation.39