Таблица 2 Термодинамические константы некоторых веществ Вещество ΔH 0 298, кДж/моль ΔG 0 298, кДж/моль S 0 298, Дж/моль⋅град. 1 2 3 4 Al(к) 0 0 28,4 Al 2 O 3 (к) –1676,8 –1583,3 50,95 Al 2 (SO 4 ) 3 (к) –3444,1 –3102,9 239,4 BaCO 3 (к) –1217,1 –1137,2 113,0 BaO(к) –553,9 –525,4 70,5 BeCO 3 (к) –982 –944,7 67,29 BeO(к) –598 –582 14,1 C(графит) 0 0 5,740 CO(г) –110,5 –137,27 197,4 СO 2 (г) –393,51 –394,38 213,6 CS 2 (ж) 87,8 63,6 151,0 CH 4 (г) –74,86 –50,85 186,44 C 2 H 2 (г) 226,75 209,2 200,8 C 2 H 4 (г) 52,28 68,12 219,45 CH 3 OH(ж) –238,7 –166,31 126,7 CaO(к) –635,1 –604,2 39,7 CaC 2 (к) –62,7 –67,8 70,3 Ca(OH) 2 –986,2 –896,76 83,4 Ca 3 (PO 4 ) 2 (к) –4125,0 –3899,5 240,9 CaCO 3 (к) –1206,0 –1128,8 92,9 HCl(г) –92,30 –95,27 186,67 Сr(CO) 6 (к) –1077,4 –970,4 314 Cs 2 O(к) –317,6 –274,5 123,8 СsOH(к) –406,5 –355,2 77,8 Fe(к) 0 0 27,2 FeO(к) –265,0 –244,5 60,8 FeS(к) –100,5 –100,8 60,3 Fe 2 O 3 (к) –822,7 –740,8 87,5 Fe 3 O 4 (к) –1117,9 –1014,8 146,3 H 2 (г) 0 0 130,6 H 2 O(г) –241,84 –228,8 188,74 H 2 O(ж) –285,84 –237,5 69,96 H 2 O 2 (ж) –187,36 –117,57 105,86 HgCl 2 (к) –230,12 –185,77 144,35 Hg 2 Cl 2 (к) –264,85 –210,66 195,81 K 2 O(к) –361,5 –193,3 87,0 KOH(р) –477,3 –440,5 91,6 KOH(к) –425,8 –380,2 79,32 KH(к) –63,4 –34,0 50,2 KNO 2 (к) –370,3 –218,6 117 KNO 3 (к) –493,2 –393,1 132,93 Li 2 O(к) –595,8 –560,2 37,9 LiOH(к) –487,8 –443,1 42,81 110
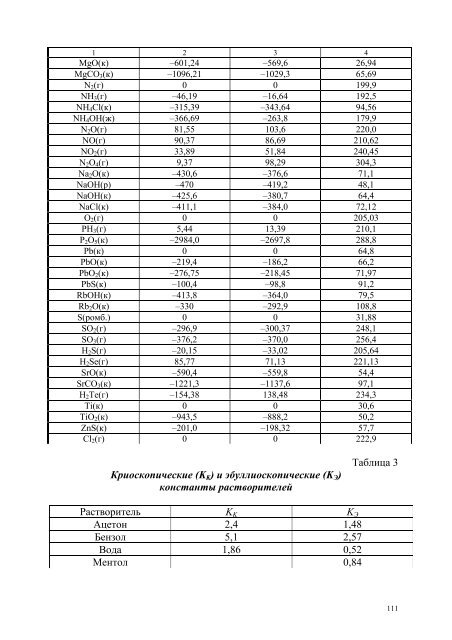
1 2 3 4 MgO(к) –601,24 –569,6 26,94 MgCO 3 (к) –1096,21 –1029,3 65,69 N 2 (г) 0 0 199,9 NH 3 (г) –46,19 –16,64 192,5 NH 4 Cl(к) –315,39 –343,64 94,56 NH 4 OH(ж) –366,69 –263,8 179,9 N 2 O(г) 81,55 103,6 220,0 NO(г) 90,37 86,69 210,62 NO 2 (г) 33,89 51,84 240,45 N 2 O 4 (г) 9,37 98,29 304,3 Na 2 O(к) –430,6 –376,6 71,1 NaOH(р) –470 –419,2 48,1 NaOH(к) –425,6 –380,7 64,4 NaCl(к) –411,1 –384,0 72,12 O 2 (г) 0 0 205,03 PH 3 (г) 5,44 13,39 210,1 P 2 O 5 (к) –2984,0 –2697,8 288,8 Pb(к) 0 0 64,8 PbO(к) –219,4 –186,2 66,2 PbO 2 (к) –276,75 –218,45 71,97 PbS(к) –100,4 –98,8 91,2 RbOH(к) –413,8 –364,0 79,5 Rb 2 O(к) –330 –292,9 108,8 S(ромб.) 0 0 31,88 SO 2 (г) –296,9 –300,37 248,1 SO 3 (г) –376,2 –370,0 256,4 H 2 S(г) –20,15 –33,02 205,64 H 2 Se(г) 85,77 71,13 221,13 SrO(к) –590,4 –559,8 54,4 SrCO 3 (к) –1221,3 –1137,6 97,1 H 2 Te(г) –154,38 138,48 234,3 Ti(к) 0 0 30,6 TiO 2 (к) –943,5 –888,2 50,2 ZnS(к) –201,0 –198,32 57,7 Cl 2 (г) 0 0 222,9 Криоскопические (K K ) и эбуллиоскопические (K Э ) константы растворителей Таблица 3 Растворитель K K K Э Ацетон 2,4 1,48 Бензол 5,1 2,57 Вода 1,86 0,52 Ментол 0,84 111
- Page 1 and 2:
Федеральное агентс
- Page 3 and 4:
УДК 54 (076) Шапкина В.
- Page 5 and 6:
Данная масса углер
- Page 7 and 8:
Например, эквивале
- Page 9 and 10:
Пример 6. Определит
- Page 11 and 12:
ΔЕ = h·ν, где ΔЕ - эне
- Page 13 and 14:
Квантовые числа оп
- Page 15 and 16:
так что возникает э
- Page 17 and 18:
40. Составьте электр
- Page 19 and 20:
Первый, второй и тр
- Page 21 and 22:
Если полярности св
- Page 23 and 24:
При обменном механ
- Page 25 and 26:
отвечает значитель
- Page 27 and 28:
Молекула NH 3 не може
- Page 29 and 30:
Раздел термодинами
- Page 31 and 32:
Определите стандар
- Page 33 and 34:
беспорядку (+ΔS). При
- Page 35 and 36:
При определении из
- Page 37 and 38:
Хлор или кислород в
- Page 39 and 40:
Скорость гетероген
- Page 41 and 42:
179. Реакция выражае
- Page 43 and 44:
Решение. KT E ⎛ 1 1 Из
- Page 45 and 46:
Для гомогенной реа
- Page 47 and 48:
константу равновес
- Page 49 and 50:
235. При некоторой те
- Page 51 and 52:
m 2 - масса раствора.
- Page 53 and 54:
( 124,7 + ) , или ,4 ⋅124,7 =
- Page 55 and 56:
262. Какую массу Na 2 SO
- Page 57 and 58:
Коэффициенты раств
- Page 59 and 60: где с - удельная теп
- Page 61 and 62: 291. При растворении
- Page 63 and 64: расчете состава ан
- Page 65 and 66: 310. Раствор сахара (
- Page 67 and 68: равен содержанию 20,
- Page 69 and 70: Таким образом, коли
- Page 71 and 72: K Д = 2 2 αC⋅αC α C α = = (
- Page 73 and 74: молекул кислоты, и
- Page 75 and 76: 364. Вычислите конст
- Page 77 and 78: 366. Насыщенный раст
- Page 79 and 80: Логарифмируя соотн
- Page 81 and 82: 391. Чему равна конст
- Page 83 and 84: Как правило, степен
- Page 85 and 86: 403. Напишите в ионно
- Page 87 and 88: РАЗДЕЛ 7. ЭЛЕКТРОХИ
- Page 89 and 90: n - число ионов желе
- Page 91 and 92: 445. Вычислите потен
- Page 93 and 94: −3 E 2 H + H = 0, 059lg 5, 664⋅
- Page 95 and 96: ΔG 0 обр.(Сu 2+ ) = +66,2 кД
- Page 97 and 98: На практике вследс
- Page 99 and 100: никелировании в те
- Page 101 and 102: электроды нераство
- Page 103 and 104: расплава, если терм
- Page 105 and 106: растворенного кисл
- Page 107 and 108: 516. Какое покрытие м
- Page 109: СПИСОК ЛИТЕРАТУРЫ 1
- Page 113 and 114: периоды 1 ряды I ПЕР
- Page 115 and 116: Таблица 7 Произведе
- Page 117 and 118: 3.4. 146. Реакция 1 и 2; 14
- Page 119 and 120: 295. 11,46 г; 297. -77,7 кДж/м
- Page 121 and 122: 438. 2,46; 3,4⋅10 -2 ; 439. -0,29