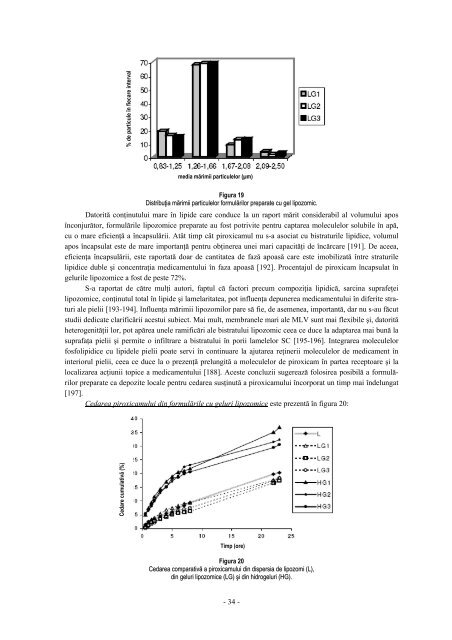
Figura 19 Distribuţia mărimii parti<strong>cu</strong>lelor formulărilor preparate <strong>cu</strong> gel lipozomic. Datorită conţinutului mare în lipi<strong>de</strong> care conduce la un raport mărit consi<strong>de</strong>rabil al volumului apos înconjurător, formulările lipozomice preparate au fost potrivite pentru captarea mole<strong>cu</strong>lelor solubile în apă, <strong>cu</strong> o mare eficienţă a încapsulării. Atât timp cât piroxicamul nu s-a asociat <strong>cu</strong> bistraturile lipidice, volumul apos încapsulat este <strong>de</strong> mare importanţă pentru obţinerea unei mari capacităţi <strong>de</strong> încărcare [191]. De aceea, eficienţa încapsulării, este raportată doar <strong>de</strong> cantitatea <strong>de</strong> fază apoasă care este imobilizată între straturile lipidice duble şi concentraţia medicamentului în faza apoasă [192]. Procentajul <strong>de</strong> piroxicam încapsulat în gelurile lipozomice a fost <strong>de</strong> peste 72%. S-a raportat <strong>de</strong> către mulţi autori, faptul că factori pre<strong>cu</strong>m compoziţia lipidică, sarcina suprafeţei lipozomice, conţinutul total în lipi<strong>de</strong> şi lamelaritatea, pot influenţa <strong>de</strong>punerea medicamentului în diferite straturi ale pielii [193-194]. Influenţa mărimii lipozomilor pare să fie, <strong>de</strong> asemenea, importantă, dar nu s-au fă<strong>cu</strong>t studii <strong>de</strong>dicate clarificării acestui subiect. Mai mult, membranele mari ale MLV sunt mai flexibile şi, datorită heterogenităţii lor, pot apărea unele ramificări ale bistratului lipozomic ceea ce duce la adaptarea mai bună la suprafaţa pielii şi permite o infiltrare a bistratului în porii lamelelor SC [195-196]. Integrarea mole<strong>cu</strong>lelor fosfolipidice <strong>cu</strong> lipi<strong>de</strong>le pielii poate servi în continuare la ajutarea reţinerii mole<strong>cu</strong>lelor <strong>de</strong> medicament în interiorul pielii, ceea ce duce la o prezenţă prelungită a mole<strong>cu</strong>lelor <strong>de</strong> piroxicam în partea receptoare şi la localizarea acţiunii topice a medicamentului [188]. Aceste concluzii sugerează folosirea posibilă a formulărilor preparate ca <strong>de</strong>pozite locale pentru cedarea susţinută a piroxicamului încorporat un timp mai în<strong>de</strong>lungat [197]. Cedarea piroxicamului din formulările <strong>cu</strong> geluri lipozomice este prezentă în figura 20: Cedare <strong>cu</strong>mulativă (%) % <strong>de</strong> parti<strong>cu</strong>le în fiecare interval media mărimii parti<strong>cu</strong>lelor (µm) Timp (ore) Figura 20 Cedarea comparativă a piroxicamului din dispersia <strong>de</strong> lipozomi (L), din geluri lipozomice (LG) şi din hidrogeluri (HG). - 34 -
Probe similare ale cedării piroxicamului au fost înregistrate pentru toate formulările, ceea ce indică faptul că concentraţia agentului <strong>de</strong> gelifiere într-un domeniu <strong>de</strong> 1,5 - 2%, afectează uşor viteza <strong>de</strong> cedare. Pentru a evalua efectul încorporării piroxicamului în lipozomi, asupra vitezei <strong>de</strong> cedare, comparativ, a fost estimată viteza cedării din dispersia lipozomică <strong>de</strong> bază (L), din gelurile lipozomice (LG1, LG2 şi LG3) şi din hidrogelurile corespunzătoare (HG1, HG2, HG3). Cedarea piroxicamului din lipozomii împăturiţi în baza <strong>de</strong> gel a fost semnificativ mai mică (aproximativ 18% cedare în cadrul a 24 <strong>de</strong> ore) <strong>de</strong>cât cea din hidrogelurile <strong>de</strong> carbopol 940 (32 - 37%), ceea ce confirmă faptul că încapsularea piroxicamului în lipozomi conduce la o viteză prelungită a cedării acestuia [182]. O viteză <strong>de</strong> cedare mai mică, din sistemele <strong>de</strong> geluri lipozomice comparativ <strong>cu</strong> dispersia lipozomică <strong>de</strong> bază, poate fi un rezultat al influenţei vâscozităţii matriţei gelului, urmată <strong>de</strong> o penetrare mai mică a medicamentului la nivelul pielii. Depen<strong>de</strong>nţa exponenţială a cantităţii <strong>de</strong> medicament cedat în funcţie <strong>de</strong> timp, a fost evi<strong>de</strong>nţiată în tabelul XV. Pentru hidrogeluri exponentul <strong>de</strong> difuziune n a fost <strong>de</strong> 0.5, ceea ce indică difuzia Fick (cedarea a avut loc după mo<strong>de</strong>lul <strong>de</strong> difuziune Higuchi), în timp ce pentru gelurile lipozomice exponenţii <strong>de</strong> difuziune au fost superiori valorii <strong>de</strong> 0,5 (0,67 pentru dispersia lipozomică şi 0,8 - 0,98 pentru gelurile lipozomice). Indicând difuzia anormală <strong>de</strong> caz II, ceea ce sugerează posibila umflare a sistemului în solvent înainte ca cedarea să aibă loc [198]. Ori<strong>cu</strong>m, după 3 ore, s-au obţinut coeficienţi <strong>de</strong> corelare mari pentru cinetica cedării medicamentului <strong>de</strong> ordin zero, pentru geluri lipozomice, sugerând că lipozomii pot acţiona ca sisteme-rezervor pentru eliberarea continuă a piroxicamului încapsulat [178-179]. În scopul <strong>de</strong> a furniza o formulare stabilă pentru aplicarea locală, în care lipozomii sunt distribuiţi uniform şi în care structura a fost păstrată, gelurile lipozomice au fost ţinute timp <strong>de</strong> 3 săptămâni la temperatura <strong>de</strong> 4°C. Tabel XV Compararea coeficienţilor <strong>de</strong> corelare a datelor <strong>de</strong>spre cedarea medicamentului obţinute pe baza mo<strong>de</strong>lului Higuchi şi a celui <strong>de</strong> ordin zero şi valorile exponentului <strong>de</strong> cedare (n), obţinut din e<strong>cu</strong>aţia Mt/Mo = ktn a formulărilor preparate (n =3). Mo<strong>de</strong>l Higuchia Cinetică <strong>de</strong> ordin zerob Probă “n” R Mecanism <strong>de</strong> cedare k ( % h –1/2 ) R k ( % h –1 ) R LG1 Proaspăt prep. După 1 săpt. După 2 săpt. După 3 săpt. LG2 Proaspăt prep. După 1 săpt. După 2 săpt. După 3 săpt. LG3 Proaspăt prep. După 1 săpt. După 2 săpt. După 3 săpt. HG1c HG2c 0,80 0,87 0,98 0,52 0,49 HG3c 0,48 a b c 0 – 3 ore; 3 – 24 ore; 0 – 24 ore 0,971 0,989 0,980 0,995 0,991 0,994 Non-Fickian Non-Fickian Non-Fickian Fickian Fickian Fickian - 35 - 4,45 3,18 4,21 4,16 2,99 3,87 3,34 3,94 3,47 3,87 3,68 3,48 7,55 6,80 6,14 0,997 0,998 0,982 0,987 0,989 0,997 0,997 0,980 0,983 0,996 0,999 0,989 0,996 0,983 0,986 0,62 0,70 0,78 0,77 0,69 0,62 0,68 0,77 0,71 0,67 0,62 0,68 – – – 0,994 0,998 0,998 0,999 0,997 0,998 0,998 0,997 0,998 0,995 0,999 0,990 – – – De-a lungul acestor experimente nu au apărut modificări ale proprietăţilor organoleptice ale formulărilor preparate, iar valoarea pH a tuturor gelurilor a fost în intervalul limitelor <strong>de</strong> ± 0,3 unităţi pH <strong>de</strong> la valoarea iniţială. De asemenea, nu s-a observat modificări esenţiale în ceea ce priveşte mărimea parti<strong>cu</strong>lelor lipozomilor, p < 0,05 (figura 18). Unii autori indică faptul că pier<strong>de</strong>rea medicamentului <strong>cu</strong> mai puţin <strong>de</strong> 5% din încărcătura iniţială într-o perioadă <strong>de</strong> 4 săptămâni, în condiţii <strong>de</strong> refrigerare, a fost bună în intervalul limitelor, atunci când vezi<strong>cu</strong>lele au fost utilizate pentru aplicarea locală [188]. Cum se poate ve<strong>de</strong>a în figura 21 procentul <strong>de</strong> piroxicam asociat în lipozomi, din gelurile lipozomice a rămas stabil. De asemenea, nu s-au