Materiais moleculares funcionais contendo n-heterociclos - capes
Materiais moleculares funcionais contendo n-heterociclos - capes Materiais moleculares funcionais contendo n-heterociclos - capes
Resultados e Discussão 106com fótons de λ abs.max . Os deslocamentos de Stokes foram obtidos a partir da diferença doscomprimentos de onda máximos de emissão e absorção nos espectros, e ficaram em torno de90 nm. Os rendimentos quânticos de fluorescência (Φ F ) foram obtidos pelo mesmo método jáempregado anteriormente, 96 relativos ao padrão sulfato de quinina (H 2 SO 4 1M, solvente), e osbaixos valores obtidos, principalmente os referentes aos compostos finais 77-82 variando de0,3% a 1%, mostra que esses compostos são pobres fluoróforos em solução de CHCl 3 (opróprio solvente pode ser o responsável pelos baixos valores obtidos). Ainda que isso nãodescarte suas possíveis aplicações tecnológicas.Os espectros de absorção e emissão dos intermediários 57 e 59 em solução sãomostrados na Figura 59. Note que a presença de grupos fenólicos livres, no composto 59, levaa um deslocamento hipsocrômico (blue-shift) de cerca de 10 nm em relação ao observado parao composto 57 O-protegido. Também é observado redução de pelo menos metade norendimento quântico de emissão, explicado devido à supressão de fluorescência provocadapelos grupos hidroxilas livres.Absorbancia Normalizada5759Intensidade Normalizada250 300 350 400 450 500 550 600Comprimento de onda (nm)Figura 59. Espectros normalizados de UV (esquerda) e fluorescência (direita) dos compostosintermediários 57 e 59 em CHCl 3 .Os compostos finais 77-82 apresentaram um perfil similar em suas curvas de absorçãoe emissão em solução, mostrados na Figura 60, só que ao contrário do obtido para os
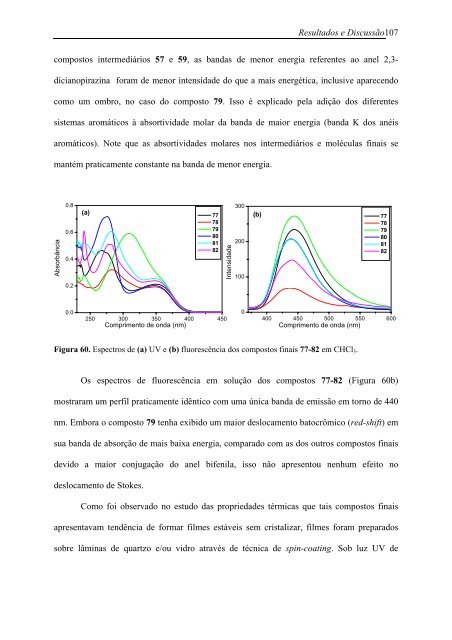
Resultados e Discussão 107compostos intermediários 57 e 59, as bandas de menor energia referentes ao anel 2,3-dicianopirazina foram de menor intensidade do que a mais energética, inclusive aparecendocomo um ombro, no caso do composto 79. Isso é explicado pela adição dos diferentessistemas aromáticos à absortividade molar da banda de maior energia (banda K dos anéisaromáticos). Note que as absortividades molares nos intermediários e moléculas finais semantém praticamente constante na banda de menor energia.Absorbância0.80.60.40.2(a)777879808182Intensidade300200100(b)7778798081820.0250 300 350 400 450Comprimento de onda (nm)0400 450 500 550 600Comprimento de onda (nm)Figura 60. Espectros de (a) UV e (b) fluorescência dos compostos finais 77-82 em CHCl 3 .Os espectros de fluorescência em solução dos compostos 77-82 (Figura 60b)mostraram um perfil praticamente idêntico com uma única banda de emissão em torno de 440nm. Embora o composto 79 tenha exibido um maior deslocamento batocrômico (red-shift) emsua banda de absorção de mais baixa energia, comparado com as dos outros compostos finaisdevido a maior conjugação do anel bifenila, isso não apresentou nenhum efeito nodeslocamento de Stokes.Como foi observado no estudo das propriedades térmicas que tais compostos finaisapresentavam tendência de formar filmes estáveis sem cristalizar, filmes foram preparadossobre lâminas de quartzo e/ou vidro através de técnica de spin-coating. Sob luz UV de
- Page 59 and 60: RESULTADOS EDISCUSSÃO
- Page 61 and 62: Resultados e Discussão 57aromátic
- Page 63 and 64: Resultados e Discussão 59Esquema 3
- Page 65 and 66: Resultados e Discussão 61mantendo-
- Page 67 and 68: Resultados e Discussão 63(ν C≡C
- Page 69 and 70: Resultados e Discussão 65funcional
- Page 71 and 72: Resultados e Discussão 67ROORROOO4
- Page 73 and 74: Resultados e Discussão 69Uma rota
- Page 75 and 76: Resultados e Discussão 71baNNOc d
- Page 77 and 78: Resultados e Discussão 73Tabela 3.
- Page 79 and 80: Resultados e Discussão 75Para o co
- Page 81 and 82: Resultados e Discussão 77porque o
- Page 83 and 84: Resultados e Discussão 795. CLs cu
- Page 85 and 86: Resultados e Discussão 81gerado a
- Page 87 and 88: Resultados e Discussão 835.2. Prop
- Page 89 and 90: Resultados e Discussão 85(a)Cr-CrC
- Page 91 and 92: Resultados e Discussão 87(a)(b)Fig
- Page 93 and 94: Resultados e Discussão 89Esses com
- Page 95 and 96: Resultados e Discussão 91catalíti
- Page 97 and 98: Resultados e Discussão 93a complet
- Page 99 and 100: Resultados e Discussão 95A banda l
- Page 101 and 102: Resultados e Discussão 97constante
- Page 103 and 104: Resultados e Discussão 99A não-pl
- Page 105 and 106: Resultados e Discussão 101(a)(b)T
- Page 107 and 108: Resultados e Discussão 103(e)trans
- Page 109: Resultados e Discussão 1056.5. Pro
- Page 113 and 114: Resultados e Discussão 109composto
- Page 115 and 116: Resultados e Discussão 1117. Tris-
- Page 117 and 118: Resultados e Discussão 113Esquema
- Page 119 and 120: Resultados e Discussão 115A caract
- Page 121 and 122: Resultados e Discussão 117ppm rela
- Page 123 and 124: Resultados e Discussão 1197.2. Est
- Page 125 and 126: Resultados e Discussão 121Figura 7
- Page 127 and 128: Resultados e Discussão 123N21-N22
- Page 129 and 130: Resultados e Discussão 125método
- Page 131 and 132: Resultados e Discussão 127após lo
- Page 133 and 134: Resultados e Discussão 129baseado
- Page 135 and 136: Resultados e Discussão 131aquecime
- Page 137 and 138: Resultados e Discussão 133composto
- Page 139 and 140: Resultados e Discussão 1357.5. Est
- Page 141 and 142: Resultados e Discussão 137estabili
- Page 143 and 144: Conclusões 1398. CONCLUSÕESEm ger
- Page 145 and 146: SEÇAO EXPERIMENTAL
- Page 147 and 148: Seção Experimental 143respectivam
- Page 149 and 150: Seção Experimental 1457,08 (m, 2H
- Page 151 and 152: Seção Experimental 147K 2 CO 3 (7
- Page 153 and 154: Seção Experimental 149H, -CH 2 NC
- Page 155 and 156: Seção Experimental 1512918, 2851,
- Page 157 and 158: Seção Experimental 153Esse compos
- Page 159 and 160: Seção Experimental 155Espectro de
Resultados e Discussão 107compostos intermediários 57 e 59, as bandas de menor energia referentes ao anel 2,3-dicianopirazina foram de menor intensidade do que a mais energética, inclusive aparecendocomo um ombro, no caso do composto 79. Isso é explicado pela adição dos diferentessistemas aromáticos à absortividade molar da banda de maior energia (banda K dos anéisaromáticos). Note que as absortividades molares nos intermediários e moléculas finais semantém praticamente constante na banda de menor energia.Absorbância0.80.60.40.2(a)777879808182Intensidade300200100(b)7778798081820.0250 300 350 400 450Comprimento de onda (nm)0400 450 500 550 600Comprimento de onda (nm)Figura 60. Espectros de (a) UV e (b) fluorescência dos compostos finais 77-82 em CHCl 3 .Os espectros de fluorescência em solução dos compostos 77-82 (Figura 60b)mostraram um perfil praticamente idêntico com uma única banda de emissão em torno de 440nm. Embora o composto 79 tenha exibido um maior deslocamento batocrômico (red-shift) emsua banda de absorção de mais baixa energia, comparado com as dos outros compostos finaisdevido a maior conjugação do anel bifenila, isso não apresentou nenhum efeito nodeslocamento de Stokes.Como foi observado no estudo das propriedades térmicas que tais compostos finaisapresentavam tendência de formar filmes estáveis sem cristalizar, filmes foram preparadossobre lâminas de quartzo e/ou vidro através de técnica de spin-coating. Sob luz UV de