R. Ã fogo-Quest - Ufrgs
R. Ã fogo-Quest - Ufrgs
R. Ã fogo-Quest - Ufrgs
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
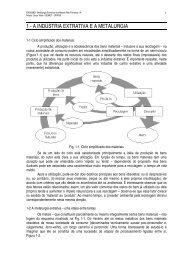
ENG06632 - Metalurgia Extrativa dos Metais Não-Ferrosos II-A<br />
Nestor Cezar Heck – UFRGS / DEMET<br />
1<br />
Refino à <strong>fogo</strong><br />
Status 2004/2<br />
<strong>Quest</strong>ões para fixar o conteúdo:<br />
1) Escreva a reação genérica do refino à <strong>fogo</strong> e descreva o significado de seus componentes.<br />
2) Pelas características, o refino à <strong>fogo</strong> se enquadra na classe química ou física de refino<br />
3) O refino à <strong>fogo</strong> não pode ser usado no alumínio. Diga para que classe de metais melhor se<br />
emprega o refino à <strong>fogo</strong> e dê alguns exemplos.<br />
4) Qual a importância de se ter X em uma nova fase, XO (Lembre que, no resultado de uma<br />
análise química do metal, permanece constante o teor da impureza X se o produto do refino é<br />
uma dispersão de XO no metal de valor, mas, metalurgicamente, há uma diferença entre essa<br />
situação e aquela inicial, onde a impureza X estava dissolvida na matriz metálica)<br />
5) O estado físico de XO podem ser importante no refino. Explique.<br />
6) Qual a importância de se ter XO formando uma camada no topo do banho<br />
7) Que fatores são importantes para se transformar uma dispersão de XO no metal de valor em<br />
uma camada sobrenadante<br />
8) Quais são as técnicas para se fornecer oxigênio ao metal<br />
9) O que são “elementos residuais” (tramp elements) Exemplifique.<br />
10) Quais são as duas etapas do refino à <strong>fogo</strong><br />
11) Quais são as duas técnicas empregadas na etapa final do refino<br />
12) Qual o grau máximo de pureza no refino à <strong>fogo</strong><br />
13) Por qual motivo existe uma saturação (teor máximo) de O no banho<br />
14) No caso dela ser atingida, o que acontece com o oxigênio adicional fornecido ao banho<br />
15) Explore a relação entre a atividade do óxido do metal de valor e a atividade máxima do O e<br />
responda: quais as conseqüências de uma diminuição da atividade do óxido do metal de valor<br />
16) O quê pode fazer a atividade do óxido do metal de valor diminuir<br />
17) Mostre, por meio de um diagrama atividade de X versus atividade de O, a lógica do refino à <strong>fogo</strong>.<br />
Justifique a análise.<br />
18) A desoxidação pode ser feita sob vácuo; qual é o seu alcance no metal líquido<br />
19) No refino à <strong>fogo</strong> do Si no banho podemos alterar a sua atividade usando CaO. Compare a<br />
questão acima e faça conjecturas a respeito do alcance dessa medida no metal líquido.<br />
20) No caso do emprego de vácuo na desoxidação, queremos que o produto XO(g) tenha, no<br />
equilíbrio, uma pressão parcial elevada ou baixa<br />
21) A presença de um terceiro elemento dissolvido no banho (interação medida pelo coeficiente de<br />
atividade) pode influenciar a atividade da impureza X dissolvida no metal de valor. Qual o<br />
significado prático disso, quando o coeficiente de atividade do X se torna maior do que a<br />
unidade<br />
22) Para o refino à <strong>fogo</strong> preferimos temperaturas moderadas, ou elevadas Explique usando um<br />
gráfico.<br />
23) Qual uso damos ao calor gerado pelas reações exotérmicas do refino à <strong>fogo</strong><br />
<strong>Quest</strong>ões para o desenvolvimento do tema:<br />
1) A variação da energia livre padrão de Gibbs pode ser usada para dar a provável ordem de<br />
eliminação de elementos no banho durante o refino à <strong>fogo</strong>; use ∆G° para a reação de formação<br />
dos compostos SnO 2 , As 2 O 3 , e SbO 2 à temperatura de 500°C, em Joule, dada por mol de óxido<br />
(cuidado: o diagrama de Hellingham dá esse valor por mol de O 2 (g)! ): -4,15E+05; -4,51E+05; e -<br />
3,11E+05; para dar a provável ordem de eliminação de estanho, arsênio e antimônio do chumbo.<br />
2) Uma segunda informação pode ser usada para dar a provável ordem de eliminação de elementos<br />
no banho durante o refino à <strong>fogo</strong>. Guthrie nos dá uma pista quando diz que, à 1550°C, em uma<br />
solução líquida de Cu-Fe, o valor de γ° Fe = 10,57, enquanto que γ° Ni ≈ 1,91 para uma solução<br />
líquida de Cu-Ni. Faça um diagrama aproximado atividade versus fração molar do soluto e
ENG06632 - Metalurgia Extrativa dos Metais Não-Ferrosos II-A<br />
Nestor Cezar Heck – UFRGS / DEMET<br />
2<br />
responda, com base nele, quem seria oxidado mais facilmente, entre o Fe e o Ni, durante o refino<br />
do cobre (aqui vale o princípio de Le Chatelier)!<br />
3) O refino do cobre inclui a eliminação do enxofre remanescente do processo de conversão por<br />
meio da reação:<br />
S + 2O = SO 2 (g) .<br />
Rosenqvist nos dá o seguinte valor, com base na reação acima, à temperatura de 1150°C e<br />
baixas pressões de SO 2 , para a equação:<br />
2<br />
([ S] ⋅[ O]<br />
)<br />
K'<br />
= 0,012 =<br />
.<br />
p SO<br />
2<br />
a) Complete a tabela com os valores apropriados, usando pSO 2 = 1 [atm]; (b) faça o gráfico<br />
correspondente usando, na ordenada, a concentração de oxigênio (ao final do processo, o teor de<br />
oxigênio é ~0,9 [%]) e, na abcissa, o teor de enxofre.<br />
[S] [%] [O] [%] [S] [%] [O] [%]<br />
0.01 0.4<br />
0.025 0.6<br />
0.07 0.8<br />
0.2 1<br />
4) Ajustando-se o valor da constante para reproduzir valores mostrados por Habashi, para a<br />
temperatura de 1400°C, encontramos K' = 0,06 . Qual é o novo teor de enxofre final, se a<br />
temperatura do refino à <strong>fogo</strong> subir até esse valor (Use, também, o quociente entre os valores<br />
encontrados, para ter uma idéia da grandeza da mudança!)<br />
5) Para o aço, mais valores fundamentais são conhecidos. Para a equação (Guthrie):<br />
½ O 2 (g) = O(%) ,<br />
∆G° = -28000-0,69T ,<br />
com T em [°C]; use a equação ∆G° = f(T), T em [K], e faça um diagrama concentração de [O] [%]<br />
em função da pressão de O 2 (g). Note que, se [O] = 0,226%, a atividade da FeO = 1.<br />
6) Numa escória básica, a atividade da sílica pode ter um valor muito menor do que a unidade. Isso<br />
pode afetar fortemente o teor da impureza Si durante o refino à <strong>fogo</strong>. Compare os teores mínimos<br />
de Si [%] no aço, à 1600°C, para 0,02 [%] de [O] dissolvido no aço, quando o valor da atividade<br />
da escória for igual à 1 e 0,01 , sabendo que (Ros. p. 385.):<br />
a SiO<br />
[ Si] ⋅[ ] 2<br />
⋅ 2,8E<br />
− 5 = O .<br />
2<br />
7) Sob condições fortemente oxidantes, também o metal base pode se oxidar. No caso do cobre, há<br />
a formação de Cu 2 O, com a cor vermelho-telha. Estude o fenômeno usando dados para o<br />
manganês dissolvido no aço à 1600°C (Ros. p. 386.). Construa - num único gráfico - o teor de<br />
[O] [%] em função do teor de [Mn] [%], contemplando duas situações: a) oxidação de apenas o<br />
Mn:<br />
0 ,047 = [ Mn] ⋅[ O]<br />
.<br />
b) oxidação do Fe junto com o Mn, formando uma escória:<br />
0 ,074 = [ Mn] ⋅[ O] + 0, 33[ O]<br />
.<br />
Use como valor mínimo de oxigênio: 0,05 [%]; observe o comportamento do Mn à medida que o<br />
teor de oxigênio aumenta.<br />
8) Quantos Nm 3 de gás natural devem ser soprados em 5 toneladas de cobre, após o refino à <strong>fogo</strong>,<br />
para reduzir o teor de oxigênio para 0,05 [%], considerando um rendimento no processo de<br />
apenas 2/5