Termodinâmica Metalúrgica I Prof. Nestor 1ª Lista de ... - Ufrgs
Termodinâmica Metalúrgica I Prof. Nestor 1ª Lista de ... - Ufrgs
Termodinâmica Metalúrgica I Prof. Nestor 1ª Lista de ... - Ufrgs
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Termodinâmica Metalúrgica I<br />
<strong>Prof</strong>. <strong>Nestor</strong><br />
1ª <strong>Lista</strong> <strong>de</strong> exercícios<br />
1. Sabe-se, da observação, que o quociente V/n (consi<strong>de</strong>rando os gases i<strong>de</strong>ais)<br />
apresenta um valor constante. Dê um exemplo da ‘vida real’ que <strong>de</strong>monstre isso.<br />
2. Sabe-se, da observação, que o produto T⋅n (consi<strong>de</strong>rando os gases i<strong>de</strong>ais) apresenta<br />
um valor constante. Dê um exemplo da ‘vida real’ que <strong>de</strong>monstre isso.<br />
3. O coeficiente isobárico <strong>de</strong> expansão térmica dos gases, α, (expansivida<strong>de</strong> térmica<br />
isobárica) é <strong>de</strong>finido por:<br />
⎛ ∂V<br />
⎞<br />
α = 1 ⎜ ⎟ ,<br />
Vo<br />
⎝ ∂T<br />
⎠P<br />
on<strong>de</strong> V o é o volume molar do gás à temperatura <strong>de</strong> 0 [ºC] e pressão P. Henri Victor<br />
Regnault 1 mostrou, em 1847, que, para os gases i<strong>de</strong>ais, α = 1/273.<br />
a) comprove, fazendo um diagrama <strong>de</strong> V como uma função <strong>de</strong> T, com a temperatura<br />
dada em graus Celcius (este diagrama ofereceu a base para a <strong>de</strong>scoberta da escala<br />
absoluta <strong>de</strong> T), com P = cte. b) Depois, divida a equação por V o e comprove<br />
analiticamente que o valor <strong>de</strong> α mencionado acima está correto.<br />
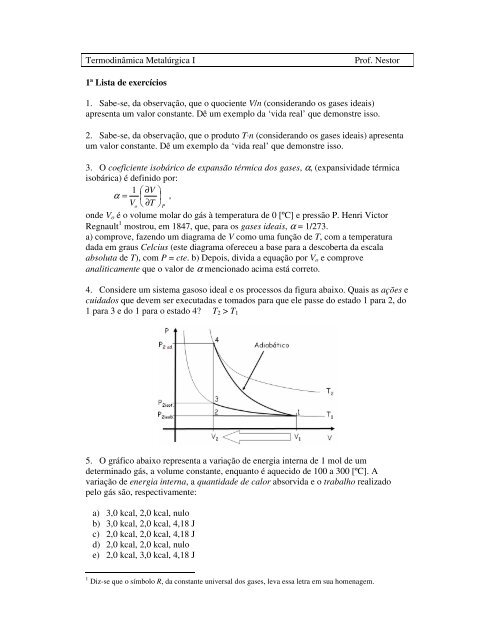
4. Consi<strong>de</strong>re um sistema gasoso i<strong>de</strong>al e os processos da figura abaixo. Quais as ações e<br />
cuidados que <strong>de</strong>vem ser executadas e tomados para que ele passe do estado 1 para 2, do<br />
1 para 3 e do 1 para o estado 4 T 2 > T 1<br />
5. O gráfico abaixo representa a variação <strong>de</strong> energia interna <strong>de</strong> 1 mol <strong>de</strong> um<br />
<strong>de</strong>terminado gás, a volume constante, enquanto é aquecido <strong>de</strong> 100 a 300 [ºC]. A<br />
variação <strong>de</strong> energia interna, a quantida<strong>de</strong> <strong>de</strong> calor absorvida e o trabalho realizado<br />
pelo gás são, respectivamente:<br />
a) 3,0 kcal, 2,0 kcal, nulo<br />
b) 3,0 kcal, 2,0 kcal, 4,18 J<br />
c) 2,0 kcal, 2,0 kcal, 4,18 J<br />
d) 2,0 kcal, 2,0 kcal, nulo<br />
e) 2,0 kcal, 3,0 kcal, 4,18 J<br />
1 Diz-se que o símbolo R, da constante universal dos gases, leva essa letra em sua homenagem.
6. Consi<strong>de</strong>re as afirmativas abaixo, relacionadas aos processos <strong>de</strong> um sistema gasoso<br />
i<strong>de</strong>al mostrados na figura, abaixo:<br />
I - No processo a→c, o sistema realiza trabalho e recebe calor.<br />
II - Os processos a→c e b→c têm a mesma variação <strong>de</strong> energia interna.<br />
III - No processo b→c, o trabalho é nulo e o sistema ce<strong>de</strong> calor à vizinhança.<br />
Entre as alternativas seguintes, a opção correta é:<br />
a) apenas I e III são verda<strong>de</strong>iras<br />
b) apenas II e III são verda<strong>de</strong>iras<br />
c) todas são verda<strong>de</strong>iras<br />
d) apenas I e II são verda<strong>de</strong>iras<br />
e) todas são falsas<br />
7. Certa massa <strong>de</strong> um gás i<strong>de</strong>al sofre as transformações representadas na figura abaixo.<br />
A temperatura, no ponto A, é igual a 300[K]. R = 8,31 [J/mol⋅K]<br />
a) Qual é o número <strong>de</strong> mols do sistema<br />
b) Calcule a temperatura correspon<strong>de</strong>nte ao ponto B.<br />
c) Como se <strong>de</strong>nomina o processo entre os estados B→C<br />
d) Qual é o valor do trabalho líquido<br />
e) Na transformação C→D, a energia interna cresce ou <strong>de</strong>cresce (por quê)
8. O gráfico abaixo ilustra o comportamento <strong>de</strong> duas amostras gasosas (rotuladas<br />
amostra I e amostra II) submetidas a processos isocóricos. Ambas são compostas pelo<br />
mesmo gás, que se comporta i<strong>de</strong>almente. Com base nele, é CORRETO afirmar que:<br />
a) se os volumes das duas amostras são iguais, a amostra I tem maior número <strong>de</strong><br />
mols que a amostra II;<br />
b) se o número <strong>de</strong> mols das duas amostras são iguais, o volume da amostra I <strong>de</strong>ve<br />
ser maior do que o volume da amostra II;<br />
c) tanto a amostra I quanto a amostra II realizam trabalho mecânico sobre o<br />
ambiente quando a temperatura aumenta;<br />
d) para as duas amostras, quanto maior a temperatura, menor a pressão;<br />
e) para as duas amostras vale a afirmação <strong>de</strong> que a variação da energia interna<br />
ocorrida com o aumento da temperatura é menor que o calor recebido do meio<br />
externo.<br />
9. O gás A tem um calor específico molar muito mais elevado que o gás B. Compare,<br />
apenas com base na teoria, o calor absorvido (trocado entre a vizinhança e o sistema)<br />
pelos gases numa mesma expansão isotérmica. Cada sistema tem exatamente o mesmo<br />
número <strong>de</strong> mols.<br />
10. Enunciado idêntico ao do problema anterior. Consi<strong>de</strong>re, no entanto, que o sistema A<br />
tem o dobro do número <strong>de</strong> mols <strong>de</strong> B.<br />
11. Mostre que a variação <strong>de</strong> entalpia <strong>de</strong> uma compressão isotérmica <strong>de</strong> um gás i<strong>de</strong>al é<br />
igual a zero.<br />
12. Desenhe um ciclo <strong>de</strong> Carnot utilizando os eixos P versus V e outro com T versus S.<br />
I<strong>de</strong>ntifique os quatro estados finais dos processos do ciclo como A, B, C e D sobre os<br />
dois diagramas, certificando-se da correta correspondência entre eles. Mostre, no<br />
diagrama T versus S, qual área correspon<strong>de</strong> ao calor absorvido da vizinhança pela<br />
máquina térmica e qual correspon<strong>de</strong> ao calor que é <strong>de</strong>volvido à vizinhança por ela, com<br />
base na equação q = T dS.<br />
13. Explique como se <strong>de</strong>termina a variação da entropia do universo usando para o<br />
raciocínio um sistema e sua vizinhança; Determine (ou indique) o valor <strong>de</strong>sta variação:<br />
(a) com o sistema sofrendo um processo isotérmico reversível, e, (b) com o sistema<br />
sofrendo um processo irreversível.<br />
Respostas para algumas questões:<br />
5 c; 6 a; 8 a