Química Básica - Estrutura - Departamento de Química ...
Química Básica - Estrutura - Departamento de Química ...
Química Básica - Estrutura - Departamento de Química ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
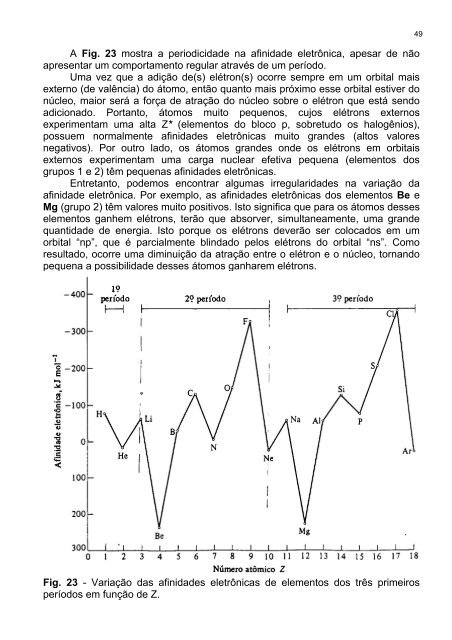
A Fig. 23 mostra a periodicida<strong>de</strong> na afinida<strong>de</strong> eletrônica, apesar <strong>de</strong> não<br />
apresentar um comportamento regular através <strong>de</strong> um período.<br />
Uma vez que a adição <strong>de</strong>(s) elétron(s) ocorre sempre em um orbital mais<br />
externo (<strong>de</strong> valência) do átomo, então quanto mais próximo esse orbital estiver do<br />
núcleo, maior será a força <strong>de</strong> atração do núcleo sobre o elétron que está sendo<br />
adicionado. Portanto, átomos muito pequenos, cujos elétrons externos<br />
experimentam uma alta Z* (elementos do bloco p, sobretudo os halogênios),<br />
possuem normalmente afinida<strong>de</strong>s eletrônicas muito gran<strong>de</strong>s (altos valores<br />
negativos). Por outro lado, os átomos gran<strong>de</strong>s on<strong>de</strong> os elétrons em orbitais<br />
externos experimentam uma carga nuclear efetiva pequena (elementos dos<br />
grupos 1 e 2) têm pequenas afinida<strong>de</strong>s eletrônicas.<br />
Entretanto, po<strong>de</strong>mos encontrar algumas irregularida<strong>de</strong>s na variação da<br />
afinida<strong>de</strong> eletrônica. Por exemplo, as afinida<strong>de</strong>s eletrônicas dos elementos Be e<br />
Mg (grupo 2) têm valores muito positivos. Isto significa que para os átomos <strong>de</strong>sses<br />
elementos ganhem elétrons, terão que absorver, simultaneamente, uma gran<strong>de</strong><br />
quantida<strong>de</strong> <strong>de</strong> energia. Isto porque os elétrons <strong>de</strong>verão ser colocados em um<br />
orbital “np”, que é parcialmente blindado pelos elétrons do orbital “ns”. Como<br />
resultado, ocorre uma diminuição da atração entre o elétron e o núcleo, tornando<br />
pequena a possibilida<strong>de</strong> <strong>de</strong>sses átomos ganharem elétrons.<br />
Fig. 23 - Variação das afinida<strong>de</strong>s eletrônicas <strong>de</strong> elementos dos três primeiros<br />
períodos em função <strong>de</strong> Z.<br />
49