Química Básica - Estrutura - Departamento de Química ...
Química Básica - Estrutura - Departamento de Química ...
Química Básica - Estrutura - Departamento de Química ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
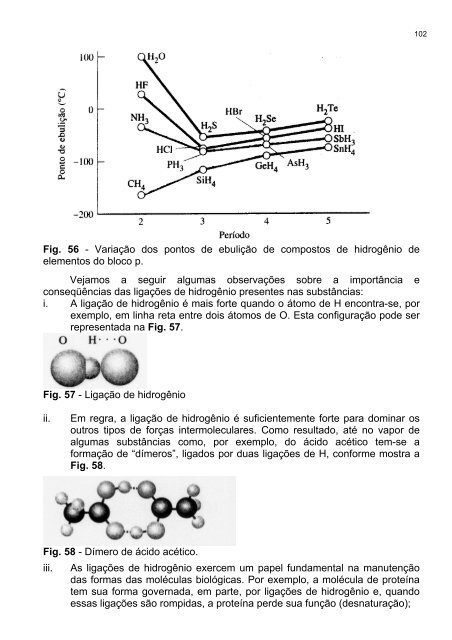
Fig. 56 - Variação dos pontos <strong>de</strong> ebulição <strong>de</strong> compostos <strong>de</strong> hidrogênio <strong>de</strong><br />
elementos do bloco p.<br />
Vejamos a seguir algumas observações sobre a importância e<br />
conseqüências das ligações <strong>de</strong> hidrogênio presentes nas substâncias:<br />
i. A ligação <strong>de</strong> hidrogênio é mais forte quando o átomo <strong>de</strong> H encontra-se, por<br />
exemplo, em linha reta entre dois átomos <strong>de</strong> O. Esta configuração po<strong>de</strong> ser<br />
representada na Fig. 57.<br />
Fig. 57 - Ligação <strong>de</strong> hidrogênio<br />
ii. Em regra, a ligação <strong>de</strong> hidrogênio é suficientemente forte para dominar os<br />
outros tipos <strong>de</strong> forças intermoleculares. Como resultado, até no vapor <strong>de</strong><br />
algumas substâncias como, por exemplo, do ácido acético tem-se a<br />
formação <strong>de</strong> “dímeros”, ligados por duas ligações <strong>de</strong> H, conforme mostra a<br />
Fig. 58.<br />
Fig. 58 - Dímero <strong>de</strong> ácido acético.<br />
iii. As ligações <strong>de</strong> hidrogênio exercem um papel fundamental na manutenção<br />
das formas das moléculas biológicas. Por exemplo, a molécula <strong>de</strong> proteína<br />
tem sua forma governada, em parte, por ligações <strong>de</strong> hidrogênio e, quando<br />
essas ligações são rompidas, a proteína per<strong>de</strong> sua função (<strong>de</strong>snaturação);<br />
102