Doença micronodular difusa
Doença micronodular difusa
Doença micronodular difusa
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Doença</strong> <strong>micronodular</strong> <strong>difusa</strong><br />
Autores<br />
Karin Storrer-Pós-graduanda em doenças intersticiais-UNIFESP-SP<br />
Lilian Kuranishi-Pós-graduanda em doenças intersticiais-UNIFESP-SP<br />
Naienne Stecca-Ex-residente do Serviço dePneumologia da UNIFESP-SP<br />
Rimarcs G Ferreira-Docente, serviço de Anatomia-Patológica-UNIFESP<br />
Cássio Gomes Reis Jr-Radiologista-HSPE-SP.<br />
Carlos AC Pereira-Orientador de PG, <strong>Doença</strong>s Intersticiais-UNIFESP<br />
Caso<br />
Homem, 33 anos, negro, procedente de São Paulo, natural da Bahia, dois filhos,<br />
polidor de ferro. Procurou serviço médico de referência após alteração em exame de<br />
radiografia de tórax, realizado de rotina na empresa. Na ocasião era assintomático do<br />
ponto de vista respiratório, não se queixava de alterações nos diversos aparelhos e<br />
sistemas, não era portador de nenhuma comorbidade e não fazia uso de nenhuma<br />
medicação. Nunca havia fumado e negou contato com pássaros e mofo. Há 12 anos<br />
trabalha polindo peças de ferro com lixadeiras e soldando-as com solda elétrica; faz uso<br />
de máscara facial para proteção, porém não em tempo integral.<br />
Ao exame físico estava em bom estado geral, acianótico, afebril, anictérico,<br />
eupneico, FR= 16 irpm, FC= 78 bpm, PA= 120/80 mmHg, Sat O2=97%, ausculta<br />
pulmonar e cardíaca sem alterações, abdome e membros sem particularidades.<br />
Espirometria com VEF1/CVF: 0,83 (98%), CVF: 4,36 L, (84%), VEF1: 3,61 L<br />
(84%), dentro dos limites da normalidade.<br />
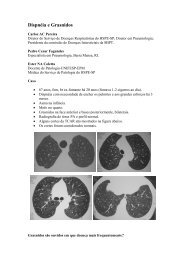
Figura 1.Tomografia de alta resolução
Questão 1. As causas mais comuns de nódulos miliares difusos, dentre as abaixo,<br />
são:<br />
A) Pneumoconioses<br />
B) Carcinoma bronquíolo-alveolar<br />
C) Sarcoidose<br />
D) Tuberculose<br />
E) Metástases<br />
As causas mais comuns de nódulos miliares são: tuberculose e metástases. Micoses<br />
(histoplasmose e raramente paracoccidiodomicose e outras micoses) e sarcoidose<br />
podem dar padrão miliar. As metástases miliares tem como fontes mais comuns o<br />
carcinoma renal, carcinoma de tireóide e o melanoma, lesões altamente vascularizadas.<br />
O carcinoma de tireóide pode resultar em padrão miliar assintomático. Ocasionalmente<br />
a origem das metástases miliares é o próprio pulmão, situação na qual uma lesão maior<br />
é usualmente visível. Em casos de metástases, achados de disseminação pelos linfáticos<br />
e gânglios mediastinais podem ser encontrados.<br />
Alguns casos de sarcoidose um padrão miliar pode ser observado.<br />
O carcinoma bronquíolo-alveolar pode resultar em nódulos de aspecto miliar. Em geral<br />
são de padrão centro-lobular, pela disseminação broncogênica das lesões, e mal-<br />
definidos.<br />
As infecções pulmonares em geral resultam em nódulos pulmonares centrolobulares,<br />
com padrão de árvore em brotamento, porém algumas infecções virais, tais como<br />
pneumonia por varicela, e infecção pelo CMV podem resultar em nódulos miliares. Na<br />
tuberculose miliar, lesões residuais, ou focos de consolidação com ou em cavidades<br />
podem estar presentes. Na tuberculose miliar em não idosos e não hospedeiros
comprometidos, perda de peso, febre e debilidade são esperados. Linfopenia é<br />
freqüente, bem como anormalidades da função hepática, especialmente elevação da<br />
fosfatase alcalina (em torno de 90% dos casos). Esplenomegalia é também comum.<br />
Quando escarro é obtido, a cultura é positiva em torno da metade dos casos. Na<br />
ausência de escarro, broncoscopia com biópsia trans-brônquica poderá revelar<br />
granulomas, com ou sem caseose e com ou sem baciloscpia positiva.<br />
Outras condições que podem resultar em padrão miliar são as pneumoconioses<br />
(pneumoconiose dos trabalhadores do carvão, silicose, siderose), histiocitose de células<br />
de Langerhans, amiloidose e microlitíase alveolar.<br />
As alterações iniciais da silicose são de nódulos de 1-3 mm, bem definidos,<br />
especialmente nas partes posteriores e superiores dos pulmões. Na TC em geral os<br />
nódulos são centrolobulares e perilinfáticos.<br />
Resposta correta: D e E<br />
Questão 2. O padrão tomográfico mostrado corresponde a:<br />
A) Nódulos centrolobulares<br />
B) Nódulos de distribuição perilinfática<br />
C) Nódulos de distribuição randômica<br />
D) Padrão de árvore em brotamento<br />
A radiografia de tórax mostra nódulos pulmonares às vezes mais facilmente do que a<br />
TCAR, por efeito de somação. Entretanto, a TCAR permite localizar os nódulos<br />
pulmonares em sua forma de distribuição (principalmente se simétrica ou assimétrica) e<br />
sua relação com o lóbulo pulmonar secundário. Três padrões são clássicos na<br />
caracterização dos nódulos pulmonares: centrolobular, perilinfático e randômico.<br />
Além disso, os nódulos são classificados em grandes (>1 cm), médios e pequenos ou<br />
micronódulos (≤0,3 cm).<br />
O lóbulo pulmonar secundário é a menor porção do pulmão separada por septos<br />
conjuntivos. Nos septos interlobulares encontram-se veias e linfáticos (figura 2). No<br />
centro do lóbulo encontram-se a arteríola e o bronquíolo centrolobular. Proximalmente<br />
ao bronquíolo terminal, e correndo junto ao feixe broncovascular, encontram-se<br />
linfáticos.
Figura 2. Lóbulo pulmonar, com destaque para arteríola e bronquíolo centrolobular, e<br />
linfáticos e vênulas perilobulares.<br />
Os nódulos de distribuição centrolobular, refletem na maioria das vezes doenças<br />
bronquiolares. Estes nódulos situam-se a pequena distância da pleura, mas o contorno<br />
pleural, habitualmente liso na TCAR, não é afetado. Em geral os nódulos centro-<br />
lobulares são de contorno mal-definido, por expressarem processos inflamatórios<br />
bronquiolares. Nas doenças por inalação de poeiras inorgânicas, os nódulos<br />
centrolobulares podem ser bem definidos, como na silicose. Quando os nódulos<br />
centrolobulares são ramificados, o padrão é denominado de árvore em brotamento<br />
(“tree-in-bud”), que expressa em geral bronquiolites infecciosas ou inflamatórias não<br />
infecciosas.<br />
O padrão perilinfático se caracteriza por distribuição dos nódulos ao longo do feixe<br />
broncovascular, nos septos interlobulares e nas regiões subpleurais, onde se situam os<br />
linfáticos. Na TCAR, nódulos situados nas cissuras, refletem o envolvimento dos<br />
linfáticos subpleurais.<br />
O padrão de distribuição randômica, ou ao acaso, expressa o comprometimento de<br />
diversos compartimentos pulmonares, envolvidos aleatóriamente, de modo que se pode<br />
observar nódulos centrolobulares e subpleurais, mas a característica é a distribuição<br />
simétrica e <strong>difusa</strong> de nódulos bem definidos, sem predomínio de envolvimento. Este<br />
padrão reflete em geral doenças de disseminação hematogênica.<br />
Exemplos de distribuição são mostrados abaixo.
A B C<br />
Figura 3. Padrões perilinfático (A), árvore em brotamento (B) e randômico (C).<br />
Um algoritmo para caracterização da distribuição dos nódulos pulmonares é mostrado<br />
abaixo.<br />
No presente caso os nódulos poupam as regiões subpleurais e/ou perifissurais, distam<br />
pequena distância da pleura e em alguns cortes, como no último da figura 1, são mal-<br />
definidos, sendo, portanto, caracterizados como centrolobulares.<br />
Resposta correta: A (nódulos centrolobulares).<br />
Referências<br />
1. Lee KS, Kim TS, Han J, Hwang JH, Yoon JH, Kim Y, Yoo SY. Diffuse<br />
<strong>micronodular</strong> lung disease: HRCT and pathologic findings. J Comput Assist<br />
Tomogr. 1999;23(1):99-106.<br />
2. Nunes H, Brillet PY, Valeyre D, Brauner MW, Wells AU. Imaging in<br />
sarcoidosis.Semin Respir Crit Care Med. 2007;28(1):102-20.
3. Akira M. High-resolution CT in the evaluation of occupational and<br />
environmental disease. Radiol Clin North Am. 2002;40(1):43-59.<br />
4. Akira M, Atagi S, Kawahara M, Iuchi K, Johkoh T. High-resolution CT findings<br />
of diffuse bronchioloalveolar carcinoma in 38 patients. AJR Am J<br />
Roentgenol. 1999;173(6):1623-9.<br />
5. Andreu J, Mauleón S, Pallisa E, Majó J, Martinez-Rodriguez M, Cáceres J.<br />
Miliary lung disease revisited.Curr Probl Diagn Radiol. 2002;31(5):189-97.<br />
6. Raoof S, Amchentsev A, Vlahos I, Goud A, Naidich DP. Pictorial essay:<br />
multinodular disease: a high-resolution CT scan diagnostic algorithm. Chest.<br />
2006;129(3):805-15.<br />
Questão 3. A maioria das fumaças de solda contém:<br />
A) Manganês<br />
B) Cromo<br />
C) Ferro<br />
D) Níquel<br />
E) Silicatos<br />
As soldas de arco elétricas servem para unir metais e ligas que se tornam<br />
macias ou líquidas depois de submetidas a temperaturas elevadas que podem atingir até<br />
12.000°C assim que a eletricidade passa de um condutor ao outro. Este processo produz<br />
substâncias gasosas e poeiras compostas de um conjunto de metais e outras substâncias<br />
químicas volatilizadas dos eletrodos. Os fumos de solda são partículas sólidas muito<br />
finas de óxidos de metais formadas durante o processo de soldagem. Os tipos de<br />
substâncias e as respectivas quantidades que um soldador inala dependem do método de<br />
soldagem, das condições nas quais a soldagem é realizada e dos tipos de metais a serem<br />
soldados. Os componentes primários dos fumos de soldagem são óxidos de metais<br />
usados na manufatura dos eletrodos consumidos durante o processo de soldagem. A<br />
maioria das fumaças geradas contém ferro (80–95%) e manganês (1–15%). Eletrodos<br />
de aço inoxidável são comumente usados na indústria de soldagem e contém cromo<br />
(15–30%) e níquel (5–10%) em adição ao ferro e manganês. Dependendo do processo e<br />
materiais usados, outros elementos podem ser encontrados nos fumos de solda,<br />
incluindo alumínio, zinco, cádmio, cobre, chumbo, fluoretos, sílica, bário, magnésio,<br />
cálcio, estanho, cobalto e berílio.
O processo de soldagem pode ser feito por várias técnicas e equipamentos,<br />
estimando-se que existam mais de 80 tipos de soldagem.<br />
Embora o termo “pulmão da solda” tenha sido usado como sinônimo de siderose, o<br />
termo deve ser evitado, desde que é inespecífico. Pneumoconiose em um soldador pode<br />
representar a resposta a um componente individual, ou o efeito cumulativo de<br />
exposições mistas. Um diagnóstico mais preciso deve ser feito, como siderose,<br />
pneumopatia por metal duro, beriliose, sidero-silicose e outros.<br />
Resposta correta:C<br />
Referências<br />
1. Antonini JM, Lewis AB, Roberts JR, Whaley DA. Pulmonary effects of welding<br />
fumes: review of worker and experimental animal studies. Am J Ind Med.<br />
2003;43(4):350-60.<br />
2. Beckett WS. Welding. In: Harber P, Schenker MB, Balmes JR (eds).<br />
Occupational and environmental respiratory disease, Mosby, St Louis, 196, 704-<br />
717.<br />
3. Meo SA, Al-Khlaiwi T. Health hazards of welding fumes. Saudi Med J. 2003<br />
;24(11):1176-82.<br />
O paciente foi submetido à biopsia pulmonar a céu aberto por toracotomia<br />
direita. O exame anatomopatológico evidenciou achados de siderose (figura 4).<br />
Após o diagnóstico o paciente foi orientado a se afastar da exposição.<br />
Figura 4. Achados anatomopatológicos
Questão 4.Assinale a alternativa correta em relação à siderose pulmonar:<br />
A) Não há fibrose associada<br />
B) A ferritina sérica pode estar elevada<br />
C) Mesmo com o afastamento da exposição a doença não regride<br />
D) O tempo de latência entre início de exposição e doença é menor que cinco anos<br />
E) Deposição de ferro de causa endógena, como na hemossiderose pulmonar,<br />
Comentários<br />
resulta em achados histológicos idênticos à siderose exogena<br />
A siderose pulmonar é uma pneumoconiose causada por inalação de poeiras<br />
contendo óxido de ferro. Embora descrita inicialmente em soldadores de arco elétrico<br />
ocorre em numerosas ocupações: polidores, fundidores, lixadores, extratores de minério<br />
de ferro, produtores de pigmentos naturais contendo óxidos de ferro.<br />
Estudos epidemiológicos apontam prevalências diversas entre os expostos. Em<br />
1978 um estudo com 661 soldadores mostrou prevalência de 3,4%. É aceito um período<br />
mínimo de cinco anos de exposição para o aparecimento das lesões, no entanto o tempo<br />
de latência varia amplamente.<br />
A lesão pulmonar na siderose se deve ao acúmulo de macrófagos carregados de<br />
grânulos de ferro, porém sem espessamento septal ou alveolite e, portanto, a doença é<br />
descrita como uma pneumoconiose benigna em que há pouca incidência de sintomas e<br />
as provas de função pulmonar são próximas dos limites da normalidade. Quando os<br />
sintomas ocorrem a queixa respiratória mais comum é a bronquite, porém uma<br />
associação definitiva entre a solda e asma ocupacional ainda carece de mais estudos.<br />
Alguns estudos relatam que quando a siderose apresenta sintomas pode estar<br />
associada com silicose. No entanto alguns estudos têm mostrado que soldadores de ferro<br />
podem ter fibrose pulmonar sem a coexistência de silicose. Billings e Howard<br />
encontraram aumento da incidência de câncer pulmão e de doença obstrutivas das vias<br />
aéreas, causada por exposição a oxido de ferro e outros agentes. O risco maior estaria<br />
nos indivíduos expostos à mistura de ferro com maiores quantidades de cromo e níquel,<br />
ambos sabidamente carcinogênicos. Em outro estudo de soldadores não se observou<br />
aumento no número de neoplasias pulmonares. Outros fatores confundidores nesta<br />
relação podem ser o tabagismo e exposição simultânea a asbesto.
Há relatos de siderose associada a acúmulo de ferro sérico em pacientes<br />
sem doenças hematológicas que pudessem explicar tal acúmulo, nem história de<br />
múltiplas transfusões ou consumo alcoólico. Aumento da concentração de ferritina<br />
sérica pode vista nestes indivíduos, e o mecanismo para esta elevação envolve<br />
fagocitose das partículas inaladas de ferro pelos macrófagos alveolares, que são<br />
gradualmente transportadas do espaço alveolar para o interstício e deste para o estoque<br />
corporal. Outras causas de elevação da ferritina devem ser excluídas.<br />
A apresentação radiológica mais comumente observada nas radiografias destes<br />
pacientes são micronódulos distribuídos <strong>difusa</strong>mente em ambos os pulmões, que podem<br />
predominar nas regiões peri-hilares. Os nódulos representam acúmulo das partículas de<br />
ferro no macrófagos agregados nos espaços alveolares peribronquiolares e linfáticos<br />
peribroncovasculares. Na TCAR nódulos centrolobulares com ou sem ramificações são<br />
observados na maioria dos casos.<br />
O diagnóstico dever ser feito com história bem documentada de exposição ao<br />
metal e alteração radiológica compatível. Alguns estudos mostram dosagem aumentada<br />
de ferritina no fluido do lavado broncoalveolar, podendo este dado ser útil no<br />
diagnóstico de alguns casos. A biopsia pulmonar deve ser feita em casos de dúvida, e a<br />
principal diferenciação deve ser com a silicose pulmonar.<br />
A biópsia pulmonar revela deposição perivascular e peribronquiolar de pigmento<br />
de ferro. O pigmento, o qual consiste predominantemente de óxido de ferro, típicamente<br />
é marron escuro ou preto, frequentemente com um halo dourado. Siderose deve ser<br />
diferenciada de deposição endógena de ferro, por exemplo, por congestão passiva<br />
crônica, situação na qual numerosos macrófagos estão carregados de hemossiderina.<br />
Embora a hemossiderina e o pigmento de ferro exógeno se corem com o azul da Prússia,<br />
a hemossiderina não tem os centros escuros característicos do óxido de ferro.<br />
O tratamento é o afastamento do trabalhador do local de exposição, ou mudança<br />
de setor. Em alguns casos há reversão completa das lesões. Nos casos em que há<br />
exposição a outras poeiras lesivas, pode haver progressão para formas graves de fibrose.<br />
A prevenção deve ser feita com uso de equipamento proteção individual, radiografias e<br />
espirometrias freqüentes.<br />
Resposta correta:B
Referências<br />
1. Attfield MD, Ross DS. Radiological abnormalities in electric-arc welders. Br J<br />
Ind Med. 1978:35 (2):117-22.<br />
2. Mendes R. <strong>Doença</strong>s profissionais causados por poeira. In:Mendes R. Medicina<br />
do trabalho, doenças profissionais. 1ª Ed. São Paulo: Sarvier, 1980; 218-229.<br />
3. Billings CG, Howar P. Occupational siderosis and welder´s lung: a review.<br />
Monaldi Arch Chest Dis. 1993; 48: 304-314.<br />
4. Danielsen TE, Lang rd S, Andersen A. Incidence of lung cancer among shipyard<br />
welders investigated for siderosis. Int J Occup Environ Health. 1998:4 (2): 85-8.<br />
5. Akira M. Uncommon pneumoconioses: CT and pathologic findings. Radiology<br />
197:403-409, 1995.<br />
6. Yoshi C, Matsuyama T, Takazawa A, et al. Welder´s Pneumoconiosis:<br />
Diagnostic Usefulness of High-resolution Computed Tomography and ferritin<br />
determinations en bronchoalveolar lavage fluid. Int Med. 2002: 41 (12): 111-<br />
117.<br />
7. Capitani E M de, Algranti E.. Outras pneumoconioses. J Bras Pneumol.<br />
2006;32(Supl 2):S72-S7<br />
8. Algranti E, Morrone LC, Morrone N, Furlaneto JA, Garcia RC, Cardoso RS.<br />
Siderose pulmonar por óxido de fero em trabalhadores: uma poeira inerte? Rev<br />
Paul Med.1985;103(5):259-64.<br />
9. Modrykamien A, Christie H, Farver C, Ashton R W. A 38-Year-Old Welder<br />
With Dyspnea and Iron Overload. Chest 2009;136;310-313.<br />
10. Antonini M A, Taylor M D, Zimmer A T, Roberts J R. Pulmonary responses to<br />
welding fumes: role of metals constituents. J Toxicology and Environmental<br />
Health 2003; 67:233-249.<br />
11. Han D, Goo JM, Im JG, Lee KS, Paek DM, Park SH. Thin-section CT findings<br />
of arc-welders’ pneumoconiosis. Korean J Radiol 2000;1:79–83.