prova de 1ª certificação - química geral - Colégio Pedro II - UE Centro
prova de 1ª certificação - química geral - Colégio Pedro II - UE Centro prova de 1ª certificação - química geral - Colégio Pedro II - UE Centro
COLÉGIO PEDRO II U.E. CENTRO DIRETOR: FLÁVIO NORTE 1. Em uma estação de tratamento de água, alguns processos de separação são utilizados a fim de obtermos água potável. Em uma das etapas desse tratamento, é preciso deixar a água em repouso por algumas horas (processo 1) e em outra etapa faz-se a água atravessar camadas de areia com granulações diferentes (processo 2). Identifique, através de seus nomes, os processos 1 e 2. (1,0) 1 ____________________________________________ 2 ___________________________________________ DEPARTAMENTO DE QUÍMICA CHEFE DE DEPARTAMENTO: A.C. BARBOSA COORD. PED. CLEISE PADRÃO PROVA INSTITUCIONAL 1ª CHAMADA - 1ª CERTIFICAÇÃO QUÍMICA PROF: ADRIANA E LUIZ ANTÔNIO 1ª SÉRIE ENS. MÉDIO DATA: 02/ 05/ 2012 ALUNO: Nº: TURMA: Leia atentamente as instruções abaixo: 1. Esta avaliação consta de 8 questões que totalizam 10 pontos e uma TABELA PERIÓDICA com A ORDEM CRESCENTE DE ENERGIA DOS SUBNÍVEIS. 2. Esta avaliação corresponde a 70% do total de pontos obtidos na 1ª certificação. 3. Esta avaliação deverá ser feita TODA A CANETA AZUL OU PRETA (desenvolvimento e resposta). Ao optar por fazê-la a lápis, você estará abrindo mão do seu direito de fazer revisão de correção. 4. Não são permitidos os usos de corretivos e de calculadoras. 5. Questões que necessitem de cálculos, só serão consideradas acompanhadas dos mesmos corretos. 6. A interpretação de cada questão faz parte da avaliação. Os professores NÃO irão às salas para tirar dúvidas. PROCESSO 1 PROCESSO 2 NOTA Página 1 de 6
- Page 2 and 3: 2. Numa entrevista a Revista n°163
- Page 4 and 5: 5. A e B são isótopos. A e C são
- Page 6: ORDEM CRESCENTE DE ENERGIA 1s 2 , 2
COLÉGIO PEDRO <strong>II</strong><br />
U.E. CENTRO<br />
DIRETOR: FLÁVIO NORTE<br />
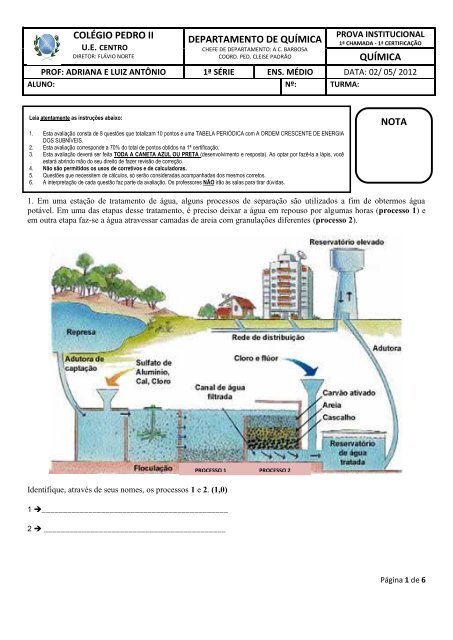
1. Em uma estação <strong>de</strong> tratamento <strong>de</strong> água, alguns processos <strong>de</strong> separação são utilizados a fim <strong>de</strong> obtermos água<br />
potável. Em uma das etapas <strong>de</strong>sse tratamento, é preciso <strong>de</strong>ixar a água em repouso por algumas horas (processo 1) e<br />
em outra etapa faz-se a água atravessar camadas <strong>de</strong> areia com granulações diferentes (processo 2).<br />
I<strong>de</strong>ntifique, através <strong>de</strong> seus nomes, os processos 1 e 2. (1,0)<br />
1 ____________________________________________<br />
2 ___________________________________________<br />
DEPARTAMENTO DE QUÍMICA<br />
CHEFE DE DEPARTAMENTO: A.C. BARBOSA<br />
COORD. PED. CLEISE PADRÃO<br />
PROVA INSTITUCIONAL<br />
<strong>1ª</strong> CHAMADA - <strong>1ª</strong> CERTIFICAÇÃO<br />
QUÍMICA<br />
PROF: ADRIANA E LUIZ ANTÔNIO <strong>1ª</strong> SÉRIE ENS. MÉDIO DATA: 02/ 05/ 2012<br />
ALUNO: Nº: TURMA:<br />
Leia atentamente as instruções abaixo:<br />
1. Esta avaliação consta <strong>de</strong> 8 questões que totalizam 10 pontos e uma TABELA PERIÓDICA com A ORDEM CRESCENTE DE ENERGIA<br />
DOS SUBNÍVEIS.<br />
2. Esta avaliação correspon<strong>de</strong> a 70% do total <strong>de</strong> pontos obtidos na <strong>1ª</strong> <strong>certificação</strong>.<br />
3. Esta avaliação <strong>de</strong>verá ser feita TODA A CANETA AZUL OU PRETA (<strong>de</strong>senvolvimento e resposta). Ao optar por fazê-la a lápis, você<br />
estará abrindo mão do seu direito <strong>de</strong> fazer revisão <strong>de</strong> correção.<br />
4. Não são permitidos os usos <strong>de</strong> corretivos e <strong>de</strong> calculadoras.<br />
5. Questões que necessitem <strong>de</strong> cálculos, só serão consi<strong>de</strong>radas acompanhadas dos mesmos corretos.<br />
6. A interpretação <strong>de</strong> cada questão faz parte da avaliação. Os professores NÃO irão às salas para tirar dúvidas.<br />
PROCESSO 1 PROCESSO 2<br />
NOTA<br />
Página 1 <strong>de</strong> 6
2. Numa entrevista a Revista n°163, um astrofísico brasileiro conta que propôs, em um artigo cientifico, que uma<br />
estrela bastante velha e fria (6.000 K), da constelação <strong>de</strong> Centauro, tem um núcleo quase totalmente cristalizado. Esse<br />
núcleo seria constituído principalmente <strong>de</strong> carbono e a estrela estaria a caminho <strong>de</strong> se transformar em uma estrela <strong>de</strong><br />
diamante, com a cristalização do carbono. O pesquisador relata ter i<strong>de</strong>ntificado mais 42 estrelas com as mesmas<br />
características e afirma: Enquanto não termina o processo <strong>de</strong> cristalização do núcleo, as estrelas <strong>de</strong> diamante<br />
permanecem com a temperatura constante. No que diz respeito à temperatura, in<strong>de</strong>pen<strong>de</strong>ntemente <strong>de</strong> seu valor<br />
absoluto, ele complementa essa afirmação fazendo uma analogia entre o processo que ocorre na estrela e a<br />
solidificação da água na Terra. Com base no conhecimento científico, você concorda com a analogia feita pelo<br />
pesquisador? Justifique. (1,0)<br />
3. Os radioisótopos são utilizados na medicina nuclear para diagnóstico ou terapia, tais como os mostrados na tabela<br />
abaixo:<br />
Radioisótopo Principais usos<br />
Sódio-24 (11Na 24 ) Detecção <strong>de</strong> constrições do sistema circulatório<br />
Cobalto-60 (27Co 60 ) Tratamento do câncer.<br />
Gálio-67 (31Ga 67 ) Varredura do corpo inteiro para i<strong>de</strong>ntificar tumores<br />
Selênio-75 (34Se 75 ) Varredura do pâncreas.<br />
Iodo-131 (53I 131 ) Diagnóstico <strong>de</strong> mau funcionamento da tireoi<strong>de</strong> e tratamento do<br />
câncer tireoidal e do hipertireoidismo.<br />
Mercúrio-197 (80Hg 197 ) Varredura dos rins<br />
Fonte: www.qmcweb.org<br />
a. Através dos cálculos, <strong>de</strong>termine o número <strong>de</strong> partículas <strong>de</strong> carga elétrica neutra do átomo que é utilizado na<br />
varredura <strong>de</strong> i<strong>de</strong>ntificação <strong>de</strong> tumores. (0,5)<br />
b. Um elemento X é isóbaro do radioisótopo utilizado no tratamento do hipertireoidismo e isótopo do radioisótopo<br />
usado na varredura do pâncreas. Qual o número <strong>de</strong> nêutrons do elemento X? (0,75)<br />
Página 2 <strong>de</strong> 6
TEXTO PARA A PRÓXIMA Q<strong>UE</strong>STÃO:<br />
A festa <strong>de</strong> 15 anos da Maria Eduarda foi um arraso! Um final <strong>de</strong> semana inteiro <strong>de</strong> comemoração. Na sextafeira<br />
fomos <strong>de</strong> ônibus para Cabo Frio. Durante a viagem infelizmente o motorista precisou frear bruscamente e por<br />
sorte todos estavam <strong>de</strong> cinto <strong>de</strong> segurança. Passado o susto, todos se divertiram com o comportamento do valentão da<br />
turma, Rutherford, que havia ficado com muito medo e queria sentar no assento que Vanessa já estava sentada. Na<br />
estrada, vimos várias salinas, é muito interessante apren<strong>de</strong>r como se obtém o sal bruto.<br />
No sábado acordamos bem cedo para ir à praia. Dona Joana, mãe da aniversariante, uma dona <strong>de</strong> casa<br />
dinâmica levantou bem cedo e realizou diversas tarefas durante a manhã, fez café e adoçou com açúcar comum<br />
(sacarose), lavou uma dúzia <strong>de</strong> roupas à mão, que ficaram secando ao Sol <strong>de</strong> 40 ºC e preparou para nosso almoço<br />
arroz, separando a sujeira e o refogando, no óleo quente, com alho e cebola.<br />
Maria Cecília aproveitou o sol para dourar os pelos do corpo passando água oxigenada. Bohr e Maria Clara<br />
separaram um monte <strong>de</strong> areia para fazer um castelo <strong>de</strong> areia. Eu aproveitei o sol antes das 10 horas para ficar<br />
bronzeada.<br />
À tar<strong>de</strong> <strong>de</strong>scansamos e à noite fomos para a festa. Havia uma gran<strong>de</strong> pista <strong>de</strong> dança com fumaça branca e<br />
tudo. Dançamos a noite toda. Enfim, a festa foi muito legal!<br />
4. Faça o que se pe<strong>de</strong>:<br />
a. Explique como é o processo <strong>de</strong> obtenção do sal bruto nas salinas. (0,5)<br />
b. Qual seria a classificação da mistura do sal contaminado com areia? (0,25)<br />
c. Cite um método <strong>de</strong> separação <strong>de</strong> misturas para purificar o sal do item anterior. (0,25)<br />
d. Sabendo que a fórmula do açúcar é C12H22O11 .Como o açúcar po<strong>de</strong> ser classificado? (0,25)<br />
e. Qual a mudança <strong>de</strong> estado envolvida em <strong>de</strong>ixar as roupas secando ao Sol? (0,25)<br />
f. Qual o método <strong>de</strong> separação <strong>de</strong> misturas que a dona <strong>de</strong> casa utilizou para preparar o almoço? (0,25)<br />
Página 3 <strong>de</strong> 6
5. A e B são isótopos. A e C são isótonos. B e C são isóbaros. Sabemos ainda que: a soma dos números <strong>de</strong> prótons<br />
existentes em A, B e C é 79, a soma dos números <strong>de</strong> nêutrons existentes em A, B e C é 88 e o número <strong>de</strong> massa <strong>de</strong> A<br />
é 55. I<strong>de</strong>ntifique, utilizando a Tabela Periódica em anexo, os símbolos reais dos elementos aqui representados pelas<br />
letras A, B e C, respectivamente. (1,5)<br />
6. Arqueólogos usam diferença <strong>de</strong> <strong>de</strong>nsida<strong>de</strong> para separar as misturas que obtêm por escavação. Para uma amostra<br />
com a composição abaixo, foram feitas algumas afirmações.<br />
Composição Densida<strong>de</strong> (g / cm 3 )<br />
Afirmações:<br />
Carvão 0,3 – 0,6<br />
Ossos 1,7 – 2,0<br />
Areia 2,2 – 2,4<br />
Solo 2,6 – 2,8<br />
Pedras 2,6 – 5,0<br />
I. Se a mistura acima é adicionada a uma solução que tem <strong>de</strong>nsida<strong>de</strong> <strong>de</strong> 2,1 g/cm 3 , o material correspon<strong>de</strong>nte a<br />
ossos e carvão <strong>de</strong>verá flutuar.<br />
<strong>II</strong>. É possível separar os ossos dos <strong>de</strong>mais componentes usando-se um líquido que tenha <strong>de</strong>nsida<strong>de</strong> no intervalo<br />
<strong>de</strong> 0,6 g/cm 3 a 1,7 g/cm 3 .<br />
<strong>II</strong>I. A utilização da água não é recomendada, pois nesse solvente todos os componentes da mistura afundarão.<br />
IV. Em soluções <strong>de</strong> <strong>de</strong>nsida<strong>de</strong> 2,5 g/cm 3 , a fração da mistura correspon<strong>de</strong>nte à pedra e ao solo flutuará e os <strong>de</strong>mais<br />
afundarão.<br />
V. Líquido <strong>de</strong> <strong>de</strong>nsida<strong>de</strong> 2,2 g/cm 3 separará os componentes pedra e solo dos <strong>de</strong>mais.<br />
Agora, com base nos seus conhecimentos, i<strong>de</strong>ntifique a única afirmação correta. Justifique sua resposta. (1,0)<br />
Página 4 <strong>de</strong> 6
7. Alimentos <strong>de</strong>sidratados são isentos <strong>de</strong> água em sua composição. O processo utilizado na <strong>de</strong>sidratação dos alimentos<br />
é a liofilização que consiste em congelar o alimento a uma temperatura <strong>de</strong> - 197 ºC e <strong>de</strong>pois submeter o alimento<br />
congelado a pressões muito baixas. Nesta temperatura, a água contida no alimento encontra-se no estado sólido e, com<br />
o abaixamento da pressão, passa diretamente para o estado vapor, sendo então eliminada.<br />
No processo <strong>de</strong> liofilização são dadas as seguintes afirmações:<br />
I. A água passa por uma transformação <strong>química</strong>, produzindo H2 e O2, que são gases.<br />
<strong>II</strong>. A água passa por um processo físico conhecido como evaporação.<br />
<strong>II</strong>I. O alimento sofre <strong>de</strong>composição, per<strong>de</strong>ndo água.<br />
IV. A água sofre <strong>de</strong>composição.<br />
V. A água passa por uma transformação física <strong>de</strong>nominada sublimação.<br />
Agora, com base nos seus conhecimentos, i<strong>de</strong>ntifique a única afirmação correta. Justifique sua resposta. (1,0)<br />
8. Um homem <strong>de</strong> 70 kg po<strong>de</strong>rá apresentar, aproximadamente, 2,8 kg <strong>de</strong> sais minerais em seu organismo. A seguir<br />
estão alguns minerais e algumas <strong>de</strong> suas funções no corpo humano.<br />
- Magnésio: ativa as enzimas que participam na síntese das proteínas.<br />
- Zinco: componente das enzimas que participam na digestão.<br />
- Cobre: componente das enzimas associadas ao metabolismo do ferro.<br />
- Potássio: transmissão <strong>de</strong> impulso.<br />
- Cálcio: formação dos ossos e <strong>de</strong>ntes.<br />
- Ferro: compõe a hemoglobina e as enzimas que atuam no metabolismo energético.<br />
(Marta Pires, "Interativida<strong>de</strong> Química". Volume único, 2003 FTD)<br />
Faça a distribuição eletrônica em subníveis e níveis do cátion trivalente do ferro. (1,0)<br />
Página 5 <strong>de</strong> 6
ORDEM CRESCENTE DE ENERGIA<br />
1s 2 , 2s 2 , 2p 6 , 3s 2 , 3p 6 , 4s 2 , 3d 10 , 4p 6 , 5s 2 , 4d 10 , 5p 6 , 6s 2 , 4f 14 , 5d 10 , 6p 6 , 7s 2 , 5f 14 , 6d 10 , 7p 6<br />
Página 6 <strong>de</strong> 6