Efeito da preparação nos sítios de cromo....pdf
Efeito da preparação nos sítios de cromo....pdf Efeito da preparação nos sítios de cromo....pdf
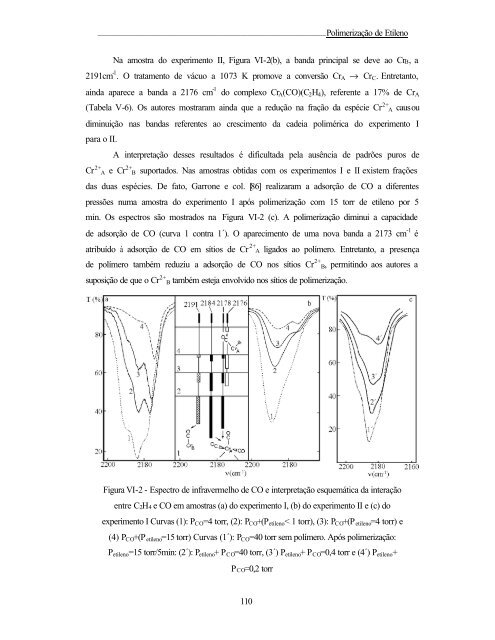
___________________________________________________________________Polimerização de Etileno Na amostra do experimento II, Figura VI-2(b), a banda principal se deve ao CrB, a 2191cm -1 . O tratamento de vácuo a 1073 K promove a conversão CrA → CrC. Entretanto, ainda aparece a banda a 2176 cm -1 do complexo CrA(CO)(C2H4), referente a 17% de CrA (Tabela V-6). Os autores mostraram ainda que a redução na fração da espécie Cr 2+ A causou diminuição nas bandas referentes ao crescimento da cadeia polimérica do experimento I para o II. A interpretação desses resultados é dificultada pela ausência de padrões puros de Cr 2+ A e Cr 2+ B suportados. Nas amostras obtidas com os experimentos I e II existem frações das duas espécies. De fato, Garrone e col. [86] realizaram a adsorção de CO a diferentes pressões numa amostra do experimento I após polimerização com 15 torr de etileno por 5 min. Os espectros são mostrados na Figura VI-2 (c). A polimerização diminui a capacidade de adsorção de CO (curva 1 contra 1´). O aparecimento de uma nova banda a 2173 cm -1 é atribuído à adsorção de CO em sítios de Cr 2+ A ligados ao polímero. Entretanto, a presença de polímero também reduziu a adsorção de CO nos sítios Cr 2+ B, permitindo aos autores a suposição de que o Cr 2+ B também esteja envolvido nos sítios de polimerização. Figura VI-2 - Espectro de infravermelho de CO e interpretação esquemática da interação entre C2H4 e CO em amostras (a) do experimento I, (b) do experimento II e (c) do experimento I Curvas (1): PCO=4 torr, (2): PCO+(Petileno< 1 torr), (3): PCO+(P etileno=4 torr) e (4) PCO+(P etileno=15 torr) Curvas (1´): PCO=40 torr sem polímero. Após polimerização: Petileno=15 torr/5min: (2´): Petileno+ PCO=40 torr, (3´) Petileno+ PCO=0,4 torr e (4´) Petileno+ PCO=0,2 torr 110
___________________________________________________________________Polimerização de Etileno Garrone e col. [86] ressaltam que seus resultados foram obtidos com uma versão simplificada do catalisador Phillips: (i) teor de cromo de 0,5% contra 1% do comercial, (ii) redução com CO ao invés de etileno, (iii) preparo do catalisador com sílica Aerosil, não porosa e (iv) polimerização à 298 K e pressão de 1-20 torr. Embora a escolha de alguns desses parâmetros se deva a restrições experimentais (ii e iv), o preparo de catalisadores mais semelhantes ao industrial ajudará a caracterizar melhor o sítio ativo. Para obter a espécie ativa de cromo, o catalisador pode ser reduzido previamente com CO, com a adição de alquil-alumínio (AlR 3) ou ainda com etileno, in situ. A adição de alquis a catalisadores Cr/SiO2 tem sido reportada na literatura [93, 94, 95, 96]. Segundo Bade e Blom [93], alquis de metais são usados em catalisadores à base de cromato de silila como co-catalisadores (catalisador Union Carbide), de modo a obter suficiente atividade para polimerização e ajustar a distribuição de peso molecular (DPM). No catalisador tipo Phillips, que é pré-ativado com CO, os alquis metálicos são usados para aumentar indiretamente a atividade do catalisador, já que reagem com impurezas do meio reacional e provocam alterações nas propriedades dos polímeros obtidos. Esta última característica está ligada ao tempo de contato do catalisador reduzido com o alquil. Quando o alquil é adicionado ao meio previamente à adição de catalisador, as propriedades do polímero formado pouco são alteradas [95]. Bade e Blom [93] estudaram a modificação de um catalisador Cr/SiO2, à base de CrO3 (1% Cr) reduzido com CO, por adição de t-butil-lítio (t-BuLi) antes da polimerização, numa razão Li/Cr=3,0. Segundo os autores, a adição de t-butil-lítio resulta em maior atividade para polimerização e o polímero formado apresenta menor densidade e peso molecular. As mudanças nas características do polímero foram associadas à formação de dois tipos de sítios ativos: um que é ativo para oligomerização e outro para polimerização. O primeiro seria responsável pela formação de produtos de baixo peso molecular. O segundo tipo se comportaria como um sítio de catalisador Cr/SiO 2 não modificado, produzindo polietileno de alto peso molecular e com baixa sensibilidade ao hidrogênio. McDaniel e Johnson [95] estudaram catalisadores Cr/SiO 2 e Cr/AlPO4 preparados com nitrato de cromo (1% Cr). Os catalisadores foram submetidos à polimerização de etileno a 368 K e pressão de 37 bar, após serem tratados com CO a 623 K, etileno ou trietil-boro (TEB) a 368 K. A Tabela VI-1 apresenta o índice de fusão a alta carga (HLMI, high-load melt index) que varia inversamente com o peso molecular do polímero. A variação do índice de fusão, e, por conseqüência, do peso molecular do polímero é muito 111
- Page 73 and 74: ___________________________________
- Page 75 and 76: ___________________________________
- Page 77 and 78: ___________________________________
- Page 79 and 80: ___________________________________
- Page 81 and 82: ___________________________________
- Page 83 and 84: ___________________________________
- Page 85 and 86: ___________________________________
- Page 87 and 88: ___________________________________
- Page 89 and 90: ___________________________________
- Page 91 and 92: ___________________________________
- Page 93 and 94: ___________________________________
- Page 95 and 96: ___________________________________
- Page 97 and 98: ___________________________________
- Page 99 and 100: ___________________________________
- Page 101 and 102: ___________________________________
- Page 103 and 104: ___________________________________
- Page 105 and 106: ___________________________________
- Page 107 and 108: ___________________________________
- Page 109 and 110: ___________________________________
- Page 111 and 112: ___________________________________
- Page 113 and 114: ___________________________________
- Page 115 and 116: ___________________________________
- Page 117 and 118: ___________________________________
- Page 119 and 120: ___________________________________
- Page 121 and 122: ___________________________________
- Page 123: ___________________________________
- Page 127 and 128: ___________________________________
- Page 129 and 130: ___________________________________
- Page 131 and 132: ___________________________________
- Page 133 and 134: ___________________________________
- Page 135 and 136: ___________________________________
- Page 137 and 138: ___________________________________
- Page 139 and 140: ___________________________________
- Page 141 and 142: ___________________________________
- Page 143 and 144: ___________________________________
- Page 145 and 146: ___________________________________
- Page 147 and 148: ___________________________________
- Page 149 and 150: ___________________________________
- Page 151 and 152: ___________________________________
- Page 153 and 154: ___________________________________
- Page 155 and 156: ___________________________________
- Page 157 and 158: ___________________________________
- Page 159 and 160: ___________________________________
- Page 161 and 162: ___________________________________
- Page 163 and 164: Intensidade (u.a.) ________________
- Page 165 and 166: ___________________________________
- Page 167 and 168: ___________________________________
- Page 169 and 170: ___________________________________
- Page 171 and 172: ___________________________________
- Page 173 and 174: ___________________________________
___________________________________________________________________Polimerização <strong>de</strong> Etileno<br />
Na amostra do experimento II, Figura VI-2(b), a ban<strong>da</strong> principal se <strong>de</strong>ve ao CrB, a<br />
2191cm -1 . O tratamento <strong>de</strong> vácuo a 1073 K promove a conversão CrA → CrC. Entretanto,<br />
ain<strong>da</strong> aparece a ban<strong>da</strong> a 2176 cm -1 do complexo CrA(CO)(C2H4), referente a 17% <strong>de</strong> CrA<br />
(Tabela V-6). Os autores mostraram ain<strong>da</strong> que a redução na fração <strong>da</strong> espécie Cr 2+ A causou<br />
diminuição nas ban<strong>da</strong>s referentes ao crescimento <strong>da</strong> ca<strong>de</strong>ia polimérica do experimento I<br />
para o II.<br />
A interpretação <strong>de</strong>sses resultados é dificulta<strong>da</strong> pela ausência <strong>de</strong> padrões puros <strong>de</strong><br />
Cr 2+ A e Cr 2+ B suportados. Nas amostras obti<strong>da</strong>s com os experimentos I e II existem frações<br />
<strong>da</strong>s duas espécies. De fato, Garrone e col. [86] realizaram a adsorção <strong>de</strong> CO a diferentes<br />
pressões numa amostra do experimento I após polimerização com 15 torr <strong>de</strong> etileno por 5<br />
min. Os espectros são mostrados na Figura VI-2 (c). A polimerização diminui a capaci<strong>da</strong><strong>de</strong><br />
<strong>de</strong> adsorção <strong>de</strong> CO (curva 1 contra 1´). O aparecimento <strong>de</strong> uma nova ban<strong>da</strong> a 2173 cm -1 é<br />
atribuído à adsorção <strong>de</strong> CO em <strong>sítios</strong> <strong>de</strong> Cr 2+ A ligados ao polímero. Entretanto, a presença<br />
<strong>de</strong> polímero também reduziu a adsorção <strong>de</strong> CO <strong>nos</strong> <strong>sítios</strong> Cr 2+ B, permitindo aos autores a<br />
suposição <strong>de</strong> que o Cr 2+ B também esteja envolvido <strong>nos</strong> <strong>sítios</strong> <strong>de</strong> polimerização.<br />
Figura VI-2 - Espectro <strong>de</strong> infravermelho <strong>de</strong> CO e interpretação esquemática <strong>da</strong> interação<br />
entre C2H4 e CO em amostras (a) do experimento I, (b) do experimento II e (c) do<br />
experimento I Curvas (1): PCO=4 torr, (2): PCO+(Petileno< 1 torr), (3): PCO+(P etileno=4 torr) e<br />
(4) PCO+(P etileno=15 torr) Curvas (1´): PCO=40 torr sem polímero. Após polimerização:<br />
Petileno=15 torr/5min: (2´): Petileno+ PCO=40 torr, (3´) Petileno+ PCO=0,4 torr e (4´) Petileno+<br />
PCO=0,2 torr<br />
110