Leerfiches chemie 3 FRWET 2012-2013
Leerfiches chemie 3 FRWET 2012-2013
Leerfiches chemie 3 FRWET 2012-2013
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Naam : __________________________________<br />
Klas : ___________________________
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
0. Een woordje uitleg bij de LPF <strong>chemie</strong><br />
Wat zijn leerfiches en hoe werk je ermee?<br />
1. De leerfiches (LPF) <strong>chemie</strong> zijn een reeks opdrachten, vragen en oefeningen die je dit jaar<br />
moet oplossen, beantwoorden en maken en waarmee je het volledige leerplan voor <strong>chemie</strong><br />
afwerkt (behalve de leerlingenproeven). Aan de leerfiches werk je tijdens het zelfstandig<br />
werk (ZW) of thuis. Je mag er natuurlijk ook tijdens de pauzes aan doorwerken.<br />
2. De leerfiches staan niet op zich alleen! Bij alle hoofdstukken (behalve het eerste hoofdstuk<br />
over veiligheid) horen experimenten in het labo, klasdiscussies en herhalingslessen. Een<br />
aantal experimenten zul je trouwens zelf uitvoeren. Bij die proefnemingen schrijf je telkens<br />
ook een verslag. Het labowerk en de leerfiches vormen dus één geheel.<br />
DRIE GULDEN REGELS<br />
1. Vul de leerfiches zelfstandig in. Samenwerken mag, afschrijven mag niet!<br />
Ga op zoek naar de antwoorden en maak de oefeningen zonder eerst naar de oplossing<br />
te kijken 1 . Als je de fiches op die manier invult, zul je daarna maar weinig moeten<br />
“blokken” voor <strong>chemie</strong>.<br />
2. Houd de ingevulde fiches goed bij in je portfolio.<br />
3. Laat je door anderen helpen: vraag om uitleg! Vraag eerst je medeleerlingen om hulp,<br />
daarna de leraar.<br />
Alle URL’s (webadressen) op deze fiches vind je ook op http://www.mathima.be/<strong>chemie</strong>-2u.html.<br />
Dat is handig: je hoeft de webadressen niet over te tikken. (Dit geldt NIET voor de verwijzingen naar<br />
de CD Elementaire Chemie).<br />
1 De juiste oplossing of het juiste antwoord zul je vaak ook zelf moeten opzoeken in het leerboek Explosief 1.2.<br />
of op de CD-rom Elementaire Chemie.<br />
Chemie <strong>2012</strong>-<strong>2013</strong> 0. Een woordje uitleg bij de LPF <strong>chemie</strong><br />
3 ASO - Freinetschool Villa da Vinci Pagina 1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Hoe werk je met leerfiches?<br />
1. LOS DE VRAGEN EN OPDRACHTEN VAN ELKE FICHE ZELFSTANDIG OP (TENZIJ ANDERS VERMELD).<br />
Om de antwoorden te vinden heb je een hele resem bronnen ter beschikking: de leerboeken in<br />
de klas (bv. Explosief 1.2, Chemie in contexten, Chemie Plus 3), andere boeken in de<br />
klasbibliotheek (bv. ABC van de <strong>chemie</strong>), de CD-rom Elementaire Chemie, het internet (bv.<br />
Wikipedia). Je mag natuurlijk ook zelf naar andere bronnen op zoek gaan!<br />
De leerfiches zijn niet moeilijk. Ze zijn niets anders dan de leerplandoelstellingen, als vraag<br />
geformuleerd. Er zijn dus geen strikvragen bij en je vindt de antwoorden altijd duidelijk (en vaak<br />
bijna letterlijk) in een van de vele beschikbare bronnen.<br />
Voor sommige opdrachten moet je wel zelf op zoek gaan naar een geschikte bron. Vermeld in dat<br />
geval deze bron bij je oplossing.<br />
2. HEB JE TWIJFELS OVER HET JUISTE ANTWOORD? VERGELIJK JOUW ANTWOORDEN MET EEN ANDERE<br />
LEERLING DIE DE FICHES OOK AL OPGELOST HEEFT. BEN JE NOG ALTIJD NIET ZEKER? VRAAG DAN EEN<br />
WOORDJE UITLEG AAN JE LERAAR.<br />
En nu… aan de slag !<br />
Chemie <strong>2012</strong>-<strong>2013</strong> 0. Een woordje uitleg bij de LPF <strong>chemie</strong><br />
3 ASO - Freinetschool Villa da Vinci Pagina 2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
I. Inleiding: <strong>chemie</strong> als wetenschap<br />
1. Chemie als wetenschap<br />
Wat is <strong>chemie</strong> eigenlijk? Wat is het verschil met de fysica? In welke sectoren en beroepen is de<br />
<strong>chemie</strong> belangrijk?<br />
Dit is een (kleine) opzoekopdracht. Je gaat zelf op zoek naar de antwoorden. Je mag gebruik maken<br />
van het internet, boeken (in de klasbib of de openbare bib, of thuis), …<br />
Je mag deze opdracht per tweeën maken. Elke leerling moet de antwoorden wel apart opschrijven.<br />
Opgave : Zoek de antwoorden op deze vragen op. Schrijf je antwoorden op een apart blad en voeg<br />
dit aan je portfolio toe.<br />
Noteer bij elk antwoord de bronnen die je gebruikt hebt!<br />
1) Wat bestudeert de <strong>chemie</strong>?<br />
2) Wat is het verschil tussen <strong>chemie</strong> en fysica?<br />
3) Noem vijf sectoren van de chemische industrie.<br />
4) Noem vijf beroepen die met <strong>chemie</strong> te maken hebben. Geef telkens een kort woordje uitleg.<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Chemie en veiligheid (1) : gevaarlijke stoffen<br />
1.<br />
2.<br />
3.<br />
4.<br />
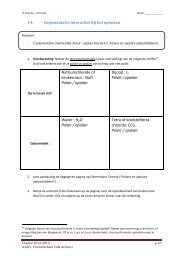
1. Gevaarlijke stoffen vind je op veel plaatsen : in de industrie, in het labo, in de thuisapotheek,<br />
in de keuken enz.. In de EU moeten de fabrikanten van gevaarlijke producten de gevaren<br />
aangeven met de zogenaamde GHS-pictogrammen.<br />
Opgave :<br />
Hieronder vind je de negen GHS-pictogrammen. Zoek (op het internet) op wat elk pictogram<br />
betekent. Schrijf de betekenis achter het pictogram. Geef een woordje uitleg bij de<br />
vaktermen, zodat alle termen voor jou duidelijk zijn. (Je moet van deze negen symbolen de<br />
betekenis kennen!)<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5.<br />
6.<br />
7.<br />
8.<br />
9.<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—3
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Leg de volgende termen uit (geef een synoniem of een verklaring). Zoek de antwoorden zelf<br />
op (internet of woordenboek).<br />
GHS : ________________________________________________<br />
Explosief : ________________________________________________<br />
Corrosief: ________________________________________________<br />
Oxiderend: ________________________________________________<br />
Toxisch : ________________________________________________<br />
3. De oude gevarenpictogrammen waren tot voor kort in voege. Ze zijn vierkant met een<br />
oranjekleurige achtergrond. Op sommige producten kun je deze pictogrammen nog<br />
terugvinden.<br />
Schrijf onder elk pictogram wat het betekent (zoek dit zelf op).<br />
1. 2. 3. 4.<br />
5. 6. 7.<br />
3.1.) Welke pictogrammen bestonden niet in het oude systeem? __________________________<br />
_______________________________________________________________________________<br />
3.2.) Test je kennis : Maak deze zelfevaluatie (met de oude pictogrammen) :<br />
http://www.gortzen.eu/vca/vcatoets3e(gevarensymbolen)/vca3e(gevarensymbolen).htm<br />
Opm. : je moet alleen de nieuwe pictogrammen kennen<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—4
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Chemie en veiligheid (2) : H- en P-zinnen<br />
1. Zoek op wat H- en P-zinnen zijn en geef hieronder telkens een korte omschrijving. Waarvoor<br />
staan de symbolen H en P ?<br />
H-zinnen.<br />
P-zinnen.<br />
Definitie : H –zinnen zijn _______________aanduidingen. De H staat voor<br />
___________________________ (Nederlands: ________________________)<br />
Wat betekent H227 ? ______________________________________________<br />
Wat betekent H330 ? ______________________________________________<br />
Wat betekent H400 ? ______________________________________________<br />
Vroeger sprak men niet van H-zinnen, maar van R-zinnen. R betekent ____________<br />
(Nederlands: ____________________________).<br />
Definitie : P–zinnen geven de te nemen _________________maatregelen aan. De P<br />
staat voor ________________________ (Ned.: ____________________)<br />
Wat betekent P103 ? ______________________________________________<br />
Wat betekent P271 ? ______________________________________________<br />
Wat betekent “H302+P 352” ? ______________________________________________<br />
Wat betekent P410 ? ______________________________________________<br />
De P-zinnen heetten vroeger S-zinnen. S betekent ______________________ (Nederlands:<br />
___________________________ ).<br />
2. Ga naar de website http://www.gortzen.eu/vca/vergiftiging/r_ens_zinnen.htm en los de 21<br />
vragen van de zelftest op. Schrijf je score hieronder (met potlood, tot je het maximum haalt).<br />
Score op de zelftest<br />
Mijn score op de laatst uitgevoerde zelftest : _____/100.<br />
Op veiligheid valt niet af te dingen! Herhaal daarom deze<br />
zelftest tot je 100 % behaalt.<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—5
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. EXTRA: leerrijke online oefeningen/tests over veiligheid en vergiftiging.<br />
1) http://www.gortzen.eu/vca/vergiftiging/gevarensymbolen2.htm<br />
2) http://www.gortzen.eu/vca/vcatoets3b(giftige%20stoffen)/vca3b(gif1).htm (Giftige stoffen,<br />
invuloefening)<br />
3) http://www.gortzen.eu/vca/vcatoets3f(r%20en%20s%20zinnen)/vca3f(rszinnen).htm (R- en<br />
S-zinnen)<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—6
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
4. Chemie en veiligheid (3) : Veiligheid in het laboratorium<br />
Om op de onderstaande vragen de antwoorden gebruik je het “Labo-boek”. Dat krijg je in de klas. Je<br />
vindt het ook online op mathima.be / jaar 3 / <strong>chemie</strong>.<br />
Antwoord kort maar volledig.<br />
1. Welke drie veiligheidsmaatregelen neem je in verband met je kledij wanneer je proeven<br />
uitvoert?<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
2. Wat doe je na elke labosessie, alvorens je het lokaal verlaat?<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
3. A) Wat is de juiste techniek om aan een stof of mengsel te ruiken?<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
B) Wat mag je zeker niet doen?<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—7
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
4. Lees aandachtig de instructies over het gebruik van een bunsenbrander.<br />
a. Geef aan hoe je een bunsenbrander aansteekt (5 stappen).<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
b. Welke veiligheidsvoorschriften moet je in acht nemen in verband met je haar, de<br />
gastoevoer, de juiste opstelling van een proefbuisje boven een bunsenbrander.<br />
Mijn haar: __________________________________________________________________<br />
_______________________________________________________________________<br />
De gastoevoer: ____________________________________________________________<br />
______________________________________________________________________<br />
Proefbuisje boven bunsenbrander:<br />
A) Hoe houd je het proefbuisje? __________________________________________<br />
_____________________________________________________________________<br />
B) Hoe houd je de vloeistof in de vlam?____________________________________<br />
_____________________________________________________________________<br />
5. Waarom mag je nooit een afgesloten fles of kolf verwarmen?<br />
______________________________________________________________________<br />
______________________________________________________________________<br />
6. Waarop moet je letten wanneer je een vloeistof uit een recipiënt giet? Waarom? (tip: etiket)<br />
_____________________________________________________________________<br />
_____________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—8
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
7. EXTRA: een reeks filmpjes over veiligheid (van kakkerlakken verdelgen en explosies tot<br />
whiplash) vind je op http://www.gortzen.eu/vca/vca%20films.html<br />
8. Onderteken het laboreglement en voeg het aan je portfolio toe.<br />
<strong>2012</strong>-<strong>2013</strong> Inleiding: <strong>chemie</strong> als wetenschap<br />
Freinetschool Villa da Vinci I—9
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
II. Stoffen en mengsels<br />
Inleiding : mengsels, zuivere stoffen, scheidingstechnieken<br />
In de <strong>chemie</strong> worden zuivere stoffen onderzocht. Zuivere stoffen zijn stoffen<br />
die zich van andere stoffen onderscheiden door welbepaalde stofeigenschappen<br />
zoals smeltpunt, kookpunt, dichtheid, e.a.<br />
In de natuur vinden we praktisch geen zuivere stoffen, wel mengsels, zodat de<br />
chemicus, vooraleer hij zuivere stoffen kan onderzoeken, de “kunde van het<br />
scheiden” moet beoefenen. Vandaar de benaming schei-kunde als synoniem voor<br />
<strong>chemie</strong> (maar de moderne scheikunde is veel meer dan alleen maar scheikunde!).<br />
Tijdens de eerste weken van het schooljaar zul je in de <strong>chemie</strong>lessen veel leren<br />
over het verschil tussen mengsels en zuivere stoffen, over de verschillende<br />
soorten mengsels, en vooral over de technieken om mengsels in zuivere stoffen<br />
te scheiden. Tijdens deze lessen leer je ook enkele belangrijke laboratoriumtechnieken.<br />
Motivatie<br />
In de <strong>chemie</strong> bestuderen we de eigenschappen van zuivere stoffen. Het is<br />
dan ook belangrijk:<br />
(1) goed het verschil te kennen tussen een zuivere stof en een niet zuivere<br />
stof (een mengsel),<br />
(2) te weten hoe je mengsels in zuivere stoffen kunt scheiden (fysische<br />
scheidingstechnieken)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5. Het onderscheid tussen voorwerpen en stoffen.<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\303_Voorwerpen en stoffen.htm (of klik op: de groene pijl<br />
“Start” 1.2. Mengsels en scheiden van mengsels Voorwerpen en stoffen).<br />
!! Zorg dat je altijd het GROENE LEERPAD volgt op Elementaire Chemie !!<br />
Beantwoord de vragen:<br />
1) Hoe kun je een stof herkennen? ________________________________________________<br />
___________________________________________________________________________<br />
2) Wat is een voorwerp? ________________________________________________________<br />
___________________________________________________________________________<br />
3) Noem tien voorbeelden van stofeigenschappen (nummer elk voorbeeld):<br />
4) Vul de volgende definities aan:<br />
Smeltpunt: _____________________________________________________________<br />
______________________________________________________________________<br />
Kookpunt: _____________________________________________________________<br />
______________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5) Vul telkens “voorwerp”/“voorwerpen” of “stof”/“stoffen” in.<br />
Elk _________________ bestaat uit één of meerdere _____________ . Een ____________<br />
heeft een typische vorm, een bepaald volume en een bepaalde massa.<br />
Een (leeg) cola- of conservenblikje is een _________________ dat bestaat uit de<br />
______________ aluminium of blik. ).<br />
6) Oefening. Stoffen en voorwerpen.<br />
Rangschik volgende stoffen en voorwerpen in de tabel. Verbind de voorwerpen via een lijn<br />
met de stoffen waaruit ze kunnen gemaakt zijn.<br />
suiker – radiator – polypropyleen (een van de vele soorten plastic) – keukenzout – spoorstaaf<br />
– spuitfles – suikerklontje – kookpot – ijzer – emmer – aluminium<br />
Stoffen Voorwerpen<br />
De oplossing vind je op C:\elementaire <strong>chemie</strong>\303_Voorwerpen en stoffen.htm.<br />
7) Herhaling : de aggregatietoestanden.<br />
a) vast, gasvormig of vloeibaar? Wat is de aggregatietoestand van water (H20) bij :<br />
- 20° C : _________________<br />
+3 ° C : _________________<br />
+92 ° C : _________________<br />
+102 ° C : _________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—3
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
b)<br />
STOF SMELTPUNT (°C)<br />
KOOKPUNT<br />
(°C)<br />
ammoniak - 78 - 33<br />
dibroom - 7 59<br />
dichloor - 101 - 35<br />
dijood 113 sublimeert(*)<br />
dizuurstof - 219 - 183<br />
ether - 116 35<br />
looddichloride 501 950<br />
water 0 100<br />
natriumchloride 801 1441<br />
zwavel 112 445<br />
In de bovenstaande tabel vind je het smeltpunt en kookpunt van tien stoffen. Rangschik deze stoffen<br />
in de volgende tabel, rekening houdend met de aggregatietoestand ervan bij kamertemperatuur<br />
(20°C).<br />
VASTE STOF VLOEISTOF GAS<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—4
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
8) Vul in. Kies uit : aggregatietoestanden, verdampen, smeltpunt, gasvormig, verwarmen, vast,<br />
constant, vloeibaar, koken, kookpunt<br />
Een stof kan onder drie vormen (____________________________) voorkomen: ___________,<br />
vloeibaar, ____________________. Wanneer we een vaste stof ___________________, dan zal<br />
die bij een bepaalde temperatuur (= het _________________) ________________ worden.<br />
Wanneer we blijven verwarmen zal de vloeistof bij een bepaalde temperatuur<br />
(=het ____________________) beginnen te ________________ en _____________. Tijdens het<br />
smelten van een zuivere stof blijft de temperatuur ___________________, evenals<br />
tijdens het koken van een zuivere stof.<br />
Oplossing: zie elementaire <strong>chemie</strong>, §1.2., voorwerpen en stoffen<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—5
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
6. Mengsels (1). Mengsels en zuivere stoffen.<br />
Voor deze fiche gebruik je twee bronnen:<br />
C:\elementaire <strong>chemie</strong>\304_Mengsels en zuivere stoffen.htm (of via: Start Stoffen en<br />
mengsels 1.2. : Mengsels en zuivere stoffen)<br />
Handboek Explosief 1.2. p. 15-18<br />
Bekijk aandachtig de filmpjes op Elementaire Chemie en lees de uitleg die erbij staat.<br />
1) Vul vervolgens deze tekst aan:<br />
a) Een m_____________________ is een geheel van met elkaar gemengde stoffen. De<br />
bestanddelen van een mengsel noemen we de c_________________________ .<br />
b) Als je de componenten van een mengsel niet van elkaar kunt onderscheiden, spreken we<br />
van een h_______________________ mengsel (geef één voorbeeld:<br />
_________________________________).<br />
Als je de componenten wel (op het oog of met een microscoop) van elkaar kunt<br />
scheiden, spreken we van een h______________________________ mengsel (geef één<br />
voorbeeld: __________________________________).<br />
2) Wat is het verschil tussen een mengsel en een zuivere stof? We leren dit aan de hand van<br />
enkele voorbeelden.<br />
Opgave: vul de tabel aan (bekijk eerst het voorbeeld : ongefilterd zeewater). Werk eerst met<br />
potlood!<br />
Vb. Ongefiltreerd<br />
zeewater<br />
A<br />
Koffie (zwart,<br />
zonder melk,<br />
zonder suiker)<br />
B Mayonaise<br />
Zuivere<br />
stof<br />
Mengsel Indien mengsel: Homogeen of<br />
heterogeen?<br />
X Heterogeen<br />
(bevat zichtbare zandkorreltjes,<br />
soms plankton, …)<br />
Hoofdbestanddeel<br />
water<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—6
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
C<br />
Gefiltreerd<br />
zeewater<br />
D Witte wijn<br />
E<br />
Inhoud van een<br />
spuitbus met<br />
haarlak<br />
F Jenever<br />
De oplossing (met uitleg) vind je op C:\elementaire <strong>chemie</strong>\Oplossingen\Oefening 1.4.htm.<br />
3) Alle begrepen? Beantwoord dan de zeven meerkeuzenvragen onderaan op de pagina<br />
Mengsels en Zuivere stoffen van Elementaire Chemie (C:\elementaire <strong>chemie</strong>\304_Mengsels<br />
en zuivere stoffen.htm).<br />
Ik heb de zeven meerkeuzenvragen beantwoord (kruis aan).<br />
Lees Explosief 1.2.p. 15-17. Maak vervolgens de opgaven 4 en 5 hieronder.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—7
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
4) Vul de tabel in. Kies uit de volgende woorden:<br />
Kolom (1) : homogeen mengsel, emulsie, mengsel, suspensie, zuivere stof, heterogeen mengsel<br />
Kolom (2) : gedestilleerd water, zout water, kalkmelk, kalkmelk, keukenolie + water (meteen na het<br />
schudden)<br />
Eigenschap<br />
Kun je niet meer scheiden<br />
in componenten (is dus<br />
geen mengsel). Kenmerken<br />
zich door een constant<br />
kook- of smeltpunt.<br />
Mengsel met overal<br />
dezelfde samenstelling. De<br />
componenten zijn dus niet<br />
te onderscheiden.<br />
Mengsel met ongelijkmatig<br />
verdeelde componenten.<br />
Kun je scheiden in<br />
componenten.<br />
Heterogeen mengsel van<br />
een vaste stof en een<br />
vloeistof (de vaste deeltjes<br />
‘hangen’ of ‘zweven’ in de<br />
vloeistof)<br />
Heterogeen mengsel van<br />
twee vloeistoffen<br />
Vul de juiste vakterm in :<br />
Dit is een … (1)<br />
Voorbeeld: (2)<br />
Suikerwater, betonerts, wijn<br />
De verzamelnaam voor zuivere stoffen en mengsels is ____________________ .<br />
De bestanddelen van een mengsel noemen we de _____________________ .<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—8
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5) a) Neem het waarnemingsschema uit Explosief op p. 17 hieronder over.<br />
b) Plaats vervolgens de volgende zes materies op de juiste plaats in het schema:<br />
Spuitwater (= water + kooldioxidegas) – gedemineraliseerd (= gedestilleerd) water<br />
Ongefilterd zeewater - Melk - Rode wijn - Fruitsap<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—9
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
7. Mengsels (2). Fysische scheidingsmethoden.<br />
Je las het al in de inleiding (leerfiche 1) : in de scheikunde interesseren we ons vooral voor de<br />
eigenschappen van zuivere stoffen en de reacties daartussen. Maar hoe verkrijgen we zuivere<br />
stoffen, als we in de natuur bijna overal (homogene en heterogene) mengsels vinden? Het<br />
antwoord luidt: dankzij verschillende scheidingsmethoden (de zogenaamde fysische<br />
scheidingsmethoden).<br />
In deze fiche leer je enkele fysische scheidingsmethoden kennen. Je zult ze in het labo zelf<br />
toepassen.<br />
Opdrachten:<br />
1. Voer de LEERLINGENPROEF “Water: zuivere stof of mengsel?” uit. Dien je onderzoeksverslag in<br />
[noot: deze proeven voeren we in het labo uit].<br />
2. Voer de LEERLINGENPROEVEN uit voor de volgende scheidingstechnieken: scheiden met een<br />
scheitrechter, filtreren (filtratie), extraheren (extractie), chromatografie, adsorptie [noot:<br />
deze proeven voeren we in het labo uit].<br />
Taak <strong>chemie</strong> (10 punten)<br />
Beantwoord de vragen 3-9 op een apart blad. Dien je antwoorden in (taak <strong>chemie</strong> op 10 pt.)<br />
Voeg het verbeterde blad aan je portfolio toe.<br />
Nuttige bronnen:<br />
Explosief 1.2. p. 19-23<br />
Elementaire <strong>chemie</strong>\305_Scheiden van mengsels.htm<br />
3. a) Leg uit: afgieten (decanteren). Hoe pas je deze methode toe?<br />
b) Wanneer kun je deze methode toepassen?<br />
c) Wat is een andere benaming voor “afgieten” of “afschenken”?<br />
d) Met welk toestel kun je de lagen volledig van elkaar scheiden? (+ schets)<br />
4. a) Beschrijf een eenvoudige opstelling voor destillatie (schets + uitleg).<br />
b) Geef de functie van de verschillende onderdelen aan.<br />
c) Geef een voorbeeld van destillatie uit de praktijk.<br />
d) In het labo lieten we een watermengsel (zoutwater of suikerwater) uitkoken, tot alleen het<br />
zout (of de suiker) overbleef. Was dit een voorbeeld van destillatie? Waarom (niet)?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—10
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5. a) Beschrijf een eenvoudige opstelling voor filtratie (schets + uitleg).<br />
b) Benoem de verschillende onderdelen.<br />
c) Geef een voorbeeld van filtratie uit de praktijk.<br />
6. a) Beschrijf de proefopstelling voor extractie (schets + uitleg). Benoem de onderdelen.<br />
b) Geef een voorbeeld van extractie uit de praktijk.<br />
7. Beschrijf hoe je in het labo met adsorptie blauwe inkt gescheiden hebt in een kleurloos<br />
filtraat en een zwart residu. Welke stof heb je daarvoor gebruikt? Hoe ging de adsorptie in<br />
zijn werk?<br />
8. Chromatografie: deze scheidingsmethode oefenen we in het labo in (je leest er meer over in<br />
Explosief 1.2. p. 33).<br />
9. a) Teken de opstelling voor gefractioneerde destillatie.<br />
b) Benoem alle onderdelen.<br />
c) Wanneer kun je deze scheidingsmethode toepassen? (Waaraan moet het mengsel<br />
voldoen?)<br />
d) Geef een voorbeeld van gefractioneerde destillatie in de praktijk.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—11
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
8. Fysische en chemische verschijnselen<br />
In deze korte fiche leer je het verschil tussen de begrippen “fysisch verschijnsel” en “chemisch<br />
verschijnsel”.<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\309_Stoffen en reacties.htm (Start 2 Chemische reacties<br />
2.1. Stoffen en reacties). Bekijk de filmpjes.<br />
1. Leg met je eigen woorden het verschil uit tussen de verhitting van titanium en de<br />
verbranding van magnesium.<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
2. Schrap wat niet past:<br />
Bij een fysisch verschijnsel ontstaan er wel / geen nieuwe stoffen.De optredende<br />
veranderingen zijn blijvend / tijdelijk. Een fysisch verschijnsel kan dus wel / niet ongedaan<br />
maken.<br />
Bij een chemisch verschijnsel (= een chemische reactie) ontstaan wel / geen nieuwe stoffen<br />
en zijn de optredende veranderingen blijvend / tijdelijk.<br />
3. A) Hoe noemen we de stoffen die bij een chemische reactie verdwijnen (dus de stoffen<br />
waarmee je begint) ? De ______________________________.<br />
B) Hoe heten de stoffen die je op het einde van de reactie overhoudt? De<br />
__________________ of ________________________ .<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—12
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
9. Herhaling: het deeltjesmodel (corpusculair model)<br />
Lees C:\elementaire <strong>chemie</strong>\308_Corpusculaire bouw.htm en bekijk alle afbeeldingen en animaties.<br />
1. In de eerste graad leerde je al wat het deeltjesmodel is. Men noemt dit ook het<br />
corpusculaire model van de materie (naar het Latijnse woord corpusculum = lichaampje).<br />
Vul aan en schrap wat niet past:<br />
Alle stoffen bestaan uit ______ _____________ _______________, die we voorlopig<br />
voorstellen als __________________________ . Een zuivere stof bestaat uit __________<br />
soort deeltjes. Een mengsel bestaat uit evenveel deeltjes als er ______________________ in<br />
het mengsel zijn.<br />
Tussen de deeltjes zijn er lege ____________________ ________________ .<br />
De deeltjes worden samengehouden door krachten, de zgn. __________________________ .<br />
De cohesiekrachten zijn het grootst in de vaste / vloeibare / gasvormige aggregatietoestand<br />
en het kleinst in de vaste / vloeibare / gasvormige toestand.<br />
De deeltjes zijn altijd in _________________ (dit noemen we de _________________<br />
beweging).<br />
2. Teken hieronder met het deeltjesmodel :<br />
a. een vaste stof (zuivere stof)<br />
b. een vloeistof (zuivere stof),<br />
c. een gas (zuivere stof).<br />
d. Een gasmengsel (met twee componenten). Zorg dat het verschil tussen de<br />
componenten duidelijk zichtbaar is<br />
a) b)<br />
c) d)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—13
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
10. Het deeltjesmodel : extra-opdracht voor de liefhebbers<br />
Wetenschappers hebben bijna 2000 jaar lang geruzied over de vraag of de wereld<br />
opgebouwd is uit zeer kleine ondeelbare deeltjes (men noemde ze atomen, van het Griekse<br />
a-tomos = ondeelbaar).<br />
Wil je graag meer weten over het ontstaan van het deeltjesmodel? Kies dan één van de<br />
volgende opzoekopdrachten, a of b (je mag natuurlijk ook beide maken!). Dien je werk in, of<br />
stel je bevindingen voor aan de klas. (Extra quotering mogelijk als taak voor DW).<br />
a) Het idee dat de wereld uit kleine, ondeelbare deeltjes is opgebouwd, bestaat al sinds de<br />
Oude Grieken, maar het was tot de 19 e eeuw niet algemeen aanvaard.<br />
- Wat was (al sinds Aristoteles) het grote argument tegen het deeltjesmodel? Met andere<br />
woorden: welke voorstelling, die vanzelf uit het deeltjesmodel volgt, konden<br />
wetenschappers, theologen en filosofen vroeger maar niet aanvaarden? {Als je het antwoord<br />
niet vindt: vraag een tip bij Geert}<br />
- Hoe noemden de Grieken (of toch zij die in een “deeltjesmodel” geloofden) die kleine,<br />
ondeelbare deeltjes? Waarom die benaming?<br />
- In de 19 e eeuw gebruikte de Engelse wetenschapper John Dalton dezelfde benaming voor<br />
de in zijn tijd kleinste deeltjes. Vandaag gebruiken wie die benaming nog altijd. Maar zijn die<br />
deeltjes inderdaad ondeelbaar? Verklaar je antwoord.<br />
b)<br />
– De Schotse plantkundige Robert Brown voerde in 1827 een experiment uit dat het<br />
deeltjesmodel een stevige duw in de rug gaf. Welk experiment was dat? Kunnen we het in<br />
ons labo nabootsen? (Uitdaging voor jou: Wie demonstreert het voor de klas?)<br />
– Vandaag noemt men het door Brown beschreven verschijnsel “Brownse beweging”. Wat is<br />
dat precies? Welke voorbeelden kennen we daarvan in het dagelijks leven? Waarom noemt<br />
men dit fenomeen ook “dronkemanswandeling”?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—14
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
11. Oefeningen : stoffen en mengsels<br />
1. Schrap wat fout is (doordenkertje):<br />
Zuivere stoffen kunnen we van elkaar onderscheiden door hun fysische/chemische<br />
eigenschappen.<br />
2. Los het kruiswoordraadsel “stoffen en mengsels” op de volgende bladzijde op<br />
3. Leg met behulp van het deeltjesmodel uit, waarom zand wel van water gescheiden kan<br />
worden door filtreren, maar zout (of suiker) niet.<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
4. Toepassing (denkvragen). Hoe zou je de volgende mengsels kunnen scheiden?<br />
a. Modder in afvalwater<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
b. Een mengsel van zand en zout<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
___________________________________________________________________________<br />
5. Opzoekvraag. Illustreer met een voorbeeld hoe men chloorgas zowel ten goede als ten<br />
kwade kan toepassen.<br />
6. “Ijzersulfide is een verbinding van ijzer en zwavel.” Leg het begrip “verbinding” uit.<br />
7. Wat is het verschil tussen een fysisch en een chemisch verschijnsel?<br />
8. Juist of fout? “Ijzersulfide is een mengsel van ijzer en zwavel.”<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—15
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
9. Is het ontstaan van sneeuw in een wolk een fysisch of een chemisch verschijnsel? Waarom?<br />
10. Kruis aan of het om fysische of chemische verschijnselen gaat (zoek de optredende<br />
processen op als je twijfelt):<br />
FYSISCH CHEMISCH FYSISCH CHEMISCH<br />
Ijs smelten Voedsel verteren<br />
Boter bruinen Roesten<br />
Water koken Papier verbranden<br />
Koffie<br />
Mayonaise bereiden<br />
extraheren<br />
Groenten<br />
diepvriezen<br />
Vlees bakken<br />
De oplossingen vind je op mathima.be (geef een seintje aan je leraar als dat nog niet het geval is).<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—16
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en mengsels<br />
Freinetschool Villa da Vinci II—17
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
III. Stoffen en reacties<br />
In hoofdstuk II leerde je het verschil kennen tussen mengsels en zuivere stoffen. Daarnaast leerde je<br />
met welke (fysische) scheidingstechnieken we mengsels in hun componenten kunnen scheiden. Nu<br />
kan de echte <strong>chemie</strong> van start gaan! Immers, in de scheikunde gaat het vanouds in de allereerste<br />
plaats om de reacties die stoffen met elkaar aangaan.<br />
12. Fysische en chemische eigenschappen<br />
Let op : in deze fiche gaat het over het verschil tussen fysische en chemische eigenschappen. Blader<br />
nog eens terug naar fiche 8. Waarover ging het daar? Antwoord: over fysische en chemische<br />
_________________________).<br />
Wat is het verschil tussen verschijnsel en eigenschap? Onthoud:<br />
Als we in de <strong>chemie</strong>les over een “verschijnsel” spreken (fysisch of chemisch), bedoelen we altijd dat<br />
er een verandering optreedt (bv. water kookt en verdampt, een magnesiumlint verbrandt).<br />
Als we het over een “eigenschap” hebben (fysisch of chemisch), stellen we vast dat een stof of een<br />
voorwerp een bepaald kenmerk heeft (bv. “water kookt bij 100 ° C” is een fysische eigenschap van<br />
water, ook al is het koken zelf een fysisch verschijnsel).<br />
Bron: Lees aandachtig Elementaire Chemie 2.1, § Stoffen en reacties (C:\elementaire<br />
<strong>chemie</strong>\309_Stoffen en reacties.htm). Bekijk opnieuw de twee filmpjes en lees de tekst.<br />
1. Leg het verschil uit tussen een fysisch verschijnsel en een chemisch verschijnsel.<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Bij de verbranding van magnesium treedt een verandering van de stof op. Schrijf deze reactie<br />
hieronder in korte vorm (dit noemen we een reactieschema) :<br />
_______________________ + ____________________ _____________________ .<br />
Vul aan. Kies uit: eindproduct, magnesiumoxide, reactieproduct, uitgangsproduct<br />
Bij de bovenstaande reactie is een nieuwe stof ontstaan, namelijk _____________________ .<br />
De ________________________ magnesium en zuurstofgas (of dizuurstof, O2) zijn<br />
verdwenen. Het ___________________ of ______________________ is magnesiumoxide.<br />
3. Duid in het reactieschema hierboven aan met een pijl : uitgangsproducten, eindproduct of<br />
reactieproduct.<br />
4. Schrap wat fout is :<br />
“Zuivere stoffen kun je van elkaar onderscheiden door hun fysische eigenschappen / chemische<br />
eigenschappen, zoals het smeltpunt of het kookpunt.”<br />
5. Geef nog drie voorbeelden van fysische eigenschappen (naast smeltpunt/kookpunt).<br />
___________________________________________________<br />
___________________________________________________<br />
___________________________________________________<br />
ZELFEVALUATIE MENGSELS EN ZUIVERE STOFFEN (5 vragen) : Klik hier.<br />
(http://project.kahosl.be/<strong>chemie</strong>/basiscursus/oefeningen/basis_reeks_01a.htm#)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
13. Stoffen en reacties<br />
Bronnen: Elementaire <strong>chemie</strong>, deel 2 : chemische reacties (C:\elementaire<br />
<strong>chemie</strong>\309_Stoffen en reacties.htm)<br />
Explosief 1.2. blz. 37 en volgende<br />
1. Wat is een chemische reactie (of een chemisch verschijnsel)? Geef een sluitende definitie.<br />
Een chemische reactie is een verschijnsel_____________________________________________<br />
______________________________________________________________________________<br />
______________________________________________________________________________<br />
2. Een reactieschema is een schematische weergave van een chemische reactie. Geef een<br />
voorbeelden naar keuze van een reactieschema.<br />
Schrijf eventueel de reactie boven de pijl.<br />
Gebruik de volledige benaming van de stoffen (gebruik nog geen symbolen : die voeren<br />
we pas later in).<br />
3. Duid in het reactieschema hierboven aan met een pijltje: uitgangsstof, eindproduct (=<br />
reactieproduct).<br />
4. (Herhaling) Wat is het verschil tussen een chemisch verschijnsel en een fysisch verschijnsel?<br />
Geef telkens ook een voorbeeld<br />
Chemisch verschijnsel (= chemische reactie) :______________________________________<br />
___________________________________________________________________________<br />
Voorbeeld:<br />
Fysisch verschijnsel : _______________________________________________________<br />
Voorbeeld :<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—3
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
14. Analysereacties en synthesereacties<br />
Bronnen:<br />
A<br />
B<br />
1. Wat is een analysereactie?<br />
- C:\elementaire <strong>chemie</strong>\310_Analyse.htm<br />
- C:\elementaire <strong>chemie</strong>\311_Synthese.htm<br />
- Explosief 1.2. Hoofdstuk 11 p. 41 en volgende<br />
a) Een analysereactie (ook kortweg analyse of ________________ genoemd) is een reactie<br />
waarbij ___________________________________________________________________ .<br />
b) Geef een voorbeeld van een analysereactie (met een reactieschema).<br />
2. Wat is een synthesereactie?<br />
a) Een synthesereactie (ook kortweg synthese genoemd) is een reactie waarbij<br />
___________________________________________________________________ .<br />
b) Geef een voorbeeld van een synthesereactie (met een reactieschema).<br />
3. Oefening. Zijn de volgende reacties analyse- of synthesereacties? Noteer telkens ook de<br />
uitgangsstoffen en eindproducten.<br />
De verbranding van<br />
koolstof. Hierbij reageert<br />
koolstof met dizuurstof<br />
(uit de lucht) en er<br />
ontstaat koolstofdioxide.<br />
natrium + dizuurstof <br />
natriumoxide<br />
Analyse<br />
of synthese?<br />
Uitgangsstoffen Eindproducten<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—4
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
C<br />
zwavelzuur water +<br />
zwaveltrioxide<br />
D A + B C + D<br />
E<br />
distikstof + diwaterstof <br />
ammoniak<br />
De oplossing vind je onderaan op C:\elementaire <strong>chemie</strong>\311_Synthese.htm.<br />
SAMENVATTING ANALYSE EN SYNTHESE<br />
Vul aan: analyse; synthese; analyse noch synthese<br />
A + B C _______________________________<br />
A B + C _______________________________<br />
A + B C + D _______________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—5
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
15. Enkelvoudige en samengestelde stoffen<br />
In hoofdstuk II leerde je het verschil kennen tussen mengsels en zuivere stoffen. Je leerde ook<br />
verschillende soorten mengsels kennen.<br />
In deze fiche zul je leren dat ook zuivere stoffen nog verder onderverdeeld worden, namelijk in<br />
enkelvoudige stoffen en samengestelde stoffen.<br />
Lees aandachtig Explosief 1.2. blz. 52-53. Beantwoord vervolgens de onderstaande vragen met<br />
behulp van het samenvattend schema op blz. 53 (dit schema moet je perfect begrijpen en kunnen<br />
uitleggen!).<br />
Aanvullende bron: C:\elementaire <strong>chemie</strong>\312_Enkelvoudig en samengesteld.htm (§ 2.2.)<br />
Vooraf: wat is een molecule?<br />
Vorig jaar leerde je al over atomen en moleculen. Hier volgt een korte herhaling, met als voorbeeld<br />
water (H2O) .<br />
Definitie :<br />
1) Een molecule is het kleinste deeltje van een stof dat nog de chemische eigenschappen van<br />
die stof bezit.<br />
2) Atomen zijn de bouwstenen van moleculen (dit is een<br />
voorlopige definitie – later dit jaar leer je meer over<br />
atomen).<br />
Een watermolecule is een verbinding van waterstof (H) en zuurstof<br />
(O). Elke H2O-molecule bezit, ook al is ze minuscuul, alle chemische<br />
eigenschappen van water.<br />
Elke H2O-molecule bestaat uit twee H-atomen en één O-atoom<br />
(waterstofatomen en zuurstofatomen). Deze atomen hebben ANDERE eigenschappen dan water.<br />
Begrepen? Vul dan de volgende zinnen aan, bij wijze van oefening.<br />
Kies uit: molecule, atomen, atoom<br />
Een _____________________________ koolstofdioxide (CO2) bestaat uit twee<br />
zuurstof_______________ (O) en één koolstof ________________ (C).<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—6
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
1. Neem het schema op blz. 53 over op een apart blad.<br />
(Dit schema moet je goed kennen; je moet ook alle gebruikte termen kennen)<br />
Kruis hier aan als je deze opdracht hebt uitgevoerd:<br />
2. Beantwoord kort de volgende vragen aan de hand van het schema:<br />
a) In welke twee categorieën deelt men de materie in?<br />
b) In welke twee subcategorieën deelt men de zuivere stoffen in?<br />
c) Hoe noemen we de reactie waarbij uit zuivere stoffen een samengestelde stof ontstaat ?<br />
Antwoord: _______________<br />
d) Hoe noemen we de reactie waarbij uit een samengestelde stof zuivere stoffen ontstaan?<br />
Antwoord: _______________<br />
e) Definieer de volgende begrippen:<br />
enkelvoudige stof : ________________________________________________<br />
samengestelde stof: _______________________________________________<br />
atoom : _________________________________________________________<br />
element: ________________________________________________________<br />
3. Leg het verschil uit tussen een mengsel en een samengestelde stof. Geef twee voorbeelden<br />
van elk.<br />
________________________________________________________________________<br />
________________________________________________________________________<br />
________________________________________________________________________<br />
________________________________________________________________________<br />
Twee voorbeelden van mengsels : __________________________________________<br />
Twee voorbeelden van een samengestelde stof: ___________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—7
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
4. Enkelvoudig of samengesteld? Kruis aan.<br />
Stoffen Enkelvoudig Samengesteld<br />
Octazwavel (S8)<br />
Dizuurstof (O2)<br />
IJzersulfide (FeS)<br />
Distikstof (N2)<br />
Natriumchloride (NaCl) of<br />
keukenzout<br />
Dibroom (Br2)<br />
Zinksulfide (ZnS)<br />
Natriumoxide (Na2O)<br />
Oplossing: C:\elementaire <strong>chemie</strong>\312_Enkelvoudig en samengesteld.htm<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—8
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
16. De belangrijkste elementen en hun symbolen<br />
Bronnen:<br />
1. Vul aan (tip: Explosief):<br />
- C:\elementaire <strong>chemie</strong>\313_Atomen-Elementen-Symbolen.htm (hoofdstuk<br />
2.2.)<br />
- Explosief 1.2. p. 53 (onderaan) en p. 54<br />
Er bestaan _____ natuurlijke elementen. Zij vormen de bouwstenen van de natuur. Alle<br />
natuurlijke _____________ zijn uit één of meerdere van deze elementen opgebouwd.<br />
Elk element wordt voorgesteld door een ________________ . De eerste letter van het symbool is<br />
altijd een _____________letter. Eventueel kan een tweede letter volgen. Dat is altijd een<br />
_________ letter.<br />
2. Vul in de kolom op de volgende bladzijde bij elk element het overeenkomstige symbool in.<br />
Let erop dat je de symbolen juist schrijft!<br />
Soms is de Latijnse naam gegeven om je te helpen.<br />
Je moet de symbolen + de (Nederlandse) namen van deze elementen uit het hoofd leren!<br />
3. Zoek ook de Engelse benaming van de elementen op. Wat merk je als je de Nederlandse en<br />
de Engelse en Latijnse benamingen vergelijkt?<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
Tip: Je kunt jezelf met dit tooltje ondervragen (klik op “overhoor online”):<br />
http://www.woordjesleren.nl/questions.php?chapter=64586.<br />
Deze lijst kun je ook naar Wrts exporteren en zelf aanvullen.<br />
Wie er niet genoeg van krijgt, vindt hier een lijstje met nog veel meer elementen:<br />
http://www.woordjesleren.nl/questions.php?chapter=34923<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—9
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
De belangrijkste elementen en hun symbolen:<br />
NAAM SYMBOOL Latijnse naam Engelse naam<br />
Aluminium<br />
Broom<br />
Calcium<br />
Chloor<br />
Fluor<br />
Fosfor<br />
Goud<br />
Helium<br />
IJzer<br />
Jood<br />
Kalium<br />
phosphorus<br />
aurum<br />
ferrum<br />
Koolstof carboneum<br />
Koper cuprum<br />
Kwik hydrargyrum<br />
Lood plumbum<br />
Magnesium<br />
Natrium<br />
Neon<br />
Stikstof nitrogenium<br />
Waterstof hydrogenium<br />
Zilver argentum<br />
Zink<br />
Zuurstof oxygenium<br />
Zwavel<br />
sulfur<br />
De namen van deze elementen (in het Nederlands) en hun symbolen moet je uit het hoofd leren<br />
(de Latijnse benaming niet) en in beide richting kennen: element symbool, symbool element.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—10
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
17. Voorbeelden van chemische reacties: synthese- en analysereacties<br />
Vul deze fiche in NA de les waarbij we in het labo water ontleedden in waterstofgas en zuurstofgas<br />
en ijzer en zwavel synthetiseerden tot ijzersulfide. Je kunt deze fiche ook voorlopig overslaan en de<br />
volgende fiche afwerken.<br />
Lees aandachtig de onderstaande tekst. Schrap wat fout is en vul aan waar nodig.<br />
A) Bij een fysisch / chemisch verschijnsel (zoals verbranding) worden één of meer stoffen omgezet<br />
in één of meer andere stoffen met andere eigenschappen.<br />
Bij een fysisch / chemisch verschijnsel daarentegen (zoals smelten, koken, mengen, breken, …),<br />
ontstaan geen nieuwe stoffen.<br />
B) In het labo leerde je…<br />
1) … dat een mengsel van de zuivere stoffen ijzermetaal (Fe) en zwavel (S) door verhitting<br />
(afgesloten van de lucht) omgevormd kan worden tot een nieuwe samengestelde zuivere<br />
stof : ijzersulfide (chemisch symbool: FeS).<br />
Het ontstaan van ijzersulfide uit ijzer en zwavel is een voorbeeld van een fysische / chemische<br />
reactie.<br />
De reactie is een analysereactie / synthesereactie.<br />
Ijzersulfide is een verbinding / verschijnsel / element.<br />
Vervolledig het reactieschema (in woorden) van de verbinding van ijzersulfide:<br />
ijzer + _________________ ______________________<br />
Het reactieproduct ijzersulfide (FeS) is een zuivere stof / mengsel. Het is enkelvoudig /<br />
samengesteld.<br />
Het kleinste deeltje ijzersulfide dat nog alle fysische eigenschappen van ijzersulfide bezit, dus<br />
één enkele FeS-deeltje, noemen we een element / atoom / molecule.<br />
Ijzersulfide bestaat uit twee elementen / atomen / moleculen : ijzer en zwavel (sulfur).<br />
Elke molecule ijzersulfide (FeS) bestaat uit twee atomen / moleculen : een ijzer__________<br />
en een zwavel_________ .<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—11
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2) … dat we water met een elektrische stroom kunnen ontleden in waterstofgas en<br />
zuurstofgas 2 .<br />
Dit is een voorbeeld van een fysische /<br />
chemische reactie, omdat de fysische<br />
eigenschappen van de uitgangsstoffen<br />
veranderd zijn (bv. smelt- en kookpunt,<br />
aggregatietoestand, dichtheid, kleur,<br />
smaak).<br />
Dit is een voorbeeld van een<br />
analysereactie / synthesereactie.<br />
Schrijf hier het reactieschema : _________________________________________________<br />
In wat nu volgt houden we geen rekening met het zwavelzuur in het water, omdat dit niet<br />
betrokken is bij de chemische reactie (zie de voetnoot).<br />
Het uitgangsproduct van de reactie, gedestilleerd water (H2O), is een zuivere stof /<br />
mengsel. Het is enkelvoudig / samengesteld, want we kunnen het wel / niet ontleden in<br />
andere stoffen.<br />
De reactieproducten waterstofgas (H2) en zuurstofgas (O2) zijn zuivere stoffen / mengsels.<br />
Ze zijn enkelvoudig / samengesteld, want we kunnen ze wel / niet ontleden in andere<br />
stoffen.<br />
Vul in.<br />
Elk(e) m__________________ zuurstofgas (O2) bestaat uit twee a_____________ van het<br />
e________________ zuurstof (O).<br />
2 Aan het water voegden we wat zwavelzuur toe om de elektrische stroom beter te geleiden (zuiver water is<br />
namelijk een slechte geleider). Dit zwavelzuur (H2SO4) neemt niet deel aan de chemische reactie zelf: als we al<br />
het water zouden ontleden, zou het zwavelzuur achterblijven; dat doen we echter niet omdat het zuur de<br />
elektroden zou aantasten<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—12
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
18. Reactieschema en elementvergelijking<br />
Je leerde al wat een reactieschema is en hoe je het opstelt. Tot nu toe gebruikten we daarvoor de<br />
benaming (= in woorden) van de betrokken stoffen en elementen. In de <strong>chemie</strong> gebruikt men liever<br />
de elementsymbolen, omdat ze korter zijn én omdat ze over heel de wereld dezelfde zijn.<br />
Voorbeeld. Voor de synthese van ijzersulfide (uit ijzer en zwavel) geldt:<br />
Reactieschema met woorden: ijzer + octazwavel ijzersulfide<br />
Elementvergelijking: (Fe) + (S) (Fe, S)<br />
Je schrijft dus elke afzonderlijke stof (zuivere of samengestelde stof) tussen haakjes : de zuivere stof<br />
(Fe) en de zuivere stof (S) verbinden zich tot de samengestelde stof (Fe, S).<br />
Maak nu de onderstaande oefening. Je vindt ze ook op de CD “Elementaire <strong>chemie</strong>” (313_Atomen-<br />
Elementen-Symbolen.htm).<br />
Lees aandachtig de beschrijving van het chemisch verschijnsel in de linkerkolom. Je hebt geen<br />
andere informatie nodig om de reactie- en de elementvergelijking op te schrijven.<br />
Chemisch<br />
verschijnsel<br />
De reactie tussen<br />
diwaterstof en<br />
dizuurstof waarbij<br />
water ontstaat.<br />
Water is een<br />
samengestelde<br />
stof en bevat de<br />
elementen<br />
waterstof en<br />
zuurstof.<br />
De analyse van<br />
ammoniak, een<br />
samengestelde<br />
stof die de elementen<br />
stikstof en<br />
waterstof bevat.<br />
Reactieschema (met woorden) Elementvergelijking<br />
diwaterstof + dizuurstof water (H) + (O) (H,O)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—13
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
De synthese van<br />
natriumchloride,<br />
een<br />
samengestelde<br />
stof die de<br />
elementen<br />
natrium en chloor<br />
bevat.<br />
De reactie tussen<br />
diwaterstof en<br />
dichloor waarbij<br />
waterstofchloride<br />
ontstaat.<br />
De reactie tussen<br />
water en<br />
zwaveltrioxide<br />
(samengestelde<br />
stof, bevat de<br />
elementen zwavel<br />
en zuurstof). Bij<br />
deze reactie<br />
ontstaat er<br />
zwavelzuur (=<br />
samengestelde<br />
stof, bevat DRIE<br />
elementen).<br />
Oplossing: zie CD elementaire <strong>chemie</strong>, 313_Atomen-elementen-symbolen.htm<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—14
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
19. Exo- en endo-energetische reacties<br />
Bronnen : Gebruik voor deze LPF best Elementaire <strong>chemie</strong> §2.3. Exo- en endo-energetische reacties<br />
(C:\elementaire <strong>chemie</strong>\314_Exo- en endo-energetische reacties.htm).<br />
Je kunt ook het boek Explosief 1.2 gebruiken (hoofdstuk 19 en vooral blz. 81), maar daarvoor moet<br />
je eigenlijk de verbranding al kennen, die we pas in de volgende fiche leren kennen.<br />
1. Definities. Definieer de volgende begrippen:<br />
Exo-energetische reactie : _____________________________________________________<br />
___________________________________________________________________________<br />
Endo-energetische reactie : _____________________________________________________<br />
___________________________________________________________________________<br />
Zoek nu ook de volgende begrippen op<br />
Exotherme reactie : een reactie waarbij _____________ vrijkomt (de gemeten<br />
temperatuur stijgt).<br />
Endotherme reactie : een reactie waarbij ____________ opgenomen wordt (de<br />
gemeten temperatuur daalt).<br />
2. Wat betekenen de voorvoegsels (prefixen) exo- en endo- ? (tip: woordenboek)<br />
Exo = __________ Endo = ______________<br />
Je weet nu wat exo-energetisch en endo-energetisch betekenen. Prima! Maar weet je ook wat<br />
energie is? Het is een woord dat we in heel verschillende omstandigheden gebruiken (“Ik heb geen<br />
energie meer.” – “Neem toch een energiedrankje!” – “Electrabel is een energieleverancier.” – “Een<br />
bewegend voorwerp heeft kinetische energie.” Enz.) – maar toch vaak zonder dat we precies weten<br />
waarover we het hebben.<br />
De volgende leerfiche is volledig gewijd aan het begrip energie. Je zult verschillende vormen van<br />
energie leren kennen, en ook het verschil tussen energie en warmte.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—15
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
20. Wat is energie?<br />
Definitie: "Energie is de mogelijkheid van een systeem om arbeid te<br />
verrichten.”<br />
Met “systeem” bedoelen we hier bv. een mens, een molecule, een hoeveelheid vloeistof,<br />
een machine, …<br />
Het woord "mogelijkheid" is onderstreept omdat je energie niet per se hoeft op te<br />
gebruiken. Je kunt energie bewaren, bijvoorbeeld in voedsel (in de koelkast) of in een<br />
batterij.<br />
Een belangrijke eigenschap van energie is : je kunt energie nooit<br />
vernietigen, alleen omzetten in andere vormen van energie!<br />
Wanneer je de energie gebruikt hebt, is deze niet weg. Hij gaat alleen in<br />
een andere toestand over.<br />
Wanneer een auto rijdt met de energie uit de benzine wordt deze energie<br />
omgezet in warmte. Hij gaat de lucht in maar is niet echt weg. De<br />
elektrische energie die een lamp uit het stopcontact haalt, verdwijnt niet<br />
maar wordt omgezet in licht (stralingsenergie) en warmte. Energie blijft<br />
dus altijd bestaan!<br />
Energiesoorten<br />
Hoewel het steeds dezelfde energie is, geven we die energie in verschillende<br />
situaties een andere naam. Voor alle energiesoorten geldt: je kunt er iets mee<br />
doen.<br />
Vul in : elektrische energie – magnetische energie – kernenergie -<br />
stralingsenergie – chemische energie – zwaarteënergie – bewegingsenergie -<br />
veerenergie – thermische energie – kinetische<br />
1) _________________: dit is de energie die voorwerpen hebben<br />
die kunnen veren en in gespannen toestand staan. (Als de veer niet<br />
opgespannen is heeft ze dus geen _____________: je moet eerst een andere<br />
energiesoort gebruiken om de veer op te spannen).<br />
2) _________________: dit is de energie die in straling zit. De meeste straling<br />
is trouwens pure energie (bv. licht).<br />
3) ________________: dit is de energie die opgeslagen zit in de moleculen van<br />
een stof. Bij exo-energetische chemische reacties (zoals verbrandingsreacties)<br />
komt deze energie vrij als warmte en stralingsenergie. ________________ zit<br />
bv. in voedsel en brandstoffen.<br />
4) __________________: dit is de energie die voorwerpen hebben die<br />
bewegen. Deze energiesoort wordt ook _____________ energie genoemd.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—16
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5) _____________: dit is de energie die voorwerpen hebben die kunnen vallen.<br />
Je mag zelf bepalen waar je de _______________nul noemt. Meestal is dit op<br />
de grond maar het kan bijvoorbeeld ook de bodem van een kuil zijn (daarover<br />
meer in de fysicalessen).<br />
6) ___________________: dit is de energie die voorwerpen hebben die<br />
elektrisch geladen zijn en waar dus elektrische spanning op staat. Deze energie<br />
zit in spanningsbronnen zoals een batterij en een accu.<br />
7) _____________: dit is de energie die opgeslagen zit in de kernen van<br />
atomen. Bij kernreacties komt deze energie vrij als warmte en stralingsenergie.<br />
8) __________________: dit is de energie die voorwerpen van ijzer, nikkel of<br />
kobalt hebben die zich in de buurt van een magneet bevinden.<br />
9) ___________________: dit is de bewegingsenergie van de moleculen. Deze<br />
neemt toe als de temperatuur stijgt.<br />
Enzovoort. Er zijn nog verscheidene andere energiesoorten.<br />
Bij chemische reacties kan energie onder verschillende vormen<br />
vrijkomen (of bij endo-energetische reacties: opgenomen worden),<br />
zoals:<br />
WARMTE 3 Voorbeeld: verbranding<br />
BEWEGING Voorbeeld: bruistablet in water<br />
GELUID Voorbeeld: bruistablet in water<br />
Een ontploffing is een reactie waarbij (behalve warmte en beweging van deeltjes = kinetische<br />
energie) energie in de vorm van geluid vrijkomt. (Eigenlijk is geluid niets anders dan de<br />
verplaatsing van luchtdeeltjes.)<br />
Het hoeft echter niet altijd een knal te zijn : ook het geluid van sissen of pruttelen wijst erop<br />
dat energie vrijkomt.<br />
LICHT Voorbeeld: verbranding, luminescentie<br />
ELEKTRICITEIT Voorbeeld: batterij of accu<br />
3 Later zul je leren dat warmte energie is die “onderweg” is ten gevolge van een temperatuurverschil en dat<br />
warmte veroorzaakt wordt door de beweging van deeltjes. Warmte is dus geen aparte vorm van energie.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—17
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
21. Verbranding (1)<br />
Bronnen:<br />
- C:\elementaire <strong>chemie</strong>\315_Verbranding.htm (Hoofdstuk 2.4.).<br />
- Explosief 1.2. p. 57 en volgende<br />
1. Wat is een verbranding? (Antwoord zo precies mogelijk!)<br />
2. Geef een voorbeeld dat aantoont dat een ontstekingsbron (bv. een vlam) niet altijd nodig is<br />
om verbranding mogelijk te maken.<br />
3. Welke drie voorwaarden zijn noodzakelijk opdat verbranding mogelijk wordt?<br />
Voorwaarde 1: De stof in kwestie moet brandbaar zijn.<br />
Voorwaarde 2 : _____________________________________________________<br />
Voorwaarde 3 : _____________________________________________________<br />
In Explosief 1.2. vind je deze drie voorwaarden samengevat in een schets. Neem deze schets<br />
hieronder over (tip: driehoek):<br />
4. Is verbranding een exo- of een endo-energetische reactie? Waarom?<br />
Antwoord:<br />
Verbranding is een _____________________________ reactie omdat<br />
________________________________________________________<br />
_______________________________________________________ .<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—18
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5. We maken een onderscheid tussen “snelle verbranding” en “trage verbranding”. Geef van elk<br />
twee voorbeelden (zie Explosief 1.2. hoofdstuk 15):<br />
a) Voorbeelden van snelle verbranding : ________________________________________ en<br />
____________________________________________<br />
b) Voorbeelden van trage verbranding : _________________________________________ en<br />
____________________________________________<br />
6. Leg uit wat er tijdens het roesten van ijzermetaal in een omgekeerde reageerbuis boven<br />
water gebeurt (Explosief 1.2. p. 64).<br />
7. IJzeren voorwerpen roesten. Deze eigenschap vormt een grote beperking voor het gebruik<br />
van ijzer in de techniek of voor het maken van gebruiksvoorwerpen.<br />
Procedé 1 :<br />
Procedé 2 :<br />
Zoek op (internet of klasbibliotheek): welke twee oplossingen laten toe om het element ijzer<br />
toch op grote schaal te gebruiken? Omschrijf kort waaruit elke oplossing bestaat. Noem ook<br />
van beide procedés telkens een nadeel.<br />
Wat? ___________________________________________________________________<br />
Omschrijving? ___________________________________________________________<br />
_______________________________________________________________________<br />
_______________________________________________________________________<br />
Nadeel? ________________________________________________________________<br />
Wat? ___________________________________________________________________<br />
Omschrijving? ___________________________________________________________<br />
_______________________________________________________________________<br />
_______________________________________________________________________<br />
Nadeel? ________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—19
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
22. De samenstelling van lucht<br />
Bronnen:<br />
- C:\elementaire <strong>chemie</strong>\316_Lucht.htm (hoofdstuk 2.4.)<br />
- Explosief 1.2. p. 57 en volgende<br />
1. Wat zijn de twee hoofdbestanddelen van lucht?<br />
Antwoord: Ongeveer 4/5 van de lucht bestaat uit ____________________, ongeveer<br />
1/5 van de lucht bestaat uit _________________________ .<br />
2. Vul aan (zie Explosief 1.2. H 16).<br />
100 % droge lucht is een (schrap wat niet past) mengsel / verbinding van:<br />
1) ___________________________ (_____________ %)<br />
2) ___________________________ (_____________ %)<br />
3) ___________________________ (_____________ %)<br />
4) ___________________________ (_____________ %)<br />
5) ___________________________ (_____________ %)<br />
Welke stoffen kan onzuivere of vervuilde lucht voorts nog bevatten? Geef drie voorbeelden:<br />
1)<br />
2)<br />
3)<br />
3. Welk bestanddeel van lucht is noodzakelijk voor de verbranding? _____________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—20
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
23. Verbranding (2); oxidatie en reductie<br />
Bronnen:<br />
1) Leerfiche 21 Verbranding (1)<br />
2) Handboek Explosief 1.2., blz. 69-70 (2)<br />
3) C:\elementaire <strong>chemie</strong>\317_Oxidatie en reductie.htm (hoofdstuk 2.4). (3)<br />
De meeste antwoorden vind je in de bronnen 2 en 3, maar Elementaire <strong>chemie</strong> is ongetwijfeld<br />
duidelijker en makkelijker (het bevat ook filmpjes van de besproken experimenten).<br />
1. We laten kopermetaal reageren met zuurstofgas (= dizuurstof of O2). Zie het filmpje op<br />
Elementaire Chemie.<br />
Wat neem je waar? ________________________________________________________<br />
_________________________________________________________________________<br />
Geef van deze reactie het reactieschema (in woorden) en de elementvergelijking (met de<br />
symbolen tussen haakjes):<br />
Reactieschema (in woorden):<br />
Elementvergelijking (met symbolen tussen haakjes):<br />
2. Vul de juiste termen in:<br />
a) Een dergelijke reactie, waarbij een element (hier: Cu) zich verbindt met het element<br />
zuurstof (O) noemen we een o_________________reactie 4 .<br />
b) Het eindproduct van zo’n reactie (hier de verbinding (Cu,O) of CuO) noemen we een<br />
o__________________ . In ons voorbeeld gaat het om koper________________ .<br />
c) De omgekeerde reactie, waarbij het element zuurstof aan een verbinding onttrokken<br />
wordt, noemen we een r ____________________reactie of kortweg ________________ .<br />
4 Het gaat hier dus wel degelijk om een verbinding, niet om een mengsel. Wat is het verschil ook weer?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—21
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Thermietreacties bieden een spectaculair voorbeeld van oxidatie<br />
(en reductie). Op http://www.youtube.com/watch?v=iniulPUFrM<br />
vind je de video-opname van een experimenten dat<br />
je zelf waarschijnlijk nooit zult kunnen uitvoeren.<br />
En dit is de reden waarom we dit niet in het schoollabo doen:<br />
http://www.youtube.com/watch?v=qqvQwfH_wGQ (tot 1:30).<br />
Hier verloopt het experiment iets beter:<br />
http://www.youtube.com/watch?v=li7K4DCeFiQ<br />
3. Vul in. Kies uit: zuurstof (2x), oxidatiereactie, natriumoxide, oxide, reductie, geoxideerd,<br />
explosie, gereduceerd, redox-.<br />
Een ___________________ is een verbinding van een element met<br />
_______________ . De reactie waarbij een oxide ontstaat noemen we een<br />
_________________________ .<br />
De omgekeerde reactie noemen we een _________________ : hier wordt<br />
_______________ aan een verbinding (een samengestelde zuivere stof) onttrokken.<br />
In de reactie (Na) + (C, O) -> (Na, O) + (C)<br />
reageren de uitgangsproducten natrium (Na) en koolstofdioxide (CO2) met elkaar en<br />
vormen ________________________ (NaO) en koolstof (C).<br />
Aangezien het element natrium zich met zuurstof verbindt, zeggen we dat het<br />
natrium __________________________ wordt. De koolstofdioxide daarentegen<br />
wordt __________________________ : het zuurstof wordt eraan onttrokken.<br />
Opmerking: Aangezien elke oxidatiereactie met een reductie gepaard gaat<br />
(de zuurstof die aan het met het ene element verbonden wordt, wordt aan<br />
het andere element onttrokken), spreken we ook kortweg van<br />
____________reacties.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—22
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Welk woord gebruiken we voor een extreem snelle verbranding?<br />
Antwoord: Een o_______________ . Dat is een extreem snelle chemische reactie, gekenmerkt door<br />
een grote gas- en warmteontwikkeling, met als gevolg een plotse drukverhoging. Die drukverhoging<br />
kan grote schade aanrichten.<br />
Een ontploffing is dus een zeer snelle exotherme/endotherme reactie (schrap wat niet past).<br />
Zorg dat je de termen uit deze LPF goed begrijpt en kunt toepassen!<br />
4. Onderaan op de pagina C:\elementaire <strong>chemie</strong>\317_Oxidatie en reductie.htm vind je vier<br />
prima oefeningen om deze leerstof in te oefenen!<br />
Opgave: maak deze vier oefeningen. Vul de checklist in.<br />
Checklist<br />
Oxidatie en reductie, oefening 1<br />
Oxidatie en reductie, oefening 2<br />
Oxidatie en reductie, oefening 3<br />
Oxidatie en reductie, oefening 4<br />
Schrijf “OK” als je<br />
de oefening hebt<br />
afgewerkt en<br />
begrepen<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—23
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
24. Verbranding (3) : oefeningen en toepassingen<br />
2<br />
3<br />
1. Waarom is verbranding een chemisch (en geen fysisch) verschijnsel?<br />
Verbranding is een chemisch verschijnsel omdat bij de reactie een nieuwe<br />
_____________________ gevormd wordt, namelijk een o_______________.<br />
2. Branden blussen.<br />
Herlees de drie voorwaarden voor verbranding (leerfiche 21).<br />
Wanneer men een brand wil blussen, tracht men te bereiken dat minstens één van deze<br />
voorwaarden niet meer vervuld is. Geef met een voorbeeld aan, welke blustechniek op welke<br />
voorwaarde inwerkt (voor de voorwaarden 2 en 3). Vul dat in de tabel in:<br />
Voorwaarde voor verbranding Blustechniek<br />
Sommige hardnekkige branden (bv. oliebranden) blust men wel eens met dynamiet. Hoe verklaar je<br />
dat een explosie een vuur kan blussen?<br />
__________________________________________________________________________________<br />
__________________________________________________________________________________<br />
__________________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—24
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Invuloefening<br />
Kies uit (je moet niet alle woorden gebruiken): dizuurstof, endo-, exo-, papier, lucht, zuurstofgas,<br />
energie, fijnverdeelde, ijzer<br />
Verbranding van een stof is een reactie van die stof met ________________ (synoniem:<br />
_______________). Dat is aanwezig in de _______________ .<br />
Bij elke verbrandingsreactie komt ______________ vrij. Daarom is verbranding een<br />
_________-energetische reactie.<br />
We onderscheiden brandbare stoffen (bv. __________) en niet brandbare stoffen (bv.<br />
___________), maar dat onderscheid is niet absoluut: in _________________________ vorm<br />
kan praktisch elke stof branden.<br />
De temperatuur die een stof doet ontbranden noemen we de _________________________<br />
(dit woord staat niet in het lijstje).<br />
4. Los de vijf meerkeuzevragen op Elementaire <strong>chemie</strong> op (je vindt ze op C:\elementaire<br />
<strong>chemie</strong>\Evaluaties\Verbranding.htm).<br />
Schrijf hieronder de nummers van de vragen op waarmee je moeite had (keer later naar deze<br />
vragen terug) :<br />
5. Thermiet. Surf naar http://nl.wikipedia.org/wiki/Thermiet.<br />
a) Wat is thermiet?<br />
____________________________________________________________________________<br />
____________________________________________________________________________<br />
b) Noem drie toepassingen van thermiet<br />
1. __________________________________________________<br />
2. __________________________________________________<br />
3. __________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—25
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
25. Elementvergelijkingen van oxidatie- en reductiereacties.<br />
Je leert in deze LPF hoe je oxidatie- en reductiereacties met een elementvergelijking weergeeft.<br />
Bronnen die je kunt gebruiken:<br />
- Explosief 1.2. p. 68-76<br />
- C:\elementaire <strong>chemie</strong>\317_Oxidatie en reductie.htm<br />
1. Verbranding van enkelvoudige stoffen<br />
a) Hieronder vind je de reactieschema’s voor de verbranding van enkelvoudige stoffen. Schrijf<br />
onder elk reactieschema de juiste elementvergelijking (met haakjes, bv. (Cu) of (Cu,O)).<br />
Vergelijk daarna met de oplossing in Explosief 1.2. p. 69.<br />
i) Kopermetaal + zuurstofgas<br />
( ______) + (________)<br />
ii) Witte fosfor + zuurstofgas<br />
→ koperoxide<br />
→ ( ____, _____ )<br />
→ fosforoxide<br />
_______________________________________________________<br />
iii) IJzermetaal + zuurstofgas<br />
→ ijzeroxide<br />
_______________________________________________________<br />
Bij de bovenstaande oxidatiereacties verbindt een enkelvoudige stof zich met<br />
________________________ en vormt een ________________ .<br />
b) Oefen nu zelf:<br />
i) Schrijf de elementvergelijking voor de verbranding van magnesium:<br />
→<br />
ii) Schrijf de elementvergelijking voor de verbranding van koolstof:<br />
→<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—26
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
c) Oxidatie en reductie.<br />
Herhaling<br />
Wanneer een element zich met zuurstofgas verbindt en een oxide vormt, spreken we dus van<br />
oxidatie. Maar dat zuurstofgas (dizuurstof of O2) moet ergens vandaan komen : het wordt<br />
meestal onttrokken aan een andere verbinding. Die laatste reactie noemen we een<br />
reductiereactie of kortweg reductie (bij de reacties in LPF 23 wordt het zuurstofgas aan de<br />
lucht onttrokken, maar ook andere verbindingen kunnen gereduceerd worden, zoals we<br />
zullen zien).<br />
Omdat oxidatie en reductie altijd samen voorkomen, spreekt men ook kortweg van<br />
“_____________-reacties”<br />
Alvorens we dieper ingaan op oxidatie en reductie grijpen we even vooruit op de leerstof:<br />
Wet van behoud van elementen<br />
In LPF 26 zul je leren dat bij chemische reacties NOOIT elementen 5 ontstaan of verdwijnen. Wel<br />
worden bij chemische reacties elementen anders gegroepeerd :<br />
VOORBEELD<br />
- sommige verbindingen worden verbroken, (H,O) (H), (O)<br />
- andere (nieuwe) verbindingen ontstaan , (Cu,O) + (H) (H,O) + (Cu)<br />
- of enkelvoudige stoffen verbinden zich tot één nieuwe stof (Mg) + (O) (Mg,O)<br />
Dat is dus ook het geval bij oxidatie- en reductiereacties : er verdwijnen geen elementen, er komen<br />
geen nieuwe elementen bij, er worden enkel nieuwe verbindingen gevormd (of bestaande<br />
verbindingen worden ontbonden).<br />
Een voorbeeld van een reductiereactie is de verwarming van koperoxide (Cu, O) en houtskoolpoeder<br />
(C).<br />
Bekijk deze reactie op Elementaire <strong>chemie</strong>, C:\elementaire <strong>chemie</strong>\317_Oxidatie en reductie.htm.<br />
Beantwoord nu de volgende vragen:<br />
1) Schrijf de elementvergelijking (met haakjes) van de reductie van koperoxide met koolstof:<br />
→<br />
5 Ken je het verschil nog tussen ‘element’, ‘stof’, ‘verbinding’, ‘atoom, ‘molecule’?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—27
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2) Vul aan : Een reductie is een reactie waarbij _____________________________<br />
__________________________________________________________________.<br />
3) De stof die het zuurstof aan een ander stof onttrekt noemen we de _________________ . In<br />
deze reactie is dat ____________________ .<br />
4) Bij de reductie van koperoxide door koolstof wordt de koolstof geo_________________,<br />
terwijl het koperoxide gere__________________ wordt. Het koolstof is dus de<br />
r________________ . We noemen deze reactie kortweg een ____________-reactie.<br />
We hebben hier dus tegelijk de oxidatie van _____________ en de reductie van<br />
______________ .<br />
5) Opgave:<br />
a. Neem hieronder de elementvergelijking van deze reactie over (de bruinrode<br />
vergelijking op Elementaire <strong>chemie</strong>).<br />
b. Duid in de reactie met pijlen aan: oxidatie, reductie, oxidator, reductor,<br />
oxidatieproduct, reductieproduct.<br />
Zorg dat je dit schema goed begrijpt!<br />
6) Reactie tussen magnesium en koolstofdioxide. Zie Elementaire <strong>chemie</strong> C:\elementaire<br />
<strong>chemie</strong>\317_Oxidatie en reductie.htm)?<br />
Bekijk het filmpje van de reactie: het is best spectaculair en we kunnen ze in het schoollabo<br />
niet uitvoeren.<br />
Neem de elementvergelijking (met haakjes) over:<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—28
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Wat is er bijzonder bij de reactie tussen magnesium en koolstofdioxide?<br />
Zoek zelf op: wat is droog ijs? Waarvoor wordt het gebruikt?<br />
7) Maak (nogmaals) de vier oefeningen over oxidatie/reductie op C:\elementaire<br />
<strong>chemie</strong>\317_Oxidatie en reductie.htm (onderaan op de pagina).<br />
2. Verbranding van samengestelde stoffen<br />
Lees Explosief 1.2. blz. 74-76. Beantwoord de vragen:<br />
1. Schrijf een algemene elementvergelijking (reactiepatroon) op van de verbranding van een<br />
a) enkelvoudige stof<br />
b) samengestelde stof :<br />
2. Wat is anders bij de verbranding van een samengestelde stof tegenover verbranding van een<br />
enkelvoudige stof?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—29
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
26. Wet van behoud van elementen<br />
Bronnen :<br />
- C:\elementaire <strong>chemie</strong>\319_Behoud van een element.htm (of via start 2.5. Behoud van<br />
een element tijdens een chemische reactie).<br />
- Explosief 1.2. p. 68-71<br />
Lees aandachtig in Elementaire Chemie : C:\elementaire <strong>chemie</strong>\319_Behoud van een element.htm.<br />
Bekijk de video’s van de experimenten en bestudeer de elementvergelijkingen.<br />
a) Onder welke verschillende vormen was het element koper in al deze reacties aanwezig?<br />
(1) ___________ (2) ________________ (3) ________________ (4) __________<br />
b) Welk belangrijk chemisch principe wordt door deze reeks experimenten bevestigd?<br />
(Gebruik Explosief 1.2. p. 70 (kadertje) om te antwoorden)<br />
Tijdens een chemische reactie _________________________________________________<br />
__________________________________________________________________________<br />
__________________________________________________________________________<br />
Dit is de wet van “behoud van elementen”<br />
c) Denkvraag: Wat is het verband tussen het principe van het behoud van elementen en het<br />
deeltjesmodel?<br />
d) De volgende reactie vindt plaats:<br />
Magnesiummetaal + kokend water waterstofgas + magnesiumoxide<br />
i) Geef de elementvergelijking:<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—30
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
ii) Toon het behoud van elementen aan (schrap wat niet past)<br />
Het element Mg : wel behouden / niet behouden<br />
Het element H : wel behouden / niet behouden<br />
Het element O : wel behouden / niet behouden<br />
iii) Duid in de elementvergelijking (met pijlen) de oxidatie en de reductie aan.<br />
e) Opgelet ! De wet van behoud van elementen geldt alleen voor … elementen. Dit mag je niet<br />
verwarren met atomen, moleculen of verbindingen.<br />
We bekijken deze reactie (dezelfde als voorheen):<br />
koper + salpeterzuur koperdinitraat + stikstofdioxide + water<br />
(Cu) + (H,N,O) (Cu,N,O) + (N,O) + (H,O)<br />
Cu + 4 HNO3 Cu(NO3)2 + 2 NO2 + 2 H2O<br />
Vul in.<br />
Kies uit (enkelvoud of meervoud) : elementen, atomen, moleculen (2x), verbindingen (3x).<br />
i) In deze reactie blijven de _________________ Cu, H, N, O steeds bewaard<br />
ii) In deze reactie wordt de _________________ salpeterzuur verbroken<br />
iii) In deze reactie worden de nieuwe ____________________ koperdinitraat,<br />
stikstofoxide en water gevormd.<br />
iv) In deze reactie gaan de _________________ van het koper, waterstof, zuurstof en<br />
stikstof nieuwe _________________________ met elkaar aan.<br />
v) Vóór de reactie zijn __________________ HNO3 aanwezig.<br />
vi) Na de reactie zijn er _____________________ van koperdinitraat, stikstofoxide en<br />
water aanwezig.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—31
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
27. De wet van behoud van massa (wet van Lavoisier)<br />
Bronnen: 1) Elementaire <strong>chemie</strong> (C:\elementaire <strong>chemie</strong>\318_Massabehoud.htm) (of via Start<br />
jaar 3 hoofdstuk 2 2.5. Wet van massabehoud<br />
2) Explosief 1.2. p. 88-93<br />
1) Lees aandachtig de onderstaande tekst.<br />
De wet van behoud van massa<br />
(of: de “wet van Lavoisier”)<br />
Als je in een afgesloten systeem stoffen met elkaar laat reageren, geldt altijd de volgende<br />
regel:<br />
de totale massa vóór de reactie = de totale massa na de reactie<br />
(We praten in dit verband natuurlijk over de massa van de deelnemende stoffen)<br />
Deze wet berust eigenlijk op de resultaten van proefjes. Uit vele experimenten hebben<br />
scheikundigen de wet afgeleid 6 .<br />
-----------<br />
Bij berekeningen aan reacties kun je van deze regel gebruik maken. Als je namelijk van alle<br />
stoffen die aan een reactie deelnemen, op één na de massa kent, dan moet je met deze<br />
regel in het achterhoofd, die onbekende massa kunnen uitrekenen.<br />
De controle van deze wet ligt verscholen in de reactievergelijking. Bij het opstellen van een<br />
reactievergelijking moet je er altijd voor zorgen dat het aantal atomen per atoomsoort voor<br />
reactie even groot is als het aantal atomen per atoomsoort na reactie 7 .<br />
Omdat alle atomen die er voor de reactie al zijn, na de reactie terugkomen, blijft de totale<br />
massa van al die atomen natuurlijk ook even groot.<br />
6 Zo’n wet die uit experimenten is afgeleid, noemt men een “experimentele wet”. Daartegenover staan<br />
“theoretische wetten”, die uit theoretische overwegingen afgeleid zijn (en vervolgens door experimenten<br />
bevestigd worden). Voor de wetenschap zijn beide soorten wetten belangrijk.<br />
7 Dit is een andere manier om te zeggen dat bij chemische reacties nooit nieuwe elementen ontstaan, zie LPF<br />
23 (bij nucleaire reacties kan dat wel gebeuren, maar dus niet bij chemische reacties).<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—32
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Formuleer nu zelf de wet van behoud van massa:<br />
Bij een chemische reactie is ______________________________________________ altijd<br />
gelijk aan _________________________________________________, op voorwaarde dat de<br />
reactie _______________________________________ plaatsvindt.<br />
2) We verduidelijken de wet van behoud van massa met een cijfervoorbeeld:<br />
Stel, 2,5 gram van stof A reageert met 11,4 gram van stof B. Hierbij ontstaat 7,7 gram van stof C en<br />
een onbekende hoeveelheid van stof D. Stof D is namelijk een gas en dus heel moeilijk te wegen.<br />
Veralgemeend reactieschema :<br />
stof A + stof B stof C + stof D<br />
Dankzij de wet van Lavoisier kun je berekenen hoeveel de massa van stof D (het gas) bedraagt (als je<br />
de massa’s van de stoffen A, B en C bepaald hebt).<br />
Vul aan:<br />
Besluit:<br />
stof A stof B stof C stof D<br />
2,5 g 11,4 g 7,7 g ??? g<br />
De totale massa van stof A + stof B = 2,5 g + 11,4 g = ________ g<br />
De totale massa van stof C + stof D = De totale massa van stof A + stof B = ________ g<br />
Dus: 7,7 g + ??? g = 13,9 gram.<br />
De massa van stof D is dus 13,9 g - 7,7 g = ________ gram<br />
Als in een verhoudingstabel voor berekeningen aan reacties alle massa's op één na bekend zijn, dan<br />
kun je de massa van de laatste stof uitrekenen met de wet van behoud van de massa.<br />
(bron: http://www.cybercomm.nl/~boginfo/scheikunde/tutor%203e%20klas/wet-massabehoud.htm)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—33
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3) In het labo zul je experimenten uitvoeren om de wet van behoud van massa zelf te<br />
controleren.<br />
Opdracht: Bereid je op dit leerlingenpracticum voor, door aandachtig blz. 88-89 in Explosief<br />
1.2. te lezen.<br />
4) Afgesloten systeem. Lees aandachtig C:\elementaire <strong>chemie</strong>\318_Massabehoud.htm op<br />
Elementaire Chemie. Beantwoord vervolgens deze vraag:<br />
Waarom geldt de wet van behoud van massa alleen in een afgesloten systeem?<br />
___________________________________________________________________<br />
___________________________________________________________________<br />
___________________________________________________________________<br />
___________________________________________________________________<br />
5) EXTRA opgave (niet verplicht; je mag ze als extra-taak voor <strong>chemie</strong> indienen).<br />
Lees de volgende tekst over de ontdekking van de wet van behoud van massa (bron:<br />
Wikipedia) en beantwoord vervolgens de vragen.<br />
De wet van behoud van massa werd in 1789 geformuleerd door Antoine Lavoisier.<br />
Om deze reden is deze regel ook bekend als de Wet van Lavoisier. Lavoisier wordt<br />
om deze reden vaak gezien als de grondlegger van de moderne scheikunde.<br />
Echter, Michail Lomonosov had al veel eerder (in 1748) soortgelijke beweringen<br />
gedaan en ze in experimenten bewezen. Historisch gezien bleef de wet van behoud<br />
van massa duizenden jaren onbekend door het effect van gassen. Deze verdwenen<br />
ongezien in de atmosfeer (koolstofdioxide bij verbranding), of werden daar ongezien<br />
uit opgenomen (zuurstofbij oxidatie). Dit effect werd niet begrepen totdat<br />
de vacuümpomp als eerste de mogelijkheid gaf gassen te wegen. Eenmaal begrepen,<br />
werd de wet van behoud van massa de sleutel tot de overgang van de al<strong>chemie</strong> naar<br />
de moderne <strong>chemie</strong>. Toen wetenschappers zich realiseerden dat substanties nooit<br />
verdwenen uit metingen, konden ze zich voor de eerste maal bezig gaan houden met<br />
kwantitatieve studies naar de veranderingen van substanties. Deze ommekeer leidde<br />
tot het idee van het bestaan van chemische elementen en het idee dat alle chemische<br />
processen en veranderingen (inclusief vuur en metabolisme) eenvoudige reacties zijn<br />
tussen niet van gewicht veranderende elementen.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—34
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Vragen:<br />
Waarom werd de wet van behoud van massa pas zo laat ontdekt?<br />
Antoine Lavoisier wordt vaak de “grondlegger van de moderne <strong>chemie</strong>” genoemd. Waarom<br />
is dat een controversiële uitspraak?<br />
A) Wat is metabolisme?<br />
B) Wat heeft metabolisme met <strong>chemie</strong> te maken? Geef daarvan een voorbeeld.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—35
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
28. De wet van de constante massaverhouding (wet van Proust)<br />
Bronnen: - Explosief 1.2. p. 91-94<br />
- Elementaire <strong>chemie</strong>: C:\elementaire <strong>chemie</strong>\320_Constante massaverhouding.htm<br />
(of via Start jaar 3 hoofdstuk 2.5)<br />
Lees aandachtig de bronnen (tip: lees eerst “Elementaire Chemie”, dan Explosief 1.2.)<br />
1) Formuleer de wet van de constante massaverhouding (de wet van Proust):<br />
Wet van Proust (constante massaverhouding) :<br />
______________________________________________________________________________<br />
______________________________________________________________________________<br />
______________________________________________________________________________<br />
______________________________________________________________________________<br />
2) Wat gebeurt er bij een reactie (A) + (B) (A,B) wanneer je van product A meer gebruikt (dus<br />
meer massa) dan er met product B kan reageren?<br />
______________________________________________________________________________<br />
______________________________________________________________________________<br />
3) Hoeveel gram kopermetaal verbindt zich met 1 g zwavelbloem in kopersulfide (Cu, S) ?<br />
4) Neem de tabel in Explosief p. 93, oef. 6 hieronder over.<br />
Bereken uit deze tabel de massaverhouding van de elementen Fe en S in (Fe,S)<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—36
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
29. De atoomtheorie van Dalton (1)<br />
Bronnen: - Elementaire <strong>chemie</strong> : C:\elementaire <strong>chemie</strong>\321_Atoommodel van Dalton.htm<br />
- Explosief p. 94-95<br />
1) Lees aandachtig het onderstaande stuk (uit ‘Elementaire <strong>chemie</strong>’).<br />
ATOOMMODEL VAN DALTON<br />
Alle stoffen bestaan uit zeer kleine deeltjes (Corpusculaire bouw).<br />
Deze deeltjes zijn opgebouwd uit atomen. Er zijn zoveel verschillende atoomsoorten als er<br />
elementen zijn (een honderdtal). Elke atoomsoort heeft een bepaalde massa.<br />
Waterstofatomen hebben de kleinste massa, de massa van uraanatomen is zeer groot. In een<br />
bepaalde stof zijn die atomen op een bepaalde manier, in een bepaalde verhouding, met elkaar<br />
gebonden (Wet van de constante massaverhouding).<br />
Zo bestaat water (H2O) bijv. uit allemaal identieke deeltjes die opgebouwd zijn uit één<br />
zuurstofatoom en twee waterstofatomen. De atomen zijn in die verhouding (2/1) onderling<br />
gebonden. Er zitten dus geen deeltjes tussen die bestaan uit één zuurstofatoom en drie<br />
waterstofatomen bijvoorbeeld.<br />
Er bestaan wèl deeltjes die opgebouwd zijn uit twee waterstof- en twee zuurstofatomen<br />
(verhouding 1/1). Die deeltjes treffen we echter nooit in water aan, wel in een andere stof:<br />
waterstofperoxide (H2O2). Die stof heeft echter heel andere eigenschappen dan water.<br />
Bij een chemische reactie in een afgesloten ruimte blijft de totale massa constant (Wet van<br />
massabehoud). De verklaring is eenvoudig: er kunnen geen<br />
atomen verdwijnen of bijkomen. Daaruit volgt ook dat er geen<br />
elementen verdwijnen of ontstaan: behoud van een element<br />
tijdens een reactie (Behoud van een element). Bij een chemische<br />
reactie worden de aanwezige atomen enkel maar herschikt.<br />
John Dalton (1766-1844) was de eerste die de atoomtheorie op<br />
dze manier uitwerkte. stelde de (toen gekende) atomen voor met<br />
bolletjes (cirkeltjes). Hij vulde die bolletjes voor elk atoom op een<br />
verschillende manier in. Toen wat dat betreft zijn inspiratie hem<br />
in de steek liet, schreef hij de eerste letter van de naam in het<br />
cirkeltje. Hij is dus eigenlijk voor het eerst symbolen gaan<br />
gebruiken. Dit blijkt uit bijgaande figuur. De getallen stellen de<br />
massa’s (W t = Weight) van de atomen voor.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—37
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2) De verhouding waarin atomen gebonden zijn kan nogal verschillen van de ene stof tot de<br />
andere. Maar voor elke stof is die verhouding vast en onveranderlijk! Dat volgt vanzelf uit het<br />
atoommodel van Dalton.<br />
Oefening<br />
Hoeveel atomen waterstof bevat elke molecule van de volgende stoffen? Vul de tabel aan.<br />
Naam van de stof<br />
Chemisch<br />
symbool<br />
Aantal atomen<br />
waterstof per<br />
molecule van<br />
de stof<br />
Waterstofchloride HCl H: 1 Cl : 1<br />
Aantal andere<br />
atomen per<br />
molecule<br />
Water H20 H: _____ O : _____<br />
Ammoniak NH3 H: _____ N : _____<br />
Methaan CH4 H: _____ C : _____<br />
Zwavelzuur<br />
(diwaterstofsulfaat) H2SO4 H: _____<br />
Vul deze zinnen aan:<br />
S : _____<br />
O : _____<br />
Eén ___________________ water bevat twee _______________ waterstof en één<br />
______________________ zuurstof.<br />
Eén molecule zwavelzuur bevat twee atomen ____________________, één atoom<br />
__________________ en vier atomen _______________________ .<br />
Formuleer dezelfde zinnen voor waterstofchloride, methaan en ammoniak.<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—38
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
30. Oefeningen : chemische reacties<br />
In deze fiche oefen je de wet van behoud van massa (Lavoisier), de wet van de constante<br />
massaverhoudingen (Proust) en de atoomtheorie van Dalton. Voor sommige oefeningen is het<br />
nuttig om eerst enkele fiches terug te bladeren en de leerstof te herhalen.<br />
Oefeningen op oxidatiereacties (verbranding)<br />
1. Noteer de juiste elementvergelijking (met haakjes).<br />
a) de verbranding van kalium tot dikaliumoxide.<br />
(_____) + (______)<br />
b) de analyse van kwikoxide<br />
(______,_______)<br />
c) de synthese van ammoniak (N,H)<br />
d) de analyse van dialuminiumtrioxide<br />
e) de synthese van ijzertrichloride<br />
f) de analyse van methaan (C, H)<br />
→<br />
→<br />
→<br />
→<br />
→ (_______, ______)<br />
→ (______) + (______)<br />
Oefeningen op de wet van Proust (constante massaverhouding)<br />
1. Verklaar de betekenis van de volgende zin: De massaverhouding van (Cu,S) (kopersulfaat)<br />
bedraagt 3,95.<br />
2. Hoeveel g Cu verbindt zich met 1 g S in (Cu,S) ?<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—39
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Magnesium reageert met 2,54 g jood tot vorming van 2,78 g magnesiumiodide.<br />
Elementvergelijking : (Mg) + (I) (Mg,I)<br />
a) Bereken de massaverhouding van de elementen<br />
b) Hoeveel gram magnesium is nodig om 10 g (Mg,I) te bereiden?<br />
Deze vraag is niet makkelijk. Tip: stel een vergelijking op, waarbij je gebruik maakt van de<br />
massaverhouding. Als de massaverhouding A is, ziet die vergelijking er (in dit geval) als<br />
volgt uit : A . x + x = 10 g.<br />
Uit die vergelijking kun je x afzonderen (distributiviteit).<br />
<strong>2012</strong>-<strong>2013</strong> Stoffen en reacties<br />
Freinetschool Villa da Vinci III—40
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
31. Fysische eigenschappen van metalen (1/2)<br />
Lees aandachtig Elementaire Chemie, 3.1 Fysische eigenschappen (C:\elementaire <strong>chemie</strong>\330_M<br />
en NM fysisch.htm) 8 .<br />
1. Beantwoord de vragen, vul in waar nodig.<br />
a) Noem vier stoffen die de elektrische stroom geleiden en vier stoffen die de stroom niet<br />
geleiden:<br />
Geleider Isolator (= niet-geleider)<br />
b) Wat gebeurt er met een loden staaf, wanneer je er met een hamer op klopt?<br />
c) Wat gebeurt, wanneer je met een hamer op een stukje octazwavel (of bv. ook grafiet) klopt?<br />
d) “Metalen zijn goede warmtegeleiders, niet-metalen niet”. Is dit juist of fout?<br />
e) Wat is de aggregatietoestand van de meeste metalen bij kamertemperatuur?<br />
Antwoord: vast / vloeibaar / gasvormig<br />
f) Wat is de aggregatietoestand van de meeste niet-metalen bij kamertemperatuur?<br />
Antwoord: vast / vloeibaar / gasvormig<br />
g) Wat is er bijzonder aan koolstof (C)?<br />
Antwoord: Koolstof is geen metaal en toch __________________________________ .<br />
h) Wat is er bijzonder aan kwik (Hg)?<br />
Antwoord: Kwik is een metaal en toch ___________________________________ .<br />
8 Je vindt deze pagina het makkelijkst via het start-menu (groene kleur!): C:\elementaire <strong>chemie</strong>\00_Start<br />
GO3.htm<br />
<strong>2012</strong>-<strong>2013</strong><br />
Freinetschool Villa da Vinci 41
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
i) Gebruik voor de volgende vraag de tabel “aggregatietoestand”.<br />
Je wil ijzer, lood, koper, diamant en witte fosfor (tetrafosfor) doen smelten. Vul in de tabel<br />
aan of het om een metaal of een niet-metaal gaat en bij welke temperatuur deze stof zal<br />
smelten. Geef ook telkens de kooktemperatuur aan.<br />
Stof Symbool<br />
IJzer Fe<br />
Lood<br />
Koper<br />
Diamant<br />
Witte fosfor of<br />
tetrafosfor<br />
P4<br />
Metaal of nietmetaal?<br />
Smeltpunt Kookpunt<br />
j) Wat valt op als je in de bovenstaande tabel het smeltpunt van de metalen en de nietmetalen<br />
vergelijkt?<br />
k) Bekijk opnieuw de tabel op Elementaire Chemie.<br />
i) Welke aggregatietoestand heeft dizuurstof (O2) bij kamertemperatuur? ____________<br />
ii) Bij welke temperatuur wordt zuurstofgas vloeibaar? ______________________<br />
iii) Bij welke temperatuur wordt zuurstofgas een vaste stof? __________________<br />
<strong>2012</strong>-<strong>2013</strong><br />
Freinetschool Villa da Vinci 42
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2) Samenvatting : fysische eigenschappen van metalen. Vul de tabel aan:<br />
Fysische eigenschap Metalen Niet-metalen<br />
Elektrische geleiding<br />
Vervormbaarheid<br />
Warmtegeleiding<br />
Uitzicht<br />
Aggregatietoestand bij<br />
kamertemperatuur<br />
Welke twee uitzonderingen heb je in dit hoofdstuk leren kennen (een metaal en een niet-metaal)?<br />
Geef ook de eigenschap die de uitzondering uitmaakt.<br />
Metaal: _________________________________________________________________<br />
Niet-metaal: _____________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong><br />
Freinetschool Villa da Vinci 43
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
32. Fysische eigenschappen van metalen (2/2)<br />
1) Metalen en niet-metalen (vervolg en uitdieping)<br />
Lees aandachtig Explosief 2.1. p. 101-104.<br />
a) Hoeveel natuurlijke elementen bestaan er? __________<br />
b) Allotropie. Wat is allotropie?<br />
Antwoord: Allotropie betekent dat _______________________________________<br />
____________________________________________________________________<br />
c) Geef allotrope vormen van<br />
* koolstof (C): ___________________, _________________ en ________________<br />
* fosfor (P) : _____________ en _________________<br />
d) Juist of fout?<br />
Bewering Juist of fout?<br />
Kalium (kaliummetaal) zinkt in water.<br />
Diamant smelt bij een lagere temperatuur dan grafiet en amorfe<br />
kool.<br />
Het kookpunt van diamant, grafiet en amorfe kool is hetzelfde. (*)<br />
(*) Sta hierbij eens wat langer stil : hoe verklaar je dat?<br />
e) Wat is ‘galvaniseren’? (Zoek dit op in Wikipedia). Op welke eigenschap van metalen is<br />
galvaniseren terug te voeren? (dit vind je op p.103 terug)<br />
<strong>2012</strong>-<strong>2013</strong><br />
Freinetschool Villa da Vinci 44
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
f) “Metalen zijn glanzend, niet-metalen dof”. Dat heb je in dit hoofdstuk geleerd. Hoe komt het<br />
dan dat een magnesiumlintje (= een metaal) pas glanzend wordt nadat je het met<br />
schuurpapier hebt afgeschuurd?<br />
2) Indeling van de elementen<br />
Open de PowerPoint-presentatie “Chemie – de elementen” op mathima/jaar 3/<strong>chemie</strong>.<br />
Bekijk de dia’s 2, 3 en 4. Beantwoord vervolgens de vragen:<br />
a) In welke drie categorieën worden de elementen hier onderverdeeld?<br />
b) Van welke soort zijn er veruit de meeste elementen?<br />
c) Noem 10 metalen en geef telkens ook het chemisch symbool (maak van deze oefening<br />
gebruik om NIEUWE symbolen te leren kennen – kies dus niet simpelweg elementen die je al<br />
kent)<br />
d) Noem 10 niet-metalen en geef telkens ook het chemisch symbool<br />
e) Hoeveel edelgassen zijn er? ______ . Noem ze (met symbool). [Over de edelgassen leer je<br />
later meer.] _______________________________________________________________<br />
_________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong><br />
Freinetschool Villa da Vinci 45
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
IV. Atoombouw en periodiek systeem<br />
In dit hoofdstuk leer je (1) wat atomen zijn, (2) hoe ze opgebouwd zijn en (3) hoe ze ingedeeld<br />
worden op basis van hun opbouw en eigenschappen (in het zogenaamde “periodiek systeem der<br />
elementen”). We beginnen met de vraag “Wat zijn atomen en hoe zijn ze opgebouwd?”<br />
Vroeger dacht men dat atomen de allerkleinste bouwsteentjes van de natuur waren. Zulke atomen<br />
konden, zo dacht men toen, niet verder opgedeeld worden in kleinere deeltjes. Vandaar de naam<br />
“atoom”, van het Griekse woord voor “ondeelbaar” (a-tomos).<br />
Sinds het begin van de twintigste eeuw weten we dat die voorstelling van ondeelbare atomen niet<br />
klopt: atomen bestaan wel degelijk uit kleinere deeltjes: protonen, neutronen en elektronen.<br />
Protonen en neutronen bestaan op hun beurt uit kleinere deeltjes, de zogenaamde quarks, maar die<br />
behoren niet tot de leerstof van dit jaar. Voor de scheikunde zijn quarks overigens niet belangrijk (de<br />
studie van quarks en elementaire deeltjes behoort tot het domein van de (deeltjes)fysica).<br />
33. De lange geschiedenis van het atoommodel : meer dan 2000 jaar!<br />
Lees aandachtig Elementaire Chemie, “Evolutie van het atoommodel” (C:\elementaire<br />
<strong>chemie</strong>\340_Evolutie atoommodel.htm) 9 . Beantwoord daarna de onderstaande vragen en vul de<br />
leemten in. Als je de tekst volledig en aandachtig leest, kun je alles hieronder invullen!<br />
1. Vragen bij “Evolutie van het atoommodel”<br />
1.1. De Oude Grieken<br />
Wie is de “peetvader” van het atoommodel? ______________________ .<br />
Wanneer leefde hij ? _______________________ (zoek dit zelf op).<br />
Hoe kwam hij op het idee van het bestaan van atomen? _______________________________<br />
_____________________________________________________________________________<br />
_____________________________________________________________________________<br />
Wat is de oorsprong (etymologie) van de benaming “atoom”? __________________________<br />
_____________________________________________________________________________<br />
9 Je vindt deze pagina ook als volgt: start Elementaire Chemie op en ga naar de thuispagina (C:\elementaire<br />
<strong>chemie</strong>\00_Start.htm). Klik op de GROENE tekst “Derde leerjaar” (groen staat op deze cd-rom voor<br />
Gemeenschapsonderwijs: C:\elementaire <strong>chemie</strong>\00_Start GO3.htm). Scroll naar beneden en klik onder “4.1.<br />
Elektronenmantel” op “Evolutie van het atoommodel”.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
1.2. Dalton en de corpusculaire bouw van de materie<br />
Wie wordt beschouwd als de “vader” van het moderne atoommodel? ______________________ .<br />
Wanneer leefde hij? ___________________________ .<br />
Hoeveel tijd verstreek dus (ongeveer) alvorens de moderne wetenschap het model van Democritus<br />
bevestigde? ________________________________ .<br />
Vul in (de antwoorden vind je in de tekst):<br />
In het moderne atoommodel zijn er evenveel verschillende atoomsoorten als er<br />
___________________ zijn (dat zijn er in totaal ongeveer _______).<br />
Elke atoomsoort heeft een bepaalde ___________________ . Van alle natuurlijke elementen<br />
heeft _______________________ de kleinste massa, uranium (of uraan) de grootste 10 . Waterstof<br />
is element 1, uranium is element 92 : zie later.<br />
1.3. Na Dalton : atomen zijn tóch deelbaar !<br />
Dalton dacht dat atomen ondeelbaar waren (daarom nam hij de Griekse benaming over). Later<br />
ontdekte men dat dit niet klopte. Vandaag weten we dat atomen uit drie verschillende soorten<br />
deeltjes opgebouwd zijn :<br />
1. De e__________________. Deze zijn _____________________ geladen.<br />
2. De p__________________ . Deze zijn ____________________ geladen.<br />
3. De n__________________ . Deze hebben een neutrale lading (vandaar ook hun naam).<br />
Positief geladen? Negatief geladen? Neutraal? Wat is eigenlijk het verschil?<br />
Het antwoord op deze vraag vind je op C:\elementaire <strong>chemie</strong>\340b_Ladingen.htm<br />
(je bereikt deze pagina ook door in de tekst over het atoommodel op “positief geladen”<br />
of “negatief geladen” of “zonder lading” te klikken).<br />
Lees deze pagina en kijk naar de animatie. Vul vervolgens de leemten in.<br />
Kies uit : trekken elkaar aan, stoten elkaar af, hebben geen invloed op elkaar<br />
Gelijknamige ladingen _____________________________________________ .<br />
Tegengestelde ladingen ____________________________________________.<br />
Een neutrale lading en een positieve (of negatieve) lading<br />
______________________________ .<br />
10 Er bestaan ook elementen met een grotere massa dan uraan (de zgn. trans-uranen), maar die zijn kunstmatig<br />
door de mens gemaakt en vallen na korte tijd weer uit elkaar.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
34. Het atoommodel van Rutherford-Bohr<br />
Het atoommodel werd in de twintigste eeuw nog verder ontwikkeld. Een belangrijke vraag was onder<br />
meer: waar precies bevinden zich protonen, neutronen en elektronen in het atoom? Liggen ze<br />
gewoon door elkaar of zijn ze op een bepaalde manier geordend? Bewegen ze, of net niet?<br />
Het model dat wij in de les zullen hanteren (en dat je in het secundair onderwijs steeds weer zult<br />
gebruiken en dus goed moet kennen), is het zogenaamde Rutherford-Bohr-model. Het is genoemd<br />
naar Ernest Rutherford (1871-1937, Nobelprijs scheikunde in 1908) en Niels Bohr (1885-1962,<br />
Nobelprijs natuurkunde in 1922), twee van de belangrijkste wetenschappers uit de twintigste eeuw.<br />
Door deze fiches in te vullen zul je het Rutherford-Bohr-model stap voor stap leren kennen.<br />
1. Elektronen, protonen, neutronen<br />
Opmerking over neutronen. Om historisch helemaal correct te zijn, zouden we in wat volgt alleen over<br />
elektronen en protonen mogen spreken. Het neutron werd immers pas later ontdekt (in 1932, hoewel Rutherford<br />
het bestaan van neutronen al in 1920 voorspeld had) en aan het model toegevoegd. Dat verklaart waarom je<br />
soms in het Rutherford-model geen neutronen terugvindt (bv. in Explosief 1.2. op p. 139). Maar wij gaan aan deze<br />
historische haarklieverij voor het gemak voorbij.<br />
De massa van ____________________ en _____________________ is (ongeveer) even groot: zowat<br />
1,6.10 -27 kg 11 . De massa van het elektron daarentegen is verwaarloosbaar klein: het bedraagt<br />
ongeveer 1/2000 van de protonmassa. Omdat de massa van het elektron zo klein is, doet men vaak<br />
alsof het elektron helemaal geen massa heeft (zie ook hieronder).<br />
2. Het atoommodel volgens Rutherford<br />
Op C:\elementaire <strong>chemie</strong>\340_Evolutie atoommodel.htm, onderaan de pagina, vind je een<br />
voorstelling van een atoom volgens het Rutherford-model (hier: een lithium-atoom met drie<br />
elektronen). Teken dit atoommodel hieronder over en duid aan in de tekening: protonen,<br />
neutronen, elektronen, kern, elektronenschillen.:<br />
11 Of met andere woorden: om één gram neutronen bij elkaar te krijgen heb je zowat een miljoen miljard<br />
miljard neutronen nodig.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 3
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Bestudeer het lithium-model nauwkeurig en beantwoord de vragen:<br />
- Welke deeltjes bevinden zich in de kern? _________________ en ___________________<br />
Welke deeltjes zweven in banen rond de kern? _______________________________<br />
- Hoeveel neutronen heeft een Li-atoom? _______<br />
Hoeveel protonen heeft een Li-atoom? _________<br />
Hoeveel elektronen heeft een Li-atoom? __________<br />
- Elektrische lading. Wat is de totale elektrische lading van dit atoom? (Tel de positieve en de<br />
negatieve ladingen op) : ____ positieve ladingen + ____ negatieve ladingen => de totale<br />
lading is ________ .<br />
Besluit. Vul in en schrap wat niet past:<br />
De kern van een atoom bevat _________________ en __________________ .<br />
Rond de kern bewegen de _______________________ .<br />
De kern van een atoom is positief geladen / negatief geladen / elektrisch neutraal.<br />
De elektronenbanen zijn positief geladen / negatief geladen / elektrisch neutraal.<br />
Het atoom zelf is positief geladen / negatief geladen / elektrisch neutraal.<br />
Denkvraag 1. Waarom noemt men het Rutherford-model ook wel het “zonnestelsel”-model?<br />
_________________________________________________________________<br />
_________________________________________________________________<br />
Denkvraag 2. Waar bevindt zich de 99,999 % van de massa van het atoom? (het antwoord<br />
vind je door de tekst hierboven met het Rutherford-atoommodel te vergelijken).<br />
_________________________________________________________________<br />
_________________________________________________________________<br />
Een grote nieuwigheid van het Rutherford model is de voorstelling dat het atoom grotendeels<br />
bestaat uit … NIETS (of “vacuüm”): tussen de kern en de elektronen lijkt een “enorme” (nou ja,<br />
alles is relatief) leegte te gapen. Want inderdaad, de kern is véél kleiner dan het atoom zelf. De<br />
volgende vergelijking toont dat goed aan: als je een waterstofatoom (met één elektron) zou<br />
vergroten tot de afmetingen van een voetbalveld, dan zou de kern ongeveer een speldenkop<br />
groot zijn, terwijl het elektron zich aan de rand van het veld bevindt! Daartussen gaapt de leegte.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 4
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Het Rutherford-Bohr-model van het atoom.<br />
Lees de korte alinea over Bohr op C:\elementaire <strong>chemie</strong>\340_Evolutie atoommodel.htm.<br />
Vul in:<br />
Uit de studie van waterstof en enkele andere elementen leidde Niels Bohr af dat de<br />
elektronen in de __________________________ niet zomaar in het wilde weg bewegen. Hun<br />
beweging is aan bepaalde regels gebonden. Volgens Bohr zijn er een beperkt aantal<br />
___________________________ waarop de elektronen voorkomen. Hij noemt die niveaus<br />
_________________. De verdeling van de elektronen over de schillen noemt men de<br />
________________________________ van het atoom.<br />
- Elektronenschillen. De elektronen bevinden zich in een elektronenwolk rond de kern, op<br />
zogenaamde schillen.<br />
Hoeveel elektronenschillen heeft een lithium-atoom (zie de schets op p. 3) ? _________<br />
Met welk symbool wordt de binnenste (= de eerste) Li-schil aangeduid? _____ .<br />
Met welk symbool wordt de tweede Li-schil aangeduid? ______ .<br />
Ga nu naar het volgende hoofdstuk van Elementaire Chemie, “Atoommodel van Rutherford-Bohr”.<br />
Klik daarvoor op de (groene !) pijl “volgend” of gebruik de URL C:\elementaire<br />
<strong>chemie</strong>\341_Atoommodel Rutherford-Bohr.htm.<br />
Lees deze tekst aandachtig. Je moet niet alles kennen. De volgende vragen behandelen de verplichte<br />
leerstof.<br />
- Lading.<br />
Zoals we al zagen, zijn elektronen ________________ geladen, protonen positief.<br />
We zeggen dat één elektron de lading -1 heeft, één proton de lading +1. De grootte 1<br />
noemen we de ______________slading.<br />
Test je inzicht<br />
Hoe groot is de lading van twee elektronen? _______________ .<br />
Hoe groot is de totale lading van 3 elektronen en 4 protonen? ________________ .<br />
Hoe groot is de totale lading van 2 elektronen en een neutron? _______________ .<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 5
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
- Atoommassa-eenheid.<br />
Uit de vorige fiche weet je dat neutronen en protonen ongeveer dezelfde massa hebben<br />
(1,6.10 -27 kg). Om de massa’s eenvoudig te kunnen uitdrukken noemen we deze massa de<br />
______________________________ (symbool : ____).<br />
Dus geldt 12 :<br />
massa van 1 proton = massa van 1 neutron = ___u .<br />
Omdat de massa van een elektron (0,0005 u) zeer klein is in vergelijking met een<br />
neutron/proton, zeggen we :<br />
massa van 1 elektron = 0 u.<br />
Samengevat: lading en massa. Vul de tabel aan (andere volgorde dan op de CD-rom!):<br />
Deeltje Lading Massa<br />
Elektron<br />
Proton<br />
Neutron<br />
- Het protonengetal of atoomnummer Z<br />
De aard van een atoom wordt bepaald door het aantal ______________ in de kern. Dit aantal<br />
noemt men het _________________ of het ______________________ (symbool: Z)<br />
Enkele voorbeelden (gebruik hiervoor het periodiek systeem):<br />
1. Een H-atoom (element: w________________ ) heeft één proton in de kern. Het<br />
atoomnummer van H is dan ook ___ .<br />
2. Een atoom met Z = 2 heeft ___ protonen in de kern. Dit is het element ______________ .<br />
3. Een barium-atoom (Ba) heeft 56 protonen in de kern. Het atoomnummer van Ba is dus<br />
____ .<br />
4. Wat is het atoomnummer of protonengetal van zuurstof? Antwoord: Z = ____<br />
12 Later zullen we deze definitie aanpassen (1 u = 1/12 van de massa van een 12 C-atoom). Maar dat is voor later.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 6
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Omdat het aantal (negatief geladen) ____________________ in de elektronenwolk steeds gelijk<br />
is aan het aantal (positief geladen) _________________ in de kern, is een atoom steeds<br />
elektrisch _______________.<br />
Nu kun je ook deze vragen beantwoorden:<br />
1. Hoeveel elektronen heeft een H-atoom? Antw: _______<br />
2. Een atoom met Z = 2 heeft ___ elektronen.<br />
3. Een barium-atoom (Ba) heeft ____ elektronen.<br />
4. Een O-atoom heeft ____ elektronen.<br />
Besluit: het protonengetal of atoomnummer Z geeft niet alleen het aantal<br />
_________________, maar ook het aantal ____________________ weer.<br />
- Het massagetal of nucleonengetal 13 A<br />
Als we de totale massa van een atoom (uitgedrukt in u) willen kennen, moeten we het aantal<br />
__________________ en het aantal ___________________ in de kern optellen. De<br />
______________________ (u = 0) spelen geen rol bij de massabepaling.<br />
De totale massa van een atoom drukken we uit met het massagetal (of nucleonengetal) A :<br />
massagetal A = aantal protonen (Z) + aantal neutronen<br />
A = Z + aantal neutronen<br />
Meestal wordt het aantal neutronen niet apart opgegeven. Maar met de bovenstaande<br />
formule is het makkelijk te berekenen (vul aan):<br />
Aantal neutronen = ____ – ____<br />
Samengevat: Locatie en aantal. Vul de tabel aan (andere volgorde dan op de CD-rom!):<br />
Deeltje Locatie Aantal<br />
Elektron<br />
Proton<br />
Neutron<br />
13 “nucleonen” is een verzamelterm voor protonen en neutronen. Het zijn de deeltjes die zich in de nucleus, de<br />
kern, bevinden.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 7
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Schematisch overzicht (goed kennen!)<br />
u = de atoommassa-eenheid (1 u = de massa van een ____________________ )<br />
Z = het “_______________getal” of “____________nummer”<br />
= het aantal ____________________ in de kern<br />
A = het “_________________getal” of “______________getal”<br />
= de totale massa van het atoom uitgedrukt in u.<br />
Het aantal protonen in (de kern van) een atoom is gelijk aan __ .<br />
Het aantal elektronen in (de schillen van) een atoom is gelijk aan __ .<br />
Het aantal neutronen in (de kern van) een atoom is gelijk aan __________ .<br />
Een atoom heeft evenveel protonen als elektronen en is dus steeds elektrisch neutraal.<br />
Toepassingen en oefeningen<br />
1) Het broom-atoom (Z = 35, A = 80). Vul zelf de juiste getallen in. Vergelijk vervolgens met de<br />
oplossing op C:\elementaire <strong>chemie</strong>\341_Atoommodel Rutherford-Bohr.htm.<br />
Br-atoom : Z = 35 , A = 80<br />
Br<br />
80<br />
35<br />
Aantal protonen in de kern (Z) ____<br />
Aantal neutronen in de kern (A – Z) ____<br />
Aantal elektronen rond de kern (Z) ____<br />
Massa van de protonen ___ u<br />
Massa van de neutronen ___ u<br />
Massa van de elektronen ___ u<br />
Massa van het Br-atoom ___ u<br />
Lading van de protonen in de kern ____<br />
Lading van de neutronen in de kern ____<br />
Lading van de volledige kern ____<br />
Lading van de elektronen rond de kern ____<br />
Lading van het volledige Br-atoom ____<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 8
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2) Vul de tabel in. Zoek de ontbrekende gegevens op in het periodiek systeem.<br />
Atoom Z A Aantal<br />
He 4<br />
C 12<br />
N 14<br />
Na 23<br />
protonen<br />
Aantal<br />
neutronen<br />
Aantal<br />
elektronen<br />
Massa<br />
De oplossing vind je op C:\elementaire <strong>chemie</strong>\341_Atoommodel Rutherford-Bohr.htm.<br />
3) Meerkeuze-oefening.<br />
Beantwoord de 15 meerkeuzevragen op C:\elementaire <strong>chemie</strong>\341_Atoommodel<br />
Rutherford-Bohr.htm (onderaan op het scherm: Atoombouw 1).<br />
4) Matching-oefening.<br />
Maak de oefening Atoombouw 2 op C:\elementaire <strong>chemie</strong>\341_Atoommodel Rutherford-<br />
Bohr.htm (onderaan op het scherm).<br />
Meer weten? Een overzichtelijke presentatie over het atoommodel vind je op<br />
http://www.slideshare.net/mol/het-atoommodel<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 9
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
35. Elektronenconfiguratie<br />
Achtergrondinformatie (lezen!)<br />
Je weet nu hoe je het aantal elektronen, protonen en neutronen in een atoom kunt bepalen als je<br />
het atoomnummer en het massagetal kent. Nu blijft nog een laatste stap, namelijk de vraag:<br />
Hoe verdelen de elektronen zich over de elektronenschillen?<br />
Het antwoord op die vraag is zeer belangrijk voor de <strong>chemie</strong>. In de <strong>chemie</strong> bestudeert men eigenlijk<br />
niets anders dan het gedrag van de elektronen in de buitenste schillen van atomen. De andere<br />
deeltjes (de protonen en neutronen in de kern, de elektronen in de binnenste schillen) spelen bij<br />
chemische verschijnselen 14 geen rol : het volstaat te weten dat ze er zijn.<br />
Je zult later leren dat zowat alle belangrijke eigenschappen van de elementen en de stoffen<br />
UITSLUITEND afhangen van wat er met de elektronen gebeurt in de buitenste schillen van de<br />
atomen:<br />
Waarom geleiden metalen de stroom?<br />
Waarom reageren sommige elementen zeer hevig met water en andere<br />
niet?<br />
Waarom valt grafiet makkelijk uiteen en diamant net niet (herinner je: beide<br />
bestaan uitsluitend uit C)?<br />
Waarom reageren de edelgassen zo moeilijk met andere elementen?<br />
Waarom gaat H makkelijk een verbinding aan met O en met Cl en niet met<br />
Fe?<br />
Ja, zelfs vragen zoals: Waarom trillen watermoleculen in een magnetron?<br />
Het is belangrijk dat je de elektronenconfiguratie van atomen begrijpt en de achterliggende principes<br />
kunt toepassen. Volgens het leerplan moet je de elektronenconfiguratie van alle atomen tot en met Z<br />
= 18 / Z = 20 kunnen geven.<br />
14 Ter herinnering: chemische verschijnselen zijn verschijnselen waarbij de eigenschappen van stoffen of<br />
elementen veranderen. Of, nog preciezer: verschijnselen waarbij nieuwe (chemische) verbindingen tussen<br />
stoffen of elementen ontstaan.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 10
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Elektronenconfiguratie : 4 REGELS<br />
1) REGEL 1. Het aantal elektronenschillen van een atoom ligt tussen 1 en 7<br />
(bv. waterstof heeft 1 elektronenschil, helium 2, uranium 7).<br />
2) REGEL 2. De schillen hebben een nummer n (n = 1, 2, 3, 4, 5, 6, 7) en een naam (K-schil, Lschil,<br />
M, N, O, P, Q). De K-schil heeft n=1, de L-schil heeft n=2 enz.<br />
3) REGEL 3. Het maximum aantal elektronen op een schil met nummer n is 2n²<br />
(bv. n = 2 => 2n²=2.2² = 8).<br />
Maar! 3a) REGEL 3a. De buitenste schil van een atoom heeft maximum 8 elektronen!<br />
3b) REGEL 3b. De voorlaatste schil van een atoom heeft maximum 18 elektronen!<br />
4) REGEL 4. De elektronen “willen” zoveel mogelijk op de binnenste schillen “zitten”. Pas als alle<br />
vrije plaatsen op de binnenste schil ingenomen zijn, nemen elektronen de plaatsen op een<br />
volgende schil in (maar vergeet de REGELS 3, 3a en 3b niet!) 15 .<br />
Deze vier regels moet je goed kennen en kunnen toepassen. Je moet immers zelf de<br />
elektronenconfiguratie van de eerste 20 elementen kunnen geven en verklaren.<br />
Toepassing van regels 1-3. Vul de tabel aan:<br />
Schil<br />
Nummer<br />
n<br />
Naam<br />
Maximaal aantal elektronen<br />
= 2n²<br />
1 K 2<br />
2<br />
3<br />
4<br />
De oplossing vind je op C:\elementaire <strong>chemie</strong>\342_Elektronenconfiguratie.htm<br />
15 Deze regels gelden heel streng voor de elementen 1 t.e.m. 18. Voor Z > 18 zijn er uitzonderingen. Die<br />
uitzonderingen worden verklaard in de kwantum<strong>chemie</strong>/kwantumfysica, maar dat behoort niet tot de leerstof<br />
van het secundair onderwijs. De fundamentele verklaring is altijd dat systemen in de natuur bij voorkeur de<br />
toestand met de kleinste energie innemen.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 11
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Voorbeeld 1 – Wat is de elektronenconfiguratie van Be (Z = 4) ?<br />
Stap 1 Beryllium heeft atoomnummer 16 Z = 4.<br />
Stap 2 Een Be-atoom heeft dus 4 protonen en dus ook 4 elektronen.<br />
Stap 3 De K-schil (n = 1) kan maximum 2 elektronen bevatten (regel 3).<br />
Stap 4 Er zitten dus nog 2 elektronen op de L-schil.<br />
Antwoord : De elektronenconfiguratie van Be is 2-2 (of, in een andere notatie: K 2 L 2 ).<br />
Schematisch:<br />
Voorbeeld 2 – Wat is de elektronenconfiguratie van Br (Z = 35) ? Vul de leemten aan.<br />
Stap 1 Broom heeft atoomnummer Z = ______.<br />
Stap 2 Een Br-atoom heeft dus ____ protonen en daarom ook ____________________.<br />
Stap 3 De K-schil (n = 1) kan maximum 2.1² = ____ elektronen bevatten. De L-schil (n = 2)<br />
kan maximum 2.2² = ____ elektronen bevatten (regel 3).<br />
Stap 4 In totaal zijn 10 elektronen geplaatst en blijven er nog 25 over. Op de M-schil (n = 3)<br />
kunnen maximum ____ elektronen zitten.<br />
Stap 4 De overige 7 elektronen zitten op de N-schil..<br />
Antwoord : De elektronenconfiguratie van Br is 2-8-18-7 (K 2 L 8 M 18 N 7 ).<br />
Schematisch:<br />
16 Ofwel krijg je bij zulke opgaven het atoomnummer als gegeven, ofwel moet je het zelf opzoeken in het<br />
periodiek systeem.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 12
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Eenzaam elektron of elektronenpaar (doublet)<br />
Bij de schematische weergave van elektronenconfiguraties staan de elektronen nu<br />
eens uit elkaar (= eenzaam elektron), dan weer per tweeën gegroepeerd (=<br />
elektronenpaar of doublet).<br />
In het Be-atoom bijvoorbeeld zien we twee doubletten. De verklaring heeft te maken<br />
met de spin van de elektronen: elektronen groeperen zich bij voorkeur in een<br />
doublet, waarbij één elektron opwaartse spin (“spin up”) heeft en het<br />
andere neerwaartse spin (“spin down”). Spin is een verschijnsel uit de<br />
kwantumfysica, we gaan er dus niet verder op in. Het is voldoende<br />
dat je weet dat er zoiets bestaat als eenzame elektronen en<br />
elektronenparen (doubletten).<br />
Soms groeperen elektronen zich “liever” in een doublet dan dat ze de regels van de<br />
elektronenconfiguratie volgen. Dit verklaart waarom Ca (Z = 20) de configuratie 2-8-<br />
8-2 heeft (en niet 2-8-9-1) : de elektronen op de buitenste schil van een Ca-atoom<br />
vormen een doublet. (Extra-vraag: Vind je nog andere vergelijkbare atomen in het<br />
periodiek systeem?)<br />
- Oefening : Schrijf de elektronenconfiguratie van volgende elementen op twee manieren.<br />
Be<br />
Na<br />
Cl<br />
Ne<br />
Ca<br />
De oplossing vind je op C:\elementaire <strong>chemie</strong>\342_Elektronenconfiguratie.htm<br />
Je moet de elektronenconfiguratie van de eerste twintig elementen van het periodiek systeem (Z =<br />
1 tot Z = 20 zelf kunnen opstellen.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 13
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
36. Nucliden en isotope nucliden; gemiddelde atoommassa<br />
Lees aandachtig Explosief 1.2. p. 156, “nucliden”. Vul vervolgens de fiche in.<br />
1. Wat heb je geleerd? Vat de kernboodschap van blz. 156 in één of twee zinnen samen.<br />
______________________________________________________________________<br />
______________________________________________________________________<br />
______________________________________________________________________<br />
______________________________________________________________________<br />
2. Juist of fout?<br />
- Het aantal protonen van een element kan nooit veranderen. JUIST / FOUT<br />
- Het aantal neutronen van een element kan variëren. JUIST / FOUT<br />
- Een nuclide is een atoom met een welbepaald protonen- en nucleonengetal. JUIST / FOUT<br />
- De nuclidemassa, uitgedrukt in units u, is altijd een positief geheel getal<br />
(geen cijfer na de komma). JUIST / FOUT<br />
- Het massagetal A van een element (= de atoommassa die in het periodiek<br />
systeem vermeld wordt) is het gemiddelde van de nuclidemassa’s van de<br />
isotope nucliden, rekening houdend met hun procentueel voorkomen<br />
in de natuur. JUIST / FOUT<br />
-<br />
-<br />
-<br />
39 K, 12 C, 14 C en 16 O : dit zijn vier verschillende nucliden. JUIST / FOUT<br />
235 U en 238 U zijn isotope nucliden van uranium 17 . JUIST / FOUT<br />
12 C heeft zes neutronen in de kern. 13 C heeft zeven neutronen in de kern 18 .<br />
JUIST / FOUT<br />
- De atoommassa’s in het periodiek systeem zijn meestal geen gehele<br />
getallen, omdat het om gemiddelden van nuclidemassa’s gaat. JUIST / FOUT<br />
17<br />
Uranium heeft 92 protonen. Uraniumatomen kunnen tussen 233 en 238 nucleonen (= protonen + neutronen)<br />
hebben.<br />
18<br />
Het atoomnummer van C vind je in het periodiek systeem (linksboven bij elk element).<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 14
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Leg aan de hand van broom uit wat isotope nucliden zijn.<br />
4. Leg aan de hand van Cl uit hoe je de gemiddelde atoommassa berekent uit de nuclidemassa’s<br />
(ter herinnering: 75 % = 75/100 = 0,75).<br />
5. Hoeveel neutronen bevatten de volgende nucliden?<br />
Nuclide:<br />
Neutronengetal:<br />
6. Geef uit de vorige reeks de isotope nucliden.<br />
7. Bereken de gemiddelde atoommassa van de volgende elementen:<br />
- Uraan U<br />
- Koolstof C<br />
0,7 % voorkomen in de natuur<br />
99,3 % voorkomen in de natuur 19<br />
98,9 % voorkomen in de natuur<br />
1,1 % voorkomen in de natuur<br />
19 Om helemaal correct te zijn zou je ook 234 U moeten opnemen in de berekening. Maar dat element is zo<br />
zeldzaam (0,0055 %) dat het de berekening nauwelijks beïnvloedt. 233 U en 236 U komen in de natuur niet voor<br />
(synthetische isotopen = door de mens gemaakt); ook 14 C is synthetisch.<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 15
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
37. Het periodiek systeem der elementen (P.S.E.)<br />
Alle materie in de natuur en in de kosmos is opgebouwd uit slechts 92 verschillende elementen, die<br />
op hun beurt uit drie deeltjes (protonen, neutronen en elektronen) bestaan: je schrijftafel, de Mont-<br />
Blanc, de bomen in het bos, het water in de rivier, de wolken in de lucht, de fruitvlieg, de witte haai,<br />
de mens, onze hersenen, ja zelfs de maan, de planeten en de sterren.<br />
Deze 92 natuurlijke elementen verschillen maar heel weinig van elkaar : het verschil tussen een<br />
goudatoom en een kwikatoom (of tussen een zuurstof- en een fluoratoom) bedraagt één proton in<br />
de kern en één elektron in de elektronenwolk! Toch hebben goud en kwik (of zuurstof en fluor)<br />
totaal verschillende eigenschappen.<br />
De Russische chemicus Dmitri Mendelejev 20 (1834-1907) rangschikte de in zijn tijd gekende<br />
elementen in één overzichtelijk schema, dat vandaag nog altijd hét werkinstrument van de <strong>chemie</strong><br />
bij uitstek is: het periodiek systeem der elementen (P.S.E.). In deze fiche zul je leren hoe het<br />
periodiek systeem der elementen is opgebouwd.<br />
A) Een eerste blik op het P.S.E.<br />
Neem het periodiek systeem er al even bij. Je vindt het bij fiche 37 of in Explosief 1.2. op p. 205 (of<br />
op het internet: zoek “periodiek systeem”).<br />
Wat valt op?<br />
- Het P.S.E. bevat geen 92, maar zo’n _____ elementen. Hoe kan dat nu, als de natuur<br />
opgebouwd is uit 92 elementen?<br />
Verklaring: Alleen de eerste ____ elementen zijn natuurlijke elementen. De elementen met<br />
Z > 92 zijn kunstmatige, door de mens in laboratoria gemaakte elementen. De meeste van<br />
deze elementen bestaan slechts gedurende een kleine fractie van een seconde alvorens ze<br />
opnieuw uit elkaar vallen.<br />
- Er zijn ____________ rijen. Deze rijen zijn genummerd. Dit noemen we de zeven perioden.<br />
- Er zijn in totaal _______________ kolommen. Deze zijn genummerd met een Romeins cijfer<br />
en ze hebben ook een naam. Deze achttien kolommen noemen we de groepen.<br />
B) De informatie per element<br />
Laten we nu eens kijken welke informatie bij elk element gegeven wordt. Uit wat je in de vorige<br />
fiches leerde, moet je dit nu zelf kunnen afleiden.<br />
Als voorbeeld nemen we het element xenon. De informatie bij elk element is op een vast manier<br />
geordend.<br />
20 ook “Mendeleev” geschreven<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 16
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Vul aan. Kies uit : massagetal, elementsymbool, nucleonengetal, elektronenconfiguratie,<br />
protonengetal, atoomnummer.<br />
__________________<br />
(= __________________)<br />
____________________<br />
_____________________<br />
(= ___________________)<br />
54 2<br />
8<br />
Xe<br />
18<br />
18<br />
8<br />
131,3<br />
______________________<br />
- Tot welke groep behoort het element xenon (naam van de groep)? __________________<br />
- In de hoeveelste kolom staat xenon (begin van links te tellen, maar tel alleen de<br />
hoofdgroepen – de “overgangselementen” tel je dus niet mee!)? _____________<br />
- Hoeveel elektronen heeft xenon op de buitenste schil? _____________<br />
- Tot welke periode behoort xenon? ____________________<br />
- Hoeveel elektronenschillen heeft xenon? ______________<br />
C) De plaats van de elementen in het P.S.E.<br />
Bestudeer het P.S.E. en beantwoord deze vragen:<br />
a) Wat is het verband tussen de periode en het aantal elektronenschillen voor elk<br />
element?<br />
b) Wat is het verband tussen de groep en het aantal elektronen op de buitenste schil?<br />
(Laat de zgn. “overgangselementen” voor deze vraag buiten beschouwing; je kijkt dus<br />
alleen naar de acht zgn. “hoofdgroepen”: Ia, IIa, IIIa, IVa, Va, Via, VIIa en 0.)<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 17
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
D) De elementen van eenzelfde groep hebben vergelijkbare eigenschappen<br />
In het labo zul je proefondervindelijk leren dat elementen van eenzelfde groep bepaalde<br />
eigenschappen met elkaar delen.<br />
Voor onderstaande vragen en invuloefeningen (alinea’s D en E) gebruik je Elementaire Chemie,<br />
C:\elementaire <strong>chemie</strong>\345_Periodiek Systeem.htm. (De Lewis-voorstelling hoef je niet te kennen.)<br />
1. Vul in.<br />
Dmitriv Mendelejev rangschikte de in zijn tijd (rond 1870) gekende elementen volgens<br />
______________________ _________________________. Hij stelde vast dat, als hij op het<br />
geschikte moment met een nieuwe ________ begon, de __________________ met<br />
vergelijkbare eigenschappen __________ _______________ kwamen te staan. Af en toe liet<br />
hij een lege plaats in het systeem en _________________ dat daar een nog niet ontdekt<br />
________________ thuishoorde. Van die elementen voorspelde hij zelfs een aantal<br />
_______________ .<br />
2. Noem twee elementen (met hun moderne benaming + symbool + atoomnummer) waarvan<br />
Mendelejev het bestaan en enkele eigenschappen voorspelde.<br />
Element 1:<br />
Element 2:<br />
Moderne naam Symbool Z<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 18
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
E) Het huidige periodiek systeem der elementen : samenvatting (goed kennen!)<br />
Vul in. Kies uit : perioden, groepen, nevengroepen, analoge eigenschappen, van links naar rechts,het<br />
protonengetal, onder elkaar, hoofdgroepen, edelgassen.<br />
In het huidige P.S.E. zijn de elementen gerangschikt volgens twee criteria:<br />
1) ______________________ (atoomnummer) Z neemt toe _________________________ .<br />
2) Elementen met __________________________ staan _______________________ .<br />
Horizontaal telt het P.S.E. telt zeven _______________ (rijen)<br />
Verticaal telt het P.S.E. achttien ________________ (kolommen). Deze worden<br />
onderverdeeld in acht __________________ en acht ___________________ (waarvan de<br />
laatste uit drie kolommen bestaat).<br />
De acht hoofdgroepen zijn genummerd: Ia tot VIIa + 0.<br />
De acht nevengroepen zijn genummerd: Ib tot VIIb + VIII.<br />
De hoofdgroep met het nummer 0 is de groep van de __________________ .<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 19
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
F) Valentie-elektronen<br />
Gebruik C:\elementaire <strong>chemie</strong>\345_Periodiek Systeem.htm om dit onderdeel in te vullen. Voor<br />
sommige vragen moet je het P.S.E. gebruiken.<br />
1) Wat zijn valentie-elektronen?<br />
2) Wat is het belang van valentie-elektronen?<br />
3) Wat hebben alle elementen uit eenzelfde hoofdgroep in het P.S.E. met elkaar gemeen<br />
(uitzondering: He)?<br />
4) Hoeveel valentie-elektronen heeft:<br />
- Na (groep Ia) :<br />
- Al (groep IIIa) :<br />
- O (groep ____):<br />
- Bi (groep ____):<br />
- Rn (groep 0) :<br />
5) Verklaar het aantal valentie-elektronen van de edelgassen helium (!!), neon, argon en<br />
krypton. Of, met andere woorden: wat kun je zeggen over de buitenste elektronenschil van<br />
deze elementen van de achtste hoofdgroep? Waarom is helium een uitzondering?<br />
<strong>2012</strong>-<strong>2013</strong> Atoombouw en periodiek systeem<br />
Freinetschool Villa da Vinci 20
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
V. Chemische binding<br />
In het vorige hoofdstuk leerde je hoe de elektronenconfiguratie van atomen bepaald wordt. Je leerde<br />
ook begrippen zoals elektronenschil, valentie-elektronen, elektronenlading kennen.<br />
In dit hoofdstuk leer je hoe atomen verbindingen aangaan en moleculen vormen. Na dit hoofdstuk<br />
zul je drie soorten chemische binding kennen:<br />
1) De ionbinding<br />
2) De atoombinding (ook ‘covalente binding’ genoemd)<br />
3) De metaalbinding<br />
Je zult ook begrijpen waarom deze verschillende soorten bestaan en je zult meer weten over hun<br />
eigenschappen.<br />
Opdracht: maak de inleidende oefening op de volgende bladzijde (= herhaling + enkele nieuwe<br />
begrippen). Probeer alles te begrijpen, moeilijk is het overigens niet.<br />
Deze oefening maak je zonder hulpbronnen. Gewoon nadenken moet volstaan.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 1
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Vul in : stabiel, valentie-elektronen, opnemen, willen, chemische bindingen, reageren.<br />
De eigenschappen van een element worden bepaald door de elektronen in de buitenste<br />
schil (= de ______________________).<br />
Vraag: Wanneer is een atoom stabiel?<br />
Het aantal valentie-elektronen bepaalt namelijk of een atoom al dan niet zal<br />
_____________ met andere atomen.<br />
Elementen of atomen die niet (of bijna niet) reageren met andere elementen<br />
of atomen, noemen we “____________”.<br />
Atomen “___________” graag zo stabiel mogelijk zijn.<br />
Een atoom met een volledig gevulde buitenste schil is altijd stabieler dan een<br />
atoom met een niet volledig gevulde buitenste schil.<br />
Een element (of een atoom) met acht valentie-elektronen is dus stabieler /<br />
minder stabiel dan een element (atoom) met één, twee, zeven, … valentieelektronen.<br />
Daarom zullen sommige atomen elektronen afstaan om een volle buitenste schil te<br />
verkrijgen, terwijl andere atomen elektronen zullen _____________.<br />
Antw. : wanneer het atoom _____________________________________________________ .<br />
Atomen die “graag” elektronen afstaan, zullen reageren (“samenwerken”) met atomen die “graag”<br />
elektronen opnemen. Zo ontstaan _____________ _______________ zoals water (H20),<br />
aluminiumoxide (Al2O3), zuurstofgas (O2) enz.<br />
In wat volgt zul je leren hoe en waarom atomen elektronen afstaan of opnemen en hoe daardoor<br />
chemische bindingen tot stand komen.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 2
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
38. Edelgasconfiguratie en het ontstaan van ionen<br />
1. De Lewisvoorstelling van het atoom [dit is zeer eenvoudig! ]<br />
Lees op Elementaire Chemie C:\elementaire <strong>chemie</strong>\345_Periodiek Systeem.htm (of Start 4.<br />
Atoombouw en periodiek systeem 4.4. Periodiek systeem) de paragraaf over de Lewisvoorstelling<br />
van het atoom (onderaan op de pagina).<br />
Opgave: Schrijf de lewisvoorstelling van<br />
A Een atoom uit groep IIIa (neem een willekeurig atoom X).<br />
B Het atoom met 12 elektronen<br />
C Een atoom X met 4 elektronen in de buitenste schil<br />
D Een edelgasatoom X (niet He)<br />
E Een atoom X uit de alkalimetalengroep<br />
F Een fosforatoom<br />
G Een halogeenatoom X<br />
H Een atoom X uit de zuurstofgroep<br />
De oplossing vind je op Elementaire Chemie (klik op “oplossing”).<br />
Opm. 1: de plaats waar je de bolletjes of de streepjes zet in de Lewisvoorstelling heeft geen<br />
belang. Vanaf het vijfde elektron moet je de elektronen gepaard tekenen.<br />
Opm. 2: de twee elektronen op de buitenste schil van helium (He) zijn altijd gepaard.<br />
Teken de Lewisvoorstelling van helium:<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 3
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Wat is een ion?<br />
Definitie: Een ion is een geladen deeltje dat ontstaat uit atomen.<br />
Een + ion (ook “kation” genoemd) is een positief geladen deeltje (atoom of molecule). Het<br />
heeft dus meer positieve dan negatieve deeltjes. Dat gebeurt wanneer een neutraal atoom een<br />
elektron of elektronen afstaat / opneemt.<br />
Een – ion (ook “anion” genoemd) is een negatief geladen deeltje (atoom of molecule). Het<br />
heeft dus meer negatieve dan positieve deeltjes. Dat gebeurt wanneer een neutraal atoom een<br />
elektron of elektronen afstaat / opneemt.<br />
Opgave: teken de elektronenconfiguratie van (geef het verschil met een pijl of met een kleurtje<br />
aan)<br />
a) Een Ca-atoom Een Ca 2+ -ion<br />
b) Een Cl-atoom Een Cl – -ion<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 4
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
3. Wat is een elektrische stroom?<br />
Definitie: een elektrische stroom is een verplaatsing van (positief of negatief) geladen deeltjes.<br />
Juist of fout?<br />
- Een stroom van protonen veroorzaakt een elektrische stroom . JUIST / FOUT<br />
- Een stroom van elektronen veroorzaakt een elektrische stroom . JUIST / FOUT<br />
- Een stroom van neutronen veroorzaakt een elektrische stroom . JUIST / FOUT<br />
4. De edelgasconfiguratie<br />
Atomen “willen” graag een volle buitenste elektronenschil hebben. Dan worden ze namelijk het<br />
minst beïnvloed door andere omringende atomen. Atomen “willen” zo stabiel mogelijk zijn.<br />
Opgave. Zorg dat je voor deze opgave het P.S.E. bij de hand hebt.<br />
1) Herlees de invuloefening op p. 95. Zorg dat je dit goed begrijpt.<br />
2) Lees daarna aandachtig C:\elementaire <strong>chemie</strong>\348_Edelgassen.htm (Start 5. Chemische<br />
binding 5.1. Moleculen en ionen).<br />
3) Beantwoord de volgende vragen:<br />
Wanneer spreken we van een edelgasconfiguratie? ________________________________<br />
____________________________________________________________________<br />
____________________________________________________________________<br />
Bestudeer het PSE. Hoeveel elementen hebben een edelgasconfiguratie? _____ .<br />
Noem deze elementen (geef de naam én het elementsymbool mét de Lewisvoorstelling):<br />
Tabel : de zes edelgassen<br />
Welk van deze elementen heeft geen octetstructuur? ______ .<br />
Wanneer spreken we van een octetstructuur? _____________________<br />
___________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 5
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Vul in (met Elementaire Chemie):<br />
Alle atomen proberen de _______________ __________________________ te verkrijgen.<br />
Dit kan op verschillende manieren gebeuren:<br />
1) Door het vormen van ________________ (= de ______binding).<br />
2) Door het vormen van _______________ (= de _____________binding).<br />
Hoe deze bindingen tot stand komen, leer je in de volgende fiches.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 6
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
39. Positieve en negatieve ionen<br />
1. Positieve ionen<br />
We bekijken eerst de metalen in het P.S.E.<br />
Opdracht: Lees zeer aandachtig C:\elementaire <strong>chemie</strong>\349_Positieve ionen.htm (5.2. Positieve<br />
ionen).<br />
Bekijk zeker ook de simulaties voor het natrium-, magnesium- en aluminiumatoom (klik op de groene<br />
‘play’-knop onderaan rechts op het applet)!<br />
Maak nu de volgende opgaven zonder naar de tekst op Elementaire Chemie te kijken. Verbeter<br />
daarna jezelf met behulp van Elementaire Chemie.<br />
Vul in of schrap wat niet past.<br />
Juist of fout?<br />
De metalen staan hoofdzakelijk links / rechts in het P.S.E.<br />
De meeste metalen hebben meer / minder dan vier valentie-elektronen. Zij kunnen dus het<br />
makkelijkst een edelgasconfiguratie (= volle buitenste schil) bereiken door elektronen af te<br />
staan / op te nemen.<br />
Metalen zijn wel / niet stabiel. De meeste metalen kunnen echter een stabiele<br />
________________configuratie verkrijgen door één, twee of drie ___________________ af<br />
te geven. Dan worden ze positief / negatief geladen. Als voorbeeld bekijken we Na.<br />
Een natriumatoom heeft _______ elektron(en) in de buitenste schil. Door dit ene elektron af<br />
te geven wordt de K / L / M / N - schil de buitenste schil, met daarin ____ elektronen. Het<br />
deeltje dat op die manier ontstaat heeft een stabiele edelgasconfiguratie, maar is niet meer<br />
elektrisch _______________, want de elektronenmantel bevat slechts ____ negatieve<br />
elektronen meer, terwijl er nog altijd 11 positieve ________________ in de kern zitten. Het<br />
neutrale natriumatoom is een positief geladen natrium____ Na+ geworden.<br />
1. Een metaal is een stabiel element. JUIST / FOUT<br />
2. K 1+ is stabiel. JUIST / FOUT<br />
3. Ca 1+ is stabiel. JUIST / FOUT<br />
4. Al 3+ heeft een stabiele edelgasconfiguratie. JUIST / FOUT<br />
De antwoorden vind je onderaan op de volgende pagina.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 7
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Oefening op de nomenclatuur (naamgeving) van de metaalionen. Geef de juiste benaming voor de<br />
volgende ionen (opl. zie Elementaire Chemie):<br />
Na+ __________________________ Fe2+ _______________________<br />
Ca2+ __________________________ Al3+ _______________________<br />
Opdracht: lees Explosief 1.2. p. 164 – 165.<br />
Vraag: Wat zijn elektropositieve elementen?<br />
Antwoord: ________________________________________________________________<br />
________________________________________________________________<br />
Vraag : Welke elementen zijn elektropositief?<br />
Antwoord: De ___________________, omdat ze veel / weinig valentie-elektronen hebben.<br />
Opdracht : Neem het P.S.E. en vergelijk K en Na.<br />
Vul in:<br />
Zowel K als Na hebben _____ elektron(en) in de buitenste schil. Maar omdat _____ meer schillen<br />
heeft dan ____ , bevindt zich het valentie-elektron van ____ verder van de positief geladen kern en<br />
wordt dus sterker / minder sterk door die kern aangetrokken<br />
=> Daarom kan het valentie-elektron van Na zich makkelijker / minder makkelijk van het atoom<br />
losmaken.<br />
=> Daarom zeggen we dat K minder / meer elektropositief is dan Na. (Opl. zie Explosief p. 165) 21<br />
21 Opl. vorige blz. Antw. 1. Fout ; 2. Juist; 3. Fout; 4. Juist; 5. Juist; 6. Fout (geen 8 valentie-elektronen).<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 8
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Negatieve ionen<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\350_Negatieve ionen.htm. Bekijk ook de simulaties voor<br />
chloor en zwavel (chloride-ion en sulfide-ion).<br />
Opgaven:<br />
1) Welke elementen staan uiterst rechts in het P.S.E.? Metalen / niet-metalen<br />
2) Hoe vormen de niet-metalen een edelgasconfiguratie? Ze staan elektronen af /<br />
Ze nemen elektronen op.<br />
3) Wat is de lading van een niet-metaal-ion? Positief / negatief<br />
4) Wat is het enige element dat meer dan twee (dus drie)<br />
Elektronen kan opnemen? ____________<br />
5) Een zwavelatoom (symbool : ____) neemt 2 elektronen op en<br />
vormt een sulfide-ion. Geef de korte schrijfwijze van dat ion : ____________<br />
6) Neem het PSE en leid zelf de ion-schrijfwijze van de volgende<br />
elementen af. Vergelijk daarna met Elementaire Chemie.<br />
Schrijfwijze: Naam van het ion:<br />
Br : _________________ ________________-ion<br />
O : _________________ ________________-ion<br />
S : _________________ ________________-ion<br />
I : _________________ ________________-ion<br />
Opdracht: lees Explosief 1.2. p. 166.<br />
Vraag: Wat is het verschil tussen elektropositieve en elektronegatieve elementen?<br />
Antwoord: ________________________________________________________________<br />
________________________________________________________________<br />
Vraag : Welke elementen zijn elektronegatief?<br />
Antwoord: De ___________________, omdat ze veel / weinig valentie-elektronen hebben.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 9
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Opdracht : Neem het P.S.E. en vergelijk Cl en I (jodium).<br />
Vul in:<br />
Zowel Cl als I hebben _____ elektron(en) in de buitenste schil. Maar omdat _____ meer schillen heeft<br />
dan ____ , bevindt zich de buitenste schil van ____ verder van de positief geladen kern. Het elektron<br />
dat er op de buitenste schil bij moet komen wordt en wordt dus sterker / minder sterk door die kern<br />
aangetrokken.<br />
=> Daarom zal Cl makkelijker / minder makkelijk een extern elektron opnemen dan I.<br />
=> Daarom zeggen we dat Cl minder / meer elektronegatief is dan I. (Opl. zie Explosief p. 166)<br />
Beantwoord de volgende vraag zelf: Waarom is O meer elektronegatief dan S ?<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
Lees het besluit in Explosief 1.2. op p. 166 en neem hieronder (of op de achterzijde) over wat je zelf<br />
belangrijk vindt (of wat je moeilijk zult onthouden). Bestudeer ook de tabel op p. 167 bovenaan.<br />
Begrijp je de plus- en mintekens en de pijlen?<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
________________________________________________________________________________<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 10
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Oefeningen:<br />
1) Rangschik de volgende elementen van meest naar minst elektropositief en leg uit waarom:<br />
Mg O B Al K Ca<br />
2) Rangschik de volgende elementen van meest naar minst elektronegatief en leg uit waarom:<br />
O S F<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 11
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
40. De ionbinding<br />
1. De ionbinding<br />
Vraag : Wat zal er gebeuren wanneer een negatief geladen ion in de buurt van een positief<br />
geladen ion komt?<br />
Antwoord: Ze zullen elkaar aantrekken / afstoten / niet beïnvloeden.<br />
Waarom? Omdat tegengestelde ladingen ____________________________________ .<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\351_Ionbinding.htm.<br />
Opdracht: Bekijk (en beluister!) het filmpje “Reactie tussen natrium en dichloor”.<br />
Een woordje uitleg bij het filmpje: terwijl het natrium smelt, wordt het (positief) geïoniseerd<br />
(de warmte maakt de valentie-elektronen los). Het chloor reageert met de natrium-ionen en<br />
met de vrije elektronen: het ionrooster wordt gevormd. Bij die reactie stijgt de temperatuur<br />
tot meer dan 1000° C (het is dus een zeer exotherme / endotherme reactie).<br />
Beantwoord de vragen:<br />
1) Hoeveel elektronen staat elk Na-atoom af tijdens het smeltproces? _____ .<br />
2) Waarom reageert het gesmolten Na niet met het Ar in de buis?<br />
_________________________________________________________________<br />
3) Waarom reageert het Na wel met het Cl in de buis?<br />
_________________________________________________________________<br />
4) Zoek op : wat is een andere naam voor het eindproduct natriumchloride (NaCl) ?<br />
_____________________________<br />
Leerstof<br />
- Je moet het ontstaan van het ionrooster begrijpen en kunnen uitleggen voor alle gevallen (dus<br />
ook bv. AlBr3 of Al2O3 of andere ion-verbindingen)<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 12
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Lees in de tekst op Elementaire Chemie hoe een ionrooster van NaCl ontstaat.<br />
Neem hieronder het schema over (schema met de groene achtergrond op Elementaire Chemie)<br />
Schrijf de formule voor natriumchloride op drie verschillende manieren (steeds eenvoudiger) :<br />
Bestudeer grondig de simulatie met als titel “Natriumchloride” op Elementaire <strong>chemie</strong> (zorg dat<br />
je elke stap begrijpt!).<br />
Ik heb elke stap begrepen : ja / nee<br />
Bestudeer ook aandachtig de schema’s voor MgS, AlBr3 en Al2O3, tot je het principe beet hebt.<br />
Neem eventueel een of enkele van deze schema’s op de achterzijde over.<br />
Hoeveel broom-ionen zijn er voor elk aluminium-ion in een AlBr3-ionrooster? ____ .<br />
Herhaling : zouten<br />
Alle in deze fiche behandelde ion-verbindingen zijn verbindingen tussen metalen en niet-metalen. In<br />
LPF 33 (pagina Fout! Bladwijzer niet gedefinieerd.) zagen we dat we zulke (M,NM)-verbindingen<br />
zouten noemen. Weet je nog of zouten de elektrische stroom geleiden? (Blader even terug…)<br />
Oefening : Schrijf de juiste verhoudingsformules van de volgende zouten (zoals in het voorbeeld):<br />
A Ca … I … Ca I2<br />
B Cu + … S… <br />
C K… N… D Fe 3+ … S… <br />
E Ca… N… F Li… F… <br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 13
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
G Mg… O… H Ga… Br… <br />
I Rb… S… J Pb 4+ … O… <br />
K Pb 4+ … N… L Al… Cl… <br />
Oplossing: zie C:\elementaire <strong>chemie</strong>\351_Ionbinding.htm.<br />
Samenvatting : de ionbinding<br />
Metalen geven graag één of meer elektronen af. Hierbij ontstaan _______________<br />
metaalionen (+ , 2+ , 3+ , 4+).<br />
Niet-metalen nemen graag één of meer elektronen op. Hierbij ontstaan _____________<br />
niet-metaalionen (- , 2- , 3-).<br />
Deze __________________-geladen ionen trekken elkaar zeer sterk aan: er wordt een<br />
__________________ gevormd. Het ion___________ dat ontstaat bevat positieve<br />
metaal- en negatieve niet-metaalionen. Het aantal van beide ionen hangt af van de<br />
ladingen. Uiteraard is het totaal aantal elektronen dat afgegeven werd door het metaal<br />
gelijk aan / groter dan / kleiner dan het totaal aantal elektronen dat opgenomen werd<br />
door het niet-metaal. Met andere woorden: het totaal aantal positieve ladingen is gelijk<br />
aan het totaal aantal negatieve ladingen (_______________________).<br />
Opgelet!<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 14
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
2. Het ionrooster<br />
Lees C:\elementaire <strong>chemie</strong>\351b_Ionroosters.htm (5.2. Ionroosters).<br />
Beantwoord de vragen:<br />
1) Hoe ontstaat een ionrooster?<br />
2) Waarom liggen smelt- en kookpunt van zouten (ionverbindingen) doorgaans hoog?<br />
3) a) Bij welke temperatuur smelt NaCl (keukenzout) ? ______________________<br />
b) Bij welke temperatuur kookt NaCl ? ______________________<br />
4) Waarom geleiden zouten (in vaste toestand) de elektrische stroom niet?<br />
5) Waarom geleiden zouten in vloeibare toestand de elektrische stroom wel?<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 15
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Teken schematisch een ionrooster in vaste toestand en daarnaast de deeltjes in gesmolten toestand:<br />
Vast Vloeibaar<br />
3. Nomenclatuur (alleen 2u, maar wel zeer nuttig voor 1u – en niet zo moeilijk)<br />
Di-ijzer-tri-sulfide : diijzertrisulfide is de naam voor Fe2S3. De naamgeving van chemische<br />
verbindingen lijkt heel complex, maar is eenvoudiger dan je zou denken!<br />
Lees C:\elementaire <strong>chemie</strong>\352_Nomenclatuur ionverbindingen.htm. Je leert er, hoe de namen van<br />
ionverbindingen tot stand komen.<br />
Vul de Griekse voorvoegsels aan :<br />
1 __________ (meestal weggelaten)<br />
2<br />
3<br />
4<br />
5<br />
6<br />
Vul de namen in (alle oplossing op C:\elementaire <strong>chemie</strong>\352_Nomenclatuur ionverbindingen.htm):<br />
I)<br />
Zout Naam van het zout<br />
FeCl2<br />
FeCl3<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 16
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Cu2O<br />
CuO<br />
FeS<br />
Fe2S3<br />
II) Geef de namen van de volgende zouten (soms zijn twee namen mogelijk)<br />
A CaI2 (geen tweede naam)<br />
B Cu2S<br />
C K3N (geen tweede naam)<br />
D Fe2S3<br />
E Ca3N2 (geen tweede naam)<br />
F LiF (geen tweede naam)<br />
G MgO (geen tweede naam)<br />
H GaBr3 (geen tweede naam)<br />
I Rb2S (geen tweede naam)<br />
J PbO2<br />
K Pb3N4<br />
L AlCl3 (geen tweede naam)<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 17
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Geef de formule en minstens één naam van de volgende zouten:<br />
A Fe 3+ …O…<br />
B Hg + …S…<br />
C Cu + …Cl…<br />
D Pb 2+ …Br…<br />
E Cu 2+ …Cl…<br />
F Fe 2+ …O…<br />
G Pb 4+ …O…<br />
H Hg 2+ …S…<br />
Op C:\elementaire <strong>chemie</strong>\352_Nomenclatuur ionverbindingen.htm, onderaan op de pagina vind je<br />
vier afsluitende oefeningen over zouten : formules en nomenclatuur.<br />
Als je deze oefeningen goed beheerst, word je nog een echte kampioen in chemische formules en<br />
naamgeving!<br />
Tip: maak vooral oefeningen 1 en 4. De oefeningen 2 en 3 zijn extra’s voor de liefhebbers.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 18
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
41. De atoombinding (covalente binding)<br />
Na de ionbinding leer je in deze fiche een tweede binding kennen: de atoombinding. In de volgende<br />
fiche sluiten we dit hoofdstuk af met een derde soort binding, de metaalbinding.<br />
1. Eerste kennismaking met de atoombinding : de dichloormolecule<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\353_Atoombinding.htm (of: start => 5.3. Atoombinding). Vul<br />
vervolgens in:<br />
Stel je voor dat in een bepaalde ruimte alleen maar chlooratomen aanwezig zijn.<br />
Vul de tabel aan:<br />
Element Protonengetal<br />
Elektronenconfiguratie<br />
Cl __________ ____________<br />
Lewisvoorstelling<br />
Om de stabiele ____________________configuratie (= een volle ________________ elektronenschil)<br />
te bereiken, moet elk chloor-atoom slechts één ____________________ opnemen. Dat proberen alle<br />
aanwezige chlooratomen dan ook te doen.<br />
Er zal dus geen enkel Cl-atoom bereid zijn om een elektron _________________________. Toch<br />
kunnen de chlooratomen een stabiele edelgasconfiguratie verkrijgen en wel op de volgende manier:<br />
De chlooratomen zullen, per twee, hun ongepaarde elektronen omvormen tot een<br />
________________________ elektronen_________. Daardoor krijgen __________<br />
___________________ een stabiele edelgasconfiguratie. Dit is echter slechts het geval zolang de<br />
beide chlooratomen samenblijven: m.a.w. ze zijn aan elkaar gebonden door middel van een<br />
zogenaamde _________________________ (vaak ook ________________ binding genoemd).<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 19
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Opgave : Teken een dichloormolecule (Cl2) schematisch op drie verschillende manieren:<br />
1. Met alle valentieelektronen<br />
(gebruik<br />
twee kleuren):<br />
2. Met een<br />
bindingsstreepje<br />
voor het<br />
gemeenschappelijk<br />
elektronenpaar<br />
3. Met streepjes voor<br />
alle gepaarde<br />
elektronen (de<br />
gangbare voorstelling<br />
van<br />
atoombindingen)<br />
Dergelijke _________________ deeltjes, bestaande uit twee of meer atomen die aan elkaar<br />
gebonden zijn door middel van ____________bindingen, noemen we ________________________.<br />
In het bovenstaande voorbeeld (atoombinding van Cl) spreken we van een<br />
_______________molecule, die we kortweg voorstellen als _____.<br />
Bekijk de simulatie “dichloor” op C:\elementaire <strong>chemie</strong>\353_Atoombinding.htm (klik op de groene<br />
“play”-knop)<br />
3. Andere voorbeelden van atoombindingen<br />
Bestudeer nu de andere voorbeelden op C:\elementaire <strong>chemie</strong>\353_Atoombinding.htm : H2, HCl,<br />
CH4, CCl4, 02 en N2. Bekijk ook telkens de simulaties.<br />
Beantwoord vervolgens de vragen, zonder naar Elementaire Chemie te kijken. Daarna kun je je<br />
antwoorden controleren.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 20
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
1) Geef van elke molecule de naam en de symbolische schrijfwijze.<br />
Formule Naam<br />
H2 ____________stof<br />
HCl water______________ide<br />
CH4 meth_____n<br />
CCl4 tetra__________methaan<br />
O2 di____________<br />
N2 di___________<br />
Symbolisch (met<br />
elektronen)<br />
2) Wat is er speciaal aan de diwaterstofmolecule (bv. in vergelijking met dichloor)?<br />
4. Besluit (goed kennen!)<br />
Symbolisch (met<br />
gepaarde elektronen)<br />
Wanneer ______________________ onderling reageren, ontstaan neutrale<br />
__________________, waarin de atomen aan elkaar gebonden zijn door de<br />
aanwezigheid van één of meer gemeenschappelijke ______________________. Dit soort<br />
bindingen noemen we __________________________ .<br />
We spreken van enkelvoudige, dubbele of drievoudige atoombindingen als er _____,<br />
_____ of _______ gemeenschappelijke elektronenparen zijn tussen de twee atomen.<br />
Structuurformule (met A en B) voor de bindingen (met streepjes voor alle gepaarde elektronen):<br />
Enkelvoudige atoombinding Dubbele atoombinding Drievoudige atoombinding<br />
A B<br />
A B<br />
A B<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 21
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
5. Oefening<br />
1) Geef de structuurformule van de moleculen waaruit de volgende stoffen opgebouwd zijn<br />
(onder de opgave vind je een stappenplan om zulke oefeningen te maken):<br />
A H2S B I2<br />
C ICl D NH3<br />
E Br2 F H2O<br />
G CO2 H HF<br />
I PCl3 (J) HCN<br />
Tip! Vraag: Hoe los je deze oefening het makkelijkst op?<br />
Antwoord: stappenplan<br />
(oef. J: facultatief)<br />
(1) Teken van alle atomen de Lewis-voorstelling.<br />
(2) “Leg de puzzel” tot je een atoombinding hebt (alle buitenste schillen zijn gevuld,<br />
enkele elektronen zijn gemeenschappelijk voor twee atomen).<br />
(3) Controleer je resultaat : tel het aantal valentie-elektronen voor elk atoom. Het<br />
moet gelijk zijn aan 8 (Uitzondering: waterstof H 2 valentie-elektronen).<br />
Uitgewerkt voorbeeld : diwaterstofsulfide, H2S.<br />
Deze molecule bestaat uit twee H-atomen en één S-atoom.<br />
(1) Teken (Lewisvoorstelling) tweemaal een waterstofatoom en eenmaal een zwavelatoom.<br />
(2) Vraag je af hoe de valentie-elektronen zich zo kunnen verbinden, dat alle atomen (door<br />
“samen te werken”) een edelgasconfiguratie verkrijgen (er is maar één mogelijkheid).<br />
Stel de structuur voor met gepaarde elektronen (vul aan!):<br />
H S H<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 22
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
(3) Controleer of alle atomen in de atoombinding (hier: H2S) een edelgasconfiguratie hebben.<br />
Edelgasconfiguratie? Waterstof: JA / NEE Zwavel: JA / NEE<br />
Begrepen? Maak dan nu de oefening voor alle verbindingen in de tabel. De laatste oefening (HCN)<br />
moet je niet maken, maar is wel een ultieme test: als je dit kunt, beheers je de atoombinding!<br />
De oplossingen vind je op C:\elementaire <strong>chemie</strong>\353_Atoombinding.htm (of: start => 5.3.<br />
Atoombinding), onderaan op de pagina.<br />
6. Atoom- en molecuulroosters<br />
Bij de ionbinding leerde je : ionen trekken elkaar aan omdat ze een tegengestelde elektrische lading<br />
hebben. Zo ontstaat een “ionrooster” van miljarden moleculen: dit noemen we zouten.<br />
De elektrische aantrekkingskrachten in een ionrooster zijn zeer sterk => zouten hebben een hoge<br />
smelttemperatuur.<br />
Dat wist je al. Maar hoe sterk is de binding van moleculen?<br />
Kennen:<br />
De moleculen die bij de atoombinding ontstaan (bv. HCl of CO2) zijn elektrisch neutraal. Deze<br />
moleculen trekken elkaar weliswaar aan, maar niet door (sterke) elektrische krachten, wel door een<br />
zwakke aantrekkingskracht die we de vanderwaalskracht noemen 22 .<br />
Net zoals bij ionen ontstaan door de aantrekkingskracht tussen moleculen van de atoombinding ook<br />
roosters. Deze noemen we “molecuulroosters”. Omdat de vanderwaalskracht zo zwak is, kunnen<br />
molecuulroosters makkelijk uit elkaar vallen.<br />
Gevolg:<br />
Molecuulverbindingen hebben een laag _________punt. Vele zijn op kamertemperatuur al vloeibaar.<br />
Zelfs wanneer ze op kamertemperatuur vast zijn, verdampen ze snel. Sommige (bv. dijood)<br />
sublimeren zelfs 23 .<br />
22 Vanderwaalskrachten kun je je nog het best voorstellen als cohesie- en adhesiekrachten op microscopische<br />
schaal.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 23
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Vul de tabel aan:<br />
NAAM FORMULE<br />
SMELTPUNT<br />
(°C)<br />
KOOKPUNT<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 24<br />
(°C)<br />
AGGREGATIETOESTAND<br />
(normale omstandigheden:<br />
kamertemperatuur, p=1<br />
atm.)<br />
diwaterstof H2 -259 -253 gasvormig<br />
dizuurstof O2 -218 -183 gasvormig<br />
dichloor Cl2 -101 -35 gasvormig<br />
dibroom Br2 -7 59 vloeibaar<br />
dijood I2 114 sublimeert vast<br />
koolstofdioxide CO2 sublimeert bij -78 gasvormig<br />
water H2O 0 100 vloeibaar<br />
difosforpentaoxide P2O5 580 sublimeert bij 300 vast<br />
fosforpentachloride PCl5 -92 75 vloeibaar<br />
zwaveldioxide SO2 -74 -10 gasvormig<br />
23 Sublimeren : rechstreeks overgaan van vast naar gasvormig, zonder eerst te smelten [op elementaire<br />
<strong>chemie</strong> staat verkeerdelijk: “van vloeibaar naar gasvormig”. Dat moet dus zijn: van vast naar gasvormig!].
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Besluit:<br />
Deze vaststellingen wijzen er op dat de _______________krachten tussen de moleculen<br />
onderling (dit noemen we ________moleculaire krachten) eerder klein zijn. We spreken<br />
in dit geval van “van__________________krachten”.<br />
De atoombindingen, dus de bindingen tussen de atomen in de moleculen<br />
(___________moleculaire krachten) zijn sterker.<br />
Bij het verwarmen van een vaste molecuulverbinding komen de moleculen uit het<br />
m_________________________ los. De _______________ blijven echter wel aan elkaar<br />
gebonden. Om die atoombindingen te breken is __________________________ nodig.<br />
*Het belangrijkste begrepen? Omcirkel het juiste antwoord<br />
1) Welke krachten zijn het sterkst bij de atoombinding (covalente binding) ?<br />
De krachten tussen de atomen / De krachten tussen de moleculen<br />
2) Wat valt dus het snelst uit elkaar?<br />
Het molecuulrooster / De moleculen zelf<br />
3) Welk rooster heeft meer energie (bv. warmte) nodig om uit elkaar te vallen?<br />
Het ionrooster (van de ionbinding) / het atoomrooster (van de atoombinding)<br />
*Vul de tekening aan. Gebruik twee kleuren.<br />
Het ________________rooster valt uiteen bij het smelten. De<br />
______________ blijven echter wel aan elkaar gebonden (zowel in vloeibare<br />
als in gasvormige toestand).<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 25
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Geleidt water (H20) de elektrische stroom?<br />
Bekijk de proef “geleidingsvermogen van water” (video) op C:\elementaire <strong>chemie</strong>\354_Atoom- en<br />
molecuulroosters.htm.<br />
Dezelfde waarneming geldt ook voor andere atoombindingen.<br />
Besluit. Vul in: neutraal / geleidend; wel / niet:<br />
Moleculen zijn elektrisch __________________ en geleiden dus de elektrische stroom zelfs in<br />
gesmolten toestand ________________.<br />
7. Diamant en grafiet : allebei zuiver koolstof<br />
Lees de alinea “atoomrooster” op C:\elementaire <strong>chemie</strong>\354_Atoom- en molecuulroosters.htm.<br />
Zijn de volgende beweringen juist of fout?<br />
1) Diamant is opgebouwd uit C-atomen. JUIST / FOUT<br />
2) Grafiet is opgebouwd uit C-atomen. JUIST / FOUT<br />
3) Diamant en grafiet zijn dus uit identiek dezelfde atomen opgebouwd. JUIST / FOUT<br />
4) Diamant geleidt de stroom. JUIST / FOUT<br />
5) Grafiek geleidt de stroom. JUIST / FOUT<br />
6) Diamant heeft een hogere dichtheid dan grafiet. JUIST / FOUT<br />
7) *Diamant is een molecuulrooster. JUIST / FOUT<br />
8) *Grafiet is een molecuulrooster. JUIST / FOUT<br />
Noem twee voorbeelden van het gebruik van grafiet :<br />
Noem twee voorbeelden van het gebruik van diamant:<br />
Leg met je eigen woorden uit waarom diamant een harde stof is, terwijl grafiet (dat<br />
uit dezelfde C-atomen bestaat) een zeer zachte stof is:<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 26
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Teken links een diamantrooster en rechts de structuur van grafiet (zie ook Explosief<br />
1.2. p. 188-189).<br />
8. Nomenclatuur van molecuulverbindingen<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\355_Nomenclatuur molecuulverbindingen.htm (of via “start<br />
=> 5.3. Atoombinding). Bestudeer de voorbeelden tot je het systeem van naamgeving begrijpt.<br />
Oefening. Geef de naam van de volgende molecuulverbindingen.<br />
A SF2<br />
B BH3<br />
C SF4<br />
D PCl3<br />
E ClF3<br />
F BrF5<br />
G SF6<br />
Oplossing: C:\elementaire <strong>chemie</strong>\355_Nomenclatuur molecuulverbindingen.htm (onderaan de<br />
pagina). 24<br />
Slotoefening: maak de drie oefeningen “Niet-zouten” op C:\elementaire <strong>chemie</strong>\355_Nomenclatuur<br />
molecuulverbindingen.htm (onderaan de pagina).<br />
24 Oplossing vorige blz.: 1) juist, 2) juist, 3) juist, 4) fout, 5) juist, 6) juist, 7) fout (het is een atoomrooster:<br />
bestaat uit louter atoombindingen), 8) fout (elke laag is een atoomrooster; de lagen zelf zijn door<br />
vanderwaalskrachten verbonden en dus makkelijk te scheiden).<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 27
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
42. De metaalbinding<br />
Lees aandachtig C:\elementaire <strong>chemie</strong>\356_Metaalbinding.htm (of start => 5.4.<br />
Metaalbinding). Beantwoord vervolgens de vragen.<br />
1. Vul in en schrap wat niet past:<br />
In een metaalrooster geven alle metaalatomen _________________ af, om op die manier een<br />
________________ _________________ te verkrijgen.<br />
Zo ontstaat een rooster van positieve / negatieve ionen, die elkaar aantrekken / afstoten.<br />
De vrije _________________ vormen een “________________zee” : ze kunnen zich vrij door het<br />
rooster bewegen. Door hun positieve / negatieve lading houden deze vrije elektronen het rooster<br />
samen.<br />
Metaalbinding van zink (bron: Wikipedia) 3D-voorstelling van een metaalrooster. Positieve ionen worden<br />
omringd door gedelocaliseerde elektronen.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 28
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Uitsmijter :<br />
De tekening rechts op de vorige pagina vond ik op een webpagina in het Afrikaans. De tekst bij de<br />
afbeelding luidde: “Positiewe atoomkerne (+) omring deur gedelokaliseerde elektrone (∙)”<br />
Afrikaans, dat vooral in Zuid-Afrika en Namibië gesproken wordt, lijkt zeer goed op Nederlands (het is<br />
ontstaan uit het Nederlands). Met wat volgt kun je een stukje <strong>chemie</strong> in het Afrikaans herhalen.<br />
Begrijp je alles? (Luidop lezen helpt)<br />
Die eienskappe van metale (Ndl.: De eigenschappen<br />
van metalen)<br />
Metale het (= hebben) verskeie unieke eienskappe wat as volg opgesom<br />
word:<br />
Termiese geleiers. Metale is goeie geleiers van hitte en word daarom<br />
in kosmaaktoerusting soos potte en panne gebruik.<br />
Elektriese geleiers. Metale is goeie geleiers van elektrisiteit en word<br />
daarom in elektriese geleidingsdrade gebruik.<br />
Blink metaliese skyn. Metale het 'n kenmerkende blink voorkoms en<br />
word gereeld gebruik in juweliersware. Die vrybewegingde elektrone<br />
is in staat om lig teen alle frekwensie te absorbeer en weerkaats, wat<br />
metale blink en gepoleer laat voorkom.<br />
Smeebaar en pletbaar. Hiermee word bedoel dat metale in<br />
verskillende vorme gebuig kan word sonder om te breek (smeebaar)<br />
en gerek kan word tot dun drade (pletbaar) soos koperdraad, wat<br />
gebruik kan word om eletrisiteit te gelei. Bogenoemde is moontlik<br />
omdat die bindings nie in 'n bepaalde rigting vas is nie en die atome<br />
maklik oor mekaar kan gly.<br />
Smeltpunt. Metale het gewoonlik 'n hoë smeltpunt en kan daarom<br />
gebruik word om artikels wat hoë temperature moet weerstaam, soos<br />
kookpotte, te vervaardig. Die hoë smeltpunt kan toegeskryf word aan<br />
die sterkte van metaalbindings.<br />
Digtheid. Metale het 'n hoë digtheid omdat hul atome styf teen<br />
mekaar geleë is.<br />
Meer Afrikaans lezen? Meer weten?<br />
Het vervolg van de tekst over de metaalbinding vind je op:<br />
http://cnx.org/content/m39162/latest/<br />
Tien wenken voor Afrikaans sprekenden die Nederlands willen leren:<br />
http://nederlandsvirafrikaanses.weebly.com/top-10-wenke.html<br />
Zie ook http://nl.wikipedia.org/wiki/Afrikaans<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 29
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
43. Samenvatting : de chemische binding<br />
Tot slot van dit hoofdstuk over chemische bindingen maak je een schematisch overzicht van de drie<br />
bindingen (ionbinding, atoombinding, metaalbinding) met hun eigenschappen.<br />
TAAK<br />
Opdracht: Leg aan de hand van een overzichtelijke tabel uit welke de verschillende chemische<br />
bindingen zijn, bij welke soorten stoffen ze optreden en waarom die stoffen een hoog of laag<br />
smeltpunt hebben.<br />
Dien je taak in op de afgesproken datum.<br />
Let op : je moet je eigen schema kunnen gebruiken om de bindingen aan andere leerlingen (met 1<br />
lesuur <strong>chemie</strong> per week) uit te leggen.<br />
Tip: lees Explosief 1.2. p. 187 – 190 alvorens je de taak maakt.<br />
1. Oefeningen<br />
1) Tot welk verbindingstype behoren de volgende stoffen?<br />
Kruis aan om welke binding het gaat.<br />
Symbool Ionbinding Atoombinding Metaalbinding<br />
Na2S<br />
H2S<br />
S8<br />
Na<br />
CO2<br />
BaCl2<br />
Cu<br />
He<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 30
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
Overzicht van de drie soorten bindingen<br />
De ionbinding : sterke binding tussen positieve metaal-ionen (M+) en negatieve niet-metaal-ionen<br />
(NM–). Vier belangrijke kenmerken :<br />
1. Ontstaan. Eén (M-)atoom staat elektronen af, een ander (NM-)atoom neemt deze<br />
elektronen op. Zo ontstaan twee tegengesteld geladen deeltjes. Die trekken elkaar<br />
aan => Er ontstaat een “rooster” van ionbindingen. Men noemt dit “zouten”.<br />
2. Neutraal. Per binding is het totale aantal positieve ladingen steeds gelijk aan het<br />
totale aantal negatieve ladingen (equivalentieregel). Een ionbinding is dus elektrisch<br />
neutraal => zouten geleiden de elektrische stroom niet (in de vaste toestand).<br />
3. Sterk. Door de elektrische aantrekkingskracht tussen de ionen is de ionbinding zeer<br />
sterk. Daarom hebben zouten een hoog smeltpunt (er is veel warmte (energie) nodig<br />
om de binding los te maken).<br />
4. Vast. De ionbinding bestaat alleen in de vaste toestand : bij het smelten wordt de<br />
binding verbroken => de ionen maken zich los uit het rooster => geladen deeltjes<br />
zweven rond in de vloeistof => gesmolten zouten geleiden de stroom.<br />
<strong>2012</strong>-<strong>2013</strong> Chemische binding<br />
Freinetschool Villa da Vinci 31
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
VI. Formules en reactievergelijkingen<br />
44. Formules en reactievergelijkingen<br />
<strong>2012</strong>-<strong>2013</strong> Formules en reactievergelijkingen<br />
Freinetschool Villa da Vinci 32
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
<strong>2012</strong>-<strong>2013</strong> Formules en reactievergelijkingen<br />
Freinetschool Villa da Vinci 33
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
<strong>2012</strong>-<strong>2013</strong> Formules en reactievergelijkingen<br />
Freinetschool Villa da Vinci 34
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
<strong>2012</strong>-<strong>2013</strong> Formules en reactievergelijkingen<br />
Freinetschool Villa da Vinci 35
LPF Chemie – 3 <strong>FRWET</strong> Naam: ____________<br />
<strong>2012</strong>-<strong>2013</strong> Formules en reactievergelijkingen<br />
Freinetschool Villa da Vinci 36