La spettroscopia - danielegasparri.com
La spettroscopia - danielegasparri.com
La spettroscopia - danielegasparri.com
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Possiamo immaginare ogni atomo <strong>com</strong>e il classico modello planetario, con il nucleo centrale e gli<br />
elettroni che vi ruotano intorno.<br />
L’elettrone ha delle orbite fissate, alle quali <strong>com</strong>pete una ben determinata energia. Quando<br />
l’elettrone incontra un fotone esattamente dell’energia necessaria per poter passare da un livello<br />
energetico ad un altro (cambiare orbita), allora il fotone viene assorbito e l’elettrone si sposta su<br />
un’orbita più esterna.<br />
L’elettrone però ha la tendenza a tornare spontaneamente nel livello energetico (orbita) con energia<br />
minore (più vicino al nucleo) e quando viene <strong>com</strong>piuto questo salto, esso emette un fotone pari alla<br />
differenza di energia delle due orbite, in una direzione casuale.<br />
I processi di assorbimento ed emissione sono quindi legati.<br />
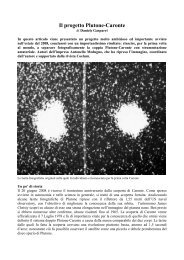
Assorbimento ed emissione di un fotone da parte di un elettrone legato al proprio nucleo atomico. Quando il fotone<br />
incidente ha esattamente la stessa energia che serve all’elettrone per <strong>com</strong>piere uno o più salti orbitali, esso viene<br />
assorbito e l’elettrone si porta su un livello energetico maggiore. Se l’energia del fotone non è esatta, esso non viene<br />
assorbito. Questi stadi non sono stabili e dopo circa 1 miliardesimo di secondo l’elettrone torna al livello fondamentale,<br />
emettendo un fotone che ha un’energia pari alla differenza energetica tra due livelli. Questo meccanismo è alla base<br />
dello spettro a righe.<br />
Ad ogni assorbimento corrisponde un’emissione successiva. <strong>La</strong> situazione però non è totalmente<br />
simmetrica, almeno dal punto di vista numerico e dinamico.<br />
L’elettrone ad esempio può assorbire un fotone che gli permette di fare un doppio salto e poi cedere<br />
la sua energia con due salti distinti, emettendo quindi due fotoni di energia minore rispetto a quello<br />
assorbito (ma l’energia totale sarà la stessa!); la direzione del fotone emesso inoltre è casuale.<br />
Quando si ha assorbimento si ha anche emissione, sebbene noi possiamo osservare solo uno di<br />
questi effetti.<br />
Nel caso del Sole e delle stelle, il gas presente nell’atmosfera è più freddo della fotosfera. <strong>La</strong> luce<br />
proveniente dalla fotosfera viene intercettata dal gas, che assorbe le lunghezze d’onda opportune.<br />
Subito dopo si verifica l’emissione, solo che questa avviene in direzione casuale; ne consegue che<br />
l’effetto netto è quello di un assorbimento della luce diretta verso l’osservatore. Supponiamo infatti<br />
che un atomo assorba 10 fotoni e ne riemetta 10 identici l’istante successivo. I 10 fotoni che assorbe<br />
provengono dalla fotosfera e sono diretti tutti verso l’osservatore.