4. Nombra los siguientes óxido metálicos: Nomenclatura tradicional ...
4. Nombra los siguientes óxido metálicos: Nomenclatura tradicional ...
4. Nombra los siguientes óxido metálicos: Nomenclatura tradicional ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Formulación: Compuestos binarios y ternarios. Respuestas a <strong>los</strong> ejercicios.<br />
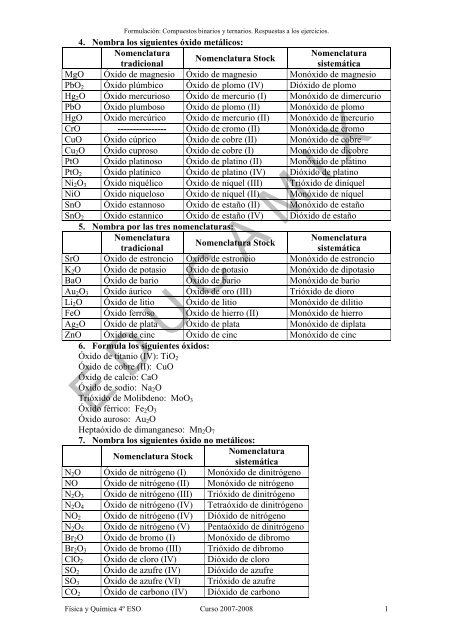
<strong>4.</strong> <strong>Nombra</strong> <strong>los</strong> <strong>siguientes</strong> <strong>óxido</strong> <strong>metálicos</strong>:<br />
<strong>Nomenclatura</strong><br />
<strong>tradicional</strong><br />
<strong>Nomenclatura</strong> Stock<br />
<strong>Nomenclatura</strong><br />
sistemática<br />
MgO Óxido de magnesio Óxido de magnesio Mon<strong>óxido</strong> de magnesio<br />
PbO2 Óxido plúmbico Óxido de plomo (IV) Di<strong>óxido</strong> de plomo<br />
Hg2O Óxido mercurioso Óxido de mercurio (I) Mon<strong>óxido</strong> de dimercurio<br />
PbO Óxido plumboso Óxido de plomo (II) Mon<strong>óxido</strong> de plomo<br />
HgO Óxido mercúrico Óxido de mercurio (II) Mon<strong>óxido</strong> de mercurio<br />
CrO ---------------- Óxido de cromo (II) Mon<strong>óxido</strong> de cromo<br />
CuO Óxido cúprico Óxido de cobre (II) Mon<strong>óxido</strong> de cobre<br />
Cu2O Óxido cuproso Óxido de cobre (I) Mon<strong>óxido</strong> de dicobre<br />
PtO Óxido platinoso Óxido de platino (II) Mon<strong>óxido</strong> de platino<br />
PtO2 Óxido platínico Óxido de platino (IV) Di<strong>óxido</strong> de platino<br />
Ni2O3 Óxido niquélico Óxido de níquel (III) Tri<strong>óxido</strong> de diníquel<br />
NiO Óxido nique<strong>los</strong>o Óxido de níquel (II) Mon<strong>óxido</strong> de níquel<br />
SnO Óxido estannoso Óxido de estaño (II) Mon<strong>óxido</strong> de estaño<br />
SnO2 Óxido estannico Óxido de estaño (IV) Di<strong>óxido</strong> de estaño<br />
5. <strong>Nombra</strong> por las tres nomenclaturas:<br />
<strong>Nomenclatura</strong><br />
<strong>tradicional</strong><br />
<strong>Nomenclatura</strong> Stock<br />
<strong>Nomenclatura</strong><br />
sistemática<br />
SrO Óxido de estroncio Óxido de estroncio Mon<strong>óxido</strong> de estroncio<br />
K2O Óxido de potasio Óxido de potasio Mon<strong>óxido</strong> de dipotasio<br />
BaO Óxido de bario Óxido de bario Mon<strong>óxido</strong> de bario<br />
Au2O3 Óxido áurico Óxido de oro (III) Tri<strong>óxido</strong> de dioro<br />
Li2O Óxido de litio Óxido de litio Mon<strong>óxido</strong> de dilitio<br />
FeO Óxido ferroso Óxido de hierro (II) Mon<strong>óxido</strong> de hierro<br />
Ag2O Óxido de plata Óxido de plata Mon<strong>óxido</strong> de diplata<br />
ZnO Óxido de cinc Óxido de cinc Mon<strong>óxido</strong> de cinc<br />
6. Formula <strong>los</strong> <strong>siguientes</strong> <strong>óxido</strong>s:<br />
Óxido de titanio (IV): TiO2<br />
Óxido de cobre (II): CuO<br />
Óxido de calcio: CaO<br />
Óxido de sodio: Na2O<br />
Tri<strong>óxido</strong> de Molibdeno: MoO3<br />
Óxido férrico: Fe2O3<br />
Óxido auroso: Au2O<br />
Hepta<strong>óxido</strong> de dimanganeso: Mn2O7<br />
7. <strong>Nombra</strong> <strong>los</strong> <strong>siguientes</strong> <strong>óxido</strong> no <strong>metálicos</strong>:<br />
<strong>Nomenclatura</strong> Stock<br />
<strong>Nomenclatura</strong><br />
sistemática<br />
N2O Óxido de nitrógeno (I) Mon<strong>óxido</strong> de dinitrógeno<br />
NO Óxido de nitrógeno (II) Mon<strong>óxido</strong> de nitrógeno<br />
N2O3 Óxido de nitrógeno (III) Tri<strong>óxido</strong> de dinitrógeno<br />
N2O4 Óxido de nitrógeno (IV) Tetra<strong>óxido</strong> de dinitrógeno<br />
NO2 Óxido de nitrógeno (IV) Di<strong>óxido</strong> de nitrógeno<br />
N2O5 Óxido de nitrógeno (V) Penta<strong>óxido</strong> de dinitrógeno<br />
Br2O Óxido de bromo (I) Mon<strong>óxido</strong> de dibromo<br />
Br2O3 Óxido de bromo (III) Tri<strong>óxido</strong> de dibromo<br />
ClO2 Óxido de cloro (IV) Di<strong>óxido</strong> de cloro<br />
SO2 Óxido de azufre (IV) Di<strong>óxido</strong> de azufre<br />
SO3 Óxido de azufre (VI) Tri<strong>óxido</strong> de azufre<br />
CO2 Óxido de carbono (IV) Di<strong>óxido</strong> de carbono<br />
E D U C A M I X<br />
Física y Química 4º ESO Curso 2007-2008 1
Formulación: Compuestos binarios y ternarios. Respuestas a <strong>los</strong> ejercicios.<br />
8. Formula <strong>los</strong> <strong>siguientes</strong> <strong>óxido</strong>s:<br />
Óxido de fósforo (III): P2O3<br />
Penta<strong>óxido</strong> de difósforo: P2O5<br />
Óxido de boro: B2O3<br />
Tri<strong>óxido</strong> de diyodo: I2O3<br />
Óxido de selenio (VI): SeO3<br />
Tri<strong>óxido</strong> de teluro: TeO3<br />
Óxido de arsénico (III): As2O3<br />
Tri<strong>óxido</strong> de difósforo: P2O3<br />
Óxido de yodo (V): I2O5<br />
9. <strong>Nombra</strong> <strong>los</strong> <strong>siguientes</strong> hidruros <strong>metálicos</strong>:<br />
<strong>Nomenclatura</strong><br />
<strong>tradicional</strong><br />
<strong>Nomenclatura</strong> Stock<br />
<strong>Nomenclatura</strong><br />
sistemática<br />
NaH Hidruro de sodio Hidruro de sodio Hidruro de sodio<br />
LiH Hidruro de litio Hidruro de litio Hidruro de litio<br />
KH Hidruro de potasio Hidruro de potasio Hidruro de potasio<br />
CaH2 Hidruro de calcio Hidruro de calcio Dihidruro de calcio<br />
SnH4 Hidruro estannico Hidruro de estaño (IV) Tetrahidruro de estaño<br />
PbH2 Hidruro plumboso Hidruro de plomo (II) Dihidruro de plomo<br />
FeH2 Hidruro ferroso Hidruro de hierro (II) Dihidruro de hierro<br />
FeH3 Hidruro férrico Hidruro de hierro (III) Trihidruro de hierro<br />
AlH3 Hidruro de aluminio Hidruro de aluminio Trihidruro de aluminio<br />
CuH2 Hidruro cúprico Hidruro de cobre (II) Dihidruro de cobre<br />
AuH Hidruro auroso Hidruro de oro (I) Monohidruro de oro<br />
NiH2 Hidruro nique<strong>los</strong>o Hidruro de níquel (II) Dihidruro de níquel<br />
CuH Hidruro cuproso Hidruro de cobre (I) Monohidruro de cobre<br />
10. Formula <strong>los</strong> <strong>siguientes</strong> hidruros:<br />
Hidruro de cesio: CsH<br />
Hidruro de cinc: ZnH2<br />
Hidruro de magnesio: MgH2<br />
Hidruro de titanio (IV): TiH4<br />
Hidruro de estaño (IV): SnH4<br />
Hidruro de cobalto (II): CoH2<br />
Hidruro de cromo (III): CrH3<br />
Dihidruro de estaño: SnH2<br />
11. <strong>Nombra</strong> las <strong>siguientes</strong> sales binarias:<br />
<strong>Nomenclatura</strong><br />
<strong>tradicional</strong><br />
<strong>Nomenclatura</strong> Stock<br />
<strong>Nomenclatura</strong><br />
sistemática<br />
CaF2 Fluoruro de calcio Fluoruro de calcio Difluoruro de calcio<br />
FeCl2 Cloruro ferroso Cloruro de hierro (II) Dicloruro de hierro<br />
FeCl3 Cloruro férrico Cloruro de hierro (III) Tricloruro de hierro<br />
PbI2 Yoduro plumboso Yoduro de plomo (II) Diyoduro de plomo<br />
KBr Bromuro de potasio Bromuro de potasio Bromuro de potasio<br />
CuBr2 Bromuro cúprico Bromuro de cobre (II) Dibromuro de cobre<br />
CuBr Bromuro cuproso Bromuro de cobre (I) Monobromuro de cobre<br />
AgI Yoduro de plata Yoduro de plata Yoduro de plata<br />
CaCl2 Cloruro de calcio Cloruro de calcio Dicloruro de calcio<br />
FeS Sulfuro ferroso Sulfuro de hierro (II) Monosulfuro de hierro<br />
Fe2S3 Sulfuro férrico Sulfuro de hierro (III) Trisulfuro de dihierro<br />
CuS Sulfuro cúprico Sulfuro de cobre (II) Monosulfuro de cobre<br />
E D U C A M I X<br />
Física y Química 4º ESO Curso 2007-2008 2
Formulación: Compuestos binarios y ternarios. Respuestas a <strong>los</strong> ejercicios.<br />
12. Formula <strong>los</strong> <strong>siguientes</strong> compuestos:<br />
Cloruro de plomo (II): PbCl2<br />
Bromuro de calcio: CaBr2<br />
Fluoruro de plata: AgF<br />
Yoduro de hierro (III): FeI3<br />
Bromuro de manganeso (III): MnBr3<br />
Cloruro de cobalto (III): CoCl3<br />
Dicloruro de níquel: NiCl2<br />
Pentafluoruro de bismuto: BiF5<br />
Trifluoruro de aluminio: AlF3<br />
13. <strong>Nombra</strong> <strong>los</strong> <strong>siguientes</strong> compuestos:<br />
<strong>Nomenclatura</strong> sistemática<br />
BrCl Cloruro de bromo<br />
ICl Cloruro de yodo<br />
ClF Fluoruro de cloro<br />
IBr3 Tribromuro de yodo<br />
NCl3 Tricloruro de nitrógeno<br />
Si3N4 Tetranitruro de trisilicio<br />
BP Fosfuro de boro<br />
1<strong>4.</strong> Formula <strong>los</strong> <strong>siguientes</strong> compuestos:<br />
a. Carburo de silicio: SiC<br />
b. Trisulfuro de diboro: B2S3<br />
c. Pentabromuro de fósforo: PBr5<br />
15. <strong>Nombra</strong> <strong>los</strong> <strong>siguientes</strong> compuestos:<br />
Fórmula Notación <strong>tradicional</strong> Notación stock<br />
Pb(SO4)2 Sulfato plúmbico Sulfato de plomo (IV)<br />
Hg2SO4 Sulfato mercurioso Sulfato de mercurio (I)<br />
Fe(NO3)3 Nitrato férrico Nitrato de hierro (III)<br />
Au2(CO3)3 Carbonato áurico Carbonato de oro (III)<br />
Li2SO4 Sulfato de litio Sulfato de litio<br />
AlPO4 Fosfato de aluminio Fosfato de aluminio<br />
HNO3 Ácido nítrico -----<br />
CaCO3 Carbonato de calcio Carbonato de calcio<br />
Hg(OH)2 Hidr<strong>óxido</strong> mercúrico Hidr<strong>óxido</strong> de mercurio (II)<br />
CuOH Hidr<strong>óxido</strong> cuproso Hidr<strong>óxido</strong> de cobre (I)<br />
Ca(OH)2 Hidr<strong>óxido</strong> de calcio Hidr<strong>óxido</strong> de calcio<br />
NaOH Hidr<strong>óxido</strong> de sodio Hidr<strong>óxido</strong> de sodio<br />
16. Formula <strong>los</strong> <strong>siguientes</strong> compuestos:<br />
Nombre Fórmula<br />
Sulfato sódico Na2SO4<br />
Ácido sulfúrico H2SO4<br />
Carbonato de sodio Na2CO3<br />
Hidr<strong>óxido</strong> férrico Fe(OH)3<br />
Sulfato cúprico CuSO4<br />
Nitrato de aluminio AlNO3<br />
Nitrato de cobre (I) CuNO3<br />
Sulfato de estaño (IV) Sn(SO4)2<br />
Fosfato de calcio Ca3(PO4)2<br />
E D U C A M I X<br />
Física y Química 4º ESO Curso 2007-2008 3