pagina 2.pdf - Genetica e Immunologia Pediatrica
pagina 2.pdf - Genetica e Immunologia Pediatrica
pagina 2.pdf - Genetica e Immunologia Pediatrica
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Rivista Italiana di <strong>Genetica</strong> e <strong>Immunologia</strong> <strong>Pediatrica</strong> - Italian Journal of Genetic and Pediatric Immunology<br />
Anno III numero 3 - luglio 2011 | direttore scientifico: Carmelo Salpietro - direttore responsabile: Giuseppe Micali<br />
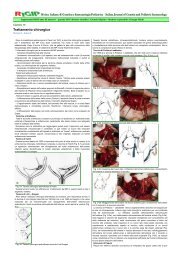
Malformazioni congenite delle basse vie aeree<br />
Congenital malformations of the lower airways<br />
Miriam Di Stefano, Maria Papale<br />
Dipartimento di Pediatria, Università degli Studi di Catania<br />
Le malformazioni delle basse vie aeree sono patologie rare ed in passato quasi<br />
sempre letali. La loro presentazione clinica è estremamente variabile, da una grave<br />
dispnea alla nascita a modesti sintomi da ostruzione delle vie aeree in bambini più<br />
grandi. I sintomi più caratteristici sono rappresentati dallo stridore e le alterazioni del<br />
pianto e della tosse. Possono verificarsi episodi di cianosi e retrazioni della parete<br />
toracica con l'esercizio fisico. Nelle forme più gravi in cui le anomalie determinano<br />
grave ostruzione sono presenti i sintomi di una bronchiolite persistente atipica o di<br />
una grave difficoltà respiratoria che può portare a morte improvvisa. I sintomi<br />
possono peggiorare improvvisamente con il verificarsi di un'infezione respiratoria e<br />
richiedere l'intubazione [2].<br />
Derivano da un alterato sviluppo della gemma polmonare primitiva (che dà vita a<br />
tutto l’albero bronchiale), o da alterato sviluppo del IV arco aortico del tronco<br />
arterioso primitivo (che da vita a tutto l’albero vasale polmonare) [3]. Ciò spiega la<br />
frequente associazione con altre malformazioni del tratto respiratorio,<br />
cardiovascolare e dell'esofago.<br />
Richiami embriologici<br />
Lo sviluppo del polmone inizia intorno al 25° giorno di vita intrauterina, da<br />
un’estroflessione ventrale dell’intestino primitivo all’altezza della porzione esofagea,<br />
(rivestita da endoderma e ricoperta da mesenchima) e sarà pressocchè completo<br />
intorno all’8°anno di età [3]. L’epitelio di trachea, bronchi e alveoli ha origine<br />
dall’endoderma; muscoli, cartilagine, tessuto connettivo e strutture vascolari hanno<br />
origine dal mesoderma [4]. Questa si sviluppa prima in senso cranio caudale e<br />
successivamente si ramifica nelle destra e sinistra le quali daranno origine ad<br />
altri 16 ordini di ramificazioni per formare l’albero bronchiale dei polmoni [5]. Il tratto<br />
dell’albero respiratorio prossimale rispetto alla prima biforcazione si trasforma in<br />
laringe e trachea, e i tratti corrispondenti alle gemme bronchiali destra e sinistra si<br />
trasformano nei bronchi principali destro e sinistro. Il terzo ordine di ramificazioni che<br />
si origina all’inizio della quinta settimana, dà origine a tre gemme bronchiali<br />
secondarie a destra e due gemme a sinistra. queste gemme danno origine ai lobi<br />
polmonari: tre nel polmone destro e due nel sinistro (periodo embrionale). Nel corso<br />
della 16ᵃ settimana l’albero respiratorio produce piccoli rami chiamati bronchioli<br />
terminali (fase pseudo ghiandolare). Fra la 16ᵃ e la 28ᵃ settimana si formano i<br />
bronchioli respiratori e il mesenchima circostante diventa riccamente vascolarizzato<br />
(fase canalicolare). In questa fase inizia anche la differenziazione dell’epitelio<br />
respiratorio periferico in pneumociti di tipo I e II, la formazione delle prime barriere<br />
aria-sangue, e l’inizio della produzione di tensioattivi da parte degli pneumociti di II<br />
tipo [4]. Nella 28ᵃ settimana dai bronchioli respiratori si formano i sacchi terminali o<br />
alveoli primitivi che alla 30 settimana verranno avvolti da una fitta rete di capillari<br />
(fase sacculare). I neonati partoriti a quest’epoca spesso muoiono per insufficienza<br />
respiratoria, essendo gli alveli pochi e immaturi. Gli alveoli continuano a moltiplicarsi<br />
anche dopo la nasciata fino a raggiungere i 300-400 milioni nel polmone maturo<br />
all’età di circa 8 anni. Poco prima della nascita l’epitelio pavimentoso che tappezza i<br />
sacchi terminali comincia ad assottigliarsi progressivamente, si assottiglia pure il<br />
tessuto connettivo tra gli spazi aerei, matura il surfattante, finchè gli alveoli primitivi<br />
si differenziano in alveoli maturi (fase alveolare). Contemporaneamente allo sviluppo<br />
del polmone ha luogo la progressiva separazione dall’intestino primitivo, attraverso<br />
la formazione del setto tracheoesofageo che origina da una laterale invaginazione<br />
del mesoderma. L’incompleto o difettoso processo di separazione tra le strutture<br />
respiratorie dalle alimentari è una delle più frequenti anomalie congenite [4-5].<br />
Lo sviluppo dell’albero vasale è simile a quello bronchiale e subordinato a quello<br />
dell’albero bronchiale: l'arteria polmonare si sviluppa dal sesto arco aortico e dà<br />
origine ai rami che seguono parallelamente lo sviluppo delle vie aeree (vasi<br />
preacinari) e degli alveoli (vasi intraacinari).[3-5].<br />
Le principali malformazioni della trachea sono la tracheomalacia e la stenosi<br />
tracheale. Malformazioni congenite molto più rare sono l'atresia tracheale e il bronco<br />
tracheale. A livello bronchiale le principali malformazioni sono la broncomalacia, la<br />
stenosi bronchiale ed l’atresia bronchiale.<br />
Tracheomalacia<br />
Consiste in un indebolimento della parete tracheale causata da un’anomalia degli<br />
anelli cartilaginei e da un ridotto tono muscolare della pars membranacea. Alla<br />
nascita la cartilagine nelle vie respiratorie dei bambini normalmente non è rigida, e<br />
quindi tutti i bambini hanno un certo grado di collasso dinamico durante<br />
l'espirazione, quando la pressione esterna alla trachea supera la pressione<br />
all'interno. Nella tracheomalacia la struttura cartilaginea della trachea non è in grado<br />
di mantenere la pervietà delle vie aeree e il collasso dinamico porta ad ostruzione<br />
delle vie aeree [4, 7]. Perché un collasso tracheale possa creare ostacolo alla<br />
ventilazione polmonare deve essere superiore al 50% del diametro tracheale [8].<br />
Pertanto la tracheomalacia viene distinta in :<br />
• parziale: per ostruzioni >50% e 90%<br />
Si distinguono le forme primitive (lesioni isolate) dalle forme secondarie (correlate a<br />
compressione estrinseca della trachea) [2, 8]. La tracheomalacia primaria si pensa<br />
sia dovuta ad immaturità congenita della cartilagine tracheale. Nella tracheomalacia<br />
secondaria, la cartilagine in precedenza normale va incontro a degenerazione. La<br />
forma secondaria può essere associata ad altri difetti dello sviluppo per esempio alla<br />
presenza di un anello vascolare o ad fistola tracheoesofagea [4].<br />
La malacia può interessare un breve segmento tracheale, tracheomalacia<br />
segmentaria, o più raramente quasi tutta la sua lunghezza, tracheomalacia<br />
generalizzata [8].Tutti i tipi di tracheomalacia sono rare e non sono note predilezioni<br />
di razza o di sesso [9].<br />
Il quadro clinico è correlato all’ostruzione delle vie aeree. Nelle forme a<br />
localizzazione toracica (terzo medio e inferiore della trachea) è tipico lo stridore<br />
espiratorio, il respiro rumoroso sibilante in fase espiratoria, durante il pianto o<br />
l’espirazione forzata; il tirage e dispnea inspiratoria prevalgono invece nelle<br />
localizzazioni cervicali [1, 8]. Talora è difficile differenziare la sintomatologia della<br />
tracheomalacia da quella asmatica. Infatti i pazienti affetti da tracheomalacia spesso<br />
hanno una storia wheezing persistente o restistente alla terapia broncodilatatrice.<br />
Sono riportati in letteratura casi di tracheomalacia posta solo in età adulta dopo anni<br />
di impropria terapia asmatica. Nelle forme più gravi il quadro clinico può essere<br />
complicato da broncopolmoniti recidivanti, crisi di dispnea, tachipnea e cianosi [1,<br />
10].<br />
La diagnosi può essere sospettata con una radiografia laterale del torace che può<br />
mostrare un restringimento della trachea quando si immette il respiro (fig1a) oppure<br />
con un esofagogramma, che evidenzia una caratteristica impronta sull' esofago nel<br />
caso di una compressione vascolare. La diagnosi di certezza viene comunque posta<br />
esclusivamente sui seguenti reperti tracheobroncoscopici: diminuito diametro anteroposteriore<br />
della trachea, riduzione del suo lume superiore al 40%, scarsa<br />
visualizzazione degli anelli tracheali [2, 10].<br />
Durante la broncoscopia si può osservare direttamente come la parete anteriore<br />
della trachea collabisce sulla parete posteriore e allo stesso tempo (fig1b), possono<br />
essere diagnosticate o escluse altre lesioni per esempio anelli vascolari o corpi<br />
estranei. Si preferisce usare il broncoscopio flessibile in anestesia leggera perché il<br />
bambino respira spontaneamente e viene mantenuta la dinamica respiratoria.<br />
Inoltre, il broncoscopio rigido può agire come uno stent sulle vie aeree,<br />
mascherando la diagnosi. La RMN o la TC si possono eseguire per distinguere le<br />
forme secondarie correlate ad anelli vascolari o ad altre compressioni estrinseche su<br />
cui intervenire chirurgicamente. La ph-metria si può eseguire nel sospetto di un<br />
reflusso gastroesofageo Le malformazioni delle basse vie aeree sono patologie rare<br />
ed in passato quasi sempre letali. La loro presentazione clinica è estremamente<br />
variabile, da una grave dispnea alla nascita a modesti sintomi da ostruzione delle vie<br />
aeree in bambini più grandi. I sintomi più caratteristici sono rappresentati dallo<br />
stridore e le alterazioni del pianto e della tosse. Possono verificarsi episodi di cianosi<br />
e retrazioni della parete toracica con l'esercizio fisico. Nelle forme più gravi in cui le<br />
anomalie determinano grave ostruzione sono presenti i sintomi di una bronchiolite<br />
persistente atipica o di una grave difficoltà respiratoria che può portare a morte<br />
improvvisa. I sintomi possono peggiorare improvvisamente con il verificarsi di<br />
un'infezione respiratoria e richiedere l'intubazione [2].<br />
Derivano da un alterato sviluppo della gemma polmonare primitiva (che dà vita a<br />
tutto l’albero bronchiale), o da alterato sviluppo del IV arco aortico del tronco<br />
arterioso primitivo (che da vita a tutto l’albero vasale polmonare) [3]. Ciò spiega la<br />
frequente associazione con altre malformazioni del tratto respiratorio,<br />
cardiovascolare e dell'esofago.<br />
Richiami embriologici<br />
Lo sviluppo del polmone inizia intorno al 25° giorno di vita intrauterina, da<br />
un’estroflessione ventrale dell’intestino primitivo all’altezza della porzione esofagea,<br />
(rivestita da endoderma e ricoperta da mesenchima) e sarà pressocchè completo<br />
intorno all’8°anno di età [3]. L’epitelio di trachea, bronchi e alveoli ha origine<br />
dall’endoderma; muscoli, cartilagine, tessuto connettivo e strutture vascolari hanno<br />
origine dal mesoderma [4]. Questa si sviluppa prima in senso cranio caudale e<br />
successivamente si ramifica nelle destra e sinistra le quali daranno origine ad
altri 16 ordini di ramificazioni per formare l’albero bronchiale dei polmoni [5]. Il tratto<br />
dell’albero respiratorio prossimale rispetto alla prima biforcazione si trasforma in<br />
laringe e trachea, e i tratti corrispondenti alle gemme bronchiali destra e sinistra si<br />
trasformano nei bronchi principali destro e sinistro. Il terzo ordine di ramificazioni che<br />
si origina all’inizio della quinta settimana, dà origine a tre gemme bronchiali<br />
secondarie a destra e due gemme a sinistra. queste gemme danno origine ai lobi<br />
polmonari: tre nel polmone destro e due nel sinistro (periodo embrionale). Nel corso<br />
della 16ᵃ settimana l’albero respiratorio produce piccoli rami chiamati bronchioli<br />
terminali (fase pseudo ghiandolare). Fra la 16ᵃ e la 28ᵃ settimana si formano i<br />
bronchioli respiratori e il mesenchima circostante diventa riccamente vascolarizzato<br />
(fase canalicolare). In questa fase inizia anche la differenziazione dell’epitelio<br />
respiratorio periferico in pneumociti di tipo I e II, la formazione delle prime barriere<br />
aria-sangue, e l’inizio della produzione di tensioattivi da parte degli pneumociti di II<br />
tipo [4]. Nella 28ᵃ settimana dai bronchioli respiratori si formano i sacchi terminali o<br />
alveoli primitivi che alla 30 settimana verranno avvolti da una fitta rete di capillari<br />
(fase sacculare). I neonati partoriti a quest’epoca spesso muoiono per insufficienza<br />
respiratoria, essendo gli alveli pochi e immaturi. Gli alveoli continuano a moltiplicarsi<br />
anche dopo la nasciata fino a raggiungere i 300-400 milioni nel polmone maturo<br />
all’età di circa 8 anni. Poco prima della nascita l’epitelio pavimentoso che tappezza i<br />
sacchi terminali comincia ad assottigliarsi progressivamente, si assottiglia pure il<br />
tessuto connettivo tra gli spazi aerei, matura il surfattante, finchè gli alveoli primitivi<br />
si differenziano in alveoli maturi (fase alveolare). Contemporaneamente allo sviluppo<br />
del polmone ha luogo la progressiva separazione dall’intestino primitivo, attraverso<br />
la formazione del setto tracheoesofageo che origina da una laterale invaginazione<br />
del mesoderma. L’incompleto o difettoso processo di separazione tra le strutture<br />
respiratorie dalle alimentari è una delle più frequenti anomalie congenite [4-5]. Lo<br />
sviluppo dell’albero vasale è simile a quello bronchiale e subordinato a quello<br />
dell’albero bronchiale: l'arteria polmonare si sviluppa dal sesto arco aortico e dà<br />
origine ai rami che seguono parallelamente lo sviluppo delle vie aeree (vasi<br />
preacinari) e degli alveoli (vasi intraacinari).[3-5]. Le principali malformazioni della<br />
trachea sono la tracheomalacia e la stenosi tracheale. Malformazioni congenite<br />
molto più rare sono l'atresia tracheale e il bronco tracheale. A livello bronchiale le<br />
principali malformazioni sono la broncomalacia, la stenosi bronchiale ed l’atresia<br />
bronchiale.<br />
Tracheomalacia<br />
Consiste in un indebolimento della parete tracheale causata da un’anomalia degli<br />
anelli cartilaginei e da un ridotto tono muscolare della pars membranacea. Alla<br />
nascita la cartilagine nelle vie respiratorie dei bambini normalmente non è rigida, e<br />
quindi tutti i bambini hanno un certo grado di collasso dinamico durante<br />
l'espirazione, quando la pressione esterna alla trachea supera la pressione<br />
all'interno. Nella tracheomalacia la struttura cartilaginea della trachea non è in grado<br />
di mantenere la pervietà delle vie aeree e il collasso dinamico porta ad ostruzione<br />
delle vie aeree [4, 7]. Perché un collasso tracheale possa creare ostacolo alla<br />
ventilazione polmonare deve essere superiore al 50% del diametro tracheale [8].<br />
Pertanto la tracheomalacia viene distinta in :<br />
• parziale: per ostruzioni >50% e 90%<br />
Si distinguono le forme primitive (lesioni isolate) dalle forme secondarie (correlate a<br />
compressione estrinseca della trachea) [2, 8]. La tracheomalacia primaria si pensa<br />
sia dovuta ad immaturità congenita della cartilagine tracheale. Nella tracheomalacia<br />
secondaria, la cartilagine in precedenza normale va incontro a degenerazione. La<br />
forma secondaria può essere associata ad altri difetti dello sviluppo per esempio alla<br />
presenza di un anello vascolare o ad fistola tracheoesofagea [4].<br />
La malacia può interessare un breve segmento tracheale, tracheomalacia<br />
segmentaria, o più raramente quasi tutta la sua lunghezza, tracheomalacia<br />
generalizzata [8].Tutti i tipi di tracheomalacia sono rare e non sono note predilezioni<br />
di razza o di sesso [9].<br />
Il quadro clinico è correlato all’ostruzione delle vie aeree. Nelle forme a<br />
localizzazione toracica (terzo medio e inferiore della trachea) è tipico lo stridore<br />
espiratorio, il respiro rumoroso sibilante in fase espiratoria, durante il pianto o<br />
l’espirazione forzata; il tirage e dispnea inspiratoria prevalgono invece nelle<br />
localizzazioni cervicali [1, 8]. Talora è difficile differenziare la sintomatologia della<br />
tracheomalacia da quella asmatica. Infatti i pazienti affetti da tracheomalacia spesso<br />
hanno una storia wheezing persistente o restistente alla terapia broncodilatatrice.<br />
Sono riportati in letteratura casi di tracheomalacia posta solo in età adulta dopo anni<br />
di impropria terapia asmatica. Nelle forme più gravi il quadro clinico può essere<br />
complicato da broncopolmoniti recidivanti, crisi di dispnea, tachipnea e cianosi [1,<br />
10].<br />
La diagnosi può essere sospettata con una radiografia laterale del torace che può<br />
mostrare un restringimento della trachea quando si immette il respiro (fig1a) oppure<br />
con un esofagogramma, che evidenzia una caratteristica impronta sull' esofago nel<br />
caso di una compressione vascolare. La diagnosi di certezza viene comunque posta<br />
esclusivamente sui seguenti reperti tracheobroncoscopici: diminuito diametro anteroposteriore<br />
della trachea, riduzione del suo lume superiore al 40%, scarsa<br />
visualizzazione degli anelli tracheali [2, 10].<br />
Durante la broncoscopia si può osservare direttamente come la parete anteriore<br />
della trachea collabisce sulla parete posteriore e allo stesso tempo (fig1b), possono<br />
essere diagnosticate o escluse altre lesioni per esempio anelli vascolari o corpi<br />
estranei. Si preferisce usare il broncoscopio flessibile in anestesia leggera perché il<br />
bambino respira spontaneamente e viene mantenuta la dinamica respiratoria.<br />
Inoltre, il broncoscopio rigido può agire come uno stent sulle vie aeree,<br />
mascherando la diagnosi. La RMN o la TC si possono eseguire per distinguere le<br />
forme secondarie correlate ad anelli vascolari o ad altre compressioni estrinseche su<br />
cui intervenire chirurgicamente. La ph-metria si può eseguire nel sospetto di un<br />
reflusso gastroesofageo [9].<br />
Fig. 1a - Radiografia laterale durante l'inspirazione e l'espirazione. Il collasso<br />
tracheale di oltre il 50% durante l'espirazione è diagnostica di tracheomalacia.<br />
[9]<br />
Fig1b - Broncoscopia: tracheomalacia di forma ovale con lieve appiattimento<br />
anteriore [40]<br />
La terapia è conservativa nelle forme lievi considerato il frequente miglioramento<br />
clinico con la crescita del bambino La chirurgia diventa necessaria in quelle<br />
gravemente sintomatiche [2, 4]. La cura specifica della tracheomalacia consiste<br />
nell'ampliare e stabilizzare il lume tracheale mediante il posizionamento di uno stent<br />
metallico espansibile endoluminale di grandezza.<br />
Stenosi tracheale<br />
La stenosi tracheale è una patologia rara caratterizzata da un'ostruzione fissa della<br />
trachea, considerata quasi sempre fatale fino agli anni '80, e attualmente<br />
considerata correggibile, pur con un tasso di mortalità e morbilità non trascurabile [1,<br />
2]<br />
La stenosi può essere determinata:<br />
- da un ispessimento sottomucoso limitato ad un breve tratto della trachea;<br />
- da un anello tracheale più piccolo con una pars membranacea più ristretta;<br />
- da anelli cartilaginei completi.<br />
Le stenosi da anelli cartilaginei completi si distinguono a loro volta in tre tipi:<br />
- 1° tipo: uniformemente ristretto, coinvolgente tutta la trachea;<br />
- 2° tipo: progressivamente ristretto in direzione da prossimale a distale, spesso<br />
accompagnato anche da una trachea abnormemente più lunga, contenente più di 24<br />
anelli;<br />
- 3° tipo: stenosi segmentale, coinvolgente 3-5 anelli (fig 2)<br />
Fig 2 [12<br />
Circa il 50% delle stenosi tracheali congenite sono focali, il 30% generalizzate, e il<br />
20% a forma di imbuto (2° tipo). Le stenosi focali di solito coinvolgono il terzo<br />
inferiore della trachea e le dimensioni dei bronchi sono in genere normali [2, 4]. Si<br />
distinguono forme primitive e secondarie. Le forme primitive possono essere solo un<br />
reperto occasionale rilevato durante indagini eseguite per indagare altre patologie; le<br />
forme più severe, però, possono determinare un quadro respiratorio ingravescente<br />
legato al ristagno delle secrezioni distalmente alla stenosi con conseguenti frequenti<br />
episodi infettivi. Le forme secondarie sono legate a compressione estrinseca dovuta<br />
o a masse mediastiniche o ad anelli vascolari. Rimosse le cause della stenosi,<br />
possono persistere i sintomi di tracheomalacia dovuta all'alterato sviluppo della<br />
struttura cartilaginea tracheale a causa della compressione [1]. La stenosi tracheale<br />
da anelli completi può essere associata ad un'anomala origine dell'arteria polmonare<br />
sinistra (50%) o ad anomalie bronchiali (20%), come l'aplasia bronchiale con<br />
assenza di un polmone, il bronco tracheale, e un’ampia angolazione tra i due bronchi<br />
principali. Infine, può associarsi, seppur raramente, a malformazioni del tratto<br />
digestivo superiore [12].<br />
I sintomi compaiono nel 50% dei casi entro primo mese di vita. Caratteristici sono lo<br />
stridore bifasico, il wheezing e la dispnea con una prolungata fase espiratoria.<br />
Episodicamente può verificarsi un'ostruzione respiratoria acuta determinata da tappi<br />
di muco che riducono il lume dell'area stenotica. Nelle stenosi brevi è presente<br />
anche un atteggiamento di iperestensione della testa perchè questa postura<br />
conferisce in parte rigidità alla trachea, minimizza la compressione della trachea<br />
toracica e migliora la ventilazione [2]. La severità dei sintomi è legata più al grado<br />
che alla lunghezza della stenosi, poichè la resistenza al flusso dell’aria nelle vie<br />
aeree è linearmente proporzionale alla lunghezza ma aumenta di quattro volte in<br />
relazione alla diminuzione raggio del lume [4].<br />
Determinare la causa della stenosi in un bambino sintomatico è fondamentale<br />
anche perché piccole quantità di secrezioni o un lieve edema possono causare un'<br />
ostruzione completa. Quando questa si verifica, è necessario ricorrere<br />
all'intubazione. È importante, nell'attesa di una diagnosi, umidificare i gas per
minimizzare le lesioni della mucosa respiratoria e somministrare broncodilatatori e<br />
steroidi per ridurne l'edema. La radiografia del collo e del torace in proiezione laterolaterale,<br />
focalizzata sulla trachea, è spesso sufficiente per porre diagnosi di stenosi<br />
tracheale. Anche due radiografie antero-posteriori in ispirazione ed espirazione<br />
profonde, possono suggerire la presenza di un' ostruzione, soprattutto se il volume<br />
del polmone affetto non varia in modo significativo durante l'espirazione.<br />
L'ecocardiografia è molto utile nell'evidenziare eventuali anomalie vascolari arteriose<br />
associate, quali un doppio arco aortico, o difetti intracardiaci. L’esofagogramma<br />
suggerisce la stenosi quando è visibile un'indentazione anteriore che è dovuta ad<br />
uno "sling" dell’arteria polmonare, o un'indentazione posteriore determinata da un<br />
doppio arco aortico. La broncoscopia permette la visualizzazione di anelli tracheali<br />
completi nella trachea superiore, segno che anche la trachea sottostante è alterata.<br />
In tal caso non si deve tentare di superare la stenosi perché ciò provocherebbe<br />
edema aggravando l'ostruzione. La broncografia con contrasto è stata sostituita<br />
dalla TC assiale che è in grado di mostrare le reali dimensioni del lume tracheale e<br />
di evidenziare eventuali patologie compressive estrinseche associate. [2, 4]. La<br />
terapia endoscopica con dilatazione e/o laser resezione, viene utilizzata nelle<br />
stenosi molto corte dovute ad un ispessimento sottomucoso o limitate ad un anello<br />
tracheale più piccolo con pars membranacea ristretta [2]. Nelle altre forme di stenosi<br />
è sempre indicato l'intervento chirurgico. L'intervento ideale è la resezioneanastomosi,<br />
che può essere attuata soltanto nelle stenosi corte non superiori a 2, 5<br />
cm o interessanti non più di 3-5 anelli tracheali. Nelle stenosi tracheali più lunghe<br />
necessario ricorrere alle tecniche di tracheoplastica [2, 12, 13].<br />
Atresia e stenosi bronchiale<br />
L’atresia bronchiale è una rara anomalia che interessa più spesso i bronchi<br />
segmentali in prossimità della loro origine, tuttavia, anche i bronchi subsegmentali o<br />
lobari possono essere coinvolti. I bronchi del lobo superiore sono i più<br />
frequentemente colpiti. I bronchi distali alla stenosi riempendosi di muco formano un<br />
broncocele che appare radiologicamente come un nodulo rotondo. A causa<br />
dell’ostruzione, in genere il polmone omolaterale è atresico o ipoplasico e<br />
radiologicamente opaco, mentre quello contro laterale è sovradisteso. Talora però gli<br />
alveoli forniti dai bronchi atresici sono ventilati da vie collaterali (fori di Kohn e dotti di<br />
Lambert) e si verifica un fenomeno di air trapping per cui il polmone o il lobo<br />
coinvolto appaiono iperdistesi e radiologicamente iperdiafani. Anche i batteri<br />
possono entrare nel tessuto polmonare attraverso le vie collaterali e determinare un<br />
ascesso polmonare [2, 4].<br />
L’atresia bronchiale in genere è asintomatica e in circa il 50% dei casi il suo<br />
riscontro avviene in maniera incidentale, tramite radiografia del torace, in età adulta<br />
[4]. Possibili manifestazioni cliniche sono la dispnea, l’affaticamento, le infezioni<br />
polmonari ricorrenti [2]. Certamente la TC è la tecnica più sensibile per visualizzare<br />
l’atresia e le sue caratteristiche [4]. Il trattamento è chirurgico e consiste nella<br />
resezione della parte polmonare affetta per evitare l’insorgenza di processi infettivi<br />
[6].<br />
Nella stenosi bronchiale il polmone può essere ancora in parte ventilato, ma appare<br />
piccolo. Raramente si ha air-trapping, e in tal caso il polmone o il lobo interessati<br />
radiologicamente appaiono iperdistesi e iperdiafani. La broncoscopia ci permette di<br />
porre diagnosi di stenosi, ma la RM e la TC permettono di ottenere le informazioni<br />
indispensabile per pianificare l’intervento. Le stenosi bronchiali non fibrotiche,<br />
possono trarre beneficio dalla dilatazione endoscopica con il palloncino ripetuta<br />
periodicamente. Le stenosi rigide e fibrotiche richiedono intervento chirurgico di<br />
resezione-anastomosi e le stenosi molto lunghe, una broncoplastica d'ampliamento<br />
con pericardio o cartilagine costale [2, 14].<br />
Broncomalacia<br />
La broncomalacia, similmente alla tracheomalacia, consiste nell’indebolimento degli<br />
anelli cartilaginei bronchiali che si collassano durante l'espirazione, favorendo un air<br />
trapping, responsabile di difficoltà respiratoria e di infezioni broncopolmonari<br />
ricorrenti. Raramente è primitiva, invece spesso è secondaria ad una compressione<br />
estrinseca, legata ai grossi vasi (arterie polmonarie dilatate o anomalo decorso dei<br />
vasi polmonari), ad un atrio sinistro dilatato oppure alla presenza di una massa,<br />
come nel caso di una cisti bronchiale [2]. Il bronco principale sinistro è il più<br />
frequentemente interessato perché più lungo rispetto al destro, con minor numero di<br />
biforcazioni e più suscettibile a compressione. Clinicamente può presentarsi con<br />
tosse e asma non responder oppure con quadri ostruttivi severi associati a gravi<br />
infezioni polmonari. La diagnosi è endoscopica, mentre la TC spirale conferma e<br />
definisce la lunghezza dell’occlusione e chiarisce i rapporti con le strutture<br />
circostanti [8]. Il trattamento prevede l’eliminazione di eventuali cause di<br />
compressione estrinseca; nelle forme gravemente sintomatiche il posizionamento di<br />
uno stent endoluminale per via endoscopica o in alternativa di uno splint esterno [2].<br />
Le malformazioni polmonari sono determinate da insulti di diverso tipo che possono<br />
intervenire in qualsiasi momento dello sviluppo dell’abbozzo polmonare. I quadri<br />
clinici sono variabili da situazioni incompatibili con la vita, a condizioni di normalità.<br />
Si distinguono:<br />
• malformazioni legate allo sviluppo di abbozzi ectopici o soprannumerari (cisti<br />
bronchiale, sequestro polmonare)<br />
• malformazioni legate a difettoso sviluppo dell'abbozzo bronchiale durante il<br />
passaggio dallo stadio canalicolare a quello alveolare (malattia adenomatoide cistica<br />
polmonare).<br />
• malformazioni caratterizzate da aumento od una riduzione di tessuto polmonare<br />
(enfisema lobare congenito, ipoplasia o agenesia polmonare o lobare o segmentale)<br />
od una sua diversa morfologia (variazione delle segmentazioni e delle commissure).<br />
Non rara in questi casi è la coesistenza di una connessione con l'intestino anteriore<br />
e di malformazioni artero-venose.<br />
Cisti broncogena e cisti polmonare congenita<br />
La cisti broncogena prende origine dall’anomalo sviluppo di trachea e bronchi<br />
dall’intestino primitivo. È una cisti uniloculare, ripiena di muco, con una parete<br />
tappezzata da epitelio di tipo respiratorio e non comunica solitamente con le vie<br />
aeree. Può localizzarsi a livello della trachea cervicale o toracica, a livello dei<br />
bronchi ilari o più frequentemente a ridosso dei bronchi intraparenchimali. Sono più<br />
rare le sedi ectopiche, vicino alle vertebre e all'esofago.<br />
La cisti polmonare congenita prende origine dallo sviluppo anomalo delle vie aeree<br />
più distali, compresi gli alveoli, il tessuto linfatico e quello pleurico. Può essere uni o<br />
biloculare, con parete rivestita da epitelio respiratorio e contenente tessuto<br />
cartilagineo, connettivale e talora muscolo liscio. Le manifestazioni cliniche sono<br />
correlate alla compressione sulle vie aeree e sull' esofago oppure legate ad un<br />
inadeguato drenaggio delle secrezioni bronchiali con infezioni secondarie. Il neonato<br />
può presentare distress respiratorio, il bambino dispnea, stridore espiratorio, cianosi,<br />
e disfagia se c’è compressione toracica [2, 4].<br />
Talora le cisti broncogene e polmonari vengono diagnosticate nel corso di controlli<br />
radiologici del torace per una polmonite a lenta risoluzione [2, 4]. La radiografia del<br />
torace evidenzia una massa solida paratracheale o ilare, sferica, a contorni lisci,<br />
senza calcificazioni, che sposta le vie aeree adiacenti e frequentemente crea un<br />
enfisema distale, anche in bambini asintomatici. La presenza di un livello idro-aereo<br />
indica una comunicazione con l'albero tracheo-bronchiale, soprattutto se viene<br />
rilevato dopo un'infezione acuta. La cisti polmonare congenita può situarsi ovunque,<br />
anche in sede sub pleurica e spesso è difficile distinguerla da un ascesso polmonare<br />
o da una malattia adenomatoidecistica. La TC e la RM ci offre una migliore<br />
definizione anche dei rapporti anatomici tra la cisti e le strutture circostanti. La<br />
terapia è chirurgica, consiste nell’asportazione della cisti broncogena o polmonare,<br />
per via toracotomica o in toracoscopia [2, 4].<br />
Malformazione adenoido-cistica congenita polmonare<br />
La malformazione adenoido-cistica congenita (CCAM) è una delle più comuni<br />
anomalie polmonari congenite. L'incidenza stimata è tra 1 :25.000 e 1 :35.000 nati<br />
[2]. Si tratta di una rara alterazione polmonare caratterizzata dalla presenza di<br />
tessuto polmonare displastico o amartomatoso frammisto a tessuto polmonare<br />
normale [15]. La lesione verosimilmente è conseguente ad un insulto che interviene<br />
durante la vita embrionale prima dei 50 giorni di gestazione, e determina un arresto<br />
del normale sviluppo del’abbozzo polmonare con abnorme crescita dei bronchioli<br />
terminali e soppressione dello sviluppo alveolare [4, 16].<br />
La storica classificazione di Stoker ed altri distingue tre tipi istologici :<br />
• tipo I: caratterizzato da cisti di dimensioni > 2 cm di diametro rivestite da epitelio<br />
cuboidale o colonnare pseudostratificato ciliato, con presenza di cellule muscolari<br />
lisce e tessuto elastico. La cartilagine è raramente presente. Le strutture alveolari<br />
negli spazi adiacenti o interposti tra le cisti sono relativamente normali; questa è la<br />
forma più comune (75%) e ha una buona prognosi;<br />
• tipo II: caratterizzato da numerose cisti di dimensioni inferiori a 1 cm, con istologia<br />
simile al tipo II. Si associa in genere ad altre anomalie e ha una prognosi peggiore.<br />
• tipo III: coinvolge tutto il lobo, non sono presenti cisti macroscopicamente visibili,<br />
ma masse di strutture canalicolari, bronchiolo-simili, strettamente affiancate,<br />
delimitate da epitelio cuboide ciliato. È la forma a prognosi peggiore [2, 4].<br />
Dal punto di vista clinico, si fa riferimento alla suddivisione ecografica, proposta da<br />
Adzick, in due categorie:<br />
• forma macrocistica, caratterizzata da cisti sopra i cinque millimetri<br />
• forma microcistica, caratterizzata da cisti più piccole di cinque millimetri o dall’<br />
aspetto di massa solida.<br />
Diversamente dalla cisti broncogena intrapolmonare, la CCAM è irrorata da<br />
un'arteria di origine polmonare; tutti i tre tipi comunicano con un albero bronchiale e<br />
sono limitate ad un lobo polmonare. La CCAM può causare ipoplasia polmonare e<br />
inadeguatezza del drenaggio tracheo-bronchiale. Il 30% dei neonati affetti da CCAM,<br />
si presenta clinicamente con distress respiratorio acuto o progressivo per l’ipoplasia<br />
del polmone omolaterale (in misura minore di quello contro laterale) determinante<br />
un'ipertensione polmonare. Nel corso dei primi anni di vita, per l'inadeguatezza del<br />
drenaggio tracheo-bronchiale causata dalla mancanza di meccanismi di clearance, i<br />
piccoli affetti dalla malformazione presenteranno ricorrenti infezioni respiratorie,<br />
ascessi polmonari, polmoniti recidivanti sempre nello stesso lobo. In alcuni casi le<br />
cisti di piccole dimensioni rimangono asintomatiche e rappresentano un reperto<br />
occasionale in occasione di indagini radiologiche [2, 18] La diagnosi della<br />
malformazione viene posta in utero in oltre il 50% dei casi ed è possibile a partire<br />
dalla 16a settimana. Il follow-up prenatale include la sorveglianza della comparsa di<br />
segni di complicanze quali l’estensione della lesione all’intero emitorace, la<br />
compressione cardiaca e mediastinica (20% dei casi), la comparsa di segni di<br />
impegno cavale quali il polidramnios e l’idrope. Dopo la nascita la radiografia del<br />
torace può evidenziare una lesione a carico di un lobo, microcistica, macrocistica o<br />
solida che nei casi gravi determina spostamento del mediastino, compressione del<br />
polmone adiacente e appiattimento del diaframma omolaterale. Di aiuto nella<br />
diagnosi differenziale con un enfisema lobare congenito, una cisti broncogena o<br />
un'ernia diaframmatica sono la TC o la RM. La TC è raccomandata inoltre, nei<br />
neonati asintomatici con diagnosi prenatale di CCAM in cui la radiografia è negativa.<br />
La valutazione istologica rappresenta la conferma diagnostica [4, 16]. La terapia è<br />
chirurgica e consiste nella resezione chirurgica del lobo polmonare interessato. Nei<br />
casi urgenti e gravi viene eseguito in utero il drenaggio delle cisti di grosse<br />
dimensioni o la rimozione di masse solide di grandi dimensioni [2, 17]. La lobectomia<br />
è raccomandata in tutti i casi sintomatici per evitare la comparsa di infezioni<br />
ricorrenti e per la segnalazione di aumentata incidenza di neoplasie polmonari<br />
primitive. Alcuni studi propongono per i casi asintomatici un approccio più<br />
conservativo considerata la possibilità di risoluzione spontanea nei primi mesi dopo<br />
la nascita [19, 20]. La prognosi dipende prevalentemente dalla grandezza e dalla<br />
progressione della lesione. Lesioni di grosse dimensioni possono determinare,<br />
attraverso la compressione del tessuto adiacente, un'ipoplasia polmonare. In alcuni<br />
casi la lesione può regredire o scomparire spontaneamente; in casi a decorso più<br />
severo può invece progredire e causare morte fetale per idrope o morte neonatale
secondaria ad ipoplasia polmonare. I reperti ecografici in utero che suggeriscono<br />
una prognosi peggiore includono polidramnios, idrope, ascite, sbandieramento<br />
mediastinico, lesioni completamente adenomatose, coinvolgimento polmonare<br />
bilaterale [16]. La prognosi a lungo termine, dei pazienti con CCAM con o senza<br />
lobectomia è generalmente buona [19, 20].<br />
Sequestro polmonare<br />
È una malformazione caratterizzata da tessuto polmonare anomalo, non connesso<br />
all’albero tracheobronchiale, fornito di vascolarizzazione arteriosa sistemica<br />
proveniente spesso dall'aorta discendente toracica e meno frequentemente<br />
dall'aorta sottodiaframmatica. Il suo drenaggio venoso avviene attraverso il sistema<br />
azygos, le vene polmonari o la vena cava inferiore. Si distinguono due tipi di<br />
sequestro: intralobare, localizzato all'interno della pleura viscerale del polmone<br />
normale (75%), ed extralobare, localizzato al di fuori del polmone e rivestito di una<br />
pleura propria (25%) [4, 21].<br />
Il sequestro polmonare congenito si forma per un anomalo sviluppo<br />
broncopolmonare dall'intestino anteriore, pertanto è possibile l'associazione con<br />
altre anomalie quali la malattia adenomatoide cistica soprattutto di tipo II, ernia<br />
diaframmatica, fistola tracheoesofagea, duplicazione intestinale, cardiopatie, oppure<br />
il riscontro di una comunicazione, anche non pervia, del bronco del sequestro con<br />
l'esofago o lo stomaco.<br />
La diagnosi di sequestro extralobare, spesso viene fatta in utero. All' ecografia<br />
appare come una massa solida iperecogena situata nel mediastino posteriore o<br />
sottodiaframmatica, e al doppler si visualizza una vascolarizzazione arteriosa di tipo<br />
sistemico. Se di grandi dimensioni, può determinare un effetto massa con<br />
spostamento del mediastino, idrope e morte del feto. Quando il sequestro sfugge<br />
alla diagnosi prenatale, viene diagnosticato occasionalmente talora in corso di<br />
intervento per ernia diaframmatica, o più frequentemente nei primi mesi o anni di vita<br />
tramite indagini radiologiche eseguite per distress respiratorio, difficoltà<br />
all’alimentazione, o complicanze quali, emorragie e scompenso cardiaco per shunt<br />
artero-venoso nel suo interno. A meno che vi sia una comunicazione con l’esofago,<br />
raramente causano infezione, non essendo connessi con l'albero tracheobronchiale<br />
[22]. Il sequestro intralobare invece generalmente viene diagnosticato più<br />
tardivamente, dopo i primi anni di vita, per polmoniti ricorrenti o persistenti, per un<br />
ascesso polmonare oppure per emottisi dovuta ad alterazioni arteriosclerotiche dei<br />
vasi arteriosi anomali. I batteri arrivano al tessuto sequestrato attraverso i pori di<br />
Kohn (ventilazione collaterale) dove per la scarsa ventilazione e l'assenza<br />
meccanismi di rimozione delle secrezioni, proliferano e determinano l’infezione.<br />
Talora l’infezione si instura nel parenchima polmonare adiacente anatomicamente<br />
normale, a causa del drenaggio inadeguato secondario a compressione da parte del<br />
tessuto sequestrato [2]. Alla radiografia del torace il sequestro intralobare,<br />
tipicamente appare come una opacità persistente a livello dei segmenti basale e<br />
posteriore del lobo inferiore (più spesso il sinistro), raramente coinvolge il lobo<br />
superiore o è bilaterale. Il sequestro extralobare appare nel 75-90% dei casi come<br />
un'opacità retrocardiaca, posteriore al lobo sinistro, a livello del diaframma.<br />
L’angio-TC è la tecnica di prima scelta per la valutazione ottimale del polmone<br />
sequestrato, il suo apporto vascolare, e nella valutazione preoperatoria del<br />
sequestro (Fig 3) ; l’ angio-RM è utile nei casi in cui la TC è controindicata per<br />
esempio nei pazienti con ipersensibilità al mezzo di contrasto iodato. L’angiografia in<br />
quanto invasiva è riservata a casi selezionati e prima di un’embolizzazione<br />
preoperatoria dell’arteria anomala che irrora il sequestro [21, 23].<br />
Fig - 3a Immagine Angio-tc di in un bimbo di 7 anni: arteria sistemica<br />
aberrante che origina dall'aorta (singola freccia) e fornisce un segmento<br />
sequestrato nel lobo inferiore destro<br />
Fig - 3b drenaggio venoso del sequestro attraverso la vena polmonare in atrio<br />
sinistro (doppia freccia) caratteristica tipica di sequestro intralobare [23]<br />
Il trattamento di scelta consiste nella resezione chirurgica del sequestro, anche se<br />
asintomatico, per la conferma istologica, e per i rischi di emorragia, infezione e<br />
trasformazione neoplastica. In genere per il sequestro intralobare è preferita<br />
l’asportazione dell’intero lobo interessato. Diversi autori descrivono la possibilità di<br />
un trattamento toracoscopico (VATS o Video Assisted Thoracic Surgery) anche a<br />
pochi mesi di vita per entrambe le forme di sequestro [21, 23, 24].<br />
Per il trattamento del sequestro extralobare è stata suggerita anche<br />
l'embolizzazione del vaso arterioso anomalo. Tale intervento non è però radicale<br />
perché rimangono i rischi di complicanze legati alla lesione (infezione e neoplasia).<br />
Alcuni autori suggeriscono l’ embolizzazione preoperatoria dell’arteria anomala<br />
prima della resezione di un sequestro intralobare [21, 23].<br />
Enfisema lobare congenito<br />
È una rara anomalia del polmone caratterizzata dall’abnorme accumulo post-natale<br />
di aria in un lobo polmonare. Il lobo interessato per l’intrappolameto di aria si<br />
distende progressivamente causando compressione del circostante tessuto<br />
polmonare e spostamento del mediastino [25].<br />
L’enfisema lobare è secondario ad un’ostruzione bronchiale estrinseca o intrinseca,<br />
primitiva o secondaria, oppure ad un'anomalia alveolare. In circa i 2/3 dei casi è<br />
correlato ad un’anomalia strutturale primitiva quale broncomalacia, atresia, stenosi<br />
bronchiale. Tra le anomalie alveolari primitive si include il lobo polialveolare, cioè un<br />
lobo ipersviluppato con un'istologia alveolare e vascolare normale ma con un<br />
eccessivo numero di alveoli, che agisce sugli altri lobi con un effetto massa.<br />
L’ostruzione bronchiale può essere secondaria a lesioni endobronchiali parzialmente<br />
reversibili (muco viscido, tappi di muco, tessuto di granulazione) o a lesioni<br />
estrinseche compressive (linfoadenopatie, anormalità dei grossi vasi, cisti<br />
broncogene) [2, 25]. In molti casi comunque la causa di un enfisema rimane<br />
sconosciuta. L' enfisema lobare congenito è una patologia molto rara, 2-3 volte più<br />
frequentemente nei maschi, interessa solitamente un lato, colpendo più<br />
frequentemente il lobo superiore sinistro (40-50% dei casi), il lobo medio destro nel<br />
30-40%, il lobo superiore destro nel 20%, raramente i lobi inferiori o più lobi. Non è<br />
nota la causa di questa distribuzione. Fino al 12-20% dei casi può associarsi a<br />
cardiopatie congenite [25, 27]. I disturbi respiratori quali tachipnea, dispnea, tosse,<br />
cianosi, irrequietezza, secondari all’air-trapping e all’espansione progressiva del lobo<br />
affetto, compaiono nei primi giorni di vita nel 50% dei casi. Il 50% dei bimbi affetti<br />
diventano sintomatici più tardi ma comunque entro i primi 6 mesi di vita. La gravità<br />
del distress respiratorio è correlata all’estensione del tessuto polmonare funzionante.<br />
L’esame obiettivo del bambino con enfisema lobare può rilevare un'asimmetria del<br />
torace, un' iperfonesi focale con diminuzione del murmure vescicolare nel lato<br />
affetto. La radiografia del torace è di aiuto nella diagnosi anche se non definitiva.<br />
Aspetti radiologici indicativi di enfisema sono l’iperdiafania del lobo coinvolto, un<br />
ampliamento degli spazi intercostali, lo spostamento controlaterale del mediastino, la<br />
compressione o l’atelettasia del polmone adiacente, l’appiattimento del diaframma<br />
omolaterale (fig 4).<br />
Fig 4 - Rx torace di un neonato di 22 giorni con enfisema polmonare sinistro:<br />
sovra distensione del lobo superiore sinistro con spostamento del mediastino<br />
a destra, e il collasso del polmone omolaterale [27<br />
La diagnosi differenziale si pone con il pneumotorace radiologicamente simile:<br />
nell’enfisema è quasi sempre visibile la trama broncovascolare del polmone<br />
adiacente compresso, mentre nel pneumotorace l’intero polmone appare collassato<br />
all’ilo [2, 4]. La TC o la RM sono utili nei casi dubbi e forniscono migliori dettagli<br />
anotomici. La broncoscopia può essere utile per escludere tappi di muco, corpi<br />
estranei endobronchiali anomalie strutturali dei bronchi su cui poter intervenire.<br />
Potrebbe essere usata in tutti i pazienti che sono candidati al trattamento<br />
conservativo o prima di un intervento chirurgico [2, 25]. Nei neonati e nei bambini<br />
con grave distress respiratorio il trattamento di scelta è la lobectomia perché la storia<br />
naturale della malformazione prevede la progressione verso l'insufficienza<br />
respiratoria, un’elevata mortalità e persistenza dell' enfisema nel 75% dei<br />
sopravvissuti. Diversi studi sono a favore di un atteggiamento conservativo nel<br />
bambino asintomatico poiché la probabilità di un improvviso scompenso è molto<br />
bassa [25, 27].<br />
L'enfisema lobare congenito è tipico del bambino piccolo a termine, e va distinto<br />
dalla malattia enfisematosa tipica del neonato prematuro sottoposto a ventilazione<br />
meccanica a pressione positiva che colpisce soprattutto il lobo inferiore destro e si<br />
presenta con un enfisema interstiziale ed aree multiple di iperinflazione locale.<br />
Nell’enfisema acquisito del pretermine il trattamento medico di supporto è la terapia<br />
di scelta, perché in genere va incontro a risoluzione nell'arco di mesi. La chirurgia è<br />
indicata solo in alcuni casi non rispondenti nel tempo al trattamento medico. A lungo<br />
termine i risultati della lobectomia sono buoni, con bassa mortalità.<br />
Agenesia e aplasia polmonare<br />
L’agenesia polmonare consiste nella mancanza dell'intero polmone con il suo<br />
albero bronchiale, determinata dalla mancata formazione dell'abbozzo bronchiale<br />
dalla trachea. L’eziologia non è nota, sebbene fattori genetici, teratogeni e meccanici<br />
siano stati proposti come possibili cause. È una patologia molto rara (nella sua<br />
forma isolata, 1 ogni 10.000-15.000 autopsie), e colpisce con uguale incidenza i due<br />
lati del polmone e i due sessi [2, 4]. Generalmente è unilaterale ma sono stati<br />
descritti anche rari casi di agenesia polmonare bilaterale. Si associa in oltre il 50%<br />
dei casi ad altre anomalie congenite, quali cardiopatie, atresia dell'esofago,<br />
anormalità scheletriche, malformazioni genitourinarie, sindrome di Vater [28]. Dal<br />
punto di vista anatomico manca la cavità pleurica dal lato affetto e il polmone<br />
controlaterale ha una struttura normale, ma presenta un’ipertrofia compensatoria,<br />
anche nel feto [2].
La classificazione storica di Schneider prevede 2 tipi principali di agenesia<br />
polmonare:<br />
• I tipo: caratterizzato dall'assenza completa di tessuto bronchiale e alveolare;<br />
• II tipo: caratterizzato dalla presenza di elementi bronchiali maggiori con assenza<br />
di alveoli.<br />
In quest'ultimo tipo si parla anche di aplasia polmonare [2, 29]. La differenza tra<br />
agenesia e aplasia polmonare effettivamente è solo radiologica ed endoscopica con<br />
la dimostrazione della presenza di un abbozzo bronchiale.<br />
La presentazione clinica dell’agenesia è variabile: occasionalmente può essere<br />
asintomatica, a volte si manifesta con sintomi respiratori specifici, altre volte con i<br />
sintomi relativi alla malformazione associata. I sintomi respiratori specifici vanno<br />
dalla dispnea all'intolleranza allo sforzo, alla mancata crescita, alle bronchiti e<br />
polmoniti ricorrenti. Frequentemente i pazienti affetti vanno incontro a insufficienza<br />
polmonare cronica progressiva e alla morte. Ciò avviene più frequentemente in caso<br />
di agenesia polmonare destra che si associa ad una rotazione in senso orario e<br />
verso destra del cuore e dei grossi vasi, alla deviazione delle strutture mediastiniche<br />
nell'emitorace destro vuoto, che viene occupato dall'erniazione compensatoria<br />
dell’unico polmone. Questo arrangiamento delle strutture mediastiniche porta ad una<br />
compressione della trachea distale e del bronco principale sinistro tra arco aortico,<br />
arteria polmonare sinistra, dotto arterioso e colonna vertebrale. All'esame obiettivo si<br />
può osservare: asimmetria del torace e nei bambini più grandi scoliosi, riduzione o<br />
assenza del murmure vescicolare [2, 30]. La diagnosi di agenesia polmonare può<br />
essere inizialmente sospettata alla radiografia al torace che mostra un emitorace<br />
piccolo, completamente opaco associato a spostamento delle strutture mediastiniche<br />
e del diaframma (fig 5). Generalmente il polmone controlaterale è normale ma<br />
presenta iperinflazione compensatoria e formazioni di ernie lungo la linea mediana. I<br />
corpi delle vertebre toraciche possono a loro volta presentare una segmentazione<br />
anomala [4].<br />
Deve essere differenziata dall’atelettasia e dall’ernia diaframmatica con l’ausilio<br />
delle indagini strumentali. La TC convenzionale in genere conferma la diagnosi<br />
rivelando l’assenza del parenchima polmonare e dell’albero bronchiale.<br />
L’ecocardiografia, in maniera non invasiva mostra l’assenza del ramo principale<br />
dell’arteria polmonare. Altre indagini più invasive quali broncografia, broncoscopia e<br />
angiografia possono essere riservate a casi particolari [4, 31].<br />
L’aspettativa di vita nel neonato affetto da agenesia polmonare, anche isolata, è<br />
inferiore rispetto al bambino normale: per l’agenesia polmonare destra si calcola sia<br />
in media di 6 anni, mentre per l'agenesia polmonare sinistra di 16 anni [2, 31].<br />
Probabilmente questa differenza è dovuta alla più frequentemente associazione<br />
dell’agenesia destra con lo spostamento mediastinico con distorsione di grossi vasi<br />
e bronchi [28]. Coloro che sopravvivono presentano difficoltà respiratoria e muoiono<br />
quasi tutti per polmonite o insufficienza respiratoria. L’agenesia bilaterale è<br />
incompatibile con la vita. La prognosi è anche influenzata dalla presenza di altre<br />
anomalie associate. La terapia prevede il supporto respiratorio non invasivo e<br />
soprattutto il trattamento aggressivo delle infezioni. Gli interventi chirurgici devono<br />
essere limitati al trattamento delle principali malformazioni associate. Nei casi con<br />
importante sintomatologia respiratoria, può essere preso in considerazione il<br />
posizionamento di una protesi per prevenire lo spostamento del mediastino e le sue<br />
complicanze [2, 32]. Alcuni autori suggeriscono la traslocazione omolaterale del<br />
diaframma quale valida alternativa nei pazienti con aplasia polmonare con distress<br />
respiratorio non responsivo ad altro trattamento [33, 34].<br />
Fig 5 - Rx in proiezione postrero-anteriore in un bambino di 5 anni: opacità<br />
totale dell’emitorace destro e spostamento del cuore e del mediastino verso<br />
destra [4].<br />
È importante citare in questo contesto anche l’agenesia e l’aplasia lobare<br />
segmentale, condizioni molto rare che, probabilmente, non vengono diagnosticate<br />
come tali o vengono classificate come ipoplasia polmonare. Rimangono<br />
asintomatiche, a meno che si associno ad altre malformazioni soprattutto<br />
cardiovascolari (ritorno venoso polmonare anomalo, sindrome della scimitarra). Alla<br />
radiografia del torace si presentano con riduzione di volume del polmone<br />
interessato, spazi intercostali ristretti e sollevamento omolaterale del diaframma. La<br />
diagnosi si fa con la broncoscopia o la broncografia che dimostrano la mancanza di<br />
un lobo o la presenza di un abbozzo di bronco con mancanza di tessuto polmonare.<br />
Il trattamento è legato alle anomalie vascolari e alle infezioni polmonari [2].<br />
Ipoplasia polmonare<br />
Per ipoplasia polmonare s’intende uno sviluppo incompleto o deficitario del<br />
polmone [4], e si caratterizza per la presenza di un ridotto numero di unità broncoalveolari.<br />
Si può presentare in forma isolata e monolaterale, ma molto più<br />
frequentemente in forma bilaterale [2]. La maggior parte dei casi di ipoplasia<br />
polmonare sono secondari a condizioni che direttamente o indirettamente<br />
compromettono lo spazio toracico disponibile per la crescita del polmone fetale,<br />
determinado una compressione intratoracica intrinseca (ernia diaframmatica,<br />
malattia adenomatoide cistica, stenosi bronchiale) o estrinseca (distrofie della parete<br />
toracica che impediscono i normali movimenti respiratori fetali). L’ipoplasia è stata<br />
osservata inoltre nell’oligoidramnios (secondario a malattie renali bilaterali o a<br />
prolungata rottura prematura delle membrane) [35] e in varie patologie<br />
extratoraciche che causano compressione del torace del feto da parte dell’utero.<br />
Altre cause sono la riduzione della perfusione vascolare polmonare (tetralogia di<br />
Fallot) e l’assenza unilaterale dell'arteria polmonare [4]. L’ipoplasia polmonare<br />
primaria è, invece estremamente rara e può essere causata da difetti embriologici<br />
del polmone o dei tessuti vascolari (come nella displasia congenita degli acini) o a<br />
un danno vascolare durante le prime settimane di gestazione (trombosi dell’arteria<br />
polmonare sinistra) [35, 36, 37]. Dopo la nascita, la presentazione clinica è variabile<br />
in base all’estensione del polmone coinvolto e alla presenza di anomalie associate.<br />
Alcuni neonati presentano un distress respiratorio severo nelle prime ore di vita, che<br />
può complicarsi ulteriormente per l’insorgenza di un pneumotorace e di ipertensione<br />
polmonare. Altri neonati possono essere completamente asintomatici [4, 35].<br />
Nell’ipoplasia estesa o bilaterale la morte può essere immediata o rapida,<br />
nonostante l'utilizzo di tutti i presidi terapeutici di cui è oggi fornito un reparto di<br />
terapia intensiva neonatale. Nelle forme meno gravi e quando non vi sono anomalie<br />
associate, l’ipoplasia può essere asintomatica e compatibile con una normale<br />
sopravvivenza [2]. Anche l’età di scoperta di tali malformazioni dipende<br />
dall’estensione dell’ipoplasia e dal volume polmonare funzionante [35].<br />
La diagnosi di ipoplasia polmonare può essere sospettata durante la gravidanza<br />
per i cambiamenti nell'immagine ecografica del parenchima polmonare e per<br />
l'evidenza di patologie che comprimono il polmone, quali un'effusione liquida, una<br />
massa cistica entro il torace, un'ernia diaframmatica, un oligoidramnios od un torace<br />
piccolo [2]. La RM prenatale fornisce ulteriori preziose informazioni permettendo di<br />
valutare il volume dei polmoni. Nell’ipoplasia unilaterale, in genere rileva anche uno<br />
spostamento del mediastino verso il lato dell’ipoplasia, accentuata durante<br />
l'inspirazione a causa dell’aumentata ventilazione compensatoria da parte dell’altro<br />
polmone [4, 35]. In alcuni casi si riscontra un aspetto cistico, che potrebbe essere<br />
dovuto ad un difetto di sviluppo a livello della giunzione bronchiolo-alveolare. Si<br />
rende pertanto necessaria la diagnosi differenziale con la malformazione<br />
adenomatoide cistica congenita [4]. Quando l’ipoplasia unilaterale isolata sfugge alla<br />
diagnosi prenatale, alla nascita la diagnosi viene sospettata con la radiografia del<br />
torace e deve essere differenziata dalle altre cause di dispnea neonatale associata<br />
ad opacità toracica unilaterale: atelettasia, ernia diaframmatica, sequestro<br />
polmonare, chilotorace, cisti broncogena, tumore toracico (neuroblastoma, teratoma,<br />
fibrosarcoma), malformazione adenomatoide cistica congenita [34, 36]. Nel sospetto<br />
di ipoplasia polmonare è utile inoltre eseguire un ecocardiogramma per individuare o<br />
escludere difetti cardiaci congeniti associati e per valutare il drenaggio venoso<br />
polmonare. La diagnosi di ipoplasia bilaterale si basa sulla combinazione di un<br />
precoce distress respiratorio, pneumotorace precoce e ripetuto e di un quadro<br />
radiologico caratterizzato da un piccolo polmone iperlucente per ridotta<br />
vascolarizzazione e persistente circolazione fetale [2]. È essenziale il rigoroso<br />
follow-up dei bambini affetti da ipoplasia polmonare anche se moderata, unilaterale e<br />
inizialmente asintomatica. Bisogna monitorare la funzionalità respiratoria in quanto<br />
questi pazienti spesso sviluppano una patologia polmonare ostruttiva associata a<br />
tracheo-broncomalacia, iperreattività bronchiale o a compressione bronchiale da<br />
parte dei vasi circostanti [38]. La scintigrafia, l’angiografia e la broncoscopia e la RM<br />
sono preziosi strumenti di indagine per il follow-up come per la diagnosi [37]. Il<br />
trattamento consiste nel prevenire le infezioni polmonari e nel trattarle<br />
aggressivamente quando si presentano. Si ricorre alla chirurgia per la correzione<br />
delle anomalie vascolari associate e, nelle forme unilaterali, alla resezione del<br />
polmone ipoplasico in caso di gravi infezioni ricorrenti [35].<br />
Malformazioni vascolari<br />
Tra le malformazioni più rilevanti si annoverano gli anelli vascolari, le malformazioni<br />
arterovenose polmonari, e il ritorno venoso anomalo. Si parla di anello vascolare<br />
quando un’anomalia vascolare, determina per compressione estrinseca<br />
un'ostruzione delle vie aeree. L'anello si dice completo o incompleto a seconda che<br />
la trachea e l'esofago siano completamente o parzialmente avvolti dal vaso<br />
anomalo. Quelli completi sono il doppio arco aortico e l'arco aortico destroposto con<br />
presenza a sinistra del legamento arterioso. L’anomalia più frequentemente<br />
riscontrata è il doppio arco aortico, altre anomalie sono l'arteria innominata<br />
aberrante, lo sling dell'arteria polmonare, l'arteria succlavia sinistra aberrante. Gli<br />
anelli vascolari si manifestano comunemente con stridore spesso bifasico<br />
(esacerbato durante l'alimentazione), tosse secca, cianosi, difficoltà respiratoria,<br />
sibili con espirazione prolungata e rumorosa. L’esordio può avvenire alla nascita o in<br />
periodi successivi, specie in concomitanza di episodi flogistici a carico delle vie<br />
aeree. In alcuni casi l'anomalia anatomica può passare misconosciuta anche per<br />
anni poiché la ricorrenza o la persistenza di episodi di dispnea, stridore, wheezing<br />
vengono impropriamente interpretati e trattati come episodi flogistici o asmatici. Per<br />
la diagnosi è utile l'esofagogramma che può evidenziare incisure riferibili a<br />
compressione estrinseca sulla trachea. Ma sono l’endoscopia, l'angio-RMN o<br />
all'angio-TAC che permettono la conferma diagnostica e l'esatta valutazione<br />
anatomica delle malformazioni vascolari. La terapia consiste nella correzione<br />
chirurgica dell’anomalia. La prognosi è generalmente buona, ma talora residuano<br />
disturbi respiratori legati alla malacia dovuta proprio alla compressione esercitata<br />
sulla trachea [2, 38]. Le malformazioni arterovenose sono molto rare e sintomatiche<br />
nel 50% dei casi. I segni clinici caratteristici sono: dispnea da sforzo, cianosi e dita a<br />
bacchetta di tamburo. La cianosi è causata da un importante shunt destro-sinistro.<br />
All’asculatazione del torace può apprezzarsi un soffio continuo in corrispondenza<br />
della lesione. La malformazione può complicarsi con una massiva emottisi o un<br />
imponente emotorace. Alla radiografia del torace appare come una massa rotonda,<br />
ovalare o plurilobata di varie dimensioni; alla TC o all’angiografia è dimostrata la<br />
natura vascolare della lesione. Frequentemente si riscontrano nel contesto della<br />
sindrome di Osler-Weber-Rendu. Il trattamento consiste nella resezione della lesione
(lobectomia o resezione cuneiforme) ed è curativo. Quando indicata può essere<br />
eseguita anche l'embolizzazione con buoni risultati [2]. Il ritorno venoso anomalo<br />
consiste nel drenaggio di sangue dai polmoni al cuore destro e può essere totale o<br />
parziale, unilaterale o bilaterale, isolato o associato ad altri difetti, ostruito o non<br />
ostruito. Un tipo di ritorno venoso polmonare anomalo parziale è rappresentato dalla<br />
Sindrome della Scimitarra, una rara anomalia congenita (1-3 casi ogni 100.000<br />
nascite), caratterizzata da un polmone destro ipoplastico, un ritorno venoso anomalo<br />
dal polmone nella vena cava inferiore (di solito nel tratto infradiaframmatico) e<br />
un'anomala vascolarizzazione arteriosa, comunemente proveniente dalla<br />
circolazione sistemica. In molti casi una parte del polmone destro riceve sangue<br />
arterioso dall'aorta toracica o dal primo tratto dell' aorta sottodiaframmatica. Il<br />
termine scimitarra deriva dall’immagine radiografica determinata da un vaso<br />
anomalo che originando dal polmone destro scende contornando l’atrio destro, per<br />
confluire nella vena cava inferiore. La sindrome si associa frequentemente a<br />
cardiopatia, destrorotazione cardiaca, ipoplasia o altre malformazioni dell’arteria<br />
polmonare destra, ad anomalie anatomiche dei bronchi, del diaframma, del tratto<br />
genitourinario, ad emivertebre [4, 39]. Il quadro clinico e la prognosi della sindrome<br />
della scimitarra dipendono in larga misura dall’ampiezza dello shunt destro-sinistro.<br />
In genere si manifesta clinicamente intorno alla II o III decade di vita con fatica e<br />
dispnea da sforzo, più raramente con ricorrenti infezioni polmonari. Nella forma<br />
infantile si riscontra una maggiore prevalenza di ipertensione polmonare [4]. La<br />
diagnosi si basa sulla radiografia del torace, l’ecocardiocolordoppler, la TC o la RM.<br />
All'esame radiografico il polmone appare di dimensioni ridotte ed è visibile a destra<br />
un’opacità convessa, nastriforme che si allontana dall’ilo [39]. La TC mostra la<br />
dimensione dell'emitorace destro, le anomalie bronchiale, e la vena anomala.<br />
L’ecodoppler può mostrare l'ingresso del vena anomala nella vena cava inferiore ed<br />
è in grado di verificare il flusso venoso. L’angio-RM o TC permettono un’eccellente<br />
visualizzazione dell’anatomia vascolare polmonare ed sono indispensabili prima<br />
dell’intervento chirurgico [4.]. In genere la correzione comporta la deviazione<br />
nell'atrio sinistro del ritorno venoso anomalo polmonare destro. Raramente si rende<br />
necessaria la pneumonectomia [2].<br />
Bibliografia<br />
1 Guidi R, MidullaF, Mileto F, Scalercio F, Korn D, Marabotto C, Tuccinardi R, C<br />
Moretti Le malformazioni congenite delle alte vie aeree: aspetti clinici e diagnostici;<br />
Pneumologia <strong>Pediatrica</strong> 2004;14: 30-46;<br />
2 Locatelli G, Migliazza L, Locatelli C, Alberti D Divisione di Chirurgia Pediatriea,<br />
Ospedali Riuniti di Bergamo Malformazioni congenite delle basse vie aeree e dei<br />
polmoni; Pneumologia <strong>Pediatrica</strong> 2004; 14: 47-62<br />
3 Cittadini G. Malformazioni Polmonari; Diagnostica per immagini e radioterapia<br />
2003; XV: 285-289<br />
4 Berrocal T, Madrid C, Novo S, Gutiérrez J, Arjonilla A, N G León Congenital<br />
Anomalies of the Tracheobronchial Tree, Lung, and Mediastinum: Embryology,<br />
Radiology, and Pathology; Radiographics 2004; Jan-Feb;24 (1) :e17<br />
5 Larsen W J I polmoni cominciano a svilupparsi nella quarta settimana e<br />
cominciano a maturare poco prima della nascita Embriologia umana 1995; 126-131<br />
6 G. Crepaldi, A. Baritussio Trattato di medicina interna vol 3; 2003<br />
7 Berdon WE. Ring, sling, and other things: vascular compression of the infant<br />
trachea updated from the mid century to the millennium — the legacy of Robert<br />
E.Gross, and Edward B. D. Neuchauser; Radiology 2000; Sep; 216 (3) : 624-32<br />
8 Briganti V, Mirabile L Quadri Clinici Endoscopici Patologia interventistica 2007;<br />
60:635-36<br />
9 Bye M. R Tracheomalacia Medscape reference 2009; Aug 27<br />
10 Namara VM Mc, Crabbe DC Trocheomolocia Paediatr Respir Rev 2004; 5:<br />
147-154<br />
11 Filler RM, Forte V, Fraga JC, Matute J The use of expandable metallic airway<br />
stents for trachea-bronchial obstruction in children J Pediatr Surg. 1995 Jul;30 (7)<br />
:1050-6<br />
12 P Monnier Pediatric Airway Surgery: Management of Laryngotracheal Stenosis<br />
in Infants and children;2011<br />
13 Kim HK, Kim YT, Sung SW, JD Park, Kang CH, Kim JH, Kim YJ Management of<br />
congenital tracheal stenosis; YJEur J Cardiothorac Surg. 2004 Jun; 25 (6) :1065-71<br />
14 Antón-Pacheco JL, Galletti L, Cabezalí D, Luna C, González de Orbe G,<br />
Sánchez-Solis de Querol M Management of bilateral congenital bronchial stenosis in<br />
an infant; Journal of Pediatric Surgery 2007 November; 42 (11) :1-3<br />
15 Kliegman R M, Stanton B, Geme J St., Schor N, Behrman R E.; Nelson Textbook<br />
of Pediatrics 19th edition 2010<br />
16 Wei-Shiu Chen, Guang-Perng Yeh, Horng-Der Tsai, Charles Tsung-Che Hsieh<br />
Prenatal diagnosis of congenital cystic adenomatoid malformations: evolution and<br />
outcome; Taiwan J Obstet Gynecol 2009 September;Vol 48 N. 3<br />
17 Horak E, Bodner J, Gassner I, Schmid T, Simma B, Grässl G, Sawyer SM<br />
Congenital cystic lung disease: diagnostic and therapeutic considerations; Clin<br />
Pediatr (Phila) 2003 Apr; 42 (3) :251-61<br />
18 Wilson RD, Hedrick HL, Liechty KW, Flake AW, Johnson MP, Bebbington M,<br />
Adzick NS Cystic Adenomatoid Malformation of the Lung: Review of Genetics,<br />
Prenatal Diagnosis and in Utero Treatment; Am J Med Gen 2006;140A:151-55<br />
19 Sauvat F, Michel JL, Benachi A., Emond S, Revillon Y Management of<br />
Asymptomatic Neonatal Cystic Adenomatoid Malformations; J Pediatr Surg. 2003<br />
Apr;38 (4) :548-52<br />
20 Butterworth SA, Blair GK Postnatal spontaneous resolution of congenital cystic<br />
adenomatoid malformations; J Pediatr Surg; 2005 May;40 (5) :832-4<br />
21 Gonzalez D, J Garcia, Fieira E, Paradela M Video-assisted thoracoscopic<br />
lobectomy in the treatment of intralobar pulmonary sequestration; Interact<br />
Cardiovasc Thorac Surg 2011 Jan;12 (1) :77-9<br />
22 Boetzkes S, Wojciechowski M, de Beukelaar T, Ramet J, Van Schil P Intralobar<br />
bronchopulmonary sequestration with mixed venous drainage in a 10-year-old girl;<br />
Acta Chir Belg; 2009 Jul Aug;109 (4) :501-3<br />
23 Abbey P, Das CJ, Pangtey GS, Seith A, Dutta R, Kumar A Imaging in<br />
bronchopulmonary sequestration; J Med Imaging Radiat Oncol; 2009 Feb;53 (1)<br />
:22-31<br />
24 Jesch NK, Leonhardt J, Sumpelmann R, Gluer S, Nustede R Ure<br />
BMThoracoscopic resection of intra- and extralobar pulmonary sequestration in the<br />
first 3 months of life; J Pediatr Surg 2005; Sep;40 (9) :1404-6<br />
25 Ulku R, Onat S, Ozçelik C Congenital lobar emphysema: differential diagnosis<br />
and therapeutic approach; Pediatr Int 2008 Oct;50 (5) :658-61<br />
26 Tempe DK, Virmani S, Javetkar S, Banerjee A, Puri SK, Datt V Congenital lobar<br />
emphysema: pitfalls and management Ann Card Anaesth 2010; Jan-Apr;13 (1) :53-8<br />
27 Datta AK, Mandal S, Jana JK Congenital lobar emphysema: a case report;<br />
Cases J.2009; Jan 20;2 (1) :67<br />
28 Viora E, Sciarrone A, Bastonero S, Errante G, Campogrande M Prenatal<br />
diagnosis of isolated unilateral pulmonary genesis in the second trimester;<br />
Ultrasound Obstet Gynecol. 2002 Feb;19 (2) :206-7<br />
29 Lee KA, Cho JY, Lee SM, Jun JK, Kang J, Seo JW Prenatal Diagnosis of<br />
Bilateral Pulmonary Agenesis: a Case Report; Korean J Radiol 2010;11:119-122<br />
30 Wexels P Agenesis of the lung; Thorax 1951; 6: 171-192<br />
31 Valle AR. Agenesis of the lung. AmJSurg 1955; 89: 90-100<br />
32 Sharma S, Kumar S, Yaduvanshi D, Chauhan D Isolated unilateral pulmonary<br />
agenesis; Indian Pediatr. 2005 Feb;42 (2) :170-2<br />
33 Krivchenya DU, Rudenko EO, Lysak SV, Dubrovin AG, Khursin VN, Krivchenya<br />
TD Lung aplasia: anatomy, history, diagnosis and surgical management Eur J<br />
Pediatr Surg 2007; Aug17 (4) :244-50<br />
34 Krivchenya DU, Dubrovin AG, Krivchenya TD, Khursin VN, Lysak CV Aplasia of<br />
the right lung in a 4-year-old child: surgical stabilization of the mediastinum by<br />
diaphragm translocation leading to complete recovery from respiratory distress<br />
syndrome J Pediatr Surg.2000 Oct;35 (10) :1499-502<br />
35 Demaret P, Menten R, Debauche C, Moniotte S Imaging of primary unilateral<br />
pulmonary hypoplasia: a case report Eur J Pediatr. 2009 Sep;168 (9) :1151-3<br />
36 Abrams ME, Ackerman VL, Engle WA. Primary unilateral pulmonary hypoplasia:<br />
neonate through early childhood - case report, radiographic diagnosis and review of<br />
the literature; J Perinatol. 2004 Oct;24 (10) :667-70<br />
37 Elhassan NO, Sproles C, Sachdeva R, Bhutta ST, Szabo JS A neonate with left<br />
pulmonary artery thrombosis and left lung hypoplasia: a case report J Med Case<br />
Reports. 2010 Aug 23;4:284<br />
38 Chou AK, Huang SC, Chen SJ et al Unilateral lung agenesis-detrimental roles of<br />
surrounding vessels Pediatr Pulmonol. 2007 Mar;42 (3) :242-8<br />
39Guidi R, Midulla F, Mileto F, Scalercio F, Korn D, Marabotto C, Tuccinardi R,<br />
Moretti C Le malformazioni congenite delle alte vie aeree: aspetti clinici e diagnostici<br />
Pneumologia <strong>Pediatrica</strong> 2004; 14: 30-46<br />
40 Stasolla A, Manganaro F, Pepino D, Matrunola M La diagnostica per immagini<br />
delle malformazioni dell'apparato respiratorio Pneumologia <strong>Pediatrica</strong> 2004; 14:<br />
20-29<br />
Trimestrale di divulgazione scientifica dell'Associazione <strong>Pediatrica</strong> di <strong>Immunologia</strong> e <strong>Genetica</strong><br />
Legge 7 marzo 2001, n. 62 - Registro della Stampa Tribunale di Messina n. 3/09 - 11 maggio 2009<br />
Direttore scientifico Carmelo Salpietro - Direttore responsabile Giuseppe Micali - Segreteria redazione Basilia Piraino - Piera Vicchio<br />
Direzione-Redazione: UOC <strong>Genetica</strong> e <strong>Immunologia</strong> <strong>Pediatrica</strong> - AOU Policlicnico Messina<br />
www.geneticapediatrica.it/rigip