Sbobinature complete Anatomia Patologica - SunHope
Sbobinature complete Anatomia Patologica - SunHope
Sbobinature complete Anatomia Patologica - SunHope
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
ANATOMIA PATOLOGICA 18/10/2010<br />
L'anatomia patologica ci da un'impostazione pratica, perché con questa materia trasferite in<br />
campo clinico quello che ci proviene dalle discipline di base.<br />
Queste sono le tabelle di mortalità dell'american cancer society del 2009, in queste tabelle<br />
vediamo che in rapporto all'età, il cancro incomincia a diventare la prima causa di morte nei<br />
maschi e nelle femmine nell'età che va dai 60 ai 79 anni e nei maschi addirittura già nell'età<br />
che va dai 40 ai 59 anni; al secondo posto troviamo le malattie cardiache o di altro tipo.<br />
Vedendo le casistiche autoptiche ci rendiamo conto che il cancro è sottodiagnosticato<br />
soprattutto nell'anziano, nei confronti del quale vi è un aspetto rinunciatario a causa del quale<br />
si sottovalutano alcune patologie neoplastiche per esempio il cancro del pancreas, del fegato<br />
ed anche in parte quello della prostata sono sottovalutati (superati i 60 anni il cancro della<br />
prostata è diffusissimo).<br />
Secondo questa tabella verso gli anni '90 si è avuta un'inversione cioè le malattie cardiache<br />
cadono mentre il cancro rimane stabile.<br />
Tra le cause di morte c'è il cancro della mammella nella donna che incide per il 27% dei casi e<br />
al secondo posto c'è il cancro polmonare; nel maschio al primo posto la prostata che molto<br />
spesso, ma non sempre, è un cancro di serie B come mortalità, mentre al secondo posto c'è il<br />
cancro del polmone.<br />
Un epitelio pavimentoso stratificato è caratterizzato dal fatto che le cellule che stanno in basso<br />
sono cellule piccole, hanno un nucleo piccolo, un piccolo citoplasma e tendono a disporsi a<br />
palizzata e questo strato rappresenta il compartimento proliferativo di tutto l'epitelio perché qui<br />
troviamo le cellule che si moltiplicano.<br />
Man mano che da questo strato saliamo in alto, le cellule si specializzano, si differenziano<br />
quindi non si moltiplicano più, fino a diventare strato corneo e così morire.<br />
Questo sistema ovviamente deve essere stabile perché il numero delle cellule che entra nel<br />
sistema deve essere uguale al numero delle cellule che escono dal sistema.<br />
Più saliamo in alto più vediamo che il citoplasma aumenta e il nucleo diventa più grande<br />
perché assume una specializzazione che prima non aveva.<br />
Le cellule che costituiscono lo stato basale stanno in contatto con una struttura fondamentale<br />
che si chiama membrana basale. La membrana basale è quella struttura che divide il<br />
compartimento epiteliale dal compartimento connettivale che sta in basso.<br />
Tra le cellule basali si nascondono le cellule staminali.<br />
Quali sono quei processi o quelle alterazioni che possiamo avere in questo epitelio? Sono:<br />
l'iperplasia e la metaplasia.<br />
L'iperplasia che è un aumento numerico delle cellule, numerico per unità di volume, ma dal<br />
punto di vista dinamico, biologico, si caratterizza per una serie di proprietà.<br />
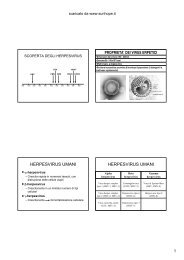
Nella figura voi vedete queste X rosse che rappresentano le cellule mitotiche.<br />
Nell'epitelio normale queste X le possiamo ritrovare solo nello strato basale mentre in un<br />
epitelio iperplastico c'è un'espansione del compartimento proliferativo, per cui possiamo<br />
trovare anche figure mitotiche (normalmente presenti solo nello strato basale) anche verso<br />
l'alto, cioè nel rapporto tra proliferazione e differenziamento, la proliferazione prende il<br />
sopravvento e quindi il numero delle cellule aumenta. Questo non è cancro, è iperplasia.<br />
Nell'epitelio cilindrico vi faccio l'esempio della metaplasia.<br />
La metaplasia è un cambio di specializzazione, passiamo da un epitelio monostratificato ad un<br />
epitelio pluristratificato.<br />
La metaplasia ha un significato non cattivo: prendiamo ad esempio la mucosa endocervicale,<br />
se ha degli stimoli infiammatori o se c'è un'erniazione, un po' di endocervice esce fuori e va<br />
nell'esocervice, soprattutto dopo il parto, allora questo epitelio che si trovava tranquillo nel<br />
canale endocervicale viene esposto agli agenti esterni, ai batteri ecc. e allora che fa?<br />
scaricato da www.sunhope.it
Si protegge diventando pavimentoso stratificato, però non sempre accade ciò infatti ci sono<br />
delle volte che esprime disordine assoluto.<br />
Dall'iperplasia alla metaplasia c'è una linea tratteggiata che rappresenta la displasia. Perché c'è<br />
la linea tratteggiata? Perché non sempre si verifica questo passaggio.<br />
La displasia la possiamo definire come un'alterazione dell'architettura dell'organo, del tessuto e<br />
anche come presenza di atipie citologiche.<br />
La displasia quindi non ha niente a che vedere con l'iperplasia e la metaplasia, nella displasia<br />
c'è questo disordine che coinvolge l'architettura e la citologia.<br />
In genere noi gradiamo la displasia in 3 livelli:<br />
- displasia lieve o G1, quando è coinvolto il 1/3 inferiore dell'epitelio perché tutto parte dalle<br />
cellule che hanno un'attività replicativa<br />
- displasia moderata o G2, quando le atipie strutturali coinvolgono i 2/3 dell'epitelio<br />
- displasia grave o G3 o carcinoma in situ, quando è coinvolto tutto lo spessore dell'epitelio.<br />
Alcuni testi fanno una distinzione tra displasia grave e carcinoma in situ, ma il prof non la<br />
condivide, per cui la displasia grave è assimilabile al carcinoma in situ.<br />
Diciamo in situ perchè la membrana basale non è stata superata quindi è un cancro potenziale<br />
che però non ha ancora esplicato la sua aggressività.<br />
Le cellule displasiche hanno delle caratteristiche:<br />
1) aumento delle figure mitotiche, questa componente displastica evidenzia un'aumentata<br />
attività proliferativa<br />
2) il polimorfismo<br />
EPITELIO PLURISTRATIFICATO EPITELIO DISPLASTICO<br />
1) Le cellule non sono uguali, sono 1) Le cellule sono molto diverse le<br />
molto simili a seconda dello strato une dalle altre, c'è un caos, un<br />
disordine architettonico<br />
2) E' possibile osservare un gradiente 2) Non è presente gradiente<br />
maturativo cioè man mano che saliamo maturativo, anzi c'è un disordine<br />
verso l'alto le cellule si ingrandiscono e totale<br />
mostrano caratteristiche di maggiore<br />
specializzazione<br />
Adesso descrive un vetrino:<br />
questo è un epitelio pavimentoso stratificato, vedete come le cellule basali sono piccole e si<br />
dispongono perpendicolarmente rispetto al connettivo e man mano che saliamo queste cellule<br />
si ingrandiscono (soprattutto nel citoplasma) fino ad arrivare in alto.<br />
Nella displasia lieve, voi vedete che soprattutto a livello del 1/3 inferiore c'è un disordine,<br />
manca questa polarità delle cellule che si dispongono a palizzata, le cellule si dispongono in<br />
maniera caotica ma verso l'alto vedete che prosegue la maturazione.<br />
Nella displasia grave non è più possibile distinguere i vari strati perchè c'è un caos<br />
generalizzato, quindi le cellule che stanno in basso sono uguali a quelle che stanno sopra, c'è<br />
questo pleomorfismo di fondo e c'è questo aumento dell'attività mitotica.<br />
Altra distinzione che facciamo è tra: lesione pre-cancerosa e condizione pre-cancerosa.<br />
La lesione pre-cancerosa è una tappa che può essere obbligata o non verso il cancro, ad<br />
esempio se il viaggio che fa il cancro è Napoli/Milano, Bologna è una lesione pre-cancerosa.<br />
Non è detto che sia obbligato, perchè tutto può finire a Bologna cioè non è che ci debba essere<br />
il cancro invasivo propriamente detto, anche se però ci sono dei casi in cui una lesione precancerosi<br />
è obbligata, ma sono molto rari.<br />
scaricato da www.sunhope.it
In genere la pre-cancerosi è facoltativa perchè il cancro può nascere anche nascere d'emblée,<br />
senza passare per la displasia cioè nasce già come cancro, però in linea di massima c'è questa<br />
progressione.<br />
L'iperplasia e la metaplasia possono essere una condizione pre-cancerosa, possono essere<br />
innocenti o possono essere come una spia che si accende e che ci dice che in questa persona<br />
c'è un aumentato rischio di avere il cancro, per esempio nei bronchi voi sapete che c'è un<br />
epitelio cilindrico, in un fumatore è frequente trovare nei bronchi, per irritazione da fumo, un<br />
epitelio pavimentoso stratificato corneificato come la cute.<br />
Questa metaplasia squamosa è una condizione pre-cancerosa e non è strano perchè il primo<br />
cancro del polmone in ordine di incidenza è il carcinoma squamoso.<br />
Il carcinoma squamoso che compare in un organo come il polmone dove normalmente l'epitelio<br />
squamoso non c'è.<br />
Anche l'iperplasia in alcuni organi come l'intestino e così via di per se non è un indice di<br />
malignità ma può essere una spia debole o forte (debole se il rischio è aumentato di una volta<br />
e mezzo, forte se il rischio è aumentato di 10, 20 volte).<br />
Cosa succede a questo punto della storia?<br />
La displasia come lesione pre-cancerosa si può arrestare, la displasia lieve è reversibile cioè<br />
può anche scomparire a differenza di quella moderata e grave che tendono a persistere o a<br />
progredire verso il cancro invasivo.<br />
A questo punto queste cellule così polimorfe, così atipiche, si trovano schiacciate contro la<br />
membrana basale perchè è aumentato il numero delle cellule nella stessa unità di superficie<br />
rispetto all'epitelio normale e per questo stanno una addosso all'altra.<br />
Queste cellule schiacciate si trovano in crisi energetica perchè le risorse energetiche sono<br />
quelle che sono, il nucleo delle cellule è aumentato e si trovano di fronte ad una barriera<br />
notevolissima che si chiama membrana basale che è molto complessa e può sembrare<br />
insormontabile tranne che per queste cellule.<br />
Un metodo da loro utilizzato per superare questa barriera è la clonalità, l'evoluzione clonale<br />
cioè quel clone dopo essere arrivato sotto la membrana basale, muore, e farà posto a nuovi<br />
cloni, quindi dei cloni muoiono mentre altri invece nascono.<br />
Clonale vuol dire alterazione adattiva.<br />
Ovviamente i cloni che sopravvivono, cioè che hanno un vantaggio biologico sono quelli che<br />
non hanno bisogno di determinate proteine, di determinate tensioni di ossigeno, ecc.<br />
A questo punto cosa succede? Nascono dei cloni che acquisiscono delle capacità litiche<br />
progressive perchè per rompere la membrana basale c'è necessità di rompere tutta una serie<br />
di strati. L'acquisizione delle capacità litiche ce la spieghiamo con il concetto della selezione<br />
clonale cioè nasce un clone che comincia a rompere il primo strato della membrana basale e<br />
questo clone muore per far posto al clone che sta dietro di lui che sarà in grado di rompere gli<br />
altri strati della membrana basale essendo più specializzato.<br />
Se andiamo a guardare sotto la membrana basale, troviamo un numero di vasi molto<br />
aumentato, come se le cellule che stanno sopra in qualche modo si preparassero la strada<br />
perchè in effetti l'obiettivo di queste cellule è quello di raggiungere le fonti energetiche e cioè i<br />
vasi dove c'è ossigeno, sostanze nutritizie ecc.<br />
Queste cellule sono inchiodate l'una all'altra e alla membrana basale e quindi affinché questa<br />
storia continui è necessario il detachment cioè il distacco tra di loro.<br />
Queste cellule si devono distaccare in modo tale che possano andare oltre la membrana<br />
basale, inoltre devono acquisire capacità litiche per cui ci sarà un clone più cattivo, più<br />
specializzato degli altri, che riuscirà a superare la membrana basale.<br />
Dopo aver attraversato la membrana basale, le cellule si trovano in un ambiente ostile<br />
rappresentato dal connettivo quindi devono acquisire altri enzimi litici in grado di rompere gli<br />
strati del collagene.<br />
scaricato da www.sunhope.it
A questo punto ci troviamo di fronte ad un bivio:<br />
1) questo tessuto neoplastico, canceroso che ha superato la membrana basale può rimanere<br />
così (soprattutto nell'anziano) e questa condizione è definita tumor dormancy cioè una specie<br />
di dormiveglia del cancro in cui si realizza un equilibrio biologico instabile tra i poteri di difesa<br />
dell'organismo (linfociti, macrofagi) e l'aggressività del cancro<br />
2) oppure questo tessuto neoplastico progredisce e quindi parliamo di progressione tumorale.<br />
Qual è la tappa successiva della progressione tumorale?<br />
La tappa successiva è l'invasione di organi che si esplica attraverso le metastasi perchè il<br />
problema centrale del cancro è la metastasi perchè condiziona la sopravvivenza del cancro.<br />
La metastasi è diversa dall'invasività tra organi adiacenti.<br />
Parliamo di invasività quando abbiamo ad esempio un cancro dell'utero che può coinvolgere le<br />
tube, le ovaie; mentre le metastasi implicano un concetto di diffusione a distanza.<br />
Possiamo avere delle METASTASI PER CADUTA, esempio classico è quello del cancro gastrico.<br />
Ci sono cancri gastrici che si presentano in maniera clinicamente subdola perchè non danno<br />
delle masse quindi se uno si fa l'endoscopia non si vede nulla però anche essendo piccoli,<br />
bucano la parete e cadono sull'ovaio, si forma il cosiddetto tumore di Krukenberg che è<br />
bilaterale.<br />
Quando non c'è diagnosi di cancro dello stomaco, per l'anatomo-patologo è difficile stabilire se<br />
sono primitivi o secondari.<br />
Le metastasi più classiche sono quelle che avvengono per via linfatica e che raggiungono i<br />
linfonodi o quelle per via ematica che ci spaventano di più perchè vanno più lontane.<br />
Le cellule che abbiamo lasciato nel connettivo vanno incontro all'intravasation cioè la<br />
penetrazione di queste cellule nel vaso. Anche questa fase è complessa perchè il vaso ha vari<br />
strati che sono rotti grazie a capacità litiche dei cloni, quindi anche qui ci sono cloni che<br />
muoiono per lasciare il posto ad altri cloni che hanno capacità litiche più specifiche grazie alle<br />
quali entrano nel sangue.<br />
Una volta penetrate nel sangue, si verifica l'embolizzazione cioè la presenza di cellule tumorali<br />
nei vasi è l'evento più sfortunato che può capitare a queste cellule, infatti più del 99% di<br />
queste cellule tumorali muoiono perchè nel vaso c'è una tensione di ossigeno che loro non<br />
sopportano in quanto più elevata rispetto a quella dei tessuti.<br />
La loro morte inoltre è dovuta anche al fatto il loro genoma è più fragile rispetto a quello delle<br />
cellule normali; questa fragilità del genoma è stata definita PLASTICITA' DEL GENOMA ed è<br />
dovuta al fatto che durante le varie mitosi, importanti per la nascita di nuovi cloni, si hanno<br />
mutazioni quindi non c'è una stabilizzazione del genoma come invece accade nelle cellule<br />
normali.<br />
Oltre alla fragilità del genoma, dobbiamo considerare che nel torrente circolatorio queste<br />
cellule sono attaccate dalle cellule natural killer, per cui alla fine sopravvive solo l'1% di queste<br />
cellule.<br />
Nel caso in cui il clone dovesse sopravvivere nel vaso, attraverso complessi meccanismi che poi<br />
vedremo, ad un certo punto del suo viaggio si arresterà in un vaso così da raggiungere un altro<br />
sito.<br />
La fase di metastatizzazione può prescindere dall'embolizzazione, nel senso che<br />
l'embolizzazione è frequentissima in tutti i tumori maligni, ma la metastatizzazione no infatti<br />
riguarda soli il 20-30% dei casi.<br />
Cosa significa ciò? Significa che per metastatizzare questa popolazione cellulare, deve trovare<br />
delle condizioni adatte, perchè può anche arrivare in un altro organo, ma ciò non basta perchè<br />
può trovare delle condizioni di pH, delle condizioni ambientali, delle condizioni umorali che non<br />
gli consentono di sopravvivere.<br />
Quindi c'è embolizzazione ma non c'è metastasi.<br />
scaricato da www.sunhope.it
La metastasi quando trova condizioni favorevoli si comporta come il tumore primitivo quindi<br />
ricomincia tutto da capo cioè deve arrivare a nuovi vasi e così via, fino ad arrivare a colpire un<br />
organo cosiddetto chiave che funziona da serbatoio di disseminazione del cancro, per cui segue<br />
come un processo miliarico canceroso. Miliarico nel senso che c'è una disseminazione<br />
generalizzata, ovviamente questa è la parola fine.<br />
Gli organi chiave sono il fegato, il polmone, dipende dai casi.<br />
Perchè si verificano tutti questi fenomeni?<br />
Se vogliamo fare un sommario di tutto quello che abbiamo visto, noi diciamo che:<br />
1) c'è una clonalità in evoluzione continua legata a fenomeni di selezione naturale e a stimoli<br />
adattivi, a seconda dell'ambiente che ha un'importanza fondamentale perchè noi in genere<br />
consideriamo solo la cellula tumorale ed invece l'ambiente ha un'importanza fondamentale.<br />
2) la proliferazione e differenziamento a favore della proliferazione<br />
3) la presenza di figure mitotiche atipiche (la figura mitotica tipica che vediamo anche in<br />
microscopia ottica presenta simmetria), così definite perchè presentano asimmetria cioè si<br />
incomincia a vedere che tra due cellule il materiale nucleare è distribuito tra l'una e l'altra in<br />
quantità diversa<br />
4) il polimorfismo aumenta<br />
5) aumentano le capacità invasive<br />
6) aumentano le capacità metastatizzanti. Perchè ci sono delle preferenze circa le sedi di<br />
metastatizzazione? Queste preferenze possono essere legate a motivi di anatomia topografica,<br />
per esempio un cancro dell'intestino che metastatizza il fegato ce lo spieghiamo, ma nella<br />
maggior parte dei casi ci sono delle preferenze che non ci spieghiamo in termini di anatomia<br />
topografica<br />
7) la selezione clonale cioè il fatto che si formano dei cloni che hanno la capacità di adattarsi e<br />
quindi hanno una selezione vantaggiosa<br />
Come mai si realizza questo squilibrio tra proliferazione e differenziamento a favore della<br />
proliferazione?<br />
Qui dobbiamo parlare di oncogeni, oncosoppressori e dei meccanismi di apoptosi che sono<br />
presenti in queste cellule<br />
ONCOGENI<br />
E' un termine improprio perchè questi geni si trovano normalmente anche in cellule normali,<br />
per cui quando si scoprì questo fatto, si introdusse il termine proto-oncogene per indicare il<br />
gene normale.<br />
Quindi il proto-oncogene è il gene normale mentre l'oncogene è il proto-oncogene attivato.<br />
I geni come funzionano? I geni funzionano attraverso le proteine perchè i geni codificano delle<br />
proteine.<br />
I primi due meccanismi cioè l'amplificazione ed il riarrangiamento, determinano un aumento<br />
della proteina, la quale rimane la stessa.<br />
Per esempio se c'è un'amplificazione di quella sequenza genica cioè quella sequenza viene<br />
ripetuta un numero anche notevole di volte nel cromosoma, avremo un numero di proteine<br />
maggiore.<br />
Per quanto riguarda il riarrangiamento genico, voi sapete che nel DNA abbiamo 30.000 geni<br />
attivi che sono seguiti o preceduti da altre sequenze che ne facilitano o bloccano l'espressione.<br />
Questi geni si possono trovare in una posizione tale per cui c'è una sequenza che ne inibisce<br />
l'espressione cioè la capacità di trascrizione e tutto il resto.<br />
scaricato da www.sunhope.it
Se trasloca la sequenza, il gene potrà esprimersi; oltre alla sequenza può traslocare anche il<br />
gene stesso e come conseguenza avremo un aumento della produttività però dal punto di vista<br />
qualitativo la proteina è la stessa, quindi c'è una mutazione quantitativa.<br />
La mutazione puntiforme invece è quella che determina una proteina biologicamente alterata<br />
che poi vedremo questa alterazione darà una serie di conseguenze.<br />
La proteina può non essere alterate completamente oppure può essere alterate solo una parte<br />
che però è in grado di compromettere la sua azione biologica.<br />
Gli oncogeni agiscono in maniera dominante cioè basta che un solo allele sia mutato per<br />
scatenare l'effetto oncogenico anche se l'altro allele è normale.<br />
Quali sono questi prodotti oncogenici? I più importanti sono:<br />
- i recettori per i fattori di crescita<br />
- i trasduttori di segnali, per esempio le protein-chinasi perchè il recettore si lega al ligando e<br />
poi si ha la trasduzione del segnale<br />
- i fattori di crescita propriamente detti<br />
- i rimodellatori della cromatina<br />
- i fattori di trascrizione, ormai ne conosciamo parecchi perchè quel gene può stare lì però la<br />
sua attività è condizionata dai fattori di trascrizione cioè può essere attivo o non attivo a<br />
seconda della disponibilità e dell'attività di questi fattori di trascrizione.<br />
Questi fattori di trascrizione spesso sono organo-specifici, per esempio TTF-1 è del polmone<br />
per cui noi possiamo sfruttare questa proprietà ai fini diagnostici<br />
- regolatori dell'apoptosi e del ciclo cellulare<br />
Una cellula più recettori per i fattori di crescita ha e più è disponibile a proliferare rispetto ad<br />
una cellula che ha meno recettori per i fattori di crescita e quindi è meno stimolabile.<br />
I recettori per i fattori di crescita sono tantissimi, quelli più importanti sono:<br />
- epidermal growth factor (EGF)<br />
- HER-1, HER-2, HER-3, HER-4. Il recettore HER-2 è importantissimo nel cancro della<br />
mammella<br />
Questi recettori hanno quasi sempre un dominio tirosin-chinasico composto da:<br />
- una porzione extracellulare<br />
- una porzione intramembranosa<br />
- una porzione intracellulare che quasi sempre corrisponde ad una tirosin-chinasi<br />
Vediamo che cosa succede: se questo recettore trova il suo ligando specifico, rappresentato da<br />
una serie di sostanze per esempio TGF-α (Transforming growth factor alpha) ed altre sostanze,<br />
si dimerizza (e quindi abbiamo un monodimero o un eterodimero o un omodimero) e abbiamo<br />
l'attivazione di questo recettore.<br />
Cosa succede a questo punto? Non succede niente perchè abbiamo la tirosin-chinasi che deve<br />
essere fosforilata, attraverso particolari proteine, per trasdurre il segnale alle cellule, quindi se<br />
è fosforilata abbiamo l'attivazione completa di quel sistema.<br />
L'HER-2 è amplificato nel 25-30% dei cancri della mammella, questo significa che molto spesso<br />
sono quelle forme più aggressive perchè se amplificato vuol dire che c'è una capacità di<br />
crescita maggiore, ma sono anche le forme che ci giovano notevolmente nelle nuove terapie<br />
biologiche di cui parlerete in farmacologia.<br />
Come si fa a vedere se un cancro esprime o meno questa amplificazione?<br />
Siccome si tratta di recettori di membrana, se c'è un'amplificazione tutta la superficie della<br />
cellula viene ricoperta da questi recettori.<br />
Se utilizziamo un anticorpo contro l'HER-2 e un substrato diciamo un metodo<br />
immunoenzimatico per esempio la perossidasi che in presenza di un substrato specifico come<br />
la diaminobenzidina che è incolore, precipita e da un colorito nero-marroncino.<br />
Quando l'HER-2 è amplificato osserveremo delle immagini ad occhiello.<br />
Questi pazienti non devono essere sottoposti alla chemioterapia, ma alla terapia biologica che<br />
costa un sacco di soldi.<br />
scaricato da www.sunhope.it
Se abbiamo dei risultati dubbi, ricorriamo alla biologia molecolare cioè adottiamo una tecnica<br />
di ibridazione in situ cioè andiamo a cercare direttamente il gene per vedere se è amplificato o<br />
meno. Il problema è che a volte le cellule possono essere tetraploidi, aneuploidi cioè avere un<br />
contenuto di DNA maggiore e quindi io posso trovare questa sequenza pluriespressa nella<br />
cellula, però si tratta di una falsa iperesppressione legata all'aumento del contenuto di DNA.<br />
Cosa facciamo? Qui vedete due colori e cioè il verde (isocianato di fluorescina) ed il rosso<br />
(rodamina). Andiamo a cercare una sequenza del DNA sempre conservata, che non si altera<br />
neppure nel cancro ad esempio qualcosa che ha a che fare con il tratto prossimale dei telomeri<br />
o qualsiasi altra sequenza che non si altera nel cancro e che mi da un segnale verde.<br />
Io mi devo trovare in una cellula due segnali verdi e due segnali rossi in condizioni normali; se<br />
invece troverò due segnali verdi e 9 o 10 segnali rossi, allora diremo che l'amplificazione è<br />
notevole. Per motivi economici dobbiamo riservare questa tecnica ai casi dubbi.<br />
Cosa significa ibridazione in situ? Se vogliamo identificare un gene dobbiamo disporre di una<br />
sequenza di DNA complementare alla sequenza cercata e leghiamo questa sequenza sonda ad<br />
un tracciante fluorescinato.<br />
Prima di tutto dobbiamo denaturare il DNA della cellula in modo da ottenere due monoidi (si<br />
denatura col calore, con degli acidi ecc).<br />
Una volta ottenuti i monoidi, la sequenza sonda ha una forte affinità per il suo omologo e<br />
poiché c'è una sostanza fluorescinata che funge da sistema di rilevazione, noi troveremo quindi<br />
la sequenza in questo modo.<br />
E' definita ibridazione perchè avviene un ibrido tra la sequenza originale e la sequenza sonda.<br />
Da alcuni anni si è scoperto che l'HER-1 ha un ruolo nella cancerogenesi del colon-retto ed ha<br />
un significato prognostico notevole; c'è una minoranza di cancri del colon-retto che esprime<br />
questa amplificazione e che quindi si avvale di questa terapia biologica.<br />
Qual è il senso della terapia biologica? Bloccare in qualche modo questi recettori.<br />
I recettori li possiamo bloccare con:<br />
- inibitori delle tirosin-chinasi<br />
- anticorpi rivolti contro questi recettori, in modo da bloccare i recettori. Abbiamo avuto<br />
risultati nel colon-retto, invece lo stomaco è una new entry cioè è entrato nella realtà da un<br />
anno, altri tumori stanno in fase di studio<br />
Parliamo dei fattori di crescita.<br />
A livello sperimentale si tolsero i fattori di crescita dal mezzo di coltura perchè senza questi<br />
fattori il cancro si dovrebbe arrestare. Si scoprì che le cellule neoplastiche attraverso la<br />
selezione clonale si producono loro i fattori di crescita in maniera autocrina o paracrina, per<br />
esempio uno di questi fattori è il TGF perchè si riteneva che lo producessero solo le cellule<br />
tumorali. Si scoprì poi che il TGF può essere prodotto anche dalle cellule dello stroma<br />
connettivale che accompagna il cancro.<br />
Altri fattori di crescita sono quelli legati al microambiente cioè quelli che incidono sui fibroblasti<br />
e sul tessuto connettivale e qui abbiamo: l'IGF (insuline-like growth factor), l'EGF (epidermal<br />
growth factor) e tutta una serie di recettori e fattori di crescita in grado di determinare delle<br />
modificazioni dello stroma connettivale del cancro, tale da favorire lo sviluppo del cancro<br />
stesso.<br />
Per esempio il TGF ha due facce, a seconda delle condizioni in cui si trova, degli stimoli che ci<br />
sono nell'ambiente può agire con un'attività di soppressione o con un'attività pro-oncogenica,<br />
quindi favorendo l'angiogenesi e favorendo lo sviluppo e la proliferazione del tumore.<br />
I rimodellatori della cromatina appartengono a diverse classi. Cosa vuol dire rimodellatore è<br />
propriamente la disposizione del filamento rispetto al nucleosoma ed ha una funzione<br />
importantissima perchè può essere accessibile o non accessibile ai fattori di trascrizione.<br />
Queste proteine che si chiamano rimodellatori della cromatina, favoriscono l'accessibilità o<br />
meno di questa sequenza genica.<br />
I fattori di trascrizione già li conoscete (dita di zinco, elica giro elica)<br />
scaricato da www.sunhope.it
La morte cellulare programmata che coinvolge una serie di geni e cioè:<br />
- geni induttori<br />
- geni effettori<br />
- geni della fagocitosi<br />
- geni modulatori<br />
Tra i geni più importanti abbiamo la p53 che è un gene oncosoppressore e il gene myc.<br />
Tra i geni modulatori assumono importanza quelli appartenenti alla famiglia bax, bcl-2 ed altri<br />
geni appartenenti alla famiglia bcl.<br />
La fagocitosi segue alla morte cellulare come la flippasi ecc.<br />
La morte programmata ha due vie:<br />
- una via estrinseca, quando sono coinvolti i recettori sulla membrana<br />
- una via intrinseca quando sono coinvolti i mitocondri<br />
In questa cascata di eventi è importante il ruolo delle caspasi perchè determinano la morte<br />
cellulare.<br />
Come può crescere un cancro? Attraverso la proliferazione o attraverso l'immortalizzazione cioè<br />
l'inibizione della necrosi apoptotica.<br />
Nella norma proliferazione e necrosi si equivalgono per cui il numero delle cellule che entra è<br />
uguale al numero delle cellule che esce dal sistema; invece può succedere che la capacità<br />
proliferativa di un tessuto rimane inalterata ma che diminuisce la morte programmata e anche<br />
in questo caso avremo una crescita.<br />
La radioterapia, i chemioterapici sono attivi sulle cellule in attiva replicazione per cui se un<br />
tumore non ha un'alta frazione proliferante, i farmaci non agiscono bene<br />
Definiremo refrattari quei tumori che non hanno alta frazione proliferativa.<br />
ONCOSOPPRESSORI<br />
Il retinoblastoma è un tumore rarissimo della retina. Studiando in coltura queste cellule<br />
Knudson si rese conto che mancava qualcosa nel cromosoma 17.<br />
Anche qui abbiamo visto che la delezione è una delle possibilità perchè in questo caso il gene<br />
oncosoppressore agisce in maniera recessiva cioè se c'è una mutazione o una delezione di un<br />
allele non succede niente perchè l'altro allele continua a produrre queste proteine; però che<br />
succede, che spesso alla nascita ereditiamo queste situazioni di eterozigosi cioè che c'è un<br />
allele che non funziona e quindi possiamo essere predisposti a determinati cancri.<br />
E' importante sapere che i geni oncosoppressori agiscono in maniera recessiva<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA: seconda lezione 19/10/2010<br />
Allora, abbiamo lasciato molti punti insospesi. Parlavamo dei geni oncosoppressori. Questi ultimi<br />
costituiscono un capitolo fondamentale dell’oncologia, perché, quando voi non eravate ancora in<br />
programma e quando si andava ai congressi di oncologia, c’erano due tendenze che si scontravano: quelli<br />
che erano portatori di istanze di ……ambientale perchè, avendo fatto studi sugli animali, dicevano che<br />
l’ambiente, il fumo e tutto il resto avevano un ruolo fondamentale; poi c’erano i genetisti che portavano<br />
avanti il discorso sulla genomica che secondo loro era alla base del cancro. I geni oncosoppressori sono stati,<br />
per anni, la sintesi di queste due tendenze. Mo vi risveglio un po’ qualche concetto hegeliano: quello di tesi<br />
antitesi e sintesi. Perché questo concetto? Perché si può ereditare e sicuramente si verifica questo, una<br />
delezione o comunque una mutazione di un gene oncosoppressore. Questo non determina alcun effetto xkè<br />
c’è l’altro allele che funziona e l’azione protettiva del gene oncosoppressore, come bloccare la cellula<br />
durante il ciclo cellulare, indurre la differenziazione permane. Ma se su quell’altro allele intervengono<br />
fattori ambientali, quindi cancerogeni, allora c’è una doppia condizione di omozigosi( di entrambi gli alleli)e<br />
crolla questo sistema protettivo. Il primo gene oncosoppressore codificato è stato l’rb, da retino blastoma.<br />
C’è stato un napoletano che ha studiato la storia degli rb e che si chiama Giordano. Egli ha trovato che gli rb<br />
sono una famiglia di geni, ha scritto un articolo che si chiama “who is the boss?”: chi è il boss della famiglia<br />
delle rb?! Perché poi c’è rb1, rb2,rb3, p105 e così via! Alla fine si è giunti a dire che non c’è proprio un boss,<br />
ma c’è una cooperativa.<br />
Allora, può succedere che vi sia una delezione doppia, in tal caso non c’è proteina, e questa proteina nel<br />
caso di rb1, rb2, p105 manca; oppure ci può stare una mutazione doppia, in tal caso viene fuori una<br />
proteina difettosa, quindi biologicamente non attiva ed anche in tal caso crolla questo sistema difensivo.<br />
Oppure possiamo avere ad un allele una mutazione e all’altro allele una delezione, ed è quello che si verifica<br />
più spesso, oppure ci può stare un doppio riarrangiamento per cui, per effetto di questa nuova posizione<br />
che assumono le sequenze o proprio il gene rb o anche moltissimi altri geni oncosoppressori, non c’è piu la<br />
produzione di questa proteina. E’ chiaro?<br />
Questa scatola che ci ha aperto i geni oncosoppressori ci ha spiegato anche una ipotesi per il cancro emessa<br />
trenta anni fa da Knudson, la cosiddetta “ipotesi dei due colpi”. Vi ricordate che abbiamo parlato della<br />
precancerosi, quindi in un primo tempo c’è una delezione o comunque una mutazione che uno eredita;<br />
questo rappresenta un terreno predisponente. Poi dopo abbiamo tutta una serie di mutazioni che<br />
coinvolgono il secondo allele o un riarrangiamento dello stesso per cui viene a mancare questa azione<br />
protettiva. Vi faccio vedere ora un’immagine dell’international cancer insitute di bethesda che riguarda le<br />
automobili! Una volta avevamo un’idea relativamente semplificata del problema perché ormai le cose sono<br />
diventate complessissime. Allora se ci stanno entrambi gli alleli dei due geni oncosoppressori, questa<br />
macchina non va a sbattere contro il muro del cancro, se si verifica nella seconda ipotesi una mutazione di<br />
un oncogene, cioè l’attivazione di un oncogene, se ci sono i geni oncosoppressori neanche succede niente;<br />
se c’è una delezione o una mutazione di un allele oncosoppressore,unita ad una mutazione dell’oncogene<br />
che agisce in maniera dominante,neanche succede niente. Quando succede? Quando c’è una mutazione<br />
comunque dei due alleli dei due geni oncosoppressori e la mutazione di un oncogene, è piu facile che possa<br />
insorgere il cancro. Quindi ricordatevi che da una parte c’è un’attività di tipo recessivo, dall’altra c’è<br />
un’attività di tipo dominante.<br />
Vediamo, per esempio, un gene oncosoppressore notissimo che è p53! p53 in oncologia è, come si dice a<br />
napoli , un po’ il prezzemolo: ce lo ritroviamo in quasi tutti i cancri. Può andare incontro a tutta una serie di<br />
scaricato da www.sunhope.it
mutazioni, delezioni e ovviamente, perché si abbia l’azione oncogenica deve essere bilaterale. Cosa succede<br />
se questa p53 o non c’è o è mutata? Qualcuno che ha preso il caffè avrà notato che questo gene si chiama<br />
con la p davanti, perché? Per un fatto storico: perché venne identificata prima la proteina e poi il gene ed è<br />
l’unico caso in cui il gene viene chiamato con la p come se fosse una proteina.<br />
Allora, se c’è un danno del DNA (cosa che avviene quotidianamente!) e c’è la p53 che funziona, la p53 e la<br />
proteina da esso codificata arrestano la cellula in fase G1, cioè la cellula non va più avanti. Allora abbiamo<br />
due possibilità: che la cellula va in apoptosi, oppure c’è la riparazione del DNA prima che vada incontro a<br />
divisione. Ma se la p53 o non c’è proprio, o è mutata, questa cellula può andare verso il cancro, o può<br />
andare verso la necrosi apoptoica. Mutazioni della p53, sopratt quelle puntiformi che coinvolgono due alleli,<br />
li ritroviamo in tutta una serie di tumori. In alcuni casi, questa mutazione assume un significato prognostico,<br />
come ad es. nella sfera genitale femminile, sfera geitale maschile, tiroide, anche nell’apparato del colon<br />
retto, nella cute e così via; quindi è un gene oncosoppressore molto importante. Ecco, se ritorniamo sempre<br />
a questi aspetti cinematografici, questa storia se vogliamo, è una serie di mutazioni e delezioni di pezzi; il<br />
cancro del colon retto, è proprio come una specie di perdita di pezzi per la strada. Anzi noi possiamo vedere<br />
in questa storia, un po la storia della riparazione delle strade di napoli, per cui prima si forma un buco, poi si<br />
forma una falla, poi c’è un’anima buona tipo un commerciante della zona che non ce la fa più a vedere<br />
automobili distrutte e ci mette sopra qualcosa in attesa(un’attesa molto vana!!) che venga questa impresa<br />
che deve riparare le strade e che è la romeo immobiliare. Bene: c’è un’impresa di vigilanza anche a livello<br />
genico. Questi geni guardiani o stabilizzatori, costituiscono la squadra di riparazione dei danni del DNA,<br />
fortunatamente non appartiene alla romeo immobiliare se no saremmo tutti defunti perché funziona bene,<br />
e poi abbiamo una new entry: sono stati identificati non molto tempo fa dei geni, dei micro RNA cioè delle<br />
piccole sequenze di RNA che esercitano una funzione di controllo e di regolazione.<br />
Io non mi soffermerò su queste cose. Voi sapete già che un danno al DNA può avere cause esogene e cause<br />
endogene. Molto importante è il cosiddetto “mismatch” cioè l’errore di appaiamento delle basi perché ci<br />
stanno poi tutti dei sistemi di riparazione, e come avviene questa riparazione? A livello nucleare e a livello<br />
mitocondriale sono coinvolti tutta una serie di enzimi. Ovviamente questi danni sono più evidenti in età<br />
avanzata. Per es. se noi vediamo un pap test di una donna anziana e uno non sa le alterazioni che<br />
presentano le cellule in una donna anziana,(infatti in una donna anziana non si dovrebbe fare il pap test) ma<br />
parecchi consultori di napoli questo non lo sanno e ci arrivano pap test di donne di ottanta anni, che hanno<br />
cioè venti anni in più di quella che è l’età in cui si fa il pap test), ebbene possono uscire delle cellule<br />
atipiche ma così atipiche che se uno non lo sa piglia fischi per fiaschi. Se non c’è una riparazione si va verso<br />
la senescenza o verso il cancro. E’ inutile che vi dico tutti gli enzimi che sono coinvolti in questa riparazione,<br />
dalle endonucleasi, le polimerasi, le ligasi e così via…C’è un meccanismo che ha una sincronizzazione quasi<br />
di tipo svizzero per arrivare a riparare quel danno. Molto importante è la velocità di riparazione, per es.noi<br />
abbiamo in natura(non so se ve lo hanno detto) un batterio chiamato “conan il batterio”volgarmente<br />
(deinococcus), che ha una enorme velocità e i cui enzimi sono di una efficienza spaventosa. Un altro<br />
fenomeno che noi vediamo nel cancro è quando non funzionano questi sistemi di riparazione: la polimerasi<br />
gira a vuoto, va avanti e indietro come un pennello, si formano dei microsatelliti che sono delle sequenze<br />
ripetute per cui quella parte di cromosoma si gonfia e questo fenomeno prende il nome di “instabilità dei<br />
microsatelliti”. Possiamo trovarlo in molti tipi di cancro ed è espressione di una alterazione di quei geni, di<br />
quelle proteine e di quegli enzimi coinvolti nella riparazione(geni MLH1,MLH2 ed altri geni coinvolti nella<br />
riparazione). Per quanto riguarda i microRNA vi do solo due notizie: noi sappiamo che questo microRNA può<br />
rivelare, a seconda delle circostanze, attività oncogenica o oncosoppressiva; sono dei filamenti brevi che<br />
hanno una attività di regolazione. Noi sappiamo che per la formazione di questi filamenti di microRNA sono<br />
fondamentali due sistemi enzimatici chiamati sistema DROSHA e DICER e quando questi sistemi enzimatici<br />
scaricato da www.sunhope.it
sono molto elevati, cioè molto attivi e in quantità abnormi, questo è un brutto segno per la prognosi del<br />
cancro.<br />
Ed ora andiamo ad analizzare tutta una serie di fenomeni: il fuso cellulare, la mitosi (che voi sapete!) ecc. Vi<br />
ricordo solo che vi sono delle protein chinasi molto importanti chiamate AURORA, soprattutto auroraA e<br />
auroraB che sono coinvolte nell’assemblaggio e nell’orientamento del fuso, quindi la simmetria della<br />
moitosi dipende molto da queste protein chinasi. Esse sono coinvolte nel sistema chiamato SACK(?) che<br />
presiede alla fomazione e alla strutturazione del fuso cellulare. Perché ne parliamo? Perché quando questi<br />
enzimi, queste protein chinasi non funzionano bene, andiamo verso la aneuploidia, cioè andiamo verso un<br />
contenuto di DNA anomalo e una certa instabilità dei cromosomi che ovviamente, quando c’è una<br />
generazione, cioè si formano le cellule figlie, poiché si avranno delle mitosi asimmetriche ci saranno delle<br />
deviazioni rispetto al normale. Noi sappiamo che mutazioni dell’auroraA e dell’auroraB le ritroviamo in<br />
molti tipi di cancro. Tutto questo che io vi sto dicendo in linea teorica, poi vi spiegherò ha già un approccio<br />
di tipo terapeutico.<br />
Allora, riepilogando: che può succedere a questi cromosomi sfortunati in una cellula di un soggetto che va<br />
verso il cancro (d’altronde questi fenomeni li possiamo ritrovare anche nella displasia). Allora possiamo<br />
avere un’alterazione bilanciata dei cromosomi (quindi senza alterazioni macroscopicamente evidenti) con<br />
formazione di geni di fusione chimerici cioè di geni che normalmente non ci sono perché nascono dalla<br />
fusione di varie fasi del cromosoma. Possiamo avere poi un’espressione sregolata dei geni normali per cui<br />
c’è un aumento delle proteine. Nel primo caso avremo delle proteine anomale oppure possiamo vedere<br />
un’alterazione proprio del numero dei cromosomi( trisomie, monosomie). Possiamo avere ancora delle<br />
delezioni, quindi submicroscopiche o un’amplificazione intracromosomica e quindi un gene amplificato; o<br />
addirittura possiamo avere un’amplificazione extracromosomica quando vediamo dei minuti frammenti di<br />
DNA che si trovano aldifuori del cromosoma e che rappresentano delle sequenze amplificate di un genoma.<br />
Ecco un’altra immagine in questo delirio da power point! C’è una cosa che veramente ci stupisce ed è<br />
rappresentata da questo schema:le cellule normali sono incastrate l’un l’altra da una chiusura lampo che è<br />
difficile da rompere, così come sono tutte tenacemente aderenti alla membrana basale. Perché queste<br />
cellule si staccano? Perché abbiamo visto nella preistoria che una delle caratteristiche della displasia<br />
avanzata è che una di queste cellule comincia a staccarsi,poi invade la membrana basale. Perché queste<br />
cellule se ne vanno? Chi ha dato loro il permesso di andare a fare una gita?<br />
E quali sono queste chiusure lampo? La prima chiusura lampo che c’è tra due cellule epiteliali è questa che<br />
voi vedete al centro e che si chiama E-CADERINA. Questa è una molecola di adesione importantissima<br />
perché è la chiusura lampo che tiene strette le due cellule. Dopo la caderina troviamo lo strato delle<br />
cosiddette BETA-CATENINE che è attaccato alla caderina. Le catenine prendono rapporto poi con tutti questi<br />
filamenti qui segnati in verde e che rappresentano una componente importante del citoscheletro: le<br />
ACTINE. C’è quindi un sistema triplice: caderine, catenine ed actine. Se andiamo a vedere sulla membrana<br />
basale, ci sono le INTEGRINE che rappresentano come dei ganci per cui la cellula si aggancia alla membrana<br />
basale. Queste integrine sono una forma molto complessa: la forma normale è questa qui alfa3-beta1 che<br />
troviamo nelle cellule normali. Ma ora che, per una serie di alterazioni geniche che possono riguardare il<br />
gene cph1 che è quello che codifica e che produce la E-caderina o di alcuni fattori di trascrizione, si può<br />
bloccare o si può alterare questa produzione di elementi che conducono alla formazione di queste chiusure<br />
lampo così come può capitare che intervengono fattori post-traslazionali, cioè quelli che vengono dopo la<br />
formazione delle proteine, uno dei più importanti è sicuramente la fosforilazione. Che succede? Che, per<br />
una serie di meccanismi complessi, la caderina viene fosforilata e addirittura, da che si trovava tra le cellule,<br />
viene ad essere inglobata nel citoplasma. Ma la conseguenza più grave per le cellule è la presenza di<br />
scaricato da www.sunhope.it
catenine che, non solo sono inglobate nel citoplasma, ma vanno a finire nel nucleo dove esercitano<br />
un’azione pro-oncogenica. Addirittura vediamo un fenomeno strano: che al posto della E-caderina troviamo<br />
l’ N-CAM, altra molecola di adesione espressa soprattutto dalle cellule mesenchimali e dalle cellule nervose;<br />
quindi assistiamo ad un fenomeno davvero strano, molto importante nella regolazione dei rapporti intercellulari<br />
e/o fra le cellule e lo stroma e quindi la membrana basale e questo sistema FAK (focal adesion<br />
kinase) che controlla un po’ tutto. Ora che succede? Facciamo un riepilogo: per azione di fattori tra cui le<br />
COX,IL TNF, il TGFbeta, la beta-catenina se ne va nel nucleo e lì esercita azione pro-oncogenica perché<br />
determina un aumento dell’attività proliferativa e soprattutto un’attività angiogenetica. Ecco questa è una<br />
cosa strabiliante, noi anatomo patologi abbiamo dei punti fermi, ma molti di questi punti fermi oggi sono<br />
diventati deboli! Avevamo l’idea che una cellula epiteliale fosse epiteliale ed una mesenchimale fosse<br />
mesenchimale, questo concetto è saltato. Questa cellula che esprimeva un fenotipo epiteliale, non solo da<br />
un punto di vista morfologico, ma anche da un punto di vista molecolare, (esprimeva le citocheratine, l’Ecaderina<br />
che è tipica delle cellule epiteliali come molecola di adesione e che esprimeva le integrine alfa3beta1)si<br />
trasforma in un'altra razza di cellule che esprime la VIMENTINA (che è un marcatore delle cellule<br />
mesenchimali), l’N-CAM,la beta catenina intracitoplasmatica e le integrine anomale. Ma ha un senso<br />
questo cambiamento? Sì, è un’altra furbizia, una furbizia che fino ad un anno fa nessuno avrebbe mai<br />
sospettato perché la cellula mesenchimale è molto più intraprendente della cellula epiteliale che non è<br />
abituata a muoversi nello stroma ed è più esigente dal punto di vista metabolico. Questo cambiamento è un<br />
cambiamento vantaggioso per il clone che assume queste capacità , tanto che, in condizioni anche di un<br />
cancro ben differenziato, noi possiamo vedere la caderina come un’immagine ad occhiello perché la<br />
caderina si trova alla periferia della membrana citoplasmatica. Vedete che succede invece in un cancro<br />
meno differenziato: questa caderina va nel citoplasma; ancora più evidente è la beta-catenina che si trova in<br />
periferia (qua invece vedete marca pure il nucleo, il marroncino è il colore della reazione enzimatica, la<br />
ritroviamo nel nucleo delle cellule e la riroviamo nel citoplasma). Vedete quindi come stà avvenendo questo<br />
fenomeno detto di “trans differenziazione”. Poi, come si muove questa cellula? Vi dico solo che i movimenti<br />
sono ameboidi e sono complessi, si formano dei lamellopodi e in senso laterale degli invado podi che hanno<br />
una particolare struttura di filamenti. Mi ricordo per esempio il CD44 che poi vedremo più avanti. Le cellule<br />
quindi riescono a distaccarsi. Il distacco delle cellule prende un nome: dal greco “anoibis” che vuol dire<br />
“senza patria”, cioè la cellula perde la sua patria. V sono dei geni che proteggono da questo distacco di cui<br />
non vi stò a parlare.<br />
Ecco, vedete quanti passaggi si devono avere affinchè vi sia il cancro. (ah, in America l’anatomia patologica<br />
si chiama “surgical pathology”ossia “patologia chirurgica”).<br />
Proseguiamo adesso con i TELOMERI. Sapete tutti cosa sono i telomeri:sono dei cappucci di protezione che<br />
si trovano al termine dei bracci dei cromosomi e che hanno una funzione importantissima. La loro funzione<br />
è molteplice: impediscono che si formino dei legami inter o intra cromosomici, permettono la replicazione<br />
completa del materiale nucleare e della cellula impedendo tutta una serie di incidenti che potrebbero<br />
avvenire; contribuiscono anche a stabilizzare il materiale cromosomico perché sono legati alla membana<br />
nucleare. Ora, il problema di questi telomeri qual è? È che sono una specie di orologio biologico del corpo<br />
umano, e penso a quel passo della Bibbia che dice che l’età media dell’uomo è 70, 80 anni, 90 per i più<br />
robusti!! Quindi c’è quest orologio biologico, tanto è vero che le cellule somatiche, ad ogni generazione,<br />
perdono dei pezzi di telomero, quando il telomero diventa corto la cellula non replica più e questo succede<br />
nell’anziano. Per esempio, se calcoliamo le cellule di un neonato in coltura, si possono dividere circa cento<br />
volte, le cellule di un cinquantenne in coltura si possono dividere solo dodici volte. Quindi sono una specie<br />
di orolgio. Ma perché ne parliamo? Perché questo fenomeno è alterato nelle cellule neoplastiche e<br />
displastiche. È alterato non solo il telomero, ma anche le telomerasi che sono delle trascrittasi inverse<br />
scaricato da www.sunhope.it
deputate alla sintesi dei pezzi di DNA mancanti del telomero. Queste telomerasi agiscono in maniera molto<br />
complessa(ma non ve ne parlo). Si è visto che le cellule della linea germinale (cioè gli spermatozoi nell’uomo<br />
e gli ovociti nella donna)sono ricchissimi di telomerasi, così come le cellule staminali, le cellule embrionali e<br />
le cellule maligne nel 99% dei casi, questo ci spiega questa grande capacità re plicativa che hanno queste<br />
cellule. Nella cellula somatica adulta, invece, la telomerasi è poco espressa. Vedete c’è una differenza<br />
profonda che ci dà lo spunto per una nuova strategia terapeutica del cancro.<br />
Adesso ci fermiamo per fare un discorso un po’ più ad ampio raggio. Abbiamo analizzato tutti questi<br />
fenomeni, adesso ci rendiamo conto che tutti questi fenomeni sono pezzi di un mosaico più complesso.<br />
Questi sono i due numeri delle riviste di “science”del 2000 e del 2001 in cui, con una certa concorrenza,<br />
veniva riportata la conclusione del cosiddetto “progetto Manattan”cioè la caratterizzazione del DNA umano.<br />
Quando avvenne questo si gridò finalmente ad un’epoca nuova della medicina; bhè, questo non è niente di<br />
nuovo. Voi non lo sapete, ma già verso la fine dell’800 il medico si credeva onnipotente, e se non riusciva a<br />
concludere niente, si diceva che era solo questione di tempo. La scienza può spiegare il “come”, ma mai il<br />
“perché”. Ecco la teoria dell’ultimo vagone, cioè non si riesce mai ad arrivare alla motrice, perché il big ben<br />
sì, ma chi ha premuto il grilletto? il brodo primordiale sì, ma chi è che è stato il dado? Ecco imparate che<br />
nella ricerca si oscilla tra l’ottimismo e la depressione, si fa un po’ sta ginnastica (che poi è la ginnastica che<br />
si fa anche nella vita!). Comunque, per mostrarvi delle realtà molto complesse c’è chi adopera un’orchestra,<br />
uno spartito musicale, ma non si presta bene. Diciamo che il DNA in un sistema ferroviario corrisponde ai<br />
binari, allora noi avevamo conosciuto tutta la rete ferroviaria, ma dovevamo conoscere il percorso dei treni,<br />
quindi sapere dove vanno. Poi abbiamo saputo che ci sono anche gli scambi, che un binario può essere<br />
morto e un binario può essere molto attivo; nasce così l’epigenetica. L’epigenetica sono tutte quelle<br />
alterazioni funzionali che possono determinare l’espressività o il silenzio( cioè il gene ci stà però non è<br />
espresso; non è espresso significa che è presente però non funziona). Si arriva poi ad una cosa che fa<br />
mettere le mani nei capelli, la cosiddetta “post-genomica”che si è aperta un po’ più di un anno fa perchè si è<br />
visto che, in fin dei conti, per avere un’idea del traffico ferroviario, sì ci stanno i binari, ma ci stanno anche i<br />
rapporti fra i vari treni, le coincidenze da rispettare, la cooperazione tra i vari capistazione, tutta una serie di<br />
problemi che sono di una complessità enorme, tanto è vero che c’è ancora chi è convinto che si può fare<br />
una diagnosi basandoci su un gene: è una stupidaggine perché se voi avete già studiato queste cose, sapete<br />
che, nel cancro, non c’è nessuna caratteristica molecolare-genetica che ci possa far fare diagnosi, tranne che<br />
non si parli di malattie genetiche, ma anche lì ci sarebbe da discutere. Non so se vi sono chiari questi tre<br />
compartimenti. È nato anche il problema di definire che cos’è quest’era post genomica, si parla anche di<br />
“proteomica”, perché? Se andiamo a fare un confronto, il numero delle proteine è almeno tre volte in più<br />
del numero dei geni, anche perché il dogma “un gene,una proteina” è saltato! Esiste anche una<br />
“trascrittomica” che è quella che studia i fattori di trascrizione perché, in effetti il gene ci può stare, può<br />
essere mutato quanto volete voi, i geni oncosoppressori sono sottratti, non c’è capacità di trascrivere. Poi<br />
c’è l’interazione tra i geni: i cosiddetti “microarray”. Ovviamente se io dovessi fare una diagnosi con un<br />
microarray nella regione campania, dopo una decina di diagnosi io mi mangerei già tutto il bilancio della<br />
regione campania!!<br />
A questo punto si parla di un “effetto Rashomon”,eeh, quando voi ancora dovevate nascere, i vostri genitori<br />
non si erano ancora sposati, uscì questo film giapponese che fece epoca. Quindi che cosa fa il microarray? Il<br />
microarray fotografa tutti geni che sono attivi in quel momento(perché non è importante il singolo gene, ma<br />
l’insieme di quelli che sono attivi in quel momento), in modo da avere un’idea complessa della situazione.<br />
Voi capite come fare ricerca oggi, è qualcosa di terribile perché implica non solo la biologia, la chimica ma<br />
anche l’ingegneria, il computer, perché per fare queste palline(del microarray)di tutti i colori ci vuole<br />
scaricato da www.sunhope.it
un’elaborazione. Questo Rashomon è un film giapponese che poi molti hanno copiato in cui c’è una…<br />
storia(?) di una grande violenza, in cui ci sono poi una serie di testimoni ognuno dei quali dice una realtà<br />
diversa e quindi c’è la soggettività di ognuno. Ecco nella scienza questo effetto è molto discusso e si chiama<br />
“effetto Rashomon”. D’altra parte c’è la cosiddetta “concordia discordante”, cioè quando chiamate più<br />
testimoni ad un fatto, esiste un’area di concordanza e poi un’area di discordanza; questa è una prova della<br />
verità. Se invece esiste che tutti hanno esattamente la stessa versione, cioè la concordans completa, è un<br />
brutto segno:vuol dire che si sono messi d’accordo; tanto è vero che se voi tra un esame e l’altro, tra una<br />
lezione e un’altra date uno sguardo ai vangeli, vedete che i quattro vangeli hanno delle differenze. Queste<br />
differenze che potrebbero sembrare un segno di discordanza invece sono segno di concordanza, vuol dire<br />
che c’è una componente di verità. Allora cosa succede? Che per avere una visione unitaria si deve trovare un<br />
punto centrale in cui convogliano quei tre insiemi che sono la visione di un fenomeno da parte di una<br />
persona, cioè bisogna trovare un’area centrale, cosa complicatissima. Per esempio nella nostra università<br />
sono oltre trenta anni che questa visione centrale non l’abbiamo trovata!!<br />
Per esempio, quando parliamo di epigenetica, un fenomeno importantissimo dell’epigenetica è la situazione<br />
degli istoni e dei nucleo somi: ci sono tutta una serie di fenomeni che vanno dalla metilazione alla<br />
acetilazione. In effetti, quando è possibile la trascrizione, cioè quando è che quel gene funziona perché può<br />
intervenire la trascrizione e quindi ad esso la proteina? Si può intervenire quando non c’è metilazione,<br />
vedete queste palline bianche che implicano assenza di metilazione, mentre questi segni sopra vuol dire<br />
quando gli istoni sono acetilati, quindi la massima espressività e la capacità trascrittiva di un gene si<br />
raggiunge in assenza di metilazione e in presenza di acetilazione. Nel cancro si realizzano spessissimo questi<br />
eccessi di metilazione con conseguente soppressione dei geni oncosoppressori, i quali però possono essere<br />
anche normali. Questo implica tutta una serie di attività, le metiltrasferasi, l’acetiltrasferasi, le deacetilasi,<br />
insomma tutta una cascata complessa. Per esempio i geni oncosoppressori si possono inattivare per la<br />
metilazione tanto è vero che c’è il termine “silenzio epigenetico”che vuol dire che quel gene si trova in una<br />
situazione di inattività.<br />
Ma a questo punto, veniamo all’altro problema che abbiamo lasciato insospeso: e le barriere naturali? E il<br />
sistema immunitario? Come è possibile che questo cancro che già ha i guai suoi, le displasie, la battaglia con<br />
l’epigenetica, come è possibile che superi anche queste barriere naturali? Noi abbiamo tutta una serie di<br />
meccanismi, non solo statici come la membrana basale, ma anche dinamici come i linfociti, i macrofagi e<br />
così via. Negli ultimi anni si sono susseguiti tutta una serie di scoperte e ormai sappiamo che il sistema<br />
immunitario si comporta così: come dr Jeckie e mr hyde, a seconda dei casi!! E questa è una cosa<br />
importantissima che ha delle ripercussioni notevoli nella nostra diagnostica. Per esempio qui il tumore può<br />
crescere o può regredire a seconda del tipo di macrofagi e linfociti che ci sono. Più avanti c’è un’altra<br />
immagine tratta da un lavoro molto recente: il macrofagoM1 è quello che produce l’IL-12 ed ha un’attività<br />
antitumorale, antiangiogenica; il macrofagoM2 è quello che produce invece VEGF, che è un fattore di<br />
crescita dei vasi, che produce particolari tipi di prostaglandine, particolari fattori angiogenetici, il TNF ecc…e<br />
così potremmo proseguire con i neutrofili, le cellule dendritiche che sono cellule immunocompetenti che<br />
presentano l’antigene ai linfociti T , per arrivare poi ad altri tipi di cellule. Poi vedremo come fa la cellula<br />
tumorale a bypassare il sistema immunitario, come fa questa cellula molto furba, molto “partenopea” a<br />
raggirare il sistema immunitario e a porlo addirittura al suo servizio.<br />
Di un ultima cosa non abbiamo parlato: del recettore accoppiato a proteine G, di cui in patologia generale vi<br />
avranno fatto dei trattati. Voi sapete che la proteina G ha tre componenti:alfa, beta e gamma. Perché ne<br />
parliamo adesso? Perché è una famiglia di recettori enorme, più di mille recettori diversi che rispondono ad<br />
una serie di stimoli extracellulari. Ora sappiamo che attraverso modificazioni e stimolazioni di particolari tipi<br />
scaricato da www.sunhope.it
di recettori appartenenti a questa categoria, come sappiamo per particolari alterazioni del gene<br />
WHE(??)possiamo avere dei fenomeni come la comparsa di attività enzimatica, tipo attivatore del<br />
plasminogeno che è un enzima proteolitico molto forte, le metalloproteasi che sono anch’esse molto forti,<br />
soprattutto attive per il connettivo, possiamo anche avere un aumento della mobilità e del potenziale di<br />
metabolizzazione delle cellule; ma soprattutto abbiamo che detti recettori legati a proteine G sono molto<br />
più sensibili a molti tipi di peptidi, tra questi, le chemochine che sono quelle capaci di esercitare una<br />
chemiotassi, una chiamata alla mobilità,di regolare l’omeostasi, l’embriogenesi; tanto è vero che quando<br />
mancano queste chemochine e i corrispondenti recettori, possiamo avere delle malformazioni ed io adesso<br />
vi parlo solo di due: 1) il recettore cosiddetto CXCR4 che ha avuto un grande sviluppo conoscitivo, e che si<br />
lega a CXCL12 .Questo è importante nell’organogenesi. Il problema è che c’è un’iperespressione del CXCR4<br />
in molti tipi di tumori che non dovrebbe esserci; così come c’è una secrezione autocrina o paracrina di<br />
questo fattore CXCR12, come sappiamo che l’espressione poi di quest altro recettore CCR7 e del ligando<br />
CCR21, è espresso nei tumori che hanno una alta potenzialità di metastatizzare nei linfonodi. Quindi<br />
l’espressione di questi recettori, di CCR21 e CCR7, la ritroviamo nelle metastasi e nei tumori che hanno un<br />
alto potenziale di metastatizzazione linfoghiandolare. Vedremo come per esempio nella tiroide c’è il<br />
carcinoma papillifero che ha un’alta capacità di metastatizzare nei linfonodi, mentre il carcinoma follicolare<br />
tende a metastatizzare per via ematica. Ancora, vedete ancora la furbizia partenopea: quando il tumore, le<br />
cellule si trovano in una tensione di ossigeno diminuita (per il problema che abbiamo detto prima, cioè sono<br />
aumentate le cellule, c’è un’attività re plicativa molto forte, i fattori energetici sono sempre quelli), che<br />
succede? Produce CXCL12 e aumentano i recettori CXCR4. Tutto questo può essere aiutato anche dai<br />
fibroblasti e dai macrofagi che si trovano insieme alle cellule tumorali. Vedete il microambiente come<br />
coopera. Questo cosa determina? La presenza di questi recettori e la presenza di questi ligandi, determina<br />
anche una mobilità delle cellule, e siccome le sedi dove è più presente questo fattore è anche il sangue, c’è<br />
anche una chemiotassi verso i vasi; va bene?<br />
Per finire, vedete cosa succede: ancora una volta, anche la transizione epiteliale-mesenchimale si lega<br />
all’espressione di questo CXCR4 che in genere viene espresso soprattutto dalle cellule mesenchimali. Il fatto<br />
che le esprimano le cellule tumorali è un’altra furbizia, perché viene potenziata la capacità di mobilitazione<br />
e viene potenziata la loro capacità di andare nel sangue. Terminiamo con i vasi: la neoangiogenesi. I vasi del<br />
tumore(questa è una domanda classica) fanno parte dello stroma, quindi dell’ospite, o fanno parte del<br />
tumore? D’altra parte bloccare i vasi del tumore è un altro approccio terapeutico, di grande attualità.<br />
Comunque ne parleremo la prossima volta!!<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> - Metastasi<br />
Prof. Rossiello<br />
Lezione n°3<br />
23/10/2010<br />
Neoangiogenesi:<br />
Nello sviluppo della neoplasia i vasi hanno un ruolo fondamentale, perché rappresentano il<br />
supporto nutritizio di questa nuova massa che si sta formando.<br />
La neaoangiogenesi è mediata da citochine che non vengono prodotte dalle cellule tumorali,<br />
ma paradossalmente vengono prodotte anche da cellule non tumorali come macrofagi,<br />
linfociti e altre cellule. Si realizza così una “cooperazione al male”.<br />
Questi vasi neoformati sono uguali ai vasi normali? No! Questi vasi non fanno parte del<br />
tumore perché non sono formati da cellule atipiche, ma sono vasi con particolari proprietà<br />
come la permeabilità vascolare, maggiore capacità di perfusione (sono vasi “potenziati”) e<br />
posseggono tante caratteristiche che favoriscono la progressione tumorale. Hanno una<br />
capacità di dare supporto nutritizio maggiore dei vasi normali.<br />
Questi vasi possono essere un bersaglio terapeutico tant'è vero che uno dei protocolli in<br />
sperimentazione clinica, prevede una terapia con fattori anti-angiogenetici e sembra che, in<br />
alcuni casi, ci siano interessanti risultati.<br />
Metastasi:<br />
Questo è il problema dei problemi del cancro. Un cancro che non ha capacità di dare<br />
metastasi è un cancro poco preoccupante; è sempre da considerarsi cancro per caratteristiche<br />
morfologiche, biologiche, di invasività e anatomopatologiche, ma dal punto di vista clinicobiologico<br />
è come se non lo fosse perché, se non ha capacità di metastatizzare, il problema è<br />
facilmente risolvibile da un intervento locale.<br />
Perché avviene la metastatizzazione non ci è del tutto chiaro.<br />
Ci sono fattori importanti che concorrono alla capacità di metastatizzare:<br />
• Fattori Stocastici:<br />
dove stocastico si attribuisce ad un processo che procede attraverso<br />
tentativi e attraverso successi e insuccessi, è un divenire a cascata con blocchi e<br />
riprese. Questi sono riconducibili alle mutazioni, legate ad un divenire clonale e a<br />
mutazioni trasformanti, che fanno divenire un cancro da invasivo a metastatizzante, e<br />
da tante mutazioni silenti che col tempo si accumulano. Quelli di cancerogenesi sono<br />
processi che possono sembrare molto caotici, contrapposti all'ordine di un tessuto<br />
sano, ma è lo stesso caos un ordine che forse non riusciamo a comprendere, e questa<br />
è la definizione di stocastico.<br />
• Fattori Ambientali:<br />
dove l'ambiente inteso come stroma circostante alle cellule<br />
tumorali e citochine infiammatorie stimolanti la crescita della neoplasia<br />
• Back-ground Tissutale:<br />
che dipende da dove vanno a svilupparsi queste celllule<br />
• Back-ground Genetico:<br />
dove la metastatizzazione è faorita dalla predisposizione<br />
genetica del soggetto, che possono riguardare parti più o meno vaste del genoma.<br />
• Capacità di cooperatività con altre cellule<br />
L'insieme di tutti questi fattori definisce la predisposizione del soggetto a sviluppare<br />
metastasi, ed è una importante caratteristica in quanto la capacità del cancro di sviluppare<br />
metastasi è strettamente legata alla mortalità del soggetto.<br />
scaricato da www.sunhope.it
Ipotesi della genesi delle metastasi:<br />
Ipotesi del seme e del terreno: fu la prima ipotesi, e voleva spiegare la relazione tra il<br />
processo di embolizzazione, e la metastasi. Infatti perché se tutti i tumori embolizzano, solo<br />
alcuni metastatizzano? perché se l'embolo neoplastico è il seme, questo darà un risultato<br />
solo se cade nel terreno-tessuto adatto. Questo è giusto perché un embolo in un tessuto non<br />
ricettivo non sarà mai in grado di poter sviluppare una metastasi.<br />
Ipotesi della cooperazione tra fattori predisponenti: furono fatte altre ipotesi, più attuali, e<br />
si cominciò a pensare che la suscettibilità a sviluppare metastasi come dovuto ai fattori detti<br />
su.<br />
Ipotesi della trans-differenziazione epiteliale-mesenchimale: è l'ipotesi più recente che<br />
definisce una transizione in entrata ed una in uscita;<br />
• transizione in entrata: ovvero quando il cancro ha il processo di intravasation e di<br />
embolizzazione c'è la transizione della differenziazione cellulare epitelio--<br />
>connettivo<br />
• transizione in uscita: quando la cellula poi esce dal vaso c'è la transizione inversa<br />
dove da connettivale torna ad essere epiteliale!<br />
La cellula si adatta di nuovo ad un nuovo ambiente, manifestando una grande capacità<br />
adattativa. Il muro della membrana basale diventa un muro molto relativo, facilmente<br />
attraversabile.<br />
Homing cellulare:<br />
Un'altra furbizia alla base di un altro approccio terapeutico è che queste cellule riescono a<br />
esprimere recettori tipici di macrofagi e altre cellule, e di queste il più importante è il CD44,<br />
che dovrebbe essere espresso solo nelle cellula in grado di migrare attraverso i tessuti.<br />
Questa proteina lega l'acido ialuronico, proteine della matrice connettivale, collagene e<br />
molecole presenti in molti tessuti. La cellula così si lega a tanti tipi di tessuto grazie alla<br />
espressione di molti recettori che sono in grado di riconoscere molecole presenti in tessuti<br />
anche diversi da quelli di origine.<br />
Questo diventa un potenziale approccio terapeutico ancora sperimentale.<br />
Nicchia di metastatizzazione:<br />
in questa situazione di metastasi molte cellule finiscono per cooperare allo sviluppo delle<br />
metastasi, come macrofagi, linfociti, cellule tumorali.<br />
Addirittura la cell tumorale nel sangue è capace di produrre una serie di chemochine<br />
(integrine, fattori chemiotattici, angiogenetici) tali da creare una nicchia in un tessuto ancora<br />
prima di averlo invaso, quindi programma il suo arrivo in quel tessuto, preparando, a<br />
distanza, una nicchia nella quale potere impiantarsi. Avviene in una fase di<br />
premetastatizzazione.<br />
Paradossalmente questi fattori che favoriscono le metastati cerebrale, ematica, polmonare,<br />
ossea, linfonodale necessitano di cooperazione tra chemochine, fattori di crescita, affinchè<br />
quel terreno possa accogliere quella metastasi.<br />
scaricato da www.sunhope.it
Dedifferenziazione:<br />
un'altra cosa che sconvolge il professore è che le cellule squamose sono le più differenziate,<br />
allora com'è possibile che esistano dei cancri che sono detti “squamosi”; cioè una cellula<br />
differenziata come quella squamosa come fa a formare un cancro? Oppure ci sono tumori<br />
come plasmocitomi, mielomi, melanoma, che sono composti da elementi terminali di una<br />
linea differenziativa, altamente differenziati!<br />
Come può un melanocita, altamente specializzato, impazzire e iniziare a fare un tumore?<br />
Esiste la trans-differenziazione, ma questa interviene in una fase avanzata, mentre qui<br />
stiamo parlando di come nasce un tumore.<br />
Si riteneva allora che ci sono cellule specializzate e il tumore deriva proprio da queste<br />
cellule specializzate: One Cell –> One tumor.<br />
Ci sfuggiva però che probabilmente tutto nasce dalle cellule staminali, con il fenomento<br />
della dedifferenziazione, dove le staminali rappresentano delle cellule di riserva presenti in<br />
tutti gli organi e sono situate in posizioni strategiche.<br />
Queste cellule, anche se pluripotenti perché cellule staminali stanziali, sono in grado di<br />
riprodurre tutte le cellule di quel tessuto.<br />
(Metaplasia) Sono quelle cellule staminali per esempio che si posizionano strategicamente<br />
nella giunzione tra epitelio endocervicale, formato dal canale endocervicale, e epitelio<br />
esocervicale, composto da epitelio squamoso.<br />
Le cellule staminali sono posizionate in quella giunzione per poter riparare la parte di<br />
epitelio che può danneggiarsi, sia dell'epitelia endocervicale, e sia dell'epitelio esocervivale.<br />
Sono cellule molto sensibili agli stimoli ambientali, e se durante il parto, una parte del<br />
canale cervicale forma un ectropion, parte delle cell endocervicale fuoriescono verso la<br />
vagina. In questa situazione la cell staminale, stimolata da fattori diversi, differenzia verso<br />
una specie cellulare diversa, ovvero di epitelio squamoso, dando una metaplasia.<br />
Questo accade nei bronchi, nello stomaco,....<br />
Le cellule staminali possono essere totipotenti (ovocita), pluripotenti (blastula, morula),<br />
multipotenti (midollo osseo). Le cellule staminali del midollo osseo hanno un potenziale<br />
evolutivo maggiore di quelle periferiche presenti in tutti i tessuti, e per questo si parla di<br />
auto-trapianto di midollo.<br />
Quelle periferiche sono già parzialmente commissionate verso il loro tessuto.<br />
Nella mammella per esempio sono presenti cellule epiteliali e cellule mioepiteliali provviste<br />
di filamenti di actine e proprietà tipiche di cell muscolari. La staminale ha quindi una doppia<br />
potenzialità.<br />
Se la cell staminale non è regolata comincia ad avere delle alterazioni, come un perdita di<br />
adesività, pur mantenendo la cheratina.<br />
Oppure può andare incontro a trans-differenziazione, oppure può diventare una cellula<br />
mesenchimale diventando vimentina positiva, e questo rappreenta un ritorno indietro nel<br />
tempo.<br />
Questo spiega perché il melanoma è uno dei tumori più metastatizzanti: perché il<br />
melanocita, derivando dalla cresta neurale, e da questa colonizzando tutta la cute, possiede<br />
delle capacità enormi di migrazione!<br />
(displasia) Un ruolo fondamentale ce l'ha anche la nicchia, il microambiente in cui è situata<br />
la cellula staminale. Se però accade un evento, come un forte processo infiammatorio locale,<br />
che distrugge anche le cellule staminali, questo tessuto, attraverso fattori chemiotattici<br />
richiama cellule staminali da fuori, e spesso vengono dal midollo osseo.<br />
Quando la staminale multipotente del midollo osseo si trova in questa nicchia che non è la<br />
sua, si ritrova anche con segnali contraddittori ai segnali che aveva nel midollo, e questa è la<br />
scaricato da www.sunhope.it
ase per la displasia.<br />
La cell staminale è l'unica cellula che può avere la mitosi asimmetrica, perché una cellula<br />
deve tornare staminale, e l'altra subisce un parziale commissionamento a seconda del tessuto<br />
in cui si trova.<br />
Queste cellule hanno anche la caratteristica alla resistenza ai farmaci, perché sono ricche di<br />
telomerasi e altri fattori di protezione che le dnano la capacità di resistere.<br />
Nell stomaco per esempio il precursore del cancro è l'atrofia gastrica, che spesso coesiste<br />
con la displasia e la metaplasia intestinale. L'Helicobacter pilori è fondamentale in questo<br />
processo perché, nonostante la sua eleganza, ha la capacità di generare un'onda d'urto<br />
infiammatoria che può distruggere le cellule staminali; questo fa venire altre cellule<br />
staminali dal midollo che occupano le nicchie dove in precedenza si trovavano le nicchie<br />
delle staminali, e possono dare origine anche a cellule stromali, sviluppando un cancro che<br />
diventa di un tessuto simile al circostante. Si crea un habitat favorevole allo sviluppo del<br />
cancro.<br />
Chemioterapia e cellule staminali:<br />
Anche se in minima percentuale tutti i tumori maligni hanno una componente staminale<br />
alterata con marcatori specifici di alterazione.<br />
Una chemioterapia tradizionale non agisce sulle cellule staminali, avendo cicli replicativi<br />
infiniti e hanno una crescita molto più lenta. Questo le rende più indifferenti alla<br />
chemioterapia. Con la chemio si distrugge tutto il tumore, ma restano le staminali, e si<br />
riforma il tumore. Si sta sperimentando di riuscire a distruggere le cellulari, per far venir<br />
meno quel 2-3% di cell indistruttibili del tumore.<br />
Le cell staminali hanno duplicazione lenta ma illimitata, al contrario delle tumorali che<br />
hanno duplicazione rapida e limitata.<br />
Differenziazione alternativa<br />
Siamo sicuri che il cancro sia un'anomalia? E non sia una via di “differenziazione<br />
alternativa” già scritta nel DNA, dato l'elevato numero di cancri?<br />
Infatti dopo una certa età, il cancro diventa quasi una regola, come l'epitelioma basocellulare<br />
è un cancro, ma non dando metastasi non viene neanche considerato cancro... ma se<br />
considerassimo cancri anche quelli che non danno metastasi, l'incidenza sarebbe molto<br />
elevata. Stessa cosa per il ca.della prostata che colpisce la maggioranza degli uomini oltre<br />
una certa età.<br />
Il cancro che si sviluppa in un anziano è un cancro che ha una capacità trasformativa molto<br />
bassa, che evolve con molta meno aggressività.<br />
La correlazione con le cellule staminali infatti spiega la plasticità del genoma e la capacità<br />
differenziativa multipla; infatti nell'ambito di un carcinoma sono presenti multiple specie<br />
cellulari! Questo rende poco agevole la diagnosi istologica.<br />
Perché si muore per cancro?<br />
• tumore infiltrante<br />
• metastasi infiltranti organi vitali come il cervello<br />
• sindromi neoplastiche<br />
• produzione di tossine tumorali<br />
• cachessia da produzione di citochine.<br />
scaricato da www.sunhope.it
Tailored therapy:<br />
o terapia sartoriale dove la terapia deve essere fatta su misura, perché per esempio nel ca.<br />
della mammella ci sono tante terapie possibili (chemio, radio, chirurgia, con migliaia di<br />
protocolli diversi).<br />
In questa situazione è l'anatomo patologo che deve definire non solo le dimensioni del<br />
tumore, ma anche quanto questo possa essere suscettibile a chemioterapia.<br />
Parametri Anatomopatologici:<br />
Classificare il cancro ha una sua funzione. Esempio: nel carcinoma della cute si possono<br />
avere il basocellulare, melanoma, squamoso.<br />
Il basocellulare (o epitelioma) ha una capacità invasiva molto relativa, e spesso non è<br />
neanche consigliato toglierlo, anche se c'è possibilità di metastatizzare.<br />
Lo squamoso metastatizza nel
Valore della chirurgia:<br />
la chirurgia oncologica ha uno spazio sempre più ridotto perché si è passati da una mentalità<br />
più grossolana, dove si operava con il concetto “più è demolitivo l'intervento e più è<br />
curativo”.<br />
Ora invece si è visto quanto può essere controproducente un intervento demolitivo, che<br />
magari è R0 ma per quanto l'intervento possa essere perfetto, il PZ muore prima.<br />
Competizione tumore primitivo-metastasi: questo fa si che la rimozione di un tumore<br />
primitivo fa si che rendi più potente la metastasi, la quale si espanderà molto più<br />
rapidamente. Allora ci dovrebbe essere il problema di “quando operare”, infatti molto<br />
spesso il chirurgo improvvisa e durante l'intervento vede quanto più cancro può eliminare.<br />
Questo tipo di improvvisazione è molto pericolosa, e dovrebbe essere sempre definita dai<br />
risultati dei parametri anatomo-patologici.<br />
Per esempio nel ca. della mammella non è chiesto solo una resezione completa, ma anche<br />
una qualità di vita migliore.<br />
Infatti la mastectomia si riserva a pochi casi e l'intervento più frequente oggi è la<br />
quadrantectomia e tumorectomia per assicurare un risultato estetico adeguato. Se però poi<br />
vengono tolti anche il linfonodi ascellari in toto ci sarà elefantiasi dell'arto, anche qui<br />
pregiudicando l'estetica. I linfonodi tolti venivano studiati per vedere se c'era un loro<br />
coinvolgimento.<br />
Oggi invece con la tecnica del linfonodo sentinella si inietta un mdc in punti strategici del<br />
tumore e il radiologo vede quale è il linfonodo che drena per primo il tracciante.<br />
Allora si toglie prima solo quel linfonodo e l'anatomopatologo lo analizza in tempo reale e<br />
se negativo non si fa linfoadenectomia, altrimenti la si fa.<br />
Ci può essere solo la possibilità rara che la metastasi abbia saltato il linfonodo.<br />
Errori in anatomia patologica<br />
La anatomo-patologia di un tumore ha un forte valore prognostico perché variazioni<br />
diagnostiche portano a gravi risultati. L'errore può essere “patologico” dovuto a ignoranza,<br />
negligienza superficialità, ma esistono anche limiti che possono essere:<br />
• Limiti intrinseci: dovuti alla complessità e alla eterogenicità anche nell'ambito dello<br />
stesso tumore.<br />
• Limiti estrinseci: che sono invece dovuti ad personali capacità interpretative del<br />
nostro cervello di percepire la forma di un oggetto che può variare con lo sfondo e da<br />
persona a persona.<br />
Questo fa si che tra il maligno e il benigno ci sia una zona borderline tra il maligno ed il<br />
benigno, frequenti per esempio nel ca dell'ovaio. Spesso il buono e il cattivo li distinguiamo,<br />
ma ci può essere un brutto che è molto soggettivo se visto come brutto=cattivo o<br />
brutto=bonario.<br />
Esiste quindi una variabilità inter-observed e intra-observed, dove lo stesso<br />
anatomopatologo può cambiare il proprio risultato diagnostico anche a distanza della stessa<br />
osservazione fatta in tempi diversi, più anatomopatologi possono dare risultati contrastanti.<br />
Per questo è sempre preferibile usare anche tecniche oggettive che possano oggettivare un<br />
risultato. Esiste poi l'errore da eccesso di sopravvalutazione da esperienza che non fa vedere<br />
cose che invece ci sono.<br />
Esempio: la diagnosi di melanoma: la diagnosi è molto soggettiva però è anche vero che i<br />
nevi spuntano continuamente, specialmente alla vostra età, seguendo uno sviluppo<br />
scaricato da www.sunhope.it
metamerico. C’è poi una maggiore conoscenza da parte della popolazione, e consapevolezza<br />
da parte del dermatologo. L'aumento della incidenza è dovuto anche allo sviluppo della<br />
dermoscopia (tecnica di ingrandimento e visualizzazione della lesione nevica) e perciò si<br />
scoprono lesioni sempre più piccole. Quando le lesioni sono piccole, sono all’inizio della<br />
loro storia naturale, in una zona grigia dove le precancerosi e cancro iniziale si<br />
confondono.Questo spiega la grande variabilità delle diagnosi.<br />
Inoltre si cimentano in questa diagnostica persone non competenti, per cui se uno scrive:<br />
“nevo displastico con immagini fino al melanoma”; dà un’immagine dinamica che<br />
comprende tutto, è una sorta di diagnosi politica (tutto e il contrario di tutto).<br />
Esempio: Diagnosi di linfom: si diceva che questa era la tomba dell’anatomopatologo;<br />
fortunatamente oggi abbiamo delle tecniche ausiliarie che ci aiutano nella diagnostica.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA lezione del 25 ottobre ‘10<br />
Ci sono alcune lesioni per cui c’è una grandissima difficoltà nella diagnosi differenziale; queste<br />
lesioni sono quelle melanocitarie. La difficoltà deriva dal fatto che oggi c’è un’aumentata sensibilità<br />
da parte della popolazione verso questo tipo di lesione. Le lesioni melanocitarie sono in grande<br />
aumento, l’incidenza è aumentata molto; però è anche vero che i nevi spuntano continuamente,<br />
specialmente alla vostra età, seguendo uno sviluppo metamerico (può succedere che uno<br />
facendosi la doccia si spaventa). C’è questa difficoltà perché c’è una maggiore conoscenza da parte<br />
della popolazione, c’è una maggiore consapevolezza da parte del dermatologo, c’è anche lo<br />
sviluppo della dermoscopia (tecnica di ingrandimento e visualizzazione della lesione nevica) e<br />
perciò si scoprono lesioni sempre più piccole. Quando le lesioni sono piccole, sono all’inizio della<br />
loro storia naturale, in una zona grigia dove le precancerosi e cancro iniziale si confondono un<br />
po’.Questo spiega la grande variabilità. Inoltre si cimentano in questa diagnostica persone non<br />
competenti, per cui se uno scrive: ; da<br />
un’immagine dinamica che comprende tutto, è una sorta di diagnosi politica (tutto e il contrario di<br />
tutto). Altro problema è nella diagnostica dei linfomi e si diceva che era la tomba<br />
dell’anatomopatologo; fortunatamente oggi abbiamo delle tecniche ausiliarie che ci aiutano nella<br />
diagnostica. Per concludere c’è un grafico che voi vedete, fatto da un anatomopatologo di nome<br />
Taylor: mette a confronto due anatomopatologi, uno con una grande esperienza con una fama e un<br />
prestigio che cresce in maniera esponenziale, uno che è un anatomopatologo medio con una curva<br />
che non è lineare come quella di prima, ma fa un po’ schifo; con l’ausilio delle tecniche<br />
diagnostiche come l’immunoistochimica e la biologia molecolare, il patologo A ha tutto da perdere<br />
perché diceva un santo :” più alto è il piedistallo, più rovinosa è la caduta”. Il patologo B invece ha<br />
tutto da guadagnare perché può fare anche lui delle belle figure. Se andiamo a vedere le casistiche<br />
giudiziarie, i contenziosi, che interessano molto anche l’anatomopatologo perché il giudizio<br />
diagnostico di una glicemia, di un’azotemia è molto diverso da una diagnosi anatomopatologica e<br />
l’anatomopatologo entra spesso in questi contenziosi per chiarire la situazione (tra l’altro in Italia<br />
abbiamo una difficoltà enorme a creare dei dati statistici su questo, infatti queste sono statistiche<br />
americane; questo perché c’è una sfiducia enorme nei confronti della medicina e se voi andate su<br />
internet e scrivete mala sanità, vi escono una infinità di siti e su uno di questi trovate la frase di<br />
uno sconosciuto che dice “la malattia più grande dell’umanità è la diagnosi”). La causa maggiore di<br />
contenziosi giudiziari in America è il PAP TEST: questo perché quando è negativo e la persona<br />
sviluppa il cancro dopo un anno, subito denuncia chi ha letto il vetrino; anche se può succedere<br />
benissimo che questo cancro si sviluppa in questo periodo di tempo (1 anno). Da questo nasce la<br />
medicina difensiva che anziché pensare al paziente, pensa al rispetto dei protocolli ecc. A parte la<br />
biologia molecolare, noi abbiamo una tecnica che usiamo tutti i giorni che è l’immunoistochimica;<br />
questa è una tecnica immunoenzimatica cioè all’anticorpo è legato un enzima. Quando avviene la<br />
reazione antigene-anticorpo non vediamo niente, ma se mettiamo un enzima particolare che<br />
reagisce con un substrato specifico, dove c’è l’enzima il substrato precipiterà e cambierà colore. Noi<br />
usiamo spesso la DIAMINOBENZIDINA che precipitando diventa marrone. Inutile dirvi che noi<br />
abbiamo una grande variabilità di metodiche in questo settore, che hanno una grande capacità di<br />
amplificare il segnale, cioè un antigene viene amplicifato fino a 10000-100000; quello che vi ho<br />
scaricato da www.sunhope.it
descritto è il metodo banale che non si usa più da 30 anni ed è il metodo diretto. Con questi<br />
sistemi noi andiamo a cercare dei marcatori che sono:<br />
Marcatori immunoistochimici 1:<br />
-marcatori oncofetali<br />
-marcatori di benignità<br />
-marcatori istiocito specifici<br />
-marcatori linfocitari<br />
-marcatori di funzione<br />
-marcatori trofoblastici<br />
-antigeni virali<br />
-enzimi correlati all’invasività<br />
Si tratta degli stessi marcatori che si vanno a vedere nel sangue; ma anche il tessuto li presenta o li<br />
può presentare. Marcatori oncofetali: sono antigeni che sono espressi durante il periodo fetale poi<br />
scompaiono nelle cellule adulte per ricomparire nei tumori. Abbiamo visto una dispositiva che<br />
faceva vedere la macchina del tempo, un ritorno indietro. E’ come se la cellula tumorale tornasse<br />
indietro ed esprimesse marcatori fetali. Probabilmente l’espressione di questi marcatori è legata ad<br />
un processo di semplificazione biochimica; siccome la cellula tumorale ha un accelerato turnover<br />
non fa in tempo a specializzarsi e d’altra parte non vuole specializzarsi perché ha altre finalità. La<br />
cellula tumorale si limita a fare dei precursori espressi anche nella vita fetale e non delle proteine<br />
finali espresse nelle cellule adulte. Possiamo in alcuni casi sfruttare ai fini diagnostici tali propietà.<br />
Appartengono a questo gruppo il CEA, l’alpha-fetoproteina, molti anticorpi monoclonali tra cui il<br />
B72-3 che io conosco molto bene perché l’ho tipizzato proprio io. Marcatori di benignità: vi sono<br />
alcuni marcatori che al contrario sono espressi solo dalle cellule normali e si perdono nelle cellule<br />
atipiche. Questi sono gli antigeni dei gruppi sanguigni ABH. Forse pochi sanno che questi qui, oltre<br />
che sulle emazie, sono presenti su tutte le cellule epiteliali dell’organismo, come ad es. l’epitelio<br />
uroteliale. Marcatori istiocitospecifici: tenete presente che non esiste questa classificazione, ma<br />
l’ho preparata io per voi; in genere si utilizza una classificazione di tipo biochimico, invece questa è<br />
una classificazione funzionale che serve a capire anche a che serve. I marcatori istiocito specifici<br />
sono quei marcatori che sono legati all’istogenesi del tessuto. Per esempio se io voglio cercare<br />
tessuto epiteliale, andrò a vedere se esprime o meno la citocheratina e la citocheratina in linea di<br />
massima viene espressa specificamente dalle cellule epiteliali; esistono comunque molte<br />
citocheratine alcune espresse dall’epitelio squamoso, altre dall’epitelio cilindrico ecc e queste<br />
vengono identificate da anticorpi diversi. Se voglio sapere se è mesenchimale, allora faccio la<br />
vimentina che viene espressa da tutti i tessuti di origine mesenchimale. Esistono tantissimi<br />
marcatori per ogni tipo di tessuto. Un altro esempio è il tessuto cerebrale, voglio sapere se queste<br />
cellule sono gliali(quindi cellule di supporto) o no: queste cellule hanno marcatori istiocitospecifici<br />
scaricato da www.sunhope.it
che molto spesso fanno parte del citoscheletro di quelle cellule come la GFAP (glial fibrillary acidic<br />
protein), una proteina gliale acida implicata. Marcatori linfocitari: non parliamo poi dei linfociti<br />
perché dei linfociti posso, come si dice a Napoli, sapere vita, morte e miracoli; questo perché<br />
esistono tanti di quei CD che sono marcatori linfocitari: posso sapere la popolazione, la<br />
sottopopolazione a cui un gruppo di linfociti appartiene ecc. Marcatori di funzione: molto spesso<br />
le cellule tumorali e le cellule normali possono esprimere, anche se le cellule normali esprimono al<br />
massimo mentre le cellule tumorali un poco meno, dei marcatori che ne individuano la loro<br />
funzione specifica; per esempio, la presenza di recettori ormonali, ER recettore per gli estrogeni,<br />
PgR recettore per il progesterone sono importanti per determinati campi, come ad esempio per la<br />
mammella, ma ce ne sono tantissimi. Già se voglio sapere se una una metastasi viene ad esempio<br />
dalla tiroide, ci vado a fare la tireoglobulina, T3, T4 perché è vero che è una metastasi, però un po’<br />
di T3, di T4 e di tireoglobulina le troverò dentro. Questo è importante per esempio nelle metastasi<br />
da cancro occulto; la TC total body non mostra niente e abbiamo questa metastasi. Quello che ci<br />
interessa sapere è capire da dove viene, perché se non capiamo da dove viene non possiamo fare<br />
niente e perciò ricorriamo a questi espedienti. Quasi tutti i tessuti hanno dei marcatori specifici.<br />
Marcatori trofoblastici: sono antigeni che noi ritroviamo nelle neoplasie trofoblastiche. Non so se<br />
voi avete mai sentito parlare di coriocarcinoma, ad esempio, ovvero quelle neoplasie imparentate<br />
con la placenta che possono venire anche in donne non in gravidanza e anche uomini. Questi<br />
marcatori sono l’HCG, gonadotropina umana corionica, la proteina SP1 e tutta una serie di ormoni<br />
sintetizzati dal trofoblasto. La cosa interessante è che cellule tumorali che non appartengono alla<br />
linea trofoblastica possono esprimere comunque questi antigeni; tumori che quindi non<br />
c’azzeccano niente son la linea trofoblastica. Questo accade soprattutto quando sono tumori<br />
particolarmente indifferenziati. Trovare antigeni trofoblastici esprime un grande ritorno<br />
all’indietro, nel passato perché sono alcuni degli antigeni che vengono espressi per prima dalle<br />
cellule. Questa è un’altra conferma del ruolo delle cellule staminali. Antigeni virali: su cui non mi<br />
soffermo (papilloma virus ecc.); molti di questi virus si è visto che hanno un ruolo oncogeno.<br />
Enzimi correlati all’invasività: questo ci può consentire di acquisire informazioni sulle propietà<br />
delle cellule tumorali. Uno di questi enzimi è l’urochinasi, attivatore del plasminogeno, che se<br />
espresso dalle cellule tumorali è un brutto segno.<br />
Marcatori immunoistochimici 2:<br />
-marcatori cinetici<br />
-prodotti oncogenici<br />
-fattori di crescita e recettori<br />
-prodotti di geni oncosoppressori<br />
-indicatori di chemioresistenza<br />
-fattori di trascrizione<br />
-altri<br />
scaricato da www.sunhope.it
Marcatori cinetici: tutte le fasi e le sottofasi del ciclo cellulare hanno delle proteine specifiche,<br />
proteine di innesco, che consentono poi a quella cellula di passare alla fase successiva del ciclo<br />
cellulare. Se io voglio sapere di una popolazione quante cellule si trovano in fase proliferativa e<br />
quante in fase G0, userò un anticorpo molto diffuso, il Ki67; questo anticorpo marca tutte le cellule<br />
tranne quelle in fase G0. Se io voglio essere ancora più specifico e sapere quante cellule si trovano<br />
in fase S, allora proverò la proteina PCNA (proliferating cellular nuclear antigen). Se io voglio sapere<br />
quante cellule si trovano in fase G1 o G2 andrò a cercare le cicline e ci sono vari tipi di cicline nella<br />
fase G1 e nella fase G2. Se io voglio sapere quante cellule si trovano in fase G0 userò la statina.<br />
Quindi se il Ki67 mi da per esempio una quota del 30%, faccio la statina e mi dovrò trovare il 70%<br />
come risultato. Prodotti oncogenici: non ne parliamo perché ne abbiamo a lungo parlato; vi<br />
ricordo solo c-erb-B2 per l’apparanto gastroenterico e il gene myc che ha un ruolo prognostico<br />
fondamentale in determinati tumori neuroectodermici. C’è quindi valore diagnostico, ma anche un<br />
valore prognostico. Fattori di crescita e loro recettori: già ne abbiamo parlato, per esempio<br />
l’espressione o meno TGF-beta ha un grande significato, poi lo vedremo più avanti. Prodotti di geni<br />
oncosoppressori: in effetti qua sembra un paradosso, tanto è vero che all’inizio fu un paradosso<br />
che nessuno riusciva a spiegare perché nel cancro trovavamo più proteine 105(P105) del gene RB<br />
rispetto ad un tessuto normale. Questo è un paradosso; una proteina oncosoppressore la troviamo<br />
più nel cancro che nel tessuto normale. Stessa cosa accade per la P53. Poi ce lo siamo spiegati<br />
dopo molti anni che sembrava crollare tutta la dottrina sui geni oncosoppressori: solitamente<br />
questi geni oncosoppressori nelle cellule normali e quindi le loro proteine hanno un’emivita molto<br />
breve e vengono degradate subito; viceversa si accumulano nella cellula anche quando c’è una<br />
piccola motazione puntiforme che l’anticorpo non riesce a riconoscere ( non la riconosce perché<br />
pensate che si sia modificata una sola base e quindi un solo amminoacido in una proteina che ha<br />
milioni di amminoacidi ). Noi troveremo quindi accumuli di queste proteine in determinati tipi di<br />
cancro proprio perché sono mutati. Indicatori di chemio resistenza : questa è una novità. Nella<br />
cellula esistono tante pompe in grado di espellere tante sostanze. Una delle pompe più importanti<br />
è quella che appartiene alla P170 che è l’antigene strutturale più importante; questa pompa in<br />
effetti viene utilizzata per epellere dalla cellula normale determinate tossine legate ai funghi<br />
velenosi; alcuni chemioterapici che noi usciamo appartengono un poco a questa famiglia, ad<br />
esempio vincristina, vinblastina, adriamicina. Se utilizziamo questi chemioterapici per tumori che<br />
esprimono questa pompa, noi al tumore facciamo un baffo. Questo spiega anche perché tra 10<br />
persone che hanno ingerito funghi “velenosi” o comunque non raccomandabili, solo 1 o 2 persone<br />
vanno incontro a intossicazione e agli altri non succede niente, proprio perché c’è una certa<br />
variabilità genetica. Fattori di trascrizione: questi fattori sono una famiglia enorme molto spesso<br />
specifici di un tessuto; per esempio il TTF1 lo troviamo in tumori della tiroide o del polmone. Ce ne<br />
sono molteplici di questi fattori ristretti per alcuni tessuti. Possiamo quindi sapere questo tumore<br />
di che parte è. Altri: ci sono tutta una serie di marcatori che stanno nascendo di cui non parleremo<br />
perché non è ancora noto il loro significato clinico.<br />
Vi ho fatto una rapida carrellata, adesso vi faccio qualche esempio: vedete qua il CD20; se voi<br />
vedete un linfonodo e noi ne vediamo molti, a cui è stato fatto il CD20, questo CD20 che marca i<br />
linfociti B andrà a marcare tutte le aree. Ci sono aree fortemente marcate e come vedete da questa<br />
immagine, aree quasi negative. Già guardando questa immagine posso capire che difficilmente è<br />
scaricato da www.sunhope.it
un linfoma. Se faccio la prova del 9 col CD3 che marca le cellule T vedrò che si andranno a marcare<br />
le aree che erano negative al CD20 mentre quelle che prima erano positive al CD20 adesso saranno<br />
negative. Trovo quindi rispettata la distribuzione, nel linfonodo, delle aree T e delle aree B quindi<br />
posso escludere un processo neoplastico.<br />
Quest’altro invece è un caso di una cinese: è un caso dubbio di un cancro della mammella.<br />
L’immunoistochimica ci aiuta perché nella normalità della gh mammaria, le cellule epiteliali sono<br />
circondate da uno strato di cellule mio epiteliali che aiutano la secrezione perché spremono. Se<br />
usiamo un marcatore come l’actina, esiste un’actina per il muscolo liscio e un’actina per il muscolo<br />
striato, ci rendiamo conto che è un cancro perché in alcune aree c’è un anello di cellule positive<br />
disposte tutt’intorno, questo non è cancro; ma in quest’altra area questo anello si perde e abbiamo<br />
la conferma che si tratta di un cancro. Questo discorso lo facciamo per la prostata e per altri tipi di<br />
tessuto. Se facciamo i recettori per l’estrogeno, in questo caso come vedete, c’è oltre il 90% delle<br />
cellule positive quindi questo cancro è sensibile all’endocrinoterapia. Vedete che c’è un’immagine<br />
ad occhiello di cui già vi ho parlato e c’è amplificazione di questo recettore. Sono tutte immagini<br />
che somigliano ad un alveare marroncino.<br />
Questa è una lesione sub-ungueale all’alluce; questo è il quadro morfologico. Come antigene<br />
esplime il Melan A e HMB45 che sono antigeni istiocitospecifici del melanoma: Questo quindi si<br />
tratta di un melanoma acrale sub ungueale che è tra i più terribili. E’ un melanoma che sta vicino ai<br />
vasi e tende a metastatizzare rapidamente. Se vediamo il piede, alla base dell’alluce c’è un altro<br />
nodulo che a volte fanno i melanomi molto maligni; è il nodulo satellite detto anche melanoma in<br />
transito perché è un segnale di meta statizzazione, ha già metastatizzato.<br />
DIAGNOSI IN ANATOMIA PATOLOGICA:<br />
Si fa attraverso paramentri istologici, ovvero l’architettura, attraverso l’immunoistochimica,<br />
attraverso paramentri citologici, avvero la morfologia cellulare, parametri macroscopici,<br />
paramentri molecolari, attraverso la clinica (perché l’anatomia patologica è una disciplina clinica),<br />
l’esperienza e poi attraverso un tassello fondamentale che è il buon senso.<br />
RUOLO DELL’ANATOMIA PATOLOGICA:<br />
il professore mostra il papiro di Smith detto anche papiro chirurgico del 3000 a. C. che è<br />
lunghissimo 16 m e poi un papiro di un anatomo patologo del 1500 a.C. lungo pochi cm; in<br />
quest’ultimo c’è scritto che quest’uomo quando vedeva un cacro mammario, con molta umiltà,<br />
non sapeva cosa fare. Nel papiro chirurgico il cancro mammario veniva trattato con la<br />
causticazione. Alla fine del papiro di pochi cm c’è la scritta tumore il geroglifico. Il prof vuole dire<br />
che i chirurghi più scrivono, più pubblicano e più si sentono importanti oggi come 3000 anni prima<br />
di Cristo.<br />
Oggi c’è un carico enorme di lavoro per l’anatomopatologo che va dalla citologia aspirativa,<br />
all’indagine molecolare, alla prevenzione, alla diagnosi in estemporanea(ovvero intra-operatoria),<br />
linfonodo sentinella ecc ecc. e se è vero che vale il concetto di terapia sartoriale, noi dobbiamo<br />
estrarre dal tumore tutta una serie di informazioni di cui prima non si sentiva il bisogno. L’anatomia<br />
scaricato da www.sunhope.it
patologia interviene nella prevenzione, ne abbiamo già parlato per le vie genitali femminili, ma si fa<br />
per il polmone, per la prostata. La prevenzione è molto importante perché un paziente che ha un<br />
tumore costa moltissimo al sistema sanitario nazionale, quindi una buona prevenzione consente<br />
un risparmio notevole anche in termini di giornate lavorative. Interviene,inoltre, nella fase<br />
diagnostica: un nodulo a livello intestinale, una lesione cutanea non chiara e prima di intervenire si<br />
fa la biopsia. Interviene a livello intraoperatorio, ovvero in estemporanea; a livello post operatorio<br />
in cui si fa la diagnosi conclusiva con la stadiazione, il tipo di tumore e tutti quei paramentri che<br />
intervengono per fare una terapia di tipo sartoriale. L’anatomia patologica è implicata anche nella<br />
valutazione di una terapia, come ad esempio per valutare i risultati di una radioterapia attraverso<br />
tutta una serie di parametri . Noi siamo attivi molto anche nei trapianti: per esempio nel trapianti<br />
cardiaci o di altri organi,nelle cosiddette fasi di rigetto lieve, moderato ecc. la biopsia si positivizza<br />
molto prima dei parametri cosiddetti bioumorali; per cui la terapia del trapiantato è una terapia di<br />
equilibrista, con farmaci immunosoppressivi contro un possibile rigetto, ma bisogna comunque<br />
calibrare il rischio di infezione ecc ecc. L’anatomopatologo rientra anche nel monitoraggio della<br />
malattia e nell’analisi della concordanza di cui parleremo tra poco (cioè il paziente ricoverato in<br />
questa struttura in tale giorno ha ricevuto una diagnosi ed un trattamento realmente appropriati?).<br />
Quali tipi di materiale vengono all’anatomopatologo? Le autopsie, quindi materiale autoptico, le<br />
biopsie che possono essere grandi come ,ad esempio esami d’organo (un rene intero, una<br />
mammella intera), incisionali quando invece non arriva un organo intero ma una piccola parte (ad<br />
esempio un polipo intestinale), biopsie escissionali quando si asporta tutta una lesione cutanea, ad<br />
esempio un carcinoma basocellulare, almeno si pensa che sia questo e allora si fa in modo di<br />
asportarlo in toto. Le biopsie si fanno attraverso un ago che consente il prelievo di un piccolo<br />
campione di tessuto. Ci sono poi i prelievi citologici che riguardano la citologia esfoliativa come ad<br />
esempio il PAP TEST, la citologia urinaria, la citologia bronchiale ecc. . Le cellule che esfoliano, però,<br />
sono cellule morte; se vogliamo favorire l’esfoliazione e reperire cioè cellule più vitali, dobbiamo<br />
fare dei trattamenti di tipo brushing (spazzolina per endocervice ad esempio) oppure washing<br />
(lavaggio che colpisce ad esempio le pareti della vescica). Questa è la citologia esfoliativa.<br />
Possiamo fare citologia anche dei versamenti, come ad esempio il versamento pleurico. La citologia<br />
da apposizione lasciamola stare. Infine c’è l’ ABC ovvero la citologia aspirativa di cui parleremo.<br />
All’anatomo patologo arrivano anche tessuti congelati: per l’estemporanea c’è bisogno di congelare<br />
il tessuto, perché non c’è il tempo di fare l’inclusione in paraffina e tagliarlo col microtomo (ci<br />
vogliono molte ore). L’apparecchio chiamato criostato congela il pezzo e lo taglia in maniera sottile;<br />
ci sono comunque degli artefatti, ma comunque la tecnica è veloce ed è adatta all’estemporanea.<br />
AUTOPSIA:<br />
Non vi interessa sapere come si fa un’autopsia. E’ una tecnica che costa molto perché bisogna fare<br />
vari prelievi dai vari organi e poi studiarli al microscopio. A volte però è necessaria; una cosa è la<br />
causa di morte, una cosa sono gli epifenomeni della morte. Se io scrivo collasso cardio-circolatorio,<br />
è una cosa ovvia perché non si è mai visto uno che muore con la pressione normale. Fummo<br />
proprio noi anatomopatologi a fare presente il fatto che in Italia la causa di morte
cardiocircolatorio>> andava per la maggiore, perché tutti scrivevano come causa di morte collaso<br />
cardio-circolatorio, ma alla fine “nun signific’ nient”. Ci sono vari motivi per fare un’autopsia: il<br />
primo è l’accertamento delle cause di morte; poi c’è l’analisi della concordanza: per esempio in<br />
America le autopsie per numero di deceduti si attesta intorno al 30% dei casi perché c’è un<br />
rapporto fatto nel 1911 detto rapporto Kesner che obbliga ad un certo numero di riscontri<br />
diagnostici autoptici, per cui ogni struttura pubblica deve avere un certo numero di riscontri<br />
diagnostici. E’ usato proprio come parametro di qualificazione della struttura pubblica oltre ad altri<br />
parametri. In Italia invece abbiamo una serie di parametri ridicoli come le infezioni ospedaliere,<br />
perché io vorrei sapere quale direttore sanitario dice la verità su questo punto. I parametri veri<br />
invece sono questi, come quello dei riscontri autoptici.<br />
Io non ricordo mai di aver fatto un’autopsia senza aver trovato almeno 7-8 cause che possono aver<br />
portato a morte il paziente. Questo è un problema perché spesso il medico si fissa su una causa<br />
specifica.<br />
Altro motivo per fare autopsie è la formazione professionale: nei paesi di lingua inglese nessuno si<br />
specializza in ambito sanitario se non ha fatto almeno un tot numero di ore in sala settoria. Infine<br />
per le applicazioni scientifiche: per esempio pochi di voi sanno che la conoscenza dell’AIDS è<br />
iniziata proprio nel settorato di New York quando degli anatomopatologi hanno segnalato una serie<br />
di morti che avevano sintomi particolari come tumori maligni, infezioni opportunistiche, sarcoma<br />
di Kaposi e così via. Le autopsie sono importanti perché ognuno può indagare il suo approccio<br />
clinico al paziente.<br />
Classifica internazionale della concordanza e della discordanza:<br />
Gli errori diagnostici di classe 1 sono quelli che hanno portato a morte il paziente: sono quegli<br />
errori gravissimi che hanno cambiato quella che era la storia naturale del paziente, la terapia e<br />
quindi c’è un nesso diretto. Tipico è l’esempio di una diverticolite multilpa che aveva determinato<br />
delle masse intestinali (diverticolite porta a fistolizzazioni che poi esitano in fibrosi). Diagnosticato<br />
con la TC come cancro inoperabile, il paziente è morto per occlusione intestinale. Il paziente si<br />
doveva sottoporre ad intervento chirurgico per togliere i diverticoli e sicuramente si sarebbe<br />
salvato.<br />
Gli errori diagnostici di classe 2: discordanza nella diagnosi principale con effetto incerto sulla<br />
prognosi. Esempio: non aver diagnosticato una polmonite da citomegalovirus è una cosa grave; ma<br />
se l’avessimo diagnosticata siamo proprio sicuri che con la terapia avremmo risolto la terapia?<br />
Gli errori diagnostici di classe 3: la discordanza non sta nella diagnosi principale, ma in una<br />
diagnosi secondaria che comunque ha causato la morte del paziente. Per esempio: polmonite ab<br />
ingestis in soggetto che già aveva cancro del polmone. Se un anatomopatologo si rende conto che<br />
ci può essere responsabilità professionale nella morte del paziente, deve subito interrompere<br />
l’autopsia e avvisare la procura che disporrà se continuare o meno l’autopsia.<br />
Classe 4: La discordanza ha solo un iteresse epidemiologico e scientifico. Esempio: aver trovato un<br />
cancro della prostata silente che non ha alcuna responsabilità nella morte del paziente.<br />
scaricato da www.sunhope.it
Classe 5: concordanza assoluta.<br />
Degli errori ci interessano quelli di classe 1 perché sono i più gravi e riguardano il 4-10% delle<br />
autopsie fatte da un anatomopatologo. Le principali cause di discordanza sono: c’è un guardare la<br />
tecnologia come una specie di divinità (spesso abbiamo attrezzature che nessuno sa adoperare),<br />
spesso non c’è un’anamnesi, c’è una progressiva mancanza di tempo; poi ci sono patologie<br />
sovrastimate come il collasso e l’infarto e ci sono patologie sottostimate come l’embolia polmonare<br />
ed i tumori. Esiste un’embolia di seconda classe: le seconde classi degli aerei hanno uno spazio per<br />
le gambe ridicolo e si può determinare una flebo trombosi soprattutto nei soggetti anziani e nei<br />
viaggi lunghi.<br />
scaricato da www.sunhope.it
TIROIDE<br />
LEZIONE DEL 26/10/2010<br />
Le patologie della tiroide sono molto diffuse e il nodulo tiroideo è solo una di queste<br />
e quando ci si trova di fronte ad un nodulo tiroideo la prima cosa che diciamo alla<br />
paziente è quella di farsi un’ecografia.Esso colpisce circa il 4-10 % della popolazione<br />
normale e nell’85 % dei casi il nodulo è legato ad una patologia non<br />
neoplastica(es.iperplasia nodulare della tiroide oppure può rientrare in un quadro di<br />
gozzo,il quale soprattutto nelle fasi iniziali non si appalesa come multinodulare,ma si<br />
pensa ci sia un nodulo che prende il sopravvento sugli altri e poi facendo l’ecografia<br />
vediamo che ci sono molti noduli).Nel 10 % dei casi si tratta di adenomi e nel<br />
soltanto nel restante 5% dei casi si tratta di carcinomi.<br />
Per quanto riguarda l’anatomia della tiroide essa risulta essere costituita da un lobo<br />
destro ed uno sinistro uniti da un istmo posto nella parte centrale della<br />
ghiandola.Indietro ci sono delle ghiandole molto piccole,nell’ordine di millimetri, che<br />
sono le paratiroidi,le quali spesso sono sovrannumerarie e di posizione<br />
variabile.Prima quando si effettuavano interventi chirurgici sulla tiroide facilmente si<br />
rimuovevano anche le paratiroidi,oggi invece si sta molto più attenti.ISTOLOGIA<br />
DELLE PARATITOIDI Le paratiroidi hanno un tessuto quasi linfoide,perchè costituito<br />
da piccole cellule.Le paratiroidi sono adese alla parete posteriore della tiroide,la<br />
quale è rivestita da una capsula che ha un ruolo molto importante.La tiroide è<br />
costituita da follicoli che sono rivestiti da cellule chiamate tireociti che sono cellule<br />
endocrine che a partire dalla tireoglobulina sintetizzano gli ormoni tiroidei e quella<br />
sostanza rosa presente all’interno dei follicoli è il materiale colloideo e facendo<br />
l’immunoistochimica si vede che si tratta molto spesso di tireoglobuline.Una tiroide<br />
con follicoli pieni di colloide in genere è una tiroide che non funziona molto<br />
bene,perché se c’è accumulo di colloide,vuol dire che produce meno ormoni.Questa<br />
colloide è molta,appare densa e adesa all’epitelio,quando invece la ghiandola è<br />
attiva,la colloide si rtitrae,si stacca dall’epitelio con la formazione di vacuoli,perché<br />
viene utilizzata per la sintesi degli ormoni tiroidei ed è come se la colloide si<br />
ritraesse.Tra i follicoli,nell’interstizio,ci sono dei gruppi di cellule molto<br />
importanti,che sono le cosiddette cellule C,appartenenti al sistema neuroendocrino<br />
diffuso e mediante immunoistochimica si è visto che esse producono calcitonina.Poi<br />
si è visto che la tiroide,come il polmone,esprime il fattore di trascrizione TTF-1.<br />
scaricato da www.sunhope.it
LOCALIZZAZIONI ANOMALE DELLA TIROIDE<br />
Spesso ci sono eterotopie delle tiroide e queste possono causare problemi di tipo<br />
diagnostico,perché all’ecografia,alla TC ecc.possono far pensare che si tratti di una<br />
metastasi.<br />
QUALI SONO LE LOCALIZZAZIONI ANOMALE?<br />
• Esistono delle eterotopie della tiroide su base embriologica,legate ad un<br />
problema di migrazione,perché la tiroide nasce in alto e poi si sposta verso il<br />
basso.<br />
• Può accadere poi che tessuto tiroideo venga sequestrato,nel senso che un<br />
gozzo molto grosso,una tiroidite o un processo che porta comunque<br />
all’ingrossamento della ghiandola come nel Basedow ,provochino fenomeni di<br />
fibrosi e di necrosi,per cui un pezzo di tiroide si va a distaccare dalla massa<br />
principale della tiroide e col tempo può allontanarsi sempre di più da<br />
essa.Questa dinamica patologica prende il nome di sequestro,in realtà non è<br />
un vero e proprio sequestro,ma è come se viene allontanata artificialmente<br />
per fenomeni infiammatori e di fibrosi.<br />
• Si può avere anche un impianto secondario ad intervento chirurgico,perché<br />
quando si fa un intervento chirurgico potrebbe scappare qualcosa,non<br />
dovrebbe succedere,ma può succedere per cui si impianta in una<br />
localizzazione anomala.<br />
• La tiroide può anche localizzarsi nei tessuti laterocervicali,soprattutto quelli<br />
alti,cioè le linfoghiandole e questo potrebbe creare confusioni<br />
diagnostiche,perché se si trova un linfonodo cervicale con cellule epiteliali si<br />
può pensare ad una metastasi e invece in questo caso si tratta di un eterotopia<br />
• Nella malattia di basedow,poiché la tiroide si ingrossa notevolemte,può<br />
accadere che del tessuto tiroideo si stacchi dando dislocazioni anomale.<br />
Dislocazioni anomale più frequenti:<br />
1) sottolinguale,perché da lì parte la tiroide durante l’embriogenesi,attraverso il<br />
dotto tireoglosso e a volte possono esserci problemi di ostruzione per cui qualcosa<br />
rimane lì.<br />
scaricato da www.sunhope.it
2) prelaringea<br />
3)sub sternale<br />
Problematiche correlate ad alterazioni dell’embriologia:<br />
L’abbozzo primitivo della tiroide è rappresentato da una piccola cisti a livello ventrale<br />
dell’abbozzo primitivo dell’intestino brachiale,da questo poi avviene un<br />
allungamento in senso caudale e la tiroide va a localizzarsi nella sede adulta.Si forma<br />
un canale che segue la tiroide che rappresenta il dotto tireoglosso,il quale collega la<br />
tiroide alla radice della lingua e normalmente esso poi va incontro ad atrofia e<br />
scompare.Se questo non avviene si può avere una serie di problemi,quali persistenza<br />
parziale o totale del dotto,oppure formazione di cisti che possono infiammarsi o<br />
fistolizzare causando la fuoriuscita all’esterno o in altri tessuti di materiale<br />
infiammatorio o necrotico.<br />
Il lobo piramidale rappresenta una specializzazione del dotto tireoglosso o di una sua<br />
parte in senso tiroideo e lo ritroviamo nel 20-30 % degli adulti ed in particolare nelle<br />
donne,forse perché già parlano troppo da piccole :D .<br />
Quando un soggetto ha una patologia da iperfunzione,es.basedow,si ha un<br />
ingrossamento anche di questo lobo piramidale che può provocare<br />
disfonia,raucedine,essendoci nelle vicinanze il nervo ricorrente oppure può<br />
succedere che in seguito a tiroidectomia per gozzo ignorando il lobo piramidale o le<br />
localizzazioni eterotopiche della tiroide,queste si sviluppano molto,creando problemi<br />
clinici,perché trovando alla scintigrafia del tessuto captante,si può pensare che oltre<br />
al gozzo ci sia qualche altra patologia quando poi non è così.<br />
GOZZO<br />
Se andate al museo di San Martino,non per infrattarvi,vedrete molti pastori del<br />
‘700-‘800 con gozzi davvero enormi.<br />
Dal punto di vista epidemiologico-patogenetico distinguiamo tre tipi di gozzo:<br />
1) gozzo endemico(oggi sta scomparendo,per l’aumentata disponibilità di iodio,ma<br />
prima in molte zone di Italia era molto diffuso,per la carenza di iodio nell’acqua e in<br />
molti altri prodotti)<br />
2)gozzo sporadico (non si conosce la causa)<br />
scaricato da www.sunhope.it
3) gozzo disormonogenetico(esiste una catena di enzimi che porta alla produzione<br />
della tireoglobulina e quindi degli ormoni tiroidei e se c’è l’alterazione di uno di<br />
questi enzimi si ha un accumulo di precursori degli ormoni e quindi una mancata<br />
funzione della ghiandola.C’è inoltre un ingrossamento della tiroide,perché esiste un<br />
meccanismo di feedback,per cui se gli ormoni non vengono prodotti il TSH aumenta<br />
e si forma il gozzo).<br />
Il gozzo può apparire:<br />
1) parenchimatoso-diffuso,con aspetto carnoso,diffuso e quindi non ha aspetti<br />
cistici o nodulari.C’è un’espansione quasi simmetrica di tutto l’organo.<br />
2) colloideo-cistico(molto diffuso) che si manifesta più facilmente durante la pubertà<br />
e la gravidanza.Ha un aspetto prevalentemente cistico,si formano delle grosse cisti<br />
(appaiono traslucide,contengono colloide e sono voluminose) che possono simulare<br />
un nodulo tiroideo.Isotologicamente si vedono delle cisti provocate spesso da un<br />
aumento del TSH,si vedono poi delle gemme,perché dato che c’è un aumento del<br />
TSH si formano dei microfollicoli che poi diventeranno macrofollicoli.Questi<br />
microfollicoli erano detti cuscinetti o noduli di Sanderson ?(non si capisce bene il<br />
nome).<br />
3) multinodulare,che è la forma più comune.E’fatto da noduli, a volte cistici a volte<br />
carnosi e nelle femmine è più frequente.Tutta la tiroide si trasforma in noduli.Alla<br />
scintigrafia si osserva un aspetto variabile,perché possono esserci aree<br />
iperfunzionanti e ipofunzionanti; aree ipercaptanti e ipocaptanti;aree<br />
macrofollicolari e aree microfollicolari poveri di colloide;aree di fibrosi,aree<br />
infiammatorie(fenomeni reversibili),perché se si rompe una cisti si ha sempre una<br />
reazione infiammatoria;aree di calcificazione. Questo gozzo,a volte,può essere così<br />
profondo da localizzarsi in sede retrosternale,determinando fenomeni di<br />
compressione sulle strutture del mediastino.In questo caso richide l’intervento<br />
chirurgico al più presto. Nei follicoli c’è poca colloide,perché questa si ritrae con la<br />
formazione di vacuoli periferici e questi sono tutti segni di un’iperfunzione.Ci sono<br />
fenomeni regressivi per fibrosi e fenomeni infiammatori.Possono essere presenti poi<br />
delle formazioni ,delle impronte cristalliformi che in realtà sono dei granulomi<br />
colesterinici che lasciano la loro impronta,perché quando si va a processare il tessuto<br />
si utilizzano dei solventi,come lo xilitolo,per cui questi aghi di colesterolo vanno via e<br />
lasciano la loro impronta.L’aspetto è quello di un vetro spaccato.<br />
scaricato da www.sunhope.it
MALATTIA DI BASEDOW O DI FLAJANI-BASEDOW<br />
Gozzo diffuso e non multi nodulare.Colpisce prevalentemente le femmine ed è<br />
caratterizzata da una classica sintomatologia costituita da<br />
ipertiroidismo,oftalmopatie come l’esoftalmo,a volte diplopia,mixedema pretibiale e<br />
acropatia(dita ippocratiche o a bacchetta di tamburo).Oltre alla presenza di anticorpi<br />
un problema di fondo è la presenza di una grande vascolarizzazione,quindi si tratta di<br />
un gozzo molto vascolarizzato.Questo gozzo poi presenta delle atipie strutturali,in<br />
qualche punto,infatti,alcuni follicoli tendono a formare delle papille,perché c’è una<br />
tale esuberante proliferazione,che all’interno dei follicoli si formano come delle<br />
papille aggettanti nel lume,fatte proprio da cellule tiroidee.Ci sono,inoltre,atipie<br />
citologiche focali,non diffuse,che fanno sì che la malattia di Basedow sia una<br />
patologia che aumenta il rischio di sviluppare il carcinoma papillifero,che<br />
rappresenta un’evoluzione di questa malattia nel 2-15 % dei casi oppure può<br />
rappresentare l’evoluzione di una tiroidite di Hashimoto o di un’Hashitossicosi(misto<br />
tra Hashimoto e tireotossicosi,perché la tiroidite è un’iperfunzione notevole della<br />
tiroide che arriva fino alla tossicosi come nella malattia di Basedow). Si osserva<br />
quindi un polimorfismo,in quanto ci sono cellule grandi,cellule piccole,cellule di<br />
forma irregolare e distribuzione irregolare della cromatina. Tutto ciò che appare di<br />
colore rosa,rosso o arancione rappresenta i vasi.<br />
GOZZO TOSSICO MULTINODULARE<br />
E’ detto anche morbo di Plummer a differenza di quanto dicono molti testi che<br />
definisocno morbo di Plummer l’adenoma iperfunzionante.La caratteristica rispetto<br />
al basedow è proprio la presenza di più noduli.Alcuni di questi hanno le stesse<br />
caratteristiche di quelli del Basedow,come la presenza di papille che sporgono nel<br />
lume,la ricca vascolarizzazione,però particolare è l’alternanza di questi noduli che<br />
somigliano a quelli del Basedow con noduli di altra natura,come colloideo-cistico o<br />
normofollicolare.Anche in questo caso si osserva il fenomeno della retrazione della<br />
colloide a contatto con i tireociti,caratteristica delle tiroidi iperfunzionanti.<br />
TIROIDITE DI HASHIMOTO<br />
In almeno il 50 % dei casi presenta un aspetto nodulare,creando a livello ecografico<br />
molti problemi di diagnosi differenziale,perché nelle fasi iniziali è caratterizzata da<br />
un’iperfunzione quasi reattiva e poi da un’ipofunzione per distruzione della<br />
ghiandola.Questa patologia ha un alto rischio di svilupparsi in linfoma e la tiroide<br />
scaricato da www.sunhope.it
costituisce la sede più frequente di linfoma extralinfoghiandolari.L’80 % dei linfomi è<br />
di tipo non Hodgkin.Questa patologia può anche favorire la comparsa di carcinomi<br />
papilliferi,carcinoma papillifero follicolare e di altri tipi di cancro della tiroide.Ha due<br />
aspetti caratteristici: la presenza di follicoli linfatici,come quelli presenti nei linfonodi<br />
secondari ,cioè che hanno un centro germinativo e poi la presenza di cellule<br />
ossifile,ovvero con un citoplasma acidofilo molto abbondante che rappresentano i<br />
tireociti esauriti.Alla ricerca degli autoanticorpi con tecniche di immunofluorescenza<br />
si trovano anticorpi antitireoperossidasi e antitireoglobulina direttamente sui<br />
tessuti.Immunofluorescenza: all’anticorpo si lega una sostanza fluorescinata e la<br />
visione avviene in campo oscuro,perché le sostanze fluorescenti quando sono<br />
eccitate da un raggio di luce monocromatica blu(LUCE INCIDENTE) emettono poi un<br />
raggio di luce verde di differente lunghezza d’onda.Quste cellule ossifile hanno un<br />
citoplasma molto grande,un nucleo piccolo e spesso hanno anche un nucleolo,che è<br />
di colore rosso ciliegia.<br />
TIROIDITE DI DE QUERVAIN<br />
E’ una tiroidite granulomatosa in cui entrano in gioco vari virus.Colpisce<br />
maggiormente i maschi.Ha tutti i segni dell’infiammazione e in genere non ha<br />
un’evoluzione maligna come la tiroidite di Hashimoto.Vedendo il quadro morfologico<br />
si osservano cellule plurinucleate,per granuloma intendiamo una lesione costituita<br />
da macrofagi e linfociti,ma soprattutto da macrofagi plurinucleati.Esistono in<br />
anatomia patologica due tipi di cellule giganti plurinucleate e sono quelle da corpi<br />
estranei in cui i nuclei si ammassano al centro,come in questo caso e la cellula<br />
giganta tipo Langherans,che si ritrovano nella tubercolosi,in cui i nuclei vanno alla<br />
periferia del citoplasma,si dispongono a ferro di cavallo.Sono cellule macrofagi che si<br />
fondono a formare un sincizio.<br />
TIROIDITE LIGNEA DI RIEDEL<br />
E’una tiroidite fibrosa che può determinare,esendo una tiroidite infiammatoria ad<br />
evoluzione fibrosa,aderenze,anche tenaci, con i tessuti circostanti causando<br />
difficoltà chirurgiche e comparsa di segni clinici come la dispnea,la disfagia,la paralisi<br />
del ricorrente .E’una fibrosi molto progressiva che porta ad ipotiroidsmo fino a<br />
distruzione della ghiandola,che viene sostituita da tessuto infiammatorio e fibrotico.<br />
RICAPITOLIAMO<br />
scaricato da www.sunhope.it
Ci sono le tiroiditi acute,di cui non abbiamo proprio parlato,perché esse sono quasi<br />
smepre secondarie.Essendo acute vuol dire che predominano i granulociti.Molto<br />
spesso si tratta di un processo secondario,perché c’è un focolaio ascessuale nei<br />
pressi che coinvolge secondariamente la tiroide.<br />
Abbiamo parlato,però,di più delle tiroiditi subacute e croniche,in cui abbiamo<br />
inserito solo queste tiroiditi specifiche che una volta si vedevano molto di più e<br />
prima nei vecchi testi si definivano processi specifici solo la tubercolosi e la<br />
sifilide,perché non si conosceva tutto il resto.<br />
Abbiamo parlato della tiroidite di De Quervain,della tiroidite lignea di Riedel,delle<br />
tiroiditi autoimmunitarie,come quella di Hashimoto,ma ci sono anche altre tiroiditi<br />
autoimmunitarie,come la :<br />
• TIROIDITE LINFOCITARIA CRONICA<br />
E’una tiroidite autoimmune caratterizzata dalla presenza di infiltrati linfocitari diffusi<br />
che non tendono a fare follicoli secondari e soprattutto non tendono a fare i centri<br />
germinativi.<br />
• TIROIDITE SILENTE<br />
E’la tiroidite post-partum,dove è facile trovare una situazione di ipotiroidismo.<br />
• MALATTIA DI BASEDOW,che non è una vera e propria tiroidite,ma riconosce<br />
un meccanismo autoimmune.<br />
Quali sono le principali cause di ipertiroidismo e tireotossicosi:<br />
1) malattia di Basedow<br />
2) malattia di Plummer o gozzo nodulare tossico<br />
3)adenoma tossico<br />
4) alcune tiroiditi che nelle fasi iniziali si presentano con ipertiroidismo(tiroidite di<br />
hashimoto, tiroidite subacuta di de quarvain, tiroidite silente post-partum in cui<br />
questa fase di ipertiroidismo è molto transitoria)<br />
Alla scintigrafia si può osservare un’ipercaptazione nodulare o diffusa,è nodulare<br />
nell’adenoma tossico e nel gozzo multinodulare tossico ,mentre è diffuso nel<br />
Basedow e nelle tiroiditi,perchè in questi casi è coinvolta tutta la tiroide.<br />
scaricato da www.sunhope.it
ADENOMA<br />
TUMORI DELLA TIROIDE<br />
Quando parliamo di adenoma intendiamo un tumore ghiandolare<br />
benigno,delimitato quasi sempre da una capsula,per cui ha margini molto<br />
netti,caratteristica che lo distingue dai tumori maligni che in genere hanno margini<br />
irregolari.Se facciamo l’ecografia di un adenoma è possibile vedere questi margini<br />
netti e se all’ecocolordoppler si osserva che c’è una vascolarizzazione solo periferica<br />
e non anche all’interno questo è un buon segno,però la diagnosi spetta sempre<br />
all’anatomopatologo.L’aspetto dell’adenoma è molto variabile,può essere carnoso,un<br />
po’ fibroso e possono anche esserci aree ricche di colloide,ch appaiono<br />
traslucide.L’adenoma poi può essere di diversi tipi.La forma più comune è la<br />
follicolare e i follicoli possono essere piccoli o grandi.In genere,inoltre,l’adenoma è<br />
ipocaptante,freddo,solo a volte è ipercaptante e quindi caldo.C’è poi l’adenoma<br />
trabecolare,detto così perché le cellule anzicchè formare i follicoli,si dispongono a<br />
formare delle trabecole,delle travate e questa struttura ricorda molto la struttura<br />
embrionale della tiroide,perché all’inizio la tiroide è così.C’è poi l’adenoma<br />
ossifilo,contenente cellule ossifile,aventi un citoplasma acidofilo e che sono cellule<br />
esaurite.Si tratta,però,di un’ossifilia non diffusa,ma granulosa,perchè è come se ci<br />
fosse una polvere all’interno del citoplasma,questo è pulverulento.Queste sono<br />
cellule che hanno esaurito le loro riserve energetiche,tanto che i loro mitocondri non<br />
funzionano più e perdono la loro forma bastoncellare,assumendo quella<br />
sferica,perché la forma sferica non costa niente dal punto di vista energetico.Sono<br />
quindi questi grandi mitocondri sferici la causa dell’ossifilia.<br />
L’adenoma tossico è l’adenoma iperfunzionante per cui la colloide quasi non c’è<br />
più,perché viene trasformata quasi tutta in ormoni tiroidei.Per cui si osservano micro<br />
follicoli poveri di colloide.<br />
TUMORI MALIGNI<br />
Solo il 2% dei tumori tiroidei è rappresentato da tumori maligni e il rapporto M/F è<br />
di 1 a 2,5-3.<br />
Se parliamo di carcinomi 3/4 di questi sono papilliferi,i quali possono manifestarsi<br />
anche in età pediatrica;un 10 % sono follicolari,un 5% midollari(carcinoma delle<br />
cellule C) ,poi meno del 5 % è rappresentato dal carcinoma anaplastico(che è quello<br />
a prognosi peggiore);il 4-5 % è rappresentato dai linfomi ;i sarcomi sono molto<br />
scaricato da www.sunhope.it
ari.Possono poi essere presenti metastasi alla tiroide,si tratta in questo caso di<br />
tumori secondari e i tumori che più facilmente danno metastasi tiroidee sono quello<br />
al polmone,mammella e il carcinoma renale.<br />
CARCINOMA PAPILLIFERO<br />
Ha un aspetto macroscopico ed ecografico molto variabile.<br />
Nella sua forma più caratteristica,quella classica(papillifera),si osservano delle<br />
rugosità e delle papille,che hanno un asse connettivale delimitato da cellule<br />
epiteliali.Questo è il carcinoma papillifero classico.Queste non sempre si<br />
vedono,perché a volte i tagli sono trasversali,ma comunque vedremo un asse<br />
connettivale con intorno le cellule tumorali.E’stato visto però,che non sempre il<br />
carcinoma papillifero è realmente papillifero,ovvero non sempre ha questa struttura<br />
papillare.Esistono,infatti altre forme oltre quella classica.<br />
C’è la variante cistica del carcinoma papillifero,che assume macroscopicamente degli<br />
aspetti cistici e quasto aspetto macroscopico può costituire una trappola,perché può<br />
sembrare inizialmente una banale cisti,una cisti colloidea,ma all’interno c’è come un<br />
settore e questo aspetto cistico del carcinoma può costituire una trappola,perché se<br />
effettuando l’ago-aspirato,che deve essere almeno eco-guidato,esso può apparire<br />
anche come una semplice cisti colloide e non come un carcinoma,in base alla<br />
regione in cui effettuiamo l’aspirazione. Ci sono anche casi in cui il tumore è<br />
intravascolarizzato,ma ci sono molti casi in cui questo non avviene.<br />
Contrariamente a quello che si credeva una volta,cioè che il carcinoma papillifero è<br />
sempre papillifero,si è visto che questo non sempre accade.Ci sono,però, delle<br />
caratteristiche citologiche sempre presenti che consentono di dire se si tratta<br />
realmente di un carcinoma capillifero,per cui queste caratteristiche costituiscono<br />
l’impronta digitale di questo carcinoma :<br />
1)la presenza di una sostanza acidofila nel nucleo(che normalmente è basofilo) ,che<br />
si scoprì essere un’ invaginazione del citoplasma,in quanto alcune cellule del<br />
carcinoma papillifero possono avere il nucleo con un vuoto al centro(come la<br />
caramella polo) in quanto il citoplasma si invagina al suo interno.<br />
2)Un’altra caratteristica peculiare è la distribuzione della cromatina nucleare,che<br />
forma una sorta di scanalature(dette grows in inglese),di sbarrette che vanno da una<br />
parte all’altra dle nucleo.<br />
scaricato da www.sunhope.it
3)l’ultima caratteristica è la presenza di un nucleo otticamente vuoto,detto anche<br />
nucleo vitreo e la membrana che lo circonda appare ispessita come se fosse<br />
disegnata con inchiostro di china.Il termine otticamente vuoto nacque in riferimento<br />
ad un pittore inglese dell’ ‘800 che si era specializzato a dipingere orfanelle;all’epoca<br />
non c’erano le telenovelas e quindi questo pittore si divertiva così e disegnava<br />
queste orfanelle sempre con un occhio che piange e uno senza pupilla.Questi sono<br />
detti gli occhi dell’orfanella Annie,la quale era la primogenita di tutte queste<br />
orfanelle.Ve lo dico,perché se andate in erasmus in Inghilterra fate bella figura.<br />
Quindi se un tumore ha queste tre caratteristiche noi lo dobbiamo sempre chiamare<br />
papillifero.<br />
Quali sono le caratteristiche del carcinoma papillifero: esso tende ad essere<br />
multifocale.E’anche il carcinoma che risente di più di quei problemi ambientali,tant’è<br />
vero che dopo il disastro di Hiroshima e Nagasaki la sua incidenza è aumentata nelle<br />
popolazioni esposte.Secondo alcune indagini epidemiologiche,però,questo non<br />
sarebbe vero.<br />
Questo tumore poi tende a dare metastasi,anche s eil carcinoma è piccolo.Le<br />
metastasi sono soprattutto linfoghiandolari e queste le ritroviamo in circa il 40 % dei<br />
casi,le metastasi ematiche,invece,sono rare e le riscontriamo in meno del 10 % dei<br />
casi.La biologia molecolare ci fa vedere che ci sono mutazioni dei geni<br />
BRAF,RET,RAS,PTC ma nessuno di questi è diagnostico.<br />
Le recidive possono esserci,anche molto tardive,però la mortalità è molto bassa(6,5<br />
%).Per questo Il trattamento di elezione è la lobectomia e non la tiroidectomia<br />
totale,soprattutto in soggetti a basso rischio di età inferiore a 45 anni e senza<br />
metastasi,per evitare di sottoporre il soggetto ad una terapia sostitutiva per tutta la<br />
vita.Se invece l’età è superiore ai 45 anni e ci sono metastasi si effettuano invece la<br />
tiroidectomia,linfoadenectomia e così via.<br />
ALTRE VARIETA’ DEL CARCINOMA PAPILLIFERO<br />
Oltre la forma classica,che è quella papillifera,ci sono:<br />
• la forma cistica,di cui abbiamo già parlato,<br />
• la forma follicolare,che simula il carcinoma follicolare,ma ha l’impronta<br />
digitale del carcinoma capillifero.<br />
scaricato da www.sunhope.it
• la forma meta?oncocitaria,perché anche le cellule tumorali si esauriscono.<br />
• la forma sclerosante diffusa ,questa ci crea dei problemi,perché è così<br />
fibrotica che all’agoaspirato non esce niente<br />
• forma a cellule alte o colonnari,che è una varietà emersa da poco.<br />
Queste sono solo le varietà più frequenti,ma in tutto ce ne sono una ventina.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> patologica prof Di Costanzo<br />
Se vogliamo partire da un campione chirurgico (un exeresi chirurgica) la prima cosa che si fa subito dopo<br />
l'intervento chirurgico è quella di prelevare il campione.<br />
il campione chirurgico lascia in genere la sala operatoria accompagnato da questo foglio di accettazione, di<br />
presentazione, che si presenta come la carta d'identità del campione che è stato prelevato. Questo perché<br />
noi non lavoriamo a diretto contatto con i chirurghi.<br />
Su questo foglio è sempre riportato, oltre alle generalità del paziente, il tipo di esame richiesto, le<br />
generalità del medico che richiedere l’ esame,poiché noi dobbiamo sempre avere la possibilità di richiedere<br />
notizie cliniche. Questo foglio va compilato quindi necessariamente dal chirurgo nel reparto in cui viene<br />
eseguito l'intervento. È altresì riportato in questo foglio il tipo di intervento. Chiediamo in genere l'aspetto<br />
macroscopico della lesione, un orientamento clinico della lesione. Chiediamo una diagnosi clinica. alcune<br />
notizie cliniche sono per noi importantissime e non sempre il medico richiedente le fornisce e noi siamo<br />
costretti a telefonare nei vari reparti per richiedere notizie più specifiche.<br />
Noi lavoriamo fondamentalmente sul tessuto. Voi sapete che la cellula è formata fondamentalmente da<br />
molecole (proteine, glucidi). Le nostre tecniche sono esclusivamente mirate a questi componenti cellulari.<br />
noi dobbiamo così cercare di lavorare sul tessuto disponibile per avere tutte le risposte possibili e<br />
immaginabili . Noi sappiamo che questi componenti cellulari hanno una caratteristica molto importante:<br />
questi costituenti non riescono a vivere una volta che sono stati allontanati dal loro ambiente naturale, la<br />
cellula stessa si distrugge: faccio un esempio, se voi prendete un pezzo di carne lo lasciate all'aria per lungo<br />
tempo dopo qualche giorno la carne chiaramente va in putrefazione, questo perché questo pezzettino di<br />
carne è stato allontanato alla sua fonte di origine. Lo stesso accede ad un pezzo chirurgico, noi riusciamo a<br />
bloccare questi processi di deterioramento con una tecnica che noi chiamiamo fissazione; perché se la<br />
cellula subisce delle variazioni in questo processo, quando andiamo ad allestire e guardare il preparato<br />
questi fenomeni di putrefazione possono essere evidenziati nel vetrino allestito creando problemi di<br />
interpretazione: quanti fenomeni possono presentare dei quadri di necrosi o quadri di alterazioni simili a<br />
quelli provocati dalla non fissazione? Allora noi dobbiamo essere certi che questo periodo di tempo<br />
dall'intervento chirurgico alla fase immediata della fissazione è quantomeno ridotto al massimo ecco<br />
perché in sala operatoria una volta effettuato il prelievo, questo viene immediatamente portato da un<br />
infermiere in un barattolino e viene effettuato il fissaggio, questo per noi è una cosa importantissima,<br />
poiché noi giochiamo con i costituenti cellulari, se una cellula subisce delle variazioni noi le ritroviamo a<br />
livello delle proteine, a livello dei lipidi, e i cambiamenti delle proteine che si possono verificare sono nella<br />
struttura stessa della proteina quindi non la ritroveremo nella struttura secondaria ma in una struttura<br />
primaria, terziaria, per cui non è la stessa proteina che in natura dovremmo trovare. quindi, come capirete<br />
la fissazione per noi è un momento molto importante, esistono moltissime tecniche ognuna delle quali ha<br />
però i suoi pro e i suoi contro.<br />
abbiamo quindi dei fissativi semplici e delle miscele fissatrici.<br />
Semplici possono avere delle caratteristiche particolari, possono essere fissativi coagulanti o non<br />
coagulanti. Fissativi coagulanti possono essere additivi o non additivi un esempio di fissativo coagulante<br />
non additivo è alcol etilico, metlico o l’acetone un esempio di coloranti additivi è l'acido picrico (?) mentre i<br />
fissativi non coagulanti additivi sono la formaldeide (quella che viene usata generalmente da tutti i<br />
laboratori) la glutaraldeide che viene usata nella microscopia elettronica, il tetrossido di osmio. Alla fine poi<br />
ci sono i fissativi non coagulanti non additivi come l'acido acetico. Il termine di coagulanti additivi e non<br />
scaricato da www.sunhope.it
additivi sta ad indicare quello che succede quando il fissativo entra in contatto diretto con il nostro<br />
campione chirurgico. Additivo significa che crea dei rapporti stretti con il tessuto, non additivo significa che<br />
non altera la morfologia, la composizione chimica del nostro tessuto. Uno dei motivi per i quali non sempre<br />
la formalina veniva accettata nei laboratori era perché la formaldeide è fra i coagulanti additivi cioè nel<br />
momento in cui noi fissiamo un campione con formalina, in genere viene usata la formalina al 10%, la<br />
formalina crea dei ponti metilici con il tessuto e nel momento in cui noi andavamo a fare le indagini mirate<br />
come la immunoistochimica avevamo dei falsi positivi o dei falsi negativi, si è ovviato a questo problema<br />
applicando delle metodiche che rompevano questi ponti metilici: la pentola a pressione o il forno a<br />
microonde, entrambe queste metodiche applicando una forte energia cinetica al preparato rompono i<br />
ponti metilici.<br />
esiste anche un altro sistema per fissare: le miscele fissatrici e non sono altro che un insieme di tutte le<br />
sostanze di cui abbiamo parlato prima, queste vengono usate in genere nella citologia e esfoliativa .quando<br />
l'operatore allestisce il preparato citologico le cellule vengono strisciate oppure deposte sul vetrino e subito<br />
dopo, immediatamente spruzziamo sul vetrino questo spray quando ancora la cellula e viva, viene<br />
trasportata sul vetrino e oltre essere fissata viene anche bloccato sul vetrino stesso in modo che quando<br />
eseguiremo le altre tecniche di colorazione, la cellula stessa non possa subire i vari cambiamenti di stato<br />
dell'ambiente stesso e non possa più staccarsi dalla vetrino.<br />
una volta che arriva il nostro campione e nel laboratorio, inizia il nostro lavoro.partiamo dall'esempio del<br />
semplice campione chirurgico.il campione viene messo in un contenitore pieno di liquido fissativo per<br />
bloccare tutti processi degenerativi del campione stesso e viene portato in anatomia patologica dopo che il<br />
medico stesso ha completato la scheda di presentazione. Il liquido di fissazione a un tempo di fissazione,<br />
perché il liquido deve penetrare all'interno del campione e chiaramente la velocità del liquido è<br />
direttamente proporzionale non solo alla taglia del tessuto ma anche alla compostezza del tessuto stesso.<br />
Poiché questi passaggi si effettuano per processi di diffusione in fase liquida, se un tessuto è costituito da<br />
un connettivo lasso la velocità del campione (quindi del liquido) va a rilento rispetto a un tessuto più duro;<br />
se poi addirittura abbiamo a che fare con un frammento di osso, non riusciremo mai a fissarlo ma<br />
dobbiamo fare un altro procedimento, e quindi una decalcificazione cioè dal tessuto osseo allontaniamo i<br />
sali di calcio che il tessuto stesso racchiude, dopodiché potremo fare la fissazione, l'osso è l'unico tessuto<br />
che non va fissato prima di essere decalcificato. Una volta che l'abbiamo decalcificato il tessuto diventa<br />
morbido e viene trattato regolarmente come tutti gli altri tessuti.<br />
quindi, dopo aver effettuato l'accettazione in anatomia patologica, confrontiamo i dati delle schede che<br />
sono pervenute con i campioni stessi e diamo ad ogni campione un numero, il numero di protocollo. da<br />
questo momento in poi il nostro campione viaggia con il numero di protocollo, non sarà più accompagnato<br />
né dal nome del paziente né dalla sede del prelievo. La lavorazione del campione da parte<br />
dell'anatomopatologo inizia con una prima descrizione macroscopica di quello che è arrivato, descriviamo<br />
l'organo la lesione il colore le dimensioni di quello che vediamo e subito dopo facciamo dei prelievi, questi<br />
prelievi vengono effettuati nell’area sospetta perché noi vogliamo sapere che cos'è quell'area che non è<br />
una struttura chiara che non è, almeno macroscopicamente ben definita. Una volta fatti questi campioni in<br />
base ai protocolli che usiamo, questi campioni vengono inseriti in queste cellette(immagine) che sono<br />
bucate, queste cellette si chiudono e a lato di queste cellette c'è una scalanatura dove viene inserito il<br />
numero di protocollo. Questo campione che ha le dimensioni di 3 cm per 2 cm e lo spessore di massimo 5<br />
mm viene sistemato in questa celletta. Capirete quindi che se oggi nel nostro laboratorio sono arrivate due<br />
mammelle con il nostro numero di protocollo noi le abbiamo separate; ogni mammella cammina con il suo<br />
numero di protocollo. Quando andiamo a fare prelievi ogni celletta cammina con il suo numero di<br />
scaricato da www.sunhope.it
protocollo questo per non confondere i vari campioni. una volta che ho messo questi campioni in queste<br />
cellette questo materiale deve seguire una serie di processi, appunto, una processazione per disidratare il<br />
campione perché così com'è il campione è fissato, ma così com'è io non posso vedere al microscopio, devo<br />
dare un colore al campione, per arrivare a questo stadio io faccio una serie di pro cessazioni che mi<br />
portano a colorare il mio campione, e allora questo campione cosa fa? Viene immerso in una serie di alcol a<br />
concentrazione crescente, quindi passa dalla formalina ad una serie di alcol a concentrazione crescente<br />
dopodiché il campione va in paraffina. facendo passare questo campione in questa serie di alcol ho estratto<br />
tutta l'acqua che è racchiusa nel campione e al posto dell'acqua alla fine di questo processo includo il<br />
campione in un'altra sostanza che si chiama paraffina. La paraffina si trova allo stadio liquido in un range di<br />
temperature dai 55 a 65° centigradi, allo stato solido alla temperatura ambiente, nella paraffina, in questo<br />
modo, il tessuto viene praticamente intrappolato, immobilizzato. questo procedimento mi permette di<br />
rendere il campione rigido sì da essere pronto per il taglio, questo è il processatore (immagine) prima<br />
questi passaggi venivano fatti a mano oggi invece sono effettuati da una macchina che tramite l'esecuzione<br />
di un ciclo di passaggi del campione all'interno dei vari contenitori all'interno dei quali c'è un liquido fino ad<br />
immergere il tessuto in paraffina calda, ecco perché quando noi immergiamo nella paraffina calda un<br />
tessuto, se il tessuto è costituito da grasso, questa paraffina calda scioglie i grassi e si va ad inserire dove<br />
prima c'era la molecola del colesterolo, del grasso. ecco perché noi vediamo delle immagini, nei tessuti che<br />
contengono grassi (gli aghi vuoti nella tiroide), vediamo dei vuoti perché lì magari c'era del colesterolo, un<br />
grasso, e durante il processo di allestimento del preparato questo grasso si è sciolto, e ha dato spazio alla<br />
paraffina. per cui quando andremo a colorare quello spazio rimarrà vuoto, per cui se andremo a colorare un<br />
frammento di tessuto mammario noi troveremo degli adipociti completamente vuoti.<br />
Minuti senza microfono…<br />
tutto questo processo è necessario poiché quando il paziente non è sicuro, convinto della diagnosi e vuole<br />
consultare un altro anatomopatologo il paziente ha diritto di venire in istituto e richiedere i preparati e le<br />
inclusioni oppure può richiedere direttamente i vetrini.un'altra cosa importante è che questo materiale può<br />
rimanere così inalterato per diversi anni.<br />
Gli Istologi che ci hanno preceduto inserivano il campione o in una patata o in un pezzo di legno, poi con un<br />
coltello tagliavano la fetta è poi la coloravano. noi, con i moderni sistemi, analizziamo delle fette di<br />
preparato dallo spessore di pochi micron.<br />
dopo aver fatto queste operazioni questo blocchetto può essere conservato, mentre i i vetrini perdono di<br />
qualità nel tempo poiché i coloranti decadono. i preparati in paraffina restano intatti poiché la paraffina in<br />
trappola benissimo il tessuto. a questo punto l'inclusione viene portata al microtomo dove avviene il taglio<br />
della fetta regolando lo spessore desiderato da 10 ad 1 micron, queste fette vengono poste su un vetrino e<br />
il vetrino va alla colorazione perché così com'è la fretta che noi abbiamo tagliato è una fetta di tessuto<br />
racchiuso in paraffina, la paraffina è bianca e non è quindi assolutamente leggibile al microscopio quindi noi<br />
dobbiamo andare per forza alla colorazione. bisogna colorare ogni tipo di campione sia citologico sia<br />
istologico sia estemporaneo. Nel caso di una estemporanea si usa un particolare apparecchio: il chirurgo<br />
taglia un piccolo frammento di tessuto questo non viene fissato poiché il lasso di tempo dall'analisi deve<br />
essere brevissimo, l'infermiere raggiunge con il campione il nostro istituto l'apparecchio è sempre in<br />
funzione, è un congelatore, una volta che arriva il campione, lo inseriamo in questo congelatore e il<br />
campione si congela , una volta congelato si taglia a fettine questa volta senza usare la paraffina; il fissativo<br />
questa volta sarà il freddo, il campione si taglia facilmente poiché congelato e subito si va alla colorazione.<br />
scaricato da www.sunhope.it
chiaramente in questo caso i tempi saranno molto ridotti e quindi l'anatomopatologo potrà dare risposta in<br />
un tempo piuttosto limitato ovvero in cinque o sei minuti<br />
Le colorazioni sono quelle che più caratterizzano tutto questo processo. esistono delle colorazione fisiche,<br />
chimiche, chimico‐fisiche. riguardo Le colorazioni chimiche, noi usiamo dei reagenti di che in base alle leggi<br />
chimiche interagiscono direttamente con il substrato e danno una colorazione visibile al microscopio.<br />
esistono delle colorazione fisiche dove i coloranti per leggi fisiche vanno ad incunearsi nei tessuti per<br />
diffusione diretta entrano nel tessuto e danno la colorabilità al tessuto stesso. Ci sono poi delle colorazioni<br />
chimico‐fisiche dove vengono associati i due metodi. in genere in anatomia patologica esistono degli<br />
apparecchi specifici che effettuano la colorazione: i coloratori automatici.<br />
quello che a noi interessa è sapere quali sono le colorazioni che facciamo in anatomia patologica, abbiamo<br />
delle colorazioni morfologiche, abbiamo delle colorazioni istochimiche abbiamo delle colorazioni<br />
immunoistochimiche. l'anatomopatologo in genere fa la sua diagnosi con una colorazione morfologica cioè<br />
la ematossilina Eosina. l' ematossilina Eosina sono due coloranti , è una colorazione semplice in quanto i<br />
due coloranti colorano ognuno un solo costituente: uno il nucleo è uno il citoplasma, con due colorazioni<br />
differenti una blu scuro è un'altra violetto. esistono quindi coloranti acidi e coloranti basici a seconda della<br />
reazione che il colorante fa con il substrato noi possiamo avere delle reazioni chimiche per avere il colore.<br />
Noi useremo l'ematossilina che è un colorante naturale e basico per colorare il nucleo in blu, lega le<br />
strutture del nucleo poiché la ematossilina tramite una reazione di ossido riduzione lega substrati acidi, di<br />
rimando il citoplasma che è basico viene colorato con l'Eosina che è un colorante acido quindi noi avremo<br />
due colorazioni il citoplasma in rosa e il nucleo in blu. i contorni saranno abbastanza evidenti.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA 02/11/2010<br />
Il carcinoma follicolare è un carcinoma che ci pone tutta una serie di problemi seri, innanzitutto<br />
in rapporto alla diagnosi differenziale con l'adenoma follicolare.<br />
Come si fa una diagnosi differenziale tra adenoma e carcinoma follicolare?<br />
Ci possiamo fidare delle atipie citologiche, ci possiamo fidare dell'architettura, perchè in<br />
generale il carcinoma ha sempre delle atipie, dei disordini dell'istologia maggiori rispetto<br />
all'adenoma, tranne che in questo caso.<br />
Se devo fare una diagnosi differenziale tra adenoma e carcinoma follicolare, mi trovo in grande<br />
difficoltà perchè non mi posso fidare né delle atipie citologiche né delle atipie citologiche.<br />
Quali sono i 2 parametri di cui mi devo fidare? Sono 2 parametri molto semplici che valgono<br />
per tutti i cancri, non solo per questo caso, ma che però in questo caso assumono valore<br />
assoluto perchè la citologia e l'istologia non hanno un gran valore.<br />
I 2 parametri sono:<br />
1) l'invasione della capsula cioè io devo trovare l'espressione più evidente della malignità per<br />
dire che è un carcinoma e non un adenoma. In genere intorno all'adenoma e al carcinoma<br />
follicolare c'è una capsula fibrosa, se questa capsula è invasa io potrò dire che questo non è<br />
un comportamento da adenoma cioè da tumore benigno, ma sarà un comportamento<br />
biologico da tumore maligno.<br />
L'invasione della capsula può essere di 2 tipi:<br />
a) microinvasivo, quando vediamo un gettone chiaramente invasivo nella capsula<br />
b) macroinvasivo o ampiamente invasivo<br />
Perchè facciamo questa distinzione? Perchè la prognosi è molto diversa cioè se l'invasività<br />
della capsula è più massiccia, più evidente, allora diremo che è ampiamente invasivo ed ha<br />
una prognosi molto peggiore rispetto a quello microinvasivo.<br />
2) il secondo carattere di malignità accertato è la presenza di emboli neoplastici cioè trovare<br />
cellule tumorali all'interno dei vasi è un chiaro segno di malignità<br />
Quindi i 2 caratteri sono: invasività capsulare e l'angioinvasività.<br />
Questo che vi dico sembra molto elementare, ed invece è molto difficile trovarlo perchè dovete<br />
considerare il tutto in una dimensione spaziale (nelle 3 dimensioni), cioè non è che faccio una<br />
sezione del nodulo di 2-3 cm, non trovo né l'uno né l'altro e posso essere sicuro che non c'è né<br />
invasività capsulare né altra invasività.<br />
In questi casi dobbiamo fare un lavoro da fare di campionamento, per cui la diagnosi di<br />
adenoma si fa per esclusione cioè quando non troviamo invasività capsulare e quando non<br />
troviamo emboli neoplastici. Ovviamente questo implica un lavoro enorme per cui bisogna<br />
tagliare, bisogna fare vari vetrini, un lavoraccio.<br />
Com'è fatto un carcinoma follicolare? In effetti ha una dimensione follicolare come ce l'ha<br />
l'adenoma follicolare, ma non è un carcinoma papillifero cioè la variante follicolare del<br />
carcinoma papillare perchè ci manca l'imprint cioè quelle impronte citologiche di cui abbiamo<br />
parlato (le scanalature, i pseudo-inclusi nucleari, l'aspetto dell'orfanella Annie ecc.) e quindi<br />
diciamo carcinoma follicolare in questi casi.<br />
C'è da dire che il carcinoma follicolare è molto meno frequente del carcinoma papillifero e c'è<br />
da dire che c'è un rapporto in genere 1:9 tra carcinoma e adenoma cioè fatte 10 lesioni<br />
follicolari, uno solo è carcinoma e 9 sono adenomi; però non ci possiamo fidare delle statistiche<br />
ma dobbiamo studiarlo lo stesso per poterlo escludere.<br />
Bisogna stare attenti alla falsa invasione capsulare perchè alla periferia di un adenoma, per<br />
compressione, ci possono stare dei fenomeni di necrosi e dei fenomeni di fibrosi per cui dei<br />
gettoni di tessuto adenomatoso rimangono intrappolati all'interno di questo tessuto fibroso e<br />
sembra quasi un'invasione ma non lo è. Ci sono dei criteri ben stabiliti per distinguere la vera<br />
dalla falsa invasione,ma non ve li dico.<br />
scaricato da www.sunhope.it
Tra le lesioni c'è anche il carcinoma follicolare ossifilo, che si caratterizza perchè le cellule<br />
hanno; nucleo piccolo e nucleolato, ampio citoplasma granuloso ossifilo.<br />
Perchè ci sforziamo molto per distinguere un carcinoma follicolare da un carcinoma papillifero?<br />
Perchè hanno una storia naturale molto diversa.<br />
CARCINOMA FOLLICOLARE<br />
1) localmente poco invasivo, spesso capsulato<br />
2) raramente da metastasi linfoghiandolari, a differenza del carcinoma papillifero che da<br />
metastasi da cancro occulto cioè possiamo trovare metastasi nei linfonodi e non trovare<br />
invece il cancro perchè è molto piccolo<br />
3) può dare metastasi ematiche che arrivano in particolare alle ossa e al polmone<br />
4) possiamo trovare mutazioni del gene RAS e la formazione di geni anomali dati dalla fusione<br />
del gene PAX 8 con il PPAR-γ (non sempre si verificano queste mutazioni)<br />
5) la mortalità è: del 3% quando c'è un'invasione minima<br />
del 32% per le forme estensivamente invasive<br />
6) le recidive sono frequenti nelle forme ad alta invasività<br />
Da questo deriva un trattamento terapeutico diverso.<br />
C'è un concetto molto importante che recentemente è emerso e cioè l'età come fattore<br />
prognostico; è molto importante l'età come fattore prognostico soprattutto scegliendo come<br />
cut off il limite dei 45 anni.<br />
Quando il carcinoma follicolare e quello papillare insorgono sotto i 45 anni di età hanno una<br />
prognosi migliore rispetto ai carcinomi che insorgono in soggetti che hanno più di 45 anni di<br />
età.<br />
L'emitiroidectomia o la lobectomia sono indicate per i pazienti a basso rischio cioè che hanno<br />
invasività minima, assenza di metastasi a distanza, età superiore ai 45 anni, dimensione del<br />
carcinoma inferiore a 3.5 cm. Se ha queste caratteristiche si può essere ottimisti.<br />
Nei casi in cui i pazienti sono ad alto rischio cioè che hanno invasività più ampia, età superiore<br />
ai 45 anni ecc, si deve eseguire tiroidectomia completa con o senza radioterapia poi<br />
eventualmente anche linfoadenectomia a seconda dei protocolli e dalle varie capacità di<br />
metastatizzazione che ha ogni singolo caso.<br />
Tra i marcatori genetici e molecolari del carcinoma papillare, ce ne stanno alcuni che sono<br />
rappresentati da una particolare proteina di adesione chiamata GALECTINA 3.<br />
La GALECTINA 3 è una molecola che si trova, in genere, tra la cellula epiteliale ed il<br />
mesenchima, quindi corrisponde a quelle che sono le selectine cioè quelle molecole di adesione<br />
legate all'interazione tra stroma e cellula epiteliale. Solitamente la tiroide non esprime o<br />
esprime poco questa galectina 3.<br />
Oltre alla galectina 3 abbiamo la CK 19 (citocheratina 19) che normalmente la tiroide non<br />
esprime ed un particolare CD definito CD 44.<br />
Tra queste proteine la più importante è la galectina 3 che vale sia per il carcinoma papillifero<br />
sia per il carcinoma follicolare.<br />
CARCINOMA MIDOLLARE<br />
Il carcinoma midollare è il carcinoma che appartiene al sistema neuro-endocrino perchè queste<br />
cellule C fanno parte del sistema neuro-endocrino diffuso e sono le cellule che producono la<br />
calcitonina.<br />
E' un carcinoma che ha un'aggressività maggiore, vedete che sono noduli grigio-giallastri<br />
localizzati solitamente nella parte superiore dei lobi tiroidei dove le cellule C sono in numero<br />
maggiore.<br />
In questo caso i marcatori sono attendibili perchè c'è la calcitonina, ma comunque sono<br />
attendibili anche tutti i marcatori della serie neuro-endocrina di cui parleremo più avanti.<br />
Questo carcinoma midollare ha un quadro morfologico molto variabile.<br />
scaricato da www.sunhope.it
Le caratteristiche comuni sono che produce calcitonina e tutti quei marcatori della serie neuroendocrina,<br />
oltre al TTF-1 che è un marcatore sia della tiroide sia del polmone.<br />
La sopravvivenza dopo tiroidectomia arriva soltanto al 2% quindi ha una mortalità molto<br />
maggiore rispetto ai carcinomi papillare e follicolare, inoltre in questo tipo di cancro la<br />
radioterapia è inutile.<br />
Molto spesso, poiché c'è un rapido accrescimento, è caratterizzato da tutta una serie di sintomi<br />
clinici, come: la disfonia, la raucedine, anche sintomi legati ai neuro-ormoni e quindi diarrea (la<br />
diarrea è un sintomo caratteristico soprattutto legato a particolari amine biogene), alti livelli di<br />
CEA e di calcitonina a livello sierologico, caratterizzano questo tumore.<br />
Il carcinoma midollare può essere presente anche in certe sindromi endocrine complesse come<br />
le sindromi MEN, più precisamente in particolari sottotipi di sindromi MEN.<br />
Ci sono dei casi, in particolare della sindrome MEN-IIB, dove la tiroidectomia la si può fare per<br />
profilassi perchè è così frequente in questi soggetti il carcinoma midollare che conviene togliere<br />
la tiroide prima che si sviluppi il cancro.<br />
La mortalità di queste sindromi ed in genere il carcinoma midollare è abbastanza elevata,<br />
vedete che a 15 anni di follow-up solo il 40% sopravvive.<br />
Questo carcinoma lo si pensa ogni qual volta non risponde né al carcinoma follicolare né al<br />
carcinoma papillifero, quindi è quasi una diagnosi ad esclusione anche se però fortunatamente<br />
abbiamo come marcatore la calcitonina (c'è poi un vecchio colorante che marca l'amiloide che<br />
si chiama rosso Congo che però non si usa più).<br />
Cos'è l'amilode? E' una sostanza molto complessa, eterogenea, molto spesso fatta da Ig o da<br />
frazioni di Ig.<br />
CARCINOMA INSULARE o POCO DIFFERENZIATO<br />
Questo carcinoma fu identificato da un italiano, il prof. Zampi di Firenze, che lo definì insulare<br />
perchè è fatto da insule l'architettura in genere è solida.<br />
Questo cancro:<br />
- è fatto da inslule e l'architettura è in genere solida<br />
- tende ad estendersi oltre i confini tiroidei nel 59% dei casi<br />
- tende a dare metastasi linfoghiandolari fino al 40% dei casi<br />
ematiche fino al 44% dei casi<br />
- la recidiva è prevista nel 63% dei casi<br />
- ha una mortalità del 27% dei casi, quindi è un cancro abbastanza aggressivo rispetto al<br />
follicolare e al papillifero<br />
- la tiroidectomia e la radioterapia sono indicate in questo caso.<br />
Essendo un cancro aggressivo si fa la radioterapia per campi perchè è probabile che abbia<br />
avuto un'estensione extratiroidea.<br />
Sulla chemioterapia ci sono dubbi.<br />
CARCINOMA ANAPLASTICO<br />
Il carcinoma anaplastico ha una incidenza, rispetto a tutti i tumori maligni della tiroide, del<br />
2-5%.<br />
Come dice il nome, può assumere degli aspetti veramente abnormi, addirittura può assumere<br />
questo aspetto a cellule giganti.<br />
Questi tipi di tumori a cellule giganti che somigliano agli osteoclasti, secondo la dizione inglese<br />
si chiamano osteoclastic malign tumor, sono altamente maligni.<br />
Questo cancro raggiunge la più bassa sopravvivenza cioè a 5 anni nel 3-10% dei casi.<br />
Probabilmente è il cancro più maligno della tiroide.<br />
Poiché ha una crescita molto rapida, ovviamente presenta quei segni legati a questo rapido<br />
accrescimento e cioè: dispnea, disfagia, coinvolgimento del nervo ricorrente.<br />
scaricato da www.sunhope.it
RIEPILOGO<br />
Tra i tumori benigni abbiamo l'adenoma che può avere:<br />
1) forma microfollicolare (è la forma classica) e può essere freddo o caldo, molto spesso è<br />
freddo<br />
2) forma trabecolare, che ricorda un po' la tiroide nel periodo embrionale perchè in questo<br />
periodo ci sono trabecole e non follicoli<br />
3) forma ossifila<br />
Per quanto riguarda i carcinomi, distinguiamo:<br />
1) il papillifero<br />
2) il follicolare<br />
3) il midollare<br />
4) lo scarsamente differenziato o insulare<br />
5) l'anaplastico<br />
6) altri tipi<br />
N.B. La tiroide è una delle sedi dove sono più frequenti i linfomi extra-linfoghiandolari, ne<br />
abbiamo parlato a proposito delle tiroiditi<br />
ALTRI TUMORI<br />
I più importanti sono:<br />
1) tumori di collisione, si chiamano così quei tumori che hanno una doppia componente, in<br />
questo caso: follicolare/midollare; papillare/midollare. Quindi che sono fatti da cellule C e da<br />
tireociti anaplastici; tutto questo ce lo possiamo spiegare ricorrendo ad un problema di un<br />
origine da cellule staminali, queste cellule staminali impazzite a volte fanno una cosa, a<br />
volte fanno un'altra cosa, dipende anche dai segnali che hanno in quell'ambiente così<br />
possiamo avere il carcinoma follicolare/midollare<br />
2) linfomi, che appartengono a particolari tipi di linfomi di cui non parliamo adesso<br />
3) tumori mesenchimali (fibromi, teratomi, sarcomi, ecc.)<br />
4) una caratteristica strana che ha la tiroide è che in una minoranza di casi può fare dei tumori<br />
tipici delle ghiandole salivari (parotide, sottomandibolare) che sono particolari e di cui<br />
parleremo in seguito. Perchè ci sia questa incidenza, anche se bassa, di tumori di tipo<br />
salivare della tiroide è oggetto di molte interpretazioni; si può trattare in un'eterotopia o di<br />
un problema embrionale perchè la parotide non è molto distante dalla tiroide, quindi<br />
durante tutte quelle complesse migrazioni può succedere qualche disguido<br />
5) altri tipi di tumori di cui non parliamo<br />
STADIAZIONE CARCINOMI FOLLICOLARE E PAPILLARE<br />
Il parametro importante per i carcinomi follicolari e papillari è l'età.<br />
1) Se il carcinoma follicolare o papillare interviene in soggetti con età inferiore a 45 anni,<br />
possono essere solo STADIO I e STADIO II perchè sono considerati sempre a prognosi<br />
relativamente favorevole; addirittura quello che chiamiamo STADIO II per gli altri tumori<br />
corrisponde allo STADIO IV perchè presenta metastasi ad altri organi, polmone ed ossa,<br />
però pur avendo queste metastasi consente una sopravvivenza molto maggiore rispetto agli<br />
altri tipi di cancro.<br />
Lo STADIO I è rappresentato da tutti i tumori di qualsiasi dimensione e/o con metastasi<br />
linfonoghiandolari, ma che non infiltra altri organi.<br />
Lo STADIO II è rappresentato dal tumore che porta metastasi ematiche ad altri organi.<br />
scaricato da www.sunhope.it
L'unico parametro importante per differenziare lo STADIO I e lo STADIO II è la presenza o<br />
meno di metastasi ematiche.<br />
2) Se il carcinoma follicolare e papillare interviene in soggetti con età superiore a 45 anni,<br />
cambia il sistema di stadiazione e questo sistema di stadiazione è adottabile anche per il<br />
carcinoma midollare. In questo caso dobbiamo distinguere STADIO I, II, III, IV.<br />
Lo STADIO I (T1), tumore le cui dimensioni sono < 2 cm.<br />
Lo STADIO II (T2), tumore le cui dimensioni sono comprese tra 2 e 4 cm e che non va fuori<br />
della tiroide.<br />
Lo STADIO III (T3), tumore le cui dimensioni sono > 4 cm e/o esteso ad organi e linfonodi<br />
adiacenti.<br />
Lo STADIO IV si suddivide in diversi sottostadi:<br />
- STADIO IVa (T4a), quando abbiamo invasione dei tessuti adiacenti del collo (soprattutto<br />
muscoli, nervi) e/o linfonodi del collo e torace superiore<br />
- STADIO IVb (T4b), quando abbiamo invasione dei tessuti del collo adiacenti a colonna<br />
vertebrale e torace superiore<br />
- STADIO IVc (T4c), quando abbiamo invasione a distanza di altri organi ad esempio il<br />
polmone, che non sta vicino alla tiroide<br />
Il carcinoma anaplastico ha la stadiazione più semplice.<br />
Qualunque sia la sua presentazione clinica e la sua stadiazione, il carcinoma anaplastico è<br />
sempre STADIO IV, che si suddivide in 2 sottostadi:<br />
- IVa, quando è confinato alla tiroide ed è asportabile chirurgicamente<br />
- IVb, quando è extratiroideo e non è asportabile chirurgicamente<br />
Sia il IVa sia il IVb hanno una prognosi negativa.<br />
Questa modello di stadiazione è diverso da quello precedente per due caratteristiche:<br />
1) l'età<br />
2) la differenza in rapporto ai distrofismi<br />
NODULI<br />
Alcuni clinici sono ottimisti quando il nodulo scintigraficamente è caldo cioè quando è captante,<br />
ma in realtà sbagliano.<br />
Il nodulo tiroideo riguarda il 4-10% della popolazione, quindi lo vedrete sicuramente.<br />
Il nodulo freddo lo ritroviamo in genere nell'85% dei casi e l'incidenza del cancro rispetto ad<br />
una lesione neoplastica benigna non neoplastica è 1:6.5 cioè vi è un caso ogni 6.5 casi pari ad<br />
un'incidenza del 12% circa.<br />
Il nodulo caldo lo ritroviamo in genere nel 5% dei casi e l'incidenza del cancro rispetto alle<br />
altre forme è 1:6.5 cioè vi è un caso ogni 6.5 pari ad un'incidenza dello 0.75%.<br />
Il nodulo caldo incide meno perche ci sono meno casi, però il rapporto tra nodulo caldo<br />
normale e nodulo caldo maligno è sempre 1:6.5<br />
Il nodulo cosiddetto tiepido lo ritroviamo in genere nel 10% dei casi e ha un rapporto 1:10.<br />
In teoria questo paradosso del nodulo caldo nasce dal fatto che i noduli caldi sono di meno di<br />
quelli freddi statisticamente; per cui se andiamo a fare in valore assoluto: il 12% dei cancri è<br />
freddo e lo 0.75% è caldo, ma questo dipende solo dall'incidenza più bassa dei noduli caldi<br />
rispetto ai noduli freddi.<br />
scaricato da www.sunhope.it
Tabella noduli<br />
INCIDENZA N. CANCRI % CANCRO<br />
FREDDO 85% 1:6.5 12%<br />
TIEPIDO 10% 1:10 1%<br />
CALDO 5% 1:6.5 0.75%<br />
CITOLOGIA ASPIRATIVA<br />
Perchè vi parlo della citologia, cosa che negli altri tumori faremo di meno? Perchè nel caso<br />
della tiroide assume una dimensione clinica notevole.<br />
Si può utilizzare:<br />
- la tecnica di striscio su vetrino cioè si usa una siringa con la quale si aspira dal nodulo, si<br />
striscia sul vetrino, si fissa il vetrino, si colora e poi si va a vedere.<br />
- la citologia per strato sottile (Thin prep) ha un grande vantaggio perchè quando io faccio il<br />
prelievo semplice con la siringa, insieme alle cellule viene molto sangue.<br />
Se invece faccio la citologia per strato sottile io non devo liberare l'ago di quanto contiene o la<br />
siringa perchè tutto viene messo in una provetta che sarà citocentrifugata, il sangue viene<br />
emolizzato e solo la parte centrale del vetrino mostrerà le cellule.<br />
In questo modo si risparmia tempo perchè anziché vedere il vetrino in lungo ed in largo in cui<br />
troveremo sempre molto sangue, troviamo solo cellule in un punto centrale<br />
- la tecnica di citoinclusione che è sempre un derivato della citologia per strato sottile perchè<br />
raccogliendo molte cellule noi le possiamo includere in paraffina e tagliare come se fosse<br />
tessuto e poi fare delle metodiche molecolari o immunoistochimiche.<br />
L'ecografia ha un ruolo importante per eseguire l'agoaspirato.<br />
L'agoaspirato deve essere ecoguidato o ecoassistito.<br />
Per esempio questa è la storia di una cisti che sembra un nodulo, quando l'ago penetra dentro<br />
e aspiriamo, la cisti scompare quasi. Anche in questo caso facciamo l'esame di agoaspirato<br />
perchè ci sono dei tumori cistici; se è una cisti troveremo solo tireociti, macrofagi, colloide<br />
perchè le cisti sono ricche di colloide.<br />
SENSIBILITA' E SPECIFICITA'<br />
Quando parliamo di tecniche di citologia ma anche di altre tecniche, tenete in mente che ci<br />
sono 2 rapporti fondamentali e cioè la sensibilità e la specificità.<br />
1) La sensibilità è il rapporto tra veri positivi (VP) e veri positivi più falsi negativi (FN) tutto<br />
moltiplicato per 100. [SENSIBILITA' = VP/VP+FN x 100]<br />
Che cosa significa falsi negativi? Vuol dire che gli ho dato il citologico negativo ma poi di<br />
fatto l'istologia mi ha detto che è positivo. Se i falsi negativi sono uguali a 100 questo<br />
rapporto diventa 1 e quindi abbiamo una sensibilità del 100%.<br />
Quindi sensibilità significa la capacità che ha una metodica di evitare o ridurre i falsi<br />
negativi.<br />
Nella tiroide la sensibilità è dell' 80-93%.<br />
Poniamo il caso che ho una casistica di 100 casi, ho 99 positivi e 1 falso negativo avremo:<br />
99/99+1 x 100 = 99. Più aumentano i falsi negativi e più questo rapporto si abbassa e<br />
questo è un grosso problema per la tiroide perchè è un organo molto vascolarizzato e<br />
perchè molti non sanno fare i prelievi.<br />
2) La specificità è il rapporto tra veri negativi (VN) e veri negativi più falsi positivi (FP) tutto<br />
moltiplicato per 100. [SPECIFICITA' = VN/VN+FP x 100]<br />
scaricato da www.sunhope.it
In questo caso se non ci sono falsi positivi il rapporto sarà uguale a 1 e quindi abbiamo una<br />
specificità del 100%.<br />
Il falso positivo ha delle conseguenze immediate perchè quando abbiamo un caso di cancro<br />
che non era cancro quel paziente è inoperabile.<br />
Anche il falso negativo ha delle conseguenze perchè ritarda il momento terapeutico e quindi<br />
ci possono essere conseguenze sulla vita del paziente.<br />
La specificità per la tiroide si avvicina al 99% e questo vuol dire che se mi trovo di fronte ad<br />
un positivo il rischio è dell'1% e quindi ho 1 probabilità su 100 di sbagliare; se invece mi<br />
trovo di fronte ad un negativo (nel senso che dico una tiroidite, un'iperplasia, un gozzo ecc)<br />
io posso avere dal 7 al 20% di probabilità di sbagliare.<br />
Quindi non c'è una tecnica che non abbia i suoi limiti.<br />
FATTORI CRITICI<br />
1) esperienza dell'operatore<br />
2) caratteristiche del nodulo, in genere il nodulo può essere troppo piccolo o troppo grande e<br />
per questo motivo deve essere ecoguidato perchè può presentare aree di fibrosi, aree di<br />
calcificazione e tutti questi fattori condizionano molto la qualità del campione perchè se<br />
vado a pungere aree di fibrosi o aree di calcificazioni non viene fuori niente, posso aspirare<br />
quanto voglio che tanto non esce fuori niente.<br />
Una volta infilato l'ago, dobbiamo retrarlo un po' e cambiare più volte angolazione (4-5<br />
cambiamenti) così da avere un campionamento più vasto possibile.<br />
3) tecniche di prelievo adoperate:<br />
a) aspirazione o FNA (Fine Needle Aspiration), in genere si usano aghi molto sottili,<br />
numerati da 23-25 con calibro inferiore a 0.5 mm quindi più piccoli della siringa<br />
intramuscolo ed inoltre possono essere anche molto lunghi se si devono raggiungere<br />
organi molto profondi.<br />
La tiroide deve essere aspirata poco perchè è molto vascolarizzata e viene fuori molto<br />
sangue, per questo motivo si deve aspirare poco.<br />
b) FNC (Fine Needle Capillary biopsy)Alcuni hanno sviluppato un'altra tecnica per cui non<br />
utilizzano proprio l'aspirazione ma seguono la capillarità cioè infiggono l'ago un po' alla<br />
volta per cui per capillarità prendono le cellule senza aspirare<br />
c) c'è poi una tecnica mista cioè capillarità più aspirazione<br />
d) LNA (Large Needle Aspiration biopsy) prevede l'uso di aghi con calibro maggiore. Questa<br />
tecnica è utilizzata quando gli agoaspitati sono poco cellulati. E' poco usata<br />
e) CNB (Core Needle Biopsy) prevede l'uso di aghi grandi per poter eseguire la biopsia e<br />
prelevare così "torsoli" di tessuto<br />
Nell'aspirato possiamo:<br />
- non trovare niente e ciò può voler dire che il campione che è stato aspirato è inadeguato,<br />
insufficiente o contiene soltanto materiale ematico e diciamo che non è diagnostico.<br />
Secondo l'OMS si può considerare adeguato un vetrino citologico quando contiene almeno 6<br />
gruppi cellulari, ognuno con almeno 10 tireociti quindi in totale 60 cellule.<br />
Se un preparato citologico ha un numero di cellule inferiore a questo viene considerato<br />
inadeguato o insufficiente<br />
- oppure possiamo trovarci di fronte ad una patologia benigna che può essere un nodulo cistico<br />
(ad esempio una cisti colloide), un'iperplasia nodulare cioè un nodulo iperplastico, una<br />
tiroidite o altre lesioni tiroidee benigne<br />
scaricato da www.sunhope.it
Quando ci troviamo di fronte ad un preparato inadeguato:<br />
- dobbiamo valutare i caratteri del nodulo in quanto può essere inadeguato perchè è un nodulo<br />
fibrotico, calcifico<br />
- possiamo ripetere l'agoaspirato<br />
- possiamo utilizzare aghi più larghi<br />
- possiamo ricorrere alla microbiopsia<br />
- possiamo ricorrere all'escissione o all'esame intraoperatorio (sono traumatici per il paziente)<br />
ma solo nel caso in cui la citologia non dovesse essere risolutiva.<br />
Per l'uso di aghi larghi e di microbiopsia c'è il rischio di disseminazione lungo il tragitto,<br />
mentre per la citologia aspirativa è stato dimostrato che questo rischio non c'è.<br />
Quando si cominciò ad utilizzare la citologia aspirativa ci si chiese: se aspiriamo un cancro, le<br />
cellule maligne si possono diffondere in altri tratti? No, con la citologia questo non accade.<br />
GOZZO<br />
Quando ci troviamo di fronte ad un gozzo nodulare, in linea di massima apparirà colloide e<br />
qualche volta si osserverà qualche tireocita disperso e qualche macrofago e questo è indice di<br />
benignità.<br />
I macrofagi li ritroviamo quasi sempre perchè soprattutto nei gozzi cistici quando la colloide va<br />
fuori, si crea sempre una reazione in cui troviamo linfociti e macrofagi.<br />
Un paziente con un gozzo nodulare ha lo stesso rischio del resto della popolazione di avere un<br />
cancro, non ha un rischio più elevato come invece si pensava in un primo momento.<br />
Inoltre non dobbiamo dimenticare che ci sono delle forme cistiche di cancro per esempio il<br />
carcinoma papillifero in cui dobbiamo stare bene attenti a non andare a pungere la parte<br />
liquida, ma la parte solida cioè quei gettoni che stanno nel lume.<br />
La probabilità di avere una lesione benigna con una sola FNA è pari al 90%, cioè ho il 10% di<br />
possibilità di avere un falso negativo; se ripeto a distanza di tempo l'agoaspirato la possibilità<br />
aumenta e raggiunge quasi il 98%, quindi non ci dobbiamo accontentare di un negativo per<br />
questo lo dobbiamo cercare due volte per avere un livello di accettabilità.<br />
VERI E FALSI NEGATIVI<br />
Le possibili strategie sono la ripetizione dell'agoaspirato determina un aumento della sensibilità<br />
(13.8%) e della specificità (6.2%)<br />
Vi è una zona grigia a livello dei noduli tiroidei che ha 2 facce:<br />
- da una parte abbiamo atipie sospette ma non conclusive cioè vediamo qualcosa ma non è<br />
tutto quindi possiamo emettere solo un sospetto ma non concludere che c'è una lesione<br />
maligna<br />
- dall'altra parte abbiamo lesioni indeterminate o follicolari; per il discorso che abbiamo fatto<br />
prima tra adenoma follicolare e carcinoma follicolare, se io trovo una lesione follicolare posso<br />
stabilire a livello citologico se è un carcinoma o un adenoma? No<br />
Anche nel caso di un adenoma ossifilo e di un carcinoma ossifilo non posso stabilire a livello<br />
citologico se è un carcinoma o un adenoma.<br />
Secondo la casistica aspirativa:<br />
- gli inadeguati rappresentano il 17% dei casi<br />
- il benigno rappresenta più del 60% dei casi<br />
- il maligno 4-14% dei casi<br />
- l'indeterminato 8-33% dei casi<br />
- il sospetto 4-10% dei casi<br />
scaricato da www.sunhope.it
CATEGORIE DIAGNOSTICHE<br />
Le diagnosi di agoaspirato della tiroide sono state classificate in 5 settori:<br />
- THY 1, non diagnostico (quando ci sono poche cellule, quando ci sono degli artefatti)<br />
- THY 2, lesione non neoplastica<br />
- THY 3, lesione follicolare, sospetto tumore follicolare che può corrispondere ad iperplasia<br />
nodulare, ad adenoma o carcinoma follicolare<br />
- THY 4, sospetto ma non conclusione di malignità<br />
- THY 5, lesione sicuramente maligna<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA: lezione del 04/11/10 prof. Rossiello<br />
Allora riprendiamo dall’immagine dell’altra volta. Noi abbiamo due zone grigie: da una parte quelle atipie<br />
citologiche che noi consideriamo sospette ma non conclusive (cioè c’è qualcosa di atipico ma il quadro non<br />
è completo), e poi vi sono le cosiddette lesioni indeterminate, termine che in Italia non piace molto perché<br />
è come se uno il vetrino non lo avesse visto; indeterminato è in effetti sinonimo di lesione follicolare.<br />
Abbiamo visto che per fare una diagnosi differenziale tra adenomi e carcinomi follicolari, così come tra<br />
adenoma ossifilo e carcinoma ossifilo, è necessario cercare dei parametri istologici, cioè di angioinvasività o<br />
di invasività capsulare; ovviamente a livello citologico noi non lo vediamo, né sappiamo che in questo caso,<br />
ai fini della diagnosi differenziale, è utile vedere le atipie cellulari. Infatti, in questo caso, noi possiamo avere<br />
una apparente lesione ben differenziata, che però invade la capsula e invade i vasi, allora il carcinoma<br />
follicolare sarà pure ben differenziato, ma è comunque un carcinoma.<br />
Andiamo avanti. Vi ho già spiegato questa classificazione internazionale sulle varie categorie diagnostiche<br />
della citologia aspirativa della tiroide in cui T5 corrisponde a CAD(?), T1 corrisponde a inadeguato, T2 a<br />
lesione benigna, T3 sono lesioni follicolari, T4: sospetto ma non diagnostico. Quindi T3 e T4 corrispondono<br />
al semaforo giallo.<br />
Come appare una lesione follicolare? Come vedete nell’immagine vi sono piccoli gruppi di cellule, questo è<br />
sangue( perché nella tiroide il sangue non manca mai), colloide ne vedete? No, non ce n’è, in genere queste<br />
lesioni follicolari non hanno molta colloide. Ecco, qui (immagine) possiamo vedere meglio le caratteristiche<br />
citologiche: c’è un po’ di colloide però sta dentro a queste strutture che sono dei piccoli follicoli. Due<br />
caratteristiche ci colpiscono: primo, l’aspetto plurifocale,cioè i nuclei stanno più a livelli focali,tanto è vero<br />
che alcuni nuclei sono sfocati e soprattutto l’aspetto sinciziale, sinciziale vuol dire che i nuclei stanno uno<br />
addosso a un altro per cui non si distinguono chiaramente i contorni cellulari. Quindi, aspetto sinciziale e<br />
plurifocale. Quando ci troviamo di fronte ad una lesione del genere ci dobbiamo fermare e dire “lesione<br />
follicolare”, non posso dire di più. C’è sempre la domanda stupida del chirurgo “ma è benigno o è<br />
maligno?”quasi come se io avessi un servizio segreto di citodiagnostica che mi dice la parola giusta!!<br />
Questa (immagine) è una lesione ossifila. Il citoplasma non appare rosa come siete abituati a vedere perché<br />
questa è un’altra colorazione, diversa da quella a cui siete abituati (è la colorazione di Papanicolau), il<br />
citoplasma è molto granuloso e il nucleo è relativamente piccolo rispetto al citoplasma. Queste sono le<br />
atipie citologiche sospette ma non conclusive. Qua vediamo dei nuclei grandi, qualche aspetto sinciziale,<br />
una distribuzione un poco anomala, diciamo c’è qualcosa che non quadra però non abbiamo proprio i<br />
caratteri della malignità. Cosa possiamo fare in questi casi? I markers immunoistochimici, ma ci vorrebbe un<br />
punto interrogativo perché vi ho detto che la galectina, la citocheratina 19 non hanno un valore assoluto.<br />
Possiamo fare un esame definitivo dopo escissione chirurgica, cioè dire “non ti posso dire più niente adesso,<br />
togli il nodulo, te lo esamino dopo l’intervento chirurgico”; quindi si fa una chiruria in due tempi: primo<br />
tempo si toglie il nodulo e si aspetta la diagnosi conclusiva. Se è un carcinoma follicolare probabilmente<br />
l’intervento si estenderà, se è un adenoma follicolare, l’intervento è risolutivo.<br />
La diagnosi intra-operatoria sta scritto “non valida”. Perché non valida? Perché a livello di estemporanea<br />
non si può fare una valutazione completa di quelli che sono i vasi, di quella che è la capsula; l’estemporanea<br />
è un esame che dura poco, pochi minuti, il paziente sta in sala operatoria, né si può dire al chirurgo io te lo<br />
esamino in toto, rimani in anestesia fino al giorno dopo!!! Ecco perché, in questi casi, l’approccio preferibile<br />
scaricato da www.sunhope.it
è in due tempi. Ecco qua vedete la galectina, la citocheratina3, si può dire che è benigno, però onestamente<br />
è pericolosa questa strada perché la galectina e la citocheratina possono dare dei falsi positivi e dei falsi<br />
negativi, quindi il problema non è che lo risolviamo. La diagnosi intraoperatoria qui è valida, perché molto<br />
spesso non si tratta di una diagnosi differenziale tra adenoma follicolare e carcinoma follicolare, si tratta di<br />
cellule atipiche che non si riesce a capire, può essere valida, ma può essere valida anche la chirurgia in due<br />
tempi. Se l’esame intraoperatorio non ci dà notizie utili al fine di stabilire la benignità o la malignità, si usa il<br />
termine di “diagnosi differita” cioè ritardata, dopo l’intervento chirurgico. I carcinomi sono quelli che già<br />
sapete. Ecco, che cos’è questo? Degli inclusi citoplasmatici: carcinoma papillifero. Il carcinoma papillifero si<br />
presenta molto modestamente a livello citologico, non presenta queste grandi atipie; un occhio inesperto<br />
direbbe “però queste sono belle cellule, separate le une dalle altre”, però è un carcinoma papillifero. Qua si<br />
vedono bene questi inclusi nucleari, qua si vede ancora bene un grande pseudo-incluso. Qua invece notate<br />
questo anello: è una mitosi che noi chiamiamo “da scoppio”, come se ci fosse stata una bomba. E’ una figura<br />
mitotica atipica, per cui anzicchè esserci il fuso mitotico classico,romboidale, ci stà un cerchio per cui è<br />
come se esplodesse il materiale cromosomico. La diagnosi di carcinoma midollare è una diagnosi difficile<br />
dal punto di vista morfologico perché vi ho detto che il carcinoma midollare è molto fusiforme, può avere<br />
aspetti fusati, cellule globose e così via. Però se facciamo la calcitonina, anche su citologico,e la vediamo<br />
positiva, non abbiamo dubbi che si tratta di un carcinoma midollare. Ora, ecco il concetto clinico: se mi<br />
arriva una diagnosi a me “medico”, a voi “prossimi medici”, citologica di positività per carcinoma papillifero,<br />
midollare, la probabilità che ci sia veramente un cancro maligno, si avvicina al 100%, quindi posso stare<br />
relativamente sicuro; è lo stesso discorso vi ricordate della sensibilità e specificità. Vi ricordo che la<br />
specificità è alta, è la sensibilità che è un poco bassa. Se mi arriva una diagnosi di “sospetta”, ma non<br />
conclusiva malignità, mettendo insieme tutti questi casi, in genere il 65% dei casi corrisponde, dal punto di<br />
vista istologico, ad una lesione maligna. Se mi arriva una diagnosi di lesione papillare o indeterminata, la<br />
possibilità che vi sia una lesione maligna, oscilla tra il 10 e 30%, più vicina al 10%. Se mi arriva una diagnosi<br />
di lesione negativa per malignità consistente con tiroidite, possiamo essere quasi certi che non c’è malignità.<br />
Ok, le altre categorie non ci interessano.<br />
C’è un altro problema. Lavorando noi con un sacco di ospedali che operano alla tiroide, abbiamo visto come<br />
c’è una certa incidenza del micro-adenoma papillifero, questo si chiama anche carcinoma incidentale perché<br />
non aveva dato segni di sé. Si chiamano incidentali perché nell’ecografia, nella citologia, ci aveva fatto una<br />
diagnosi di malignità, anche perché la citologia vede un campo,le altre metodiche ne vedono un altro.<br />
Questi sono cancri piccoli che non hanno un’evidenza. Ovviamente questo ci getta in un certo sgomento per<br />
quanto riguarda questa tecnica, però questo è un falso problema, perché il carcinoma papillifero, in genere<br />
inferiore ad un centimetro, quindi carcinoma incidentale, molto raramente dà problemi, molto raramente<br />
darà metastasi. Questi carcinomi non hanno una grande rilevanza clinica, anche perché hanno una<br />
propensione a metastatizzare quasi pari allo 0%. Noi però scriviamo nella diagnosi “si precisa che un<br />
carcinoma di tali dimensioni, incidentale, ha in genere una prognosi favorevole; lo facciamo perché se no il<br />
clinico o il chirurgo che non sa questo problema, a questo povero paziente lo distrugge.<br />
Ma allora scusate, questa benedetta tecnica citodiagnostica, con tutte le sue falle(lesioni indeterminate,<br />
lesioni sospette), non è che fa acqua da tutte le parti? In effetti noi abbiamo anche il coraggio di dirle queste<br />
falle, i radiologi non ce l’hanno!! Potremmo dire allora che questo approccio è fallimentare, però non è così,<br />
come dice Jack Nicholson, qualcosa è cambiato nella pratica chirurgica, l’approccio antico al nodulo tiroideo,<br />
che potremmo definire giurassico, era addirittura elementare: esami strumentali, chirurgia, anatomia<br />
patologica, benigno o maligno? Cioè non c’era altro modo per saperlo, quindi si facevano un sacco di<br />
interventi. Oggi noi sappiamo che per l’avvento della citologia aspirativa, il numero delle tiroidectomie si è<br />
scaricato da www.sunhope.it
idotto di meno del 62%, anzi anche aldisotto del 50% se vogliamo; quindi un’utilità c’è: ha più che<br />
dimezzato il numero di interventi chirurgici.<br />
Allora riepilogando tra di noi, cosa deve fare il clinico in questi casi? Se si tratta di una lesione inadeguata o<br />
benigna, ripetere l’FNA. Se è benigna lo ripetiamo perché abbiamo detto che due agoaspirtati fatti a<br />
distanza di alcuni mesi, un anno, se tutti e due negativi, ci danno un’elevata sensibilità. Se invece è<br />
inadeguato si fa la biopsia, oppure si fa la chirurgia perché non c’è altro modo per saperlo. Se siamo nella<br />
zona rossa non c’è dubbio, bisogna fare la chirurgia e la terapia oncologica senza perdere tempo. Se siamo<br />
nella zona grigia non facciamo altro che ripetere che si può fare la diagnosi dopo chirurgia, l’intraoperatoria<br />
per le lesioni sospette e la chirurgia dopo. Il ruolo dei marcatori sinceramente si è un po’ ridimensionato<br />
perché si è visto che questi marcatori, dati per assoluti un po’ di tempo fa, hanno delle falle anche loro,<br />
dando dei falsi positivi e dei falsi negativi. Quindi se vi viene un paziente che è spaventato da un oncologo,<br />
perché poi gli oncologi sono specializzati in questo, vi sono alcuni oncologi la cui strategia, nell’approccio<br />
con il paziente, altro che alleanza terapeutica, è un approccio terroristico tanto che il paziente si spaventava<br />
e quando poi stava bene, chiaramente sviluppava una devozione ed esprimeva una disponibilità economica<br />
maggiore.<br />
Allora, parliamo di un altro sistema la cui esistenza si è cominciata a chiarire dagli anni’ 50, per poi definirsi<br />
negli ultimi 15-20 anni, tanto è vero che ha assunto diversi nomi: sistema neuroendocrino diffuso, sistema<br />
neuroendocrino, una volta chiamato sistema APUD(non so se avete mai sentito questa definizione che è<br />
sbagliata perché la caratteristica apud è una caratteristica che hanno solo alcune di queste cellule). Sistema<br />
neuroendocrino diffuso vuol dire un sistema di cellule che si vanno a mettere dappertutto, una specie di<br />
prezzemolo di tutti gli organi! Poi abbiamo ghiandole endocrine propriamente dette e quindi la tiroide,<br />
l’ipofisi e così via e poi abbiamo dei clusters, cioè degli aggregati endocrini(pancreas esocrino e pancreas<br />
endocrino), ma adesso parliamo solo del sistema endocrino diffuso, la tiroide invece appartiene alle<br />
ghiandole endocrine storiche, cioè quelle propriamente dette.<br />
Che cos’è questo sistema? In linea di massima questo sistema è molto penalizzato, tanto è vero che nei libri<br />
di testo è difficile trattarli in maniera unica, cioè in un unicum; sono invece sparpagliati in tutti gli organi(ad<br />
es nel polmone, nell’intestino si parla di carcinoide), mentre invece appartengono ad un sistema<br />
nosologicamente unico. Ovviamente, a seconda dell’organo in cui originano, assumono delle caratteristiche.<br />
Noi comunque tratteremo questo sistema in maniera unitaria. Da dove vengono queste cellule? Mi pare che<br />
già abbiamo parlato di questo traffico che c’è dalla cresta neurale. La cresta neurale è una specie di<br />
elicottero da cui decollano un sacco di cellule: i melanociti, che andranno a colonizzare tutta la pelle,<br />
(talvolta si bloccano, per motivi di traffico, in organi che non sono la cute e possono nascere i melanomi<br />
delle parti profonde); nascono le cellule appartenenti al sistema simpatico e parasimpatico e nascono<br />
queste cellule neuroendocrine, addirittura c’è stato uno studio che le cellule endocrine nascono da questa<br />
porzione(immagine) della cresta neurale, una porzione medio-bassa della cresta neurale. Da lì poi partono e<br />
colonizzano quasi tutti gli organi, tanto è vero che queste cellule le troviamo nella mammella, nell’apparato<br />
gastro-intestinale, nell’apparato respiratorio e si stanno scoprendo un po’ dappertutto, perfino negli organi<br />
genitali. Perché la natura ha provveduto a dare questa dispersione di cellule endocrine? Sembra quasi un<br />
surplus, una cosa inutile, invece non è una cosa inutile. Se noi andiamo a fare un esame banale di una cripta<br />
intestinale e usiamo un marcatore di queste cellule, vedremo che queste cellule le ritroviamo soprattutto a<br />
livello basale. Sappiamo anche che la cellula staminale di quell’organo è in grado anche di differenziarsi in<br />
cellula neuroendocrina e in cellula epiteliale. Questo spiega parecchie cose, cioè a livello staminale ha in sé<br />
la potenzialità di seguire due strade: la strada epiteliale e la strada neuroendocrina ma anche il fenotipo<br />
neuro ectodermico di cui parleremo. Qualcuno vi ha parlato delle cellule peace-maker? Ecco vedete, loro<br />
scaricato da www.sunhope.it
attono il tempo, come il batterista che pratica un po’ di musica sa che due sono le figure fondamentali in<br />
un complesso: il bassista, che sembra che non faccia niente, invece sulle sue note si regola un po’ tutta la<br />
melodia e il batterista; quindi loro battono il tempo. Quindi se ci stanno delle ghiandole cosa significa? Che<br />
se non ci fossero queste cellule, ogni ghiandola se ne andrebbe per i fatti suoi; invece loro, attraverso<br />
mediatori chimici, riescono a dare il tempo, a dire “è il momento di secernere”!! Allora per esempio tutto il<br />
lobulo mammario si trovava nella situazione di tranquillità finchè non arriva questo stimolo<br />
neuroendocrino e improvvisamente le cellule secernono; quindi AZIONE DI COORDINAMENTO. Queste<br />
cellule, come vi dicevo, sono diffuse in tutto il corpo umano. Tenete a mente, ma poi ne parleremo, che vi<br />
sono dei tumori che subiscono un processo di “transdifferenziazione” dall’istotipo epiteliale a quello<br />
neuroendocrino. Per esempio la prostata fa questi scherzi. Ovviamente tumori e cellule neuroendocrine<br />
hanno una diffusione notevole, per esempio nella tiroide le cellule C appartengono al sistema<br />
neuroendocrino, mentre la tiroide in se è una ghiandola endocrina propriamente detta. Poi pure nella cute<br />
ci sono le cellule neuroendocrine, si piazzano anche loro a livello basale, pure loro hanno un’azione di<br />
coordinamento e prendono il nome da colui che le ha scoperte per prime: cellule di Merkel.<br />
Le incidenze di NET, per esempio in Italia ci sono dai 1500 ai 2000 casi all’anno, dove per NET intendiamo<br />
tutti i tumori neuroendocrini. C’è una leggera prevalenza nel sesso femminile, il follow up a 5 anni<br />
globalmente inteso di tutti questi tumori, follow up intermedio di questi pazienti è grosso modo del 67%,<br />
cioè il 67% di questi pazienti, a 5 anni dalla diagnosi, sopravvive. Le casistiche autoptiche, però, ci dicono<br />
che l’incidenza è molto maggiore, è almeno quattro volte quella clinica solo che molte volte questi tumori<br />
non sono funzionanti.<br />
Possono appartenere a diverse categorie e questa vedete è ancora una conferma del ruolo delle cellule<br />
staminali. Abbiamo tumori neuroendocrini fatti tutti da cellule neuoendocrine e allora sono “tumori<br />
neuroendocrini puri”, ma possiamo avere dei “tumori anficrini”, cosiddetti perché la stessa cellula possiede<br />
degli aspetti epiteliali e degli aspetti neuroendocrini, cioè coesistono due fenotipi nella stessa cellula;<br />
vedete, c’è qualche cosa che riguarda le cellule staminali. Poi abbiamo tumori misti o composti, cioè un<br />
tumore che ha delle aree diverse, di carcinoma classico(per esempio) e delle aree di carcinoma<br />
neuroendocrino; così come abbiamo carcinomi compositi dove cellule neuroendocrine e cellule epiteliali<br />
sono mischiate tra di loro, quindi non abbiamo aree distinte, ma le cellule stanno insieme. Per esempio, c’è<br />
un organo come il colon retto dove prevalgono questi tumori compositi. Il 15-30% dei cancri del colon retto<br />
ha una componente neuroendocrina abbastanza importante. Allo stato attuale non è stato ancora studiato<br />
a fondo se questa componente incide o meno sulla prognosi. Cmq sono in corso diversi studi. Come<br />
facciamo a definire l’appartenenza al sistema neuroendocrino? Vi sono dei marcatori generali della<br />
categoria, ce ne stanno un sacco, in effetti noi ne utilizziamo solo due o tre che sono: le CROMOGRANINE,<br />
che si possono dosare anche nel plasma e che sono delle proteine dell’envelope, cioè di quella pellicola che<br />
avvolge il granulo neuroendocrino, per cui se è presente questo antigene, vuol dire che c’è anche la<br />
sostanza neuroendocrina; poi c’è l’ENOLASE NEURONALE SPECIFICA (ENS), che è un enzima caratteristico di<br />
tutta la serie di queste cellule e poi abbiamo la SINAPTOFISINA che pure è un enzima che si ritrova solo in<br />
queste cellule, quindi se noi ci poniamo un problema di diagnosi differenziale, non so, è un carcinoma tipico<br />
o è un carcinoma neuroendocrino? Bhè, basta fare questi due o tre metodi immunoistochimici per la<br />
ricerca di questi antigeni e lo sapremo. Una volta esaurita questa fase, quando noi sappiamo che è un<br />
tumore neuroendocrino, è utile dal punto di vista clinico passare alla seconda fase, cioè utilizzare dei<br />
marcatori specifici per sapere questa cellula che cosa produce. E qua abbiamo una produzione molto<br />
variegata: può produrre catecolamina, calcitonina, encefalina, gastrina, motilina, ove mai sia necessario da<br />
un punto di vista clinico. Facciamo adesso un discorso nosografico perché c’è una certa confusione in<br />
letteratura. Per esempio: CARCINOIDE è un termine storico perché il primo ad identificare questi tumori fu<br />
scaricato da www.sunhope.it
un tedesco che mise il nome “carzinoid”in tedesco, da cui poi è derivato carcinoide. Carcinoide perché sono<br />
delle cellule che, a vederle, sono delle cellule carine, piccoline e poi presentano una serie di problemi;<br />
quindi un carcinoide è un tumore che vuole somigliare ad un cancro, ma non è un cancro, invece può anche<br />
essere peggio di un cancro, poi vedremo il perché. Allora, come si distinguono questi tumori? Possono<br />
essere benigni o maligni. Possono avere due linee differenziative diverse, a seconda se prevale un fenotipo<br />
neuro epiteliale, o un fenotipo neuro ectodermico che è più vicino al sistema nervoso; nel primo caso vuol<br />
dire che è più vicino all’epitelio, tanto è vero che esprime comunemente le citocheratine, a dimostrare che<br />
ha un fenotipo neuroendocrino, ma anche un fenotipo epiteliale. Le altre cellule, quelle che hanno una<br />
differenziazione neuro ectodermica, non esprimono le citocheratine, ma esprimono i neuro filamenti e<br />
quindi è confermato dall’immuno-istochimica che la loro differenziazione si spinge di più verso il fattore<br />
neuro ectodermico.<br />
Per quanto riguarda i tumori BENIGNI, l’iperplasia e l’adenoma sono quelli a differenziazione più epiteliale,<br />
mentre poi ci sono i paragangli, il gangliocitoma che nasce dalle cellule gangliari, quindi è fatto soprattutto<br />
da queste voluminose cellule gangliari.<br />
I tumori MALIGNI si distinguono in : basso grado, grado intermedio e alto grado di malignità. Appartengono<br />
al fenotipo citocheratina positivo i carcinoidi che oggi noi possiamo più modernamente etichettare come<br />
carcinomi neuroendocrini di basso grado, cioè basso grado di malignità. Poi abbiamo quelli che una volta si<br />
chiamavano carcinoidi atipici, che appartengono ad un grado intermedio di malignità, e poi abbiamo l’alto<br />
grado che può essere a piccole e a grandi cellule. Un carcinoma neuroendocrino molto diffuso a piccole<br />
cellule è il MICROCITOMA POLMONARE (ovviamente nella casistica NET che vi ho fatto vedere prima non<br />
sono considerati i microcitomi polmonari perché se no la loro incidenza saliva notevolmente e loro sono più<br />
considerati tra i cancri del polmone). Tra i tumori che sono neurofliamenti positivi, abbiamo il<br />
GANGLIONEUROBLASTOMA, che è un tumore che ha una componente neuroblastica insieme alle cellule<br />
gangliari e poi abbiamo, tra i tumori altamente maligni, il NEUROBLASTOMA che, come sapete è un tumore<br />
tipicamente infantile, il SARCOMA DI EWING che è un tumore osseo ma anche extra osseo. Poi ci sono altri<br />
tumori di cui non parliamo. Quindi, ricapitolando, se vi dicono CARCINOIDE, è un tumore neuroendocrino di<br />
basso grado, se vi dicono carcinoide atipico, capite che si tratta di carcinoma neuroendocrino di grado<br />
intermedio e così via; se vi dicono invece a grandi e a piccole cellule, voi capite che è un tumore di malignità<br />
elevata. Come facciamo noi a vedere se è a medio grado, basso grado o alto grado? Abbiamo dei parametri<br />
universalmente riconosciuti. Innanzitutto le dimensioni: solitamente il tumore di basso grado è piccolo, in<br />
genere inferiore a 2 cm, intermedio e alto grado è maggiore di 2 cm. Le atipie citologiche nel basso grado<br />
sono qualche volta visibili, ovviamente aumentano di numero man mano che ci avviciniamo all’alto grado.<br />
Le figure mitotiche anche seguono questo percorso. Il marcatore più oggettivo della malignità è il Ki67 che<br />
marca tutte le cellule in attività proliferativa, tutte le cellule tranne quelle in fase G0. Allora, se meno del 2%<br />
delle cellule mostra positività nucleare per il Ki67 è in genere di basso grado, se supera questo grado di<br />
percentuale di positività, andiamo verso i gradi maggiori di malignità. Ovviamente vi sono altri caratteri: la<br />
necrosi, l’invasività, l’invasione dei vasi che vi fanno capire come siamo già a livelli più elevati di invasività.<br />
Quindi l’invasività, la capacità di embolizzare nei vasi, di fare necrosi sono fattori correlati ad un grado di<br />
invasività più elevato. Vi sono poi altri parametri che sono variabili a seconda della sede. Per esempio per<br />
quanto riguarda il pancreas, è molto importante sapere quel tumore che cosa produce(la benignità e la<br />
malignità è in rapporto soprattutto alla funzione).<br />
Andiamola a vedere in pratica. Questo(immagine) è un NET ad alto grado, vedete, sopra è a grandi cellule,<br />
sotto è a piccole cellule, e qui vedete un’area di necrosi. In tutti e due i casi, se andiamo a fare il Ki67, quasi<br />
tutte le cellule sono positive, quindi altissimo grado di malignità. A basso grado tendono ad esprimere degli<br />
scaricato da www.sunhope.it
aspetti differenziati, il Ki67 è localmente espresso, già si vede ad occhio che è inferiore al 2%. Qui vi sono<br />
alcuni esempi classici tratti proprio dalla nostra casistica. Esempio: ci arriva un’impegnativa- asportazione<br />
di neoformazione laterocervicale sinistra; questo è l’aspetto morfologico, questa è la calcitonina. E’una<br />
metastasi di carcinoma midollare occulto che pure appartiene alla famiglia dei sistemi neuroendocrini.<br />
Questo è un caso molto interessante che ricordo ancora: tutti erano convinti che si trattasse di un linfoma,<br />
tanto è vero che nell’impegnativa sta scritto “la biopsia è stata fatta in fossa sovraclaveare sinistra però da<br />
circa un mese comparsa di tumefazioni multiple toraco addominali. Diagnosi di linfoma, tac positiva per<br />
tumefazioni multiple linfoghiandolari. Siccome fecero dei prelievi molto ampi, vedete, già gli aspetti<br />
macroscopici,al vetrino, fanno pensare ad un linfoma che coinvolge molte ghiandole. Invece andiamo a<br />
vedere cosa succede con l’immunoistochimica: Ki67 molto elevato, antigene leucocitario comune che marca<br />
tutta le serie linfoide negativo, quindi dobbiamo escludere un linfoma, CEA negativo quindi dobbiamo<br />
escludere vari tipi di neoplasia epiteliale; CROMOGRANINA positiva, ENOLASE positiva, TTF1 positiva: si<br />
trattava di un carcinoma neuroendocrino a piccole cellule del polmone che aveva avuto un pattern di una<br />
tale aggressività per cui il cancro non è stato visto perché corrispondeva al piccolo focolaio che però aveva<br />
metastatizzato subito e in maniera diffusa e generalizzata tanto da far pensare ad un linfoma e là fu una<br />
grande sorpresa perché il paziente già era stato trasferito in ematologia!!<br />
Ancora un’altra lesione: questa è una lesione tipica; l’impegnativa era:asportazione di neoformazione<br />
dall’avambraccio. Era un tumore cutaneo, ecco, qua vediamo come era fatto questo tumore: a trabecole,<br />
Ki67 poco espresso, cromogranina notevolmente espressa..è un carcinoma neuroendocrino cutaneo che<br />
prende il nome di MERKELOMA, dalle cellule di merkel. Attenzione perché può essere scambiato per un<br />
fenomeno infiammatorio. Andiamo avanti: lesione epatica verosimilmente secondaria a carcinoma<br />
polmonare, metastasi di microcitoma polmonare.<br />
Molto frequente è l’appendicectomia. Dovete sapere che un caso ogni duecento di appendiciti croniche<br />
corrisponde ad un carcinoma neuroendocrino che invece passava sotto il nome di appendice flemmonosa.<br />
Anche qui sembra un tumore linfocito simile, questo è epitelio intestinale, cromogranina e sinaptofisina<br />
positive quindi carcinoma neuroendocrino. Altre volte questo carcinoma assume la forma di un polipo.<br />
Questo in realtà era un caso curioso perché c’era il polipo, però nell’asse del polipo vediamo questi noduli<br />
che fanno parte del carcinoma neuroendocrino. In questo caso l’endoscopista aveva sollevato la mucosa per<br />
cui aveva l’impressione di un polipo.<br />
Stiamo per finire, introduciamo solo le paratiroidi. Vi ho spiegato il perché la natura ci ha forniti di quattro<br />
paratiroidi, che i più fortunati ce ne hanno addirittura di più. Sapete la sede delle paratiroidi che è retro<br />
tiroidea, però vedete hanno una sede un po’ variabile, per esempio quelle superiori possono stare qui,<br />
indietro un po’ alla cartilagine cricoide, in rari casi a livello paraesofageo; quelle inferiori stanno in genere<br />
verso la tiroide bassa, ma possono stare anche verso il timo e il mediastino. Questa variabilità di<br />
presentazione macroscopica ci spiega anche un po’ i problemi che ha il chirurgo quando si trova di fronte ad<br />
una patologia delle paratiroidi. Come sono fatte le paratiroidi? Le paratiroidi presentano innanzitutto<br />
tessuto adiposo, e poi presentano due o tre tipi cellulari, probabilmente non si tratta di due o tre tipi ma<br />
dello stesso tipo che subisce delle modificazioni cicliche. Allora ci sono le cellule principali che sono piccole<br />
cellule con un nucleo scuro, un discreto citoplasma rosa; poi ci stanno le cellule chiare che hanno un ampio<br />
citoplasma, sono ricche di lipidi per cui il loro citoplasma appare vuoto perché nel processatore dei tessuti<br />
che noi utilizziamo il grasso viene sciolto dai solventi per cui, andando via il grasso,in quelle zone apparirà<br />
come un vuoto; e poi le cellule ossifile hanno un citoplasma più ampio e vacuolizzato, la funzione di queste<br />
cellule che esprimono la cromogranina è la sintesi di PTH. Le ghiandole invece sono piccolissime, parliamo<br />
di mg, 120, 130 mg, quindi inferiori al grammo. Le dimensioni vanno da 3-6 mm grosso modo, ma la<br />
scaricato da www.sunhope.it
morfologia della ghiandola varia in rapporto all’età per cui le cellule princiali diminuiscono man mano che<br />
passiamo dall’età infantile, all’età avanzata. Probabilmente sono cellule più funzionalmente attive. Le cellule<br />
chiare, invece, aumentano man mano che ci avviciniamo alla senilità, così come aumenta il tessuto adiposo<br />
e aumentano le cisti. Quindi, tutto aumenta con l’età tranne le cellule principali che rappresentano<br />
probabilmente le cellule più giovanili e attive.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> – Infiammazione 1<br />
Prof.ssa Costanzo<br />
Lezione n°8<br />
8/11/2010<br />
INFIAMMAZIONE<br />
Reazione rispetto alla azione lesiva procurata da stimoli esterni patogeni causanti la alterazione<br />
della omeostasi del nostro organismo, il quale cerca di ripristinarla mediante modifiche interne.<br />
L'infiammazione è quindi un processo reattivo e locale che porta ad una progressiva evoluzione con<br />
una serie di fenomeni che sono correlati tra di loro e che sono in una successione temporale ben<br />
stabilita. Sono fenomeni ben delimitati non sono temporalmente, ma anche spazialmente e, nella<br />
maggior parte dei casi, avvengono nel mesenchima. Qui sono presenti tessuti connettivali e organi<br />
vascolari.<br />
Il danno infiammatorio inizia con un danno subendoteliale che può arrivare ad un distruzione<br />
permanente di tessuti colpiti o ad un danno persistente verso una flogosi cronica o verso un<br />
ripristino morfologico di tutta la area colpita.<br />
Classificazione:<br />
Infiammazione acuta: dura poco tempo<br />
Infiammazione cronica: può durare settimane o mesi.<br />
Questa definizione va valutata dal punto di vista clinico basandoci sulla durata del processo, perchè<br />
l'infiammazione non è altro che la sovrapposizione di entrambe queste fasi, ma che, oltre che dal<br />
quadro temporale, sono distinte tra loro dal loro quadro patologico.<br />
Protagonisti cellulari dell'infiammazione: vaso, macrofagi, mastcellule, fibre collagene, cellule<br />
connettivali.<br />
FASE ESSUDATIVA: è la prima reazione al danno, quindi presente nella infiammazione acuta con<br />
alterazione della permeabilità vasale, quindi caratterizzata principalmente da:<br />
• fenomeni vascolari: alterazione della permeabilità vasale<br />
• fenomeni essudativi: formazione di essudato ricco di proteine e di plasma<br />
• fenomeni cellulari: che prevedono la migrazione di cellule che sono esclusivamente<br />
neutrofili e macrofagi.<br />
FASE CRONICA: dovuta a ripetizione e persistenza dello stimolo nocivo e quindi del danno,<br />
caratterizzata dalla presenza di forte componente cellulare e dal susseguirsi di:<br />
• fenomeni vascolari ed essudativi che non regrediscono<br />
• fenomeni cellulari: aumento delle cellule nell'interstizio con neutrofili, linfociti,<br />
plasmacellule, angioblasti, fibroblasti.<br />
• fenomeni necrotici<br />
• reazioni immunologiche<br />
Quindi i fenomeni dell'infiammazione possono riassumersi in due fenomeni fondamentali: reazione<br />
vascolare e reazione cellulare.<br />
Reazione vascolare: vasocostrizione transitoria immediata, e vasodilatazione successiva con<br />
aumento della permeabilità vascolare e formazione di edema ed essudato che causano stasi<br />
vascolare.<br />
Reazione cellulare: eventi riguardano le cellule mediante marginazione, rotolamento, adesione e<br />
scaricato da www.sunhope.it
successiva diapedesi delle cellule attraverso l'endotelio. Le cellule così migrano nei tessuti<br />
interstiziali.<br />
Quali sono i protagonisti dell'infiammazione? Il protagonista in assoluto non è altro che il vaso<br />
dove annesso ad esso riconosciamo un ambiente interno costituito dalle cellule ematiche,<br />
polimorfonucleati , linfociti, monociti, ma esternamente a questo c'è tutto un insieme di elementi<br />
che fanno gioco in questa situazione che sono i macrofagi, tutti gli elementi dell'epitelio<br />
connettivale, le mastcellule, le fibre collagene e delle proteine come protoglicani che contribuiscono<br />
al quadro infiammatorio.<br />
Quindi si parla di una fase acuta limitata da pochi minuti fin massimo a qualche giorno. Evento<br />
successivo è la formazione di un essudato di proteine e plasma e migrazione di leucociti, sopratutto<br />
neutrofili. La fase finale di questa può essere la guarigione, o può evolvere verso la cronicizzazione.<br />
Nella fase cronica c'è da un lato la tendenza a guarigione, ma si possono avere anche fenomeni di<br />
neoangiogenesi, fibrosi e di necrosi tissutali.<br />
Cause della infiammazione acuta:<br />
• Traumi meccanici<br />
• Lesioni di sostanze chimiche<br />
• Ustioni o congelamento<br />
• Radiazioni UV<br />
• Ischemia<br />
• Patogeni come batteri, virus, parassiti<br />
• Disimmunopatie<br />
Il modello di reazione prevede due forme principali: angioflogosi e istoflogosi:<br />
Angioflogosi: caratterizzata da fenomeni vascolo-essudativi e manifestazioni che fanno seguito a<br />
modificazioni dinamiche, di calibro, di tono e di flusso a livello del microcircolo.<br />
Di conseguenza si verifica un aumento della permeabilità dei capillari e quindi migrazione dei<br />
leucociti con aumento delle cellule all'interno dei vasi dell'interstizio. Questo essudato trascina non<br />
solo sali nell'interstizio, ma anche altre molecole organiche che si organizzano a formare l'essudato.<br />
Dal punto di vista clinico si può evidenziare con i segni dell'infiammazione: rubor, dolor, calor,<br />
tumor, fuctio lesa.<br />
Istoflogosi: permangono ed aumentano i fenomeni vascolo essudativi, ma aumenta la entità della<br />
migrazione delle cellule mononucleate nell'interstizio, e loro moltoplicazione nello stesso<br />
interstizio.<br />
Mediatori dell'infiammazione: sono molecole di origine cellulare che sono mediatori endogeni<br />
derivanti dal plasma o dal tessuto. Questi sono per esempio: sistema del complemento, citochine,<br />
fattori della coagulazione, enzimi fibrinolitici, o mediatori provenienti dai tessuti come ammine,<br />
contenuto lisosomiali, mediatori attivanti piastrine.<br />
Alterazioni vasali: il microcircolo è composto da arterie terminali costituite da endotelio che<br />
poggia sulla membrana basale che è circondata da un monostrato di cellule muscolari lisce. Stessa<br />
caratteristica e architettura è presentata dalle microarteriole con variazione di calibro del vaso<br />
durante l'infiammazione. L'endotelio invece poggia direttamente su membrana basale, che, come in<br />
tutti gli endoteli, è permeabile a diverse molecole perchè è costituita da due tipi di pori:<br />
1- pori maggiori di 50micron<br />
2- pori minori che trasferiscono molecole più piccole.<br />
L'equilibrio tra zona endovasale e zona interstiziole è spiegato da:<br />
-Legge di Starling dove il flusso attraverso la parete del vaso è dato esclusivamente dalla pressione<br />
scaricato da www.sunhope.it
idrostatica e dalla pressione osmotica. Sono fenomeni che portano anche a conseguenze come la<br />
alterazione della premeabilità capillare.<br />
-L'ultrafiltrazione è il passaggio dell'acqua mediante una barriera quale, in questo caso, è l'endotelio<br />
composto dai pori attraverso cui passano le sostanze. Il fenomeno di ultrafiltrazione è dovuto a due<br />
forze fisiche: pressione idrostatica, che in genere spinge i fluidi attraverso i pori verso proteine e<br />
verso mucopolisaccaridi, e la pressione osmotica che è una pressione che è esercitata dalla proteine<br />
sull'acqua. Queste forze si combinano fino a stabilire un equilibrio, e nell'infiammazione, quando<br />
aumenta la pressione idrostatica, una quantità di acqua passa attraverso il vaso nel compartimento<br />
extracellulare L'aumento della permeabilità del vaso fa si che vengano trascinate nel comparto<br />
extravasale sia acqua, che soluti e molecole che determinano la presenza di liquido extravasale.<br />
(Immagine) Qui si possono osservare le tipice alterazioni che si verificano in una infiammazione<br />
dove, se in condizioni normali le cellule del vaso non formano pori evidenti, quando aumenta la<br />
pressione idrostatico le cellule endoteliali si distanziano tra loro formando i pori attraverso cui<br />
possono passare le sostanze.<br />
La popolazione vasale invece è composta da cellule che intervengono nella infiammazione acuta,<br />
dove sono presenti solo granulociti eosinofili, basofili e neutrofili, mentre nella fase cronica (la prof<br />
dice di nuovo acuta...boh) sono riscontrabili anche altri tipi cellulari.<br />
I globuli rossi sono presenti anche loro in entrambe le fasi e la loro presenza nell'interstizio è<br />
conseguenza del flusso ematico che si rallenta a causa della perdita di acqua attraverso le pareti del<br />
vaso. La pressione che si ha attraverso l'endotelio dà a queste cellule una conformazione nuova che<br />
ne permette la aggregazione e il deposito alle pareti del vaso, tendendo sempre a portare ad un<br />
aumento della viscosità ematica, causata dalla formazione di “pile” di eritrociti.<br />
I neutrofili sono riscontrati come parte figurata nell'infiammazione acuta e sono presenti nel sangue<br />
e sono il 45% di tutte le cellule ematiche e sono rimpiazzabili da cellule del midollo osseo. Si<br />
muovono rapidamente rispetto alle altre cellule, e sopratutto contengono molti di quegli enzimi<br />
lisosomiali come perossidasi, fosfatasi, che sono coinvolti nel processo dell'infiammazione. Queste<br />
cellule stimolano la marginazione (tappezzando la parete vasale), migrano attraverso il vaso e il<br />
rimaneggiamento del danno vasale. Possono poi, mediante la diapedesi, espletare la loro<br />
chemiotassi che porta queste cellule nel focolaio flogistico.<br />
Inoltre con la fagocitosi possono avere parte attiva nella infiammazione.<br />
Per quanto riguarda l'aumento della permeabilità del vaso riconosciamo delle fasi dove si può avere<br />
una risposta infiammatoria o la formazione nell'endotelio di alcune aperture proprio a causa della<br />
contrazione delle stesse cellule endoteliali. La risposta può poi essere prolungata anche di molte ore<br />
dove il danno è diretto all'endotelio dallo stimolo lesivo. I fenomeni possono essere:<br />
• Risposta prolungata ritardata con riorganizzazione delle proteine delle cellule interessate e<br />
quindi del loro citoscheletro, provocando proprio l'allontanamento delle cellule le une dalle<br />
altre.<br />
• Danno mediato da leucociti che, attivati, rilasciano metaboliti tossici<br />
• Aumentata transcitosi dove c'è aumento di canali endoteliali con agglomerati di vescicole e<br />
vacuoli che vengono esocitati.<br />
• Neoangiogenesi di nuovi vasi che sono collegati tra loro fino alla formazione di una fitta<br />
rete vascolare.<br />
• Stasi venosa: dovuta al fatto che l'acqua fuoriesce con conseguente riorganizzazione delle<br />
emazie e aumento della viscosità del sangue. Il flusso quindi rallenta e i leucociti intanto si<br />
accumulano a livello dell'endotelio e vi aderiscono prima poi di migrare attraverso di esso. I<br />
leucociti nel vaso costituiscono i fenomeni della marginazione, del rotolamento e della<br />
adesione all'endotelio. Possono passare attraverso l'endotelio stesso con la diapedesi, quindi<br />
migrare nell'interstizio mediante stimoli chemiotattici e colonizzare i tessuti circostanti.<br />
scaricato da www.sunhope.it
Quindi nel processo infiammatorio si possono osservare non solo un elevata concentrazione<br />
di neutrofili, ma anche una dilatazione vasale e un accumulo di proteine che normalmente<br />
non sono presenti a tali concentrazioni.<br />
(immagine) Si ritrovano cellule nello spazio extravascolare che, nella infiammazione cronica,<br />
aumentano di numero, la parete vasale è aumentata di spessore, il letto capillare è aumentato di<br />
spessore, sono presenti cellule e liquidi nell'interstizio che normalmente non sono presenti.<br />
Tipi di essudato:<br />
• Sieroso: costituito da proteine e dovuto alla fuoriuscita di liquido povero di fibrinogeno e a<br />
bassa concentrazione di proteine. Si forma in genere su superfici rivestiti da cellule<br />
mesoteliali come le cavità articolari, pleuriche o in corso di pleuriti.<br />
• Fibrinoso: con alto contenuto proteico, grandi quantità di fibrinogeno che viene poi<br />
convertito in fibrina. Presente sulle superfici delle cavità sierose come pleura, pericardio e<br />
peritoneo. Il rivestimento mesoteliale perde il suo aspetto liscio e lucente prende aspetto<br />
opaco ed irregolare dovuto alla fibrina che si organizza. Accompagnato in genere a dolore o<br />
avvertibili alla auscultazione nelle pleuriti. La fibrina difficilmente viene digerita, quindi per<br />
esempio a livello cardiaco può essere causa di esiti cicatriziali che determinano stenosi<br />
valvolari.<br />
• Emorragico: è di tipo fibrinoso, ma in cui si è verificata una alterazione vasale, ma con<br />
fuoriuscita anche di emazie. Si osservano in genere in alcune infezioni batteriche o virali.<br />
• Purulento: la presenza del numero di neutrofili è aumentato e conferisce a questo essudato<br />
un colore opaco, e enzimi lisosomiali e batterici provocano la formazione di un centro<br />
lesionale necrotico viscido definito pus.<br />
• Fibrinoso-purulento: dovuto alla associazione di entrambi<br />
• Catarrale: quando il processo interessa anche le mucose. Nella fase iniziale questo essudato<br />
è sieroso, e poi si verifica un associata produzione delle ghiandole mucosali che converte<br />
l'essudato in un liquido più denso ed appiccicoso.<br />
Evoluzione dell'essudato.<br />
L'essudato può evolvere sia in rapporto alla densità dei tessuti lesi, sia in rapporto alla persistenza<br />
dello stimolo infiammatorio.<br />
Suppurazione: se l'infezione si realizza in un tessuto considerato come un blocco solido (fegato,<br />
rene) e se il micro-organismo è un batterio.<br />
Ascesso: Il tipo di tessuto quindi influenza molto il tipo di organizzazione che si verrà ad avere, con<br />
possibile suppurazione localizzata formando un ascesso se il tessuto è ben limitato.<br />
Cellulite: se il processo infiammatorio si diffonde nei tessuti circostanti formando la cellulite. È il<br />
caso in cui il processo infiammatorio si estenda in tessuti lassi connettivi i connettivali<br />
Flemmoni: se la raccolta è organizzata e piu estesa con scarsa tendenza all'espansione. Sono ormai<br />
rari grazie alle terapie antibiotiche.<br />
Evoluzione dell'essudato: può evolvere in rapporto alla quantità dei tessuti lesi, alla persistenza<br />
della causa stessa del processo e in rapporto alla sede del processo, dove può essere sia diffuso, che<br />
localizzato, quindi può dare ascessi, flemmoni...<br />
(immagine) nella infiammazione cronica al centro del vaso c'è presenza di emazie, ma intorno al<br />
vaso ci sono neutrofili. Col passare del tempo aumenta il calibro vasale, la viscosità ematica, e i<br />
neutrofili non stanno piu nel vaso ma sono trasferiti nel comparto extravasale ed all'interno restano<br />
solo le emazie. Nel terzo stadio i neutrofili circondano tutto il vaso e allo stesso tempo l'essudato<br />
porta alla formazione di tralci bianchi che è il fibrinogeno.<br />
(immagine 1) anche qui si vede stravaso, quindi essudato, dove nella infiammazione cronica sono<br />
scaricato da www.sunhope.it
presenti neutrofili ed emazie, e se nell'immagine può essere un primo stadio, in questa<br />
(immagine 2)si vede organizzazione della fibrina.<br />
(immagine 3) qui invece si vede tutta la parte figurata delle cellule che si organizza formando un<br />
tessuto che non si può riconoscere se non come cellule di una infiammazione cronica:<br />
plasmacellule, neutrofili, linfociti e tutti i componenti della flogosi cronica.<br />
A livello alveolare per esempio può essere sieroso. Nelle cavità può poi essere fibrinoso, o<br />
sierofibrinoso. La persistenza e la natura dell'essudato aggravano la situazione del quadro sopratutto<br />
in rapporto all'agente che ha provocato la lesione stessa. Nei tessuti l'essudato può causare forme di<br />
necrosi locale, stimolando la attività di angioblasti e fibroblasti e che, una volta eliminato il tessuto<br />
necrotico, stimolano la cicatrizzazione e quindi la guarigione dall'evento.<br />
Cenno sull'immunoistochimica:<br />
Con l'immunoistochimica, utile per chiarire alcuni quadri dell'infiammazione e anche per i tumori,<br />
andiamo a ricercare l'antigene specifico. Questa branca ha dato una grossa svolta a quelli che sono<br />
stati per anni dei dubbi dell' atonomia patologica e ha assunto dei teoremi classici dell'immunologia<br />
che sono stati trasportati a quella che è l'anatomia patologica di laboratorio. L' anatomia patologica<br />
ha fatto sua la classica reazione antigene-anticorpo . E su questo teorema ha lavorato con anticorpi<br />
specifici contro quel determinato antigene. Quelle colorazioni che voi vedrete che per esempio<br />
hanno come coloranti la ematossilina-eosina, sono diverse dalle colorazioni che si vedono<br />
nell'immunoistochimica, perchè nell'immunoistochimica noi andiamo a non solo identificare<br />
l'antigene, ma anche a caretterizzare il luogo dove è avvenuta la reazione antigene/anticorpo. Per cui<br />
gli antigeni che sono in laboratorio sono tutti antigeni prodotti in commercio e sono diversi per tutte<br />
le caratteristiche biochimiche dell'antigine in genere sono diretti verso gli specifici antigeni che noi<br />
vogliamo andare a ricercare . Tipo per esempio la cromogranina dove c'è l'anticorpo anti<br />
cromogranina che va a localizzare dove si trova la cromogranina e addirittura in quante quantità si<br />
può trovare in quel tessuto. Questo lo vedrete più chiaramente quando farete i linfomi proprio<br />
perchè l'immunoistochimica è riuscita a caratterizzare tutti i fenotipi di tutti i linfociti e quindi di<br />
tutte le patologie. Le colorazioni che vedrete sono mirate esclusivamente agli antigeni che noi<br />
vogliamo andare a ricercare. Gli antigeni sono delle macromolecole con un peso molecolare<br />
sufficiente per poter innescare una reazione antigene/anticorpo quindi non è sempre valido che noi<br />
andiamo a cercare una proteina perchè ha un peso molecolare maggiore, quindi possiamo andare a<br />
cercare dei carboidrati delle lectine o altri tipi di proteine molto più basse come peso molecolare.<br />
Per ogni antigene tissutale o cellulare sono stati costruiti in laboratorio degli anticorpi specifici<br />
verso questi antigeni e successivamente per quelli che sono gli antigeni tumorali ecco perchè noi<br />
oggi differenziamo un tumore mesoteliale da quello epiteriale perchè alcuni tumori esprimono<br />
determinati antigeni mentre nella normalità questi antigeni non li ritroviamo.<br />
scaricato da www.sunhope.it<br />
Raffaele
ANATOMIA PATOLOGICA LEZIONE DEL 09/11/2010<br />
Continuo dell’ infiammazione lez. Dell’ 8/11/2010 Prof.ssa Costanzo<br />
Continuiamo l’infiammazione con la seconda parte dell’infiammazione, l’infiammazione cronica.<br />
L’infiammazione non è che perché l’ho fatta io, il professore non la chiede, il prof la chiede. Non<br />
sottovalutate l’infiammazione perché alcune risposte, proprio mentre fate l’esame, le trovate<br />
nell’infiammazione. Ieri vi ho lasciati a questo schema dove appunto vedete un’immagine di infiammazione<br />
acuta che può avere delle evoluzioni diverse: risoluzione completa a livello del microcircolo con<br />
ricostruzione completa delle arteriole, delle venule e di tutto il resto e vedete che anche l’ambiente esterno<br />
completamente sgombro di cellule interstiziali che avevano travasato; se questo non succede, questa<br />
infiammazione acuta può seguire una strada che portava alla formazione di pus e organizzarsi poi con una<br />
capsula e andare a formare un flemmone ecc. ecc. oppure può arrivare alla fibrosi e gli esiti di questo<br />
fenomeno sono abbastanza chiari e sono anche evidenti in alcune biopsie e in alcuni prelievi istologici che<br />
noi riscontriamo oppure può andare incontro a quella che è la nostra infiammazione cronica che è<br />
strutturata e abbastanza complessa proprio perché ci sono delle situazioni e degli scenari che cambiano poi<br />
notevolmente. Ieri abbiamo visto che per quanto riguarda l’infiammazione acuta e in base all’essudato che<br />
si va a formare, un’infiammazione acuta come: sierosa, fibrinosa, suppurativa purulenta, ulcerativa con vera<br />
e propria formazione dell’ulcera. Quali sono i quadri relativi a questi eventi? Qui vedete una cute che in<br />
base all’essudato sieroso si ha un’infiammazione sierosa. Qui vedete un pericardio con infiammazione<br />
fibrinosa purulenta, c’è una flogosi in atto con necrosi e grande popolazione di neutrofili. Qui vedete<br />
un’infiammazione suppurativa più chiara rispetto a quella precedente perche vedete qui la popolazione<br />
cellulare completamente costituita dai nostri neutrofili. Oppure qui vedete un’ulcera che a differenza di<br />
tutte le altre lesioni provoca, come voi sapete, delle escavazioni dove c’è l’evento infiammatorio, ma<br />
addirittura un distacco nella zona dell’infiammazione formando delle vere e proprie ulcere e questo è quello<br />
che noi in genere ritroviamo nell’ulcera peptica; mentre se l’infiammazione ha sede da un’altra parte dello<br />
stomaco, lo scenario cambia.. ecco perché a volte nell’ulcera, quando è peptica e il gastroenterologo va a<br />
fare una gastroscopia, può avere degli esiti cicatriziali se a livello del duodeno, per esempio, si è verificata<br />
precedentemente un’ulcera e quindi un’infiammazione; un buon gastroenterologo vedendo gli esiti<br />
cicatriziali può supporre che lì precedentemente ci sia stata un’infiammazione. Riepilogando, quindi, in un<br />
danno tissutale che si costituisce, come anche una necrosi, abbiamo una risposta che è l’infiammazione<br />
acuta; ci sarà un’infiltrazione di granulociti neutrofili e se c’è distruzione di tessuto possiamo avere, come<br />
dicevamo ieri, l’organizzazione di questo tessuto per formare un ascesso e questa riorganizzazione può<br />
portare o ad un’eliminazione del danno in maniera completa con una riorganizzazione o per meglio dire una<br />
ristrutturazione della zona lesa mediante formazione di un nuovo tessuto che viene chiamato tessuto di<br />
granulazione. Oppure, se la noxa patogena continua nel tempo, con anche la distruzione del tessuto in<br />
esame, possiamo avere un’ulteriore riorganizzazione che si caratterizza proprio nell’infiammazione<br />
persistente e che dura nel tempo. La risoluzione di questo quadro è che possiamo avere una risoluzione<br />
completa, come nel caso dell’ulcera di prima, oppure una guarigione con un nuovo tessuto di riparazione<br />
che poi vedremo oppure il tutto può incanalarsi in un’altra strada che è quella dell’infiammazione cronica.<br />
Qui (figura) vediamo gli stadi di cui abbiamo parlato; quindi la risoluzione non è altro che il ripristino della<br />
struttura dove si è verificata l’infiammazione e addirittura l’essudato viene riassorbito, per cui il tessuto leso<br />
ritorna nella norma. L’importanza di questo processo è che, poiché il danno si conclude tutto sommato e<br />
quindi c’è una risoluzione netta, c’è da tener presente che il tessuto che è preso in considerazione conserva<br />
una sua capacità che è quella di completare questa risoluzione proprio perché ha delle cellule specializzate<br />
che possono in un certo senso rigenerarsi; ecco perché si può avere la risoluzione del processo. Non che si<br />
debba per forza guarire, ma quelle cellule che sono situate in quella determinata zona hanno appunto la<br />
scaricato da www.sunhope.it
capacità e quindi la funzionalità di rientrare in rigenerazione. Con questo ci si spiega perchè alcune ferite<br />
guariscono in un certo periodo di tempo senza lasciare esiti cicatriziali mentre altre no. Questo è il classico<br />
esempio, come vi dicevo, nelle ustioni che ognuno di noi ha subito qualche volta, sia con l’esposizione al<br />
sole oppure con il fuoco, in cui poi la cute ritorna come prima; oppure nella classica polmonite lobare…<br />
questo (figura) è un classico quadro di polmonite dove vedete alcuni alveoli deformati dall’evento<br />
infiammatorio.. qui vedete c’è addirittura la formazione del pus.. qui invece c’è ancora una raccolta di<br />
macrofagi .. ma, tutto sommato, alla fine del processo questa situazione rimane piuttosto così. La<br />
rigenerazione è un altro evento dove entrano in gioco delle cellule, dove c’è stata appunto l’infiammazione,<br />
che hanno la facoltà di rigenerarsi. Esempio è dato dal’evento di guarigione della polmonite lobare in cui<br />
abbiamo la restituzione totale dello stesso epitelio oppure, altro esempio, la rigenerazione totale di alcuni<br />
assoni - c’è un errore.. vabbè (si riferisce alle slide)- dei nervi periferici dopo l’evento di un trauma. La<br />
guarigione per cicatrizzazione ha un’esecuzione piuttosto riorganizzativa perché in effetti si sostituisce al<br />
tessuto di prima un tessuto di struttura completamente diverso, quindi un nuovo tessuto connettivo<br />
vascolare, che va incontro a questa nuova organizzazione; questo è un processo che completa il tessuto<br />
colpito dalla lesione proprio perché va incontro a delle modificazioni, per esempio sostituzione di collagene<br />
e va a costituire quella che sarà la nostra cicatrice fibrosa. L’esempio si vede in questo caso che se noi<br />
abbiamo una ferita da taglio con un coltello, superficialmente non vediamo niente ma se facciamo una<br />
sezione longitudinale nella zona della lesione noi vedremo che in superficie tutto sommato la lesione si è<br />
ristabilita, ma all’interno, nel derma sottostante il taglio ci sono due colorazioni.. una più intensa, l’altra più<br />
pallida .. questo perché la zona che costeggia la zona più chiara è costituita da tessuto normale, quindi da<br />
derma che non ha subito la lesione, mentre la zona qui è più pallida perché si è avuta una trasformazione,<br />
una rigenerazione per sostituire la lesione avuta con la formazione di fibre collagene ; se noi facessimo delle<br />
colorazioni specifiche per mettere in evidenza il collagene noi avremmo questa zona molto più colorata<br />
perché vengono messe in evidenza queste fibre- Vedo che la signorina continua a ridere con il vostro collega<br />
a fianco .. evidentemente è molto preparata ( ahahahahaha ) .. vabbè! – Il processo di organizzazione,<br />
invece – ma voi pensate che chi sta da questa parte non vede niente???.. sn stata pure io dalla vostra parte<br />
(prufessorè .. molto e molto tempo fa!) – allora … per quanto riguarda invece le caratteristiche<br />
dell’infiammazione cronica (la prof si è persa il periodo di prima) cominciamo a definire quelli che sono i<br />
passaggi: per prima un’infiltrazione di alcune cellule, non più neutrofili, ma cellule mononucleate come<br />
macrofagi, linfociti e plasmacellule.. quindi vedete che lo scenario cambia. Quest’immagine l’avevo<br />
proiettata ieri e si vede che ci sono delle cose che non vanno. Vi sto facendo questi esempi non perché mi<br />
piace farli, ma perché più avanti il professore vi farà vedere dei quadri e vi chiederà un giudizio.. quindi non<br />
sottovalutate queste immagini. Quindi se io vi dico: “non abbiamo più neutrofili“.. voi capite il perché e<br />
quando il prof vi presenterà delle immagini con l’infiammazione voi, se siete stati attenti, dovete capire se si<br />
tratta di un’infiammazione acuta o cronica proprio perché la morfologia e lo scenario di determinate cellule<br />
cambia completamente. Il danno tissutale diciamo che dipende dalla persistenza dell’agente<br />
lesivo e nello stesso tempo dalla quantità delle cellule infiammatorie che in un certo senso accorrono alle<br />
lesione. I tentativi di guarigione possono creare un nuovo connettivo, un neoconnettivo, con, a monte, i due<br />
processi di angiogenesi ma anche di fibrosi. Quello che è importante nell’infiammazione cronica è che è<br />
caratterizzata da due fenomeni: 1)degenerativo, quindi l’infiammazione cronica può portare ad una<br />
degenerazione ed arrivare alla necrosi; ecco perché alcune volte quando vediamo dei preparati, la necrosi ci<br />
fa capire che c’è stata prima un’infiammazione cronica. Per noi la necrosi è molto importante, perché, se vi<br />
ricordate quando abbiamo parlato di fissativi, l’obiettivo principale della fissazione è proprio quello di non<br />
andare incontro alla necrosi.. perché è una difesa, badate bene , cioè l’organismo (penso volesse dire un<br />
tessuto) nel momento in cui non si trova in un ambiente suo, dove è abituato ad essere, perché viene tolto<br />
ad esempio per un intervento chirurgico o quant’altro, la prima cosa che fa è difendersi.. è un meccanismo<br />
scaricato da www.sunhope.it
sbagliato, ma si difende con l’espulsione di alcuni enzimi lisosomiali che non fanno altro che distruggere,<br />
autodistruzione della cellula stessa, creando quelli che sono gli spazi e i relativi vuoti che noi ritroviamo in<br />
alcuni reperti.. proprio perché la fissazione non è stata fatta bene. Questa però è la necrosi da mancata<br />
fissazione. Esiste, invece, una necrosi diversa che deriva invece da un processo infiammatorio, quindi ha<br />
patogenesi completamente diversa, non da mancata fissazione. Le necrosi da cattiva fissazione noi le<br />
riconosciamo a livello microscopico perché ci sono delle caratteristiche diverse. L’altro fenomeno<br />
caratteristico dell’infiammazione cronica sono 2) gli eventi proliferativi dello stroma perché si attivano le<br />
cellule specializzate del tessuto connettivo, che sono i fibroblasti, iniziando la sintesi di nuovo collagene..<br />
ecco perché abbiamo una cicatrice piuttosto pallida, perché il collagene appena formato è collagene ancora<br />
non maturo, un neocollagene.. per cui da le caratteristiche tintoriali che abbiamo visto prima. Gli eventi<br />
proliferativi possono anche coinvolgere la rigenerazione di alcune cellule parenchimali. Per quanto riguarda<br />
la classificazione della flogosi, c’è una classificazione anatomo-patologica che definisce questa flogosi in due<br />
fasi: possiamo avere una flogosi interstiziale oppure una flogosi granulomatosa. Noi, in genere, quando<br />
diamo delle diagnosi di infiammazione stabiliamo nell’ambito dell’infiammazione cronica se è<br />
un’infiammazione interstiziale oppure un’infiammazione granulomatosa. Gli eventi sono diversi per gli<br />
scenari che adesso vedremo e questa è una nostra classificazione anatomopatologica e a volte non<br />
possiamo esprimerci in questi senso perché a volte c’è il chirurgo dall’altra parte che ci chiama per chiederci<br />
che cosa significa granuloma oppure che cosa vuol dire flogosi interstiziale; per noi, invece, è una<br />
classificazione perché si tratta di due eventi distinti e separati anche perché hanno un’evoluzione diversa.<br />
GRANULOMA: il granuloma non ci deve ricordare solo il granuloma tubercolare. In alcuni tessuti noi<br />
possiamo avere delle immagini e quindi delle morfologie che ricordano, in un certo senso, il granuloma.<br />
Tutto questo succede perché ci sono alcune cellule, come vi dicevo prima, i fibroblasti, i macrofagi e gli<br />
angioblasti che sono i responsabili di questi quadri. I fibroblasti sintetizzano collagene, i macrofagi vanno a<br />
fagocitare il materiale corpuscolato mentre gli angioblasti intervengono nella formazione della nuova<br />
angiogenesi. Ecco che si viene a determinare quello che noi chiamiamo tessuto nuovo o tessuto di<br />
organizzazione, dove i granuli superficiali di tessuto neoformato assumono, per esempio nelle ferite<br />
cutanee se noi togliamo la crosticina che si è formata, ci accorgiamo che c’è sotto un tessuto<br />
completamente diverso che è il nostro tessuto di granulazione. In più riconosciamo in questo processo, una<br />
fase di vascolarizzazione perché chiaramente anche gli angioblasti hanno dato il loro contributo; quindi c’è<br />
la creazione di nuovi vasi, c’è la formazione di collagene da parte dei fibroblasti e poi c’è una fase di ritorno<br />
alla normalità con una fase di devascolarizzazione dove questi vasi, una volta formati e una volta espletata<br />
la loro funzione, vengono poi degradati.<br />
Quali sono le cellule dell’infiammazione cronica? Nell’infiammazione acuta abbiamo le emazie e i neutrofili.<br />
Ieri vi ho fatto vedere uno schema di tutte le cellule che intervengono nell’infiammazione perché, come vi<br />
ho detto ieri, il processo non è scisso. Noi anatomopatologi consideriamo, in genere, i due processi come in<br />
un unico evento a meno che non abbiamo una risoluzione del problema quando abbiamo la ricostituzione<br />
completa perché abbiamo quelle cellule che hanno la potenzialità di rigenerarsi e quindi c’è la completa<br />
guarigione. Le cellule dell’infiammazione cronica sono neutrofili ( ma prima non aveva detto che non<br />
c’erano neutrofili? Forse ce ne sono pochi ), plasmacellule, ci sono pure le emazie, i linfociti che hanno una<br />
predominanza in questo processo, gli eosinofili e anche i macrofagi. Quello che noi vediamo è l’effetto del<br />
macrofago perché il macrofago è il protagonista principale dell’infiammazione cronica; questo perché nasce<br />
balle cellule del midollo con un processo immunoblastico e quando c’è un’azione lesiva subisce delle<br />
trasformazioni arrivando così dal monocita al macrofago maturo. Una volta che viene stimolato da tutte<br />
quelle sostanze e quelle macromolecole che si vengono a scaturire dal danno tissutale, questo si attiva<br />
attraverso quindi citochine, endotossine batteriche e altri mediatori chimici. In più, però, questo ruolo dei<br />
scaricato da www.sunhope.it
macrofagi attivati è particolare perché danno una serie di risposte, secernono una serie di sostante, una<br />
serie di prodotti. L’azione dipende dal tipo di attivazione che ha avuto: possiamo avere la differenziazione in<br />
macrofagi normali oppure quando vengono attivati dai linfociti T ad esempio possono andare incontro o a<br />
necrosi del tessuto stesso o formazione di fibrosi. Quali sono le fasi? In un primo momento abbiamo un<br />
reclutamento dei monociti nel tessuto a livello del microcircolo; questi, una volta reclutati riescono a<br />
superare il vaso e una volta arrivati nella zona extravasale iniziano una serie di divisioni e alcuni diventano<br />
macrofagi della zona, mentre altri continuano la divisione in base agli stimoli che hanno avuto. Come vi<br />
dicevo, le altre cellule che concorrono a questo processo sono i leucociti che a seconda del loro agente<br />
stimolate possono addirittura trasformarsi in neutrofili, per esempio, o addirittura in macrofagi oppure<br />
riformarsi come neutrofili (ragazzi, mi dispiace ma questa secondo me sta dando i numeri … io vi sto solo<br />
riportando le sue testuali parole.. varrà la pena controllare poi dalle slide quello che sta dicendo). Abbiamo,<br />
poi, le plasmacellule che in genere originano dai linfociti B; a volte noi ritroviamo nell’infiammazione i<br />
prodotti delle plasmacellule e quindi riconosciamo la cellula per la stimolazione che ha dato e per la<br />
morfologia della cellula stessa.. la plasmacellula è classica perché ha il nucleo caratteristico tipo a ruota di<br />
carretto, quindi c’ha queste raggiere che ci dicono che è una plasmacellula e quindi queste agiscono<br />
direttamente con una risposta immunitaria verso l’antigene specifico dando immunoglobuline specifiche e<br />
aspecifiche. Possiamo avere gli eosinofili che si ritrovano molto nelle infiammazioni in genere provocate da<br />
parassiti, nelle infiammazioni allergiche; l’azione degli eosinofili caratterizza quello che è un processo<br />
infiammatorio totalmente allergico. Possiamo avere i mastociti che contribuiscono a produrre delle sostanze<br />
per la formazione di fibrosi.<br />
Abbiamo definito l’infiammazione come infiammazione interstiziale e infiammazione granulomatosa. Gli<br />
eventi sono molto diversi. Nell’ infiammazione INTERTSTIZIALE abbiamo come protagonisti sempre le solite<br />
cellule che però hanno una distribuzione piuttosto sparsa, non solo nella zona lesa.. abbiamo una<br />
ristrutturazione piuttosto disordinata; queste infiammazioni possono essere associate ad alcuni quadri di<br />
sclerosi nell’organo colpito. La ritroviamo in alcuni quadri come ad esempio quelli dell’appendicite cronica ..<br />
L’infiammazione GRANULOMATOSA oltre a riconoscere dei fenomeni vascolari essudativi, con in genere<br />
essudati anche copiosi, vi possono essere delle modificazioni molto particolari costituite da quelle che<br />
chiamiamo cellule giganti. Le cellule giganti sono dei segni patognomonici per quanto riguarda alcune<br />
infiammazioni. Le cellule giganti, chiamate così nell’infiammazione cronica, hanno la caratteristica di avere<br />
dei nuclei in numero superiore alla norma., cioè ha più di un nucleo e questi nuclei sono organizzati in un<br />
certo modo. Ricordate la forma dell’organizzazione nucleare, perché in base all’organizzazione nucleare si<br />
distinguono altre cellule giganti … quando farete il linfoma di hodgkin vi ricorderete di questo concetto;<br />
quindi sono cellule chiamate epitelioidi oppure cellule giganti. Questa (figura) è una colecistite, anzi no ..<br />
scusatemi.. è un’appendice (iamm che cazz!).. è un’appendicite cronica macroscopicamente. Questo è il<br />
nostro reperto, invece, che abbiamo prodotto in laboratorio… e vediamo che è un’infiammazione<br />
granulomatosa perchè gli infiltrati sono sparsi e invadono completamente la zona, ma vedete queste zone<br />
chiare? Queste zone chiare non sono altro che cellule epitelioidi. Questa invece (figura) è una colecisti dove<br />
l’infiltrato infiammatorio è completamente sparso però non c’è la presenza di cellule epitelioidi. Com’è la<br />
composizione del granuloma? Questa immagine è molto didattica : fondamentalmente vediamo che è<br />
circoscritto ed è costituito da una serie di cellule completamente diverse le une dalle altre; esternamente<br />
c’è una corona di cellule che sono le nostre cellule fibroblastiche, internamente troviamo una corona di<br />
leucociti e all’interno troviamo una corona di macrofagi che se vengono attivati da determinati stimoli, da<br />
determinate citochine, vanno a formare le cellule giganti; vi ricordo di guardare attentamente la morfologia<br />
di queste cellule e la disposizione nucleare perché vedete che tutta la cellula è un unico citoplasma unito tra<br />
di loro, incastrato e omogeneizzato allo stesso tempo l’uno dentro l’altro, ma i nuclei si spostano alla<br />
scaricato da www.sunhope.it
periferia di tutta la composizione della cellula neoformata; quindi si formano circolarmente attorno ad un<br />
citoplasma.. perché vi ripeto, si sono fusi i citoplasma.. si sono omogeneizzati tra di loro. Questa invece<br />
(figura) è la formazione di un granuloma, però vedete che la composizione del granuloma è completamente<br />
diversa da quello precedente. Se volessimo tornare indietro, una cosa che ho dimenticato e ci tengo a dirla<br />
è che quello che è importante e va sempre valutato è l’interno del granuloma. Potremmo avere che questo<br />
interno può essere costituito da qualcos’altro; in questo caso abbiamo una necrosi caseosa e questo è<br />
quello che succede nelle infiammazioni tubercolari; però è pur vero che possiamo avere altre sostanze.<br />
Quindi noi riconosceremo l’interno del granuloma e in base a quello che contiene possiamo risalire al tipo di<br />
granuloma e quindi al tipo di infiammazione. Qui (figura) vedete un corpo estraneo e il processo di<br />
infiammazione è andato oltre proprio perché il corpo estraneo non è stato completamente espulso e come<br />
obiettivo finale da parte dell’organismo c’è la formazione del nostro granuloma per neutralizzare<br />
completamente l’agente patogeno che nel nostro caso è un corpo estraneo e quindi c’è l’organizzazione<br />
morfologica di queste cellule, macrofagi, cellule epitelioidi ecc. che addirittura circoscrivono l’agente. Qui<br />
(figura) vedete sempre la formazione di un granuloma, però la differenza sta nel fatto che lungo la<br />
maturazione del granuloma stesso, poiché è una risposta immune, questa ci può portare alla formazione di<br />
necrosi. Quindi se abbiamo di fronte un granuloma caseoso, noi risaliamo a un’infiammazione polmonare;<br />
se invece nel granuloma abbiamo una cavità dove c’è una necrosi, allora la situazione cambia<br />
completamente e questo si verifica spesso nelle reazioni immunologiche. Qual è l’evoluzione dei granulomi?<br />
Vedete qui che i nuclei sono completamente alla periferia della cellula, sono 4. Questa è appena appena<br />
evidente perché il taglio è fatto a questo livello.. badate che qui la corona si chiude e non la vedete bene<br />
perché il taglio è stato fatto ad un piano più alto rispetto ad un piano del tessuto che stiamo esaminando.<br />
Questo ve lo dico perché non si tratta di una formazione a ferro di cavallo come a volte succede in altre<br />
cellule epiteliali. Questi granulomi possono andare incontro ad un’evoluzione cavitaria, ad una fibrosi<br />
oppure ad una calcificazione. Quali sono le caratteristiche più importanti dei granulomi? La fugacità dei<br />
fenomeni vascolari, la presenza di fenomeni produttivi, la presenza esclusiva di cellule giganti e<br />
un’evoluzione che può portare alla necrosi oppure una guarigione in sclerosi. Noi<br />
ieri abbiamo parlato dell’essudato, però quello che mi interessa è che l’evoluzione di questo essudato<br />
nell’infiammazione cronica si può organizzare e caratterizzare nella classica infiammazione cronica<br />
aspecifica, speciica oppure granulomatosa. INFIAMMAZIONE CRONICA ASPECIFICA: processo che avviene<br />
con una retrazione e una cicatrizzazione della lesione stessa. Abbiamo il prevalere degli effetti nocivi, vi è<br />
necrosi, infiltrazione neutrofila e modesta fibrosi che prevalgono nella zona marginale della lesione. Questo<br />
è il castrico esempio dell’ulcera gastrica, nelle brochiectasie, nella fibrosi polmonare e addirittura nel lupus.<br />
Questa è l’imagine che stabilisce questa forma di infiammazione cronica aspecifica perché questo è uno<br />
stomaco.. questo è l’epitelio normale e qua c’è un’escavazione, questi sono gli strati della muscolaris<br />
mucosae , mentre dove c’è l’escavazione la struttura è completamente cambiata e a questo livello troviamo<br />
una necrosi e al di sotto della necrosi vediamo la zona di fibrosi che si è venuta a creare per reagire alla<br />
lesione. Qui c’è un tessuto di granulazione nuovo, formato e qui invece è una zona prettamente<br />
vascolarizzata … quindi vedete che dopo l’escavazione che si è avuta nel tessuto sottostante c’è questa<br />
nuova rigenerazione. Questo (figura) è u polmone dove c’è appunto un’infiammazione aspecifica e vedete<br />
che qui c’è del pus e ci sono dei neutrofili; intorno possiamo trovare altre cellule tipo macrofagi, linfociti,<br />
plasmacellule ecc.. Vedete che c’è un’infiammazione quasi interstiziale perché è un’infiammazione proprio<br />
diffusa, nn solo a livello della cavità alveolare, ma anche nella zona circostante. Questo vedete è un polipo<br />
dell’intestino tagliato a livello longitudinale proprio lungo l’asse del polipo e qui invece vedete un’altra<br />
sezione di taglio.. si evince nel peduncolo del polipo una flogosi granulomatosa in questo caso e l’infiltrato<br />
che si evince vi fa capire che è un’infiammazione cronica aspecifica(ma non era granulomatosa? Mah!).<br />
Questo (figura) è un polmone con esiti cicatriziali dopo l’evento infiammatorio, dove vedete gli alveoli<br />
scaricato da www.sunhope.it
completamente deformati perché c’è la sostituzione in questi spazi della fibrosi, mentre qui invece si vede il<br />
processo di infiammazione. Questo (figura) è invece un derma, dove si evince chiaramente la fomazione di<br />
noduli mente il derma sottostante è caratterizzata da un’infiammazione espansiva. Questo( figura ) è un<br />
derma con cellule bianche che sono cellule adipose che con i processi di allestimento del preparato è<br />
andato via il grasso e determinano degli spazi.. ma nell’ambito di questo quadro quello che ci interessa non<br />
sono le cellule adipose, ma l’infiltrazione di queste altre cellule che sono macrofagi e c’è la formazione di<br />
cellule epitelioidi. INFIAMMAZIONE CRONICA SPECIFICA: c’è una risposta dei tessuti agli agenti infettivi e<br />
prevalgono sia le cellule linfoidi, i macrofagi, e c’è anche una diversa morfologia della fibrosi. L’infiltrato è<br />
costituito prevalentemente da linfociti come succede nell’epatite cronica attiva oppure come succede nei<br />
classici granulomi. Questo (figura) è un granuloma tubercolare, è facile dire che è un granuloma per la<br />
presenza delle cellule giganti e vedete che la morfologia è sempre la stessa con i nuclei alla periferia di tutta<br />
la cellula gigante e tutto intorno c’è un tessuto di granulazione specifico, in questo caso. Qui vedete il<br />
granuloma a piccolo ingrandimento, vedete i linfociti e non c’è la strozzatura nucleare dei neutrofili. Questo<br />
(figura) è quello che si evince dopo un infarto con il tessuto sano qui alla mia destra, mentre qui è un<br />
tessuto di granulazione che si sta realizzando poiché voi sapete che nell’infarto se l’infarto non ha<br />
un’intensità piuttosto massiva si può arrivare anche alla cicatrizzazione della lesione. In questa regione<br />
vedete tantissimi granulomi e mano mano questo tessuto viene sostituito in tessuto sano ma che ha una<br />
morfologia un po’ diversa rispetto al tessuto normale. Questo (figura) è un tessuto di granulazione ed è<br />
molto caratteristico perché ha le cellule dell’infiammazione abbastanza evidenti a piccolo ingrandimento e<br />
vedete che è un tessuto di granulazione piuttosto misto dove ci sono rappresentate tutte le cellule<br />
dell’infiammazione. Questa (figura) è una risoluzione del processo infiammatorio e questi tondini che<br />
vedete sono dei vasi, l’angiogenesi che abbiamo ricordato prima; oltre a questi vasi ci sono anche macrofagi<br />
e si viene a costituire quella che è la nostra fibrosi fino alla sostituzione, quindi alla formulazione in<br />
quest’altra immagine che vedete in cui i vasi sono completamente scomparsi mentre il tessuto è<br />
caratterizzato da fasci di fibrosi; se lo guardiamo a piccolo ingrandimento vediamo che sono rimasti solo<br />
pochi vasi. Questo è un po’ quello che abbiamo detto prima e quando non c’è la capacità di digerire l’agente<br />
patogeno possiamo avere l’infiammazione acuta che porta ad una persistenza dell’agente patogeno e dare<br />
una risposta immunocellulata oppure un sequestro all’interno dei macrofagi con un richiamo e la classica<br />
formazione della cellula epitelioide che va a costituire quella che è la fase del granuloma. In quest’altra<br />
figura (non ho capito che tessuto è) vedete che i granulomi sono piuttosto organizzati e tutt’intorno la<br />
popolazione è rappresentata da linfociti.. queste sono le classiche diagnosi differenziali che vengono fatte<br />
quando si ha il sospetto di un linfoma di hodgkin (non mi sembra che prima dica linfonodo, poi non so) e<br />
quello che noi andiamo a ricercare sono proprio le cellule giganti; il nostro piacere è trovare questa<br />
situazione qui e non trovare un non hodgkin. Questo (figura) è quello che vi dicevo prima e ricordatevelo: è<br />
una cellula gigante da corpo estraneo.. vedete che i nuclei sono tutti ammassati quasi al centro perché si<br />
sono addossati tutti attorno al corpuscolo estraneo. Qui (figura) è la classica cellula gigante dove i nuclei si<br />
organizzano alla superficie della cellula stessa a ridosso della membrana. Qui (figura) c’è un corpo estraneo<br />
e vedete che le cellule sono organizzate un po’ intorno. Abbiamo finito … (cià prufessorè)<br />
scaricato da www.sunhope.it
PARATIROIDI CONTINUAZIONE<br />
Le cellule delle paratiroidi più che diverse rappresentano parti di sviluppo diverse, cellule<br />
principali, cellule chiare e cellule ossifile, abbiamo visto l’altra volta come con il passare dell’età<br />
diminuiscano le principali mentre aumentano le chiare e le ossifile, quindi probabilmente queste<br />
ultime rappresentano una fase di evoluzione ma anche di regressione di queste cellule in rapporto<br />
all’età. Non vi parlo dell’ iperparatiroidismo, lo vedrete direttamente sul libro, si tratta di particolari<br />
sindromi come il morbo di Recklinghausen, cioè iperparatiroidismo primario perché legato ad 1<br />
ipersecrezione autonoma di PTH, che nella maggior parte dei casi ritroviamo in adenomi, iperplasie<br />
e solo nell’1% in carcinomi che per le paratiroidi sono piuttosto rari; poi secondario quando c’è<br />
un’ipersecrezione legata ad altre cause, per esempio in una condizione di ipocalcemia cronica come<br />
si viene a verificare in un’acidosi tubulare renale, secondario, quindi, perché c’è 1 altra causa;<br />
terziario, invece, quando in corso di iperparatiroismo secondario si sviluppano dei cloni cellulari<br />
autonomi, che non sono più sensibili ai meccanismi di feedback, quindi si comportano come se<br />
fossero delle cellule di adenoma. Analogamente per l’ipoparatiroidismo abbiamo 1 ipop. Primario,<br />
1 secondario e il cosiddetto pseudoipoparatiroidismo, non legato tanto ad 1carenza di patatormone,<br />
quanto ad 1carenza di una proteina, l’EGFα che ha un’azione stimolante quando il PTH si lega ai<br />
recettori specifici, tutto questo lo trovate sul libro. Siccome questa è una patologia “di nicchia”, a<br />
Napoli c’è un reparto che lavora molto su questo. Iperplasia, adenoma e adenoma atipico sono<br />
situazioni diverse, certamente, ma che presentano dei punti di tangenza e quindi bisogna<br />
comprendere che è molto difficile la diagnosi differenziale in alcuni casi, in altri casi basta 1<br />
ragionamento corretto; per esempio, sappiamo che il rischio di iperplasia e tumori nelle paratiroidi<br />
spesso è legato a queste sindromi MEN, soprattutto nella MEN 1 il rischio di avere iperplasia o<br />
tumore delle paratiroidi si avvicina al 90%, nelle altre sindromi MEN, invece, abbiamo percentuali<br />
minori;qui abbiamo già un concetto da capire: quando parliamo di adenoma, l’adenoma è unico, le<br />
paratiroidi invece sono 4 nella norma (perché possiamo anche avere delle paratiroidi<br />
soprannumerarie), ma se sono 4, se c’è un’iperplasia, sono coinvolte tutte e 4, quando, invece, c’è<br />
un adenoma noi dobbiamo trovare un nodulo ben sviluppato e le altre 3 o normali, o (più spesso)<br />
quasi atrofiche perché c’è un’iperfunzione di una, già questo fa capire ai clinico-anatomici la<br />
differenza tra iperplasia e adenoma.<br />
L’iperplasia delle paratiroidi è spesso asimmetrica, normalmente il peso delle paratiroidi si esprime<br />
in mg, talvolta il peso di queste paratiroidi invece può raggiungere i 10g; sappiamo che le superiori,<br />
per motivi che non riusciamo ancora a spiegare, tendono ad essere più grosse delle inferiori,<br />
possono avere diversi pattern, a cellule chiare, etc, li troverete sul libro di testo.<br />
[IMMAGINE]Questa è un’iperplasia, vedete 2 ghiandole paratiroidi abbastanza grosse.<br />
Per l’adenoma delle paratiroidi c’è una preferenza per il sesso femminile di 3:1; la forma è<br />
aumentata, e tutti hanno 1 capsula, in questo caso è sottile ma ben evidente.<br />
L’istologia può essere varia ma è follicolare molto spesso, quindi ricorda la tiroide, raramente può<br />
essere pseudopapillare o alveolare; anche in questo caso,come per la tiroide, troviamo delle atipie<br />
citologiche; atipie citologiche e pleiomorfismo si possono ritrovare sia per gli adenomi che per i<br />
carcinomi, quindi se vogliamo fare 1 diagnosi differenziale tra iperplasia e adenoma: nell’adenoma<br />
possiamo trovare tessuto paratiroideo normale alla periferia del nodulo, nell’iperplasia, invece, no<br />
perché c’è un coinvolgimento diffuso di tutta la ghiandola; pleiomorfismo e atipie sono più<br />
dell’adenoma, all’interno del quale difficilmente troviamo lipidi, nella paratiroide normale così<br />
come nell’iperplasia possiamo trovare cellule chiare e legami lipidici soprattutto.<br />
Il carcinoma nella maggior parte dei casi è iperfunzionante, però più raramente da la sintomatologia<br />
tipica perché non ha un’iperfunzione tale da trasformarsi in una sindrome clinica.<br />
Quali sono le caratteristiche che ci consentono la diagnosi differenziale con l’adenoma?<br />
Le stesse del carcinoma follicolare:l’invasività capsulare, vascolare, cioè degli emboli nei vasi e in<br />
questo caso anche l’invasione perineurale, perché le neoplasie maligne oltre alle vie linfatica e<br />
scaricato da www.sunhope.it
vascolare seguono anche le guaine nervose, questo è 1 di quei casi. La prognosi a 5 anni è dell85%,<br />
a10anni scende all’80%.Ci sono delle caratteristiche cliniche o dei parametri che ci aiutano nella<br />
diagnosi differenziale? Sì. In genere, sia nell’iperplasia che nell’adenoma troviamo la parafibromina<br />
che è 1 proteina che non viene espressa dal carcinoma, è quindi un marker di benignità; nella<br />
situazione di benignità possiamo anche trovare 1 amplificazione di 1 gene oncosoppressore e della<br />
proteina relativa, cioè del p53, mentre nel cancro troviamo soprattutto un espressione della lectina3<br />
come nel carcinoma della tiroide, così come possiamo trovare un notevole aumento del Ki67,<br />
marcatore cinetico come detto altre volte e la ciclina D1. Dei caratteri citologici invece, abbiamo<br />
detto che non ci possiamo fidare molto. Mentre nell’adenoma l’iperparatiroidismo è sempre<br />
presente, nel carcinoma c’è l’iperfunzione ma non è tale da dare 1 quadro clinico.<br />
[IMMAGINI]Vedete c’è un punto lì dove c’è la freccia rossa dove si può vedere come il tumore ha<br />
raggiunto la capsula però non si può dire che l’abbia superata. In quest’altra immagine a fungo, il<br />
tumore si espande dopo aver superato la capsula fibrosa che offre una certa resistenza all’invasività:<br />
il tumore riesce a superarla e poi si espande. Il Ki67 è molto aumentato nel carcinoma, la PCL2,<br />
invece è aumentato nell’adenoma insieme con la parafibromina; questa la troviamo iperespressa in<br />
iperplasia e adenoma, non la troviamo nel carcinoma.<br />
Nelle sezioni criostatate per gli stessi motivi, come nelle diagnosi intraoperatorie per la tiroide sono<br />
inefficaci per capire da una sola sezione l’invasività e tutto il resto; per la citologia per aspirazione<br />
non c’è una grossa applicazione perché si tratta di ghiandole molto piccole, e poi non è escluso il<br />
rischio di disseminazione che succede per rari tumori, come per le neoplasie embrionarie del rene o<br />
per le neoplasie embrionarie in generale e questi tipi di carcinomi non si prestano alla citologia<br />
aspirativi perché lungo il tragitto con l’ago può determinare fenomeni di disseminazione tumorale,<br />
sono quindi controindicate.<br />
CERVICE UTERINA<br />
E’ fondamentale la giunzione squamo-colonnare. Perché? L’esocervice ha un epitelio pavimentoso<br />
stratificato perché è esposta ad 1 cavità aperta,è in un ambiente acido, come acido è l’ambiente della<br />
vagina per la funzione principale dei lattobacilli, presenti in particolari momenti dello sviluppo,<br />
addirittura oggi si osserva che l’abuso di detergenti, di lavande e così via può altrerare la<br />
composizione della flora, in modo tale da inibire lo sviluppo dei lattobacilli e favorire invece quello<br />
di cocchi, quindi coccobacilli, o miceti, paradossalmente la patologia da coccobacilli può derivare<br />
da eccesso di igiene. Perché la giunzione squamo-cellulare è all’orgine di tutto? Perché, ormai ne<br />
abbiamo l’evidenza,in questa zona abbiamo le cellule di riserva, le staminali, che si piazzano<br />
furbamente in punti strategici perché se c’è qualcosa che non va nell’epitelio cilindrico<br />
endocervicale loro se ne vanno sopra a riparare, se c’è qualcosa che non va in basso, loro vanno giù<br />
a riparare l’epitelio pavimentoso stratificato; sono quindi cellule con potenzialità elevate, di<br />
ricostruire tutto l’organo volendo e si trovano in un posto da dove dominano sia il versante<br />
superiore, sia quello inferiore, endo e esocervice. Se un processo preneoplastico, una precancerosi<br />
ha origine, il suo punto di origine è proprio lì, quindi si spiega come queste cellule siano implicate e<br />
protagoniste della cancerogenesi, tant’è vero che quando si va a fare un PAP-test ( e pochi lo sanno<br />
fare, perché bisogna prendere proprio questa zona) poi ve ne parlerò.<br />
[IMMAGINE]Ecco la giunzione: questo è l’epitelio pavimentoso stratificato e questa è<br />
l’endocervice dove si nota la posizione basale dei nuclei e questo è l’epitelio colonnare in cui il<br />
nucleo appunto sta alla base vicino al connettivo, mentre il citoplasma sta su ed è un citoplasma<br />
mucoide.<br />
Come varia questa giunzione squamo colonnare in rapporto all’età? Importante anche per la tecnica<br />
del PAP-test. In fase pre-puberale l’orifizio squamo colonnare si localizza all’interno del canale<br />
endocervicale, durante l’adolescenza c’è però questo movimento, quasi che si retraesse l’epitelio<br />
squamoso e possiamo avere una piccola eversione, perché una parte dell’endocervice si viene a<br />
trovare quasi aperta fuori che è un fenomeno parafisiologico che si vede anche colposcopicamente<br />
scaricato da www.sunhope.it
come un’area rossastra perché è una mucosa endocervicale che si trova accanto ad 1epitelio<br />
squamoso, questo fenomeno si chiama eversione e quando è particolarmente evidente, può<br />
succedere anche in donne che hanno avuto gravidanze o particolari patologie infiammatorie, quando<br />
quest’eversione è particolarmente estesa allora parliamo di ectropion; cmq nell’adolescenza c’è<br />
questa eversione, poi, nella fase post-adolescenziale che succede?Questa zona di eversione<br />
dell’endocervice,a contatto con i lattobacilli che normalmente non ci sono nell’endocervice, per<br />
l’acidità e per gli stimoli ambientali va incontro ad1metaplasia squamosa ed è allora che la<br />
giunzione “sembra”risalire(perchè non è 1risalita) perché quella parte di epitelio endocervicale che<br />
sporgeva 1po’ verso l’esterno si è trasformata in metaplasia squamosa, quindi non ha in questo caso<br />
significato oncologico. Nella menopausa, per 1serie di infiammazioni, gravidanze e così via<br />
abbiamo il fenomeno inverso di inversione, cioè la giunzione squamo-colonnare se ne sale sopra, è<br />
1risalita secondaria indotta da questi fenomeni progressivi di metaplasia squamosa. Questo significa<br />
che in periodo post-menopausa se noi andiamo a fare 1colposcopia è difficile che riusciamo a<br />
vedere la giunzione, non perché non c’è ma perché sta dentro.<br />
[IMMAGINI] La metaplasia squamosa.Questo è 1epitelio pavimentoso stratificato, potreste dirmi<br />
che è un’esocervice, chi mi dice che è una metaplasia squamosa? Questa è una ghiandola mucoide<br />
che ci dice che siamo nel canale. Questo è frequentissimo nelle donne, che a volte cioè ci siano dei<br />
sanguinamenti, delle perdite, non tanto legate all’endometrio ma all’endocervice;inoltre possiamo<br />
avere episodi di endocervicite cronica, dove la mucosa endocervicale rimane cilindrica e fa delle<br />
micropapille, il termine tecnico è endocervicite micropapillare, quando le vedete così è perché la<br />
lama del microtomo le ha tagliate di trasverso,fenomeno frequente; così come sono frequenti queste<br />
che nell’antichità chiamavamo uova di Naboth, cioè che queste ghiandole endocervicali soprattutto<br />
con l’età tendono a diventare cisti dove col passare degli anni qualche dotto escretore si blocca e<br />
allora la ghiandola che sta sotto forma 1struttura cistica, si chiamano uova di Naboth perché Naboth<br />
pensava fossero uova, invece sono delle cisti. Questa è 1iperplasia microghiandolare e qui le<br />
ghiandole sono così piccole che a stento si vedono; si sa che queste iperplasie microghiandolari di<br />
cui si discute sono legate soprattutto all’assunzione di estrogeni e progesterone, quindi soprattutto<br />
all’uso della pillola, anche se non si conosce ancora bene il significato e se possa essere correlato a<br />
quale cosa. E questa è 1delle patologie più frequenti, i cosiddetti “polipi” polipi tra virgolette perché<br />
spesso le infiammazioni determinano 1 spinta verso l’alto dell’epitelio endocervicale e si formano<br />
come delle protrusioni che non hanno significato oncologico, vedete qua c’è un’emorragia,<br />
un’infiammazione che determina una fibrosi, una protrusione e quindi un polipo cervicale.<br />
Le infezioni HPV possono essere di vario tipo dal punto di vista macroscopico, innanzitutto<br />
possono non avere alcun segno, nei portatori di HPV se andiamo a fare l’esame colposcopico non<br />
troviamo niente, talvolta il PAP-test è positivo ,ma andando a fare lo colposcopia non si trova<br />
niente; ma laddove c’è una lesione possiamo avere il condiloma acuminato che in sede cervicale è<br />
molto raro, più frequente a livello perianale, acuminato perché assume una forma un po’ a<br />
cavolfiore, molto esuberante; il condiloma piatto quando, invece, non assume questa forma<br />
esofitica, vegetante, ma è solo piatto e molto spesso corrisponde a quelle aree biancastre che si<br />
vedono, biancastre perché a volte l’epitelio reagisce formando uno strato corneo, anomalo di cui<br />
parleremo, quasi per reagire all’infezione virale, vi hanno parlato di colposcopia? Sapete che ci<br />
sono anche dei coloranti come l’acido acetico, il Lugol e così via…e poi possiamo avere il<br />
papilloma che è una lesione unica con uno o più assi connettivo-vascolari delimitati da<br />
quest’epitelio pavimentoso stratificato e, addirittura, in casi rari, possiamo avere un papilloma<br />
invertito perché mentre solitamente il papilloma tende a crescere all’esterno, nel canale<br />
endocervicale, l’invertito, invece, se ne va dentro, in profondità, però questo fortunatamente<br />
succede raramente perché può creare dei problemi dal punto di vista della diagnostica; ma<br />
soprattutto tutte queste lesioni, microscopicamente diverse, hanno una caratteristica citologica<br />
comune che si chiama COILOCITOSI, poi la vedremo.<br />
scaricato da www.sunhope.it
[IMMAGINI]Ecco il condiloma, vedete, sono tutte queste creste, queste papille, spesso tagliate<br />
trasversalmente che danno l’impressione di insulae con un piccolo asse connettivale al centro<br />
tutt’intorno delimitato da epitelio pavimentoso stratificato; questo è il condiloma piano, quello che<br />
voi vedete qui, vedete queste zone, queste cellule particolari? Queste corrispondono ad 1 coilocitosi,<br />
qual è la loro caratteristica di base?Anzitutto possiamo vedere una zona che presenta un alone<br />
chiaro perinucleare ben evidente, il nucleo sembra immerso nel vuoto, poi la membrana<br />
citoplasmatica sembra ispessita, come se si condenssasse alla periferia, dentro c’è il vuoto, e poi la<br />
caratteristica più importante, qui non la vedete ma la vedrete dopo, eccola,[altra immagine] i<br />
margini della zona chiara sono netti, quasi una nettezza geometrica, come se tagliati, legati alla<br />
condensazione del citoplasma per cui si crea una nicchia geometrica in cui si trova il nucleo che poi<br />
difficilmente ha 1forma ovalare ma spesso è raggrinzito, gli americani usano il termine a “uva<br />
passa”che è grinzosa, forma delle pieghe, e così è questo nucleo; quindi le3caratteristiche:<br />
vacuolizzazione del citoplasma, la marginalizzazione del citoplasma che crea una chiara<br />
evidenziazione di questa zona vacuolizzata e poi il nucleo ad uva passa.<br />
[IMMAGINE]Qua vedete un’altra caratteristica, guardate questi filamenti sopra a tutto, sembrano<br />
lamelle cornee, ma vedete qualcosa in queste lamelle cornee? Come si chiama questa situazione?<br />
Questo è 1indizio di un disordine cinetico, perché solitamente lo strato corneo è rappresentato da<br />
citoplasma, cellule cornee, se arriva il nucleo lì vuol dire allora che le cellule non sono ancora<br />
completamente cornee, vuol dire che c’è 1accelerazione cinetica tale che le cellule arrivano sopra a<br />
formare lo strato corneo quando non sono ancora pronte , questo fenomeno prende il nome di<br />
PARACHERATOSI, differente dalla discheratosi, lo vedremo più avanti.<br />
Parliamo della DISPLASIA.<br />
Quest’immagine voi già la conoscete, non la commento, ricordate che la displasia lieve riguarda il<br />
terzo inferiore, la grave riguarda tutto lo spessore dell’epitelio, quindi cellule atipice identificate in<br />
tutto lo spessore dell’epitelio, la moderata è 1situazione intermedia quando sono coinvolti i 2/3<br />
dell’epitelio; vi ricordo anche altre 2 cose molto importanti: la displasia si chiama lieve quando<br />
parte dal basso, perciò si chiama lieve quando è in partenza, quando invece ha coinvolto tutto<br />
l’epitelio è arrivata al suo top e ancora ricordate che la membrana basale non dev’essere superata,<br />
nel caso non è più displasia. Tra displasia grave e carcinoma in situ potremmo avere uno di quei<br />
dibattiti differenzivi che non finiscono più, pensate che praticamente, clinicamente e dal punto di<br />
vista terapeutico ma anche anatomo-patologico sono 2situazioni talmente simili che è inutile<br />
bombardarvi di nozioni inutili, perché sono praticamente la stessa cosa anche se non tutti sono<br />
d’accordo. Nella valutazione di queste displasie si confrontano 2sistemi: il sistema CIN è quello più<br />
antico, il sistema SIL quello più moderno. Quali sono le differenze tra i 2?<br />
Il sistema CIN (neoplasia intracervicale) è il sistema tradizionale, SIL significa squamose intra<br />
lesion. CIN si differenzia in:<br />
CIN1 displasia lieve;<br />
CIN2 displasia moderata;<br />
CIN3 displasia grave.<br />
A questo punto a Bethesda ( in America) c’è un istituto oncologico dall’immagine prestigiosa in tutt<br />
il mondo perché parte delle classificazioni partono da questo istituto, creò il SIL che riconosce solo<br />
due classificazioni:<br />
L-SIL basso grado;<br />
H-SIL alto grado.<br />
L-SIL corrisponde solo al basso grado (CIN1) e alla coilocitosi perchèla displasia lieve può esserci<br />
da sola, ma nella maggior parte dei casi è associata alla coilocitosi e allora se scriviamo L.SIL<br />
dobbiamo precisare se c’è coilocitosi, se displasia, se entrambe sono presenti.<br />
E’ quindi una semplificazione del sistema CIN che nasce dal fatto che il ginecologo se ha una<br />
displasia grave sa cosa fare, fa 1conizzazione, ma se ha displasia moderata, non sa come<br />
comportarsi e allora si è risolto il problema facendo una categorizzazione netta (che io non<br />
scaricato da www.sunhope.it
condivido), quindi nell’H- SIL noi troviamo la displasia moderata e la grave;ovviamente questo<br />
impone delle forzature, perché se il patologo mette displasia moderata destina la paziente alla<br />
conizzazione, in realtà già la classificazione è 1forzatura.<br />
Nel sistema CIN, inoltre c’era maggiore considerazione dell’adeguatezza del campione(del PAPtest),<br />
per cui questo poteva essere adeguato, inadeguato o valutabile ma limitato da scarsità<br />
cellulare, etc. ora è adeguato o inadeguato, sì o no.<br />
Qual è l’evoluzione clinica di un L-SIL? Questo può andare in regressione, scompare nel 62% dei<br />
casi quindi la conizzazione non è giustificata tranne quando l’L-SIL è diffusa un po’ a tutta<br />
l’endocervice, l’estensione può essere un motivo; può mostrare resistenza nel 22% dei casi, può<br />
progredire in una minoranza del 16% dei casi e l’atteggiamento più razionale è quello di attendere.<br />
H-SIL, invece, è un carcinoma e può essere invasivo,in 3 anni può essere del11%, a 5 anni il22%, a<br />
9 anni il 33% quindi è giustificata la conizzazione.<br />
Nell’endocervice abbiamo un adenocarcinoma che quindi si differenzia dal carcinoma squamoso<br />
dell’esocervice, un 15% dei tumori della cervice ha 1struttura ghiandolare. Anche in questo caso<br />
abbiamo una displasia di basso grado, una displasia di alto grado e un carcinoma in situ che è<br />
assimilabile all’alto grado, però questa situazione del’endocervice è meno conosciuta, meno<br />
studiata, meno analizzata nel suo significato clinico perché tutti abbiamo focalizzato la nostra<br />
attenzione su significato CIN e SIL.<br />
[IMMAGINE] Qui vi ho segnato con delle frecce tutti quei nuclei più a uva passa, questa, vedete,<br />
è1mitosi iniziale. Vedete qui c’è una situazione di displasia lieve perché colpisce il terzo inferiore,<br />
anche qui non vediamo più le cellule disposte a palizzata come dovrebbero essere e in superficie<br />
vediamo questa coilocitosi e addirittura qua vediamo la paracheratosi, quindi troviamo le<br />
3caratteristiche basi. Inizialmente la gravità del carcinoma non veniva correlata al virus, perché<br />
laddove questo era presente potevamo non trovare cellule coilocitiche( la coilocitosi è1effetto<br />
citopatico indotto dal virus) , ma ciò testimonia un’altra caratteristica di questo virus, che si integra<br />
nel menoma; la vacuolizzazione del citoplasma nella coilocitosi è legata alla replicazione del virus,<br />
invece questo virus si può integrare nel genoma, anche in maniera episomiale, e questo succede<br />
soprattutto nel cancro; se noi facciamo l’immunoistochimica non possiamo identificare il DNA,<br />
l’RNA e così via , ma possiamo identificare gli antigeni dell’envelope, della capsula, e trovavamo<br />
queste positività nella displasia lieve che tendevano a scomparire nella displasia grave e nel cancro,<br />
perché lì non c’era replicazione matura dell’envelope e di tutto il resto e allora una corrente di<br />
pensiero pensò che il virus non aveva niente a che vedere con il cancro, si è visto invece che ha a<br />
che vedere e poi vedremo perché.<br />
[IMMAGINE]Questa è 1displasia severa però vedete queste cose qui, queste sono emazie, sono i<br />
vasi, incomincia a gettare il suo sguardo maligno sullo stroma, vedete come la membrana basale si<br />
assottiglia o si ispessisce, insomma sta subendo fenomeni di oscillazione e talvolta questa displasia<br />
si estende alle ghiandole, questa ghiandola è normale ma questa no, è metaplasma squamosa con<br />
displasia di alto grado, quindi quando si fa la conizzazione bisogna stare ben attenti a prendere<br />
anche le ghiandole perché il processo può persistere, conizzazione che va fatta rispettando<br />
l’anatomia dell’utero a seconda anche della paziente.<br />
Se andiamo a fare il Ki67, a testimonianza di quanto vi dicevo nella parte generale c’è 1disordine<br />
cinetico, in un epitelio normale le cellule in fase proliferativi sono quelle dello strato basale e<br />
parabasale, che sono le cellule meno differenziate, se invece andiamo a vedere la displasia vedete<br />
che queste tendono ad estendersi verso l’alto, a testimonianza del fatto che si è perso un gradiente<br />
maturativo.<br />
Noi sappiamo che il 16 e il 18 sono i virus più frequentemente coinvolti nel cancro e la<br />
vaccinazione riguarda solo questi 2ceppi, molti altri ceppi incidono in misura minore ma per un<br />
totale superiore al20% e sono considerati a rischio intermedio o a basso rischio; allora io ho molti<br />
dubbi sulla vaccinazione, anzitutto perché noi siamo coperti per il63%, ma per un 37%dei casi<br />
questa non ci copre, poi non ci sono ancora studi sufficienti per dirci quanto è durevole questa<br />
vaccinazione o che ci dicono bene i risultati, inoltre la certezza di essere completamente coperti<br />
scaricato da www.sunhope.it
induce dei comportamenti sessuali ad alto rischio e quindi aumenta il rischio di contrarre uno di<br />
questi altri virus; e poi c’è un altro problema, l’adenocarcinoma della cervice, che addirittura per<br />
quanto riguarda la malignità è molto maggiore dello squamoso e poi non sono d’accordo che ad<br />
1bambina di11-12 anni, nonostante i tempi siano evoluti, vadano spiegate tutte queste cose, credo<br />
che in alcuni casi possa rappresentare 1traumatismo e ci sono d’altronde degli interessi economici<br />
spaventosi, inoltre l’efficacia del vaccino dipende molto anche dal tipo e dal numero di rapporti<br />
contratti che ovviamente fanno aumentare il rischio. Ma perché il 16 e il 18 hanno un potenziale<br />
maggiore?Perchè questi virus producono delle proteine che hanno una qualche diversità fra di loro,<br />
soprattutto l’E6 e l’E7 molto efficaci a bloccare sia la proteina codificata dall’Rb sia la p53, sia altri<br />
oncosoppressori, mentre le proteine codificate da altri virus sono meno efficaci. Quindi interazione<br />
con Rb, p53, effetti sulla proliferazione e sull’immortalizzazione della cellula, quindi inibizione<br />
dell’apoptosi, aumenta la spinta verso il processo neoplastico; in condizioni invece normali può<br />
succedere che si determinano un’inibizione delle telomerasi, una instabilità dei centrosomi, una<br />
metilazione dei promotori, per cui si va verso la senescenza replicativi, come è normale che quando<br />
una cellula devia vada verso una senescenza replicativase questo non succede ha inizio un processo<br />
che coinvolge tutta una seri di proteine oncosoppressori; ed è così perché se confrontiamo<br />
l’incidenza di infezione virale con il cancro, c’è un rapporto molto particolare: vedete l’infezione da<br />
papilloma virus tra i24 e i 29 anni raggiunge il suo apice per poi discendere fino ai 64; il cancro,<br />
invece , raggiunge il suo apice ad 1distanza di 10, 15 anni, questo è il tempo di latenza affinché<br />
accadano tutta una serie di fenomeni che determinano il cancro; il PAP- test soprattutto in occidente<br />
ha avuto un grande successo, lo dimostra il fatto che nel 1948 l’incidenza del cancro alla cervice era<br />
di 34/100000casi oggi l’incidenza è inferiore a 10/100000casi, quindi c’è stata una riduzione<br />
drastica del cancro alla cervice e, inoltre, quando vengono trovati dei cancri, vengono trovati in uno<br />
stadio iniziale che non era quello di una volta che invece era piuttosto invasivo ed aggressivo.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> Patologia 15/11/2010<br />
Prof. Rossiello.<br />
Concludiamo la cervice.<br />
Questo che vedete è una specie di mappamondo dell’American Cancer Society (A.C.S)<br />
che rappresenta l’incidenza del cancro della cervice uterina nelle diverse aree<br />
geografiche. Come potete vedere,l’incidenza va da quest’area a righe,fino al rosso,dove<br />
c’è l’incidenza più alta. I paesi musulmani per ovvi motivi hanno una bassa incidenza,per<br />
altri motivi l’Australia,mentre le regioni occidentali,compresa l’Italia si situano in una zona<br />
bassa comunque,con un’incidenza tra i 7.3 e 16.2 per 100.000 donne per anno. Ci sono<br />
paesi dell’America latina e della zona centro africana che hanno un’incidenza che arriva a<br />
superare 42 per 100.000 casi,che poi non si discosta molto dall’incidenza che avevamo<br />
dalle nostre parti 50-60 anni fa.<br />
Per definizione,il carcinoma della cervice è il carcinoma squamoso,ed è quello più<br />
importante. Per squamoso s’intende che tende ad una differenziazione squamosa,tende<br />
perché può avere comunque vari gradi di differenziazione.<br />
Quindi le cellule vagamente(perché sono cellule atipiche) ricordano cellule che hanno un<br />
citoplasma acidofilo. Però qui c’è un concetto fondamentale che condiziona tutto il<br />
trattamento chirurgico e anche tutta la valutazione prognostica: dipende dall’estensione<br />
del cancro. In che modo?<br />
Noi distinguiamo un carcinoma microinvasivo e un carcinoma invasivo.<br />
Per arrivare a questa categorizzazione ci sono voluti decenni di studi e si è visto che<br />
quando un carcinoma della cervice viene preso in tempo utile,certamente è meglio<br />
prenderlo quando c’è la displasia,ma anche se abbiamo superato la fase di displasia e di<br />
ca in situ,l’importante è che non sia diventato invasivo e non abbia superato questi limiti:<br />
cioè che abbia una profondità secondo un asse longitudinale che non superi i<br />
5mm,ovviamente è una valutazione che si fa al microscopio,e abbia un’estensione<br />
laterale, quindi trasversale che non superi i 7mm. Quindi sono due i parametri:la profondità<br />
e l’estensione. Se il carcinoma è al di sotto di questi due limiti (5 e 7 mm) lo classifichiamo<br />
come carcinoma microinvasivo,e questo ha grande importanza ai fini della prognosi e del<br />
trattamento chirurgico.<br />
scaricato da www.sunhope.it
Il carcinoma invasivo invece può essere di tre tipi istologici:<br />
a grandi cellule: -cheratinizzante<br />
a piccole cellule<br />
-non cheratinizzante<br />
Cheratinizzante è quando fa materiale corneo,cheratina,non cheratinizzante quando<br />
questa formazione non c’è. Quindi i tipi sono 3:a grandi cellule,suddiviso in due<br />
sottotipi:cheratinizzante e non cheratinizzante e a piccole cellule.<br />
Poi ovviamente abbiamo anche qui un grading di cui parleremo più avanti: T1 ben<br />
differenziati, T2 moderatamente differenziati,T3 poco differenziati.<br />
Poi abbiamo il carcinoma verrucoso ,molto spesso legato all’infezione da Papilloma virus<br />
in maniera proprio intima,tant’è vero che a volte troviamo addirittura la coilocitosi. E si<br />
chiama verrucoso perché somiglia ad una verruca,cioè ad un’escrescenza,ed ha anche<br />
un’altra caratteristica,cioè che è cosi ben differenziato,perché forma cheratina,molta, che<br />
presenta qualche difficoltà nella distinzione con le lesioni benigne da HPV,anche perché è<br />
difficile trovare l’invasività. Dal punto di vista istologico è il tipo più differenziato che esiste.<br />
Abbiamo poi il carcinoma a cellule fusate. Questo carcinoma è come se assumesse un<br />
fenotipo quasi mesenchimale: abbiamo transdifferenziazione.<br />
Però,come ci accorgiamo che è un carcinoma e non è un sarcoma? Perché se le cellule<br />
sono fusate,per prima cosa uno pensa ad un sarcoma. Allora se uno ha esperienza con gli<br />
occhi se ne accorge subito,ma se si vuole una conferma,basta fare la citocheratina.<br />
Queste cellule esprimono la citocheratina e possono anche coesprimere la vimentina;coè<br />
è come se fossero cellule che non hanno ancora deciso se essere epiteliali o<br />
mesenchimali. Le cellule fusate del sarcoma sono invece sempre citocheratina negative.<br />
Quindi possiamo capire che si tratta di un carcinoma squamoso a cellule fusate perché ha<br />
la citocheratina.<br />
Poi abbiamo il carcinoma a cellule basalioidi, che non ha niente a che vedere con il<br />
carcinoma basocellulare che è un cancro di serie b. In questo caso è un cancro di serie a.<br />
Il basalioma è un tumore cutaneo,maligno relativamente perché non da mai<br />
metastasi,quindi si può essere relativamente ottimisti sui basaliomi. Questo invece no,è un<br />
scaricato da www.sunhope.it
carcinoma abbastanza aggressivo.<br />
Basalioide perché queste sono cellule che hanno scarso citoplasma,quindi somigliano,ma<br />
è solo una somiglianza,alle cellule basali,che sono costituite soprattutto da nucleo e da<br />
scarso citoplasma.<br />
E poi abbiamo altre varietà di cui non parliamo proprio.<br />
Poi abbiamo l’adenocarcinoma. Fortunatamente incide per il 15% su tutte le neoplasie<br />
epiteliali maligne della cervice,mentre il carcinoma squamoso o carcinomi imparentati al<br />
carcinoma squamoso,come quello verrucoso incidono per l’85% sui carcinomi della<br />
cervice uterina. Fortunatamente,perché questo cancro,sotto il profilo della<br />
malignità,diciamo che ha una marcia in più!<br />
Perché è un carcinoma che nasce nell’endocervice e che tende precocemente a<br />
metastatizzare. Inoltre,poiché le cellule sono più profonde,è più difficile da cogliere nel<br />
Pap-test rispetto alla displasia grave. Abbiamo visto che nel concetto di SIL c’è anche la<br />
displasia delle ghiandole endocervicali e lo vedremo tra poco.<br />
L’adenocarcinoma è il carcinoma classico endocervicale. Può essere microinvasivo o<br />
invasivo. Valgono gli stessi concetti espressi prima per il carcinoma squamoso,cioè gli<br />
stessi limiti;però vi devo dire che raramente cogliamo l’adenocarcinoma nello stadio<br />
microinvasivo. Ne esistono diversi tipi,legati all’embriogenesi della sfera genitale<br />
femminile,per farvi capire che l’organizzazione di questi tessuti ha un comune<br />
denominatore di partenza e questo poi determina una serie di patologie strettamente<br />
correlate. Ne parleremo dopo.<br />
Può essere di tipo endocervicale,cioè un carcinoma che fa muco,oppure endometrioide<br />
cioè che somiglia a un carcinoma dell’endometrio e si vede perché il citoplasma è<br />
sieroso,ovvero eosinofilo,mentre nel tipo mucoide il citoplasma tende ad essere<br />
bianco,cioè non si colora,o debolmente basofilo,il muco cosi si vede. Poi abbiamo il tipo<br />
intestinale,pensate che aberrazione. Ma quando faremo l’embriogenesi vedremo che non<br />
è proprio un’aberrazione. Poi abbiamo il carcinoma villoghiandolare,che per ora non<br />
capirete e lo capirete quando parleremo dell’intestino. Tende comunque ad avere uno<br />
sviluppo villoso,immaginate un vegetale che ha uno sviluppo villoso,o immaginate le guglie<br />
del duomo di Milano: un carcinoma con delle digitazioni. Questo somiglia ad un tipo di<br />
carcinoma che abbiamo nell’intestino. Tipo “glassy cell”: cellula vitrea,cioè con una<br />
scaricato da www.sunhope.it
membrana nucleare molto spessa,una zona chiara centrale. Questa glassy cell somiglia<br />
alla gemella dell’orfanella anni.(?????)<br />
Tipo adenosquamoso vuol dire che in una stessa ghiandola possiamo trovare una<br />
componente di un carcinoma squamoso e una struttura di adenocarcinoma,come se ci<br />
fosse stata in questa ghiandola una metaplasia squamosa maligna. Quindi una parte è<br />
ghiandolare e una parte è squamosa. Tutte queste confusioni sono una ulteriore conferma<br />
del ruolo che hanno le cellule staminali,perché essendo cellule cosi come stanno nel<br />
momento in cui agisce una noxa neoplastica,nel momento in cui impazziscono,possono<br />
darci diversi quadri. A noi interessano questi quadri perché ognuno di essi poi ha una sua<br />
storia,un suo grado di malignità,e questo poi ci consente di esprimere un giudizio. A parte<br />
che poi c’è anche un problema di diagnosi,perché se uno non conosce che esiste il glassy<br />
cell nell’intestino,cioè a cellule vitree,può anche pensare ad una metastasi.<br />
Quindi c’è un problema di diagnosi e di prognosi.<br />
Per concludere,c’è un carcinoma che sta dovunque,nella mammella,nelle ghiandole<br />
salivari,nella cute,ecc,ne sentirete parlare moltissimo,ed è un carcinoma molto<br />
interessante che si chiama carcinoma adenoideo-cistico.<br />
L’aspetto più classico,gli americani dicono, somiglia ad un pattern a canne d’organo.<br />
Immaginate le canne d’organo tagliate trasversalmente: ha delle cavità geometriche. Ora<br />
vedere un cancro che fa dei cerchi geometrici,è una novità. Ma perché fa questi cerchi<br />
geometrici?non lo potete sapere,e fino a 10 anni fa non lo sapevamo neanche noi. Il<br />
motivo è che questo cancro non è fatto proprio di cellule epiteliali,ma è fatto da cellule<br />
cosiddette mioepiteliali. Molto spesso in quasi tutte le strutture ghiandolari,noi abbiamo<br />
parlato del sistema neuroendocrino,abbiamo detto che le cellule neuroendocrine hanno un<br />
ruolo di batterista,sono dei pace maker che danno il ritmo,però chi risponde a questi<br />
mediatori chimici sono queste cellule mioepiteliali che si dispongono alla periferia di<br />
queste strutture ghiandolari e sono delle cellule che hanno un fenotipo misto,muscolare ed<br />
epiteliale. Qual è la loro funzione? Quando si contraggono esce fuori la secrezione. È<br />
ovvio che la capacità di fare queste cellule mio epiteliali in un tessuto ghiandolare,risiede<br />
anche nelle cellule staminali,per cui questo cancro è un falso adenocarcinoma perché<br />
queste non sono ghiandole,ma sono cavità,perché queste cellule mio epiteliali secernono<br />
come un muco,il quale allontana le cellule tra di loro per compressione,e si creano delle<br />
cavità geometriche. Secerne oggi,secerne domani,si viene a creare un buco riempito da<br />
scaricato da www.sunhope.it
questo liquido. Questo tipo di cancro,che ha anche un aspetto strano,non è un cancro<br />
molto maligno,però ha una caratteristica quasi unica,pensate che anziché diffondersi per<br />
via ematica o per via linfatica, per motivi che non riusciamo ancora a spiegare,diffonde<br />
seguendo le guaine nervose. Noi vediamo che queste cellule si insinuano nei nervi tra le<br />
cellule di Shwann. Se vogliamo è una malignità locale estesa. Possono dare le<br />
metastasi,ma più raramente.<br />
Poi abbiamo,come in quasi tutti gli organi,il carcinoma neuroendocrino.<br />
Vediamo ora alcuni esempi istologici.<br />
Il carcinoma microinvasivo. Ecco voi vedete sopra che è un carcinoma sicuramente, e poi<br />
vedete l’invasività. Per esperienza vi posso dire che in questo caso è inferiore anche a<br />
2mm di profondità. Ma anche in superficie deve essere inferiore a 7mm. Qua vediamo solo<br />
un pezzo,ma si presume che sia circoscritto. Questo concetto di microinvasività vi deve<br />
essere chiaro perché è molto importante.<br />
Qui vediamo un altro esempio di carcinoma microinvasivo,vedete,qui vediamo il cancro,e<br />
poi vedete questo gettoncino,è un carcinoma microinvasivo,poco distante<br />
dall’epitelio,quindi non c’è una franca invasività massiva,ma qualche gettone che è<br />
sfuggito un poco al controllo.<br />
Questi poi sono i carcinomi invasivi,fortunatamente però noi di questi non ne vediamo più<br />
grazie alla colposcopia e ai Pap-test. Vedete qua un’esocervice,vedete come è presa<br />
l’eso,si capisce che si approfondisce anche nell’endocervice, e qua si vede già a occhio<br />
che non siamo nei microinvasivi.<br />
Addirittura vedete cosa succede quando si sfugge al controllo del cancro della cervice.<br />
Vedete qua è un cancro della cervice che si è esteso all’utero in maniera massiva,vedete<br />
questa è la cavità uterina che è diventata adesso una fessura,queste masse biancastre<br />
sono il cancro che lambisce un po’ anche la parete della vescica. Anche questa vescica<br />
non è normale,perché ha tutti questi fasci muscolari,sembra quasi la parete del cuore,si<br />
chiama vescica a colonne,ed è caratteristica di una donna che soffre di cistite cronica con<br />
fenomeni ostruttivi,per cui la vescica si ipertrofizza. D’altra parte si spiega anche questa<br />
vescica ipertrofica in questo caso,perché vedete che questo cancro comprime a livello<br />
della regione del trigono,quindi questa è una reazione a questi fenomeni di<br />
compressione,per cui la vescica si ipertrofizza. Questo è molto frequente nelle donne.<br />
scaricato da www.sunhope.it
Qua invece vedete un’estensione diretta alla vescica, e si estende anche alla parete<br />
vaginale,va verso l’alto,va verso la vescica, e anche alla parete del retto,in alcuni punti si<br />
ulcera proprio. Quindi questo è un cancro veramente massivo,la paziente è stata<br />
operata,ma discutibilmente. Se il cancro non è colto in tempo,vedete che catastrofe.<br />
Vedete questo è un carcinoma squamoso invasivo,e in genere quando è ben differenziato<br />
ha una caratteristica: le cosiddette perle cornee. Sono delle strutture lamellari<br />
concentriche di cellule cornee che mantengono il nucleo. Quindi sono cellule che in<br />
qualche modo vorrebbero imitare il processo di cheratizzazione normale,ma non ci<br />
riescono perché c’è una paracheratosi,sono cellule atipiche. Le perle cornee sono una<br />
caratteristica dei carcinomi ben differenziati. Talvolta questi cancri si presentano in una<br />
maniera non proprio tipica e possono assumere quest’andamento polipoide.<br />
Questo è un carcinoma squamoso che sembrava un polipo,e questo è il motivo per cui il<br />
polipo va sempre esaminato,perché nella stragrande maggioranza dei casi è un polipo di<br />
quelli di cui abbiamo parlato l’altra volta,ma in rari casi può essere invece un cancro<br />
polipoide,che ha cioè i caratteri macroscopici di un polipo e invece è un cancro.<br />
Questo è quello a cellule basalioidi. Vedete già a occhio che mentre nei cancri di prima<br />
vedevamo un ampio citoplasma,qui le cellule sono addirittura disposte quasi in sincizi,una<br />
addosso all’altra,perché hanno scarso citoplasma.<br />
Questo è l’adenocarcinoma in situ,che è un’entità virtuale,perché è difficile da<br />
acchiappare. Perché in situ. Vedete qua questa ghiandola mantiene ancora il carattere<br />
mucoide,quindi è una ghiandola normale. A un certo punto nell’ambito di questa ghiandola<br />
molto irregolare e molto dilatata,vedete un epitelio atipico,pluristratificato,e questo è il<br />
carcinoma in situ,però vedete che non supera mai la membrana basale esterna della<br />
ghiandola. È difficile però osservare il cancro in questa fase,perché non riusciamo ancora<br />
a cogliere il cancro in questa fase così precoce.<br />
Questo è quello endometrioide,l’endometrioide ha un’altra caratteristica,ovvero che è<br />
papillare. Oltre ad essere sieroso questo ha un citoplasma acidofilo,non più mucoide,però<br />
soprattutto qui si vede bene la tendenza a formare papille all’interno di queste cisti<br />
ghiandolari. Questa è una caratteristica del carcinoma endometriale che è quasi sempre<br />
papillare.<br />
Questo è l’adenocarcinoma mucoide,vedete questi grandi laghi di muco,perché è un<br />
scaricato da www.sunhope.it
carcinoma che produce tanto di quel muco che si formano queste aree bianche o poco<br />
colorate.<br />
Qua l’adenosquamoso,voi vedete le strutture ghiandolariformi affianco a strutture<br />
squamoidi.<br />
Qui è l’adenoideo-cistico. Vedete sono tutte belle cavità con dentro del materiale che<br />
spesso non si vede perché quando si taglia non sempre viene. Vedete come sono<br />
geometriche queste cavità,per cui uno rimane colpito, perché in genere un cancro non è<br />
mai cosi rispettoso della geometria.<br />
Questo è il carcinoma neuroendocrino,a piccole cellule. La conferma che è un carcinoma<br />
neuroendocrino viene dalla ricerca della cromogranina.<br />
Altri tumori della cervice. E qui c’è un elenco enorme,però mi soffermo solo su 2 o 3 forme.<br />
Il cosiddetto rabdomiosarcoma botrioide. È un tumore in effetti dei bambini che coinvolge<br />
la cervice,ma anche tutti gli organi genitali,anche la vagina.<br />
Anni fa ci fu un caso clamoroso da un punto di vista giudiziario,di una bambina che morì in<br />
ospedale,non vi dico come,ma addirittura ci fu un medico legale che di fronte ad una cosa<br />
del genere avanzò il sospetto che il padre l’avesse violentata,per cui questo andò in galera<br />
fin quando un anatomopatologo disse che quelle masse non erano un segno di<br />
violenza,ma erano un rabdomiosarcoma botrioide. Il termine botrioide è un termine un po’<br />
antico per dire a grappolo d’uva.<br />
Tumori mulleriani misti. Questi adesso li lasciamo in sospeso,perché l’epitelio mulleriano è<br />
l’epitelio primitivo da cui deriveranno tutti gli organi genitali. Tutti questi tumori mulleriani<br />
misti fanno degli scherzi notevoli,per cui hanno una grande varietà di aspetti morfologici.<br />
Certamente la loro caratteristica essenziale è che sono dei tumori che hanno una<br />
componente epiteliale maligna ed una componente mesenchimale pure maligna. Quindi<br />
sono tumori particolari. Non ne parleremo adesso perché sono più caratteristici in altri<br />
organi genitali.<br />
Poi abbiamo tumori muscolari lisci.<br />
Il tumore mulleriano maligno,vedete che qui ha una componente epiteliale che esprime<br />
anche la citocheratina e una componente mesenchimale anch’essa maligna. Quindi è un<br />
scaricato da www.sunhope.it
tumore misto,doppiamente maligno.<br />
La stadiazione FIGO(federazione internazionale ostetrici e ginecologi) è quella più seguita.<br />
Questa stadiazione è molto simile a quella TNM,con poche differenze.<br />
Ia => ha le caratteristiche che vi ho detto prima,cioè 5 e 7mm. Si suddivide in 2 sottotipi:<br />
Ia1 quando l’invasione inferiore a 3mm. Ia2 quando l’invasione è tra 3 e 5 mm.<br />
Ib=> già cambia perché l’invasione è maggiore,ma comunque non c’è estensione oltre la<br />
cervice. Quindi l’ Ib è il cancro della cervice che eccede o i 5mm o i 7mm,o<br />
entrambi,purché rimanga ancora alla cervice.<br />
Lasciamo stare queste altre sottocategorie che non ci interessano.<br />
Allo stadio II il cancro va fuori dalla cervice,quindi interessa altri organi ma non alla pelvi e<br />
ad altri organi pelvici. Quindi può avere infiltrazioni alla vagina,non al terzo inferiore né ai<br />
parametri,mentre IIb da infiltrazioni alla vagina e ai parametri,però mai al terzo<br />
inferiore,quindi è un’estensione che è più vicina alla sede del cancro.<br />
Stadio III quando c’è un’estensione alla pelvi,oppure al terzo inferiore della vagina.<br />
Stadio IV quando c’è un’astensione addirittura extrapelvica,cioè retto,vescica ecc,però<br />
questo per fortuna si vede raramente.<br />
La cosa più importante è capire se è stadio I o stadio II,perché lì c’è il taglio netto. Perché<br />
fino al primo stadio si può fare un tipo di chirurgia conservativa,dallo stadio II in poi è una<br />
chirurgia demolitiva,nello stadio III e IV è discutibile l’utilità dell’intervento chirurgico e<br />
molto spesso si preferisce radioterapia o altri tipi di terapia.<br />
Vedete la sopravvivenza come cambia,queste sono tabelle dell’American Cancer Society:<br />
stadio Ia1 la sopravvivenza è 99% a 5 anni,quindi quasi totale,anche perché bisogna<br />
vedere se quell’1% era stato stadiato bene,perché la stadiazione implica per<br />
l’anatomopatologo un grande impegno,perche bisogna fare tante sezioni e vedere che in<br />
nessuna sezione si eccedano i limiti.<br />
Stadio Ib già scendiamo all’80%. Al II arriviamo al 70%. Al III attorno al 30%. Al IV<br />
arriviamo attorno al 10%.<br />
Quindi vedete,c’è un rapporto diretto tra l’estensione del cancro, l’aggressività, lo stadio in<br />
scaricato da www.sunhope.it
cui noi l’abbiamo trovato.<br />
In genere fino allo stadio Ia1,se si tratta di un soggetto giovane si può fare una semplice<br />
conizzazione,o l’isterectomia semplice se magari il soggetto lo richiede o se si tratta di una<br />
donna più anziana. Noi abbiamo un record di isterectomie in Campania. Le isterectomie<br />
causano molti problemi nella statica del pavimento pelvico.<br />
Dallo stadio Ia2 fino allo stadio Ib deve essere fatta l’isterectomia radicale con diverse<br />
estensioni,a seconda dello stadio e dell’estensione. Ci deve essere anche la<br />
linfoadenectomia. Qui è un grave errore fare il linfonodo sentinella perché è difficile da<br />
identificare,poiché c’è un incrocio di vie linfatiche tra destra e sinistra,che in genere non<br />
c’è nella mammella. Si può fare anche la radioterapia a campi interni o campi<br />
esterni,mediante degli aghi.<br />
Dallo stadio II è opportuno forse non fare neanche più la chirurgia,ma limitarsi solo alla<br />
radioterapia.<br />
Come va fatta la conizzazione.<br />
Tutto va fatto secondo uno schema di quadranti. Chi fa l’intervento dovrebbe indicare un<br />
punto di repere per l’orientamento. Questo è molto importante perché nel caso di<br />
reintervento bisogna capire a che livello c’è la maggiore invasività,e anche per chi ha fatto<br />
la colposcopia. In genere il punto di repere si mette alle ore 12,se uno vuole essere<br />
proprio preciso ne mette un altro alle ore 6. Poiché i prelievi vanno fatti secondo uno<br />
schema radiante,almeno 12 sono prescritti, a spicchi,seguendo lo schema di un orologio.<br />
E poi con dei coloranti vitali,che persistono ai processi di fissazione,si dovrebbero indicare<br />
i margini (prossimale,mediale,laterali),per sapere dove è avvenuta l’invasione. Ma questa<br />
è la teoria,in pratica il sistema a volte salta,perché non c’è il punto di repere. È molto<br />
importante anche valutare l’estensione all’endocervice,perché lì c’è l’apice del<br />
cono,mentre la base sta verso il basso. Nasce un problema:a volte anche le ghiandole<br />
endocervicali che stanno sotto,partecipano a questo processo neoplastico e quindi noi<br />
troviamo delle aree di carcinoma,di metaplasia squamosa con displasia grave,o di<br />
carcinoma squamoso che coinvolge anche le ghiandole. Tant’è vero che ci sono delle<br />
raccomandazioni sull’apice,ma non vi voglio appesantire.<br />
Quindi bisogna andare a vedere anche le ghiandole,in modo che poi nel giudizio finale<br />
dell’anatomopatologo potrà essere scritto in modo chiaro che i margini sono<br />
scaricato da www.sunhope.it
indenni,perché se i margini sono indenni a tutti i livelli dei quadranti,vuol dire che<br />
l’intervento è stato risolutivo,altrimenti bisogna re intervenire.<br />
E adesso parliamo del Pap-test. Qui vedete un francobollo americano per la<br />
commemorazione di Papanicolau,medico di origine greca,a cui dobbiamo il Pap-test.<br />
Anche la colorazione che usiamo per questo test si chiama colorazione di Papanicolau. È<br />
una colorazione molto complessa. È un metodo tetra cromico,cioè con 4 coloranti diversi<br />
che ci permettono di avere una serie di informazioni di cui parleremo. Come si fa il Pap-<br />
test.<br />
Si va con una specie di microspatolina anche nell’endocervice perché sappiamo che la<br />
giunzione sta la,perché è quella la zona da vedere: la giunzione e l’endocvervice,perché è<br />
capitato tante volte che fuori non c’era niente,ma dentro si. O si deve usare questa spatola<br />
particolare che è tipo spazzolino,oppure questo tipo di spatole bicorni,con un braccio più<br />
sottile che va nell’enocervice e uno più smussato,più grosso che va nell’esocervice.<br />
Anche sul vetrino quindi dopo lo striscio,avremo su una parte le cellule endocervicali e<br />
sopra o sotto tutte le cellule esocervicali. Vi ricordo che le cellule endocervicali sono<br />
cilindriche,mucoidi, e che è indispensabile vederle in un soggetto che non è ancora in<br />
menopausa per i criteri di adeguatezza. In post menopausa non è più obbligatorio vederlo.<br />
Se mi arriva un Pap-test di una donna di 40 anni,io devo dire inadeguato se non trovo<br />
cellule endocervicali o muco. Nel periodo perimenopausale invece l’epitelio endocervicale<br />
se ne sale sopra,la spatola non ci arriva più. In tal caso anche se non vediamo cellule o<br />
materiale endocervicale dobbiamo accettare per buono il prelievo.<br />
Vedete come si scrive un Pap-test. Già vi ho parlato del sistema Bethesda. Sul Bethesda<br />
3 io non sono molto d’accordo, infatti continuo ad usare il Bethesda 2. In effetti c’è un<br />
primo giudizio che riguarda l’adeguatezza del campione: adeguato,inadeguato o<br />
parzialmente adeguato. Parzialmente adeguato vuol dire valutabile,ma limitato da. Le<br />
limitazioni sono per esempio il periodo,perché il prelievo non si fa mai in periodo<br />
perimestruale,per la presenza di sangue. Questo giudizio significa tra colleghi: ripetilo in<br />
un giorno più consono!<br />
Oppure da un errore di fissazione,perché una volta fatto il Pap-test ci sono dei fissativi e<br />
spesso se li scordano e ci arriva avvolto nella carta (un cart-test). Oppure se il ginecologo<br />
sta nervoso e striscia forte,oppure striscia avanti e dietro con la spatola,le cellule si<br />
scaricato da www.sunhope.it
ompono e allora si dice che quel test è limitato da difetti di stesura. Oppure può capitare<br />
che il ginecologo distrattamente usi strumenti non idonei,come il cotton fiock,che spesso<br />
viene utilizzato,ma il pap-test non serve a niente. Alcuni addirittura usavano l’abbassa<br />
lingua.<br />
Il giudizio successivo è se il pap-test è normale,il ginecologo però ci deve dare anche la<br />
data del ciclo,perché se il pap-test va fatto nei periodi centrali del ciclo,quindi lontano dalle<br />
mestruazioni. Per questo ci sono delle linee guida internazionali. Noi possiamo dare<br />
anche giudizi ormonali,su come procede questa persona,a seconda della maturazione<br />
cellulare. Possiamo dire se ci sono alterazioni cellulari benigne,e in questo caso abbiamo<br />
infiammazioni e infezioni. La presenza di miceti è dovuta a scarsa igiene o eccessiva<br />
igiene. Per quanto riguarda l’herpes,oggi si vede molto meno,20 anni fa,il posto del<br />
papilloma virus lo teneva l’herpes e le lesioni erpetiche erano molto frequenti mentre ora<br />
sono molto rare. Il lattobacillo è bastoncellare;se trovo invece cocco bacilli vuol dire che<br />
c’è un’infezione da alterazione della flora batterica vaginale. Oppure il famoso trichomonas<br />
che una volta era diffusissimo,ma oggi si vede molto meno. O altre infezioni come la<br />
gardnerella vaginalis.<br />
Oppure possiamo avere alterazioni reattive riparative,perché quando si va a prendere<br />
l’endocervice,in quella zona spesso ci possono essere dei fenomeni metaplastici,per<br />
irritazione o per infiammazione. Una di queste alterazioni è l’atrofia. L’atrofia,soprattutto in<br />
soggetti vicino ai 50 anni,cioè in periodo perimenopausale,ha un suo significato,soprattutto<br />
quando è moderato-severa,perché allora abbiamo dei segni di distrofia per carenze<br />
ormonali,diciamo che se ne cade quasi l’epitelio e troviamo nello striscio cellule<br />
appartenenti agli strati inferiori che normalmente non devono comparire nello<br />
striscio:cellule basali,parabasali,c’è una tendenza alla cheratosi. In questi casi consigliamo<br />
al ginecologo di fare una terapia ormonale locale,con ovuli e di ripetere il Pap-test dopo 1-<br />
2 mesi,il quale ritornerà normale se si trattava di una distrofia,normale come se si trattasse<br />
di una ragazza,anche se è un soggetto più avanti d’età.<br />
Veniamo alla terza possibilità: abbiamo normale,reazioni infiammatorie o reattive,quindi<br />
anche infettive e anomalie cellulari. Quali sono le anomalie cellulari. Noi possiamo avere<br />
L-SIL che corrisponde a due categorie:HPV quindi coilocitosi o CIN-I. H-SIL invece è CIN-<br />
II o CIN-III. CSASI(cellule squamose atipiche di significato indeterminato). In questo caso<br />
diciamo al ginecologo che ci troviamo di fronte a delle atipie che non corrispondono<br />
scaricato da www.sunhope.it
perfettamente alla displasia,però c’è un sospetto,allora in questo caso è come dire al<br />
collega di fare una colposcopia e se trovi una lesione fai una biopsia,o ripeti il pap-test.<br />
Oppure carcinoma squamoso,cioè qualcosa in più della displasia,oppure cellule atipiche<br />
ghiandolari,quindi c’è tipo una displasia delle porzioni ghiandolari;c’è anche la dizione<br />
“cellule ghiandolari atipiche di significato indeterminato”,cioè guarda,io trovo delle<br />
atipie,ma non riesco a capire se sono su base reattiva,infiammatoria ecc. o se sono atipie<br />
su base preneoplastica. Poi abbiamo cellule maligne,probabilmente tali perché può<br />
succedere che nel pap-test possono sgocciolare dall’alto cellule atipiche che provengono<br />
dall’endometrio;oppure cellule endometriali in menopausa.<br />
Finiamo con i consigli che noi diamo:<br />
• ripetere lo striscio,subito se abbiamo dei sospetti;a distanza dopo terapia specifica<br />
• Colposcopia<br />
• Biopsia cervicale<br />
• Biopsia endometriale<br />
• Altro.<br />
Facciamo anche un breve commento finale se c’è qualche considerazione da fare.<br />
scaricato da www.sunhope.it
LEZIONE DEL 16/11/2010<br />
CONTINUO CARCINOMA DELLA CERVICE<br />
Pap-test normale :con la colorazione di Papanicolaou si possono osservare cellule<br />
grandi con nuclei piccoli(perché le cellule stanno per andare in apoptosi) e scuri che<br />
sono le cellule superficiali,le quali hanno un citoplasma acidoflo per cui appaiono di<br />
colore rosa o orange,le cellule superficiali-intermedie appaiono,invece,di colore<br />
blu.L’epitelio in genere non è corneificato tranne in menopausa e in premenopausa.A<br />
volte queste cellule si ammassano e questo vuol dire che il pap-test è<br />
stato effettuato quasi alla metà del ciclo,quando c’è l’ovulazione.Il pap-test ci indica<br />
quindi anche lo stato ormonale della paziente.Al pap-test lo Pseudomonas appare<br />
come un pezzo di cellula con un nucleo quasi fantasma,molto piccolo con all’interno<br />
delle granulazioni(ha quindi un aspetto foliaceo).<br />
A volte si osservano cellule con un citoplasma avente i bordi ripiegati e queste cellule<br />
sono dette navicolari.Si vedono poi numerosi trattini che rappresentano i<br />
lattobacilli,i quali sono essenziali nella flora batterica vaginale.Essi possono anche<br />
impilarsi formando dei filamenti e questo potrebbe far sospettare che vi sia<br />
un’infezione da leptothrix che ha un aspetto capelliforme.<br />
Oltre alle cellule superficiali possono esserci cellule con citoplasma basofilo e nucleo<br />
grosso che sono le cellule parabasali.Normalmente esse non dovrebbero comparire<br />
nel pap test e se compaiono vuol dire o che c’è un’infiammazione o che c’è atrofia.<br />
Ci sono poi cellule eosinofile colorate con un colorante detto orange che colora le<br />
cellule di arancione e si tratta di cellule che iniziano a cheratinizzare,processo che<br />
inizia in genere dopo i 40 anni.<br />
La presenza di cellule endocervicali (cellule cilindriche mucoidi)costituisce la prova<br />
che il pap-test sia stato eseguito correttamente.Queste cellule in genere si<br />
aggregano a nido d’ape,altre volte appaiono come cellule allungate,a foglia.<br />
In corso di fenomeni di riparazione a causa di lesioni all’endocervice,possono esserci<br />
poi cellule in attiva proliferazione e si trata di cellule con un grosso nucleo e un<br />
nucleolo evidente.<br />
scaricato da www.sunhope.it
Ci sono poi batteri,ovvero i cocchi,che danno un aspetto pulverulento a differenza<br />
dei lattobacilli,formano una sorta di pulviscolo.<br />
La presenza quindi di cellule basali,para basali,granulociti in disfacimento i cui nuclei<br />
si frammentano,cellule orangiofile e quindi cheratinizzate e tutto quetso fa pensare<br />
alla presenza di un’atrofia con flogosi.Se quest’atrofia è molto marcata ci saranno<br />
cellule molto atipiche e quindi non essendo sicuri se si tratta di atrofia,distrofia o di<br />
qualcosa di più grave,si consiglia di ripetere lo striscio dopo terapia ormonale,perché<br />
se si tratta di distrofia queste atipie scompaiono.<br />
Coriocitosi:c’è un alone chiaro perinucleare con dei bordi molto evidenti<br />
perifericamente.<br />
Displasia moderata:distribuzione grossolana della cromatina,nuclei più grandi e<br />
irregolari.<br />
Displasia grave:Ci sono cellule ipercromiche,dicromiche(irregolarità di<br />
colorazione,alcune più chiare alcune più scure ),il citoplasma quasi scompare,forme<br />
cellulari abnormi.La differenza col carcinoma in situ è molto aleatoria e la diagnosi<br />
differenziale con esso e col carcinoma invasivo non è agevole,quindi è meglio dire<br />
che c’è una displasia e chiedere una colposcopia oppure scrivere nelle annotazioni<br />
finali che si deve effettuare una biopsia,importante per vedere se si tratta di<br />
carcinoma invasivo,per stabilirne il livello di invasività e per poter poi procedere con<br />
l’intervento chirurgico.Se c’è transdifferenziazione vuol dire che c’è invasività,ma<br />
anche in questo caso bisogna parlare di atipie gravi e dire che si consiglia la biopsia.<br />
RACCOMANDAZIONI DELL’A.C.S. :<br />
1) fare il pap-test tre anni dopo il menarca e comunque non dopo i 21 anni,perché la<br />
massima incidenza del cancro si abbassa sempre di più.<br />
2)Farlo ogni anno e ogni due anni se si utilizza la citologia con strato sottile<br />
3)Le femmine con 2-3 risultati normali dopo i 30 anni possono farlo anche ogni 2-3<br />
anni.<br />
4) dopo isterectomia e dopo i 70 anni la citologia cervicale si può anche<br />
interrompere<br />
scaricato da www.sunhope.it
5)intensificare i tempi dello screening nei soggetti in cui ci sono dei rischi di<br />
sviluppare il cancro,come negli immunodepressi,se c’è patologia da papilloma virus<br />
ecc.<br />
Importante è effettuare il pap-test intorno alla metà del ciclo,dall’ottavo al<br />
ventesimo giorno,perché il ciclo si accompagna a tutta una serie di artefatti<br />
infiammatori,necrotici,ecc.<br />
UTERO<br />
Effettuando una sezione trasversale dell’utero si osservano una<br />
cavità,delle ghiandole e due strati muscolari,uno longitudinale e uno<br />
circolare e questa muscolatura liscia è così elastica che consente durante il<br />
parto alla cavità uterina di allargarsi molto.<br />
Distinguiamo due porzioni dell’endometrio,una superficiale e una<br />
profonda.L’endometrio che sta in alto è quello funzionale o<br />
reciduale,ovvero quello che cade durante la mestruazione,quello che sta<br />
in basso è quello basale,ovvero quello che deve rigenerare.Un ruolo<br />
importante ce l’hanno anche le arteriole spirali,che percorrono<br />
l’endometrio e che rimangono beanti durante il ciclo,favorendo il distacco<br />
dell’endometrio necrotico.La fase proliferativa è sotto il controllo degli<br />
estrogeni e quando il follicolo scoppia rimane il corpo luteo che produce<br />
progesterone che consente la maturazione dell’endometrio per cui si ha la<br />
fase secretiva.<br />
Quando si effettua un raschiamento endometriale è importante sapere se<br />
il giorno del ciclo biologico corrisponde a quello del ciclo storico.<br />
FASE PROLIFERATIVA:si vedono un po’ di emorragia,ghiandole<br />
tubulari,figure mitotiche,perchè l’endometrio si sta ricostituendo,c’è poco<br />
materiale nelle ghiandole e anche lo stroma partecipa questa dinamica<br />
ormonale e dato che eso risponde agli ormon,viene detto stroma<br />
citogeno,con cellule linfocito-simili.C’è poi pseudo stratificazione(i nuclei<br />
delle cellule si dispongono ad altezze diverse dando l’impressione che<br />
l’epitelio sia pluristratificato).<br />
scaricato da www.sunhope.it
FASE SECRETIVA:i contorni ghiandolari appaiono molto irregolari,il nucleo<br />
cellulare si sposta in una posizione parabasale,per la presenza di un<br />
vacuolo al di sotto di esso(fenomeno che avviene al quattordicesimo<br />
giorno).La cellula si riporta in posizione basale,incomincia a secernere,e le<br />
cellule stromali assumono aspetto epitelioide,perché il citoplasma<br />
aumenta.L’epitelio è anche edematoso,infatti le cellule sono distaccate<br />
per la presenza di edema nell’interstizio.<br />
ALTERAZIONI POSSBILI<br />
Il fenomeno di ARIAS-STELLA è caratterizzato dalla presenza di atipie particolari<br />
nell’endometrio.Le cellule assumono un aspetto a chiodi,che può aversi per un’<br />
iperfunzione in senso estro-progestinico,su base farmacologica,nelle gravidanze<br />
extrauterine,per cause iatrogene(tamoxifen),per uso di contraccettivi orali e possono<br />
esserci anche fenomeni di adenoacantosi che è una metaplasia squamosa<br />
dell’endometrio con scomparsa del lume ghiandolare.<br />
CAMPIONI PER INDAGINI ISTOLOGICHE<br />
Il raschiamento,che si fa dopo dilatazione del canale cervicale,può avere una<br />
funzione sia diagnostica che terapeutica.Esso può anche essere frazionato quando<br />
non si conosce bene la sede della lesione.Si possono effettuare,inoltre,la biopsia e la<br />
microbiopsia che per essere meno traumatica usa un meccanismo di suzione<br />
piuttosto che un taglio.Dopo 3-4 giorni si ha la restituito ad integrum.<br />
ENDOMETRITI<br />
Quelle acute possono essere legate ad aborto,al post-partum,ad interventi<br />
chirurgici.Una volta erano molto più frequenti,oggi si sono ridotte notevolmente per<br />
l’utilizzo di tecniche che mantengono la condizione di asepsi.<br />
Le endometriti croniche sono caratterizzate soprattutto dalla presenza di<br />
plasmacellule.Bisogna tener presente che nell’endometrio dei granulociti sono<br />
presenti sempre,perché sono moltissimi durante la fase mestruale,per cui a volte si<br />
fanno diagnosi errate di endometrite.<br />
Cause: dispositivi intrauterini anticoncezionali,post-gravidanza,post-abortive ecc.<br />
scaricato da www.sunhope.it
Le endometriti croniche possono avere anche un pattern granulomatoso con la<br />
presenza di un nodulo costituito da cellula giganti e macrofagi molto grandi detti<br />
epitelioidei.<br />
Piometra:l’infezione è così forte da ostruire l’utero causando una serie di<br />
problemi,perché si impedisce anche il flusso mestruale.<br />
Ematometra: ostruzione più bassa dell’utero( a livello cervicale) con raccolta di<br />
sangue che non riesce ad uscire.<br />
Metaplasie endometriali:<br />
1) squamosa(morule squamose ben differenziate.Si chiamano morule,perché si<br />
tratta di aggregati di cellule squamose che ricordano le morule dell’embrione e sono<br />
cellule normali,non atipiche)Sono soprattutto post-menopausali queste metaplasie.<br />
2)tubarica (sono cellule ciliate)<br />
3)ossifila<br />
4)mesonefrica(per problemi di tipo embriologico,perché gli abbozzi dei reni e dei<br />
genitali si trovano vicini durante l’embriogenesi)<br />
5)intestinale(molto rara)<br />
ADENOMIOSI E ENDOMETRIOSI<br />
ADENOMIOSI:Quando c’è un fenomeno reattivo,ripartivo,le cellule endometriali<br />
vengono spinte verso il basso e quindi entrano nello spessore della muscolatura<br />
liscia dove vanno a formare delle ghiandole,che sono ghiandole prive di lume,che si<br />
trasformano in raccolte ematiche,perché anch’esse vanno incontro al normale ciclo e<br />
che causano dolore pelvico.Provocano metrorragie quando diventano di grandi<br />
dimensioni.Si tratta,quindi,di un’eterotopia.Questo può essere una delle cause di<br />
mestruazioni molto dolorose.<br />
ENDOMETRIOSI: presenza di ghiandole endometriali in molte sedi e che subiscono i<br />
normali flussi mestruali.Possiamo ritrovarle a livello della tuba,dell’ovaio (in questo<br />
caso spesso si associano ad infertilità)della cute,del rene,della vescica e anche a<br />
livello delle cicatrici chirurgiche,ad esempio lungo la cicatrice di un parto cesareo<br />
.Una di queste strutture poi può diventare cistica,può rompersi e determinare un<br />
emoperitoneo.Le cause sono varie:una è la presenza di un flusso retrogrado,il quale<br />
scaricato da www.sunhope.it
va verso le tube,fino a raggiungere il peritoneo dove queste cellule endometriali<br />
possono impiantarsi.Un’altra ipotesi è quella secondo la quale alcune cellule entrino<br />
nelle arteriole e portarsi lontano colonizzandosi in altri organi.L’ultima ipotesi è che<br />
segnali abnormi inducano le cellule staminali di qualsiasi altro organo a differenziarsi<br />
in cellule endometriali.Talvolta succede che l’emorragia recidivante può causare la<br />
formazione di cisti fibrotiche e le cellule endometriali possono anche scomparire<br />
rendendo più difficile la diagnosi di endometriosi e possiamo ritrovare anche solo lo<br />
stroma(in questi casi si ricorre a recettori ormonali da questo espressi a differenza<br />
degli altri tipi di stroma)Si possono vedere anche macrofagi con infiltrati<br />
emosiderinici.<br />
MENORRAGIE E METRORRAGIE<br />
La menorragia è la perdita di sangue notevole durante il normale flusso mestruale,è<br />
quindi un ciclo abnorme.La metrorragia è la perdita di sangue al di fuori del ciclo.<br />
AUB: abnormal uterine bleeding =perdita di sangue abnorme.Queste sono più<br />
pericolose dopo la menopausa,perché si può pensare che ci sia una neoplasia.<br />
Cause:presenza di adenomiosi, leiomiomi (questi possono impedire il normale<br />
svolgimento del ciclo e mantenere aperte le arteriole),polipi,carcinoma,atrofia.<br />
Le cause possono essere anche disfunzionali(DUB): cicli anovulatori,insufficienza<br />
della fase luteinica(accorciamento del ciclo) o iperfunzione di questa<br />
fase,insufficienza ovarica,asincronismo maturativo(alcune ghiandole vanno in ciclo<br />
prima e altre dopo,per la diversa sensibilità recettoriale e questo può causare la<br />
presenza di emorragie al di fuori del ciclo).Un’altra causa è l’aumento degli<br />
estrogeni(morfologicamente si vedrà un endometrio molto proliferante in una fase<br />
in cui non dovrebbe esserlo) o la riduzione del progesterone(si osserverà un<br />
endometrio insufficientemente luteinizzante,che non va verso la fase<br />
secretiva,perché non ha un apporto progestinico sufficiente) ,oppure le cause<br />
possono essere iatrogene.<br />
IPERPLASIE DELL’ENDOMETRIO<br />
1) semplice :non c’è ramificazione ghiandolare;spesso la ghiandola diventa<br />
cistica,perché si dilata.La semplice poi può essere tipica e atipica a seconda<br />
dell’aspetto citologico.Nell’iperplasia semplice,però,è difficile trovare atipie(solo nel<br />
17 % dei casi).<br />
scaricato da www.sunhope.it
2)complessa: le ghiandole endometriali diventano ramificate,lo stroma si<br />
riduce,perché le ghiandole si addossano l’una all’altra(back to back).Anche queste<br />
possono essere tipiche o atipiche(in oltre il 38 % dei casi).Queste complesse possono<br />
associarsi nel 20-30 % dei casi a cancro in altra sede.<br />
scaricato da www.sunhope.it
IPERPLASIE DELL’ENDOMETRIO E CANCRO DELL’ENDOMETRIO 18/11/2010<br />
Le iperplasie si dividono in due sottofamiglie: l'iperplasia semplice e l'iperplasia complessa , semplice e<br />
complessa dipende dalla strutturazione perché nell’ iperplasia complessa c'è una tendenza alla<br />
ramificazione delle ghiandole, come ce ne accorgiamo noi? Ce ne accorgiamo quando vediamo che le<br />
ghiandole sono una addosso all'altra, quando invece le ghiandole vediamo che hanno una certa distanza fra<br />
di loro vuol dire che non sono ramificate. Questa quì, vedete, è un'iperplasia semplice, vedete che c'è<br />
stroma tra una ghiandola e l'altra e molto spesso c'è una tendenza alla dilatazione cistica.<br />
ecco l'iperplasia complessa, vedete, già vedete che c'è un cambiamento. Le ghiandole sono in una posizione<br />
"back to back” cioè una addosso all'altra. Vedete che addirittura non si coglie la distinzione tra la fine di una<br />
ghiandole e l'altra, è evidente che questa è un'iperplasia complessa perché c'è la ramificazione delle<br />
ghiandole. Se andiamo a vedere poi la presenza di atipie, (sapete una delle prime espressione delle atipie è<br />
il polimorfismo), vedete cellule molto diverse le una dalle altre e anche una tendenza alla pseudo<br />
stratificazione o anche alla vera stratificazione dipende dai casi, molto spesso è pseudo stratificazione<br />
perché dipende dalla posizione dei nuclei, se voi immaginate 20 cellule che hanno un nucleo sopra, uno<br />
intermedio, uno sotto, abbiamo quasi l'impressione che siano disposte a più strati, però è un'impressione<br />
perché lo strato e unico; e le atipie come il pleomorfismo più diverse atipie discromiche e così via.<br />
Le iperplasie dell'endometrio sono una patologia diffusissima fra le donne ovviamente nel periodo della<br />
loro età che si avvicina ai quarant'anni ma può succedere anche prima, molto spesso sono sostenute da un<br />
certo iperestrogeni smo che può avere cause varie, una delle cause più frequenti e la famosa cisti ovarica,<br />
sono poche le persone che si sottopongono ad una ecografia e non si trova una cisti ovarica. L'iperplasia<br />
dell'endometrio è come vedete molto diffusa. Ora, se vogliamo distinguere queste categorie in maniera un<br />
po' diversa da come le abbiamo presentate prima parleremo di iperplasia non atipica e iperplasia atipica.<br />
L'iperplasia atipica la distinguiamo in semplice e complessa e l’ iperplasia atipica in semplice e complessa<br />
(ma non sono sicuro che abbia detto così)(min 00,21) vedete che nel peggiore dei casi l'iperplasia atipica<br />
complessa ha una possibilità di regressione intorno al 50% ma un indice di progressione che si avvicina al<br />
30% progressione vuol dire che si trasforma in cancro. mentre era l'iperplasia non atipica vedete, grosso<br />
modo c'è un rischio di progressione intorno al 2-3%. quindi è vero che la complessità incide me incide molto<br />
il tipico o l'atipico. all'inizio c’è un substrato comune cioè l’ iperestrogeni smo, però poi c'è una biforcazione<br />
in due strade: c’è un iperestrogeni smo che porta all'iperplasia semplice; ma si può sviluppare nell'ambito di<br />
queste iperplasia semplice, tra le cellule, un clone può avere quelle ramificazioni di cui sopra, questo clone<br />
poi avendo un vantaggio biologico prolifera e qui osserviamo tutto una serie di modificazioni e di mutazioni<br />
molecolari tra cui pten che è un gene fondamentale nelle neoplasie dell'endometrio, il k-ras che lo troviamo<br />
un po' dappertutto , una instabilità dei microsatelliti e anche una mutazione della p 53 , una volta che è<br />
avvenuta questa cascata di eventi molecolari abbiamo la precancerosi quindi l'iperplasia atipica. Sull<br />
iperplasia atipica è più facile che, per quel meccanismo di cui vi ho parlato di instabilità cromosomica,<br />
possono avvenire altre mutazioni dei cromosomi uno-otto-10 e la netta prevalenza di un clone su tutti gli<br />
altri. a un certo momento si è visto che pure questo sistema di classificazioni e molto diffuso in tutto il<br />
mondo presenta delle falle cioè, io posso prevedere come clinico l'andamento di questa iperplasia? Cioè<br />
qual è il rischio che si sviluppi il cancro? E allora è nato un nuovo concetto, tutto oggi attuale che tiene<br />
conto di alcun parametri (di non semplice applicazione), si chiama EIN (endometrial intra neoplasia) come<br />
il cin, ma questo è particolare perché tiene conto di alcuni parametri morfologici e di altri parametri non<br />
morfologici per calcolare se questa iperplasia semplice o complessa rientra nelle E. I. N. Cioè in una<br />
precancerosi o è fuori dall’EIN. Quali sono questi parametri? Uno) il volume percentuale dello stroma. Cosa<br />
vuol dire volume percentuale? se prendiamo una dimensione standard (1 mm²) del vetrino con un<br />
scaricato da www.sunhope.it
analizzatore di immagine vediamo quanto stroma c'è in ogni uno di questi quadrati in modo da avere un<br />
valore medio è ovvio che più stroma c'è più stiamo tranquilli, difficilmente una atipia a si accompagna a un<br />
stroma normale, c'è sempre una riduzione dello stroma poiché c'è un esuberante crescita ghiandolare. Due)<br />
perimetro delle membrane basali:più è grande questo perimetro più vuol dire che la ghiandola non solo si<br />
ramifica, ma ha anche dei contorni irregolari, non ha il contorno sferico classico della ghiandola<br />
endometriale semplice. Tre) il pleomorfismo nucleare: non si calcola l'asse nel senso della lunghezza ma<br />
l'asse nel senso trasversale cioè praticamente se il nucleo è più “grasso o più secco” piuttosto che il più<br />
lungo o più corto. Quattro) e poi un parametro molecolare, cioè pten, le ghiandole prive di questo gene<br />
sono quelle che hanno la atipia citologica. Alla fine si fa un calcolo matematico molto complesso e ne viene<br />
fuori un punteggio che se è inferiore a zero indica una EIN. Tutto ciò che invece è superiore a uno è una no<br />
EIN, diventa dubbio quando siamo tra zero e uno.si comincia a discutere anche del gene p-53 ma non è<br />
stato ancora accreditato. Perché questo sistema EIN? questo è un lavoro abbastanza recente che analizza<br />
come questo sistema rappresenta una discriminante all'interno di tutte le categorie classiche che noi<br />
abbiamo visto, ad esempio nel iperplasia complessa atipica solo il 79% delle lesioni è EIN c'è un 21% che<br />
presenta i caratteri dell'iperplasia complessa atipica ma non È EIN . Nel iperplasia complessa solo il 44% è<br />
EIN, nel iperplasia semplice il 5% è EIN, ecco il razionale di questa classificazione. in alcuni studi prospettic,i<br />
tassi di sopravvivenza mostrano quali possibilità ci sono che non ci sia un carcinoma associato: se è una<br />
situazione di no EIN quindi non precancerosi la possibilità che ci sia il cancro praticamente è uguale a zero,<br />
se invece noi abbiamo EIN la possibilità che ci sia associato un cancro è poco meno del 40% quindi abbiamo<br />
un parametro che è più discriminante rispetto alla aggressività della lesione che sembra distinguere allo<br />
stato attuale, anche se approssimativamente, quelle lesioni che più frequentemente possono essere<br />
addirittura associate al cancro.<br />
Cosa noi dobbiamo fare quindi sulla base di questa classificazione EIN, dal punto di vista pratico? Se ci<br />
troviamo di fronte a una situazione non EIN allora, noi sappiamo che non ci doVREBBE essere rischio di<br />
trasformazione, non ci dovrebbe essere il rischio di un carcinoma associato, allora si può stare tranquilli, e<br />
fare tutt'una serie di terapie ormonali di cui certamente vi parleranno i ginecologi. Se invece ci troviamo di<br />
fronte a EIN che cosa possiamo fare? In linea di massima una EIN accertata significa che c'è il rischio di<br />
progressione di carcinomi associati, c'è anche il rischio di falsi negativi cioè che la biopsia è andata a colpire<br />
un'area di EIN ma che magari lì vicino ci può essere un cancro, allora qual è il comportamento più logico<br />
razionale? L'isterectomia associata a diagnosi intraoperatoria, diagnosi intraoperatoria perché devo<br />
escludere che non ci sia un cancro, ovvero un cancro aggressivo lì vicino, quindi disponibilità del chirurgo e<br />
dell'anatomopatologo. Ma ci sono delle eccezioni, ci possiamo trovare a volte di fronte a donne giovani o<br />
relativamente giovani (a causa dell’innalzamento dell’età del primo figlio) che sono portatrici di questa<br />
patologia, e allora si può accettare, anche se questo è un comportamento a rischio, nell'ambito della<br />
consapevolezza del rischio quindi con un consenso informato intensificando il follow-up, molto spesso c'è<br />
anche un certo rapporto con l'obesità ovvero con la quantità di grasso corporea<br />
il polipo dell'endometrio è una situazione molto frequente, bisogna distinguere i veri polipi dai falsi polipi.<br />
per esempio un falso polipo dell'endometrio è quando c'è un'iperplasia dell'endometrio circoscritta e non<br />
diffusa a tutta la mucosa; in questo caso, cosa succede? C'è un'area della mucosa che si solleva, e se si fa<br />
una visita e si riesce a vedere nella cavità, questa lesione si vede come un polipo e, la richiesta che viene<br />
fatta all’ anatomopatologo è quella di individuare la natura di questo polipo anche se in realtà questo non è<br />
un vero polipo, ma è solo un endometrio iper plastico che in questo caso si chiama iperplasia focale perché<br />
avrebbe solo un'area. Il vero polipo dell'endometrio invece, che è più raro, deve avere per definizione un<br />
asse connettivo-vascolare. Quindi non lo stroma citogeno come nel primo caso (falso polipo), qui vediamo<br />
solo una fibrosi nell’asse poi vedete le ghiandole endometriale intorno. poi abbiamo dei polipi che possono<br />
scaricato da www.sunhope.it
insorgere nel corso del trattamento con tamoxifen (farmaco molto diffuso che si usa…..), in questo caso è un<br />
polipo molto particolare perché presenta una metaplasia mucoide e sapete voi che l'endometrio è invece di<br />
norma sieroso non mucoide e invece in questo caso possiamo avere un polipo endometriale con ghiandole<br />
che producono muco. Possiamo avere poi che lo stroma si decidualizza cioè uno stroma con aspetto<br />
epitelioide come abbiamo visto in una fase secretiva avanzata. e poi il polipo cosiddetto adeno-miomatoso<br />
in cui se andiamo a vedere all'interno del polipo troviamo tessuto muscolare liscio insieme a strutture<br />
ghiandolari. i polipi, in linea di massima, non hanno un rischio di trasformazione ovvero hanno un rischio<br />
trascurabile. (immagine) questo è l'aspetto dello pseudo polipo cioè, questa è una iperplasia cistica, vedete<br />
queste ghiandole dilatate, è certamente endometrio ovviamente quest'area di iperplasia fa si che sporga<br />
rispetto alla mucosa circostante ed ha un aspetto macroscopico di polipo. (immagine) questo è un polipo<br />
particolare (bisogna sempre stare attenti a questi polipi) perché sporge dal endocervice ed è sanguinante<br />
(in questo caso si potrebbe trattare di un cancro polipoide, ma ne parleremo dopo.) (Immagine) questo è il<br />
polipo adenomiomatoso e come possiamo vedere nella sua struttura ci sono ghiandole ma, vedete queste<br />
strie? È tessuto muscolare sono cellule fusate non stroma citogeno, addirittura lo stroma citogeno e quasi<br />
distrutto e da quest'aspetto linfocito simile, il resto sono tutte le bande di tessuto muscolare liscio e questo<br />
(immagine) è il polipo da tamoxifen, c'è una metaplasia mucosa perché vedete questo materiale qui è<br />
materiale mucoide che sta all'interno di queste strutture ghiandolari<br />
il carcinoma dell'endometrio<br />
La più forte precancerosi dell'endometrio è proprio l'iperplasia atipica, anzi è una evoluzione diciamo, logica<br />
dell’ iperplasia atipica non trattata: parliamo del carcinoma dell'endometrio. Sappiamo che esiste una<br />
profonda differenza anche epidemiologica fra il cancro della cervice e quello dell'endometrio perché il<br />
cancro della cervice riguarda donne relativamente giovani (quarta quinta decade), il cancro dell'endometrio<br />
invece è più incidente nella fase post menopausa nell'80% dei casi. possiamo avere un carcinoma de novo o<br />
ex novo cioè senza una storia pregressa di iper estrogenismo ma nella maggior parte dei casi possiamo<br />
rintracciare nella storia naturale, clinica di queste pazienti dei segni di iper estrogenismo anche se la<br />
paziente non era a conoscenza di questo problema, ma noi rifacendo l'anamnesi ci accorgiamo di tutta una<br />
storia di cicli anovulatori, irregolarità mestruali… e può essere associata ad obesità, diabete e ipertensione,<br />
infertilità e a tante sindromi particolari di cui parleremo fra cui l'ovaio policistico, la sindrome di Turner…<br />
molto spesso può anche essere associato a tumori ovarici anche benigni che secernono ormoni che<br />
determinano quindi un quadro ormonale sbilanciato in senso estrogenico. Ci sono delle alterazioni<br />
molecolari che fanno parte del quadro del carcinoma dell'endometrio anche se non c'è niente di assoluto in<br />
questo campo e sono: pten il k-ras il p-53, l’rb2 (oncosoppressore) e anche un aumento delle<br />
cicloossigenasi-2. Nell’ endometrio abbiamo un aspetto immunofenoticpico caratteristico. vi sono dei casi<br />
in cui il cancro dell'endometrio si estende all’ endocervice e viceversa, per cui, il quesito che ci poniamo è: è<br />
un carcinoma dell'endometrio o un carcinoma della endocervice? Anche perché il carcinoma della<br />
endocervice, che dovrebbe essere mucoide, quando non è bene differenziato non è che fa il muco… questa<br />
distinzione non è solo accademica perché questi due cancri hanno una storia naturale molto diversa.<br />
volendo semplificare il carcinoma della endocervice è più aggressivo del carcinoma dell'endometrio; il<br />
carcinoma dell'endometrio ha delle "regole" e molto spesso può essere meno maligno di quello che può<br />
sembrare alla diagnosi e poi vedremo quali sono questi fattori positivi per la prognosi.<br />
abbiamo un fenotipo diverso rispetto al carcinoma dell'endometrio(dice endometrio ma pens che voleva<br />
dire cervice) la cellula endometriale neoplastica esprime un doppio fenotipo: è citocheratina e vimentina<br />
scaricato da www.sunhope.it
positivo a differenza del cancro della cervice che è solo citocheratina positivo.può presentare anche una<br />
amplificazione di her-2 come il cancro della mammella però, mentre il cancro della mammella, è codificato<br />
che l ‘iper espressione, o comunque la amplificazione di questo gene e delle proteine a questo gene<br />
collegate ha un significato terapeutico, perché significa che questo cancro della mammella sarà sensibile ad<br />
una particolare terapia, questo non è valido o comunque, non ancora codificato in letteratura per il cancro<br />
dell'endometrio(53,00), esprime spesso i recettori ormonali anche se, anche in questo contesto non è<br />
codificata una eventuale relazione clinica come invece è nella mammella per i recettori degli estrogeni e del<br />
progesterone. Metastasi ematiche e linfatiche,le dà al polmone e al fegato , alle ossa, al sistema nervoso<br />
centrale e nella regione testa-collo, ma deve essere un cancro abbastanza avanzato, adesso vediamo il<br />
perché. Il carcinoma endometriale può assumere un aspetto polipoide, vedete questa è la cavità<br />
endometriale, poi andiamo verso l'endometrio poi l’ endocervice, ecco questo sembra apparentemente un<br />
polipo, invece è un cancro. Ancora qui, questo ha un aspetto pluripolipoide e in questo caso il problema con<br />
il polipo (di diagnosi differenziale) si pone solo relativamente in quanto in questo caso ci sono aree di<br />
necrosi e di emorragia e di infiltrazione e ciò fa capire subito che è un cancro.<br />
nell'80% dei casi l’ adenocarcinoma endometriale si chiama adenocarcinoma endometroide, differenziato<br />
in g1 g2 e g3 in rapporto al grado di differenziazione. poi abbiamo altre varietà:<br />
l’adeno acantoma è un cancro proprio in fase iniziale, cioè, è un cancro che presenta una metaplasia<br />
squamosa e questa metaplasia squamosa non è proprio così atipica come il carcinoma adeno squamoso<br />
questa è la differenza<br />
poi l’adeno squamoso cui tutte due le componenti sono atipiche sia quella squamoide sia quella<br />
ghiandolare (glassy cell, cioè cellule vitree è una varietà, anzi una sotto varietà di questo adenocarcinoma)<br />
poi abbiamo il ciliato, che sarebbe di tipo tubarico poiché le cellule ciliate si trovano solitamente solo nella<br />
tuba<br />
poi abbiamo il mucoide<br />
il sieroso papillifero (un tipo di cancro tipico dell’ ovaio)<br />
poi abbiamo il neuroendocrino<br />
ed è possibile seppure raramente, Un carcinoma squamoso che, è una stranezza in un organo<br />
endometriale. Evidentemente c'è questo passaggio intermedio di una metaplasia squamosa che giustifica<br />
anche questo istotipo che pure è raro.<br />
il carcinoma endometroide ben differenziato, ben differenziato perché presenta una struttura ghiandolare,<br />
non vi sto a dire come sia complesso, molto spesso anche su piccole biopsie una diagnosi differenziale fra<br />
iperplasia complessa atipica e carcinoma endometroide perché si assomigliano molto anche come vedete,<br />
in questo caso c'è una situazione spalla spalla delle strutture ghiandolari le due entità si differenziano per<br />
una serie di criteri che non sto qui a dirvi e anche con un po' di buon senso.<br />
ovviamente, quando è così (immagine) noi capiamo che è un carcinoma perché qui vedete, è<br />
moderatamente differenziato si vedono delle ghiandole ma si vedono anche delle espressioni solide quindi<br />
si capisce subito che è un cancro<br />
ancora di più, in questo tipo di cancro (immagine) che poco differenziato dove è addirittura difficile capire<br />
che è un carcinoma, tant'è vero che in questo caso non si capisce bene che è un carcinoma per saperlo<br />
scaricato da www.sunhope.it
dobbiamo fare citocheratina e altri marcatori per escludere che si tratti di sarcomi o tumori<br />
neuroendocrini... E così via<br />
ecco, questo è il caso di questa signora è un adeno acantoma che presentava anche delle aree squamoidi,<br />
vedete all'interno di questa ghiandola c'è una metaplasia squamosa che è considerato un carcinoma di<br />
basso grado quindi questa signora che teneva una iperplasia complessa atipica, nello stesso utero si trovava<br />
una massa legata a questo, abbiano un acantoma (carcinoma di basso grado)<br />
questo (immagine) è il carcinoma sieroso papillifero che ha un aspetto già particolare macroscopicamente,<br />
ha un aspetto un po' a cavolfiore per queste vegetazioni che presenta, istologicamente ci sono delle papille,<br />
ma vedete che atipie che ci sono in queste cellule epiteliali, atipie molto spiccate. Somiglia molto a un<br />
cancro ovarico di cui parleremo dettagliatamente in seguito.<br />
questo è il carcinoma neuroendocrino a piccole cellule, ne abbiamo già parlato.<br />
Questa è la stadiazione del carcinoma dell'endometrio (immagine) stadiazione FIGO<br />
il primo stadio (1a) vuol dire confinato all'endometrio , endometrio che vuol dire? Che non tocca proprio gli<br />
strati muscolari, quindi e solo mucosale, quindi possiamo chiamarlo anche carcinoma intra mucosale poiché<br />
si estrinseca solo nella mucosa, ovviamente è l'evenienza più favorevole.<br />
il carcinoma di stadio 1b vuol dire che coinvolge il miometrio, questo, ricordatevi, è un parametro<br />
fondamentale ai fini della prognosi però questo coinvolgimento del miometrio è inferiore al 50% dell'intero<br />
spessore del miometrio, quindi potremmo definirlo un coinvolgimento superficiale, perché quando supera il<br />
50% dello spessore dell'intero miometrio abbiamo già lo stadio 1c, la differenza stadio 1b e quello 1c ha una<br />
notevole importanza ai fini della prognosi come vedremo più avanti<br />
Lo stadio 2a corrisponde all’ 1c con un fattore di gravità in più: cioè coinvolge anche le ghiandole<br />
endocervicali, si estende anche verso l’ endocervice<br />
il carcinoma 2b non solo infiltra l’ endocervice come mucosa ma infiltra anche lo stroma endo cervicale,<br />
cioè sia appprofonda nel connettivo testa sotto le ghiandole endocervicali, quindi c’è un coinvolgimento più<br />
esteso della endocervice<br />
lo stadio 3 è quando c'è il coinvolgimento di altri organi per esempio della vagina oppure della tuba, o degli<br />
annessi oppure dei linfonodi pelvici<br />
lo stadio quattro invece prevede il coinvolgimento di organi distanza quali la vescica o la mucosa intestinale<br />
(4a) o, metastasi a distanza: stadio 4b<br />
volendo esprimere il tutto in maniera più sintetica: il primo stadio è confinato comunque tutto all'utero. Il<br />
secondo stadio abbiamo un coinvolgimento della cervice, il terzo e il quarto stadio abbiamo il<br />
coinvolgimento di altri organi degli organi sono distanti e il quarto stadio degli organi sono vicini (come<br />
appunto vagina, tuba ,annessi) lo stadio è 3. Questa è in sintesi la logica di questa stadiazione.<br />
La prognosi grezza fino allo stadio 1b supera il 90% fino a scendere, allo stadio quattro a percentuale di<br />
sopravvivenza inferiori al 20%. Quindi la stadiazione è un parametro prognostico vero, ovviamente in questo<br />
caso parliamo soprattutto di stadiazione anatomopatologica, è quella vera; la stadiazione clinica è una<br />
stadiazione presunta perché si basa su dati che da la tac o altre indagini strumentali ed è una stadiazione<br />
preoperatoria.<br />
scaricato da www.sunhope.it
quali sono i fattori prognostici del carcinoma endometriale?<br />
La stadiazione, il grading, l’ istotipo. gli istotipi più aggressivi sono il sieroso papilifero e l’ adeno squamoso.<br />
L’ endometroide così come l’adeno acantoma appartengono a quegli istotipi meno aggressivi.<br />
poi, l'estrogeno dipendenza, in linea di massima le forme più differenziate mantengono questa presenza di<br />
recettori estrogenici.<br />
La presenza di emboli ematici, le mutazioni di p53 e pten già abbiamo visto che assumono qui un ruolo<br />
importante, l’ aploidia, ovviamente più ci allontaniamo dalla diploidia che la norma, più aumenta<br />
l'aggressività<br />
l'attività mitotica e le mutazioni del gene RB2.<br />
scaricato da www.sunhope.it
TUMORI STROMALI DELL’ENDOMETRIO<br />
I tumori stromali d,ell’endometrio fanno un po’ storia a sé, perché abbiamo il tessuto mesenchimale<br />
e, quindi, tumori del tessuto mesenchimale, leiomiomi, leimiosarcomi, del tessuto fibroso, fibromi,<br />
liposarcomi, dei vasi, i vari tipi di angioma- sono 1 centinaio- , angiosarcoma e così via e altri<br />
tumori del mesenchima, fibroistiocitomi, etc.<br />
Lo stroma dell’endometrio è citogeno, cioè fatto da cellule specializzate, uno stroma che partecipa<br />
all’andamento ciclico di tutte le fasi del ciclo mestruale; fino a 20 anni fa era sconosciuto che anche<br />
lo stroma potesse dare tumori e nacque un termine che probabilmente oggi fa ridere perché è stato<br />
eliminato, si chiamava “stromaloma”,invece oggi si chiama nodulo stromale benigno.<br />
Questi tumori hanno un profilo immunoistochimico che ci aiuta molto, perché? Abbiamo come<br />
marcatore specifico il CD10 che è anche un marcatore, come poi vedremo, dei follicoli linfatici, ma<br />
comunque è 1marcatore diagnostico insieme ad altri markers come la vimentina, l’actina ( che<br />
posseggono nonostante non siano cellule muscolari ). Il nodulo stromale è fatto da stroma citogeno,<br />
in genere le cellule sono piccole, ha un colorito giallognolo, a differenza dei tumori stromali che<br />
sono duri, questo ha una consistenza molle; è poco conosciuto anche per la notevole differenza<br />
nell’incidenza del leomioma che è quasi ubiquitario, rispetto al tumore stromale benigno che è una<br />
rarità. Esiste poi il sarcoma stromale (ne abbiamo visti molti di questi); ovviamente ci sono criteri<br />
istologici e citologici che ci aiutano a fare la diagnosi differenziale rispetto ad una lesione stromale<br />
benigna; i criteri istologici sono i soliti e cioè il pattern infiltrante, quando vediamo che manda delle<br />
lingue di tessuto, che non è ben demarcato rispetto al tessuto adiacente, vediamo invasione di altre<br />
strutture, vasi ad esempio; dal punto di vista citologico, vediamo delle atipie maggiori rispetto al<br />
tumore stromale benigno, figure mitotiche in numero maggiore, in proporzione anche alla prognosi;<br />
infatti, diciamo sarcoma mitotico di basso grado quando il numero delle figure mitotiche, calcolato<br />
con un metodo statistico, cioè random, in 10 campi a 400 ingrandimenti è inferiore<br />
complessivamente a 10 figure mitotiche, complessivamente vuol dire che se osserviamo i 10campi<br />
avremo dei campi ove non si osservano figure mitotiche –tenendo conto che 400ingrandimenti è<br />
molto per un microscopio ottico- se ne vediamo invece più di 10, ci sarà almeno qualche campo che<br />
avrà più di una figura mitotica e quindi passiamo ad 1grado maggiore; un altro criterio utile sono le<br />
dimensioni: in genere un tumore stromale benigno è piccolo, quello maligno eccede di qualche<br />
centimetro; e poi la ploidia. Poi abbiamo, oltre al sarcoma stromale, un sarcoma indifferenziato, lo<br />
potremmo chiamare anche mesenchimoma, perché fa di tutto, può anche non esprimere determinati<br />
marcatori, ad esempio esprime il CD10 soltanto in alcune aree, è talmente indifferenziato che perde<br />
anche questi marcatori.<br />
[IMMAGINE] Questo è un nodulo stromale, ovviamente perché ha dei margini ben definiti il<br />
chirurgo lo può togliere, vedete che ha un colorito giallino mentre il leiomioma è bianco perché è<br />
fatto di muscolatura liscia; ha inoltre ( il nodulo stromale)una consistenza molle.<br />
[IMMAGINE (microscopica)] Nodulo stromale benigno: sono tutte cellule linfocito-simili con poco<br />
citoplasma, però se facciamo il CD10 è positivo, se facciamo i recettori ormonali è positivo, se<br />
vogliamo essere proprio scrupolosi facciamo anche un antigene leucocitario comune, un antigene<br />
che viene, cioè, espresso da tutte le cellule linfoidi, anche se già una persona esperta capisce che<br />
non può essere un linfoma, il perché lo vedremo più avanti.<br />
[IMMAGINE] Sarcoma stromale. Già si può vedere come si comporta di fronte al muscolo liscio, al<br />
miometrio, qui c’è un’immagine a clessidra perché infiltra il tessuto muscolare che va incontro a<br />
fenomeni di necrosi.[IMMAGINE] Questo è il sarcoma stromale di alto grado, tumore altamente<br />
maligno, guardate che atipie ci sono dal punto di vista morfologico.<br />
TUMORI MULLERIANI<br />
Sono per definizione tumori misti che si manifestano in età avanzata e tendono ad avere un grosso<br />
pattern infiltrante e aggressivo nei confronti dei tessuti normali, vediamo infatti diverse aree<br />
scaricato da www.sunhope.it
emorragiche o necrotiche legate all’invasività di questi tumori. Le masse sono polipoidi e<br />
coinvolgono precocemente sia l’endometrio che il miometrio; ha una strutturazione che noi<br />
definiamo bifasica perché notiamo aree epiteliali atipiche cioè tipo adenocarcinoma e anche lo<br />
stroma è maligno, quindi bifasico perché notiamo cellule fusate maligne e cellule epiteliali maligne.<br />
Lo chiamiamo mulleriano ( però questo è qualcosa che ha sempre a che fare con le cellule<br />
staminali) perché l’epitelio mulleriano ( cioè quello da cui deriveranno tutti gli organi genitali) ha in<br />
sé la capacità di differenziarsi, come vedremo. sia in tessuto mesenchimale, sia in tessuto epiteliale.<br />
La componente stromale può anche fare qualche scherzo, può addirittura dare cartilagine, per cui<br />
possiamo trovare aree di condrosarcoma, osteosarcoma, leomiosarcoma, rabdomiosarcoma, è un<br />
tumore che può dare qualsiasi cosa, soprattutto nella componente stromale; è ovvio che trovandoci<br />
un quadro così eterogeneo, chi non lo conosce può restare molto perplesso per la sua complessità.<br />
Esprime CD10, nelle aree epiteliali esprime la citocheratina, in quelle mesenchimali esprime la<br />
vimentina, tutte queste caratteristiche sono bifasiche perché ci fanno comprendere che ha una<br />
componente epiteliale e una mesenchimale maligna. Esistono anche varietà, ad esempio:<br />
adenosarcoma, significa che la componente ghiandolare è normale o quasi – comunque non<br />
neoplastica- e la componente fibrosa è maligna e si chiama adenosarcoma, non tumore misto perché<br />
la componente ghiandolare è benigna; l’adenofibroma è la sua varietà benigna in entrambe le<br />
componenti, epiteliale e mesenchimale, quindi tumore mulleriano misto ma benigno.<br />
[IMMAGINE]Tumore mulleriano misto maligno. Vedete la componente ghiandolare atipica,<br />
maligna e il sarcoma, fatto di cellule atipiche: la coesistenza delle aree mesenchimali maligne ci a<br />
fare diagnosi di tumore mulleriano misto. Addirittura possiamo trovare nello stroma delle cellule<br />
che si differenziano in senso di cellule muscolari striate, ad esempio la mioglobina è un marker del<br />
tessuto muscolare striato, quindi tipo rabdomiosarcoma.[IMMAGINE]Questo è l’adenosarcoma<br />
perché voi vedete la componente ghiandolare pressappoco normale perché somiglia all’endometrio,<br />
è questa [mesenchima]che è la componente atipica;[IMMAGINE]E poi l’adenofibroma in cui sono<br />
tutte e due normali, sia la componente epiteliale, sia quella stromale che tende ad assumere un<br />
andamento polipoide.<br />
LEIOMIOMI<br />
Questi sono i tumori più frequenti. E’ un tumore che può avere localizzazione varia e, a seconda di<br />
questa, abbiamo una sintomatologia corrispondente. Abbiamo il leiomioma sottosieroso che sta<br />
all’esterno perché l’utero è rivestito da una membrana sierosa, sta quasi all’esterno e dà meno<br />
fastidio pur raggiungendo dimensioni voluminose; io ho visto leiomiomi grandi come un feto<br />
meravigliandomi di come l’organismo si adatti, perché un leiomioma di queste dimensioni<br />
determina tutta una serie di sconvolgimenti soprattutto a livello intestinale perché è una massa<br />
enorme che preme sulle anse intestinali, quindi può determinare fenomeni di stipsi di vario tipo<br />
quando raggiunge queste grosse dimensioni; abbiamo invece l’intramurale che sta nello spessore del<br />
miometrio e può determinare, poiché ostacola le arteriole spirali, le metrorragie e quindi dà segni di<br />
sé, così come metrorragie le può dare il sottomucosale che si trova subito sotto l’endometrio,<br />
potendo dar luogo anche ad ulcerazioni e può succedere che a furia di erniare in superficie si<br />
distende nella cavità. E’ un tumore che parte dall’alto, si estende, dovendo crescere, nella cavità che<br />
trova davanti e si chiama in questo caso mioma nascens perché sembra nascere dalla cervice invece<br />
no, la sua radice è più in alto. Il leiomioma colpisce in oltre il 40% di donne di età maggiore ai<br />
50anni, le casistiche autoptiche però ci dicono che è difficile trovare un cadavere che non abbia un<br />
leiomioma per cui probabilmente è molto più diffuso, solo si tratta di leiomiomi che non hanno dato<br />
fastidio, le dimensioni possono essere variabili, qui sono descritte indagini molecolari di questi geni<br />
HMGIC, HMGIY che però hanno scarsa importanza perché si tratta di tumori benigni, una<br />
degenerazione maligna è eccezionale, pensare che un leiomioma possa diventare un leomiosarcoma<br />
è molto difficile; quindi il leiomioma è una lesione benigna che impone il trattamento chirurgico in<br />
determinati casi, quando per la sede può determinare metrorragie o altro, quando si tratta di una<br />
donna giovane che voglia avere figli; a volte si può fare l’intervento in laparoscopia se è esterno, o<br />
scaricato da www.sunhope.it
lo si fa in corso di travaglio di parto, ma richiede una notevole competenza perché può creare non<br />
pochi problemi; recentemente una paziente è deceduta in corso di travaglio di parto, proprio per<br />
questo intervento perché può avvenire una perforazione di parete, perché nel corso della gravidanza<br />
il leiomioma può addirittura ostacolare lo sviluppo della gravidanza può impedire l’allungamento e<br />
l’allargamento della cavità dell’utero e determinare delle asimmetrie della cavità, quindi bisogna<br />
intervenire tempestivamente anche perché questi miomi fatti di fibrocellule muscolari risentono del<br />
quadro ormonale, per cui tendono a crescere di più in gravidanza proprio per una certa disponibilità<br />
di ormoni, trofoblasti, cioè di altra natura che favoriscono, in generale la crescita. Cosa si può fare?<br />
Si può fare una miomectomia se si tratta di un mioma facilmente aggredibile in una donna giovane,<br />
si può fare l’isterectomia come si fa in caso di leiomiomatosi multipla, oppure possiamo optare per<br />
una terapia ormonale, visto che sono tumori molto sensibili agli ormoni, inoltre un intervento su cui<br />
si discute è l’embolizzazione arteriosa: se noi togliamo a questo mioma il suo supporto vascolare ed<br />
embolizziamo i vasi ci sarà la necrosi e il tumore scompare, sinceramente sono un po’ scettico verso<br />
questo intervento che appare come il meno traumatico di tutti, ma credo che possa risolvere il<br />
problema per un certo periodo di tempo, però dopo un po’ il mioma si riforma perché non è stata<br />
un’asportazione radicale. Le varietà. Vi sono leiomiomi, soprattutto nei soggetti giovani, che sono<br />
ricchi di figure mitotiche ma non presentano altre atipie, si è coniata la definizione, allora di<br />
leiomioma mitoticamente attivo, per non definirlo leiomiosarcoma in pratica, anche perché non lo<br />
è; poi esiste un leiomioma cellulato,quando ha una densità cellulare enorme che potrebbe indurci in<br />
errore con un leiomiosarcoma; leiomioma fissato pleiomorfo, ora lo vedremo, che presenta delle<br />
atipie così brutte e mostruose che esiste un concetto generale e cioè, quando le cose sono così brutte<br />
difficilmente sono brutte davvero, infatti abbiamo tutta una serie di tumori pleiomorfi o meglio<br />
bizzarri, con delle grosse cellule, ebbene quando sono così marcati questi segni bizzarri, non sono<br />
da considerare come segno bizzarro; leiomioma parassita, mi sono trovato a fare delle<br />
intraoperatorie con questo tipo, il leiomioma è molto spesso sottosieroso, guarda verso la superficie<br />
esterna, cresce,cresce,cresce, tende quasi a distaccarsi dall’utero e siccome vicino ci sono tube e<br />
ovari, per un fatto di compressione, determina lì un’azione un po’ di necrosi e un po’ di emorragia,<br />
si crea un nuovo supporto vascolare a spese della tuba e dell’ovaio e diventa quindi un leiomioma<br />
parassita perché si serve del supporto vascolare di altri organi e si distacca dall’utero; visto<br />
ecograficamente, il leiomioma parassita, sembra un tumore ovarico, anche perché raggiunge<br />
notevoli dimensioni, quindi diagnosticare una lesione del genere che viene indicata come “massa<br />
ovarica”, richiede una certa competenza; angioleiomioma è un tumore muscolare che nasce dalla<br />
parete muscolare liscia dei vasi, quindi può coinvolgere qualsiasi organo, anche l’utero, e, poiché<br />
nasce dalla parete dei vasi, noi vediamo delle immagini quasi a cipolla, cioè vediamo un vaso e<br />
tutt’intorno questo anfiteatro, queste fila di cellule muscolari lisce che fanno parte del tumore, non<br />
raramente può essere multiplo e coinvolgere più sedi dell’organismo, il caso più eclatante che ho<br />
visto –e che poi pubblicammo visto che raramente può raggiungere queste dimensioni-è quello di<br />
una paziente che aveva tanti di quegli angioleiomiomi a livello intestinale, TAC, RMN dicevano<br />
che si trattava di una cancerosi diffusa, una diffusione metastatica diffusa, il chirurgo, però, volle<br />
fare un intervento esplorativo per vedere di cosa si trattava, anche per fare una terapia relativa e<br />
grande fu la sua sorpresa quando trovammo, a tutti i prelievi che ci mandava –poiché non era<br />
convinto della diagnosi fece più di un prelievo- noi trovavamo angioleiomioma, al quarto, quinto<br />
prelievo si convinse; noi consigliammo anche la terapia e in questo caso la paziente può giovarsi di<br />
una terapia anti-endocrina, ormono dipendente attraverso cui queste masse tendono un po’ a<br />
regredire,ma bisogna fare questa terapia per tutta la vita.<br />
Domanda: Il profilo immunoistochimico di questi tumori è sempre lo stesso nelle diverse sedi?<br />
Risposta: Sì, è uguale in tutte le lesioni ed esprime tutti i markers delle cellule muscolari lisce, ma<br />
soprattutto vedremo sempre un pattern particolare di un vaso al centro e tutt’intorno questa<br />
stratificazione di cellule muscolari, quando è diffuso in realtà lo chiamiamo angioleiomiomatosi.<br />
[IMMAGINE]Questo è un leiomioma, vedete che è bianco, a volte abbiamo degli uteri così<br />
deformati, così pieni di leiomiomi, non è questo il caso perché qua si vede la cavità, che non si<br />
scaricato da www.sunhope.it
iconoscono le componenti dell’utero, sembra una massa pluribernoccoluta che non c’è più la cavità<br />
dell’utero; in quest’immagine, invece, vediamo il sottosieroso, il sottomucosale, questo se non si<br />
operava era destinato o ad andare in necrosi o a diventare parassita.[IMMAGINE] Questa anche è<br />
un’altra varietà di leiomioma che, improvvisamente, poiché cresce rapidamente, può andare<br />
incontro ad un’emorragia massiva che può poi determinare anche delle conseguenze sul piano<br />
generale perché c’è un consumo di piastrine locale notevole, legato all’emorragia, perché tutto il<br />
leiomioma appare così[IMMAGINE] questo successe a mia sorella.<br />
L’aspetto del leiomioma è classico, si tratta di cellule muscolari, vedete,[IMMAGINE] un po’<br />
ondulanti che hanno una caratteristica, di tanto in tanto questi vacuoli vicino al nucleo, questa<br />
vacuolizzazione perinucleare è una caratteristica della cellula muscolare liscia; [IMMAGINE]<br />
questa è la varietà cellulata ed è così cellulata che può simulare un fibrosarcoma; [IMMAGINE]<br />
questa è quella bizzarra, questa cellulosa qui sembra quasi un fantasma, con tutte queste immagini<br />
così anomale che solitamente si formano quando c’è un problema di vascolarizzazione, perché le<br />
cellule, in un ambiente ischemico, tendono ad assumere delle forme bizzarre che non sono atipie,<br />
sono solo aspetti bizzarri, infatti, osservandole bene non c’è una figura mitotica; [IMMAGINE]<br />
questo è un leiomioma intravenoso, pericoloso perché nasce dalle vene dell’utero, in questo caso si<br />
accresce a spesa delle vene e potete immaginare cosa può determinare arrivando al sistema cavale,<br />
delle trombosi, flebotrombosi, tromboflebite. Per quanto riguarda il leiomiosarcoma, a parte la<br />
presenza di aree necrotico-emorragiche, i caratteri di malignità sono quasi sempre quelli noti, da<br />
una parte abbiamo le mitosi, maggiori a 10*10 campi ( questo criterio lo ritrovate spesso), questo<br />
non vuol dire che dobbiamo avere più di 10 mitosi per ogni campo, ma che nel complesso, se<br />
sommiamo le mitosi osservate in 10campi devono essere superiori a 10 per fare diagnosi di<br />
leiomiosarcoma, figure mitotiche atipiche, una necrosi, immagini del tumore che presentano<br />
malignità, fermo restante che esistono situazioni in cui il “mosaico”pieno della malignità non si<br />
realizza e allora è bene dire “ad incerto potenziale di malignità”, questo succede raramente, quando<br />
ci si trova in quella “zona grigia” di incertezza.<br />
Dal punto di vista immunoistochimico e molecolare abbiamo mutazioni della p53, l’amplificazione<br />
del c-myc, queste cellule muscolari sono anch’esse estrogeno-dipendenti e hanno pure recettori per<br />
il progesterone.<br />
[IMMAGINE] Ecco un leiomiosarcoma, microscopicamente non possiamo fare la diagnosi di<br />
certezza, però già vedete che non tende ad essere ben delimitato ed è accompagnato da aree di<br />
necrosi ed emorragia. [IMMAGINE] Qua vedete un leiomiosarcoma con una figura mitotica<br />
veramente mostruosa perché è a croce; [IMMAGINE] Qua vedete un aspetto, che abbiamo già visto<br />
altre volte, questi sono i tumori chiamati “osteoclast-like”, e cioè, come gli osteoclasti sono delle<br />
cellule giganti che si trovano nell’osso e sono deputate al riassorbimento osseo, queste cellule,<br />
vedete, possono trovarsi nei tumori maligni ma anche nei carcinomi e in genere sono tumori molto<br />
maligni.<br />
Tra gli altri tumori non epiteliali non ci sono novità, abbiamo: l’angiosarcoma, il rabdomiosarcoma,<br />
l’istiocitoma fibroso maligno, il condrosarcoma ( che nasce da una metaplasia cartilaginea,<br />
probabilmente ) che si può verificare nei tessuti in condizioni particolari; poi abbiamo un termine<br />
nuovo, di cui forse parleremo più avanti che è il PNET ( primitive neuro-ectodermal tumor ), che è<br />
un tumore fatto da cellule nervose molto primordiali e che si manifestano al di fuori del sistema<br />
nervoso per un errore di migrazione, forse qualche cellula nervosa resta lì intrappolata o qualche<br />
cellula staminale che, ad un certo punto, va incontro a questo destino; poi abbiamo il “tumore<br />
adenomatoide”, si è chiamato così per lungo tempo, ma, in effetti, è un tumore mesoteliale benigno,<br />
perché adenomatoide? Perché riflettete su quello che fa la cavità celomatica che, in età adulta<br />
diventerà il mesotelio; ebbene, quando c’è un’invaginazione del mesotelio all’interno tende a<br />
formare delle ghiandole; molte ghiandole si formano, infatti, embriologicamente, per un<br />
invaginazione, cioè un po’ di questo epitelio va sotto e si formano strutture ghiandolari; quindi,<br />
adenomatoide vuol dire come se formasse delle ghiandole molto rozze e le cellule che compongono<br />
queste ghiandole sono uguali a quelle che si trovano nello stroma e quindi noi capiamo che la<br />
scaricato da www.sunhope.it
matrice è la stessa; si tratta di un tumore benigno che presenta tutte le caratteristiche<br />
immunochimiche dei tumori mesoteliali, di cui avremo modo di parlare.<br />
L’utero può anche essere sede di metastasi, il cancro della mammella può dare metastasi all’utero,<br />
il cancro dell’apparato gastrointestinale, il rene, il melanoma ( che è un tumore maligno che può<br />
dare metastasi ovunque, pensate, ci sono organi come , il cuore che, essendo un organo mobile, non<br />
consente facilmente il processo di metastatizzazione, ebbene l’unico tumore che può dare metastasi<br />
maligne è il cuore ) e poi l’appendice e così via.<br />
MAMMELLA<br />
La mammella, oltre ad avere un grosso impatto sociale, è stata, spesso, trasformata da molte<br />
persone in un’industria; addirittura sono venuti dall’America con un nuovo apparecchio che sono<br />
venuti a spiegarci qui a Napoli, poiché, avendo noi una grossa casistica, pensavano che potevamo<br />
fornire le basi per il funzionamento di questo nuovo apparecchio chirurgico che era in grado di<br />
estrarre il nodulo mammario attraverso un potenziale elettrico, creando poi un’area di necrosi,<br />
intorno alla lesione, che proteggeva da eventuali neoplasie o eventuali metastasi o eventuali<br />
estensioni; sostenevano la superiorità di questo strumento, in realtà la necrosi che si veniva a<br />
formare era piuttosto estesa, non aveva funzione protettiva, oltre a determinare tutta una serie di<br />
problemi ( vascolari e altro ).<br />
Per quanto riguarda la mammella, abbiamo un notevole sviluppo delle tecniche diagnostiche, se, ad<br />
esempio, paragoniamo i mammografi di oggi con quelli di 5-10 anni fa c’è stato uno sviluppo<br />
tecnologico spaventoso, soprattutto nell’acquisizione di capacità di discriminazione, di<br />
visualizzazione del dettaglio che prima non avevamo, queste capacità di discriminazione che hanno<br />
queste nuove tecniche consentono di individuare lesioni anche di 1-2 mm e quando la lesione è così<br />
piccola ci troviamo di fronte all’inizio della storia naturale della lesione, del tumore e anche la<br />
diagnosi diventa molto più difficoltosa, come se il tumore non avesse estrinsecato pienamente la sua<br />
malignità che “si trova ancora in culla”. Il cancro della mammella è tra quelli più studiati, se voi<br />
andate su PUBMED e cercate BREST, mettete gli ultimi5 anni, vi troverete di fronte un mare di<br />
pubblicazioni, di queste, per mio parere, solo l’1-2% dicono cose vero, il resto o scopiazzano o<br />
mettono idee bislacche che non resisteranno al tempo.<br />
C’è un approccio chirurgico molto diverso oggi; in genere la chirurgia è molto più conservativa<br />
perché si è visto che l’approccio “radicale”, non solo è inutile, ma spesso è controproducente,<br />
perché se io , ad esempio, tolgo un tumore maligno ramificato e così via e lascio le metastasi in<br />
sede, ho fatto un grande regalo alle metastasi, è vero che l’intervento è stato eseguito<br />
magistralmente, ma io ho reso un pessimo servizio alla paziente; c’è anche un altro problema: oggi<br />
le opzioni terapeutiche sono migliaia tant’è vero che lo stesso Veronesi qualche anno fa disse che se<br />
paragoniamo tutti i parametri e tutti i protocolli possibili arriviamo a diverse migliaia di opzioni<br />
terapeutiche <strong>complete</strong> perché radioterapia, non radioterapia, chemioterapia, che tipo di<br />
chemioterapia, terapia biologica, non terapia biologica, linfadenectomia, non linfadenectomia, che<br />
tipo di linfadenectomia, che tipo di intervento chirurgico…se mettiamo insieme tutte queste<br />
variabili, otteniamo migliaia di protocolli diversi ed è evidente che si va nella cosiddetta terapia<br />
“sartoriale”, cioè verso una personalizzazione della terapia di cui l’anatomo-patologo definisce un<br />
po’ la “taglia”. Com’è fatta la mammella?<br />
[IMMAGINE] Questo è un modello base dell’istologia perché sapete tutto della cellula mammaria,<br />
dei filamenti e così via, ma magari vi sfugge come è fatta una mammella normale. Qua abbiamo un<br />
dotto galattoforo che si dirama in altri dotti, cioè c’è una suddivisione dicotomica di questi dotti<br />
galattofori che sono diversi e che sbucano nell’areola mammaria fino al punto in cui abbaimo una<br />
dotto, vedete “extra-lobulare”.<br />
scaricato da www.sunhope.it
[Il prof. si assenta perché lo chiamano per controllare un estemporanea di polmone, torna e ci<br />
racconta] Quello che vuol sapere il chirurgo toracico quando opera una lesione polmonare non è il<br />
sottotipo, l’istotipo, ma si pone questo problema: è un carcinoma a piccole cellule (o microcitoma),<br />
molto frequente? Nel qual caso si cambia il tipo di intervento perché si sa che questo è un tipo di<br />
cancro molto diffusivo per cui l’intervento chirurgico è inutile e si limita a chiudere; se, invece, è un<br />
carcinoma non a piccole cellule, procede con l’intervento, procederà con la lobectomia se è piccolo,<br />
altrimenti con un intervento più grande se è più grande; in questo caso mi sono limitato a dire<br />
questo, che è quello che il chirurgo voleva sapere, personalmente credo che sia 1 carcinoma raro,<br />
non un adenocarcinoma, ma un carcinoma bronchiolo-alveolare, che è quello più subdolo, cresce a<br />
colate e riveste gli alveoli, aveva questo pattern particolare, ma lo confermeremo dopo,lui ora,<br />
dunque, procederà e ci manderà un intero lobo, l’intera grandezza della lesione, poi vorrà conoscere<br />
i margini dell’escissione, se, per esempio, ha fatto una lobectomia,o ci manderà i linfonodi per<br />
vedere se deve procedere ad una linfoadenectomia, l’estemporanea, infatti, non è un atto solo, ma<br />
può richiedere anche una giornata intera.<br />
Eravamo rimasti al dotto extralobulare da cui si dipartono i dotti terminali o intralobulari che<br />
terminano nei duttuli, cioè negli acini, e abbiamo, quindi, le unità dutto-lobulari, costituite dal ramo<br />
terminale che è una diramazione del dotto galattoforo che termina con gli acini. In una mammella<br />
non in gravidanza questi acini sono piccoli, addirittura non funzionalmente attivi, in gravidanza<br />
questi acini, invece, si allargano, si moltiplicano perché devono provvedere alla secrezione del latte.<br />
In passato si era tutti d’accordo che il punto in cui il dotto trapassa nell’acino ( lo vedete qui-> c’è<br />
1immagine) è un punto critico (come la giunzione per l’endocervice), quindi il dotto terminale<br />
intralobulare, perché il lobulo ha anche la sua simmetria, perché noi vediamo un tipo di connettivo<br />
che avvolge l’insieme di questi acini, l’unità funzionale, dunque, della mammella è questa unità<br />
dutto-lobulare, vedete, questo rappresenta il lobulo e questo rappresenta il sistema duttale terminale.<br />
Partendo da questo presupposto e dagli studi sperimentali, si vide che proprio questa porzione<br />
duttale terminale era la porzione da cui nasceva tutto, si vedeva che quando nasceva il processo<br />
neoplastico nasceva lì, comunque è rimasta la classificazione del carcinoma duttale e di quello<br />
globulare, perché desumevamo, erroneamente, che uno nascesse dai dotti e un altro dai lobuli, è che<br />
hanno una storia diversa. Prima voglio, però, darvi altre 2 nozioni: l’areola mammaria, soprattutto<br />
nell’area in cui si aprono i dotti galattofori è pigmentata, questo è un processo che compare<br />
soprattutto dopo l’adolescenza, quindi riconosciamo anche dei melanociti responsabili della<br />
pigmentazione e cellule particolari, la cui funzione non è ancora ben chiara, le cellule chiare di<br />
Toker, sono delle cellule epitelioidi dal citoplasma molto chiaro che hanno sede solo lì, una<br />
particolare patologia è stata erroneamente attribuita a queste cellule, lo vedremo più avanti. Se<br />
facciamo una sezione istologica voi vedete subito che il lobulo mammario ha un connettivo diverso<br />
dal connettivo esterno e che ha una strutturazione che già a occhio fa capire che si tratta di un’unità<br />
funzionale.[IMMAGINE] All’interno di questo lobulo riconosciamo il dotto terminale intralobulare<br />
che, in questo caso, è stato preso in 3 parti, in genere la sezione è in 2 dimensioni ma poiché il piano<br />
reale è tridimensionale, noi lo vediamo 3 volte, ma è lo stesso dotto; questo, invece, che voi vedete<br />
all’esterno [IMMAGINE] è il dotto terminale extraglobulare che, poi, in un piano inferiore o<br />
superiore si vedrà distaccarsi un ramo che diventerà intralobulare; [IMMAGINE] Ecco l’esempio di<br />
un dotto intralobulare in fase di quiescenza, qui vediamo gli acini appena appena rappresentati,<br />
queste cellule chiare che voi vedete intorno, vedete ci sono vacuoli e cellule appiattite che creano<br />
come un rivestimento all’esterno, sono cellule mioepiteliali, sempre presenti negli organi<br />
ghiandolari perché, quando si contraggono, la ghiandola butta fuori il secreto. [IMMAGINE]<br />
Questo è l’aspetto mammografico di 2 mammelle perché la mammella cambia la sua struttura a<br />
seconda dell’età; in un soggetto giovane la mammella è molto densa, tant’è vero che la<br />
mammografia, nei soggetti giovani, ha una maggiore percentuale di errore, proprio perché è<br />
piuttosto densa; la mammella anziana, invece, ha un fondo più pulito, per cui se c’ha un nodulo lo<br />
scaricato da www.sunhope.it
cogliamo subito. [IMMAGINE] Questo è quello che succede in allattamento, se facciamo una<br />
biopsia mammaria in allattamento, qui vedete i dotti pieni di secreto, ma tutte quelle ghiandoline<br />
che sembravano sparpagliate nell’unità globulare funzionale si moltiplicano enormemente, per cui<br />
tutta la mammella diventa un immenso tappeto di unità acidari, ghiandolari.<br />
Ci sono molto utili, anche in questo caso, l’actina e la p63. L’actina è un marcatore di benignità, qua<br />
vediamo degli acini e un dotto probabilmente terminale, vedete [IMMAGINE] come sono<br />
circondati da questi filamenti actino-positivi che derivano da queste cellule; se andiamo a fare la<br />
p63 che marca i nuclei delle cellule mioepiteliali vedete tutt’intorno quest’anello di cellule che<br />
rappresenta le cellule mioepiteliali, questo è un quadro benigno, perché il primo segno di invasività<br />
si ha quando si rompe quest’anello, il che vuol dire che le cellule devono andare fuori, tranne che<br />
non sia un carcinoma in situ, ma nel caso si trattasse di un carcinoma in situ, l’anello è vero che non<br />
si interrompe, ma ha dei punti focali in cui è irregolare.<br />
PRINCIPALI LESIONI INFIAMMATORIE DELLA MAMMELLA<br />
Sono molto frequenti. Un tipo, ad esempio, molto frequente è l’ectasia duttale; può succedere,<br />
come succede alle ghiandole sebacee, anche nei dotti mammari che ci siano punti di ostruzione<br />
legati al secreto, al muco e le strutture ghiandolari che stanno sotto si dilatano e a volte vi possono<br />
essere delle secrezioni sierose della mammella; in questo caso si fa l’esame del secreto e si vede che<br />
tipo di cellule ci sono, ci capita questo esame, se troviamo macrofagi, detriti cellulari e qualche<br />
linfocito, vuol dire che è un’ectasia duttale su cui si è sovrapposta l’infiammazione, perché laddove<br />
c’è ristagno è più facile che vi sia infiammazione. Poi abbiamo le mastiti, acute e croniche e<br />
soprattutto la mastite granulomatosa, fatta da granulomi con cellule giganti, tra queste mastiti<br />
granulomatose c’è quella “da silicone”, in effetti, prima, questa era una mastite diffusissima, oggi,<br />
con i nuovi tipi di silicone e di protesi in commercio, questa complicanza è diventata meno<br />
frequente, ma comunque possibile, in passato ho visto mammelle distrutte da queste protesi,<br />
addirittura casi di intraoperatorie in cui il chirurgo era convinto che fosse un cancro, perché la<br />
mastite granulomatosa deforma anche la struttura ghiandolare e determina fenomeni di retrazione<br />
della cute, fenomeni, questi, che fanno subito pensare al cancro, così come il cosiddetto aspetto “a<br />
buccia d’arancia”, cioè con queste cribrosità legate a delle minime trazioni, ma che possono essere<br />
anche legate alla mastite. Poi abbiamo un quadro particolarmente problematico, la cosiddetta<br />
lobulite sclerosante idiomatica, che è una patologia autoimmunitaria della mammella, che, quindi,<br />
corrisponde alla tiroidine, una sorta di “lobulite di Yashimoto”(battuta!), che può simulare un<br />
linfoma. In ultimo abbiamo la steatonecrosi, cioè la necrosi del grasso molto spessa legata a fattori<br />
traumatici o compressivi, perché possono determinare necrosi del tessuto adiposo che, a sua volta,<br />
chiama macrofagi, linfociti e così via.<br />
[IMMAGINI DEI QUADRI MENZIONATI] Ectasia duttale: una volta si faceva anche il<br />
duttogramma che oggi difficilmente si fa; perché lo si faceva? Perché c’è un’altra condizione che<br />
può verificarsi nei dotti e può dar luogo a questa secrezione ed è il papilloma dei dotti, che, a volte,<br />
può essere un carcinoma papillifero dei dotti, però, in genere, queste lesioni papillari non hanno una<br />
secrezione sierosa o siero-mucoide, ma hanno una secrezione in cui c’è anche sangue, ma basta fare<br />
un’esame citologico della secrezione per capirlo, in genere; torniamo all’ectasia: all’esame della<br />
secrezione, in genere, troviamo macrofagi, che sono cellule-spazzino, e poi una reazione di linfociti<br />
che stanno intorno e determinano infiammazione; ci può essere anche dolore, a volte retrazione del<br />
capezzolo e possono nascere problemi di diagnosi differenziale, infatti, a volte, c’è anche la fibrosi,<br />
per cui la stessa mammografia può dar luogo ad immagini dubbie.<br />
Mastite granulomatosa: vedete, questa è la protesi mammaria che viene inserita all’interno del<br />
muscolo pettorale o sopra il muscolo pettorale, dipende dal tipo di intervento programmato in<br />
relazione all’anatomia della persona e dal risultato che vuole; vedete, qui si è determinata questa<br />
situazione di irregolarità intorno alla protesi, in alcuni casi si può avere anche la rottura della<br />
protesi, in alcuni eventi traumatici; e questa è la mastite granulomatosa, vedete queste cellule<br />
scaricato da www.sunhope.it
giganti, plurinucleate, miste a linfociti e in questi buchi, ci sono altre sostanze dentro miste a<br />
sostanze oleose; può succedere di avere mastiti granulomatose anche per altre cause, anche in<br />
gravidanza, per esempio, perché in gravidanza fuoriesce del latte, si rompe qualche dotto e si può<br />
avere una reazione granulomatosa, anche per batteri e potete ancora vedere cellule giganti e<br />
osservate questi corpi all’interno di queste cellule giganti, questi si chiamano corpi asteroidi, perché<br />
hanno un nucleo centrale con dei filamenti, in passato si dava molta importanza a questi corpi che<br />
ritroveremo in un’altra patologia; ci può essere una mastite granulomatosa anche nelle aree<br />
adiacenti al cancro, però questo succede raramente e a volte il processo ma stitico può mascherare<br />
la presenza del cancro, raramente succede, e poi ci sono mastiti granulomatose da altre cause.<br />
Steatonecrosi: qui vedete l’aspetto mammografico con aree di varia densità, cistiche, ma non sono<br />
aree cistiche, piuttosto aree di necrosi; può essere associato anche a delle calcificazioni che voi<br />
vedete qui, vedete ancora cellule giganti e la necrosi del tessuto adiposo, che a volte assume un<br />
aspetto membranoso perché resta solo la membrana della cellula, non si vede più il nucleo perché la<br />
cellula è andata in necrosi.<br />
La lobulite linfocitaria sclerosante è caratterizzata d aqueste cuffie di linfociti che circondano i dotti<br />
e i lobuli; il problema nasce perché c’è un tipo di linfoma che fa pure questo pattern, ne parleremo.<br />
Si sa che questa è una patologia autoimmunitaria e gli infiltrati che conosciamo sono fatti da<br />
linfociti e plasmacellule e talora, a testimonianza di una forte sollecitazione immunitaria, troviamo<br />
anche i follicoli linfocitari secondari, quelli che solitamente troviamo nei linfonodi.<br />
La malattia fibrocistica,anche,è diffusissima, nelle casistiche settorie questa patologia incide per il<br />
60%, nelle casistiche cliniche per il 30%, l’età di massima incidenza è tra i 25 e i 45 anni.La<br />
diffusione di questa patologia ci rende consapevoli anche di un problema: intervento o non<br />
intervento? Dipende dai casi. La malattia fibrocistica non è considerata un fattore di rischio del<br />
cancro, ma bisogna dire che la stessa, però non esclude la presenza di un cancro all’interno, per cui<br />
l’interpretazione di un quadro mammografico di un cancro insorto su mastopatia fibrocistica è<br />
molto più problematico. Dal punto di vista clinico, la paziente stessa avverte delle cisti e delle<br />
noularità mammarie, la cisti è più molle, si riconosce, il nodulo è più forte perché corrisponde alla<br />
fibrosi; avvertirà anche dei cambiamenti in rapporto al ciclo mestruale, perché vi ho detto che gli<br />
estrogeni e il progesterone condizionano, per cui avvertirà un senso di tensione mammariain<br />
coincidenza con il ciclo e addirittura le cisti possono modificare le loro dimensioni in rapporto al<br />
ciclo mestruale e molto spesso sono bilaterali; ovviamente, questa bilateralità insieme agli altri<br />
segni clinici ci fa capire che è una mastopatia fibrocistica, quindi se si fa lo screening, l’avere una<br />
mastopatia fibrocistica non è una condizione per includere e seguire le pazienti con un maggiore<br />
follow-up, ma seguono gli screening comuni, con il solo problema che questa patologia di fondo<br />
può mascherare altre situazioni, talora troviamo foci di calcificazioni, spesso c’è di fondo un<br />
iperestrogenismo; in genere, poi, questa sintomatologia tende a scomparire durante la menopausa e<br />
ciò conferma che c’è un rapporto di retto con l’iperestrogenismo. Voglio chiarirvi questa patologia<br />
perché dai libri non si capisce bene; e ve la voglio rappresentare con un ombrello: la malattia<br />
fibrocistica è un modello base, quali sono le altre categorie? Le cisti semplici, delimitate da un<br />
epitelio sieroso;le cisti apocrine (sapete che la secrezione apocrina avviene per decapitazione) che<br />
normalmente nella mammella non ci sono;la fibrosi, che contribuisce a dare queste modularità e poi<br />
l’adenosi, ovvero una iperplasia dei lobuli e delle strutture duttali; queste fanno parte del modello<br />
base, ci può, poi, essere infiammazione, calcificazione. Sotto questo ombrello, poi, abbiamo altri<br />
tipi di lesioni che possono far parte di un quadro di mastopatia fibrocistica come avviene spesso o,<br />
addirittura, più raramente possono venire da sole, senza far parte del quadro della mastopatia<br />
fibrocistica, possiamo avere, quindi, lesioni iperplastiche e canceromatose che possono essere<br />
frequentemente associate alla mastopatia fibrocistica o venire da sole; infatti vedete che tutte le<br />
lesioni stanno sotto lo stesso ombrello, ma queste (lesioni iperplastiche e canceromatose) stanno ai<br />
margini perché possono anche venire da sole.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> (mammella) 23-11-<br />
2010<br />
Prof. Rossiello<br />
Ci soffermeremo un po’ di più sul cancro della mammella perché è la patologia più importante della<br />
sfera genitale femminile. Eravamo rimasti a parlare di quell’ombrello che è la mastopatia<br />
fibrocistica che ha delle caratteristiche di base e altre caratteristiche invece opzionali. Ecco come<br />
la mastopatia può apparire in una sezione trasversa,vedete queste sono delle cisti e questa è la<br />
fibrosi. Questo è un quadro di mastopatia molto avanzata. Poi ci sono quadri diversi in rapporto<br />
all’intensità dei diversi fenomeni,per esempio ci sono mastopatie in cui prevale l’aspetto cistico o<br />
l’aspetto fibrotico,altre mastopatie in cui l’aspetto fibrotico è meno rappresentato. Qui la fibrosi<br />
sono questi tratti bianchi che vedete in mezzo a questo tessuto giallo che è il grasso. Qui potete<br />
vedere un punto di repere metallico. Questa è una cosa che facciamo insieme ai radiologi e ai<br />
mammografisti,poiché ci troviamo sempre dinanzi a lesioni piccole di pochi mm,anche ai fini<br />
chirurgici sono lesioni che nell’ambito di una mastopatia è difficile poi identificarle. Allora il<br />
radiologo immette un punto di repere,un filo metallico per identificare il nodulo sospetto,in modo<br />
che poi il chirurgo lo trovi più facilmente. Poi vediamo perché la mastopatia a volte può presentare<br />
dei dubbi diagnostici,ne parleremo più avanti. Vedete che il punto di repere ha già risolto il<br />
problema di questo nodulo,perché si è determinata un’area di necrosi emorragica. Mi è capitato più<br />
volte di vedere che in dei tumori,facendo l’ago aspirato, si determini la trombosi di un vaso per<br />
puro caso e il nodulo scompaia,cioè non scompare,va in necrosi,quindi in fibrosi,per cui non ci sta<br />
più. Mi è capitato varie volte anche nella mammella. Se facciamo l’ingrandimento più forte<br />
vedremo i due tipi di cisti:questa è una cisti semplice; queste qui che voi vedete hanno un fondo<br />
blu come colore naturale:sono le cisti apocrine. Tutte queste trabecole bianche sono tutti fasci di<br />
fibrosi. Questa è l’immagine mammografica. L’immagine mammografica della mastopatia<br />
fibrocistica a volte può presentare qualche dubbio interpretativo. Qui vediamo certamente una<br />
mastopatia in cui c’è un rinforzo della fibrosi,nell’ambito della quale vediamo questo nodulo che<br />
pure è cistico e che può presentare dei problemi. In questi casi si fa l’agoaspirato in quella zona.<br />
La citologia aspirativa,come nella tiroide,può evere un ruolo determinante dal punto di vista<br />
diagnostico. Qui vedete una fibrosi notevole,delle opacità e poi un nodulo. Molto spesso i noduli<br />
nella mastopatia fibrocistica sono benigni. Poi cercheremo insieme una spiegazione del perché<br />
nella mastopatia fibrocistica possiamo trovare questi noduli che escono fuori dal resto della trama.<br />
Ecco una panoramica di un nodulo della mastopatia fibrocistica. Vedete cisti,una fibrosi notevole,<br />
quest’area di adenosi dove si addensano le strutture ghiandolari. L’adenosi è un aumento<br />
numerico delle ghiandole e fa parte del quadro base della mastopatia fibrocistica.<br />
Qua vediamo una piccola cisti,qua una fibrosi che può essere così intensa che questo<br />
scaricato da www.sunhope.it
lobulo,questa unità funzionale mammaria,viene quasi compressa e va in atrofia.<br />
Quindi vi sono delle forme di mastopatia dove prevale la fibrosi,altre dove prevale l’adenosi,altre<br />
dove prevale il quadro cistico,altre dove vediamo tutto;cioè c’è una notevole variabilità di aspetti.<br />
Possiamo trovare anche aree di iperplasia o di adenosi talmente intensa che le ghiandole stanno<br />
una addosso all’altra,e queste sono quelle aree che poi,quando si va a fare la citologia<br />
aspirativa,possono offrire qualche dubbio interpretativo.<br />
E questa è la cisti apocrina. A differenza della cisti semplice che ha un epitelio cubico o cilindrico,di<br />
tipo mucoide,qua vediamo che alcune cellule hanno una protuberanza apicale,perché c’è una<br />
secrezione apocrina,come qui vedete del materiale che si è staccato e viene secreto con un<br />
meccanismo cosiddetto apocrino,vi ricordo che la secrezione apocrina avviene per decapitazione<br />
della cellula.<br />
Un altro problema dal punto di vista interpretativo che possono presentare le mammografie sono le<br />
calcificazioni,a cui il radiologo da molta importanza,alla loro conformazione e disposizione,però<br />
sono sempre dati presuntivi,è sempre l’anatomopatologo a dare la diagnosi.<br />
Qua vedete questo materiale che addirittura sembra a scaglia,perché siccome la calcificazione è<br />
dura,quando la lama la taglia,salta e rimane fuori questo materiale che è duro;rimangono dei<br />
residui che si vedono anche alla mammografia come dei punti. È molto importante anche<br />
un’interconnessione tra patologo,chirurgo,radiologo,perché cosi ci si scambia informazioni.<br />
Il radiologo ha visto queste calcificazioni,noi gli diciamo che cosa sono e da questo confronto<br />
nasce un miglioramento per tutti!<br />
Ecco l’adenosi classica,vedete tutte queste piccole strutture ghiandolari una addosso all’altra,però<br />
non abbiamo dubbi,e in questo caso non abbiamo nessun dubbio,anche morfologicamente,ma<br />
comunque se facciamo la T63(?) che marca le cellule mio epiteliali,vediamo come queste strutture<br />
ghiandolari,per quanto disposte l’una addosso all’altra,sono delimitate perfettamente da queste<br />
cellule mioepiteliali.<br />
Le lesioni varie. Vedete che qua l’ombrello si è ristretto perché queste lesioni varie non sempre le<br />
troviamo nella malattia fibrocistica,cioè possono più spesso essere isolate.<br />
Vediamo quali sono. Lesioni a cellule colonnari rappresenta ancora un mezzo giallo perché in<br />
effetti è una metaplasia se vogliamo:al posto delle cellule acinari noi ritroviamo delle cellule<br />
colonnari che sono anche ciliate (indicate dalle frecce) che ricordano più la tuba. Questa lesione<br />
noi la ritroviamo spesso nelle adiacenze di un cancro. Questo ci insospettisce però non è chiaro il<br />
potenziale di questo tipo di lesione.<br />
scaricato da www.sunhope.it
E poi veniamo a due grossi problemi che abbiamo. Ce l’ha il patologo,il chirurgo e il radiologo,e voi<br />
questo lo dovete sapere perché dovete consigliare bene,cosa difficilissima perché c’è una grande<br />
confusione su questo argomento e una grande pubblicità su internet,per cui è anche difficile<br />
distinguere le cose vere dalle informazioni false che trovate su internet.<br />
Vediamo che cos’è l’adenosi sclerosante. Abbiamo parlato dell’adenosi,ma l’aggettivo sclerosante<br />
cosa vuol dire?vuol dire che qua la fibrosi assume un tale aspetto che determina fenomeni di<br />
distorsione. Mentre nell’adenosi vediamo chiaramente tutte strutture tubulari,nell’adenosi<br />
sclerosante,la fibrosi è cosi intensa che comprime queste strutture tubulari che addirittura possono<br />
assumere un aspetto a filiera,quasi trasecolare,per cui è difficile capire che è un’adenosi. Ecco<br />
queste sono delle “trappole” diagnostiche per tutti,ma soprattutto per noi anatomopatologi perché<br />
la diagnosi anatomopatologica ha un peso maggiore. Allora questo tessuto fibroso,determinando<br />
una tale deformazione,rende difficile capire che si tratta di una adenosi. Immaginate che un quadro<br />
del genere se fatto in intraoperatoria,dove la sezione congelata non ha una morfologia<br />
eccellente,è una delle trappole più forti perché noi anziché vedere un pattern ghiandolare,ci<br />
fissiamo a vedere queste irregolarità architetturali e questa è una delle trappole più grosse.<br />
A volte,papille e ghiandole sono compresse,i nuclei anche soffrono e anche le cellule;si può avere<br />
anche un’apparenza di stratificazione,cioè una pseudo-stratificazione. Quindi abbiamo una serie di<br />
dati che ci insospettiscono dal punto di vista della malignità.<br />
Radial scar è invece una situazione ben evidente mammograficamente e anche dal punto di vista<br />
anatomopatologico. Scar vuol dire cicatrice,dove si vede un punto centrale che è un’area di fibrosi<br />
e stranamente di diselastosi. Quindi non c’è solo la fibrosi,ma anche un accumulo di fibre<br />
elastiche. Il perché non lo sappiamo.<br />
Molto spesso il problema è che esiste una radial scar benigna e una radial scar carcinoide.<br />
Cioè il carcinoma che sembra essere una cicatrice,cioè un punto centrale di addensamento,e poi<br />
come dei raggi che partono da questo punto centrale. Questa immagine ovviamente implica un<br />
approfondimento diagnostico. Spesso si tratta di una cosiddetta radial scar,ci sono degli studi che<br />
stanno facendo,molto interessanti,che dicono che questa radial scar carcinoma potrebbe essere il<br />
primo step del carcinoma. Però tutte e due le lesioni,soprattutto la radial scar possono essere<br />
associate a varie displasie di cui parleremo più avanti.<br />
Vediamo un’immagine di adenosi sclerosante. L’adenosi sclerosante determina anche a livello<br />
mammografico delle immagini di difficile interpretazione. Ecco,qua per esempio vediamo un nodulo<br />
di addensamento che presenta già alla mammografia,una distorsione;che è un addensamento<br />
diverso dal resto del parenchima. Vedete qui sembra proprio che c’è una compressione,<br />
un’irregolarità della trama,degli addensamenti,insomma ci sono tutta una serie di caratteri<br />
scaricato da www.sunhope.it
adiologici che inducono al sospetto. Qual è il quadro morfologico,vedete questa è una adenosi<br />
sclerosante facile per motivi didattici;vedete in quest’area qui i tubuli non ci sono più. Qua invece<br />
vedete dei tubuli e delle aree che tendono ad essere solide,vedete questi sono fenomeni legati<br />
proprio alla compressione. Quindi vi sono dei casi in cui i tubuli non si vedono più e dei casi in cui<br />
si vedono come qui,vedete,questo materiale un po’ blu,sono calcificazioni;quindi abbiamo delle<br />
micro calcificazioni associate ad una distorsione dell’architettura e un quadro difficile da<br />
interpretare per tutti,in questo caso è facile. Se non si tratta di un’intraoperatoria e quindi abbiamo<br />
il tempo,andiamo a fare l’actina e vedete che tutte le strutture ghiandolari però,pur essendo<br />
abnormi,pur essendo trasecolate e irregolari,presentano sempre questo anello periferico di cellule<br />
actino-positive,il che ci fa capire che non c’è stata invasività e che si tratta di una lesione benigna.<br />
La radial scar,in questo caso benigna,è rappresentata da un’area centrale,come questa,vedete<br />
questo materiale un po’ basofilo,un po’ fibroso,se andiamo a fare dei metodi per le fibre<br />
elastiche,di cui non parliamo proprio,noi abbiamo dei metodi speciali,o ricorriamo<br />
all’immunoistochimica, vediamo che questa zona è ricca di fibre elastiche e tutt’intorno,secondo<br />
una disposizione radiale,si dispongono queste strutture tubulari,al centro c’è quest’area di<br />
fibrosi,molto spesso c’è una cisti al centro e tutta un’area di fibroelastosi intorno. Radiologicamente<br />
vedete,l’immagine si appalesa cosi:un nucleo centrale con tutti questi raggi intorno. È un’immagine<br />
sospetta.<br />
Veniamo ora ad un altro problema. Vedete qui l’ombrello si restringe un po’(l’immagine è<br />
sbagliata!) perché abbiamo l’iperplasia duttale,l’iperplasia lobulare e l’iperplasia a cellule colonnari.<br />
Fino ad ora abbiamo parlato di lesioni varie;ora parliamo delle iperplasie. Le iperplasie possono<br />
venire da sole,o possono venire inquadrate nell’ambito di una mastopatia fibrocistica.<br />
Vediamoli un po’. Questa è l’iperplasia duttale. Vi ricordate come era fatto il lobulo? Qua invece<br />
vedete tutti questi dotti che proliferano,stanno uno addosso all’altro,quasi scompaiono gli acini. Poi<br />
cercheremo di unificare tutte queste lesioni e di dare un’interpretazione clinica a tutti questi quadri<br />
anatomopatologici. Comunque ricordatevi che l’iperplasia duttale è un aumento numerico dei dotti<br />
che tendono a fare degli agglomerati. Ecco questo è un particolare. A volte possiamo avere degli<br />
aspetti quasi papillari prechè c’è un’iperplasia di fondo e voi sapete che molto spesso la ghiandola<br />
ha uno scheletro fibroso intorno che le impedisce di dilatarsi esageratamente,allora succede che<br />
per fare spazio alle nuove cellule,si solleva in papille,cosi da aumentare la superficie utile e far<br />
spazio alle nuove cellule che proliferano,perché c’è uno squilibrio tra proliferazione e<br />
differenziamento.<br />
Iperplasia lobulare,qui vedete il duttulo terminale che si sfiocca,,vedete che il lobulo mammario,che<br />
normalmente è piccolo, si è ingrandito enormemente e vedete che proliferano tutte le strutture<br />
acinari.<br />
scaricato da www.sunhope.it
Interrompiamo ora questa trattazione sulla mastopatia,,che riprenderemo quando facciamo la<br />
precancerosi, e passiamo ai tumori benigni della mammella:<br />
• fibroadenoma<br />
• papilloma<br />
• tumore filloide<br />
• adenoma<br />
e poi altri tumori di cui vi parlerò, i tumori connettivali, i soliti angiomi,i soliti fibromi e cosi via.<br />
Il fibroadenoma è un tumore frequentissimo soprattutto in età giovanile (seconda,terza decade).<br />
In genere,come accade anche mammograficamente,è un nodulo ben delimitato,quindi anche<br />
chirurgicamente asportabile dal contesto del parenchima mammario. È un nodulo mobile,in genere<br />
non è doloroso,e qui c’è scritto che la citologia aspirativa può fare degli errori diagnostici e vi<br />
spiego il perché.<br />
Noi anatomopatologi siamo fissati sulla descrizione accurata di tutto quello che vediamo.<br />
Distinguiamo un fibroadenoma intracanalicolare e un fibroadenoma pericanalicolare. Questi termini<br />
ve li spiego perché a volte sui testi non si trovano queste spiegazioni.<br />
Il fibroadenoma pericanalicolare è questo,quindi un lesione che ha una capsula,che qui non si<br />
vede, e dentro vediamo dei duttuli e che cosa notate di strano rispetto alla norma? Che non c’è più<br />
quell’architettura lobulare,perché normalmente ogni lobulo è separato da un diverso tipo di<br />
connettivo e poi c’è un altro lobulo,e cosi via. Qui invece vediamo una diffusione che è uguale,è<br />
l’adenoma,e questo tessuto fibroso separa l’uno dall’altro. Dal punto di vista clinico peri ed<br />
intracanalicolari sono uguali. Che cosa succede,il connettivo penetra nella ghiandola,la comprime<br />
e a un certo punto la ghiandola si arcua sempre più,fino a diventare una struttura bi stratificata ed<br />
arrivare a questo aspetto vedete, che il lume non si vede più. Diciamo intracanalicolare perché<br />
sembra quasi che al centro di questa struttura c’è il connettivo. In effetti è una falsa<br />
immagine,perché non so se avete capito tutta la dinamica: immaginate una specie di ghiandola<br />
grande,che poi il connettivo al centro la deforma,determina una distorsione,e poi si salda sotto. Al<br />
centro vediamo il connettivo e alla periferia rimane un epitelio bi stratificato. Questo epitelio bi<br />
stratificato,per effetto di questa compressione pericanalicolare dovuta soprattutto ad una iperplasia<br />
dello stroma,presenta delle atipie all’agoaspirato,delle atipie di tipo reattivo ovviamente,non di tipo<br />
neoplastico, e se uno non è abile a capire può prendere una cantonata. L’agoaspirato del<br />
fibroadenoma può essere pericoloso per questo, perciò è importante la discussione con il<br />
radiologo e gli altri specialisti.<br />
scaricato da www.sunhope.it
Il fibroadenoma giovanile,viene addirittura in soggetti nella prima decade,l’età di massima<br />
incidenza è tra i 10 e i 20 anni. Cresce rapidamente e può raggiungere enormi dimensioni,tanto da<br />
insospettire il clinico,la pz e la famiglia. Può diventare maggiore di 20cm. In effetti è un<br />
fibroadenoma con una marcia in più perché c’è un’iperplasia cosi spiccata dell’epitelio e dello<br />
stroma,che l’epitelio si solleva ancora più caratteristicamente in papille. Però se facciamo l’actina ci<br />
rendiamo conto che tutte le strutture ghiandolari addossate in maniera irregolare molto sospetta<br />
perché c’è questa immagine “back to back”,sono sempre delimitate dall’actina,quindi si fa la<br />
diagnosi di fibroadenoma giovanile che spiega tutte queste caratteristiche.<br />
Poi abbiamo il papilloma intraduttale. Questa è un’immagine chiara mammograficamente,ma<br />
radiologicamente vedete che uno dei dotti,molto spesso riguarda i grandi dotti,i dotti galattofori,si<br />
dilata per fare spazio a queste protuberanze che sono proprio i papillomi. Sono lesioni dei dotti<br />
galattofori. Accompagnate molto spesso da una secrezione dal capezzolo,che non sempre,ma<br />
spesso, è ematica e presenta spesso citologicamente dei caratteri particolari,per cui la persona<br />
esperta capisce che si tratta di un papilloma. In questo caso la mammografia si fa dopo che<br />
l’anatomopatologo esprime questo dubbio.<br />
Queste lesioni,pur essendo benigne,sono legate ad un elevato rischio,e talvolta possiamo avere<br />
dei quadri molto strani di papillomatosi multiple,cioè che tutti i dotti sono colpiti da questi papillomi.<br />
Sono collegati ad un alto rischio perché rappresentano un disordine cinetico,e c’è anche un<br />
problema grosso di cui parleremo più avanti,ovvero la diagnosi differenziale con il carcinoma<br />
papillifero. Tale diagnosi non è sempre agevole e non si può basare solo sui dati citologici perché<br />
anche nel papilloma ci sono atipie,infatti per analogia seguiamo gli stessi criteri per la distinzione<br />
tra adenoma e carcinoma follicolare della tiroide; cioè dobbiamo cercare l’invasività e gli emboli,ma<br />
soprattutto l’invasività in questo caso,quindi dobbiamo studiare ben bene i margini,sempre se<br />
siano stati asportati dal chirurgo. Ecco l’aspetto morfologico:qui vediamo la parete del dotto che si<br />
è enormemente dilatata per effetto della compressione di questo papilloma. Perché capiamo che è<br />
un papilloma?perché nel connettivo e nella base di impianto non ci sono segni di invasività. Se<br />
questo dato è confermato in più sezioni,possiamo dire che è un papilloma. Qua vediamo un<br />
particolare di questa immagine. In particolare vediamo che ci sono delle atipie,la pseudo<br />
stratificazione anche nel papilloma normale,questo è il motivo per cui dobbiamo cercare segni di<br />
malignità per la diagnosi differenziale. Questo vuol dire anche che quando facciamo una diagnosi<br />
intraoperatoria e c’è una lesione papillifera,ci lasciamo sempre un margine per dire che<br />
successivamente analizzeremo in toto la lesione,per vedere se ci sono segni di invasività o meno.<br />
In ogni caso si tratta di lesioni giovanili. Il tumore filloide è un tumore che come massima incidenza<br />
si presenta nella 3-4 decade,però può riguardare anche i giovani. Si chiama filloide dal greco che<br />
significa foglia,perché anche macroscopicamente presenta un aspetto foliaceo,confermato poi<br />
anche a livello istologico. La caratteristica di fondo di questa lesione è che c’è una tale iperplasia<br />
scaricato da www.sunhope.it
sia della componente epiteliale,sia di quella connettivale che si determinano come delle foglie nelle<br />
strutture duttali che si dilatano enormemente,queste cisti poi penetrate da questi cunei di<br />
connettivo diventano enormi e avremo tutta una struttura connettivale che vi spiegherò poi.<br />
Questa lesione si chiama tumore filloide attualmente,perché il termine antico (cistosarcoma filloide)<br />
dava luogo a dei dubbi.<br />
In linea di massima è un tumore benigni,ma vi sono dei casi in cui può essere maligno. La<br />
malignità si basa sulle solite caratteristiche:figure mitotiche,atipie e tutto il resto. La lesione è<br />
maligna se su 10 campi osservati ci sono almeno 10 figure mitotiche (almeno 1 per campo<br />
osservato).<br />
Ecco qui l’aspetto istologico,vedete le foglie,si solleva questo connettivo e questo connettivo può<br />
presentare anche delle atipie morfologiche,però non vediamo figure mitotiche. Anche l’epitelio può<br />
presentare una tendenza alla pseudo stratificazione.<br />
A proposito il prof racconta la storia di una suora di Pompei che gli portò la mammella di<br />
un’orfanella,a cui era stata asportata dopo essere stata fatta diagnosi di cancro. Lui però<br />
analizzando il pezzo disse che si trattava invece di una lesione benigna e la suora fu felicissima e<br />
gli fu molto grata.(l’ho riassunto nel caso in cui dovesse chiederlo,visto che gira voce che chieda<br />
anche questi fatti)!<br />
L’adenoma del capezzolo è molto raro.<br />
Molto spesso si presenta come una retrazione del capezzolo. Mammograficamente si vede un<br />
nodulo retroareolare. Questo adenoma che oggi viene spesso in corso di allattamento, è una<br />
lesione delimitata che può erodere anche l’areola mammaria e quindi assumere una caratteristica<br />
molto sospetta che fa pensare ad un cancro,ma non è un cancro perché è un adenoma.<br />
Parleremo ora di iperplasia duttale atipica,di carcinomi in situ,iperplasia lobulare atipica,iperplasia<br />
epiteliale piatta che è una novità inserita da pochi anni..<br />
Su queste lesioni precancerose ci soffermiamo un po’ di più perché è un capitolo relativamente<br />
nuovo perché per molti anni non si è capito niente circa gli stadi preliminari del cancro.<br />
Tutte queste aree le ritroviamo adiacenti al carcinoma in una percentuale variabile dal 50 al 90%, e<br />
questo conferma che queste alterazioni sono comunque correlate alla cancerogenesi mammaria.<br />
Quando esaminiamo un cancro andiamo a vedere le aree adiacenti e vediamo queste lesioni. E ci<br />
dimostrano anche un’altra cosa,cioè che il cancro non è una malattia localizzata,ma molto spesso<br />
riguarda tutto l’organo,solo che in un punto ci da il cancro e in altri punti ci da iperplasie,displasie e<br />
così via. Questo molto spesso ci dice anche che dobbiamo seguire i pazienti quando hanno avuto<br />
scaricato da www.sunhope.it
un intervento di tipo conservativo.<br />
Il rischio di carcinoma nell’iperplasia tipica,rispetto alla popolazione che non ha questa lesione,<br />
aumenta di 2 volte. Il rischio di carcinoma coesistente o metacrono,cioè che insorgerà<br />
dopo,aumenta di 4-6 volte; se vediamo un carcinoma in situ,il rischio che si abbia un carcinoma<br />
invasivo aumenta di 10-12 volte. E la mastopatia fibrocistica? La mastopatia è stata spesso fonte<br />
di discussioni,perché c’erano studi prospettici epidemiologici che dimostravano che comunque un<br />
rischio debole ce l’aveva e altri studi che invece dicevano che il rischio era uguale alla popolazione<br />
generale. Questa controversia si è un po’ risolta,perché non conta tanto la mastopatia,cioè il<br />
“modello base”,ma contano le lesioni associate,perché se c’è una mastopatia con iperplasia<br />
tipica,allora anche la mastopatia darà un rischio 2 volte maggiore,se c’è una mastopatia con un ca<br />
in situ,il rischio aumenta di 10-12 volte. Quindi era proprio sbagliata l’impostazione del problema.<br />
Iperplasia duttale atipica. Perché atipica?Si capisce bene perché c’è un aspetto back to back, c’è<br />
una tendenza alle atipie citologiche,alla pseudo stratificazione e un certo disordine strutturale,ma<br />
non c’è invasione e non si può parlare ancora di ca in situ,ma è una diagnosi ancora più sottile di<br />
cui non vi parlo proprio,come si fa a distinguere un’iperplasia atipica da un ca in situ è un problema<br />
molto complesso. L’iperplasia a volte può assumere anche questi aspetti cribrosi,vedete questo<br />
tessuto sembra tarlato,con delle cribrosità spugnose.. Se vediamo un particolare,ci rendiamo conto<br />
di cosa vuol dire l’atipia,di cosa sia una tendenza alla pseudo e alla vera stratificazione,perché si<br />
osserva sia pseudo stratificazione che stratificazione con delle atipie. ; è sempre mantenuto però<br />
questo straterello esterno che è fatto di cellule mio epiteliali,fino ad arrivare al ca in situ. Il<br />
carcinoma duttale in situ è un grosso problema. La forma più classica radiologicamente è questa<br />
qui,vedete,noi abbiamo questo aspetto tipo comedocarcinoma,perché comedocarcinoma? Perché<br />
riguarda quelle lesioni comedoniche della cute,per cui al centro c’è un’area di necrosi,molto spesso<br />
calcifica e tutt’intorno ci sono delle atipie evidenti,però mai invasive,altrimenti non sarebbe un<br />
carcinoma in situ. Quindi noi diciamo carcinoma in situ,tipo comedocarcinoma,perché giustifica<br />
anche il quadro mammografico,perché ognuna di queste strutture mammograficamente da queste<br />
calcificazioni.<br />
Questo è il tipo di carcinoma in situ cosiddetto a cintura. A cintura perché non ha un’area di necrosi<br />
centrale,ma c’è come una cintura intorno di cellule atipiche,molto atipiche,che però non superano<br />
mai la membrana basale.<br />
Carcinoma in situ solido. Le forme solide sono quelle di più facile interpretazione,perché vedete,<br />
questo è un dotto e addirittura non c’è più il lume,quindi è un carcinoma in situ che ha perso anche<br />
il lume. A volte può assumere degli aspetti papilliferi o degli aspetti cribriformi analoghi a quelli<br />
della iperplasia duttale,solo che qui ci sono più atipie che ci fanno pensare ad un ca in situ. Alcuni<br />
hanno introdotto il termine di DIN,come CIN,perché il ischio per il carcinoma intraduttale diventa<br />
scaricato da www.sunhope.it
anche delle atipie citologiche. Queste atipie citologiche si classificano come C1, C2, C3 nel<br />
carcinoma intraduttale. L’evoluzione dell’iperplasia duttale atipica e maggiore rispetto all’ipeplasia<br />
duttale,l’intervallo di manifestazione si riduce sempre di più,perché per un’iperplasia duttale<br />
vediamo un 2.6 – 4% dei casi che può evolvere verso il cancro,con un intervallo che può arrivare a<br />
14 anni;per l’iperplasia duttale atipica,questo intervallo si riduce a 7-8 anni,per il carcinoma<br />
intraduttale c’è un intervallo molto variabile,a seconda del grado di differenziazione. Ovviamente il<br />
C3 corrisponderà al 45%,il C1 al 15%,l’intervallo entro cui si manifesta questa trasformazione e<br />
degenerazione maligna in cancro è molto più breve,cioè dai 4 ai 6 anni. Il grading viene valutato in<br />
base ai soliti parametri: atipie citologiche,dimensioni,figure mitotiche,necrosi,e cosi via.<br />
Ecco questo è un esempio di G1,vedete cellule piccole un aspetto un po’ cribroso,e qua vedete le<br />
atipie più marcate,però mai superata la membrana basale. Ovviamente il rischio di un carcinoma<br />
sincrono o metacrono in G3 è molto più elevato. E poi questo carcinoma in situ ha anche un altro<br />
difettuccio serio,cioè che quando noi troviamo questo carcinoma in situ cosi,oppure aree di<br />
carcinoma in situ inserite in un carcinoma duttale,per cui possiamo avere delle aree di carcinoma<br />
invasivo adiacenti ad aree di carcinoma in situ,dobbiamo sempre stare attenti alla bilateralità e alla<br />
multicentricità. Diciamo che quando troviamo lesioni intraduttali,in situ, c’è la tendenza ad essere<br />
multicentrici,cioè a riguardare entrambe le mammelle,quindi dobbiamo controllare anche la<br />
mammella apparentemente sana.<br />
L’iperplasia lobulare atipica. Qui vedete un’immagine molto chiara. Questo è il dotto terminale<br />
intralobulare,guardate come si è dilatato,e per forza,perché tutti questi acini sono diventati solidi.<br />
Qui si vede DIN1, DIN2, DIN3,io non vi do i dati statistici di queste tre cose perché vi darei i<br />
numeri,ma la cosa importante è che il rischio di carcinoma è 6 volte ,maggiore a seconda del<br />
grado ed evoluzione che riguarda il 15-43% dei casi.<br />
Si possono trovare questo tipo di lesioni anche adiacenti a carcinomi invasivi. Ecco,questo è un<br />
DIN1, vedete l’acino è diventato solido però è fatto da piccole cellule,e qua un DIN3 cioè con delle<br />
atipie molto spiccate e ovviamente aumenta il rischio.<br />
Fino ad arrivare al carcinoma lobulare in situ. Ecco,vedete il lobulo è diventato enorme,solido,in<br />
effetti le cellule acinari sono piccole;qua si vede qualche struttura ghiandolare residua,però se<br />
andiamo a fare l’actina,ci rendiamo conto che è una situazione in situ,perché c’è sempre un anello<br />
di actina intorno e questo ci da maggiore sicurezza..<br />
L’alterazione a cellule colonnari è un’alterazione che è emersa recentemente. Si parla di iperplasia<br />
a cellule colonnari,si parla di un’atipia epiteliale piatta,che molto spesso è associata a carcinoma<br />
duttale in situ. Queste alterazioni a cellule colonnari possono essere associate nella metà dei casi<br />
a iperplasie lobulari atipiche,a carcinoma lobulare in situ,a carcinoma duttale in situ e carcinoma<br />
scaricato da www.sunhope.it
tubulare,che è un tipo particolare di carcinoma,fatto da tubuli,di cui parleremo più avanti. Quindi<br />
diciamo che questa alterazione a cellule colonnari che adesso ha ancora una componente<br />
misteriosa,è comunque una precancerosi,perché nella mtà dei casi è associata a lesioni<br />
precancerose note di tipo lobulare,duttale,lesioni atipiche o anche carcinomi in situ. Come è fatta<br />
l’iperplasia? Ecco qui vediamo una stratificazione,qui si capisce bene che è un’atipia di tipo<br />
apocrino,a volte infatti può essere anche apocrina,ma non vuol dire niente se è apocrina o meno,<br />
ed è piatta,perché non determina delle atipie papillariformi. Quindi quali sono i precursori del<br />
carcinoma mammario:iperplasia atipica e carcinoma duttale in situ,l’atipia epiteliale piatta,il<br />
papilloma atipico e il carcinoma papillare in situ di cui non abbiamo parlato ancora,e vedete una<br />
novità:i carcinomi microinvasivi. È una novità perché tecnicamente dal punto di vista biologico e<br />
rigorosamente anatomopatologico,il carcinoma microinvasivo è un carcinoma invasivo. Però si è<br />
detto che da un punto di vista clinico evolutivo che se il carcinoma risponde a questi criteri di<br />
invasività,cioè una sola area invasiva inferiore a 2mm di distanza dall’area di carcinoma in<br />
situ,quindi è un’invasione iniziale vicina all’area di carcinoma in situ. Oppure 2 o 3 aree inferiori a<br />
1mm le possiamo assimilare a delle precancerosi,anche se è una forzatura perché il rischio di<br />
metastasi,che poi la metastasi rappresenta il grosso rischio del tumore della mammella, è cosi<br />
basso (dall’1 al 5% dei casi) che possiamo assimilarlo ad una lesione precancerosa. Questa è una<br />
novità che vale in assoluto,perchè non vale per altri organi, vale solo per la cervice,dove i<br />
carcinomi microinvasivi hanno i limiti di 5 e 7mm,mentre qui il limite è rappresentato dalla<br />
membrana basale dell’area di carcinoma in situ,se a distanza è inferiore a 2mm o inferiore a 1mm.<br />
Ecco il carcinoma papillare in situ:atipie notevoli,però non è mai superata la membrana basale;<br />
anche qui non è superato l’asse connettivo vascolare.<br />
Questo è un carcinoma microinvasivo,questo è un comedocarcinoma; anche questo è un<br />
carcinoma “comedo” perché al centro c’è un’area di necrosi però è invasivo perché vedete queste<br />
celluline, questi tubulini che stanno qui? Questa è un’area di invasione e se andiamo a<br />
misurare,vediamo che la distanza del gettone maligno più lontana dal cancro non supera i<br />
2mm,per cui rientra nella classificazione di carcinoma microinvasivo.<br />
Qualcuno fa una domanda che non si capisce e la risposta è:immaginate di avere un salvagente e<br />
con una sbarra di legno ci andate dentro,questo salvagente si piegherà,e poiché si tratta di cellule,i<br />
margini di questo salvagente tenderanno a saldarsi e quindi cosa succederà?che al centro rimarrà<br />
la trave che corrisponde al connettivo e tutt’intorno questo salvagente disposto in due strati perché<br />
noi lo abbiamo piegato in due strati. Questa è la forma intracanalicolare. Se non conoscessi questa<br />
dinamica,potrei credere che il connettivo sia una ghiandola,perché sembra quasi una ghiandola<br />
che circonda un connettivo al centro,invece questo vuol dire intracanalicolare. Vi ho detto questo<br />
peerchè quando si fa l’agoaspirato,queste cellule sono vittime di questa esuberante proliferazione<br />
scaricato da www.sunhope.it
connettivale,si deformano,si sagomano le une con le altre,per cui assumono irregolarità<br />
nucleari,delle atipie. Questo è un fenomeno che si realizza sempre quando una cellula si trova in<br />
situazioni di agonia tenta di moltiplicarsi,quasi a voler conservare la vita. Questa è una cosa che<br />
sanno bene gli esperti di diagnostica intraoperatoria,perché per esempio se io faccio una diagnosi<br />
intraoperatoria di lesione cerebrale e non conosco il problema,molto spesso nei tumori cerebrali<br />
sono molto importanti le figure mitotiche,nel pezzo congelato queste cellule vanno in mitosi,e<br />
quindi mi trovo un numero di mitosi sproporzionato alle atipie del tessuto legato proprio a questa<br />
situazione di sofferenza. Questa sofferenza di queste cellule,poi si traduce in atipie,perché cercano<br />
di moltiplicarsi,probabilmente è difficile anche moltiplicarsi una situazione in cui stanno una<br />
addosso all’altra e quindi si deformano,anche il materiale nucleare si disperde e nascono tutta una<br />
serie di problemi. Vi ho spiegato questa dinamica non per un fatto accademico,ma perché può<br />
essere causa di un errore diagnostico.<br />
Questi sono dei dati che ci provengono dall’ American Cancer Society nel 2008,e questo riguarda<br />
la mortalità per cancro,e vedete che la mortalità per tumore della mammella negli ultimi anni si è<br />
ridotta e questo è indicativo di successo della terapia. Vediamo invece dal punto di vista<br />
dell’incidenza e della mortalità,vedete, per quanto riguarda l’incidenza nella femmina la mammella<br />
è al primo posto,perché da solo il cancro della mammella rappresenta il 26% di tutti i tumori maligni<br />
che si possono manifestare;per quanto riguarda la mortalità però la mammella scende al secondo<br />
posto,perché sale al primo il polmone. Quindi il polmone,pur avendo una minore incidenza,ha una<br />
mortalità maggiore rispetto alla mammella e questo vuol dire che il trattamento del carcinoma<br />
mammario ha riscontrato dei progressi che non si sono registrati nel carcinoma polmonare.<br />
Questo è il tasso grezzo di questa associazione nazionale dei registri,registrato per paese. In Italia<br />
ci situiamo vicino alla media che è 109 casi per 100000 abitanti per anno. In paesi come la Grecia<br />
e l’Irlanda l’incidenza è minore,perché anche per il cancro alla mammella ci sono dei fattori<br />
protettivi,cioè l’allattamento al seno,la gravidanza precoce ecc. Anche in Spagna l’incidenza è<br />
abbastanza bassa,mentre ci sono dei paesi come la Svezia,il Belgio,la Danimarca dove l’incidenza<br />
è maggiore che in Italia. È molto interessante uno studio fatto un po’ di tempo fa,dove alla base<br />
della storia naturale del cancro alla mammella non c’è solo un fattore razziale,ma ci sono anche<br />
delle abitudini. In America fu fatto uno studio sulle donne giapponesi. In Giappone c’è una bassa<br />
incidenza di cancro della mammella,ma se le donne giapponesi si trasferiscono in America,questa<br />
incidenza cambia e aumenta molto,avvicinandosi a quella americana. Già nella prima generazione<br />
c’è un aumento,nella seconda poi quasi si eguaglia all’incidenza americana che è più alta che in<br />
Europa. Questo vuol dire che indubbiamente c’è una predisposizione genetica,ma l’incidenza è<br />
anche legata ad abitudini di vita.<br />
Per quanto riguarda l’età di incidenza,per alcuni autori ci sono due picchi:uno in età giovanile ed<br />
scaricato da www.sunhope.it
uno in età più avanzata;invece dai risultati dei dati raccolti nei registri tumori italiani riscontriamo un<br />
picco tra i 50 e i 70 anni; la curva comincia a salire dai 30-35 anni in su. Ci sono anche cancri più<br />
giovanili,e il tal caso esiste l’ereditarietà. Nel 10% dei casi infatti esiste una predisposizione<br />
genetica ereditaria,e quando si trasmette di generazione in generazione,c’è sempre una maggiore<br />
precocità. Questi sono i dati dell’Istituto Superiore di Sanità che dimostrano che sia tra i 45 e i 64<br />
anni e sia dopo i 65 anni sta sempre in testa la mammella. Per quanto riguarda la mortalità e<br />
l’incidenza,vedete,in totale, in una vita da 0 a 84 anni c’è 1 possibilità su 9 di prendere un cancro<br />
alla mammella per tutte le donne,quindi si può comprendere l’interesse per questo tipo di cancro.<br />
Più aumenta l’età,più aumenta anche la mortalità.<br />
Questo è un grafico per le regioni d’Italia. In Campania per esempio si registrano circa 3000 casi<br />
all’anno. Un tasso grezzo risulta tra i più bassi,cioè 99 su 100000,sarà vero?perchè già vi ho<br />
spiegato che diversi ospedali non inviano i dati e non hanno nemmeno il registro tumori,per cui ci<br />
dobbiamo fidare dei dati parziali; mentre abbiamo regioni come il Piemonte dove questo tasso è<br />
182/100000,quindi molto molto elevato.<br />
Vi risparmio tutta la storia naturale del cancro della mammella perché in effetti già abbiamo fatto<br />
una parte generale,ma in effetti sappiamo che ci sono tutta una serie di cose che noi già abbiamo<br />
visto,dall’attività telomerasica,la ciclina ,le caderine e cosi via,quello su cui mi soffermo sono le<br />
forme ereditarie che rappresentano il 5-10% di tutti i cancri della mammella e sono legate<br />
soprattutto a mutazioni dei geni BRCA-1 e BRCA-2,come mi è successo nel caso di una<br />
studentessa,infatti anche la sorella aveva una lesione. Lei fu sottoposta ad una mastopatia<br />
bilaterale della mammella e il caso fu risolto.<br />
I tumori epiteliali maligni della mammella.<br />
Questa è una sintesi,perché ci sono una marea di forme,ogni anno escono 7, 8 forme<br />
nuove,perché c’è un interesse pazzesco su questo tumore della mammella.. I carcinomi in<br />
situ,allora abbiamo già visto il lobulare,il duttale,il papillare, ovviamente il duttale fa la parte del<br />
leone perché è il 5% di tutti i tumori maligni,il lobulare il 2%.il papillifero è molto raro perché è<br />
meno dell’1%. Per quanto riguarda i carcinomi invasivi,il carcinoma duttale rappresenta il 70-72%<br />
dei casi di tumori maligni. Vi ricordo che qua c’è una sigla: NOS che significa “not otherwise<br />
specified”,cioè lo chiamano duttale perché ha delle precise caratteristiche però può assumere<br />
aspetti molto vari. Poi abbiamo un carcinoma lobulare che riguarda un 12%dei casi,il carcinoma<br />
tubulare il 3%, il carcinoma mucoide, e il carcinoma midollare l’1%. Si chiama midollare un<br />
cancro,a prescindere da quello della tiroide che rappresenta un caso particolare perché è un<br />
carcinoma neuroendocrino, ma quando diciamo midollare non intendiamo un carcinoma<br />
neuroendocrino,ma midollare vuol dire povero di stroma,che assume consistenza midollare,cioè<br />
quasi gelatinosa,molle. Poi abbiamo altre varietà di cui parliamo proprio per cenno, e poi abbiamo<br />
scaricato da www.sunhope.it
carcinomi con particolari manifestazioni cliniche,tra cui la famosa malattia del Paget del capezzolo<br />
e il carcinoma infiammatorio,che è un carcinoma veramente terribile che simula una<br />
mastite,perché la mammella si ingrossa enormemente e ha una consistente componente<br />
infiammatoria,ma tende a metastatizzare ed è forse la forma più grave di cancro,si chiama<br />
infiammatorio perché da un quadro macroscopico di una mammella con aree eritematose e una<br />
infiammazione estesa a tutta la mammella.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> Prof. Rossiello 25/11/2010<br />
E’ uscita adesso una classificazione molecolare del cancro della mammella; ve ne do notizia, ma<br />
personalmente credo poco a queste cose perché sono tutti studi fatti a posteriori, cioè si piglia una<br />
casistica, si va nell’archivio di anatomia patologica e si vanno a studiare questi casi. Ovviamente<br />
che succede? Se io voglio dimostrare qualcosa, anche se è difficile dirlo, io lo dimostro perché,<br />
magari, anche casi che non corrispondono non li prendo in considerazione pensando che non sia<br />
stato bioptizzato bene ecc. … quindi alla fine riesco sempre a dimostrare quello che volevo<br />
dimostrare; lascia perciò il tempo che trova. Un mio carissimo amico, toscano, ha portato ad un<br />
convegno a Salerno altri valori su questa cosa, ma mi sono accorto che lui stesso non la segue.<br />
Questa classificazione si basa su alcuni geni, sul criterio del microarray. Poiché il cancro della<br />
mammella ha una certa eterogeneità prognostica e così via … e noi ci avviciniamo ad una<br />
valutazione prognostica con tutta una serie di parametri, con l’istologia e con tutte le cose di cui<br />
poi parleremo.. si è voluto fare qualcosa in più col microarray e con l’identificazione di questi<br />
geni .. geni legati alla capacità cinetica della cellula, geni legati alla capacità invasiva, geni legati ai<br />
recettori per gli estrogeni (ne nomina altri ma non si capisce)e tutta una serie di geni arrivando<br />
addirittura a 60-70 geni. Ora, voi sapete che ogni diagnosi di questa è una diagnosi molto<br />
impegnativa e io sono sempre un po’ restio alle classificazioni a posteriori. È come fare le previsioni<br />
del tempo il giorno dopo per il giorno prima e infatti tutti questi studi che sono stati fatti hanno<br />
sempre rivelato qualche falla.<br />
Quali sono i fattori di rischio per il cancro della mammella? Su questo mi soffermo poco perchè li<br />
trovate su tutti i testi e sono ormai codificati…1) i fattori geografici: il cancro della mammella ha<br />
una maggiore incidenza nei paesi avanzati;2) gravidanza e fattori sessuali: è un fattore di rischio il<br />
menarca precoce, una prima gravidanza dopo i (non si capisce bene se 25 o 35 anni).. sono a<br />
maggior rischio le nullipare e questi sono tutti casi che aumentano il rischio, ma i dati non è che<br />
siano tutti concordi, nel senso che non sono quantitativi; 3) abitudini alimentari .. non vi dico<br />
quanti studi sono stati fatti su queste abitudini alimentari. Da uno studio fatto in America risulta<br />
che il 70-80% di quello che mangiamo, l’altro 20% se lo sono scordati, è cancerogeno… perciò è<br />
preferibile morire di fame, però si ha la soddisfazione di scrivere sull’epitaffio “ non ebbe mai il<br />
cancro”; sono andati ad analizzare perfino il tipo di cottura.. comunque sembrerebbero implicate<br />
di più le carni rosse e anche il metodo di cottura (il prof dice qualcosa ma chi aveva il registratore a<br />
fianco teneva l’arteteca e non m’a fatt capì nient!... sembrerebbe che il prof dica qualcosa sui<br />
fattori di rischio dicendo che ce ne sono molteplici) ma alla fine … tra i fattori di rischio, una cosa<br />
che mi sorprende molto, non c’è il fumo. Il fumo è stato fatto entrare dovunque come fattore di<br />
rischio .. certamente il fumo fa male, è stato però utilizzato troppo spesso come capro espiatorio..<br />
l’unico nesso di casualità diretta è con fattori pressori, con il cuore e con il cancro squamoso del<br />
polmone. 4) terapie ormonali in menopausa che vanno sempre giustificate perché si ritiene che<br />
queste terapie ormonali ne favoriscano l’insorgenza. 5) fattori familiari : tra i fattori familiari ci sono<br />
delle famiglie in cui non sempre riusciamo a dimostrare l’esistenza di geni specifici, ma in cui<br />
comunque è più elevata l’incidenza di questo cancro; così come invece ci sono dei casi<br />
documentati, come vi ho detto prima, con BRCA1 e BRCA2 per cui si può parlare di ereditarietà<br />
perché sono geni molto forti. 6) Alcol … e poi vedete l’attività fisica (la mette tra i fattori<br />
scaricato da www.sunhope.it
proteggenti.. lo vedremo dopo). Vedete, quindi, come non ci sia una cosa che non è stata calcolata.<br />
Se voi domani mettete su Pubmed “breast cancer” vedrete che non c’è stata un’abitudine<br />
dell’uomo, anche degli indigeni della Papuasia, che non sia stata analizzata e relazionata al cancro<br />
… per esempio, fare attività fisica riduce il rischio di cancro. Questi però sono studi molto delicati,<br />
su cui ho molti dubbi perché anche tra gli sportivi c’è chi aveva o non aveva ereditarietà per il<br />
cancro e altri fattori di rischio. 7) metodi contraccettivi: ho messo il punto interrogativo perché non<br />
è che se ne sappia molto, ma comunque sia, anche se fosse, si tratterebbe di una elevazione di<br />
rischio molto bassa.<br />
E veniamo adesso al carcinoma della mammella per eccellenza, vale a dire il CARCINOMA DUTTALE<br />
INVASIVO. Il carcinoma duttale invasivo, non so se qualcuno di voi l’ha visto in istituto, tende ad<br />
avere non un colore bianco, ma un po’ grigiastro e tende ad avere un atteggiamento un po’ di<br />
retrazione rispetto al grasso circostante; però queste sono impressioni . Qui vedete la cute e<br />
vedete questo cancro che infiltra la cute (incide molto sulla stadiazione) . Mammograficamente il<br />
fatto non è semplice. Ci vuole molta esperienza nel vedere queste mammografie perché in genere<br />
il cancro non è che da un’area di opacità molto netta, ma un’opacità media oppure possiamo<br />
vedere delle calcificazioni molto irregolari che naturalmente sono molto sospette. Possiamo avere<br />
un quadro di malattia fibrocistica che può oscurare un quadro di cancro .. vedete qui ci sono delle<br />
aree di fibrosi … Ci vuole comunque una certa esperienza. Volendo fare una panoramica di un<br />
cancro classico duttale, vedete che si presenta come una masserella, in questo caso è piccola, ma<br />
può essere comunque molto grande, con i bordi un po’ sellati (sembra che dica così … boh!) o forse<br />
dice sollevati.. e questa caratteristica è tipica dell’infiltrazione. Questo cancro duttale chiamato<br />
NOS oppure in italiano NAS (non altrimenti specificabile) vuol dire che è un cancro che può<br />
assumere delle forme molto diverse (tubulari, solide, trabecolari.. ) . Qua vediamo le aree di<br />
carcinoma intraduttale delle aree di coleocarcinoma(?? Ragà nn si capisce) con aree di necrosi e<br />
paradossalmente la presenza di queste aree di carcinoma intraduttale indica spesso la presenza di<br />
interessamento contro laterale.. quando vediamo queste aree quindi dobbiamo andare sempre ad<br />
analizzare la mammella contro laterale… in alcuni casì quindi sarebbe preferibile un cancro invasivo<br />
perché un cancro invasivo è molto spesso un nodo unico. Spesso possiamo trovare delle<br />
calcificazioni, molto irregolari (grandi, medie, piccole), che hanno un significato prognostico( nn si<br />
capisce niente). Vedete che qui è mantenuta, in qualche modo, una differenziazione tubulare..<br />
altre volte invece c’è la tendenza a formare delle strutture più solide (sempre l’arteteca di chi ha<br />
registrato) … quando c’è un solo lume ghiandolare (forse vuole dire che le strutture più solide<br />
hanno un solo lume … boh!). Sono stati fatti molti sforzi dagli studiosi per capire da un punto di<br />
vista prognostico quali sono i carcinomi duttali che andranno meglio e quali sono quelli che<br />
andranno peggio. Oltre al criterio malpighiano(ragà veramente è na tragedia.. nn si capisce niente)<br />
usato correntemente nella nostra diagnostica .. c’è il criterio di Bloom e Richardson che poi è stato<br />
anche rivisitato, modificato .. comunque questo è il modello base. Vengono modificati perché c’è<br />
sempre qualcuno che non è mai contento… e queste modifiche prendono il nome da una città<br />
Nottingham tant’è vero che si potrebbe parlare di criteri di Bloom – Richardson – Nottingham.<br />
Questa classificazione si basa su 3 parametri: 1) capacità di formare tubuli, 2)atipie nucleari,<br />
3)nuclei in mitosi-figure mitotiche. A ciascuno di questi parametri diamo un punteggio da 1 a 3;<br />
quindi il punteggio oscilla da 3 a 9. Quando il punteggio totale è basso, la prognosi è più<br />
scaricato da www.sunhope.it
favorevole, quando è alto la prognosi è peggiore. Capacità di formare tubuli: metteremo 1 quando<br />
ci sono tubuli, metteremo 3 quando i tubuli non ci sono. Atipie nucleari: se le atipie sono blande<br />
metteremo 1 se sono marcate metteremo 3. Figure mitotiche: più ne sono più ci avviciniamo al 3.<br />
Abbiamo alla fine tre livelli di grading .. 1(primo) quando ….(gran boato e nun si capisce niente…<br />
forse si riferisce alla somma dei paramentri di prima) 2 (secondo) tra 6 e 7 .. 3(terzo)..<br />
Quindi quando voi leggerete sulla diagnosi secondo i criteri di Bloom – Richardson – Nottingham<br />
gradind 1 vuole dire che la prognosi è buona. Va bene? Vi faccio alcuni esempi: questo è quello di<br />
tipo 1, vedete ancora i tubuli .. grado 2 non vedete più i tubuli .. grado 3 vedete anche le figure<br />
mitotiche, magari trovate pure qualche tubulo… però le atipie sono comunque moltissime.<br />
(vengono poi una serie di parole che non si capiscono) un 30-40% dei cancri della mammella ……..<br />
sensibile alle nostre terapie … voi già lo avete studiato.. ci sono diversi criteri … un farmaco<br />
utilizzato è il tamoxifen ..<br />
Il ki67 ha anche un valore prognostico; vedete tutte queste palline marroni.. indicano che i nuclei<br />
di queste cellule sono in fase proliferativa, mentre le altre stanno in fase G0, cioè una fase di<br />
quiescenza.<br />
La famiglia erb già la conoscete.. nella mammella chiamato meglio c-erb-b2. Cosa dire di questo<br />
erb-b2? Il 25% dei cancri della mammella è erb-b2 positivo. Questa è stata una grande scoperta<br />
perché questi cancri erb-b2 erano quelli meno sensibili alle terapie tradizionali . In Italia, dei 38000<br />
casi circa di cancro della mammella, 9000 casi sono erb-b2 positivi . Qual è l’approccio? Oggi<br />
paradossalmente questi casi vanno meglio degli altri perché si avvalgono della terapia biologica e<br />
possiamo avere sopravvivenze libere dalla malattia, a 5 anni, superiori al 70%. Il rovescio della<br />
medaglia è che queste terapie hanno però un costo molto elevato.. costa 50000 euro solo avere<br />
questi farmaci .. che sono: anticorpi monoclonali che si legano ai recettori per il fattore di crescita<br />
(Trastuzumab, Cetuximab e così via..) .. in altre parole questi recettori è come se fossero<br />
mascherati rispetto al ligando specifico. Sono in fase di sperimentazione altri farmaci che sono gli<br />
inibitori delle tirosinchinasi… voi sapete che l’attività tirosinchinasica è presente nella parte<br />
intracitoplasmatica di questi recettori. Ai fini terapeutici si è scoperto che questa terapia biologica<br />
unita alla terapia tradizionale da i risultati migliori perché questi farmaci biologici potenziano<br />
l’attività dei chemioterapici. La stessa cosa è stata vita, ad esempio, con i linfomi: nei linfomi a<br />
cellule T abbiamo anticorpi contro il CD20 delle cellule B che, uniti alla terapia tradizionale,<br />
garantiscono risultati che una volta erano impensabili. Come<br />
facciamo a vedere la positività dell’erb-b2? Attraverso l’immunoistochimica. Abbiamo delle scale<br />
con 0,1,2,3. 0 vuol dire che non ci sta proprio… vediamo un attimo il 3 la cellula sta qui e<br />
tutt’intorno alla cellula c’è un notevole accumulo di positività che corrisponde ad una notevole<br />
amplificazione genica, perché quando sono amplificati i geni sono amplificati di numero anche i<br />
recettori e diciamo che le cellule sono più disponibili a questi fattori di crescita che la stimolano a<br />
moltiplicarsi (questa, quindi, è l’immagine immunoistochimica di un’amplificazione). Nello stadio 2<br />
abbiamo comunque la rappresentazione di questi recettori.. qua pure c’è l’immagine ad occhiello<br />
di questi recettori intorno alle cellule, ma non tutti ce l’hanno come lo stadio 3 e in questi casi qui<br />
scaricato da www.sunhope.it
è opportuno ricorrere ad altre tecniche molecolari .. ad esempio si una molto il cosiddetto FISH<br />
(Fluorescent In Situ Hybridization) che sono tecniche di ibridazione in situ. E’ una tecnica molto<br />
semplice: prima dobbiamo utilizzare un trattamento che serve a spezzare la doppia elica di DNA e<br />
quindi le due eliche si allontanano. L’allontanamento ci serve perché dobbiamo legare qualcosa alla<br />
sequenza del gene erb-b2. La “sonda” che si lega alla sequenza erb-b2 deve avere una sequenza<br />
nucleotidica omologa. A questo punto abbiamo questo marcatore genetico, questa sequenza<br />
genetica che si va a legare viene marcata con un tracciante fluorescente …. Però, perché c’è sempre<br />
un però .. mettiamo il caso che noi abbiamo una cellula tetraploide, quindi con un contenuto<br />
genetico superiore a quello di una cellula normale, noi troveremo che questo gene è espresso<br />
normalmente 2 volte perché espresso sui 2 alleli.. in questo caso sarà espresso 4 volte. Quindi,<br />
quest’immagine di amplificazione, non è in realtà un’amplificazione.. ma è dovuta solo all’aumento<br />
del contenuto del nucleo della cellula. Come si fa allora? Si una un controllo interno. Si usano 2<br />
traccianti fluorescinati e per uno si usa sempre una sequenza conservata, cioè una sequenza<br />
omologa a quella di un DNA che per qualunque malattia non si modifica mai. In questa maniera<br />
possiamo vedere l’amplificazione non solo del gene erb-b2, ma anche del gene normale sempre<br />
conservato … se i due traccianti sono 1 verde e 1 rosso, la normalità dovrebbe essere 2 rossi e 2<br />
verdi… se i rossi (tracciante per erb-b2) eccedono rispetto ai verdi allora possiamo parlare<br />
effettivamente di un’amplificazione genica. Questa è quindi una tecnica che serve a confermare i<br />
casi dubbi all’immunoistochimica per il recettore. Il CARCINOMA LOBULARE si<br />
presenta al secondo posto come frequenza..il primo è il carcinoma duttale.. (non riesco a capire<br />
bene ma mi sembra che il prof dica anche che si presenta in età un po’ più avanzata rispetto al<br />
carcinoma duttale). Rappresenta il 10-12% dei cancri della mammella. Non si presenta tanto come<br />
una massa unica, ma si presenta come un’entità molto eterogenea e mammograficamente è più<br />
difficile da vedere (non si capisce un c……. forse dice che simula una mastite). Mentre nel<br />
carcinoma duttale noi vediamo una massa ben definita … nel carcinoma lobulare vediamo un<br />
aspetto macroscopico più sfilacciato, sfumato, fatto da tante piccole aree con una conformazione<br />
molto irregolare. La caratteristica di questo carcinoma è il pattern di distribuzione a fila indiana<br />
(delle cellule).. vedete? (lo fa vedere nell’immagine) . Questo cancro, rispetto a quello duttale forse<br />
è meno aggressivo, ma tende a ….. (grrrrrr .. che nervi!!! Sembra che dica “fare brutti scherzi”).<br />
Ecco, qua vediamo un particolare .. vediamo che queste cellule, oltre ad avere la distribuzione a fila<br />
indiana, hanno un alone chiaro peri-nucleare. Ci sono dei casi in cui è molto difficile capire se è<br />
duttale o lobulare. Abbiamo un marcatore molto utile che noi utilizziamo ed è la caderina E che è<br />
espressa dal carcinoma duttale ma non da quello lobulare. Qui vediamo (sembra che dica “i nuclei<br />
normali”) che esprimono la caderina E e qui le cellule del carcinoma lobulare che non la<br />
esprimono. Se fosse stato un carcinoma duttale avremmo avuto forte positività di membrana<br />
perché questa molecola di adesione è presente nel carcinoma duttale.<br />
Adesso Rossiello fa vedere l’impegnativa in cinese di quella signora che veniva da Kanton per un<br />
caso di cancro alla mammella molto complesso che era arrivato al suo centro. Poi riferendosi al<br />
vetrino della signora: qui vedete che si tratta di un caso di carcinoma lobulare con le cellule mio<br />
epiteliali sparpagliate perché quando c’è un’attività tumorale, la massa tumorale spinge queste<br />
cellule, le comprime e le confina in vari punti. Quindi alla fine, si capì che la signora aveva un<br />
carcinola lobare invasivo .<br />
scaricato da www.sunhope.it
Poi abbiamo il RADIAL SCAR CARCINOMA . Noi abbiamo già parlato del radial scar come una<br />
lesione benigna, ma adesso vediamo i radial scar che da un punto di vista mammografico non si<br />
distingue bene se benigno o maligno (forse per questo si aggiunge carcinoma). Vedete<br />
quest’immagine ad astro, con un punto centrale che corrisponde a quell’area di cicatrizzazione e di<br />
fibrosi .. con poi tutti questi rami. Qui vedete un altro radial scar carcinoma con quest’area di<br />
fibrosi al centro e tutt’intorno queste aree bianche.<br />
Il CARCINOMA TUBULARE statisticamente incide poco; mi sembra che sia intorno all’1-2% dei<br />
cancri della mammella. E’, però, un carcinoma particolare perché se parliamo di un cancro<br />
piccolo(1-2mm), l’incidenza di questo cancro aumenta superando anche il 30-40% (un cancro di 1-<br />
2 mm nel 30 % dei casi sarà un carcinoma tubulare, mentre un cancro di 5mm solo nel 2% sarà<br />
tubulare). Questo significa che è una forma molto frequente nei minimal breast cancer (quindi nei<br />
cancri piccoli). Tutto questo ha suffragato l’ipotesi che il cancro della mammella parte come<br />
tubulare, poi cresce, si differenzia ancora di più e diventa qualche altra cosa. Il rischio di meta<br />
statizzazione di questo cancro è bassissimo, cioè inferiore al 6%.<br />
Il CARCINOMA MUCOIDE è quello che vedete qui, con queste aree di muco. Presenta sempre le<br />
stesse caratteristiche con aree chiare in cui sono immersi questi centroni neoplastici. Talvolta può<br />
assumere anche l’aspetto di cellule ad anello con castone .. mi pare che questo già ve l’ho<br />
spiegato .. ma comunque cos’è che succede? Queste cellule hanno perso la capacità di secernere il<br />
proprio prodotto e questo prodotto si accumula all’interno della cellula e schiaccia il nucleo alla<br />
periferia. Questo nucleo schiacciato da la forma del castone. Questo è un cancro brutto .. anche<br />
perché oltre alle altre caratteristiche del tessuto normale ha perso pure la capacità di secernere.<br />
Il CARCINOMA MIDOLLARE, già ne abbiamo parlato ha alcune cellule atipiche e ha poche<br />
fibre(sembra che dica così).<br />
Il CARCINOMA PAPILLIFERO ne abbiamo già parlato così come dell’ adenoma .. vedete che è un<br />
carcinoma che inizia sempre dai grandi dotti, però qui vedete che è infiltrante e c’è l’invasività<br />
verso l’esterno .. quindi possiamo dire con certezza che è un cancro.<br />
Il CARCINOMA METAPLASTICO assume le forme più strane e si chiama metaplastico perché può<br />
fare di tutto. Alcune volte assume un’espressione a cellule fusate che simula un sarcoma però<br />
capiamo che non è un sarcoma perché ci sono cellule positive per i marcatori epiteliali. Altre volte<br />
assume un aspetto a cellule giganti e addirittura a volte può formare tessuto osseo.. qui infatti<br />
vedete proprio osso (sembra che poi dica “osteoblast like”). Nelle cellule giganti i nuclei sono molto<br />
addensati .<br />
Qui vedete quella che si chiama MALATTIA DEL PAGET DELLA MAMMELLA ... (ci sono poi una serie<br />
di parole che non si capiscono) .. che coinvolge il capezzolo ed in genere tutta l’areola mammaria.<br />
Ci vuole un occhio esperto per distinguere una banale dermatite da contatto da una patologia di<br />
questo tipo. Il quadro anatomopatologico è: qui vediamo un epitelio pavimentoso stratificato<br />
dell’areola mammaria, infiltrato da cellule chiare che si intromettono proprio . Visto così uno<br />
potrebbe pensare pure ad un melanoma, perché il melanoma ha un po’ questa tendenza. .. e le<br />
cellule melanocitarie sono bianche . In quest’altra immagine vedete queste cellule molto<br />
scaricato da www.sunhope.it
pleomorfe, molto bislacche che si insinuano tra le cellule epiteliali. Noi, però, non ci facciamo<br />
ingannare e non lo confondiamo col melanoma. Ce ne accorgiamo attraverso la citocheratina 7 che<br />
viene espressa dalle cellule ghiandolari … quindi ci accorgiamo che sono cellule ghiandolari. Cosa ci<br />
fanno queste cellule tipiche ghiandolari nell’ambito dell’areola mammaria? Dopo molti anni si è<br />
capito questo fatto strano … probabilmente c’entrano anche le cellule staminali.. comunque noi<br />
troviamo, in alcuni carcinomi, queste cellule che sono le cellule del Pachet. Se andiamo a vedere<br />
sotto l’areola, in una percentuale del 95%, troviamo carcinoma in situ o carcinoma invasivo. Chi sa<br />
se negli altri casi in cui troviamo queste cellule ma non vediamo cancro se si tratta di cancri<br />
talmente piccoli che non riusciamo a vedere. Queste cellule di Paget vengono dal basso, dal dotto,<br />
e acquisiscono le capacità migratorie grazie al fenomeno della trans differenziazione di cui già<br />
abbiamo parlato. La migrazione è stimolata da fattori chemio tattici che sono ancora in fase di<br />
studio. Così avviene nel 95% dei casi, forse l’altro 5% sta nel nostro difetto nel trovare un cancro<br />
che sta sotto. Comunque, quando vediamo quel tipo di lesione dobbiamo fare un citologico o<br />
comunque un vetrino anche con la scarificazione della lesione.<br />
Il CARCINOMA INFIAMMATORIO per definizione è, come minimo, uno stadio 4. La mammella si<br />
presenta molto ingrandita, assume un aspetto turgido. All’esame istologico vediamo cellule<br />
atipiche sparse insieme all’infiltrato infiammatorio e vediamo, soprattutto, il coinvolgimento di<br />
tutta la mammella.<br />
Il prof fa vedere un quadro di Rembrandt – Betsabea nel bagno – e comincia a raccontare la storia<br />
di Betsabea (Uria suo marito, il re Davide che era innamorato di sua moglie ecc ecc.). Faccio vedere<br />
questo quadro perché, questa modella che si chiamava Sto…… e mi sembra fosse olandese, aveva<br />
un cancro della mammella. Questo Rembrandt, forse senza accorgersene, risprese anche il cancro<br />
della mammella. Addirittura possiamo fare pure la stadi azione perché vediamo che è impegnata<br />
pure l’ascella<br />
La STADIAZIONE del tumore alla mammella fa un po’ eccezione perché varia un po’ anche la<br />
sopravvivenza. Se la grandezza è inferiore a 2 cm la sopravvivenza sta nella prima curva (il prof fa<br />
vedere una tabella); quindi molto più alta rispetto alle altre. Vedete che c’è una notevole<br />
dirrerenza tra 2 cm e 2-5 cm. Meglio ancora se inferiore ad 1 cm. Questo è importante perché ha<br />
risvolti anche sul comportamento dei medici .. perciò lo screening per il cancro della mammella.<br />
Altra cose importante sono i linfonodi. Se ha linfonodi negativi, in genere, la curva è così…<br />
ovviamente noi dobbiamo pensare che se la grandezza è piccola e i linfonodi sono negativi,<br />
probabilmente la sopravvivenza starà qui.. perché si sommano due fattori positivi. Ci fermiamo per<br />
la pausa ….<br />
Quell’immagine di prima mi ha ricordato una cosa.. Fui invitato ad un convegno … (e inizia a<br />
raccontare una storia in cui parla di un suo amico senologo con una fiorente attività privata che,<br />
quando vide il quadro di Rembrandt, esclamò “lo conosco, lo conosco” e il prof gli rispose<br />
“neanche quella ti sei fatto sfuggire”).<br />
La stadiazione che si segue, apparentemente sembrerebbe complessa ma non è complessa. T sta<br />
sempre per tumore e i carcinomi in situ hanno la sigla is e abbiamo:<br />
scaricato da www.sunhope.it
Tis[DCIS] :Carcinoma duttale in situ<br />
Tis[LCIS] :Carcinoma lobulare in situ<br />
Tis[Paget] :M. di Paget senza tumore (perché se c’è tumore, nella malattia del Paget, la<br />
stadiazione segue quella del tumore principale).<br />
Poi abbiamo : nell’ambito dei T1<br />
T1 mic : microinvasione < 0,1 cm [m] (quando il carcinoma è mini-invasivo )<br />
T1a : 0,1 cm < T < 0,5 cm<br />
T1b : 0,5 cm< T > 1 cm<br />
T1c : 1 cm < T > 2 cm<br />
Però il T1 è il più favorevole tra i tumori invasivi.<br />
Poi abbiamo T2 che è tra 2 e 5 cm. Il T3 quando è maggiore di 5 cm. Il T4 quando, a prescindere<br />
dalle dimensioni, si estendono alla parete toracica o da edemi, ulcerazioni, satellitosi e in questo<br />
caso la pelle della mammella assume un aspetto a buccia d’arancia. E’ T4 anche se, a prescindere<br />
dalla forma, si stratta di carcinoma infiammatorio.<br />
I linfonodi: per i linfonodi della mammella abbiamo 3 livelli di linfonodi ascellari. In linea di<br />
massima il livello 1 è il livello più basso, il livello 2 è l’intermedio, il livello 3 è quello più difficile a<br />
dire( e poi nn si capisce). Oltre a questi abbiamo i linfonodi della linea mammaria interna, spesso<br />
trascurati perché si pensa solo ai linfonodi ascellari. Voi sapete che in chirurgia si usa la tecnica del<br />
linfonodo sentinella, di cui mi sembra di aver già parlato. Ricapitoliamo un po’ questa tecnica:<br />
partiamo dal presupposto che innanzitutto questo linfonodo sia identificabile, cosa che fa il medico<br />
nucleare iniettando una sostanza radioattiva a breve emivita nella zona adiacente al cancro; dopo<br />
va a visualizzare qual è il primo linfonodo che capta. Essendo quello il linfonodo di confine,<br />
appunto il linfonodo sentinella, dobbiamo presumere che non ci sia il cosiddetto salto della<br />
metastasi e che ci sia una sequenzialità di eventi, cioè il primo linfonodo, poi il secondo, poi il terzo<br />
e così via. Se il primo linfonodo è indenne (tutto questo, naturalmente, si fa a livello di diagnosi<br />
intraoperatoria), quindi se il linfonodo sentinella è indenne (all’analisi anatomopatologica .. questo<br />
ce l’ho aggiunto io), allora il chirurgo non fa una linfoadenectomia. Molto spesso si fa un intervento<br />
conservativo della mammella, per esempio si fa una quadrantectomia o addirittura una<br />
tumorectomia e poi, se non si fa il linfonodo sentinella, si tolgono i linfonodi ascellari e questo<br />
porta a tutta una serie di conseguenze tra cui elefantiasi, infiammazione… quindi il linfonodo<br />
sentinella risponde anche ad una serie di esigenze come, ad esempio, la qualità di vita. Tutto<br />
questo però deve presumere che non ci siano le skip metastasis ovvero le metastasi a salto…<br />
fenomeno che può avvenire, ma in percentuali così basse da essere considerato trascurabile.<br />
Questo è lo studio di Veronesi di qualche anno fa che ha preso due popolazioni, una con la<br />
dissezione dei linfonodi ascellari e l’altra con il linfonodo sentinella. Ha dimostrato che la prognosi<br />
in tutte e due le popolazioni non è statisticamente diversa, anzi c’è una leggera superiorità nella<br />
sopravvivenza nel gruppo che era stato trattato con la tecnica del linfonodo sentinella. Questa<br />
tecnica vale, naturalmente, per lesioni di certe dimensioni; ma quando abbiamo già evidenza di<br />
metastasi linfoghiandolari bisogna fare la linfoadenectomia. In realtà la linfoadenectomia ha un<br />
valore un po’ così, perché se i linfonodi sono stati interessati, chi mi dice che non siano stati<br />
interessati anche altri linfonodi? Paradossalmente quindi la linfoadenectomia aveva soltanto uno<br />
scaricato da www.sunhope.it
scopo diagnostico, cioè per fare una stadiazione corretta e così via. Il linfonodo sentinella non<br />
sempre è identificabile. A volte possiamo avere anche più di un linfonodo sentinella, quindi<br />
dobbiamo tagliare tutti e due o tutti e tre. C’è anche da dire che il tasso di identificabilità del<br />
linfonodo sentinella è operatore dipendente, quindi meglio andare in centri che hanno una certa<br />
esperienza a riguardo. Ad un certo punto cosa si vide: si vide che l’estemporanea, quella per il<br />
linfonodo sentinella, aveva una percentuale di falsi negativi. Questo perché l’estemporanea,<br />
essendo un esame rapido, si poteva presentare con metastasi che sfuggivano alla visione.. anche<br />
perché noi vediamo una sezione del linfonodo, non il linfonodo in toto… e questo ha scatenato<br />
tutta una serie di polemiche e di problemi. Fu allora che il TNM misa una categoria nuova che ci<br />
creò non poche confusioni: l’ N0 classico si tramuto in una serie di sottocategorie l’N0i- che è il<br />
vero N0 e l’N0i+ che all’immunoistochimica dimostrava positività alla citocheratina. Ci furono<br />
addirittura alcuni che andarono a fare studi con la PCR. Tutto questo però creava confusione sul da<br />
farsi.. cioè qual era il giusto approccio poi per questi pazienti? Innanzitutto si vide che con dati<br />
statistici che, quando noi troviamo linfonodi ascellari o linfonodi sentinella positivi ma con<br />
metastasi inferiore a 0,2mm, la possibilità che ci siano metastasi negli altri linfonodi è bassissima.<br />
C’è più del 90% di probabilità di non trovare altre metastasi…. Soprattutto ancora se il cancro è<br />
piccolo, cioè ci troviamo di fronte ad un T1. Il rischio di trovare altre metastasi, in questo caso, è<br />
inferiore al 5%. Il TNM che uscì dopo 2 anni e che si segue attualmente, stabilì che c’è una<br />
differenza tra meta statizzazione ed embolizzazione; cioè che piccoli aggregati di cellule che<br />
passano nei linfonodi, si hanno in tutti i casi di cancro della mammella. Per cui tutti gli studi che<br />
fecero di micro array ecc sui linfonodi .. trovando una cellula atipica su un miliardo, non servivano<br />
proprio a niente.. perché una cellula atipica la trovi sempre. Il TNM stabilì che quando sono<br />
inferiori a 0,2 mm non vanno considerate metastasi.. e se non ha segni di attecchimento della<br />
metastasi. Il segno di attecchimento della mestastasi è una reazione desmospastica, una reazione<br />
fibrosa tutt’intorno. Non basta quindi il seme, ci vuole anche il terreno. Se abbiamo il seme che<br />
passa, questo non ha significato. Qui vedete la metastasi nel linfonodo e vedete che c’è una<br />
reazione fibrotica e anche infiammatoria e quindi possiamo dire che è una metastasi. Concludiamo<br />
allora con questa cosa: pN1mi (microscopico) vuol dire che è inferiore a 0,2 mm ... invece il pN1 è<br />
quando troviamo massimo 3 stazioni linfoghiandolari oppure quando troviamo coinvolto 1<br />
linfonodo della linea mammaria interna. Il coinvolgimento della linea mammaria interna assume<br />
un aspetto prognostico più sfavorevole., perché più distante. pN1c quando sono coinvolte<br />
mammaria interna e ascellari. pN2 da + di 4 a 9 linfonodi coinvolti. pN3 quando abbiamo più di 9<br />
linfonodi coinvolti o quando sono coinvolti i linfonodi sopraclaveari; il coinvolgimento dei linfonodi<br />
sopraclaveari è un evento prognostico molto sfavorevole. Lunedì parleremo di quando è<br />
controindicato fare il linfonodo sentinella . Arrivederci …<br />
scaricato da www.sunhope.it
MAMMELLA<br />
LINFONODO SENTINELLA<br />
La tecnica del linfonodo sentinella risponde ad 1 esigenza, sentita dal popolo femminile, di una<br />
migliore qualità di vita, quindi quell’atteggiamento del chirurgo-ginecologo di 1volta che toglieva<br />
tutto (muscolo grande pettorale, piccolo pettorale, ascella,…).Ma quando e perché si fa?<br />
Non si può fare quando c’è 1precedente biopsia che creando un traumatismo della zona ha potuto e<br />
spesso si è verificato determinare delle distorsioni linfo-ghiandolari per cui non siamo più sicuri che<br />
c’è questa sequenzialità di linfonodi; non si può fare quando c’è una linfoadenopatia palpabile a<br />
livello ascellare, quando c’è anche una TAC di conferma dove abbiamo grandi linfonodi, perché<br />
sembra inutile ricercare linfonodi, tutt’al più questa linfoadenopatia palpabile andrebbe esaminata;<br />
non si può fare in rapporto alle dimensioni del nodulo primario ( anche se questo è 1 punto<br />
controverso), alcuni dicono che T1 come grandezza del tumore, cioè fino a 2cm, è il limite, un’altra<br />
scuola di pensiero considera come limite 3cm, ma la più accreditata è quella che considera come<br />
limite 2cm; non si può fare quando una persona ha avuto già una chemioterapia neoadiuvante; non<br />
si può fare quando il soggetto ha un carcinoma in situ perché è multicentrico, quindi ovemai ci fosse<br />
stato un focolaio di invasività, dove lo prendiamo questo linfonodo sentinella? Se tutta la mammella<br />
è coinvolta e probabilmente anche la mammella controlaterale,e non si deve fare perché se è in situ,<br />
per definizione, non dovrebbero esserci metastasi, se è 1falso negativo, cioè sembrava in situ, ma ha<br />
avuto delle metastasi, dove lo andiamo a fare per localizzarlo? E’ inutile; non si può fare in caso di<br />
allergie, perché bisogna inoculare sostanze oleose, tecnezio e così via.<br />
C’è un problema, inoltre, per il linfonodo sentinella, ma questa è una mia opinione personale:<br />
spesso, a parte i falsi negativi, che, però abbiamo visto sono relativi perché abbiamo visto che la<br />
micrometastasi o il piccolo embolo non incide sul coinvolgimento degli altri linfonodi, c’è il<br />
problema che se il cancro è piccolo e il linfonodo sentinella è negativo c’è un certo atteggiamento<br />
ottimistico e rinunciatario da parte della paziente, ma soprattutto del clinico che è convinto che tutto<br />
è andato bene; non è proprio così, o meglio lo è statisticamente, ma non in maniera assoluta e,<br />
quindi, c’è una sottovalutazione del problema, anche perché, anche se succede raramente, la<br />
paziente, dopo 8-10 anni, dall’intervento pregresso da cui tutto sembra a posto può manifestare una<br />
metastasi, evidentemente per la presenza di un focolaio metastatico che già c’era ma che si trovava<br />
in una situazione di dormiveglia; poi c’è un altro problema, e cioè che non ci sono solo i linfonodi,<br />
ma ci sono 2 situazioni spesso sottovalutate nel cancro della mammella, che gli anatomo-patologi<br />
conoscono bene: la prima è il midollo osseo, non raramente coinvolto come sede di metastasi<br />
insieme con l’osso, e la seconda è che tende a coinvolgere l’ipofisi ( pochi sanno questa cosa, che<br />
non sta scritta sui libri ) , emerge dalle casistiche autoptiche e si hanno anche dei sintomi endocrini.<br />
Ci sono, poi, delle voci contrarie, come gruppi internazionali molto quotati che, a differenza di<br />
Veronesi, però questi non hanno preso il sopravvento, per esempio l’American College dei<br />
chirurghi oncologi che dice che c’è uno svantaggio prognostico rispetto alla linfoadenectomia che<br />
oscilla tra l’1 e il 4%, in effetti queste incertezze risiedono anche nel fatto che questa metodologia<br />
non è stata codificata nei dettagli, ad esempio: c’è chi usa il colorante vitale, chi usa la scintigrafia,<br />
chi usa il contatore Geiger all’atto operatorio per visualizzare il linfonodo sentinella, chi va a vedere<br />
pure la linea mammaria interna, poi a che distanza dal prelievo si va a fare l’indagine strumentale<br />
per vedere, che tipo di reattivo si usa…non è stato codificato, per cui, quando diciamo linfonodo<br />
sentinella, in effetti corriamo il rischio di paragonare procedure e metodologie anche diverse, questo<br />
secondo i risultati dell’American College dei chirurghi oncologi, cioè che ogni chirurgo questo<br />
linfonodo sentinella lo vive in maniera “pirandelliana”.<br />
Nonostante questi problemi, c’è un trend favorevole verso questo linfonodo sentinella, la stessa<br />
paziente lo chiama, lo chiede per i problemi che vi ho detto prima: le sedi metastatiche della<br />
mammella possono essere midollo, fegato, polmone, ossa; se ci troviamo di fronte ad un T1 il<br />
follow-up a 5 anni è certamente molto favorevole, man mano che scendiamo la prognosi è molto<br />
scaricato da www.sunhope.it
sfavorevole. Il nostro problema è quello di fare un identikit del tumore, prendere le sue impronte<br />
digitali, vedere un po’ questo tumore che intenzioni ha, cercando di estrarre nell’inconscio dei<br />
tessuti tutte le capacità di T, sia per la scelta di una terapia, sia perché adesso si va verso una<br />
personalizzazione dell’approccio terapeutico, quindi basiamo questo identikit su parametri<br />
tradizionali e su parametri nuovi. Il problema principale che deve stabilire l’anatomo-patologo è<br />
capire con quale velocità viaggia quel cancro, perché sì, le dimensioni sono importanti, perché una<br />
lesione
Tailor Therapy: ha parecchi significati, dall’inglese significa “sartoriale”, un termine che oggi va<br />
scomparendo, ma in effetti è anche un acronimo perché significa Trial Assigning IndividuaLized<br />
Options for Treatment; questo raccomanda di identificare 1 trattamento personalizzato per ogni<br />
paziente che abbia un fondamento scientifico, ma anche un fondamento pratico da un punto di vista<br />
clinico, per una risposta adeguata all’entità dell’aggressione e al momento in cui si trova quella<br />
storia. Nella mammella l’anatomo-patologo interviene a più livelli: nella citologia aspirativa, le<br />
microbiopsie, tecnica in accrescimento, anche qui abbiamo una “Brest-Unit” che fra poco dovrebbe<br />
decollare proprio per l’anatomia patologica, i locali sono quelli sotto la clinica ostetrica, c’è stato un<br />
finanziamento europeo che ha cercato di identificare in varie parti dell’Europa dei centri<br />
specializzati, anche questo policlinico sarà sede di Brest Unit perché sono arrivate tutte le<br />
attrezzature tra cui un apparecchio chiamato MammuTOM che consente di fare una microbiopsia in<br />
stereotassi: voi date le coordinate su un apparecchio tridimensionale e l’ago colpisce proprio quella<br />
zona e ne viene fuori un piccolo frustolo di tessuto, oppure si può fare una microbiopsia ecoguidata,<br />
però non c’è dubbio che MammuTOM rappresenti un’innovazione, perché , dopo avergli dato le<br />
coordinate se la vede lui, in automatico. Citologia aspirativi versus Microbiopsia, perché l’una,<br />
perché l’altra? Lo vedremo. Poi interviene la fase post-operatoria, in cui bisogna definire tutta una<br />
serie di parametri, il grading e così via e poi la fase intra-operatoria perché al tavolo operatorio<br />
arrivano non solo casi dubbi, per cui si richiede l’intervento anatomo-patologo e la diagnosi, ma è<br />
richiesta anche la problematica del linfonodo sentinella, si chiedono i margini di escissione, perché<br />
se io devo fare un intervento conservativo si richiede l’integrità dei margini di escissione e allora mi<br />
serve anche a livello intraoperatorio questa informazione, per vedere se è stato rimosso tutto o c’è<br />
ancora qualche focolaio un po’ distante dal tumore primitivo, quindi è un intervento quello<br />
dell’anatomo patologo abbastanza complesso nel corso di questo intervento.<br />
L’ American Cancer Society, ma anche il gruppo europeo della UICC, Unione Internazionale<br />
Contro il Cancro, hanno stabilito degli obiettivi per i prossimi 10 anni: l’America dice riduzione di<br />
mortalità del cancro alla mammella del 20-35% e inizio screening mammografico all’età di 40 anni,<br />
ogni nazione in realtà ha un’età diversa in relazione alla diversa incidenza di questo cancro nell’età<br />
alle diverse latitudini, il gruppo europeo mira soprattutto a ridurre la mortalità , ridurre la differenza<br />
tra gli stati, tra Grecia, Germania, Francia, Italia ci sono delle differenze, ridurre queste differenze<br />
in modo che vi siano degli standard abbastanza omogenei, perché si è constatata una differente<br />
sopravvivenza a seconda degli stati, addirittura à 39 raccomandazioni!<br />
Quali tecniche quindi per una diagnostica sulla mammella?<br />
Se utilizziamo la Citologia aspirativi, FNAB , un ago piccolo e sottile che fa venir fuori le cellule<br />
abbiamo una sensibilità, che vi ricordo è data da falsi negativi, pari all’85%, superiore certamente a<br />
quella della tiroide, però non ottimale perché ho comunque il 15% di falsi negativi, la Microbiopsia,<br />
invece è superiore al 95% per ovvi motivi, lavoriamo su frustoli di tessuto;per la specificità,<br />
invece,sono equipollenti, ma con la Microbiopsia ci avviciniamo al 100%; se facciamo un confronto<br />
con la clinica, ovviamente per i linfonodi palpabili, per i non- palpabili non esiste proprio, la<br />
correttezza della diagnosi è intorno al 50% se lo prendo per positivo, se, invece lo prendo per<br />
negativo è intorno al 70%; anche la mammografia ha un range molto variabile a seconda delle<br />
casistiche, in rapporto anche all’età della paziente perché già vi dissi che per le donne giovani<br />
l’interpretazione mammografia è molto più complessa che per le donne più anziane, solo che non<br />
tutti i centri sono attrezzati con questa microbiopsia, quindi nell’attesa di attrezzare tutti i centri e le<br />
strutture è importante fare la Citologia aspirativi e riservare la Microbiopsia ai casi dubbi dal punto<br />
di vista mammografico ma anche citologico.<br />
Ecco la citologia aspirativi [IMMAGINE], molto importante è il background dei cosiddetti “nuclei<br />
nudi” e quest’aspetto arborizzante oltre che questa densità notevole, pensate queste sono le<br />
impronte dell’istologia e questo è l’aspetto di un fibroadenoma, guardate come nella forma<br />
intracanalicolare l’epitelio può mostrare delle atipie; [IMMAGINE] questa è ancora una patologia<br />
benigna, vediamo addirittura il lobulo e immaginate un lobulo, perché l’azione è soprattutto<br />
aspirante della citologia aspirativa, come se il lobulo lasciasse un’impronta, e qui troviamo anche<br />
scaricato da www.sunhope.it
cellule giganti, se c’è una mastite granulomatosa; [IMMAGINE] qui si vedono elementi molto<br />
sospetti, una grande importanza ce l’ha la forma del nucleo, ma anche la distribuzione della<br />
cromatina, con una distribuzione “molding”, s’intende cioè quando un nucleo si sagoma sull’altro,<br />
vedete, questo nucleo si deforma e paradossalmente questa cellula tumorale è più fragile di una<br />
cellula normale, la quale è più dura di una cellula tumorale, resiste alle aggressioni, vedete qua c’è 1<br />
mitosi cosiddetta da scoppio, perché tutto il materiale cromosomico si è disposto a colori;<br />
[IMMAGINE] questo è un caso di cancro ad alto grado, guardate la distribuzione irregolare dei<br />
cromocentri e della cromatina in grado; [IMMAGINE] il carcinoma lobulare, vedete, è formato da<br />
piccole cellule; [IMMAGINE] qui è rappresentato il classico “anello con castone”, quindi si tratta di<br />
un carcinoma mucoide;questo è un altro carcinoma; [IMMAGINE] questo è uno dei motivi per cui<br />
il carcinoma può essere detto secco, quando ci troviamo dinanzi ad una fibrosi così forte che<br />
addirittura la lama del microtomo ha difficoltà a tagliare, questo spiega perché ci sono queste<br />
grinze, queste ripiegature, legate proprio al fatto che la lama sobbalza, di fronte alla durezza ha<br />
delle oscillazioni, per le quali l’ago aspirato risulta insufficiente; [IMMAGINE] ecco il<br />
mammuTOM e questi sono i frustoletti di tessuto, sono aghiformi, piccole carotine, anche di<br />
spessore inferiore a 1mm che ci danno però una dimensione realistica del cancro, se fatto bene, ora<br />
c’è una valutazione morfologica accurata, un’elevata specificità e sensibilità e c’è anche un altro<br />
vantaggio, mentre sul citologico posso avere difficoltà a fare dei metodi speciali, sulla microbiopsia<br />
posso fare tutti i metodi possibili e immaginabili, perché è materiale incluso, quindi posso ricercare<br />
i recettori, l’ER2, il Ki67 e tutti i marcatori, in modo che la microbiopsia rappresenta anche un<br />
superamento della biopsia incisionale, cioè che uno prelevava un pezzo di tessuto e lo analizzava,<br />
invece ora con la microbiopsia si salta questa fase.[IMMAGINE] Ecco come appare ingrandito un<br />
frustolo di tessuto, qua vedete delle cellule a fila indiana di un carcinoma globulare, quest’altro,<br />
invece, è un carcinoma duttale, lo spessore di questa carotina è < 1mm, voi la vedete ingrandita.<br />
Quindi, se una mammografia è positiva o sospetta facciamo una citologia aspirativa, ma oggi si dà<br />
preferenza alla microbiopsia, ma rimaniamo in condizioni standard dei centri che non hanno ancora<br />
questa strumentazione, quindi se il FNAB è positivo, la possibilità di avere un cancro si avvicina al<br />
100%, se però è negativo non siamo sicuri al 100%, così se il FNAB è sospetto, o addirittura può<br />
essere inadeguato per fibrosi, calcificazioni, o quando la neoplasia è talmente piccola che si ha<br />
difficoltà a prendere qualcosa. Ove mai ci siano dei problemi, se il FNAB ad esempio è negativo,<br />
ma il mammografista non è convinto, c’è la microbiopsia e l’intraoperatoria è inutile fare la<br />
citologia aspirativa se sappiamo, ad esempio che il nodulo è molto calcifico, fibrotico, piccolo, con<br />
l’ago aspirato probabilmente non otterremo risultato.<br />
Questo è uno schema che ci serve per riunire le informazioni cliniche, biologiche, anatomopatologiche<br />
e terapeutiche insieme. Cosa sappiamo noi di come il cancro della mammella evolve?<br />
Quando è a 0,3 mm, invisibile alla mammografia, già è a 10alla quarta[ non lo so segnare al pc ]<br />
=10000 cellule e ha già avuto 12 generazioni e anche a 2,4mm oscilla tra 10alla quarta e 10 alla<br />
settima e ha avuto 23 generazioni, fino a questo livello è pT1a, il follow-up è del97%; se già ci<br />
troviamo a pT1b e quindi ci troviamo tra 0,5 e1cm, il cancro è arrivato a un numero di cellule pari a<br />
10 alla nona=1000000000 e 30 generazioni e il follow-up scende all’89%, il pT1c, stiamo tra 1 e<br />
2cm, 10 alla decima cellule e 33 generazioni, il follow-up è dell80%; però, vedete, se passiamo a<br />
pT2, cioè tra 2 e 5cm, ecco, questo è il momento critico che ci aiuta a capire la razionalità di uno<br />
screening, il follow-up scende al 50%, abbiamo in numero di cellule pari solo a 10alla undicesima<br />
che corrisponde a 10 miliardi, però, vedete, ci sono state solo 3generazioni in più, quindi 33, in un<br />
tempo relativamente breve, poi se scendiamo a pT3 arriviamo al 30% di sopravvivenza, e, per<br />
arrivare a quest’aggravamento della prognosi non è necessario un numero enorme di generazioni,<br />
ma solo 3, vedete, da 33 a 36, mentre ovviamente il tumore ha avuto una crescita esponenziale,<br />
perché siccome le cellule sono molte saranno numerose soprattutto le cellule neoformate, però<br />
facciamo anche una valutazione in rapporto alle tecniche: con la mammografia noi possiamo<br />
cogliere una lesione anche di pochi mm, per vederli con la clinica, invece, devono essere almeno di<br />
1cm, il nodulo dev’essere palpabile.<br />
scaricato da www.sunhope.it
Le metastasi decorrono in quest’intervallo di tempo, tra pT1c e pT3 e si calcola che quando<br />
arriviamo, in genere, a questo livello c’è un intervallo pari a pochi mesi da quando un cancro è pT1<br />
a pT2 ci vogliono pochi mesi perché ci sono tra essi poche generazioni di differenza, il cancro<br />
arriva a 33 generazioni per superare i 2cm, per arrivare a 5cm ci vogliono 36 generazioni, quindi<br />
solo 3 generazioni di differenza, perciò si spiega questo breve intervallo di tempo, quindi il fattore<br />
tempo è un fattore determinante; anche sotto il profilo medico legale: un ritardo diagnostico in<br />
oncologia ha un valore notevole per la paziente e anche per le implicazioni medico legali.<br />
Cosa deve, quindi, fare il povero anatomo-patologo?<br />
Un lavoro enorme! Come si fanno i prelievi? Secondo le direttive dell’OMS solo per l’areola<br />
mammaria e il capezzolo, tutti i linfonodi che ci sono, bisogna esaminarli, toglierli,tagliarli a uno a<br />
uno, alla fin fine ve risultano una marea di vetrini istologici che ci servono per stabilire l’istotipo, il<br />
grading, i margini di escissione, i margini del tumore, la cinetica cellulare, l’ER2, i marcatori<br />
endocrini, i recettori per il progesterone e le indagini molecolari, per vedere se c’è familiarità e<br />
questa è solo la fase post-operatoria, perché c’è ancora la fase pre-operatoria e quella<br />
intraoperatoria.<br />
C’è una classificazione oggi, addirittura, molecolare del tumore alla mammella. Inoltre, un altro<br />
concetto che si sta diffondendo soprattutto nei Paesi più ricchi, cioè l’ipotesi di poter fare dei test di<br />
screening predittivi del rischio di un tumore, che costano moltissimo, perché si tratta di analizzare<br />
moltissimi geni insieme con la tecnica del microarray, per un giudizio articolato quasi a dire se sei<br />
predisposto o non sei predisposto; è uscito un test, il “mammaprint”-che più correttamente dovrebbe<br />
chiamarsi “mammasold”da un punto di vista commerciale- che analizza una serie di geni, è stato<br />
approvato dalla Food & Drug Administration che in USA è un organismo di grande potenza, che<br />
abbassa e risolleva le industrie, non come in Italia, dove abbiamo le authority, che cosa fanno io non<br />
so, dovrebbero vigilare su tutta una serie di procedimenti che coinvolgono i consumatori. Ma il<br />
problema è: possiamo fidarci di questo test? Quando uscì il CEA tutti gridarono al miracolo; ne<br />
nacque poi un contenzioso perché si vide che c’erano molti falsi negativi e anche molti falsi<br />
positivi, per cui tutti andavano a fare questo CEA-TPA 3.4 marcatore , pensando di aver risolto il<br />
problema; il problema è che a molti si dava un giudizio positivo anche se questi non avevano niente,<br />
visto che il CEA lo si ritrova anche in fumatori o in soggetti che prendono l’aspirina, per cui anche<br />
su questo ultimo test, uscito nel 2007, io ho qualche perplessità, perché risponde a un desiderio<br />
culturale molto diffuso nell’uomo medio, soprattutto nei paesi avanzati, che si illude di potersi<br />
assicurare contro tutto e per tutto.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA lezione del 30/11/10<br />
Prof. Rossiello<br />
Oggi parliamo dell’ovaio. L’ovaio, tra gli organi genitali, è sicuramente quello più complicato. La<br />
volta precedente abbiamo parlato dell’embriologia, ho cercato di semplificarvela quanto più<br />
possibile; l’embriologia è importante per capire alcune patologie che si ripercuotono su tutta la<br />
sfera genitale femminile. Dal punto di vista embriologico vi sono molte analogie con la sfera<br />
genitale feminile, almeno per un determinato periodo di tempo. Tutto comincia a livello della<br />
CAVITA’ CELOMATICA, una cavità che si forma precocemente già dopo poche settimane. Ecco<br />
(immagine), questa è la struttura dell’ovaio che è pochi centimetri(in gravidanza aumentano le<br />
dimensioni) dove vediamo una corticale, (qua vediamo una piccola cisti)e una midollare che è fatta<br />
da uno stroma particolare perché può fare di tutto; poi c’è l’ilo che è questa parte vicino alla tuba<br />
che è la parte dove ci sono i vasi, la rete ovarii. Cosa succede in questa cavità celomatica? Vi<br />
risparmio tutti i meccanismi molecolari e genetici, vedete che tutto deve procedere con dei<br />
meccanismi di precisione di tipo svizzero. C’è infatti una certa frequenza di malformazioni genitali,<br />
soprattutto dell’utero (utero bisettato, utero bicorne ecc). Comunque nella maggior parte dei casi<br />
questo meccanismo funziona perfettamente. Allora, dal sacco vitellino,( che molti di voi pensano<br />
sia una membrana, un sacchetto) in particolare dalla faccia ventrale, incominciano a migrare delle<br />
cellule, che sono cellule germinali primordiali, cioè quelle che andranno a formare gli ovociti; esse<br />
fanno una migrazione enorme, e dove si vanno a posizionare? Si vanno a posizionare sulle creste<br />
genitali. In questa cavità(immagine), si formano due creste, in realtà tre, solo che quella centrale<br />
andrà a formare una parte dell’intestino. Queste due creste sono chiamate le creste genitali. Da<br />
queste creste, voi vedete una struttura qui che è quasi simile ad un tubulo con un occhiello finale,<br />
ecco questi sono i dotti paramesonefrici(poi vedremo cosa sono). Andiamo avanti: queste piccole<br />
cellule bianche, sono le cellule che vengono dal sacco vitellino. Queste cellule si vengono a<br />
posizionare alle spalle, cioè un po’ dietro alla cresta genitale, il connettivo incomincia a proliferare<br />
e si forma lo stroma ovarico che dovrà accogliere le cellule germinali primordiali che diventeranno<br />
ovociti. Cosa succede poi? Si forma un’incisura, un’invaginazione a livello delle due creste, una di<br />
qua e una di là; l’ epiltelio invaginato si chiama “mulleriano”, perché da questo epitelio<br />
deriveranno gli organi genitali, cioè deriverà la vagina, la tuba, l’utero e così via. Un'altra struttura è<br />
il dotto mesonefrico o “wolfiano”a forma di S, da cui deriverà l’abbozzo renale; questo spiega la<br />
vicinanza con l’ovaio e certi residui wolfiani a volte possono rimanere nell’ovaio. Tutta questa<br />
struttura (immagine) è rivestita dall’epitelio celomatico che è importantissimo perché una parte<br />
andrà a rivestire l’ovaio, il resto formerà il mesotelio. Vediamo un’immagine ingrandita: ecco qui<br />
vediamo questa invaginazione con l’epitelio mulleriano da cui prenderà origine utero, vagina tuba,<br />
mentre quest’altra struttura è il dotto tagliato di trasverso che si chiama anche wolfiano. Questo<br />
epitelio celomatico di rivestimento può mostrare nell’adulto tutta una serie di<br />
metaplasie( metaplasia sierosa, ciliare, endometroide, mucoide e una tradizionale che solitam si<br />
trova nelle vie urinarie)probabilmente sempre per un contatto embriologico con organi circostanti.<br />
Questo è l’ilo ovarico, queta è la rete ovarii che è molto simile nella sua struttura alla rete testis.<br />
Andiamo avanti: questa è la dinamica ciclica del follicolo. Ci sono le cellule germinali primordiali;<br />
scaricato da www.sunhope.it
c’è ina morìa di ovociti tra il periodo embrionale e il periodo dell’adulto, voi sapete che meno di<br />
500 ovociti nella donna andranno a formare i follicoli, quindi le possibilità sono, per così dire,<br />
contate. Allora, dal follicolo primordiale si forma il follicolo primario, le cellule stromali si<br />
trasformano in cellule tecali e cellule della granulosa, esse circondano l’ovocita perché hanno una<br />
funzione di sostegno. Questo follicolo primario cresce sempre di più e diventa secondario. Qui la<br />
cellula uovo rimane ancora al centro ma tutto intorno c’è una proliferazione delle cellule della<br />
granulosa, mentre più all’esterno ci sono le cellule tecali( teca interna ed esterna). Vedete le cellule<br />
fibrose che stanno nello stroma ovarico quante modificazioni subiscono. Alcune di queste<br />
rimangono cellule fusate che però sono ormono-poietiche. A questo punto si forma il follicolo di<br />
graaf; già prima qui si formano degli spazi chiari tra le cellule della granulosa, questi spazi si<br />
chiamano di “cool exstener”, in genere succede che più follicoli subiscono questa maturazione però<br />
si verificherà la prevalenza di uno, cioè c’è uno che blocca tutti gli altri(il boss dei follicoli!!). A<br />
questo punto si forma il cumulo ooforo, questo spazio qui si amplia e l’uovo si prepara ad essere<br />
espulso attraverso la corticale ovarica che è un tessuto fibroso(ci sono delle patologie di questa<br />
corticale che si ripercuotono sull’ovulazione). Tutto questo processo richiede tutta una serie di geni<br />
ed enzimi che non solo devono esserci, ma devono cooperare tra loro. Ora, ciò che resta del<br />
follicolo (il quale non sa ancora se l’ovocita verrà fecondato o no)si trasforma in corpo luteo,il quale<br />
si chiama così perché queste cellule della granulosa e tecali si riempiono di grasso. Esse sono<br />
deputate al rilascio di alcuni ormoni tra cui il progesterone( il progesterone prepara l’utero ad un<br />
eventuale annidamento). Trascorso un periodo di circa 14 giorni, questo corpo luteo che si era<br />
ingrandito, se non è avvenuta la fecondazione, capisce che non è successo niente e se ne va in<br />
atrofia; i corpi albicanti rappresentano l’involuzione, la senescenza (la cicatrice) del corpo luteo. Se<br />
noi vediamo un ovaio, dal numero dei corpi albicanti possiamo risalire quasi all’età di questo ovaio.<br />
L’epitelio celomatico è in fin dei conti costituito da uno straterello di cellule appiattite,<br />
mesoteliformi, eppure è fondamentale, poi vedremo perché. Queste sono alcune immagini del<br />
corpo luteo: esso è giallo, talvolta pure un po’ emorragico. Qual è la caratteristica del corpo luteo?<br />
È che queste cellule che sembravano fusate, diventano grandi cellule ricche di un citoplasma<br />
eosinofilo perché producono ormoni; questo si chiama processo di “luteinizzazione”, la cellula<br />
diventa quasi epiteliomorfa, ma non è una cellula epiteliale, chiamiamo epiteliomrfe tutte le<br />
cellule che hanno un citoplasma abbondante. Qui entrano in gioco le gonadotropine, perché sotto<br />
lo stimolo dell’LH , queste cellule della granulosa e della teca si trasformano in cellule in grado di<br />
produrre il progesterone. Quindi in questo gioco l’ipofisi ha un ruolo dominante, l’ipofisi è come il<br />
direttore d’orchestra e poi ci sono i vari solisti giù. Prima di diventare corpo albicante, il follicolo<br />
subisce un’involuzione; una volta che si è avuta l’espulsione dell’ovocita, rimane un follicolo grosso,<br />
non c’è più la cellula uovo, qui si forma una fessura, poi questa fessura scompare, ecco queste sono<br />
le fasi del follicolo atresico. I corpi albicanti appaiono di un tessuto chiaro che, ad occhio si vede, è<br />
bianco, perciò si chiamano corpi albicanti. In gravidanza questo corpo luteo diventa enorme, le<br />
cellule diventano ancora più grandi; in questo caso non si forma il corpo albicante in quanto il<br />
corpo luteo deve sostenere la gravidanza con la sintesi di ormoni tra cui soprattutto il<br />
progesterone. Quali sono le cellule che producono ormoni nell’ovaio? Un sacco di cellule: abbiamo<br />
le cellule stromali che producono ormoni di vario tipo, le cellule luteinizzate sono le cellule stromali<br />
che hanno subito un processo di ingrandimento per cui assumono la forma epitelioide, poi<br />
scaricato da www.sunhope.it
abbiamo, a livello dell’ilo ovarico, ci sono altre cellule che producono ormoni e poi sempre qui, nel<br />
15-20% dei casi, possiamo trovare residui surrenalici e poi delle cellule molto simili anche<br />
funzionalmente alle cellule di Leydig( voi sapete che sono cellule dell’interstizio dei tubuli<br />
seminiferi), si preferisce comunque chiamarle “cellule ilari” per non creare confusione. La parete<br />
fibrosa che circonda l’ovaio si chiama “tunica albuginea”, e che comprende questa tunica? La<br />
sierosa, che sarebbe epitelio celomatico e un sottile straterello di tessuto fibroso. Vediamo un po’<br />
le principali CISTI OVARICHE. La cisti è la principale patologia dell’ovaio. Ci sono vari tipi di cisti. Tra<br />
quelle più comuni, ricordiamo la “cisti da inclusione”e che cos’è? Come è successo nel periodo<br />
embrionale, può succedere che anche nell’adulto, si formi un’invaginazione probabilmente dove è<br />
scoppiato il follicolo, cioè laddove sbocca il follicolo, ci può essere un’invaginazione dell’epitelio<br />
celomatico che non si limita a rimanere in superficie, ma va sotto; con il tempo poi, grazie<br />
all’azione del tessuto fibroso, questa struttura si distacca dalla superficie e diventa una cisti da<br />
inclusione; questa è una cisti che in genere non dà alcun fastidio. Le “cisti follicoliniche”o follicolari<br />
possono rappresentare diverse cose: possono rappresentare dei follicoli che non hanno avuto la<br />
prevalenza, possono dare un leggero fastidio, specialmente se ne sono molte perché producono<br />
estrogeni, non raramente in una persona con iperplasia dell’endometrio possiamo trovare delle<br />
cisti. Si possono formare ancora perché i follicoli non riescono a scoppiare e se non riescono a<br />
scoppiare l’ovocita stà là e il corpo luteo persiste. Poi abbiamo le “cisti del corpo luteo”, abbiamo<br />
detto che il corpo luteo può formare delle cisti, se il corpo luteo è inferiore a 3cm non si parla di<br />
cisti, ma di “corpo luteo cistico”; per diventare “cisti del corpo luteo”deve superare i 3cm (questo<br />
per convenzione internazionale). Poi ci sono le “cisti endometriosiche”(le tube, le ovaie e i tessuti<br />
paraovarici sono una sede preferenziale dell’endometriosi). L’endometriosi è un grosso problema<br />
perché è legata alla sterilità, molto spesso infatti le ovaie sono colpite bilateralmente. Poi ci sono le<br />
“cisti mulleriane”: i residui mulleriani, invece di andarsene in atrofia, possono rimanere e formare<br />
delle cisti. La cisti per definirla tale deve avere una parete; ci sono le cosiddette “cisti pseudo<br />
emorragiche” che non hanno una parete epiteliale, ma hanno solo connettivo, possono<br />
rappresentare spesso una evoluzione di una endometriosi, cioè queste isole endometriosiche si<br />
dilatano misticamente, vanno incontro a tutte le modificazioni del ciclo, poi vanno incontro a<br />
necrosi, emorragie, l’epitelio scompare e noi vediamo solo dei macrofagi, in questo caso noi<br />
dobbiamo fare tutta una serie di metodi per capire che le cellule che stanno intorno è stroma<br />
endometriale in quanto non abbiamo più la parete dell’endometrio o se no scriviamo “pseudo cisti<br />
emorragica compatibile con una cisti endometriosica”. Poi abbiamo le “cisti di Walthard”che pure<br />
derivano da residui embrionali, ma ne parleremo più avanti. Vediamo con qualche immagine le<br />
cisti da inclusione: un segno favorevole è vedere che queste cisti hanno dimensioni diverse. La cisti<br />
follicolinica invece può raggiungere voluminose dimensioni, qui vediamo una parete ripiena di<br />
materiale amorfo, detriti; se è inferiore a 2cm: follicolo cistico; se è superiore parliamo di cisti<br />
follicolinica. La cisti del corpo luteo abbiamo detto che deve superare i 3cm, qui è grandissima,<br />
addirittura occupa tutto l’ovaio. La presenza di queste cisti luteiniche è quella che dà più prolemi<br />
perché producono progesterone che va ad interferire con la regolarità del ciclo mestruale, i cicli<br />
saranno quindi molto irregolari. Per quanto riguarda le cisti endometriosiche, se si aprono<br />
prendono il nome di “cisti cioccolata”, somigliano molto al sanguinaccio. Il problema di queste cisti<br />
è che se si rompono all’esterno possono determinare un emoperitoneo. Sono spesso responsabili<br />
scaricato da www.sunhope.it
di dolore pelvico che è un problema perché a volte si riesce a spiegare(con l’endometriosi per es.),<br />
altre volte non si riesce a spiegare, può determinare infiammazione, adesioni perché a furia di<br />
avere queste emorragie, la parete dell’ovaio si assottiglia, si infiamma e si determinano poi<br />
aderenze con la tuba o con altri organi vicini, talvolta si formano come delle sacche che poi vanno<br />
incontro a fibrosi e che prendono contatto con organi vicini dando come l’impressione di un<br />
tumore maligno. Questa invece è una pseudo cisti emorragica, vedete, non distinguete più la<br />
parete, ma vedete questi grandi macrofagi, sangue e probabilmente questa cisti rappresenta<br />
l’evoluzione di un’endometriosi. Le cisti del Morgagni hanno un contenuto molto limpido, qual è la<br />
caratteristica di questa cisti? Che ha un epitelio simil-tubarico, le cellule tubariche hanno una<br />
caratteristica, che insieme alle cellule classiche colonnari vediamo delle cellule chiare, la presenza<br />
di queste cellule chiare è un marcatore morfologico delle cellule tubariche, ma un’altra<br />
caratteristica rispetto alle altre cisti è che nella parete notiamo anche un tessuto muscolare, perciò<br />
sono dette anche “mulleriane”, quando sentite mulleriane vuol dire che c’è sempre qualche<br />
tessuto in più (ricordate che dall’epitelio mulleriano si formerà anche il miometrio, quindi ha delle<br />
potenzialità anche muscolari). La cisti da Walthard la possiamo trovare soprattutto nei tessuti<br />
paraovarici e paratubarici e rappresenta una metaplasia a cellule transazionali(per es. le vie<br />
urinarie hanno questo epitelio caratteristico detto “transazionale”che in condizioni di riposo è<br />
pluristratificato, in condizioni di distensione sembra monostartificato, quindi è un epitelio molto<br />
elastico). I residui di Walthard sono questi: vediamo un epitelio di tipo transazionale.<br />
La sindrome di Stein Leventhal o sindrome dell’ovaio policistico non è così rara. La patogenesi è<br />
complessa e non ben definita perché riguarda un po’ tutto, io vorrei limitarmi a discutere un po’<br />
sulla situazione dell’ovaio. Ora, se andiamo a fare un’ecografia e l’ecografista è bravo, cos’è che ci fa<br />
pensare ad una Stein Leventhal? Quando vediamo queste cisti e tutta la corticale ne è piena, la<br />
bilateralità(sia ovaio di dx che di sn), la geometricità del reperto cioè cisti simili, molto spesso tutte<br />
inferiori ad 1cm, quindi già quando vede questo deve pensare ad una sindrome dell’ovaio<br />
policistico, poi ci sono una serie di test ormonali; in più se non è un ecografista abusivo, ma bravo,<br />
può vedere la corticale ispessita come un’area di iperdensità. Ovviamente c’è un’iperproduzione di<br />
estrogeni, perché si tratta di cisti essenzialmente follicolari, e l’iperestrogenismo, come abbiamo<br />
visto, è una condizione di rischio per il carcinoma dell’endometrio. Quindi macroscopicamente noi<br />
vediamo tutta una costellazione di cisti tutte inferiori al cm. C’è poi un ispessimento della tunica<br />
albuginea, il numero di follicoli primordiali è normale, ma vi è un aumento dei follicoli atresici<br />
perché il follicolo non riesce a scoppiare e questi follicoli si affollano per scoppiare, perché manca il<br />
follicolo dominante, e quindi ci sono cisti follicoliniche. La teca cerca di reagire a questa situazione,<br />
attraverso il feed-back ipofisario ,aumentando la luteinizzazione dello stroma e pensando che<br />
questo possa favorire questo scoppio. Ora, che questo sia un fatto importante nella patogenesi lo<br />
dimostra la terapia, una volta, ma anche adesso, si usava la terapia medica(anche perché questa<br />
sindrome dà anche obesità, virilizzazione e così via), poi si praticava la resezione cuneiforme che<br />
era un intervento un po’ doloroso perché si resecava a cuneo l’ovaio e in alcune aveva successo. Si<br />
è visto poi che si può risparmiare questo intervento praticando una terapia che è detta<br />
“imprinting”; ecco, non so se avete mai visto come si fanno le salsicce in casa, si prende la carne di<br />
maiale e si mette nella pelle di intestino e si legano, se uno mette a cuocere queste salsicce così e<br />
non lo sa, queste si gonfiano. Il macellaio che lo sa, prendeva un pezzo di sughero, si infilavano<br />
scaricato da www.sunhope.it
tanti spilli dentro e poi con questo sughero si premeva sopra le salsicce in modo da creare tanti<br />
forellini. Questa è la tecnica chirurgica, cioè andiamo a bucare la tunica albuginea creando tanti<br />
piccoli forellini.<br />
Esiste anche una “ooforite immunitaria” che talvolta è responsabile della menopausa precoce, cioè<br />
donne che vanno in menopausa a 40 anni ed è legata alla presenza di autoanticorpi verso le cellule<br />
che producono steroidi.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong><br />
Arterie e Vene<br />
Prof.ssa Costanzo<br />
Lezione n°20<br />
3/12/2010<br />
L'apparato vascolare è costituito dalla pompa vascolare cardiaca e due sistemi di vasi<br />
che vanno a costituire il piccolo circolo della circolazione polmonare, e il grande circolo<br />
della circolazione sistemica che permette la distribuzione del sangue in tutti gli organi<br />
del corpo.<br />
Arterie<br />
Le più importanti sono la aorta e la polmonare e in base al calibro di questi vasi<br />
distinguiamo 3 gruppi:<br />
• arterie di grande calibro: aorta e suoi rami, che posseggono una forte<br />
componente elastica<br />
• medio calibro di 2-9mm di diametro: muscolari, renali, che sono di distribuzione<br />
• piccolo calibro, dette anche arteriole, che decorrono in organi e tessuti.<br />
Istologicamente la arteria è divisa in 3 strati:<br />
• Tonaca Interna (intima): è costituita da un rivestimento monostratificato di<br />
endotelio, ed è uno strato sottile che poggia sul connettivo sottoendoteliale,<br />
caratterizzato dall'avere, sopratutto nelle a. più grandi, due membrane, interna<br />
ed esterna, che delimitano questo connettivo. Queste membrane posseggono<br />
fissurazioni che permettono il passsaggio di sostanze attraverso l'endotelio.<br />
Sono fenestrazioni presenti solo nella membrana elastica interna. La strutture<br />
dell'intima delle arteriole è uguale a quella delle arterie do grande calibro.<br />
(Sbob: La prof prima fa capire che le fenestrazioni sono in entrambe le<br />
membrane e poi dice che stanno solo nella interna...).<br />
• Tonaca media, costituita da fibrocellule muscolari lisce che si dispongono in<br />
modo longitudinale o circolare e si uniscono a fibre elastiche e possono<br />
intrecciarsi direttamente con gli strati fenestrati che mettono in comunicazione<br />
queste cellule.<br />
Nelle arteriole questo strato è più sottile di quanto non sia nelle arterie di<br />
grande calibro.<br />
• Tonaca avventizia (esterna): formata da fibroblasti e fibre connettivali che<br />
hanno lo stesso orientamento longitudinale del vaso. Questo connettivo<br />
permette il passaggio di altri vasi più piccoli (sbob: immagino si riferisca ai vasa<br />
vasorum).<br />
Nelle arteriole ci sono meno fibroblasti.<br />
Osservando la sezione trasversale di una arteria e di una vena, si vede che le<br />
dimensioni della parete delle arterie è maggiore, che ha una parete più spessa. La<br />
maggiore grandezza del calibro della arteria è dato dalle dimensioni maggiori della<br />
tunica media, e questo è dovuto a variazione del contenuto di fibre elastiche e<br />
collagene. Le vene invece hanno dimensioni minori, e lo spessore dei vari strati è<br />
molto più proporzionato.<br />
scaricato da www.sunhope.it
Vene<br />
Anche queste possono essere di piccolo, medio e grande calibro.<br />
Sono dette di medio calibro solo quelle vene che hanno le dimensioni da 2-9mm.<br />
Le vene hanno un'<br />
• Tonaca interna (intima): costituita da cellule endoteliali con forma poligonale e<br />
confini più irregolari. Le vene di piccolo calibro hanno un intima costituita da un<br />
singolo strato di endotelio.<br />
• Tonaca media: invece è costituita da fibrocellule muscolari lisce e fibre collagene<br />
che hanno un decorso longitudinale e pochi fibroblasti. È più sottile rispetto a<br />
quella delle arterie.<br />
• Avventizia ha sempre tessuto connettivo lasso e ci sono anche fasci di fibre<br />
collagene che hanno decorso longitudinale intrecciato a reti elastiche. Questo<br />
strato è in proporzione più esteso nelle vene di grande calibro.<br />
Patologie dei vasi<br />
Sono rappresentate principalmente da due grossi meccanismi:<br />
1. Ipoperfusione del tessuto irrorato dal vaso che porta all'ischemia<br />
2. Sanguinamento da danno vasale<br />
L'emodinamica è il flusso ematico del sangue che deve essere mantenuto in genere<br />
costante, e se non lo è ci sono le manifestazioni patologiche come edema, congestione<br />
vascolare, emorragia, trombosi, embolia, infarto, shock; tutti segni visibili nei<br />
preparati anatomopatologici.<br />
Per esempio di una trombosi è visibile l'effetto, ma si può vedere il trombo solo nella<br />
autopsia, quando è stato il trombo che ha causato la morte.<br />
Solo così ci si può andare ad accertare delle caratteristiche dell'embolo.<br />
Edema<br />
Accumulo di liquido negli spazi extracellulari o nel tessuto interstiziale che viene<br />
danneggiato. I fattori che causano l'edema sono per esempio la<br />
– infiammazione come aumento della pressione idrostatica intracapillare<br />
– diminuzione della pressione osmotica delle proteine extracellulari<br />
– ritenzione di sali e di acqua.<br />
sono tutti meccanismi che portano alla formazione di liquido che può essere trasudato<br />
o essudato.<br />
Tipi di edema:<br />
1. Sistemico: si vede macroscopicamente un gonfiore nella zona danneggiata,<br />
mentre a livello microscopico si trova un rigonfiamento cellulare anche molto<br />
evidente che, al microscopio, si traduce come scolorimento della sezione<br />
istologica perchè le cellule sono rigonfie di acqua e questo fenomeno può<br />
riguardare cute, polmoni, cervello,...<br />
2. Localizzato: la manifestazione è in genere macroscopica dove si evidenzia per<br />
esempio nella gravidanza, nella trombosi venosa occlusiva, nelle vene varicosi.<br />
Può essere causato da aumento localizzato della permeabilità vascolare anche<br />
nella infiammazione acuta o nelle reazione di ipersensibilità di tipi I (orticaria o<br />
nell'adema angioneurologico per esempio)<br />
3. Linfedema: drenaggio linfatico alterato o ostruito<br />
scaricato da www.sunhope.it
Iperemia e congestione<br />
Iperemia: quantità di sangue maggiore del normale presente in un dato organo o in<br />
un dato tessuto, dovuto a due meccanismi fondamentali che danno la specifica<br />
classificazione anatomopatologica:<br />
• Iperemia attiva: che è l' aumento dell'afflusso<br />
• Congestione passiva: diminuzione dell'efflusso<br />
Il tessuto colpito è arrossato per la presenza di sangue ossigenato. Esempi di<br />
congestione:<br />
– Congestione polmonare: nella congestione polmonare acuta microscopicamente<br />
nella vicinanza dei capillari si trova sangue con edema nei setti alveolari e si<br />
osservano le classiche emorragie negli spazi interalveolari.<br />
Nella congestione polmonare cronica questi setti danno spazio a quella che è la<br />
fibrosi per cui i setti diventano piuttosto spessi, e gli spazi possono contenere<br />
dei macrofagi che, andando a pulire la zona danneggiata, assumono una<br />
morfologia che li fa definire “cellule dell'insufficienza cardiaca” e sono cellule<br />
patognomoniche di questa patologia.<br />
– Fegato: si può avere congestione epatica acuta dove la vena centrale e i<br />
sinusoidi sono colpiti fino a degenerazione centrale degli epatociti. Gli epatociti<br />
periportali, che sono più ossigenati, sviluppano più tardivamente ipossia e<br />
quindi questa fase porta le cellule epatiche allo stadio di steatosi epatica.<br />
Nella congestione cronica del fegato invece è colpita la zona centrale, dove il<br />
fegato appare di colore rosso bruno e le cellule cominciano ad andare in<br />
apoptosi e aree intere vanno in necrosi e queste aree assumono colore marrone<br />
dando un fegato a “noce moscata”. Microscopicamente si vede come necrosi<br />
“centrolobulare” e perdita di epatociti, con emorragie e macrofagi che<br />
contengono emosiderina.<br />
Emorragia<br />
fuoriuscita di sangue dai vasi per rottura del vaso.<br />
• Ematoma: emorragia racchiusa nell'ambito di un tessuto.<br />
• Petecchie: emorragie piccole di 1-2mm cutanee o presenti sulle mucose. A<br />
livello macroscopico si evidenziano per esempio in alcune sierose, e osservate al<br />
microscopio per possono aiutare nella diagnosi.<br />
• Porpora: manifestazione emorragica di dimensioni >3mm. Sono in genere<br />
associate in infiammazioni locali vascolari come nelle vasculiti, o anche quando<br />
c'è fragilità vascolare.<br />
• Ecchimosi: emorragie maggiori di 1-2cm causata da fagocitosi di eritrociti<br />
danneggiati in seguito ad un trauma.<br />
• Emopericardio/emoperitoneo/emotorace: sono quadri di emorragie più ampie in<br />
cavità sierose<br />
scaricato da www.sunhope.it
Emostasi<br />
I processi coagulativi in condizioni normali tengono il sangue allo stato liquido mentre<br />
stimolano la formazione del coagulo in presenza di danno vasale.<br />
Il processo di emostasi in seguito ad un danno vascolare la linea della emostasi<br />
presenta più fasi:<br />
• I fase: vasocostrizione arteriolare dovuta ad un meccanismo neurogeno riflesso<br />
e da secrezione locale di endotelina<br />
• II fase: adesione ed attivazione delle piastrine con rilascio di alcuni granuli<br />
secretori che costituiscono il tappo emostatico<br />
• III fase: il fattore tissutale (o precoagulante) agisce sulle piastrine per attivare<br />
la cascata della coagulazione attivando la trombina A, che converte il<br />
fibrinogeno circolante in fibrina insolubile che va a depositarsi localmente.<br />
La fibrina e le piastrine cosi aggregate vanno a formare il tappo che può<br />
arrestare l'emorragia e prevenirne di ulteriori.<br />
Trombosi<br />
Formazione di masse solide che si possono formare nel cuore, nelle arterie, nelle vene<br />
e nei capillari a partire da elementi circolanti. Si spiega come una inappropriata<br />
attivazione del processo emostatico che si ha quando c'è formazione di coagulo di<br />
sangue in un vaso non danneggiato e quando si ha occlusione trombotica di un vaso in<br />
seguito ad un danno. La patogenesi è spiegata con la triade di Virchow dove c'è:<br />
1- danno endoteliale<br />
2- turbolenza o stasi del flusso sanguigno<br />
3- ipercoagulabilità del sangue<br />
I trombi possono svilupparsi nelle cavità cardiache ed in particolare a livello delle<br />
cuspidi valvolari e in tutti i vasi. La sede da cui hanno origine ne determina la forma.<br />
I trombi arteriosi sono originati da danno endoteliale, dove sono presenti turbolenze a<br />
livello per esempio della biforcazione del vaso e tendono a crescere in maniera<br />
retrogada rispetto al loro punto di attacco.<br />
Quelli formati nel cuore e nella aorta presentano laminazione dette “strie di zahn” che<br />
microscopicamente sono strati chiari costituiti da fibrina e piastrine, e da strati più<br />
scuri che sono costituiti da eritrociti. I trombi in queste sedi sono detti “murali”.<br />
• Trombi arteriosi sono in genere occlusivi e possono essere originati da una<br />
placca di aterosclerosi o altri danno vasali come nelle vasculiti o nei traumi. Si<br />
presentano con colorito grigiastro, sono friabili e sono costituiti da un reticolo<br />
irregolare di piastrine, fibrina, eritrociti e leucociti, che si presentano degenerati<br />
e per questo causano la friabilità.<br />
• Trambi venosi: causati da stasi, si espandono in direzione del flusso sanguigno<br />
e possono formare emboli. Portano ad occlusione del vaso e sono detti “trombi<br />
rossi” perchè contengono quantità di eritrociti maggiore a quelli arteriosi.<br />
La flebotrombosi origina prevalentemente dalle vene delle estremità inferiori e<br />
dalle valvole cardiache quando sono presenti endocarditi batteriche o fungine.<br />
In pazienti con ipercoagulabilità si sviluppano endocarditi trombotiche non<br />
batteriche e si ritrovano anche in pazienti con LES che possono sviluppare<br />
endocarditi verrucose, formando complessi antigene-anticorpo circolanti.<br />
Evoluzione del trombo:<br />
1. Fase di propagazione, dove il trombo accumula piastrine e fibrina provocando<br />
occlusioni vascolari<br />
2. Fase di embolizzazione quando il trombo si stacca ed arriva in altre sedi<br />
3. Fase di dissoluzione possono essere rimossi ed eliminati dalla attività fibrolitiche<br />
del vaso stesso, o possono andare incontro a organizzazione formando<br />
infiammazione e fibrosi. Possono anche essere inglobati a livello dello stesso<br />
vaso causando ispessimento dell'intima vasale.<br />
scaricato da www.sunhope.it
Embolia<br />
massa anomala di materiale solido o gassoso che viene trasportata lungo il flusso<br />
ematico fino ad arrivare ad un vaso il cui diametro è inferiore a quello dell'embolo<br />
stesso e causando quindi impedimento al flusso.<br />
Possono essere costituiti da trombi, coaguli ematici, gassosi (aria, azoto), adiposi<br />
(come nelle fratture), neoplasici, da frammenti di midollo osseo, frammenti di placche<br />
aterosclerotiche.<br />
La maggioranza degli emboli di grandi dimensioni deriva da trombi e la conseguenza<br />
dell'evento è la necrosi ischemica del tessuto a valle dell'ostruzione, come succede in<br />
tutti i tipi di infarto.<br />
Esempi di emboli:<br />
• Tromboembolia polmonare dove l'embolia è causato spesso da trombi formati<br />
nelle vene profonde e, attraverso il cuore dx, arriva al circolo polmonare.<br />
A seconda delle dimensione può occludere una arteria principale, fermarsi ad<br />
una biforcazione o arrivare ad arterie più piccole.<br />
• Tromboembolia sistemica : l'embolo viaggia attraverso circolo arterioso, e l'<br />
80% dei trombi sono intramurali intravascolari e di questi i 2/3 spesso sono<br />
associati ad infarto transmurale del ventricolo sn ed 1/3 sono associati a<br />
dilatazione dell'atrio sn.<br />
Il restante 20% origina da aneurismi dell'aorta, placche aterosclerotiche,<br />
frammentazioni di vegetazioni creando emboli paradossi (sbob: cito<br />
testualmente). Gli emboli arteriosi viaggiano partendo da sedi che<br />
frequentemente sono gli arti inf e il cervello dando infarti.<br />
• Embolia lipidica: sono gocce di grasso frequenti nelle fratture delle ossa lunga,<br />
nei traumi di tessuti molli o nelle ustioni.<br />
• Nella embolia gassosa c'è la presenza di bolle di gas nella circolazione con<br />
ostruzione del flusso sanguigno che causa danno ischemico a valle del vaso.<br />
• Embolia di liquido amniotico: complicanza del parto dove la causa non è altro<br />
che infusione di liquido amniotico nella circolazione materna da rottura della<br />
placenta e delle vene uterine.<br />
Ischemia<br />
è definita tale una condizione in cui la perfusione arteriosa di un organo o di un<br />
tessuto è insufficiente rispetto al suo fabbisogno metabolico con conseguente<br />
riduzione della funzione d'organo.<br />
Cause di ischemia sono: trombosi ed embolia.<br />
L'ischemia da occlusione venosa è dovuta a impossibilità da parte del sangue di<br />
bypassare l'occlusione mediante circoli collaterali e il blocco provoca congestione e<br />
infarcimento emorragico del tessuto coinvolto.<br />
Ischemia da distruzione dei capillari può essere dovuto a danno fisico della parete dei<br />
capillari, dal congelamento, da ostruzione da parte di parassiti, eritrociti anomali,<br />
anemie autoimmuni, emboli, compressione, piaghe da decubito.<br />
Ischemia arteriosa comporta successiva necrosi del tessuto che dovrebbe essere<br />
irrorato.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA 07/12/2010<br />
Ci sono alcune situazioni patologiche, non neoplastiche, che vedremo in rapida successione<br />
perché le troverete fatte bene sul libro.<br />
Consideriamo la cosiddetta ipereazio luteinalis (è il nome latino). Cosa si intende per questa<br />
patologia? In occasione di una patogenesi trofoblastica, avete sentito parlare di mola<br />
vescicolare in ginecologia?<br />
Il trofoblasto che è fatto da sinciziotrofoblasto e citotrofoblasto cioè due tipi cellulari,<br />
rappresenta quell'intercapedine che si pone a livello placentare tra i tessuti e la placenta e<br />
sono i villi coriali che sono rivestiti da queste cellule che producono vari tipi di ormoni, tra cui<br />
soprattutto l'hCG. Su quest’ormone si basa il test di gravidanza.<br />
Una donna soggetta a patologia trofoblastica (che poi può essere più o meno grave, ci sono<br />
delle forme che consentono anche di portare avanti, fino ad un certo punto, la gravidanza)<br />
avrà un'iperstimolazione da parte di questi ormoni e si possono formare nell'ovaio molte cisti<br />
luteiniche che regrediscono dopo il parto.<br />
L'iperstimolazione da parte di questi ormoni può anche portare:<br />
- a virilizzazione, perché producono anche ormoni androgeni<br />
- a dolore pelvico<br />
- e a un enorme ingrandimento dell'ovaio. Quando l'ovaio s’ingrandisce, per un fenomeno ti<br />
torsione può andare incontro ad una necrosi ischemica.<br />
LUTEOMA GRAVIDICO<br />
Il luteoma gravidico, che regredisce dopo la gravidanza, è rappresentato da uno sviluppo<br />
abnorme del corpo luteo gravidico che può arrivare ad occupare tutto l'ovaio.<br />
Possiamo avere, poiché produce testosterone, virilizzazione sia della madre sia del neonato<br />
IPERPLASIA STROMALE<br />
L'iperplasia stromale è un fenomeno molto diffuso, non riguarda la gravidanza in quanto tale,<br />
ed è determinato da un'iperplasia dello stroma ovarico che è anch'esso funzionante dal punto<br />
di vista ormonale. Molto spesso questa situazione è correlata ad un iperestrogenismo e non ad<br />
un iperandrogenismo, quindi quando c'è un'iperestrogenismo ci stanno tutta una serie di<br />
patologie di accompagnamento compreso iperplasia dell'endometrio ed altre cose di cui<br />
abbiamo parlato.<br />
IPERTECOSI<br />
L'ipertecosi invece sarebbe un'iperplasia stromale, solo che le cellule fibrose si trasformano in<br />
cellule tecali e assumono un aspetto un po' epiteliode e producono testosterone quindi<br />
abbiamo segni di virilizzazione, obesità, ipertensione ecc.<br />
Questa situazione può determinare anche carcinoma endometriale<br />
TORSIONE DELL'OVAIO<br />
La torsione dell'ovaio è un evento acuto che determina un addome acuto.<br />
In caso di addome acuto, si pensa sempre all'appendicite, ma in realtà ci sono altre cause di<br />
addome acuto.<br />
scaricato da www.sunhope.it
TUMORI OVARICI<br />
I tumori ovarici sono terribili perché:<br />
- riguardano sempre un'età giovanile, adulta<br />
- non danno segni di se precoci, quindi li identifichiamo in uno stato più avanzato di sviluppo<br />
- sono tumori che hanno un'elevata mortalità<br />
In linea di massima le neoplasie benigne, che pure sono molto espresse, cioè l'80% dei tumori<br />
ovarici sono benigni prevalgono in un'età più giovanile mentre le forme maligne prevalgono in<br />
età più adulta però l'età media è di 45 anni quindi vuol dire che l'incidenza va dall'età quasi<br />
pediatrica, possiamo avere tumori anche a 15-16 anni, mentre è difficile avere tumori del<br />
genere dopo i 60 anni.<br />
La sintomatologia è tardiva, aspecifica, possiamo avere:<br />
- dissezione e dolore addominale però se abbiamo questo vuol dire che il tumore già è<br />
diventato grande<br />
- irregolarità mestruale<br />
- turbe urinarie, gastroenteriche ecc<br />
Il 75% dei casi viene identificato nello stadio III e IV che sono degli stadi avanzati.<br />
I fattori di rischio sono:<br />
- l'obesità. L'obesità è sempre correlata perché il tessuto adiposo non è un tessuto inerte, può<br />
produrre degli ormoni ed è esso stesso legato a problemi ormonali<br />
- contraccettivi orali, anche se alcuni sostengono che sono fattori protettivi, altri dicono che<br />
non sono fattori protettivi invece altri dicono che sono indifferenti<br />
- fattori genetici, come BRCA1 e BRCA2 che coinvolgono anche l’ovaio (ne abbiamo parlato<br />
nella mammella) e poi esistono altri fattori genetici che determinano un elevato rischio di<br />
carcinoma ovarico<br />
Abbiamo dei marcatori che si utilizzavano molto una volta, anche adesso si utilizzano, però<br />
sappiate che non esiste un marcatore assoluto.<br />
Tra i marcatori, molto noti sono i CA125, CA15-3, CA-72-4. Questi marcatori aumentano<br />
soprattutto in particolari tumori epiteliali dell’ovaio, mentre altri tumori, che sono la maggior<br />
parte dei tumori, hanno altri marcatori.<br />
Questa è la casistica della mortalità dell’American Cancer Society che è una valutazione<br />
globale.<br />
Come vedete la mortalità dei tumori dell’ovaio sta al quinto posto (nelle donne il polmone ha<br />
superato la mammella), al terzo posto c’è il colon-retto.<br />
L’ovaio incide per il 5%, però dovete calcolare che non è una neoplasia molto frequente<br />
rispetto ai polmoni quindi se incide per il 5% della mortalità, vuol dire che è un’elevata<br />
mortalità. Pensate che la mammella che è molto più frequente dell’ovaio, incide per il 15%.<br />
Se vedete l’andamento della mortalità in questo grafico che raggruppa i dati dal 1930 fino ai<br />
nostri giorni, vedete che l’ovaio ha una curva stazionaria e ciò vuol dire che è migliorata la<br />
sopravvivenza perché invece la mammella e il colon-retto hanno curve in discesa.<br />
Lo possiamo vedere meglio confrontando due annate e cioè 1991-2005. Il guadagno che c’è<br />
stato nella mortalità per il cancro ovarico in questi 15 anni è bassissimo e cioè 9,36%.<br />
Paragonate questo guadagno invece al guadagno che c’è stato nella mammella che è del 27%,<br />
al colon-retto dove arriviamo al 28%, ai linfomi non-Hodgkin che si avvicinano al 19% oggi<br />
l’hanno anche superato grazie alle nuove terapie.<br />
Diciamo che l’ovaio è uno di quei casi che ha registrato un miglioramento molto basso.<br />
LINEE DIFFERENZIATIVE DEI TUMORI OVARICI<br />
Vi ricordate che abbiamo parlato di un epitelio di superficie che deriva dall’epitelio celomatico,<br />
poi abbiamo parlato di uno stroma fibroso, poi abbiamo parlato delle cellule della granulosa e<br />
scaricato da www.sunhope.it
della teca che sono quelle che rivestono il follicolo nella sua maturazione, quindi i tumori<br />
ovarici vanno verso tre strade differenziative.<br />
Vi faccio uno schema classico nosologico perché poi vedremo che anche le cellule staminali<br />
entrano in questa complessa architettura.<br />
Distinguiamo i tumori ovarici in tre categorie:<br />
1) I tumori dell’epitelio superficiale rappresentano da soli il 55% di tutti i tumori ovarici e a loro<br />
volta rappresentano il 95% di tutti i tumori maligni.<br />
Pensate che il testicolo che ha gli stessi tumori dell’ovaio non ha però i tumori epiteliali<br />
perché manca questo rivestimento di epitelio celomatico.<br />
Quindi la maggiore incidenza nell’ovaio è legata a questi tumori epiteliali imparentati con<br />
l’epitelio di superficie<br />
2) I tumori a cellule germinali che nascono dalle cellule germinali cioè dagli ovociti. Questi<br />
tumori sono di diverso tipo. I tumori a cellule germinali rappresentano il 30% dei tumori,<br />
ma nel 95% dei casi sono benigni<br />
3) I tumori dello stroma, della teca, dei cordoni sessuali cioè tumori dello stroma specializzato,<br />
nel senso che quando diventano cellule della granulosa, cellule tecali perché sempre dallo<br />
stroma derivano queste cellule. Questi tumori incidono nell’8% dei tumori ovarici e la<br />
maggior parte sono benigni<br />
4) Poi abbiamo altri tumori che sono meno dell’8%<br />
TUMORI DELL’EPITELIO SUPERFICIALE<br />
Vedete già c’è una cosa che in effetti è nata proprio con la classificazione dell’ovaio di cui<br />
parleremo. Vedete che qui è codificato proprio in letteratura che le categorie sono 3:<br />
- tumori benigni<br />
- tumori borderline (possiamo definirli come tumori di confine)<br />
- tumori maligni<br />
I tumori dell’epitelio superficiale possono essere:<br />
- sierosi, sono pari al 30% del 55% di tutti i tumori ovarici<br />
- mucoidi perché producono muco<br />
- endometriodi perché mostrano una differenza dell’epitelio in senso endometriale e<br />
rappresentano il 2-4% dei tumori<br />
- tumore di Brenner che ha due componenti e cioè una epiteliale ed una connettivale e questo<br />
tumore incide per il 2%<br />
- i carcinomi a cellule chiare che rappresentano la degenerazione maligna endocervicale.<br />
Vi ricordate che abbiamo parlato di epitelio mulleriano che può assumere una conformazione<br />
endometriale, può assumere una metaplasia ghiandolare e quindi ci spieghiamo benissimo<br />
che ci possono essere carcinomi a cellule chiare<br />
- poi abbiamo i tumori misti e altri tipi di tumori perché a volte i tumori hanno degli istotipi per<br />
esempio siero-mucoidi cioè alcune aree sierose altre invece mucoidi<br />
Parliamo adesso dei tumori sierosi.<br />
Se uno ha un tumore sieroso, a volte con i markers tumorali non è che abbiamo un valore<br />
assoluto, però ci sono dei markers più specifici per i tumori sierosi ed altri invece più specifici<br />
per i tumori mucoidi però si tratta sempre di prevalenze e non di valore assoluto.<br />
In genere un tumore sieroso nel 60% è benigno, nel 30% è maligno e nel 10% è borderline.<br />
Quindi i tumori sierosi, che sono la categoria più frequente dei tumori ovarici, hanno questa<br />
distinzione per quanto riguarda la benignità e la malignità.<br />
Il più frequente tra i tumori sierosi è il cistoadenoma sieroso semplice che può apparire come<br />
una specie di “pellecchia”, una specie di cellofan ripieno di liquido (come nel caso della figura).<br />
scaricato da www.sunhope.it
Altre volte invece all’interno della parete che sembra di plastica sottile osserviamo dei rilievi<br />
sporgenti e in questo caso parleremo di cistoadenoma sieroso papillifero.<br />
Entrambe queste forme sono benigne, sono molto frequenti, il contenuto è quasi sempre<br />
limpido e la cisti può essere uniloculare o multiloculare.<br />
IMMAGINE: questa è una sezione trasversale di un ovaio e questo è il caso di un cistoadenoma<br />
sieroso multiloculare per cui vedete che fa molte cisti<br />
Com’è la parete del cistoadenoma sieroso semplice? La parete, poiché ha accumulato liquido e<br />
questo liquido preme sulla parete che si sciaccia, assume molto spesso questo andamento di<br />
cellule appiattite. E’ un epitelio di tipo sieroso, non fa muco quindi è una parete molto sottile.<br />
Nel cistoadenoma sieroso papillifero possiamo osservare delle papille cioè un asse connettivo<br />
vascolare delimitato da un epitelio di tipo sieroso, non ci sono segni di invasività quindi ci<br />
troviamo di fronte ad un tumore benigno.<br />
IMMAGINE: qui vediamo ancora un tumore papillifero, questa è una papilla, ha un asse<br />
connettivale molto sottile ma se vedete l’epitelio non è normale come abbiamo visto prima.<br />
Vedete c’è una tendenza alla stratificazione e alla pseudo-stratificazione, ci sono<br />
evidentemente delle atipie citologiche quindi quando ci troviamo di fronte a delle atipie<br />
citologiche anche più marcate di queste, ma non riscontriamo fenomeni di invasività o di<br />
embolie neoplastiche cioè di gettoni tumorali nei vasi, pur di fronte a delle atipie più spiccate di<br />
queste che vediamo qui, dobbiamo usare la dizione borderline.<br />
Borderline sta a significare un tumore che tecnicamente è maligno però io non trovo<br />
l’invasività.<br />
Grossomodo questi tumori borderline si comportano all’80-90% come tumori benigni e un 10%<br />
che si comportano come tumori maligni.<br />
Allo stato attuale non abbiamo sistemi per capire quali di questi borderline corrispondono<br />
all’80-90% e quali invece al 10%, però prevalgono le forme benigne.<br />
IMMAGINE: qui vediamo delle atipie ancora più spiccate però non c’è invasività sotto, c’è lo<br />
stroma, le atipie sono spiccate. Paradossalmente possiamo trovare dei tumori con atipie<br />
citologiche molto serie però non hanno invasività ed è borderline mentre possiamo avere dei<br />
tumori con atipie meno gravi ma hanno invasività ed in questo caso è un carcinoma e non un<br />
tumore borderline quindi non ci possiamo fidare delle atipie citologiche<br />
IMMAGINE: questo è un carcinoma e lo capiamo benissimo perché qui vedete i gettoni invasivi<br />
che invadono lo stroma.<br />
I carcinomi sierosi papilliferi possono presentare un’estensione alla pelvi nel 16% dei casi,<br />
estensioni addominali nell’11% dei casi, tendono a dare frequentemente metastasi<br />
linfoghiandolari nel 55% dei casi e più raramente metastasi ematiche.<br />
Altra caratteristica del tumore papillifero è la presenza di calcificazioni che sono evidenti anche<br />
ad un quadro radiologico. Queste calcificazioni hanno una strutturazione particolare e cioè sono<br />
stratificate all’interno come la cipolla, per cui quando assumono questa stratificazione (simili ai<br />
giri che osserviamo sui tronchi di un albero tagliato) li definiamo CORPI PSAMMOMATOSI e<br />
sono calcifici. La calcificazione avviene per apposizione perciò abbiamo questa stratificazione<br />
(tipo la merendina girella).<br />
scaricato da www.sunhope.it
CISTOADENOMA MUCOIDE<br />
Nel cistoadenoma mucoide abbiamo una maggiore prevalenza di forme benigne (75%), una<br />
riduzione delle forme maligne (15%) e le forme borderline sono le stesse (10%).<br />
La caratteristica è che tende a formare queste cisti biancastre o incolori perché sono ripiene di<br />
muco.<br />
A volte che succede, per quei giochi di metaplasia, di cellule staminali di cui parleremo,<br />
possiamo avere anche un cistoadenoma mucoide di tipo intestinale perché qui vedete le cellule<br />
caliciformi, le cellule follicolari e così via.<br />
Altre volte invece somiglia più all’endocervice che è mucoide.<br />
Il tipo borderline presenta delle atipie spiccate, tendenza alla pseudo-stratificazione, ma non<br />
c’è invasività.<br />
Il carcinoma invece in alcuni punti presenta un’invasione che può andare al di fuori della<br />
ghiandola quindi possiamo dire adenocarcinoma<br />
CARCINOMA ENDOMETRIOIDE<br />
Il carcinoma endometrioide rappresenta l’8-21% dei carcinomi ovarici.<br />
Questo tumore è maligno nell’85% dei casi però la malignità è di basso grado, nel 10% dei casi<br />
è benigno e in meno del 10% è borderline.<br />
Questo tumore pur essendo più frequentemente degli altri maligno, però ha la tendenza a<br />
raggiungere grosse dimensioni, pur essendo in uno stadio precoce di sviluppo, per cui la<br />
maggior parte di queste forme le identifichiamo nel I e nel II stadio ed ha un follow-up a 5<br />
anni.<br />
Questo tumore è relativamente vantaggioso rispetto ad altre forme, vedete che il I stadio può<br />
arrivare al 97% mentre il II stadio può arrivare al 68% dei casi.<br />
Quindi ricordiamo che il carcinoma endometrioide molto spesso è un carcinoma di basso grado<br />
che consente dei tassi di sopravvivenza relativamente migliori rispetto ad altri.<br />
CARCINOMA A CELLULE CHIARE<br />
Il carcinoma a cellule chiare è maligno nel 90% dei casi e nel 10% dei casi è benigno o<br />
borderline, quindi le forme benigne di questa neoplasia sono rare.<br />
Questo carcinoma ha una notevole aggressività e può presentarsi con tutta una serie di<br />
sindromi, sapete le sindromi paraneoplastiche molto spesso legate a tutta una serie di segni<br />
clinici soprattutto connessi a produzione di ormoni vari per cui c’è tutta una sintomatologia<br />
complessa. Questo carcinoma oltre alle sindromi paraneoplastiche può dare stranamente anche<br />
ipercalcemia e può dar luogo a manifestazioni trombotiche o emboliche legate molto spesso a<br />
questa ipercalcemia.<br />
TUMORE DI BRENNER<br />
Il tumore di Brenner è costituito da un tessuto fibroso nel cui contesto vediamo delle isole<br />
molto spesso fatte da epitelio transizionale (questo epitelio lo ritroviamo a livello della vescica,<br />
dell’uretra quindi delle vie urinarie) quindi questo tumore è frutto di una metaplasia<br />
transizionale. Questo tumore molto spesso è benigno (92% casi), mentre in meno dell’8% dei<br />
casi è maligno e borderline.<br />
Noi riconosciamo delle insule di epitelio che può essere transizionale, ghiandolare, mucoide, o<br />
di altro tipo cioè questa doppia componente stromale e questi gettoni epiteliali inclusi dentro<br />
sono la caratteristica di questo tumore che prende il nome da Brenner.<br />
In alcuni casi assume proprio la classica dimensione di un carcinoma a cellule transizionali.<br />
Il tumore di Brenner è molto raro.<br />
IMMAGINE: vedete questo è un epitelio transizionale che ha questa caratteristica rispetto allo<br />
squamoso e cioè che i limiti cellulari non sono ben distinti per cui si vedono le stratificazioni<br />
scaricato da www.sunhope.it
anche se mantiene un po’ le caratteristiche dell’epitelio transizionale normale che sapete è<br />
pseudo-stratificato nel senso che in condizioni di distensione diventa monostratificato.<br />
In alcuni casi possiamo avere un carcinoma papillifero come quelli che si manifestano nella<br />
vescica, solo che sta nell’ovaio, se non sapessimo che è un ovaio, potremmo fare diagnosi di<br />
carcinoma uroteliale della vescica.<br />
IMPIANTI E MATASTASI PERITONEALI<br />
La stadiazione è molto importante perché cambia la terapia e la valutazione prognostica.<br />
Un punto cruciale di questa stadiazione è quando il chirurgo va ad operare e innanzitutto è<br />
tenuto a fare un’ispezione attenta del peritoneo pelvico o anche più in là per vedere se ci sono<br />
delle localizzazioni di questa neoplasia ovarica e poi deve raccogliere il liquido citologico, molto<br />
spesso lo fa nello scavo del Douglas o dove trova più liquido peritoneale.<br />
Questo liquido viene poi mandato al patologo che deve esaminarlo per vedere se in questo<br />
liquido ci sono o meno cellule atipiche perché cambia la stadiazione.<br />
Le localizzazioni peritoneali possono essere di vari tipi, pensate che anche i tumori benigni lo<br />
possono fare, per esempio il cistoadenoma mucoide o il cistoadenoma sieroso papillifero che<br />
può nascere anche dalla superficie ovarica e protrudere da essa, può dare per sgocciolamento<br />
delle cellule che vanno a finire sul peritoneo.<br />
Il peritoneo deriva dall’epitelio celomatico quindi queste cellule si trovano a casa loro, si<br />
ingrossano e il chirurgo le vede. In questo caso non parliamo di metastasi ma di impianto<br />
quindi si tratta di una colonizzazione che non ha un significato maligno perché questi gettoni<br />
sono un impianto ma non sono invasivi, non sono metastatizzati e questo ai fini della<br />
stadiazione è ininfluente.<br />
Oltre a trattarsi di impianti invasivi e non invasivi, possiamo trovarci di fronte ad altre<br />
situazioni che abbiamo scoperto nel corso degli anni.<br />
In occasione di un tumore ovarico, il peritoneo può subire delle metaplasie in senso tubarico e<br />
quindi avere delle aree cosiddette di endosalpingiosi in cui l’epitelio, normalmente piatto, si<br />
solleva a formare questo epitelio cilindrico tipo l’epitelio tubarico cioè endosalpingiosi.<br />
Possiamo avere poi il mesotelio irritato dalla presenza del tumore anch’esso fatto da cellule<br />
mesoteliali che possono andare incontro a iperplasia e rilevarsi e in questo caso parleremo di<br />
IPERPLASIA REATTIVA DEL MESOTELIO.<br />
Una particolare circostanza chiamata PSEUDOMIXOMA PERITONEI in cui il peritoneo è<br />
tappezzato da queste lesioni biancastre. Questa situazione può essere legata, molto spesso, o<br />
a un carcinoma dell’appendice (perché l’appendice raramente da carcinomi che molto spesso<br />
sono neuro-endocrini e poi ci sono quelli mucoidi) oppure può essere legato ad un carcinoma<br />
ovarico.<br />
Quindi per pseudomixoma peritonei si intende tutto il peritoneo costellato da tutte queste<br />
lesioni biancastre legate ad una disseminazione o di un carcinoma mucoide appendicolare o di<br />
un carcinoma mucoide che appartiene all’ovaio.<br />
Un impianto è caratterizzato dal fatto che non ha un’aggressività, cresce, ma non c’è una<br />
reazione (vedete questo è un impianto sieroso papillifero), molto più subdolo è l’impianto<br />
desmoplastico in cui non solo c’è l’impianto di queste cellule ma è molto difficile fare questa<br />
diagnosi differenziale con una metastasi peritoneale perché il tessuto connettivale reagisce e<br />
ha una reazione desmoplastica anche se questi gettoni sono benigni, quindi c’è bisogno di<br />
molta esperienza in questi casi per vedere poi che queste cellule non sono atipiche e non si<br />
tratta di una vera invasività ma ci troviamo di fronte ad una reazione esagerata di tessuto<br />
connettivale che finisce con l’intrappolare queste cellule e dare l’impressione di una falsa<br />
invasività quindi si tratta di una pseudo-invasione.<br />
scaricato da www.sunhope.it
STADIAZIONE FIGO<br />
La stadiazione dei tumori ovarici prevede vari stadi.<br />
Lo STADIO I è quando il tumore è confinato all’ovaio quindi non va al di fuori della parete<br />
esterna dell’ovaio, dell’epitelio celomatico che riveste l’ovaio.<br />
Questo stadio si distingue in:<br />
- IA, se coinvolge un solo ovaio<br />
- IB, se coinvolge entrambe le ovaie<br />
- IC, quando la capsula che circonda l’ovaio si è rotta e quindi si può presumere che sia andato<br />
fuori, quando è positivo il liquido quindi c’è un’ascite positiva e quando la localizzazione è<br />
superficiale, in questo caso si presume anche che possa esserci disseminazione, soprattutto il<br />
sieroso papillifero può essere superficiale e vediamo delle estroflessioni proprio sulla<br />
superficie; non si tratta in questo caso di un’invasione da sotto ma è proprio il tumore che ha<br />
sede lì cioè anziché andare verso l’interno va verso l’esterno<br />
Lo STADIO II invece è caratterizzato da un’invasione degli organi più vicini.<br />
Questo stadio si distingue in:<br />
- IIA, se sono coinvolte le tube o l’utero<br />
- IIB, quando l’estensione va oltre le tube e l’utero<br />
- IIC, quando non solo c’è l’estensione pelvica ma quando è positivo il liquido citologico quindi<br />
nel IIC noi notiamo un’estensione ad organi pelvici qualunque essi siano compreso utero e<br />
tube e liquido citologico positivo<br />
Lo STADIO III è caratterizzato da metastasi peritoneali, se sono metastasi cioè ci dobbiamo<br />
accertare che siano metastasi.<br />
Questo stadio si distingue in:<br />
- IIIA, se sono metastasi microscopiche cioè molto piccole<br />
- IIIB, se sono metastasi macroscopicamente visibili ma comunque inferiori a 2 cm<br />
- IIIC, se sono metastasi peritoneali maggiori di 2 cm<br />
Lo STADIO IV è caratterizzato da metastasi a distanza che in genere riguardano il polmone, il<br />
fegato, i linfonodi distanti per esempio i latero-cervicali, i sovraclaveari che sono molto distanti<br />
dall’ovaio vanno considerati in questo stadio<br />
Questa stadiazione ha un valore prognostico? Si, a prescindere dai sottostadi.<br />
Lo STADIO I ha un tasso di sopravvivenza a 5 anni che va dal 71 all’87% ovviamente l’87% si<br />
riferisce allo stadio IA.<br />
Nello STADIO II la prognosi scende dal 55 al 67%.<br />
Nello STADIO III la prognosi scende dal 23 al 41%.<br />
Nello STADIO IV la prognosi scende al 5-10% e non lascia molte speranze.<br />
Ovviamente cambia anche la terapia.<br />
Nello STADIO IA forse anche IB, la terapia può essere la salpingo-ooforectomia e poiché questi<br />
tumori non raramente possono essere bilaterali, l’intervento chirurgico in genere è bilaterale<br />
quando una donna ha una certa età. L’intervento può anche essere monolaterale se la donna è<br />
giovane e ha desiderio di avere gravidanze, tenendola ovviamente sotto controllo.<br />
Nello STADIO II si procede con l’isterectomia, con la salpingo-ooforectomia bilaterale. In<br />
questo stadio vi ricordo che c’è già un’estensione pelvica e si procede anche con la<br />
chemioterapia.<br />
Nello STADIO III si procede con l’isterectomia, con la salpingo-ooforectomia bilaterale e con<br />
una chemioterapia aggressiva.<br />
Nello STADIO IV si procede con una chemioterapia aggressiva e si può anche rinunciare a fare<br />
l’intervento di asportazione globale perché è un cancro che coinvolge vari organi e si parla in<br />
questi casi se c’è un approccio chirurgico di una chirurgia riduttiva cioè nel senso di ridurre la<br />
massa per facilitare l’azione della chemioterapia sperando di migliorare la prognosi che di per<br />
sé in questo stadio già è negativa.<br />
scaricato da www.sunhope.it
Quando il chirurgo si trova di fronte ad un tumore borderline deve sottoporre a controlli<br />
periodici la paziente e poiché c’è un’alta % di comportamenti benigni in questi tumori<br />
borderline, non conviene essere aggressivi sia dal punto di vista chirurgico sia da altri punti di<br />
vista e si rimane in attesa degli eventi. Ci sono dei protocolli che stabiliscono dei tempi di<br />
controllo seguendo una scadenziario fatto di date.<br />
TUMORI A CELLULE GERMINALI<br />
Questi tumori nascono dall’ovocita.<br />
Una delle ipotesi più suggestive è che queste cellule uovo che normalmente vanno avanti<br />
attraverso una riproduzione sessuale per cui devono essere fecondate dallo spermatozoo,<br />
invece partono per i fatti loro attraverso la partenogenesi che è una forma di riproduzione che<br />
riguarda gli esseri inferiori e i vegetali e cioè che non prevede una fecondazione eterologa.<br />
Queste cellule possono seguire tre strade:<br />
- o sono costituite da vere e proprie cellule germinali cioè che rimangono tali come ovociti e<br />
allora abbiamo il DISGERMINOMA che nel testicolo cambia nome e si chiama SEMINOMA però<br />
è lo stesso tumore perché questi tumori sono analoghi nell’ovaio e nel testicolo.<br />
Vi ricordo che nel testicolo non ci sono i tumori epiteliali<br />
- oppure queste cellule decidono di differenziarsi in senso extraembrionario, voi sapete che<br />
oltre al feto c’è il sacco vitellino, il coriale e queste strutture decidono di differenziarsi negli<br />
annessi e quindi abbiamo il tumore del sacco vitellino oppure abbiamo il coriocarcinoma che è<br />
un tumore molto maligno che nasce dalle cellule trofoblastiche perché le cellule trofoblastiche<br />
fanno parte della gravidanza perché rappresentano il rivestimento dei villi coriali quindi ai<br />
primordi proprio della gravidanza<br />
- oppure la differenziazione è intraembrionaria cioè come se volessero fare un feto per fatti<br />
loro, allora abbiamo i TERATOMI che possono essere ricchi di peli, di sebo maleodorante e poi<br />
abbiamo il cosiddetto CARCINOMA EMBRIONARIO che vorrebbe differenziarsi ma non ci riesce<br />
e quindi vediamo solo delle strutture tipo morula cioè degli aggregati cellulari molti atipici ma<br />
è un carcinoma molto maligno che sta anche nel testicolo.<br />
I teratomi sono quelli più abbondanti e nell’ovaio trovano la loro sede più frequente.<br />
Infine abbiamo i TUMORI MISTI cioè tumori che sono un po’ dell’uno e un po’ dell’altro cioè<br />
possiamo trovare un teratoma che ha un carcinoma embrionale dentro o un teratoma che ha<br />
un’area di disgerminoma<br />
DISGERMINOMA<br />
Il disgerminoma è raro, nel testicolo è più frequente. In genere ha una buona prognosi perché<br />
è piccolo, il tasso di sopravvivenza è del 95%; se da metastasi può coinvolgere l’ ovaio<br />
controlaterale, i linfonodi e la cavità peritoneale.<br />
Quali sono le sue caratteristiche di base? Noi possiamo avere:<br />
- un disgerminoma puro, fatto solo da cellule germinali. Abbiamo dei markers che sono il PLAP e<br />
il CD 117 che sono dei markers proprio delle cellule germinali<br />
- può avere delle aree trofoblastiche cioè all’interno del tumore vediamo delle cellule sinciziali<br />
che sono delle cellule trofoblastiche e abbiamo anche la conferma se facciamo<br />
l’immunoistochimica perché queste cellule producono HCG<br />
- oppure possiamo avere con aree del tumore del sacco vitellino.<br />
Quindi oltre al disgerminoma puro possiamo avere disgerminomi associati ad altre<br />
differenziazioni.<br />
La terapia è l’asportazione dell’ovaio, si può fare radio o chemioterapia negli stadi più avanzati.<br />
scaricato da www.sunhope.it
Il disgerminoma ha un colorito rosa salmone, ha una struttura alveolare e questi alveoli hanno<br />
delle cellule dentro e nello stroma, tra alveolo e alveolo, vedete queste piccole cellule che sono<br />
dei linfociti (non si sa come mai queste cellule gonadiche maligne richiamano la presenza di<br />
linfociti)<br />
TUMORE DEL SACCO VITELLINO<br />
I tumori del sacco vitellino sono tipici dell’età giovanile e possono essere associati a teratomi.<br />
Ha una prognosi peggiore rispetto al disgerminoma perché tende a metastatizzare<br />
frequentemente e presenta positività alla citocheratina (cosa che non fa il disgerminoma<br />
perché è un tumore epiteliale) e all’alfa-feto proteina.<br />
Tende a dare metastasi precoci e la sopravvivenza a tre anni è bassissima e in questi casi si<br />
tenta una polichemioterapia che mostra qualche miglioramento della prognosi che comunque<br />
rimane severa.<br />
La caratteristica di questo tumore è che è un pattern reticolare o microcistico e che presenta<br />
questi corpi detti di SCHILLER-DUVAL che hanno un centro di materiale eosinofilo e tutto<br />
intorno queste cellule che si dispongono così oppure possiamo avere dei CORPI IALINI sempre<br />
vicini a queste strutture dove al centro possiamo trovare un vaso o del materiale amorfo.<br />
Quindi o corpi ialini o corpi di Schiller-Duval.<br />
A volte può assumere un aspetto tipo carcinoma epatocellulare perché è un aspetto più solido<br />
però capiamo che è un tumore del sacco vitellino perché è positivo alla citocheratina e all’alfafeto<br />
proteina.<br />
CARCINOMA EMBRIONARIO<br />
Il carcinoma embrionario ha prognosi abbastanza severa, ha una differenziazione molto<br />
primordiale perché non tende ad una differenziazione più spinta con delle atipie ben evidenti,<br />
anche qui abbiamo l’alfa-feto proteina ma il marker più essenziale per la diagnosi è il CD30<br />
cioè è positivo al CD30.<br />
La prognosi è severa e si tenta una chirurgia radicale e una chemioterapia molto aggressiva.<br />
A volte queste cellule atipiche si dispongono come se volessero formare qualche tubulino, altre<br />
volte hanno degli aspetti glomeruloidi o morulari cioè dei piccoli aggregati di cellule e diciamo<br />
che vorrebbe ma non riesce a differenziarsi.<br />
CORIOCARCINOMA<br />
Il coriocarcinoma è un tumore molto maligno però fortunatamente abbiamo delle terapie molto<br />
efficaci per questo carcinoma che è raro.<br />
Distinguiamo:<br />
- delle forme gestazionali cioè che ricorrono nel periodo della gravidanza o a breve distanza<br />
dalla gravidanza<br />
- delle forme extra-gestazionali cioè al di fuori della gravidanza che raramente possono<br />
mostrarsi anche nel maschio per esempio una delle sedi di queste forme extra-gestazionali è<br />
rappresentata dal mediastino per motivi che non conosciamo.<br />
Qual è la caratteristica di questo trofoblasto? Il trofoblasto è fatto da cellule che accompagnano<br />
i villi coriali in un’operazione di approfondimento delle radici cioè rappresentano le radici su cui<br />
si poggerà la cellula uovo e tutto l’embrione per cui hanno una grande tendenza a scavare<br />
sotto e ad entrare in contatto con i vasi; questa tendenza è mantenuta da questo cancro che è<br />
molto vascolarizzato, tende molto alla necrosi e tende a metastatizzare precocemente per via<br />
ematica proprio per queste sue caratteristiche.<br />
Le forme non gestazionali, più rare, sono quelle più resistenti alla chemioterapia mentre le<br />
forme gestazionali in genere hanno tassi di sopravvivenza oggi accettabili perché si sono<br />
trovate delle polichemioterapie efficaci per questo tipo di tumore.<br />
scaricato da www.sunhope.it
Vedete che sono sempre tumori molto emorragici, le atipie sono marcate e soprattutto vedete<br />
sempre queste emorragie, questi vasi, questa penetrazione nei vasi che è una caratteristica di<br />
questo tumore.<br />
TERATOMI<br />
I teratomi sono tra i tumori ovarici più frequenti, nel testicolo non sono così frequenti come<br />
nell’ovaio.<br />
Come possono essere? L’ipotesi più accreditata è che si formano per coalescenza di due follicoli<br />
o di due cellule uovo che si fondono tra di loro e danno luogo ad uno sviluppo di tessuti<br />
eterotopici.<br />
Il teratoma può essere:<br />
- monofillico<br />
- difillico<br />
- trifillico<br />
Cosa vuol dire? Monofillico se è fatto solo da tessuto ectodermico, da tessuti mesodermici o da<br />
tessuti endodermici. Il teratoma più complesso è quello che ha in se differenziazioni in tutti e<br />
tre i tessuti e quindi in qualche modo seppur in maniera disordinata tenta di riprodurre lo<br />
sviluppo embrionario.<br />
Il teratoma fatto da un solo strato è definito cisti epidermoidi.<br />
Sui teratomi, se fatti da epiteli, si può impiantare un carcinoma monofillico che se fatto da una<br />
cisti epidermoide possiamo vedere che questa cisti in qualche punto diventa carcinoma<br />
squamoso o di altro tipo.<br />
Per quanto riguarda i teratomi più complessi e maligni, usiamo la dizione di teratomi immaturi<br />
cioè non tendono alla differenziazione ma rappresentano tessuti embrionali e questo è segno di<br />
malignità. La componente più legata alla malignità è la componente neuro-ectodermica<br />
(ricordate che il tessuto nervoso nasce dal tubo neurale quindi ha questa tendenza a formare<br />
questi corpi intorno ad una cavità).<br />
L’immaturità può essere suddivisa in gradi in base alla presenza o meno di questi foci<br />
neuroepiteli e quindi diremo:<br />
- GRADO 1, se abbiamo rari foci<br />
- GRADO 2, se ci sono da 1 a 4 campi/vetrino<br />
- GRADO 3, oltre i 4 campi<br />
IMMAGINE: questo è un teratoma cistico nel quale potete osservare la presenza di peli, di<br />
sebo, cartilagine, osso cioè tessuti di vario tipo. In alcuni casi possiamo trovare denti, fino ad<br />
arrivare all’homunculus cioè un teratoma, benigno, che vuole riprodurre seppur in maniera<br />
rozza l’embrione.<br />
Il teratoma più classico è la cisti epidermoide quando è fatta solo da epitelio squamoso oppure<br />
cisti dermoide quando sono presenti anche gli annessi (strutture pilo-sebacee e peli).<br />
scaricato da www.sunhope.it
PATOLOGIA DEI VASI (Prof.ssa Costanzo)<br />
Continuiamo a parlare della patologia dei vasi e iniziamo col definire quali sono.Le<br />
principali malattie vascolari che colpiscono le arterie sono:<br />
• Aterosclerosi<br />
• Ipertensione,che non tratteremo,perché è un argomento piuttosto<br />
complesso,è solamente clinica e siccome è un argomento un po’ pesante e<br />
non mi ascolterete evitiamo di parlarne,però vi invito a studiarla,perché il<br />
Professore all’esame la vuole sapere.<br />
• Anomalie vascolari<br />
• Anomalie congenite,che possiamo anche trascurare.<br />
Per quanto riguarda le anomalie vascolari a livello clinico queste vengono<br />
evidenziate esclusivamente attraverso due meccanismi: 1) restringimento o<br />
completa ostruzione del lume vasale,dando così attraverso una forma progressiva<br />
quella che è la nostra aterosclerosi,mentre nel secondo caso possiamo andare<br />
incontro ad un fenomeno improvviso,per esempio con la formazione di un trombo<br />
che porta di conseguenza ischemia tissutale dell’organo colpito o anche un infarto 2)<br />
indebolimento della parete vasale con la dilatazione e quindi rottura del vaso stesso.<br />
Questa è l’immagine di una vena.La volta scorsa abbiamo visto la morfologia di un<br />
vaso in generale,la cui tunica media ha un’ ampiezza maggiore rispetto a quella della<br />
vena;la caratteristica che avevo sottolineato era la presenza di una lamina interna<br />
ed esterna aventi aperture dette fenestrazioni attraverso cui avvengono determinati<br />
meccanismi;in quest’altra immagine si vedono meglio le fenestrazioni e poi si<br />
osserva l’intima che è costituita da cellule epiteliali con la presenza della media che<br />
è più ampia e poi dell’avventizia.<br />
Per cui riepilogando a livello morfologico riconosciamo che gli elementi cellulari che<br />
costituiscono un vaso sono esclusivamente di due tipi:le cellule endoteliali e le<br />
muscolari vascolari lisce,cellule che abbiamo visto si andavano ad insinuare tra i fasci<br />
collagene e le fibre elastiche dei vari vasi.<br />
Cellule endoteliali:vanno a costituire un unico strato nella parete<br />
vasale,mantengono l’omeostasi all’interno del vaso stesso e l’equilibrio funzionale<br />
della circolazione.Hanno in genere una forma poligonale,sono allungate e formano<br />
scaricato da www.sunhope.it
complessi giunzionali l’una con l’altra.Esse svolgono anche altre funzioni :1)hanno<br />
una membrana semipermeabile 2) regolano un’interfaccia non trombo genica tra il<br />
sangue e il tessuto 3) modulano il tono vascolare ed il flusso sanguigno 4)<br />
metabolizzano ormoni 5) controllano le reazioni infiammatorie e le reazioni<br />
immunitarie per l’interazione dei leucociti che avvengono al momento del fenomeno<br />
6) modificano le lipoproteine nella parete delle arterie 7) regolano,inoltre,la crescita<br />
di altri tipi cellulari.<br />
La loro lesione quindi può contribuire alla patogenesi non solo dei trombi ma anche<br />
all’insorgenza dell’aterosclerosi.<br />
Cellule muscolari lisce: in genere allo stato di quiescenza hanno una forma fusata,un<br />
nucleo piuttosto allungato e somigliano un po’ ai fibroblasti.Svolgono diverse<br />
funzioni :1) determinano vasocostrizione e vasodilatazione 2)sintetizzano varie<br />
sostanze,ovvero fibre collagene,fibre elastiche e proteoglicani a seconda della<br />
costituzione del vaso stesso 3) elaborano fattori di crescita e citochine 4) sono in<br />
grado di migrare e proliferare nei processi non solo riparativi,ma anche nelle<br />
malattie appunto dei vasi.<br />
ATEROSCLEROSI<br />
La parola viene divisa in due parti,da una parte c’è il suffisso greco ATHERA che vuol<br />
dire “polpa o poltiglia” e dall’altra c’è la SCLEROSI che significa indurimento.Il<br />
termine quindi significa “indurimento delle arterie” e indica tre particolari condizioni<br />
patologiche che hanno in comune non solo l’ispessimento,ma anche la perdita<br />
dell’elasticità della parete vasale.Il quadro è caratterizzato dalla formazione di<br />
placche intimali fibrose che presentano un nucleo centrale ricco di lipidi oppure<br />
possiamo avere una sclerosi calcifica mediale detta di Monckeberg caratterizzata<br />
dalla calcificazione dell’arteria in questo caso muscolare,di media taglia,la quale può<br />
andare incontro ad ossificazione nella media e formare così degli anelli trasversali<br />
che sono visibili nelle normali radiografie che vengono fatte a pazienti sospetti;a<br />
carico delle arterie di piccolo calibro possiamo avere un altro tipo di variante che è<br />
quella ialina o iperplastica,la quale determina un ispessimento della parete vascolare<br />
portando ad una stenosi dle lume con conseguente danno ischemico.<br />
Quual è la morfologia di questo processo?Si ha innanzitutto :<br />
1)un ispessimento focale dell’intima 2) successivamente si vanno ad accumulare<br />
lipidi,quindi colesterolo e suoi esteri,e si va a costituire quello che viene detto<br />
scaricato da www.sunhope.it
cappuccio fibroso. Questo in genere ha un colorito bianco-giallastro e tende a<br />
protrudere nel lume del vaso.Esso è costituito da tre elementi principali:<br />
• Le cellule muscolari lisce,macrofagi e leucociti per quanto riguarda la<br />
componente cellulare<br />
• Si determina un tessuto connettivo detto della matrice extracellulare ricco di<br />
fibre elastiche e proteoglicani<br />
• In più in quest’area troveremo anche depositi lipidici intra ed extra-cellulari.<br />
Al danno vascolare segue la crescita delle cellule muscolari lisce e si ha così la<br />
ricostruzione della parete vascolare danneggiata che conduce alla formazione di un<br />
nuovo tessuto che chiameremo neo-intima,la quale è costituita proprio dalla<br />
migrazione e dalla proliferazione di queste cellule muscolari lisce e dalla<br />
moltiplicazione di queste cellule intimali e sintesi e deposizione delle proteine della<br />
matrice extracellulare.<br />
STRIA LIPIDICA: com’è costituita?Abbiamo detto che questo cappuccio fibroso,che<br />
costituisce la placca aterosclerotica non è altro che il precursore della malattia<br />
stessa.Per cui le lesioni iniziano con la comparsa di macchie giallastre multiple,che in<br />
genere hanno un diametro piuttosto piccolo,di 1 mm,che successivamente<br />
confluiscono a formare una stria di dimensioni variabili,può essere anche piuttosto<br />
lunga,di 2 cm e più.Queste strie sono costituite da cellule schiumose che vanno in<br />
supporto ai lipidi per fagocitare e spazzare questo materiale.<br />
Questo è lo schema che interviene nella formazione del cappuccio fibroso:si ha la<br />
migrazione delle cellule muscolari lisce nella media,dove dallo stato di quiescenza in<br />
cui si trovano vanno incontro a proliferazione e migrazione attraverso le<br />
fenestrazioni della lamina esterna,si portano nell’intima per fagocitare i lipidi che si<br />
sono depositati a questo livello con successiva proliferazione dell’endotelio che<br />
racchiude tutto il processo.Questa è poi la fine del processo:il cappuccio fibroso,che<br />
chiude il core centrale dove vengono ad essere racchiusi i macrofagi(cellule con<br />
pallini gialli) che hanno assorbito gli esteri di colesterolo,i vari lipidi e<br />
successivamente si è venuto a creare il cappuccio fibroso,con le cellule muscolari<br />
lisce,una nuova vascolarizzazione e il processo della migrazione delle cellule in<br />
questo caso termina.<br />
CONTINUO TUMORI GERMINALI DELL’OVAIO (Prof.Rossiello)<br />
scaricato da www.sunhope.it
TECOMI E FIBROMI<br />
Che differenza c’è tra i tecomi e i fibromi?Voi credete che io lo sappia,ma ne so un<br />
po’.<br />
I tecomi come i tumori delle cellule della granulosa è costituito da cellule altamente<br />
specializzate che si dispongono intorno all’ovocita essenziale già nel follicolo<br />
primordiale e sono quelle che vengono dette anche cordoni sessuali,sessuali perché<br />
si dispongono intorno all’ovocita e poi daranno luogo alle cellule della granulosa,alle<br />
cellule tecali,che poi andranno a far parte del follicolo secondario,follicolo di Graaf e<br />
così via.Lo stroma fibroso ha anch’esso una sua specializzazione,perché esso può<br />
essere anche ormonopoietico.I tecomi sono tumori dell’età avanzata,si associano<br />
spesso a iperplasia dell’endometrio,a carcinoma dell’endometrio,perché hanno un<br />
iperestrogenismo di fondo.Ovviamente è un tessuto abbastanza duro,solo che le<br />
cellule anzicchè essere solo fusate,hanno un citoplasma più ampio,luteinizzato,cioè<br />
più esteso,proprio perhè hanno capacità ormonogeniche molto elevate,in genere<br />
sono iperestrogeniche.<br />
Il fibroma è costituito da tessuto fibroso,non ha una grande capacità<br />
ormonopoietiche,però ha la capacità di crescere molto rapidamente pur essendo<br />
benigno,per cui determina una grande pressione endoaddominale che può<br />
determinare la fuoriuscita di liquido dalla cavità addominale al di là del diaframma e<br />
quindi nelle pleure e nella cavità mediastinica,determinando una particolare<br />
sindrome che è la sindrome di MEIG.<br />
Il tecoma si distingue dal fibroma,perché ci sono delle cellule fusate,cellule con un<br />
citoplasma più chiaro,perché spesso sono ricche di lipidi.A differenza del fibroma poi<br />
mostra la presenza dell’alfa-inibina,che è un marker generale di tutti i tumori della<br />
serie tranne del fibroma.Le cellule sono spesso distanziate l’una dall’altra.<br />
Il fibroma è caratterizzato da una densità cellulare,tutte cellule fusate,quindi niente<br />
da dire.<br />
TUMORI A CELLULE DEL SERTOLI-LEYDIG<br />
Le cellule del Sertoli sono quelle cellule che stanno nei tubuli seminiferi e che hanno<br />
una funzione di sostengo sui precursori degli spermatozoi,gli spermatogoni.Questi<br />
tumori sono abbastanza rari,però si associano a iperandrogenismo,per cui<br />
compaiono dei caratteri di mascolinizzazione,come ipertrofia del clitoride,irsutismo.<br />
scaricato da www.sunhope.it
Presenta tre varietà istologiche:può essere ben differenziato o poco<br />
differenziato.Quand’è che è ben differenziato?Quando queste due componenti,le<br />
cellule del Sertoli e le cellule del Leydig,che normalmente si trovano nell’interstizio<br />
tra i tubuli seminiferi,sono ben distinguibili.quindi noi distinguiamo dei tubuli e degli<br />
ammassi cellulari che sono le cellule del leydig.Il terzo stadio si ha quando questo<br />
non si distingue più,c’è un pattern un po’ sarcomatoide,cellule fusate molto<br />
irregolari.Il secondo stadio è un pattern intermedio.Ovviamente il primo tipo ha una<br />
malignità molto bassa,quasi virtuale,il terzo tipo,invece,ha una malignità molto alta.<br />
1)Meyer I :tubuli ben separati<br />
2)Meyer II :vi riconosciamo dei tubuli,cellule stromali e cellule del leydig,per cui c’è<br />
una certa confusione nell’architettura.<br />
3)Meyer III:pattern sarcomatoide.Non si riconosce più nulla,i tubuli mancano<br />
proprio,ci sono cellule del Leydig e del Sertoli.<br />
TUMORE A CELLULE LIPIDICHE<br />
Mentre il tumore di prima era a cellule del Sertoli e del Leydig,questo è solo a cellule<br />
del Leydig.In genere si chiama anche tumore a cellule lipidiche,perché sono<br />
chiare.E’un tumore che come dice il nome,perché le cellule del leydig sono<br />
localizzate principalmente nel testicolo, producente androgeni per cui dà una<br />
sindrome virilizzante.In ¼ dei casi è maligno.In genere la malignità si basa sulle<br />
dimensioni(7 cm),sulla presenza di aree di necrosi e di emorragie e sulla presenza di<br />
atipie citologiche.<br />
Questo è il caratteristico aspetto morfologico:poiché abbiamo detto che i lipidi se ne<br />
vanno nel normale procedimento di fissazione queste cellule appariranno<br />
chiare.Queste cellule del Leydig a volte hanno dei cristalli che si colorano di<br />
arancione,detti cristalli di Reinke,che è un materiale cristallino.<br />
A proposito della sindrome virilizzante,anche in passato ce n’erano molti di casi.Un<br />
pittore spagnolo,Jusepe de Ribera,venuto a Napoli divenne amico di un certo<br />
Giovanni Azzolino,un boss che abitava sopra i quartieri.Siccome jusepe de Ribera era<br />
basso di statura i napoletani lo chiamavano “lo spagnoletto” .La moglie aveva questa<br />
sindrome ed è ritratta mentre allatta la figlioletta e si vede che ha la barba.Questo li<br />
fece arricchire molto,perché questa donna divenne un specie di fenomeno da<br />
scaricato da www.sunhope.it
araccone e la gente pagava per andare a vederla.Ovviamente non è detto che<br />
questa avesse il tumore a cellule di leydig,ma è probabile,perché è il più virilizzante<br />
di tutti.<br />
GINANDROBLASTOMA<br />
E’un tumore misto comprendente cellule stromali e cellule della<br />
granulosa/tecali.Quindi ha due componenti,una stromale che sarà vimentina<br />
positivo,ma alfa-inibina negativo e una componente a celluele della granulosa/tecali<br />
che sono positive all’a-inibina.<br />
TUMORE DEI CORDONI SESSUALI CON TUBULI ANULARI<br />
E’un tumore strano,non si sa ancora cosa sia.<br />
TUMORI WOLFFIANI<br />
Voi sapete che gli annessi wolffiani sono i residui mesonefrici.<br />
TUMORI NON CLASSIFICATI<br />
TUMORI MISTI<br />
In questi non si capisce niente,perché ci possono essere teratomi,tumori a cellule<br />
stromali insieme a tumori della serie tecale/cellule della granulosa.In questi casi,che<br />
sono rari fortunatamente,per l’aspetto clinico e prognostico bisogna sempre riferirsi<br />
alla componente maggiore.<br />
Il ginandroblastoma vedete è fatto da cellule della granulosa,qui addirittura si<br />
vedono dei follicoli con tutte le cellule intorno e poi accanto ci sono le cellule del<br />
Sertoli;a volte si vede qualche tubulo.Il comportamento di questo<br />
tumore,però,nonostante il disordine è da considerare benigno.<br />
Il tumore con tubuli anulari è molto elegante nella sua strattura;esso è fatto da<br />
insule rotonde,tutt’intorno ci sono le cellule del sertoli e al cnetro ci sono i tubuli che<br />
corrispondono ad una componente a cellule della granulosa,tanto che se andiamo<br />
ad effettuare l’immunoistochimica l’a-inibina risulta positiva soprattutto in queste<br />
aree centrali.Questi sono detti anulari,perché sono dei tubuli abbastanza<br />
regolari.Dato che si tratta di un tumore raro non abbiamo delle casistiche attendibili<br />
per sapere quanto è maligno e quanto benigno,sappiamo solo che in un 20 % dei<br />
casi circa può essere maligno.<br />
scaricato da www.sunhope.it
Il tumore wolffiano è un tumore benigno,fatto da tubuli,cordoni e da stroma fibroso<br />
che in genere è poco rappresentato,non produce ormoni.<br />
TUMORE MULLERIANO MALIGNO<br />
Già l’abbiamo conosciuto parlando dell’endometrio e delgi altri organi genitali.E’un<br />
tumore che si ritiene derivato direttamente dall’epitelio mulleriano e che è capace<br />
quindi di qualsiasi differenziazione,sia in senso mesenchimale che in senso<br />
epiteliale.Qui vediamo delle cellule atipiche,anomale,disposte in strati che sono i<br />
rabdomioblasti tipo rabdomiosarcoma,cioè cellule muscolari striate e a volte si<br />
osserva la presenza di strie all’interno di queste cellule.Se facciamo il metodo<br />
immunoistochimico vediamo che esprimono mioglobina.<br />
Conclusione:quali sono i tumori benigni dell’ovai più frequenti?<br />
• TERATOMA CISTICO BENIGNO: rappresenta più del 50% di tutti i tumori<br />
benigni,in tutte le sue varietà,con denti senza denti,peli,ghiandole sebacee<br />
ecc.<br />
• CISTOADENOMA SIEROSO<br />
• CISTOADENOMA MUCINOSO e così via<br />
Quali sono,invece,i tumori maligni più frequenti?Sono:<br />
• SIEROSI,che da soli rappresentano quasi la metà di tutti i tumori maligni.<br />
• ENDOMETRIOIDI di meno<br />
• I TUMORI STROMALI E DEI CORDONI SESSUALI 7%<br />
• TUMORI A CELULE GERMINALI 6 %<br />
Questa tabella però non ci dice niente in rapporto all’età;se andiamo a vedere l’età al<br />
di sotto dei 30 anni il tumore più frequente è quello a cellule germinali.Dai 30 ai 64<br />
anni i tumori epiteliali maligni e anche dopo i 65 anni.Quindi soltanto in età giovanile<br />
predominano i tumori a cellule germinali e i borderline.<br />
Un altro problema è rappresentato dalla bilateralità,perché spesso si preferisce fare<br />
un intervento di asportazione chirurgica bilaterale.Nei tumori sierosi o misti questa<br />
bilateralità va dal 30 al 40 % e anche nei borderline,nel disgerminoma è del 15 % ,nei<br />
tumori endometrioidi del 20 %.Quindi se ci si trova di fronte ad un tumore epiteliale<br />
scaricato da www.sunhope.it
è opportuno fare un intervento chirurgico bilaterale,perchè anche se all’ecografia<br />
può sembrarci dle tutto normale,possono esserci dei focolai che non si riescono a<br />
vedere,a meno che non si tratti di una donna giovane che voglia avere delle<br />
gravidanze,per cui in questo caso si tiene in osservazione la donna e si opera un solo<br />
ovaio.<br />
METASTASI<br />
Il 7 % delle metastasi ovariche somiglia a tumori primitivi,ma in realtà sono<br />
metastasi,che possono venire dall’apparato gastrointestinale,ma anche dalla<br />
mammella,dall’utero,dal polmone.<br />
C’è un pattern immunoistochimico particolare,noi sappiamo che il Ca ovarico è CK7<br />
positivo e CK20 negativo,se si tratta di metastasi intestinale le proprietà sono<br />
invertite,è negativo alla CK7 e positivo alla citocheratina 20.Nel tumore di<br />
krukenberg,che è una metastasi bilaterale che coinvolge entrambe le ovaie,derivante<br />
molto spesso da un cancro dello stomaco o molto spesso anche di cancro a cellule<br />
ad anello con castone.In questi casi,poiché anche molti tumori ovarici,sierosi o<br />
mucoidi,sono spesso bilaterali non è facile distinguere se sono questi tumori o se si<br />
tratta di metastasi provocate dal tumore di krukenberg,però l’immunoistochimica ci<br />
viene in aiuto in questi casi.Questo è un tumore di krukenberg classico,vedete la<br />
bilateralità dominante,perché quando c’è una bilateralità da tumore ovarico,c’è un<br />
sito più grande ed uno più piccolo dall’altro lato,in questo caso invece sono grandi in<br />
tutti e due i lati.Questo è un tumore a cellule ad anello con castone,vedete il<br />
castone,il citoplasma chiaro e il nucleo schiacciato alla periferia.<br />
Per molto tempo le cellule staminali nell’ovaio sono state un po’ trascurate,perché<br />
l’ovaio è la patria della cellula staminale per eccellenza,che è l’ovocita.Questo ha una<br />
potenzialità notevole,perché fecondato dà origine al corpo umano.Si è visto<br />
comunque che ci sono e in genere stanno sull’epitelio ovarico superficiale,quindi<br />
l’epitelio celomatico nasconde delle cellule staminali che non sono potenti come la<br />
cellula uovo,ma comunque sono in grado di riprodurre tutto l’ovaio.Allora questa<br />
cellula staminale si può differenziare in cellule epiteliali o in cellule germinali e<br />
anche le cellule stromali possono avere delle cellule in grado di differenziarsi in<br />
cellule epiteliali e in cellule germinali.Addirittura si può avere anche un processo di<br />
dedifferenziazione o di trans differenziazione,per cui da una cellula della granulosa<br />
può derivare una cellula staminale.E’possibile quindi anche un processo inverso.<br />
scaricato da www.sunhope.it
CUTE<br />
Le patologie della cute sono numerosissime,tanto che in anatomia patologica si sta<br />
formando un processo di ultraspecializzazione,per cui c’è il dermatopatologo,il<br />
ginecopatologo ecc,perché la patologia cutanea rappresenta un universo proprio a<br />
sé.<br />
Com’è fatta l’epidermide?Epitelio pavimentoso stratificato.Quelli che hanno la vista<br />
migliore distingueranno delle creste;questo è il derma e questi sono i follicoli piliferi<br />
che a volte sono presi in filata,a volte in sezione trasversale.Il cuoio capelluto si<br />
riconosce,perché ha un epitelio molto assottigliato ed è ricco di annessi piliferi,vicino<br />
ai quali ci sono ghiandole sebacee per la lubrificazione del pelo.Sotto l’epidermide<br />
c’è il derma,distinto in superficiale e profondo e poi c’è il sottocutaneo,che si<br />
riconosce per la presenza di tessuto adiposo,che sono questa specie di buchi<br />
chiari,All’interno del tessuto adiposo ci sono delle ghiandoline che sono le ghiandole<br />
sudoripare.Se ci troviamo in un altro distretto il quadro cambia:se non ci sono peli( e<br />
non vuol dire che il soggetto ha perso i capelli,perché comunque i follicoli<br />
rimarrebbero e dipende dal tipo di alopecia che c’è),con uno strato corneo molto<br />
sviluppato,le creste un po’ schiacciate,indice che su di esse viene esercitato un certo<br />
peso,vuol dire che si tratta della piante dei piedi.Anche a questo livello ci sono<br />
ghiandole sebacee,per questo i piedi sudano in estate.<br />
STRATO CORNEO:la patologia dello strato corneo è vastissima.Quando è normale,lo<br />
strato corneo è fatto a canestro di basket,perché presenta delle maglie;poi c’è lo<br />
STRATO GRANULOSO,che è fatto da cellule che hanno dei granuli basofili ed una<br />
cheratoialina iniziale;qui ci sono le PAPILLE DERMICHE ,ovvero delle digitazioni di<br />
derma che si vanno ad approfondire nell’epidermide e queste sono le CRESTE<br />
EPIDERMICHE.A volte succede,per una questione di taglio,che quando il taglio è<br />
trasversale non si vede più questo continuum,ma si vede come un cerchio all’interno<br />
dell’epidermide,che corrisponde ad una papilla dermica solo che è stata tagliata<br />
trasversalmente.Il DERMA SUPERFICIALE che ha una struttura più fine e poi c’è il<br />
DERMA PROFONDO,che ha una struttura più grossolana.In alcune<br />
regioni,soprattutto quelle esposte al sole,ci sono delle cellule chiare,molto spesso in<br />
posizione basale,che corrispondono ai melanociti e a volte si vedono così,perché<br />
sono poveri di pigmento e altre volte sono carichi di pigmento(dipende dalla<br />
carnagione,dall’esposizione al sole ecc.).Queste sono le cellule granulose che stanno<br />
subito sotto lo strato corneo e che contengono granuli basofili.Quest’immagine ci fa<br />
scaricato da www.sunhope.it
capire poi,perché le cellule intermedie o superficiali sono dette spinose,perché<br />
presentano delle spine,come delle cerniere lampo.In quest’altra immagine vediamo<br />
delle ghiandole sudoripare,che sono ghiandole piccole,che in alcuni distretti,come<br />
quello ascellare,hanno una secrezione apocrina.Qui,invece,ci sono ghiandole<br />
sierose,che hanno anche un marcatore topografico,cioè queste ghiandole segnano il<br />
confine tra il derma profondo e il sottocutaneo.<br />
COMPLICANZE DEI TATUAGGI<br />
Sono molto frequenti,perché nonostante il ministero abbia dato delle disposizioni<br />
molto severe,spesso il tatuaggio si improvvisa con conseguenze molto gravi.Questi<br />
tatuaggi possono dare:<br />
• Reazioni allergiche<br />
• Flogosi granulomatose,quindi a cellule giganti<br />
• Cheloidi,sono una forma di cicatrizzazione ipertrofica<br />
• Malattie infettive<br />
• Interferenze e reazioni abnormi durante MRI<br />
• Altre patologie<br />
Addirittura c’è bisogno per farsi il tatuaggio ci compilare un modulo per il consenso<br />
informato.Ci sono tatuaggi fatti con dei minerali che non consentono al soggetto di<br />
poter fare una RM,sia perché il macchinario impazzisce,sia perché possono<br />
comparire delle lesioni nella regione del tatuaggio.Spesso nasce anche il problema di<br />
togliere il tatuaggio,però anche se si può togliere comunque rimane la cicatrice.I<br />
materiali che si usano sono :il cadmio,il potassio dicromato ecc.<br />
Ci sono delle infezioni batteriche frequenti,come quella da micobatteri atipici,per la<br />
scarsa igiene dei tatuatori.Il piercing poi è ancora più frequentemente causa di<br />
infezioni,come quella del mollusco contagioso o infezioni virali,come la verruca<br />
volgare.C’è anche il rischio di epatite e di AIDS.<br />
IMMAGINI:<br />
Qui vediamo una dermatite eczematosa,tale da non consentire più di distinguere il<br />
disegno originale.Qui il disegno si riconosce,sono due serpenti intrecciati<br />
,probabilmente era una coppia un po’ particolare, e il tatuaggio sembra più<br />
scaricato da www.sunhope.it
ello,perché ci sono come delle scaglie che però sono dovute ad una reazione<br />
infiammatoria.Qui c’è una reazione di ipersensibilità ritardata.Qui una reazione<br />
granulomatosa,la quale poi non se ne va.Qui c’è un ascesso da pseudomonas<br />
aeruginosa.I papillomi virali.Qui vediamo una dermatite allergica da<br />
contatto(facendo il patch test e quindi mettendo a contatto la pelle con l’allergene,si<br />
vede che c’è un’ipersensibilità al colorante usato per fare il tatuaggio).Qui si vede un<br />
cheloide e la dermatite lichenoide.<br />
Il piercing è diffusissimo,si calcola che in America oltre il 50% dei giovani ce l’abbia.Il<br />
piercing classico nasce dall’orecchio,oggi però è frequente il piercing all’ombelico<br />
nelle donne e stranamente alla mammella nell’uomo.Al secondo posto c’è il naso e<br />
al terzo la lingua nelle donne,nell’uomo predomina la palpebra e la mammella oltre<br />
che il naso,molto diffuso è il piercing al sopracciglio.Le complicanze dei piercing sono<br />
molto frequenti e le percentuali variano dal 10 al 90 % dei casi.Pososno essere lievi e<br />
gravi,pensate che 1 caso su cento richiede il ricovero ospedaliero.Le complicanze<br />
locali sono :<br />
• dermatite da contatto(dipende dal materiale di cui è fatto,il solfato di<br />
nichel è uno dei più allergenici)<br />
• infiammazioni di vario tipo che possono causare serie<br />
conseguenze,come pericondriti a livello dell’orecchio per estensione del<br />
processo infiammatorio alla cartilagine e che tende poi ad estendersi in<br />
profondità)<br />
• ematomi<br />
• emorragie<br />
• necrosi<br />
• traumatismi con lacerazioni(soprattutto per i piercing e i tatuaggi a<br />
livello dei genitali)<br />
• cheloidi<br />
Complicanze sistemiche:<br />
scaricato da www.sunhope.it<br />
• infezioni:si va dai banali pneumoococchi e streptococchi a epatiti,HIV<br />
ecc.Un problema è rappresentato dalle endocarditi<br />
batteriche,soprattutto perché il piercing determina la presenza di
una porta aperta per la penetrazione di germi e quindi è importante<br />
prendere delle precauzioni,come disinfettare la zona con degli spry<br />
• malattie neurologiche e neuromuscolari<br />
• alterazioni di vario tipo<br />
Le complicanze dipendono anche dalla sede del piercing,quella che più facilmente va<br />
incontro a complicanze è rappresentata dai genitali.Se consideriamo il cavo orale<br />
possono aversi fratture dei denti,salivazione,alitosi,problemi nel parlare e nel<br />
masticare,problemi nella respirazione e nella digestione,emorragie,recessioni<br />
gengivali.<br />
Quali sono i materiali più sensibilizzanti?sono iI solfato di<br />
Nichel,cobalto,palladio,oro,argento,mentre il niobio e l’ossido di titanio sono meno<br />
sensibilizzanti e più costosi.<br />
IMMAGINI:<br />
Qui vediamo un’infiammazione della lingua,si vede che c’è una gengivite serie con<br />
una retrazione gengivale.Qui c’è una lacerazione.Qui vediamo infezioni di vario tipo e<br />
poi i cheloidi.La crescita dei cheloidi dipende dalle ciclossigenasi,questi sono dati<br />
recentissimi.Il cheloide è imprevedibile.Dopo un intervento chirurgico possono<br />
aversi due patologie:1) il cheloide che va al di là dei confini della cicatrice 2)la<br />
cicatrice ipertrofica che per definizione rimane a livello della cicatrice solo che c’è<br />
una reazione esuberante.<br />
Qui vediamo un granuloma piogenico che è un tumore vascolare.Il granuloma si<br />
forma ogni volta che c’è del materiale estraneo non eliminabile attraverso i<br />
macrofagi,per cui si devono formare queste celule complesse,giganti per cercare di<br />
circoscrivere questa invasione di materiale estraneo.L’unico problema del<br />
granuloma è che essendo una forma di resistenza circoscritta diventa poco sensibile<br />
alla terapia,è difficile che un farmaco riesca a penetrarvi e si crea un meccanismo di<br />
self perpetuation.<br />
scaricato da www.sunhope.it
I TUMORI DELLA CUTE<br />
volendo fare uno schema didattico utile, possiamo avere che l'inquadramento nosologico classico dei<br />
tumori del acute, di cui parleremo solo in piccola parte poiché, vi assicuro, ci sono tumori della cute<br />
veramente sconvolgenti, sconvolgenti per la diversità, per la complessità. Pensate, che solo il pelo (le<br />
strutture pilo-sebacee) hanno centinaia di tumori.<br />
diciamo squamosi quei cancri che somigliano alle cellule squamose: le caratteristiche base di una cellula<br />
squamosa sono, come voi sapete, un grande citoplasma eosinofilo e la tendenza a cheratinizzare come le<br />
cellule squamose più mature.<br />
Diciamo baso-cellulare di quei cancri che somigliano alle cellule baso cellulari: le caratteristiche base di<br />
queste cellule sono che hanno uno scarso citoplasma che non tende a maturare in senso acidofilo e non<br />
tende a cheratinizzare.<br />
poi abbiamo i melanomi che hanno le caratteristiche della loro controparte normale, cioè i melanociti. Sono<br />
delle neoplasie di grande attualità la cui tendenza è in aumento in riguardo alle quali c'è sempre stato un<br />
certo allarme sociale (nel medioevo uno dei segni della diavoleria era la presenza dei nevi in particolari<br />
posizioni) . I nevi si manifestano fino all'età di cinquant'anni e seguono molto spesso uno sviluppo<br />
metamerico.<br />
Poi abbiamo quei tumori che hanno una differenziazione sebacea: le ghiandole sebacee sono annessi ai<br />
follicoli piliferi, hanno la funzione di lubrificare il pelo<br />
abbiamo poi dei tumori della serie follicolare: ovvero del follicolo pilifero cioè proprio dal pelo<br />
e poi abbiamo tumori della serie eccrina ed apocrina perché in alcune parti del corpo umano queste<br />
ghiandole eccrine diventano apocrine per esempio a livello mammario, ascellare; apocrina significa che<br />
hanno un tipo di secrezione diversa da quelle eccrina.<br />
carcinoma epitelioma baso cellulare<br />
questo è quello più diffuso e, badate bene non è contemplato neanche nelle tabelle di incidenza della<br />
organizzazione mondiale della sanità, perché se lo contemplassimo è il tumore che sta al primo posto come<br />
incidenza. hanno un'incidenza altissima(407mila/anno) . È un tumore che, soprattutto dopo una certa età<br />
(sessant'anni) è difficile non averlo. c'è una leggera prevalenza nei maschi (e quasi il doppio) e, nella sesta<br />
decade poiché risente molto della esposizione ai raggi uV tant'è vero che nei paesi tropicali l'età di massima<br />
incidenza è più bassa, risente anche di particolari occasioni professionali che hanno a che fare con la<br />
cancerogenesi cutanea, per esempio i lavoratori addetti alla lavorazione delle strade che usano la pece e<br />
altre strumentazioni vanno più soggetti rispetto alla popolazione generale a questo tipo di neoplasia. Le<br />
sedi più frequenti sono il volto e le mani, badate bene, non la faccia dorsale delle mani, il collo, il tronco, le<br />
estremità, altre volte genitali esterni, il dotto lacrimale (ma questi ultimi sono molto rari). Le parti più<br />
colpite, genericamente, sono le parti più esposte al sole. Dal punto di vista anatomopatologico questo è un<br />
cancro, ma vi dico che io non uso mai la dizione "carcinoma baso cellulare" poiché spaventa le persone, uso<br />
sempre la dizione "epitelioma baso cellulare” poiché questo cancro ha un tasso di metastatizzazione che si<br />
avvicina allo 0%.l'unico problema è che ci sono alcune forme aggressive che tendono recidivare o<br />
comunque forme destruenti soprattutto a livello del volto. quindi possiamo parlare di una aggressività o<br />
invasività locale ma non possiamo parlare di una invasività a distanza. Il carcinoma baso cellulare o<br />
epitelioma è l'unico caso in cui se i margini chirurgici di escissione non sono indenni in genere, non si fa<br />
scaricato da www.sunhope.it
nulla poiché si da per scontato che non ci sia il rischio di metastasi, pensate come sia ottimistico<br />
l'atteggiamento nei riguardi di questo tumore. Queste sono le varietà più frequenti di questo tumore:<br />
1) forma nodulare ulcerativa: cioè che si presenta come un'ulcerazione, vedete che più della metà dei casi e<br />
così. La forma infiltrante morfeiforme(?) cioè che tende ad infiltrare il connettivo sottostante attraverso<br />
trabecole, attraverso dei gettoni molto ristretti di cellule che si vedono a livello cutaneo poiché la cute si<br />
rileva. vi è una forma superficiale multifocale che pure è frequente la quale tende ad estendersi in<br />
superficie ma non tende ad andare in profondità, quindi si diffonde un po' a macchia d'olio in una certa<br />
area.<br />
La forma che più presenta dei problemi è la forma 2)cosiddetta pigmentata: è problematica poiché simula<br />
un melanoma. Quindi l'epitelioma baso cellulare pigmentato presenta dei problemi di diagnosi differenziale<br />
(io vi parlerò solo di alcuni problemi di non concordanza fra diagnosi istologica e diagnosi in dermoscopica,<br />
che poi sono problemi seri, poiché una cosa è un epitelioma baso cellulare un'altra è un melanoma, è come<br />
una formica nei riguardi di un elefante riguardo alla malignità) e poi altre forme rare di cui non parleremo.<br />
come può apparire? Può apparire a volte rilevato (forma più rara), più frequentemente è una forma appena<br />
escavata o più escavata. Alcune sedi tipiche sono a livello palpebrale o addirittura può apparire una forma<br />
molto escavata (angolo dell'occhio, tra il naso è l'occhio).<br />
Altre volte abbiamo la lesione pigmentata, molto frequente al volto. altre volte invece abbiamo delle<br />
forme non pigmentate, quasi eritematose.<br />
Qual è l'aspetto classico di un epitelioma baso cellulare? Somigliano proprio alle cellule basali cioè sono<br />
relativamente piccole, hanno uno scarso citoplasma, tant'è vero che a volte non si coglie la diversità fra le<br />
diverse cellule che sembrano accollate l'una sull'altra, un'altra caratteristica di base è la tendenza delle<br />
cellule in periferia di disporsi a palizzata come succede nell'epitelio normale: le cellule baso cellulari sono<br />
disposte perpendicolarmente rispetto alla membrana basale e parallelamente fra di loro.<br />
Questa è la forma classica (immagine).<br />
Questa è la forma pigmentata (immagine) in cui c’è del pigmento, però questo pigmento non deriva dalle<br />
cellule basali che non sono in grado di produrne ma dai melanociti che reagiscono, formano più pigmento ,<br />
questo viene raccolto da cellule macrofagiche chiamate melanofagi che si intramettono nella struttura del<br />
tumore, per cui anche macroscopicamente anche il dermatologo ha la percezione di una lesione<br />
pigmentata.<br />
Questa è la forma morfeiforme (immagine) , vedete anziché essere fatta da grossi gettoni è fatta da piccoli<br />
gettoni che s'infiltrano nel tessuto connettivale e lo dissociano. In genere queste sono le forme che vanno<br />
più in profondità, ma vi ripeto il problema è relativo, poiché, come vi ho detto, si tratta di un cancro che<br />
soltanto in situazioni eccezionali può dare metastasi.<br />
Ecco quello superficiale (immagine) vedete, qui si capisce proprio bene: questo è un epitelio normale, si<br />
forma questa proliferazione di cellule basali diciamo, è un epitelioma baso cellulare "in culla", mantiene<br />
ancora i suoi rapporti con le epitelio ed è caratteristica anche questa retrazione che ha rispetto al connettivo<br />
perché legato proprio alla “pressione”, alla crescita per cui si distacca il connettivo. Talvolta si forma come<br />
una bolla.<br />
scaricato da www.sunhope.it
Questo è multicentrico, vedete tanti piccoli epiteliomi baso cellulari si diffondono uno a fianco all'altro, o<br />
anche a distanza.<br />
questo è un carcinoma molto raro e particolare (immagine), è un carcinoma baso-squamoso. a un occhio<br />
esperto non sfuggirà che questa cellula avrà una tendenza ad essere baso cellulare (vedete come le cellule<br />
tendono a disporsi a palizzata nella periferia) mentre questi altre cellule qui, vedete hanno un citoplasma<br />
più grande, hanno degli ampi nucleoli ed hanno una tendenza a cheratinizzare, quindi va più verso il<br />
carcinoma squamoso. Quindi la coesistenza di cellule atipiche baso cellulari e cellule atipiche di tipo<br />
squamoso far sì che questo cancro si chiami baso-squamoso o meta tipico. Da un punto di vista prognostico<br />
questo cancro si comporta, come è da attendersi, in una maniera intermedia tra l'epitelioma baso cellulare<br />
e il carcinoma squamoso che ovviamente ha una maggiore tendenza a metastatizzare.<br />
La cheratosi seborroica è diffusissima, una volta veniva correlata alla seborrea che è anch'essa molto<br />
diffusa ma con la quale non ha niente a che vedere, oggi è considerato un tumore benigno. La cheratosi<br />
seborroica molto spesso ha manifestazioni multiple, si tratta quasi sempre di manifestazioni rilevate e<br />
cheratinizzante. Anch'essa può essere pigmentata(e questo è un altro problema) però in genere e molto<br />
elevata, ha degli aspetti un po' a cavolfiore alcune volte e molto spesso si manifesta al volto, al torace e al<br />
dorso. Talvolta quando le manifestazioni sono multiple rientra in una sindrome particolare chiamata di<br />
Lesier-trelà(?) che è una sindrome para neoplastica , ovvero è una di quelle dermatosi fatta da tanti tumori<br />
benigni che nasconde un cancro profondo; quindi se una persona vede che c'è uno sviluppo di molte<br />
cheratosi seborroiche bisogna pensare che questa persona possa avere un cancro, sia pure occulto. La<br />
caratteristica essenziale di questa neoplasia benigna è che presenta queste strutture, vedete (immagine)<br />
chiamate impropriamente cisti cornee. In effetti queste non sono cisti cornee, appaiono come tali ma sono<br />
delle invaginazioni cornee. Se l’ epitelio di superficie subisce un processo di invaginazione con tutto il<br />
materiale corneo, se viene tagliato di trasverso avremo questa immagine così (immagine). Mentre qui<br />
vedete (immagine) una invaginazione che si sta formando. Quindi si forma un avvallamento che si<br />
approfondisce con il tempo e quando noi la andremo a tagliare ci sembra una cisti cornea. Poi c'è una<br />
proliferazione di cellule intermedie, cioè di quelle cellule che non sono proprio squamose mature ma non<br />
sono neppure para basali, quindi a differenziazione intermedia. ecco, questa (immagine) è una<br />
invaginazione cornea che appare in tutto e per tutto come una cisti cornea, da non confondere con le perle<br />
cornee che vedremo fra poco che sono del carcinoma squamoso. Ecco l'aspetto di queste cellule: vedete<br />
sono celluline con un po' di citoplasma che non sono proprio le squamose differenziate ma non sono<br />
neanche le baso cellulari.<br />
Questa è la forma pigmentata , quindi la cheratosi seborroica pigmentata (immagine) e questa è la forma<br />
ipertrofica (immagine) anche qui vedete le invaginazioni cornee che sono una caratteristica di questa<br />
neoplasia e ci può essere anche la pigmentazione in alcune aree, e addirittura ci sta anche l’ infiammazione<br />
superficiale poiché a volte, quando queste lesioni sono grosse danno luogo ad un fenomeno di<br />
impetiginizzazione poiché la persona si gratta e grattandosi, ovviamente c'è una sopra infezione in genere è<br />
sostenuta da cocchi.<br />
La cheratosi attinica è anch'essa frequentissima. Queste lesioni possono avere un aspetto superficiale, o un<br />
po' ulcerato. È caratteristica dell'età più avanzata, è caratteristica delle persone che si espongono<br />
facilmente al sole, la sede più tipica è il volto. questa è considerata una precancerosi, quindi il rischio di<br />
carcinoma squamoso c'è. Spesso bisogna stare attenti perché queste cheratosi attinica nella metà dei casi è<br />
associata ad epitelioma baso cellulare in un'altra sede adiacente o, in una minoranza dei casi a carcinoma<br />
squamoso. Quindi può coesistere con un epitelioma baso cellulare o può essere un indicatore di rischio per<br />
scaricato da www.sunhope.it
l'insorgenza di un carcinoma metacrono, quindi a distanza di tempo, nello stesso soggetto. Questa è una<br />
degenerazione da raggi ultravioletti del collagene, perché vedete che il collagene, che normalmente deve<br />
avere un aspetto più acidofilo, diventa basofilo; quindi una degenerazione basofila del collagene che<br />
coinvolge anche le fibre elastiche che sono distrutte. E poi, anziché avere un andamento fusato ondulante<br />
com'è nel derma, tende a formare degli ammassi omogenei. Vediamo quindi degli ammassi omogenei di<br />
sostanza basofila che è legata alla colliquazione del connettivo ormai degenerato. Il problema è che<br />
l'epitelio di superficie mostra delle atipie cellulari (tecnicamente sono delle displasie) il che ci fa capire come<br />
poi questa possa essere una precancerosi. Vedete l'epitelio come poi tende pure all'atrofia nella maggior<br />
parte dei casi, in altri casi invece reagisce con una iperplasia molto violenta. Vedete che ci sono delle atipie<br />
strutturali notevoli che sono previste nel quadro della cheratosi attinica. Questa è una delle precancerosi<br />
più classiche del cancro squamoso<br />
il cheratoacantoma che è anch'esso molto diffuso, si chiama così poiché ha un aspetto crateriforme.<br />
Vedete è un cratere con un'ulcerazione dove a volte si raccoglie materiale corneo. I nostri testi classici,<br />
spesso sono stati in contrasto su come inquadrare questo cheratoacantoma e nel definire rapporti che<br />
questo avesse con il carcinoma squamoso, dopo molto penare su questo argomento si è capito che il<br />
cheratoacantoma è una forma di carcinoma squamoso di basso grado. Qual è la sua caratteristica biologica?<br />
È un cratere dove c'è una proliferazione papillariforme e sono caratteristici i margini, che vengono descritti<br />
in questo tumore come "a becco di clarino" vedete i margini sono netti perciò questo è un carcinoma<br />
squamoso ma di bassissimo livello, ci sono delle atipie strutturali.<br />
Veniamo al carcinoma squamoso: la forma iniziale (che può rimanere anche così) è il carcinoma in situ. Il<br />
carcinoma in situ squamoso della cute può essere anche multicentrico soprattutto in determinate categorie<br />
di lavoratori professionali. La sua sede più caratteristica è nelle regioni esposte al sole, ma anche nelle aree<br />
genitali e anali. Può assumere vari aspetti: un aspetto più eritematoso o un aspetto più caratterizzato da<br />
croste e cheratinizzazione, tende molto spesso a recidivare , in effetti non si tratta di una recidiva legata ad<br />
un'incompleta asportazione, si tratta di una recidiva biologica perché è un po' tutto il comparto, tutta<br />
quell'area, che ha questa tendenza all'instabilità genetica e quindi si possono riformare varie aree di<br />
carcinoma in situ. La progressione è prevista verso il carcinoma invasivo in circa l'8-10% dei casi. Anche<br />
questa quindi la possiamo considerare una precancerosi.<br />
Ecco l'aspetto caratteristico (immagine) Voi vedete che in questo epitelio c'è un atipia diffusa strutturale,<br />
anche citologica (vedete questi nuclei iper cromici), non c'è più una tendenza a maturare dall'epitelio baso<br />
cellulare, alle cellule sopra basali, alle cellule cheratiniche ma vedete anche che la membrana basale non è<br />
mai superata. Così come in questo caso (immagine) si è formata anche una reazione linfocitaria che è un<br />
tentativo quasi di opporsi a questa anomalia cellulare. Qui vediamo (immagine) come le cellule non hanno<br />
più tendenza a maturare, ma non c'è più differenza fra lo strato basale e lo strato superficiale. Qui<br />
(immagine) notiamo la tendenza alla para cheratosi (cioè la presenza di nuclei nelle cellule cornee), ma<br />
siccome in nessun punto è superata la membrana basale questo, tecnicamente non è cancro poiché è in<br />
situ.<br />
il carcinoma squamoso e invece è un cancro che qualche problema lo da. Le sedi più esposte sono volto,<br />
mani e anche le braccia, raramente al piede. L'incidenza e di 81-136 per 100 mila casi all'anno, è molto<br />
inferiore nelle donne. Questo tipo di cancro tende a recidivare e tende a dare metastasi, ovviamente vi sono<br />
delle sedi in cui è più frequente la metastatizzazione , per esempio l'orecchio e il labbro. L'orecchio è la sede<br />
più frequente nella quale vengono ritrovati questi epiteliomi siano essi squamosi o baso cellulari perché<br />
questa è una delle aree cui uno non si mette mai la crema protettiva. Un'aggravante del suo<br />
scaricato da www.sunhope.it
comportamento biologico e la presenza di ulcerazione e cheratinizzazione, aggravante nel senso che è<br />
correlata ad un maggior rischio di metastasi. Può insorgere anche dopo radio terapia, ustioni e traumi. Quali<br />
sono i fattori prognostici? 1)La sede abbiamo già visto che orecchio e labbra sono sedi sfavorevoli 2) il livello<br />
di invasione, cioè dove è arrivato in profondità 3) il grading (forme ben differenziate, forme<br />
indifferenziate...) 4) le dimensioni, più grandi sono e più hanno un potenziale di malignità 5) la tendenza ad<br />
aree di ulcerazione.<br />
Come appare? Vedete (immagine) questo è un carcinoma squamoso in fase iniziale: vediamo questi gettoni,<br />
questo gettone che sta più in qua e cogliete la tendenza all'invasività, ovviamente è un invasività<br />
superficiale, non va in profondità. una caratteristica di questi cancri è la presenza di queste strutture, che<br />
non sono cisti cornee ma perle cornee. La perla cornea ha un andamento concentrico , però all'interno<br />
riconosciamo di nuclei atipici. Riconosciamo in altre parole delle cellule cornee paracheratosiche. Questa<br />
caratteristica delle perle cornee si vede solo nei carcinomi ben differenziati. Qui vedete (immagine) un<br />
carcinoma meno differenziato, vedete la tendenza alla cheratinizzazione che però non si esprime attraverso<br />
una perla cornea ma attraverso un lago di materiale cheratino-simile molto irregolare, e qui vedete in alto<br />
una figura mitotica molto asimmetrica e molto atipica, vedete pure delle atipie citologiche come vedete<br />
pure che queste cellule hanno il citoplasma acidofilo il che è dovuto proprio alla tendenza a cheratinizzare.<br />
Talvolta il carcinoma squamoso tende ad assumere degli aspetti a cellule fusate. Noi abbiamo la conferma<br />
che si tratti di carcinoma squamoso attraverso l’immunoistochimica con la citocheratina ed altri marcatori<br />
della serie epiteliale e poi confrontiamo con altri marcatori della serie mesenchimale. Quindi questo, per<br />
essere carcinoma deve esprimere i marcatori della serie epiteliale.<br />
anche qui c'è la malattia di bagè (?) extramammaria (?). Dove viene a livello cutaneo? Viene soprattutto<br />
nella cute adiacente le regioni ano-genitali perché lì vi sono delle ghiandole, il meccanismo è lo stesso, per<br />
cui molto spesso questa malattia di bagè e legata alla presenza di adenocarcinoma al di sotto, per cui c'è<br />
questa migrazione di queste cellule epiteliali.<br />
il carcinoma neuroendocrino o tumore di meckel (?) è un tumore tutt'ora un po' sconosciuto. viene<br />
difficilmente diagnosticato e in vari casi questa patologia ha una storia di diagnosi errate alle spalle.<br />
L'incidenza è molto bassa (0,23 / 100.000 all'anno). Sedi preferenziali sono alla regione della testa del collo<br />
e delle estremità. Recidiva nel 40% dei casi e tende a dare metastasi a fegato, ossa e polmoni. la<br />
sopravvivenza media si attesta 55% a tre anni. nella prognosi rientrano le alterazioni citologiche, le mitosi,<br />
l'istotipo e la necrosi. i carcinomi che hanno una peggiore prognosi sono i microcitomi e quelli a grandi<br />
cellule atipiche, ovviamente questi istotipi sono quelli che hanno la prognosi peggiore. La sua tendenza è<br />
quella di dare noduli satelliti, quindi viene rimosso un modulo e se ne riforma un altro a breve distanza<br />
spaziale. Alla microscopia può simulare quasi un linfoma a volte può avere un aspetto trabecolare,<br />
raramente al livello cutaneo assume un aspetto tubulare. Ovviamente esistono delle caratteristiche<br />
istologiche e di immunoistochimica che ci consentono di fare agevolmente la diagnosi. La prima<br />
caratteristica sono i nuclei ad aspetto “sale e pepe” per cui il nucleo sembra una commistione di zone chiare<br />
e zone scure. I marcatori positivi sono la cromogranina e la enolasi.<br />
veniamo adesso alle lesioni melanocitarie:<br />
come considerare queste lesioni (lentiggine, nevo) tecnicamente? È un tumore benigno? Non si comporta<br />
come un tumore benigno. Un amartoma? è una semplice iperplasia? Sono quesiti a cui io non so dare una<br />
risposta ma credo che nessuno sappia darne, probabilmente non sono neanche tumore considerando anche<br />
scaricato da www.sunhope.it
il fatto che si sviluppano continuamente, nevi che sorgono fino all'età di cinquant'anni sono normali, tutto<br />
ciò che viene dopo 55 anni va guardato con un certo sospetto.<br />
La lentiggine è una lesione molto diffusa, che è solo un'area di iper pigmentazione. può essere legata ad<br />
un'iperplasia delle cellule melanocitarie o anche, non ad un'iperplasia ma ad una iperfunzione delle cellule<br />
melanocitarie. Ovviamente i portatori di queste lesioni sono dei soggetti predisposti che hanno una pelle<br />
lentigginosa<br />
I nevi si distinguono in nevi melanocitari comuni e nevi melanocitarie particolari. i nevi melanocitari<br />
comuni si dividono in nevo giunzionale, nevo intra dermico e nevo composto.<br />
il nevo giunzionale e poco rilevato e molto superficiale, mano a mano che diventa composto e poi solo intra<br />
dermico allora tende a rilevarsi, a volte può essere molto rilevato fino ad assumere una forma polipoide.<br />
Fra i nevi melanocitari particolari parleremo del nevo blu, il nevo con alone, il nevo di Spitz che è un nevo<br />
in genere o non pigmentato o poco pigmentato, la sua variante pigmentata si chiama nevo di Rid ed è<br />
chiamato anche melanoma giovanile e poi il nevo congenito ovvero che alla nascita è già presente.<br />
La lentigo<br />
è un aumento della pigmentazione, il numero dei melanociti (che si distinguono in genere perché hanno<br />
questo alone chiaro) non è che sia molto aumentato<br />
i nevi comuni<br />
il nevo giunzionale ha questo aspetto qui (immagine), il nevo composito ha questo aspetto qui (immagine),<br />
il nevo intra dermico invece tende a rilevarsi poiché si forma nel derma e spinge in alto formando un rilievo<br />
sulla cute. Quando invece è un nevo composto, vedete che ha un aspetto rilevato che è legato alla<br />
componente intra dermica e un aspetto non rilevato che è legato alla componente giunzionale (non capisco<br />
se dice giunzionale o funzionale), più diventa intra dermico e più si rileva.<br />
ecco il nevo comune<br />
(immagine) il nevo comune giunzionale: qui vedete le teche, cosa sono le teche? Le teche sono delle<br />
raccolte di melanociti che si formano a livello della giunzione epiteliale dermica, vedete che c'è una<br />
iperplasia delle cellule melanocitarie e c'è anche una pigmentazione. Si capisce già da questa immagine che<br />
questi melanociti, cellule che si dispongono in questa teca, non hanno una disposizione affastellata,<br />
irregolare, ma c'è un divenire quasi ordinato fra di loro, si capisce da questo che è un nevo benigno.<br />
questo è il nevo composto (immagine): in linea di massima il nevo nasce giunzionale poi diventa composto<br />
Perché oltre alle teche esiste una componente intra dermica, quindi a una componente giunzionale e una<br />
componente intra dermica. Ovviamente nel nevo giunzionale c'è anche l'attivazione dei melanociti,<br />
un'iperplasia lentigginosa cioè tutto l'epitelio partecipa al nevo. Anche nel nevo composto, vedete qui tutte<br />
queste cellule chiare,tendono ad aumentare<br />
il nevo intra dermico invece, nell’ epitelio non c'è più quell'attivazione, la componente melanocitaria è solo<br />
intra dermica, non c'è più la componente giunzionale. molto spesso questo nevo comune può presentare<br />
una dinamica sequenziale ovvero prima è un nevo giunzionale poi diventa composito e poi intra dermico.<br />
Non sempre così, a volte possiamo avere un nevo che nasce all'inizio come un nevo intra dermico.<br />
scaricato da www.sunhope.it
Il nevo giunzionale è quello che presenta più problemi dermoscopici perché è il nevo più attivo, è un nevo<br />
giovanile che può presentare delle irregolarità di pigmentazione ma è benigno<br />
il nevo blu, come dice il termine è di un caratteristico blu intenso, questo blu intenso è legato ad un<br />
caratteristico effetto Tindall, perché il pigmento in questo nevo è profondo perché le cellule melanocitarie<br />
sono nel derma profondo. Così per un effetto di passaggio attraverso i vari strati cutanei si ha questo<br />
colorito che dovrebbe essere marroncino e invece diventa blu. Vedete che le cellule neviche sono molto<br />
pigmentate, sono fusate (nel nevo blu) e vedete che nell'epidermide non c'è niente, stanno sotto e sono<br />
ricche di pigmento questo da l’aspetto blu al nevo.<br />
il nevo con alone è un nevo che tutto intorno presenta un alone chiaro. Questo alone chiaro è legato ad una<br />
spiccata reazione infiammatoria, non sappiamo perché questa si verifichi. Questo nevo ci pone dei problemi<br />
diagnostici notevoli, perché paradossalmente nel melanoma, laddove ci sono dei fenomeni regressivi, cioè<br />
infiammatori che tendono addirittura a ridurre la superficie del melanoma( a lungo andare questa superficie<br />
del nevo si riduce poiché prevale l'infiammazione) nel melanoma questi fenomeni regressivi hanno un<br />
significato prognostico molto negativo poiché se da un lato questa componente infiammatoria favorisce la<br />
risoluzione locale dall'altro facilita la mobilizzazione delle cellule cancerose e quindi la metastatizzazione,<br />
vedete come un evento che in altri casi verrebbe considerato come positivo in questo viene considerato<br />
molto negativo<br />
il nevo di Spitz: è un nevo molto spesso dei bambini e dei giovani anche se si può manifestare a 30,40 anni e<br />
più. Molto spesso non è pigmentato quando è pigmentato presenta dei problemi perché se seguiamo i<br />
criteri classici ABCDE questo ci entra, poiché presenta delle irregolarità nella pigmentazione, presenta dei<br />
margini irregolari, presenta anche delle dimensioni particolari presenta anche un certo sviluppo evolutivo,<br />
tende ad accrescersi. A livello istologico ritroviamo delle atipie molto spesso questo nevo è fatto da grandi<br />
cellule epitelioidee talvolta con atipie. La cellula gigante, fa parte del neo si chiama cellula di Tuton (?). Il<br />
nevo di Spitz presenta anche delle asimmetrie (fondamentale per la diagnosi differenziale con il melanoma<br />
dal punto di vista dermoscopico dal punto di vista istologico) in effetti una lesione benigna Tende ad avere<br />
una certa simmetria. Qui ù, guardate questi corpi acidofili (immagine) nello spessore dell'epitelio, questi<br />
corpi pedofili si chiamano corpi del CAMINO, sono segno di una avvenuta necrosi apoptoica per cui non c'è<br />
più il nucleo, sono degli inclusi eosinofili caratteristici, però la diagnostica è molto più complessa. Questo<br />
nevo sembra molto un melanoma: hA caratteri del melanoma fra cui l'invasione dell'epitelio, non trovate<br />
più lo strato basale, sembra che abbia quasi un atteggiamento invasivo e addirittura degli aspetti pagetoidi<br />
che rientrano però nel quadro di nevo di Spitz. D'altra parte l'età non è un criterio sufficiente per escludere<br />
il melanoma poiché stiamo osservando melanomi anche nei giovani. Questa è una diagnosi molto<br />
impegnativa.<br />
il nevo congenito presenta una caratteristica che a volte ci permette di dire che è congenito anche se il<br />
clinico dice che non lo è e la paziente non se lo ricorda (cosa che succede spesso): il nevo congenito<br />
presenta delle atipie che non presenta il nevo acquisito ovvero il nevo comune. La caratteristica che<br />
distingue il nevo congenito, quella più importante, è che le cellule neviche , a differenza di quelle del nevo<br />
comune acquisito, seguono anche gli annessi pilo sebacei. Ritroviamo l'annesso pilifero circondato da<br />
queste cellule chiare che sono cellule neviche, e quindi non ci spaventiamo. (Esiste però anche il melanoma<br />
su un nevo congenito) Il nevo congenito può assumere anche varie dimensioni: ovviamente più grande è il<br />
nevo maggiore il rischio di poter osservare il melanoma.<br />
il nevo displastico è stato una novità di 20 anni fa. In un primo tempo si credeva che esistesse una sindrome<br />
del nevo displastico, e in effetti esistevano famiglie che avevano una certa tendenza su basi genetiche ad<br />
scaricato da www.sunhope.it
avere dei melanomi e quindi rientrava in una sindrome chiamata di clark (?). Presenta dei caratteri molto<br />
sovrapponibili a quelli del melanoma se seguiamo i criteri ABCDE. Questi sono pazienti vanno osservati e<br />
sottoposti ad un follow-up intensivo, spesso questi pazienti sono affetti da molti nevi displastici e il<br />
dermatologo decide quale togliere in base all'aspetto. Quali sono i criteri per dire che quel nevo è un nevo<br />
displastico: innanzitutto la asimmetria , cioè come se fossero melanoma, tendenza a dare degli aspetti<br />
pagetoidi, una tendenza delle teche a fondersi fra di loro, all'interno di queste teche c'è anche una certa<br />
irregolarità nella disposizione, c'è anche una reazione linfocitaria che pure un segno molto sospetto che a<br />
parte il nevo con alone, la presenza di infiltrati linfocitari, adiacente alla popolazione melanocitaria è in<br />
genere più una Caratteristica del melanoma. Quindi coalescenza e asimmetria poi una iperplasia<br />
lentigginosa esplosiva. a parte queste teche coalescenti vedete queste cellule melanocitarie aumentano di<br />
numero (iperplasia).<br />
I melanomi: sono<br />
il melanoma in situ che può avere una fase di crescita orizzontale, in cui o non è invasivo o è poco invasivo e<br />
una fase di crescita verticale. queste fasi possono essere susseguenti ma abbiamo anche dei melanomi che<br />
nascono con una fase di crescita già verticale ma nella maggior parte dei casi va avanti la dinamica per fasi.<br />
Questo significa che se noi prendiamo il melanoma prima che è cominciato una fase di crescita verticale noi<br />
avremo buone speranze di risolvere il problema.<br />
I marker del melanoma: non solo per capire se la lesione neoplastica è melanocitaria o no, ma è molto utile<br />
anche per capire se è un nevo displastico o melanoma…i marker comunque sono il MELAN-A E L’hm3 45<br />
(??) sono quelli più vecchi e più utilizzati poi abbiamo il CD 63 E LE TIROSINASI. Questi marcatori ci<br />
consentono non solo di capire se una lesione è melanocitaria o no ma ci consentono, studiando la loro<br />
distribuzione nella lesione melanocitaria, di capire se si tratta di lesioni tendenzialmente benigne o maligne,<br />
in altre parole, questi marcatori si distribuiscono solo nella parte superficiale se siamo davanti ad un nevo<br />
(benigno). Perché questo avviene? Perché in genere nel nevo, a dimostrazione del fatto che il nevo è di<br />
origine neuro-ectodermica, andando verso il basso le cellule tendono diventare più piccole ed acquisire un<br />
fenotipo più neuro-epitaliale anziché melanocitario, tendono ad un fenomeno di neurotizzazione cioè a<br />
diventare cellule nervose. Se andiamo verso il basso vedete questa tendenza alla maturazione nel senso più<br />
propriamente nervoso, questo è un segno di benignità, questo spiega perché alcuni marcatori li troviamo<br />
sopra e non li troviamo sotto. un segno di malignità importante è trovare le figure mitotiche, magari<br />
atipiche (che noi andiamo a cercare nei casi dubbi).<br />
quali sono le principali varietà?<br />
1)il melanoma in situ<br />
2)la lentigo maligna (che può essere in situ o lentigo maligna melanoma quando già ha avuto una crescita<br />
in senso verticale) la lentigo maligna è una forma molto diffusa negli anziani per cui c'è una pigmentazione<br />
che è atipica. La lentigo maligna corrisponde ad un melanoma in situ particolare. Quando invece è lentigo<br />
maligna melanoma c'è già la fase di crescita verticale.<br />
3) melanoma a diffusione superficiale: è il più frequente e si chiama a diffusione superficiale perché tende<br />
ad avere comunque un pattern pagetoide, però se è in fase di crescita verticale mostra l'uno e l’altro cioè il<br />
pattern di crescita intra epidermico ed anche la componente che va in profondità. Questo melanoma<br />
rappresenta il 60-70% di tutti i melanomi<br />
scaricato da www.sunhope.it
4) poi abbiamo il melanoma nodulare che è la forma più maligna di melanoma perché addirittura l'epitelio<br />
non mostra più alcun segno di alterazione,corrisponde a quello che è il nevo intra dermico, per cui questi<br />
nuclei maligni stanno all'interno, in superficie non si vede più niente, nasce proprio così.<br />
5) e poi abbiamo il cosiddetto melanoma acrale lentigginoso (acrale vuol dire che la periferia è molto<br />
interessata, anche la pianta del piede per esempio, c'è un nevo particolare chiamato anche nevo plantare di<br />
cui non vi ho parlato perché il nevo plantare a furia di camminarci sopra sviluppa delle atipie e mette a dura<br />
prova l'esperienza dell'anatomopatologo, ho visto dei casi di nevo plantare diagnosticati come melanoma).<br />
Si chiama melanoma acrale LENTIGGINOSO perché si associa anche ad un pattern è lentigginoso.<br />
Questo è il melanoma in situ (immagine) : tutte cellule atipiche, vedete però sono confinate nello spessore<br />
dell'epitelio.<br />
La lentigo maligna (immagine): questa non è ancora melanoma, c'è una iperplasia lentigginosa, molto<br />
spesso è una lesione del volto di cellule pigmentate e non pigmentate e c'è un continuum, cosa che non si<br />
verifica nell'iperplasia lentigginosa, vedete tutte queste cellule tendenzialmente fusate che rivestono<br />
l'epitelio, però non c'è superamento e ci sono molte atipie.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> 16/12/2010<br />
Prof. Rossiello<br />
Questo è il melanoma a diffusione superficiale,quello più frequente. I criteri A,B,C,D,E già li<br />
conoscete. Questo melanoma che credo rappresenti il 70% grossomodo di tutti i melanomi è quel<br />
melanoma dove è più evidente la storia naturale di cui vi ho parlato,cioè di crescita orizzontale e<br />
poi verticale. In linea di massima la crescita verticale si desume macroscopicamente da un rilievo<br />
che in genere ha il melanoma,vedete ci sono queste aree rilevate e in questo caso rispetta tutti i<br />
criteri,però ricordatevi che la diagnosi la fa sempre l’anatomopatologo,perché a livello istologico<br />
possono uscire parecchie sorprese nonostante il parere del dermatologo.<br />
Racconta di un prof universitario che morì per un errore del dermatologo che gli aveva tolto una<br />
lesione,perché il melanoma può apparire anche come papillare,e dopo pochi mesi ebbe una<br />
metastasi cerebrale.<br />
Come è fatto questo melanoma. In una fase di crescita orizzontale,vedete che ha quel pattern un<br />
po’ pagetoide,che voi conoscete,perché voi trovate queste cellule melanocitarie pigmentate e non<br />
che infiltrano l’epitelio. Sotto c’è una reazione linfocitaria con dei melanofagi,cioè delle cellule<br />
macrofagiche cariche di pigmento; se andiamo più avanti vedete questa crescita<br />
intraepidermica,ma inizia una invasione del tessuto connettivo sottostante. Questa è una invasione<br />
minima. Alcuni chiamano questo tipo di melanomi melanomi sottili,poi vedremo perché è<br />
importante. Poi più avanti vedete che c’è ancora un’infiltrazione orizzontale,ma ormai è cominciata<br />
pienamente la fase di crescita verticale e vedete in basso molto spesso c’è una reazione<br />
linfocitaria.<br />
Il melanoma nodulare rappresenta 1/4, 1/5 di tutti i melanomi,ma c’è una profonda differenza<br />
rispetto a quello a diffusione superficiale:vedete che l’epitelio sembra insensibile,non c’è un’attività<br />
né giunzionale,né melanocitaria,né un’infiltrazione dell’epidermide,ma si presenta già dall’inizio<br />
come intradermico, quasi sempre rilevato, e presenta delle cellule molto atipiche,con grandi<br />
nucleoli. Può essere anche pigmentato,in una minoranza di casi, e questo rappresenta un grosso<br />
problema. Questo (figura) è pigmentato,vedete le cellule come sono atipiche,con dei nucleoli ben<br />
evidenti,alcune infiltrano il connettivo in maniera molto diffusiva,nel senso che queste sono fibre<br />
connettivali dissociate e infiltrate da queste cellule maligne.<br />
Il melanoma acrale lentigginoso è raro,e come suggerisce il nome,si localizza soprattutto alle<br />
estremità. Qui vedete una pianta del piede,qui un dito del piede. È caratterizzato da questa<br />
infiltrazione apparentemente lentigginosa a cellule fusate. Vedete che c’è un’infiltrazione che arriva<br />
fin sopra,quasi allo strato corneo;in questo caso c’è anche un’infiltrazione nel derma papillare.<br />
Due sottovarietà di melanomi sono particolarmente subdoli: il melanoma desmoplastico che si può<br />
prestare a un errore diagnostico,soprattutto perché vedete che sopra c’è un’iperplasia lentigginosa<br />
scaricato da www.sunhope.it
atipica, e poi vedete al di sotto queste cellule fusate immerse in un abbondante stroma<br />
connettivale:questo vuol dire desmoplastico. Quindi uno può avere l’impressione che non sia un<br />
melanoma,ecco qui l’aspetto,voi vedete queste cellule fusate un po’ irregolari,se andiamo a fare i<br />
marcatori della serie melanocitaria,quindi il MELAN-A, la tirosinasi,o altri marcatori che abbiamo a<br />
disposizione,vedremo le positività,in questo caso il sistema di rivelazione non comprende la<br />
diaminobenzidina che da un colorito marroncino,proprio perché il pigmento del melanoma è anche<br />
marroncino ,quindi non si distinguerebbero le positività dal pigmento. Usiamo invece un sistema di<br />
rivelazione chiamato aec,il quale da un prodotto cromogeno rosso.<br />
C’è anche il melanoma a cellule fusate,però capiamo che è un melanoma facendo i marcatori<br />
specifici.<br />
Ha assunto sempre più maggior rilievo il tipo di infiltrato infiammatorio che ha il melanoma come<br />
fattore prognostico:l’infiltrato può essere brisk e non-brisk. Per infiltrato brisk, che in genere ha un<br />
significato prognostico negativo, si intende quando i linfociti anzicchè disporsi in un solo strato che<br />
sembra opporsi all’invasione melanocitaria,li troviamo frammisti,come in questo caso,alle cellule<br />
melanocitarie,ecco, quando troviamo linfociti e cellule melanocitarie confuse insieme è un segno<br />
prognostico negativo.<br />
Tutta questa classificazione istologica che vi ho presentato e che viene riportata perché è la<br />
classificazione storica dei melanomi,si è visto che ha una relativa importanza, perché a<br />
prescindere dal tipo di melanoma,nodulare(più profondo), a diffusione superficiale,questo è il<br />
parametro prognostico più importante,cioè lo spessore massimo secondo Breslow. Lo spessore<br />
massimo significa misurare con molta precisione il livello di profondità,quindi di crescita verticale<br />
che ha raggiunto il melanoma. Si misura partendo dallo strato di cellule granulose e si traccia una<br />
linea fino al punto più profondo che ha raggiunto il melanoma. Se questa linea di profondità è<br />
inferiore a 0.76mm(alcuni parlano di 0.9,altri di 1mm) le percentuali di sopravvivenza sono molto<br />
elevate (96%) quindi è un melanoma preso in fase iniziale. In un melanoma che supera i 0.76,fino<br />
ad arrivare a 0.69,la prognosi scende, fino ad arrivare al 29% quando supera i 3mm,perché più<br />
aumenta lo spessore massimo,più aumenta la capacità di metastatizzare.<br />
I livelli di Clark rappresentano parametri di significato prognostico inferiore,ma nelle diagnosi fatte<br />
bene troverete entrambi i parametri: spessore di Breslow e livelli di Clark. I livelli di Clark<br />
esprimono la profondità da un punto di vista topografico. Quindi noi parleremo di livello 1 quando il<br />
melanoma è grossomodo in situ; di livello 2 quando ha raggiunto la parte superficiale del<br />
derma,ovvero il derma papillare; livello 3 quando ha raggiunto il limite del derma papillare,senza<br />
superarlo; livello 4 quando arriva al derma profondo,livello 5 quando arriva al sottocutaneo.<br />
Ovviamente questo è un parametro anche molto soggettivo,per esempio tra 2 e 3,bisogna capire<br />
bene,perché 2 dice lo strato superficiale del derma papillare,3 dice lo strato profondo del derma<br />
papillare. C’è da dire che quando c’è un melanoma il derma si espande,quindi è un po’ difficile<br />
capire qual era il derma superficiale,qual era il derma profondo,cioè il derma subisce delle<br />
scaricato da www.sunhope.it
modificazioni. Questo spiega anche perché questo parametro ha un significato prognostico<br />
inferiore rispetto allo spessore di Breslow.<br />
Questo è un analizzatore di immagine. Questo è un melanoma superficiale in fase di crescita<br />
verticale e in questo caso possiamo essere ottimisti perché la profondità dalle cellule dello strato<br />
granuloso al punto di maggiore invasività delle cellule melanocitarie è 0.3,cioè di gran lunga<br />
inferiore ad 1mm. Qui quindi le possibilità di sopravvivenza si avvicinano al 100%.<br />
Gli altri fattori prognostici. Sapete tutti il linfonodo sentinella, se è positivo o negativo anche qui ha<br />
una notevole importanza per la prognosi,cosi come le metastasi linfoghiandolari,che abbiamo visto<br />
essere in rapporto allo spessore e alla profondità del melanoma. La presenza di ulcerazioni è un<br />
fattore che aggrava la prognosi, cosi come la presenza di figure mitotiche,la presenza di fenomeni<br />
di regressione,cioè una forte componente infiammatoria macrofagica che tende quasi a ridurre la<br />
massa tumorale,in questo caso è un fattore prognostico negativo. Recentemente la stadi azione ha<br />
introdotto dal punto di vista generale anche i livelli di LDH. L’LDH è un enzima che aumenta<br />
quando c’è necrosi,quando c’è un turn-over cellulare; e si è visto che un aumento dei livelli di<br />
LDH,per quanto riguarda i linfomi e molti tipi di neoplasie, rappresenta un fattore prognostico<br />
negativo.<br />
Ora per concludere,anche se sulla cute abbiamo fatto un discorso molto generale,parliamo di<br />
questa che è una malattia strana,ve ne parlo perché è un prototipo,anche come modello della<br />
cancerogenesi. Tutto deriva da questo signore che si chiamava Moritz Kon già vi hgo raccontato<br />
qualcosa dell’intimità di questo signore che sposò la figlia del direttore della clinica medica di<br />
Vienna. Come disse un mio amico che morì di melanoma,le vie per rimanere nell’università sono<br />
3:la via genetica,la via talamica e la via greca(una tragedia)….<br />
Questo signore nacque in una città vicino al fiume Kaposi,e cambiò il suo cognome con quello di<br />
Kaposi,per distinguersi dalla massa. Questo signore scoprì una malattia:il sarcoma di Kaposi.<br />
Questa malattia è rimasta un mistero fino a qualche anno fa. Già si presentava con manifestazioni<br />
cliniche molto varie,ma con quadri anatomopatologici sovrapponibili. Le varietà ono:la forma<br />
classica,che tuttora si verifica e riguarda soggetti anziani. Molto spesso le prime manifestazioni di<br />
cui vi parlerò tra poco,sono piccole macule,papule,molto spesso eritematose,rilevate o non<br />
rilevate,che si manifestano agli arti inferiori in soggetti di una certa età(dopo i 60 anni). Poi esiste la<br />
forma endemica linfoadenopatica,caratterizzata non solo da manifestazioni cutanee,ma anche<br />
linfoghiandolari. Vi sono delle regioni dell’Africa soprattutto centro-equatoriale, dove l’incidenza di<br />
questa forma è molto elevata,addirittura rappresenta una parte consistente delle neoplasie<br />
maligne. E ci sono anche delle zone della Sardegna dove questa malattia di Kaposi ha una sua<br />
incidenza,che in genere è molto più rara della forma classica. Poi abbiamo una forma più diffusa<br />
che è nata con l’AIDS. All’inizio,al settorato di New York,gli anatomopatologi iniziarono a vedere<br />
persone morte per forme sarcoma di Kaposi un po’ anomale,associate a infezioni opportunistiche e<br />
immunodepressione,e iniziarono a capire che si trattava di una malattia nuova.<br />
scaricato da www.sunhope.it
Oltre a questa esistono anche forme iatrogene,cioè legate all’uso di farmaci soprattutto<br />
immunosoppressori,come nei pazienti trapiantati. Nei pazienti immunodepressi, si evidenziano<br />
presentazioni molto più aggressive del sarcoma di Kaposi classico.<br />
C’è da dire che la forma classica è < 0.1 caso per 100000 abitanti,la forma endemica ha<br />
un’incidenza molto maggiore,quasi 30 per 100000 casi in Africa (in Sardegna sono 2 per 100000).<br />
Per la forma epidemica si parla invece del 35% dei soggetti con AIDS, quindi se vogliamo è una<br />
tipica manifestazione dell’AIDS.<br />
Sono 3 gli stadi clinici a livello cutaneo. All’inizio abbiamo una macula,poi una placca,perché si<br />
rileva,e poi un nodulo.<br />
L’estensione poi dal punto di vista dello stadio della malattia riguarda linfonodi gastrointestinali<br />
però in linea di massima la forma classica ha un decorso molto lento,tant’è vero che in un paziente<br />
in cui viene fatta diagnosi di sarcoma di Kaposi per la prima volta nell’anziano,la terapia è niente!<br />
cioè attesa.<br />
Queste sono le manifestazioni classiche. Si tratta di lesioni molto piccole,quasi eritematose,c’è<br />
anche un po’ di crosta. Ci vuole una grande esperienza del dermatologo per individuarlo. Quasi<br />
sempre però c’è un segno,ovvero una tumefazione linfatica,ma non dei linfonodi,non dico una vera<br />
elefantiasi,ma un turgore legato ad una congestione dei vasi linfatici,poi capiremo il perché.<br />
Questo è uno stadio di placca e questo è uno stadio di nodulo. Con i noduli rilevati,talvolta con<br />
ulcerazione,siamo in una fase più avanzata della malattia.<br />
Cosa succede invece nell’AIDS? Abbiamo localizzazioni anomale,per esempio al volto che è<br />
sempre risparmiato nella forma classica;abbiamo manifestazioni anche alle mucose,quindi nel<br />
cavo orale,al dorso e anche ai visceri profondi. Ci sono casi di sarcoma di Kaposi che colpiscono<br />
l’apparato gastrointestinale anche senza manifestazioni cutanee. Queste localizzazioni anomale<br />
fanno parte di un quadro dell’immunodepressione.<br />
Vediamo qual è al quadro clinico,il che spiega perché c’è una profonda differenza tra gli stadi<br />
iniziali che corrispondono alla macula,fino ad arrivare alla placca. In uno stadio iniziale vediamo dei<br />
reperti quasi banali,cioè una dilatazione cistica soprattutto dei vasi linfatici,che può sembrare una<br />
cosa banale,sapete,noi abbiamo anche il linfangioma,cioè una lesione dei vasi linfatici, c’è una<br />
componente infiammatoria quasi sempre rappresentata da plasmacellule,e poi vedete dei<br />
vasi,apparentemente di tipo linfatico sempre di forma irregolare. L’aspetto più suggestivo,che è<br />
difficile da cogliere soprattutto nell’ early Kaposis sarcoma,che è una diagnosi molto impegnativa,<br />
è vedere questi vasi e queste cellule sparse. La caratteristica è che nel connettivo troviamo delle<br />
emazie. Questo fenomeno si chiamava anticamente intrappolamento delle emazie. In effetti non<br />
sono delle emazie intrappolate,ma sono dei vasi irregolari,come questo che vedete,molto<br />
fenestrati,che non si vedono le pareti. A volte questi vasi assumono delle forme strane,si chiamano<br />
clef(?) cioè come delle incisure,degli slarghi,cosi. Se andiamo a vedere il connettivo,questo è<br />
ancora più subdolo,vediamo che i fasci di connettivo sono dissociati da questa proliferazione,cosi<br />
scaricato da www.sunhope.it
modesta,che noi riconosciamo qualche piccolo vasellino,qualche emazia che sembra<br />
intrappolata,questa è la fase iniziale. Nei pazienti sieropositivi una diagnosi del genere è<br />
importante anche per definire la fase, perché è sufficiente per fare una diagnosi di AIDS<br />
conclamata. Quindi nel paziente sieropositivo per HIV,trovare anche un early Kaposis sarcoma<br />
indica che è entrato in una fase di AIDS conclamata.<br />
Questa invece è la fase più avanzata della malattia. Riconosciamo una proliferazione a cellule<br />
fusate,un po’ atipiche,ma non molto,in cui vediamo delle emazie intrappolate in queste cavità,che<br />
sembrano delle cribrosità,dei buchi,ma in realtà sono dei vasi. Se facciamo il CD34 che è un<br />
marker degli endoteli restiamo meravigliati per il fatto non che i vasi risultino positivi,ma perché<br />
queste cellule fusate sono anch’esse positive,e questo è un fatto anomalo che indica che se è una<br />
neoplasia,è una neoplasia delle cellule endoteliali e delle cellule endoteliali linfatiche,ecco perché<br />
molto spesso c’è una tumefazione legata a una stasi linfatica. Fino a questo punto siamo arrivati<br />
qualche anno fa. Oggi sappiamo che questo è un modello di cancerogenesi particolare, virale,<br />
perché una condicio sine qua non perché si instauri questa lesione è l’infezione da herpes virus 8,<br />
però non è condizione sufficiente,perché solo in una parte di soggetti con infezione da herpes virus<br />
8 sviluppa il sarcoma di Kaposi. Nei primi 2 stadi,quando non compaiono ancora tutte queste<br />
cellule fusate,la malattia non è ancora neoplastica, ma rappresenta solo una reazione abnorme<br />
legata ad una serie di chemochine evocate dall’infezione da herpes virus 8 che determina una<br />
proliferazione vascolare dei vasi,ma siamo ancora a livello di iperplasia,non di tumore. Il III stadio è<br />
il cancro,per cui il termine di sarcoma di Kaposi si dovrebbe riservare allo stadio III,ossia lo stadio<br />
finale che è una forma di sarcoma vascolare,linfatico e questo è stato dimostrato anche da un<br />
punto di vista molecolare, per cui vedete come passiamo da una forma di infezione virale,di<br />
infiammazione che presenta iperplasia,inibizione dell’apoptosi,una neoangiogenesi indotte dal<br />
virus,attraverso l’attivazione di varie chemochine,per arrivare poi alla fase finale dove c’è il vero e<br />
proprio sarcoma,cioè la neoplasia.<br />
Facciamo ora un breve excursus sulla placenta.<br />
In una placenta distinguiamo due superfici:una fetale(piatto coriale) dove si inserisce il cordone<br />
ombelicale e una materna che guarda nella cavità uterina(piatto basale). Nella placenta avviene lo<br />
scambio tra sangue materno e fetale. I responsabili di questo scambio sono i villi. Nello spazio<br />
intervilloso,dove si trovano le cellule trofoblasti che,avvengono questi scambi. I villi si dipartono dai<br />
cotiledoni,le unità funzionali che sembrano alberi. Distinguiamo i villi di prim’ordine,quelli che si<br />
staccano subito,villi di secondo ordine e villi terminali a seconda di come va il processo di<br />
ramificazione dicotomica. Abbiamo 3 cellule di tipo trofoblastico,di cui due sono le più importanti:il<br />
citotrofoblasto(basale)e il sincizio trofoblasto. Tra i due si trova il trofoblasto intermedio. Hanno<br />
proprietà immunoistochimiche importanti perché il sincizio trofoblasto è il maggior responsabile<br />
scaricato da www.sunhope.it
della produzione di gonadotropina corionica,il trofoblasto intermedio ne produce molto meno; poi ci<br />
sono proprietà immunoistochimiche diverse sul tipo di citocheratina di cui non parliamo proprio.<br />
Questo è il piatto coriale,questa è la suddivisione dei villi, fino ad arrivare al piatto basale e alla<br />
decidua,ossia l’endometrio che ha subito quelle modificazioni secretive tipiche della gravidanza.<br />
Quando c’è un aborto spontaneo,è l’anatomopatologo che viene chiamato per fare una diagnosi.<br />
Nel 56% dei casi non c’è nessuna anomalia genetica. In altri casi invece delle anomalie genetiche<br />
determinano l’arresto della gravidanza intorno al 3-4 mese. L’aborto,secondo i nostri dati riguarda<br />
un 10-15% dal punto di vista clinico. In altre casistiche invece,per esempio quelle autoptiche, la<br />
percentuale è molto maggiore. Spesso l’aborto nelle fasi iniziali non viene avvertito e passa come<br />
metrorragia. Si parla di aborto ovulare quando il periodo di gravidanza è inferiore ad un<br />
mese,quando l’abbozzo embrionale è appena all’inizio. Si parla di aborto embrionale se avviene<br />
tra la 4 e la 12 settimana; dopo questo periodo si parla di aborto fetale.<br />
Gli aborti sono occasionali,abituali,ripetuti e poi c’è il problema dell’aborto ritenuto,di cui avrete<br />
sentito parlare sui giornali perché si tende a non accettare l’evento avverso.<br />
La macerazione interviene quando avviene la morte intrauterina in presenza di liquido,per cui nella<br />
decomposizione degli organi entra questo liquido,per esempio il liquido amniotico e si formano<br />
come delle bolle.<br />
La mummificazione invece avviene in ambienti dove c’è carenza di liquido,e lo strato cutaneo<br />
assume una durezza come il cuoio.<br />
Fa vedere delle foto di un feto mummificato e di uno macerato.<br />
Il feto papiraceo è una variante della mummificazione e si ha quando del feto resta solo la forma<br />
esterna,come se fosse fatto da carta di papiro. È una forma estrema di disidratazione.<br />
Questi sono problemi anche di rilevanza medico-legale.<br />
Le principali cause di aborto sono quelle infettive,come la rosolia,la listeria,l’herpes,il toxoplasma e<br />
così via; le anomalie e malattie del funicolo di cui parleremo:può essere un funicolo troppo breve e<br />
quindi sottoposto a lacerazione,un funicolo troppo lungo,detto a bandoliera, che può andare<br />
incontro a torsioni,spiralizzazioni e cosi via; malattie materne,la più nota è l’incompatibilità dei<br />
gruppi sanguigni; alterazioni placentari e disturbi vascolari materni o fetali.<br />
L’anatomopatologo nei casi di aborto è chiamato anche a dire alla famiglia se possono avere altri<br />
figli. Se si tratta di una gravidanza intrauterina siamo chiamati ad analizzare non solo il feto e gli<br />
annessi fetali quindi stabilire un’età biologica in rapporto all’età cronologica,perché se per esempio<br />
c’è un problema di irrorazione ci sarà una discordanza. Noi abbiamo una serie di parametri per<br />
definire l’età biologica del feto che non sto a dirvi. Per un’analisi più estesa esaminiamo i villi<br />
coriali.<br />
Se la gravidanza è extrauterina analizziamo comunque l’endometrio,perché troviamo quelle aree a<br />
stella,perché anche quando l’ovulo non è impiantato nell’utero,l’endometrio reagisce come in una<br />
normale gravidanza.<br />
scaricato da www.sunhope.it
L’iperplasia gestazionale è caratterizzata da un’iperproduzione di ormoni legata soprattutto ad un<br />
corpo luteo gravidico enorme e in cui è caratteristica la presenza di un tessuto deciduale tipico<br />
della gravidanza sovrapposto ad un tessuto endometriale secretivo. Poi ci sono vari fatti<br />
infiammatori che possono riguardare la placenta,il corion,il funicolo o l’amnios,di cui non parliamo.<br />
Molto importante è la posizione della placenta. La placenta accreta è quella che si poggia<br />
direttamente sul miometrio quindi senza uno strato deciduale intermedio; è increta quando invade<br />
il miometrio; è percreta quando attraversa tutto lo spessore dell’utero.<br />
Si chiama placenta previa quando si trova in una posizione che crea molti problemi,ovvero al di<br />
sopra dell’istmo.<br />
Poi esiste l’ematoma,che si chiama anche abruptio placenta,che può avere varie localizzazioni:al<br />
di sotto del corion,al di sotto dell’amnios,marginale,retro placentare,ecc. Ovviamente questi<br />
ematomi possono poi provocare un infarto della placenta. Normalmente una placenta a termine<br />
presenta delle piccole aree infartuali,delle micro calcificazioni,ma il problema è l’entità di questi<br />
fenomeni,perché quando c’è una necrosi maggiore del 20% c’è la morte fetale,se è di entità<br />
minore c’è ipossia.<br />
La cosiddetta placenta circumvallata è questa,vedete, le membrane espongono questa faccia della<br />
placenta con il rischio di ulteriori lacerazioni e di emorragie.<br />
Fa vedere foto di placenta previa,accreta e increta.<br />
Possiamo avere poi un’inserzione velamentosa, cioè il funicolo non ha un’inserzione netta,ma è<br />
come se si dividesse in un fascio velamentoso di vasi,per cui si determina anche qui una<br />
situazione di ipossiemia, e c’è rischio di morte soprattutto nel travaglio.<br />
Vediamo i problemi del funicolo. Si hanno soprattutto quando è troppo lungo,perché presenta nodi<br />
o pseudo nodi,con presenza di torsioni o spiralizzazioni. Noi dobbiamo sempre misurare il funicolo.<br />
Nel funicolo dobbiamo trovare 2 arterie ombelicali,ma non sempre è cosi,e questo determina<br />
un’ipossiemia fetale. Ecco,questi sono tutti i parametri in rapporto alla settimana di gestazione.<br />
L’amnio nodosum nasce quando c’è un problema di oligoidramnios che significa poca acqua,poco<br />
liquido amniotico,per cui si creano delle aderenze e nodularità, la presenza di fimbrie, e tutto<br />
questo crea difficoltà di sviluppo dell’embrione e del feto. Vedete per esempio qui per una banda<br />
amniotica si è formato un encefalo meningocele,cioè non si è formata la scatola cranica,oppure<br />
malformazioni delle dita. Sono anomalie complesse.<br />
Per quanto riguarda le malformazioni dei villi noi analizzando i villi dopo un aborto possiamo<br />
vedere com’era la vascolarizzazione. In una situazione di ipossia cronica noi troviamo una iper<br />
ramificazione e iper capillarizzazione,cioè c’è una reazione dei villi per compensare la carenza di<br />
ossigeno. Si possono trovare poi depositi di fibrina,perché quando diminuisce la quantità di<br />
sangue,per mantenere costante la portata deve aumentare la velocità del flusso,se aumenta la<br />
velocità si formano degli ingorghi a livello degli scambi,quindi della superficie intervillosa e quindi si<br />
scaricato da www.sunhope.it
possono avere dei depositi di fibrina che ostacolano maggiormente gli scambi di ossigeno tra<br />
sangue materno e fetale.<br />
Possiamo avere anche edema,chiamato anche idrope, a causa di squilibri idro-salini.<br />
Microcalcificazioni possono essere legate ad ipercalcemia, iperparatiroidismo e cosi via.<br />
Questa è l’ipervascolarizzazione,vedete quanti capillari si sono formati a livello del villo.<br />
L’edema determina un ingrossamento dei villi legata all’imbibizione edematosa dei villi.<br />
Ancora le calcificazioni,le aree di necrosi ecc.<br />
Noi possiamo stabilire anche la data di morte,ma questo ve lo dico solo per ragioni medico legali.<br />
Per esempio se il feto muore a livello intrauterino in acuto,uno dei primi fenomeni è l’emissione di<br />
meconio che normalmente avviene solo in fasi avanzate,invece vediamo già le membrane ripiene<br />
di questo materiale verdastro. Se il meconio è stato emesso da poco rispetto alla morte del<br />
feto,non ci sono alterazioni,se invece compaiono queste iperplasie delle membrane sono legate<br />
all’irritazione da meconio e cosi possiamo stabilire una cronologia della morte. Cosi anche questi<br />
macrofagi,vedete,sono carichi di meconio,ed è la prima reazione,poi arrivano i linfociti,si formano<br />
come dei granulomi,c’è tutta una cronologia.<br />
Poi vedete i residui embrionali,vedete questo è il residuo del canale neuro ectodermico; e dal tipo<br />
di residui che troviamo stabiliamo l’età e il tempo di maturazione.<br />
Ora il prof fa un elenco di patologie che accenna solo,come la gestosi,eclampsia,necrosi<br />
fibrinooide,complicanze post abortive da germi Gram positivi e Gram negativi,perforazione<br />
dell’utero,evento molto grave.<br />
Concludiamo con la cosiddetta malattia trofoblastica.<br />
La mola idatiforme,o mola vescicolare. Mola parziale,mola completa,mola invasiva,corio<br />
carcinoma, queste 4 lesioni messe insieme costituiscono la patologia trofoblastica. Ci sono poi<br />
lesioni trofoblastiche di secondaria importanza: il tumore trofoblastico del sito di presentazione cioè<br />
l’impianto e la reazione esagerata del sito d’impianto.<br />
La mola completa è incompatibile con il termine della gravidanza ed è incompatibile con la<br />
formazione dell’embrione e del feto,ma la gravidanza va avanti apparentemente,anche senza la<br />
formazione del feto,c’è un elevatissimo livello di hcg,perché è una lesione del trofoblasto,quindi ci<br />
sono molte cellule del sinciziotrofoblasto. Si presenta in genere tra l’11 e la 25 settimana. Si può<br />
accompagnare a preeclampsia e ad iperreatio luteinalis.Si determina quindi un ingrossamento del<br />
corpo luteo che da una iperreatio luteinalis legata alla eccessiva produzione di hcg. Con<br />
l’espulsione della mola vescicolare si risolve il problema.<br />
Per quanto riguarda la mola parziale,il concetto è che abbiamo dei villi molto grandi,caratteristici<br />
della mola totale,associati a villi normali,perciò si chiama parziale,quindi sono villi normali che<br />
subiscono una degenerazione molare. In questo caso è possibile che la gravidanza vada<br />
avanti,ma c’è l’aborto nel secondo trimestre,per varie malformazioni del feto spesso incompatibili<br />
con la vita. Dopo l’aborto scompaiono i sintomi.<br />
scaricato da www.sunhope.it
Nella mola invasiva,poiché c’è stata un’invasività di queste cellule trofoblasti che nello spessore<br />
del miometrio,l’ipersecrezione dell’hcg continua anche dopo l’espulsione,per cui l’unico sistema per<br />
ridurre i livelli di hcg diventa l’isterectomia. In questi casi si parla di persistenza di malattia<br />
trofoblastica. Vediamo come è fatta la mola vescicolare. Ecco,abbiamo un’immagine a grappolo<br />
d’uva. Questa conformazione particolare è legata ad un rigonfiamento idropico dei villi che<br />
assumono grandi dimensioni che presentano delle cavitazioni centrali legate all’eccesso di<br />
edema,che si chiamano anche canali o cavità centrali,anticamente si chiamavano cisterne.<br />
Troviamo in genere un’irregolarità del sincizio trofoblasto che in genere reagisce con un’iperplasia.<br />
Talvolta il sincizio trofoblasto funge da ponte tra villi contigui,formando come delle travate che<br />
uniscono più villi. Qua vediamo questa iperplasia del sincizio trofoblasto. Se andiamo a fare il Ki67<br />
vediamo che è soprattutto aumentato a livello del sinciziotrofoblasto come è intuitivo perché sono<br />
cellule in attiva proliferazione. La mola vescicolare parziale è caratterizzata dal fatto che ci sono<br />
questi villi superiori al cm di diametro che fanno parte del quadro della mola totale,associati a villi<br />
normali,più piccoli. C’è una proteina particolare,la P57 Kip che sembra aumentare nella mola<br />
parziale,per cui la usiamo soprattutto quando è in dubbio la diagnosi differenziale tra mola<br />
completa e mola parziale,anche perché vedremo che non si tratta solo di un fatto quantitativo ma<br />
si tratta di una patogenesi e di un’evoluzione molto diversa.<br />
Foto della mola parziale e malformazioni del feto(sindattilia); mola invasiva,in cui il sincizio<br />
trofoblasto arriva ad invadere più di metà dello spessore del miometrio,quindi è impossibile<br />
eliminare questa causa di ipersecrezione di hcg senza togliere l’utero. Questo è un aspetto<br />
istologico,qui vediamo chiaramente che la mola è invasiva perché nello spessore del miometrio<br />
vediamo un villo coriale. In questi casi la paziente non solo non porta a termine la gravidanza,ma<br />
perde anche l’utero.<br />
Veniamo alla patogenesi di queste malattie.<br />
Nella mola completa c’è un corredo diploide di origine paterna,cioè la fecondazione avviene con<br />
una cellula uovo vuota,cioè priva di un corredo cromosomico. Per cui il corredo è sempre di 46<br />
cromosomi,perché poi avviene la duplicazione,e può essere 46xx (se lo spermatozoo è x) e quindi<br />
abbiamo la mola completa, se il cromosoma è y abbiamo prima 23y, e questo non è vitale,per cui<br />
già da subito si arresta e non va avanti la crescita. La colpa di questa situazione è in parte del<br />
padre,in parte dell’uovo che era vuoto.<br />
Poi abbiamo la malattia trofoblastica persistente che corrisponde molto spesso alla mola<br />
invasiva,ed è quando abbiamo 2spermatozoi, uno x e uno y, che fecondano contemporaneamente<br />
la stessa cellula uovo vuota,per cui ne risulta una cellula 46xy solo paterna.<br />
La mola parziale è invece caratterizzata dalla triploidia,perché in tal caso la cellula uovo possiede<br />
un corredo cromosomico a volte diploide e a volte la metà, 23x,quindi possiamo avere, a seconda<br />
degli spermatozoi che fecondano l’uovo,diverse combinazioni,quella più frequente è un complesso<br />
di 69 cromosomi:2 serie da 23 di origine paterna e 23 di origine materna.Questa possibilità<br />
scaricato da www.sunhope.it
corrisponde al 70%. Altre possibilità sono:un corredo 3x se i 2 spermatozoi sono xx,oppure un<br />
xyy.In tutti questi casi abbiamo un aborto precoce. Quando invece la mola è diginica,cioè quando il<br />
corredo dell’uovo è diploide,può evvenire lo sviluppo fino al secondo trimestre di gravidanza,ma<br />
con gravi malformazioni. Quindi nella mola parziale il risultato è sempre una triploidia,mentre nella<br />
mola completa è una diploidia,perché in quest’ultima la cellula uovo è vuota.<br />
Il corio carcinoma nella metà dei casi si può manifestare dopo una mola vescicolare;in ¼ dei casi<br />
si può manifestare in seguito ad aborto,a gravidanza ectopica,o a una gravidanza normale.Quasi<br />
mai si sviluppa durante la gravidanza,molto spesso a distanza e in media dopo un anno,ma in<br />
alcuni casi anche dopo molti anni. In questo caso abbiamo delle emorragie,ma il parametro che ho<br />
sottolineato,che lo distingue dalle mole,è che non abbiamo villi,ma abbiamo grandi atipie. Questo<br />
tumore tende a dare metastasi. Il corio carcinoma gestazionale,ossia correlato alla gravidanza,<br />
anche se a distanza dalla gravidanza stessa risponde abbastanza alla chemioterapia, mentre il<br />
corio carcinoma extragestazionale non risponde bene alla chemioterapia. Con questa terapia<br />
chiamata MAC: metotrexate-actinomicina-clorambucile c’è una sopravvivenza a 5 anni superiore<br />
all’ 80% nel coiriocarcinoma gestazionale,che fino a poco tempo fa era impensabile. Questo è<br />
grossomodo l’aspetto,ossia una struttura molto emorragica. Come sapete questa formazioni hanno<br />
una straordinaria capacità di mettersi a contatto con i vasi e quindi è un tumore che tende ad<br />
embolizzare facilmente.<br />
Il tumore trofoblastico del sito d’impianto placentare è un tumore dei trofoblasti intermedi. Questi<br />
hanno una modesta secrezione di hcg,per cui il tumore,dal punto di vista clinico può restare un po’<br />
nascosto,anche se tende ad invadere i vasi.Si può presentare come un leiomioma,però un<br />
leiomioma che penetra nella parete,tanto è vero che in questi casi bisogna stare molto<br />
attenti,perchè se si fa un raschiamento uterino si rischia di facilitare la penetrazione in profondità di<br />
queste cellule trofoblastiche,al punto da rendere necessaria l’isterectomia. Questa situazione è<br />
resistente alla chemioterapia,ha un tasso di mortalità più basso,intorno al 20%. Queste cellule non<br />
sono cellule trofoblasti che né sinciziotrofoblastiche; presentano una debole positività per l’hcg.<br />
Placche e noduli della sede d’impianto lasciamoli stare. Quella invece che noi vediamo<br />
frequentemente è una complicanza della gravidanza,praticamente dopo il parto,si forma il<br />
cosiddetto globo di sicurezza,cioè la parete dell’utero si contrae,finiscono le emorragie,a volte con<br />
l’aiuto di farmaci che bloccano le arteriole.<br />
Può succedere però una metrorragia che persiste. Questo è legato ad un errore,che non sappiamo<br />
ancora perché avviene,le cellule trofoblastiche,anziché limitarsi ad infiltrare la parte deciduale<br />
dell’endometrio,vanno più in profondità nel miometrio,e si chiama reazione esagerata del sito<br />
d’impianto,il cui nome antico è quello di endometrite sinciziale.<br />
Anche questa è una sorpresa che può capitare sui giornali,perché l’ostetrico può non intervenire<br />
tempestivamente a fermare l’emorragia che può essere anche grave,vedete qua il miometrio come<br />
scaricato da www.sunhope.it
è dissociato da queste cellule. Si tratta di una patologia non neoplastica,ma può essere mortale se<br />
non si interviene tempestivamente.<br />
Arrivederci e buone feste!!!<br />
Carolina<br />
scaricato da www.sunhope.it
LEZIONE DI ANATOMIA PATOLOGICA DEL 3 MARZO 2010<br />
Prof Rossiello<br />
“ Non hai veramente capito qualcosa se non sei in grado di spiegarlo a tua nonna” ( A. Einstein)<br />
Oggi parliamo del sistema più complesso che c’è nel corpo umano: Il<br />
Sistema emo-linfopoietico<br />
Il sistema emo-linfopoietico è stato forse il sistema che ha subito e subisce i più violenti scossoni a<br />
causa di conoscenze tumultuose che si accavallano e che hanno reso spesso la situazione proprio<br />
nebulosa.<br />
Parliamo prima della normalità, ammesso che esista una normalità, parliamo quindi dell’istologia<br />
normale.<br />
Quando parliamo del sistema emo-linfopoietico ci riferiamo ai linfonodi, alla milza, al timo e al<br />
midollo osseo. Possiamo dire che:<br />
-i linfociti B hanno la propria “culla” nel midollo osseo,<br />
-i linfociti T nel timo.<br />
In queste sedi essi nascono e crescono, mentre potremmo dire che la loro “università” siano i<br />
linfonodi e gli altri organi linfoidi. Una volta “specializzati” o lavorano, divenendo cellule effettrici,<br />
o si dispongono in attesa.<br />
Topografia del linfonodo<br />
Immagine istologica:<br />
-osserviamo un linfonodo. Abbiamo una struttura concentrica con al centro una zona più chiara e<br />
intorno un mantello, rappresentato dai follicoli linfatici. Quello che vediamo all’esterno sono<br />
dunque i follicoli. Vediamo poi queste strutture che sono i vasi (inizialmente più di questo non<br />
sapevamo, solo dal 1975 in poi si è avuto un vero e proprio boom dell’immunologia e si è avuta<br />
maggiore consapevolezza dell’immuno-topografia del linfonodo).<br />
Volendo schematizzare, questi follicoli possono talvolta presentare un centro chiaro, detto “centro<br />
germinativo” e in tal caso i follicoli si chiamano follicoli secondari o talvolta piuttosto possono non<br />
presentarlo e in questo caso i follicoli si chiamano follicoli primari. Abbiamo, nella struttura<br />
linfonodale, dei vasi linfatici afferenti e dei vasi linfatici efferenti, cioè che escono dall’ilo che è<br />
questa parte ricurva molto ricca di vasi. Il linfonodo può vedersi, in effetti, come un “sandwich” che<br />
presenta due aree B, una corrispondente alla corticale in cui sono presenti i follicoli e una<br />
rappresentata invece dall’ilo cioè dalla midollare del linfonodo, la parte di esso più profonda, e in<br />
mezzo un’area detta T, in realtà prevalentemente T, non esclusivamente. Questo corrisponde al<br />
criterio funzionale della cooperazione tra B e T. Nell’area T ci sono delle strutture, dei vasi<br />
scaricato da www.sunhope.it
particolari, in genere sapete che i vasi hanno un endotelio schiacciato, hanno nuclei filiformi,<br />
invece in questo caso abbiamo venule ad endotelio florido, un endotelio così rigoglioso da far<br />
somigliare le cellule che lo costituiscono a cellule epiteliali, qualcuno le chiama venule<br />
“epitelioidee”. Queste venule ad alto endotelio, che sono una caratteristica dell’area T, hanno un<br />
funzione importantissima di cui parleremo a breve, per molto tempo non chiara.<br />
Immagini istologiche:<br />
-osserviamo i follicoli, nel follicolo secondario c’è un centro chiaro e tutto intorno questi piccoli<br />
linfociti, disposti attorno all’area chiara, che rappresentano la corona del centro germinativo.<br />
Vediamo poi un follicolo primario che sta per diventare secondario, questo perché noi sappiamo<br />
che il follicolo secondario rappresenta in effetti la forma attiva, diventa ossia secondario quando<br />
lavora.<br />
Parliamo del centro germinativo:<br />
- Innanzitutto ha delle cellule particolari, cellule che sembrano quasi dei “fantasmi” avendo un<br />
nucleo chiaro, un citoplasma chiaro e spesso dei detriti nucleari nel citoplasma, cellule che gli<br />
americani chiamano “starry sky”. Tali cellule, macrofagiche, hanno funzione in effetti di “operatori<br />
ecologici” del linfonodo. Sono chiamate starry sky perché se noi immaginiamo che la luce viene da<br />
sotto, dal microscopio, e qua vedete un addensamento di nuclei, la luce passa soprattutto in<br />
queste aree chiare, per cui danno quasi l’impressione di “stelle in un mare di blu” che sono poi<br />
tutti i nuclei. Inoltre nel centro germinativo incontriamo due tipi di cellule principali che sono,<br />
secondo la scuola europea:<br />
- centrociti cellule che a vederle superficialmente sembrano rotonde e piccole, ma in realtà non<br />
sono così, non sono proprio rotonde, bensì presentano sempre qualche incisura, qualche<br />
deformità che non le rende perfettamente sferiche (Il centrocita, secondo la letteratura americana<br />
si chiama anche cellula “clivered” ossia “clivata” appunto avendo un’incisura).<br />
-centroblasti cellule più grandi con un nucleo più chiaro (sono indicate con una freccetta<br />
sull’immagine corrispondente) che presentano una caratteristica ossia il nucleolo è alla periferia, il<br />
nucleolo è addossato alla membrana nucleare (i nucleoli possono essere anche più di uno).<br />
-Inoltre nel centro germinativo è possibile osservare figure mitotiche essendo anche una struttura<br />
altamente proliferante. E’ proprio nel centro germinativo che i linfociti B si “laureano” diciamo.<br />
Gli immunoblasti sono poi delle cellule che somigliano ai centroblasti, ma hanno, in confronto ad<br />
essi un nucleo più grosso, con un nucleolo ugualmente più grosso e molto spesso in posizione<br />
centrale. Osservandoli al microscopio, l’immagine che vediamo è, diremo, a “occhio di civetta”.<br />
Inoltre gli immunoblasti presentano anche un’altra caratteristica, hanno un po’ di citoplasma, in cui<br />
possiamo trovare qualche immunoglobulina, l’immunoblasto quindi comincia a produrre qualche<br />
immunoglobulina, seppure in “maniera artigianale”. Gli immunoblasti non si trovano mai nel<br />
follicolo linfatico, se non raramente. Li incontriamo invece verso l’esterno, verso la periferia e<br />
hanno un marcatore che è CD30, ma ne parleremo nuovamente più avanti.<br />
scaricato da www.sunhope.it
Ora vista la topografia del linfonodo, cerchiamo di capire come si studia un linfonodo. Per esempio<br />
un linfonodo sito nei pressi di una formazione tumorale, anche se non è metastatico, ci può dare<br />
informazioni sul tipo di immunità che sta lavorando in quella situazione.<br />
Se c’è una stimolazione di tipo B : la para-corticale (area verde nell’immagine indicata a lezione) si<br />
riduce, mentre la corticale aumenta e i follicoli diventano più grandi e tendono anche a confluire<br />
talvolta. Quando vediamo un linfonodo con queste caratteristiche vuol dire che c’è una forte<br />
reattività in senso B.<br />
Se invece c’è una stimolazione T: I follicoli sono quasi atrofici, vediamo soprattutto follicoli primari,<br />
raramente i secondari. L’area para-corticale aumenta e aumenta il numero di quelle venule ad alto<br />
endotelio, o epitelioidee, di cui abbiamo precedentemente parlato.<br />
Se sono coinvolti i due sistemi, B e T: avremo un’espansione sia delle aree B che dell’area T.<br />
Abbiamo visto come attorno al centro germinativo era identificabile una corona, si è visto che tale<br />
corona è fatta in realtà di due zone che sono una zona più interna, vicina al centro germinativo, che<br />
è la zona “mantellare” e una zona più esterna che è detta “marginale”, ultima zona del follicolo<br />
linfatico. Tale zona marginale è rappresentata nel linfonodo ma la ritroviamo particolarmente<br />
ingrandita soprattutto nelle zone extra-linfoghiandolari, per esempio nella milza raggiunge<br />
un’espansione maggiore. Ai confini della zona marginale ci sono dei linfociti chiamati linfociti B<br />
“monocitoidi” , che hanno un evidente citoplasma (in genere il linfocita piccolo non ha un<br />
citoplasma ben evidente). Morfologicamente nella zona mantellare incontriamo cellule disposte in<br />
maniera molto fitta con un pattern più omogeneo, mentre nella zona marginale le cellule sono più<br />
distanziate e possiamo riconoscere anche cellule monocitoidi perché l’area monocitoide confina<br />
con la zona marginale per cui è molto facile che rimangano anche degli elementi monocitoidi. Le<br />
cellule B monocitoidi, che presentano come detto un evidente citoplasma, aumentano in<br />
determinati processi patologici, neoplastici e non.<br />
Percorso caratteristico dello sviluppo dei linfociti B :<br />
Abbiamo parlato della<br />
-“culla” dei linfociti, sono organi extra-linfoghiandolari in cui incontriamo i pre-linfociti, (…)-parola<br />
non chiara- e il B maturo vergine che non ha ancora incontrato l’antigene. Tutti questi precursori<br />
delle cellule linfoidi esprimono il Tdt , terminal-desossi-transferasi, caratteristica comune a tutti i<br />
precursori, anche T. E in questa fase non esprimono ancora i marcatori di maturazione.<br />
-A questo punto la cellula B entra nel linfonodo e la sua prima tappa è rappresentata dal divenire<br />
cellula mantellare ( anch’essa cellula “clivata”, somiglia difatti al centrocita, non essendo il nucleo<br />
perfettamente sferico) poi la maggior parte delle cellule entra nel centro germinativo, ma c’è una<br />
-via secondaria quella dell’evoluzione a immunoblasto. In questo caso matura fino alle cellule<br />
linfoplasmocitoidi e rappresenta una risposta più immediata immunitaria. Questi immunoblasti<br />
presentano un nucleolo abbondante e nel citoplasma sono presenti immunoglobuline. In realtà la<br />
cellula che ne produce di più è la cellula linfoplasmocitoide. Si è visto che molto spesso questa via<br />
più rapida produce catene pesanti, soprattutto le IgE ( noi sappiamo che se abbiamo un’infezione<br />
scaricato da www.sunhope.it
in atto spesso andiamo a cercare le IgE). La cellula linfoplasmocitoide vuole emulare la<br />
plasmacellula ma presenta in realtà a confronto un citoplasma scarso (la plasmacellula ha un<br />
citoplasma abbondante, un reticolo e un apparato di Golgi molto sviluppati e una sintesi di<br />
immunoglobuline elevatissima), un nucleo simile ( detto a “ruota di carro” anche se in realtà non è<br />
mai effettivamente a ruota di carro, pur presentando questa caratteristica disposizione periferica di<br />
cromatina tipo a barre).<br />
---Se entra invece nel centro germinativo, cosa che interessa la maggior parte dei linfociti ( la<br />
maturazione completa richiederà più tempo), diventa centroblasta, diventa centrocita (somigliante<br />
molto quindi alla cellula mantellare) diventa cellula monocitoide e i centrociti e le cellule<br />
monocitoidi incominciano a produrre Ig e poi abbiamo la più alta specializzazione B che è la<br />
plasmacellula, anello terminale di questa maturazione.<br />
Cosa facciamo per vedere se questi linfociti sono B?<br />
-Marcatore classico dei linfociti B maturi è il CD20, tranne la plasmacellula, che perde il CD20;<br />
-Linfocita meno maturo presenta invece il CD19;<br />
Alcuni anni fa capitò che non riuscivamo a trovare più CD20. Siccome una delle terapie possibili per<br />
linfomi è l’uso di anticorpi anti-CD20, alla base della nuova terapia biologica dei linfomi, quando<br />
furono introdotti detti anticorpi, il linfocita B, che ha diciamo una sua “furbizia”, non espresse più il<br />
CD20 appunto; e ci è capitato quindi che in alcuni casi di recidiva non si vedeva più CD20. In questi<br />
casi, si è ricorso allora alla ricerca, tramite un anticorpo diciamo “di riserva”, di -----una particolare<br />
proteina nucleare dei linfociti B PAX 5. Questa proteina viene appunto presa in considerazione<br />
quando CD20 crea dei problemi, solo che è una positività nucleare mentre CD20 è una positività di<br />
membrana;<br />
-Cellule mantellari e marginali hanno innanzitutto marcatori comuni la bcl 2, perché a questo<br />
livello, nella corona dei linfociti, viene inibita la necrosi apoptotica ( e la bcl 2 ha un ruolo proprio<br />
nei meccanismi molecolari e biochimici preposti alla apoptosi). Le cellule mantellari hanno inoltre<br />
la ciclina D1, poi il CD 5 e poi il ki 67, marcatore di proliferazione;<br />
Quindi per le cellule della zona marginale c’è un criterio: faccio la bcl 2 e così so che sono cellule<br />
della corona esterna del follicolo, se sono ciclina D1 e CD5 positive e esprimono il ki 67 allora sono<br />
cellule mantellari, se sono ciclina D1 e CD5 negative sono allora cellule della zona marginale.<br />
Quindi allo stato attuale delle nostre conoscenze la zona marginale si identifica per sottrazione,<br />
non esprimendo marcatori delle cellule mantellari;<br />
-Per il centro germinativo abbiamo marcatori quali soprattutto il CD 10 e la bcl 6 quindi per sapere<br />
se sono cellule del follicolo ricerco questi due marcatori; Cellule scarry sky sn marcate da CD 68.<br />
-Per le cellule B monocitoidi il marcatore è T-bet, fattore di trascrizione specifico;<br />
Quindi noi disponendo di otto, nove anticorpi possiamo ricavare una serie di informazioni. (Sono<br />
CD20 + tutte le cellule B sia quelle del mantello (in senso lato) che quelle del centro germinativo)<br />
scaricato da www.sunhope.it
Ritorniamo un attimo alla descrizione del linfonodo: sotto la capsula abbiamo il “seno linfatico<br />
marginale” che rappresenta la porta di ingresso degli antigeni e corpi estranei, e dello seno<br />
linfatico marginale, all’interno del linfonodo si dirada in seni linfatici intermedi. All’interno di<br />
questi seni linfatici possiamo trovare macrofagi, linfociti e materiale estraneo. Vedremo che ci<br />
sono particolari processi infiammatori in cui questi seni linfatici si ingrandiscono. Il seno linfatico<br />
esprimerà, o meglio l’endotelio che lo costituisce esprimerà, il marcatore dei vasi, il CD 34. ( i<br />
macrofagi esprimeranno invece il CD 68, marcatore di quasi tutti i macrofagi). Il processo di<br />
dilatazione dei seni, che solitamente sono “fessuriformi”, prende il nome di seno-istiocitosi<br />
essendo soprattutto presenti nei seni istiociti macrofagi.<br />
Ritornando infine sulle venule ad alto endotelio che hanno un’importanza strategica. Potremmo<br />
immaginare questo sistema di venule come una “dogana” che disciplina la ri-circolazione dei<br />
linfociti, il transito cellulare, attraverso particolari recettori. E in alcuni casi può aversi una<br />
“chiusura” di dette venule, che divengono “impermeabili” ai segnali esterni, per situazioni<br />
problematiche linfonodali che richiedano l’”isolamento” del linfonodo in qualche modo. Altrimenti<br />
attraverso i messaggi veicolati soprattutto dai linfociti T il linfonodo viene eventualmente reclutato.<br />
Hanno dunque una loro centralità di funzione. Le cellule endoteliali che le costituiscono esprimono<br />
il CD 34 e sono cellule globose, cellule abbondanti ed in genere il loro lume è molto piccolo in<br />
quanto funzionano da filtro.<br />
Osserviamo adesso i linfociti T<br />
Dei linfociti T in effetti non sappiamo molto, anche se comunque ne riparleremo poi a proposito<br />
del timo. Sappiamo che c’è un piccolo linfocita T e un grande linfocita T che somiglia<br />
all’immunoblasta. Ma c’è una differenza l’immunoblasta T ha un nucleo simile al B ma presenta<br />
uno scarso citoplasma, anche perché non deve produrre immunoglobuline. Marcatore comune<br />
della serie T è il CD 3. Qualche cellula T può essere presente anche a livello del follicolo linfatico, in<br />
quanto veicola informazioni, ma comunque l’area in cui sono maggiormente presenti è<br />
sicuramente l’area para-corticale, sotto ai follicoli linfatici. Possiamo vedere se sono attivati, ma è<br />
poco importante, lasciamo perdere. Possiamo vedere con marcatori quali CD 4 e CD 8<br />
rispettivamente se sono T helper o T soppressor. Nella paracorticale del linfonodo abbiamo un<br />
rapporto caratteristico tra CD 4 e CD 8 tale che i CD 4 sono almeno tre volte più numerosi dei CD 8,<br />
quindi avremo un rapporto almeno di 3:1 o 4:1. Vedremo delle patologie in cui questo rapporto o<br />
si inverte o comunque non viene mantenuto. Volendo essere proprio pignoli, una volta noi<br />
parlavamo di macrofagi genericamente, mentre oggi distinguiamo macrofagi e cellule dendritiche<br />
che hanno pure un nucleo chiaro, ma presentano dei prolungamenti citoplasmatici caratteristici<br />
( da cui appunto dendritiche) e che sono di vari tipi:<br />
-Le prime cellule dendritiche (vedremo che ci sono patologie che coinvolgono soprattutto queste<br />
cellule) si distribuiscono soprattutto vicino ai seni linfatici e sono le cellule di Langherans che<br />
troviamo anche in distretti extra-linfoghiandolari, come la cute, e hanno funzione di primo<br />
contatto con gli antigeni. Loro marcatore è il CD 1a. (nei miei appunti ho trovato questo dato sul<br />
scaricato da www.sunhope.it
marcatore ma non nella sbobbinatura, probabilmente l’avrò preso dalle slides, comunque volevo<br />
segnalarvelo).<br />
-Poi abbiamo cellule dendritiche site all’interno dei follicoli, cellule follicolari che sono a nucleo<br />
chiaro, con un citoplasma particolare, con dei prolungamenti diciamo, come in generale tutte<br />
queste cellule e che sono CD 23 + e hanno funzione di produzione proteine a funzione antiapoptotica.<br />
Sono importanti in quanto se noi in un linfonodo, a seguito di un processo patologico<br />
più o meno importante, vogliamo sapere dove si trovava il centro germinativo prima di tale<br />
processo, se facciamo il CD 23 ritroviamo la precedente sede di detto follicolo, e se saranno<br />
dispersi in qualche modo, disordinati nel contesto linfonodale, risaliremo al fatto che è accaduto<br />
qualche fenomeno che ha determinato questo sconvolgimento. Il centro germinativo è pieno di<br />
queste cellule.<br />
-Infine abbiamo le cellule interdigitate che partecipano al trasporto dei linfociti, per esempio verso<br />
i linfociti B, per la produzione poi di anticorpi.<br />
Per quanto riguarda poi la zona midollare del linfonodo, c’è in realtà poco da dire. E’ un’area<br />
prevalentemente B, ricca di vasi, e ricca di plasmacellule. La plasmacellula non esprime il CD 20 ma<br />
un suo marcatore specifico che è il CD 138.<br />
Cosa fa l’anatomopatologo quando è dinanzi ad un linfonodo?<br />
Innanzitutto deve scegliere il trattamento. Oggi la maggior parte degli antigeni resiste al<br />
trattamento in formalina-paraffina, che è il trattamento classico. Solo particolari antigeni non<br />
resistono a detto trattamento, bensì vengono denaturati e si deve dunque in questi casi congelare<br />
il linfonodo, ma questo oggi si verifica molto raramente;<br />
- C’è una morfologia tradizionale, che è alla base di tutto, ossia si procede all’osservazione del<br />
linfonodo.<br />
-Possiamo ricorrere ad indagini istochimiche, ad esempio è importante il reticolo, che ci da<br />
informazioni riguardo all’impalcatura ed in genere il reticolo in un linfonodo è un reticolo sottile.<br />
Già in base al reticolo possiamo distinguere leucemie e linfomi, in genere nel linfoma il reticolo è<br />
distrutto, mentre nella leucemia c’è una forma di sostituzione delle cellule che lo costituiscono.<br />
-Poi abbiamo l’immuno-istochimica, con la ricerca di tutti i marcatori prima visti ed anche altri;<br />
-Metodiche di ibridazione in situ ossia metodiche FISH;<br />
-l’analisi molecolare per particolari applicazioni;<br />
-oggi si va molto diffondendo la cito-fluorimetria sui linfonodi che è una metodica molto semplice,<br />
che prevede la possibilità di estrarre con una siringa i linfociti dal linfonodo, metterli nel citofluorimetro<br />
mediante anticorpi e avere già un’analisi quantitativa delle diverse popolazioni e<br />
scaricato da www.sunhope.it
sottopopolazioni linfoidi così d avere già un orientamento riguardo alla dominanza eventuale di<br />
alcune di esse. Che già darà informazioni sulla possibilità che sia o meno un processo neoplastico.<br />
-e ancora ci sono altre tecniche di cui però non parleremo, come per esempio il “ micro-array”, che<br />
si usa solo per applicazioni scientifiche e difficilmente diagnostica. Una tecnica, che però si utilizza,<br />
seppur raramente, quando ci troviamo di fronte a dei linfomi anaplastici in cui non riusciamo a<br />
capire mediante marcatori se ci troviamo di fronte a cellule B, T o altro, ricorriamo a tecniche di riarrangiamento<br />
genico. Tenendo presente che ci sono ad esempio delle regioni per le Ig espresse<br />
solo dai linfociti B, se troviamo un ri-arrangiamento già possiamo fare diagnosi di linfoma, o regioni<br />
che codificano per i recettori dei linfociti B. Così da risalire alla popolazione di appartenenza di<br />
cellule non identificate precedentemente mediante marcatori.<br />
Quando facciamo la biopsia linfoghiandolare?<br />
Non è mai da ritenersi una prima scelta. Bensì come un’ultima spiaggia, in condizioni in cui non<br />
abbiamo altri mezzi per fare diagnosi o abbiamo necessità di confermare una diagnosi. Indicazioni<br />
sono:<br />
-linfo-adenopatia persistente da cause ignote (la linfo-adenopatia è la patologia più frequente nel<br />
mondo ed è necessario quindi che sia persistente e da causa ignota);<br />
-una sintomatologia clinica sospetta ( ad esempio, paradossalmente, le febbricole soprattutto<br />
intermittenti accompagnate a sudorazione, ci fanno considerare anche un linfoma);<br />
-conferma diagnostica;<br />
-stadiazione ( esempio il linfonodo sentinella);<br />
-follow-up ( ad esempio in un paziente HIV+, con un rigonfiamento linfo-ghiandolare, vogliamo<br />
sapere se è già AIDS, se è un infezione opportunistica, se c’è una neoplasia, non abbiamo altro<br />
sistema se non u a biopsia linfo-ghiandolare).<br />
RACCOMANDAZINI:<br />
-notizie cliniche accurate;<br />
-sede idonea (non ascellare, non inguinale in quanto sono tipicamente sedi “inquinate” in cui si<br />
hanno linfonodi irritati di cui spesso non si ha conoscenza ad esempio da sudore, deodorante,<br />
processi fibrotici di vecchia data, certo se abbiamo solamente questi linfonodi a disposizione<br />
questa raccomandazione non sarà valida, altrimenti sono da preferirsi ad esempio i linfonodi<br />
latero-cervicali);<br />
-dimensioni adeguate, prendere il linfonodo più grande (più grande è più vuol dire che il processo<br />
è andato avanti, più è diagnostico);<br />
scaricato da www.sunhope.it
-asportazione in toto (evitare traumatismi). Sono possibili aderenze per cui si rischia,<br />
erroneamente, di prendere il linfonodo a “pezzetti” così alterando la topografia del linfonodo.<br />
La citologia aspirativa può sostituire la biopsia linfonodale?<br />
Se la diagnosi si basa anche su dei criteri topografici, no. Difficilmente ad esempio in un linfoma<br />
troveremo delle atipie marcatissime come in un cancro della mammella, per cui il criterio<br />
principale è topografico. Quando prendiamo delle cellule disperse non sappiamo bene la zona<br />
dalla quale le abbiamo prese e non possiamo ricostruire bene la topografia di una struttura, per cui<br />
saremo in grado poi di fare una diagnosi? Abbiamo sicuramente altri ausili, come ad esempio la<br />
cito-fluorimetria, ma sicuramente quello che si fa con l’istologia non si può fare in altri modi. Nella<br />
diagnostica differenziale tra linfomi e linfoadeniti o comunque linfo-adenopatie di vario tipo, la<br />
diagnostica citologica ha scarsa sensibilità e specificità. Se invece il quesito che ci poniamo è<br />
diverso, ad esempio non ci interessa sapere se è linfoma o altro, o che tipo di linfoma è, ma ci<br />
interessa sapere piuttosto se questo ingrossamento è legato ad un processo primitivo o<br />
secondario, ossia vogliamo sapere se è una metastasi allora la citologia aspirativa serve. Perché ci<br />
consente di vedere le cellule epiteliali atipiche che ci permettono di escludere il linfoma. Tuttavia<br />
va considerato che soprattutto a livello latero-cervicale possiamo incontrare alcune problematiche<br />
che possono essere causa di errore diagnostico. Per esempio nei linfonodi cervicali alti è probabile<br />
incontrare isole di tessuto salivare, così come possiamo trovare delle isole di linfonodo presenti<br />
nella parotide (per cause embriologiche che non stiamo a trattare). E trovare cellule epiteliali in un<br />
linfonodo potrebbe erroneamente farci pensare ad una metastasi, invece conoscendo il problema<br />
posso andare a vedere che cellule epiteliali sono, come sono disposte e considerare un eterotopia,<br />
ossia dislocazione anomala all’interno del linfonodo; ancora è possibile incontrare siti di<br />
endometriosi.<br />
scaricato da www.sunhope.it
Lezione 2 –secondo semestre<br />
Linfoadeniti<br />
Linfoadeniti granulomatose<br />
Identifichiamo tre categorie di linfoadeniti granulomatose:<br />
• Da materiale esogeno (penetrato all’interno)<br />
• Con necrosi ascessuale<br />
• Con necrosi non ascessuale<br />
La caratteristica comune di queste linfoadeniti è il granuloma.Il granuloma è una struttura<br />
costituita da cellule macrofagiche altamente specializzate che prendono il nome di cellule<br />
epitelioidi (cioè cellule che hanno abbondante citoplasma acidofilo e pertanto somigliano<br />
lontanamente alle cellule epiteliali;questa ricchezza di citoplasma si associa ad abbondanza<br />
di enzimi ed attività metaboliche citoplasmatiche); oltre alle macrofagiche, ci sono le cellule<br />
giganti plurinucleate, che sono sempre macrofagi e hanno molti nuclei disposti<br />
perifericamente a ferro di cavallo (in tal caso si chiamano cellule di Langhans e sono<br />
caratteristiche di certi processi morbosi) oppure al centro (in tal caso sono dette cellule da<br />
corpo estraneo). Attorno a questa “struttura di base” c’è un alone periferico costituito da<br />
linfociti e plasmacellule.<br />
Nella formazione del granuloma i linfociti T CD4 hanno un ruolo fondamentale nella<br />
stimolazione macrofagica, infatti nei pazienti immunodepressi e particolarmente nei<br />
pazienti con AIDS non si trovano granulomi, poiché mancano i linfociti T CD4. Il granuloma si<br />
forma quando la reattività dei linfociti B e T non è adeguata alla difesa: ad esempio, in caso<br />
di penetrazione materiale esogeno, la reazione granulomatosa si origina nel tentativo di<br />
circoscrivere la penetrazione di sostanze estranee all’organismo.<br />
Il granuloma può evolvere in necrosi , in calcificazione o fibrosi.<br />
Linfoadeniti da materiale esogeno<br />
Uno dei materiali esogeni che più frequentemente origina queste linfoadeniti è il silicone,<br />
che può produrre delle vere e proprie patologie deformanti(specie nell’ambito della<br />
chirurgia plastica), nonché processi autoimmuni. Nelle moderne protesi mammarie ci sono<br />
invece siliconi che danno più raramente problemi del genere, ma possono comunque<br />
determinare delle reazioni granulomatose talmente imponenti e deformanti da poter essere<br />
in alcuni casi confuse con cancro infiammatorio della mammella.<br />
Anche il materiale usato per i tatuaggi può causare linfoadeniti.<br />
scaricato da www.sunhope.it
Tra le altre cause di linfadenite granulomatosa da corpo estraneo ci sono i mezzi di<br />
contrasto lipidici (che si iniettano nei linfonodi per eseguire linfoangiografie),<br />
l’iperlipidemia, l’oro ( i Sali d’oro sono dei farmaci che si usano nel trattamento di malattie<br />
autoimmuni), i materiali dentari, le protesi metalliche ( come le protesi d’anca: è stato<br />
pubblicato tempo fa il caso di un paziente che sviluppò una reazione granulomatosa e lupus<br />
eritematoso sistemico).<br />
Il prof commenta delle slide:<br />
slide1: all’esame anatomopatologico un granuloma appare come formato da “bolle”: i lipidi<br />
vengono eliminati dai processi di lavorazione (xilolo, alcool)e rimane la cavità che prima lo<br />
conteneva; sono visibili le cellule giganti plurinucleate.<br />
slide2: i mdc lipidici possono dare senoistiocitosi, con seni molto dilatati e ripieni di<br />
materiale lipidico.<br />
slide3: è relativa al caso del paziente che sviluppa reazione alla protesi d’anca. Visibile il<br />
materiale nerastro proveniente dalla protesi che ha scatenato il processo autoimmune.<br />
Linfoadeniti con necrosi ascessuale<br />
In questo caso c’è il granuloma e al centro la necrosi, con granulociti. Comprende<br />
moltissime forme.<br />
La linforeticulosi da inoculazione (malattia da graffio di gatto) è causata da Bartonella<br />
Henselae, la quale non può da sola oltrepassare la barriera cutanea e ha bisogno di una<br />
lesione per entrare (graffi di gatto o altri tipi di lesioni). Nel sito di inoculazione compare<br />
una lesione cutanea, tumefazione, papula o eritema, che tende a scomparire. I germi si<br />
propagano ai linfonodi per cui dopo qualche settimana si determina una linfoadenite con<br />
tumefazione nei linfonodi di drenaggio e focolai ascessuali che si possono associare a rash<br />
cutanei e varie complicanze.<br />
Il linfogranuloma venereo è sessualmente trasmissibile e il responsabile è la Clamidia<br />
Trachomatis. Nella sede di inoculazione (genitali) compaiono piccole vescicole, poi il<br />
processo si estende ai linfonodi dove si forma una megalinfoadenopatia, talmente<br />
ascessuale che tende a fistolizzarsi e a determinare dei tragitti fistolosi a livello inguinale, da<br />
cui fuoriesce materiale necrotico e ascessuale. Nella donna la malattia può assumere un<br />
andamento più pericoloso perché sono colpiti anche i linfonodi pelvici, con quadro di<br />
maggiore gravità perché per la fistolizzazione si può avere una disseminazione extranodale.<br />
Il prof commenta delle slide sulla linforeticulosi:<br />
slide1: linforeticulosi da inoculazione;si vede il graffio da gatto;<br />
scaricato da www.sunhope.it
slide2: si vedono due piccole tumefazioni nella sede di inoculazione;<br />
slide3: rigonfiamento di linfonodo sottomandibolare, associato a rash e roseole della cute.<br />
Slide4:con esami immunoistochimici si isola la bartonella, in fase iniziale. All’esame<br />
istologico si vedono macrofagi epitelioidi, alone di linfociti e plasmacellule. In fase più<br />
avanzata si distinguono al centro del granuloma dei granulociti in disfacimento.<br />
Il prof commenta ora delle slide sul linfogranuloma venereo:<br />
slide1:si vedono masse linfonodali molto grosse, in sede inguinale, perivulvare. A differenze<br />
della linforeticulosi c’è abbondante necrosi linfonodale, con tragitti fistolosi e<br />
coinvolgimento di linfonodi adiacenti sicchè si formano masse di notevoli dimensioni.<br />
Linfoadeniti granulomatose non necrotiche o con necrosi non ascessuale<br />
• La tubercolosi primaria, spesso polmonare, non forma granulomi, ma c’è una<br />
essudazione a causa di una reazione aspecifica; in fase post primaria c’è invece la<br />
presenza di granulomi. Le linfoadeniti tubercolari sono processi primitivi del linfonodo,<br />
non si tratta della tubercolosi classica. Ricordiamo infatti che, nella tbc classica, il focolaio<br />
primario ha tre fondamenta :il focolaio polmonare, il linfonodo che partecipa al processo<br />
e la linfangite(interessamento dei vasi linfatici). In questo caso però non è così, perché<br />
non si tratta di una tbc linfoghiandolare secondaria al focolaio polmonare, ma il<br />
linfonodo è la sede di ingresso e del processo principale. In tal caso sono responsabili dei<br />
micobatteri atipici di varia natura: era una patologia quasi scomparsa nelle nostre zone,<br />
ma ricomparsa a causa della presenza di extracomunitari. Questa forma di tbc è anche<br />
detta scrofula perché conferisce al volto la forma della testa di un maiale, per<br />
ringonfiamento dei linfonodi laterocervicali, retromandibolari , sottomandibolari. I<br />
micobatteri atipici responsabili della linfoadenite tubercolare primitiva possono dare tre<br />
tipi di pattern clinici e anatomopatologici:<br />
• Forma fibroepitelioidea: piccoli granulomi ad evoluzione fibrotica, si formano quando le<br />
difese dell’organismo sono molto efficienti<br />
• Forma caseosa: quando la virulenza dei germi supera la capacità di difesa dell’organismo<br />
si ha una necrosi caseosa, non mediata da granulociti. E’ la forma che determina<br />
maggiormente deformazione del volto.<br />
• Forma mista<br />
•<br />
scaricato da www.sunhope.it
• La sarcoidosi può coinvolgere i linfonodi in forma secondaria o in forma primitiva. In<br />
quest’ultimo caso si tratta di linfoadenite granulomatosa primitiva senza necrosi ( si può<br />
però osservare al centro del granuloma del connettivo).<br />
•<br />
• Il prof commenta slide su tbc:<br />
• slide1: si osserva il ringonfiamento linfonodale presente nella scrofula<br />
• slide2: necrosi caseosa di un linfonodo<br />
• slide3:necrosi caseosa centrale dall’aspetto eosinofilo, perifericamente tessuto<br />
granulomatoso.<br />
• Slide4: cellula gigante con nuclei a ferro di cavallo(caratteristico ma non specifico della<br />
tbc);il metodo ancora oggi usato in questi casi è la colorazione di zihel nielsen con la<br />
fucsina, poiché i micobatteri sono alcol-acido resistenti.<br />
•<br />
• Il prof passa alle slide sulla sarcoidosi:<br />
slide1: granuloma simile alla tbc, ma non ha necrosi, è più piccolo e i suoi limiti sono più<br />
netti, presenta i cosiddetti corpi asteroidi(cellule con prolungamenti acidofili.<br />
•<br />
•<br />
•<br />
Linfoadeniti non granulomatose<br />
La mononucleosi infettiva è causata dall’Epstein Barr virus. In realtà la sua diagnosi non<br />
dovrebbe basarsi sulla biopsia, dovrebbe essere riconosciuta prima. Nella sua forma classica<br />
si presenta con angina violenta ed esplosiva , segue poi tumefazione linfonodale testa-collo<br />
e dei linfonodi retronucali(a differenza della tbc); può associarsi a epatomegalia. In genere si<br />
risolve in poco tempo, sono molto diffuse forme subcliniche che non vengono nemmeno<br />
riconosciute. Facendo un esame ematologico accurato si evidenziano linfociti atipici (cellule<br />
di Pfeiffer). Ci sono poi delle forme di mononucleosi che sono meno acute e vanno verso la<br />
cronicizzazione, si presentano con febbricola, sudorazione, astenia. Se si fa la biopsia<br />
linfoghiandolare , si osserva:<br />
• una iperplasia follicolare esplosiva ( con iperreattività dei linfociti B), tanto che<br />
facendo un agoaspirato si potrebbe confondere con un linfoma a causa della grande<br />
presenza di centrociti e centroblasti.<br />
scaricato da www.sunhope.it
• Una iperplasia delle cellula monocitoidi B (sono i precursori delle plasmacellule)<br />
• Presenza di voluminosi monoblasti con immagini atipiche; addirittura vi sono cellule<br />
simili alle cellule di reid-stenberg del linfoma di hodgkin (anche questo può creare<br />
dubbi diagnostici<br />
• I sinusoidi sono conservati<br />
Commento di slide:<br />
slide1:si osserva un voluminoso centro germinativo, con cellule starry sky<br />
slide2: cellula con 2 nucleoli, cellule con macronucleoli, cellule molto pleomorfe..insomma ,<br />
molte atipie, fequenti in infezione da epstein barr. Si possono ricercare le proteine<br />
codificate dal virus.<br />
slide3: cellula di hodgkin, mononucleata, con un grosso nucleolo a occhio di civetta;nella<br />
mononucleosi troviamo invece delle cellule immunoblastiche(somiglianti alle cellule di<br />
hodgkin) che hanno nucleolo acidofilo (normalmente l’immunoblasto ha nucleolo basofilo),<br />
sono CD30+ ( e questo dimostra che sono immunoblasti)e sono circondate “ a rosetta” dai<br />
linfociti T ( i linfociti T si raccolgono attorno a questi immunoblasti anomali); si osservano<br />
anche numerose cellule CD20 essendoci una”esplosione”dei follicoli linfatici.<br />
Linfoadenite hiv correlata: si manifesta nel sieropositivo e può precedere o accompagnare<br />
l’AIDS conclamato. Tale linfoadenite , se osservata in stadi avanzati, può da sola essere<br />
sufficiente a fare diagnosi di AIDS conclamato anche se il paziente ancora non mostra<br />
infezioni opportunistiche o certi tipi di cancro tipici dell’AIDS conclamato. L’infezione da hiv<br />
cominciò a diffondersi negli anni ’80 in tutto il mondo e c’erano determinate categorie a<br />
rischio come i tossicodipendenti e gli omosessuali. C’è una fase iniziale con iperplasia<br />
esplosiva dei follicoli ma non c’è niente di specifico e non si può parlare di AIDS (può<br />
trattarsi anche solo di una normale iperplasia reattiva); successivamente c’è una fase tipica<br />
dell’AIDS caratterizzata dai seguenti elementi diagnostici:<br />
• follicololisi(la corona attorno al centro germinativo si rompe)<br />
• disordine architetturale dei linfonodi con spostamento delle venule ad alto endotelio<br />
verso l’interno (normalmente le venule ad alto endotelio si trovano nella zona<br />
paracorticale, il loro spostamento è molto caratteristico di AIDS)<br />
• Alterazione o inversione del rapporto CD4/CD8; infatti il virus ha tropismo per le CD4<br />
e le cellule dendritiche, per cui si ha un rapporto CD4/CD8 di 1:1 o addirittura<br />
invertito; tale rapporto si inverte anche nella sarcoidosi, ma qui la diminuzione di CD4<br />
scaricato da www.sunhope.it
è relativa, dovuta ad un eccessivo consumo di CD4 nei tessuti( quindi ci sono meno<br />
CD4 solo nel sangue). Invece in AIDS questa diminuzione di CD4 si riscontra in sangue<br />
e tessuti, specialmente in fase di deplezione, in cui mancano cd4 e cellule dendritiche<br />
anche a livello infonodale.<br />
Il prof commenta slide:<br />
slide1:iperplasia esplosiva di follicoli, che confluiscono; visibile anche la follicololisi.<br />
Slide2:le venule ad alto endotelio penetrano nei follicoli. Già a piccolo ingrandimento si<br />
vede che sono diminuite le cellule CD4 e quindi aumentano gli spazi ( le cd4 sono una<br />
importante componente percentuale del linfonodo).<br />
La linfoadenite di Piringer –Kutchinca è causata nel 90% dei casi da Toxoplasma Gondii,<br />
piuttosto endemica nelle zone mediterranee. E’una linfoadenopatia non esplosiva,<br />
moderata, che si manifesta nel giovane (quasi mai nel bambino) e questo può creare delle<br />
difficoltà di diagnosi differenziale con i linfomi. Non si hanno dei granulomi, ma degli<br />
accumuli molto piccoli di cellule epitelioidee ( il prof li definisce granulomi “bonsai” ma ci<br />
invita a non usare questo termine all’esame);inoltre c’è aumento di B monicitoidi; infine, c’è<br />
senioistiocitosi con linfociti anziché che con macrofagi.<br />
Slide1: cellule con citoplasma acidofilo in regione paracorticale formano i granulomi<br />
“bonsai”; cellule monocitoidi con citoplasma nel quale è possibile trovare delle<br />
immunoglobuline.<br />
scaricato da www.sunhope.it
Prof costanzo<br />
Le malattie vascolari piu’ importanti sono:<br />
aterosclerosi;<br />
ipertensione;<br />
le malattie vascolari;<br />
anomalie congenite.<br />
Le anomalie congenite non le tratteremo,le potete trovare tranquillamente sui libri, è<br />
un argomento piuttosto semplice. Tratteremo solo l’ aterosclerosi e le malattie<br />
vascolari.<br />
Le anomalie vascolari sono causa di patologie piuttosto evidenti sia nella clinica<br />
attraverso 2 meccanismi principali:<br />
1) un restringimento del lume con la manifestazione come aterosclerosi o trombosi<br />
2)indebolimento del vaso con ripercussioni sulla membrana del vaso quindi<br />
dilatazione e rottura.<br />
la localizzazione dell’ aterosclerosi è a livello dell’ intima, al di sotto dell’ endotelio<br />
c’è uno piccolo spazio occupato da tessuto connettivo poi c’è la media e l’<br />
avventizia. Le cellule endoteliali e le cellule muscolari lisce sono i protagonisti<br />
principali. le cellule muscolari lisce migrano all’ interno dell’ intima quando c’è la<br />
patologia dell’ intima cercando di ricostruire sintetizzano molecole specifiche come il<br />
collagene i proteoglicani e aiutano la formazione del nuovo tessuto perché c’è la<br />
secrezione di fattori di crescita e citochine.<br />
Aterosclerosi: il termine aterosclerosi è costituito da due parole: poltiglia e sclerosi<br />
ovvero indurimento del vaso questo porta a perdita di elasticità della parete vasale<br />
questo è il risultato di una formazione che noi abbiamo definito placca ateromasica<br />
queste placche possono essere costituite da placca semplice o andare in contro a<br />
calcificazione o aterosclerosi ialina e iperplastica che si evidenzia nei piccoli vasi.<br />
All’ inizio abbiamo ispessimento focale dell’ intima con accumulo di lipidi che<br />
possono essere molecole di colesterolo e poliesteri e si va a costituire il cosiddetto<br />
pasticcio fibroso, assume un colorito bianco giallastro ed è costituito da 3 cellule<br />
principali che sono:<br />
le cellule muscolari lisce, i macrofagi, leucociti, un tessuto connettivo di nuova<br />
formazione, deposito di lipidi in una matrice che viene chiamata extra e intra<br />
cellulare.<br />
Questo ispessimento intimale porta alla creazione di una nuova membrana, un nuovo<br />
endotelio che chiamiamo neointima ed è costituito dalla migrazione delle cellule<br />
muscolari lisce e dalla moltiplicazioni delle cellule intimali con sintesi delle proteine<br />
della matrice extracellulare.<br />
La stria lipidica è il precursore della placca ateromasica , si ritrova anche in età<br />
precoce anche a ragazzi di 20 anni.<br />
Una domanda che in genere fa il professore agli esami è :qual’ è l’ animale che non<br />
presenta la stri a lipidica? È il pollo!!(interessante)<br />
scaricato da www.sunhope.it
Le dimensioni sono variabili ,1 cm, colorito giallastro<br />
Descrivendo una slide: questo è il meccanismo con il quale si viene a costituire la<br />
placca, vedete la migrazione delle cellule muscolari lisce con un aumento dello<br />
spessore dell’ intima dove si va a determinare il cappuccio fibroso ,è l’ epitelio che si<br />
ricostituisce ex novo. Questa è la fine del processo: c’è la ricostruzione completa<br />
della placca con cappuccio fibroso e core centrale costituito da :nitriti cellulari,<br />
cristalli di colesterolo, cellule schiumose, istiociti che cercano di riparare il danno e<br />
restano intrappolati al centro della lesione. Mentre internamente c’è Una matrice<br />
extracellulare data dalle cellule muscolari lisce che sono partite dalla media.<br />
Questo è un riassunto di tutto il procedimento: si ha un danno vasale( provocato da<br />
iperlipidemia ipertensione fumo) e una prima risposta a questo danno con adesione<br />
leucocitaria risposta infiammatoria aumento permeabilità e i monociti aderiscono e<br />
migrano nel luogo del danno, successivamente le cellule dell’ intima si vanno a<br />
costituire al di sotto dell’ epitelio.<br />
questo è il primo stadio dove si evidenzia la stria lipidica con formazione del<br />
cappuccio ateromasico che come vedremo puo’ avere diversi quadri e poi si viene a<br />
determinare l’ateroma. Questo è un vaso ,dove stanno le frecce c’è una stria lipidica<br />
quali sono le lesioni dell’ aterosclerosi una volta formatisi gli ateromi:<br />
questi possono presentare delle calcificazioni che si possono evidenziare con normali<br />
rx tendono a far si che il vaso si trasformi in tubo rigido con rischio di rottura del<br />
vaso.<br />
si puo’ avere il caso in cui oltre alla placca si posso avere ulcerazione della placca<br />
con formazione di trombi che causano ischemia a valle con rottura del cappuccio<br />
fibroso e rottura della placca stessa.<br />
a volte si possono avere processi di organizzazione della placca<br />
nelle arterie di maggior calibro si possono avere atrofia del vaso a livello della media<br />
con ischemia o compressione per cui possiamo avere gli aneurismi vasali e morte del<br />
soggetto, è il caso di ricordare che in alcuni casi quando si hanno degli aneurismi il<br />
processo che sta a monte non è mai riconosciuto.<br />
Questa è un’ immagine che racchiude quello che abbiamo detto fino ad esso:<br />
la formazione della stria lipidica,una riorganizzazione della stessa ,<br />
formazione della placca, con l’ aumento della placca stessa possiamo avere<br />
aneurisma ,rottura totale del vaso,occlusione, formazione del trombo con<br />
occlusione,stenosi totale del vaso con ischemia nella zona irrorata dal vaso.<br />
Questo è un reperto microscopico:intima che è aumentata di spessore con formazione<br />
del cappuccio nella parte centrale,la parte fibrosa al di sopra del cappuccio<br />
ateromasico, queste sono placche di spessore rilevante<br />
Questo è lo stesso colorato con 1 metodo particolare per evidenziare la distribuzione<br />
dell’ elastina,questa è la membrana elastica esterna e qui la parte centrale del<br />
cappuccio ateromasico<br />
scaricato da www.sunhope.it
Qui è a maggiore ingrandiemnto si mettono in evidenza(i vuoti bianchi sono gli spazi<br />
precendetemente occupati dalle molecole del colesterolo che si scioglie in paraffina).<br />
Questa è una placca di medie dimensioni, è importante vedere non solo l’ aumento<br />
della media ma anche che l’ intima inizia a circoscrivere e incorporare la placca<br />
stessa, questo è un particolare del centro della placca ateromasica queste sono le<br />
cellule schiumose e questi gli aghi di colesterolo che sono otticamente vuoti per i<br />
motivi spiegati prima (26 min)<br />
Questo è un particolare :questi sono gli aghi di colesterolo,questo è il cappuccio e<br />
questa è una zona di fibrosi mentre questa è l’ intima e questo lo spazio della media<br />
anche qui il punto di attacco della placca,qui il tessuto è diverso qui stiamo andando<br />
in contro a un’ ulcerazione della placca dove a livello del cappuccio si va a sostituire<br />
un nuovo tessuto vascolarizzato con possibile rottura e emorragie.<br />
Qui c’è un altro esempio ed è la formazione…mentre il tessuto emorragico chiuso<br />
dall’ endotelio che circoscrive la zona tende a chiudere il vaso,questo è il caso in cui<br />
la neoformazione può staccarsi e andare in circolo come embolo.<br />
Questo è un altro esempio una situazione di completa occlusione del vaso dove<br />
vedete l’ ateroma è al di sotto il trombo è superiormente mentre questo piccolo<br />
coagulo che puo’ andare in contro a riorganizzazione o rottura del coagulo stesso e<br />
ritorniamo all’ esempio precedente.<br />
A livello clinico possiamo evidenziare infarti ictus e quando la media perde la sua<br />
elasticità possiamo avere aneurisma aortico. Per quanto riguarda la diminuita<br />
perfusione possiamo avere vasculopatia agli arti inferiori, occlusioni di grossi vasi<br />
come la mesenterica, morte cardiaca improvvisa, vasculopatia coronarica.<br />
Prima hanno una distribuzione focale e successivamente invasione della media con i<br />
classici aneurismi. Nelle arterie di piccolo calibro gli ateromi vano incontro a<br />
occlusione del vaso stesso e quindi avremo lesioni ischemiche mentre nei vasi di<br />
grande calibro possiamo avere aneurismi o trombi.<br />
Riepilogando le caratteristiche piu’ importanti dell’ ateroma sono la stenosi che tende<br />
a chiudere parzialmente o totalmente il flusso con ischemie o infarto del tessuto<br />
servito;una trombosi dove un’ ulcerazione endoteliale stimola la formazione di<br />
trombi che possono occludere il vaso con effetti gravi a distanza a seconda dell’<br />
entità del coagulo, oppure possiamo avere gli aneurismi per indebolimento del vaso<br />
stesso.<br />
Questa è una classificazione che sta nei testi perché clinicamente la malattia si<br />
manifesta con una fase silente invece noi grazi alle autopsie siamo riusciti a<br />
ricostruire la lesione.<br />
La lesione di fase prima: presenza di macrofagi isolati con molecole di colesterolo.<br />
Il secondo stadio: inizio e preparazione della stria lipidica, che vedete è ancora<br />
clinicamente silente<br />
Terzo stadio: accumulo di lipidi maggiore,c’è la costituzione della placca con<br />
componente extracellulare a livello della media.<br />
Quarto stadio: composizione dell’ ateroma.<br />
scaricato da www.sunhope.it
Infine c’è la costituzione del cappuccio ateromasico con processi di fibrosi in un<br />
secondo momento come risposta alla durata del danno.<br />
Quinto stadio: formazione del trombo di colesterolo o emorragico o altro.<br />
La malattia si manifesta clinicamente se c’è un aneurisma o altre complicanze.<br />
Fattori di rischi:<br />
l’ eta, la stria lipidica si forma anche precocemente nei giovani(reperto autoptico)<br />
sesso maschile; predisposizione familiare;stile di vita;dieta;abitudini personali;<br />
elevata iperlipidemia con elevata colesterolemia ,elevati livelli di ldl, ipertensione,<br />
fumo di sigaretta, diabete, iperomocisteinemia, fattori che agiscono sulla<br />
coagulazione o altri fattori.<br />
Le cause: noi anatomo patologi la identifichiamo in un’ ipotesi di reazione a danno<br />
vasale ,l’ aterosclerosi è una risposta infiammatoria a livello del danno vasale<br />
precisamente dell’ endotelio, il danno endoteliale porta a disfunzione dell’ endotelio<br />
con aumento della permeabilità e adesione e migrazione dei leucociti<br />
successivamente c’è un apporto di ldl ,successivamente adesione di mociti e altri<br />
leucociti seguito da migrazione con trasformazione in macrofagi adesione di piastrine<br />
e leucociti per fattori che si liberano da piastrine e macrofagi si ha la migrazione delle<br />
cellule vascolari lisce a livello dell’ intima con proliferazione delle stesse e<br />
costituzione del cappuccio ateromasico e vanno a definire il materiale extracellulare.<br />
(39.00)<br />
Le vasculiti:<br />
inquadrare tutte le patologie da un punto di vista anatomo patologico no clinico.<br />
Alcune vasculiti sono correlate ad alcune malattie.<br />
Aspetto clinico:febbre ,mialgia, artralgia, malessere generale<br />
Aspetto istologico:danno della parete vasale puo’ essere provocato da agenti infettivi<br />
o da processi infiammatori mediati immunologicamente<br />
Le cause:possiamo avere cause infettive, causa immunologica, e una causa ignota<br />
Classificazione: 3 gruppi a seconda delle 3 cause. ma da un punto di vista anatomo<br />
patologico è meglio la classificazione che si basa sulla morfologia del vaso. Dei<br />
grandi vasi,dei vasi medi e dei piccoli vasi.<br />
Per i grandi vasi abbiamo:<br />
l’ arterite a cellule giganti è una vasculite granulomatosa in genere dell’ aorta e dei<br />
sue rami principali con una predilezione per le sue collaterali exracraniche, in genere<br />
si manifesta in pazienti oltre 50 anni e si associa a una polimialgite reumatica.<br />
Arterite di (takaiazu)???……:infiammazione granulomatosa dell’ aorta o rami<br />
principali colpisce pazienti di età inferiore a 50 anni.<br />
Per i vasi di medio calibro abbiamo:<br />
la poliaerterite nodosa<br />
la malattia di Kawasaki<br />
scaricato da www.sunhope.it
La poliartrite nodosa: è un’infiammazione necrotizzante(piccole e medie arterie) non<br />
è associata alla patologia delle glomerulonefriti ma la posisamo ritrovare in alcune<br />
patlogie cutanee<br />
La malattia di Kawasaki: associata a patologie cutanee, spesso sono interessate le<br />
coronarie, si puo’ spesso ritrovare nel bambino.<br />
Per i vasi di piccolo calibro:<br />
…….:c’è un’ infiammazione granulomatosa che interessa esclusivamente l’ apparato<br />
respiratorio portando delle lesioni necrotizzanti, è presente anche nelle<br />
glomerulonefriti necrotizzanti.<br />
sindrome di....strauss: la classica infiammazione di eosinofili, è associata anche a<br />
un’infiammazione granulomatosa respiratoria, spesso è associata all’ asma nei<br />
bambini.<br />
Poliangite microscopica: si manifesta con depositi di IG porta a un’arterite quasi(?)<br />
necrotizzante<br />
Porpora di henloch sheloch: ci sono depositi di immunocopmplessi di IGa<br />
caratterizza alcune patologie del tratto gastroenterico, della cute e renale ,delle<br />
glomerulonefriti<br />
Vasculiti crioglobulinemiche essenziali: a livello cutaneo e del glomerulo con<br />
deposizione di complessi immuni di crioglobuline o con crioglobulinemia<br />
esclusivamente sierica<br />
Angioite luecocitoplastica cutanea:si manifesta a livello cutaneo e glomerulare con<br />
prevalenza delle cellule leucocitarie con degranulazione delle cellule leucocitarie e<br />
percio’ leucocitoplastica (1.00).<br />
Qui c’è un’altra classificazione che troviamo spesso nei testi dove associano le cause<br />
e la grandezza dei vasi ed è quindi più completa ma l’ ho portata giusto per farvela<br />
vedere(grazie !!)<br />
Per quanto riguarda l’ arterite a cellule giganti: è la più comune di queste patologie, è<br />
un processo infiammatorio granulomatoso che colpisce le arterie elastiche grandi<br />
medie e piccole con sede esclusivamente a livello dei vasi cranici temporale<br />
vertebrali e oftalmico.le arterie possono sviluppar un restringimento nodulare perché<br />
c’è una riduzione del lume e c’è una deposizione di alcuni neoformazioni che<br />
chiameremo trombi ma da non confondere con i trombi arteriosclerotici infatti la<br />
diagnosi differenziale va fatta prorpio con l’ aterosclerosi. gli aspetti microscopici<br />
possono essere classificati in base a dei quadri<br />
1)arterite granulomatosa a punta …:abbiamo un processo infiammatorio dove è<br />
confinato a livello della media(no del’ intima come l’ aterosclerosi)ma la<br />
caratteristica importante è una lesione che parte a livello della membrana elastica<br />
interna, c’è un infiltrato infiammatorio cellulare dove predominano dei linfociti<br />
plasmacellule e macrofagi essendo una infiammazione granulomatosa abbiamo la<br />
presenza delle cellule tipo langhans tutto ciò proprio a livello del confine tra intima e<br />
media e quindi in alcune zone c’è la rottura della membrana elastica esterna ciò porta<br />
a una reazione della zona dove c’è la lesione.<br />
scaricato da www.sunhope.it
Un secondo quadro è dato dall’a arterite atipica: è atipica perché non è granulomatosa<br />
,se ci sono sono rarissimi, c’è una panarterite con infiltrato costituito da linfociti<br />
macrofagi neutrofili ma non le cellule di langhans.e c’è necrosi fibrinoide.<br />
Terzo caso,arterite a cellule giganti: si crea un ispessimento intimale con una cicatrice<br />
a livello della media data dalla formazione, maturazione di fibre collagene che vanno<br />
a sostituire le lamine elastiche del vaso con rivestimento fibromuscolare per cascate<br />
di citochine e fattori di crescita durante la flogosi attiva e perciò la formazione dei<br />
classici noduli. La patogenesi è sconosciuta ma si pensa che ci sia un danno<br />
provocato da una reazione immunologia al livello della parete arteriosa .<br />
Descrizione di immagini:<br />
Questo è un quadro microscopico:la colorazione è bicromica il contorno piu’ marcato<br />
è la lamina esterna la rottura della lamina per invasioned ella flogosi e localizzazione<br />
del processo flogistico a livello della media vedete il vaso quasi ostruito la media<br />
travolta con oinfiltrazione anche dell’ intima c’è anche una partecipazione dell’<br />
avventizia cpon invasione a tutto il vaso questa è una cellula gigant eocn nuclei alla<br />
periferia quindi c’è infiammazione granulomatosi,qui c’è una colorazione speciale<br />
che mettein evidenza l’ elastina, vedete in alcuni casi la membrana elastica esterna è<br />
interrotte e in alcuni casi c’è la chiusura del vaso per l’ infiltrazione del processo<br />
flogistico anche qui la freccia indica la rottura della lamina esterna,qua c’è una<br />
necrosi fibrinoide con invasione a tutto spessore.infiltrato granulomatoso che invade<br />
completamente. Qui la media si è ridotta mentre nell’a avventizia c’è la migrazione<br />
dell’ infiltrato.qui vedete c’è una colorazione specile vedete l’0 infiammazione<br />
granulomartosa con rottura della lamina esterna .questa è l’ occlusione di 1 vaso d<br />
anon confondere ocn arteriosclerosi qua vedete la caratteristica delle cellule del<br />
langans che ci fanno capire che è un trombo ma di un infiltrato granulomatosi di<br />
vasculite.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong> 18\03\2011<br />
Oggi chiudiamo il capitolo delle linfoadeniti per passare poi ai linfomi.<br />
Linfoadenite dermatopatica.<br />
Allora, questa che vedete è una linfoadenite frequentissima; già vi ho detto, d’altronde che la<br />
patologia linfoghiandolare è la patologia in senso assoluto più frequente; da cosa è caratterizzata<br />
questa? Dal fatto che le dermatiti di vario tipo, la psoriasi, le eritrodermie, dermatiti esfoliative, cioè<br />
quelle dermatiti e dermatosi che provocano prurito; il prurito poi provoca grattamento e questo<br />
determina un traumatismo a livello locale che consente la distruzione di alcune cellule, con perdita<br />
di lipidi e di melanina; questa melanina, poi, attraverso i linfatici della cute va ai linfonodi e<br />
determina questa linfoadenite; può succedere che siccome c’è un periodo di latenza tra la dermatite<br />
e la linfoadenopatia, il paziente stesso non riferisce proprio all’anamnesi di aver avuto una<br />
dermatite pruriginosa, anche perché magari è guarita con trattamenti opportuni e quindi non ricorda<br />
più e le variazioni linfoghiandolari possono spesso essere eccessive, abbiamo anche delle<br />
megalinfoadenomegalie che possono destare allarme nel paziente e nel clinico, perciò si arriva alla<br />
biopsia. Cosa osserviamo a livello bioptico? La cosa più seria è che possiamo avere un<br />
sovvertimento completo dell’architettura linfoghiandolare, per esempio non si vedono bene i<br />
follicoli, il linfonodo è un po’ stravolto dall’accumulo di queste cellule chiare, la maggior parte<br />
delle quali sono cellule dendritiche di cui abbiamo parlato, S-100 positive e che si accumulano per<br />
smaltire questi depositi lipidici che noi vediamo, ma soprattutto vediamo i depositi di melanina.<br />
Quando vediamo questo sappiamo che è una linfoadenite dermatopatica.<br />
[IMMAGINE] Qua vedete un linfonodo, questa è la capsula, qui vedete delle strutture linfoidi,<br />
addirittura non ci sono più i follicoli secondari che frequentemente troviamo nei linfonodi mentre<br />
qui vediamo questo aspetto un po’ chiaro delle cellule che si accumulano sia a livello corticale che<br />
paracorticale, queste caratteristiche ti danno l’impressione di una cosa seria, perché c’è lo<br />
sconvolgimento dell’architettura e c’è una popolazione che infiltra diffusamente i linfonodi; se<br />
andiamo a vedere a più forte ingrandimento qui vedete del pigmento melanocitario e qui vedete<br />
queste cellule più chiare, le cellule non le vedete ancora perché è un piccolo ingrandimento, se<br />
andiamo a fare un grande ingrandimento qui vedete la melanina che si accumula nelle cellule che<br />
sono cellule dendritiche, difficili da dimostrare, ma hanno dei nuclei chiari, sono positive al CB-1a,<br />
così come sono positive all’S-100 e allora abbiamo la conferma che si tratta di un accumulo di<br />
queste cellule con melanina e tutto il resto ed il quadro della linfoadenite dermatopatica a questo<br />
punto è completo.<br />
Altre linfadeniti:<br />
Malattia di Rosai-Dorfman<br />
Tipica dell’età pediatrica che si presenta con un esordio clinico anche violento, ma poi, guarisce da<br />
sola. Si presenta con un ingrossamento massivo dei linfonodi del collo e coinvolge tutte le mucose,<br />
quindi la congiuntiva, la mucosa orale, del labbro, con lesioni eritrodermiche, desquamative, quindi<br />
il quadro di una sindrome catarrale generale con una linfoadenopatia generalizzata. Se andiamo a<br />
fare una biopsia linfoghiandolare (in un bambino questo quadro desta allarme, soprattutto per chi<br />
non conosce questa patologia) troviamo un quadro allarmante perché vediamo i seni linfatici zaffati<br />
da cellule macrofagiche un po’ anomale, atipiche decisamente, le quali hanno un’evidente azione<br />
macrofagica e all’interno di queste cellule vediamo dei detriti cellulari e dei linfociti, un fenomeno<br />
che ha un nome impronunciabile e si chiama “enperì covè”[(?)ho scritto come ha pronunciato]<br />
ovvero la presenza di nuclei picnotici nei linfociti e all’interno del citoplasma.<br />
Malattia di Kikuchi<br />
Molto più frequente in Giappone, ma si verifica anche dalle nostre parti, è una linfoadenite<br />
necrotizzante, anche questa caratterizzata, a volte, da linfociti circolanti atipici; fa parte del gruppo<br />
di malattie senza ancora una precisa definizione eziopatogenetica.<br />
scaricato da www.sunhope.it
Malattia di Kawasaki<br />
E’ una vasculite trombotica perché coinvolge l’intera parete dei vasi di piccolo calibro e che spesso<br />
esordisce con una linfoadenite, anche se poi è sistemica, è quindi una malattia su base<br />
autoimmunitaria.<br />
[IMMAGINI] Ecco la malattia di Rosai-Dorfman: vedete che c’è un ingrossamento dei linfonodi, a<br />
volte anche dei fenomeni erosivi o ulcerativi e la partecipazione degli occhi, delle palpebre, delle<br />
congiuntive e un grossi pacchetti linfoghiandolari; cosa straordinaria è che questo guarisce entro<br />
qualche settimana.[IMMAGINE] E qui vediamo invece come appare il quadro morfologico: questi<br />
sono dei seni linfatici enormemente dilatati, anche qui l’architettura è scomposta perché i seni<br />
linfatici si ingrandiscono enormemente e sono zaffati di queste cellule che adesso<br />
vediamo[IMMAGINE] vedete queste cellule hanno un ampio citoplasma, è una malattia ancora<br />
sconosciuta, abbiamo qualche cosa, ma non abbiamo ancora il quadro completo, vediamo<br />
all’interno del citoplasma, vedete, questi sono tutti nuclei di linfociti moribondi o anche già morti e<br />
qui vedete anche una cellula gigante plurinucleata, vedete c’è una cavità lisosomiale e all’interno<br />
c’è un linfocita e ci sono anche detriti cellulari, queste cellule sono S-100 positive a conferma che,<br />
probabilmente, appartengono anch’esse alla linea dendritica.[IMMAGINE] La malattia di Kikuchi è<br />
molto rara da noi, caratterizzata da un’area di necrosi centrale, circondata da macrofagi,<br />
immunoblasti e cellule linfocitarie e plasmacellulari, anche questa ha un decorso benigno, si<br />
presenta con febbre modesta e in realtà tutte e tre queste linfoadeniti che vi ho descritto possono<br />
associarsi a dei rush cutanei, per cui magari in un bambino si può pensare si tratti di una malattia<br />
esantematica e invece non è così. La malattia di Kawasaki presenta alcune caratteristiche cliniche<br />
caratteristiche: la lingua a fragola, perché si sollevano tutte le papille, poi il labbro è rosso,<br />
screpolato e poi vediamo questi rush cutanei, se andiamo a osservare l’esame istologico vediamo<br />
dei vasi che tendono a trombizzare e tutta la parete è coinvolta da un infiltrato costituito da linfociti<br />
e granulociti, si tratta di una vasculite autoimmune che coinvolge anche vasi e linfonodi.<br />
Malattia di Castleman<br />
E’ ancora una malattia affascinante perché ci presenta dei problemi. Esistono due forme: una forma<br />
localizzata- a me sono capitati diversi casi- e una forma multicentrica, ovvero che coinvolge più<br />
stazioni, la forma multicentrica è caratteristica dei soggetti sieropositivi AIDS e molto spesso<br />
l’associazione con questa malattia rappresenta un aggravamento della prognosi perché esprime un<br />
disordine del sistema immunitario, questo nei pazienti con AIDS, mentre la forma localizzata è una<br />
forma benigna, talvolta può venire con una massa mediastinica, a me è capitato un caso con<br />
un’enorme forma mediastinica che comprimeva le strutture mediastiniche; in entrambe le forme il<br />
quadro morfologico è lo stesso: si vedono delle strutture follicolari, follicoli secondari centrati da<br />
dei vasi, proprio delle arteriole, in un’architettura che ricorda la milza, in cui voi sapete che nella<br />
polpa bianca il follicolo è centrato da un’arteriola e una delle ipotesi è che possa trattarsi di<br />
un’amartoma, cioè di un’eterotopia di tessuto splenico in un’arteria anomala, ma in realtà non è<br />
così, perché poi si presenta anche con una sintomatologia: c’è febbre, anemia,<br />
ipergammaglobulinemia e quella massa mediastinica di cui vi parlavo, ovviamente se rimuoviamo<br />
questa massa il paziente non ha più problemi. La diagnosi non è semplice, ma la malattia è benigna.<br />
Esiste anche una varietà di questa forma che si accompagna ad una grande ricchezza di<br />
plasmacellule, la “varietà plasmacellulare”ma è una sottovarietà perché in tutte queste forme c’è<br />
sempre quel quadro angiofollicolare che è la caratteristica esclusiva di questa patologia, eccolo<br />
qui[IMMAGINE], qui vedete una struttura che sembra una milza, quasi una polpa bianca,<br />
all’interno vediamo delle strutture ampie che sono dei vasi, un’altra caratteristica comune con la<br />
milza è che non ha i seni linfatici linfoistoghiandolari; ecco qui cosa succede all’interno del<br />
follicolo, vedete, questo è il centro germinativo, all’interno penetrano questi vasi che a volte<br />
formano come dei glomerulomi, dei grovigli vascolari e hanno una tipica struttura “ad anfiteatro”,<br />
cioè tutti i linfociti si dispongono intorno[IMMAGINE]questa è la varietà plasmacellulare perché è<br />
ricca di plasmacellule.Questo è un riepilogo:<br />
Linfoadeniti granulomatose, sono tutte quelle di cui abbiamo parlato:<br />
scaricato da www.sunhope.it
- da materiale estraneo, compresi coloranti e tatuaggi;<br />
- con necrosi ascessuale, la cosiddetta linforeticulosi da inoculazione,il linfogranuloma<br />
venereo ed altre linfoadeniti meno frequenti tra cui la tularemia o la Yersinia, che dà un<br />
quadro da addome acuto che è in realtà una linfadenite mesenterica che determina anche<br />
necrosi sia dell’appendice, sia di altri organi, di altre strutture intestinali e può esordire<br />
anche con una peritonite con difficile individuazione della Yersinia;<br />
- con necrosi non ascessuale, la tubercolosi, la sarcoidosi, attualmente sto studiando una<br />
famiglia con linfogranulomi nelle sedi più inopportune, il padre in sede laterocervicale, il<br />
figlio al cuoi capelluto, la madre in sede ascellare, siccome è una famiglia di provincia<br />
desumo che ci sia qualche corpo estraneo o qualche insetto che io non conosco, ho<br />
consigliato di fare un’indagine sierologia, non è sicuramente tubercolosi, ma tra i casi che<br />
possono venire all’osservazione anche la brucellosi rientra in questo capitolo che è una<br />
classica malattia degli allevatori di bestiame;<br />
- linfoadeniti non granulomatose: mononucleosi, della Piringer –Kuchinka, linfoadenite<br />
correlata ad HIV, della Rosai-Dorfmann, Kikuchi, malattia di Castleman e così via.<br />
Abbiamo esaurito così un argomento molto complesso, in realtà ne esistono tantissime. Sui libri<br />
di testo spesso si fa l’errore di classificare per eziologia, dando l’impressione che l’anatomo<br />
patologo sempre possa risalire all’eziologia, ma non è così; per esempio, nel caso della<br />
toxoplasmosi, nel 90% corrisponde a Toxoplasma, ma c’è un 10% che non corrisponde; inoltre<br />
esistono una marea di linfadeniti virali; in realtà l’anatomopatologo da l’input, questo quadro è<br />
così e così, si consigliano le seguenti indagini(SPECT, o altro).Ad esempio quando facciamo<br />
diagnosi di Piringer-Kuchinka,chiediamo al clinico anche il test per il toxoplasma.<br />
Esistono anche delle linfoadenopatie cosiddette “reattive”, nei bambini possiamo trovare il<br />
cosiddetto “timo linfatico”, caratterizzato da un’iperplasia dell’anello del Waldeyer di tutti i<br />
linfonodi e sono quasi reattivi, ci sono dei soggetti predisposti, “stato linfatico” si chiamava una<br />
volta, ora non conosco il termine moderno. Abbiamo anche la linfoadenopatia reattiva ai<br />
tumori, il linfonodo che si toglie quando si fa l’intervento di chirurgia di un cancro nelle varie<br />
sedi anche quando non è sede di metastasi manifesta una reattività; ricordate all’inizio, parlando<br />
del linfonodo normale, abbiamo parlato di una reattività di tipo B e di tipo T, la reattività con<br />
prognosi migliore è quella legata ai linfociti T, paradossalmente i linfociti B non sono efficaci;<br />
quindi quando vediamo una iperplasia delle aree B nei linfonodi adiacenti ad un cancro, non è<br />
un buon segno, se , però, troviamo una forte reattività T, possibilmente con cellule epitelio idee<br />
è un buon segno, vuol dire che il linfonodo reagisce bene e difficilmente è sede di metastasi.<br />
Abbiamo poi una forma che può derivare anche da linfonodi piccoli, quando la diagnosi non è<br />
ancora conclamata, l’iperplasia linfoide è detta “atipica”, che può avere molte cause, che però<br />
va fatta in via del tutto eccezionale perché è imprecisa. Linfadeniti iatrogene, tra cui alcune<br />
molto note come quella da methotrexate, che rappresenta un farmaco di terzo-quarto livello nel<br />
trattamento delle psoriasi gravi, aggressive, o nell’artrite reumatoide; nei trapiantati; poi<br />
abbiamo le forme nei pazienti con trattamento per piccolo male,soprattutto con<br />
anticonvulsivanti che danno un quadro di linfadenite addirittura pseudolinfomatosa. Questo<br />
succede pure nel lupus eritematoso,però se togliamo il farmaco,il linfonodo ritorna nelle<br />
condizioni normali. Ci sono anche forme legate al segreto,un farmaco molto usato,o<br />
all’indometacina. Le collagenopatie. Talvolta c’è un’altra lesione che non conosciamo<br />
bene,dove i seni linfatici,che sono dei seni che hanno solo un endotelio sottile, seni linfatici<br />
intermedi e marginali,invece ci sono delle patologie caratterizzate da una trasformazione<br />
vascolare dei seni,cioè questi anziché avere solo endotelio,acquisiscono la parete propria dei<br />
vasi,con tutti gli strati. Perché avvenga questo non lo sappiamo.<br />
E poi abbiamo centinaia di eterotopie,che sono localizzazioni anomale di tessuti che<br />
normalmente non dovrebbero stare qui. Tra quelle più frequenti abbiamo l’endometriosi,mi è<br />
capitato un caso di una donna con linfoma di Hodgkin, era stata bene per diversi anni,si ingrossa<br />
scaricato da www.sunhope.it
enormemente il linfonodo inguinale,tutti pensano a una recidiva,che in questi casi non è rara,ma<br />
alla biopsia linfoghiandolare si vede che non era una recidiva,ma un’endometriosi.<br />
E l’eterotopia salivare,che riguarda i linfonodi laterocervicali alti. Abbiamo già parlato della<br />
presenza di isole di tessuto di ghiandole salivari all’interno di linfonodi laterocervicali,cosi<br />
come è frequente la presenza di tessuto linfoide all’interno di ghiandole salivari.<br />
Linfomi di Hodgkin.<br />
Sono i linfomi più facili. Tutto risale a questo Thomas Hodgkin…(storia di Hodgkin…).Una<br />
volta i linfonodi si chiamavano “ghiandole assorbenti”,perché si riteneva che la loro unica<br />
funzione fosse di assorbire la linfa. Si conservano ancora in formalina alcuni casi di linfoma di<br />
Hodgkin.Anni fa ci fu un gruppo che volle rivedere questi 7 casi, e videro che 4 di questi erano<br />
casi di mononucleosi,con cellule di Reed-Stenberg simili a quelle del linfoma.<br />
Marcello Malpighi fu uno dei padri fondatori dell’anatomia patologica italiana.<br />
Questo linfoma rappresenta solo il 20-30% dei linfomi non-Hodgkin,anche se qualche testo non<br />
aggiornato riporta un’incidenza più elevata. Se andiamo a vederel’incidenza tra HD(Hodgkin<br />
desease) e NHL(non-Hodgkin lymphoma),vediamo 2 picchi di incidenza:uno in età giovanile,in<br />
cui rientrano anche le donne e uno in età più avanzata verso gli 80 anni. L’incidenza è in<br />
aumento,soprattutto il picco dell’età avanzata;mentre la mortalità è in netta diminuzione,grazie<br />
ai progressi che ci sono stati nella terapia. Negli anni 50-60 il linfoma di Hodgkin era<br />
mortale,oggi non lo è più. I rapporti tra linfomi di Hodgkin e non-Hodgin sono molto curiosi,e<br />
ancora oggi necessitano di una definizione.<br />
I linfomi non-Hodgkin si possono presentare insieme ai linfomi di Hodgkin e si chiamano<br />
linfomi composti.Sono cose che accadono raramente,ma sono una testimonianza di come i<br />
confini tra questi due linfomi non siamo cosi netti. I pazienti con linfoma di Hodgkin,nella loro<br />
storia clinica,hanno un rischio maggiore di presentare un linfoma non-Hodgkin. Alcuni casi di<br />
linfomi di Hodgkin possono evolvere in non-Hodgkin,ache se sono casi molto rari. E poi ci sono<br />
casi in cui la diagnosi differenziale è molto difficile.<br />
Vediamo le caratteristiche cliniche e anatomopatologiche essenziali del linfoma di Hodgkin,i<br />
sintomi cosiddetti costituzionali. Quando faremo la stadi azione,vedremo che le lettere a e b<br />
indicano rispettivamente sottostadi senza e con sintomi costituzionali. In genere questa<br />
incidenza varia in base all’istotipo e ne parleremo tra poco. Questi sintomi sono: febbre<br />
intermittente,febbricola,caratteristica anche dei linfomi non-Hodgkin;quindi non è la febbre alta<br />
che spaventa,ma le febbricole,perciò la mononucleosi desta allarme; sudorazione notturna;<br />
sindrome della vena cava superiore,che si ha quando c’è un coinvolgimento del mediastino e<br />
ostruzione della vena cava superiore che determina un rallentato svuotamento e quindi gonfiore<br />
delle regioni testa-collo; perdita di peso; prurito.<br />
Gli aspetti morfologici distintivo sono: la presenza di cellule di Reed-Stenberg e delle cellule di<br />
Hodgkin,che sono cellule mononucleate. C’è una particolarità,queste cellule rappresentano una<br />
piccola parte della popolazione cellulare del linfonodo,costituita per la maggior parte da cellule<br />
dette “di accompagnamento”:intorno a queste cellule anomale si raccolgono e si attivano<br />
macrofagi,granulociti,ecc. Il virus di Epstein-Barr,responsabile anche della mononucleosi, si<br />
ritrova nel 50% dei casi di linfoma di Hodgkin,soprattutto in particolari forme come la sclerosi<br />
nodulare e la cellularità mista,ma possiamo trovarlo anche in forma episomiale e possiamo<br />
avere delle conforme attraverso l’espressione dell’RNA del virus,soprattutto vedendo la<br />
proteina r e la mnp1,cioè la proteina latente di membrana che possiamo identificare attraverso<br />
tecniche molecolari nei tessuti ddei soggetti con linfoma di Hodgkin. È ancora dda spiegare<br />
perché in alcuni casi abbiamo la mononucleosi e in altri il linfoma. Vi ricordo però che<br />
l’EBV,anche se in forma silente,è presente nella maggior parte della popolazione.<br />
Eccola qui,questa è la cellula di Reed-Stenberg (foto). L’aspetto più caratteristico di questa<br />
cellula è che è plurinucleata. La forma più classica è chiamata “mirror cell”,cellula<br />
specchio,perché i due nuclei sono uguali ed è come se un nucleo si guardasse allo specchio. La<br />
scaricato da www.sunhope.it
caratteristica essenziale è che presenta un meganucleolo acidofilo. Questa è la cellula<br />
diagnostica dei linfomi di Hodgkin, diagnostica nel senso che se non la troviamo non possiamo<br />
fare diagnosi di linfoma di Hodgkin,ma se la troviamo non è detto che sia necessariamente un<br />
linfoma,perché troviamo anche nella mononucleosi e in altre linfadeniti virali ed<br />
eccezionalmente in alcune forme di non-Hodgkin, per cui la diagnosi non si deve basare solo su<br />
queste cellule,ma su questa popolazione di accompagnamento che non ritroviamo in altre<br />
patologie.<br />
Qui abbiamo la cosiddetta sub variante polimorfa,polimorfa perché ha molti nuclei, ha una certa<br />
irregolarità, e poi esistono delle varianti di cellule di Reed-Stenberg che si trovano solo in un<br />
particolare istotipo come vedremo tra poco,è quando la cellula di Reed-Stenberg giace come in<br />
una lacuna,queste cellule di Reed-Stenberg si chiamano cellule lacunari. Vedete,c’è uno spazio<br />
chiaro intorno,che sembra un edema ma non lo è, è un artefatto,che si realizza solo in un istotipo<br />
particolare di linfoma di Hodgkin,di cui parleremo più avanti. In poche parole è un artefatto<br />
legato alla fissazione in formalina: questo tipo di fissazione,che è la più usata nei reparti di<br />
anatomia patologica al mondo,determina una retrazione di citoplasma; retraendosi il citoplasma<br />
determina la formazione di un vacuolo intorno alla cellula e la cellula sembra giacere in una<br />
lacuna. Questa cellula prende appunto il nome di cellula lacunare,ma è sempre la cellula di<br />
Reed-Stenberg. C’è una domanda che non si capisce…<br />
La cellula di Hodgkin non è altro che questa cellula mononucleata,però presenta le stesse<br />
caratteristiche,cioè il macronucleolo, il nucleo chiaro. Ma chiariremo il giallo della cellula di<br />
Reed-Stenberg più avanti. Da studi di microscopia elettronica è venuto fuiori che quella che noi<br />
vedevamo come “mirror cell” in realtà è un’apparenza,in effetti è una cellula come se avesse un<br />
nucleo cilindrico a ferro di cavallo,per cui quando la lama taglia,noi vediamo due nuclei singoli.<br />
Quando muoiono le cellule di Reed-Stenberg diventano mummificate,il nucleo va in apoptosi e<br />
diventa picnotico,e il citoplasma si addensa. Però non sono diagnostiche. La caratteristica<br />
immunoistochimica è che queste cellule presentano dei marcatori specifici,uno di questi è il<br />
CD30. Però il CD30 non è una caratteristica solo delle cellule di Reed-Stenberg,perché si è visto<br />
che è anche degli immunoblasti,quindi è passato un po’ in secondo piano. Marcatore più<br />
specifico è questa particolare proteina,la fascina. Quindi se abbiamo dei dubbi,possiamo<br />
ricorrere a questi marcatori specifici.<br />
Vedete da questa immagine presa da …. del 2009,si è chiarito perché c’è questa popolazione di<br />
accompagnamento,vedete al centro quelle due ‘uova’. Questa cellula ha la capacità di secernere<br />
svariate sostanze, chemochine,per cui esercita quella attrazione che noi non capivamo, verso i<br />
fibroblasti,i granulociti eosinofili,i mastociti,le cellule CD4,le cellule dendritiche e cosi via. Non<br />
sappiamo ancora se questo rappresenta un meccanismo di difesa dell’organismo o comunque di<br />
questa cellula che è impazzita,perché la cellula tumorale è questa qua,tutto il resto della<br />
popolazione non è neoplastica,perciò la chiamiamo popolazione di accompagnamento,è una<br />
popolazione reattiva,attivata,ma non neoplastica. Nella maggior parte dei casi la cellula di Reed-<br />
Stenberg è negativa per il CD20,che insieme al CD19 è un marcatore dei linfociti B,tutt’intorno<br />
vedete questi linfociti B attivati che sono richiamati da questa azione attrattiva delle cellule di<br />
Reed-Stenberg. Nel 10-15% dei casi,la cellula può esprimere il CD20 che è un marcatore di<br />
membrana. Come ci spieghiamo questa cosa? Innanzitutto che la cellula di Reed-Stenberg è<br />
neoplastica non si discute,ma presenta alcune mutazioni caratteristiche per cui anche se nel 90%<br />
dei casi la cellula non esprime il CD20, è un linfocita B,perché si è visto che questa cellula<br />
subisce delle mutazioni geniche che vengono a bloccare l’espressione di alcuni fattori di<br />
trascrizione chiamati OCT-2 e BOB-1 che sono implicati nella produzione di CD20,allora<br />
diciamo che è una cellula B,che nella maggior parte dei casi ha perso la capacità di esprimere<br />
CD20;in alcuni casi questa perdita non è completa,ma solo in una minoranza dei casi possiamo<br />
trovare qualche cellula CD20 positiva. Quindi è un linfocita B difettoso. Questo vuol dire che<br />
nella maggioranza dei casi se andiamo a fare il CD20 troviamo negativo,ma soprattutto che se<br />
andiamo a cercare attraverso anticorpi il BOB-1 e l’OCT-2 troveremo che è negativo.<br />
scaricato da www.sunhope.it
Questo la può differenziare dalle cellule molto simili che troviamo nella mononucleosi infettiva.<br />
Quali sono gli istotipi del linfoma di Hodgkin.<br />
Per molti anni sono stati 4 (che troverete nei testi come forme classiche) ma se ne è aggiunto un<br />
quinto che si chiama “predominanza linfocitaria”. È una minoranza, (5% dei casi). Quali sono le<br />
caratteristiche essenziali di questo istotipo (io vi spiego e vi chiedo solo l’essenzialità) . Questo<br />
istotipo ha una elevata densità cellulare di linfociti e istiociti. Le cellule di Reed-Stenberg sono<br />
rare,quindi ha una prognosi migliore,proprio perché le cellule tumorali sono poche. L’ipotesi è<br />
che questa ricchezza di linfociti sia determinata da un equilibrio che si raggiunge proprio per la<br />
scarsità di cellule tumorali.<br />
La “sclerosi nodulare” è la forma più frequente. Il primo picco si ha nei giovani e c’è una<br />
leggera prevalenza nel sesso femminile,mentre per tutte le altre forme predomina il sesso<br />
maschile. La caratteristica di questa forma è che il linfonodo viene come suddiviso in noduli da<br />
tralci di connettivo. All’interno dei noduli troviamo il tessuto tipico dei linfomi di Hodgkin cioè<br />
lke cellule di Reed-Stenberg con le cellule di accompagnamento, e troviamo soprattutto quelle<br />
cellule che prima abbiamo definito lacunari. Questo è l’istotipo in cui le cellule di Reed-<br />
Stenberg presentano questo artefatto,cioè questa retrazione citoplasmatica. Questa è una forma<br />
in cui non è raro anche il coinvolgimento dei linfonodi mediastinici.<br />
La “cellularità mista” è la seconda forma per incidenza perché si manifesta nel 15-30% dei casi.<br />
È proprio il linfoma di Hodgkin classico,perché qui troviamo molte cellule di Reed-Stenberg e<br />
molte cellule di accompagnamento molto diverse tra loro. È il quadro caratterizzato dalla<br />
maggiore varietà di cellule, vediamo soprattutto molti eosinofili,quindi molte cellule di Reed-<br />
Stenberg.<br />
La “deplezione linfocitaria” è la forma più grave,ma fortunatamente riguarda poco meno<br />
dell’1% dei casi. È una forma caratterizzata appunto da una deplezione cellulare,e ce ne<br />
accorgiamo perché le cellule sono separate le une dalle altre,e poi presenta delle cellule giganti<br />
atipiche che raramente presentano le caratteristiche della cellula diagnostica di Reed-<br />
Stenberg,però la cellula diagnostica di Reed-Stenberg la dobbiamo necessariamente<br />
trovare,altrimenti non possiamo fare la diagnosi. Quindi le cellule neoplastiche molto spesso<br />
sono pleomorfe,cioè non somigliano alla cellula di Reed-Stenberg che in qualche modo ha delle<br />
sue regole.<br />
Abbiamo esaurito i 4 istotipi classici.<br />
L’ultima novità è questa: ”la predominanza linfocitaria nodulare” che rappresenta grossomodo il<br />
5%. Presenta,oltre alla predominanza linfocitaria che qui è fatta a noduli, una caratteristica<br />
distintiva: non troviamo la cellula di Reed-Stenberg classica troviamo una cellula cosiddetta<br />
pop-corn. Questa forma,dopo molti anni,è stata assimilata al linfoma di Hodgkin,perché facendo<br />
delle analisi molecolari,si è visto che questa cellula,pur essendo morfologicamente<br />
diversa,presenta delle caratteristiche molecolari simili alla cellula di Reed-Stenberg classica.<br />
Immagini.<br />
Vediamo un po’,questa è la predominanza linfocitaria nodulare. È una forma a bassa<br />
aggressività, che si presenta in stadi clinici favorevoli. Può avere possibili recidive e può<br />
evolvere verso il linfoma non-Hodgkin a grandi cellule. Se non si verificano questi due<br />
eventi,possiamo dire che è una forma a buona prognosi. Qui vedete queste cellule pop-corn,che<br />
presentano contorni policiclici. Questa cellula ha una caratteristica anche immunofenotipica<br />
particolare:a differenza della cellula di Reed-Stenberg esprime l’OCT-2 e il BOB-1,ciò vuol<br />
dire che il difetto che ha la cellula di Reed-Stenberg,lei non ce l’ha, e non esprime il CD30<br />
come la cellula di Reed-Stenberg,ma ha una caratteristica che potrebbe essere il segreto della<br />
prognosi relativamente favorevole di questa forma: spesso questa cellula è circondata da<br />
linfociti CD3+ e la C57positiva che è un segno ancora più evidente che sono i Natural<br />
Killer,che sono delle cellule citotossiche molto attive.<br />
La predominanza linfocitaria ha una prognosi lievemente peggiore della forma nodulare;<br />
grossomodo le caratteristiche sono simili,però qua c’è la cellula di Reed-Stenberg,sia pure<br />
scaricato da www.sunhope.it
aramente riscontrata,in un quadro di aumentata densità di cellule linfoidi,e non c’è un aspetto<br />
nodulare. Quindi queste due forme,la predominanza linfocitaria nodulare e la predominanza<br />
linfocitaria diffusa, sono due forme con prognosi relativamente favorevole. Più favorevole nella<br />
forma nodulare. Eccola qui,vediamo una popolazione di cellule linfoidi molto abbondante e al<br />
centro una cellula di Reed-Stenberg, con un aspetto lacunare,CD30+.<br />
Concludiamo la prossima volta.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA 24/03/2011<br />
Proseguiamo con il linfoma di Hodgkin.<br />
SCLEROSI NODULARE<br />
La sclerosi nodulare è l’istotipo più frequente. Nella sua presentazione classica, questo è l’unico<br />
istotipo dove si registra una leggera prevalenza nel sesso femminile rispetto a quello maschile.<br />
Si tratta di una forma che colpisce i giovani, quindi giovani donne, non sempre, ma spesso si<br />
presenta come una massa mediastinica con tutti i sintomi che questo può determinare quindi<br />
possiamo avere anche segni di compressione mediastinica. Età media 88 anni.<br />
Nell’ambito di questo stesso istotipo, che è maggioritario, abbiamo un grading che è G1 e G2.<br />
Il grading è utilizzato perché si è visto che questa sclerosi nodulare a volte va un po’ meglio e<br />
a volte va un po’ peggio.<br />
Le forme G1 sono quelle che hanno una prognosi ancora migliore. Come sono fatte? Il tessuto<br />
linfoghiandolare è suddiviso in noduli da tralci, bande di tessuto fibroso. All’interno di questi<br />
noduli, in genere, è un buon segno se prevale l’architettura e la morfologia della forma che noi<br />
chiamiamo PREDOMINANZA LINFOISTIOCITARIA, quindi sono rare le cellule di Reed-Sternberg<br />
(che poi sono le cellule tumorali) e c’è una elevata densità di linfociti e di istiociti.<br />
Ricordate che nella forma con grading G1 ci sono i noduli e le cellule di Reed-Sternberg in<br />
questa forma assumono quella morfologia che abbiamo definito prima lacunare.<br />
Si dice G2 quando interviene almeno una di queste due caratteristiche:<br />
- più del 25% dei noduli presenta una ricchezza di cellule di Reed-Sternberg, quindi non va più<br />
nella forma a predominanza linfoistiocitaria perché la le cellule di Reed-Sternberg sono rare<br />
ed assumono un aspetto polimorfo cioè non la classica MIRROR CELL che abbiamo visto, ma<br />
forme molto variabili<br />
- più del 25% dei noduli presenta un pattern che corrisponde a quell’istotipo detto deplezione<br />
linfocitaria che è caratterizzato, al contrario della predominanza, dalla diminuita densità<br />
cellulare e anche dall’abbondanza di cellule molto anaplastiche tipo Reed-Sternberg e tipo<br />
cellule giganti anaplastiche<br />
Quindi quando osserviamo una di queste due condizioni, noi diremo G2 altrimenti diciamo G1.<br />
Vedete che c’è una differenza in termini di prognosi, per cui:<br />
- G1 ha una sopravvivenza libera da malattia a 5 anni del 54% (ovviamente quando vi dico<br />
queste sopravvivenze, sono sopravvivenze naturali)<br />
- G2 ha una sopravvivenza libera da malattia a 5 anni del 36%. Queste forme si presentano<br />
molto spesso in stadi avanzati e la risposta terapeutica non è adeguata rispetto alla prima<br />
forma perché in genere dopo alcuni cicli di chemioterapia anche questa grande massa<br />
mediastinica si riduce enormemente.<br />
Adesso le possibilità di sopravvivenza con questo linfoma di Hodgkin sono molto migliorate.<br />
IMMAGINE: questo che vedete è un fegato con noduli biancastri legati alla fibrosi. Il pattern è<br />
nodulare anche se i noduli assumono un aspetto più giallo perché evidentemente predominano<br />
i macrofagi.<br />
Da un punto di vista istologico osserviamo tutto tessuto fibroso all’interno del quale<br />
osserviamo i vari noduli<br />
Dal punto di vista citologico vediamo una binucleazione che come abbiamo detto molto spesso<br />
è legata al taglio perché il nucleo assume un aspetto un po’ a ferro di cavallo.<br />
Vediamo poi le cellule lacunari che giacciono tutte come in una lacuna perché c’è una<br />
retrazione del citoplasma.<br />
scaricato da www.sunhope.it
CELLULARITA’ MISTA<br />
La cellularità mista è il secondo istotipo in ordine di frequenza, grossomodo coinvolge un<br />
15-20% dei casi mentre la sclerosi nodulare arriva al 70% dei casi di linfomi di Hodgkin.<br />
È predominante nei maschi ed è caratterizzata dal fatto che presenta una certa ricchezza di<br />
cellule di Reed-Sternberg e di cellule di Hodgkin cioè che poi sono quelle mononucleate ed è la<br />
forma classica di linfoma di Hodgkin perché qui si raggiunge il massimo dell’eterogeneità<br />
cellulare.<br />
Queste cellule che voi vedete più eosinofile, sono granulociti eosinofili; vi ricordo che queste<br />
sono una popolazione cellulare di accompagnamento.<br />
Le cellule di Hodgkin e le cellule di Reed-Sternberg sono positive per i marcatori CD30 e CD15<br />
DEPLEZIONE LINFOCITARIA<br />
La deplezione linfocitaria è una forma rara, la % è molto bassa e cioè al di sotto del 5%<br />
(fortunatamente).<br />
Una volta non era così perché come vedremo più innanzi, c’era una certa confusione con alcuni<br />
tipi di linfomi non Hodgkin che venivano assimilati ai linfomi Hodgkin, per cui questo istotipo<br />
sembrava più frequente.<br />
Oggi sappiamo che fortunatamente è raro perché è la forma peggiore dal punto di vista<br />
prognostico.<br />
Età media 51 anni, anche qui c’è una leggera predominanza maschile che ritroviamo in tutti gli<br />
istotipi, tranne nella sclerosi nodulare. Dato che è una forma abbastanza aggressiva, si<br />
presenterà in stadi avanzati e presenterà quei segni costituzionali rappresentati da febbre,<br />
sudorazione, astenia, perdita di peso cioè tutti quei segni che si indicano con la lettera B.<br />
Quando faremo la stadiazione, aggiungeremo una lettera A o una lettera B:<br />
- la lettera A vuol dire che non ha sintomi di questo tipo<br />
- la lettera B vuol dire che ha questi sintomi<br />
La prognosi è severa, c’è decesso dell’80% dei casi in 3 anni.<br />
Alcuni distinguono 2 sottovarietà istologiche della deplezione (non tutti sono d’accordo):<br />
- la fibrosi diffusa, fibrosi vuol dire che il connettivo è grossolano cioè è fatto da tralci di<br />
connettivo in cui ci stanno queste cellule<br />
- la forma reticolare, in cui il reticolo non è fibroso ma è fatto, come dice il termine, da fibrille<br />
molto sottili e quindi si parla di forma reticolare.<br />
Questa distinzione non ha una grande rilevanza sul piano clinico, insomma per una deplezione<br />
linfocitaria c’è poco da stare allegri.<br />
IMMAGINE: c’è una fibrosi, qualche cellula abnorme. È difficile trovare cellule di Reed-<br />
Sternberg tipiche perché qui predominano le forme anaplastiche delle cellule di Reed-<br />
Sternberg, le forme atipiche, pleomorfe e soprattutto vedete la distanza che c’è tra un linfocita<br />
e un altro (non c’è una distribuzione fitta delle cellule linfoidi)<br />
PROGNOSI DEL LINFOMA DI HODGKIN<br />
Vediamo ora la sopravvivenza naturale a 5 e a 15 anni. [non è importante ricordare le %]<br />
La PREVALENZA LINFOCITARIA NODULARE ha una sopravvivenza a 5 anni maggiore del 90% e<br />
a 15 anni, a seconda delle diverse casistiche, è dell’85-95%<br />
La PREDOMINANZA LINFOCITARIA ha una sopravvivenza a 5 anni del 92% e a 15 anni del<br />
64%<br />
La SCLEROSI NODULARE ha una sopravvivenza a 5 anni dell’81-66% e a 15 anni del 62-49%.<br />
Questi dati sono in rapporto allo stadio e al grading.<br />
La CELLULARITA’ MISTA ha una sopravvivenza a 5 anni del 72% e a 15 anni del 50%<br />
scaricato da www.sunhope.it
La DEPLEZIONE LINFOCITARIA ha una sopravvivenza a 5 anni del 40% e a 15 anni è zero ed è<br />
quindi la forma più grave<br />
TERAPIA<br />
Vediamo cosa è successo nella terapia.<br />
Fino all’anno 1988 questo linfoma faceva paura.<br />
Queste varie curve che voi vedete, evidenziano la sopravvivenza in persone con linfoma di<br />
Hodgkin in rapporto a diversi regimi terapeutici.<br />
Fino agli anni ’40 non c’era trattamento poi nel 1965 cominciano a comparire (questa è la<br />
seconda curva, che mostra un leggero miglioramento) gli agenti alchilanti che però avevano<br />
diverse controindicazioni.<br />
Nel 1988 cominciano a comparire delle nuove terapie che si basavano sulla miscela di<br />
chemioterapici, molto spesso tossici.<br />
Sono in fase di sperimentazione nuovi regimi terapeutici che stanno dando dei risultati<br />
eccezionali che però complicano la spesa sanitaria.<br />
Ai nostri giorni, con queste ultime terapie, dove si raggiunge a 7 anni una sopravvivenza<br />
impensabile cioè si è arrivati dalla quasi sicurezza di morire alla quasi certezza di sopravvivere<br />
per i linfoma di Hodgkin perché stiamo vicini al 90%.<br />
La possibilità di sopravvivere non c’era fino agli anni ’60-’70.<br />
STADIAZIONE<br />
La stadiazione è molto importante ed è una delle poche cose che è rimasta ferma da molti anni<br />
e si chiama STADIAZIONE DI ANN ARBOR (Ann Arbor è il nome di una località famosissima).<br />
Adesso sono stati introdotti anche dei fattori di rischio che aggravano la prognosi e che sono<br />
indipendenti dalla stadiazione.<br />
I fattori prognosticamente sfavorevoli sono rappresentati da:<br />
- stadio IV<br />
- albumina inferiore a 4 grammi<br />
- emoglobina inferiore a 10 grammi<br />
- globuli bianchi maggiori di 15000, soprattutto c’è una granulocitosi mentre i linfociti sono<br />
pochi.<br />
Se i pazienti hanno massimo uno di questi fattori, la sopravvivenza supera il 90% e questo<br />
succede nella maggior parte dei casi.<br />
Se invece i pazienti presentano quasi tutti questi fattori, la sopravvivenza peggiora fino al 59%<br />
COMPLICANZE<br />
Perché si moriva di linfoma di Hodgkin e perché si può morire di linfoma di Hodgkin.<br />
Paradossalmente è difficile morire proprio di linfoma di Hodgkin, anche in passato era difficile,<br />
ma si moriva e si può morire per delle complicanze.<br />
Allo stato attuale, in queste miscele chemioterapiche che si usano per i linfomi, non è un<br />
evento molto raro la possibilità che si sviluppino delle cardiomiopatie, delle malattie polmonari<br />
(tipo fibrosi, polmonite interstiziale, ecc), neoplasie metacrone (metacrone vuol dire a<br />
distanza) perché i primi segnali del linfoma di Hodgkin li troviamo nelle aree paracorticali.<br />
Nelle aree paracorticali cominciano a comparire le prime cellule di Reed-Sternberg perché<br />
abbiamo l’evidenza che queste cellule si formano anche per un deficit dell’immunosorveglianza.<br />
In passato, i pazienti con linfoma di Hodgkin morivano per complicanze infettive soprattutto da<br />
virus erpetici (a conferma di una compromissione del sistema immunitario).<br />
Quindi difficilmente si può morire per una localizzazione metastatica cerebrale o perché viene<br />
leso un centro vitale, ma si può morire per le complicanze che oggi sono diventate più rare<br />
anche perché l’idea di fare un cocktail chemioterapico ha un vantaggio e cioè si diluisce la<br />
scaricato da www.sunhope.it
tossicità di ogni farmaco e si ha maggior possibilità di colpire più cloni perché agiamo su più<br />
fronti.<br />
Tra le complicanze dobbiamo ricordare anche l’ipotiroidismo anche se rappresenta la<br />
complicanza più banale.<br />
GRAFICO: la linea blu segna l’incidenza di seconde malattie maligne e vedete come aumentano<br />
a distanza di molti anni, anche gli eventi cardiovascolari si comportano allo stesso modo<br />
mentre la recidiva del linfoma di Hodgkin ha un giro di boa a 5 anni.<br />
Quindi se non c’è una recidiva nei primi 5 anni, difficilmente ci potrà essere nel resto della vita<br />
però dobbiamo stare attenti per le complicanze di tipo cardiopolmonari e complicanze<br />
neoplastiche di altra natura.<br />
Siccome il linfoma di Hodgkin non ha una pre-cancerosi, così come tutti i linfomi, si è fatto un<br />
grosso sforzo per identificare lesioni che precedono lo sviluppo di un linfoma.<br />
Si parla di centri progressivamente trasformati. Che cosa vuol dire trasformati?<br />
Questo è un centro germinativo dove possiamo vedere che il mantello penetra all’interno del<br />
centro germinativo; quindi per centri progressivamente trasformati intendiamo la penetrazione<br />
di aree del mantello, della corona all’interno del centro germinativo. Questa condizione una<br />
volta si riteneva che fosse una pre-cancerosi evidente, oggi si è visto che è una pre-cancerosi<br />
molto debole nel senso che il rischio di sviluppare un linfoma di Hodgkin a predominanza<br />
linfocitaria varia da 0 fino al massimo al 5% (dipende dalle varie casistiche).<br />
GIUSEPPE MOSCATI<br />
Fu uno dei primi a Napoli ad interessarsi di linfoma di Hodgkin.<br />
LINFOMI NON HODGKIN<br />
Perché la slide lavori in corso? Perché a partire dagli anni ’70 con le rivoluzioni introdotte<br />
dall’immunologia, incominciò una rivoluzione dei linfomi che non è finita più.<br />
I linfoma non-Hodgkin hanno un’incidenza maggiore rispetto ai linfoma di Hodgkin.<br />
I linfoma non-Hodgkin si situano come incidenza al 5° posto tra le neoplasie maligne, ma come<br />
causa di morte scende molto cioè fino al 9-10°, ciò vuol dire che c’è stato un grande vantaggio<br />
sulla mortalità di questi linfomi che in genere sono più aggressivi rispetto ai linfomi di Hodgkin.<br />
Se noi vediamo le possibilità di ammalarsi di linfoma non-Hodgkin in rapporto all’età,<br />
vediamo che il rischio cresce con l’aumentare dell’età per cui la possibilità su<br />
100.000 casi arriva al 2-3% ed è un’incidenza ragguardevole. Dobbiamo però<br />
considerare un altro problema e cioè quello economico. Se guardiamo la spesa<br />
sanitaria per patologia, vediamo che i linfomi<br />
non-Hodgkin si situano al 4° posto ed è quasi vicino alla spesa per il polmone pur<br />
avendo un’incidenza molto inferiore perché i linfomi non-Hodgkin richiedono dei<br />
trattamenti continui, delle verifiche continue (TAC, RM, ecc) per vedere come sta<br />
andando avanti la malattia.<br />
CLASSIFICAZIONI DEI LINFOMI NON-HODGKIN<br />
Esistono vecchie classificazioni come RAPPAPORT, di cui non parliamo.<br />
I due pilastri fondamentali di questa classificazione sono stati un tedesco e un inglese negli<br />
anni ’75. Le loro classificazioni sono rimaste in piedi per molti anni e anche le nuove<br />
classificazioni risentono della loro impostazione.<br />
Per la prima volta nel ’75 loro introdussero il concetto di linfoma non-Hodgkin a cellule B e T.<br />
scaricato da www.sunhope.it
Successivamente ci furono due scuole di pensiero e cioè quella americana e quella europea.<br />
Si cercò di fare un’unica classificazione dei linfomi non-Hodgkin che venne definita REAL.<br />
REAL è un acronimo che sta per Revised European American Lymphoma Classification e questo<br />
fu un tentativo diplomatico di fare una classificazione unica, ma ne uscì fuori un pasticcio.<br />
Poco più di 2 anni fa, l’OMS (o WHO), ha fatto una serie di libretti (blue book) dedicati a<br />
patologie tumorale e patologie non tumorali dal punto di vista anatomo-patologica.<br />
Il WHO distingue i linfomi non-Hodgkin in 3 grosse categorie:<br />
- linfomi dei precursori delle cellule B e T cioè di quei linfociti pre-linfoghiandola (ricordate la<br />
slide dove c’erano le culle con i linfociti B e T che stavano aspettando di maturare). Questi<br />
linfomi sono chiamati anche linfomi linfoblastici a cellule B e T.<br />
Qui crolla pure un caposaldo della didattica che qualche testo si ostina ancora a contemplare<br />
e cioè quel muro che esisteva tra leucemie linfoidi e linfomi non-Hodgkin perché noi sappiamo<br />
che tutti i linfomi non-Hodgkin possono essere leucemici o possono avere delle fasi<br />
leucemiche durante il loro decorso, ovviamente ci sono alcuni che sono di regola leucemici<br />
per altri invece è più difficile però possono essere leucemici quindi parliamo di fasi leucemiche<br />
o di fasi aleucemiche<br />
- linfomi a cellule B, cellule B vuol dire che sono cellule B mature e rappresentano la<br />
stragrande maggioranza dei linfomi<br />
- linfomi a cellule T e NK (i linfomi a cellule NK sono estremamente rari)<br />
LINFOMA LINFOBLASTICO A CELLULE T<br />
Il linfoma linfoblastico a cellule T è per definizione molto spesso leucemico, è un linfoma<br />
pediatrico anzi nell’infanzia è il linfoma più frequente.<br />
La caratteristica di questo linfoma è che molto spesso si associa ad una massa mediastinica<br />
cioè la sua sede di insorgenza è il mediastino.<br />
Dal punto di vista morfologico è fatto da cellule convolute perché hanno una membrana<br />
nucleare dentellata quasi un po’ cerebriforme anche se non tutte le cellule sono così.<br />
Queste cellule sono anche definite “cellule a zampa di gallina”.<br />
Questi linfomi non esprimono frequentemente dei marcatori di maturazione T, ma esprimono il<br />
TdT (terminal deossinucleotidil transferasi) che è un enzima che si trova in tutti i precursori,<br />
anche in quelli B.<br />
Oltre al TdT questi linfomi possono esprimere anche i CD3, mentre per il CD4 e per il CD8 ha<br />
un comportamento molto bizzarro e cioè se li esprime (anche se raramente li esprime)<br />
contemporaneamente vuol dire che è impazzito e quando li esprime non hanno neanche una<br />
localizzazione di membrana ma a volte nel citoplasmatica. Quindi è anomala la co-espressione<br />
ma è anomala anche la posizione nel citoplasma perché questi CD si riferiscono ad antigeni di<br />
membrana.<br />
LINFOMA LINFOBLASTICO A CELLULE B<br />
Il linfoma linfoblastico a cellule B è più raro di quello T, è fatto dai precursori, è molto<br />
aggressivo, età giovanile, spesso associato a leucemia.<br />
Esprime il TdT però il CD20 è negativo perché sappiamo che è un marcatore di membrana che<br />
viene espresso dai linfociti più maturi, può esprimere il CD19 che è un marcatore espresso dai<br />
linfociti meno maturi oppure può esprimere un altro antigene e cioè il PAX5 che è un marcatore<br />
nucleare.<br />
Se andiamo a fare il Ki67, vediamo che molte di queste cellule stanno in fase proliferativa.<br />
LINFOMI A PICCOLI LINFOCITI<br />
Questo è il caso in cui un linfoma prende due nomi: linfoma a piccoli linfociti e leucemia<br />
linfatica cronica.<br />
scaricato da www.sunhope.it
Questi due nomi sono sinonimi anche se può sembrare strano perché questo linfoma non-<br />
Hodgkin a piccoli linfociti molto spesso è leucemico e corrisponde alla leucemia linfatica<br />
cronica, così come molto spesso se troviamo un paziente con leucemia linfatica cronica<br />
troviamo un linfoma.<br />
Nello stesso decorso dei pazienti con questo linfoma, possiamo vedere che esordisce con una<br />
fase leucemica oppure con una fase non leucemica e poi durante il suo decorso si può<br />
sviluppare una fase leucemica.<br />
Questo è un linfoma molto frequente e raramente può succedere che questo linfoma, dopo<br />
molti anni, perché questo è un linfoma dell’anziano che appartiene ai cosiddetti linfomi<br />
indolenti cioè che hanno una lentissima crescita, possono improvvisamente trasformarsi dal<br />
punto di vista anche clinico evidente cioè che questi linfonodi che crescevano molto<br />
lentamente, improvvisamente e tumultuosamente diventano delle masse enormi; può<br />
succedere la cosiddetta SINDROME DI RICHTER cioè che un linfoma a basso grado si<br />
trasforma in un linfoma ad alto grado così come può succedere che questo linfoma possa poi<br />
trasformarsi in un linfoma di Hodgkin anche se però questo rischio è molto basso.<br />
È un linfoma dell’età avanzata, il quadro clinico è indolente e fatto di recidive e di remissioni<br />
(ovviamente noi parliamo della storia naturale), è frequente la leucemia la quale molto spesso<br />
si associa anche ad un midollo osseo positivo, astenia, frequente epatosplenomegalia,<br />
febbricola (è una caratteristica del linfoma).<br />
Il quadro morfologico è fatto da un pattern diffuso cioè anziché vedere l’architettura normale<br />
del linfonodo, in linea di massima noi vediamo un pattern diffuso di una popolazione<br />
apparentemente omogenea, fatta di piccoli linfociti, ma che non lo è quando adiamo ad<br />
osservarla a forte ingrandimento.<br />
Questo linfoma può mostrare anche degli aspetti falsamente follicolari, non sono follicoli, ma<br />
siccome non ha una crescita veloce, può avere dei centri di proliferazione attivi che appaiono<br />
più chiari perché sono cellule un po’ più grandi e quindi se facciamo un Ki67, dove sono rare le<br />
positività, vedete degli aggregati fortemente positivi che corrispondono ai centri di<br />
proliferazione che possiamo trovare nel contesto di questo linfoma.<br />
L’immunofenotipo è CD20 positivo, CD5 positivo e altra caratteristica importante è che si<br />
tratta non di prelinfociti ma cmq di linfociti non maturi (la massima maturazione del linfocita B<br />
è la plasmacellula) e questi linfociti no esprimono come immunoglobuline di membrana le IgM<br />
(i linfociti nella loro storia iniziale esprimono come immunoglobuline di membrana le IgM)<br />
quindi anche nell’espressione dell’immunoglobulina riflette questa sua scarsa differenziazione.<br />
IMMAGINE:non esiste solo il piccolo linfocita classico che è sferico, ma ci sono anche queste<br />
cellule che somigliano agli immunoblasti, ma sono molto più piccoli per cui è stato coniato il<br />
termine paraimmunoblasti.<br />
Ci sono poi cellule più sagomate, meno sferiche definite pro-linfociti che presentano delle<br />
irregolarità nella membrana e cioè delle rientranze, delle piccole sporgenze.<br />
Quello che a piccolo ingrandimento sembra una popolazione monomorfa, può avere una<br />
componente prolinfocitica e una componente paraimmunoblastica; ovviamente più aumenta<br />
questa componente prolinfocitica e paraimmunoblastica più questo linfoma tende ad essere di<br />
poco più aggressivo perché di base siamo sempre nell’ambito dei linfomi cosiddetti indolenti.<br />
Questo è il centro di proliferazione, se facciamo il Ki67 vediamo che ogni tanto nelle aree<br />
adiacenti troviamo qualche cellula positiva invece vi sono delle aree in cui sono più compatte le<br />
cellule in fase di proliferazione.<br />
Questa è la variante prolinfocitica perché le cellule non sono più sferiche però presentano le<br />
stesse caratteristiche fenotipiche, immunofenotipiche.<br />
Questa è la sindrome di Richter cioè quanto vediamo piccoli linfociti e poi dei grandi linfociti. In<br />
genere i linfomi a grandi cellule sono linfomi più aggressivi.<br />
scaricato da www.sunhope.it
LINFOMA A CELLULE MANTELLARI<br />
Lo stato più interno del centro germinativo si chiama mantello, quello più esterno si chiama<br />
zona marginale.<br />
Il linfoma a cellule mantellari non è un linfoma raro ed è più aggressivo della leucemia linfatica<br />
cronica, ha un’età media di 63 anni, tende a coinvolgere frequentemente la milza e il midollo<br />
osseo e quindi a presentare un quadro leucemico.<br />
Il pattern istologico ricalca un po’ quella che è la topografia e la conformazione morfologica<br />
delle cellule mantellari.<br />
Qual è l’immunofenotipo? A parte il CD20 che è positivo e questa è una caratteristica di tutti i<br />
linfomi, fanno eccezione solo le forme pre-B che esprimono il CD19 perché non sono ancora<br />
mature per poter esprimere il CD20.<br />
La caratteristica diagnostica differenziale di questo linfoma è di esprimere la ciclina D1, di<br />
essere molto positivo al Ki67, di esprimere la bcl2 come è nella norma, vi ricordate che la<br />
corona esprimeva questa proteina che è implicata nel blocco della necrosi apoptotica quindi è<br />
logico che anche il suo linfoma ha un blocco di maturazione perché le cellule invece di<br />
maturare si fermano quindi è un blocco di regressione.<br />
Ci sono varie mutazioni però vi devo dire la verità le ho messe in tabella solo per <strong>complete</strong>zza<br />
perché non sono specifiche, tranne questa traslocazione 11-14 in prossimità del sito che<br />
codifica per le catene pesanti delle Ig che viene ritrovato nel 60% dei casi.<br />
IMMAGINE: in questa immagine il pattern morfologico può presentare ancora i centri<br />
germinativi però poi qui vediamo che il centro germinativo è scomparso perché poiché sono<br />
proliferate tutte queste cellule mantellari e hanno preso il sopravvento sul centro germinativo.<br />
Questo lo dico perché a volte vedendo questi centri germinativi uno può avere l’impressione<br />
che sia un linfonodo reattivo e invece non è così perché il linfoma si trova ancora in uno stadio<br />
iniziale e non ha avuto ancora il tempo di “mangiarsi” il centro germinativo quindi abbiamo<br />
delle forme che mantengono ancora i centri germinativi e altre forme che invece tendono ad<br />
essere diffuse. La cosa più importante è che non c’è in tutto il linfonodo un tessuto mantellare<br />
normale cioè se noi trovassimo un follicolo che ha un mantello normale, si metterebbe in<br />
dubbio la diagnosi perché la malattia è sistemica.<br />
Le cellule sono tutte sagomate ed hanno delle incisioni, un piano di clivaggio quindi non nuclei<br />
sferici come nella leucemia linfatica cronica ma sono cellule che somigliano ai prolinfociti anche<br />
se però sono più grandi rispetto a quest’ultimi<br />
Pur essendo un linfoma a piccole cellule, presenta frequentemente figure mitotiche ed ha CD20<br />
positivo, CD5 positivo e ha anche una componente di CD3 reattiva che non fa parte del<br />
linfoma.<br />
La ciclina D1, che è un marcatore nucleare ed è coinvolto in quelle cicline che sono delle<br />
proteine legate alla proliferazione cellulare e quindi al ciclo proliferativo, è molto espressa<br />
come anche il Ki67 è espresso diffusamente a differenza della leucemia linfatica cronica dove<br />
troviamo solo dei centri di proliferazione ma il Ki67 è meno espresso.<br />
LINFOMI DELLA ZONA MARGINALE TIPO MALT<br />
Il linfoma della zona marginale di tipo MALT è un linfoma che molto spesso può avere una sede<br />
extralinfoghiandolare o che si può associare a localizzazioni linfoghiandolari e<br />
extralinfoghiandolari. È il linfoma più frequente nei siti extralinfoghiandolari perché in questi<br />
siti la zona marginale è molto espressa. C’è un organo linfoide in cui questa zona marginale è<br />
molto espressa e cioè la milza infatti quella della milza è il linfoma più frequente, ma può<br />
colpire anche organi viscerali tipo lo stomaco, l’intestino, dove anche nelle strutture follicolari<br />
(follicoli linfatici e non linfonodi) che normalmente si trovano nella parete dell’intestino, tipico<br />
scaricato da www.sunhope.it
esempio è quello dell’intestino tenue per non parlare delle placche del Peyer, noi possiamo<br />
trovare questo enorme sviluppo della zona marginale.<br />
Questo linfoma, che fa parte dei linfomi indolenti, è meno aggressivo del linfoma mantellare,<br />
tende però a localizzazioni multiple, ha delle lunghissime guarigioni ed è un linfoma dove è<br />
prevista la guarigione completa al 100% per le forme gastriche legate all'helicobacter, anzi è<br />
l’unico caso che nei linfomi gastrici legati all'helicobacter si può anche non fare la terapia per i<br />
linfomi perché in alcuni tipi se si eradica l’helicobacter scompare anche il linfoma quindi in<br />
questo caso la causa è nota ed è rappresentata dall’helicobacter soprattutto le forme<br />
superficiali cioè quelle forme che non invadono la mucosa a tutto spessore (stadio iniziale).<br />
La popolazione cellulare è simile ai centrociti, ma se vi ricordate il linfonodo normale, vi<br />
ricordate che vicino al mantello c’erano quelle cellule bimonocitoidi, qui invece troviamo una<br />
certa eterogeneità cioè cellule un po’ clivate, un po’ come le cellule mantellari però con una<br />
maggiore variabilità di aspetti perché troviamo anche queste cellule monocitoidi ed una minore<br />
densità.<br />
La diagnosi si fa dal punto di vista della negatività, nel senso che comprendiamo che si tratta<br />
di un linfoma comunque della corona però se non esprime la ciclina D1 è della zona marginale.<br />
Il CD20 è positivo come in tutti i linfomi, bcl-2 positivo però la diagnosi differenziale con il<br />
mantellare dal punto di vista immunofenotipico è dato dalla ciclina D1 che sarà negativa e<br />
anche un’attività proliferante Ki67 inferiore.<br />
IMMAGINE: a differenza del linfoma di prima, qui non solo possiamo trovare il centro<br />
germinativo ma possiamo trovare anche il mantello normale.<br />
La proliferazione neoplastica è esterna, in una fase iniziale noi troviamo il centro germinativo,<br />
un anello di mantello e poi la zona marginale molto espansa ma è fatta da linfociti neoplastici e<br />
questo si verifica anche nei tessuti.<br />
È difficile decidere se è un linfoma di un viscere ad esempio dello stomaco perché c’è la<br />
gastrite e tutta una serie di infiltrati infiammatori e quindi dobbiamo stare attenti perché per<br />
alcune forme è difficile la diagnosi differenziale.<br />
Questi linfomi però hanno un carattere morfologico, a parte la caratterizzazione immunologica<br />
che ci aiuta moltissimo, particolare perché mostrano aggressività nei riguardi dell’epitelio cioè<br />
quindi ritroviamo quello che noi chiamiamo COMPLESSI LINFOEPITELIALI cioè voi vedete qui il<br />
residuo di una ghiandola (vi ho messo due frecce) che è stata mangiucchiata dai linfociti.<br />
Questa commistione di ghiandole con aspetti regressivi, infiltrate da questi linfociti, prendono il<br />
nome di COMPLESSO LINFOEPITELIALE ed è molto diagnostico di un pattern aggressivo che ci<br />
aiuta nella diagnosi.<br />
scaricato da www.sunhope.it
ANATOMIA PATOLOGICA: lezione del 25/03/11<br />
Continuiamo il discorso dell’altra volta: siamo sempre nell’ambito dei linfomi a piccole<br />
cellule B. Un’altra categoria è rappresentata da quei linfomi che sono imparentati con le<br />
plasmacellule e con le cellule linfoplasmocitoidi di cui abbiamo parlato. La plasmacellula la<br />
conoscete bene, le cellule plasmocitoidi sono quelle che si atteggiano a plasmacellule, ma<br />
gli manca un po’ di citoplasma! Molto spesso queste cellule, che hanno il nucleo delle<br />
plasmacellule, ma il citoplasma è scarso, anzicchè produrre tutte le catene pesanti e<br />
leggere, si limitano a produrre IgM (solo le catene pesanti) perché sono le<br />
immunoglobuline più antiche dal punto di vista ontologico. Quando questi linfomi<br />
presentano una differenziazione plasmacellulare più spinta, allora andiamo verso il<br />
plasmocitoma o verso il mieloma. Ovviamente il termine mieloma lo riserviamo ad una<br />
neoplasia che colpisce soprattutto il midollo osseo; se colpisce il linfonodo cambia nome:<br />
si chiama PLASMOCITOMA. Il mieloma ha tutta una presentazione clinica particolare<br />
perché coinvolge molte ossa, quelle del cranio e della colonna vertebrale. Quindi<br />
plasmocitomi e linfomi linfoplasmocitoidi sono di pertinenza dei linfonodi.<br />
Che cosa possiamo dire sul piano clinico? Si tratta di linfomi INDOLENTI, cioè che hanno<br />
un lungo decorso, non hanno una storia clinica acuta o esplosiva. Esordiscono talvolta con<br />
anomalie delle IG come paraproteine, crioglobuline e catene pesanti. Cosa determina tutta<br />
questa situazione? E’ un ipergammaglobulinemia. Nelle forme classiche possiamo trovare<br />
anche la monoclonalità per catene K o catene lambda. Questa aumentata quota di IG può<br />
determinare un’iperviscosità del sangue e quindi può causare delle trombosi o comunque<br />
delle ostruzioni a livello dei vasi oculari( con riduzione del visus), o anche neuropatie(se<br />
sono coinvolte strutture nervose), e può determinare anche nefropatie o coaguolopatie<br />
(legate al fatto che le catene pesanti delle IgM possono legarsi a fattori della coagulazione<br />
o alle piastrine). Come vedete, la popolazione cellulare può essere costituita da<br />
plasmacellule, cellule linfoplasmocitoidi in varia misura. Ovviamente parliamo di<br />
linfoplasmocitomi o di mielomi quando si è nell’osso, quando c’è una quota di<br />
plasmacellule che deve essere almeno superiore al 20-30%. Per quanto riguarda il<br />
fenotipo, come vedete, la plasmacellula non esprime il CD20, ma esprime il CD38.<br />
Ovviamente se usiamo anti sieri anti Ig, vedremo che il citoplasma è pieno di catene<br />
pesanti o di catene leggere a seconda dei casi, e cercheremo anche la monoclonalità<br />
quando abbiamo dei dubbi: ci troviamo di fronte ad una popolazione cellulare, vogliamo<br />
sapere se è reattiva o se è neoplastica, cosa facciamo? Ci andiamo a vedere se c’è<br />
monoclonalità, quindi quello stesso test che voi fate sul siero, noi lo facciamo sul tessuto.<br />
Vabbè possiamo vedere traslocazioni, riarrangiamenti della regione B, della regione che<br />
codifica per il PAX5 che è un marcatore nucleare delle cellule B, mentre per il mieloma ci<br />
sono tutta una serie di mutazioni che riguardano vari geni.<br />
Riconoscerete in questa figura il nucleo della plasmacellula che viene descritto nei libri<br />
come “a ruota di carro”, secondo me questa ruota di carro si vede raramente, io dico che<br />
somiglia un poco a quei palloni di calcio che hanno tutti quegli esagoni, c’è una<br />
marginalizzazione della cromatina, cioè la cromatina tende a distribuirsi soprattutto alla<br />
scaricato da www.sunhope.it
periferia. Il concetto della ruota di carro è che ci sono dei filamenti di cromatina che si<br />
dispongono perpendicolarmente alla membrana nucleare. Andiamo avanti: a volte<br />
possiamo trovare questi CORPI ROSSI , inclusi citoplasmatici rossi, anche con il PAS e<br />
che sono depositi di immunoglobuline. Sono chiamati CORPI DI DATCHER. Ovviamente<br />
se si tratta di un plasmocitoma e andiamo a fare catene K e lambda, vedete che le K qui<br />
sono molto espresse, le lambda ce ne stanno pochissime, è evidente quindi che c’è una<br />
monoclonalità e questa monoclonalità ci permette di dire che si tratta di una neoplasia. Se<br />
c’era una plasmocitosi reattiva avremmo trovato le due catene K e lambda grosso modo<br />
equivalenti. Questo è il linfoplasmocitoide: vedete il nucleo, con la caratteristica un po’<br />
della plasmacellula, però il citoplasma è scarso. Dicemmo l’altra volta che le cellule<br />
plasmocitoidi si formano dagli immunoblasti, la plasmacellula invece è il prodotto più<br />
naturale di una lunga catena di produzione che, attraverso il follicolo linfatico, germinativo,<br />
arriva alla plasmacellula.<br />
.<br />
LINFOMI FOLLICOLARI<br />
I linfomi follicolari sono quelli che somigliano un po’ alle cellule del centro germinativo. Vi<br />
ricordo che sono cellule che noi chiamammo “centrociti- centroblasti” oppure cellule<br />
clivate(cioè che hanno irregolarità della membrana) e cellule non clivate. Anche questo è<br />
un linfoma INDOLENTE, tende a coinvolgere, nel suo progressivo sviluppo, molti organi.<br />
Questa forma può essere anche leucemica, ma raramente. Può evolvere anche questo<br />
verso il linfoma a grandi cellule. Questo è l’unico linfoma che può avere vari tipi di<br />
architettura: può essere FOLLICOLARE, quando il linfoma è ancora “nella culla”(coinvolge<br />
solo il centro germinativo), DIFFUSO quando ha superato gli argini e quindi non si vedono<br />
più “follicoli” neoplastici ma ha invaso tutti i linfonodi, FOLLICOLARE-DIFFUSO quando<br />
vediamo aree ancora iniziali e aree più avanzate. Ovviamente la popolazione sarà<br />
costituita da centrociti, centroblasti,( secondo la dizione europea “cellule clivate”). Qui<br />
abbiamo dei marcatori diagnostici; vi ricordo che nella parte generale vedemmo che il<br />
centro germinativo ha tanti marcatori,ma quello che viene utilizzato più di routine è il<br />
CD10. Quindi sono linfomi CD10 positivi. Anche bcl-2 e bcl-6 positivi. Lasciamo stare le<br />
mutazioni, le traslocazioni che non sono diagnostiche e quindi hanno un’importanza<br />
relativa.<br />
Cosa succede se confrontiamo un’iperplasia follicolare con un linfoma follicolare?<br />
Paradossalmente l’iperplasia è più polimorfa, cioè vediamo follicoli di grandi dimensioni, a<br />
volte confluenti, follicoli di piccole dimensioni, mentre il linfoma follicolare è più geometrico,<br />
poiché è un processo sistemico che coinvolge il linfonodo, i follicoli neoplastici si<br />
somigliano, come dimensione e come tutto. Vedete questo follicolo, stà per perdere la<br />
corona, vedete questo alone, sta per diventare diffuso, stà per perdere il carattere<br />
follicolare.<br />
C’è un GRADING di questo linfoma, si è visto che più aumentano i centroblasti più il<br />
linfoma ha un maggior grado di malignità. Il grading è diviso in tre classi. Vedete, Questo è<br />
il centroblasta classico: grossa cellula con nucleolo alla periferia. Questi sono tutti centro<br />
scaricato da www.sunhope.it
citi. Se i centroblasti sono inferiori a 5 per campo, ad alto ingrandimento, allora si parla di<br />
GRADO1. Se sono tra 5 e 15 GRADO2, oltre 15 per campo GRADO3.<br />
Prima dell’avvento dei marcatori, fare la diagnosi era molto complicato, cioè fare la d.d tra<br />
iperplasia e linfoma follicolare non sempre era facile. Però in questa immagine notiamo<br />
qualche differenza: a sinistra quello iperplastico, a destra quello neoplastico. Il follicolo<br />
iperplastico, per definizione, ha delle aree più chiare che sono occupate da quei macrofagi<br />
di tipo “starry sky” che in genere non si trovano nel follicolo neoplastico, non perché se ne<br />
sono scappati da là, ma perché la proliferazione neoplastica ha distrutto questi macrofagi.<br />
C’è anche una maggiore densità cellulare e mancano questi spazi chiari. Se abbiamo<br />
qualche dubbio, e i dubbi ci vengono soprattutto nelle forme diffuse dove non<br />
riconosciamo più il target follicolare, vedete come qua tutti i follicoli sono positivi per CD10,<br />
e il CD10 è un marker dei centri germinativi, sia normali che neoplastici. Quindi il CD10<br />
non si può usare per fare diagnosi di malignità, ma si può usare utilizzare per definire<br />
un’istogenesi, cioè è un linfoma mantellare? È una leucemia linfatica cronica? Il Cd10 ci<br />
permette di rispondere. Molto importante è anche il comportamento della Bcl-2. Se<br />
ricordate nel linfonodo normale la Bcl-2 si localizzava soprattutto nella corona mentre il<br />
cento germinativo era negativo. Se invece il follicolo è neoplastico, sia il centro, sia la<br />
corona sono positivi, cioè diciamo che queste cellule del centro neoplastico, hanno<br />
acquisito la bcl-2 perché si accrescono anche grazie all’inibizione della necrosi apoptotica.<br />
Un’altra conferma ci è data dal Ki67 che paradossalmente è maggiormente espresso nei<br />
follicoli normali iperplastici mentre, nel follicolo neoplastico quantitativamente è meno<br />
espresso perché questo linfoma si accresce, non solo per l’attività linfoproliferativa, ma<br />
anche per l’inibizione della necrosi apoptotica che detemina quasi un’immortalizzazione di<br />
una delle cellule. Il linfoma follicolare è un linfoma “dell’adulto”, difficilmente possiamo<br />
avere forme aldisotto di 25 anni, quindi se vi arriva un giovane con meno di venti anni e<br />
diagnosi di linfoma follicolare, la prima cosa a cui dovete pensare è un errore diagnostico.<br />
Qui vedete il GRADO1: i centroblasti sono pochi, sicuramente inferiori a 5 per campo.<br />
Questo è il GRADO2: i centroblasti sono quelle cellule più chiare, più grandi, nucleolo alla<br />
periferia.<br />
Questo è il GRADO3: dominano i centroblasti che sono queste cellule con nucleo<br />
distribuito generalmente in periferia.<br />
LINFOMI A GRANDI CELLULE B<br />
Comprendono: il LINFOMA CENTROBLASTICO, quando la popolazione centroblastica<br />
prende il sopravvento. Sale un po’ come livello di malignità. Può essere primitivo, nel<br />
senso che nasce d’emblè, o può essere secondario in un paziente che ha avuto già<br />
diagnosi di linfoma centrocitico-centroblastico, quindi rappresenta un’evoluzione graduale<br />
verso un maggior grado di malignità. Questo è il linfoma monoblastico: sono grandi cellule<br />
con un magro nucleolo quasi sempre centrale, sono tutti e due ad alto grado di malignità.<br />
Questo è un linfoma particolare su cui ci soffermiamo un po’perché veniva confuso con il<br />
scaricato da www.sunhope.it
linfoma di Hodgkin, infatti vedete la dizione inglese è “ T-cell rich B cell lymphome”, cioè<br />
vuol dire che è un linfoma a cellule B ma la popolazione B è una minoranza, come<br />
succede nei linfomi di hodgkin, mentre la maggior parte delle cellule reattive è T. Qui<br />
vedete delle cellule giganti, ricordano vagamente ma non hanno le caratteristiche del<br />
nucleo chiaro, a specchio (mirror cell) dei linfomi di Hodgkin. Questo linfoma, fino a<br />
qualche tempo fa, veniva assimilato al linfoma di Hodgkin perché se andiamo a fare<br />
l’immunoistochimica vediamo che queste cellule possono anche esprimere il CD20 ma<br />
esprimono anche l’ox2 e questa è una caratteristica distintiva rispetto alla cellule di reedsternberg.<br />
Inoltre, se andiamo a fare il CD3, uno che non conosce il problema dice-questo<br />
è un linfoma a cellule B. Però se vedete le grandi cellule B, esse sono negative, perciò<br />
diremo: Tcell rich B cell limphome, cioè un linfoma a cellule B ricco di cellule T.<br />
Abbiamo poi un altro linfoma che pure è stato una novità: LINFOMA ANAPLASTICO.<br />
Anaplastico perché vediamo delle cellule mostruose, giganti, pensate che, non molti anni<br />
fa, se uno vedeva un linfonodo così, pensava ad una metastasi. Invece si è visto che è un<br />
linfoma. Questo linfoma a grandi cellule anaplastiche può essere B e come vedremo<br />
anche T, molto spesso esprime una particolare chinasi chiamata ALK. Ecco alk vuol dire<br />
proprio “linfoblastico a grandi cellule”poiché viene espresso solo da grandi linfomi<br />
anaplastici. Vedremo più avanti che la forma B è più rara di quella T.<br />
Allora facciamo una ricapitolazione. Tutta quella sbarra gialla è rappresentata dai linfomi a<br />
piccole cellule o a piccoli linfociti che rappresentano quasi una metà dei linfomi a cellule B<br />
che sono: leucemia linfatica cronica o linfoma a piccole linfociti che incide per un 7%; i<br />
linfomi a cellule mantellari che grosso modo hanno la stessa incidenza; i linfomi della zona<br />
marginale ( tipo malt, balt, a seconda della zona in cui viene identificato) l’8% ; i linfomi<br />
plasmacitici 1-5%; i linfomi follicolari che rappresentano una grossa percentuale(è più<br />
corretto parlare di linfomi del centro follicolare)ossia il 23%. Il totale di questi linfomi fa il<br />
47%. Poi abbiamo i linfomi a grandi cellule che rappresetano un 30%, i linfomi a cellule<br />
anaplastiche 2,5% ; il linfoma di Burkitt fa storia a sé perché non è né tra le grandi, né tra<br />
le piccole cellule ma è a cellule intermedie ed incide per il 2%; e poi ci sono altre forme<br />
che sono il 5%. In questo 5% ci stanno almeno 70-80 forme di linfomi non Hodgkin che vi<br />
risparmio.<br />
LINFOMA DI BURKITT<br />
Siamo sempre nell’ambito dei linfomi a cellule B. Vi risparmio la storia di Burkitt!! Oggi<br />
sappiamo, cosa che non sapeva Burkitt, che esistono tre forme, diverse dal punto di vista<br />
clinico-epidemiologico, ma uguali dal punto di vista del quadro istologico. Anche<br />
l’espressione macroscopica è però diversa.<br />
FORMA ENDEMICA: riguarda le zone all’equatore. Innanzitutto questo è un linfoma legato<br />
al virus di Epstein-Barr. In queste aree centrali dell’Africa, paradossalmente, è difficile<br />
avere delle leucemie acute, ma il vuoto epidemiologico lasciato dalle leucemie acute,<br />
viene occupato da questi linfomi. In queste aree in cui è più diffuso, il linfoma ha una<br />
presentazione clinica del tutto particolare perché coinvolge le ossa della regione testa-<br />
scaricato da www.sunhope.it
collo, cioè soprattutto il mascellare, tanto è vero che si presenta con una tumefazione del<br />
mascellare ed è molto aggressivo cioè tende a diffondere facilmente.<br />
FORMA SPORADICA: è più caratteristica delle nostre parti, io l’ho vista diverse volte, in<br />
cui pur avendo lo stesso quadro microscopico della forma endemica; qui però non si<br />
localizza alle ossa,ma all’apparato intestinale tanto è vero che spesso sfugge perché<br />
spesso colpisce soggetti in età pediatrica o cmq molto giovani come la forma africana. Si<br />
presenta con sintomi da malassorbimento perché c’è in coinvolgimento dei linfonodi non<br />
solo mesenterici, intestinali, ma anche della mucosa intestinale. Quindi spesso si arriva<br />
alla diagnosi tardivamente. Un’altra caratteristica di questo linfoma rispetto al suo gemello<br />
africano è che in genere tende ad essere più indolente e risponde bene alla terapia per cui<br />
ha ampi periodi di remissione.<br />
FORMA IATROGENA O AIDS ASSOCIATA: è uno dei linfomi che rientra nella malattia da<br />
HIV(aids) oppure può essere associato all’immunodepressione(vi ricordo che il virus<br />
dellEpstein-Barr è molto diffuso, per motivi che non conosciamo ancora bene, e in seguito<br />
ad infezione può rimanifestarsi in condizione di immunosoppressione dando luogo ad un<br />
linfoma del genere).<br />
Quali sono le caratteristiche morfologiche fondamentali? Ve lo faccio vedere attraverso le<br />
immagini. Il fenotipo è CD20 positivo, esprime le IgM, la Bcl-6, esprime anche il CD10 per<br />
cui uno può pensare al linfoma del centro germinativo però queste cellule sono più grandi<br />
e non esprimono la bcl-2 ma la bcl-6. Presenta poi un quadro morfologico particolare che<br />
ci consente di risolvere il problema diagnostico. Innanzitutto c’è un aspetto istologico<br />
dominante che si chiama aspetto “starry sky”, in questo caso non è un centro germinativo,<br />
ma è tutto il linfonodo. Vedete tutti questi spazi chiari che sono occupati da cellule<br />
macrofagiche, le stesse cellule macrofagiche che ritroviamo nei follicoli linfatici, che<br />
evidentemente sopravvivono in questo caso e conferiscono l’aspetto tipo “cielo stellato”.<br />
Questa era la prima caratteristica. La seconda caratteristica è che , come vedete, sono<br />
cellule di dimensioni intermedie, ricche di cromatina nucleare e che tendono a disporsi in<br />
“ammassi sinciziali”, cioè è difficile distinguere la singola identità delle cellule, sono così<br />
ammassate che non si distinguono i confini delle diverse cellule (aspetto sinciziale). Oltre<br />
ad essere CD20 positive, questi sono i linfomi più positivi per Ki67. Non c’è una cellula<br />
negativa per questo marker, mentre se facciamo il tdt, perché potremmo avere dubbio di<br />
linfoma linfoblastico, vediamo come il tdt è negativo. E siamo all’ultima categoria, di cui<br />
parleremo solo di poche forme, i linfomi a cellule NK che rappresentano il 10-12% di tutti i<br />
linfomi.Sono pochi ma pieni di devozione perché sono centinaia di forme. Noi parleremo<br />
solo di quelle più frequenti.<br />
LINFOMI A CELLULE NK<br />
Linfomi a cellule T mature, mature vuol dire che esprimono i marcatori di maturazione.<br />
E’un linfoma T periferico, tipico dell’età avanzata. Talvolta può essere associato a malattia<br />
autoimmunitaria. Si può localizzare a vari organi, il midollo è spesso positivo, si<br />
accompagna ad un ipergammaglobulinemia. Qual è l’aspetto istologico dominante? Voi<br />
scaricato da www.sunhope.it
sapete che le aree paracorticali ricche di cellule T hanno queste venule ad alto endotelio,<br />
questi linfomi si caratterizzano per un’ampia proliferazione ed arborizzazione delle venule<br />
ad alto endotelio perché si trovano “in terra loro” come si suol dire, rappresentano il<br />
pabulum di linfocitiT. Un altro aspetto caratteristico è la “compartimentalizzazione dello<br />
stroma”, cioè lo stroma si compartimentalizza in tante nicchiette per cui vediamo<br />
un’immagine quasi ad alveolare, ogni cellula stà un po’ nella sua nicchitta e questa è un<br />
po’ una caratteristica che hanno tutti i linfomi a cellule T. L’immunofenotipo esprime il CD2<br />
e il CD3, il CD4 e il CD8 a seconda dei singoli casi. In alcuni casi una cellula può<br />
impazzire del tutto ed esprimere addirittura marker tipici delle cellule B. Se andiamo a fare<br />
il CD3, vedete, sono tutte cellule positive; questo CD3 può essere di membrana ma può<br />
essere anche citoplasmatico a dimostrazione della pazzia che si discosta dalla norma!<br />
Questo in figura è un linfoma angioimmunoblastico a cellule T. Questo ha<br />
rappresentato per noi, per molti anni, un bel grattacapo; addirittura 10-15 anni fa non si<br />
chiamava linfoma ma veniva inquadrato tra le linfoadenopatie. Era caratterizzato da un<br />
decorso molto variabile, alcune forme sembravano andare bene, altre erano più<br />
aggressive per cui non vi dico i volumi, i lavori che sono usciti in letteratura perché ognuno<br />
poi aveva una sua interpretazione! E’ un linfoma a cellule T, ma perché<br />
angioimmunoblastico? Perché la sua caratteristica è di avere questa grande ricchezza di<br />
vene ad alto endotelio, e di avere anche questo immunoblasto. L’immunofenotipo è lo<br />
stasso: sempre CD2 e CD3. Ecco, queste figure che vedete sono venule ad alto endotelio,<br />
a stento ci passa un linfocita, un monocita. Se facciamo il CD34 vediamo questa grande<br />
abbondanza di vasi che è una caratteristica di questo linfoma, esprime il CD3, anche qui<br />
spesso a livello citoplasmatico, e c’è anche una componente CD20 positiva reattiva.<br />
LINFOMA T ASSOCIATO AD ENTEROPATIA<br />
Di questo mi ricordo un caso: era un ragazzo, uno sportivo, anche abbastanza famoso nel<br />
suo campo. Mi ricordo il dolore della sua famiglia quando fu fatta la diagnosi. Questo<br />
linfoma può essere associato alla CELIACHIA che è un’intollerranza al glutine (in questo<br />
caso al glutine, ma il fenomeno delle tolleranze è fortemente in aumento ed anche per<br />
tante altre sostanze). La prognosi è severa. Oltre a celiachia, è associato a dermatite<br />
erpetiforme, è associato a masse intestinali quindi è un linfoma prettamente intestinale ed<br />
è un linfoma a cellule T. Si spiega perché noi pensavamo che era una metastasi, perché<br />
se andiamo a guardare queste cellule abnormi, mostruose, addirittura possono esprimere<br />
degli antigeni epiteliali; ma la loro caratteristica è che esprimono questo marcatore: l’ALK,<br />
sia citoplasmatica che di membrana.<br />
LINFOMA ANAPLASTICO A CELLULE T DELLA CUTE<br />
Questo ve lo racconto perché paradossalmente, rispetto al suo gemello che non coinvolge<br />
la cute, questo è migliore. Se facciamo un follow-up vediamo che, a 5 anni dalla diagnosi,<br />
presenta una sopravvivenza pari al 90% a differenza dei linfomi a grandi cellule che<br />
scaricato da www.sunhope.it
coinvolgono gli altri organi. Addirittura è prevista una regressione spontanea di questo<br />
linfoma in una certa percentuale di casi.<br />
MICOSI FUNGOIDE<br />
E’ il linfoma più classico a cellule T. La micosi fungoide si chiama così perché, a fine ‘800,<br />
un medico francese che si chiamava Albert vide questo linfoma (che è un linfoma cutaneo)<br />
e, poiché la Francia aveva delle colonie, e il linfoma presentava delle placche rilevate nel<br />
suo decorso, la chiamò micosi, anche se questo è un nome improprio! E’ un nome<br />
improprio perché questo è un linfoma a cellule T. Evolve in diverse fasi. La sua<br />
caratteristica è di dare queste manifestazioni cutanee, che prima sono delle papule<br />
eritrodermiche, poi sono dei noduli e poi diventano placche, placche molto dure, quasi<br />
come il legno. E’ legato a queste cellule T micotiche che hanno un “nucleo cerebriforme”<br />
con molte incisure, tanto è che alcuni anni fa un autore fantasioso le paragonò a quelle<br />
palle di carta che i ragazzini facevano per giocare a pallone(cioè pieni di incisure,<br />
irregolarità). E’ un linfoma dell’anziano ed ha una prognosi relativamente favorevole, con<br />
un decorso molto lento. Pensate che, in uno stadio iniziale, l’opzione terapeutica più<br />
frequente è quella di non fare niente, sempre che non si capiti in mano ad un pesce cane,<br />
il pesce cane fa sempre qualcosa!!<br />
PAPULOSI LINFOMATOIDE<br />
Si tratta di papule o noduli che possono persistere o regredire. Si tratta di una situazione<br />
instabile che può andare verso la micosi fungoide. Sono presenti linfociti T atipici, anche<br />
un po’ cerebriformi, che ricordano proprio la micosi fungoide.<br />
Vedete sopra che stà scritto: SINDROME DI CEZARY. Non è altro che una micosi<br />
fungoide con un quadro erpetico(?). Se queste cellule anomale, atipiche, si manifestano<br />
anche nel sangue periferico, prende il nome di sindrome di Cezary.<br />
Vediamo i quadri clinici della micosi fungoide: le manifestazioni cliniche sono queste<br />
papule, che tendono a diventare noduli e poi placche dure, ulcerate che coprono molte<br />
aree perché tendono a confluire. Il quadro istologico da che cosa è caratterizzato? Questa<br />
è una cosa che noi vediamo spesso; ogni settimana ci capita qualche caso. C’è un<br />
dermotropismo evidente dei linfociti, qui vedete l’epitelio squamoso e qui ancora vedete<br />
tutti questi linfociti; dei linfociti che hanno un aspetto un po’ irregolare. In alcuni casi,<br />
soprattutto quando la malattia avanza di più, troviamo come dei noduli all’interno<br />
dell’epitelio, pieni di queste cellule linfoidi, che siccome hanno un aspetto cerebriforme, ci<br />
possono spiegare il modo errato con cui vengono chiamati questi complessi: “ascessi di<br />
Pautrier”. Si chiamano così perché questo Pautrier pensava che erano ascessi fatti di<br />
granulociti, perché vedeva questi nuclei irregolari! Invece non sono ascessi ma sono<br />
infiltrati tumorali. Se vediamo l’immagine, questa è una tipica cellula micoide, cioè CD4 e<br />
CD5 positive, alcune cellule di queste le troviamo anche nell’epidermide. All’inizio i linfociti<br />
sono pochi per cui è difficile fare la diagnosi nello stadio iniziale.<br />
scaricato da www.sunhope.it
Questa è l’immagine della papulosi linfomatoide: vedete delle papule, anche qui cellule<br />
molto irregolari, cerebriformi. E’ comunque un quadro di difficile inquadramento e non è<br />
ancora chiara la patogenesi.<br />
Questo invece è il linfoma a cellule NK: sono dei linfomi particolari, una delle sedi preferite<br />
è il naso, oppure la regione testa-collo; sono legati anch’essi al virus di Epstein- Barr,<br />
hanno una sopravvivenza mediocre però, dopo terapie recentemente introdotte, la<br />
sopravvivenza è molto migliorata. La caratteristica di queste cellule NK è che sono CD56<br />
positive e presentano anche il CD3 intracitoplasmatico. Siccome si tratta di cellule anche<br />
citotossiche perché sono NK, esprimono anche dei marcatori tipici dei natural killer (per<br />
esempio la perforina o altre sostanze) che ci aiutano ad identificare questo tipo di linfomi.<br />
La caratteristica principale è che questo tipo di linfoma tende ad infiltrare i vasi, a<br />
distribuirsi intorno ai vasi e a distruggere i vasi, quindi ha un pattern angiocentrico ed<br />
angiodestruente. Può poi distribuirsi nella regione testa-collo. Anche qui, come vedete,<br />
sono cellule irregolari, come in tutti i linfomi a cellule T. Tra le proteine possiamo trovare<br />
EBER che è caratteristica dell’infezione da Epstein-Barr.<br />
RIEPILOGO: incidenza relativa dei linfomi a cellule T ed NK----12%dei linfomi non<br />
hodgkin.<br />
Linfomi a cellule T maturi---6%<br />
Linfomi angioimmunoblastico<br />
Linfoma T associato ad enteropatia<br />
Linfoma anaplastico a grandi cellule T<br />
Micosi fungoide(che comprende anche sindrome di cezary e papulosi<br />
linfomatoide)<br />
Linfoma a cellule NK<br />
Esiste anche un’altra malattia che non è proprio imparentata coi linfomi però la citiamo. Voi<br />
sapete che abbiamo parlato di cellule dentritiche, di questi istiociti….c’è una ISTIOCITOSI<br />
A CELLULE DI LANGHERANS. Una volta veniva chiamata “istiocitosi X”, perché era<br />
sconosciuta. Si caratterizza perché hanno questi nuclei con queste scanalature, questa<br />
ricchezza di eosinofili, e possono essere forme come il “granuloma eosinofilo”, quindi<br />
banali(per cui una volta operati non ci sono problemi), oppure forme progressive.<br />
Interessano l’età giovanile, esprimono il CD1A, l’Ex100, la langherina. Quando abbiamo<br />
forme non localizzate, ma multicentriche, in genere la prognosi è severa e prendono nomi<br />
tutti strani che è meglio che non vi dico.<br />
Esiste anche la patologia maligna che interessa i macrofagi “starry sky”: è l’istiocitosi<br />
maligna e poi linfangioma, il sarcoma di kaposi, tutte cose di cui parleremo più avanti.<br />
scaricato da www.sunhope.it
<strong>Anatomia</strong> <strong>Patologica</strong><br />
Prof.Rossiello<br />
31/3/2011<br />
Se la freccia non coglie il bersaglio non ve la prendete con il bersaglio, con le frecce o con l'arco, ma con<br />
chi l'ha tirata. [Confucio]<br />
LINFOMI NON-HODGKIN (...continuo)<br />
Stadiazione di Ann-Arbor<br />
Questa stadiazione, chiamata "Ann Arbor" riferendosi ad una località degli Stati Uniti, è una delle<br />
cose più universalmente riconosciute che ci sono in anatomia patologica.<br />
Questa stadiazione vale sia per i linfomi di Hodgkin che per i linfomi non Hodgkin e i suoi criteri<br />
base sono:<br />
- interessamento di sedi linfoghiandolari da un solo lato o entrambi del diaframma.<br />
- il coinvolgimento o meno del midollo<br />
- estenzione della malattia a più organi.<br />
Basandosi su questi criteri si può fare la stadiazione:<br />
• Stadio I: interessamento di una singola stazione linfonodale<br />
◦ Ie: un solo organo o una sede extra-linfatica (e = extralinfatica)<br />
• stadio II: interessamento di due o più stazioni linfoghiandiolari, ma che sono dallo stesso<br />
lato del diaframma; per cui ad esempio si può parlare di stadio II se c'è un linfonodo<br />
inguinale e la milza coinvolti. Ovviamente se c'è un linfonodo laterocervicale e inguinale<br />
coinvolti non è più uno stadioII perchè sono da entrambi i lati del diaframma.<br />
• stadio III: linfonodo o siti extralinfoghiandiolari da entrambi i lati del diaframma con<br />
sotto-categorie:<br />
◦ IIIe: interessamento localizzato contiguo di organo o una sede extralinfatica<br />
◦ IIIs: è coinvolta la milza<br />
◦ IIIes: coinvolgimento sia della milza, sia un altro sito extralinfatico<br />
• stadio IV: quando c'è un'infiltrazione diffusa o disseminata di uno o più organi<br />
extralinfatici con o senza interessamento linfonodale associato.<br />
Per questo stadio è molto importante il midollo osseo; per esempio se è colpito il midollo<br />
dal linfoma di Hodgkin è già stadio 4 perchè questo vuol dire che c'è già una<br />
disseminazione e il midollo stesso viene considerato fonte di disseminazione anche se c'è<br />
solo un organo coinvolto.<br />
◦ IV Bulky: presenza di una massa che ha un diametro pari o superiore ai 10cm. Ha<br />
valore prognostico molto negativo. (è una sottostadiazione definita da Cotswold)<br />
Ognuno di questi stadi presenta due sottostadi:<br />
A = assenza di segni sistemici ( astenia, febbricola, sudorazione, perdita di peso >10% in 6 mesi)<br />
B = presenza di questi sintomi<br />
scaricato da www.sunhope.it
In passato era data alla milza un'importanza notevole tanto è vero che i pazienti venivano sottoposti<br />
a splenectomia sopratutto se la milza non era interessata.<br />
È un paradosso perchè si pensava che la milza funzionasse da serbatoio di disseminazione dei<br />
linfomi di Hodgkin e allora si preferiva togliere la milza non presa per evitare in ogni caso questo<br />
potenziale rischio di disseminazione. Per lo stesso motivo per cui per esempio nel cancro della<br />
mammella si procedeva alla ovariectomia: perchè non avevamo delle terapie endocrine adeguate<br />
È tale l'importanza del midollo che in tutti questi pazienti si fa la biopsia osteomidollare con un ago<br />
"Jamshidi" a livello della cresta iliaca. Questo è stato anche un progresso della medicina perchè una<br />
volta si faceva la biopsia sternale che non era scevra di inconvenienti, dolori e così via, mentre<br />
l'agobiopsia della cresta midollare in mani esperte diventa relativamente semplice e poco dolorosa.<br />
Categorie prognostiche: il buono, il brutto e il cattivo<br />
se vogliamo fare una valutazione sommaria di linfomi non-Hodgkin, di cui abbiamo parlato,<br />
- il buono è rappresentato dai linfomi a piccole cellule (40-50% dei casi)<br />
- il brutto che è rappresentato da linfomi a grandi cellule B, da linf anaplastici,da linfomi NK,<br />
anaplastici<br />
- i cattivi sono i linfomi linfoblastici fatti dai precursori delle cellule T e B e dai linfomi Burkitt<br />
Volendo ancora semplificare molti distinguono :<br />
- linfomi indolenti sono tumori di "vecchia cilindrata" che avanzano lentamente, crescono<br />
lentamente, e proprio per questa loro indolenza non rispondono bene alla terapia, sono refrattari a<br />
qualunque tipo di stimolo sia positivo che negativo, ha un solo problema: tende a recividare.<br />
- linfomi dolenti paradossalmente il linfoma aggressivo risponde di più alla terapia probabilmente<br />
perchè gran parte dei chemioterapici agiscono in rapporto alla fase proliferativa, ed essendo questi<br />
linfomi caratterizzati da un'elevata attività proliferativa, rispondono di più (risposta o tutto o niente),<br />
e se rispondono c'è anche un periodo di remissione molto piu lungo.<br />
Se paragoniamo in generale la sopravvivenza dopo trapianti (l'autotrapianto è quello più efficace),<br />
la sopravvivenza a 5 anni riguarda oltre il 90% dei pazienti (che avrebbero avuto 6 mesi di vita<br />
senza una terapia adeguata), e la sopravvivenza libera da malattia arriva al 60%.<br />
10 anni viene considerato il limite, il giro di boa per cui si parla di guarigione; tutti questi soggetti<br />
festeggiano la data del trapianto come una seconda nascita come se fossero ritornati alla vita.<br />
La sopravvivenza èmigliorata a 5 anni per i linfomi aggressivi e si va dal 35% (sopravvivenze<br />
libere da malattie) al 77% nell'ultimo periodo sopratutto per quanto riguarda la polichemioterapia<br />
con rituximab più autotrapianto perchè c'è una sequenzialità di eventi nel trattamente di questi<br />
pazienti.<br />
Fattori di rischio<br />
c'è un'indice internazionale applicato dagli ematologi che contempla i fattori di rischio che sono:<br />
- stadio avanzato (stadio 3 o 4)<br />
- eta >60 anni<br />
- condizioni generali ( indice di performance con parametri a cui si da un punteggio) soddisfacenti<br />
o non soddisfacenti<br />
- LDH aumentato<br />
- più di due siti extralinfoghiandolari (rientriamo nella stadiazione)<br />
E quindi si valuta il rischio, più fattori sono presenti, più arriviamo a un alto rischio (4 o 5 di questi<br />
fattori) fino ad arrivare a basso rischio se non è presente nessuno di questi fattori o uno solo.<br />
scaricato da www.sunhope.it
Terapia<br />
Chirurgia: serve quando c'è una grande massa e in genere, trattandosi di una malattia sistemica, la<br />
chirurgia non è una terapia efficace. Così come la radioterapia serve solo quando permane una<br />
grande massa e non si riesce con gli altri mezzi terapeutici ad ottenere la scomparsa della massa<br />
Immunoterapia: grande novità è rappresentata da questa nuova tipologia di terapia che si pratica<br />
con gli anticorpi anti-CD20 come il Rituximab. È un anticorpo chimerico molto utilizzato con la<br />
maggior parte dei linfomi non-Hodgkin (è una terapia diversa da quella utilizzata per i linfomi di<br />
Hodgkin). Qualcuno adopera anche l' α-interferone.<br />
Immunoradioterapia: è un'ulteriore sviluppo della tecnica con anticorpi monoclonali. Non solo<br />
abbiamo un anticorpo che colpisce il bersaglio (microciti B), ma coniughiamo a questo ancticorpo<br />
anche una sostanza radioattiva, tossica, per cui non solo colpiamo una volta, ma è come nella box<br />
quando si attacca con un doppio gancio, quindi colpiamo il linfoma due volte.<br />
Per i linfomi non Hodgkin abbiamo una faretra molto ricca di frecce (cit.) e bisogna scegliere quella<br />
giusta nel momento giusto.<br />
Possiamo coniugare questi anticorpi con ittrio o con iodio 131 e in genere questa è una terapia di II<br />
livello e di quando c'è stata una recidiva. una delle frecce a nostra disposizione è usare questo<br />
anticorpo come il Rituximab però marcato con una sostanza radioattiva tossica .<br />
Mono/poli-chemioterapia: che si usano in combinazione con la terapia biologica con l'anticorpo<br />
anti-CD20, per la maggior parte dei linfomi.<br />
Il CHOP è una miscela di chemioterapici ed in particolare c'è l' R-CHOP dove R sta per Rituximab.<br />
Se si osservano le curve di sopravvivenza, la sopravvivenza arriva al 60% se si usa R-CHOP e<br />
scende sotto il 40% se usiamo la polichemioterapia tradizionale.<br />
La situazione è migliorata se andiamo a vedere anche questi sono i dati american cancer society del<br />
2010 che fotografano la situazione fino al 2007. C'è stato un guadagno della mortalità per i linfomi<br />
non Hodgkin pari al 20-25 %; questo è stato un importante obbiettivo raggiunto.<br />
Anticorpo anti-CD20: È un anticorpo chimerico perchè è fatto da regioni variabili murine e<br />
regioni costanti invece umane.<br />
Si è visto che il CD20 non solo è molto specifico per il linfocita B, e quindi è utilizzabile per<br />
identificare la cellula, ma è anche legato alla sopravvivenza della cellula.<br />
Se blocchiamo il CD20 la cellula si indebolisce molto e quindi questo trattamento insieme alla<br />
polichemioterapia ha la stessa azione del "doppio gancio" se poi ci mettiamo pure la radioterapia<br />
abbiamo tre colpi e il linfoma va a tappeto.<br />
C'è però un problema: alcune cellule sopravvivono e le cellule "ex-CD20" che sopravvivono sono<br />
delle cellule staminali; è interessante notare che queste nuove cellule B non esprimono piu il CD20;<br />
segno dalla plasticità che ha l'organismo.<br />
Questo fenomeno risulta ancora più importante quando noi dobbiamo diagnosticare una recidiva;<br />
cioè abbiamo un soggetto con il linfoma di Hodgkin a distanza da 3 o 4 anni dalla cura si presenta<br />
un linfonodo ingrossato. Se noi andiamo a fare i marcatori per sapere che tipo di linfoma è, e gli<br />
facciamo il CD20, probabilmente ci risulterà negativo, perchè è come se il linfoma ragionasse "non<br />
mi conviene esprimere questo CD20" e si è creato un clone, normale o neoplastico che sia, che non<br />
esprime il CD20, ma esprime il PAX-5 che è un marcatore nucleare pure dei linfociti B.<br />
scaricato da www.sunhope.it
In alcuni casi si possono fare degli errori perchè abbiamo una recidiva e non vediamo i linfociti<br />
CD20, così possiamo pensare che è un altro linfoma invece è lo stesso linfoma che ha cambiato<br />
espressività antigenica.<br />
Quindi il CD20:<br />
1. Interagisce con la sopravvivenza cellulare<br />
2. è espresso solo dalle celluleB<br />
3. Non è presente nelle cellule staminali emopoietiche<br />
4. Tutti i linfomi nonHodgkin a cellule B esprimono il CD20<br />
Terapia metronomica: è una terapia con la quale si somministra un basso dosaggio di farmaco in<br />
modo continuo. Rappresenta una grande novità perchè prima quando si facevano i dosaggi si<br />
davano giornalmente grosse botte (cicli) di chemioterapia.<br />
La si somministra in modo da evitare di arrivare vicini alla dose massima letale, c'è un continuum,<br />
si può usare una dose ravvicinata, si possono usare particolari pompe che somministrano<br />
continuamente questo chemioterapico evitando di raggiungere le dosi massimali in una soluzione,<br />
dando questa dose diluita nell'arco delle 24 ore.<br />
Una delle ultime novità per la quale si adopera molto la terapia metronomica, sono i fattori antiangiogenetici.<br />
questa è una terapia che si sta estendento non solo ai linfomi (dove c'è un protocollo<br />
utilizzato), ma anche altri tipi di tumori per il tipo di attività, dato che tutti i tipi di tumori sono<br />
caratterizzati da attività neoangiogenetiche. Bloccando questa attività, attraverso uno stimolo<br />
continuo di fattori antiangionetetici, non risolviamo il problema, ma creiamo una situazione di stallo<br />
tra ospite e tumore. L'obiettivo che si pone la terapia quando non riesce a risolvere il problema è<br />
quanto meno provare a bloccarlo.<br />
Andiamo incontro a un cambio completo dell'assetto clinico della patologia che si presentava acuta<br />
e noi tendiamo invece a cronicizzarla. In vari casi noi vedremo per esempio che con queste terapie<br />
anche un carcinoma che avremmo considerato fatale, tende a diventare cronico, per cui il paziente<br />
può convivere con questa patologia anche per vari anni.<br />
Oligonucleotidi antisenso: si producono oligonucleotidi di DNA che sono speculari al mRNA per<br />
cui si vanno a localizzare lungo e a bloccare mRNA e significa che si blocca la trasmissione del<br />
segnale per cui rendono inefficaci tutta una serie di segnali.<br />
Un tipico esempio di questa terapia, già utilizzabile nei linfomi, riguarda la BCL-2 che è una<br />
proteina implicata nella apoptosi e si usano degli oligonucleotidi antisenso anche per interferire con<br />
questa proteina e con questo gene; il gene c'è, ma ne blocchiamo l'espressività.<br />
Trapianto autologo: In un soggetto già trattato con tutte quelle frecce che abbiamo visto, e che<br />
continua ad avere recidive, si esegue una trategia molto ingegnosa: prima di tutto si raccolgono le<br />
cellule staminali del soggetto o attraverso le biopsia osteo-midollari o attraverso la plasmaferesi<br />
cioè dal sangue circolante che è una pratica meno dolorosa, ma più lunga.<br />
Per essere sicuri che siano cell staminali le si mette a contatto con un anticorpo che riconosce il<br />
CD34, poi attraverso tecniche particolari tutta questa popolazione viene conservata e criopreservata<br />
con delle particolari sostanze crioprotettive che ne impediscono la distruzione; a questo punto si dà<br />
al paziente una specie di bomba atomica locale o di chemioterapia o di radioterapia in modo da<br />
distruggere tutte le cellule linfoidi, comprese le cellule staminali.<br />
Noi siamo ancora agli albori di questa terpapia perchè qualche inconveniente può succedere. Infatti<br />
si infondono le cellule staminali del paziente stesso, per cui c'è un periodo pericoloso in cui il<br />
paziente deve stare completamente isolato perchè non ha più sistema immunitario e qualunque<br />
contatto con l'esterno lo può portare a morte Si dà una degenza di 15-20 giorni circa per essere<br />
sicuri, durante la quale si fanno analisi continue e c'è pericolo per la piastrinopenia perchè tutto il<br />
midollo tutte le linee sono distrutte.<br />
scaricato da www.sunhope.it
Trapianto eterologo: Il trapianto eterologo, o trapianto allogenico, invece si usa quando il paziente<br />
non ha più il midollo osseo funzionante (per esempio i pazienti che hanno già tentato il trapianto<br />
autologo o dove la biopsia osteo-midollare non permette di raccogliere un numero di cellule<br />
staminali sufficiente). Questo è piu difficile perchè si deve superare il problema della compatibilità,<br />
diversi scelgono consanguinei, ma c'è sempre pericolo di un rigetto.<br />
Complicanze dei trapianti: Ci sono problematiche dei trapianti e del trattamento con i nuovi<br />
chemioterapici: endocrine, infezioni virali di vario tipo, ma possiamo avere tossicità più serie<br />
(fibrosi), cardiotossicità da chemioterapici o addirittura delle tossicità fatali come le leucemie, altri<br />
linfomi, carcinomi, e così via.<br />
Ipotesi del microambiente: Una volta che facciamo il trapianto, non abbiamo una percentuale di<br />
successo pari al 100%, probabilmente perchè siamo ancora alla preistoria dei trapianti. Per questo si<br />
va per ipotesi, e probabilmente una normale maturazione delle cellule staminali prevede<br />
necessariamente che si sviluppino in un microambiente adatto. Siamo quindi sicuri che le cellule<br />
che andiamo ad infondere siano state in un microambiente adatto? E siamo sicuri che le cellule che<br />
siamo andati ad infondere siano tutte normali?<br />
Il microambiente è rappresentato da markers, segnali tipo growth factors, chemochine, ed è<br />
rappresentato dal terreno su cui si impiantano queste cellule staminali. Vedremo poi in altri tipi di<br />
patologie come questo microambiente è fondamentale.<br />
Linfoma a cellule B o T<br />
Quello a cellule B è un linfoma che non si riusciva a trattare con le poli-chemioterapie tradizionali,<br />
ma con l'autotrapianto sì, e dà una sopravvivenza vicina al 50-60% a 5 anni.<br />
Il linfoma T non è che avesse assolutamente questa sopravvivenza tanto è vero che con terapia<br />
tradizionale e senza autotrapianto questa percentuale arriva al 10%, quindi con un cambio<br />
drammatico di prospettive.<br />
Questa strategia dell'autotrapianto si comincia a diffondere e si cominciano a trattare altre patologie<br />
con le cellule staminali. Considerando l'efficacia di questo trattamento le cellule staminali sono<br />
importantissime, e sono la fonte del disastro oncologico, ma possono essere anche la fonte della<br />
guarigione.<br />
Se tutto nasce dalle cellule staminali, per quale motivo un linfoma appare composto da cellule<br />
differenziate come le palsmacellule? Com'è possibile che una realtà così dinamica come la cellula<br />
staminale, che è in grado di fare qualsiasi cosa, dia origine ad una patologia da espansione di un<br />
clone ben specializzato? sembra quasi una discordanza in sè, ma che in effetti è solo apparente<br />
perchè gli eventi oncogenetici che incidono sulle cellule staminali che sono responsabili di tutto,<br />
possono indurre delle mutazioni geniche in grado di avere un effetto repressivo o derepressivo.<br />
Se un linfoma è un immunocitoma o plasmocitoma o un mieloma è evidente che è intervenuta una<br />
derepressione. Manca un controllo normale e tutte le cellule si differenziano in maniera anomala,<br />
neoplastica; quindi in seguito alla repressione mancano quei meccanismi differenziativi per cui la<br />
cellula si ferma allo stadio preB.<br />
Se le mutazioni hanno agito precocemente avremo linfomi molto anaplastici, se agiscono<br />
tardivamente avremo la tendenza a una maggiore differenziazione.<br />
Non si può pensare di dare a questi fenomeni una spiegazione semplicistica che preveda il<br />
passaggio diretto tra cellule differenziate che diventano neoplastiche; se fosse così sembrerebbe<br />
quasi che le cellule della zona marginale dicono "vabbè ci siamo scocciate di essere normali, questo<br />
è un mondo in cui tutti impazziscono prima o poi, e impazziamo anche noi".<br />
scaricato da www.sunhope.it
MILZA<br />
Istologia macroscopica: la milza è posizionata a sinistra sotto l'arcata costale, se la milza è<br />
ingrandita in genere sporge dall'arcata costale; è piu facile scorgerla quando il paziente fa<br />
movimenti respiratori per favorire l'abbassamento della milza per poterla cogliere. Possono anche<br />
essere presenti milze accessorie. La milza oltre ad avere una capsula ben evidente è fatta da una<br />
polpa bianca e una rossa. al taglio la polpa bianca è rappresentata da strutture linfoidi.<br />
Polpa rossa rappresentata da seni ematici (rossi perchè sono ricchi di sangue) e spiegano la ricca<br />
vascolarizzazione della milza (non a caso in passato si dava alla milza la funzione del cuore).<br />
Una delle funzioni della milza è quella di rimuovere le emazie ormai esauste (funzione di pulizia).<br />
I seni sono endoteliali in cui c'è una funzione di eliminazione sulle emazie di linfociti o altre cellule.<br />
Polpa bianca è costituita anche da follicoli linfatici secondari, ma ci stanno linfociti B o T?<br />
Ha un'organizzazione diversa dalle linfoghiandole perchè là dove ho messo T (immagine) c'è in<br />
genere polpa bianca e riconosciamo un vaso chiamato "arteriola centro-follicolare" che è circondata<br />
a manicotto da linfociti T. In maniera piu eccentrica rispetta all'arteriola si espande l'area B, qui<br />
vediamo follicolo secondario, qui vediamo la corona,... in questo caso nella milza le cellule<br />
mantellari sono molto meno rispetto linfonodo ma è molto espansa la zona marginale molto ben<br />
sviluppata come spessore.<br />
Lesioni non noplastiche<br />
Esempi di patologie non neoplastiche sono:<br />
• Ipersplenismo primario o secondario<br />
• iposplenismo<br />
• splenomegalie secondarie (anemia emolitica, trombocitopenia)<br />
• splenomegalia congestizia (ipertensione portale idioatica o secondaria)<br />
• splenite (acuta, granulomatosa)<br />
• infarto<br />
Splenomegalia dal punto di vista anamopatologico può essere:<br />
• congestizia quando è sopratutto legata a un accumulo di sangue; per esempio soggetto<br />
talassemico è facile che sviluppi una splenomegalia congestizia o in alcune anemie su basi<br />
congenite perchè c'è la rimozione di queste emazie abnormi.<br />
• fibrosa aumento della massa fibrosa, quindi la milza assume una consistenza più dura.<br />
• fibrocongestizia si può manifestaee nel corso degli anni in pz con talassemia. Alla<br />
splenomegalia congestizia può seguire la accentuazione dei fenomeni fibrotici.<br />
Lesioni neoplastiche della milza<br />
• Linfomi primitivi (il 3% dei linfomi)<br />
◦ Non Hodgkin:<br />
▪ LLC ▪ Zona follicolare ▪ Zona mantellare<br />
▪ Zona marginale ▪ A grandi cellule B<br />
◦ Hodgkin (multicentricità dei follicoli ovvero presente in molti follicoli linfatici e può<br />
presentarsi con masse biancastre)<br />
• Disordini mieloproliferativi (leucemia mieloide, mielodisplasia...)<br />
• Altri tumori (angioma, angiosarcoma, linfoangioma, essendo riccamente vascolarizzata)<br />
scaricato da www.sunhope.it
TIMO<br />
Il timo subisce un'involuzione nel corso di anni in genere dopo i 20-25anni; comincia involuzione<br />
nel senso che aumenta la quota di adipe e diminuisce la parte nobile di parenchima.<br />
Mantiene un'architettura lobulare e si vedono questi corpi eosinofili che sono i corpuscoli di<br />
Hassall, che si trovano in genere nella parte intermedia del lobulo timico, mentre la parte più<br />
superficiale è detta corticale timica; è inoltre visibile il tessuto adiposo che aumenta negli anni.<br />
Zona corticale: sono presenti cellule epiteliali di vario tipo, compresi i corpuscoli di Hassall.<br />
In questa zona c'è una commissione tra linfociti e cellule epiteliali.<br />
Le cellule epiteliali che si possono ritrovare sono:<br />
• cellule blastiche (sottocapsculari)<br />
• cellule nutrici vere e proprie (corticali): producono una serie di sostanze (timolina,<br />
timocrescina, timosina, timopoietina) in grado di indurre il differenziamento dei linfociti T.<br />
Possono essere di varia forma: fusate, dendritiche, rosettiformi.<br />
• Midollari<br />
• corpuscoli di Hassall (strutture concentriche fatte da cell epiteliali e materiale corneo).<br />
Sono composti da cellule con all'interno materiale corneo che rappresentano involuzione<br />
delle cellule epiteliali. Non è ancora ben nota la loro natura; non si sa perchè si formino<br />
questi corpuscoli di cellule epiteliali con del materiale corneo al centro.<br />
Sono cellule particolari perchè oltre ad esprimere i marker della serie epiteliale, esprimono il<br />
marker CD5 che è un marker linfoide ed il CD117<br />
Oltre a queste cellule abbiamo cellule:<br />
• denritiche Interdigitate (incontrate già nei linfonodi)<br />
• linfocita B (pochi)<br />
• linfociti T (sono la maggioranza)<br />
Nella corticale il primo marker che viene espresso è il TDT perchè è il marker dei linfociti T, anche<br />
quelli meno differenziati perchè negli strati superficiali della corticale ci sono i linfociti T non<br />
ancora differenziati. Facendo la citocheratina ci rendiamo conto che sopratutto gli strati superficiali,<br />
ma anche andando verso l'interno troviamo cellule epiteliali<br />
scaricato da www.sunhope.it
Maturazione dei timociti<br />
Nel timo i timociti seguono un processo di differenziazione che si traduce in una espressione di<br />
markers caratteristici per ogni fase di maturazione:<br />
Protimocita – timocita subcapsulare – timoc. corticale – timoc. midollare – linfocita periferico<br />
|------------------------------------------------------------------------|TDT<br />
|----------------------------------------------------------------------------------------------------------------| CD7<br />
|---------------------entrambi----------------<br />
|---------------------------------------------------| CD1a<br />
------------------------------------------------------------|CD4<br />
-----------------------------------------------------------|CD8<br />
|--------------------------------------------------------------------------------------| CD2 / CD5<br />
|---------cit----------------|---------------------------------sup----------------------------| CD3<br />
|----------------------------------------------------------------| TCR<br />
C'è il protimocita che in genere corrisponde al pro-linfocitaB [credo che il prof si sia confuso. Secondo<br />
logica, ma anche secondo internet, i protimociti vengono da pro-linfociti T] che si trova nel midollo osseo.<br />
Il pro-timocita viaggia, arriva nel timo e in una fase iniziale tra i marcatori più precoci esprime il<br />
TDT e il CD3.<br />
Mano a mano che diventa un timocita sub-capsulare, incontra le prime cellule epiteliali che sono le<br />
subcapsulari e incomincia ad esprimere il CD1a.<br />
In questo stadio il timocita subcapsulare sta facendo ancora le prove e non esprime selettivamente il<br />
CD4 o il CD8, ma dato che sta decidendo quale strada scegliere, c'è una coespressione di entrambi i<br />
markers nello stesso linfocita. Poi dallo stadio di timocita corticale esprimerà o l'uno o l'altro,<br />
mentre invece smetterà di esprimere il TDT.<br />
Il CD3 all'inizio è citoplasmatico e poi, quando il timocita arriva nella corticale, diventa<br />
superficiale, come nelle cellule adulte. Come abbiamo visto nei linfomi, dove nei linfomi più<br />
indifferenziati esprimono il CD3 nel citopalsma, allo stesso modo qui più la cellula è differenziata e<br />
più il CD3 sarà espresso sulla superficie.<br />
Riassumendo:<br />
• TDT e CD7 sono precoci<br />
• CD3 prima è citoplasmatico e poi è di membrana<br />
• CD4 e CD8 se sono espressi selettivamente riguardano il linfocita più differenziato.<br />
scaricato da www.sunhope.it
Lesioni non tumorali<br />
• Displasia<br />
• Atrofia (involuzione fisiologica)<br />
• Cisti timiche<br />
• Iperplasia<br />
• Timite follicolare (infiammazione, miastenia e patologie legate alla miastenia)<br />
Tumori del timo<br />
Distinguiamo tre grandi famiglie di tumori del timo<br />
Timoma:<br />
• TIPO A (benigno o quasi) costituito da cellule epiteliali poco atipiche che possono essere<br />
fusate o ovoidali. i linfociti sono pochi e tendono a esprimere come succede nella corticale,<br />
infatti questo tumore somiglia molto alla corticale, esprimono il TDT<br />
• TIPO B predominano i linfociti e le cell epiteliali sono poche. Le cellule epiteliali<br />
cominciano a manifestare delle lievi/moderate atipie. Questi linfociti possono esprimere<br />
anche altri marcatori oltre il TDT<br />
• TIPO C che di fatto è un carcinoma a tutti gli effetti, ha componente linfoide, ma è<br />
secondaria, probabilmente perchè si tratta di cellule linfoidi sopravvissute (carcinoma<br />
squamoso, etc). (lo schema sottostante l'ho copiato dalla slide).<br />
Benigno Tipo A Timoma midollare<br />
Tipo AB Timoma misto<br />
Maligno Categoria I Tipo B1 Prevalentemente corticale<br />
Tipo B2 Timoma corticale<br />
Tipo B3 Ca. timico differenziato<br />
Maligno Categoria II Tipo C Timoma maligno<br />
Timomi Benigni: capsulati, scarse atipie, recidive
Prof. Rossiello 01/04/2011<br />
TUMORI DEL TIMO:<br />
Continuiamo con i tumori del timo. Come vedete, c’è una categorizzazione: benigno, così così,<br />
maligno. Il benigno è soprattutto il tipo A, chiamato anche timoma midollare, è soprattutto<br />
caratterizzato dalla presenza di cellule epiteliali che non hanno delle atipie; se andiamo a vedere<br />
quei pochi linfociti che ci stanno, come succede nella midollare, sono dei linfociti maturi che quindi<br />
esprimono CD4, CD8 e non esprimono la TDT. Il tipo AB, invece, ha due componenti: una<br />
componente A e una componente B; quest’ultima è costituita soprattutto da cellule linfoidi,<br />
mentre la componente A somiglia al tipo A e quindi ha una componente epiteliale. Queste due<br />
componenti, molto spesso, sono separate, ma possono anche non esserlo così nettamente. Nella<br />
componente linfoide, ovvero nella componente B, i linfociti esprimono la TDT e cioè sono dei<br />
linfociti immaturi; nella componete A, invece, i linfociti sono maturi. La prognosi, intesa qui come<br />
disease free ( senza complicanze, libera da malattia ), è del 100% in questi casi.<br />
C’è poi il tipo maligno di categoria I (B),ovvero a basso grado di malignità, che è costituito da tre<br />
tipi che hanno una ricca componente linfoide; è inutile che io vi dica tutti i sottotipi … 1)c’è un tipo<br />
B1 prevalentemente corticale e cioè vuol dire che somiglia alla corticale e troveremo linfociti non<br />
maturi; 2) c’è un tipo B2 che è il timoma corticale; 3) c’è poi il B3 che sarebbe il primo passo di C<br />
(vedi dopo) , ovvero comincia a comparire una ricca componete epiteliale con delle atipie<br />
moderate. Il tipo C è, invece, un cancro, un carcinoma .. chiamato anche timoma maligno ma di<br />
fatto è un carcinoma (penso sia il tipo maligno di categoria II; l’ho dedotto dagli appunti copiati<br />
dalle slide) . Come vedete le aspettative prognostiche si riducono man mano che passiamo dal tipo<br />
A al tipo C.<br />
IMMAGINI:<br />
TIPO A: qui vedete delle cellule fusate organizzate in fasci distribuite facendo dei disegni quasi<br />
geometrici; le atipie sono lievi o insignificanti. A volte le cellule fanno delle immagini tipo rosette<br />
con cellule che si distribuiscono tutte alla periferia con un centro vuoto, oppure formano delle cisti;<br />
in ogni caso queste cellule sono citocheratina positive però hanno una caratteristica che le<br />
distingue dalle altre cellule epiteliali e cioè sono anche CD5 positive che è una caratteristica dei<br />
linfociti.<br />
TIPO AB: qui c’è una separazione tra un’area prevalentemente linfoide e un’area prevalentemente<br />
epiteliale; le aree B hanno linfociti prevalentemente immaturi.<br />
TIPO B1: vedete che qui è molto ricco di linfociti e in mezzo ai linfociti troviamo delle cellule<br />
epiteliali che hanno un citoplasma più rosa. Caratteristica di questo tipo di timoma è il fatto che i<br />
linfociti che si trovano vicino alle cellule epiteliali, non esprimono la TDT e quindi sono linfociti più<br />
maturi. I linfociti che invece stanno nelle aree povere di cellule epiteliali, lo esprimono. Questa è<br />
una conferma di quello che succede nella normalità, cioè che le cellule epiteliali sono delle cellule<br />
nutrici che determinano la maturazione dei linfociti.<br />
scaricato da www.sunhope.it
TIPO B2: spesso presenta architettura alveolare; presenta cellule epiteliali e cellule linfoidi; sia le<br />
cellule epiteliali che le cellule linfoidi presentano qualche atipia in più, ma sono sempre delle atipie<br />
moderate.<br />
TIPO B3: sono quasi tutte cellule epiteliali con atipie non molto spiccate.<br />
TIPO C: se lo vedessimo in qualche altro organo diremmo che si tratta di un carcinoma squamoso o<br />
addirittura un carcinoma linfoepiteliale .. poi vedremo cosa si intende per carcinoma linfoepiteliale<br />
(particolari tumori che vengono, ad esempio nel faringe, dove c’è una particolare commistione tra<br />
cellule epiteliali e linfociti.. ma queste cellule epiteliali mantengono sempre l’espressione del CD5).<br />
Molto importante è definire se il tumore è invasivo o meno rispetto alla capsula; questo,<br />
naturalmente, non riguarda il tipo A o il tipo AB che abbiamo visto essere benigni. Qui possamo<br />
vedere, ad esempio, questa è la capsula e qui vedete dei gettoni che sono andati oltre la capsula.<br />
Questo va riportato soprattutto nella stadiazione. La stadiazione è molto semplice: 1) stadio 1: il<br />
tumore è capsulato, non invasivo. 2) invasione transcapsulare che coinvolge il tessuto adiposo<br />
peritimico e può anche essere aderente ad organi, come pericardio, purchè non ci sia invasione ..<br />
cioè quest’aderenza non è legata a fatti infiammatori, ma a fatti reattivi .. quindi il timoma si<br />
ingrandisce, finisce per aderire col pericardio o altre membrane mediastiniche e quindi si creano<br />
delle aderenze ma non di tipo tumorale. 3) Invasione macroscopica, quindi ben evidente, degli<br />
organi adiacenti (pericardio, polmone, vasi). 4) disseminazione pleurica o pericardica e/o<br />
metastasi.<br />
Quindi, ai fini prognostici, abbiamo visto che è importante l’istotipo, l’attività mitotica: 10 figure<br />
mitotiche x 10 campi .. se l’attività mitotica è superiore a questa media la prognosi va verso il 21%;<br />
se è inferiore a questa media, superiamo l’80% di aspettativa.<br />
ALTRE NEOPLASIE DEL TIMO:<br />
Sono: carcinomi neuroendocrini; esiste anche la possibilità di microcitomi che in effetti<br />
appartengono pure alla serie neuroendocrina ( sono carcinomi neuroendocrini a piccole cellule );<br />
tumori a cellule germinali (oltre che nel mediastino, di cui non parleremo, li possiamo trovare<br />
anche nel timo) ; tumori mesenchimali tra cui tumori del tessuto adiposo, del tessuto vascolare<br />
ecc. ; linfoma di Hodgkin e coinvolge il timo soprattutto la sclerosi nodulare; tra i linfomi non<br />
Hodgkin abbiamo il linfoma mediastinico a grandi cellule B, il linfoma linfoblastico a cellule T che<br />
corrisponde a quello che chiamiamo linfoma a cellule convolute che è un linfoma dell’infazia detto<br />
anche linfoma-leucemia perché si associa spesso a leucemia e poi abbiamo il linfoma tipo MALT.<br />
APPARATO DIGERENTE:<br />
STOMACO: distinguiamo 3 o 4 regioni a seconda dei gusti. Abbiamo una regione cardiale, una<br />
regione antrale-pilorica e una regione centrale (corpo e fondo). Lo stomaco ha la caratteristica di<br />
presentare un’istologia differenziata a seconda della topografia. Nella regione cardiale vedremo<br />
una mucosa più ridotta e una mucosa fatta da epitelio cilindrico, da tessuto ghiandolare<br />
prevalentemente mucoide, mentre a livello del piloro avremo una mucosa prevalentemente<br />
scaricato da www.sunhope.it
ghiandolare e poi vedete qui una muscolaris mucosae. Cardias e piloro non si differenziano molto<br />
se non per il fatto che il piloro è un po’ più spesso. Dal punto di vista generale distinguiamo anche<br />
delle foveole che sono queste insenature, strutture ghiandolari, la cui funzione è quella di produrre<br />
soprattutto muco. Nella regione fondo-corpo vi sono le ghiandole gastriche propiamente dette; qui<br />
vi sono delle cellule più acidofile eosinofile alternate a cellule più basofile. Le cellule più acidofile<br />
sono le cellule parietali, mentre le cellule più basofile sono le cellule principali. Ovviamente nelle<br />
regioni superficiali ci sono sempre le ghiandole mucoidi che sono le stesse; sono le ghiandole sul<br />
fondo che sono diverse. Le cellule parietali sono quelle deputate alla secrezione di acido cloridrico<br />
e del fattore intrinseco. Le cellule principali secernono pepsina, lipasi e altre cose. Nello stomaco<br />
abbiamo una serie di cellule neuroendocrine altamente specializzate. Ci sono le cellule<br />
neuroendocrine D che producono somatostatina con effetto inibitore sulla secrezione acida; ci<br />
sono le cellule G che producono gastrina che stimola la produzione di acido e poi ci sono altre<br />
cellule neuroendocrine che producono grelina, istamina, serotonina.. la grelina è legata al senso<br />
dell’appetito. La produzione di HCl avviene attraverso una pompa protonica e attraverso uno<br />
scambio ioni potassio- ioni idrogeno. Le cellule della superficie producono invece bicarbonato,<br />
muco .. il bicarbonato rientra tra le soluzioni tampone. Nella secrezione acida è implicata la<br />
gastrina, l’acetilcolina prodotta dalle terminazioni nervose di tipo parasimpatico e i meccanismi<br />
paracrini come l’istamina prodotta dai mastociti e da altre cellule che ci sono nello stomaco.<br />
ERNIA IATALE: l’ernia iatale provoca dei grande dolore e può anche provocare delle sindromi<br />
cardiache per una sorta di riflesso gastro-cardiaco. E’ un’erniazione di mucosa gastrica attraverso il<br />
foro diaframmatico e ce ne sono di 2 tipi: 1) DA SCIVOLAMENTO in cui vediamo una porzione di<br />
cardias che supera il diaframma; 2) DA ROTOLAMENTO in cui il meccanismo è diverso, in gerene<br />
all’inizio è piccola ma è quella che da più fastidio. Queste ernie possono essere mobili, nel senso<br />
che uno si va a fare una radiografia e può pure non uscire niente, si formano in determinate<br />
posizioni e possono dar luogo a dei sintomi anche acuti. Complicanze: possono determinare un<br />
reflusso gastro-esofageo poiché il diaframma non partecipa più, come in condizioni normali, alla<br />
complessa dinamica muscolare che blocca il reflusso gastro-esofageo, lo sfintere esofageo<br />
inferiore. Un’altra condizione che mi è capitato vedere.. che si forma soprattutto sulla parete<br />
esterna dello stomaco.. voi sapete che il pancreas con la testa è un po’ attaccato alla parete dello<br />
stomaco … per cui mi è capitato di vedere la presenza di eterotopie pancreatiche, proprio per un<br />
problema embriologico; queste eterotopie, molto spesso, vengono scambiate per tumori e<br />
possono essere costituite dalla porzione esocrina o, come accade il più delle volte, il pancreas è<br />
completo., con porzione esocrina e le insule della porzione endocrina. Immagini: questo pancreas<br />
etero topico che vediamo nella porzione muscolare, molto spesso, può determinare anche delle<br />
emorragie perché gli enzimi pancreatici hanno un effetto litico e se si liberano possono dare delle<br />
reazioni anche gravi. Fortunatamente, questo si verifica raramente.<br />
MALATTIA DI MENETRIER: vado rapidamente … perché poi ci soffermeremo più sulle gastriti che<br />
ormai sono quasi un’epidemia. E’ una malattia su base genetica. IMMAGINE: questa è la superficie<br />
dello stomaco che normalmente è liscia e riconosciamo solo delle pliche. Qui vedete che le pliche<br />
sono molto grossolane … addirittura c’ha un aspetto tipo cavolfiore. C’è un’iperplasia delle foveole<br />
e delle ghiandole. Stranamente questa ipertrofia riguarda soprattutto le ghiandole mucose e si<br />
scaricato da www.sunhope.it
ealizza un aumento di secrezione mucoide con un’ipocloridria e l’aspetto macroscopico è quasi<br />
cerebriforme.<br />
SINDROME DI ZOLLINGER ELLISON: coinvolge il sistema neuroendocrino non coinvolgendo solo lo<br />
stomaco, ma molti organi. C’è un’iperplasia secretoria delle ghiandole del fondo; soprattutto sono<br />
implicate le cellule parietali con un’ipergastrinemia: spesso rientra in sindromi neuroendocrine<br />
dove sono presenti vari tumori.<br />
HELICOBACTER PYLORI: l’helicobacter pylori è una delle cose più interessanti che sono successe in<br />
medicina negli ultimi decenni. Per molto tempo, noi anatomopatologi abbiamo pensato che lo<br />
stomaco fosse invulnerabile ai batteri in condizione di normalità proprio per il pH così acido.<br />
Quando fu scoperto questo Helicobacter, all’inizio ci fu una sorta di scetticismo che poi si tramutò<br />
in un ottimismo esagerato e questo Helicobacter fu implicato in quasi tutto e ci furono molti studi<br />
che ora necessiterebbero di una smentita che penso non arriverà mai: trovarono l’Helicobacter<br />
perfino nell’aterosclerosi, nei trombi, negli emboli e così via. Poi alla fine c’è stato un terzo tempo,<br />
il tempo della sintesi, in cui si sono stabiliti i veri rapporti di questo Helicobacter con le varie<br />
patologie. Fu identificato da Warner e Marshall nel 1983, ma ci fu un certo scetticismo all’inizio<br />
anche tra gli anatomopatologi perché c’era questo dogma che dove c’è l’acidità, non ci possono<br />
stare batteri; ammettevamo la presenza di batteri solo in condizioni di acloridria o ipocloridria.<br />
Questo Helicobacter è in grado di bucare la parete dello stomaco e dare dei danni gravi … anche se<br />
normalmente si tratta di un germe con scarse capacità di penetrazione.. guardate com’è strano …<br />
visto che è un germe che, in genere, non troviamo mai in profondità. Questo germe, anche se non<br />
penetra molto, da fastidio lo stesso perché produce tutta una serie di sostanze: produce delle<br />
ADESINE che gli consentono di aderire alla superficie gastrica e agli interstizi.; produce l’UREASI che<br />
determina la produzione di ammoniaca che va a neutralizzare l’acidità e che quindi permette al<br />
batterio di sopravvivere all’acidità gastrica. Prima c’era un’immagine che ho dimenticato di<br />
commentare: alla fine dell’ ‘800, un anatomopatologo di nome Bizzozero di Varese identificò<br />
questo batterio, però né lui, né gli altri gli diedero importanza proprio per questo dogma<br />
dell’acidità … e tutti pensavano che la presenza di questo batterio fosse dovuta ad inquinamento;<br />
produce poi delle proteasi e produce poi tutta una serie di sostanze dai nomi strani come Gag A,<br />
Vac A, Bab A che sono delle proteine che possono indurre attivazione di vari oncogeni. Questo<br />
batterio determina inoltre un’infiammazione cronica che determina arrivo di linfociti e granulociti<br />
perché questo germe determina soprattutto una risposta granulocitaria quindi chemochine, vari<br />
mediatori chimici, interleuchine, TNF, prostaglandine .. per cui determina un cambiamento del<br />
clima e dell’ambiente gastrico.<br />
ULCERA GASTRICA: praticamente è quasi scomparsa. Voi non lo sapete, ma una volta moltissime<br />
persone si operavano di ulcera gastrica. Praticamente, poi la si diagnosticava quasi a tutti anche se<br />
non ce l’avevano … un’ulceretta non la si negava a nessuno. L’indagine era la radiografia e una<br />
zona che si riempiva di pasto opaco veniva considerata ulcera … ma molto spesso si trattava di<br />
contrazioni. Questo me lo ricordo perché all’inizio della mia carriera, io vedevo tutta una serie di<br />
stomaci .. adesso è cambiato tutto.. lo stomaco si toglie per i pazienti obesi con un intervento che<br />
passa la mutua.. si divide lo stomaco a metà proprio per ridurre la superficie gastrica. La metà dello<br />
scaricato da www.sunhope.it
stomaco tolta va dall’anatomopatologo per <strong>complete</strong>zza e a volte abbiamo trovato delle sorprese.<br />
Abbiamo trovato dei carcinomi incidentali. Ritornando all’ulcera, sappiamo che l’ulcera gastrica e<br />
quella duodenale hanno maggiore incidenza sulla piccola curva e sul duodeno.. l’ulcera peptica per<br />
così dire. La patogenesi di quest’ulcera è molto legata all’Helicobacter e all’aumentata sensibilità<br />
della mucosa all’acidità … è legata ad una necrosi progressiva che colpisce la parete e a volte si<br />
poteva verificare una perforazione dello stomaco che sfociava in una peritonite molto grave.<br />
All’inizio della mia carriera, per trovare bene l’ulcera, c’avevo un pannello di legno su cui mi<br />
stendevo la parete dello stomaco con delle punesse e guardavo bene il pezzo così da misurare<br />
bene le dimensioni dell’ulcera, la profondità; a volte, proprio perché si diagnosticava l’ulcera a<br />
tutti, perdevo delle ore su uno stomaco che l’ulcera non l’aveva…. Una volta passò il direttore; il<br />
prof. Mario Raso, che guardandomi su uno di questi pezzi mi disse: “ma non perdere tempo,<br />
questo non ce l’ha l’ulcera”. A volte era un vero problema perché dovevamo scrivere che in realtà,<br />
uno che era stato operato di ulcera, l’ulcera non ce l’aveva … allora ovviavamo mettendo ad<br />
esempio gastrite erosiva ecc.. Tutto questo si creava proprio per questa falsa immagine radiologica.<br />
L’ulcera gastrica presenta tutta una serie di caratteristiche particolari: si realizza una convergenza<br />
delle pliche gastriche che si dispongono radialmente intorno all’ulcera; abbiamo poi una sorta di<br />
retrazione, una contrattura dello stomaco reattiva rispetto alla patogenesi. Nell’ulcera attiva<br />
riconosciamo un fondo fatto di materiale necrotico, un essudato fibrinoso o purulento. Nell’ulcera<br />
cronica i margini sono dei margini molto netti, tipo a scodella. Queste sono immagini che oggi si<br />
verificano raramente poiché questa patologia si giova molto dell’eradicazione dell’ Helicobacter e<br />
dei farmaci che intervengono nella regolazione dell’acidità. Queste ulcere, quindi, tendono molto<br />
facilmente, oggi, alla cicatrizzazione. IMMAGINI: questo è l’aspetto istologico di un’ulcera cronica e<br />
potete vedere che vi è una perdita di sostanza, c’è una reazione fibrosa che coinvolge anche gli<br />
strati muscolari e c’è come un accorrere del tessuto muscolare e del tessuto fibroso ad arginare<br />
questa acidità. Nell’ulcera attiva distinguiamo,partendo dall’esterno verso l’interno, un essudato<br />
fibrino-purulento con necrosi fibrinoide , poi tessuto di granulazione in cui vediamo elementi<br />
infiammatori con qualche fibroblasto, poi un tessuto fibroso e poi, quando l’ulcera arriva alla<br />
sierosa, riconosciamo anche una fibrosi della sierosa. Anche i linfonodi regionali partecipano a<br />
questo processo per cui si possono ingrossare perché gli arrivano detriti, materiale necrotico per<br />
cui si viene a determinare una linfadenopatia. La cicatrizzazione può avvenire dopo alcune<br />
settimane grazie all’utilizzo degli H2 bloccanti. Inizialmente si riteneva che ci fosse un rapporto tra<br />
ulcera e cancro e si faceva un grosso errore. Questo accadeva perché si prendevano per ulcere dei<br />
cancri ulcerati. Oggi si sa che per dire che un cancro proviene da un’ulcera bisogna rispondere a<br />
tutta una serie di requisiti percui diventa minimale questa incidenza. Bisognerebbe fare una<br />
biopsia su tutti i margini per vedere se il cancro si forma dall’ulcera o si tratta di un cancro ulcerato.<br />
L’unica cosa che c’è da dire è che nei gastroresecati, il rischio di neoplasia è maggiore.<br />
GASTRITI CRONICHE: io vi parlerò soprattutto di 3 gastriti croniche. La classificazione seguita è<br />
quella di Dixon: gastrite tipo A, tipo B, tipo C. In A,B,C si identificano oltre il 95% delle gastriti<br />
croniche; la restante parte si identifica in delle gastriti minori che poi vi accennerò. LA GASTRITE A:<br />
incide poco ed è quella che si associa spesso ad anemia perniciosa. Si tratta di una gastrite<br />
autoimmune (anticorpi anti cellule parietali) e si localizza soprattutto nel fondo gastrico. La<br />
mancanza del fattore intrinseco produce carenza di vitamina B12 e si determinano queste anemie<br />
scaricato da www.sunhope.it
perniciose o magaloblastiche. La sede principale della gastrite di tipo A è il corpo ed il fondo.<br />
L’evoluzione è rappresentata dall’atrofia gastrica; dove si determina questa aplasia è facile<br />
osservare aree di metaplasia intestinale. Guardate com’è interessante questa cosa; se le cellule<br />
staminali che stanno nello stomaco vedono che non c’è acido, si mettono a fare la mucosa<br />
intestinale. La metaplasia la riconosciamo per la presenza delle globet cell che sono cellule<br />
caliciformi che sono chiare perché sono piene di muco e questo muco si scioglie con i comuni<br />
processi di fissazione. Nelle zone in cui sono rimaste le ghiandole gastriche, non sono le ghiandole<br />
gastriche tipiche del fondo corpo, ma sono ghiandole gastriche più tipo piloro; per questo poi si va<br />
in contro ad una sorta di atrofia. Scompaiono quindi le ghiandole gastriche che hanno le cellule<br />
parietali e le cellule principali. IMMAGINE: qui vediamo un residuo di ghiandola con dei linfociti e<br />
qui si vede proprio bene perché questa parte di ghiandola è rimasta ancora, mentre qui no. Proprio<br />
la presenza di questi aspetti morfologici che si chiamano complessi linfoepiteliali, cioè vediamo<br />
cellule linfocitarie che erodono le ghiandole gastriche, è la spiegazione della patogenesi. LA<br />
GASTRITE C: questa incide molto. E’ coinvolta anche nei disordini alimentari, stress e così via. Si<br />
viene a creare un reflusso del succo biliare pancreatico dal duodeno nello stomaco. Voi sapete che<br />
queste sostanze che refluiscono sono basiche ed il piloro è abituato a sostanze acide, non basiche.<br />
Si determina quindi questa gastrite da reflusso e la sede principale è il piloro.. difficilmente arriva<br />
oltre perché riguarda proprio quel tratto di mucosa gastrica interessata dal reflusso. Alcuni<br />
chiamano la gastrite C anche gastrite chimica … ma tecnicamente non è proprio una gastrite<br />
perché elementi infiammatori ne vediamo pochissimi perché essendo una gastrite legata al<br />
reflusso, la mucosa cerca di reagire a questo evento patologico. Reagisce con un ispessimento della<br />
mucosa, le foveole si allungano quasi come un tentativo di difesa da questo succo alcalino; i vasi<br />
che vedete qui si congestionano e poi abbiamo una caratteristica peculiare di questa gastrite, che<br />
non si verifica in altre e cioè la muscolaris mucosae che in genere rappresenta il confine tra<br />
mucosa e sottomucosa, si arborizza all’interno della mucosa; percui trovare delle fibrocellule nella<br />
mucosa (confermandolo ad esempio con un marcatore delle fibrocellule muscolari come l’actina),<br />
insieme all’iperplasia e all’ispessimento con anche edema della mucosa, è un segno della gastrite<br />
cosiddetta chimica da reflusso. LA GASTRITE B: tende ad essere multifocale partendo dal piloro ma<br />
tendendo ad estendersi alla piccola curva e anche verso la regione del fondo. E’ la gastrite che per<br />
eccellenza è legata all’ Helicobacter Pylori. Dai dati possiamo desumere l’importanza di questo<br />
germe: è presente 20-40% della popolazione.. questa è l’incidenza globale, ma ci sono molte<br />
differenze geografiche; è implicato nel 90% delle gastriti croniche, nel 60% delle ulcere gastriche,<br />
nel 95% delle ulcere duodenali e, attraverso meccanismi di cui poi parleremo, è implicato nel 50%<br />
dei carcinomi gastrici e nei linfomi gastrici. La prima sede di localizzazione del germe è<br />
probabilmente il piloro; poi però tende a diventare multicentrico e questo è il motivo per cui<br />
l’endoscopista fa biopsie al piloro, al fondo, al corpo in modo da avere un quadro completo della<br />
colonizzazione. C’è un lavoro su Nature 2010 in cui si parla del fatto che, con la scoperta<br />
dell’America, abbiamo importato oltre alle patate ecc anche un ceppo di Helicobacter più forte<br />
(però già avevamo i nostri ceppi). L’aspetto più caratteristico dell’helicobacter è l’infiltrato<br />
granulocitario. Immagine: qui vedete la distruzione della mucosa gastrica ad opera dei granulociti<br />
evocati dal’ Helicobacter. C’è un parallelismo tra numero di Helicobacter (si chiama colonizzazione)<br />
e numero di granulociti. Con la colorazione GIEMSA l’HP si vede meglio. In linea di massima rimane<br />
scaricato da www.sunhope.it
in superficie o al massimo se ne va nell’interstizio. Meglio ancora lo vediamo se facciamo<br />
l’immunoistochimica usando anticorpi anti HP. Nelle forme iniziali o se c’è una bassa virulenza del<br />
germe, la gastrite riguarda gli strati più superficiali, riguardando la metà della mucosa. Nelle forme<br />
più aggressive la mucosa è interessata in tutto il suo spessore. Possiamo ritrovare pure dei follicoli<br />
linfatici. La forma profonda si chiama anche forma atrofica, anche se non c’è atrofia; questo perché<br />
sappiamo che quando questa infiammazione coinvolge l’intera mucosa, l’esito è l’atrofia. Qui<br />
vediamo che alla fine si vengono a determinare ampie aree di mucosa gastrica vuote e qui vedete<br />
anche la metaplasia intestinale, perché laddove c’è un’atrofia si sviluppa una metaplasia intestinale<br />
per i motivi che vi ho detto prima. C’è un grading: atrofia lieve, moderata, severa. Preciseremo poi<br />
se si tratta di una gastrite B superficiale o profonda perché hanno un’evoluzione diversa. Alla fine<br />
ne uscirà una specie di protocollo che sarà utile all’endoscopista: preciseremo innanzitutto se<br />
questa patologia riguarda solo in piloro o si estende e quali sono le differenze tra le varie zone; poi<br />
diremo che tipo di flogosi c’è .. naturalmente, quello che è importante è la presenza dei granulociti<br />
in quanto sono correlati al grado di attività. Addirittura i pazienti che fanno terapia possono essere<br />
sottoposti a biopsia per valutare il grado di successo o meno della terapia .. percui parleremo di<br />
gastrite attiva in fase di lieve attività (con pochi granulociti) o moderata attività o severa attività.<br />
Diremo inoltre se si tratta di una gastrite superficiale o profonda (la profonda può anche essere<br />
definita atrofica .. profonda e atrofica sono quasi sinonimi). Secondo dei protocolli che sono<br />
internazionali, vanno indicati anche i gradi di colonizzazione .. cioè la carica batterica .. se è lieve,<br />
moderata o intensa a seconda del numero di questi HP. Infine, poi , preciseremo se c’è metaplasia<br />
e che tipo di metaplasia c’è oppure se c’è displasia .. in quanto nello stomaco c’è la possibilità di<br />
trovare displasia, come abbiamo visto in altri organi, che è una lesione precancerosa. Quando,<br />
quindi, facciamo una diagnosi di gastrite cronica di tipo B, dobbiamo tenere tutta una serie di<br />
elementi da comunicare per ogni regione dello stomaco che noi esaminiamo.<br />
ALTRE FORME DI GASTRITE: ne facciamo una rapida carrellata perché si tratta di gastriti minori.<br />
Abbiamo la gastrite linfocitica che spesso troviamo associata a celiachia. Voi sapete che la celiachia<br />
colpisce il duodeno ed in genere l’intestino tenue, però può determinare anche una gastrite<br />
cronica, in questo caso linfocitaria al contrario della gastrite cronica di tipo B, ad esempio, che è<br />
sostenuta dai granulociti. Abbiamo, poi, una gastrite allergica su cui si discute molto ..<br />
caratterizzata soprattutto dalla presenza di eosinofili. C’è da dire che insieme a queste gastriti di cui<br />
vi ho parlato, si verifica, al giorno d’oggi, anche un notevole aumento delle intolleranze alimentari,<br />
un fenomeno che andrebbe studiato più a fondo, … intolleranze alimentari a prescindere dalla<br />
malattia celiaca che è conosciuta da tempo .. e sono intolleranze nuove che si possono sviluppare<br />
anche in età adulta e sono frequentissime; uno può anche non accorgersene perché c’è una<br />
irregolarità dell’alvo ma niente di più .. però poi possono dare anche delle patologie anche gravi.<br />
Abbiamo poi la gastrite eosinofila diffusa l’abbiamo quando gli eosinofili sono numerosissimi<br />
correlati ad una patologia allergica ed anche ad un’eosinofilia periferica. Abbiamo poi altre forme<br />
come quelle legate ai farmaci: alcuni esempi sono l’aspirina oppure altri FANS, gli steroidi, l’alcool.<br />
METAPLASIE IN CORSO DI GASTRITE: questo è un argomento che riguarda anche l’oncologia. Già<br />
abbiamo parlato della metaplasia intestinale; possiamo avere una 1)METAPLASIA PILORICA di cui<br />
già abbiamo accennato.. nel corso di una gastrite autoimmune in cui c’è una distruzione elettiva<br />
scaricato da www.sunhope.it
delle ghiandole gastriche propiamente dette, al posto di queste troviamo una metaplasia pilorica.<br />
Lo stomaco quindi perde le sue capacità più nobili come la secrezione di enzimi, di acidi e così via<br />
assumendo un aspetto del tutto assimilabile al piloro. La 2)METAPLASIA INTESTINALE, invece, è<br />
divisa in due forme, forse anche in tre o comunque in due di cui una si suddivide: abbiamo la<br />
METAPLASIA COMPLETA in cui quel tratto somiglia in tutto e per tutto all’intestino tenue<br />
(nell’intestino tenue abbiamo le cellule caliciformi, cuticolari, le cellule del Paneth, cellule<br />
neuroendocrine); il marcatore istologico di questa metaplasia sono le cellule del Paneth ovvero<br />
cellule ricche di granuli acidofili.. di lisozima soprattutto; trovare queste cellule vuol dire trovarsi di<br />
fronte ad una metaplasia completa. Quella completa è la più benigna perché riproduce<br />
esattamente un tratto intestinale. Maggior significato dal punto di vista oncologico ha la<br />
METAPLASIA INTESTINALE INCOMPLETA. Qui abbiamo assenza delle cellule del Paneth ed in questo<br />
caso la mucosa sembra assumete più le caratteristiche dell’intestino crasso (dove mancano le<br />
cellule del Paneth). Questa somiglianza col crasso può essere ancora più evidente se andiamo ad<br />
esaminare il tipo di mucine. Mentre nel tenue vengono prodotti mucopolisaccaridi debolmente<br />
acidi, nel crasso vengono prodotti dei mucopolisaccaridi molto acidi, le cosiddette sulfomucine. Se<br />
ritroviamo le sulfomucine, alcuni distinguono una metaplasia intestinale incompleta con<br />
mucopolisaccaridi neutri o debolmente acidi e metaplasia incompleta con mucopolisaccaridi<br />
solforati molto acidi. Non è un caso che quest’ultima, con sulfomicine e quindi quella che più si<br />
avvicina all’intestino crasso, è quella più frequentemente legata alla displasia.. ha quindi un ruolo<br />
nella progressione tumorale. Abbiamo poi una 3)METAPLASIA A CELLULE CILIATE che possiamo<br />
trovare in altre zone dello stomaco; questa metaplasia è ancora in corso di studio. Questa<br />
metaplasia ha un fenotipo di tipo antrale e la possiamo trovare nel corpo o nel fondo dello<br />
stomaco.<br />
IMMAGINI: ecco la metaplasia intestinale completa. Qui vedete cellule ricche di granulazioni<br />
acidofile.. sono le cellule del Paneth. Qui vediamo le cellule caliciformi e possiamo vedere un<br />
ispessimento della mucosa che corrisponde alle cuticole.. quindi alle cellule cuticolari. Un metodo<br />
per vedere i mucopolisaccaridi è l’ ALCIAN. Qui vedete una metaplasia intestinale incompleta: si<br />
capisce che è incompleta perché mancano le cellule del Paneth e poi perché la differenziazione in<br />
cellule cuticolari e cellule caliciformi è meno evidente… è come se ci fosse una irregolarità nel<br />
disegno dell’intestino.. e qua possiamo trovare associata pure la displasia; questa è la displasia<br />
lieve e questa è la displasia grave. Una displasia grave può anche essere trattata chirurgicamente.<br />
Qui vedete una metaplasia con associata una displasia.. vedete cellule caliciformi molto irregolari,<br />
molto polimorfe .. alcune con un piccolo vacuolo, altre con un vacuolo più grande .. e poi vedete<br />
una disorganizzazione con delle atipie dell’epitelio.<br />
SIGNIFICATO CLINICO DELLA DISPLASIA: nei tessuti adiacenti il carcinoma la troviamo fino al 100%<br />
dei casi. Se abbiamo il G1, ricordate ne discutemmo anche per la cervice, abbiamo possibilità di<br />
regressione molto elevate e le possibilità di progressione sono basse. Se abbiamo il G3 le<br />
possibilità di regressione sono bassissime, mentre la progressione verso il cancro si realizza nel 75%<br />
dei casi. Questo spiega perché la displasia grave (G3) è un indicatore patologia molto grave. (Il G2<br />
non lo nomina proprio, ma esiste).<br />
scaricato da www.sunhope.it
ATROFIA: la dividiamo in lieve, moderata e grave, con o senza metaplasia, con che tipo di<br />
metaplasia, con o senza displasia. Nelle atrofie si verifica anche un altro fenomeno probabilmente<br />
legato ad un tentativo di compensare questa situazione.. c’è un aumento delle cellule<br />
neuroendocrine; se andiamo a fare un metodo per le cromogranine vediamo aggregati di cellule<br />
neuroendocrine per compensare questa situazione di deficit.<br />
Questa tabella alla fine riassume un po’ quello che ci siamo detti fino ad ora: la multicentricità e<br />
l’atrofia sono dei fattori fondamentali per il cancro. Il rischio di sviluppare il cancro qual è? Se c’è a<br />
livello antrale un’atrofia severa che ritroviamo anche a livello del corpo, il rischio di sviluppare il<br />
cancro rispetto alla popolazione normale è 90 volte maggiore. Se invece abbiamo un’atrofia lieve a<br />
livello antrale e con una moderata a livello del corpo, il rischio è tre volte maggiore. Quindi le<br />
atrofie della mucosa antrale sono importanti.. un’atrofia severa dell’antro porta ad un rischio 18<br />
volte maggiore, ma mano a mano che troviamo anche nel corpo lesioni atrofiche o gastriti, questo<br />
rischio raddoppia o triplica. La multicentricità e il grado di atrofia sono correlati direttamente al<br />
rischio di sviluppare il cancro. Questo spiega perché anche l’HP rientra in tutta questa patogenesi ..<br />
più avanti poi entreremo più in dettaglio su questa cosa.<br />
scaricato da www.sunhope.it
CARCINOMA GASTRICO<br />
Possiamo identificare 2 strade della cancerogenesi. Dobbiamo tenere presente una<br />
nozione preliminare, per cui c’è una vecchia classificazione del carcinoma dello<br />
stomaco, tutt’ora attuale, che distingue 2 istotipi semplici: tipo intestinale e tipo<br />
diffuso e si chiama classificazione di Lauren; Lauren partiva da questo presupposto<br />
che poi si è rivelato errato: il carcinoma intestinale ha sempre una differenziazione<br />
tubulare, cioè delle strutture che ricordano le ghiandole, cioè dei tubuli e perché<br />
intestinale?Perché pensava che nascesse sempre dalla metaplasia intestinale e in<br />
effetti è un carcinoma più differenziato; invece, il carcinoma diffuso perde questa<br />
sua tendenza dell’architettura a formare ghiandole o tubuli e apparirà così a cellule<br />
diffuse, diffuse cioè nella sua architettura, cioè cellule atipiche che non tendono a<br />
formare nessuna struttura, quindi più indifferenziate. Questi 2 tipi di cancro hanno<br />
molto probabilmente una differente storia molecolare e patogenetica. Il carcinoma<br />
diffuso, infatti, ha una predisposizione genetica, per cui sono noti almeno 10-20% di<br />
errori genetici ( ricordate nella parte generale abbiamo parlato di geni<br />
oncosoppressori, etc.) e in questo consiste la sua predisposizione, potremmo anche<br />
parlare, quindi , di suscettibilità genetica originaria; il tipo intestinale, invece, è<br />
soprattutto frutto di mutazioni acquisite. Nel primo caso, quindi, L’Helicobacter, non<br />
è tanto implicato, mentre lo è nel secondo caso, vedete che sono descritte delle<br />
situazioni o lesioni o condizioni precancerose come la gastrite da H. Pylori, l’atrofia,<br />
la metaplasia intestinale, però di tipo incompleto, quindi Lauren qualcosa di vero<br />
l’aveva identificato, oppure la displasia che possiamo trovare anche negli adenomi,<br />
gli adenomi sono dei polipi neoplastici di cui parleremo, ma questa è una strada<br />
molto secondaria, mentre la cosa importante è la displasia in corso di gastrite<br />
atrofica e di metaplasia intestinale completa fino ad arrivare al cancro di tipo<br />
intestinale. Qua vedete come l’80-90% di mutazioni sono acquisite quasi tutte, poi<br />
vedremo come. Comunque considerare le sole mutazioni rappresentano un’idea<br />
statica della genomica ormai superata, perché dobbiamo considerare non solo la<br />
presenza o meno di geni alterati ma la loro espressività, o la capacità o meno di<br />
trasdurre i segnali e tutto il resto, per cui ne deriva un modello molto più<br />
complicato.<br />
Il cancro dello stomaco ha delle particolarità epidemiologiche molto interessanti: per<br />
esempio, nei paesi asiatici ed, in particolare, in Giappone è un cancro che ha una<br />
scaricato da www.sunhope.it
elevata incidenza molto più che in altri Paesi, 80/100000 casi all’anno, se la<br />
paragonate con l’incidenza europea di 10-20/100000, vi rendete conto che è<br />
maggiore oltre 4 volte l’incidenza in Giappone, ma in genere anche nei Paesi asiatici,<br />
in Cina, in Vietnam e così via c’è una maggiore incidenza; questo spiega anche il<br />
perché proprio il Giappone è stato pioniere della scuola endoscopica, le fibre ottiche<br />
sono nate lì e sono state applicate all’endoscopia, proprio perché lì avevano questo<br />
problema e, vista l’applicazione di queste tecniche moderne, anche da loro la<br />
mortalità di questo cancro si è molto abbassata. In Italia: in Emilia è molto alta<br />
l’incidenza ( c’è una certa tendenza a mangiar bene, soprattutto i salumi), bassa in<br />
Sicilia e in Sardegna, mentre in Campania vige una situazione medio-bassa.<br />
L’atrofia gastrica incide moltissimo, soprattutto quella correlata all’Helicobacter,<br />
anche qui, però, c’è, a volte, una predisposizione genetica, soprattutto nella forma<br />
diffusa, la gastroresezione, questo è un problema da tener presente; recenti dati ci<br />
dicono che i gastroresecati hanno un 3% di rischio di sviluppare un cancro gastrico<br />
entro i 20 anni, molto maggiore rispetto alla popolazione generale, ove abbiamo<br />
visto che è molto più basso. I fattori dietetici hanno notevole importanza, ma se<br />
andiamo a vedere degli alimenti non se ne salva nessuno; tra questi maggiore<br />
imputato è il caffè. Vi faccio alcuni esempi, vi indico le due sostanze più implicate<br />
nella cancerogenesi di questo tipo:<br />
1. Le micotossine, tossine prodotte dai miceti o funghi, che sembrano molto<br />
molto diffuse soprattutto in oriente e un particolare rilievo spetta<br />
all’aflatossina; queste tossine hanno un effetto cancerogeno sia sul fegato che<br />
sull’intero apparato gastrointestinale, questo ci spiega anche perché, sempre<br />
nei Paesi asiatici, c’è una elevata incidenza anche del cancro epatico non per<br />
cirrosi ( come da noi), ma cancro epatico che insorge su fegato sano, tant’è<br />
vero che in Vietnam si è sviluppata una tecnica chirurgica per il cancro epatico<br />
e le metastasi epatiche che si chiama “digitoplasia”che si è poi diffusa un po’<br />
dappertutto, che comporta la necessità di utilizzare le mani, con una pazienza<br />
“cinese”, evitando, quindi, sanguinamenti molto violenti che possono a loro<br />
volta portare ad 1 serie di complicanze;<br />
2. Le nitrosammine, molto presenti nel pesce affumicato.<br />
Fate quindi attenzione a queste cucine orientali, che oggi vanno molto di moda.<br />
scaricato da www.sunhope.it
Poi abbiamo le lesioni precancerose: la displasia, la metaplasia intestinale<br />
incompleta, gli adenomi, la malattia di Menetrière, di cui abbiamo già parlato, che<br />
pure trattasi di precancerosi, inoltre, polichemioterapia e radioterapia utilizzate per<br />
altre cause sembrano aumentare il rischio di carcinoma gastrico; l’azione del fumo è<br />
ancora incerta; per quanto riguarda i parametri molecolari, è utile dire che<br />
l’incubazione della p53, del k-ras, sono determinanti nel condizionare sia la<br />
cancerogenesi, sia la prognosi del cancro gastrico, poi ci sono altri fattori come la<br />
pcr2, l’APC e poi altri fattori correlati alle proteine di membrana come le caderine,<br />
ma questo lo vedremo più avanti. Ancora questo benedetto Helicobacter; ma queste<br />
sostanze come la Cag-A, la Vac, determinano dei fenomeni importantissimi,<br />
innanzitutto aumentano l’attività proliferativa e la motilità delle cellule, determinano<br />
una riorganizzazione del citoscheletro ( ricordate dalla parte generale che nella<br />
cellula normale il citoscheletro ha dei poli di ancoraggio, per cui non si può muovere<br />
la cellula, ma per potersi muovere deve modificare il proprio citoscheletro e questi<br />
ponti di β-catenine che sono appostate nell’ancoraggio della membrana basale, dello<br />
stroma e così via); poi c’è un’interferenza per quanto riguarda i fenomeni<br />
angiogenetici che inducono anche l’angiogenesi, un’interferenza con i fenomeni di<br />
apoptosi; quindi, capite bene, come questo Helicobacter sia in grado di determinare<br />
tutta una serie di effetti a catena disastrosi. Questo è un recente lavoro che parla<br />
proprio di questo fenomeno: normalmente queste cellule epiteliali esprimono la<br />
Caderina che è legata alle β-catenine che intervengono non solo nelle giunzioni<br />
cellula-cellula, ma anche cellula-stroma; ora, per effetto di queste sostanze prodotte<br />
da Helicobacter si determina un danneggiamento delle Caderine, una proteolisi<br />
mediata dall’Ubiquitina e, di conseguenza, una riespressione anomala di β-catenine<br />
alterata, che sono alla base della motilità di queste cellule, vedete quante cose si<br />
determinano per questo Helicobacter. Alcuni studi hanno dimostrato che questo<br />
germe ha anche una estrema capacità di diversificarsi, già ne parlammo a proposito<br />
dell’ontogenesi dell’Helicobacter dalle Americhe, all’Europa, all’India, alle regioni<br />
asiatiche e così via, per cui è dotato di una virulenza diversa a seconda dei ceppi; ora,<br />
addirittura, può fare sia delle ricombinazioni intra-genomiche, cioè all’interno del<br />
suo stesso genoma, o inter-genomiche, cioè con genoma di altri Helicobacter.<br />
Riepilogando, L’Helicobacter, a livello dello stomaco determina tutta una serie di<br />
problemi seri:<br />
- In caso che non venga alterata la produzione di acido e si mantenga in<br />
qualche modo un’acidità nello stomaco, possiamo andare incontro ad una<br />
scaricato da www.sunhope.it
gastrite cronica predominante antrale che non si estende al fondo; è un<br />
buon segno, in questo caso possiamo avere l’ulcera duodenale o gastrica,<br />
oppure possiamo avere delle gastriti non atrofiche e possiamo avere anche<br />
un linfoma, il linfoma MALT, tant’è vero che l’eradicazione di H.Pylori è<br />
sufficiente per rimuovere il linfoma;<br />
- In caso di bassa produzione acida, noi avremo la metaplasia intestinale, la<br />
displasia, il cancro.Quest’Helicobacter interviene nel 75% dei casi, per la<br />
maggior parte di tipo intestinale mentre ha una minore incidenza nel<br />
cancro diffuso.<br />
Questo mi sembra di avervelo già mostrato, ma è molto interessante,<br />
perché riguarda le cellule staminali, è un lavoro recente in cui hanno<br />
analizzato le cellule staminali proprio dello stomaco; cosa succede? Questo<br />
Helicobacter, non direttamente, ma attraverso tutte queste tossine, non<br />
solo distrugge, ma determina anche questa gastrite che determina l’atrofia<br />
e quest’atrofia non salva neppure le cellule staminali per cui questa<br />
distruzione delle cellule staminali è quella direttamente più responsabile<br />
del cancro perché quando si distruggono le cellule staminali, queste, prima<br />
di morire, lanciano dei segnali di allarme ( chemochine di vario tipo,<br />
sostanze pro-infiammatorie ) e richiamano dal midollo osseo le cellule<br />
staminali totipotenti, queste accorrono, ma trovano un microambiente<br />
alterato, ricordate -parlammo di nicchia che io rappresentai con una bara-<br />
trovano una nicchia alterata, c’è una stimolazione aberrante del<br />
microambiente che è causa di diverse mutazioni nelle cellule, siamo arrivati<br />
a una certa comprensione della cancerogenesi nello stomaco.<br />
Come dice un detto napoletano “Vai a cercare aiuto e trovi sgarrupo”,<br />
queste cellule staminali fanno più danni che bene!<br />
Questi sono i dati dell’American Cancer Society del 2010, che in realtà sono<br />
dati retroattivi che risalgono al 2006-2008: il cancro dello stomaco si situa,<br />
tra i cancri digestivi, al terzo posto in termini di incidenza, c’è una maggiore<br />
incidenza nei maschi piuttosto che nelle femmine e la mortalità non è alta,<br />
ma si è ridotta notevolmente. Questa altra immagine analizza la situazione<br />
1990-2006: in questi 15 anni si è avuto un decremento, infatti del 43%,<br />
dato certamente ragguardevole.<br />
scaricato da www.sunhope.it
Per quanto riguarda la situazione in Italia, c’è una associazione che<br />
raggruppa questi tumori in specifici registri: si nota sempre una maggiore<br />
incidenza nei maschi e questi dati si riferiscono al rischio cumulativo, cioè<br />
ogni quante persone qualcuno rischia di ammalarsi di cancro allo stomaco?<br />
Per i maschi questo rischio è di un soggetto ogni 26 persone, la mortalità è<br />
di una persona ogni 38, nelle donne , invece, questo rischio è molto<br />
minore, uno su 53 e così anche la mortalità, uno su 81.<br />
Un altro concetto fondamentale che cambia completamente le prospettive<br />
terapeutiche è il confine tra l’early gastric cancer e il carcinoma gastrico<br />
avanzato, questa è una scoperta che dobbiamo alla scuola giapponese, che<br />
sviluppando molto l’endoscopia riuscì per prima ad identificare in fasi<br />
precoci anche macroscopicamente il cancro. Quand’è che possiamo<br />
definire un cancro gastrico early gastric cancer? C’è un confine che non è la<br />
muscolaris mucosae, ma la tonaca muscolare, quindi l’early gastric cancer<br />
può essere un cancro intramucosale, quando non supera la muscolaris<br />
mucosae o sottomucosale quando la supera e arriva alla sottomucosa, ma<br />
è sempre early gastric cancer; la prognosi di questi early gastric cancer è<br />
drammaticamente diversa dai carcinomi gastrici avanzati; il carcinoma<br />
gastrico avanzato, invece, infiltra la tonaca muscolare e arriva fino agli strati<br />
esterni o addirittura va fuori dalla parete dello stomaco; ricordate, quindi,<br />
che il confine è la tonaca muscolare, se questa è indenne possiamo parlare<br />
di early gastric cancer; ora questa è una diagnosi esclusivamente anatomopatologica,<br />
l’endoscopista può avere un impressione alla vista, ma<br />
comunque, a volte vi sono cancri piccoli ma molto invasivi, inducono<br />
all’ottimismo l’endoscopista e invece all’esame anatomo-patologico<br />
risultano molto più profondi! Addirittura la scuola giapponese fece una<br />
classificazione che è tutt’ora in validità, per cui si distingue anche<br />
macroscopicamente l’early gastric cancer dal carcinoma gastrico avanzato,<br />
cioè come si presenta poi all’endoscopista e come si presenta all’anatomo<br />
patologo. L’early gastric cancer è un cancro allo stadio iniziale che può<br />
essere di tipo 1, appena appena rilevato, il tipo2 piatto e il tipo3 escavato,<br />
che è quello con prognosi peggiore perché tende a “sfogare” ala sua<br />
aggressività verso il basso; c’è poi chi distingue il tipo2 in 2a, 2b, 2c, 2a è<br />
appena un po’ elevato, 2b è piatto piatto, 2c appena un po’ depresso, ma i<br />
tipi principali sono 1, 2, 3. Il tipo1 è appena appena sporgente, vedete,<br />
scaricato da www.sunhope.it
mentre il tipo2c ha una leggera depressione e qui vedete l’aspetto<br />
istologico, c’ha dei bordi e una leggera depressione, ovviamente ci vuole<br />
una certa esperienza per scorgere questi aspetti macroscopici del cancro<br />
gastrico, il tipo 3 , invece, sembra una piccola ulcera, non è vero quel<br />
concetto che nell’ulcera c’è la convergenza delle pliche, mentre nel cancro<br />
no, si è visto che questo concetto non è valido, tant’è vero che qua vedete<br />
la convergenza delle pliche gastriche e qua vedete un cancro che sembra<br />
una piccola ulcera; questo, invece, è un cancro gastrico intramucosale,<br />
vedete qui la muscolaris mucosae che non viene superata; il carcinoma<br />
gastrico, invece, avanzato, presenta, ovviamente degli aspetti macroscopici<br />
più eclatanti, soprattutto quando ha un aspetto ulceroso, si tratta di<br />
un’ulcera molto sanguinante, dai margini molto irregolari, a differenza<br />
dell’ulcera gastrica propriamente detta che ha margini ben definiti; c’è<br />
anche la forma polipoide, per cui, vedete, sembrerebbe un polipo, queste<br />
sono dei tagli trasversali, poi la forma vegetante e poi c’è la forma più<br />
subdola che viene chiamata, secondo il termine antico, “linite plastica” per<br />
descrivere questo tipo di carcinoma gastrico che ha questa tendenza: non<br />
abbiamo degli aspetti esuberanti dal punto di vista macroscopico, né<br />
vegetanti, né ulceranti, ma questo cancro tende a diffondersi nella<br />
sottomucosa e nella tonaca muscolare in maniera subdola, a cellule sparse,<br />
per cui si determina una reazione stromale e non abbiamo delle grosse<br />
manifestazioni esterne per le quali l’endoscopista non nota granchè, tranne<br />
qualche ispessimento della parete, l’unica cosa che ne residua è una<br />
rigidità della parete; questo tipo di cancro, pur avendo poche<br />
manifestazioni esteriori, è quel cancro che infiltra la parete a tutto spessore<br />
ed è quel tipo di cancro che da questo “sgocciolamento” per cui può<br />
coinvolgere anche l’ovaio e da luogo a quel che si chiama tumore di<br />
Krukenberg; per cui può capitare di fare l’endoscopia, non trovare nulla di<br />
eclatante e si può cadere nell’errore di ritenere questo cancro ovarico<br />
primitivo.<br />
Questa è la classificazione di Lauren, ancora valida; Il WHO ha complicato<br />
un po’ la situazione, però distingue:<br />
-il papillare;<br />
-il tubulare;<br />
scaricato da www.sunhope.it
-il mucoide;<br />
-il carcinoma a cellule con castone, di cui già abbiamo parlato, vuol dire con<br />
castone che accumulano muco,non riescono a secernerlo all’esterno, per<br />
cui il nucleo viene spinto alla periferia e sembra quasi una pietra che sta<br />
sull’anello;<br />
-il carcinoma poco differenziato (o diffuso);<br />
-altre varietà, ma non ve ne parlo.<br />
Questo è l’adeno-carcinoma gastrico, qua vediamo una mucosa iperplastica<br />
e qua vediamo l’adenocarcinoma; questo è l’adenocarcinoma diffuso, avete<br />
visto, in alcuni casi è difficile capire se è un carcinoma o un’altra patologia,<br />
perché si tratta di cellule atipiche, sparse, se facciamo, però, la<br />
citocheratina ci rendiamo conto che si tratta di carcinoma diffuso ( o<br />
indifferenziato); poi vedete che questi cancri indifferenziati hanno questa<br />
tendenza a infiltrare i tessuti a fila indiana, a cellule sparse, come in questa<br />
[IMMAGINE], qui siamo nella tonaca muscolare, bruttissimo segno, perché<br />
vuol dire che il cancro non infiltra più a macchie, come succede<br />
nell’adenocarcinoma, in cui vediamo delle lingue che hanno ancora un<br />
minimo di coesività, qua, invece, hanno perso coesività e se ne vanno per i<br />
fatti loro, in gita, diciamo, attraverso gli strati della parete, perciò dico che<br />
queste cellule hanno acquisito capacità litiche e una riorganizzazione del<br />
citoscheletro e, molto spesso, se vi ricordate la parte generale, hanno<br />
assunto delle caratteristiche fenotipiche quasi di tipo mesenchimale, per<br />
poter infiltrare meglio lo stroma. [IMMAGINE]Questo è il cancro più brutto<br />
dello stomaco, ancora più brutto dell’indifferenziato: voi vedete in questa<br />
mucosa gastrica queste cellule, vedete che sono vacuolizzate, e sopra le<br />
cellule vedete questo nucleo ridotto quasi alla lamina, sono le cellule ad<br />
anello con castone; a vederlo così la cantonata più grossa che si può avere<br />
è scambiarle per macrofagi, anche per il grasso che sembrano avere al loro<br />
interno, invece sono queste cellule ad anello con castone, la cui<br />
caratteristica principale è quella di essere molto invasive anche se con<br />
discrezione, visto che all’aspetto macroscopico, vedete, non mostra grandi<br />
alterazioni, forse appena appena un ispessimento, perché il cancro si<br />
diffonde a macchia d’olio coinvolgendo la tonaca muscolare, vedete tutti<br />
questi tralci che da e bucando la parete dell’ intestino è lui ( il cancro ) il<br />
scaricato da www.sunhope.it
principale responsabile del tumore di KruKenberg ; spesso questa forma<br />
può anche nelle biopsie, non essere colto dall’anatomopatologo, se si<br />
danno poche cellule, per capire se è un macrofago o una cellula epiteliale<br />
facciamo il CD78, che è dei macrofagi, o la citocheratina, che è delle cellule<br />
epiteliali.<br />
[IMMAGINE]Questo è, invece, il carcinoma mucoide che apparirà grandi<br />
laghi di muco nel cui contesto troviamo delle cellule così fatte, in questo<br />
caso si tratta ancora di cellule ad anello con castone, però conserva la<br />
capacità di secernere muco e lo secerne all’esterno, la cellula con castone<br />
invece ha perso questa capacità per cui il muco si accumula all’interno<br />
della cellula.<br />
Come facciamo la prognosi del carcinoma gastrico?<br />
Consideriamo:<br />
- Lo stadio;<br />
- L’istotipo, soprattutto il tipo indifferenziato, quello a cellule mucoide e ad<br />
anello con castone che hanno una prognosi peggiore perché già avanzati,<br />
anche se il quadro macroscopico o endoscopico può sembrare poco<br />
allarmante;<br />
- La sede, quelli del piloro hanno una prognosi migliore;<br />
- I margini di escissione, questi sono i caratteri plastici;<br />
- La reazione citostromale è un’altra caratteristica delle cellule ad anello con<br />
castone: la reazione citostromale di linfociti, linfoblasti è molto scarsa,<br />
questa cellula quindi si mimetizza, per cui non evoca una forte reazione da<br />
parte del tessuto ospite, quindi è molto subdola, se facesse politica<br />
avrebbe grandi probabilità di successo.<br />
Poi abbiamo la p53, cioè i marcatori molecolari, il c-erbB2, ne abbiamoricordate?-<br />
parlato sulla mammella, novità introdotta negli ultimi 2 anni,<br />
tuttora è ancora in studio, però è stato ormai accreditato, vedremo il<br />
perché; i marcatori cinetici quindi il Ki67; se dà metastasi ematiche le da<br />
soprattutto al fegato, ai polmoni, ai surreni, all’ovaio. L’invasività si esplica<br />
al di fuori dello stomaco nell’organo più vicino, il duodeno, poi l’esofago,<br />
scaricato da www.sunhope.it
per ovvii motivi, il cancro del corpo del fondo va a quel livello, spesso<br />
parliamo di cancro “della giunzione gastroesofagea” e non sappiamo se<br />
viene dall’esofago o dallo stomaco, rimandiamo questo discorso a quando<br />
affronteremo il cancro dell’esofago.<br />
L’invasione dei linfonodi sottomucosali, l’invasione dei linfatici, l’invasione<br />
sierosa e, quindi, abbiamo, vedete l’invasione all’intestino, all’omento, al<br />
pancreas, che è la forma più grave perché quando si verificano fenomeni di<br />
necrosi libera enzimi che sono molto litici e può, quindi, determinare una<br />
reazione a catena molto grave fino all’ovaio e quindi avee i tumori di<br />
Krukenberg. Una nuova notizia riguardo all’ER2, ricordate riguardo alla<br />
mammella, l’amplifcazione di questo recettore per il fattore di crescita,<br />
anche nel cancro gastrico si è visto che c’è una certa quota di carcinomi<br />
gastrici, ovviamente riguarda soprattutto il carcinoma gastrico avanzato,<br />
nell’early gastric cancer noi abbiamo molte speranze di andare bene senza<br />
ricorrere all’ER2, ma se il cancro è avanzato abbiamo visto che c’è una certa<br />
quota di tumori che esprimono un’amplificazione di questo recettore ER2;<br />
a differenza che nella mammella, nella mammella noi dicevamo che<br />
l’amplificazione si coglie attraverso delle possibilità di membrana,<br />
ricordate? Apparivano delle immagini ad occhiello perché tutte le<br />
possibilità erano sulla membrana, qua invece le possibilità sono, invece,<br />
intracitoplasmatiche e abbiamo un grading che va da 0 a 3, nella mammella<br />
è la stessa cosa, ovviamente 0 e1 sono considerati negativi dal punto di<br />
vista immunoistochimico, 2 e 3 sono considerati positivi, anche qui si può<br />
ricorrere all’ibridazione in situ, ma, in questo caso, paradossalmente, è più<br />
importante l’immunoistochimica che le tecniche molecolari, perché il<br />
cancro dello stomaco manifesta una notevole eterogeneità cellulare, per<br />
cui solo attraverso l’immunoistochimica noi possiamo cogliere<br />
un’immagine completa di cloni positivi, negativi, in modo da fare una<br />
valutazione a occhio, se facciamo, invece, l’ibridazione in situ dobbiamo<br />
prelevare un piccolo campione di cellule e vedere se a livello genico c’è<br />
quest’amplificazione e se questo campione potrebbe essere poco<br />
rappresentativo dell’intera popolazione monoblastica del cancro.<br />
Quanti sono i cancri? Qui vedete un recente lavoro che ha avuto una<br />
maggiore importanza nel 2009 che ha visto che sono soprattutto i cancri<br />
della giunzione gastro-esofagea quelli che più manifestano positività per<br />
scaricato da www.sunhope.it
l’ER2, nel 34% dei casi, nel carcinoma gastrico avanzato risulta positivo e<br />
quindi amplificato per l’ER2 nel 21% dei casi, il tipo intestinale è quello più<br />
frequentemente ER positivo, quello diffuso è invece ER negativo, concetto<br />
che può sembrare paradossale, ma, invece, è facilmente spiegabile, perché<br />
normalmente la cellula gastrica esprime questi recettori, un cancro<br />
indifferenziato può essere così indifferenziato da non esprimere più questi<br />
come altri recettori, amplificati, invece, nel cancro intestinale, perché c’è<br />
un deficit qualitativo di specializzazione di queste cellule, che, in effetti,<br />
hanno solo una logica intrinseca di proliferare, perdendo qualunque<br />
specializzazione. Se andiamo a fare un confronto tra la terapia classica del<br />
carcinoma gastrico avanzato e carcinoma gastrico trattato con Tarzuzumab,<br />
che sarebbe un anticorpo chimerico verso questi recettori e fattori di<br />
crescita ci rendiamo conto che la curva di sopravvivenza dei carcinomi<br />
gastrici avanzati è migliore dell’altra, onestamente, il vantaggio non è<br />
prorpio così eclatante, ma per un paziente ammalato di un cancro<br />
gravissimo anche una sopravvivenza e una qualità della vita migliore<br />
seppure ridotta di circa 5-6mesi ha un certo significato.<br />
Per quanto riguarda la stadiazione,qui ve l’ho rappresentata in maniera molto<br />
semplice.<br />
T1s: carcinoma intramucosale;<br />
T1: quando riguarda la mucosa e la sottomucosa;<br />
T2: quando invade la tonaca muscolare;<br />
T3: quando arriva fino alla sierosa,quindi supera la tonaca muscolare;<br />
T4: quando invade gli organi adiacenti,in questo caso probabilmente il pancreas.<br />
Quindi quando parliamo di Early Gastric Cancer,parliamo sempre di T1,che può<br />
infiltrare la mucosa e la sottomucosa.T2,vedete,quando supera la sottomucosa,e<br />
questa è la divisione più evidente,quando supera la muscolare abbiamo cancro<br />
avanzato.<br />
Per quanto riguarda i linfonodi,abbiamo:<br />
N1: da 1 a 2 linfonodi metastatizzati;<br />
N2:da 3 a 6 linfonodi metastatizzati;<br />
scaricato da www.sunhope.it
N3:più di 6 linfonodi coinvolti.<br />
M0:assenza di metastasi a distanza;<br />
M1:presenza di metastasi.<br />
Ecco qui la prognosi confrontata al follow-up tra Early Gastric Cancer e carcinoma<br />
gastrico avanzato. Vedete che il follow-up a 5 anni da una percentuale elevata:97%<br />
per l’intramucosale, 85-91% per il sottomucosale. La media dell’early gastric<br />
cancer,comunque sia,intra o sottomucosale,è del 95%. Questo è un grande successo.<br />
Vedete che invece questa media per il carcinoma avanzato scende molto,fino ad<br />
arrivare al 20-30% nello stadio T4. C’è quindi un drammatico peggioramento.<br />
Sui polipi gastrici ci soffermeremo poco. Parleremo soprattutto dei primi 3 tipi che<br />
sono comuni all’intestino,dove hanno un’incidenza maggiore,e dove sono<br />
maggiormente coinvolti nella cancerogenesi. Nello stomaco no,perché come<br />
abbiamo visto il principale indiziato è l’Helicobacter Pylori.<br />
Allora abbiamo i polipi cosiddetti iperplastici. Iperplastico indica un disordine<br />
cinetico localizzato. Immaginate cosa succede quando in una struttura ghiandolare<br />
quell’equilibrio che dovrebbe esserci tra proliferazione e differenziamento viene<br />
turbato, a favore della proliferazione. Ovviamente se aumenta l’attività proliferativa<br />
c’è minor tempo per specializzarsi,e c’è un aumentato numero di cellule. Ora questa<br />
ghiandola si può dilatare,ma fino ad un certo punto,perché al di fuori della ghiandola<br />
sapete che c’è tessuto stromale fibroso o elastico che oppone una certa resistenza<br />
alla dilatazione,allora queste cellule aumentate di numero cercano di disporsi un<br />
poco a scala. Il contorno nell’interno della ghiandola è irregolare,possiamo vedere<br />
come dei rilievi papillariformi,perché in questo modo si aumenta la superficie utile e<br />
più cellule trovano un posticino. Questo polipo iperplastico, è un polipo di per sè<br />
innocente,perché difficilmente può andare incontro ad una trasformazione,non ha<br />
un potenziale intrinseco,ma un potenziale estrinseco,perché comunque esprime un<br />
disordine cinetico che può essere una condizione predisponente ad altre noxae che<br />
possono determinare il cancro. Quindi è come una spia che si accende,un indicatore<br />
di rischio. Il polipo neoplastico è il vero polipo tumorale. Lo consideriamo una<br />
neoplasia benigna,però suscettibile di trasformazione maligna. Cioè questo è il vero<br />
polipo che ha la possibilità di trasformarsi in carcinoma. E ce ne accorgiamo anche se<br />
osserviamo la morfologia,perché questo è un polipo che per definizione è<br />
displastico,quindi presenta delle atipie citologiche,perciò lo si chiama pure polipo<br />
scaricato da www.sunhope.it
neoplastico,o più comunemente adenoma. Approfondiremo queste problematiche<br />
quando parleremo dell’intestino.<br />
Il polipo amartomatoso (il termine amartomatoso indica un disordine più<br />
quantitativo che qualitativo. Immaginate una vignetta, noi riconosciamo il<br />
personaggio,ma alcuni aspetti sono caricaturati). Quindi è un polipo che esprime<br />
anomalie soprattutto quantitative.<br />
Nello stomaco abbiamo due tipi di polipi,rari ma specifici dello stomaco. Il polipo a<br />
ghiandole fundiche è caratteristico dello stomaco. In effetti,per essere a ghiandole<br />
fundiche,è un rilievo della mucosa che insorge soprattutto in aree non fundiche,e<br />
che ha le stesse componenti delle ghiandole gastriche propriamente dette,cioè<br />
cellule principali e cellule parietali.<br />
E poi abbiamo il cosiddetto polipo fibroide infiammatorio,che non è un vero<br />
polipo,ma è una lesione vascolare,probabilmente infiammatoria,che insorge<br />
nell’antro,associato spesso ad aree di gastrite atrofica e fatto soprattutto di tessuto<br />
fibroso e vascolare,e ha anche una componente infiammatoria.<br />
Foto. Questo è il polipo iperplastico:vedete che qui,mentre questa ghiandola si è<br />
dilatata,di qua questo promontorio le consente di aumentare la superficie utile.<br />
Ancora qui vedete,la ghiandola non ha un contorno regolare ma sinuoso,perché cosi<br />
aumenta la superficie utile per l’aumentato numero di cellule a causa dello squlibrio<br />
proliferazione-differenziamento.<br />
Nel polipo a ghiandole fundiche,noi vediamo le ghiandole fundiche propriamente<br />
dette,vediamo delle dilatazioni cistiche,si distinguono delle cellule più sierose,più<br />
acidofile, e le basofile,come nella mucosa fundica normale.<br />
Questo è il polipo fibroide,vedete ha una componente granulocitica eosinofila,una<br />
componente fibrosa,è riccamente vascolarizzato. Il fatto caratteristico è che queste<br />
cellule sono positive per il CD34 che è un marcatore dei vasi.<br />
Questo è l’adenoma,vedete la differenza,l’adenoma ha questa displasia,nuclei<br />
decisamente atipici,c’è un’ipercromasia di fondo dei nuclei che si coglie facilmente.<br />
Per quanto riguarda i tumori neuroendocrini (NET),nello stomaco sono 4 i tipi<br />
principali.<br />
Il primo è associato alla gastrite autoimmune(tipo A),nel senso che si può sviluppare<br />
scaricato da www.sunhope.it
questo carcinoma neuroendocrino,che poi è a basso grado di malignità.<br />
Il tipo 2 invece è associato alla sindrome di Zollinger-Ellison.<br />
Il tipo 3 non ha nessuna condizione predisponente,ha un rischio di metastasi nel 22-<br />
75%, e una mortalità abbastanza elevata.<br />
Il tipo 4 insorge quando c’è sia un’ipercloridria che un’ipergastrinemia,ha una elevata<br />
tendenza a metastatizzare, e molto spesso è costituito da carcinomi a piccole cellule.<br />
Questi sono i soliti marcatori,in questo caso è l’enolase in un tumore<br />
neuroendocrino.<br />
Quali sono gli indicatori del comportamento clinico-biologico che possiamo trovare<br />
nel tumore neuroendocrino. Grossomodo riflettono il comportamento dei tumori<br />
neuroendocrini: delimitazione < 1cm,confinati alla mucosa e alla sottomucosa<br />
e non hanno segni di angioinvasività, cioè non troviamo emboli neoplastici nei vasi.<br />
Il tipo border-line,cioè tra il benigno e il maligno,ancora confinato alla sottomucosa,<<br />
1cm,ma con presenza di emboli neoplastici,oppure > 1 cm.<br />
Basso grado di malignità quando si estende oltre la sottomucosa,ovvero non è più un<br />
early gastric cancer.Gli altri invece rientrano nella categoria dell’early gastric<br />
cancer,pur essendo neuroendocrini,con angioinvasività o senza. L’altro carattere di<br />
malignità quando c’è una spiccata invasività,quindi la parete sottostante viene<br />
coinvolta a tutto spessore,fenomeni di necrosi,atipie citologiche e cosi via.<br />
Un’altra categoria che dobbiamo introdurre è una categoria abbastanza recente,cioè<br />
fino a 5-10 anni fa veniva usato questo acronimo che si chiama GIST (gastrointestinal<br />
stromal tumor),cioè sono i tumori dello stroma.<br />
Il GIST nello stomaco si vede abbastanza spesso,forse è una delle cellule più presenti,<br />
si può presentare in varii modi,molto spesso succede che l’endoscopista non vede<br />
niente,perché è un tumore che nasce da sotto e solo negli stadi avanzati può<br />
cogliere un rilievo,o radiologicamente o con la TAC.<br />
Questi tumori possono esprimere in vario modo diverse linee differenziative. Può<br />
avere una differenziazione muscolare, e allora avremo il leiomioma e il<br />
leiomiosarcoma; può avere una differenziazione neuroectodermica, ecc.<br />
Ovviamente tutti questi tumori hanno un marcatore caratteristico che è il CD117<br />
scaricato da www.sunhope.it
che è un recettore per la tirosin chinasi. Le sedi: nella sottomucosa il 60% dei<br />
casi,sottosierosa 30%, intramucosale 10% che è quello più evidente perché più si<br />
appalesa con un rilievo,mentre gli altri è più difficile coglierli da un punto di vista<br />
diagnostico e clinico. All’inizio non hanno questa tendenza a dare fenomeni<br />
degenerativi e necrotici.<br />
Volendoli classificare da un punto di vista istologico avremo tumori a<br />
differenziazione muscolare,quindi esprimeranno actina,miosina,tutti marcatori delle<br />
cellule muscolari. Tumori a differenziazione neurale, e questi sono quasi sempre<br />
maligni,esprimeranno enolase,neurofilamenti, e tutti i marcatori della cellula<br />
neurale. Poi abbiamo tumori misti,cioè muscolari e neurali, e tumori cosi<br />
indifferenziati che non esprimono né il CD117,né il CD34,in effetti possiamo arrivare<br />
a questa diagnosi per esclusione,perché non esprime niente,ha un aspetto di tumore<br />
stromale,però non esprime marcatori stromali, melanocitari, muscolari,<br />
linfocitari,quindi la diagnosi è per esclusione di GIST indifferenziato.<br />
Il grading è molto importante. A rischio minimo meno di 5 figure mitotiche per 10<br />
campi, a rischio intermedio da 6 a 10,ad alto rischio più di 10figure mitotiche per 10<br />
campi ad alto ingrandimento.<br />
Questo è un GIST e già si vede che è molto maligno,per le aree di necrosi e di<br />
ulcerazione multiple.<br />
Questo è il tumore a differenziazione muscolare. Il leiomioma ha la caratteristica di<br />
avere sempre questo vacuolo sopranucleare; il motivo di questa vacuolizzazione<br />
perinucleare è molto complesso e ve lo risparmio.<br />
Questo è il tumore neuroectodermico,ha una strutturazione che ricorda la primitiva<br />
crescita neurale,cioè di cellule disposte a palizzata,la struttura del tubo neurale<br />
primordiale. Riconosciamo anche delle fibre molto eosinofile che si chiamano fibre<br />
stenoidi,dal loro scopritore,che sono una caratteristica di questi tumori.<br />
Poi addirittura può essere un microcitoma,poco indifferenziato,vedete,questo è il<br />
tipo indifferenziato,possiamo cogliere anche qualche mitosi in questo campo.<br />
Ecco qui un altro poco differenziato,vediamo che assume una forma come dire<br />
globoide,però capiamo che è un tumore appartenente a questa classe perché è<br />
CD117 positivo.<br />
Tra i linfomi non-Hodgkin distinguiamo il basso grado,tipo MALT. Vi ricordo che lo<br />
scaricato da www.sunhope.it
stomaco è uno degli organi dove sono più frequenti i linfomi<br />
extralinfoghiandolari,soprattutto tipo MALT,che già abbiamo detto è legato all’<br />
Helicobacter. Poi il centroblastico e l’immunoblastico.<br />
Vi ricordo che tutti i linfomi che insorgono in organi epiteliali hanno la caratteristica<br />
di formare questi complessi linfoepiteliali. Qua vedete dei linfociti ch penetrano e<br />
distruggono la mucosa di una ghiandola gastrica.<br />
Questo è un linfoma di alto grado, a grandi cellule.<br />
Fra i tumori non epiteliali abbiamo il mioblastoma, detto anche tumore di Abrikosos,<br />
ma già ne abbiamo parlato,comunque ne parleremo più avanti,quando parleremo<br />
del cavo orale.<br />
E i tumori a cellule germinali.<br />
Lo stomaco può essere sede di metastasi. I tumori che più frequentemente possono<br />
dare metastasi gastriche sono i tumori della mammella,del polmone e i melanomi.<br />
Molto spesso la metastasi,ovvero il tumore secondario dello stomaco, assume una<br />
forma conica,crateri forme.<br />
Finiremo domani.<br />
scaricato da www.sunhope.it
CONTINUO SISTEMA LINFOEMOPOIEICO<br />
Finiamo prima questo sistema,oggi passeremo in rassegna sommariamente il<br />
midollo osseo,parlando della sua struttura normale,le sindromi mielodisplastiche,le<br />
sindromi mieloproliferative e parleremo del coinvolgimento secondario del midollo<br />
in corso di linfomi o di altre patologie,perché il midollo può essere coinvolto anche<br />
da carcinomi.Una breve rassegna di tutte le cellule che troviamo nel midollo osseo,in<br />
esso vi troviamo varie linee differenziative,anche qui ci sono cellule staminali e ci<br />
sono le cellule staminali più potenti,è una riserva importantissima del nostro<br />
organismo.Oltre le cellule staminali,di cui parleremo,ci sono altre linee<br />
cellulari,innanzitutto i linfociti.Vi ricordo che i linfociti T hanno come prima sede<br />
proprio il midollo.Come facciamo a sapere con l’immunoistochimica dove stanno i<br />
linfociti T?Basta utilizzare un marcatore comune,l’ALC,che vuol dire antigene<br />
leucocitario comune o linfocitario comune e marca tutti i linfociti.Quindi se vogliamo<br />
sapere quanti sono i linfociti li marchiamo e andiamo a vedere.Poi abbiamo le cellule<br />
mieloidi.La linea mieloide si differenzia in tre sottolinee,quella neutrofila,quella<br />
basofila e quella eosinofila e per vedere tutte le cellule mieloidi che ci stanno<br />
facciamo la mieloperossidasi,che marca tutte le cellule della categoria.I monociti<br />
pure originano dalla cellula progenitrice delle cellule mieloidi.Monocita è un termine<br />
usato dagli ematologi,l’anatomopatologo preferisce il termine macrofago,alcuni lo<br />
chiamano istiocita,ma è sempre lui.Si intende per monocita più un macrofago<br />
circolante.Cmq ha il CD68.Poi ci sono i megacariociti ,qualora non si riuscisse a<br />
vedere,perché in genere si vede dato che sono cellule plurinucleate e quindi<br />
evidenti,usiamo il loro marcatore che è il fattore ottavo( FVIII-RAg),l’antigene<br />
correlato al fattore ottavo che marca queste cellule.Gli eritroblasti,a differenza delle<br />
emazie che si vedono,non si distinguono dalle altre,dalle cellule mieloidi in una fase<br />
iniziale di sviluppo,però se facciamo la glicoforina,i precursori della serie eritroide<br />
sono marcati.Se vogliamo pure marcare i vasi,per sapere se il midollo è ricco o meno<br />
di vasi,allora usiamo il CD34 che è un marker endoteliale.Se vogliamo vedere<br />
l’impalcatura del midollo,ovvero il tessuto di sostegno,vediamo che questo è<br />
costituito da tessuto reticolare,cioè non fibroso ,perché se lo fosse non<br />
consentirebbe gli scambi.Si dice reticolare quando è formato da sottili fibrille<br />
collagene,in modo tale che è un sostegno delicato,immaginate come fili di cotone<br />
che si intrecciano e determinano così delle caselle,in ognuna della quale c’è la sua<br />
scaricato da www.sunhope.it
cellula.Se vogliamo sapere se questo reticolo sta bene o è ammalato o è<br />
ipertrofico,facciamo i metodi istochimici del reticolo che vedremo più avanti.<br />
Il midollo subisce delle oscillazioni a seconda dell’età.Ha una strutturazione ossea e<br />
degli spazi detti spazi midollari.Ci sono zone di midollo osseo particolarmente<br />
attive,per esempio la cresta iliaca,la zona retrosternale e poi ci sono zone che con<br />
l’età tendono a trasformarsi in tessuto adiposo,marcatore dell’età di un soggetto<br />
normale,però ci sono sedi sempre attive anche se aumenta il tessuto adiposo tra cui<br />
la cresta iliaca e la zona sternale. ,che sono le sedi preferite quando si va a fare una<br />
biopsia osteomidollare,soprattutto la cresta iliaca.<br />
Le cellule eritroblastiche,eritrocitiche e i megacariociti si localizzano principalmente<br />
nelle regioni centrali,le altre cellule,quelle mieloidi e così via, preferiscono le<br />
curve,ovvero la zona paratrabecolare, ,detta così perché sta vicino alle<br />
trabecole.Distinguiamo quindi due zone,una centrale e una paratrabecolare.Di<br />
linfociti non ce ne sono tanti nel midollo.Se facciamo la colorazione base,che si<br />
chiama GIEMSA,pensate che è una colorazione fatta con un solo colorante,che in<br />
teoria va sull’azzurro-bleau,questo colorerà in maniera metacromatica,cioè le cellule<br />
acquisiscono un colore diverso da quello da quello che si dà.Le cellule interagiscono<br />
con la sostanza chimica del colorante e determinano un cambio del colore.Questo ad<br />
esempio è per le cellule mieloidi e vedete che le cellule mieloidi si<br />
distinguono,perché hanno delle granulazioni che in genere sono di colore rosso.Poi<br />
questa cellula qui plurinucleata è il megacariocita chpoi darà origine alle piastrine.Si<br />
può vedere pure qualche plasmacellulina.<br />
In genere i linfociti B che si trovano nel midollo non esprimono il CD20,perché sono<br />
cellule pre-B e quindi trovare cellule CD20 positive nel midollo è sempre<br />
sospetto,perché ci orienta verso un linfoma,essendo il midollo una sede dove si<br />
possono trovare dei linfociti B.I pre-B si,ma trovare i linfociti B può far pensare ad un<br />
coinvolgimento secondario del midollo da parte del linfoma.Mentre,per motivi che<br />
non conosciamo ancora,può capitare di trovare degli aggregati di linfociti T nel<br />
midollo normale e stanno un po’ lì a controllare tutta la situazione,perché i linfociti T<br />
sono un po’ i controllori.Ecco la mieloperossidasi,la glicoforina che marca le cellule<br />
eritroidi e questo è il metodo del reticolo:queste sono le trabecole ossee,vedete il<br />
reticolo.Questo è un metodo di impregnazione,si usano dei sali,spesso d’argento,i<br />
Sali d’oro sono stati eliminati da quando è aumentato l’oro.I Sali d’argento marcano<br />
scaricato da www.sunhope.it
questo reticolo e vedete in qualche punto come delle caselle,delle fibrille molto<br />
sottili.<br />
Ora vediamo qual è la composizione:<br />
In un soggetto di età media il tessuto osseo rappresenta il 30 %,il tessuto adiposo il<br />
30 % e il tessuto emopoietico il 40%.Quali sono le oscillazioni con l’età?Dai 0-10 aa il<br />
midollo emopoietico rappresenta il 70-80%,per cui nella prima decade il midollo<br />
osseo costituisce la componente maggiore,se andiamo a vedere un soggetto di 80 aa<br />
il midollo osseo con tutte le linee differenziative che abbiamo detto prima<br />
rappresenta meno del 30 %. Quindi se vediamo un soggetto di età avanzata con un<br />
midollo osseo abbastanza ricco vuol dire che c’è una patologia.Se vogliamo vedere<br />
pure le varie composizioni,la serie eritroide incide per il 10-20%,la mieloide per il 40-<br />
65%,le plasmacellule meno del 3%,i linfociti e vi ricordo soprattutto i linfociti B<br />
immaturi,perché i linfociti B con il CD20 non li vediamo meno del 20% e i<br />
megacariociti il 2-5 in un campo ad alto ingrandimento,però si vedono chiaramente<br />
perché sono cellule molto grosse e plurinucleate.<br />
Ora vediamo le sindromi mielodisplastiche,ma le accenniamo solo per cui potete<br />
fare pure riferimento al libro.Le sindromi mielodisplastiche sono patologie non rare e<br />
sono legate ad alterazioni delle cellule staminali midollari.Quest’alterazione può dare<br />
quella che viene detta eritropoiesi inefficace.Che vuol dire?vuol dire che il midollo<br />
c’è,funziona,ma le cellule circolanti diminuiscono.Immaginate una fabbrica di<br />
automobili,la fabbrica funziona,però le macchine non escono(risata nasale)e perché<br />
non escono?per mutazioni genetiche con compromissione dell’attività<br />
maturativa,differenziativa di queste cellule che presentano quindi anomalie,per cui<br />
sono bloccate e non possono passare in circolo,ma se andiamo a vedere il midollo<br />
addirittura possiamo trovare un midollo ipercellulare,però a questa ipercellularità<br />
corrisponde una carenza periferica.L’evoluzione di queste sindromi va verso<br />
l’insufficienza o le leucemie acute,possono rappresentare pure lo stadio terminale di<br />
una leucemia acuta,per cui questi pazienti vanno seguiti.Alle sindromi<br />
mielodisplastiche appartengono le cosiddette ANEMIE REFRATTARIE,dette così<br />
perché non rispondono ai comuni farmaci che si usano nelle anemie ed è evidente il<br />
perché,perché possiamo dare tutte quelle sostanze,quei fattori di crescita,ma se c’è<br />
un errore a livello della fabbrica,queste automobili sono difettose e non escono lo<br />
stesso.Come sono queste anemie refrattarie?molto spesso succede che sono ricchi<br />
di ferro e voi sapete che il ferro entra nella struttura dell’Hb e per fattori non del<br />
scaricato da www.sunhope.it
tutto conosciuti c’è un aumento del ferro,per cui si formano delle cellule eritrocitarie<br />
o eritroblastiche dette sideroblasti,ovvero vediamo il ferro che si deposita a corona<br />
intorno alle emazie,per cui vediamo un’emazia anomala e ci sono dei metodi<br />
particolari che evidenziano il ferro. Poi c’è una citopenia refrattaria,cioè un’anemia<br />
che non si risolve con i comuni farmaci,c’è una displasia multilineare,nel senso che<br />
atipie non si trovano solo nella serie eritroide,che è la più compromessa,ma anche<br />
nella altre serie,anche s ein misura minore e troviamo quasi sempre una o più<br />
delezioni a livello del cromosoma 5 (del 5q).Poi ci sono altre patologie non<br />
classificabili o non definibili di cui non parleremo.<br />
PRINCIPALI ASPETTI ANATOMOPATOLOGICI(alterazioni primitive):<br />
-ipercellularità di una o più serie del midollo<br />
-depositi di ferro in cellule eritoridi,chiamate sideroblasti<br />
-disordini strutturali con dislocazione anomala delle varie serie emopoietiche,perché<br />
quella bella suddivisione nelle curve e nelle zone centrali salta,vi ho detto prima che<br />
le cellule eritroidi si distribuiscono nelle regioni centrali e qua invece non è così e si<br />
distribuiscono in maniera un po’ caotica in tutto il midollo.<br />
ALTERAZIONI SECONDARIE:<br />
-granulazioni irregolari delle cellule mieloidi<br />
-i granulociti che normalmente hanno un nucleo segmentato hanno alterazioni di<br />
forma o di volume<br />
-gli eritrociti possono essere più piccolo o più grandi e così anche i megacariociti.<br />
Ci sono quindi alterazioni sia citologiche che funzionali e anche delle atipie.<br />
Il Pearls è il metodo che noi utilizziamo per evidenziare il ferro,nella versione inglese<br />
si chiama Pearls,nella versione più antica si chiama blu di Prussia,detto anche blu di<br />
Berlino.Abbiamo detto che la serie più colpita è l’eritroide,ma anche i<br />
megacariociti,vedete,presentano una caratteristica anomala:innanzitutto c’è la<br />
tendenza a formare aggregati,abbiamo detto che i megacariociti sono 4-5 per campo<br />
ad alto ingrandimento,qui invece sono molti di più e sono tutti vicini,vi sono<br />
megacariociti plurinucleati e altri con 1 nucleo,1 e mezzo,2 nuclei e quindi sono<br />
atipici.<br />
scaricato da www.sunhope.it
Questi sono i sideroblasti e se facciamo il metodo Pearl si vedono queste<br />
granulazioni verdastre,perché questo metodo si basa sulla riduzione del ferrocianuro<br />
di potassio,si vedono quindi punteggiature verdognole.<br />
Un altro tipo è l’anemia refrattaria con eccesso di blasti,cioè queste cellule<br />
eritroblasti che diventano molto blastiche tant’è che non esprimono più marcatori<br />
ed esprimono,invece,un marcatore che è il CD34 che è degli endoteli,ma anche delle<br />
cellule non commissionate(parastaminali,blastiche).<br />
Le sindromi mieloproliferative<br />
L’incidenza è di 6-10/100.000 per anno.Questa malattia è caratterizzata da un<br />
disordine della cellula staminale clonale,perché colpisce un clone cellulare.Questo<br />
clone va incontro ad una proliferazione molto irregolare,però c’è un’eritropoiesi<br />
EFFICACE,perché a questo clone che va in proliferazione corrisponde poi,a seconda<br />
della linea differenziativa, un eritrocitosi,una trombocitemia,cioè un aumento delle<br />
piastrine, a differenza di prima,perché questo clone va incontro ad una<br />
proliferazione abnorme,ma l’eritropoiesi efficace,perché troviamo questa aumentata<br />
produzione anche in circolo,quindi la fabbrica fa uscire le macchine.La proliferazione<br />
è talmente incontrollata,che possiamo trovare anche una cosa che in genere si trova<br />
solo nei neonati o negli embrioni,ovvero FOCOLAI DI ERITROPOIESI<br />
EXTRAMIDOLLARI,cioè in organi come la milza,il fegato,dove non dovrebbero starci.<br />
All’inizio in genere queste sindromi hanno un atteggiamento ipercellulare,nel corso<br />
del tempo(e qui è la terapia che cerca di intervenire per evitare tale<br />
fenomeno)vanno incontro ad un’aplasia,ad una fibrosi midollare,probabilmente per<br />
l’azione di alcune citochine e fattori di crescita come il PDGF,l’FGFbeta,per cui si<br />
passa da una fase di iperfunzione ad una di depressione,di ipofunzione con<br />
successiva fibrosi del midollo.Possibile anche qui l’evoluzione verso la leucemia o<br />
verso l’insufficienza midollare,che pure è molto grave,perché è un’insufficienza<br />
totale,refrattaria ad alcuni fattori che stimolano l’attività dle midollo osseo.<br />
Quali sono le principali varietà:<br />
-la mielofibrosi cronica idiopatica,idiopatica,perché non si sanno bene le cause<br />
-la policitemia vera,ovvero un aumento degli eritrociti con tutte le relative<br />
conseguenze.Policitemia vera,perché è primitiva,perché la policitemia può essere<br />
provocata anche dalle altitudini per riduzione della P parziale dell’ossigeno,con<br />
scaricato da www.sunhope.it
policitemia secondaria.Pure se si fa qualche sforzo i primi controlli che si fanno sono<br />
l’emocromo,l’ematocrito,addirittura è in voga l’autotrasfusione,perché ad esempio<br />
un ciclista si fa un prelievo 15 giorni prima della gara e poi il giorno prima della gara<br />
si inocula il suo sangue in modo da aumentare la massa circolante,in modo che in<br />
salita ovviamente,avendo più eritrociti ha più ossigeno e quindi è avvantaggiato<br />
rispetto agli altri.Oggi è sempre più frequente il doping e quindi l’uso di<br />
sostanze,quasi mai non identificabili.Nel caso dell’autotrasfusione questa usciva fuori<br />
dall’ematocrito che risultava di 50-60 e questo è pericoloso,per aumento della<br />
densità del sangue con possibilità di trombosi.<br />
-la trombocitemia essenziale,ovvero un aumento delle piastrine con possibilità che<br />
queste si aggreghino<br />
-la leucemia mieloide cronica(cromosoma filadelfia,gene di fusione BCR/ABL)<br />
-altre forme di leucemia(eosinofila,neutrofila)<br />
-forme non classificabili<br />
IMMAGINI<br />
Nella fase cellulare della mielofibrosi idiopatica vi è un aumento cellulare,in questo<br />
caso dei megacariociti e l’antigene correlato al fattore VIII marca queste cellule.Nella<br />
fase successiva il midollo quasi scompare,perché compare al suo posto tessuto<br />
fibroso,il tessuto osseo pure subisce un fenomeno di osteosclerosi,di iperostosi,le<br />
cavità midollari si riducono e se andiamo a fare il reticolo,vedremo che non c’è più<br />
quel reticolo delicato che vedevamo rpima,ma appare molto fitto,molto grossolano.<br />
Nella leucemia mieloide cronica si osserva,già ad un piccolo ingrandimento,che c’è<br />
un midollo espanso e se vediamo il quadro citologico si osserva l’espansione di un<br />
clone a scapito degli altri,c’è questo clone mieloide e alcune cellule mostrano ancora<br />
una sepimentazione che ci ricorda un po’ i granulociti,latre cellule invece non<br />
sepimentano e sono i precursori,le cellule mieloblasti che,però con la<br />
mieloperossidasi vediamo che si tratta di cellule che appartengono alla serie<br />
mieloide.Queste forme di leucemia poi possono avere una fase blastica,prima si<br />
vedeva un po’ di citoplasma nelle cellule con qualche granulo,mentre in questa fase<br />
ci sono cellule molto blastiche,nel sneos che non c’è maturazione dle citoplasma.<br />
La policitemia,caratterizzata da un aumento di tutta la serie eritrioide,anch’essa ad<br />
un certo punto finisce nell’osteosclerosi,la tappa finale di questa malattia.Quindi<br />
scaricato da www.sunhope.it
prima c’è un aumento delle emazie e poi si ha osteosclerosi,cioè tutto il midollo<br />
osseo tende ad ossificarsi<br />
Infine c’è la trombocitemia con aumento dei megacariociti,che sono più grandi<br />
rispetto alla norma e aumento delle piastrine.<br />
Esistono poi sindromi MIELOPROLIFERATIVE DISPLASTICHE,in cui vi sono i segni un<br />
po’ dell’una e un po’ dell’altra,ma sono molto rare,per fortuna,perché sono di<br />
difficile inquadramento diagnostico.<br />
COINVOLGIMENTO DEL MIDOLLO NEL LINFOMI<br />
Nei linfomi di Hodgkin il coinvolgimento non è frequente,ksi pensa sia intorno al<br />
5%,però è molto in rapporto all’istotipo,ci sono istotipi come la prevalenza<br />
linfocitaria e la prevalenza linfocitaria nodulare in cui il coinvolgimento dle midollo è<br />
inferiore all’1% dei casi,mentre nella deplezione linfocitaria il coinvolgimento è del<br />
50% dei casi.<br />
Per quanto attiene ai linfomi non Hodgkin,i vari tipi di linfomi hanno una variabile<br />
percentuale di compromissione midollare a seconda dei tipi,perché ci sono dei tipi in<br />
cui il coinvolgimento midollare supera l’80-90%,come nella cosiddetta leucemia<br />
linfatica cronica o linfoma a piccoli linfociti e altri tipi in cui il coinvolgimento è più<br />
raro,come nel linfoma MALT.<br />
Come può essere il coinvolgimento?In linea di massima,se il coinvolgimento è<br />
minimale,la prima sede coinvolta è quella paratrabecolare,cioè troviamo qualche<br />
focolaio vicino alle trabecole ossee.Poi c’è quello interstiziale o sinusoidale,per cui<br />
troviamo degli aggregati un po’ ovunque,anche nelle regioni centrali e poi il<br />
coinvolgimento più grave è quello follicolare,in cui vedremo un grosso aggregato di<br />
cellule linfoidi.Ovviamente stiamo parlando soprattutto di linfomi a cellule B.<br />
IMMAGINI:ecco il coinvolgimento paratrabecolare,qui solo un occhio esperto riesce<br />
ad individuare aggregati linfoidi lungo le trabecole.Quello interstiziale è il più difficile<br />
da riconoscoere,per cui si devono fare i marcatori,perché tutti questi linfociti non è<br />
che tendono a formare dei grandi aggregati,ma si insinuano negli spazi.Si tratta di<br />
linfociti B,la cui presenza è anomala.Infine c’è la forma follicolare,in cui vediamo un<br />
nodulo molto grosso in una zona centrale del midollo e se facciamo il CD20 non<br />
abbiamo dubbi che si tratta di un linfoma a cellule B,anche se non c’è una<br />
scaricato da www.sunhope.it
precedente diagnosi,perché raramente un linfoma può nascere nel midollo<br />
osseo,avere questo come prima sede.<br />
DISCRASIE PLASMACELLULARI<br />
Questo è un termine poco noto,da poco usato a livello internazionale,che raggruppa<br />
sia patologie neoplastiche che preneoplastiche ad un certo inquadramento:<br />
-il mieloma multiplo è il prototipo di queste malattie.Vi è pure un mieloma<br />
osteosclerotico che rientra nella cosiddetta sindrome di<br />
Poems:polineuropatia,endocrinopatia,proteina M,”skin changes”<br />
-plasmocitoma,che è un mieloma solitario,perché la lesione è solitaria e si<br />
contrappone al mieloma multiplo che coinvolge più sedi dello<br />
scheletro,caratteristiche sono la teca cranica,le vertebre.Parliamo di plasmocitoma<br />
pure quando è colpito un linfonodo.<br />
-macroglobulinemia di Waldenstrom:se vi ricordate i linfomi,vediamo che oltre al<br />
plasmocitoma vi è anche il linfoma linfoplasmocitoide,che secerne soprattutto IgM<br />
catene pesanti e queste situazioni,non sempre,ma spesso,corrispondono a questi<br />
tipi di linfomi.<br />
-malattia delle catena pesanti,in cui sono coinvolte non solo le IgM,ma anche altre<br />
catene pesanti,può essere associata a vari tipi di linfoma non Hodgkin,soprattutto<br />
quelli della linea plasmocitoide-plasmocitaria.<br />
-gammapatie monoclonali di significato indeterminato,sono molto diffuse(possono<br />
interessare il 2-3% delle persone di oltre 65 anni) e costituiscono un grande<br />
problema per gli ematologi e per noi che vediamo le biopsie osteomi dollari.I ¾ dei<br />
casi sono benigni,ma comunque questi pazienti vanno seguiti,perché nel 25% dei<br />
casi può evolvere in mieloma.Quindi avere una gammapatia monoclonale significa<br />
essere esposti in ¼ dei casi nel corso degli anni ad un’evoluzione possibile verso il<br />
plasmocitoma,ma non ci sono dei marker predittivi che ci dicano se ci sarà o meno<br />
questa evoluzione,per cui questi pz si devono controllare periodicamente.<br />
Ecco il CD138 che marca tutte le cellule plasmocitarie e per sapere se ci troviamo di<br />
fronte ad una neoplasia o ad una plasmocitosi reattiva si fanno le catene leggere (k e<br />
lambda),ovviamente qua vedete una monoclonalità a livello del tessuto e questo<br />
indica un processo neoplastico.<br />
scaricato da www.sunhope.it
ALTRE NEOPLASIE MALIGNE DEL MIDOLLO OSSEO<br />
-linfoma linfoblastico a cellule B e T<br />
-leucemia a cellule mastocitarie<br />
-mastocitosi sistemica<br />
-leucemia mieloide acuta<br />
L’esame del midollo osseo si può fare in vari modi.Una volta si faceva lo<br />
striscio,l’ematologo lo fa ancora,ma ovviamente una maggiore accuratezza<br />
diagnostica si raggiunge con la biopsia,che in genere si fa a livello della cresta<br />
iliaca.Perchè si fa questa biopsia?-Per evidenziare patologie primitive o secondarie<br />
-per la stadiazione(stiamo parlando di linfomi,ma anche in altri tipi di cancro,come<br />
quello della mammella,non raramente si trovano metastasi a livello midollare)<br />
-per una valutazione clinico-terapeutica,nel senso che già sappiamo che c’è una<br />
patologia del midollo osseo e andiamo a valutare l’effetto della terapia con una<br />
seconda biopsia.<br />
Ci sono però problemi tecnici,perché i campioni bioptici sono frustolini di qualche<br />
millimetro di spessore e qualche centimetro di lunghezza.Nella decalcificazione,ad<br />
esempio,usata per ottenere un taglio più evidente,si altera non solo la<br />
morfologia,ma anche l’antigenicità,perché in genere si usano processi acidi di altro<br />
tipo.Il campione poi deve essere adeguato,perché ad esempio s eil midollo è<br />
fibrotico non si ottiene niente.Poi ci sono tecniche immunoistochimiche e<br />
molecolari,che sono essenziali.<br />
TUMORI CHE DANNO METASTASI MIDOLLARI<br />
1-mammella<br />
2-prostata<br />
3-polmone<br />
4-stomaco<br />
5-colon<br />
6-rene<br />
scaricato da www.sunhope.it
7-tiroide<br />
8-neuroblastoma ecc<br />
A volte succede che il cancro è occulto,però a causa del coinvolgimento<br />
midollare,possono comparire anemia,citopenie varie,per cui si va ad esaminare il<br />
midollo e si scopre la presenza del tumore.Nel midollo,quando c’è una metastasi,un<br />
buon criterio è andare a vedere anche il reticolo,perché se c’è una metastasi,c’è<br />
un’aggressività che tende a distruggere il reticolo preesistente(qui per esempio sono<br />
rimaste poche fibre reticolari) e per sapere da dove viene il tumore vediamo<br />
l’antigene leucocitario comune,che se è negativo non è un linfoma,vediamo la<br />
sinaptofisina che se positiva indica un carcinoma neuroendocrino oppure vediamo il<br />
TTF1,fattore di trascrizione del polmone,che è un marker del microcitoma<br />
polmonare.Sapete che il microcitoma polmonare ha un diametro molto piccolo,per<br />
cui può sfuggire alle indagini strumentali e può dare metastasi.Quando è positivo<br />
l’HMB45 si fa diagnosi di melanoma occulto.Vi sono dei casi in cui non si riesce a<br />
capire il melanoma dove sta,talvolta per errori di migrazione della cresta neurale<br />
raramente si può avere un melanoma in organi profondi,perché queste cellule che<br />
dovevano andare a colonizzare la cute vanno a fermarsi in organi<br />
profondi(es.melanoma intestinale),sempre che siano ,però,evidenze di un melanoma<br />
a livello cutaneo.<br />
CAVO ORALE<br />
La mucosa normale del cavo orale è costituita da epitelio pavimentoso stratificato<br />
non cornificato,per cui appare di colore rosa e non bianco come quello della cute<br />
che è corneificato.E’tappezzato da ghiandole,dette ghiandole salivari minori,che in<br />
genere sono mucoidi.<br />
Principali patologie del cavo orale(andate a vedervele meglio):<br />
-anomalie di sviluppo,come la labioschisi,detta anche labbro leporino,che talvolta si<br />
associa a palatoschisi.<br />
-patologie infiammatorie,una volta rare,l’actinomicosi adesso per esempio è in<br />
aumento<br />
-le candidosi che in genere sono pediatriche a meno che non si associno ad altre<br />
patologie per cui si possono manifestare anche nell’adulto<br />
scaricato da www.sunhope.it
-le histoplasmosi<br />
-patologie virali<br />
-ulcerazioni linguali,come l’ulcerazione eosinofila,tipica dei giovani,che alcuni dicono<br />
sia legata allo stress.Ha una guarigione spontanea dopo qualche settimana<br />
-molto nota è la lingua a carta geografica,detta così perché presenta dei rilievi,delle<br />
depressioni,che è legata all’acantosi,alla presenza di microascessi e può essere<br />
dovuta a particolari abitudini alimentari,oppure al fumo di sigaretta o comunque ad<br />
altre situazioni irritative. Del cavo orale.<br />
-il mucocele è frequentissimo.Esso deriva dal fatto che le ghiandole di tipo mucoide<br />
presenti in tutto il cavo orale,per vari fenomeni,anche infiammatori banali,possono<br />
subire un processo di ostruzione dei dotti,per cui si formano cisti.Queste cisti<br />
appaiono rossastre e contengono muco e detriti.Possono comparire anche in seguito<br />
a patologia traumatica,es.un pugno,per cui a distanza di tempo,laddove si è avuto il<br />
trauma,si avrà un’ostruzione del dotto e comparirà il mucocele.Esso appare come<br />
una cisti contenete muco e queste cellule chiare qui,sono i macrofagi,che stanno lì<br />
per cercare di ripulire un po’ la zona dal muco in eccesso.<br />
-altre lesioni non neoplastiche sono le ulcere aftose,abbastanza frequenti nei giovani<br />
e dolorosa,perché sensibile al contatto con acidi,sale e altri tipi di sostanze.Si crea<br />
quasi un cratere a margini netti,ma fortunatamente guarisce per fatti suoi in pochi<br />
giorni.<br />
ALTRE LESIONI<br />
- ci possono essere delle iperplasie,a volte anche emilaterali,ad esempio c’è<br />
un’ipertrofia gengivale che colpisce metà lato per cause sconosciute.<br />
-amiloidosi<br />
-anche la sarcoidosi può colpire il cavo orale<br />
Quelle lesioni acantolitiche di cui abbiamo parlato quando abbiamo spiegato la<br />
cute,ovvero il pemfigo e pemfigoide,possono avere una presentazione clinica nelle<br />
mucose,es.vulvare o del cavo orale.Nel pemfigo volgare la bolla si forma<br />
caratteristicamente a livello soprabasale,si forma nello spessore dell’epitelio<br />
pavimentoso stratificato poco al di sopra dello strato basale,a differenza del pemfigo<br />
ide in cui la bolla è molto superficiale.<br />
scaricato da www.sunhope.it
-le leucoplachie sono un argomento di grande interesse perché sono frequentissime.<br />
-la cheratosi.Per cheratosi intendiamo un processo per cui la mucosa,che non è<br />
corneificata,diventa corneificata in qualche modo e assume un colorito<br />
biancastro.Vedete in questa foto la radice di questo molare,è evidente che qui per<br />
una particolare anomalia,si vede subito che questo dente batte su questa parte di<br />
mucosa e si formano lesioni a livello istologico dovute ad usura,ad attrito,per cui<br />
quell’epitelio che non doveva avere lo strato corneo,forma questo strato per<br />
difendersi.Le cellule staminali hanno quindi una loro logica,per cui se c’è un trauma<br />
intervengono,come nella cute.Da che cosa è caratterizzata a livello istologico?è<br />
caratterizzata da fenomeni di acantosi,cioè aumento dell’ispessimento<br />
dell’epitelio,anche iperacantosi,se c’è allungamento delle creste e poi si vede che<br />
comincia a comparire lo strato corneo,anche se c’è una paracheratosi,perché ci sono<br />
dei nuclei in queste cellule e non dovrebbero averlo.<br />
-Lichen:è una patologia tremendamente in aumento.Io ci credo che sia legata allo<br />
stress,perché non è rara tra gli studenti.E’una lesione bianca,ma non<br />
omogeneo,presenta una struttura quasi reticolare,irregolare(ci si può confondere<br />
con un carcinoma squamoso).Non c’è una macchia bianca continua,ha quasi una<br />
struttura quadrettata,filamentosa.La sua caratteristica è anche la sua oscillazione<br />
clinica,perché si va da periodi quasi di remissione a periodi di acuzie.Diciamo che è<br />
una patologia cronica ad eziologia incerta.E’una patologia dolorosa nei periodi più<br />
acuti,perché è molto sensibile ad agenti esterni fisici o chimici,come il freddo,il<br />
caldo,l’aceto.Ci sono poi periodi in cui la patologia si riduce,sembra quasi<br />
scomparire,per poi riprendersi in determinate circostanze.E’frequente e purtroppo<br />
difficile da togliere,anzi quasi mai si toglie,però si può contenere.Una caratteristica è<br />
la presenza di un infiltrato linfocitario a banda,ma la caratteristica essenziale,a parte<br />
la cheratosi,è che si formano quasi delle bolle,perché c’è una vacuolizzazione<br />
soprattutto negli strati basali e se questa vacuolizzazione va avanti si formano quasi<br />
delle fessure tra lo strato basale e il tessuto cutaneo sottostante e non si osserva più<br />
quel limite netto tra strato basale e connettivo sottostante.Questa situazione si<br />
chiama spongiosi,anche gli strati soprabasali iniziano a vacuolizzarsi,questo nella fase<br />
di acuzie.Per quanto riguarda l’etiologia,dal quadro morfologico potremmo pensare<br />
si tratti di una patologia immunitaria,alcuni pensano sia legata allo stress e per<br />
questo è una patologia in grande aumento.<br />
scaricato da www.sunhope.it
La parola leucoplachia significa “macchia bianca”.La macchia bianca,però,può<br />
associarsi anche a displasia nel cavo orale così come in altre sedi,ad esempio la<br />
cervice.In questo caso si parla di OIN(oral intra neoplation).Con OIN 1 si intende una<br />
displasia di grado lieve,è coinvolto lo strato basale.Nella OIN 2 vedete c’è cheratosi e<br />
in questo caso la paracheratosi.L’OIN 3 è assimilabile a Ca in situ,perché la patologia<br />
coinvolge l’intero spessore dell’epitelio.<br />
Una patologia particolare è la cheratosi verrucosa,ovvero una placca<br />
dura,rilevata,molto strana.Ha un aspetto verrucoso,ovvero una spiccata iperacantosi<br />
e acantosi e corneificazioni.Questa lesione non è tanto tranquilla,perché ha un<br />
potenziale evolutivo.<br />
Parlando di displasia,vediamo che in condizioni normali,la p53 la ritroviamo soltanto<br />
negli strati basali e parabasali,in un epitelio displastico,invece,la p53 la ritroviamo in<br />
tuttol’epitelio.Può sembrare paradossale,perché la p53 è oncosoppressore,ma essa<br />
si accumula solo quando è mutata,altrimenti viene metabolizzata facilmente.<br />
Quindi queste positività anacronistiche sono dovute a queste mutazioni che<br />
determinano l’accumulo di queste proteine,le quali possono coinvolgere anche i<br />
sistemi di degradazione,perché tutte le proteine del nostro organismo hanno<br />
un’emivita,un turnover e quando ci sono mutazioni le proteine si accumulano.Anche<br />
per il Ki67 si ritrova normalmente un’attività proliferativa negli strati basali e para<br />
basali,mentre in una displasia si trova un po’ ovunque.Sono aumentate queste<br />
positività,perché è aumentata l’attività proliferativa e troviamo anche un’irregolare<br />
distribuzione di queste positività<br />
-il cavo orale è anche una sede preferenziale della coilocitosi,che già abbiamo<br />
trattato nella cervice.Qui vedete i classici coilociti,c’è anche una cheratosi,cioè una<br />
leucoplachia,che è legata alla coilocitosi e quindi al papilloma virus.ddirittura si<br />
possono avere proprio casi di papilloma squamoso.Vi ricordo che qui ci sono dei<br />
ceppi di PV soprattutto il 2,4,6,11,13 che danno queste lesioni coilocitiche piatte o<br />
papillari.Qui il PV nella cancerogenesi del cavo orale è coinvolto,ma non come nella<br />
cervice,ma misura minore.<br />
Riassiumiamo:Quali sono le leucoplachie?<br />
-CHERATOSI<br />
-LICHEN<br />
scaricato da www.sunhope.it
-LESIONI COILOCITICHE (DA PV)<br />
-LEUCOPLACHIA con displasia ED ERITROLEUCOPLACHIA,termine che usano i<br />
clinici,ma che per noiha scarso significato e usata quando questa placca bianca<br />
assume anche delle tonalità di rosso per aumento della vascolarizzazione.<br />
-CHERATOSI VERRUCOSA caratterizzata da una forte attività proliferativa<br />
-CARCINOMA SQUAMOSO(INVASIVO) che spesso appare come una macchia<br />
bianca.L’OIN 3,cioè la displasia grave,può evolvere in un carcinoma invasivo nel 4-30<br />
% dei casi<br />
PROGNOSI E SEDE DEL Ca orale<br />
Il carcinoma del cavo orale viene quasi sempre ad osservazione in fase molto<br />
avanzata e questo è paradossale,essendo una sede abbastanza accessibile,per<br />
ignoranza soprattutto.La sede condiziona la prognosi in una maniera determinante<br />
per ragioni di anatomia topografica.<br />
SEDE e FOLLOW UP A 5 ANNI<br />
-il labbro inferiore a prescindere dagli istotipi,dallo stadio ha un follow-up del<br />
90%,mentre il labbro superiore del 40 %,forse perché il labbro superiore aderisce più<br />
strettamente ai piani sottostanti per cui tende ad infiltrare precocemente le ossa<br />
mascellari,mentre quello inferiore è più mobile e tende a sporgere fuori.<br />
-parte anteriore lingua(60 %)<br />
-labbro superiore,gengiva,palato duro,parte posteriore lingua,gengiva,<br />
tonsilla(40 %).La parte posteriore della lingua per i suoi rapporti con l’ipofaringe e<br />
del faringe attraverso vasi sanguigni,linfatici subito dà infiltrazione.<br />
-la sede peggiore è il palato molle(soprattutto zona sublinguale,perché ha una<br />
particolare struttura istologica;essendo il tappeto su cui poggia la lingua,ha una<br />
struttura molto soffice,un connettivo molto lasso,ricchissimo di vasi linfatici e poi è<br />
anche la sede meno esposta,per cui il cancro tende ad infiltrare precocemente e a<br />
dare metastasi) :follow up a 5 aa del 20-30 %<br />
PRINCIPALI ISTOTIPI DEL CARCINOMA ORALE,CANCRI Più FREQUENTI:<br />
scaricato da www.sunhope.it
-Ca squamoso suddiviso in G1,G2 e G3.C’è una varietà del Ca squamoso che è il Ca<br />
verrucoso,che da alcuni è considerato a parte,come se non rientrasse nel Ca<br />
squamoso,che è un cancro così differenziato che produce un sacco di cheratina e a<br />
volte diventa difficile fare la diagnosi tra Ca squamoso,Ca verrucoso e una verruca.<br />
-adenosquamoso,cancro con struttura ghiandolare e squamoide<br />
-basaloide<br />
-Ca sarcomatoide(a cellule fusate):è sempre un Ca squamoso,però lecellule sono più<br />
indifferenziate e le cellule assumono un aspetto più a sarcoma, sono fusate come se<br />
fosse un sarcoma<br />
-Ca linfoepiteliale<br />
-Tumori ghiandole salivari minori,che tappezzano tutta la cavità orale a differenza<br />
delle maggiori che sono la parotide,la sottomandibolare e la sottolinguale.<br />
scaricato da www.sunhope.it
Sbobinatura Cavo Orale<br />
CISTI MUCOIDE<br />
Caratteristiche:si presenta all’esame istologico molto grande , non ha una spiegazione plausibile<br />
attualmente perché risiedono numerose ghiandole mucoidi.Si pensa che tutto ciò sia dovuto a<br />
dislocazioni di natura genetica e tessutale o ancora problemi di natura staminale localizzate in sedi<br />
anomali.<br />
CARCINOMA SQAMOSO<br />
Si presenta blando nell’anziano talvolta insorge mostrando in più parti aree di “follicocitosi”, spesso<br />
lo si associa al Papilloma Virus.<br />
Se prendiamo come esempio un paziente anziano in cui è stato diagnosticato un Cancro Pernicioso ,<br />
noteremo che esso appare ben differenziato con aree ricche di cheratina(infatti vedi immagine essa è<br />
ricca di parti biancastre).Esso pur avendo al sua sede a livello germinale e alveolare si estende ai<br />
tessuti sottolinguali arrivando a confinare con l’esterno in fasi molto avanzate.Essendo<br />
caratterizzato da un epitelio pavimentoso stratificato la diagnosi risulta molto difficile.Proseguendo<br />
la nostra analisi introduciamo il Carcinoma a Cellule Basali o anche detto Basaloide , la<br />
principale caratteristica è la presenza di cellule povere di citoplasma che non tendono a disporsi a<br />
baza no “balzatura” è molto invasivo e non ha nulla a che vedere con il “Carcinoma Basocellulare “<br />
che può essere definito un Carcinoma di serie B che non da fenomeni di metastasi.<br />
Diagnosi tumorale:<br />
Stadi azione<br />
Si effettua sempre e tiene conto di tali parametri:<br />
La sede anatomia ad esempio il cavo orale il quale risulta una regione anatomica molto eterogenea<br />
Classificazione :<br />
T1 inferiore a 1cm<br />
T2 tra 2 e 4cm<br />
T3 oltre i 4cm<br />
T4 invasione di organi e strutture adiacenti ex:invasione di un osso<br />
Classificazione linfonodi:<br />
n1 uso linfonodo (lato cervicale)ghiandole inferiori a 3cm<br />
n2ghiandole con dimensioni tra 3 e 6 cm a sua volta si suddividono in 2con A e 2con B<br />
2° A quando è presente un solo linfonodo<br />
2 B quando sono presenti più linfonodi nel quale almeno uno presenta un diametro di 3 6 cm<br />
Ancora ricordiamo che T1 collo alto con 5 anni di sopravvivenza<br />
T4 sopravvivenza 25 32%<br />
Le due alterazioni molecolari sono la P16 e la p53<br />
Riassumendo un identikit di Cancro del Cavo Orale tiene conto di tali parametri diagnostici<br />
Sede Anatomica<br />
Stadiazione<br />
Over Espression P53 mutata<br />
Aumento dell’attività proliferativa misurata attraverso la KI67<br />
Terapia<br />
La Chirurgia è la soluzione del problema.Ma si deve tener conto che un cancro in fase avanzata<br />
come ad esempio quello che coinvolge la parte posteriore della lingua(contro laterale) risulta<br />
impraticabile in tale sede oppure anche se ci fosse risulterebbe controproducente.<br />
Valutazione del Campo<br />
Se si esamina un cavo orale che manifesta lesione neoplastica siccome il cavo orale è una regione<br />
anatomica a cielo aperto quindi è un organo aperto che presenta aree di multiplicità e dipalstiche il<br />
chirurgo deve valutare l’intero cavo orale e osservare un fenomeno chiamato “Cancerogenesi di<br />
scaricato da www.sunhope.it
Campo” .Oggi la terapia più efficace risulta la Radioterapia .Infatti in pazienti con forme avanzate<br />
di campo o in sedi non favorevoli per interventi chirurgici l’arma più idonea risulta la Radioterapia<br />
.Essa agisce su quei campi che hanno una certa attività proliferativa .In linea di massima un Cancro<br />
che risponde bene avrà un valore di KI67 positivo in almeno il 20%cellule .La Radioterapia agisce<br />
sulle cellule in fase cellulare di proliferazione.<br />
Per ultimo abbiamo la Chemioterapia che la si attua quando le armi principali quali Radioterapia e<br />
Chirurgia non possono essere utilizzate.<br />
Sguardo ad alcuni tumori<br />
Tumori in sede dentaria:odontogenici sono quelli che formano le strutture del dente quali cemnto e<br />
smalto<br />
Tumori vascolari:sono caratteristici del cavo orale<br />
Tumori muscolari striati<br />
Tumori neuro ectodermici: Schwannoma che colpisce i nervi periferici<br />
Epulide:Escrescenze gengivali di natura infiammatoria .Patologia diffusa nei cani , banale<br />
nell’uomo.<br />
Tumore a Abrikossoff<br />
Tale tumore che prende il nome dal suo scopritore no è raro è caratterizzato da cellule a granulosa<br />
.In passato si pensava al Mio blastoma in quanto tumore muscolare oggi invece si sa che esso è un<br />
tumore neuro ectodermico .Le cellule che hanno delle granulazioni imparentato con lo<br />
Schwannoma , insorge nel connettivo sottoepiteliale del cavo orale .Per motivi sconosciuti induce<br />
nell’epitelio sovrastante delle alterazioni strutturali così gravi da far pensare che sia un Carcinoma<br />
Squamoso cosa che non è .<br />
Lesione che erroneamente viene chiamata Granuloma Piogenico:caratterizzata da una lesione<br />
riccamente vascolarizzata la cui principale sede anatomica è il cavo orale, che perifericamente<br />
presenta “necrosi ascessuali”.Si è scoperto con il tempo che essa non è affatto una lesione Piogenica<br />
ma un “Angioma” .Per la sua crescita abbastanza rapida si chiama Angioma Lobulare in quanto<br />
fatto di numerosi spicchi lobuli appunto. sso cresce in periferia mostrando aree di necrosi come già<br />
detto in precedenza e compaiono caratteristici granulociti. l termini esatto è quindi “Angioma<br />
Capillare Lobulare” e molto spesso compare nei testi con il nome di Granuloma Piogenico.In uno<br />
stadio più avanti della lesione esso passa sotto il nome di “Angioma Sclerosante”.Tutte queste<br />
terminologie riconducono a diversi stadi di una stessa patologia che è un particolarissimo<br />
“Angioma”.<br />
La Recidva del Cavo Orale<br />
Cancerogenesi da Campo :possiamo avere due tipi di cancro diversi con caratteristiche molecolari<br />
diverse, displasie , carcinoma in situ , recidive tecniche no biologiche , neurometastasi.<br />
Possiamo osservare P53 mutata , il fenomeno dell’Over espression legata alla<br />
mutazione.Esempio:se prendiamo una mucosa apparentemente normale il caso della gengiva<br />
troveremo un aumento della p53 che ci spiega questa Cancerogenesi da Campo.<br />
Passiamo ora alle epulide<br />
Epulide:Escrescenze di natura gengivale che possono raggiungere notevoli dimensioni .<br />
Epulidi caratteristiche della gravidanza sono ricche di plasmacellule .In gravidanza esse subiscono<br />
fenomeni iperplastici (un accelerazione del fenomeno)<br />
Giganto cellulari:lesioni benigne costituite da cellule giganti.Esse rappresentano la principale causa<br />
di dolore dopo l’esatrazioen di un dente.<br />
Cisti OdontogenaSi chiama così perché è associata ad un dente chiuso no completamente formato<br />
nel quale si crea una cavità dove c’è la mancata irruzione del dente (dente del giudizio)<br />
Presenta un epitelio pavimentoso stratificato che mostra cellule mucipare.<br />
Omeoblasti<br />
Parliamo di omeoblasti a proposito di abbozzo dentario.Esse sono cellule deputate a formare lo<br />
smalto e può capitare che queste cellule diano luogo ad un Ameloblastoma .L’abbozzo dentario<br />
scaricato da www.sunhope.it
scava infatti la sua nicchia nell’osso e anche l’ameloblastoma presenta questa pecularietà .Spesso<br />
appare coinvolgendo alcuni tratti quali mandibola , mascella.Questo tumore tende ad infiltrarsi nei<br />
canali di “AVERS”(vedi libro).Tumore che insorge in età giovali adulta 30 45 anni presenta queta<br />
caratteristica infiltrante e il suo modo di crescita ha questi aspetti.<br />
In periferia ha la tendenza ad un epitelio che si dispone a balze progressivamente andando verso il<br />
centro compare un edema.Questa zona è riccamente vacualizzata che si ingrandisce formando una<br />
cisti.Queste cellule per i loro prolungamenti a stella che tendono a vacualizzare formano un reticolo<br />
stellato.<br />
Analizziamo la Lesione Displastica Fibrosa può comparire in maniera monostatica o polistatica.<br />
E’ caratterizzata da un area di rarefazione dell’osso (osteolisi).Dove al posto dell’osso si sostituisce<br />
tessuto fibroso .Come si forma l’osso?attorno all’osso compare un orletto osteobalstico .Quest’osso<br />
si forma per metastasi e presenta una forma che ricorda i “caratteri cinesi”.<br />
Ghiandole salivari:<br />
Tralasciando la parte anatomica esse si dividono in Ghiandole salivari maggiori e minori.<br />
La Parotide che ritroviamo nella regione preauriculare in una zona molto innervata per il chirurgo<br />
risulta un problema in quanto essa prende contatto con il nervo facciale e quindi dovrà far<br />
attenzione alla sede precisa.<br />
E’ molto grande è prettamente di tipo sieroso.<br />
Ghiandola sottomandibolare:Ghiandola mista secrezioni:mucoide e sierosa.La secrezione mucoide<br />
presenta un citoplasma bianco debolmente bsofilo, mentre quella sierosa il citoplasma è acidofilo.<br />
Ghiandola sottolinguale :ghiandola mista con secrezione prevalentemente mucoide.<br />
Ghiandole sottolinguali minori:Esse costellano tutto il cavo orale e presentano acini mucoidi.<br />
In una sezione istologica della parotide notiamo:Molti dotti che si dividono in dotti grandi (striati)e<br />
piccoli(intercalati)che entrano in contatto con gli acini. li acini rappresentano le unità funzionali<br />
secernenti ghiandolari. Se andiamo a fare una caratterizzazione oltre alle cellule salivari che<br />
secernono saliva nelle sue parti mucoidi e sierose. ’acino ghiandolare (parte terminale albero<br />
ghiandolare)è caratterizzato da cellule mio epiteliali che hanno la funzione di contrarsi e in tal modo<br />
favoriscono al fuoriuscita del contenuto .<br />
I dotti intercalat striati non sono cellule mioepieteliali ma cellule basali<br />
Cellule mio epiteliali :positive al p53<br />
Cellule basali poste negli interstizi cellule cilindriche e rivestono i dotti : cirocheratina<br />
Patologie caratteristiche<br />
Enteropatie salivari,pseudo stoma.<br />
Cisti alle Ghiandole Salivari:<br />
Le possiamo suddividere in tre tipi:<br />
Linfoepiteliali:Follicoli linfocitari di tipo secondario<br />
Epitelio di rivestimento<br />
Cisti Bronchiali:in analogia con i pesci sono di origine embrionale.<br />
Cisti Epidermoidi:Ep Pavimentoso Stratificato Sede classica sono le ovaie.<br />
Incidenza dei tumori in generale:<br />
Parotide quasi due terzi<br />
Sottolinguale sono rari<br />
20 30% salivari minori<br />
Incidenza tumori maligni:<br />
BASSA:Parotide<br />
Alta:Salivari minori<br />
Principali Tumori epiteliali benigni:<br />
scaricato da www.sunhope.it
Adenoma Pleumorfo:Ghiandola mista salivare da solo rappresenta il 50 60% di tumore<br />
maligno.Presenta aspetti mucosi.In passato si pensava fosse un tumore misto in quanto<br />
caratterizzato da una componente mesenchimale e una epiteliale.<br />
Adenolinfoma:Ancora non si sa se sia un tumore o una malformazione<br />
Adenoma Cellulo Basale<br />
Luigi Romano<br />
scaricato da www.sunhope.it
Riepiloghiamo l’adenoma pleomorfo.E’ un tumore frequentissimo ed estremamente eterogeneo.Tutto<br />
comincia dalla cellula staminale che può formare sia cellule mioepiteliali a fenotipo mesenchimale sia<br />
elementi epiteliali,percorrendo 2 linee di differenziamento. Dal punto di vista epiteliale possono formarsi<br />
trabecole,tubuli,mucoidi o sierosi.Lo stesso vale per le cellule mesenchimali:+ tipico è il fenotipo mixoide<br />
ricco di sostanza fondamentale in cui sono disperse poche cellule,assumendo aspetti simili al mesenchima<br />
embrionario.Tali adenomi possono dare dubbi diagnostici soprattutto a livello radiologico. La parotide è a<br />
contatto con i condili mandibolari.La formazione di natura mesenchimale può simulare una lesione ossea o<br />
cartilaginea.Anatomopatologicamente la lesione si presenta eterogenea nelle sue parti e questo può<br />
renderne difficile l’interpretazione.Da non sottovalutare poi il pericolo di carcinoma in adenoma<br />
pleomorfo,non frequentissima perché per definizione l’adenoma è benigno. Tende alla recidiva,non di<br />
natura biologica bensì operatore dipendente.Le varie casistiche riportano dati discordanti riguardanti<br />
l’incidenza di recidiva e ciò è strettamente correlato alla conoscenza da parte del chirurgo di questa<br />
patologia.E’ buona norma infatti asportare lungo il perimetro dell’adenoma una piccola porzione di tessuto<br />
sano per evitare recidive.A proposito dei margini devono essere bene esaminati. In caso di dubbio<br />
diagnostico,è necessario indagare l’espressione di p53,aumentata in caso di carcinoma.<br />
Adenolinfoma è termine impropio per definire questa entità(non si sa se è tumore o meno).Tende alla<br />
multicentricità,è tipico dell’età anziana dall’aspetto orange.In tal caso c’è una tendenza alla recidiva non<br />
tecnica ma biologica,data la multicentricità.Si pensa non sia un tumore per la struttura caotica e<br />
strana.Nonostante ciò mantiene la denominazione(anzi prima era detto cistoadenolinfoma per la presenza<br />
di cisti nel suo contesto).Oltre alle cisti si riscontrano aggregati linfoidi talora con centri germinativi con<br />
doppio strato epitelilale molto eosinofilo.Non sempre si coglie il doppio strato,addirittura può sembrare<br />
triplo per la particolare disposizione dei nuclei.Le cellule epiteliali sono cellule oncocitarie o ossifile cn il<br />
nucleolo acidofilo(sherry red dal liquore sherry).Non si tratta di un linfoma.<br />
Adenoma a cellule basali monomorfo.La noxa ha agito più tardivamente sulla staminale già parzialmente<br />
commissionata.E’ un tumore benigno in cui le cellule di aspetto basalioide tendono a disporsi a palizzata.<br />
Adenoma oncocitario.Tipico dell’età adulta avanzata.Esiste anche la variante ossifila.Questo può indurre<br />
dubbio diagnostico.Le cellule appaiono con granulazioni eosinofile.Al microscopio elettronico i mitoncri<br />
sono grossi e sferici.Se usiamo anticorpi anti mitocondri appaiono le tipiche granulazioni.Probabilmente si<br />
tratta di un adenoma monomorfo con esaurimento cellulare.<br />
Mioepitelioma a differenza degli altri è costituito esclusivamente da cellule mioepiteliali e presenta un<br />
aspetto solido. Le cellule mioepiteliali che lo compongono appaiono piccole e cubiche.<br />
All’immunoistochimica esprime actina,vimentina,citocheratina tipico delle cellule mio epiteliali,che<br />
presentano questo fenotipo a metà strada tra le cellule epiteliali e quelle mesenchimali.<br />
Tumori maligni.Conclusi i tumori benigni,ecco una sintesi estrema riguardante i tumori maligni.Anche se<br />
non è più usata preferisco classificarli in tumori ad alto grado e tumori a basso grado.Quelli di basso<br />
grado,tendenti alla recidiva ma non alle metastasi sono il carcinoma adenoideo cistico,il carcinoma muco<br />
epidermoide e il carcinoma a cellule aciniche chee ricorda gli acini cioè la struttura terminale delle<br />
ghiandole salivari.Gli altri e cioè il carcinoma epiteliale e mio epiteliale,carcinoma a cellule ossifile e il<br />
tumore maligno misto corrispettivo maligno dell’adenoma pleomorfo che può nascere d’emblee oppure<br />
secondario ad adenoma pleomorfo sono considerati ad alto grado di malignità. Altri tumori sono i tumori a<br />
cellule chiare e i tumori mammari in ghiandole salivari così come nella mammella ci possono essere tumori<br />
salivari.<br />
scaricato da www.sunhope.it
CA Adenoideo cistico.Colpisce prevalentemente la ghiandola sottolinguale e tende all’ulcerazione.Non dà<br />
frequentemente metastasi a distanza che nella maggior parte dei casi colpiscono il polmone e presenta<br />
una originalità biologica consistente nel fatto che segue i perinevri cioè le guaine nervose nel processo<br />
invasivo(la ragione di questo comportamento,tipica solo di altri pochi tumori non è stata ancora<br />
spiegata).Iperesprime p53.Oltre alla forma classica esistono altre forme istologiche. Morfologicamente<br />
l’aspetto classico appare cribroso simulante una formazione ghiandolare;in realtà si tratta di cellule mio<br />
epiteliali con capacità di dare origine a secrezioni mucoidi o sierose che si raggruppano al centro<br />
comprimendo l’ epitelio conferendo un aspetto a canne d’organo.Positivo per actina e p53.<br />
CA muco epidermoide. In questo caso ci troviamo di fronte alla coesistenza di gettoni squamosi e<br />
ghiandole che formano muco da cui la denominazione.Esistono due sottotipi :uno ad alto e l’altro a basso<br />
grado di malignità.La distinzione è effettuta a seconda delle atipie citologiche. Il Ca di alto grado dà<br />
metastasi nel 10% dei casi.<br />
CA a cellule acinike Presenta cellule piccole che ricordano l’acino delle ghiandole salivari.E’ localmente<br />
aggressivo anche se a ridotto potenziale di malignità.<br />
CA in adenoma pleomorfo.Esistono varie possibilità.Prima di tutto dobbiamo ricordare il carcinoma in<br />
situ. E’ anche detto adenoma atipico per il numero maggiore di atipie citologiche ma non ha caratteristiche<br />
di invasività.Per questo potremmo considerarlo una forma borderline.Segue il Ca intracapsulare,non molto<br />
maligno.Infine ricordiamo il ca microinvasivo e francamente invasivo,richiamando la classificazione<br />
dell’adenoma follicolare tiroideo.Nel primo caso il ca non va oltre i 5 mm dalla capsula,nel secondo caso<br />
supera i 5mm.In realtà la valutazione della capsula può trarci in inganno;fenomeni di necrosi e fibrosi<br />
possono originare una falsa capsula più interna rispetto a quella vera e dare l’impressione di superamento<br />
ed invasività.A tal proposito ricordiamo che dobbiamo riferirci alla presenza di emboli neoplastici a livello<br />
vasale per renderci conto dell’invasione vera e propria.<br />
CA epiteliale-mio epiteliale Non si discosta dal prototipo e dalla struttura della ghiandola salivare<br />
normale.Presenta una struttura bistratificata o bistrutturata.In periferia troviamo cellule chiare mio<br />
epiteliali, al centro epiteliali carcinomatose. All’immunoistochimica troviamo citocheratina centrale,actina<br />
periferica,coerentemente con la distribuzione cellulare.<br />
CA ossifilo caratterizzato da cellule con nucleolo sherry red.Invasivo.<br />
CA polimorfo di basso grado vari tipi di architettura per esempio trabecole o tubuli. Insorge nelle ghiandole<br />
salivari minori,esprime la galectina 3 come il ca capillifero della tiroide e presenta una buona prognosi.<br />
CA duttale somiglia alla nos della mammella. Molto aggressivo dà metastasi nel 70% dei casi.E’ costituito<br />
da tubuli o trabecole con stroma fibroso abbondante.<br />
Storia naturale dei tumori maligni<br />
Il Ca in adenoma pleomorfo presenta il comportamento più maligno con zero sopravvissuti a 20 anni dalla<br />
diagnosi. Gli altri ed in particolare il mucoepidermide,a cellule aciniche e l’adeoideo cistico presentano una<br />
prognosi migliore<br />
La Stadiazione TNM ricalca quella del cavo orale.<br />
T1 diametro inf ai 2cm<br />
scaricato da www.sunhope.it
T2 diametro compreso tra 2 e 4 cm<br />
T3 magg 4 cm con o senza estensione ghiandolare????si considera T3 un tumore con diametro inferiore ai 4<br />
cm che però superi i limiti capsulari.<br />
T4 organi adiacenti.<br />
N1 omolat N2 omolat max 6 cm<br />
N3 magg 6 cm<br />
Fattori prognostici:istotipo, sede(sottomandibolare e palato molle aggressivi,palato molle meno aggressivi)<br />
stadi azione, grading, ploidia, p53, c-erb-B2( valore sperimentale).<br />
Nella diagnostica un ruolo importante è svolto dalla citologia aspirativa.L’inconveniente di fronte al quale ci<br />
possiamo trovare consiste nei falsi negativi per la presenza di tessuto solido,di tipo osseo o cartilagineo.Si<br />
presta meglio la biopsia escissionale.Infine sempre in ambito diagnostico è possibile effettuare esami<br />
estemporanei multipli per la visione dei margini.Questo permetterà al chirurgo di estendere la zona di<br />
escissione,se necessario e allo stesso tempo di effettuare interventi conservativi soprattutto nei soggetti<br />
giovani. La chirurgia è molto importante ai fini terapeutici.Per quanto riguarda la parotide è possibile<br />
effettuare una parotidectocmia totale o parziale,ed eventualmente linfadenectomia.Per i casi inoperabili si<br />
usa la radioterapia.<br />
I Tumori non epiteliali più frequenti sono linfomi Non Hodgkin(a grandi cellule B , follicolare, MALT) ;<br />
sarcomi;tumori muscolari ;tumori fibroadiposi tipo lipomi o liposarcomi.<br />
ESOFAGO<br />
Le patologie esofagee sono in rapida ascesa per l’incidenza.come sempre partiamo dall’istologia.La parete<br />
esofagea presenta una struttura complessa:un epitelio pavimentoso stratificat, membrana basale,lamina<br />
propria( costituita da connetivo lasso ed elastico che garantisca movimento),muscolaris mucosae(piccolo<br />
strato di tessuto muscolare anch’esso importante per la mobilità),sottomucosa, tonaca muscolare(con<br />
strato circolare interno e longitudinale esterno per favorire la peristalsi),sierosa con connettivo lasso e<br />
adipe.Molto ricco di lifatici tributari del dotto toracico che si trovano a livello di lamina propria e<br />
sottomucosa,responsabili della meta statizzazione linfatica precoce del cancro esofageo.Ha una lunghezza<br />
media di 25 cm con variabilità in base al soggetto.Nella sottomucosa ritroviamo ghiandole mucoidi<br />
soprattutto nel terzo inferiore.Molto importanti per la mobilità sono i plessi sottomucoso meisnerr e<br />
auerbach costituiti da fibre nervose e cellule gangliari,generanti un gradiente pressorio.Alcune patologie<br />
sono dovute al fatto che mancano questi plessi.Talvolta nella sottomucosa troviamo i melanociti, ciò è<br />
abbastanza fisiologico. Questo spiega per quale motivo si formino melanomi anche a livello esofageo. Nella<br />
sottomucosa si ritrovano anche cellule neuroendocrine.Anche a livello esofageo si ritrovano cellule<br />
staminali più precisamente nelle rientranze dell’epitelio a contatto con lo stroma richieste:è un punto<br />
strategico dove possono differenziarsi in ambedue le linee cellulari a seconda delle esigenze.Altra<br />
particolarità dell’esofago è rappresentata dal fatto che le cellule basali non sono mono ma<br />
pluristratificate(2-3 strati)per consentire adatta proliferazione. La patologia da reflusso è in aumento<br />
nonostante numerosi casi rimangano misconosciuti.<br />
Inserzione del diaframma a livello dell’esofago terminale e lo sfintere si posiziona al di sotto e risente della<br />
tensione diaframmatica.Il tono è aumentato dalla contrazione delle fibre diaframmatiche.La pressione a<br />
scaricato da www.sunhope.it
livello dello sfintere 10-30 mmHg superiore a quella dello stomaco. Un altro meccanismo che garantisce la<br />
continenza dello sfintere è l’angolo acuto di his. La linea zeta rappresenta la giunzione tra epitelio esofageo<br />
e gastrico e presenta un decorso a zig zag.Fino a 2 cm superiormente la giunzione è possibile ritrovare<br />
epitelio gastrico:ciò correla con l’evento del reflusso fisiologico post prandiale,quando decade la pressione<br />
dello sfintere inferiore.<br />
Principali anomalie congenite e non.<br />
Atresia e anomalie correlate cn fistolizzazione o meno incompatibili cn la vita.(il prof ha detto di dare uno<br />
sguardo dal libro).<br />
Eterotopia pancreatica e gastica distante dalla giunzione più di 2 cm.<br />
Diverticoli esofagei che possono essere da pulsione per aumento di pressione o da trazione per la<br />
formazione di aderenze(mediastinite,tumore).E’ necessario distinguere i diverticoli veri dai pseudo<br />
diverticoli:è vero quando tutta la parete forma una sacca,è uno pseudo diverticolo quando si arresta alla<br />
parete muscolare.Gli pseudo diverticoli sono comunque particolarmente dolorosi per fenomeni di stasi e<br />
disturbano la peristalsi.Si possono distinguere usando una particolare colorazione che colora i muscoli in<br />
giallo(il prof non ha menzionato il nome di questa colorazione).<br />
Diverticolo di zenker.Tipico dell’età avanzata caratterizzato da uno slittamento delle 2 pareti a livello della<br />
giunzione faringoesofagea.L’esofago si posiziona davanti e al di sopra del faringe non consentendo la<br />
normale peristalsi.<br />
Acalasia.Stessa patogenesi del megaretto.E’ una malattia dei plessi.Macroscopicamente si nota un punto di<br />
stenosi che è funzionale per mancanza delle cellule gangliari dei plessi gangliari con alterazione della<br />
coordinazione della peristalsi e alterazione del gradiente pressorio.Tale stenosi funzionale determina per<br />
compenso una dilatazione ed ipertrofia del segmento normale a monte. Questi due tratti sono divisi da un<br />
segmento di transizionein cui le cellule gangliari sono diminuite ma non mancano completamente. E’ una<br />
patologia dell’età pediatrica, responsabile di un cospicuo numero di polmoniti ab ingestis.<br />
Altre patologie.Diabete,sclerodermia,amiloidosi.<br />
Esofagite da reflusso<br />
Nel nostro organismo esistono varie barriere che si oppongono al reflusso: la pressione dello sfintere<br />
inferiore potenziata dal diaframma,angolo di his,forza di gravità,peristalsi esofagea,presenza di ghiandole<br />
mucipare dell’esofago terminale che producono bicarbonati con neutralizzazione acida.L’esposizione a<br />
molto acido per qualche ora si può considerare parafisiologica perché dopo i pasti c’è un rilasciamento<br />
dello sfintere soprattutto dopo i pasti abbondanti.L’esofagite da reflusso può verificarsi per varie cause.<br />
Per esempio un’ernia iatale che si insinua nel foro diaframmatico dimunuendone la tensione,alcuni cibi<br />
fumo e caffè ,alcuni farmaci. Un’altro dei fattori di rischio soprattutto dei paesi occidentali è l’obesità e<br />
favorisce l’insorgenza di reflusso più nei maschi che nelle femmine per la distribuzione del<br />
grasso:addominale con conformazione a mela nel maschio,sottocutaneo con conformazione a pera nella<br />
femmin a per ragioni costituzionali.E’ possibile anche che manchi la secrezione di bicarbonato da parte<br />
delle ghiandole del terzo inferiore dell’esofago. Il 2-7% della popolazione soffre di reflusso ma solo la metà<br />
va incontro ad esofagite da reflusso.Macroscopicamente nella esofagite la linea zeta si presenta risalita e si<br />
vedono delle creste mucosali a cui corrisponde microscopicamente un quadro peculiare caratterizzato da:<br />
invaginazione del connettivo,papillomatosi ed acantosi,iperplasia delle cellule basali x irrobustire<br />
scaricato da www.sunhope.it
l’epitelio,componente infiammatoria, edema interstiziale e intracellulare con vacuolizzazione<br />
cellulare,cheratosi,erosione,ulcerazione.<br />
Grading:lesione eritematosa,erosione lineare della paret,erosione circ confluente, esofago di barrett.<br />
scaricato da www.sunhope.it
Lezione del 28-04-2011 prof.Rossiello<br />
Argomenti trattati: esofagite da reflusso,esofago di Barrett, tumori benigni e<br />
maligni dell’esofago.<br />
Esofagite da reflusso<br />
Gli aspetti istologici che caratterizzano questa patologia sono facilmente<br />
intuibili.L’epitelio pavimentoso stratificato sottoposto a questa<br />
aggressione chimica va in contro a:<br />
• ACANTOSI: l’epitelio si ipertrofizza;c’è un’iperplasia perchè cerca di<br />
compensare anche attraverso lo spessore a questa aggressione<br />
chimica<br />
• IPERPLASIA DELLE CELLULE BASALI: normalmente le cellule basali<br />
occupano un unico strato,a seguito dell’insulto acido vanno ad<br />
organizzarsi in più strati<br />
• PAPILLOMATOSI: è l’altra faccia dell’iperacantosi. Normalmente<br />
nell’esofago non ci sono creste e papille evidenti,vedete come la<br />
linea che definisce l’epitelio rispetto alla sottomucosa è abbastanza<br />
regolare. L’epitelio,sottoposto a insulto chimico, fa delle creste e il<br />
connettivo interfacciandosi con esse forma delle digitazioni. Se<br />
valutiamo questo aspetto focalizzandoci sulle creste dell’epitelio<br />
parliamo di iperacantosi, se invece valutiamo l’aspetto del<br />
connettivo sottomucoso parliamo di papillomatosi<br />
• INFILTRATO INFIAMMATORIO:a livello sia intraepiteliali,sia<br />
sottoepiteliale abbiamo cellule infiammatorie che possono essere<br />
rappresentate da granulociti eosinofili( più caratteristici ),ma anche<br />
granulociti neutrofili e linfociti;<br />
L’epitelio manifesta anche alterazioni citologiche come:<br />
1. SPONGIOSI:<br />
scaricato da www.sunhope.it<br />
ovvero la vacuolizzazione o edema intracellulare
2. EDEMA EXTRACELLULARE<br />
Nell’evoluzione questo ci dà:<br />
-erosioni;<br />
-aree di ulcerazione:in casi estremi,laddove c’è ulcerazione evidente ci<br />
possono essere:<br />
-fenomeni di fibrosi: laddove c’è fibrosi,c’è retrazione e stenosi con<br />
deformazione del calibro.<br />
Dal punto di vista endoscopico si distinguono diversi gradi:<br />
• Lesione eritematosa:aspetto rossastro per l’infiammazione;<br />
• Lesione lineare: si evidenzia un tratto o una linea fessuriforme<br />
superficiale;<br />
• Lesione circolare: coinvolge circolarmente tutta la parete.<br />
Da queste lesioni si può avere poi l’evoluzione verso l’ESOFAGO DI<br />
BARRET,che implica una metaplasia;l’epitelio squamoso a causa di questi<br />
continui insulti acidi “si scoccia” e dice:”qui l’epitelio squamoso non va<br />
bene”!<br />
Ricordate il concetto delle cellule staminali,le quali cominciano ad avere<br />
delle segnalazioni dall’ambiente esterno acido e incominciano a pensare<br />
di stare in un’altro organo. Quindi alla base c’è un segnale improprio.<br />
IMMAGINE: iperacantosi-papillomatosi: l’epitelio è generalmante<br />
piatto,invece in questa immagine vedete queste lingue di tessuto<br />
connettivo che si portano all’esterno e le creste epiteliali che si spingono<br />
verso l’interno.<br />
IMMAGINE: vedete qui l’edema intra- ed extracellulare.Queste cellule<br />
ricordano vagamente una coilocitosi,ma non è una coilocitosi,piuttosto<br />
una vacuolizzazione all’interno delle cellule.Si colgono bene anche le<br />
scaricato da www.sunhope.it
distanze tra cellula e cellula, il che vuo dire che c’è edema extracellulare.<br />
Sembrano quasi delle fessure tra cellula e cellula.<br />
IMMAGINE: (sezione trasversale dell’epitelio iperacantosicopapillomatoso)si<br />
possono apprezzare come dei noduli di connettivo<br />
nell’epitelio. Inoltre si vedono nell’epitelio granulociti e linfociti,che<br />
arrivano fin all’interno dell’epitelio,ma si trovano anche al di sotto. Più<br />
caratteristico è trovarli nell’epitelio a testimoniare che lì c’è l’aggressione.<br />
Si può vedere che c’è un’iperplasia delle cellule basali,che in un epitelio<br />
normale si organizzano in un unico strato,mentre qui si organizzano in 3-4<br />
strati. Sono piccole cellule che derivano dalle cellule basali (cioè<br />
staminali); per avere la conferma facciamo i markers per cellule staminali.<br />
COMPLICANZE<br />
Innanzitutto dobbiamo stare attenti perchè c’è un rischio di evoluzione<br />
verso il Barrett e poi verso il cancro.Inoltre si possono avere:stenosi,<br />
ulcerazioni e fibrosi.<br />
Cosa si fa?<br />
Come già sapete molto importante è<br />
-la DIETA:eliminare cibi come alcool,caffè,cioccolato,cibi grassi,fritti<br />
ovvero tutti quei cibi che evocano forte produzione di acidi e che<br />
aumentano il reflusso.<br />
-cambiare ABITUDINI ALIMENTARI (nn come stanno facendo qui fuori):<br />
quindi pasti piccoli e frequenti,ridotti in numero(?). Non mangiare poco<br />
prima di andare a letto.<br />
- POSTURA :<br />
- FARMACI: antagonisti dei recettori H2 ecc...<br />
La TERAPIA CHIRURGICA può essere utile sporattutto in caso di ernia<br />
iatale, che come già detto può essere una concausa e talvolta il fattore<br />
scaricato da www.sunhope.it
determinante dell’esofagite da reflusso.<br />
C’è un intervento che si faceva fino a poco tempo fa,che è la fundoplicatio<br />
(verso cui io sono molto scettico) nel quale si innesta in una maniera<br />
particolare l’esofago nello stomaco proprio per eitare il reflusso. Come<br />
vedete se si segue questo regime alimentare e si fanno questi trattamenti<br />
c’è un’efficacia che supera l’80% di casi.<br />
Abbiamo degli altri tipi di esofagite su cui non ci fermeremo:<br />
- quelle batteriche soprattutto da stafilococco.<br />
-da candida(molto raramente ) soprattutto nei soggetti immunodepressi.<br />
La candida si arresta prima nella mucosa orale e da qui può raggiungere<br />
l’esofago; è un segno di immunodepressione. É tipica l’esofagite in pz siero<br />
positivi con AIDS conclamato.<br />
- da Citomegalovirus;<br />
- esofagite corrosiva: quando per errore o per un tentativo di suicidio<br />
(una volta andava di moda la varechina) si ingeriscono sostanze corrosive<br />
che determinano lesioni accidentali o volontarie.<br />
– esofagite da farmaci: molti farmaci possono avere un’azione lesiva sia<br />
sulla mucosa gastrica sia su quella esofagea.<br />
– esofagite eosinofila: (rara) trovare gli eosinofili fa pensare a una sorta di<br />
ipersensibilità o intolleranza.<br />
– esofagiti da radiazioni<br />
-da altre cause.<br />
ESOFAGO DI BARRETT<br />
È un “concetto” nato non molti anni fa ,precisamente nel ’57.Proprio<br />
Barrett lo chiamo “esofago corto”, perchè prima che esistesse una<br />
documentazione anatomo-patologica, ci si limitava a quelle che erano le<br />
caratteristiche macroscopiche.Macroscopicamente la mucosa esofagea ha<br />
un colorito che va dal bianco al rosa perchè si tratta di un epitelio<br />
pavimentoso stratificato, laddove invece la mucosa gastrica ha un colorito<br />
scaricato da www.sunhope.it
ossso vivo, perchè è fatto da epitelio cilindrico. Nell’ esofago di Barrett la<br />
mucosa del tratto inferiore assume un aspetto rosso vivo simile alla<br />
mucosa gastrica per questo Barrett pensava che fosse l’esofago ad essere<br />
diventato più corto. Quindi il concetto è questo: non è che l’esofago è più<br />
corto,ma è un aspetto macroscopico frutto della metaplasia,che vi<br />
mostrerò.<br />
Solitamente la giunzione gastro-esofagea,la famosa linea Z , non sempre<br />
è facilmenta visibile. Proprio perchè è una linea Z, non è una bella linea<br />
dritta. Poi c’è il problema che un certo reflusso fisiologico post-prandiale è<br />
ammissibile per tutti, quindi per convenzione si dice che questa giunzione<br />
se non la vediamo bene,sta a 2 cm di distanza dalla fine delle pliche<br />
gastriche. Quindi si individua dove finiscono le pliche gastriche , si sale 2<br />
cm e li si trova la giunzione. Perchè<br />
questa convenzione? Per definire l’ esofago di Barrett e distinguerlo dal<br />
reflusso fisiologico. Perchè tutto ciò che è al di sotto di 2 cm non è<br />
considerato esofago da Barrett,in quanto normalmente delle aree di<br />
metaplasia cardiale le possiamo trovare entro questo range di 2 cm.<br />
Tutto ciò che è al di sopra di questi 2 cm, quindi qualunque metapasia, lo<br />
possiamo assimilare a esofago di Barrett, al di sotto viene considerato<br />
para-fisiologico.<br />
L’esofago di Barrett certamente è legato a iperstimolazione,da ambiente<br />
acido,delle cellule staminali.Queste cellule stimolate dall’acidità anomala<br />
per questa sede, possono determinare questa metaplasia di cui<br />
parleremo. In linea di massima noi distinguiamo vari tipi di esofago di<br />
Barett. La distinzione più importante è quella che individua:<br />
• Segmento lungo: significa che c’è un’estensione superiore a 3cm<br />
dalla giunzione.<br />
• Segmento corto: è nella fase iniziale, non si estende oltre 3 cm dalla<br />
giunzione, quindi è confinato entro 5 cm dalla fine delle pliche<br />
gastriche.<br />
scaricato da www.sunhope.it
Dal punto di vista clinico sono stati fatti vari studi molto interessanti<br />
che fanno vedere come il segmento lungo sia legato ad una storia<br />
clinica di esposizioni al reflusso più duratura,più frequente, mentre il<br />
segmento corto è legato a esposizioni ad ambiente acido più breve e<br />
non costante.<br />
È inoltre legato anche alla pressione del LES: laddove c’è una<br />
pressione molto diminuita si va incontro a segmento lungo; laddove<br />
c’è una riduzione lieve è più facile avere un segmento corto.<br />
Cosa significa esofago di Barrett dal punto di vista anatomopatologico?<br />
Noi vediamo delle isole o lingue di epitelio colonnare; quindi<br />
proiezioni digitiformi di colore rosso vivo,che si estendono in questo<br />
epitelio biancastro,tipico dell’esofago.Questo rosso è la mucosa non<br />
più fatta da epitelio pavimentoso stratificato, ma da epitelio<br />
colonnare monostratificato.<br />
Poi ci possono essere:<br />
• Ulcere<br />
• Stenosi<br />
• Emorragie<br />
• Perforazioni<br />
Se l’endoscopista ha qualche problema può usare anche un colorante<br />
vitale,tipo Lugol,per cui l’epitelio squqmoso che è ricco di glicogeno<br />
apparirà nera, mentre l’epitelio non squamoso non apparirà colorato.<br />
EPIDEMIOLOGIA<br />
L’esofago di barrett interessa circa il 2-3% della popolazione.<br />
Non tutte le esofagiti da reflusso evolvono verso il Barrett.<br />
Le casistiche autoptiche, però dicono che in realtà l’incidenza è 17 volte<br />
più elevata rispetto a quella stimata, questo significa che<br />
scaricato da www.sunhope.it
probabilmenta interessa più di 1/3 della popolazione.Questo è molto<br />
importante perchè è una patologia in grande espansione e c’è un<br />
notevole aumento di incidenza. Solo l’8-15% dei pz con esofagite da<br />
reflusso evolve verso il Barrett(dal punto di vista clinico);ma se<br />
andiamo a vedere le casistiche autiptiche l’incidenza aumenta.<br />
Ecco come appare dal punto di vista endoscopico:<br />
si può apprezzare il colore bianco della mucosa normale e si vedono<br />
delle lingue di mucosa rossastra che si proietta nel bianco della mucosa<br />
esofagea.Talvolta la mucosa rossastra è organizzata in isole ; quindi non<br />
c’è un confine netto,geometrico. Le alterazioni sono dipendenti<br />
dall’entità e intensità del reflusso.<br />
Che tipo di metaplasia possiamo trovare?L’epitelio può essere:<br />
• di tipo cardiale: somiglia a quella porzione dello stomaco che è a<br />
contatto con l’esofago; è la metaplasia più difficile da<br />
prevenire(?).Ricordate il limite di 2 cm.<br />
• Di tipo fundico: epitelio che somiglia al fondo dello<br />
stomaco,laddove troviamo le ghiandole gastriche<br />
• Di tipo intestinale:l’epitelio di tipo intestinale era considerato il<br />
più caratteristico dell’esofago di Barrett, oggi l’epitelio di tipo<br />
intestinale è considerato patognonomico di Barrett.<br />
Si è visto che molto spesso ,soprattutto anticamente,quando si<br />
facevano poche biopsie ,poteva non comparire questa metalasia<br />
intestinale.,con un tipo di epitelio che presenta le goblet cells e<br />
cellule del Paneth, che sono tipiche dell’intestino.<br />
Oggi in genere nell’esofago di Barrett si fanno più di 10-12<br />
biopsie, perchè avete visto com’è irregolare nell’estensione per<br />
cui c’è bisogno di mappare diverse aree e capire cosa c’è. Oggi<br />
si sa,anche se non è da tutti condiviso, che se non troviamo<br />
scaricato da www.sunhope.it
l’epitelio intestinale, quindi se non c’è una metaplasia di tipo<br />
intestinale non possiamo fare diagnosi di Barrett, per cui se non<br />
lo troviamo è perchè abbiamo fatto una campionatura minima o<br />
imprecisa,perchè la dobbiamo trovare sempre o quasi<br />
sempre( perchè il sempre non esiste in medicina!).<br />
La cosa più importante è che questo Barett può dar luogo a delle<br />
lesioni precancerose cioè la displasia.<br />
Ricordate come una stimolazione impropria sulle cellule<br />
staminali può determinare delle atipie citologiche.<br />
Abbiamo un grading universalmente accettato che distingue<br />
esofago di Barrett:<br />
• Negativa per displasia<br />
• Indeterminato per displasia : che significa che non siamo sicuri<br />
che c’è displasia . C’è un’iperplasia rigenerativa ma vedendo i<br />
prelievi non siamo sicuri che si tratta di displasia. Certamente se<br />
c’è displasia si tratta di una displasia lieve.<br />
• Displasia di basso grado<br />
• Displasia di alto grado<br />
• Carcinoma intramucosale : cioè carcinoma che non ha superato i<br />
confini della mucosa.<br />
La displasia grave la troviamo soprattutto nelle forme con<br />
segmento lungo: 20-45%, mentre nel segmento corto ( poichè ha<br />
una storia di minore esposizione all’ambiente acido,con<br />
esposizioni meno frequenti o più diradate nel tempo) trovare una<br />
displasia grave è più difficile.<br />
IMMAGINE:Qui vedete l’epitelio squamoso che a un certo punto<br />
si interrompe e troviamo questo epitelio ghiandolare e qualcuno<br />
di voi con la vista buona vedrà anche la goblet cells tipiche della<br />
mucosa intestinale.<br />
scaricato da www.sunhope.it
Quindi nell’esofago di Barrett ci son tratti di mucosa intestinale<br />
che interrompono l’epitelio pavimentoso stratificato e non<br />
abbiamo dubbi in questi casi.Se invece troviamo un epitelio<br />
cardiale,abbiamo dei dubbi perchè possiamo pensare che<br />
l’endoscopista si è sbagliato Può aver fatto un prelievo nella zona<br />
di transizione (entro 2 cm dalla fine delle pliche gastriche ) o sulla<br />
lineaZ ,questa zona un pò confusa.<br />
IMMAGINE: vedete qui com’è possibile cogliere la zona di<br />
passaggio dell’epitelio stratificato a tessuto ghiandolare<br />
colonnare.<br />
Se andiamo a fare dei metodi per evidenziare i<br />
mucopolisaccaridi tipici dell’intestino possiamo vedere questo<br />
colore azzurro che ci dice che sono mucopolisaccaridi.<br />
DISPLASIA LIEVE: vediamo strutture ghiandolari e potete vedere<br />
come c’è un’irregolarità di struttura; le ghiandole sono una<br />
addosso all’altra e vedete le solite atipie citologiche con un certo<br />
pleomorfiso(?).<br />
IMMAGINE: vedete qui una displasia grave in cui le atipie sono<br />
molto più spiccate<br />
CARCINOMA INTRAMUCOSALE: è una diagnosi difficile perchè<br />
vedete che comincia a vedersi un’invasività però confinata ancora<br />
allo spessore della mucosa.Ci sono poche cellule maligne sparse.<br />
In rapporto alla storia naturale, il problema del Barrett è proprio<br />
la displasia. Il pz che ha un Barrett va seguito perchè il rischio è<br />
abbastanza elevato.<br />
Esistono dei protocolli internazionali applicati nel follow-up.<br />
Segni predittivi sono:<br />
scaricato da www.sunhope.it<br />
• L’estensione del barrett, quindi è necessario fare biopsie<br />
multiple;
• Se è presente displasia;<br />
• Che tipo di displasia c’è;<br />
• Se c’è già un cancro;<br />
Quando viene il cancro in questi pazienti (ovviamente il cancro che viene<br />
è l’adenocarcinoma) in genere viene scoperto in fase già avanzata e ha un<br />
altro difetto: tende ad avere estensione multicentrica, perchè si tratta di<br />
una mucosa già lesa.Quindi è facile ,per il concetto di cancerogenesi di<br />
campo,che possiamo avere più focolai,per cui bisogna intervenire il più<br />
presto possibile.<br />
TERAPIA:<br />
- MEDICA<br />
-CHIRURGICA: trattamento ablativo.Viene tolto questo epitelio senza fare<br />
interventi chirurgici radicali. Certo va fatta da persone esperte,va<br />
esaminato attentamente tutto quello che c’è. Si può fare attraverso una<br />
mucosectomia con particolari strumanti chirurgici(immaginate come si fa<br />
per fare i riccioli di burro!). Quindi si tolgono questi strati superficiali.<br />
-Poi c’è la terapia fotodinamica: sulla terapia fotodinamica io sono molto<br />
scettico. Qual’è il concetto? Il concetto è di dare sostanze fotodinamiche<br />
che in presenza di irradiazione danno una certa tossicità,però prima c’è<br />
bisogno che il tessuto si impregni di queste sostanze per poi esporlo a<br />
una fonte luminosa in modo che si abbia la distruzione del tessuto.<br />
-crioterapia<br />
-elettrocoaugulazione.<br />
La chirurgia va indicata:<br />
sicuramente: nel carcinoma laddove è possibile operare,<br />
ma molti sono d’accordo che va operato anche quando c’è una displasia<br />
grave, per la quale è molto probabile sia l’evoluzione in senso temporale<br />
verso il cancro,sia anche che ci sia già qualche focolaio adiacente.<br />
scaricato da www.sunhope.it
DISPLASIA GHIANDOLARE DELL’ESOFAGO: sono quelle che troviamo<br />
soprattutto associate al Barrett, però ci sono casi in cui può non esserci il<br />
Barrett, però lo presume quasi certamente.<br />
DISLASIA E CANCRO:<br />
-Se c’è displasia grave nel 59% dei casi può evolvere verso il cancro;<br />
-La displasia grave nel 40% dei casi è associata a cancro sincrono in una<br />
parte dell’esofago( ecco perchè intervenire chirurgicamente)<br />
-il tempo in cui si può sviluppare il cancro: entro 5 anni.<br />
La displasia può essere :<br />
-piatta<br />
- di aspetto polipoide<br />
-focale<br />
-multifocale: cioè già programmata per la multicentricità, ammesso che<br />
non ci siano già delle foci di carcinoma.<br />
ASPETTI MOLECOLARI:<br />
L’espressione del Ki67 viene saggiata perchè aumenta se andiamo da una<br />
displasia grave al carcinoma, così come aumenta la mutazione della p53,<br />
che è pure un marcatore nucleare ed aumenta perchè ne viene inibita la<br />
degradazione.<br />
Questa storia naturale dal Barrett,alla displasia, al cancro si caratterizza<br />
per tutta una serie di mutazioni, per tutta una serie di stimoli replicativi,<br />
per esempio il TNF-α, vari tipi di IL.<br />
Vi ho parlato nella parte generale delle modificazioni delle E-CADERINE,<br />
che fa parte di quella transizione epiteliale-mesenchimale che favorisce<br />
l’aggressività delle cellule. Ci sono poi tutta una serie di mutazioni di cui<br />
non parlerò.<br />
BARRETT SENZA DISPLASIA E RISCHIO DI ADENOCARCINOMA:<br />
scaricato da www.sunhope.it
-il rischio è 0.5-1% per anno: questo significa che in 20-30 anni il rischio è<br />
aumentato del 30%;<br />
-il rischio è 30-50(o 150 non si capisce) volte più alto rispetto alla<br />
popolazione non affetta da Barrett<br />
-il rischio è 7-8 volte maggiore nel segmento lungo rispetto al segmento<br />
corto ( quindi le persone con segmento lungo devono essere seguite con<br />
più assiduità, più accuratezza e ad intervalli più brevi).<br />
–nel 50% dei casi di adenocarcinoma troveremo stadi avanzato o<br />
multicentricità.<br />
MUTAZIONI: le mutazioni riguardano p53, p16.Oggi si parla molto anche<br />
di c-erb-b2, myc e di geni legati all’apoptosi,perchè anche questo<br />
meccanismo è alterato.<br />
Quindi l’evoluzione è: reflusso→esofagite→Barrett→displasia→cancro.<br />
Come si fa la diagnosi isto-patologica?<br />
-Innanzitutto c’è bisogno di una mappatura con biopsie multiple perchè<br />
ci può essere displasia in un’area e non esserci in un’altra.<br />
-valutazione delle aree di displasia<br />
-immunoistochimica<br />
- valutazione ploidie: perchè la displasia grave e il carcinoma tendono di<br />
più all’aneuploidia,mentre le metaplasie innocue non hanno atipie<br />
citologiche.<br />
–valutazione di altri marcatori: es. p53.<br />
Oltre alla precancerosi ghiandolare, che è legata intimamente al<br />
Barrett,possiamo avere un altro tipo di precancerosi che riguarda l’epitelio<br />
squamoso,che non ha niente a che fare con il Barrett e l’esofagite da<br />
reflusso.Vedremo poi che ha un’altra storia clinica. Ovviamente la<br />
displasia dell’epitelio pavimentoso pluristratificato sarà un quadro simile a<br />
quello che osserviamo nella cervice, quindo parliamo di : -displasia lieve<br />
o -displasia<br />
grave, a seconda che è coinvolto solo la parte inferiore dell’epitelio o tutto<br />
scaricato da www.sunhope.it
lo spessore. La progressione in<br />
cancro: -per la displasie<br />
lieve è del 20% in 60 mesi, -per la displasia<br />
grave è del 60% in 24 mesi. In altri<br />
termini possiamo dire che chi ha una displasia grave ha un rischio che è<br />
circa 73 volte più elevato di cancro. Chi<br />
ha una displasia lieve un rischio 2.2 volte maggiore.<br />
CLASSIFICAZIONE DEI TUMORI DELL’ESOFAGO:<br />
(facciamo una breve sintesi dei tumori più frequenti, con una maggiore<br />
attenzione ai più importanti cioè carcinoma e adenocarcinoma). Vi<br />
dico subito una cosa molto importante:si assiste in tutto il mondo a un<br />
cambiamento epocale ovvero mentre prima l’adenocarcinoma<br />
rappresentava il 10-15 %di tutti i cancri dell’esofago,oggi le casistiche ci<br />
dicono che in molte regioni del mondo l’adenocarcinoma ha superato per<br />
incidenza il carcinoma squamoso. In altre regioni hanno un’incidenza<br />
paritetica. Evidentemente questo è da correlare a questo reflusso.<br />
[pausa]<br />
TUMORI BENIGNI PIU’ FREQUENTI<br />
• Papilloma: di fatto il papilloma è quello che può venire dappertutto,<br />
se si presenta a livello dell’esofago da tutta una seria di problemi.<br />
(registrazione poco comprensibile)<br />
• Adenoma<br />
• Tumori tipo ghiandole salivari: in questo caso è giustificata la<br />
presenza di questi tumori perchè nell’evoluzione soprattutto della<br />
parte inferiore dell’esofago troviamo delle ghiandole mucose.<br />
Questa patologia non ha nulla a che vedere con il Barrett;possiamo<br />
trovare un quadro pleomorfo(adenoma pleomorfo)e tutti quei<br />
tumori di cui abbiamo parlato trattando il cavo orale.<br />
TUMORI MALIGNI PIU’FREQUENTI<br />
scaricato da www.sunhope.it
Carcinoma squamoso e sue varietà:<br />
-superficiale: vuol dire che o è in situ o è microinvasivo,cioè mostra<br />
solo dei piccoli gettoni di invasività. Ovviamente questa va assimilata a<br />
una forma non propriamente invasiva e quindi ha una prognosi<br />
decisamente migliore;<br />
- verrucoso: cioè un carcinoma che tende a formare cheratina e che<br />
quindi è ricco di materiale corneo perchè è altamente differenziato;<br />
-sarcomatoide: le cellule assumono questo aspetto fusato( tipo<br />
sarcoma), ma se facciamo una citocheratina vediamo che sono cellule<br />
epiteliali alterate(citocheratina +) e sono cellule che esprimono anche<br />
l’actina , il che vuol dire che sono cellule che hanno avviato quella<br />
transizione epitelio-mesenchimale.<br />
-basalioide: non ha niente a che vedere con il carcinoma basale della<br />
cute( che abbiamo detto essere un cancro di serie B,perchè non da<br />
metastasi). Questo infatti è un carcinoma vero e proprio e ha un<br />
comportamento aggressivo anche perchè e fatto da cellule simili a<br />
quelle basali ,ma che non tendono a cheratinizzare , il cui citoplasma<br />
non è eosinofilo.<br />
-carcinoma indifferenziato anaplastico: è fatto da cellule molto più<br />
brutte, per cui è difficile anche capire perchè è tanto indifferenziato<br />
che morfologicamente non somiglia neanche lontanamente a un<br />
epitelio.<br />
ADENOCARCINOMA<br />
La forma più frequente e più importante è quella associata a storia di<br />
Barrett. Altri tipi di adenocarcinomi sono quelli di tipo ghiandole<br />
salivari:<br />
-adenomioma cistico<br />
-adenocarcinoma muco-epidermoide<br />
-carcinoma adenosquamoso<br />
Poi c’è il carcinoma a piccole cellule, che come già detto è un<br />
carcinoma spesso neuroendocrino,perchè le cellule neuroendocrine<br />
scaricato da www.sunhope.it
stanno normalmente nell’esofago.<br />
IMMAGINE(papilloma): vedete questa escrescenza. In questo caso è<br />
ancora più complesso: abbiamo una papillomatosi esofagea, quindi<br />
papillomi multipli. Talora è legato all’HPV tipo 6 o 11 .<br />
Questo tipo di lesione pone il problema di diagnosi differenziale con<br />
carcinoma verrucoso.<br />
Molto spesso queste lesioni si trovano nell’esofago distale e sono<br />
piccole.<br />
[audio distrurbato da interferenze]<br />
Carcinoma squamoso: ha un’incidenza di 5-10 /100000. Incidenza<br />
stabile nei paesi sviluppati,mentre in Asia tende ad aumentare per le<br />
abitudini alimentari.<br />
In media oggi rappresenta il 50% dei carcinomi,ma nel 1976<br />
rappresentava il 90% di tutti i cancri dell’esofago. Questo non significa<br />
che l’incidenza si è ridotta ma è che aumentata in maniera<br />
esponenziale l’incidenza dell’adenocarcinoma.<br />
In Asia l’incidenza è elevata per i seguenti fattori di rischio:<br />
- fumo,<br />
- alcool,<br />
-abitudini alimentari: un certo ruolo lo hanno le bevande calde<br />
soprattutto diffuse nella cultura asiatica.<br />
- alcune muffe: (specie nei paesi asiatici) in particolare la muffa che<br />
produce l’aflotossina, una tossina prodotta da alcuni tipi di miceti che<br />
ha un ruolo cancerogeno.(per cui quando andate in questi mercati<br />
cinesi state attenti)[lunga dissertazione sui mercati cinesi] .<br />
Allora tenete anche conto del pericolo proveniente da questa terre<br />
correlato a questa aflotossina ,che ha un ruolo anche nel carcinoma nel<br />
fegato,che nelle areee asiatiche ha una maggiore incidenza rispetto agli<br />
altri paesi. -C’è<br />
un ruolo molto importante anche di una dieta povera di frutta e<br />
scaricato da www.sunhope.it
verdura fresca.<br />
Oggi per esempio si nota soprattutto tra i giovani una tendenza a non<br />
mangiare frutta;si tende a uno snack e a questi prodotti che sarebbero<br />
da studiare sotto il profilo delle conseguenze. Una volta ho fatto uno<br />
studio, che mi provocò non pochi problemi , sulla cancerogenicità delle<br />
creme solari.Vi assicuro che l’80% erano cancerogene.<br />
S<br />
EDI:<br />
-il 3° medio purtroppo rappresenta la sede dove si verifica la metà dei<br />
carcinomi squamosi e questa è una delle sedi dove l’operazione è più<br />
difficile,perchè è facile che si abbia un coinvolgimento mediastinico,<br />
anche perchè ricordate come l’esofago sia ricchissimo di linfatici nella<br />
sottomucosa e come attraverso la via linfatica gli emboli tumorali<br />
possono giungere nei linfonodi mediastinici e quando coinvolge il<br />
mediastino diciamo che il pz non è più operabile o se si opera<br />
l’operazioone porta a tutta una serie di problematiche.<br />
La sede migliore è il 3° inferiore perchè è quello più facilmente<br />
accessibile dal punto di vista chirurgico.<br />
Il 3° superiore :20% dei casi. anche qui ci sono problemi di accessibilità<br />
per il rapporto che l’esofago superiore contrae con il faringe.<br />
CARATTERISTICHE BIOLOGICHE<br />
Cancro che dà metastasi nel 75%dei casi,molto spesso è un<br />
linfonodo,ma può dare metastasi a distanza: fegato<br />
,stomaco,polmone,rene,surrene.<br />
Noi troviamo in quasi la metà dei casi l’invasione di linfatici delle<br />
sottomucose.<br />
Questo ci pone d fronte a un altro problema: i margini chirurgici di<br />
escissione.Il chirurgo toglie un tratto di esofago ,poniamo il caso che si<br />
tratti di esofago terminale, convinto di aver tolto tutto il tumore. In<br />
questo caso l’anatomo-patologo non deve solo valutare la superficie<br />
scaricato da www.sunhope.it
,ma deve stare molto attento quello che c’è sotto,perchè attraverso<br />
queste vie linfatiche che non si vedono può avvenire un’infiltrazione<br />
che coinvolge il moncone residuo dell’esofago.<br />
La chirurgia radicale è la terapia migliore,se si può fare, con o senza<br />
linfoadenectomia( dipende dai casi) per le forme operabili. Per<br />
operabili si intendono quelle che non invadono l’aorta ,le struttura<br />
tracheo-bronchiali, il pericardio ,il diaframma ,lo stomaco e soprattutto<br />
il mediastino.<br />
La mortalità dell’intervento chirurgico è del 10%,quindi è un intervento<br />
molto delicato.E importante avere ampi margini di escissione proprio<br />
per ricchezza dei linfatici sottomucosali. La radio e la<br />
chemio sono alternative nelle forme inoperabili o possono essere usate<br />
come trattamento adiuvante o neoadiuvante,cioè prima o dopo<br />
l’intervento chirurgico per contribuire al successo terapeutico. Hanno<br />
lo scopo di ridurre la massa e facilitare eventualmente una bonifica<br />
delle aree adiacenti che non sono state tolte.<br />
La sopravvivenza media a 5 anni è < 20%. Quindi è uno dei cancri più<br />
cattivi, il polmone lo supera.<br />
Fattori prognostici: sede ,stadio, grading, il pattern di crescita, i margini<br />
chirurgici, la presenza di emboli(cioè trovare emboli nei vasi linfatici o<br />
ematici, che vuol dire che è un cancro che va avanti), la p53 e si parla<br />
tanto dell’EGF-R, che riguarda soprattutto i cancri della giunzione<br />
gastro-esofagea,cioè gli adenocarcinomi, legati a Barrett.<br />
ASPETTO MACROSCOPICO<br />
-forma debolmente vegetante<br />
-forma vegetante:soprattutto nel 3° inferiore<br />
-forma polipoide o pluripolipoide<br />
-forma ulcerante<br />
-forma perforante<br />
scaricato da www.sunhope.it
-forma infiltrante: che non ha aspetti macroscopici evidenti, ma ha una<br />
tendenza alla diffusione sottomucosale,per cui si vede solo un aumento<br />
delle plicature. La mucosa presenta solo questa iperplasia.<br />
-forma stenosante: quando c’è un coinvolgimento circolare di tutta la<br />
parete fino ad arrivare a una stenosi.<br />
IMMAGINE(carcinoma squamoso):questo è un microinvasvo con pochi<br />
gettoni, vedete già un embolo.<br />
Carcinoma verrucoso:aspetto vegetante con tendenza a<br />
cheratinizzazione,con una minore tendenza a metastatizzare e infiltrare<br />
perchè ben differenziato.<br />
Carcinoma basalioide:è una forma altrettanto aggressiva solo che è<br />
fatta di cellule piccole come si vede qui,che non hanno tendenza a<br />
cheratinizzare.Si chiama basalioide perchè sono simili alle cellule basali.<br />
Carcinoma sarcomatoide:potete vedere le forme “strane”, fusate, che<br />
fanno pensare a un sarcoma più che a un carcinoma. Ha un pattern<br />
istochimico complesso perchè può esprimere vari tipi di marcatori.<br />
Adenocarcinoma della giunzione: incidenza in grande aumento in tutti<br />
i paesi industrializzati. In Gran Bretagna l’incidenza negli ultimi 10 anni<br />
è raddoppiata, quindi rappresenta una vera e propria emergenza.<br />
La sede preferenziale è la giunzione gastro-esofagea. In passato<br />
buttavano il sangue per capire se questo carcinoma veniva dallo<br />
stomaco o dall’esofago. Il problema è stato risolto,vi dirò poi come.<br />
Nella maggior parte dei casi è un carcinoma che viene dall’alto, cioè<br />
dal Barrett, in ogni caso noi lo chiamiamo adenocarcinoma della<br />
giunzione gastro-esofagea. Proviene quindi dalla porzione terminale<br />
dell’esofago e/o porzione cardiale della stomaco.<br />
CLASSIFICAZIONE ADENOCARCINOMA<br />
C’è una proteina chiamata VILLINA ,che sembra essere espressa<br />
soprattutto dai tumori provenienti dall’esofago. Quindi se vogliamo<br />
proprio avere la certezza valutiamo la villina. Se:<br />
scaricato da www.sunhope.it
- Esofagei→Villina +: vuol dire che si tratta di un carcinoma<br />
proveniente dall’esofago e questo rappresenta la quasi totalità dei<br />
casi.<br />
- cardiale→ villina Θ<br />
- subcardiale : che sono molto spesso associati a Helicobacter pylori.<br />
Quello più importante è il primo.<br />
Fattori di rischio:<br />
-durata del reflusso<br />
-esofago di Barrett<br />
-obesità: è un fattore di rischio sia legato al reflusso, sia come fattore di<br />
rischio indipendente.<br />
1. Questo tipo di cancro è caratterizzato da perdita o mutazione di geni<br />
oncosoppressori,come RB,p53.<br />
2. C’è un’iperespressione dell’EGF-R che ha delle implicazioni<br />
terapeutiche.<br />
3. Abbiamo anche una perdita dell’E-CADERINA, dell’α-catenina e<br />
un’espressione di CATENINE anomale, cioè non epiteliale e un’espressione<br />
di β-catenine. Vi ricordo che le catenine sono proteine che ancorano le<br />
cellule epiteliali allo stroma sottostante. Il cambio del citoscheletro ,quindi<br />
delle caderine tipiche,determinano aumento della motilità e aggressività<br />
da parte della cellula. 4. Spesso è<br />
multicentrico. IMMAGINE: qui<br />
possiamo cogliere la storia naturale del cancro.Vediamo aree di carcinoma<br />
ricche di granulociti e qui troviamo una ghiandola intestinale<br />
sopravvissuta,che è una testimonianza di questo primo passo nella storia<br />
naturale di questo cancro.<br />
Fine<br />
scaricato da www.sunhope.it
Lezione 29/04/2011 prof. Rossiello<br />
Argomenti trattati: esofago(tumori), tenue(eterotopie, diverticolo Meckel, celiachia, tumori), crasso<br />
(malattia Hirshprung).<br />
ESOFAGO<br />
tumori ricordiamo alcuni concetti essenziali, cioè quella sequenza, quella dinamica evolutiva, che parte<br />
dall'esofagite da reflusso, passa per il Barrett , e arriva alla displasia e poi al cancro. Oggi si assiste ad un<br />
aumento vertiginoso di questo tipo di patologia. Lo stesso aumento si ha in patologie intestinali dalla<br />
patogenesi ancora oscura (IBD).<br />
Per indicare l'adenocarcinoma dell'esofago, preferiamo la dizione ‘adenocarcinoma della giunzione<br />
gastroesofagea’, tenendo presente che in gran parte siano da ascrivere al Barrett.<br />
Fattori prognostici<br />
-stadiazione<br />
-multicentricità<br />
-età (se
Molto promettente è poi l'impiego di anticorpi anti-VEGF. Il presupposto è che l'uso di fattori a<br />
antiangiogenetici procuri una necrosi ischemica al cancro. Una delle furbizie del cancro è la produzione di<br />
fattori angiogenetici che ne aumentano il letto vascolare e gli consentono un'espansione. Adesso questi<br />
trattamenti sono ancora sperimentali<br />
altri tumori non epiteliali<br />
a) Muscolari, gist, mioblastoma a cellule granulari (T. di Abrikosoff) . Questo tipo di tumore, il<br />
mioblastoma, si caratterizza per un'iperplasia pseudo carcinomatosa a livello epiteliali; al di sotto<br />
abbiamo invece grandi cellule di origine neuromuscolare, forse neurectodermica, sono le ‘cellule<br />
granulose’ ovvero ricche di granuli.<br />
b) Altri tumori maligni come il melanoma: questo è particolarmente grave. Teniamo presente che<br />
normalmente troviamo i melanociti a livello dell'epitelio pavimentoso stratificato dell'esofago, per<br />
motivi embriogenetici non del tutto chiari.<br />
Altri tumori secondari<br />
-leucemie<br />
-linfomi<br />
lesioni pseudo-tumorali<br />
(…)<br />
immagini descritte: potete qui vedere il melanoma che si presenta come una voluminosa massa<br />
pigmentata, non dimenticate che una neoplasia rapidamente mortale. In quest'altra immagine invece<br />
appare il carcinoma a piccole cellule, è un carcinoma neuroendocrino, molto aggressivo. Può dare delle<br />
metastasi. È positivo ai marcatori neuroendocrini. Ha a una prognosi pessima, tuttavia migliore del<br />
melanoma.<br />
STADIAZIONE<br />
-sistema tnm (considera che l'espressione ‘pT1’ si riferisce alla stadiazione anatomopatologica, quella<br />
definitiva, quella effettuata su un campione anatomopatologico. Spesso differisce dalla T, calcolata in<br />
base agli esami radiologici o comunque ad esami indiretti)<br />
T1 la lesione riguarda solo la mucosa o al massimo la sottomucosa<br />
T2 arriva allo strato muscolare della parete<br />
T3 supera la parete muscolare<br />
T4 coinvolge altri organi extra esofagei(tipo la biforcazione bronchiale)<br />
quanto alla M, la registrazione poco chiara ma dovrebbe essere così:<br />
M1a coinvolgimento metastatico di linfonodi non loco-regionali (a distanza: cervicali o celiaci a seconda<br />
che sia l'esofago alto o basso); sono metastasi linfatiche non ematiche(controlla).<br />
M1b metastasi a distanza<br />
scaricato da www.sunhope.it
PROGNOSI E STADIAZIONE (AJCC) vedi slides cmq<br />
FOLLOW-UP A 5 AA<br />
STAGE SQUAMOSO ADENOCARCINOMA<br />
Tis 1 89-90% 86,70%<br />
T1 N0<br />
T2 M0 2A<br />
T3 M0<br />
T1 N1 2B<br />
T2 N1<br />
T3 N1 3<br />
T4 presc da N<br />
ogni T( M1 4<br />
Complicanze incorrono nel 40% dei pazienti, durante la storia naturale del tumore.<br />
a) Respiratorie : atelettasia (area o intero lobo polmonare sequestrato, cioè privo di aria. È legata alla<br />
compressione che si esercita sui bronchi. Più grande è il bronco, maggiore sarà l’area atelettasica. Il<br />
meccanismo di ventilazione viene ad alterarsi e viene meno anche la funzione respiratoria. Possiamo<br />
quindi avere insufficienza respiratoria, reazione pleurica, polmonite (da ristagno di aria e infezione<br />
sopraggiunta).<br />
b) Cardiache : aritmie, infarto (per meccanismi riflessi a partenza dall'esofago distale?)<br />
c) Settiche<br />
d) Anastomotic stricture si tratta di un'ostruzione post chirurgica, dopo asportazione del terzo<br />
inferiore, si possono avere fenomeni infiammatori e fibrotici che conducono alla stenosi.<br />
Come intuibile, questa chirurgia presenta un discreto tasso di mortalità.<br />
INTESTINO<br />
l'intestino tenue è caratterizzato dalla presenza dei villi, assenti nel crasso (rispetto alla mucosa, le<br />
escrescenze sono dette villi; mentre le rientranze all'interno della parete sono dette cripte).<br />
Dobbiamo ricordare che la parete è inoltre ricca di follicoli linfatici. L'ultimo tratto (ileo) presenta le<br />
placche del Peyer (indovate nella sottomucosa). Essi sono follicoli ad organizzazione simil-linfoghiandolare.<br />
Prima venivano molto studiati. In caso di tifo, questo tratto viene molto interessato, con distruzione delle<br />
placche. Il paratifo offre invece un quadro assai più blando. Chiaramente la funzione dei villi è quella di<br />
aumentare la superficie assorbente. Alla base delle cripte vi sono le cellule del Paneth. Esse contengono<br />
granuli di lisozima, che appaiono come inclusioni rosse al microscopio. Sono tipiche dei tenue, assenti nel<br />
crasso. Ancora abbiamo sporadiche cellule neuroendocrine. Le cellule che troviamo sulla superficie dei villi<br />
sono:<br />
-cellule caliciformi (Goblet cells) hanno citoplasma ripieno di muco. Poiché accumulano questo muco<br />
assumono una forma sferica.<br />
-Cellule cuticolari sono cellule assorbenti. Possiedono una cuticola striata, capace di dare un assorbimento<br />
selettivo. L’orletto cuticolare è in realtà rappresentato dai microvilli.<br />
Il rapporto tra Goblet cells e cellule cuticolari è alterato in alcuni tipi di malattie.<br />
scaricato da www.sunhope.it
L'intestino crasso non ha villi. La sua superficie è piatta e non possiede cellule di Paneth. Possiede però<br />
cellule cuticolari e caliciformi. Nel crasso abbiamo un aumento delle Goblet cells, poiché l’altra funzione,<br />
quella assorbente è minore (offerta dalle cellule cuticolari). Il terzo inferiore (la base) delle cripte di<br />
Lieberkhun ospita il compartimento proliferativo. Qui le cellule si moltiplicano, poiché vi sono gli elementi<br />
staminali. Man mano che seguono l'ascesa del villo le cellule poi si vanno a specializzare nei vari tipi<br />
(cuticolari, caliciformi, neuroendocrini). Se cerchiamo il Ki67 (marcatore cinetico) oppure evidenziamo le<br />
figure mitotiche, li troveremo tutti nel terzo inferiore. C'è una sorta di equilibrio. Le ghiandole<br />
sottomucosali di Brunner sono tipiche anche nel crasso (il libro invece sembra dire che sono tipiche del<br />
duodeno, approfondire). Soffermiamoci ora sui plessi nervosi: quello di Meissner (più superficiale,<br />
composto da cellule piccole, intercalato nel distretto della sottomucosa) e i plessi di Auerbach (nel contesto<br />
degli strati muscolari, a cellule più grandi, con citoplasma abbondante e nucleo vescicoloso.). Tali cellule<br />
sono gangliari, sono di interconnessione tramite un'innervazione soprattutto parasimpatica, ma anche<br />
simpatica, che regola tutta la peristalsi. La peristalsi è da intendere un po' come una corrente alternata: il<br />
segmento a monte si contrae e aumenta la pressione, quello a valle si distende e la fa diminuire. L'integrità<br />
del sistema neuronale è alla base della peristalsi.<br />
ETEROTOPIE<br />
-pancreas esocrino in duodeno<br />
-adenomioma (pancreas+ fibre muscolari)<br />
-epitelio fundico nel duodeno. L'epitelio gastrico si può formare nel duodeno a causa di un reflusso<br />
attraverso il piloro incontinente. È un evento raro; la penetrazione di acido gastrico nel duodeno,<br />
normalmente viene neutralizzata dal succo biliare a pH basico. Se il piloro è incontinente, questo stimolo si<br />
fa continuo e può determinare una stimolazione delle cellule staminali che si illudono di essere nello<br />
stomaco per cui formano delle isole di epitelio fundico.<br />
DIVERTICOLO DEL MECKEL<br />
riguarda il 2% della popolazione. Durante la vita fetale, l'abbozzo primitivo della cavità celomatica è in<br />
connessione con il sacco vitellino attraverso il dotto onfalo mesenterico. Nel momento dello sviluppo<br />
questo dotto si oblitera, si trasforma in una struttura fibrosa che tende ad essere assorbita e scomparire.<br />
Nel 2% della popolazione può permanere come un cordone fibroso che lega parte dell'intestino con<br />
ombelico; come una fistola entero-ombelicale (sono tre gli esiti possibili). Il diverticolo di Meckel si forma<br />
normalmente a livello dell’ileo distale a 1m dalla valvoa ileo-cecale.<br />
Complicanze:<br />
-infiammazione (diverticolite)<br />
-ulcerazione con perforazione<br />
-Volvolo (fenomeno di rotazione e inversione di un viscere tubulare su se stesso. Volgono deriva dal latino<br />
volvere e significa avvolgere. Determina un'occlusione con necrosi ischemica per strozzamento dei vasi<br />
mesenterici.<br />
-emorragia<br />
-intussuscezione (un tratto dell'intestino scivola nell'altro) determina stenosi funzionale.<br />
scaricato da www.sunhope.it
CELIACHIA<br />
è l'intolleranza al glutine. Legata alla presenza di autoanticorpi anti-gliadina. È in aumento. La vera<br />
patogenesi è da ricondurre all'attivazione dei linfociti T; gli autoanticorpi, un epifenomeno, sono utili per la<br />
diagnostica di laboratorio. La biopsia sola è diagnostica; senza biopsia i celiaci non possono ricevere<br />
alimenti dalla farmacia. Il professore tuttavia sostiene che la biopsia per la diagnosi sia un’esagerazione; il<br />
valore maggiore di questa indagine è la stadiazione della malattia celiaca. L'indagine istologica può dare un<br />
quadro di compatibilità per la diagnosi, ma l'anatomopatologo non può di per sé fare diagnosi di celiachia.<br />
Aspetti istologici: (sono da ricondurre alla superattivazione dei linfociti T CD8 e CD4 con distruzione del<br />
tenue e del duodeno in particolare)<br />
-atrofia dei villi parziale, subtotale, totale. Alcuni medici eseguono una biopsia di controllo a distanza dalla<br />
diagnosi per valutare la risposta alla dieta. L'altezza dei villi e la profondità delle cripte (il monte la valle)<br />
sono due parametri da considerare per stabilire il grado di atrofia. Il loro rapporto nella normalità deve<br />
essere > 2,5 (altezza deve essere 2,5 volte la profondità delle cripte).<br />
-pseudostratificazione dell’epitelio (ciò per un tentativo di rigenerazione) è solo un effetto ottico legato alla<br />
presenza di nuclei a diversa altezza.<br />
-infiltrato plasmacellulare e linfociti T<br />
-iperplasia epiteliale (aumento delle figure mitotiche)<br />
-iperplasia delle cellule neuroendocrine (tentativo di compenso; stimolano la secrezione delle goblet cells<br />
che stanno andando in atrofia) si evidenziano con l’enolasi.<br />
-Riduzione delle goblet cells<br />
Complicanze : dermatiti, linfomi, enteriti ulcerative, carcinoma, linfomi enteropatici a cellule T.<br />
TUMORI PICCOLO INTESTINO<br />
sono rari. Il piccolo intestino e l'unica sede in cui abbondano le forme neuroendocrine, insieme<br />
all'appendice vermiforme. Considera che non è raro trovare un carcinoma neuroendocrino associato<br />
all'appendice (1/200 appendicectomie eseguite per appendicite presentano un carcinoma neuroendocrino<br />
associato, un incidentaloma).<br />
I ¾ dei tumori dell'appendice sono:<br />
-cistoadenoma mucoide, cistoadenocarcinoma<br />
-pseudomyxoma peritonei (vedi slides per lista completa)<br />
quest'ultimo (già incontrato a proposito dell’ovaio) è una diffusione al peritoneo (una sorta di ascite) di<br />
muco con cellule (normali o atipiche) che assomiglia, ma non è, un mixoma. Tale muco e tali cellule<br />
derivano da un tumore mucoide a partenza dall'ovaio o dall’appendice.<br />
MALATTIA DI HIRSHSPRUNG(è olandese, vuole la s dopo la h)<br />
si chiama megacolon o megaretto in quanto il tratto interessato si compone di:<br />
-segmento prossimale (molto dilatato)<br />
scaricato da www.sunhope.it
-segmento intermedio (di transizione)<br />
-segmento distale(sede della patologia, molto ristretto)<br />
La regione che dà il nome alla malattia è quella sana! La regione malata in realtà è quella valle, quella<br />
ristretta.<br />
sede<br />
sigma retto 75% (zona più colpita)<br />
colon 20%<br />
ileo distale 5%<br />
zone<br />
-distale (zona patologica). È abbastanza piccola. Qui possono mancare i plessi (Meissner e Auerbach) o, se ci<br />
sono, mancano delle cellule gangliari (aganglionosi). Viene meno la funzione di coordinamento della<br />
peristalsi e assistiamo a una disorganizzazione delle fibre nervose (comunque raccolte dal ganglio). I fascetti<br />
nervosi si ipertrofizzano per compenso. Si ha una stenosi funzionale con blocco della progressione del<br />
gradiente pressorio. L'ostruzione è funzionale<br />
-intermedio (ancorché piccolo). Si ha ipoganglionosi. Le cellule presenti sono ridotte in numero<br />
-prossimale tenta un compenso. Qui gangli ci sono. Ci sono i plessi, le cellule gangliari, mucosa si<br />
ipertrofizza e dilata nel tentativo di spingere e forzare il blocco della progressione. Questo tratto non è<br />
patologico, ma lo diventa nel tempo per via dell’ipertrofia. L'anatomopatologo è convocato per confermare<br />
la diagnosi e per indicare con precisione quale tratto è interessato.<br />
Nel tratto interessato abbiamo:<br />
-assenza di cellule gangliari<br />
-ipertrofia e disorganizzazione delle cellule adrenergiche e colinergiche (le fibre diventano tozze, spesso<br />
iperplastiche)<br />
-alterata distribuzione delle cellule<br />
-aumento NE<br />
Patogenesi si basa sulla teoria del seme del terreno; in pratica possono insorgere diverse problematiche nei<br />
vari stadi che vanno dalla formazione delle future cellule gangliari come elementi staminali dalle creste<br />
neurali fino all'annidamento o differenziamento nella regione della parete intestinale. Ecco lo spettro delle<br />
cause possibili:<br />
1. arresto della migrazione (le cellule partono dalle creste neurali, ma non arrivano alla periferia; è<br />
raro); con i plessi non si formano proprio<br />
2. insorgenza di mutazione lungo il tragitto; qui arrivano nella parete intestinale cellule non più sane<br />
3. fenomeni di infiammazione e necrosi alterano il contesto ambientale in cui tali cellule dovrebbero<br />
insediarsi; l'ambiente inospitale impedisce il corretto attecchimento e la differenziazione<br />
scaricato da www.sunhope.it
4. alterazione della differenziazione per un microambiente sfavorevole. (Carenza di fibroblasti,<br />
laminina, N-Cam, VEGF; tutti elementi che dovrebbero guidare la differenziazione)<br />
varietà cliniche<br />
1. classica tratto di circa 10 cm. Inizia dal retto distale e si estende prossimalmente<br />
2. corto il segmento agangliare è meno evidente (pochi centimetri)<br />
3. ultra corto<br />
4. lungo si estende a tutto il crasso<br />
vedi slides per mutazioni geniche<br />
diagnosi<br />
l'anatomopatologo interviene nella fase preoperatoria per effettuare una diagnosi tramite suzione e<br />
non biopsia (il bambino è piccolo). In pratica si tenta un risucchio attraverso la mucosa di una piccolo<br />
strato della parete intestinale. Il problema che si apre è quello dei gangli che sono profondi e quindi<br />
difficilmente vengono pescati dal risucchio. Un aspetto saliente della patologia è l'ipertrofia della<br />
mucosa e l'ipertrofia neuronale, in particolare del parasimpatico (abbondanza di acetilcolinesterasi).<br />
Tramite un substrato marcatore del acetilcolinesterasi evidenziamo la conformazione della rete<br />
gangliare, attraverso immagine indiretta. In questo modo superiamo il problema dell'impossibilità di<br />
estrarre i gangli tramite suzione. Il patologo interviene ancora nella fase operatoria, guidando il<br />
chirurgo nell'estrazione del segmento agangliare tramite una serie di intraoperatorie. La sede più<br />
delicata è quella dell’anastomosi. essa è una sede di minore resistenza. Nel fare il prelievo dobbiamo<br />
sempre mantenerci a 2 cm dallo sfintere anale interno, in quanto in tale regione le cellule gangliari<br />
sono normalmente assenti o pochissime. Si ricorre a biopsia multiple per definire l'estensione della<br />
patologia. I marcatori (enolasi, neuro filamenti) possono evidenziare le cellule gangliari. Possibile è<br />
anche un'analisi nella fase postoperatoria per la diagnosi definitiva<br />
scaricato da www.sunhope.it
I diverticoli e la diverticolosi (diverticoliti quando si infiammano)<br />
Costituisce una patologia molto frequente.<br />
Al di sopra di una certa età , dopo i 50 anni, un circa 10% della popolazione, anche<br />
inconsapevolmente, ne è affetto (inconsapevolmente perchè sulla base dei sintomi non è facile fare<br />
diagnosi di diverticolosi soprattutto quando sono piccoli e unici)<br />
Si distinguono:<br />
-vero diverticolo: tutta la parete è coinvolta, anche tonaca muscolare, dunque c’è un’erniazione di<br />
tutta la parete<br />
-pseudodiverticolo: l’erniazione riguarda prevalentemente mucosa e sottomucosa, un po' di<br />
muscolare. Dunque il cedimento non riguarda la parete a tutto spessore<br />
Il diverticolo è più problematico perchè tende a infiammarsi e fistolizzare nei riguardi di altre anse<br />
intenstinali portando alla formazione di masse di grosse dimensioni che possono simulare anche un<br />
cancro perchè si determina una condizione di ostruzione intestinale. Inoltre la fistolizzazione esita<br />
in fibrosi e in formazione di aderenze che danno luogo a masse che alla tac possono essere confuse<br />
per masse tumorali. Importante diagnosi differenziale con carcinoma!!<br />
Le sedi preferenziali:sigma e discendente.<br />
Difficilmente operabili soprattutto quando sono multipli. Sono molto dolorosi.<br />
A monte dei diverticoli c’è una stasi terribile perchè si determina un’ostruzione totale o parziale.<br />
Le complicanze : EMORRAGIE, PANNICOLITE (perchè intorno al viscere c’è sempre questo<br />
grasso che può infiammarsi) PERFORAZIONE, FISTOLE CON VESCICA , + SPESSO LA<br />
FISTOLIZZAZIONE COINVOLGE ALTRE ANSE INTENSTINALI.<br />
Malattie infiammatorie croniche dell’intestino IBD:<br />
-CROHN<br />
-RETTOCOLITE ULCEROSA<br />
-FORME INDETERMINATE: IN CUI C’è INIZIALMENTE UNA SOVRAPPOSIZIONE TRA<br />
CROHN E RETTOCOLITE ULCEROSA che poi evolve verso una forma o verso l’altra<br />
esprimendo così la sua vera natura. Queste ultime forme sono in aumento e hanno una maggiore<br />
mortalità e vengono indicate semplicemente con la sigla IBD.<br />
Complicanze: Tromboembolie cancro, peritonite, sepsi, complicanze chirurgiche (es i margini di<br />
sutura del moncone ,dopo intervento di asportazione del tratto colpito dalla patologi, sono un punto<br />
debole su cui possono attecchire altre patologie)<br />
L’incidenza in totale delle IBD è di 10-15 nuovi casi per 100mila per anno. La prevalenza Su<br />
100mila abitanti 70-150 casi.<br />
La patogenesi è immunitaria o autoimmunitaria ma non è ancora ben definita.<br />
CROHN:<br />
INCIDENZA 2 3 CASI SU 100MILA (INFERIORE A RETTOCOLITE ULCEROSA )<br />
SEDE DEL CROHN: ILEO TERMINALE, il colon retto può essere coinvolto, inoltre<br />
scaricato da www.sunhope.it
coinvolgimento di entrambi è possibile in 17% casi.<br />
Le lesioni istologiche sono caratteristiche:<br />
• ulcerazioni fessuriformi serpigginose,o a pugnalate,cioè PICCOLE ma PROFONDE perchè<br />
c’è interessamento a tutto spessore della parete, (transmuralità) che può dar luogo a<br />
complicanze:ulcerazioni, fistolizzazioni.<br />
Caratteristica importante è la segmentarietà di queste lesioni (ce ne accorgiamo anche all’indagine<br />
radiologica perkè i limiti distali e prossimali sono privi di lesioni.<br />
Ricordiamo inoltre l’aspetto macroscopico a selciato: grosse rilevature con solchi profondi.<br />
• La mucosa adiacente può dare reazioni di iperplasia rigenerativa o formazione dei FALSI<br />
POLIPI INFIAMMATORI, cioè rilevatezze sulla mucosa, legate all’ infiltrato infiammatorio<br />
• .Inoltre c’è edema della sottomucosa. Quest’ultima può reagire all’ insulto ulcerante e, come<br />
per un tentativo di difesa, si arma di fibre muscolari.<br />
• Infiltrati transmurali di linfociti eosinofili (importante per dd con rettocolite che si arresta alla<br />
sottomucosa,) coinvolgenti tonaca muscolare, sierosa, sottosierosa , grasso periviscerale.<br />
• Vasculite:infiltrati peri o intravascolari<br />
• Granuloma a cellule giganti:questa reazione è presente nel 40 50% dei casi, dunque non è<br />
patognomonica. La forte componente eosinofila è una caratteristica degli infiltrati.<br />
È visibile l’aspetto caratteristico delle fibre muscolari che si sfioccano per infiltrazione dei<br />
linfociti.<br />
Complicanze: fistole intestinali o nel tratto genitale, perfino nello stomaco. Displasia o cancro<br />
(ma incidenza è molto bassa).<br />
Manifestazioni extraintestinali: trattasi sempre di ulcere a varie localizzazioni:<br />
cavo orale, uveiti, cute, con lesioni tipiche quali pioderma gangrenoso, eczemi refrettari, dermatite<br />
eczematoso per reazioni ulceranti o fistolizzanti granulomatose e non.<br />
Reazione particolare: spondilite anchilosante,aspetto di colonna vertebrale a canna di bambù per la<br />
calcificazione dei legamenti vertebrali.<br />
Epatopatie di vario tipo.<br />
Rettocolite ulcerosa<br />
È più frequente del Crohn.<br />
Incidenza in ascesa, 7-10casi per 100mila all’anno. La prevalenza è di 80 150casi per 100mila.<br />
Ci sono due picchi : in età giovanile 20 40 anni, ma anche in età pediatrica e in età avanzata sopra i<br />
60 anni.<br />
sede:sigma, retto, appendice ma anche ano.<br />
Talvolta la sovrapposizione di sedi quali ntestino tenue e crasso per rettocolite e morbo di crohn<br />
rende difficile dd tra le due.<br />
scaricato da www.sunhope.it
Evoluzione classica in 3 stadi clinici e anatomo patologiche.<br />
• Fase acuta: che è quella più specifica e quindi per l’ anatomo patologo è più facile far<br />
diagnosi.<br />
Predominano gli infiltrati infiammatori. Le emorragie sono superficiali ,riguardano la mucosa e la<br />
sottomucosa e danno luogo a melena, emissioni di sangue e muco.<br />
Le ulcere sono di forma irregolare e superficiali.<br />
Sono presenti anche qui pseudopolipi infiammatori nelle aree indenni.<br />
• Fase avanzata: c’è una risoluzione della fase precedente infiammatoria con comparsa di<br />
fibrosi e stenosi cicatriziali<br />
• fase di risoluzione e quiescenza: non osserviamo né infiammazione nè ulcerazione ma una<br />
particolare forma di atrofia.<br />
Aspetti istologici:<br />
fase acuta:<br />
• l’aspetto tipico è l ascesso criptico, cioè intraghiandolari. Ci sono cioè granulociti all’interno di<br />
cripte. Se li troviamo fuori non è diagnostico!<br />
• Iperplasia rigenerativa in alcune aree.<br />
• Atrofia<br />
• ulcere superficiali (mucosa e sottomucosa)<br />
• Infiltrati stromali (linfociti. Granulociti, plasmacellule, macrofagi) fermi alla sottomucosa..<br />
Talora follicoli<br />
• a volte,c’è la presenza in intestino crasso una metaplasia a cellule di Paneth<br />
• pseudopolipi<br />
• tonaca muscolare indenne<br />
• diffusione delle globbet-cells<br />
Fase di risoluzione e di quiescenza:<br />
scomparsa di infiammazione<br />
• c’è atrofia particolare: solitamente le strutture ghiandolari si dispongono perpendicolarmente<br />
alla superficie.<br />
In questo caso le strutture ghiandolari hanno un alterazione di questa disposizione, con<br />
ramificazioni e strutture che gemmano da cripte.<br />
• Metaplasia di paneth<br />
• atrofia in porzione inferiore,(cioè in zona di mucosa + vicina a muscolaris mucosae)<br />
• iperplasia a cellule neuroendocrine<br />
• a livello del connettivo della mucosa può comparire presenza di tessuto adiposo.<br />
Nessuno di questi caratteri è distintivo per questo motivo l’ anatomo patologo dice:” il quadro è<br />
compatibile con”<br />
complicanze:<br />
• perforazione con peritonite, ma è rara<br />
• ascessi<br />
• magacolon tossico,complicanza grave e acuta perchè si determina una grave ullcerazione, una<br />
necrosi di un tratto esteso intestinale coinvolgente mucosa e sottomucosa con stato di grave<br />
scaricato da www.sunhope.it
sofferenza che richiede intervento immediato per evitare shock tossico<br />
• trombosi venosa<br />
problema più grave: la displasia. Ricordate che la displasia grave è ad alto rischio di evoluzione in<br />
cancro.<br />
Dopo 10 anni da insorgenza di rettocolite il rischio aumenta notevolmente. Dunque è legato anche<br />
all’età del paziente, all’estensione della lesione. Caratteristiche di tale neoplasia sono le mutazioni<br />
di p53, di oncogene k ras<br />
Tali cancri sono in genere poco differenziati,aggressivi, inoperabili.<br />
COLITE ISCHEMICA: Spesso viene confusa con crohn o colite ulcerosa. È localizzata a livello<br />
delle flessure,in particolare la flessura splenica, dove c’è una maggiore mobilità e quindi è + facile<br />
avere una torsione Ma può esserci anche causa aterosclerotica, situazione infartuale acuta o<br />
cronica.<br />
Caratteristiche:Edema della mucosa molto spiccato. Vasi residui molto emorragici.<br />
colite pseudomembranosa: causata da clostridium difficile,in soggetti in cui c’è un’ alterazione<br />
della flora batterica intestinale causata uso smodato di antibiotici che favorisce attecchimento di<br />
clostridium.<br />
pseudomelanosi coli: legata a uso di particolari lassativi. Può simulare una lesione pigmentata.<br />
Colite cistica profonda: legata a presenza di cisti mucose a livello di mucosa che assume delle<br />
irregolarità che possono arrivare fino a necrosi.<br />
ulcera solitaria del retto:patologia rara, presente nel retto, causa sconosciuta ma non ha alcune<br />
correlazione con rettocolite.<br />
I polipi intestinali<br />
sono molto frequenti.<br />
Distinti macroscopicamente in<br />
-sessili, cioè con larga basa d’impianto che poggia direttamente su mucosa sottostante<br />
-peduncolati, cioè con un peduncolo che è facilmente asportabile, imprigionando la base<br />
d’impianto.<br />
Classificazione:<br />
• iperplastici, legati a un disordine cinetico<br />
• amartomatosi, legati a un disordine strutturale, di derivazione embrionale per cui c’è un errore<br />
soprattutto di tipo quantitavo nella strutturazione del polipo<br />
• infiammatori<br />
• neoplastici, o ADENOMI. Sono questi i veri polipi.<br />
Hanno potenziale evolutivo intrinseco verso il cancro.<br />
Questi polipi possono essere tubulari, formati soprattuto da strutture ghiandolari<br />
villosi se hanno digitazioni che conferiscono tale aspetto.<br />
scaricato da www.sunhope.it
Misto tubulo- villoso<br />
adenoma piatto, non molto rilevato sul piano della mucosa<br />
Caratteristica comune di questi ultimi polipi è la displasia che li distingue da tutti gli altri.<br />
Hanno un potenziale biologico di trasformazione molto forte(potenziale intrinseco)<br />
Costituiscono una condizione precancerosa(potenziale estrinseco)<br />
E’possibile quantificare il rischio e valutare la possibililtà di evoluzione in cancro per capire se<br />
asportare o meno il polipo.<br />
Un ulteriore categoria è costituiti dai polipi serrati suddivisi a sua volta in sessili e peduncolati.<br />
POLIPO IPERPLASTICO. Siccome c’è intorno alla ghiandola una struttura fibrosa e siccome c’è<br />
un disordine di cinetica cellulare con rapporto a favore di proliferazione e non di differenziamento,<br />
aumenta il numero di cellule. Si forma una struttura a scala che aumenta la superficie utile in modo<br />
che in quella struttura ci possano abitare più cellule. Se facciamo il K i 67 che è è un marcatore<br />
cinetico, avremo una conferma di questo disordine cinetico. Si associano anche altre<br />
alterazioni:mutazioni di k ras apc p53.<br />
Alcune volte non cogliamo più le globbet cells perchè c’è un’accellerazione del turnover cellulare<br />
cioè le cellule non fanno in tempo a specializzarsi, dunque c’è un’immaturità degli elementi<br />
celllulari che vanno successivamente in necrosi.<br />
Sono sessili spesso multipli, con diametro piccolo. Non hanno potenziale di trasformazione<br />
intrinseco in cancro.<br />
Ma hanno comunque una condizione di rischio perchè c’è un disordine cinetico di fondo.(a<br />
conferma della teoria di knudson della cancerogenesi in due tempi secondo cui c’è prima un<br />
disordine cinetico che costituisce un terreno favorevole allo sviluppo della neoplasia poi subentra<br />
noxa neoplastica che si sovrappone a questo disordine cinetico.<br />
L’ esame bioptico delle mucose in prossimità della lesione neoplastica evidenzia un disordine<br />
proliferativo, a sostegno appunto di questa teoria.<br />
Il polipo giovanile<br />
esce fuori con le feci perchè è spesso peduncolato (tipico dei bambini piccoli)<br />
Ha un lungo peduncolo ben vascolarizzato che può facilmente decapitarsi e uscire fuori durante la<br />
defecazione. È una forma di amartoma perchè mantiene la struttura intestinale ma c’è un disordine<br />
dell’epitelio che tende a formare delle cisti. Non è una lesione precancerosa né una lesione di<br />
rischio.<br />
È un polipo formato da fibrocellule provenienti dalla muscolaris mucosae che a causa di un errore<br />
embriologico tendono ad arborizzare formando la struttura portante del polipo.<br />
Sindrome di peutz-jeghers (poliposi): colpisce in età giovanile.<br />
È caratterizzata da pigmentazione a livello dell ‘e labenson(?) circum orale + polipi multipli +<br />
fibrocellule muscolari che partono dalla muscolaris mucosae e vanno all’ interno. Dunque a causa di<br />
questo disordine cinetico, c’è una predisposizione al cancro,il rischio è aumentato ma non insorge<br />
sul polipo bensì in altre sedi.<br />
scaricato da www.sunhope.it
LEZIONE N.17 6/5/2011<br />
ANATOMIA PATOLOGICA<br />
POLIPI E CANCRO INTESTINALE<br />
Questo è un argomento importante in quanto i polipi intestinali sono frequentissimi, soprattutto nei<br />
soggetti di età superiore ai 60 anni.<br />
Un concetto che vorrei assimilaste è quello del potenziale intrinseco e di indicatore di rischio, è<br />
molto importante perchè ha conseguenze cliniche rilevanti in quanto, nel caso in cui viene asportato<br />
un polipo ed esaminatolo sappiamo che non è cancro, abbiamo risolto il problema solo localmente<br />
ma non possiamo essere certi che nella restante parte della mucosa non si sviluppi il cancro, tale<br />
rischio è in proporzione a fattori legati al polipo di cui tra poco parleremo. Non solo è una spia che<br />
si accende per tutto l'intestino ma dobbiamo anche capire di che tipo di allarme si tratti.<br />
Nei polipi neoplastici o adenomi è implicito il concetto di displasia, non può essere polipo<br />
neoplastico se non c'è displasia. Vediamo ora cosa si intende per displasia: qui si vede un epitelio<br />
normale con globet cell che trapassa in un tipo di epitelio displastico → innanzitutto nell'epitelio<br />
normale c'è una dislocazione basale dei nuclei o parabasale, cioè non proprio sulla membrana basale<br />
ma vicino ad essa, a mano a mano che passiamo nell'epitelio displastico questi nuclei sono molto<br />
più irregolari, l'epitelio diventa pseudostratificato, i nuclei aumentano notevolmente quasi a<br />
raggiungere tutto lo spessore, questa rappresenta una displasia di lieve grado perchè quella di alto<br />
grado si distingue subito in quanto assimilabile a un carcinoma in situ.<br />
L' ADENOMA TUBULARE : è fatto da strutture tubulari displastiche, scendendo verso il basso vi<br />
rendete conto che non sono più displastiche riconoscete anche un asse di connettivo<br />
vascolare,questo tipo di adenoma è in prevalenza peduncolato. Il rischio di carcinoma è pari al 2-3<br />
%.<br />
Nell' ADENOMA VILLOSO il rischio cresce moltissimo, questo tipo di adenoma è<br />
prevalentemente sessile, ha una strutturazione diversa caratterizzata da villosità con esile banda di<br />
tessuto connettivale e qualche vasellino e poi epitelio displastico sovrastante. Riconosciamo questa<br />
pseudostratificazione dell'epitelio, questa dislocazione anomala dei nuclei e l'aspetto macroscopico<br />
è digitiforme - villoso.<br />
L'ADENOMA TUBULO – VILLOSO ha un rischio intermedio, vedete dei villi e delle strutture<br />
ghiandolari. Il rischio di sviluppare il cancro è del 6 – 8 % per cui l'istotipo che ha maggiore rischio<br />
è quello villoso e, non è un caso che sia prevalentemente sessile e non peduncolato.<br />
L' ADENOMA PIATTO DEPRESSO è difficile individuarlo anche per l'endoscopista perchè<br />
apparentemente è un microadenoma appena rilevato, in questo caso c'è una displasia superficiale,<br />
mentre qui vedete una struttura ghiandolare normale, in quanto ci sono le cellule caliciformi ( globet<br />
cell ) e già questo ci fa dire che non è epitelio displastico. Questo tipo di adenoma è spesso<br />
associato a displasia di alto grado, presenta un' elevata attività mitotica e può essere associato a foci<br />
di carcinoma nella sottomucosa. É questa una forma di adenoma ad alto rischio.<br />
ADENOMA SERRATO : in passato questo tipo di adenoma, di cui non si sapeva niente, veniva<br />
classificato come adenoma misto perchè aveva una strana associazione di aspetti iperplastici e<br />
displastici. Qui è possibile vedere questo aspetto a scala dovuto all' iperplasia e sotto ghiandole<br />
displastiche, per questo veniva chiamato polipo misto iperplastico adenomatoso. Oggi tale polipo<br />
viene chiamato serrato in quanto la displasia, che già di per sé ha un elevato potenziale mitotico, si<br />
associa all'iperplasia. Per tale motivo le ghiandole proliferano, si ramificano e lo stroma interposto<br />
diventa molto scarso, le ghiandole stanno una accanto all'altra secondo quello schema che avevamo<br />
scaricato da www.sunhope.it
definito già per l'endometrio come back to back. Nel 6% dei casi di cancro, nelle aree di mucosa<br />
adiacenti al cancro, possiamo trovare questo tipo di adenoma, in altri casi un polipo iperlpastico. Per<br />
tale motivo in passato veniva anche denominato polipo sentinella, a dimostrazione che spesso la<br />
malattia è sistemica e coinvolge tutto l'intestino. Ha un particolare profilo molecolare in quanto si<br />
associa a mutazioni del K – Ras, l'instabilità dei microsatelliti, mutazione del gene APC, del gene<br />
BRAF, dei geni che controllano il TGF – Beta e altri geni che sono coinvolti nella riparazione del<br />
danno del DNA( questi ultimi hanno un ruolo importante nel determinismo dei polipi e della<br />
sequenza adenoma – carcinoma ). Anche il Ki67 è alterato. L' adenoma serrato ha un rischio ancora<br />
più elevato di sviluppare il cancro rispetto a quello villoso.<br />
Il quesito a cui bisogna rispondere è questo: un carcinoma che si sviluppa su un polipo è un vero<br />
cancro e come ci si comporta?<br />
Dobbiamo distinguere innanzitutto il polipo peduncolato da quello sessile, tra quelli peduncolati<br />
abbiamo:<br />
• cancro di serie A ( il massimo della malignità) si ha quando raggiunge la base<br />
d'impianto che corrisponde alla mucosa e sottomucosa adiacente, cioè al punto di origine<br />
del polipo. É importante in quanto la vera malignità si esplica proprio in questo caso<br />
perchè a livello della sottomucosa e mucosa adiacente c'è una grande ricchezza di vasi. Un<br />
cancro di questo tipo ha bisogno di resezione chirurgica per reintervento.<br />
• Un cancro di serie C quando non interessa neanche l'asse connettivo – vascolare che<br />
è la testa del polipo ma si esaurisce all' interno della lamina propria, nel connettivo<br />
adiacente alle ghiandole displastiche. (Il presidente Reagan ebbe un cancro di serie C ).<br />
• Un cancro di serie B si ha quando interessa l'asse connettivo – vascolare.<br />
Nel polipo sessile invece, poiché non ha peduncolo, le cellule atipiche possono arrivare più<br />
facilmente là dove c'è il pericolo, abbiamo solo serie A e B:<br />
• serie A quando arriva alla sottomucosa,<br />
• serie B quando la malignità non arriva alla sottomucosa ( potenziale di malignità<br />
ridotto ).<br />
Dunque è essenziale, per capire la natura di un polipo, esaminare la base d' impianto perchè solo<br />
così facendo escludiamo la serie A.<br />
Giovanni Paolo II ebbe un polipo intestinale peduncolato di tipo tubulo – villoso , venne esaminato<br />
in sezioni seriali pari a 6 micron che permisero di escludere l'invasività proprio per il mancato<br />
coinvolgimento della base d'impianto.<br />
Ricorda → per legge i pezzi e le sezioni appartengono al paziente e devono avere lo stesso rispetto<br />
che si ha per il corpo umano, l'archivio di anatomia patologica è anche chiamato biobanca, i vetrini<br />
istologici devono essere conservati per 25 anni. Gli archivi di tessuti sono importanti per gli studi di<br />
nuovi marcatori e nuovi farmaci.<br />
I PARAMETRI CORRELATI AL RISCHIO:<br />
• ISTOTIPO → villoso 18 %<br />
tubulare 13%<br />
piatto e serrato ( non abbiamo casistiche grandi per quantificarlo precisamente ma<br />
sicuramente maggiore di quello villoso ).<br />
• DIMENSIONI → polipo < 0,5 cm possiamo trovare un carcinoma invasivo nello<br />
0.5% dei<br />
casi;<br />
“ 0,6 – 2 cm possiamo trovare il cancro nel 5% dei casi<br />
“ > 2cm possiamo trovare il cancro nel 10% dei casi.<br />
• MARDINI DI ESCISSIONE<br />
• GRADO DI DISPLASIA → l'alto grado di displasia lo troviamo nel villoso nel 16%<br />
dei casi , mentre nell'adenoma tubulare la ritroviamo in meno del 3% dei casi.<br />
scaricato da www.sunhope.it
Abbiamo poi tutta una serie di mutazioni che riguardano il K- Ras, la p53, l'APC ( gene<br />
oncosoppressore molto importante nel cancro del colon – retto ), i geni che codificano per il TGF e<br />
mutazioni dei cromosomi 12, 16, 18 e 17, particolarmente il 17 che tende a perdere pezzi.<br />
Delle varie poliposi non parliamo perchè le trovate sul libro, sono rare, la poliposi familiare è legato<br />
al gene APC, in queste patologie il rischio ti cancro è così elevato che è giustificato l'intervento<br />
chirurgico di profilassi e, quando si opera, c'è recidiva nel 59% dei casi, per cui bisogna fare un<br />
intervento che sia il più ampio possibile perchè coinvolge tutto l'intestino. ( Delle altre poliposi devi<br />
sapere solo definizione ).<br />
CARCINOMA COLON – RETTO<br />
Aree ad altro rischio: Europa, Australia, America.<br />
Aree a basso rischio: Cina.<br />
É il secondo cancro più frequente in entrambi i sessi, dopo quello del polmone nel maschio e quello<br />
della mammella nella donna. Per quanto riguarda la mortalità il polmone è quello che fa la parte<br />
principale sia nel maschio che nella femmina, poi viene la prostata per il maschio e la mammella<br />
per la femmina e poi viene il colon – retto che si attesta ad una mortalità del 9%.<br />
Questi dati non risentono del follow up delle nuove terapie biologiche che vengono usate nel cancro<br />
del colon – retto che hanno certamente migliorato la situazione. In Italia l'incidenza è di 45/100.000<br />
casi, più di noi il Giappone, la Geramania, l' Australia, la Francia sta un po' al di sotto di noi.<br />
L'incidenza è stazionaria in Italia mentre ci sono Nazioni dove c'è la tendenza al decremento<br />
dell'incidenza, sono quelle Nazioni in cui è stata applicata la prevenzione secondaria come la<br />
colonoscopia e la ricerca del sangue occulto nelle feci. I fattori genetici sono molti e sono correlati a<br />
quelle sindromi sulle quali abbiamo sorvolato come la poliposi adenomatosa familiare o il cancro<br />
ereditario non polipoide ( cioè quello che non passa attraverso il polipo ). Nel cancro sporadico<br />
sono coinvolti dei geni oncosoppressori come i geni APC, p53, Ras, c – myc e poi meccanismi di<br />
metilazione perchè attraverso la iper o ipometilazione possiamo avere il silenzio o l'iperespressività<br />
epigentica.<br />
Sono 2 le principali precancerosi, la poliposi e la displasia della rettocolite ulcerosa.<br />
Le strategie per la diagnosi precoce prevedono la ricerca del sangue occulto nelle feci che dà<br />
numerosi falsi positivi per cui prevede una strategia in 2 tempi, prima il sangue occulto e poi<br />
colonoscopia che deve definire se c'è qualcosa o no, ma essendo un programma molto costoso, è<br />
stato applicato solo su piccoli territori. I segni clinici sono in rapporto alla sede della lesione: se<br />
infatti la lesione riguarda il colon ascendente o il cieco, poiché in questa sede il cancro dà poco<br />
fastidio, può dar luogo ad anemia per perdita ematica e solo in una fase molto avanzata si può<br />
apprezzare e per questo solitamente vengono riscontrati in fase avanzata. Se riguarda il colon<br />
discendente possiamo avere emorragie, incontinenza, dolore, ostruzioni. Se riguardano il retto uno<br />
dei primi segni è il cambio del calibro e di forma delle feci, tenesmo e massa rettale. Possiamo<br />
ricostruire la storia che determina il passaggio dal polipo al cancro: il polipo raramente è unico, si<br />
sviluppa inizialmente una displasia lieve e via via nel tempo aumentano le atipie citologiche fino ad<br />
arrivare al cancro. Uno dei primi geni a modificarsi è l'APC e i meccanismi sono legati alla<br />
riparazione dei danni del DNA, poi ci sono alterazini legate alla metilazione ma già nell'adenoma<br />
troviamo modificazioni del K – Ras, del p53 e nel cancro si ha tutta una serie di mutazioni che si<br />
accumulano nel tempo, soprattutto delezioni, cioè si ha una perdita di pezzi nel tempo. La<br />
mutazione del gene APC è presente nell'85% dei casi, mutazioni del gene Ras interviene nel 35 – 45<br />
% dei casi, mutazione di alcuni geni coinvolti nella riparazione del DNA interviene anche nel 35 –<br />
40% dei casi e anche il gene BRAF in una minoranza di casi. Le forme sono:<br />
• vegetante<br />
• ulcerante<br />
• ulcero – vegetante<br />
• infiltrante, la più subdola per cui macroscopicamente non si vede niente se non un<br />
ispessimento della parete, molto spesso questa forma è legata, come abbiamo detto per lo<br />
stomaco, a quei carcinomi a cellule ad anello con castone, carcinomi mucoidi, molto<br />
scaricato da www.sunhope.it
aggressivi che tendono a diffondere a macchia d'olio prima di dare uno sviluppo estrinseco<br />
del cancro.<br />
La sede principale è il sigma - retto che da solo rappresenta oltre la metà dei cancri, poi via via<br />
vengono gli altri tratti ascendente, discendente, trasverso e così via.<br />
Il follow up a 5 anni in media è del 50%, il rischio di recidiva è molto alto, in questo caso non si<br />
tratta di recidiva tecnica ( legata ad errore del chirurgo ) ma è una recidiva biologica perchè un po'<br />
tutta la mucosa partecipa a questo disordine cinetico – proliferativo . Il rischio di recidiva a 5 anni è<br />
del 50% considerando che il cancro principale è l'adenocarcinoma, il follow up G1, G2, G3, va<br />
dall'80% al 25%, quindi anche il grading ha un ruolo prognostico.<br />
Il CARCINOMA SERRATO anche nel cancro mantiene questo carattere serrato, le cellule stanno<br />
una addosso all'altra ma se vogliamo la conferma molecolare andiamo a ricercare la metilazione dei<br />
recettori accoppiati alle cellule G. Si manifesta soprattutto nelle femmine più anziane, generalmente<br />
non è però un cancro molto aggressivo. Gli altri tipi di cancro sono :<br />
• MUCOIDE<br />
• AD ANELLO CON CASTONE<br />
• TUMORI NEUROENDOCRINI BEN DIFFERENZIATI O A PICCOLE CELLULE<br />
che nel colon – retto raggiungono elevate dimensioni. Spesso nel colon – retto possiamo<br />
avere dei tumori misti, cioè caratterizzati da una componente epiteliale e una<br />
neuroendocrina.<br />
Altri tipi di carcinoma:<br />
• BASALIOIDE → chiamato anche con un termine antico CLOACOGENICO perchè<br />
è un tipo di cancro più frequente nell'ano, è un tumore del retto basso ed è un cancro a<br />
cellule basalioidi.<br />
• MIDOLLARE → povero di stroma, presenta solo cellule.<br />
• GIST<br />
• TUMORI MUSCOLARI<br />
• SARCOMA DI KAPOSI → a livello del colon – retto solo nei pz immunodepressi<br />
( affetti da AIDS o sieropositivi ).<br />
• METASTASI da: melanomi, cancro del polmone, cancro del rene, cancro della<br />
prostata, mesotelioma.<br />
CANCRO CLOACOGENICO: sono cellule basalioidi che non hanno la tendenza a formare<br />
cheratina e questo lo dimostra la mancanza di eosinofilia.<br />
PARAMETRI PROGNOSTICI:<br />
• lo stadio<br />
• i margini di escissione<br />
• grading<br />
• emboli<br />
Tra i non morfologici:<br />
• K – Ras<br />
• p53<br />
• iperespressione dell' HER – 1 cioè del recettore dell' EGF<br />
• aploidia<br />
• Bcl – 2<br />
STADIAZIONE TNM:<br />
T1 → cancro che coinvolge la mucosa e può coinvolgere anche la sottomucosa;<br />
T2 → raggiunge gli strati muscolari ma non li supera;<br />
T3 → supera la tonaca muscolare e arriva alla sottosierosa;<br />
T4 → supera tutta la parete;<br />
N1 → positività ai linfonodi regionali fino a 3 linfonodi;<br />
N2 → 3 linfonodi metastatizzati.<br />
scaricato da www.sunhope.it
Questi linfonodi si ritrovano nel grasso periviscerale, i linfonodi metastatizzati appaiono più grandi<br />
e bianchi mentre normalmente sono piccoli e grigiastri.<br />
ASCC ( Associazione Americana Contro il Cancro ) - TNM:<br />
Follow up Metastasi<br />
I T1,T2.N0,M0 >90% ( sulla slides è sbagliato ) il 40%.<br />
IV ogni T,ogni N,M1 → il follow up
scaricato da www.sunhope.it
Lezione 18 del 12 maggio<br />
Parlando di apparato digerente facciamo adesso fegato e pancreas<br />
Fegato<br />
Concetti di base del fegato<br />
Se noi guardiamo una sezione istologica di fegato noi vediamo innanzitutto queste aree qui chiamate<br />
portali in cui riconosciamo del tessuto fibroso nel cui contesto ci stanno 3 particolari elementi: l’arteriola<br />
epatica, la venula portale e il duttulo biliare. L’arteriola si distingue subito perché presenta una parete<br />
robusta, mentre la venula ha una parete molto sottile perché non deve esercitare quella pressione che<br />
possiamo ritrovare nel sangue arterioso. Più in la vediamo un’altra struttura una venula, una volta chiamata<br />
venula centrolobulare poiché 30-40 anni fa si credeva che il centro di tutto fosse questa venula poi si è visto<br />
che è invece l’area portale il centro di tutto. Lo spazio portale è qui raffigurato in misura esagonale, in<br />
effetti nell’uomo non è mai così esagonale, mentre invece è perfettamente esagonale nel maiale. Vi sono<br />
degli spazi in cui non ci sono le aree portali che prendono il nome di punto nodale di Mall. Ora se è con<br />
l’acino epatico, è rappresentato secondo la concezione all’epoca rivoluzionaria di rappaport, perché il<br />
sangue che porta energia è il sangue arterioso e parte dalle aree portali, possiamo riconoscere un area 1, 2,<br />
3 a seconda del livello d’irrorazione, le aree più in salute sono le aree 1 che ricevono il sangue per prime, le<br />
aree 2 stanno così e così, le 3 sono quelle più distanti, tant’è vero che nelle epatopatie tossiche sono queste<br />
le aree centrolobulari quelle che soffrono per prima e vanno più frequentemente in necrosi. Quindi si<br />
capovolge il concetto non più una venula al centro ma l’area portale, in senso circolare l’area 1 è quella<br />
meglio irrorata, mentre i punti nodali corrispondono all’area 3 quelli più distanti dalle aree portali. Se<br />
vogliamo dare una rappresentazione tridimensionale scopriremo che le cellule epatiche hanno una<br />
struttura laminare di lamine bistratificate, tra queste lamine decorrono i sinusoidi epatici che hanno una<br />
parete particolare molto fenestrata per consentire uno scambio senza alcuno ostacolo tra cellule epatiche e<br />
sinusoidi e non hanno neanche una membrana basale, tra due strati di cellule epatiche decorre dall’altro<br />
versante il canalicolo biliare che inizialmente è solo uno spazio virtuale che diventa canalicolo solo nella<br />
parte terminale adiacente all’area portale, qua il flusso è inverso perché la bile si forma e va versato nel<br />
canalicolo biliare poi salire tutto a colecisti, tutto il resto dotti biliari principali, secondari e così via. Ma cosa<br />
scorre in questi sinusoidi? Ci sono degli sfinteri tra i due sistemi, tra arteriola epatica, sinusoidi e le venule,<br />
a seconda dello stato di questi sfinteri di questa regolazione, può circolare, abbiamo un flusso intermittente<br />
per cui nel sinusoidi possiamo trovare sangue arterioso venoso o misto, perché abbiamo un complesso<br />
sistema di sfinteri e tutti sono collegati tra di loro (sistema arterioso e venoso inteso sia come venula<br />
portale e centrolobulare), tutto ciò ci spiegherà la dinamica della cirrosi. Il sangue venoso va dall’area<br />
portale verso la venula centrolobulare, mentre il canalicolo biliare va dalle aree centrolobulari dove viene<br />
prodotta la bile che viene versata nel canalicolo biliare. Tra le due lamine epatiche al centro c’è questo<br />
spazio biliare che nell’ultimo tratto diventa il canale di Hering che è un precanalicolo biliare e poi si versa<br />
nel canalicolo biliare dell’area portale, invece sul versante endoteliale laddove stanno i sinusoidi c’è uno<br />
spazio tra sinusoidi e epatociti chiamato spazio di Disse uno spazio molto fenestrato per consentire lo<br />
scambio tra i vasi e gli epatociti quindi è un connettivo molto lasso. Le cellule staminali del fegato che<br />
prendevano il nome di cellule ovoidali si vanno a piazzare nell’ultimo tratto dove stanno gli epatociti che<br />
costituiscono i due lati del canalicolo biliare, perché a seconda delle circostanze le stems cell possono<br />
differenziarsi in senso biliare, epatocitario, stromale e così via, stanno in una posizione strategica, poi le<br />
cellule che seguono si chiamano cellule transizionali e mano a mano che andiamo verso la vena epatica<br />
centrale le cellule si specializzano e muoiono, quindi gli epatociti altamente specializzati li troviamo nel<br />
tratto intermedio poi vanno in declino. Se andiamo a vedere un area portale ci sono le tre strutture<br />
fondamentali l’arteriola il canalicolo e la venula, inoltre c’è del connettivo qualche raro linfocita, ma la<br />
struttura fondamentale è la membrana limitante è una membrana costituita dagli stessi epatociti che con le<br />
loro membrane basali si dispongono a ridosso di questo tessuto connettivo che rappresenta l’area portale<br />
che contiene queste tre strutture fondamentali.<br />
scaricato da www.sunhope.it
Epatiti<br />
Le principali epatiti croniche, le epatiti acute andate a vedere quali sono i segni principali, che nella maggior<br />
parte dei casi si risolvono o evolvono in epatite cronica o ancora ci sono delle forme di epatiti fulminanti<br />
che all’autopsia si presentano con una necrosi massiva del fegato ma fortunatamente di verificano<br />
raramente, un epatopatia alcolica sarebbe più corretto chiamarla dismetabolica dove è sempre l’alcol ad<br />
essere implicato, le cirrosi, e i tumori del fegato<br />
Della colecisti abbiamo le colecistiti e i tumori dove porterete solo i dati essenziali<br />
La biopsia epatica si fa con l’ago di Menghini e si fa lungo il fianco in una determinata posizione, e bisogna<br />
fare attenzione poiché il fegato si muove e ruota su di un perno che è il diaframma per cui si rischia di<br />
lacerare il fegato con ematomi inarrestabile per la ricchezza vascolare del fegato.<br />
Alcune volte nell’area portale dove c’è un’infiammazione, si vede la venula ma non il canalicolo coperto da<br />
una struttura linfatica follicolare che delle volte hanno pure un centro germinativo: questa è una<br />
caratteristica particolare del virus C, l’epatite C si caratterizza proprio per questi aggregati follicolari delle<br />
volte anche con follicoli secondari ed è quella con rischio più frequente di evoluzione cronica a cirrosi,<br />
infatti in Italia l’HCV causa l’epatite cronica per il 60% dei casi, HBV poco meno del 10%, 12% alcol,<br />
ovviamente ci sono anche delle forme associate di virus e alcol che si potenziano tra di loro.<br />
Questi elementi eosinofili sono granulociti eosinofili che sono una caratteristica delle epatiti alcoliche<br />
insieme alla presenza di corpi acidofili chiamati corpi di Mallory e ad altre caratteristiche che non stiamo a<br />
dire.<br />
Un concetto fondamentale stabilito negli anni 70 da un infettivologa e anatomopatologa a proposito di<br />
membrana laminare è che le epatiti che andavano più frequentemente in contro ad un evoluzione<br />
cirrogena erano quelle che nella loro struttura presentavano non solo la portite ma quello che si chiama il<br />
così detto spill over cioè i linfociti che normalmente sono molto addensati nell’area portale in questo punto<br />
superano della membrana limitante, questo è il confine tra un epatite cronica persistente e un epatite<br />
cronica attiva, l’infiltrazione è molto marginale, in altri casi dall’area portale c’è uno sciamare di linfociti<br />
all’interno del parenchima ci sono aree di necrosi di distruzione questa è un epatite cronica attiva in una<br />
fase di intensa attività dove c’è lo spill over che si associa spesso alla necrosi della membrana limitante<br />
perché muoiono quegli epatociti che la formano per cause infiammatorie, talvolta la necrosi della<br />
membrana limitante è confluente, e poi può risolversi anche in una fibrosi che può essere attiva o passiva.<br />
Tutto il fegato si regge sull’impalcatura di un reticolo un tessuto connettivale molto sottile fatto da fibre<br />
molto sottili, laddove c’è la necrosi delle cellule questo reticolo collassa perché prima era in una condizione<br />
di elasticità poiché doveva sostenere poi gli elastici tesi finiscono col cedere e col collabire per cui<br />
determinano una fibrosi passiva data dal collasso di tutte queste fibre, fibrille che vengono compresse con<br />
trasformazione in tessuto connettivale fibroso. La fibrosi si dice attiva quando c’è un’attiva proliferazione di<br />
fibroblasti e miofibroblasti.<br />
Ciò che caratterizza le epatiti croniche è la necrosi a ponte, a monte c’è stato lo spill over, la necrosi della<br />
membrana limitante, poi la confluenza e possono essere porto-centrali cioè da un area centrolobulare cioè<br />
dalla venula all’area portale, possono essere porto-portali e possono essere centro-centrali, ad uno sguardo<br />
acuto si vede che la necrosi confluente più breve più corta è quella centro-centrale, questa necrosi<br />
ovviamente poi darà luogo a fenomeni di fibrosi che porteranno allo sconvolgimento dell’architettura e<br />
della funzionalità del lobulo epatico e quindi alla cirrosi, non è un caso che nelle epatiti alcoliche per<br />
esempio sono soprattutto le aree centrali, le aree adiacenti la venula centrolobulare quelle che vanno più<br />
frequentemente in necrosi le aree centro-centrali, come non è un caso che l’epatite alcolica porta a quella<br />
cirrosi che si chiama micronodulare cioè dei noduli di pochi millimetri quindi tutto il fegato sembra<br />
impallinato da piccoli nodi, mentre nella cirrosi post-epatica quella legata ai virus dell’epatite e così via<br />
sono più colpite le aree porto-centrali o porto-portali, quindi abbiamo che la cirrosi può essere macro o<br />
micro nodulare si ha l’alternanza di grandi e piccoli noduli.<br />
A noi clinici cosa interessa sapere? Lo stato della paziente, ha un epatite cronica, nella classificazione delle<br />
epatiti croniche sono stati introdotti dei concetti tipici dei tumori poiché se vogliamo la cirrosi è uno<br />
sconvolgimento del parenchima epatico che ha qualche dato comune con i tumori.<br />
C’è un grading e uno staging; nel grading il grado 1 ci dice che c’è un infiammazione portale o lobulare,<br />
lobulare significa vicino alla venula centrolobulare, senza necrosi quindi è un epatite cronica più tranquilla;<br />
il grado 2 lieve infiammazione periportale, è avvenuta un po’ di necrosi nella membrana limitante e questi<br />
scaricato da www.sunhope.it
linfociti vanno fuori dall’area portale e quindi coinvolgono marginalmente in questo caso gli spazi<br />
periportali con focale necrosi epatocellulare; il grado 3 è invece quando questa infiammazione e necrosi<br />
degli epatociti è ancora più massiva; il grado 4 invece quando troviamo quella necrosi bridging cosi detta a<br />
ponte con necrosi evidente di tutta la membrana limitante, è solo questione di tempo in questo grado a cui<br />
segue sempre la fibrosi.<br />
Invece il grado di fibrosi è lo staging: stadio 0 no fibrosi; stadio 1 c’è una fibrosi portale cioè riguarda solo lo<br />
spazio portale; stadio 2 la fibrosi è totale; stadio 3 c’è una fibrosi a ponte probabilmente completa ma non<br />
c’è un evidente distorsione tipica della cirrosi quindi c’è una situazione un po’ a ponte tra l’epatite cronica<br />
attiva e la cirrosi perché ci stanno dei setti ma non cono completi quindi non si delinea ancora il nodo<br />
cirrotico che è tutto circondato da fibrosi; lo stadio 4 è cirrosi quando proprio vediamo il nodulo alla biopsia<br />
anche se incompleto sopra e sotto, in blu il connettivo con evidente necrosi porto-portale poiché da una<br />
spazio portale andiamo ad un altro c’è ancora l’infiammazione, un po’ di fibrosi, se andiamo più avanti può<br />
scomparire l’infiammazione e determinarsi la fibrosi. Una cirrosi micro-macronodulare con noduli in tutto il<br />
fegato è soprattutto un problema post-epatitico che predomina dalle nostre parti mentre in nord italia<br />
prevale quella alcolica. Cirrosi micronodulare 3 mm è questo distacco che è una cirrosi alcolica. Un’istologia<br />
ad ampio respiro vediamo tutti i noduli, come l’architettura del parenchima epatico si è completamente<br />
sovvertita. Poiché c’è una distorsione di tutto il parenchima a volte vediamo una proliferazione di duttuli<br />
biliari che cercano in qualche modo di captare quello che possono captare perché tutto quel sistema di cui<br />
abbiamo parlato con questa architettura salta perché nello spazio di disse si perde la normale fenestrazione<br />
degli spazi sinusoidali, non solo ma questi sinusoidi acquisiscono la membrana basale e si va incontro al<br />
processo di capillarizzazione di questi sinusoidi e ciò implica che quegli scambi che si facevano prima ora<br />
non si possono più fare, inoltre nello spazio di disse noi notiamo anche una proliferazione di cellule<br />
fibroblastiche e miofibroblastiche che viene ad aggravare questo muro che si trova tra spazi sinusoidali ed<br />
epatociti, gli epatociti stessi che stanno qui vicino perdono gli epatociti che pescano nei sinusoidi perché<br />
hanno una superfice villosa villi sul citoplasma, e poi si depositano e lo spazio di disse si dilata<br />
enormemente, ovviamente se mettiamo anche insieme la fibrosi delle aree portali quindi la compressione<br />
di tutti i sistemi delle resistenze, tutta la circolazione epatica, venosa viene tutta sconvolta, per il<br />
cambiamento di queste situazioni emodinamiche quella anastomosi si potenziano quindi avremo degli<br />
shunt artero-venosi, un aumento della resistenza a livello dei sinusoidi che poi sarà responsabile<br />
dell’ipertensione portale, caput medusae, ascite e tutto il resto. La ridotta irrorazione degli epatociti<br />
determina una ridotta funzionalità degli epatociti causa a sua volta di tutta una serie di problemi, per<br />
esempio l’inattivazione nel fegato di particolari ormoni se non avviene c’è la persistenza di aldosterone<br />
ormone antidiuretico e c’è una ritenzione idrosalina, c’è anche una mancata disintossicazione e andiamo<br />
incontro poi ad encefalopatie cosiddetta porto-sistemica poiché queste sostanze tossiche possono superare<br />
la BEE e arrivare al cervello. La cirrosi è una condizione con alta precancerosità, i pazienti vanno seguiti per<br />
le complicazioni quali ipertensione e altre, ma soprattutto per lo sviluppo a cancro che è frequente, dalle<br />
nostre parti il cancro epatico più frequente è quello su cirrosi, in cui all’improvviso uno dei tanti noduli<br />
cirrotici che ci stanno manifestano già alterazioni displastiche classiche come abbiamo già visto in altri<br />
organi possono poi diventare cancro, in altri paesi come asia e america abbiamo il cancro epatocellulare su<br />
fegato sano con una sola massa legato ad aflatossine e altre sostanze alimentari, quello su fegato cirrotico è<br />
multicentrico per ovvi motivi perché è colpito un po’ tutto il fegato. Nel passaggio da cirrosi a displasia a<br />
carcinoma epatocellulare c’è un rischio per anno di avere il cancro in pazienti cirrotici pari al 3-5% dei<br />
pazienti moltiplicate questi dati per 10 anni e vedete che il rischio diventa molto alto.<br />
Le principali lesioni tumorali del fegato<br />
L’iperplasia focale nodulare è una situazione molto strana in cui anche l’ecografista si può spaventare in cui<br />
vede un nodulo non ben circoscritto che è stato associato con dati molto contrastanti all’assunzione della<br />
cosiddetta pillola anticoncezionale.<br />
L’adenoma epatocellulare si differenzia dal cancro e dal parenchima epatico normale perché non ha una<br />
chiara delimitazione capsulare perché ci mancano le aree portali e quindi non è proprio un fegato normale<br />
Il carcinoma epatocellullare ha tutta una varietà da perdere il cervello, quello giovanile si chiama<br />
fibrolamellare o oncocitico perché ha uno stroma fibroso parallelo di fibre connettivali parallele e questi<br />
scaricato da www.sunhope.it
tralci di connettivo circoscrivono delle aree neoplastiche di epatociti che spesso assumono anche un<br />
aspetto oncocitario con citoplasma molto abbondante<br />
Il colangiocellulare ha un architetture più ghiandolare che ricorda vagamente i duttuli biliari e che<br />
l’epatocellulare non ha<br />
Il misto e poi tutta una serie di tumori di vario tipo<br />
Uno benigno molto pericoloso è l’angioma cavernoso perché raggiunge in genere grosse dimensioni e va<br />
tolto con molta prudenza perché se si buca vengono fuori delle emorragie anche mortali perché è un<br />
angioma ricchissimo di lacune e di sangue.<br />
Pancreas<br />
La pancreatiti acute e croniche, tumori del pancreas esocrino, cenni del pancreas endocrino<br />
La funzione del tumore endocrino è correlata alla potenza cioè a seconda del marcatore neuroendocrino<br />
vip, bombesina, noi possiamo sapere questo tumore più che sulla morfologia che atteggiamento c’ha sotto<br />
il profilo dell’aggressività.<br />
Il pancreas normale ha una componente esocrina, le insule pancreatiche rappresentano la componente<br />
endocrina, le insule esocrine sono granuli che producono molti tipi d’enzima, dei duttuli pancreatici<br />
Una patologia rara ma molto grave la necrosi pancreatica acuta emorragica che rappresenta una causa di<br />
morte non trascurabile, la patogenesi non è del tutto definita, c’è un aumento dell’incidenza in pazienti che<br />
abusano di alcol<br />
Una caratteristica: ci troviamo vicino all’omento e ci sono delle macchie bianche, una pancreatite acute<br />
determina la liberazione di questi enzimi e avviene un autodigestione, produce lipasi e altri enzimi, le lipasi<br />
andando sul tessuto adiposo ampiamente diffuso a livello peritoneale può determinare questi focolai di<br />
steato-necrosi detti a goccia di cera lungo tutto il mesentere oppure determinare delle aree di necrosi<br />
emorragica legata in questo caso ad una necrosi più proteica che può dare luogo ad un meccanismo di selfperpetuation<br />
per cui il soggetto arriva a morte in poco tempo.<br />
Prostata<br />
La strutturazione anatomica<br />
La classificazione anatomica che voi avete fatto in anatomia ha scarso valore funzionale dal punto di vista<br />
clinico perché è più importante il modello cosiddetto di Mc Neal che divide la prostata in 3 regioni<br />
particolari, la prostata ha una capsula fibromuscolare, la divide in una zona di transizione indicata in giallo,<br />
quella che circonda per una buona metà della prostata l’uretra prostatica, questo crea confusione perché la<br />
zona centrale è considerata quella esterna a questa zona, quindi la zona transizionale che passa dal tessuto<br />
prostatico cioè dall’urotelio al tessuto ghiandolare, questa zona possiede una parte ghiandolare che<br />
costituisce il 5% del tessuto di tutte le ghiandole che stanno nella prostata che è una struttura ghiandolare<br />
come altri organi con una arborizzazione di dutti, dotti, acini; poi abbiamo la zona centrale che ha una zona<br />
del 25% delle ghiandole della prostata e poi la zona periferica esterna diciamo che ha il 75% delle<br />
ghiandole; di forma piramidale con una base di 4 cm, un apice grossomodo arrotondato e una lunghezza di<br />
3 cm, in condizioni normali in rapporto alla variabilità costituzionale è di 20-25 gr. Secondo il modello di Mc<br />
Neal se facciamo una topografia alla prostata noi vedremo al centro l’uretra, e intorno all’uretra la zona<br />
transizionale, poi la zona centrale, siamo a livello della regione basale nella regione prossimale adiacente<br />
alla vescica, mentre la zona transizionale in questa zona è poco sviluppata, qui vedete i dotti eiaculatori e<br />
qui l’uretra; nella regione mediana s’incomincia a sviluppare di più la zona periferica si riduce la zona<br />
centrale e la zona transizionale, nella regione apicale della prostata che sta verso il basso scompaiono le<br />
altre zone troviamo solo la zona periferica; nella zona dove c’è il cosiddetto verum montanum, una<br />
particolare conformazione della prostata, nelle vicinanze sboccano oltre ai dotti eiaculatori anche i dotti<br />
prostatici; dal punto di vista della strutturazione ghiandolare i dotti principali della prostata in genere non<br />
sono mai più di 20; i dotti poi si sfioccano in duttuli secondari per finire poi negli acini, se andiamo a fare<br />
una risonanza magnetica una forma di diagnostica per immagini molto utilizzata per la prostata vediamo la<br />
vescica, la zona periferica è in genere la più ricca di ghiandole, la zona centrale, la zona transizionale,<br />
l’uretra e vedete l’attacco della vescichette seminali che in genere hanno questa situazione dall’alto verso il<br />
basso in posizione centrale nella prostata. Nella prostata troviamo anche tessuto fibromuscolare nello<br />
scaricato da www.sunhope.it
stroma però se andiamo a vedere come sono strutturate le ghiandole sono mucoidi talvolta soprattutto nei<br />
soggetti anziani possiamo trovare questi calcoli corpora amilacei perché molto ricchi di glicogeno e sostante<br />
saccaridi; una caratteristica fondamentale è oltre alle cellule ghiandolare c’è un anello di cellule cubiche che<br />
circonda, è una tipica architettura che abbiamo visto in altri organi in questo caso si chiamano cellule basali,<br />
quindi c’è una doppia stratificazione, queste cellule basali hanno anche una struttura mioepiteliale vedrete<br />
e che circondano le cellule ghiandolari propriamente dette, queste cellule dello strato cosiddetto basale<br />
esprimono la p63 come succedeva nella mammella e la citocheratina ad alto peso molecolare che non<br />
viene espressa invece dalle cellule ghiandolari particolarmente dette, questo è un parametro che è<br />
importante sapere. Le stems cell della prostata. Se noi andiamo a vedere come si diramano i dotti, c’è una<br />
parte prossimale, una intermedia e una distale e poi qui si formano tanti acini che sono le parti ghiandolari,<br />
noi possiamo ritrovare a livello della parte prossimale delle stems cell cosiddette di primo tipo, la parte<br />
iniziale dei dotti, mano a mano che andiamo nelle diramazioni secondarie troviamo le stems cell di secondo<br />
tipo, poi possiamo trovare anche delle cellule neuroendocrine affianco o interposte alle cellule staminali; la<br />
differenziazione tra cellule staminali primo e secondo tipo è molto importante lo vedremo poi nei tumori,<br />
quelle di primo tipo hanno maggiore capacità evolutiva, proliferative e differenziativa diciamo che sono le<br />
più totipotenti, possono evolvere e seguire varie linee differenziative e sono indipendenti dagli ormoni,<br />
mentre il secondo tipo che si trova in una parte intermedia è androgeno dipendente cioè incominciano a<br />
comparire in queste cellule i recettori per gli androgeni, questo concetto è alla base di tutta la terapia e<br />
l’evoluzione del cancro prostatico.<br />
Le prostatiti<br />
Le acute non ne parliamo proprio.<br />
Le croniche possono essere batteriche o autoimmunitarie, possono esserci anche virus e miceti, ma c’è una<br />
patologia molto emergente che la chiamiamo prostatite ma non è neanche chiaro se è una prostatite e ha<br />
dei disturbi che riguardano l’erezione, poi durante la minzione e che è legata allo stress, a particolari<br />
abitudini, come ad esempio nelle patologie testicolari già ve ne ho parlato anche il tipo d’indumento che<br />
s’indossano le aderenze e così via tali da determinare anche il cancro dei tessuti sessuali; le prostatiti sono<br />
una patologia molto diffusa e soprattutto le croniche sono anche difficilmente curabili poiché la ghiandola<br />
ha uno scheletro fibroso o fibromuscolare è difficile che gli stessi antibiotici possano intervenire in sede, ci<br />
sono dei trattamenti molto cruenti, molto pubblicizzati su internet che prevedono iniezioni dirette nella<br />
prostata. C’è un problema grosso non ancora risolto, che riguarda il fatto che certamente esiste una<br />
connessione tra intestino e prostata anche se non è stata dimostrata bene da un punto di vista anatomico,<br />
perché non raramente oggi poiché c’è anche un aumento della stipsi cronica legato a particolari abitudini<br />
alimentari ma legato anche a particolari esigenze lavorative per cui non c’è più la concentrazione che c’era<br />
una volta; per cui si determina un ipertono degli sfinteri anali, tutte patologie correlate sono tutte in<br />
aumento, per cui questo potrebbe determinare un inversione del flusso perché non raramente nella<br />
prostata, se uno si fa un esame dell’urina i batteri escono sempre anche se è stata raccolta in maniera<br />
asettica, perché molti urologi non conoscono un concetto banale, la presenza di batteri non giustifica il<br />
concetto di prostatite, per dire prostatite devo trovare gli anelli infiammatori, come trovare lattobacilli nel<br />
pap test, anche se non è dimostrato nella prostata ci sono escherichia coli in quantità.<br />
La malocoplachia è una particolare lesione che può colpire la prostata o la vescica e che è legata ad una<br />
presenza massiva di escherichia coli, ne parleremo più avanti, e determina tutta una serie di alterazioni che<br />
possono simulare il tumore, la sintomatologia è disturbi vari alla minzione, agli ureteri, eiaculazione<br />
dolorosa anche impotenza e poi la cosa più grave il PSA, ce n’è uno più specifico e uno meno specifico, ma<br />
basta che aumenta di un poco il PSA che ha un cut off molto basso, mi pare 4 o 5, appena arriva a 4,5 si<br />
scatena una paura terribile; anche la risonanza dimostra una struttura disomogenea della prostata per la<br />
presenza di queste aree di edema, di questa infiammazione, di queste atrofie ghiandolari. L’atrofia<br />
ghiandolare che pure è frequente dopo i 50 anni, spesso può determinare delle forme sclerotiche, come<br />
pure vedete in questo caso le ghiandole diventano rare, diventano anche cistiche ma c’è un aumento della<br />
fibrosi, ovviamente laddove c’è un aumento della fibrosi si scatenano tutta una serie di disturbi urinari di<br />
cui parleremo più avanti.<br />
La patologia che affligge gran parte dell’umanità maschile è l’iperplasia o ipertrofia prostatica nodulare o<br />
adenoma, in effetti è un termine improprio perché per iperplasia noi abbiamo un aumento delle cellule, un<br />
scaricato da www.sunhope.it
aumento numerico, per ipertrofia noi intendiamo un ingrossamento della cellula, sono due termini che<br />
sono utilizzati per descrivere un fatto macroscopico anche se normalmente questi termini sono utilizzati a<br />
livello citologico, il termine tecnico anatomo-patologico è iperplasia fibro-leihoadenomatosa perché<br />
riguarda il tessuto muscolare, fibroso e ghiandolare alcuni per semplificare lo chiamano adenoma ma non è<br />
un adenoma perché è un ipertrofia che coinvolge tutta la ghiandola. Nel 95% dei casi riguarda la zona<br />
transizionale e centrale proprio questa localizzazione è la causa del disturbo perché riguarda le regioni<br />
periuretrali e quindi la si determinano una serie di disturbi legati all’urinazione; raramente invece la zona<br />
periferica; vediamo alcuni esempi dove l’uretra prostatico si è ridotto enormemente, molto spesso vedete<br />
dei noduli, qua addirittura l’uretra è ridotto ad una fessura, qua addirittura quasi non si vede più,<br />
ovviamente questa è una resezione completa una prostatectomia che si fa nei casi in cui la ghiandola<br />
veramente è molto ingrossata con aumento di peso fino a superare anche i 100 gr; l’altro tipo d’intervento<br />
è il cosiddetto intervento TUR-P. L’incidenza è dell’8% fino ad arrivare al 75% nei soggetti in età tra 70 e 80<br />
anni, molti non se ne accorgono neanche. La patologia molto spesso è un androgeno dipendenza, se volete<br />
ha una patogenesi molto simile alla mastopatia fibrocistica perché si creano delle ghiandole che sono più<br />
sensibili e meno sensibili alla dipendenza androgenica per cui si stimola la fibrosi, tutti una serie di disturbi,<br />
di asincronismi maturativi di qualche cosa che procedeva prima in maniera regolare che determina poi la<br />
disfunzione; è fatta da cisti e noduli; sintomi indicativi la pollachiuria, la nicturia, sintomi ostruttivi,<br />
l’esitazione, il flusso ridotto, il senso di svuotamento incompleto legato proprio a questa ostruzione; da un<br />
punto di vista generale istologico abbiamo l’iperplasia stromale in cui ci sono fibre elastiche che sono<br />
muscolari e tessuto fibroso e iperplasia ghiandolare con aspetti variabili di cui parleremo tra poco. La<br />
terapia può essere endocrina o chirurgica a seconda dei casi; ecco qui come appare una ghiandola colpita<br />
da questa patologia, come vedete molte cisti, molto stroma fibroso, a volte le ghiandole sono iperplastiche<br />
chiaramente perché sono addossate le une alle altre e assumono anche degli aspetti pseudopapillari o<br />
aspetti cistici, qua invece domina la fibrosi c’è un quadro molto variabile da campo a campo; una<br />
particolare tecnica che si è sviluppata in questi casi è il cosiddetto resettore endoscopico che unisce un<br />
endoscopio per vedere bene, questa è la prostata, e un particolare apparecchio che praticamente taglia le<br />
regioni periprostatiche, periuretrali della prostata a pezzetti in modo da decongestionare l’urina, molto<br />
spesso questa tecnica è sufficiente però deve essere fatta da mani abili per evitare complicanze che ci<br />
possono essere, ci sono 80-100 pezzetti che noi dobbiamo esaminare poiché non raramente ci capita un<br />
soggetto anziano che c’ha qualche cosa in più e possiamo trovare il cancro cosiddetto incidentale; questo<br />
invece è un intervento di prostatectomia apicale dove vedete nelle diverse sezioni come l’uretra si è ridotto<br />
enormemente, si è ingrossato tutto fino a sconsigliare un intervento di questo tipo poiché qua si doveva<br />
addirittura tagliare dall’interno tutta la prostata, si faceva più presto a togliere la prostata.<br />
L’infarto non viene quasi mai da solo insorge sempre in un soggetto che già ha un iperplasia nodulare,<br />
ovviamente a causa di questa fibrosi ci può stare una compressione di vasi un’ischemia acuta e si determina<br />
una necrosi ma anche causa di traumi e così via e si determina un’ematuria improvvisa associata al ??<br />
scaricato da www.sunhope.it
Prostata<br />
Eravamo arrivati alla famigerata ipertrofia/iperplasia prostatica, detta anche erroneamente adenoma.<br />
C'è una serie di lesioni, come la mastopatia fibrocistica, che possono venire da sole, o rientrano<br />
nell'ambito di questa grande famiglia...di quest'ipertrofia prostatica. Vi ricordate che dicemmo l'altra<br />
volta, una di queste lesioni più classiche, è la cosiddetta iperplasia a cellule basali. Quando<br />
parlammodella prostata in generale, dicemmo che le cellule epiteliali posano su uno strato di cellule<br />
basali positive per le ck ad alto peso molecolari, e altri marker epiteliali come p63. In alcuni casi,<br />
una patologia dell'esofago, per esempio, la esofagite da reflusso, vediamo un'iperplasia dello strato<br />
basale. L'immagine che vediamo da un punto di vista morfologico, se c'è un'iperplasia delle cellule<br />
basali, le cellule epiteliali secretorie che stanno sopra sono spinte all'interno,<br />
il lume si restringe, noi vediamo un accollamento cellulare che sembra pluristratificato. Può<br />
sembrare negativo, se non conosciamo il problema. Questa stratificazione fa pensare al cancro.<br />
Vediamo uno strato di cellule secretorie, al centro del lume, schiacciato da queste cellule basali che<br />
proliferano. L'impressione è quella di un tubulo ghiandolare pluristratificato. però, c'è una furbizia.<br />
Se abbiamo dei dubbi in una situazione del genere, abbiamo detto che queste cellule sono positive<br />
alla citocheratina ad alto peso molecolare e alla p63, quindi queste cellule basali verranno fuori da<br />
questa prova immunoistochimica. Abbiamo poi antigeni prostatici specifici, la PSA e la fosfatasi<br />
acida prostatica. Saranno negative in queste cellule. queste positività solo negli elementi cellulari<br />
ghiandolari secretori.<br />
Vedete che il lume si riduce enormemente, ma se andiamo a fare la ck vediamo che tutte queste<br />
cellule sono tutte positive, e vediamo che sono PSA positive, e quindi questo ci aiuta, in una<br />
situazione del genere.<br />
Un'altra particolare situazione è l'iperplasia a cellule chiare, che pone dei problemi perchè nella<br />
prostata c'è pure il ca a cellule chiare. Ma anche qui, se facciamo la ck, la troviamo, e quindi<br />
possiamo escludere che si tratti di un cancro. Poi abbiamo una situazione che voi già conoscete,<br />
uguale a quella della mammella, la cosiddetta adenosi sclerosante, un'iperplasia del connettivo più<br />
la iperplasia del tessuto ghiandolare, e la componente connettivale schiaccia le cellule delle<br />
ghiandole, che subiscono delle coartazioni e mostrano delle atipie. Se uno non riconosce questo<br />
problema può fare una diagnosi errata. Qui è tutto stroma, queste cellule ghiandolari superstiti sono<br />
schiacciate da questo stroma molto attivo, di cellule grosse perchè è uno stroma proliferato. Ma<br />
anche qui, tutte le strutture ghiandolari sono circondate da queste cellule basali, e quindi positive<br />
alla ck ad alto peso molecolare, e possiamo escludere il ca.<br />
scaricato da www.sunhope.it
L'iperplasia adenomatosa atipica, non è rara, presente nelle aree adiacenti al ca nel 30% dei casi. fa<br />
qualche scherzo, perchè non sempre è continua la positività alla ck. Dei tratti in cui vengono a<br />
mancare le cellule. Qualche piccola atipia, qui ci vuole molta esperienza...una diagnosi<br />
impegnativa, anche quella differenziale coll'adenoca prostatico.<br />
questo già lo conoscete, cosiddetta iperplasia, metaplasia, adenoma nefrogenico, già ne abbiamo<br />
parlato della sfera genitale femminile. Può succedere anche per la prostata, in effetti molti<br />
adoperano, come nell'ipetrofia, il termine adenoma, ma in realtà si tratta di un'iperplasia/trofia di<br />
residui nefrogenici, e vi ricordo che hanno quest'aspetto obnail (?)queste cellule cubiche che<br />
sembrano singole, a chiodo di tappezziere. E poi succede tutta una serie di cose strane. Soprattutto<br />
nei soggetti che hanno avuto un intervento di Turp, resezione prostatica...lo stroma può reagire, un<br />
nodulo postoperatorio a cellule fusate, o una lesione stromale atipica. Le cellule stromali assumono<br />
a volte delle forme bizzare. Ma già vi ho detto che più è spiccata l'atipia, più non è credibile.<br />
Quando si arriva a strutture così bizzare, bisogna pensare a lesioni non maligne, paradossalmente,<br />
perchè anche le atipie hanno un limite :D<br />
Questi noduli intervengono inuna fase postchirurgica, anche dopo mesi.<br />
Nella prostata, per continuare l'analogia con la mammella, possiamo avere fibroadenomi, ma non<br />
sono frequenti. Il cosiddetto fibroadenoma giovanile (cistosarcoma filloide), simile in tutto alla<br />
lesione della mammella.<br />
Iperplasia a cellule basali, adenosi sclerosante, iperplasia adenomatosa atipica, iperplasia di resti<br />
mesonefrici, iperplasia stromale atipica, lesione stromale benigna, e nodulo postoperatorio a cellule<br />
fusate, che rispetto al fibroma presenta maggiori atipie, fibroadenoma, tumori filloidi.<br />
Pin: il pin si distingue basso grado ed alto grado.<br />
Basso grado: cellule che presentano una discromasia nucleare, ma mantiene la forma tondeggiante,<br />
e il citoplasma è regolare. Ad alto grado, il nucleo è irregolare, discromia più evidente, nucleolo più<br />
evidente, un aumento del volume del nucleo rispetto al citoplasma, e membrana nucleare ispessita.<br />
In questi casi, anche lo strato di cellule basali, che delimita l'acino ghiandolare, può essere<br />
incompleto.<br />
Se facciamo la ck ad alto peso molecolare.<br />
è una precancerosi ad alto potenziale<br />
alto grado si può estendere anche ai dotti prostatici, e dare un aspetto pagetoide, una migrazione di<br />
singole cellule sparse all'interno dei dotti prostatici. Una frequente multicentricità e si localizza<br />
molto spesso nella zona periferica dellaprostata, che è la sedeprincipale del cancro prostatico,mentre<br />
iperplasia e ipertrofia prostatica prediligono le zone centrali e transizionale. è associato ad aree di<br />
ca, quando troviamo zone di pin di alto grado, in un'altra area potremmo trovare aree di cancro con<br />
scaricato da www.sunhope.it
valori variabili nelle diverse statistiche, dal 5 al 40% dei casi. In genere quando è associato a pin<br />
insorge nei soggetti più giovani dell'età media di insorgenza è intorno ai 65-70 anni. nel 50% dei<br />
casi con pin di alto grado ecco un valore predittivo, noi sappiamo entro due anni, in una successiva<br />
biopsia. Atteggiamento di grande attenzione, follow up intensivo, c'è chi suggerisce una<br />
chemioprevenzione<br />
Poi c'è una sorta di rifugio peccatorum, una sorta di accordo internazionale. Quando non si sa che<br />
pesci pigliare, nel senso che, queste atipie sono in<strong>complete</strong>, incompleta e controversa è<br />
l'interpretazione del pattern immunoistochimico, quando in tante biopsie della prostata di uno stesso<br />
soggetto c'è un quadro di ipertrofia e solo un piccolo focolaio, magari marginale, vicino alla<br />
biopsia, presenta queste atipie, o quando c'è una coartazione meccanica, o dovuta alla modalità di<br />
prelievo, per cui non si vede bene, allora usiamo questa dizione Atypical Small Acinar Proliferation,<br />
che significa che ci sono atipie sospette, non solo citologiche ma anche riguardanti l'architettura<br />
allora noi diciamo ASAP. Riguarda il 5% dei casi. Cosa si fa in questi casi? Talvolta abbiamo lievi<br />
elevazioni di PSA, e poi, dimenticavo una cosa importante, il focolaio deve essere piccolo,<br />
guardando solo la RM. è necessaria la biopsia. è sicuramente utile il confronto tra il radiologo e<br />
l'anatomopatologo. Quando si fa il campionamento, e si vede di indirizzare l'ago, si fanno almeno<br />
12 prelievi, in aree diverse della prostata, ma se abbiamo una RM che ci dice che c'è una presenza<br />
di un focolaio sospetto, allora ci concentriamo su quella zona...<br />
Ecco come appare un cancro della prostata. Abbiamo visto che la prostata ha un'architettura<br />
lobulare. Invece vedere una certa confusione strutturale, nonc'è più la presenza di lobuli, vedere qui<br />
delle atipie, molto spesso come abbiamo visto nella displasia di altro grado, così nel cancro,<br />
compaiono i nucleoli, perdita di polarità, struttura alterata, come si vede qua, vediamo un aspetto<br />
fibroso, tanti lumi ghiandolari con la stessa struttura, qua se facciamo la ck ad alto peso molecolare,<br />
scompare. Qua vediamo solo qualche residuo. Possiamo avere l'espressione di un marcatore di<br />
malignità della prostata, che è un'attività enzimatica, la racemasi. Importantissimo è sapere il<br />
grading, fondamentale, il grading di Gleason, con una modifica degli ultimi anni. Ha una grande<br />
rilevanza clinica. Un grading doppio, perchè? poichè il cancro della prostaa ha una certa<br />
eterogeneità, per essere più precisi e più aderenti alla realtà, si considera il pattern principale, più<br />
espresso. Si danno due numeri che identificano l'entità di espressione dei pattern. Il minimo è 1 per<br />
ogni pattern, il massimo è 5 e quindi il grading può andare da 2 a 10. Se vi arriva uno con un<br />
grading 1, vuol dire ca nun ha capito niente! o come mi è capitato a me, di vedere una cartella<br />
clinica...in genere si scrive sempre per correttezza grading 2+2=4 secondo Gleason, per dire che si<br />
riferisce alla formula, perchè ci stanno altri grading di scarso successo. Uno aveva 7 livelli, per<br />
fortuna l'hanno eliminato, a volte si vuole essere troppo pignoli e si aumenta la variabilità, è peggio.<br />
Trovai scritto sulla cartella, era 4,2 secondo Gleason, venne interpetato come quattrovirgoladue.<br />
Una cartella che può girare il mondo, se arrivava in America, quelli ci telefonavano "avete un altro<br />
tipo di grading". Addirittura questi arrivano a calcolare pure i decimali, che erauna novità. Inutile<br />
dire che il collega che ha compilato la cartella era del reparto di urologia. Senza andare nel<br />
dettaglio,il primo livello è quando vediamo dell strutture ghiandolari monomorfe, con scarse atipie,<br />
si riproduce la struttura normale della prostata, ovviamente le ghiandole sono più affollate, perchè<br />
non c'è l'architettura lobulare classica, e ovviamente viene meno quel pattern immunoistochimico<br />
tipico dell'iperplasia e della prostata normale. Mano a mano che scendiamo, vedete, queste<br />
ghiandole relativamente monomorfe diventano pleomorfe, qui piccole, qui grandi, e<br />
paradossalmente aumenta lo stroma interposto, perchè c'è una maggiore irregolarità di distribuzione<br />
e di calibro. Questa variabilità aumenta nel III livello, dove possiamo trovare aspetti cribrosi, cioè<br />
dei grandi gettoni con dei lumi dentro, plurighiandolare all'interno. Nel IV livello degli ammassi<br />
ancora più cribriformi. Nel V livello, il cancro tende ad essere soprattutto solido, perde la capacità<br />
di fare tubuli, o comunque è molto marginale. Ovviamente, quest'architettura, che fa parte del<br />
grading, è. parallela anche alle atipie citologiche. Aumentano le atipie mentre andiamo dal livello I<br />
scaricato da www.sunhope.it
al V. Poi se vogliamo dire un cancro che è ben differenziato può essere 1+2, 2+2, anche 2+3. E poi<br />
diamo il punteggio totale. Qua vedete è una tabella prognostica di sopravvivenza a 5, 10, 15 anni.<br />
Vedete il Gleason 2+4 ha un'ottima aspettativa prognostica, per cui si arriva al 90% a 15 anni. Il<br />
Gleason 5+6, questa aspettativa scende al 80%, dal 7 in poi c'è una caduta, perchè si situa al 60%, il<br />
8-10, massimo grado per il Gleason, scendiamo al di sotto del 40%. Anche la mortalità è in<br />
relazione al Gleason. Una mortalità con uno score di Gleason relativamente favorevole è molto<br />
bassa, 6/1000. Se Gleason 8-10, saliamo a 121.<br />
Vedete qui, il numero 1, il primo livello, tutte strutture ghiandolari una addosso all'altra, molto<br />
monomorfe, la ck non c'è, ma è presente solo nelle ghiandole normali sopravvissute alla invasione<br />
tumorale. Nel secondo livello, lo stroma aumenta, le ghiandole si dispongono in maniera più<br />
irregolare, e sono di calibro diverse, molto piccole, più grandi addirittura cisti. In G3 abbiamo un<br />
aspetto evidente di back to back, e con una notevole irregolarità strutturale, perchè vedete ci sono<br />
anche delle immagini cribrose. Il grado 4 (3+4) con gettoni microghiandolari quasi solidi. L'aspetto<br />
ghiandolare accennato, aumentano le atipie citologiche, e l'aspetto solido. Il carcinoma della<br />
prostata nel 90% dei casi è il cancro della prostata. Le altre varianti: atrofica, caratterizzata<br />
dall'aspetto cistico, ca mucoide, con cellule ad anello con castone, il sarcomatoide, che simula un<br />
sarcoma, ma è positivo alla CK e poi il problema dei ca neuroendocrini, di cui abbiamo scoperto<br />
non molti anni fa la dinamica, l'evoluzione che spiega la presenza di questi ca. Una delle terapie che<br />
si usa per l'iperplasia ma anche per il cancro, è una terapia endocrina. Se noi facciamo una terapia<br />
antiendocrina, queste cellule non ricevono più le stimolazioni androgene, e quindi queste cellule si<br />
sdifferenziano. Possiamo avere rischio che da un cancro della prostata, possa nascere un ca<br />
neuroendocrino, come se andassimo a bloccare quelle cellule staminali, che hanno i recettori per<br />
l'ormone, e invece pigliano il sopravvento quelle più indifferenziate senza recettore. Quindi il ca<br />
neuroendocrino può essere un esito della deplezione androgenica. Cellule staminali di<br />
nicchia...quando non arrivano più questi segnali, queste cellule cambiano strada. Avendo questa<br />
deplezione androgenica su base iatrogena, si sdifferenziano e subiscono un processo di<br />
transidifferenziazione da cellule epiteliali a neuroendocrine.<br />
Abbiamo ca duttali, perchè anche nella prostata abbiamo i dotti. Il ca adenoideo cistico, il ca a<br />
cellule chiare.<br />
Alcuni consigli pratici, come si fa la biopsia prostatica (ecoguidata per via transrettale). è presente<br />
una sonda che deve fare la biopsia e la sonda ecografica. La sonda bioptica presenta una particolare<br />
strutturazione, per cui nell'attraversare il tessuto prostatico, c'è come un mandrino dentro, che<br />
chiude l'ago, che dovrebbe impedire...ma mi so' capitati dei casi, in cui uno ha avuto 12 prelievi<br />
della prostata, ma in realtà erano 12 biopsie intestinali...si è scoperto che l'aveva fatta un<br />
scaricato da www.sunhope.it
giovane...aveva avuto 12 biopsie dell'intestino. Questi sono tutti protocolli...si arriva addirittura a 24<br />
prelievi bioptici, come togliere la prostata a rate. C'è un urologo, non facciamo nomi, che fa solo 2<br />
biopsie...i tecnici godono perchè lavorano poco...(saracasmo evidente).<br />
Si segue l'orientamento della RM. Si usa una tecnica " a sè stante", la media è di 12 prelievi. Con<br />
questa tecnica, si riduce unpo' il numero dei falsi negativi. è inutile che vi spieghi la ratio che c'è<br />
dietro, perchè non è universalmente accettata. Cambiano i diversi punti di campionamento. Questo<br />
per esempio...vedete che le aree periferiche sono più avvantaggiate. Una gran parte dei cancri<br />
avviene qui, ma si rischia di non prendere campioni di cancri che si sviluppano nelle aree centrali,<br />
più rari. Quindi si preferisce nelle sedi superiori, inferiori, ma si va anche nelle aree centrali,<br />
transizionali.<br />
Ecco come appare un frustolo di tessuto prostatico. La prostata ha una struttura fibromuscolare e poi<br />
la struttura ghiandolare. Qui potete cogliere un aspetto fibroso. Se voi calcolare che ogni caso ha<br />
una media di 12 biopsie, capirete che se abbiamo 10 casi in una giornata, dobbiamo vedere un<br />
centinaio di vetrini, più l'immunoistochimica. Poi i vetrini possono essere non buoni. Poi i colleghi<br />
vogliono avere il risultato prima che arrivi il campione...<br />
Il retto...può capitare spesso che si ritrovi nei campioni che ci arrivano.<br />
Ma può succedere a volte, valutando anche la posizione anatomica delle vescichette seminali, che<br />
l'ago attraversi le vescichette seminali. Queste cellule delle vescichette sono molto reattive, molto<br />
iperplastiche, è capitato di fare diagnosi di cancro. Poi si può prendere tessuto paragangliare, oppure<br />
una cosa poco conosciuta. Pochi di voi ricorderanno che all'uscita della prostata, l'uretra viene<br />
agganciata da alcune strutture ghiandolari, del Cooper, con funzione lubrificante. Può succedere con<br />
questa tecnica a sè stante, anche perchè la tecnica ecografica non è precisa al mm, che escano fuori<br />
queste strutture ghiandolari, e simulano un grado 1 del cancro prostatico. Oppure può succedere che<br />
vengano presi i dotti eiaculatori. Possibili errori, quindi.<br />
La strategia della rebiopsia. Considerando la complessità topografica della prostata, il fatto che, e ve<br />
lo dico con certezza per esperienza personale, che su 12 campioni, uno solo potrebbe essere valido,<br />
e poi considerando i quadri vari di presentazione, PIN, ASAP. Insomma, una valutazione complessa.<br />
Si può comprendere la strategia della rebiopsia. è stata anche calcolata la sua validità: se questo<br />
paziente ha già avuto le biopsie prostatiche secondo quei protocolli che abbiamo visto, la possibilità<br />
che insorga un ca prostatico in successive biopsie è del 19%, se c'è un pin di alto grado sale al 31%,<br />
se c'è ASAP arriviamo al 41%, se c'è ASAP+PIN, allora arriviamo a oltre il 50%. I tempi della<br />
rebiopsia variano da 3 a 6 mesi. Qual è la validità? Nella stessa sede di una lesione atipica, che<br />
significa PIN soprattutto, o un'iperplasia adenomatosa atipica, abbiamo il 65% di probabilità di<br />
trovare in quella sede, in una rebiopsia, un cancro. Poi questa percentuale arriva all'88% se si fanno<br />
scaricato da www.sunhope.it
prelievi nelle aree adiacenti a queste lesioni atipiche, perchè sono predittive di quello che avverrà<br />
nella seconda biopsia. Quindi bisogna suggerire questa strategia della rebiopsia, perchè sappiamo<br />
che si riduce in maniera drammatica la possibilità di falsi negativi.<br />
La stadiazione, la facciamo ridotta, i capisaldi.<br />
T1 Un piccolo ca, identificabile in un lobo piccolo, poco visibile, venuto fuori incidentalmente, non<br />
dalla RM ma dalle biopsie. Il T2 è più grande, coinvolge uno o due lobi, e coinvolge, seguendo la<br />
classificazione anatomica che vedemmo l'altra volta, più del 50% dei lobi. T3 quando coinvolge<br />
organi adiacenti, soprattutto la vescica. E in questi casi va differenziata la massa primitiva.<br />
Frequente il coinvolgimento delle vescichette seminali. T4, altri organi, oltre vescica e vesichette,<br />
quindi retto, addirittura osso.<br />
L'intraprostatico, I e II stadio, ha una aspettativa prognostica a 10 anni eccellente, rispetto agli altri.<br />
Anche al 85-90%. Se è al secondo stadio la percentuale scende. Se c'è invasione delle vescichette,<br />
arriviamo sotto il 50%, se ci sono metastasi linfonodali, scendiamo al 25%. Questo fà sì che il<br />
cancro della prostata sia dal punto di vista prognostico molto eterogeneo.<br />
Questo è invece in rapporto al PSA, ci riguarda fino ad un certo punto. Livelli di PSA >4<br />
nanogrammi (e il volume?) sono considerati di cut-off. Altri fattori prognostici sono i margini di<br />
escissione, la fosfatasi acida prostatica, Ki67, l'amplificazione dei recettori per gli androgeni (in<br />
fase di studio) la componente neuroendocrina, che in genere è un fattore molto negativo. Le<br />
metastasi direttamente correlate anche al Glison, e quindi polmoni, fegato, surrene, mammella,<br />
SNC, osso. La terapia dipende dallo stadio, dal grading. Quelle meno aggressive nei casi con<br />
aspettative più favorevoli. Abbiamo la deplezione androgenica, ma c'è il rischio di sviluppo di cloni<br />
ormonoindipendenti. Si fa con analoghi di LH-RH, antiandrogeni, la flutamina, inibitori della 5-<br />
reduttasi. Terapie ablative, che hanno un rischio, alcune terapie conservative, perchè resta difficile<br />
la valutazione di quello che resta. La radioterapia, con brachiterapia, la chirurgia, la crioterapia,<br />
l'ipertermia, e io sono molto scettico su queste terapie alternative. Altra terapia, se ci troviamo di<br />
fronte ad un cancro piccolo uscito fuori dalla biopsia prostatica, e cioè, un'attesa, un follow up.<br />
Inutile aggredire un paziente, magari anziano, e usare tutte le frecce nell'arco subito, quando<br />
potrebbe trattarsi di un cancro incidentale.<br />
La vescica, uno dei capitoli più interessanti. Il cancro della vescica è stato uno dei primi cancri<br />
riconosciuti come malattia professionale per alcune categorie di lavoratori. Il cancro che più spesso<br />
è correlato a particolari attività lavorative. Gli anatomopatologi, soprattutto della vecchia<br />
generazione, sono tra i più esposti. La vescica ha una storia di latenza molto grande...può<br />
manifestarsi dopo 40-50 anni.<br />
scaricato da www.sunhope.it
Molto importante è sapere che la vescica deriva dalla cloaca. Che è comune trala via digestiva e la<br />
via urinaria. Una particolare struttura è l'uraco, verrà suddivisa in parte rettale e parte urinaria, un<br />
canale che mette in comunicazione cloaca e ombelico. Destinato a chiudersi e a diventare<br />
legamento vescicolo-ombelicale. Ovviamente la vescica ha un epitelio di transizione, perchè<br />
risponde alle esigenze funzionali. Se la vescica è distesa si appiattisce, se è relativamente vuota,<br />
appare stratificato. Poi c'è una tonaca propria. La vescica non ha una muscolaris mucosae sviluppata<br />
come nell'intestino, e quindi è difficile distinguere i limiti di mucosa e sottomucosa. E poi ha una<br />
robusta parete muscolare e poi un'avventizia. A livello istologico, un epitelio transizionale a riposo.<br />
La muscolaris mucosae discontinua, qui la sottomucosa, molto ricca di vasi.<br />
Le cellule che stanno più sopra nell'epitelio si chiamano ad ombrello: quando si fa la citologia<br />
urinaria, le cellule, deconnesse dal loro epitelio, assumono conformazione ad ombrello. in<br />
condizioni d'appiattimento, questa conformazione permette loro di rapportarsi alle altre cellule. in<br />
genere sono 3-7 strati, le cellule superficiali sono in grado di produrre un po' di muco. Al di sotto<br />
della membrana basale ci sono molti piccoli vasi. Altra caratteristica fisiologica della vescica,<br />
soprattutto in età superiore ai 40 anni, sono i nidi di Von Brum, legati allo sgocciolamento<br />
dell'epitelio transizionale, che sgocciolando sul tessuto connettivale, prolifera lo stesso e forma dei<br />
gettoni solidi.<br />
Le donne spesso vanno incontro a trigonite, infiammazione e infezione della vescica, mentre<br />
l'incidenza di cancro della vescica è molto bassa. Possiamo avere la presenza di stimoli irritativi<br />
cronici, la cistite, oppure la metaplasia intestinale, chiamata trigonite, che può coinvolgere anche i<br />
nidi di Von Brum. E possiamo avere anche metaplasia squamosa.<br />
scaricato da www.sunhope.it
Vescica e prima parte del polmone<br />
19-05<br />
Andrò molto velocemente , si tratta di argomenti che troverete con facilità:<br />
Problematiche connesse all’URACO: persistenza, cisti,processi flogistici, adenocarcinomi<br />
Ora vediamo una grave malformazione: Deiscenza della parete addominale a livello sotto-ombelicale, per<br />
effetto della quale anche la vescica è aperta. È associata ad altre gravi malformazioni e complicazioni degli<br />
organi genitali.<br />
Principali lesioni non neoplastiche della vescica:<br />
Nodulo a cellule fusate postchirurgico, analogo a quello della prostata. La vescica è un organo cavo<br />
e qui si realizza quello che abbiamo chiamato cancerogenesi di campo. Quando comincia qualche<br />
episodio come: polipi, pallomi, carcinomi di basso grado, si avviano delle manifestazioni che<br />
ritroviamo soprattutto nell’anziano. Tornando al Nodulo a cellule fusate : È una reazione abnorme,<br />
riparativa fibrotica che può presentare atipie,puo presentare delle delezioni, positivo alla<br />
dimetrina, all’actina quindi è composto sia di fibroblasti che miofibroblasti.<br />
Endometriosi vescicale: vedete questa aeree grossa cisti. Esiste anche l’endicervicosi in questo caso<br />
abbiamo ghiandole mucoidi endocervicali.<br />
Pseudo tumore infiammatorio, una lesione a cellule fusate ricca di cellule infiammatorie, con atipie,<br />
la sua strutturazione è fatta di cellule miofibroblastiche, simula un sarcoma ma facendo i markers<br />
(actina e d altri) ci rendiamo conto che è fatto di cellule miofibroblastiche e infiammatorie.<br />
La malocoplachia frequente nell’anziano, durante l a visita si è portati a sospettare un cancro per<br />
l’erosione della mucosa ma non è tumorale, è infiammatoria. Al posto dell’epitelio transizionale<br />
troviamo grandi macrofagi con ampio citoplasma con inclusi calcifici : i corpi di Michaelis<br />
Gutmann.’E una patologia infiammatoria quasi da esaurimento, in questi macrofagi troviamo<br />
batteri in grande quantità, rappresenta una lesione estrema dell’immunità locale attraverso i<br />
macrofagi, che viene fuori dopo una lunga serie di cistiti negli uomini, ma soprattutto nelle donne.<br />
La mucosa non riesce piu a far fronte a questa serie di insulti microbiologici, risponde con<br />
iperplasia, fino all’erosione al sanguinamento. Troviamo macrofagi pieni di batteri e corpi calcifici<br />
all’interno che forse rappresentano un altro tentativo di reazione da parte della cellula istiocitica, in<br />
cui calcifica il materiale batterico che non riesce a smaltire.<br />
tessuto prostatico ectopico<br />
Un riepilogo:<br />
nodulo a cell fusate post operatorio: dopo qualche mese dall’intervento,<br />
pseudo tumore infiammatorio<br />
la malacoplachia, flogosi xantogranulomatosa, ove troviamo macrofagi carichi di grasso e batteri<br />
scaricato da www.sunhope.it
endometriosi, endocervicosi<br />
tessuto prostatico ectopico, residuo embrionale. Si presenta come una massa polipode. Si trova alla base<br />
della vescica, del trigono.’E fortunatamente rara.<br />
Principali forme di cistiti:<br />
Cistite ghiandolare, o cistica. Ricordate le ghiandole di von brunn? Dopo un insulto infiammatorie queste<br />
formano delle cisti, si cavitano centralmente, o si trasformano in vere proprie strutture ghiandolare dopo<br />
metaplasia. In passato poteva essere confusa con un adenocarcinoma.<br />
(------------le chiama ghiandole ma sono nidi uroteliali)<br />
Cistite follicolare molto spesso legata alle salmonelle, alle infezioni batteriche. Si chiama Follicolare perche<br />
viene dai follicoli linfatici secondari.<br />
Cistite polipoide o papillare, in cui la mucosa si solleva perche assume questo aspetto polipoide ma anche<br />
granulomatoso con cellule giganti. Talvolta è su base congenita, un amartoma da iperplasia del tessuto<br />
muscolare della vescica.<br />
Cistite interstiziale molto spesso legata all’anestesia che determina una sovradistensione della vescica, crea<br />
delle screpolature con un’infiammazione transmurale di tipo cronico.<br />
Cistite enfisematosa. C’è anche presenza di gas prodotti da ceppi batterici, come gli enterobacter.<br />
Descrizione di immagini:<br />
Cistite ghiandolare: vedete nidi von brunn, con strutture ghiandolare (metaplasia)<br />
Cistite Follicolare:vedete un Follicolo linfatico secondario, con ampio centro germinativo e fusioni.<br />
Cistite polipoide: la mucosa si solleva con asse connettivo vascolare. delimitata da epitelio transizionale<br />
Metaplasia mesonefroide, ne abbiamo parlato nella prostata, legata a residui di mesonefro. Ha questo<br />
aspetto istologico hobnail, cellule singole che sporgono come chiodi dei tappezzieri. Alcuni la chiamano<br />
adenoma, altri iperplasia.<br />
Cancro della vescica:<br />
nel maschio è più frequente. Nella donna sapete che invece è frequente la cistite. La più alta frequenza nel<br />
maschio è spiegabile per la particolare cancerogenesi. Occupa il 5 posto nei maschi, nella femmina non<br />
rientra nelle prime 10 cause. La mortalità non è molto elevata. In italia l’incidenza è 57 per il maschio, per la<br />
femmina 13 (dati corretti per 100°000).Il rischio è 1 su 24 per il maschio, mentre per la donna 1 su 140. A<br />
napoli, per il maschio l’incidenza è tra le piu importanti. Per la donna invece no. C’è un motivo? Oggi forse<br />
possiamo dire di si. Il cancro della vescica è stato il primo cancro ad essere riconosciuto come malattia<br />
professionale, una delle categorie più esposte era l’anatomopatologo, soprattutto il tecnico. Si usano<br />
scaricato da www.sunhope.it
sostanze cancerogene, come ad esempio la formalina, alcuni reattivi, come coloranti, i derivati dell’anilina.<br />
In realtà non è proprio l’analina in sé, ma i procedimenti industriali, ma sono le impurità ad avere alto<br />
potenziale, la beta naftilammina, 4 aminodifenile.Tali sostanze vengono coniugate nel fegato con a .<br />
glucuronico arrivano in vescica dove per eventuali cistiti trovano un ph alterato e tale legame di scinde. E<br />
possono esplicare la loro azione direttamente in vescica. La maggior parte è accumulata in parte medio<br />
inferiore, perche c’è piu tempo per esplicare l’azione cancerogena. Ha un periodo di latenza estremamente<br />
lungo. Altre categorie a rischio sono : chi ha a che fare con le vernici, l’ industria siderurgica,<br />
automobilistica, imbianchini. Anche il fumo di sigaretta,il caffè anche se non c’è correlazione diretta. Il<br />
fumo è un fattore , pare, protettivo per malattia di crohn, retto colite ulcerosa. Pare svolga la stessa<br />
protezione il caffè. Altri fattori: schistosomiasi, diffuso nei paesi orientali, arsenico, fattori genetici(p53,<br />
alterazioni del cromosoma 9) segni : ematuria, disuria in fase avanzata.<br />
Esistono precancerosi:<br />
metaplasia squamosa: in alcuni casi, sembra avere un rischo di progressione. si tratta di una forma<br />
di difesa.<br />
Displasia e carcinoma in situ.<br />
L’importanza di queste lesioni è dimostrata dal fatto che associato al cancro troviamo zone di displasia, di<br />
carcinoma in situ.<br />
Il Carcinoma in situ ha un'altra caratteristica:trai primi segni che da vi è la denudazione, denudation, della<br />
mucosa. le cellule perdono coesività quindi le ritroviamo facilmente nelle urine.<br />
Talvolta abbiamo un’estensione di queste alterazioni in situ nella prostata, nell’uretra prostatica.<br />
La displasia è spesso associata a tumori uroteliali o in soggetti già operati per carcinoma vescicale. I<br />
soggetti operati vanno sempre seguiti, perche nelle aree adiacenti alla vescica troviamo sempre delle<br />
alterazioni potenzialmente rischiose.<br />
Immagini: carcinoma in situ: non c’è piu l’urotelio, vedete due figure mitotiche e quel fenomeno di<br />
iperplasia dei vasi sotto la muscolaris mucosae. La denudation: le cellule si stanno staccando e le ritroviamo<br />
nelle urine. Quindi quando vai a fare un esame citologico raccogli le urine delle 24 ore, usi un apparecchio<br />
chiamato citocentrifuga che condensa la parte cellulare. In questo caso il carcinoma in situ si estende pure<br />
ai nidi di von brunn.<br />
Tumori uroteliali o transizionali:<br />
Tra i Benigni: abbiamo il papilloma. molto raro , ha un asse connettivo vascolare delimitato da epitelio<br />
transizionale. Talvolta gioca qualche scherzo. Invece di crescere all’esterno lo fa all’interno.<br />
(invertito)Queste ramificazioni non si sviluppano nella cavità ma sotto alla mucosa.<br />
Poi abbiamo:<br />
Tumore uroteliale di basso grado ?<br />
Carcinoma uroteliale di basso grado<br />
Carcinoma uroteliale di alto grado<br />
Rappresentano il 90% dei cancri della vescica.<br />
Ho messo un punto interrogativo su tumori uroteliali di basso grado . Perche è un termine generico. Manca<br />
qualcosa per essere carcinoma. (Si dovrebbe parlare di borderline.) Per l’attuale classificazione vengono<br />
considerati cosi. ‘E difficile tracciare dei confini. Quello che segue è<br />
scaricato da www.sunhope.it
Carcinoma uroteliale di basso grado: la prognosi è sicuramente diversa da quella di alto grado.<br />
Puo assumere una configurazione a nidi . Solitamente quando di basso grado ben differenziato è<br />
papillomatoso, vegetante soprattutto se ben differenziato. Quando non è vegetante è brutto segno,<br />
nell’alto grado infatti non c’è vegetazione perche esaurisce le sue potenzialità maligne verso il basso,verso<br />
gli strati della parete anziché verso l’esterno. Poi quella a nidi, quella sarcomatoide peggio ancora.<br />
Poi ci sono quelli<br />
non ureteliali,cioè quelli che non hanno origine da queste strutture uroteliali transizionali come<br />
lo squamoso classico. ‘E ovvio che non è tipico della vescica.<br />
L’Adenocarcinoma con tutte le varietà che troviamo nell’intestino<br />
A piccole cellule. Analogo a quello di derivazione neuroendocrina.<br />
…accenno agli artefatti da strumenti. Le biopsie risentono degli strumenti usati per effettuarli.<br />
Descrizioni di immagini:<br />
papilloma:è quasi floreale. Piccolo asse connettivo vascolare. È molto raro, ha pochi strati, non supera i 7<br />
strati. In periferia possiamo trovare le cellule ad ombrello, con il citoplasma che va a coprire le cellule<br />
adiacenti. Mantiene la sua polarizzazione, le cellule si dispongono quasi in fila indiana. Mantiene le<br />
caratteristiche uroteliali.<br />
Papilloma invertito. Va verso il basso. Ma non sappiamo perche.<br />
Adenoma villoso. Sembra strano ma non lo è perche sappiamo che la vescica può andare incontro a varie<br />
metaplasie. Rappresenta una forte lesione precancerosa. Molto spesso è associata a cancro in altre zone.<br />
Veniamo alla nostra situazione grigia: tumori uroteliali di basso grado. la stratificazione è molto diversa. Ci<br />
sono piu strati, la polarizzazione non è mantenuta, c’è disordine nella distribuzione. La citologia:non vi sono<br />
forti atipie, vi è un modesto polimorfismo. Raramente progredisce in lesioni piu gravi(8%), ma la recidiva è<br />
frequentissima.<br />
Il carcinoma uroteliale di basso grado, vedete l’architettura si mantiene papillare,spesso abbiamo nucleoli<br />
nelle cellule. questa è una lesione esofitica . C’è un aumento di mitosi a tutti i livelli sia superficiali che<br />
inferiori, il che come sapete rappresenta un’anomalia. progressione 15%, la recidiva supera il 50%. A livello<br />
morfologico il pleomorfismo è spiccato, la polarità non ben conservata.<br />
Il carcinoma uroteliale di alto grado, rappresenta oltre il 50% di quelli uroteliali. Ha tutte le caratteristiche<br />
della malignità. Elevata attività mitotica misurata con il ki 67, elevato pleiomorfimo, macro nucleoli,<br />
possiamo avere sindrome paraneoplastiche per secrezione inappropriata di bhcg nel 10-30%. Abbiamo<br />
metastasi in oltre il 50%dei casi(Polmone fegato ossa). Il Follow up è drammatico, mortalita a 5 anni 85%.<br />
Fattori prognostici: multicentricità, aree di ca.in situ, scarsa responsività terapeutica.<br />
Il carcinoma sarcomatoide: assume le forme piu strane come quella a cell giganti, è molto aggressivo,<br />
assume fenotipo quasi mesenchimale per trans differenziazione.<br />
scaricato da www.sunhope.it
Il carcinoma uroteliale a nidi.<br />
Il micro papillare, sopra sembra normale, poi sotto vedete queste papille.<br />
Altri tipi:<br />
squamoso,<br />
mucoso in aree del medi oriente, quello piu associato a schistosoma<br />
piccole cellule<br />
adenocarcinoma, con tutte le sue varianti.<br />
la stadiazione (clinica)<br />
T1s(in situ)<br />
Ta<br />
T1 invasione connettivo subepiteliale<br />
T2 l’invasività rimane confinata al contesto muscolare<br />
T3 supera la parete a seconda se microscopica o macro<br />
T4 invasione di organi contigui<br />
N1 >2cm<br />
N2 2-5cm<br />
N3 >5cm<br />
Sopravvivenza a 5 anni: T1>90 T4 intorno al 10%<br />
Altri non epiteliali<br />
Angioma<br />
Fibroma<br />
Leiomiomi<br />
rabdomiosarcoma<br />
Paraganglioma<br />
Linfoma<br />
Tumori a cellule germinali<br />
TERAPIA:<br />
la Chemioterapia : topica o sistemica.<br />
Prima si usava la tubercolina<br />
Problemi legati:<br />
La migliore terapia è sempre la chirurgia.<br />
Biopsia<br />
Resezione trans uretrale<br />
scaricato da www.sunhope.it
Cistectomia<br />
Diversione, sfruttando segmenti di ileo<br />
Radioterapia. Se inoperabile, ma puo dare problemi agli organi, soprattutto vicini.<br />
Il problema è la multicentricità, l’età avanzata, le ricorrenze.<br />
La citologia:<br />
Tecniche di brushing, washing, (gettano un liquido ad alta pressione per facilitare il distacco delle cellule)<br />
spazzolamento della mucosa. I limiti saranno sicuramente i falsi negativi. La sensibilità non è moto alta. In<br />
quelli di alto grado è un po’ piu alta.<br />
Oggi possiamo fare la fish, la citologia a strato sottile e posso usare parametri di biologia molecolare.45.38<br />
polmoni:<br />
breve excursus sull’anatomia del polmone.<br />
Gli alveoli sono come vere e proprie sacche tra cui c’è una comunicazione:i pori di kohn , alla base di<br />
patologie ostruttive.<br />
Vascolarizzazione(da approfondire) : le arterie polmonari dal ventricolo destro, deputate allo scambio, e<br />
quelle bronchiali dalla volta toracica. Poi vedete le vene. Importanti sono le anastomosi che intervengono<br />
sia in sistemi arteriosi che artero- venosi.<br />
La struttura del polmone è semplice. I bronchioli di piccoli calibro, i membranosi,sono privi di cartilagine.<br />
Fino a un certo livello abbiamo l’anello continuo, quando finisce abbiamo delle placche che poi<br />
scompaiono.<br />
Quando hai un polmone enfisematoso, al momento del taglio non si retrae ma si espande, a causa della<br />
rottura dei setti. Esistono vari tipi di enfisema.<br />
Come è fatto un alveolo? Nel setto interalveolare, molto sottile, decorrono piccoli capillari. A livello della<br />
parete abbiamo : pneumociti di tipo I, costituiscono il 90%della superficie, hanno nuclei appiattiti. Il tipo II,<br />
più raro, è più gonfio e produce il surfattante, presenta citoplasma ampio, lamelle(costituite dalla proteina<br />
del surfattante).i due tipi sono distinguibili esaminando la proteina del surfattante.<br />
Vedete i vari bronchioli, fino ai terminali, fino agli acini che sarebbero alveoli.<br />
Com’è l’epitelio bronchiale? è pseudo stratificato, fatto di cellule ciliate, evidente nelle diramazioni<br />
terminali, da goblet cell, cellule basali, cellule di clara. In realtà nei bronchioli terminali più ci inoltriamo<br />
verso i terminali più diminuiscono le ciliate, aumentano le cellule di clara, anche esse deputate alla<br />
produzione di surfattante,ritroviamo cellule neuroendocrine e stem cells.<br />
Descrizione di un’immagine: Vedete le cell di clara, nuclei molto allungate, hanno vacuolizzazioni.<br />
scaricato da www.sunhope.it
Talvolta succede che abbiamo dei canalicoli bronchioli-alveolari chiamati di lambert , si tratta di una<br />
metaplasia bronchiolare dell’aveolo, legata al danno, forse implicata della cancerogenesi soprattutto nei<br />
fumatori.<br />
Vedete qui, questo alveolo in particolare che presenta una parete con caratteristiche da un lato alveolari e<br />
dall’altro bronchiolari.<br />
La patologia non neoplastica la fate da soli, sono cenni,<br />
non dovete sapere tutte le polmoniti, concentratevi sulla differenza tra la franca lobare (lobo<br />
sincrono nelle fasi) e broncopolmonite (avrete noduli non sincroni, ad esempio uno in emorragia<br />
l’altro in infiammazione). Ovviamente saranno diverse le manifestazioni cliniche e l’esito: Una finirà<br />
per lisi l’altra per crisi.<br />
Sindrome da distress respiratorio dell’adulto e nel bambino.<br />
Lesioni da tubercolosi: differenza tra focolaio primitivo, in cui l’organismo non è preparato né a<br />
conoscenza del micobatterio, c’è reazione essudativa generica, e postprimaria in cui c’è una<br />
reazione granulomatosa, in cui avremo cellule giganti.<br />
Complesso primario: studiate la triade: focolaio primario, linfadenite, linfangite.<br />
Atelettasia, enfisema, asma: cenni.<br />
Enfisema : ve ne sono 4 tipi, vedete la patogenesi. Pensate ai meccanismi ostruttivi, ai problemi in<br />
espirazione, in cui il bronchiolo tende a collassare. Al contrario in ispirazione avremo meccanismi attivi.<br />
Conseguenze circolatorie: da distruzione dei setti.<br />
Questi sono tutti concetti base.<br />
Danno alveolare diffuso.<br />
Pneumoconiosi.si tratta di Malattie professionali, sono situazioni a rischio di cancro. L’antracosi è<br />
considerata fisiologica, legata all’inquinamento, i polmoni diventano neri, si potevano addirittura<br />
vedere nelle carni esposte nelle macellerie, ma anche nei cani randagi, per gli scarichi delle auto.<br />
Infarto polmonare<br />
Embolia polmonare: una delle cause di morte piu frequente. Molto spesso legata a trombosi negli<br />
arti inferiori. Ricordate la Sindrome del passegero di 2 classe, legata all’insufficiente spazio per le<br />
gambe. Possiamo anche avere emboli da grasso, da lesioni ossee, da pressione.<br />
Ipertensione polmonare.<br />
Lesioni polmonari<br />
Qual è la Probabilita di sviluppare cancro polmonare? Nel maschio è stabile, nelle femmine è in<br />
aumento,per fumo, ambiente.<br />
Fino a 59 anni è inferiore all’1%. In italia è intorno al 35%. In scozia è molto bassa, in francia e usa supera il<br />
50%.<br />
La sopravvivenza , malgrado i progressi, è bassa oltre i 5 anni.<br />
Continueremo nella prossima ed ultima lezione<br />
scaricato da www.sunhope.it
scaricato da www.sunhope.it
Terminiamo con i polmoni, poi vi darò anche le indicazioni su alcuni<br />
argomenti che non siamo riusciti a fare<br />
Dove eravamo arrivati ai polmoni?<br />
Questi sono sempre i dati dell'associazione americana contro il cancro...e sono dei dati mondiali:<br />
vedete che per quanto riguarda i maschi, il cancro del polmone è al secondo posto, dopo la prostata,<br />
come incidenza, perquanto riguarda le femmine, è al secondo posto, dopo la mammella. Per la<br />
mortalità, in tutti e due casi, è al primo posto. Quindi è un cancro che rappresenta probabilmente il<br />
principale insuccesso dell'oncologia, perchè sapete che le aspettative di vita, son basse. Non mi<br />
metto a discutere la patologia molecolare del tumore del polmone. Ho preso solo una tabella<br />
riassuntiva, le mutazioni principali sono legati all'attivazione di particolare oncogeni ras, mutazioni<br />
puntiformi, traslocazioni di ras, her-2 di cui si sta parlando molto per il ca del polmone, che<br />
condizionerà anche dal punto di vista terapeutico il ca del polmone, gene myc (traslocazione), bcl-2<br />
(traslocazione), inattivazione di alcuni oncosoppressori, FHit (delezione), RB(mutazione<br />
puntiforme), p53 (delezione), inutile dirvi che uno degli argomenti che si sta studiando molto è<br />
l'attivazione delle telomerasi. Per quanto riguarda il fumo di sigaretta, pochi argomenti sono stati<br />
così visceralmente come il fumo di sigaretta, pensate che il gesto di fumare il fumo di sigaretta<br />
implica l'assunzione di 4000 sostanze diverse. Un supermercato di tossici. Non solo la nicotina,<br />
metallipesanti, microsaline, idrocarburi, prodotti di combustione, particolato, di cui è pieno anche<br />
l'ambiente. A Napoli non si circola in determinate ore bla bla bla [racconti che ben conoscete] si<br />
prendono multe mai viste per chi non ha macchine euro4 o euro5, ma si passa davanti a cumuli di<br />
spazzatura, e...[nulla di fatto, sinteticamente trascritto]<br />
Tutte queste mutazioni, determinano degli addotti a livello del DNA, si generano delle<br />
modificazioni del sistema di trasduzione del segnale, dei danni del DNA, e questo fenomeno della<br />
transizione epiteliale e mioepiteliale. [credo che parli al telefono, con i modi che ci sono noti]<br />
Principali famiglie di ca del polmone:<br />
abbiamo Ca (=carcinoma) a piccole cellule 19%, non a piccole cell. 80%, altri tipi 1%.<br />
Il ca non a piccole cell, si suddivide a sua volta in alcune sottocategorie, ca squamoso, che ha<br />
incidenza del 30-40%, adenocarcinoma, 15-20%, a grandi cellule, 10-15%.<br />
Adenocarcinoma classico, 75-90%, ca bronchoioloalveolare, 10-25% che ha un comportamento<br />
scaricato da www.sunhope.it
particolare. Un ca che a vederlo non gli si darebbe due soldi, sembra così elegante. Anche perchè è<br />
refrattario a qualsiasi terapia. Parla di un collega deceduto con un tumore di questo tipo...<br />
A piccole cellule, sempre origine peribronchiale, forse il più maligno che c'è: nei 3/4 dei casi,<br />
quando si presenta clinicamente si trova già in stadio avanzato. Da questa immagine, tutti questi<br />
focolai nel mediastino e l'altro polmone, coinvolge, la pleura, questa cotenna fibrosa esterna, i<br />
linfonodi, ha un'aggressitivà notevole. Il caso più eclatante è che tutti pensavano che fosse un<br />
linforma, il soggetto aveva una linfoadenopatia generalizzata, una lesione mediastinica piccola<br />
polmonare e si pensava ad un linfoma a grandi cellule, e invece...era a piccole cell. polmonare.<br />
Metastasi ai linfonodi mediastinici, SNC, alle ossa, al fegato, al cervello. Si presenta più<br />
frequentemente con sindromi paraneoplastiche, legate all'espressione di ACTH, ADH, etc, un<br />
quadro clinico con patologie quantomai gravi. Può produrre l'hcg. Se ci troviamo in uno stadio<br />
iniziale, raramente si vede, la sopravvivenza a 2 anni è del 45%, in una fase avanzata del 4-6%. Per<br />
la terapia, questo ca, nella gran parte dei casi, non è chirurgicamente trattabile, tende a coinvolgere<br />
strutture mediastiniche. Spesso il chirurgo toracico vuole sapere se e a piccole o a grandi cell. Se è a<br />
piccole, finisce l'intervento, se è a grandi, continua.<br />
Mostra un'immagine, polmoni con righe nere, linee di antracosi (alias pneumoconiosi), e si capisce<br />
che il soggetto vive in campagna, perchè se era di città, aveva tutto il<br />
polmone nero, e coinvolge anche l'esofago e vedete tutti queste linee bianche, sono vasi linfatici, c'è<br />
una linfangite carcinomatosa.<br />
Sappiamo che è un ca a cellule staminali con una predilezione alla differenziazione endocrina. Non<br />
sempre esprime marcatori neuroendocrini, quindi cellule con un'iniziale differenziazione<br />
neuroendocrina. Se noi guardiamo il quadro morfologico, ci ricorda un linfoma, vedete, tutte<br />
piccole cellule, myc, RB, proteina di trascrizione p53, ampie aree di necrosi, come fanno i ca<br />
neuroendocrini a piccole cell. Se vediamo a più forte ingrandimento, aspetto sale e pepe. Vuol dire<br />
che il nucleo ha spazi chiari e scuri. Un altro fenomeno, che si chiama sagomatura/moulding, questo<br />
nucleo qui [indica un'immagine] si deforma per accogliere l'altro nucleo. Relativa elasticità delle<br />
membrane nucleari, in effetti una fragilità. Come se fossero di materiale plastico.<br />
Altra caratteristica, è l'effetto crash, in questo caso significa spalmare, quando un oggetto cade<br />
dall'alto, va in frantumi, questo succede al materiale nucleare. Come se fossero cadute dall'alto e si<br />
fossero frantumati in mille pezzi. Caratteristica è che se c'è positività alla citocheratina, non è<br />
diffusa; può esprimere la sinaptolisina, può esprimere N-cam (CD56), molecola di adesione neurale,<br />
dalla cresta, ed esprime TTF1, molto utile se abbiamo dei dubbi [marcatore per neoplasie<br />
polmonari, tiroidee e neuroendocrine, anche extrapolmonari, ndr].<br />
scaricato da www.sunhope.it
Ca squamoso: macroscopicamente ha delle aree di cavitazione, di necrosi, è molto grosso, spesso<br />
deforma la trachea, i bronchi, non raramente può dare un interessamento pleurico, e va in DD con il<br />
mesotelioma. Una volta questo ca si presentava soprattutto in posizione centrale, ilare, ilo e<br />
mediastino, adesso si è invertita la tendenza, tende ad essere periferico, c'è una prevalenza<br />
periferica. Illustra un'immagine. Aspetti basialioidi, una varietà molto maligna.<br />
Qui un ca sarcomatoide, positivi alla citocheratina, e quindi un ca.<br />
L'adenocarcinoma mantiene localizzazione periferica, non raramente coinvolge la pleura, illustra<br />
un'immagine, con dei piccoli focolai bianchi, micrometastasi, e linfangite. Altre immagini. Può<br />
assumere aspetti papillari o mucinosi, anello con castone, e la varietà particolare del ca<br />
bronchioloalveolare.<br />
Anche [parola incomprensibile] è difficile da vedere, un polmone un po' irregolare, se lo tagliamo,<br />
sembra quasi una fibrosi, perchè questo ca può avere due caratteristiche, mucoide o non mucoide.<br />
Se vediamo a forte ingrandimento, il parenchima, l'aspetto a cuneo non viene perso, ci sono delle<br />
cavità, come sono gli alveoli ad altro ingrandimento, non è una massa unica, ma piccole cribrosità.<br />
Questo succede perchè questo ca ha questo difetto, tende a diffondersi agli alveoli e a sostituirne le<br />
pareti. L'aspetto macroscopico sfugge anche alla TAC. Questa è la variante mucoide (immagine), e<br />
poi abbiamo il ca [altra parola incomprensibile]<br />
Ca a grandi cell, un ca con classificazione nosologica instabile, non sappiamo perchè sono grandi,<br />
non sappiamo se è un adenocarcinoma, se è differenziato, possono essere pleomorfe, giganti,<br />
oppure un ca neuroendocrino a grandi cellule...e quindi un tumore neuroendocrino.<br />
La stadiazione non è molto complessa, va in base alle dimensioni, molto importante ai fini della<br />
prognosi. Prognosi del ca non a piccole cell è molto dipendente dalla stadiazione. Mentre quello a<br />
piccole dipende dalla stadiazione fino ad un certo punto. Per l'età, nei maschi, il ca del polmone è<br />
tra i 49-59, nella donna, tra i 60-70, dove la mammella è al secondo posto.<br />
Follow up: a 5 anni, per il ca a piccole cellule sopravvive meno del 10%, l'adenocarcinoma,<br />
sopravvive più del 25%, squamoso un po' peggio, grandi cellule, un po' meglio, 11%.<br />
Altri tipi di tumori:<br />
adenoma, papilloma squamoso, e i ca che abbiamo trovato nelle ghiandole salivari, rari,<br />
linfoepitelioma like, linf frammisti a cell epiteliali atipiche, ca pleomorfo da non confondere con<br />
l'adenocarcinoma pleomorfo, componente epiteliale relativamente benigna o blastoma renale,<br />
compontente mesenchimale maligna, neuroendocrini ("carcinoidi atipici" quando sono così e così in<br />
scaricato da www.sunhope.it
termini di malignità, "carcinoidi", quando sono maligni, nel polmone), linfomi, balt (cioè malt<br />
polmonari).<br />
Sede preferenziale delle metastasi:<br />
incidenza assoluta, le metastasi più frequenti provengono dalla mammella, colon, pancreas,<br />
stomaco, cute, rene, ovaio;<br />
incidenza relativa [vale a dire la preferenza di un tumore a dare metastasi al polmone]: il carcinoma<br />
renale (raro) preferisce il polmone, così come la cuta e la mammella.<br />
Per quanto riguarda le lesioni squamoidi abbiamo: metaplasia squamosa, displasia e il ca in situ.<br />
Per le lesioni ghiandolari: la cosiddetta iperplasia (parola incomprensibile) atipica, presenta alveoli<br />
normali e anormali, possiamo ritrovare una lesione piccola, inferiore a 5 mm, scoperta per caso,<br />
talvolta adiacente ad un adenoca, in cui un piccolo gruppo di alveoli sono delimitati non da<br />
pneumociti ma da cellule con lievi e moderate atipie. È caratteristico il fatto che esistano intervalli<br />
tra cellule e cellule, uno aspetto di hobnail(?) le cellule sono separate tra di loro. Gli alveoli normali<br />
sono caratterizzati da pneumociti di tipo I appiattiti, qui invece (nel caso patologico, ndr) cellule che<br />
sporgono.<br />
Lambertosi, (da Lambert), che possiamo trovare nei bronchioli terminali terminali, che sta nel<br />
momento in cui sta per trapassare in alveolo: può succedere che l'alveolo assuma un epitelio<br />
bronchiale, colonnare. Troviamo positività per la citocheratina. [Descrive un'immagine]<br />
I tumori della pleura sono molto rari, nelle diverse casistiche, da 2 a 30 casi per milione.<br />
femmine/maschi 3 a 1, più elevata incidenza per il polmone destro. Correlato all'asbesto, e anche<br />
alla lunghezza delle fibre di asbesto, possono dare danni meccanici a seconda delle dimensioni,<br />
devono essere sottili per determinare danni, correlato anche ad altre sostanze, ma nel 60-70% si<br />
tratta di asbesto, oppure c'è la correlazione con il SV40 (Santini docet); non raramente, asbestosi e<br />
pneumoconiosi possono essere ritrovati nel parenchima adiacente. La sopravvivenza media è 15<br />
mesi, coinvolgimento precoce del mediastino, pericardio, parete toracica.<br />
La chirurgia raramente dà risultati efficaci, ci troviamo quasi sempre davanti a forme avanzate. In<br />
altri casi, possiamo riscontrare una placca senza diffusione.<br />
Talvolta si può cercare un approccio con radio, polichemio, chirurgia.<br />
I principali istotipi sono:<br />
epiteliode, e hanno una prognosi un poco migliore;<br />
sarcomatoide, con cellule fusate,<br />
classica, a cellularità mista: il mesotelio ha un aspetto epitelioide, ma deriva dal mesenchima, dal<br />
scaricato da www.sunhope.it
foglietto intermedio. Per cui ha questa doppia natura. Ci sono altre varietà ma di queste non<br />
parleremo.<br />
La pleura spesso in soggetti esposti a particolari sostanze, all'asbesto, fattori irritanti, in caso di<br />
pleurite, può essere soggetta a reazioni di iperplasia, vediamo lungo la pleura una proliferazoine di<br />
cellule mesoteliali, cubiche, che possono crescere in forma papillariforme, che può simulare un<br />
mesotelioma, ma le cellule non sono molto atipiche, bisogna stare attenti, può succedere di<br />
confondersi.<br />
Ecco come può apparire all'inizio [immagine]: chiazze biancastre che poi in una fase successiva<br />
tendono a diffondersi, aspetto a cotenna, in una fase più avanzata va ad incarcerare i polmoni, e può<br />
avere anche localizzazioni all'interno del parenchima, e perciò può simulare un adenoca, e quando<br />
l'adenoca arriva nel cavo pleurico, il cavo pleusirco accoglie bene le cellule tumorali e possono<br />
esserci delle colate di adenoca.<br />
L'aspetto della pleura [mostra immagini] Nella cellula mesoteliale, queste cavità, vacuolizzazioni<br />
sono molto frequenti, a volte può assumere un aspetto solido; qui due figure atipiche; altre volte un<br />
aspetto sarcomatoide. A volte focolai di ossificazione, aree cartilaginee maligne, sempre in gioco<br />
cellule staminali [mesenchimali, ndr] che complicano il quadro.<br />
Racconta...episodi di vita vissuta.<br />
Marcatori: calretinina; il bto1, marker dei tumori di wilms, espresso dai mesoteliomi;<br />
trombomodulina; citocheratina 5-6; ma non esprimono TTF1, dirimente per carcinoma<br />
polmonare/mesotelioma.<br />
Vagina, non vi dissanguate a studiare questi argomenti [qui niente ndr, è proprio il prof che dice<br />
così]<br />
Cisti, adenosi e dintorni.<br />
Le lesioni precancerose, con classificazioni cin e vain;<br />
Ca squamoso e adenoca (raro);<br />
Vulva: nelle anziane, lesioni infiammatorie, e distrofiche;<br />
Lesioni precancerose, in donne molto anziane, trascurate<br />
Tuba, gravidanza tubarica, le famose sorelle di keplero, rottura della tuba!<br />
cisti della tuba, endometriosi,<br />
tumori tuba, rappresentano 1% tumori maligni<br />
scaricato da www.sunhope.it
Surrene, corticale e midollare con istogenesi ed embriologia diversa<br />
La corticale può dare adenomi, carcinomi, produce degli ormoni di vario tipo, a seconda delle zone;<br />
La midollare, di derivazione neuroectodermica, può dare 3-4 tipi di tumore: neuroblastoma,<br />
gangliocitoma, ganglioneurolastoma, feocromocitoma, cercate di capire le caratteristiche distintive.<br />
Siate sintetici!<br />
Rene, inquadramento delle glomerulonefriti, si presuppone che sappiate come è fatto un glomerulo.<br />
Glomerulopatia diabetica, streptococcica, lupoide.<br />
spt i vari tipi, le caratteristiche principali, l'eziologia può anche essere tralasciata.<br />
Ipofisi, necrosi ipofisaria, sindrome di [suono simile a Shian, Schian, boh?]<br />
adenomi, che da segno di sè per compressione o rottura del tentorio sopra la sella turcica. Si può<br />
controllare la secrezione di prolattina farmacologicamente e quindi contenere la crescita della massa<br />
tumorale.<br />
Testicolo:<br />
criptorchidismo. Quali alterazioni: ha una temperatura abnorme, processo di atrofia. Conviene<br />
rimuoverlo, perchè può essere a rischio, cioè è più facile che possa avere un tumore.<br />
Sterilità, quando si fa la biopsia, per sapere se questo soggetto ha la possibilità, vogliamo vedere i<br />
tubuli, se c'è un arresto maturativo, che percentuale di tubuli coinvolti, se mancano le cell<br />
germinali...in quest'ultimo caso solo cell del sertoli, nessuna terapia può aiutare.<br />
I tumori sono come quelli dell'ovaio, a cellule germinali, ma senza tumori epiteliali: seminoma, ca<br />
embrionale, teratoma, del sacco vitellino. Comunque, ve li ho scritte per <strong>complete</strong>zza.<br />
SNC: cenni su meningoencefaliti, anche qui...non vi dissanguate. Encefalite spongiforme<br />
(Creutzfeldt-Jakob), emorragia cerebrale (perchè? dove? che succede quando c'è un'emorragia<br />
cerebrale? è un tessuto molle, quindi si creano delle cavità) Se non determina morte, il focolaio<br />
emorragico a cosa va incontro? Si cerca di rimuovere il sangue, il focolaio subirà cambiamenti di<br />
colori, può evolvere in una cicatrice, più spesso in cisti a contenuto chiaro, perchè tutto ciò che era<br />
Hb, pigmento etc, è stato assorbito dalle cellule gliali.<br />
Le malattie demielinizzanti, di grande importanza, soprattutto la sclerosi a placche, le altre<br />
lasciamole stare.<br />
C'è una demielinizzazione, le sedi preferenziali sono a livello encefalico e del midollo spinale. C'è il<br />
cosiddetto asincronismo maturativo, solo demielinizzazione, un danno d<br />
scaricato da www.sunhope.it
Osso: classificazione dei tumori dell'osso, dovete solo sapere quali sono, che cosa comportano. Si<br />
tratta perlopiù di anatomia patologica clinica.<br />
Possono formare cartilagini, quali sono le sedi preferenziali del condroma (dita), condrosarcoma, a<br />
cellule giganti, tumori del midollo osseo, collagenopatie, lupus, sclerodermia, dermatomiosite.<br />
Laringe: "polipi", tutti si ostinano a chiamarli polipi, ma sono noduli, tipica malattia da sforzo<br />
vocale, quelli che parlano in situazioni da stress, in cui bisogna alzare la voce. Classica malattia dei<br />
cantanti. C'è edema.<br />
Lesioni precancerosi, classificate con il cin, come per la cervice.<br />
Ca della laringe, squamoso, un'idea topografica della laringe, sopra/sotto-glottide, a seconda della<br />
sede caratteristiche peculiari e conseguenze prognostiche e terapeutiche.<br />
Miocarditi, poco da dire.<br />
Pericarditi, tre tipi, sierosa, fibrinosa, sierofibrinosa.<br />
Nella fibrinosa, pericardite costrittiva, ricordate i tossicodipendenti.<br />
Pericarditi vegetanti, della MR (malattia reumatica), escrescenze di fibrina<br />
Ulcerosa, nei tossicodipendenti, quando si fanno la siringa, soprattutto eroina, iniettano anche<br />
streptococchi, che solitamente stanno sulla cute, vanno nel sangue...possono determinare lesioni<br />
devastanti a livello dell'endocardio.<br />
Cardiomiopatie, principale indicazione al trapianto, potrebbe essere anche coinvolto un virus.<br />
Massimo Troisi era in lista per trapianto per cardiomiopatia dilatativa.<br />
Infarto miocardico<br />
Aterosclerosi, principali vasculiti<br />
Stateve buono [libera trascrizione delle parole dette dal prof.]<br />
scaricato da www.sunhope.it