Download - Slidetube.it
Download - Slidetube.it
Download - Slidetube.it
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
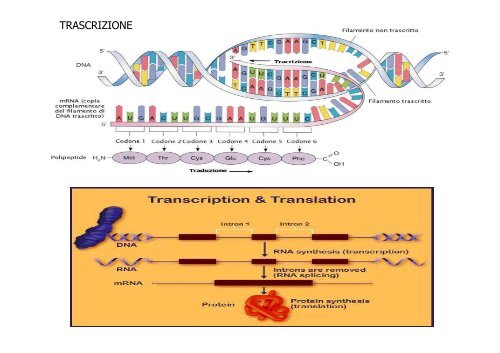
TRASCRIZIONE
Il DNA funziona da stampo per la sintesi di molecole di RNA.<br />
In questo modo l’informazione genetica<br />
diventa direttamente utilizzabile per la cellula<br />
Capac<strong>it</strong>à di esprimersi dell’informazione genetica<br />
DOGMA CENTRALE<br />
DNA<br />
(linguaggio chimico=nucleotidi)<br />
RNA<br />
(linguaggio chimico=nucleotidi)<br />
PROTEINE<br />
(linguaggio chimico=aminoacidi)<br />
TRASCRIZIONE<br />
TRADUZIONE
mRNA:<br />
porta l'informazione per la sintesi di una determinata proteina.<br />
tRNA:<br />
molecola adattatrice - ogni tRNA è specifico per il trasporto di un<br />
determinato aminoacido – converte sequenze di nucleotidi in sequenze di<br />
amminoacidi<br />
Ribosoma:<br />
INTERAZIONE TRA mRNA, tRNA e RIBOSOMI<br />
officina che permette il corretto appaiamento tra mRNA e i diversi tRNA e<br />
partecipa attivamente alla formazione della catena proteica.
Nel piano: il filamento 5'→3' assume una forma detta a quadrifoglio<br />
-zone a bracci in cui le basi sono appaiate<br />
-anse senza appaiamento per basi modificate post-trascrizionalmente<br />
Iniziando dal 5‘:<br />
- ANSA D: vi si lega l'enzima aminoacilsintetasi specifico per legare un<br />
determinato aminoacido al suo tRNA.<br />
- ANSA dell'ANTICODONE: contiene una tripletta complementare e antiparallela<br />
al codone che sull'mRNA codifica per un determinato aminoacido.<br />
- Un'ansa variabile<br />
STRUTTURA MOLECOLARE DEL tRNA<br />
- ANSA del TϕC (ϕ=pseudouracile): necessaria per il legame tra il tRNA e rRNA 5S<br />
presente nella subun<strong>it</strong>à grande del ribosoma.<br />
Il tRNA termina al 3' con un codone CCA<br />
(aggiunto postrascrizionalmente)<br />
a cui viene legato l'aminoacido specifico di quel<br />
tRNA.
Il tRNA nello spazio si ripiega in una struttura detta a L rovesciata dove<br />
rimangono bene accessibili l'ansa dell'anticodone e l'aminoacido<br />
legato.
Esempio di reazione di legame dell'aminoacido al tRNA<br />
aminoacilsintetasi leu (specifico per leucina)<br />
tRNA + LEUCINA+ ATP tRNA LEU + AMP+P+P<br />
(energia)<br />
L'aminoacido con il suo gruppo carbossilico (-COOH)<br />
si lega all'-OH del C 3 del ribosio del nucleotide (A) al<br />
3' del tRNA.<br />
Le aminoacil-sintetasi sono 20 una per ogni<br />
aminoacido.<br />
Ognuna trasferisce un AA diverso sul rispettivo tRNA.<br />
I tRNA sono più di 20 (circa 30-40 in procarioti e<br />
anche 50 in Eucarioti) per cui ad alcuni aminoacidi<br />
corrisponde più di un tRNA.
STRUTTURA MOLECOLARE DEL RIBOSOMA<br />
Il ribosoma ha una struttura molecolare complessa formata da rRNA e<br />
proteine ribosomiali.<br />
In eucarioti gli rRNA vengono prodotti nel nucleolo (tranne il 5S<br />
prodotto nel nucleo) dove entrano anche le proteine ribosomiali<br />
prodotte nel c<strong>it</strong>oplasma che si assemblano con i rispettivi rRNA per dare<br />
i ribosomi.<br />
In procarioti tutto ciò avviene nel c<strong>it</strong>oplasma.<br />
I ribosomi procariotici sono più piccoli dei ribosomi eucariotici.<br />
Le differenze tra ribosomi procariotici ed eucariotici sono dovute al<br />
numero e alle grandezze diverse degli rRNA e al numero e alle<br />
grandezze diverse delle proteine.<br />
I ribosomi sono formati da due subun<strong>it</strong>à (piccola e grande) che si<br />
assemblano solo al momento della traduzione (le due subun<strong>it</strong>à<br />
ribosomiali si assemblano e diventano funzionali solo in presenza di<br />
mRNA).
c<strong>it</strong>oplasma<br />
Proteine del<br />
ribosoma<br />
Nucleo<br />
nucleolo<br />
Assemblaggio del ribosoma<br />
c<strong>it</strong>oplasma<br />
Pori nucleari
S<strong>it</strong>o A per l’aminoacil-tRNA<br />
S<strong>it</strong>o P per il peptidil-tRNA
IN PROCARIOTI<br />
Il filamento di mRNA inizia con una sequenza detta LEADER, che non viene<br />
tradotta in proteina, contenente la sequenza di Shine-Delgarno.<br />
Tale sequenza si appaia durante la traduzione con l'rRNA 16S.<br />
La sequenza codificante inizia sempre con la tripletta AUG e termina con una<br />
tripletta detta di STOP.<br />
Segue un tratto detto TRAILER (rimorchio) non codificante.<br />
I geni che codificano per proteine sono POLICISTRONICI (ad un unico promotore<br />
seguono tutti i geni di una determinata via metabolica per cui vengono trascr<strong>it</strong>ti<br />
tutti contemporaneamente).<br />
IN EUCARIOTI<br />
L'mRNA ha struttura simile a quella dei Procarioti.<br />
In aggiunta:<br />
-5’ CAP (7-metilguanosina): si legherà all'rRNA 18S durante la traduzione<br />
-coda di poliA al 3'.<br />
STRUTTURA DEGLI mRNA<br />
I geni che codificano per proteine sono MONOCISTRONICI (ciascun gene ha il<br />
suo proprio promotore).
Perché avvenga la traduzione è necessario passare da un linguaggio<br />
fatto di NUCLEOTIDI ad un linguaggio di AMINOACIDI.<br />
Gli aminoacidi presenti in tutte le proteine sono 20 mentre le basi sono<br />
solo 4.<br />
Se ogni base specificasse per 1 amminoacido, avremmo solo 4<br />
aminoacidi specificati 4 1 =4.<br />
Se la combinazione di due basi specificasse per 1 aminoacido,<br />
avremmo:4 2 =16 aminoacidi specificati.<br />
Se la combinazione di tre basi specificasse per 1 aminoacido, avremmo:<br />
4 3 =64 combinazioni per 20 aminoacidi.<br />
Il codice pertanto è a triplette, cioè la combinazione di tre basi specifica<br />
per 1 aminoacido.<br />
Ogni tripletta è detta CODONE.<br />
IL CODICE GENETICO<br />
Esistono 3 triplette non codificano per nessun aminoacido e sono dette<br />
di STOP (UAG; UAA; UGA).
Poiché ci sono 64-3 (codoni di stop)=61 triplette per 20 aminoacidi si<br />
dice che il codice è DEGENERATO o RIDONDANTE cioè ogni<br />
aminoacido può essere specificato da più di un codone.<br />
Esempio: leucina 6 codoni, valina 4 codoni, triptofano e metionina 1<br />
codone, etc…. (Si può osservare inoltre che i diversi codoni per un<br />
aminoacido sono diversi soprattutto nella 3 base).<br />
CARATTERISTICHE DEL CODICE GENETICO<br />
Il codice genetico è UNIVERSALE cioè uguale per tutti gli esseri<br />
viventi tranne alcune eccezioni.<br />
Il codice genetico NON E' AMBIGUO cioè un determinato codone<br />
specifica per un solo aminoacido.<br />
Il codice genetico è senza punteggiature cioè viene letto linearmente<br />
(di tre basi in tre basi) e non è sovrapponibile (es. la stessa base non<br />
può essere letta come l’ultima di un codone e la prima del successivo).
MUTAZIONI PUNTIFORMI IN ZONE CODIFICANTI<br />
una base<br />
-Transizione da purina a purina (A o G) o da pirimidina a pirimidina (C o T)<br />
-Trasversione da purina a pirimidina o viceversa<br />
Conseguenze:<br />
1) nessuna se ad essere colp<strong>it</strong>a è la terza base di un codone e il nuovo codone codifica<br />
per lo stesso aminoacido<br />
2) cambio dell'aminoacido specificato dal codone ora mutato<br />
3) proteina più corta se un codone per l'aminoacido si tramuta in un codone di STOP<br />
Es. UUA→UAA<br />
(Leu→ stop)<br />
4) proteina più lunga se ad esempio da un codone di stop per mutazione si passa ad un<br />
aminoacido qualsiasi<br />
B) DELEZIONE o INSERZIONE di una base<br />
Cambio della cornice di lettura. Da quel nucleotide (deleto o inser<strong>it</strong>o) la proteina sarà<br />
tutta diversa perché a codoni diversi corrisponderanno AA diversi<br />
AUG⏐CAA⏐CCC⏐GGA⏐UAA⏐GCU⏐UAA<br />
(delezione)<br />
AUG⏐CAA⏐CCC⏐GGU⏐AAG⏐CUU⏐AA…
TRADUZIONE<br />
1) La lettura dell'mRNA procede in direzione 5'→3‘<br />
2) La sintesi proteica procede<br />
dall'estrem<strong>it</strong>à N-terminale<br />
all'estrem<strong>it</strong>à C-terminale del polipeptide<br />
3) La traduzione ha inizio sempre con<br />
Formil-metionina in Procarioti<br />
Metionina in Eucarioti.<br />
Il codone per Metionina è AUG<br />
L'anticodone è UAC.
1) INIZIO:<br />
L'mRNA si lega alla SUBUNITA' PICCOLA ribosomiale e al tRNA met (codone<br />
con anticodone) grazie a fattori di inizio (3 in procarioti, 7/8 in eucarioti) e<br />
ad 1 GTP→GMP+P+P che dona energia necessaria per il legame.<br />
L'mRNA in procarioti si lega con la sequenza SHINE-DALGARNO al 16S rRNA<br />
mentre in eucarioti l'mRNA si lega con il cappuccio (5-metilguanosina) al 18S<br />
rRNA.<br />
Successivamente si assembla la SUBUNITÀ GRANDE contenente due s<strong>it</strong>i detti<br />
A e P per accogliere i tRNA.<br />
Solo il 1° tRNA met si lega direttamente al s<strong>it</strong>o P.
2) ALLUNGAMENTO<br />
Il 2° tRNA con l‘AA corrispondente si lega all'mRNA (2°codone/anticodone) e alla<br />
subun<strong>it</strong>à grande, nel s<strong>it</strong>o A del ribosoma, grazie a fattori di allungamento (in<br />
Procarioti Ts e Tu, in Eucarioti Ef1-Ef1β) e ad 1 molecola di GTP che si scinde<br />
donando energia.<br />
Il legame che si forma tra i due AA avviene tra il gruppo carbossilico (-COOH)<br />
della metionina e il gruppo amminico (-NH 2 ) del 2° AA (legame peptidico).<br />
Enzima responsabile è la Peptidil-transferasi.<br />
Dopo la formazione del legame peptidico il 1° tRNA, rimasto scarico della<br />
metionina, viene allontanato dal s<strong>it</strong>o P.<br />
Avviene quindi la traslocazione:<br />
l'mRNA scivola di un codone trascinandosi il 2° tRNA che passa dal s<strong>it</strong>o A al s<strong>it</strong>o<br />
P, lasciando il s<strong>it</strong>o A libero per l'attacco del 3° tRNA.<br />
Questa traslocazione è mediata da un fattore di traslocazione e dalla scissione di<br />
una molecola di GTP.<br />
Il ciclo si ripete tante volte quanti sono gli AA che devono essere legati.
3) TERMINAZIONE<br />
Quando sul s<strong>it</strong>o A si trova un codone di STOP, a cui non<br />
corrisponde nessun tRNA, la sintesi si arresta.<br />
Inoltre esistono fattori di rilascio che si legano al s<strong>it</strong>o A<br />
impedendo comunque l'attacco dei tRNA.<br />
La catena polipeptidica si stacca dall'ultimo tRNA grazie<br />
ad un enzima (idrolasi) con consumo di una molecola di<br />
GTP. Le due subun<strong>it</strong>à ribosomiali si disassemblano.
IL VACILLAMENTO DELLE BASI<br />
Il legame tra codone e anticodone è complementare e<br />
antiparallelo.<br />
Esempio: 3'CAG5' (anticodone)<br />
5'GUC3' (codone)<br />
Il numero dei codoni (61) è più grande di quello degli anticodoni.<br />
61 codoni (3 sono codoni di stop) mentre i tRNA sono circa 30-40<br />
in procarioti e anche 50 in Eucarioti)<br />
Questo implica che alcune molecole di tRNA con il loro anticodone<br />
sono capaci di accoppiarsi a più di un codone.
Alcuni tRNA hanno una struttura tale da richiedere un appaiamento<br />
accurato nelle prime due posizioni del codone (5') e da tollerare un<br />
appaiamento scorretto (oscillante) in terza posizione.<br />
Questo appaiamento approssimativo rende possibile combinare 20 AA ai<br />
loro 61 codoni servendosi per esempio di solo 30/50 molecole di tRNA.<br />
Frequentemente al 5' dell'anticodone (corrispondente alla terza base<br />
del codone) esiste la base modificata inosina capace di complementarsi<br />
sia con A, C, U.
BILANCIO ENERGETICO<br />
DELLA TRADUZIONE<br />
Esempio proteina di 100 aa<br />
1 GTP per il complesso di inizio<br />
99 GTP per l'attacco dei 99 tRNA<br />
99 GTP per la traslocazione dei 99 tRNA<br />
1 GTP per il rilascio della proteina<br />
Totale 200 GTP che corrisponde a 2 GTP per ogni<br />
aminoacido.<br />
Riassumendo 1AA=2GTP
PROTEINE<br />
Le proteine sono dei polimeri di aminoacidi detti anche catene<br />
polipeptidiche.<br />
Gli aminoacidi possono essere destrogiri (D-) e levogiri (L-).<br />
Negli organismi viventi sono presenti solo L-aminoacidi. Gli<br />
aminoacidi sono 20.<br />
Ciascun aminoacido è cost<strong>it</strong>u<strong>it</strong>o da un Cα a cui sono legati un<br />
gruppo carbossilico (COOH), un gruppo amminico (NH 2 ), un H,<br />
e un gruppo variabile detto radicale. I radicali conferiscono ad<br />
ogni aminoacido la propria specific<strong>it</strong>à.
-APOLARI (idrofobici) che contengono nel radicale un gruppo idrofobico ( es.-<br />
CH3)<br />
-POLARI (idrofilici) che si suddividono in:<br />
POLARI ACIDI che contengono nel radicale un gruppo acido (es.-COOH),<br />
POLARI BASICI che contengono nel radicale un gruppo basico (es.-NH2),<br />
POLARI NON CARICHI che contengono nel loro radicale sia un gruppo acido che un<br />
gruppo basico o comunque un gruppo idrofilico per cui il loro pH è neutro.
Gli aminoacidi tra loro sono legati con un legame peptidico che si<br />
forma tra il gruppo COOH di un aminoacido e il gruppo NH 2 del<br />
successivo aminoacido con l'eliminazione di una molecola di acqua.<br />
Questo legame è un legame covalente più forte perché più breve<br />
del singolo legame e quindi si avvicina ad avere le caratteristiche<br />
di un doppio legame.
Le proteine presentano tre livelli di struttura e alcune anche un quarto<br />
livello.<br />
STRUTTURA PRIMARIA<br />
E' rappresentata dalla sequenza lineare degli aminoacidi legati da legami<br />
peptidici determinata dal gene.<br />
STRUTTURA SECONDARIA<br />
LE PROTEINE E LORO STRUTTURA<br />
Gran parte delle proteine, anche se in alcuni punti hanno una struttura<br />
irregolare, presentano lunghi tratti con una struttura regolare ad α-elica o a<br />
foglietto pieghettato β.<br />
L'α-elica e il foglietto pieghettato β sono dati da legami ad H che si<br />
instaurano tra differenti gruppi peptidici.<br />
Nell' α-elica l'ossigeno carbossilico di ciascun legame peptidico forma un<br />
legame ad idrogeno con l'idrogeno del gruppo amminico dell'aminoacido<br />
che si trova quattro residui più avanti nella sequenza lineare.<br />
Nel foglietto pieghettato β i legami ad H si instaurano tra gli atomi che<br />
formano i legami peptidici appartenenti a catene polipeptidiche diverse o a<br />
porzioni dello stesso polipeptide ripiegato su se stesso.
STRUTTURA TERZIARIA<br />
La struttura terziaria è determinata da legami che si formano tra<br />
radicali di diversi aminoacidi che organizzati nelle strutture<br />
secondarie vengono a trovarsi vicino.<br />
Tali legami possono essere di tutti i tipi<br />
( ionici, covalenti, ad idrogeno, idrofobici etc…) e determinano la<br />
struttura tridimensionale della catena polipeptidica (es. proteine<br />
globulari).<br />
La struttura terziaria viene modificata inoltre dalle interazioni degli<br />
aminoacidi con l'ambiente in cui la catena polipeptidica si trova.<br />
(es. proteine di membrana tenderanno ad esporre all'esterno gli aminoacidi<br />
idrofobici capaci di interagire con i lipidi ).<br />
STRUTTURA QUATERNARIA<br />
Alcune proteine specialmente quelle con funzione enzimatica,<br />
possono assumere una struttura quaternaria che deriva<br />
dall'associazione di più catene polipeptidiche.<br />
Se le catene polipeptidiche sono uguali si parlerà di dimeri (2 catene<br />
polipeptidiche), tetrameri (4), etc…<br />
Le catene che si associano possono essere differenti e ciascuna<br />
prende il nome di subun<strong>it</strong>à (vedi RNA-polimerasi in procarioti).
Considerando la definizione di introni indicare il rapporto corretto in<br />
ogni gene tra il numero degli esoni e degli introni:<br />
a) Esoni= introni +1<br />
b) Esoni=introni<br />
c) Esoni= introni –1<br />
d) Esoni= 2 volte gli introni
La TATA box è una sequenza presente:<br />
1. Al 5’ dei geni in procarioti<br />
2. Al 5’ dei geni per mRNA in eucarioti<br />
3. Sull’ mRNA nella sequenza leader<br />
4. Al 5’ dei geni per rRNA in eucarioti<br />
5. Al 5’ dei geni per tRNA in eucarioti
Descrivete le possibili conseguenze nella traduzione del seguente mRNA<br />
mutato rispetto a quello nativo<br />
5’ UUCCCAAUCACAUAAGUAGCC 3’ RNA mutato<br />
5’ UUCCCAAUCACAUACGUAGCC 3’ RNA nativo<br />
(codoni di stop UAG, UAA, UGA)
La polimerasi I è la polimerasi che trascrive:<br />
1. Tutti gli RNA in procarioti<br />
2. tRNA e 5S ribosomiali in eucarioti<br />
3. Gli snRNA e si trova nel nucleolo<br />
4. Gli rRNA e si trova nel nucleolo<br />
5. Gli hnRNA in eucarioti
RNA-POLIMERASI I<br />
Si trova nel nucleolo<br />
1) Trascrive un filamento precursore 45S da cui vengono poi r<strong>it</strong>agliati i tre rRNA: 28S,<br />
18S, 5,8S.<br />
2) Il DNA contenente i geni per gli rRNA si trova nel nucleolo.<br />
3) La trascrizione avviene nel nucleolo<br />
4) Le proteine ribosomiali vengono prodotte nel c<strong>it</strong>oplasma e successivamente rientrano nel<br />
nucleo e quindi nel nucleolo dove si assemblano con i rispettivi rRNA per dare le due<br />
subun<strong>it</strong>à ribosomiali.<br />
1) La polimerasi I ha bisogno di 2 fattori trascrizionali generali (B ed S) per poter<br />
iniziare la trascrizione che si legano al promotore (da -100/-50 a +20).<br />
RNA-POLIMERASI III<br />
Si trova nel nucleo.<br />
1) Trascrive i diversi tRNA e l' rRNA 5S (unico ribosomiale non prodotto nel nucleolo<br />
dove poi migrerà).<br />
2) La polimerasi III ha bisogno di fattori di trascrizione generali per iniziare (A,B,C<br />
per rRNA 5S e B,C per i tRNA).<br />
3) Le zone regolatrici di attacco dei fattori trascrizionali e RNA-polimerasi non sono a<br />
monte del trascr<strong>it</strong>to ma a valle: Promotori Interni.
RNA-POLIMERASI II<br />
Si trova nel nucleo.<br />
1) Trascrive RNA primari (hnRNA) che successivamente verranno modificati<br />
(maturazione) per dare mRNA funzionanti.<br />
2) Per iniziare ha bisogno di fattori trascrizionali generali (D, B, F, E, H).<br />
3) Tali fattori si legano ad una sequenza del promotore detta TATA BOX (-<br />
40).<br />
Esistono anche a monte della TATA BOX sequenze ricche di CG e CAAT BOX<br />
.