Download
Download
Download
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Figura 1<br />
o perdita del proprio potere filtrante e protettivo;<br />
dalla conseguente fotodegradazione si ottengono<br />
frammenti molecolari, potenzialmente pericolosi,<br />
che possono indurre sensibilizzazione allergica o<br />
processi irritativi sulla cute stessa. La fotostabilità<br />
del filtro solare pertanto rappresenta, oltre<br />
che un fattore di durata della protezione solare,<br />
anche un fattore di sicurezza. La fotodegradazione<br />
può essere impedita:<br />
f utilizzando contemporaneamente più fattori<br />
protettivi (protezione sinergica);<br />
f utilizzando filtri fotostabili a determinate lunghezza<br />
d’onda;<br />
f proteggendo gli stessi filtri tramite sistemi di<br />
complessazione, incapsulazione o inclusione come<br />
per esempio ciclodestrine o liposomi (3).<br />
Sulla base di ciò è nata l’idea di impiegare anche<br />
matrici inorganiche lamellari, che sono in grado<br />
di intercalare delle molecole organiche, e progettare<br />
formulazioni in cui queste possano svolgere<br />
azione protettiva nei confronti della molecola<br />
ospitata. Sono state quindi utilizzate delle idrotalciti<br />
sintetiche, appartenenti alla famiglia delle<br />
argille anioniche, a base di ossidi di alluminio,<br />
magnesio e zinco. Considerando che le argille:<br />
f sono costituenti di prodotti cosmetici;<br />
f sono impiegate proprio in formulazioni a uso<br />
topico per proteggere la pelle;<br />
f gli ossidi di magnesio, di alluminio e soprattutto<br />
di zinco hanno proprietà schermanti.<br />
È sembrato razionale includere in esse dei filtri<br />
solari, per ottenere un prodotto di inclusione che<br />
potesse sia stabilizzare il filtro sia aumentare la<br />
protezione dai raggi UV.<br />
Argille anioniche: idrotalciti<br />
Le idrotalciti, o argille anioniche, sono miscele di<br />
idrossidi lamellari, naturali o sintetici, contenenti<br />
anioni scambiabili e sono molto meno note e<br />
diffuse in natura rispetto alle argille cationiche. Il<br />
crescente interesse verso questi solidi lamellari è<br />
giustificato dal vasto campo delle loro applicazioni.<br />
L’ idrotalcite (HTlc), infatti, è un materiale molto<br />
versatile che trova applicazione in molti settori<br />
come catalizzatore, adsorbente, nelle preparazioni<br />
cosmetiche, in preparazioni odontoiatriche e in<br />
Kosmetica • aprile 2008<br />
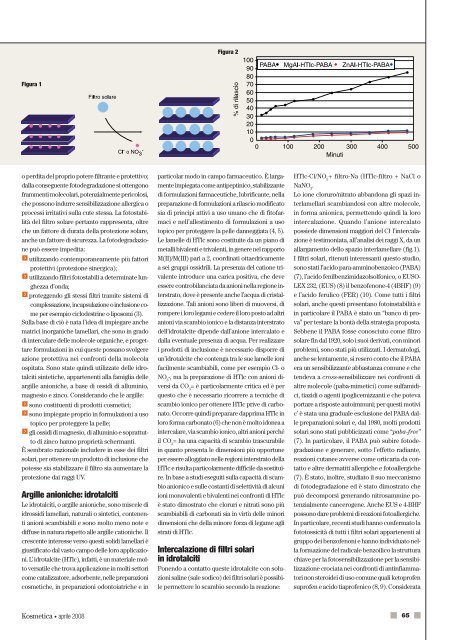
Figura 2<br />
particolar modo in campo farmaceutico. È largamente<br />
impiegata come antipeptinico, stabilizzante<br />
di formulazioni farmaceutiche, lubrificante, nella<br />
preparazione di formulazioni a rilascio modificato<br />
sia di principi attivi a uso umano che di fitofarmaci<br />
e nell’allestimento di formulazioni a uso<br />
topico per proteggere la pelle danneggiata (4, 5).<br />
Le lamelle di HTlc sono costituite da un piano di<br />
metalli bivalenti e trivalenti, in genere nel rapporto<br />
M(II)/M(III) pari a 2, coordinati ottaedricamente<br />
a sei gruppi ossidrili. La presenza del catione trivalente<br />
introduce una carica positiva, che deve<br />
essere controbilanciata da anioni nella regione interstrato,<br />
dove è presente anche l’acqua di cristallizzazione.<br />
Tali anioni sono liberi di muoversi, di<br />
rompere i loro legami e cedere il loro posto ad altri<br />
anioni via scambio ionico e la distanza interstrato<br />
dell’idrotalcite dipende dall’anione intercalato e<br />
dalla eventuale presenza di acqua. Per realizzare<br />
i prodotti di inclusione è necessario disporre di<br />
un’idrotalcite che contenga tra le sue lamelle ioni<br />
facilmente scambiabili, come per esempio Cl- o<br />
NO 3 -, ma la preparazione di HTlc con anioni diversi<br />
da CO 3 = è particolarmente critica ed è per<br />
questo che è necessario ricorrere a tecniche di<br />
scambio ionico per ottenere HTlc prive di carbonato.<br />
Occorre quindi preparare dapprima HTlc in<br />
loro forma carbonato (6) che non è molto idonea a<br />
intercalare, via scambio ionico, altri anioni perché<br />
il CO 3 = ha una capacità di scambio trascurabile<br />
in quanto presenta le dimensioni più opportune<br />
per essere alloggiato nelle regioni interstrato della<br />
HTlc e risulta particolarmente difficile da sostituire.<br />
In base a studi eseguiti sulla capacità di scambio<br />
anionico e sulle costanti di selettività di alcuni<br />
ioni monovalenti e bivalenti nei confronti di HTlc<br />
è stato dimostrato che cloruri e nitrati sono più<br />
scambiabili di carbonati sia in virtù delle minori<br />
dimensioni che della minore forza di legame agli<br />
strati di HTlc.<br />
Intercalazione di filtri solari<br />
in idrotalciti<br />
Ponendo a contatto queste idrotalcite con soluzioni<br />
saline (sale sodico) dei filtri solari è possibile<br />
permettere lo scambio secondo la reazione:<br />
HTlc-Cl/NO 3 + filtro-Na (HTlc-filtro + NaCl o<br />
NaNO 3 .<br />
Lo ione cloruro/nitrato abbandona gli spazi interlamellari<br />
scambiandosi con altre molecole,<br />
in forma anionica, permettendo quindi la loro<br />
intercalazione. Quando l’anione intercalato<br />
possiede dimensioni maggiori del Cl - l’intercalazione<br />
è testimoniata, all’analisi dei raggi X, da un<br />
allargamento dello spazio interlamellare (fig.1).<br />
I filtri solari, ritenuti interessanti questo studio,<br />
sono stati l’acido para-amminobenzoico (PABA)<br />
(7), l’acido fenilbenzimidazolsolfonico, o EUSO-<br />
LEX 232, (EUS) (8) il benzofenone-4 (4BHF) (9)<br />
e l’acido ferulico (FER) (10). Come tutti i filtri<br />
solari, anche questi presentano fotoinstabilità e<br />
in particolare il PABA è stato un “banco di prova”<br />
per testare la bontà della strategia proposta.<br />
Sebbene il PABA fosse conosciuto come filtro<br />
solare fin dal 1920, solo i suoi derivati, con minori<br />
problemi, sono stati più utilizzati. I dermatologi,<br />
anche se lentamente, si resero conto che il PABA<br />
era un sensibilizzante abbastanza comune e che<br />
tendeva a cross-sensibilizzare nei confronti di<br />
altre molecole (paba-mimetici) come sulfamidici,<br />
tiazidi o agenti ipoglicemizzanti e che poteva<br />
portare a risposte autoimmuni; per questi motivi<br />
c’ è stata una graduale esclusione del PABA dalle<br />
preparazioni solari e, dal 1980, molti prodotti<br />
solari sono stati pubblicizzati come “paba-free”<br />
(7). In particolare, il PABA può subire fotodegradazione<br />
e generare, sotto l’effetto radiante,<br />
reazioni cutanee avverse come orticaria da contatto<br />
e altre dermatiti allergiche e fotoallergiche<br />
(7). È stato, inoltre, studiato il suo meccanismo<br />
di fotodegradazione ed è stato dimostrato che<br />
può decomporsi generando nitrosammine potenzialmente<br />
cancerogene. Anche EUS e 4-BHF<br />
possono dare problemi di reazioni fotoallergiche.<br />
In particolare, recenti studi hanno confermato la<br />
fototossicità di tutti i filtri solari appartenenti al<br />
gruppo dei benzofenoni e hanno individuato nella<br />
formazione del radicale benzoilico la struttura<br />
chiave per la fotosensibilizzazione per la sensibilizzazione<br />
crociata nei confronti di antinfiammatori<br />
non steroidei di uso comune quali ketoprofen<br />
suprofen e acido tiaprofenico (8, 9). Considerata<br />
65