EM_Lezione 13.pdf
EM_Lezione 13.pdf
EM_Lezione 13.pdf
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Lezione</strong> 13<br />
Duplicazione genica ed espansione<br />
del genoma
• Lynch Capitolo 9<br />
• Grauer and Li Capitolo 6
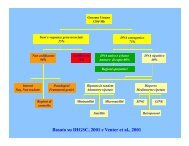
Modalità di duplicazione genica<br />
1. Duplicazione intragenica<br />
2. Duplicazione completa di un gene<br />
3. Parziale duplicazione cromosomica (polisomia paraziale)<br />
4. Duplicazione cromosomica completa (polisomia)<br />
5. Duplicazione genomica (poliploidia)
Regioni interessate<br />
dalla duplicazione<br />
Parte di un gene<br />
Intero gene<br />
Polisomia parziale<br />
Polisomia<br />
Poliploidia<br />
Frequenza<br />
Molto<br />
frequente<br />
frequente<br />
raro<br />
comune<br />
comune<br />
Effetto sulla Fitness<br />
Deleterio se cambia il reading<br />
frame.<br />
Deleterio solo in organismi in<br />
cui il genoma è replicato come<br />
un’unica molecola.<br />
Quasi sempre deleterio.<br />
Quasi sempre deleterio.<br />
L’effetto deleterio dipende dalle<br />
modalità di riproduzione
Equal & Unequal Crossing Over
Domini<br />
Dominio funzionale: una regione specifica in una<br />
proteina che svolge una funzione specifica.<br />
Esempio: dominio di legame del substrato<br />
Dominio strutturale o modulo: una regione ben definita<br />
in una proteina che costituisce un’unità strutturale<br />
stabile e compatta che può essere distinta da tutte le<br />
altre unità.
Dominio funzionale<br />
Definire i confini di un dominio funzionale spesso<br />
non è semplice perchè la funzionalità in molti casi è a<br />
carico di residui aminoacidici che sono sparsi lungo il<br />
polipeptide<br />
Cytochrome P450 2D6<br />
7
Dominio strutturale o modulo<br />
Moduli strutturali sono colineari con la sequenza<br />
aminoacidica di una proteina, quindi un modulo consiste di<br />
una sequenza continua di aminoacidi<br />
Se la funzionalità è a carico di un modulo una<br />
duplicazione aumenterà il numero di segmenti<br />
funzionali.<br />
Se la funzionalità è a carico di residui aminoacidici<br />
distribuiti in diversi moduli una duplicazione potrebbe<br />
non essere efficace dal punto di vista funzionale
Possibili relazioni tra esoni<br />
di un gene e domini<br />
strutturali della proteina<br />
codificata<br />
a e b: tipici di molte<br />
proteine globulari<br />
c: molto comune<br />
d ed e: molto rari<br />
Intron sliding<br />
Intron loss<br />
Intron acquisition
Globine dei vertebrati:<br />
4 domini<br />
3esoni<br />
Uno stesso esone può codificare più di un<br />
dominio: in questo caso l’esone 3 codifica per<br />
i due domini centrali
Perdita di introni durante l’evoluzione dei geni delle globine<br />
Il gene ancestrale aveva 4 esoni e 3 introni (il numero nel cerchio corrisponde all’introne perso)<br />
Struttura<br />
ancestrale
Duplicazione di domini<br />
Ricostruzione dell’evoluzione di un dominio dinucleotide‐binding<br />
della gliceraldeide‐3‐fosfato deidrogenasi
Duplicazione di domini<br />
immunoglobuline<br />
Possibile origine: duplicazione interna al<br />
gene ancestrale<br />
Funzione attuale molto diversa
Duplicazione di domini<br />
Il gene ovomucoide<br />
L’ovomucoide è un inibitore della tripsina, un enzima che catalizzala digestione delle<br />
proteine. Si trova nell’albume dell’uovo degli uccelli. Il polipeptide può essere diviso in 3<br />
domini, ognuno dei quali può legare una molecola di tripsina o un’altra serin proteasi<br />
Ogni dominio: 2 esoni e un introne<br />
E1 E2 E3 E4 E5 E6<br />
Ensembl:ENSGALG00000003512<br />
Duplicazione da un iniziale dominio<br />
codificato da due esoni<br />
2x<br />
E1 E2 E1 E2 E5 E6<br />
2x
Duplicazione di domini<br />
Geni antigelo nei pesci<br />
I fluidi dei teleostei ghiacciano da ‐1.0 a ‐0.7 °C<br />
Oceano Altlantico: ‐1.9 °C<br />
Nel sangue dei pesci antartici c’è una proteina che inibisce la crescita dei cristalli di<br />
ghiaccio nei fluidi corporei<br />
Una di queste proteine deriva dall’acquisizione di funzione a seguito di una duplicazione<br />
Ogni gene della famiglia codifica per un precursore (grossa poliproteina)<br />
→Traduzione → taglio enzimatico e produzione di numerose glicoproteine<br />
Abbassamento della temperatura dell’Oceano Atlantico: 10‐14 milioni di anni fa<br />
Comparsa del gene antigelo: 5‐14 milioni di anni fa<br />
E’ possibile ricostruirne l’evoluzione perché è relativamente recente
Geni antigelo nei pesci: probabile evoluzione<br />
(molti cambiamenti e funzione completamente nuova in un breve tempo: pressione selettiva)<br />
Da un gene con 6 esoni<br />
Delezione ed ‘esonizzazione’ di<br />
5 nucleotidi esonici: nuovo<br />
gene con 2 esoni<br />
4x Duplicazione di Thr‐Ala‐Ala<br />
Aggiunta di uno spaziatore<br />
(parte grigia)<br />
Ripetizioni interne = 41 repeats
Duplicazione genica<br />
Destino dei geni duplicati:<br />
1. Tutte le copie mantengono la stessa<br />
funzione.<br />
2. Alcune copie scompaiono.<br />
3. Alcune copie evolvono con una nuova<br />
funzione.<br />
X
Duplicazione genica: Tutte le copie mantengono la stessa funzione<br />
Numbers of rRNA and tRNA genes per haploid genome in various organisms<br />
__________________________________________________________________________<br />
Genome Source Number of Number of Approximate<br />
rRNA sets tRNA genes a genome size (bp)<br />
__________________________________________________________________________<br />
Human mitochondrion 1 22 2 × 10 4<br />
Nicotiana tabacum chloroplast 2 37 2 × 10 5<br />
Escherichia coli 7 ~ 100 4 × 10 6<br />
Neurospora crassa ~ 100 ~ 2,600 2 × 10 7<br />
Saccharomyces cerevisiae ~ 140 ~ 360 5 × 10 7<br />
Caenorhabditis elegans ~ 55 ~ 300 8 × 10 7<br />
Tetrahymena thermophila 1 ~ 800 c 2 × 10 8<br />
Drosophila melanogaster 120-240 590-900 2 × 10 8<br />
Physarum polycephalum 80-280 ~ 1,050 5 × 10 8<br />
Euglena gracilis 800-1,000 ~ 740 2 × 10 9<br />
Human ~ 300 ~ 1,300 3 × 10 9<br />
Rattus norvegicus 150-170 ~ 6,500 3 × 10 9<br />
Xenopus laevis 500-760 6,500-7,800 8 × 10 9<br />
__________________________________________________________________________<br />
Tutte le copie sono molto simili: selezione purificante o evoluzione concertata?
Duplicazione genica: Tutte le copie mantengono la stessa funzione<br />
Opsine<br />
Opsina λ (nm) Stimolata dalla luce cromosoma<br />
Rossa 560 Rossa Gialla Bianca X<br />
Verde 530 Gialla Bianca X<br />
Blu 430 Blu Bianca autosoma<br />
96%<br />
identità<br />
aminoacidi<br />
43%
Duplicazione genica: Tutte le copie mantengono la stessa funzione<br />
New world monkeys (NWM) Old world monkeys (OWM)<br />
1 autosomico<br />
1 X‐linked polimorfico!<br />
Nelle NWM c’è polimorfismo (più<br />
alleli con sensibilità diverse alla<br />
luce) per il gene sull’X<br />
Solo le femmine eterozigote<br />
possono essere tricromiche, i<br />
maschi sono sempre dicromici<br />
25‐35 milioni di anni fa<br />
Autos X X<br />
Dopo 25‐35<br />
milioni di<br />
anni fa<br />
Nelle OWM la tricromia è<br />
possibile in entrambi i sessi grazie<br />
alla duplicazione dei geni sull’X
Duplicazione genica: Tutte le copie mantengono la stessa funzione
Duplicazione genica: perdita di funzione di una delle copie<br />
Ci sono ~7000 malattie genetiche documentate in letteratura che<br />
testimoniano come una mutazione possa distruggere la funzione di<br />
un gene che codifica per una proteina.<br />
PERO’:<br />
“As long as there are other copies of a gene that function normally, a<br />
duplicate gene may accumulate deleterious mutations and become<br />
nonfunctional without adversely affecting the fitness of the<br />
organism.”<br />
J. B. S. Haldane (1933)<br />
“Because deleterious mutations occur far more often than<br />
advantageous ones, a redundant duplicate gene is more likely to<br />
become nonfunctional than to evolve into a new gene.”<br />
Susumu Ohno (1972)
Processati<br />
Geni retrotrasposti (es.<br />
LINE e SINE)<br />
Pseudogeni<br />
Non processati<br />
(duplicated)<br />
Perdita di funzione per<br />
silenziamento di un<br />
gene post‐duplicazione<br />
Molto comuni Comuni<br />
Unitari<br />
L’unica copia rimasta è<br />
uno pseudogene<br />
Molto rari
Duplicazione genica: perdita di funzione di una delle copie<br />
Pseudogeni unitari<br />
Come si può fissare in una popolazione la perdita di un gene?<br />
Per deriva se la selezione è rilassata<br />
Ipoascorbemia o scrobuto = incapacità di sintetisi dell’acido ascorbico<br />
Cavie<br />
Uomo si ammalano di scorbuto se non assumo acido ascorbico (vitamina C)<br />
Trote<br />
Lo pseudogene non ha una controparte funzionante: pseudogene unitario<br />
Mutazioni diverse in uomo e cavia: perdita di funzione in momenti diversi<br />
X
Duplicazione genica: perdita di funzione di una delle copie<br />
Pseudogeni non processati<br />
Molti esempi nelle globine<br />
Polyadenilation<br />
signal
Duplicazione e<br />
divergenza<br />
Clusters separati (Mammiferi e<br />
uccelli)<br />
Separazione di<br />
geni<br />
Fusione di<br />
esoni o<br />
inserzione di<br />
introni<br />
Evoluzione delle globine<br />
Espansione del cluster<br />
geni αβ uniti (Xenopus)<br />
Globina singola (lamprede) o globina ancestrale<br />
(mioglobina)<br />
Leghemoglobina (piante)<br />
700 600 500 400 300 200 100 milioni di anni
Muscolare<br />
Globulare<br />
Monomerica<br />
Prima dell’emergenza degli anellidi<br />
Hb: trasporto O 2 nel sangue, tetramerica<br />
Duplicazione genica in tandem<br />
Divergenza tra tipi<br />
adulti e non
Nell’uomo
Ipotesi sull’origine degli introni
Ipotesi sull’origine degli introni<br />
Introni di gruppo I batteri, organelli identificati circa 1500<br />
Introni di gruppo II “ identificati circa 200<br />
Introni con spliceosomi genoma nucleare di eucarioti<br />
Assenti nei procarioti,<br />
molto variabili in<br />
numero negli eucarioti
Ipotesi sull’origine degli introni<br />
L’ipotesi introns‐early<br />
(la teoria esonica dei geni)<br />
Geni ancestrali possedevano introni self‐<br />
splicing.<br />
La maggioranza di questi furono persi<br />
negli Eubatteri e negli Archaea.<br />
Negli Eucarioti, gli introni self‐splicing si<br />
sono evoluti in ‘spliceosomal introns’. Walter Gilbert
Ipotesi sull’origine degli introni<br />
L’ipotesi introns‐late<br />
I geni ancestrali non possedevano introni<br />
L’aggiunta degli introni è avvenuta dopo<br />
la formazione delle cellule ecucariotiche<br />
e il processo di endosimbiosi che ha dato<br />
origine ai mitocondri<br />
Spliceosomal introns nucleari sono<br />
derivati da introni del gruppo II (self‐<br />
splicing) che a loro volta sono derivati da<br />
elementi trasponibili<br />
Russell Doolittle
Ipotesi sull’origine degli introni<br />
Modelli di mantenimento, guadagno e perdita di introni<br />
•Non c’è un semplice modello filogenetico (specie con molti e<br />
pochi introni sono sparse nell’albero filogenetico degli eucarioti)<br />
•Se l’antenato comune fosse stato povero di introni (questi<br />
ultimi duqne derivassero da recenti inserzioni) ci<br />
aspetteremmo POCA corrispondenza nella posizione degli<br />
introni in specie distanti<br />
•Se l’antenato fosse stato ricco di introni (specie povere per via<br />
di massicce perdite di sequenze introniche) ci aspetteremmo<br />
MOLTA corrispondenza nella posizione degli introni in specie<br />
distanti
Ipotesi sull’origine degli introni<br />
Le stime indicano una perdita di introni<br />
lungo molte linee, ma assumono che:<br />
1. Che tutte le posizioni introniche<br />
condivise riflettano introni ancestrali<br />
2. Che gli introni vengano persi con lo<br />
stesso tasso in tutte le linee
Ipotesi sull’origine degli introni<br />
Intron early (IE) Intron late (IL)<br />
Buona densità intronica in antenati di<br />
eucarioti<br />
Un numero significativo viene datato a<br />
centinaia di milioni di anni fa<br />
Le linee eucariote quasi senza introni<br />
avrebbero subito una massiccia perdita:<br />
questo supporta la possibilità che nei<br />
procarioti sia successo lo stesso<br />
La maggior parte degli introni dovrebbe<br />
essere di ‘fase 0’: vero soprattutto in<br />
introni ‘antichi’<br />
Non ci sono spliceosomal introns nei<br />
procarioti<br />
Se la sopravvivenza di un introne che si<br />
inserisce in un gene integro dipende dal<br />
mantenimento della fase, allora la<br />
presenza di fase 0 supporta anche<br />
l’ipotesi IL<br />
Questo vale soprattutto se avviene un<br />
salto di esone (exon skipping)
Ipotesi sull’origine degli introni
Ipotesi sull’origine degli introni
Ipotesi sull’origine degli introni
Ipotesi sull’origine degli introni<br />
Il costo degli introni<br />
1. Diminuiscono la fedeltà e l’efficienza della trascrizione:<br />
allungamento dei trascritti eucarioti= 20‐40 bp / secondo<br />
Un gene umano 1.3 Kb DNA codificante totale con 8 introni di 4.8Kb<br />
l’uno = 22 minuti<br />
→ 30x allele senza introni<br />
2. Pericolose mutazioni ai siti di splicing (GT 5’ ; AG 3’ ; una A centrale<br />
e anche altre sequenze): numero di basi precise necessarie per ogni<br />
introne ≈25<br />
Se il tasso di mutazione è di 10 ‐9 ‐ 10 ‐7 per sito per generazione, gli<br />
introni aumentano di 25x 10 ‐9 ‐ 10 ‐7 volte la probabilità di subire<br />
una mutazione deleteria
Ipotesi sull’origine degli introni<br />
Organismi multicellulari: 5‐7 introni per gene codificante<br />
Organismi unicellulari: pochi introni in tutto il genoma<br />
Il successo di nuovi alleli che hanno guadagnato o perso introni<br />
dipende dalle dimensioni delle popolazioni!<br />
Possibili spiegazioni (Lynch)<br />
1. Selezione meno efficiente in popolazioni grandi, mantenimento di<br />
nuovi introni potenzialmente dannosi, barriera alla colonizzazione<br />
intronica in specie con N grandi<br />
2. Da qui consegue che introni con più sito‐specificità (più esigenti)<br />
hanno un coefficiente di selezione più alto, quindi a parità di N<br />
saranno meno frequenti→ mol esempi!
Ipotesi sull’origine degli introni<br />
Possibili spiegazioni (Roy and Gilbert)<br />
Sostengono che l’evoluzione degli eucarioti sia stata caratterizzata da<br />
più perdite che guadagni di introni → Intron Early<br />
Ne consegue che le differenze tra specie in numero di introni<br />
sarebbero dovute a differenti tassi di perdita di introni ancestrali<br />
Organismi che evolvono<br />
lentamente tendono a<br />
mantenere più introni<br />
ancestrali<br />
Organismi che evolvono<br />
velocemente tendono a<br />
perdere più velocemente<br />
introni ancestrali<br />
Se gli introni vengono persi con modalità Aa (RT‐mRNA + conversione genica) il tasso di<br />
perdita dipenderà dal tasso di ricombinazione tra paraloghi (geni prodotti da<br />
duplicazione intraspecifica)<br />
Se le ricombinazioni avvengono durante la meiosi specie con tempi di generazione più<br />
lunghi devono avere mantenuto più introni
Ipotesi sull’origine degli introni<br />
Possibili spiegazioni (Roy and Gilbert)<br />
Se le ricombinazioni avvengono durante la meiosi specie con tempi di<br />
generazione più lunghi devono avere mantenuto più introni<br />
Alcune osservazioni supportano questa conclusione, ma altre sembrano<br />
suggerire che ci siano specie con tassi rapidi di perdita e guadagno, e specie<br />
con tassi lenti di perdita e guadagno (anche di 10x!) → differenze dovute a<br />
specificità biomolecolari<br />
Domande ancora aperte:<br />
1. Come si creano nuovi introni? Quanto omogeneo tra diverse specie è il<br />
meccanismo?<br />
2. Perché si crearono gli introni? Ruolo attivo nel formare nuovi geni? Massiccio<br />
evento di trasposizione? Creazione di un coordinamento tra trascrizione e<br />
traduzione?<br />
3. Perché diverse specie mostrano numeri di introni così differenti?