Piede Torto Congenito: aspetti clinici e genetici Congenital clubfoot ...
Piede Torto Congenito: aspetti clinici e genetici Congenital clubfoot ...
Piede Torto Congenito: aspetti clinici e genetici Congenital clubfoot ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Rivista Italiana di Genetica e Immunologia Pediatrica - Italian Journal of Genetic and Pediatric Immunology<br />
Anno III numero 1 - gennaio 2010 | direttore scientifico: Carmelo Salpietro - direttore responsabile: Giuseppe Micali<br />
Home page Norme editoriali | Stampa l'articolo Motore di ricerca<br />
Numeri precedenti 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 ◀ Indietro pagina 7 Avanti ►<br />
<strong>Piede</strong> <strong>Torto</strong> <strong>Congenito</strong>: <strong>aspetti</strong> <strong>clinici</strong> e <strong>genetici</strong><br />
<strong>Congenital</strong> <strong>clubfoot</strong>: clinical and genetic aspects<br />
Ilaria Sanzarello 1 , Piera Vicchio, Sara Manti, Laura Colavita, Stefania Marvaso, Caterina Grosso, Valeria Ferraù<br />
1 Università Campus Bio-Medico di Roma<br />
Dipartimento di Scienze Pediatriche, UOC Genetica e Immunologia Pediatrica Università di Messina<br />
Abstract<br />
Clubfoot is one of the most common birth defects involving the<br />
musculoskeletal system. Idiopathic <strong>clubfoot</strong> is an isolated deformity of the foot<br />
and leg that is identifiable in utero and consists of four components: equinus,<br />
hindfoot varus, forefoot adductus, and cavus. Clubfoot deformity may be<br />
associated with myelodysplasia, arthrogryposis, or multiple congenital<br />
abnormalities. When untreated, children with <strong>clubfoot</strong> walk on he sides and/or<br />
tops of their feet, resulting in callus formation, potential skin and bone<br />
infections, inability to wear standard shoes, and substantial limitations in<br />
mobility and employment opportunities. Many theories have been proposed to<br />
explain the etiology of idiopathic <strong>clubfoot</strong> including vascular deficiencies,<br />
environmental factors, in utero positioning, abnormal muscle insertions, and<br />
genetic factors. Understanding the exact genetic etiology of <strong>clubfoot</strong> may<br />
eventually be helpful in determining both prognosis and the selection of<br />
appropriate treatment methods in individual patients. The primary treatment<br />
goal is to provide long-term correction with a foot that is fully functional and<br />
pain-free. To achieve this, a combination of approaches that applies the<br />
strengths of several methods may be needed. Avoidance of extensive<br />
soft-tissue release operations in the primary treatment should be a priority,<br />
and the use of surgery for <strong>clubfoot</strong> correction should be limited only after<br />
failed conservative methods.<br />
Riassunto<br />
Il piede torto congenito (PTC) è considerata una delle più frequenti<br />
malformazioni congenite presenti alla nascita in associazione con la displasia<br />
dell'anca. Si tratta di una deformità caratterizzata da uno stabile atteggiamento<br />
vizioso del piede dettata da un anomalo sviluppo delle ossa tarsali al quale si<br />
associano secondariamente alterazioni capsulari, legamentose, muscolo<br />
tendinee e delle fasce. In generale, quando si parla di piede torto congenito ci<br />
si riferisce sempre alla varietà più frequente: il piede equino-varo-addottosupinato<br />
L’eziologia è tutt’ora sconosciuta, anche se sono state avanzate varie<br />
teorie come quella genetica, quella embrionaria, quella meccanica, quella<br />
neurogena, quella vascolare etc. etc.... Nel 20% circa dei casi il piede torto è<br />
associato ad altre anomalie quali: artrogriposi distale, mielomeningocele,<br />
distrofia miotonica congenita, altre sindromi genetiche (trisomia 18, sindrome<br />
da delezione 22q11). In futuro l’approccio “genome wide association study”<br />
potrebbe essere molto utile nell’identificazione di geni di suscettibilità<br />
coinvolti nell’eziologia del PTC, al fine di individuare terapie sempre più<br />
mirate. La terapia prevede differenti approcci in base alla severità di<br />
presentazione clinica. Il trattamento è conservativo, almeno inizialmente, ma<br />
può divenire cruento se il risultato funzionale non è soddisfacente. Le forme<br />
piu' gravi richiedono necessariamente un trattamento chirurgico.<br />
Introduzione<br />
Il piede torto congenito (PTC) è una deformità, già presente alla nascita,<br />
caratterizzata da un atteggiamento viziato permanente del piede rispetto alla gamba,<br />
tale che il contatto del piede col suolo non avviene più nei punti di appoggio normali,<br />
ne conseguono alterazioni capsulari, legamentose, muscolo tendinee e delle fasce.<br />
E’ considerato una delle più frequenti malformazioni congenite, occupa infatti il<br />
secondo posto dopo la displasia dell'anca. La sua incidenza si aggira intorno all’ 1.5<br />
su 1000 nati, il rapporto maschi-femmine è 2:1 e la patologia presenta bilateralità nel<br />
65% dei casi. E’ frequente la concomitanza con altre malformazioni, in particolare la<br />
lussazione congenita dell’ anca o il torcicollo miogeno. L’ eredo-familiarità è<br />
dimostrata nel 15% dei casi ed è abbastanza frequente il suo riscontro nel contesto<br />
di osteodisplasie genotipiche o sindromi dismorfiche dello scheletro. Ha la tendenza<br />
a recidivare sino all’ età di 5-7 anni.<br />
Eziopatogenesi<br />
Rappresenta il risultato di un arresto di sviluppo, che fissa il piede in un<br />
atteggiamento che è proprio del periodo precoce della vita embrionaria: tra il 1° e il<br />
2° mese infatti, il piede è atteggiato in equinismo diretto; alla fine del 2° in<br />
supinazione e verso la metà del 3° in flessione dorsale a 90°; con l’ inizio del 4°<br />
mese comincia a ruotare in senso pronatorio, raggiungendo gradatamente l’<br />
atteggiamento definitivo. L’ evoluzione del piede può arrestarsi in questo stadio con<br />
persistenza, a sviluppo ultimato, dell’ atteggiamento in equino-varo-supinazione.<br />
L’eziologia è tutt’ora sconosciuta, anche se sono state avanzate varie teorie come<br />
quella genetica, quella embrionaria, quella meccanica, quella neurogena etc. etc..,<br />
nessuna di queste, tuttavia, confermate con certezza. Secondo la teoria genetica,<br />
l’alterazione agirebbe sullo sviluppo del piede in epoca embrionaria non<br />
consentendo il fisiologico processo di maturazione. Secondo la teoria embrionaria<br />
esistono dei fattori esterni ambientali che possono determinare l’arresto di sviluppo<br />
del piede. La teoria meccanica prevede l’esistenza di svariate condizioni uterine<br />
(briglie amniotiche, oligoidramnios, cordone ombelicale, anomalie uterine, ecc) o<br />
fetali (macrosomia, parti gemellari, ecc) in grado di determinare un alterato rapporto<br />
tra contenente (utero) e contenuto (feto). In questi casi è più opportuno parlare di<br />
malposizione che di malformazione congenita e la prognosi è sicuramente migliore.<br />
Secondo la teoria neurogena invece nel 10% dei casi circa il PTC può sottintendere<br />
un difetto di saldatura del tubo neurale fetale (spina bifida) o una patologia da<br />
acinesia fetale (artrogriposi). Le alterazioni anatomo-patologiche interessano sia l’<br />
apparato osteo-articolare che quello capsulo-legamentoso e muscolo-tendineo.<br />
Presentazione clinica<br />
In generale, quando si parla di piede torto congenito ci si riferisce sempre alla<br />
varietà più frequente; il piede si presenta in equinismo, ovvero in flessione plantare<br />
con appoggio esclusivamente sull’avampiede, in varismo, con l’asse longitudinale<br />
del retropiede deviato all’interno rispetto alla gamba, in supinazione ed in adduzione<br />
con conseguente rotazione interna della superficie plantare e deviazione<br />
dell’avampiede verso l’interno. La prognosi è correlata al grado di deformità e alla<br />
precocità del trattamento terapeutico. Clinicamente il piede torto può essere distinto<br />
in:<br />
<strong>Piede</strong> equino-varo-addotto-supinato (70%) : Deformità congenita che consiste<br />
nell'atteggiamento vizioso del piede che appare fissato contemporaneamente in:<br />
Equinismo: il piede è flesso plantarmente, l'appoggio avviene solo sull'avampiede;<br />
Varismo l'asse longitudinale del calcagno è deviato medialmente rispetto all'asse<br />
longitudinale della gamba; Cavismo la volta plantare longitudinale è accentuata;<br />
Supinazione: l'avampiede è ruotato sul suo asse longitudinale in modo tale che la<br />
pianta è rivolta all'interno In complesso il piede presenta una torsione sul suo asse<br />
longitudinale, per cui la faccia plantare guarda medialmente e l'appoggio al suolo<br />
avviene solo sul margine esterno del piede e sull'avampiede.
<strong>Piede</strong> talo-valgo-pronato (10%) : in cui si osserva talismo con flessione dorsale del<br />
piede; Valgismo in quanto l'appoggio avviene solo sul calcagno che appare deviato<br />
lateralmente rispetto all'asse longitudinale della gamba, pronazione con l'avampiede<br />
ruotato sul suo asse longitudinale in modo tale che la pianta è rivolta all'esterno e<br />
Piattismo con l'appiattimento della volta plantare longitudinale.<br />
Metatarso-addotto- varo (15%) : deformità caratterizzata dalla deviazione verso<br />
l'interno dei raggi metacarpali e delle dita.<br />
<strong>Piede</strong> valgo-convesso (5%) : rara deformità caratterizzata dall'inversione della volta<br />
plantare<br />
Forme miste (5%)<br />
La deformità in equino-varo supinato è pertanto il tipo più comune di piede torto, si<br />
tratta di una deformità complessa, difficile da correggere, con forte tendenza alle<br />
ricadute. La gravità della patologia viene valutata con la presentazione clinica della<br />
deformità e con il grado di riducibilità. Questo rappresenta infatti un ottimo criterio<br />
prognostico; più rigido è il piede, più difficile risulterà la correzione per via<br />
conservativa. In base a questo criterio vengono infatti classificati quattro stadi di<br />
gravità della patologia: un primo tipo definito posturale in cui si ha una completa<br />
riducibilità e una assenza di rigidità. Un secondo tipo con deformità moderata e una<br />
riducibilità considerevole, un terzo tipo con deformità severa e una riducibilità<br />
solamente parziale, un quarto tipo definito teratologico, con importante deformità,<br />
rigidità e assenza di riducibilità.<br />
Un altro criterio classificativo molto utilizzato è quello che fa riferimento all’entità<br />
angolare del varismo, per cui si distinguono tre gradi:<br />
• I grado: la malformazione è facilmente correggibile ed il piede forma sul piano<br />
frontale un angolo mediale maggiore di 90° rispetto all’asse longitudinale della tibia;<br />
• II grado: la malformazione risulta difficilmente correggibile ed il piede, invece,<br />
forma sul piano frontale un angolo mediale di 90° rispetto all’asse longitudinale della<br />
tibia;<br />
• III grado: la malformazione si presenta incorreggibile ed il piede forma sul piano<br />
frontale un angolo mediale inferiore di 90° rispetto all’asse longitudinale della tibia.<br />
Aspetti <strong>genetici</strong><br />
Nel 20% circa di casi il piede torto è associato ad altre anomalie quali: artrogriposi<br />
distale, mielomeningocele, distrofia miotonia congenita, altre sindromi genetiche<br />
(trisomia 18, sindrome da delezione 22q11). E’ stata suggerita un’eziologia<br />
multifattoriale con il concomitante intervento di fattori <strong>genetici</strong> e ambientali. Studi su<br />
gemelli hanno dimostrato una concordanza in gemelli dizigoti pari al 2, 9%, contro il<br />
32, 5% nei gemelli monozigoti . I parenti di I grado dei soggetti affetti, hanno un<br />
rischio molto più elevato, rispetto alla popolazione generale, di essere affetti da<br />
piede torto. In particolare, se entrambi i genitori o un figlio e un altro membro della<br />
famiglia presentano piede torto, la possibilità di avere un altro figlio affetto da tale<br />
patologia è di circa il 10-20% . In alcuni studi si prospetta la possibilità che il piede<br />
torto congenito sia dovuto alla mutazione di un singolo gene che si trasmette con<br />
modalità autosomico-dominante . L’identificazione di alcuni geni di suscettibilità,<br />
attraverso studi di associazione, suggerisce però un’eziologia poligenica e<br />
multifattoriale. I geni che nel corso degli anni sono stati associati allo sviluppo del<br />
piede torto sono diversi: HOXD12/HOXD13, NAT2 e una serie di geni regolatori<br />
dell’apoptosi tra cui CASP10 . Recentemente è stata identificata una mutazione del<br />
gene che codifica per un fattore di trascrizione PITX1 in una famiglia con piede torto<br />
isolato . Sono stati descritti inoltre diversi polimorfismi, nei casi di piede torto<br />
idiopatico, vicini ai geni Homeobox (HOX), del gene IGFBP3 e dei geni codificanti<br />
caspasi. Uno studio condotto da Ester et al ha dimostrato la presenza di diversi<br />
SNPs nei geni HOXA e HOXD responsabili, probabilmente, di piede torto congenito<br />
isolato. Tre SNPs del gene IGFBP3 (rs3793345, rs2471551 e rs13223993)<br />
risultavano over-trasmessi nella popolazione affetta studiata. Negli ultimi mesi lo<br />
studio delle Copy-number variants (CNVs) ha permesso di evidenziare, in 40<br />
famiglie, la presenza di una microduplicazione (2.2 Mb) a livello del cromosoma 17<br />
(17q23.1q23.2) [Fig.2], non evidenziabile in 700 controlli sani. La penetranza di tale<br />
mutazione sarebbe di circa il 70% in quanto solo 7 su 10 pazienti presentavano<br />
piede torto.<br />
Quello che si crea è un alterato dosaggio genico di almeno uno dei due geni che<br />
codificano per fattori di trascrizione, TBX2 e TBX4. Quest’ultimo è uno dei principali<br />
geni candidati nell’eziologia dei difetti degli arti inferiori negli uccelli.<br />
L’aploinsufficienza di TBX4, risultante dalla microdelezione 17q23.1q23.2, si<br />
presenta con anomalie scheletriche variabili incluse la rotula ipoplasica, dita<br />
assottigliate, piedi piatti, ossificazione ipoplasia della giunzione ischio-pubica.<br />
L’alterato dosaggio genico, nel senso della microduplicazione provoca effetti opposti,<br />
ovvero: dita corte e tozze, addensamento dell’osso ischiatico ecc. Infine, visto che il<br />
fattore di trascrizione TBX4 è un target trascrizionale diretto per PITX1, si crede in<br />
un ruolo eziopatogenetico del pathway PITX1-TBX4 nel determinismo del piede torto<br />
congenito. In futuro l’approccio “genome wide association study” potrebbe aiutare<br />
nell’identificazione di altri geni di suscettibilità coinvolti nell’eziologia del piede torto<br />
congenito.<br />
Diagnosi<br />
La diagnosi di PTC è essenzialmente clinica, avendo l’esame radiografico, almeno<br />
inizialmente, un valore limitato dalla presenza di cartilagine che nei primi anni di vita<br />
extrauterina non si è ancora ossificata. La radiologia convenzionale, comunque, può<br />
fornire informazioni utili, così come la risonanza magnetica, riguardo la morfologia<br />
delle singole ossa e i loro rapporti, mentre l’indagine ecografica consente una<br />
valutazione dinamica del piede torto.<br />
Diagnosi prenatale<br />
Con il miglioramento delle tecniche ecografiche ostetriche il piede torto puo' essere<br />
diagnosticato in gravidanza. Un esame ecografico di 2° livello, che consiste in una<br />
valutazione morfologica più accurata e nella sollecitazione dei movimenti fetali,<br />
permette infatti sia di valutare l’atteggiamento e la morfologia del piede quindi di<br />
porre diagnosi di patologia che di tipizzare la patologia come primaria o secondaria.<br />
L’ecografia del 2° trimestre è la più adatta a diagnosticare un piede torto equinovaro-supinato<br />
poiché, già dal terzo trimestre, la quantità di liquido amniotico è meno<br />
importante e la posizione degli arti è spesso costretta nella cavità uterina. I piedi<br />
possono presentarsi di frequente incrociati l’uno sull’altro.<br />
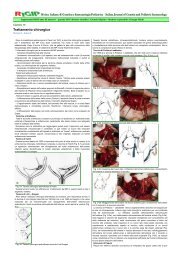
Terapia<br />
Il trattamento è conservativo, almeno inizialmente, ma può divenire cruento se il<br />
risultato funzionale non è soddisfacente (appoggio plantigrado non ottimale, scarsa<br />
mobilità, o presenza di sintomatologia dolorosa) : esso si basa sull’esecuzione di<br />
modellamenti manuali a tappe, tendenti a correggere la deformità e, sul<br />
confezionamento di apparecchi gessati femoro-podalici che devono essere rinnovati<br />
settimanalmente almeno per le prime 7-10 settimane. Tali manovre correttive devono<br />
essere graduali per evitare lo schiacciamento dei nuclei di accrescimento,<br />
consentendo nello stesso tempo l’adattamento delle strutture vasculo-nervose alle<br />
nuove posizioni. La terapia prevede quindi differenti approcci in base alla severità di<br />
presentazione clinica. Va iniziata precocemente, già dal II-III giorno di vita<br />
consistendo, inizialmente, in manipolazioni correttive da effettuare piu' volte in un<br />
giorno seguite poi dall’applicazione di apparecchi gessati correttivi che si oppongono<br />
alla deformita', da rimuovere e sostituire ogni 7/14 giorni (Metodo Ponseti).
La fase correttiva prevede pertanto 5 o 6 tappe in cui si alternano manipolazioni a<br />
gessetti settimanali correttivi. I segni <strong>clinici</strong> di una adeguata correzione sono da<br />
ricercare nella congruenza astragalo-scafoidea e nella palpazione del processo<br />
anteriore del calcagno che deve apparire in posizione neutra o di leggero valgismo.<br />
Di frequente, circa nell’80% dei casi, alle manipolazioni si accompagna la tenotomia<br />
percutanea del tendine di Achille. Dopo la procedura di tenotomia, vengono<br />
confezionati ulteriori 2 gessi, ciascuno della durata di circa 10 giorni, viene quindi<br />
applicato un particolare tutore, detto “Denis-Brown”, che manterrà la posizione di<br />
correzione ottenuta fino a questo momento. Il tutore è costituito da due scarpette<br />
che sono collegate tra loro da una barretta, e mantiene i piedini ruotati verso<br />
l’esterno. All’età di circa 8-9 mesi, il tutore viene proseguito solo di notte e quando il<br />
piccolo dorme, fino all’età di 3 anni circa.<br />
Le forme piu' gravi richiedono invece un trattamento chirurgico che non deve, in ogni<br />
caso, mai avvenire prima dei 4 mesi. L’intervento tradizionale, noto come Intervento<br />
di Codivilla, prevede una doppia incisione chirurgica (una nella parte posteriore e<br />
una nella parte interna del piede) e quindi una tenotomia Achillea, un allungamento<br />
plastico dei tendini mediali del piede, una capsulotomia delle articolazioni mediali<br />
eventualmente accompagnata da una cuboidectomia. Al termine viene confezionato<br />
un apparecchio gessato, lungo fino alla radice della coscia, che mantiene la<br />
correzione ottenuta. Fino al successivo controllo che avviene dopo 12/15 giorni in<br />
cui avviene la sostituzione dell’apparecchio gessato. Intorno all’8-9 mese di età<br />
vengono dunque confezionate delle calzature ortopediche, definite “ a biscotto” che<br />
manterranno la correzione. Il destino prognostico è strettamente correlato, non solo<br />
alla precocità ed alla razionalità del trattamento, ma anche all’ entità della<br />
deformazione iniziale ed alla capacità riparativa del piede deforme. Non va<br />
dimenticato comunque che la deformità, essendo legata ad un arresto o ad un<br />
rallentamento dello sviluppo embrionale, tende a ripresentarsi ogni qual volta vi sia<br />
una spinta evolutiva all’ accrescimento del piede, ragion per cui è necessaria una<br />
continua e stretta sorveglianza di questi pazienti per intervenire precocemente<br />
qualora si osservino i segni di un ripristino della deformità.<br />
Bibliografia<br />
1. Audrey R. Ester, Katelyn S. Weymouth, Amber Burt, et al. : Altered Transmission<br />
of HOX and Apoptotic SNPs Identify a Potential Common Pathway for Clubfoot Am J<br />
Med Genet A. 2009 December ; 149A (12) : 2745–2752<br />
2.Arjandas Mahadev, Ismail Munajat, Azura Mansor, et al. Combined Lateral and<br />
Transcuneiform without Medial. Osteotomy for Residual Clubfoot for Children. Clin<br />
Orthop Relat Res (2009) 467:1319–1325<br />
3.Bartholomew Kowalczyk Æ Tadeusz Lejman. Short-term experience with Ponseti<br />
casting and the Achilles tenotomy method for clubfeet treatment in arthrogryposis<br />
multiplex congenital. J Child Orthop (2008) 2:365–371.<br />
4.Charles EJ Docker, Simon Lewthwaite, Nigel Tkiely. The Royal College of<br />
Surgeons of England Ponseti treatment in the management of <strong>clubfoot</strong> deformity – a<br />
continuing role for paediatric orthopaedic services in secondary care centres.<br />
Orthopaedics. Ann R Coll Surg Engl 2007; 89: 510–512<br />
5.David M. Alvarado, Hyuliya Aferol, Kevin McCall, et al. Familial Isolated Clubfoot<br />
Is Associated with Recurrent Chromosome 17q23.1q23.2 Microduplications<br />
Containing TBX4. The American Journal of Human Genetics 87, 154–160, July 9,<br />
2010<br />
6.E. Bar-On, R. Mashiach, O. Inbar, et al. Prenatal ultrasound diagnosis of club foot.<br />
J Bone Joint Surg [Br] 2005<br />
7.FR Dietz, WG Cole, LL Tosi, et al. A search for the gene (s) predisposing to<br />
idiopathic <strong>clubfoot</strong> Clin Genet. 2005 April ; 67 (4) : 361–362.<br />
8.Ignacio V. Ponseti, 1914– Richard A. Brand Clubfoot: Etiology and Treatment Clin<br />
Orthop Relat Res (2009) 467:1121–1123<br />
9.Ignacio V. Ponseti, Jeronimo Campos . The Classic Observations on Pathogenesis<br />
and Treatment of <strong>Congenital</strong> Clubfoot. Clin Orthop Relat Res (2009) 467:1124–1132<br />
10 .Ignacio V. Ponseti, Eugene N. Smoley .The Classic <strong>Congenital</strong> Club Foot: The<br />
Results of Treatment. Clin Orthop Relat Res (2009) 467:1133–1145<br />
11. Matthew B. Dobbs, Christina A. Gurnett Update on Clubfoot: Etiology and<br />
Treatment Clin Orthop Relat Res (2009) 467:1146–1153<br />
12.Margaret A. Honein, Leonard J. Paulozzi and Cynthia A. Moore: Family History,<br />
Maternal Smoking, and Clubfoot: An Indication of a Gene-Environment Interaction<br />
American Journal of Epidemiology2000 Vol. 152, No. 7<br />
13.Tracy S. Chen, Debra A. Sala. Correction of Clubfoot Deformity Associated with.<br />
Weber Type I Tibial Hemimelia Using the Ponseti Method. Joint Diseases 2010;68<br />
(4) :299-303<br />
14.Jianhua Wang, Robert M. Palmer, Chin S. Chung. The Role of Major Gene in<br />
Clubfoot Am. J. Hum. Genet. 42:772-776, 1988<br />
15.William Shyy, Frederick Dietz, Matthew B. Dobbs, et al. Evaluation of CAND2<br />
and WNT7a as Candidate Genes for <strong>Congenital</strong> Idiopathic Clubfoot Clin Orthop<br />
Relat Res (2009) 467:1201–1205.<br />
16.William Shyy, Kai Wang, Val C. Sheffield, et al. Evaluation of Embryonic and<br />
Perinatal Myosin Gene Mutations and the Etiology of <strong>Congenital</strong> Idiopathic Clubfoot<br />
J Pediatr Orthop. 2010 ; 30 (3) : 231–234<br />
17. Wynne-Davies R. Family studies and the cause of congenital club foot: Talipes<br />
equinovarus, talipes calcaneo-valgus and metatarsus varus. J Bone Joint Surg Br<br />
1964;46:445–463.<br />
18. Rebbeck TR, Dietz FR, Murray JC, et al. A single-gene explanation for the<br />
probability of having idiopathic talipes equinovarus. Am J Hum Genet<br />
1993;53:1051–1063.<br />
19. Lisa M. Kruse, Matthew B. Dobbs, Christina A. Gurnett. Polygenic threshold<br />
model with sex dimorphism in <strong>clubfoot</strong> inheritance: the Carter effect. The Journal of<br />
bone & joint surgery; volume 90-A, number 12, December 2008<br />
20. Gurnett, C.A., Alaee, F., Kruse Desruisseau, et al. (2008). Asymmetric<br />
lower-limb malformations in individuals with homeobox PITX1 gene mutation. Am. J.<br />
Hum. Genet. 83, 616–622.<br />
21. David M. Alvarado et al. Familial Isolated Clubfoot Is Associated with Recurrent<br />
Chromosome 17q23.1q23.2 Microduplications Containing TBX4. The American<br />
Journal of Human Genetics 87, 154–160, July 9, 2010<br />
22. Audrey R. Ester et al. Altered Transmission of HOX and Apoptotic SNPs Identify<br />
a Potential Common Pathway for Clubfoot. Am J Med Genet A. 2009 December ;<br />
149A (12) : 2745–2752<br />
Home page 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 ◀ Indietro pagina 7 Avanti ►<br />
Scarica l'articolo: pagina 7.pdf<br />
Sommario 20 pagine<br />
Trimestrale di divulgazione scientifica dell'Associazione Pediatrica di Immunologia e Genetica<br />
Legge 7 marzo 2001, n. 62 - Registro della Stampa Tribunale di Messina n. 3/09 - 11 maggio 2009<br />
Direttore scientifico Carmelo Salpietro - Direttore responsabile Giuseppe Micali - Segreteria redazione Basilia Piraino - Piera Vicchio<br />
Direzione-Redazione: UOC Genetica e Immunologia Pediatrica - AOU Policlicnico Messina