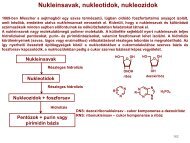
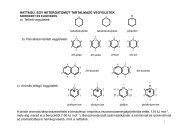
Fémorganikus reagensek - Szerves Kémiai Tanszék
Fémorganikus reagensek - Szerves Kémiai Tanszék
Fémorganikus reagensek - Szerves Kémiai Tanszék
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
3RX2 LiEt 2 OR Li LiClCuI2 R Li R 2 CuLi + LiI R: Me, 1 o , 2 o , 3 oR 2 CuLi + R'-X R-R + RCu + LiX R': Me, 1 o , 2 o , cikloalkil,arilAliciklusos szénhidrogének előállításaClClZn v. Mg+ ZnCl 2BrBr2 Zn+ ZnBr 2BrBrMechanizmus:BrCCBrMgBrCCMgBrBrCCC C + Br-Mg-BrMgBrGrignard-reagens1900-ban állította elő Grignard, 1912 Nobel-díjEtOEtMeIMgabsz. éterMeMgIEtRMgI a legreaktívabb, de bomlékonyRMgCl diszproporciónálódik, de alkalmazhatóOEt
6HalogenidNem tartalmazhatja a felsorolt csoportokat (ld. fent), de tartalmazhat szén-szénkettőskötést, nem láncvégi hármas kötést, étercsoportot, -NR 2 csoportot.Aril- és vinil-fémorganikus vegyületek előállításaBrMgEt 2 O v. THFMgBr 90-95%
7Ar-MgBr és Ar-MgI: éter v. THFAr-MgCl és vinil-magnézium-halogenidek: THFAz oldószer effektus miatt az alábbi szelektív reakció lehetséges:BrMgEt 2 OMgBrClClOka: a bróm reaktívabb, mint a klór, nem szükséges melegíteni a reakcióelegyet.Vinil-fémorganikus vegyületek: THF, mivel csökkent reaktivitásúakMgBrTHFBrMgAril- és vinil-lítium <strong>reagensek</strong> előállítása:Br2 LiLi + LiBrEt 2 OHBrH2 LiEt 2 OHLiH+ LiBrHalogéncserével történő folyamatok:In-Bu-Li / benzol-hexánLi + n-Bu-IAz egyensúly eltolódása annak köszönhető, hogy az sp 2 -hibridállapotú fenilanion (afenil-lítiumban) stabilabb, mint az sp 3 -hibridizált karbanionok (n-butil-lítiumban).65%A fémorganikus vegyületek alkalmazási korlátainak felhasználásaA Cerevitinov-féle aktív hidrogén meghatározás
8Acetilénkötést tartalmazó Grignard-reagens előállításaElőzménye: az acetilén C-H kötés savasabb, mint a metán C-H kötéseR C C H Me MgIH-fém csereR C C MgI CH 4A stabilabb anion kerül így kapcsolatba a magnéziummal.A karbanion stabilitással a következő reakció is összefügg (3 o < 2 o < 1 o ):NaNaCH 3CH 2 NaSzénhidrogén előállítás (deuterálás is)RXMgRMgXH 2 O v.D 2 OR H(D) H(D)OMgXSzubsztitúciós reakciókR Mg BrRQMgXBrQXReakció aktív halogenidekkelBenzil- vagy allil-halogenidek és alkil- vagy fenil-magnézium halogenidek reakciója,hosszabb szénláncok képződésével.BrRMgBr v.ArMgBrR(Ar)+ MgBr 2Alkinek előállítása kis szénatom számú vegyületekbőlMeMgBrMgBrBr- CH 4 - MgBr 22BrMg HC CHMgBr
11HHCORMgX1. éter2. vízROHformaldehid1 o alkoholR'HCORMgX1. éter2. vízRR'CHOHaldehidPreparatív lehetőségek: hexán-3-ol előállítása2 o alkoholHOEtMgBraaOHbbMgBrOHbutanal etil-magnézium-bromid propil-magnézium-bromid propanalReakció ketonokkal:RR'O1. R"MgBr /éter2. vízR'RR"OHketon3 o alkoholPreparatív lehetőség: 3-metilhexán-3-ol előállításaMgBrésOaMeMgBrésOba bcOHcMgBrésOReakció szén-dioxiddal:R Mg BrO C OROCO MgBrH 3 OROCOHkarbonsav
12Reakció észterekkel:RMgBrR'CR"OORR'OOR"MgBr- R"OMgBrR'RCO1. R MgBr2. H 3 OR'ROHRinstabil tetraéderes köztitermék keton 3 o alkohol, kétegyforma alkil-cs.Grignard-reagens felesleg szükséges, másképp csak a fele mennyiségű észter reagál.Ha az észter formiát, 2 o alkohol képződikHEtOCORMgBrRHOEtOHMgBr C OR1. R MgBr2. H 3 OHRCOHRaldehid2 o alkoholPreparatív példa: 3-metilpentán-3-ol előállítása2 MgBr + OMgBr+Obacaa,bMeMgBr+OcOHODietil-karbonátból (szénsav észtere) kiindulva, 3 mol Grignard-reagens szükséges, 3 o alkoholképződik, három azonos alkil-csoporttal.EtOEtOCORMgBrREtOOOEtMgBr-EtOMgBrREtOCORMgBrRROEtOMgBr-EtOMgBrPreparatív példa: 3-etilpentán-3-ol előállításaROHR RRMgBrRRCO
13EtOEtOCO+ 3 EtMgBrO+ EtMgBrOOHLítium-<strong>reagensek</strong> reakciója:O+ 2 EtMgBrOOHTHF víz2 Li + + MeOH + LiOReakció nitrilekkel:R Mg BrQ C NRCQN MgBrH 3 O- HOMgBrRCQNHH 3 OROCQHNH 2imin Mg sójaimin- NH 4RQCOHa R ≠ Q RMgBr + Q-CN vagy QMgBr + R-CNPéldául a hexán-3-on előállítása:ketonEtMgBr +NOReakció sav-kloridokkal:MgBr+N
14OCl+ Me 2 Cu Li-78 o CTHFvízO+ MeCu + LiClNOCl1. Me 2 CuLi2. vízNOOCl1. Me 2 CuLiOOO2. vízOOA keton nem reagál tovább. Ennek oka a savkloridok fokozott reakciókészsége, ami nagyobb,mint a ketoné. Ezért más csoportok jelenlétében is elvégezhető a reakció, pl. észter vagy nitril.A kadmium-vegyületek sem reagálnak tovább. A fémcserélődés hajtóereje az, hogy a MgCl 2ionosabb, mint a másik fém-halogenid.MgBr2 + CdCl 2absz. éter Cd + MgCl 2 + MgBr 2OCl+ Cdabsz. éterdietil-kadmiumO+ EtMgCl-Telítetlen karbonilvegyületek reakciója:OPh-LivízOHPhOO2. n-BuLiTHFvízOHEbben a reakcióban 1,2-addíciós termékek képződnek.
15OMe 2 CuLiéter, -78 o CvízOHHMeHHOO+ MgBrCuClétervízOOAz organo-kuprátok esetében kizárólag 1,4-addíció játszódik le, ha a szubsztrátum -teltetlen észter vagy keton. Hasonló szerkezetű aldehidek is 1,4-addíciós reakcióba lépnek, főlegalacsony hőmérsékleten.OMe 2 CuLiH 3 OOOHHéter, -50 o CH95% 5%Cu(I) jelenlétében, mint látható a konjugált addíció kedvezményezett, míg rézhiányában az 1,2-addíció. Előbbi esetben gyök-anionokon keresztül képzelhető el a folyamat,mivel a réz kiváló redukáló elektrondonor ágens. A réz egy elektront ad át az -telítetlenkarbonilvegyületnek és egy gyökanion képződik, majd az R٠ gyök a kettőskötés végéhezkapcsolódva enolát iont eredményez. A víz addíciója az enolátot telített ketonná alakítjaLiOCCCCuR 2Li O CuR 2 Li O CuR 2C CC CC COLiOLiR Cu R CCCR Cu +R CCCOR CCCOR CCCH 2 OOR CCHC+ OHA Grignard-reagenssel aztermékeket adnak:-telítetlen karbonilvegyületek 1,2- és 1,4-addíciós