TKBE0302 Szerves kémia II.
TKBE0302 Szerves kémia II.
TKBE0302 Szerves kémia II.
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Szerves</strong> Kémia <strong>II</strong>.<br />
<strong>TKBE0302</strong> –<br />
Előfeltétel: TKBE0301 <strong>Szerves</strong> <strong>kémia</strong> I.<br />
Előadás: 2 óra/hét<br />
Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu<br />
A 2010/11. tanév tavaszi félévében az előadás<br />
Helye: K/2 előadó<br />
Ideje: Csütörtök 8-10 óra<br />
Szeminárium: 1 óra/hét<br />
A tárgy alapozó tárgy, előfeltétele az „Általános <strong>kémia</strong>” című tárgy sikeres teljesítése. A tárgy<br />
heti kétórás előadáson és az azt követő heti egyórás szemináriumon kerül ismertetésre. Az<br />
előadás és a szeminárium egymástól el nem választható egységet alkot. A szemináriumokon a<br />
hallgatók a megelőző előadások anyagát oktatói irányítással konkrét példákon dolgozzák fel.<br />
A kollokviumra való jelentkezés feltétele a szemináriumi munka eredményes végzése. a<br />
szemináriumi számonkérések minimumfeltételének (összesítésben 35%-os ZH átlag,<br />
maximum 3 igazolt hiányzás) teljesítése. Ennek hiányában a félév nem kerül aláírásra,<br />
vizsgára nem lehet jelentkezni. A szemináriumra való jelentkezés és részvétel azok számára<br />
is kötelező, akik korábban már megszerezték az aláírást a tárgyból.<br />
Számonkérés: Az első („A”) vizsga írásban történik, a vizsgaidőszak első napjaiban, egy 200<br />
pontos dolgozat formájában. Az írásbeli vizsgán való részvétel kötelező, azt előzetesen a<br />
Neptunban fel kell venni. Lehetőség van a 200 pontos dolgozat kiváltására két 100 pontos<br />
dolgozattal, melyek közül az első a félév közepén, a második pedig az említett 200 pontos<br />
dolgozattal azonos napon történik. A dolgozat(ok) eredménye adja az „A” vizsga jegyét. A<br />
sikeres vizsgához az elérhető 200 pontból minimum 70 pontot kell teljesíteni. A további<br />
vizsgák szóban, kiadott tételsor alapján történnek.<br />
Tartalma:<br />
A fontosabb funkcióscsoportokat tartalmazó vegyületek szisztematikus tárgyalása;<br />
kötésrendszerük, reakcióik és előállításuk áttekintése, gyakorlati jelentőségük. Alkoholok,
fenolok, éterek és kéntartalmú analógjaik. Aminok, nitrovegyületek, diazóniumsók.<br />
Aldehidek és ketonok. Karbonsavak és karbonsavszármazékok. Szénsavszármazékok. A<br />
természetes szerves vegyületek legfontosabb csoportjainak áttekintése. Aminosavak,<br />
peptidek, fehérjék. Szénhidrátok, mono-, oligo és poliszacharidok. Nukleozidok, nukleotidok<br />
és nukleinsavak.<br />
1-2. hét<br />
Szénhidrogének hidroxiszármazékaik (alkoholok, fenolok, éterek) és kéntartalmú analógjaik<br />
csoportosítása és kötésrendszerük jellemzése. Fizikai tulajdonságaik, a kötésrendszerből<br />
levezethető halmazsajátságok. Alkoholok, fenolok és kéntartalmú analógjaik sav-bázis<br />
sajátságai, a savasságot meghatározó szerkezeti tényezők. Alkoholok és fenolok nukleofil<br />
sajátságából levezethető reakciók (alkilezés, acilezés, szulfonsavészterek, szervetlen észterek<br />
előálítása), alkoholok savkatalizált átalakításai (alkoholok halogénszármazékokká való<br />
alakítása, eliminációs reakciók). Alkoholok és fenolok oxidációja. Éterek sajátságai,<br />
éterhasítás. Különleges kötésrendszerű éterek (epoxidok, félacetálok, acetálok és enoléterek)<br />
<strong>kémia</strong>i reakcióinak jellemzése. Alkoholok, éterek, fenolok előállítása. Kumolbázisú<br />
fenolszintézis.<br />
3-4. hét<br />
C-N egyszeres kötést tartalmazó vegyületek legfontosabb típusainak ismertetése. Aminok<br />
csoportosítása, kötésrendszerük jellemzése. Fizikai tulajdonságaik, a kötésrendszerből<br />
levezethető halmazsajátságok. Aminok bázicitása, a bázicitás függése szerkezeti tényezőktől.<br />
Az aminocsoport nukleofil jellegéből levezethető reakciók, alkilezés, acilezés, szulfonamid<br />
képződés, reakció salétromossavval. Aminok oxidációja. Anilinek aromás gyűrűinek reakciói.<br />
Alifás és aromás aminok előállítása, ipari módszerek.<br />
5. hét<br />
Egyéb C-N egyszeres kötést tartalmazó vegyületek jellemzése. Nitrovegyületek, nitrocsoport<br />
kötésrendszere, elektronszívó hatás értelmezése, C-H savasság. Nitrovegyületek előállítása.<br />
Diazóniumsók előállítása, aromás diazóniumsók reakciói és gyakorlati jelentőségük.<br />
Azovegyületek és ipari jelentőségük.<br />
6-7. hét
Oxovegyületek csoportosítása, az oxocsoport kötésrendszere, a C=O kötés stabilitása. Fizikai<br />
tulajdonságok. Aldehidek és ketonok sav-bázis sajátságai, -hidrogén savassága, keto-enol<br />
tautomeria, sav- és báziskatalizált mechanizmusok. Nukleofil addíciós reakciók O-, S-, N- és<br />
C-nukleofilekkel, az addíciók reverzibilis jellege. Kondenzációs reakciók. Oxidációs és<br />
redukciós reakciók. Az -szénatomon végbemenő reakciók; aldoldimerizáció, -halogénezés.<br />
Az ,-telítetlen oxovegyületek nukleofil addíciós reakciói. Aldehidek és ketonok előállítása,<br />
oxidatív és reduktív módszerek problémái.<br />
8-9. hét<br />
Karbonsavak és származékaik csoportosítása, kötésrendszerük leírása és összehasonlítása.<br />
Savszármazékok stabilitási viszonyai, a stabilitási sor jelentősége a karbonsavszármazékok<br />
rekativitásában és egymásba alakíthatóságában. Fizikai tulajdonságaik. Sav-bázis sajátságaik,<br />
O-H, N-H és C-H savasság. Karbonsavak savasságát befolyásoló szerkezeti tényezők.<br />
Karbonsavszármazékok egymásba alakíthatósága a stabilitási sorra alapozva. Acil nukleofil<br />
szubsztitúció. Karbonsavszármazékok reduktív átalakításai, oldalláncban végmenő reakciók.<br />
Karbonsavak előállítása.<br />
10. hét<br />
-Dikarbonil vegyületek és -oxokarbonsavszármazékok <strong>kémia</strong>i tulajdonságai, C-H savasság<br />
és az abból levezethető reakciók. Enolát<strong>kémia</strong> alapjai, szén-szén kötések kiépítése,<br />
malonészter, acetecetészter és ciánecetészter szintézisek.<br />
11. hét<br />
Láncban szubsztituált (halogénezett, hidroxi és oxo) karbonsavszármazékok és egymásba<br />
alakíthatóságuk. Szénsavszármazékok és fontosabb képviselőik előállítása és egymásba<br />
alakítása. Szénsavszármazékok gyakorlati jelentősége.<br />
12. hét<br />
-Aminosavak csoportosítása. Az aminocsoport és a karboxilcsoport reakciói. A peptidkötés<br />
és a peptidek jellemzése, peptidszintézisek alapjai. Fehérjék csoportosítása, elsődleges,<br />
másodlagos, harmadlagos és negyedleges szerkezetük, biológiai jelentőségük.<br />
13. hét
Szénhidrátok előfordulása, csoportosítása. Monoszacharidok szerkezete, cukrok<br />
mutarotációja. Konfigurációs és konformációs viszonyok, anomer és epimer cukrok.<br />
Szénhidrátok <strong>kémia</strong>i sajátságai, az alkoholos és glükozidos hidroxicsoporhoz és az<br />
oxocsoportokhoz köthető reakciók. Glikozidok jellemzése. Di- és poliszacharidok,<br />
legfontosabb képviselőik.<br />
14. hét<br />
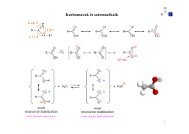
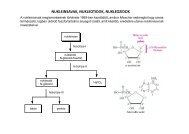
Nukleinsavak építőkövei, nukleozidok, nukleotidok, pentózok és nitrogén-bázisok szerkezete.<br />
Nukleinsavak (DNS, RNS) elsődleges, másodlagos, harmadlagos szerkezete és biológiai<br />
funkciója.<br />
Ajánlott irodalom:<br />
1. Antus Sándor - Mátyus Péter: <strong>Szerves</strong> Kémia. Nemzeti Tankönyvkiadó (2005)<br />
2. Furka Árpád: <strong>Szerves</strong> Kémia. Tankönyvkiadó (1988)<br />
3. R.T. Morrison - R.N. Boyd: Organic Chemistry, 6th Ed., Prentice-Hall (1992)<br />
4. F.A. Carey: Organic Chemistry.<br />
http://www.chem.ucalgary.ca/courses/351/Carey/Carey.html
SZERVES KÉMIA <strong>II</strong>. (<strong>TKBE0302</strong> és TKBE0312) TÉTELSOR – 2011/2012. 2. félév<br />
2011. decemberében kerül kiadásra.