Oxovegyületek
Oxovegyületek Oxovegyületek
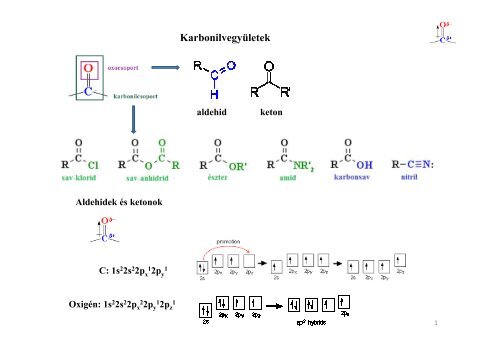
Karbonilvegyületek aldehid keton Aldehidek és ketonok C: 1s 2 2s 2 2p x1 2p y 1 Oxigén: 1s 2 2s 2 2p x2 2p y1 2p z 1 1
- Page 2 and 3: H 2 C=O 170 kcal/mol π = 84 kcal/m
- Page 4 and 5: Aldehidek és ketonok előállítá
- Page 6 and 7: Rosenmund reakcióval savlogenidekb
- Page 8 and 9: Houben-Hoesch-féle ketonszintézis
- Page 10 and 11: Vilsmeier reakció → aktivált ar
- Page 12: Reverzibilis reakciók Reakció O-n
- Page 15 and 16: enamin 15
- Page 17 and 18: Reakció nátrium-biszulfittal: ald
- Page 19 and 20: Clemmensen redukció: cink-amalgám
- Page 21 and 22: Szelektív redukció Oxidációs re
- Page 23 and 24: Oxidáció kálium-permanganáttal
- Page 25 and 26: Wittig reakció: Ad N + E ilid alde
- Page 27 and 28: Aldol reakció → híg lúg jelenl
- Page 29 and 30: Intramolekuláris aldol reakció 29
- Page 31 and 32: Benzilsav átrendeződés: diketono
- Page 33 and 34: Nitrozálás O OH O H O H RO O RO--
- Page 36 and 37: Michael addíció 36
- Page 38 and 39: Benzil előállítása benzoinból
- Page 40: Természetes aldehidek és ketonok
Karbonilvegyületek<br />
aldehid keton<br />
Aldehidek és ketonok<br />
C: 1s 2 2s 2 2p x1<br />
2p y<br />
1<br />
Oxigén: 1s 2 2s 2 2p x2 2p y1 2p z<br />
1<br />
1
H 2 C=O 170 kcal/mol π = 84 kcal/mol<br />
RCH=O 175 kcal/mol π = 89 kcal/mol<br />
R 2 C=O 180 kcal/mol π = 94 kcal/mol<br />
C–O σ-kötési energiája 86 kcal/mol, ebből<br />
következik, hogy a kettős kötés igen erős, erősebb<br />
mint az alkénekben, ezért a karbonil vegyületek<br />
reakciókészsége termodinamikailag kedvezőtlen.<br />
Az alkénekben a kötési energia kb. 146 kcal/mol.<br />
A C–C σ-kötés energiája 83 kcal/mol, tehát a π-<br />
kötés energiája 63 kcal/mol lesz.<br />
2
Nevezéktan<br />
Aldehidek<br />
a.) ha a megfelelő karbonsavnak triviális neve van, a sav latin szótöve + aldehid<br />
b.) aciklusos mono- és dialdehidek: azonos szén atomszámú szénhidrogén neve + al, dial<br />
c.) más aldehidek: alapnév + karbaldehid utótag<br />
Előtag: „formil”<br />
Ketonok<br />
a.) szubsztitúciós név: alapnév + „on”, „dion”, stb. utótag<br />
előtag: „oxo”<br />
b.) csoportfunkciós név (mono- és vicinális diketonok esetében): R,R’ csoportnevek betűrendben,<br />
kötőjellel elválasztva, + kötőjel + keton/diketon utótag<br />
Aromás ketonok esetében: „-ofenon”, „-onafton” utótag is használható<br />
3
Aldehidek és ketonok előállítása<br />
Alkoholok és alkének oxidációjával<br />
4
Alkinek hidratálásával<br />
5
Rosenmund reakcióval savlogenidekből: mérgezett katalizátor, másképp további redukció<br />
Fémorganikus vegyületek reakcióival<br />
6 6
Aromás szénhidrogénekből acilezési reakcióval<br />
Gattermann–Koch-szintézis: hátránya a szén-monoxid használata<br />
Gattermann-szintézis → aktivált aromások esetén<br />
7
Houben–Hoesch-féle ketonszintézis: a nátrium-cianidot alkil- vagy aril-cianid helyettesíti<br />
Friedel-Crafts féle acilezés<br />
8
Fries-féle átrendeződés<br />
Reimer-Tiemann szintézis<br />
Kedvező,<br />
intramolekuláris<br />
H-kötés stabilizál<br />
9
Vilsmeier reakció → aktivált aromásokra alkalmazható<br />
10
Reaktivitás → nukleofil addíciós reakciók<br />
11
Reverzibilis reakciók<br />
Reakció O-nukleofilekkel<br />
12
Reakciók N-nukleofilekkel<br />
imin<br />
14
enamin<br />
15
Oxovegyületel leválasztására alkalmas reakciók<br />
2,4-Dinitrofenilhidrazin teszt<br />
16
Reakció nátrium-biszulfittal: aldehidek leválasztása, eltávolítása<br />
Reakciók C-nukleofilekkel → cianohidrin képződés<br />
17
Ireverzibilis reakciók<br />
Redukció<br />
18
Clemmensen redukció: cink-amalgám, Zn(Hg), HCl, alkánok képződnek<br />
19
Kizsnyer-Wolff redukció, hidrazin, bázikus közeg<br />
Deszulfurálás<br />
20
Szelektív redukció<br />
Oxidációs reakciók<br />
21
Baeyer-Villiger oxidáció<br />
Aszimmetrikus aldehidek esetén, a szubsztituáltabb alkil<br />
csoport vándorol: 3 o R > 2 o R > 1 o R > -CH 3<br />
22
Oxidáció kálium-permanganáttal<br />
23
Reakció fémorganikus vegyületekkel<br />
Memo:.Grignard reagens<br />
24
Wittig reakció: Ad N + E<br />
ilid aldehid v. keton alkén<br />
oxafoszfetán<br />
25
α-Szénatomon végbemenő reakciók – az enolátanion reakciói<br />
Oxo-enol tautoméria<br />
26
Aldol reakció → híg lúg jelenlétében<br />
Sav katalízis<br />
27
Aldol dehidratálása<br />
Vegyes aldol reakció: 4 termék keveréke képződik<br />
Megoldás: csak egyik reakciópartnernek legyen α-hidrogénje<br />
28
Intramolekuláris aldol reakció<br />
29
Cannizzaro-reakció → nem enolizáló aldehidek redox diszproporcionálódása, erős bázis<br />
jelenétében<br />
α-Ketoaldehidek kiváló hozammal intramolekuláris diszproporciónálódási terméket adnak.<br />
30
Benzilsav átrendeződés: diketonokra jellemző<br />
Benzoin kondenzáció, katalitikus mennyiségű cianid ion jelenlétében<br />
31
α-Halogénezési reakció<br />
Haloform reakció<br />
32
Nitrozálás<br />
O<br />
OH<br />
O H<br />
O<br />
H<br />
RO<br />
O<br />
RO--NO<br />
- RO<br />
NO<br />
NO<br />
- ROH<br />
NO<br />
Oxocsoport halogénre cserélése<br />
Oxidáció szelén-dioxiddal<br />
O<br />
O<br />
H<br />
O Se<br />
O<br />
O<br />
Se<br />
OH<br />
O<br />
H<br />
O<br />
B<br />
O<br />
O<br />
O SeOH<br />
- BH - SeOH<br />
O SeOH<br />
O<br />
33
a,β-Telítetlen aldehidek és ketonok reakciói. Nukleofil addíció szén–szén kettős kötésre<br />
34
Michael addíció<br />
36
Robinson-anelláció<br />
37
Benzil előállítása benzoinból<br />
Benzilsav átrendeződés<br />
38
<strong>Oxovegyületek</strong> kimutatási reakciói<br />
Tollens teszt<br />
Fehling teszt<br />
39
Természetes aldehidek és ketonok<br />
40