8. - KOKI
8. - KOKI
8. - KOKI
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
2011.04. 06.<br />
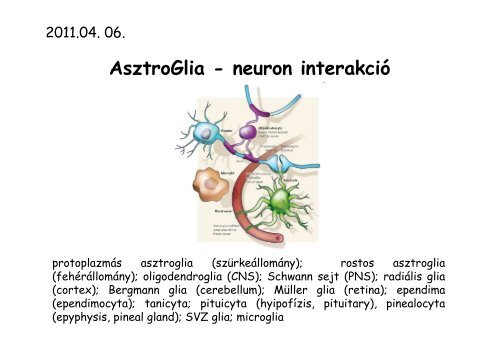
AsztroGlia - neuron interakció<br />
protoplazmás asztroglia (szürkeállomány); rostos asztroglia<br />
(fehérállomány); oligodendroglia (CNS); Schwann sejt (PNS); radiális glia<br />
(cortex); Bergmann glia (cerebellum); Müller glia (retina); ependima<br />
(ependimocyta); tanicyta; pituicyta (hyipofízis, pituitary), pinealocyta<br />
(epyphysis, pineal gland); SVZ glia; microglia
Astrocytes:<br />
"Every textbook says they don't do anything, even<br />
though they're the major cell type in the brain."<br />
(Ben Barres)<br />
Astrocyte-neuron<br />
lactate transport is<br />
required for long-term<br />
memory formation.<br />
Suzuki A. et al., Cell. 2011<br />
144(5):810-23.<br />
Neuron: glia arány<br />
1:10 human<br />
1:1 rodents<br />
6:1 nematodes
Allen and Barres, 2009
GFAP: gliális fibrilláris savas fehérje (IF)<br />
Hoechst<br />
• vér/agy gát (asztroglia-endotél)<br />
• liquor/agy gát (asztroglia-ependima)<br />
• glia limitans (asztroglia-pia mater)
In vitro<br />
In vivo<br />
GFAP: gliális<br />
fibrilláris savas<br />
fehérje (IF)<br />
Hoechst<br />
GFAP festés: az asztrocita<br />
térfogatának csak kb. 15%-<br />
át adja ki
P37<br />
hGFAP-EGFP<br />
DAPI
Asztrociták<br />
Brainbow, Lichtmann 2007<br />
www_biology_uiowa_edu_daileylab
Átlapolódó<br />
asztrocita<br />
territóriumok<br />
(domének)<br />
Bushong, Ellismann in<br />
Volterra, Meldolesi<br />
Nature Rev Neurosci, 2005
Asztroglia<br />
„szincícium”<br />
Rés-kapcsolatok<br />
Idegi hálózatok<br />
mellett<br />
Glia network !
Allen and Barres, 2009<br />
asztro<br />
neuron
- agyi mikrovaszkulatúrával<br />
- több száz neuronális nyúlvánnyal<br />
egyetlen asztrocita<br />
kapcsolatban lehet<br />
- sok neuronális sejttesttel<br />
- akár több tízezer szinapszissal<br />
- idegi őssejt-niche tagja lehet<br />
I.<br />
szinaptikus<br />
működés<br />
szabályozása<br />
II.<br />
neuro-vaszkuláris<br />
kapcsoltság;<br />
metabolikus<br />
együttműködés<br />
III.<br />
neurogenezis
„Tripartite” szinapszis<br />
Halassa 2007<br />
-Glutamát reciklizálás<br />
- K + „spatial buffering”<br />
- Gliotranszmitter ürítés
Neuronális glutaminsav reciklizálása: glutamát-glutamin ciklus<br />
glutaminase<br />
[Glu] IC<br />
~1-10 mM<br />
glutamine<br />
synthase<br />
[Glu] IV<br />
~100 mM<br />
[Glu] IC<br />
~50uM-1 mM<br />
[Glu] EC<br />
~1uM<br />
Siegel GJ, Agranoff BW, Albers RW, et al., editors. 1999
Serkentő (glutamaterg) szinapszis<br />
GLNase<br />
Bak LK. et al. 2006<br />
tricarboxylic acid cycle<br />
(TCA cycle; Krebs cycle; citric acid cycle)
- szabad ammónia keletkezik neuronban<br />
- hiperammonémia veszélyes lehet (gliózis, ödéma,<br />
ischemiás encephalopátia, felborult Glu/Gln ciklus)<br />
- agy ammónia ürítésének fő útja: gliális GS révén<br />
gyártott Gln leadása a vérbe<br />
-ha Gln[EC] olyan magas, hogy a neuronális Gln felvétel<br />
telített, akkor a gliális glutamin leadás gátlódik a „system<br />
N” transzport megfordulásával
„System L” :<br />
aminosav antiporter,<br />
gliális Gln ürítés és<br />
nem-neuroaktív<br />
aminosavakba<br />
(Leu, Ala)<br />
„csomagolt ammónia<br />
felvétele<br />
(aminosav shuttle)<br />
„System A” transzporter: neuronális Gln felvétel<br />
(„concentrative, sodium-dependent and electrogenic”)<br />
„System N”: gliális Gln leadás/felvétel<br />
(„Na+-glutamine symporter and a H+ anti-porter, sodium-dependent, yet electroneutral”<br />
Bak LK. et al. 2006
Gátló (GABA-erg) szinapszis<br />
glutamate<br />
decarboxylase<br />
GLNase<br />
Bak LK. et al. 2006<br />
- GABA-erg neuronoknál fontosabb a re-uptake mint a szintézis<br />
- GABA-erg terminálisokban kisebb a Gln raktár<br />
- GLIA az idegi gátlást tudja kontrollálni ily módon !
Neuroenergetika (alap)<br />
(thought needs food)<br />
GLUT3: neuronális<br />
glükóz transzporter<br />
GLUT1: gliális<br />
glükóz transzporter<br />
Asztro:<br />
glikogén<br />
raktár !<br />
Luc Pellerin et al. 2007, 2010<br />
MCT:<br />
laktát transzporter TCA cycle<br />
(monocarboxylate)<br />
Agyban: glükóz (majdnem) teljes oxidációja (6CO2+6H20) !!<br />
Agyi<br />
glikogén:<br />
(humán):<br />
0,5-1,5g<br />
(0,1% of<br />
total brain<br />
weight)
Glutamáterg aktiváció: korai fázis<br />
1. Glu ürülés<br />
szinapszisban<br />
AMPA receptor<br />
aktiváció, EPSP,<br />
Na+ belépés<br />
2. depolarizációs<br />
hullám, fesz. függő<br />
Na+ csatornák nyílnak,<br />
Na+/K+ ATPáz<br />
visszaállítja iongradienst<br />
- ami sok<br />
energiát használ<br />
3. oxidatív<br />
foszforiláció<br />
aktiválódik, NADH<br />
elhasználódik<br />
5. De: AMPAR<br />
aktivációra a<br />
neuronális<br />
glükóz felvétel<br />
csökken<br />
4. Citromsavciklus<br />
felpörög - piruvát<br />
elhasználódik, nő a<br />
glükóz és laktát<br />
lebontás<br />
6. főleg laktátot<br />
használ az idegsejt !
Glutamáterg aktiváció: késői fázis<br />
1. A szinaptikus<br />
résbe kerülő<br />
glutamátot az<br />
asztrocita<br />
felveszi (GLAST,<br />
GLT1 glutamát<br />
transzporterek)<br />
2. ez nagy Na+<br />
influxot is<br />
jelent, amit<br />
Na+/K+ ATPáz<br />
állít helyre<br />
3. és aktiválódik<br />
a glükóz<br />
transzport<br />
4. és a glükóz<br />
feldolgozás is a<br />
gliában<br />
5. a glikolízis<br />
nagy citoplazmás<br />
NADH szint<br />
növekedést okoz<br />
ami segíti<br />
piruvát→laktát<br />
átalakulást, és a<br />
laktát ürülést
Glutamáterg aktiváció: intenzív és hosszútávú stimuláció<br />
1. intenzív<br />
glutamate<br />
reuptake asztrocitákban,<br />
és<br />
az ec. glükóz<br />
készlet hamar<br />
kimerül<br />
2. ilyenkor a<br />
gliális glikogén<br />
mobilizálódik<br />
3. glikolízis az<br />
elsődleges<br />
energiatermelési<br />
útvonal ilyenkor<br />
4. és a laktát<br />
termelődés<br />
biztosítja a<br />
magas glikolitikus<br />
rátát
Amiről<br />
eddig<br />
beszéltünk<br />
:<br />
Asztrocita<br />
– neuron<br />
laktát sönt<br />
hipotézis<br />
(ANLSH)<br />
Dienel GA, Cruz N. 2004<br />
Pellerin et al. 2007<br />
Astrocyte<br />
- neuron<br />
lactate<br />
shuttle<br />
Hipotézis !!! arról, hogy a neuronális aktivitás<br />
és glükóz felhasználás az asztrociták aerob<br />
glikolízisét és a neuronok laktát hasznosítását vonja<br />
maga után.<br />
A „neurometabolikus community” megosztott:<br />
csak glükózt vagy laktátot is használ az agy energiaként !!
Cell 144, 810–823, March 4, 2011<br />
- Patkány HC: tanulás során ec. glikogén eredetű laktát szint nő<br />
- Gliális laktát transzporterek (MCT4 vagy MCT1) kilövése<br />
amnéziát okoz, amit L-laktát visszaállít (de a glükóz nem !!)<br />
- Neuronális laktát transzporter hiánya szintén amnéziához<br />
vezet, amit sem a laktát, sem glükóz nem állít helyre
„Spatial buffering”<br />
K+ eltávolítása a tüzelő neuronok környezetéből az<br />
asztrocita-hálózat által<br />
Orkand RK, Nicholls JG, Kuffler SW (1966)<br />
Effect of nerve impulses on the<br />
membrane potential of glial cells in the<br />
central nervous system.<br />
of Amphibia. J Neurophysiol 29:788–806.<br />
nervus opticus stimuláció<br />
a nem mielinált axonok körüli gliában<br />
lassú de- és repolarizáció<br />
később extracelluláris mező-potenciál<br />
mérések és<br />
aktivitás-függő [K+]ec mérések<br />
Kofuji and Newman, 2004<br />
optikai imaging agyszeleteken<br />
(intrinsic optic signals (IOS),<br />
ec. tér zsugorodása/tágulása)
Retina, K+ siphoning<br />
1. K+ ürül az IPL (inner<br />
plexiform layer)-ből<br />
neuronális stimulációra<br />
2. K+ bekerül a Müller gliába<br />
3. K+ a Müller gliából főleg<br />
az erekbe és az üvegtestbe<br />
jut a végtalpakon keresztül<br />
4. A fény által indukált<br />
ec. [K+] csökkenés a<br />
szubretinális térben<br />
K+ kiáramláshoz vezet a<br />
Müller gliából<br />
Newman 1996<br />
„K+ reservoir”<br />
Müller sejten belül a K+<br />
konduktancia 94%-a ide<br />
koncentrálódik !<br />
(kétéltűekben) siphoning...
Térbeli K+ pufferelés a gliasejtek nagy K+<br />
permeabilitásától és a glia szincíciumtól függ<br />
Inward rectifier kálium csatornák<br />
(Kir) nagy denzitásban és<br />
lokalizáltan a glián (pl Kir4.1)<br />
Kir és Aquaporinok együttes előfordulása, kolokalizáció<br />
Benfenati and Ferroni, 2010
Asztroglia szincícium<br />
calcium hullám „átugrik” a sejtmentes<br />
sávon<br />
Ca ++ hullám<br />
a stimulált<br />
sejt körül<br />
Ca ++ hullám<br />
amit a<br />
perfúzió<br />
eltérít<br />
Hassinger TD, 1996, PNAS 93:13268-13273
Gliotranszmisszió<br />
Asztrocita<br />
stimuláció<br />
(mechanikus,<br />
elektromos,<br />
neuronális)<br />
Gliális Ca++<br />
válasz<br />
Gliotranszmitter<br />
ürítés<br />
Parakrin hatás<br />
környező asztrocitákra<br />
Neuronális működés<br />
szabályozása
Gliotranszmitterek<br />
Volterra, Meldolesi<br />
Nature Rev Neurosci, 2005
Ca ++ függő Glutamát release asztrocitákból<br />
• In vitro több stimulus hat így: mechanikai, elektromos, Glu<br />
• A Glutamát gliális mGluRs és AMPA receptorok stimulációja<br />
által indítja be a gliális Glu ürítést<br />
• Az asztrociták is szabályozott exocitózissal képesek<br />
glutamátot üríteni (a neuronokhoz hasonlóan)<br />
• De: hemichannel is !!<br />
• Gliából ürülő Glu extraszinaptikus neuronális NMDA<br />
receptorokat tud aktiválni: ezáltal pl. piramissejtek tüzelését<br />
szinkronizálni tudja kb 100 um távolságon belül – 1 asztro koinnervál<br />
több neuront<br />
• Gliális Glu preszinaptikus mGluR vagy kainát receptorokon át<br />
növelni tudja a neuronális transzmitter ürítést
Volterra and<br />
Meldolesi<br />
2005<br />
Glutamát<br />
exocitózis<br />
asztrocitákból<br />
[Ca ++ ] ic<br />
↑ hatására<br />
FM-64 kiürül<br />
a vezikulumokból<br />
VGLUT<br />
EGFP<br />
FM-64<br />
festék<br />
TIRF<br />
együtt
ELMI<br />
Szinaptikus-szerű<br />
mikrovezikulák<br />
(SLMVs)<br />
asztrocitában<br />
(hippocampus)<br />
Méretre és formára<br />
is hasonlítanak a<br />
szinaptikus<br />
vezikulákhoz<br />
Volterra, Meldolesi<br />
Nature Rev Neurosci, 2005
(a) Normális hippocampusban az<br />
asztrociták Ca++ oszcillációja glutamát<br />
(b) ATP hatására (csillag) az asztrocitákban<br />
ürülést triggerel,<br />
Ca++ oszcilláció indul<br />
ami a piramissejtekben NMDAR-mediált<br />
(c) Ha ATP-t anti-konvulzáns valproáttal<br />
lassú, inward áramokat generál. Ezek az<br />
együtt adnak a glia Ca++ válasza gátlódik<br />
áramok szinkronizáltak klb.<br />
neuroncsoportokban. Halassa and Haydon rev. 2009
Szinaptikus transzmisszió modulációja asztrociták által<br />
Egy példa: heteroszinaptikus depresszió<br />
1. Glutamát ürül (1, piros folt) amikor a<br />
Schaffer-kollaterális (S) - piramissejt<br />
(P) szinapszis nagy frekvenciájú<br />
tüzelése stimulál egy asztrocitát<br />
2. Az asztrocita erre ATP kibocsátással<br />
reagál<br />
3. Ez gyorsan adenozinná alakul (2; kék<br />
folt), ami egy másik S-P kapcsolatot a<br />
preszinaptikus adenozin A1 receptoron<br />
keresztül szupresszálni fog<br />
Volterra, Meldolesi<br />
Nature Rev Neurosci, 2005
Szinaptikus borítottság változása<br />
A hipotalamikus szupraoptikus magban<br />
az asztrociták morfológiai<br />
plaszticitása a tejelválasztással<br />
hozható összefüggésbe<br />
1. oxytocin-termelő idegsejteken<br />
levő szinapszisokról asztrociták<br />
visszahúzzák nyúlványaikat<br />
laktáció alatt<br />
2. így a glia kevésbé tudja<br />
visszavenni a szinapszisba ömlő<br />
glutamátot, ami képes távolabb<br />
elhelyezkedő gátló mGluR<br />
receptorokat<br />
aktiválni<br />
preszinaptikusan<br />
vagy<br />
szomszédos<br />
GABAerg<br />
terminálisokon<br />
3. Ez a neurotranszmitter-ürülés<br />
homo- és heteroszinaptikus<br />
depresszióját okozza: csökken a<br />
szinaptikus hatékonyság (csökken<br />
a neuroszekretoros sejteket<br />
beidegző afferensek hatása)
D-serine mint gliotranszmitter<br />
D-serine függő metaplaszticitás<br />
Szupraoptikus magban :<br />
(a) asztrocita-eredetű D-<br />
serine el tudja érni az NMDA<br />
receptorokat, és segíti az<br />
NMDAR mediálta<br />
transzmissziót és az LTP<br />
kialakulását<br />
(b) Ha a glianyúlványok<br />
visszahúzódnak, a D-serine nem<br />
tud ko-agonistaként működni az<br />
NMDA receptorokon, LTD<br />
alakul ki inkább<br />
(c) Gyors asztrocita (zöld) –<br />
nyúlvány mozgás a dendrittüske<br />
(piros) körül<br />
Halassa and Haydon rev. 2009
Asztrociták és szinaptogenezis<br />
• Néhány hetes tiszta RGC (retinal ganglion cell) vagy<br />
gerincvelői motoneuron tenyészet:<br />
- alacsony szinaptikus aktivitás,<br />
- szinaptikus fehérjék alacsony szintje<br />
• Asztroglia + RGC kokultúra:<br />
- nagy szinaptikus aktivitás (100 X);<br />
- szinapszisszám nő (7X)<br />
• 1 héttel asztrociták eltávolítása után a kokultúrákból:<br />
- a legtöbb szinapszis eltűnik<br />
(Ullian EM. Christopherson KS, Barres BA. Glia. 2004 Aug 15;47(3):209-16.)