Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Kémiai</strong> sajátságok 9.<br />
További lehetőség: nagy szénatomszámú (n C = 20-40) szénhidrogének lánchasító oxidációja<br />
R<br />
R'<br />
O 2 (levegõ)<br />
MnO 2 vagy KMnO 4 (kat.)<br />
R COOH + R' COOH (zsírsavak keveréke!)<br />
Alkánok hőbontása (pirolízise) és dehidrogénezése<br />
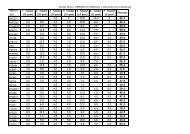
Kiindulási pont: alkánok képződési entalpia és szabadentalpia szénatomszám függése<br />
n C (grafit) + (n+1) H 2 C n H 2n+2<br />
+ H k<br />
o<br />
Alkán H ko<br />
(kJ/mol) S o (kJ/mol.K) G ko<br />
(kJ/mol)<br />
CH 4<br />
-75 0.186 -51<br />
Következmény: n C > 6 esetén a<br />
szétesés termodinamikailag<br />
kedvezményezett!<br />
C 4<br />
H 10<br />
-126 0.310 -17<br />
C 6<br />
H 14<br />
-167 0.388 0<br />
C 9<br />
H 20<br />
-229 0.506 +25<br />
C 10<br />
H 22<br />
-250 0.545 +33<br />
(Forrás: Furka: <strong>Szerves</strong> Kémia)<br />
Krakkolás: kőolajfrakciók (n C = 5-13<br />
alkánok, cikloalkánok) rövid idejű,<br />
lánctöredezést eredményező hőkezelése<br />
Alacsony hőmérsékletű (6-700 o C)<br />
krakkolás:<br />
közepes szénatomszámú telített és<br />
telítetlen láncok (krakkbenzin) + krakkgáz<br />
Magasabb hőmérsékleten a krakkgáz (C 2 -<br />
C 4 alkének) dominál etén, propén,<br />
butadién + H 2 (petrolkémia!)<br />
C 8 H 18 4 CH 2 =CH 2 + H 2 (termodinamikai adatok)<br />
T (K) H (kJ/mol) TS (kJ/mol) G (kJ/mol)<br />
298 416 161 +255<br />
500 420 273 +147<br />
700 415 381 +34<br />
800 416 433 -17<br />
1000 412 536 -124<br />
(Forrás: Furka: <strong>Szerves</strong> Kémia)