Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
Alkének kötésrendszere 2. - Szerves Kémiai Tanszék
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Szerves</strong> Kémia 1. (TKBE0301)<br />
előadási ábraanyag<br />
(<strong>2.</strong> rész)<br />
Patonay Tamás
Alkánok és cikloalkánok <strong>kötésrendszere</strong>,<br />
konformációs viszonyaik. <strong>Kémiai</strong><br />
tulajdonságaik, gyökös szubsztitúció,<br />
láncreakció. Statisztikus termékarány,<br />
regioszelektív halogénezés és értelmezése.<br />
Alkánok egyéb reakciói, petrolkémiai<br />
alapfolyamatok (pirolízis, krakkolás,<br />
izomerizáció), jelentőségük. Előfordulásuk és<br />
legfontosabb előállításaik.
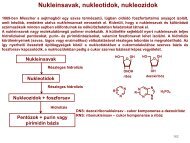
Alkánok fogalma, kötésrendszerük<br />
Telített, nyílt láncú szénhidrogének. Általános képlet: C n H 2n+<strong>2.</strong><br />
Homológ sor: a sor tagjai egy meghatározott, azonos egységben különböznek egymástól<br />
(itt ez a metiléncsoport: -CH 2 -) CH 3 -(CH 2 ) n -H n 0<br />
Cikloalkánok: telített, gyűrűs (egy vagy több gyűrű!) szénhidrogének<br />
Egyetlen gyűrűt tartalmazó cikloalkánok általános képlete: C n H 2n<br />
Nyílt láncú alkánok csoportosítása<br />
- egyenes láncú (elágazást nem tartalmazó) alkánok (n-alkán)<br />
- elágazó láncú alkánok<br />
Kapcsolódó fogalom: szénatomok rendűsége (meghatározó: adott szénatomhoz kapcsolódó<br />
további szénatomok száma)<br />
H<br />
C C<br />
H<br />
H<br />
C<br />
C C<br />
H<br />
H<br />
C<br />
C C<br />
H<br />
C<br />
C<br />
C C<br />
C<br />
C<br />
primer (1 o ) szekunder (2 o ) tercier (3 o ) kvaterner (4 o )<br />
Kötésrendszer – kiindulás: sp 3 hibridállapotú (tetraéderes orientációjú) szén + 1s hidrogének<br />
-kötések; hengerszimmetrikus, bicentrumos MO-k<br />
a szén négy egyenértékű AO-jából négy egyenértékű MO<br />
+<br />
tetraéderes elrendeződés!<br />
Kötéstávolságok: r C-C = 0.153-0.154 nm (1.53-1.54 Ǻ); r C-H = 0.109 nm (1.09 Ǻ)<br />
Kötésszögek: 109 o 28’ (szabályos tetraéder – pl. metánban)<br />
nem szimmetrikus szubsztitúció esetén kötésszögtorzulás (ok: szubsztituensek eltérő<br />
térigénye)<br />
Kötéstorzulás eredménye: destabilizáció (energianövekedés)<br />
H H<br />
Szögfeszültség (Baeyer-feszültség) E = f() 2<br />
C C-C-C = 112 o<br />
azaz 1 o különbség 0.07 kJ/mól, de 10 o különbség 7 kJ/mól C C
Alkánok fogalma, kötésrendszerük <strong>2.</strong><br />
Kötési energiák: E C-C = 345-355 kJ/mól, E C-H = 400-415 kJ/mól ÁTLAGÉRTÉK!<br />
erős, kevéssé polározott kötések. És! E C-H > E C-C (C-C kötéshasadás könnyebb lehet)<br />
Alapállapotú polározottság: EN C = <strong>2.</strong>5, EN H = <strong>2.</strong>1<br />
<br />
De!! Rövid C-H kötéstáv kis dipólmomentum ()<br />
C H<br />
0.4 D<br />
További szempont: tetraéderes elrendezés, vektoriális eredő 0 D<br />
(nincs permanens dipólmomentum!!)<br />
Alkánok konformációja – rotáció az egyes kötés mentén<br />
Diéderes szög fogalma – két egymással kötésben nem levő<br />
csoport és az összekötő szénatomok síkjai által bezárt szög<br />
(A-C-C és C-C-B síkok szöge)<br />
A<br />
C<br />
C<br />
B <br />
Legegyszerűbb eset: etán<br />
nyitott<br />
fedő<br />
Nyitott állás<br />
H<br />
H H<br />
H<br />
H<br />
H<br />
Newmanprojekció<br />
Fedő állás<br />
H H<br />
H<br />
H H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
Fűrészbak<br />
ábrázolás<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
Energiakülönbség (energiagát) - E ~ 12-1<strong>2.</strong>5 kJ/mól (Pitzer-feszültség). Termikus energia<br />
fedezi, de eltérő populációk (egyensúlyi elegy). Alapvető rendezőelv: energiaminimumra<br />
törekvés!
Alkánok konformációja <strong>2.</strong><br />
Bután konformációk<br />
Me Me Me<br />
Me<br />
H<br />
H H<br />
H H<br />
H H H<br />
szinperiplanáris (sp)<br />
H<br />
H<br />
Me<br />
Me<br />
Me<br />
H H Me H<br />
H<br />
H<br />
H<br />
szinklinális (sc)<br />
MeH<br />
H<br />
H H<br />
Me<br />
H<br />
Me<br />
H<br />
H H<br />
antiklinális (ac)<br />
Me<br />
Me<br />
Me<br />
H H<br />
H H H H<br />
H H<br />
Me<br />
Me<br />
antiperiplanáris (ap)<br />
ac<br />
sp<br />
Megjegyzés: a két nyitott állás (sc és ap)<br />
energiaállapota eltérő – ez az ún. gauche<br />
kölcsönhatás (destabilizál!!)<br />
sc<br />
ap<br />
25 kJ/mól<br />
Ez a kölcsönhatás általános, bonyolultabb<br />
nyílt láncú vagy gyűrűs rendszerekben is<br />
jelen van.<br />
3.4 kJ/mól<br />
15 kJ/mól<br />
Hosszabb szénláncú alkánok konformációja<br />
- folyadékfázisban statisztikus gombolyag<br />
- szilárd fázisban (kristály) teljesen nyújtott („cikk-cakk”) konformáció<br />
- elágazások deformálják a fentiekben jellemzett ideális állapotot (kötésszögtorzulás a<br />
növekvő térigény miatt, legvalószínűbb konformer az energiaminimum)
Fizikai sajátságok<br />
Kiindulási pont: gyengén polarizált kötések gyenge másodlagos (indukált dipól - indukált<br />
dipól) kölcsönhatások.<br />
Következmények:<br />
1. Halmazállapot: alacsony op., fp.; szénatomszám növekedéssel erősödő összetartó erők<br />
Legegyszerűbb eset: n-alkánok<br />
Olvadáspont szénatomszámfüggése: két különböző görbe! Ok: eltérő kristályszerkezet<br />
(n c = páros: monoklin, n c = páratlan: triklin)
Fizikai sajátságok <strong>2.</strong><br />
Elágazó láncú alkánok olvadás- és forráspontja – bonyolultabb összefüggések<br />
Általánosságban<br />
- elágazások számának növekedésével csökken a fp. ( gömbalak, kevesebb összetartó erő)<br />
- molekula szimmetriájának növekedésével általában nő az op.<br />
<strong>2.</strong> Sűrűség: < víz d pentán = 0.626 d pentadekán = 0.769 (határérték ~ 0.8)<br />
3. Oldékonyság: vízben alig, apoláros szerves oldószerekben jól, erősen poláros szerves<br />
oldószerekben gyengén (nem képes az oldószer saját struktúráját „felrobbantani”)<br />
Általános alapelv: „simili similis gaudet” (hasonló a hasonlóban oldódik…)<br />
<strong>Kémiai</strong> sajátságok<br />
Kiindulási pont: kevéssé polarizált, erős kötések homolitikus kötéshasadás preferált<br />
<br />
C<br />
<br />
H<br />
igen kis érték!<br />
<br />
C<br />
<br />
C<br />
0<br />
Eltérő rendűségű szénatomok C-H kötéseihez tartozó kötéshasadások energiája (kJ/mól)<br />
Általános szabály: heterolízis<br />
(ionképződés) energiaigénye nagyobb.<br />
Gázfázisra igaz, oldatokban a<br />
szolvatáció ellensúlyozhatja.<br />
De! az alkánok tipikus reakciói<br />
gázfázisúak
<strong>Kémiai</strong> sajátságok <strong>2.</strong><br />
Kérdés: hogyan tovább – a gyökképződést követő folyamatok lehetőségei<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
- H<br />
+ G<br />
C C<br />
C<br />
H<br />
C<br />
G<br />
elimináció<br />
szubsztitúció<br />
Egy hipotetikus gyökös intermedier<br />
utóélete…<br />
Kötési energiákat (entalpia faktor) tekintve a szubsztitúció kedvezményezett, a többszörös<br />
kötés kötési energiája relatíve kisebb<br />
C-C + C-H + C-G > C=C v.ö. 2•C-C (690-710 kJ/mól) vs. C=C (545-555 kJ/mól)<br />
Ez egy durva, csak az entalpiára koncentráló közelítés! Az entrópiatényező (magasabb T)<br />
átírhatja – ld. később (krakkolás, stb.)<br />
viszonylag alacsonyabb hőmérsékleteken<br />
kis reakciókészség, gyökös folyamatokra (elsősorban gyökös szubsztitúcióra) való hajlam<br />
„paraffin” = „parum affinis”<br />
Tényleges reakciók<br />
1. Sav-bázis reakciók (elsődlegesen a Brönsted-elmélet szerint)<br />
Protonálódás (szénhidrogén, mint bázis<br />
– protonmegkötés a - kötőpár révén)<br />
Deprotonálódás (szénhidrogén, mint sav)<br />
CH 4<br />
bázis<br />
H<br />
CH 5<br />
:B<br />
CH 4<br />
-HB<br />
sav<br />
:CH 3<br />
A kis EN és a preferált homolízis miatt kedvezőtlen folyamatok gyenge savak és bázisok.<br />
Reakció csak igen reaktív, erőteljes reakciópartnerekkel („szupersavak”, Oláh György)
<strong>Kémiai</strong> sajátságok 3.<br />
<strong>2.</strong> Alkánok gyökös szubsztitúciója (S R )<br />
alapeset: metán halogénezése – gyökös láncreakció
<strong>Kémiai</strong> sajátságok 4.<br />
Metán szukcesszív halogénezése – további halogének belépése<br />
Pl. az első lépés<br />
H 3 C Cl + Cl<br />
- HCl<br />
H 2 C Cl<br />
Összességében: termékkeverék, nehéz<br />
irányíthatóság!<br />
H 2 C Cl + Cl 2 - Cl<br />
CH 2 Cl 2<br />
CH 4 CH 3 Cl CH 2 Cl 2 CHCl 3 CCl 4<br />
Alkánok reakciója különböző halogénekkel – a reakciósebesség függése a halogén minőségétől<br />
K<br />
CH 4 + Hlg 2<br />
CH 3 -Hlg + HHlg<br />
Megjegyzés: elvben minden reakció megfordítható<br />
(Forrás: Furka: <strong>Szerves</strong> Kémia)
<strong>Kémiai</strong> sajátságok 5.<br />
Következmény<br />
Fluorozás: robbanásszerű hevességgel (lavinaszerűen induló láncok perfluorszármazékok,<br />
C-C kötéshasadás lehetősége – E C-F 550 kJ/mól!! (a legerősebb kémiai kötés)<br />
Klórozás, brómozás: kezelhető módon megy végbe, gyakorlati alkalmazás lehetséges<br />
Jódozás: S R mechanizmus szerint nem megy végbe, sokkal inkább a fordított reakció<br />
(reduktív dehalogénezés jodidionok jelenlétében – szintézis céljára is!)<br />
CH 3 -Hlg + HI<br />
CH 4 + l-Hlg<br />
Komplex (n C 3 és/vagy elágazó láncú) szénhidrogének halogénezése<br />
Alapkérdés: ugyanazon S R mechanizmus mellett van-e különbség az eltérő helyzetű<br />
hidrogének reakciókészségében<br />
Ha nincsen termékarány ~<br />
hidrogének számával<br />
ún. statisztikus termékarány<br />
H 3 C H C CH 3<br />
Cl<br />
2-klórpropán<br />
25%<br />
H 3 C CH 2 CH 3 H 3 C CH 2 CH 2<br />
Cl<br />
1-klórpropán<br />
75%<br />
Ha nem a statisztikus termékarány érvényesül: szelektivitás!!<br />
Jelen esetben ez azt jelenti, a hidrogénabsztrakció a két különböző termékhez vezető reakció<br />
sebességmeghatározó lépésében nem azonos valószínűséggel megy végbe bizonyos gyökök<br />
képződése preferált<br />
Kísérleti tapasztalat: alacsonyabb hőmérsékleten (350 o C) a 2-Cl-propán képződés előtérbe kerül<br />
H 3 C H C CH 3<br />
Cl<br />
2-klórpropán<br />
55%<br />
H 3 C CH 2 CH 3 H 3 C CH 2 CH 2<br />
Cl<br />
1-klórpropán<br />
45%
<strong>Kémiai</strong> sajátságok 6.<br />
A halogénezés mechanizmusában az 1. láncvivő lépés a sebességmeghatározó a<br />
szénhidrogén gyök képződéséhez vezető lépés G ‡ értéke dönt (ha kinetikus kontroll van)<br />
G ‡<br />
2-Cl-propán + HCl<br />
‡ R H Cl<br />
2 ‡ 4<br />
‡ 3<br />
H 3 C CH CH 3<br />
‡ 1<br />
A<br />
H 3 C CH 2 CH 2<br />
B<br />
Pr-H + •Cl<br />
1-Cl-propán + HCl<br />
‡<br />
Kompetitív reakciók – a termékarányt a G 1‡ és a G 2‡ viszonya állítja be feladat: az<br />
átmeneti állapotok közelítése (intermedierszerű/gyökszerű TS)<br />
Hammond-elv szomszédos gyök intermedierek stabilitásának meghatározása<br />
Gyökstabilitási sorrend: CH 3 < 1 o < 2 o < 3 o<br />
Ok: alkil csoportok elektronküldő jellege (EN sp2 > EN sp3 miatt<br />
+I, illetve hiperkonjugáció) elektronhiányos centrum<br />
stabilizációja<br />
Következmény: az A gyök stabilabb G 1‡ kisebb 2-klórpropánhoz vezető reakció<br />
gyorsabb regioszelektivitás<br />
Cl<br />
Cl<br />
Cl 2<br />
Cl<br />
További<br />
Cl<br />
példa:<br />
300 o C<br />
50% 25% 16.7% 8.3% statisztikus<br />
30% 15% 33% 22%<br />
<br />
kísérleti
<strong>Kémiai</strong> sajátságok 7.<br />
Halogénezések szelektivitásának összevetése<br />
H 3 C H C CH 3<br />
Hlg<br />
2-Hlg-propán<br />
25%<br />
55%<br />
97%<br />
H 3 C CH 2 CH 3 H 3 C CH 2 CH 2<br />
Hlg<br />
statisztikus<br />
szelektív klórozás<br />
szelektív brómozás<br />
Indoklás: reaktivitás-szelektivitás elve<br />
Nagyobb méretű brómatom párosítatlan elektron<br />
nagyobb térrészben oszlik el nagyobb stabilitás,<br />
kisebb reaktivitás, erősebb szelekció<br />
1-Hlg-propán<br />
75%<br />
45% G<br />
3%<br />
‡<br />
Brómozás esetén nagyobb<br />
szelektivitás!<br />
‡ 1<br />
‡ 2<br />
Pr-H + •Cl<br />
Pr-H + •Br<br />
Az R-H + •Hlg •R + HHlg reakció aktiválási energiái<br />
<br />
Megjegyzés: létezik más értelmezés is (korai/késői átmeneti állapotok = kisebb/nagyobb gyökös karakter<br />
(ld. pl. Furka könyv)<br />
A szelektivitás feltétele a kinetikus kontroll érvényesülése magasabb hőmérsékleteken<br />
csökken a regioszelektivitás, 500 o C már a statisztikus termékarány érvényesül!
<strong>Kémiai</strong> sajátságok 8.<br />
További gyökös mechanizmusú reakciók<br />
Szulfoklórozás<br />
(halogénezéssel analóg gyökös láncreakció)<br />
Szulfonálás<br />
R H SO 2/H 2 O/h<br />
vagy<br />
SO 3 /gõzfázis<br />
R H<br />
SO 2/Cl 2 /h<br />
R SO 2 Cl<br />
hidrolízis<br />
R SO 2 OH Jelentőség: mosószergyártás<br />
(R = nagy szénatomszámú lánc)<br />
R SO 2 OH<br />
Nitrálás<br />
(gyökös, de nem láncreakció)<br />
Alkánok oxidációja<br />
1. Teljes oxidáció (égés)<br />
R H<br />
híg HNO 3<br />
vagy<br />
N 2 O 4 /p<br />
R NO 2<br />
2 C n H 2n+2 + (3n + 1) O 2 2n CO 2 + (2n + 2) H 2 O + H<br />
Égéshő: 1 mólnyi standard állapotú szénhidrogén standard állapotú oxigénnel<br />
történő elégetését kísérő energiaváltozás<br />
Jelentős érték (pl. CH 4 : 804 kJ/mól). Szénhidrogének felhasználása<br />
energiatermelésre (hatékony, de célszerűtlen…)<br />
<strong>2.</strong> Részleges (parciális) oxidáció – „szintézisgáz” gyártás<br />
szintézisgáz (szűkebb értelemben): CO + H 2 tartalmú gázkeverék<br />
szervetlen és szerves vegyipar H 2 igénye, ammónia-, metanol-, formaldehidgyártás,<br />
aldehidek/alkoholok gyártása, szénhidrogének előállítása Fischer-Tropsch-szintézissel, stb.<br />
Bővebben: http://www.muszeroldal.hu/assistance/c1kemia.pdf<br />
2 CH 4 + O 2 2 CO + 4H 2 vagy CH 4 + H 2 CO + 3 H 2 O (termikusan vagy Ni-kat./700 o C)<br />
CH 2 + 1/2 O 2 CO + H 2 H = - 92 kJ/mól CH 2 + H 2 O CO + H 2 H = + 151 kJ/mól
<strong>Kémiai</strong> sajátságok 9.<br />
További lehetőség: nagy szénatomszámú (n C = 20-40) szénhidrogének lánchasító oxidációja<br />
R<br />
R'<br />
O 2 (levegõ)<br />
MnO 2 vagy KMnO 4 (kat.)<br />
R COOH + R' COOH (zsírsavak keveréke!)<br />
Alkánok hőbontása (pirolízise) és dehidrogénezése<br />
Kiindulási pont: alkánok képződési entalpia és szabadentalpia szénatomszám függése<br />
n C (grafit) + (n+1) H 2 C n H 2n+2<br />
+ H k<br />
o<br />
Alkán H ko<br />
(kJ/mol) S o (kJ/mol.K) G ko<br />
(kJ/mol)<br />
CH 4<br />
-75 0.186 -51<br />
Következmény: n C > 6 esetén a<br />
szétesés termodinamikailag<br />
kedvezményezett!<br />
C 4<br />
H 10<br />
-126 0.310 -17<br />
C 6<br />
H 14<br />
-167 0.388 0<br />
C 9<br />
H 20<br />
-229 0.506 +25<br />
C 10<br />
H 22<br />
-250 0.545 +33<br />
(Forrás: Furka: <strong>Szerves</strong> Kémia)<br />
Krakkolás: kőolajfrakciók (n C = 5-13<br />
alkánok, cikloalkánok) rövid idejű,<br />
lánctöredezést eredményező hőkezelése<br />
Alacsony hőmérsékletű (6-700 o C)<br />
krakkolás:<br />
közepes szénatomszámú telített és<br />
telítetlen láncok (krakkbenzin) + krakkgáz<br />
Magasabb hőmérsékleten a krakkgáz (C 2 -<br />
C 4 alkének) dominál etén, propén,<br />
butadién + H 2 (petrolkémia!)<br />
C 8 H 18 4 CH 2 =CH 2 + H 2 (termodinamikai adatok)<br />
T (K) H (kJ/mol) TS (kJ/mol) G (kJ/mol)<br />
298 416 161 +255<br />
500 420 273 +147<br />
700 415 381 +34<br />
800 416 433 -17<br />
1000 412 536 -124<br />
(Forrás: Furka: <strong>Szerves</strong> Kémia)
Kitérő: természetes szénhidrogénforrások és feldolgozásuk
<strong>Kémiai</strong> sajátságok 10.<br />
Kőolajból és földgázból értékes szerves vegyipari kiindulási anyagok nyerhetők +<br />
motorhajtóanyagok az „értéktelenebb” desztillációs frakciókból<br />
További lehetőségek:<br />
Katalitikus krakkolás (Al-szilikátok, zeolitok)<br />
ionos folyamat, izomerizációs folyamatok, elágazások<br />
száma nő (v.ö. oktánszám)<br />
R<br />
CH2<br />
CH 2<br />
CH3<br />
R<br />
Hidrokrakkolás<br />
nagy nyomású hidrogén atmoszférában, szilicium-aluminium-oxid vagy zeolitokon<br />
végzett krakkolás alacsony forráspontú termékek (benzin, gázolaj)<br />
CH CH 3<br />
CH 3<br />
Dehidrociklizáció (Cr-Al-oxidok)<br />
dehidrogéneződéssel gyűrűzáródás, majd<br />
aromatizáció (kőolajok aromás tartalma<br />
csekély, igény a BTX-frakcióra)<br />
R<br />
R<br />
R<br />
= - H 2<br />
- H 2<br />
R<br />
Magas hőmérsékletű pirolízis C 2 H 4 CH 4 C 2 H 2<br />
etén<br />
etin
Cikloalkánok sajátságai<br />
Kötésrendszer alapvetően azonos (kisebb tagszámú gyűrűknél szögfeszültség [Baeyer-feszültség],<br />
fedőállásokból fakadó Pitzer-feszültség destabilizált rendszerek)<br />
Feszültségek csökkentése (energiaminimalizáció) – konformációváltozások (részletesen:<br />
„Sztereokémia és reakciómechanizmusok” (TKBE 0304))<br />
Ciklopentán<br />
Pitzer-feszültség<br />
Ciklohexán<br />
szófa („sofa”)<br />
Szék („chair”) konformáció (sem<br />
Baeyer, sem Pitzer-feszültség, de 6<br />
db gauche-kölcsönhatás)<br />
axiális és ekvatoriális hidrogének,<br />
két ekvivalens konformáció, átrezgés<br />
Kád („boat”) konformáció<br />
(Baeyer-feszültség nincs,<br />
Pitzer-feszültség van<br />
csavart kád<br />
("twist-boat")<br />
enyhülő Baeyer- és<br />
Pitzer-feszültség<br />
félszék<br />
("half-chair")<br />
erős Baeyer- és<br />
Pitzer-feszültség<br />
Energiaviszonyok: szék < csavart kád < kád < félszék<br />
Szék konformációban az ekvatoriális helyzet<br />
energetikailag kedvezőbb, mint az axiális!
Cikloalkánok sajátságai <strong>2.</strong><br />
Ciklohexán energiadiagramja<br />
Monoszubsztituált ciklohexán<br />
H<br />
H<br />
R<br />
H<br />
H<br />
R<br />
destabilizáló<br />
1,3-kölcsönhatás<br />
Szubsztituensek ekvatoriális elhelyezkedése preferált!<br />
metil-ciklohexán
Cikloalkánok sajátságai 3.<br />
<strong>Kémiai</strong> reakciók – hasonlatosság az alkánokhoz (tipikus: S R )<br />
Kivétel: ciklopropán, ciklobután<br />
(nagy szögfeszültség miatt gyűrűfelnyílás –<br />
addíciós reakciók! – alkénszerű sajátságok)<br />
H 2 /Ni<br />
50 o C<br />
H<br />
H<br />
Br 2<br />
Br<br />
Br<br />
Alkánok és cikloalkánok előállítása<br />
1. Alkánszintézisek változatlan hosszúságú szénlánc esetén<br />
1a. Redukciós módszerek<br />
R C C R 1<br />
H H R<br />
R 1 R C C R 1<br />
alkén<br />
alkin<br />
• Katalitikus redukció: H 2 /katalizátor (Pd-C; Pt, PtO 2 , Raney-Ni)<br />
• Egy-elektron transzfer (SET): fém (M) (Al, Zn, Fe, Sn, stb./ sav vagy lúg<br />
SET reakció: felváltva elektron és H belépése
Alkánok és cikloalkánok előállítása <strong>2.</strong><br />
1b. Funkcióscsoport módosítása<br />
Hlg<br />
R R 1<br />
Mg/Et 2 O<br />
cc. HI/<br />
vagy P/I 2 /<br />
reduktív<br />
dehalogénezés<br />
MgHlg<br />
R R 1<br />
Grignard<br />
vegyület<br />
H 3 O<br />
R R 1<br />
P/I 2 /<br />
Clemmensenredukció<br />
Kizsnyer-Wolfredukció<br />
R'O Na<br />
<br />
Zn(Hg)/H<br />
NH<br />
N 2<br />
R R 1<br />
hidrazon<br />
NH 2 NH 2<br />
O<br />
R R 1<br />
aldehid/keton<br />
OH<br />
R R 1<br />
alkohol<br />
<br />
<strong>2.</strong> Alkánszintézisek láncrövidítéssel R COOH<br />
R H + CO 2 dekarboxilezés<br />
Nemcsak szabad karbonsavak, hanem karbonsavsók is adják. A dekarboxilezéshez szükséges<br />
hőmérséklet az R csoport szerkezetétől függ!<br />
3. Alkánszintézisek lánchosszabbítással<br />
Wurtz-szintézis<br />
R<br />
I<br />
Na<br />
abs. Et 2 O<br />
Csak szimmetrikus alkánok előállítására alkalmas.<br />
R R
Alkánok és cikloalkánok előállítása 3.<br />
Cikloalkánok előállítása – valamennyi korábban tárgyalt módszer, gyűrűsw kiindulási<br />
anyagból<br />
Gyűrű kiépítésével járó szintézisek<br />
• diszjunkt dihalogenidek (,-dihalogén alkánok) gyűrűzárása<br />
R<br />
CH 2 Hlg<br />
CH 2 Hlg<br />
M<br />
R<br />
CH 2<br />
CH 2<br />
M = Na (intramolekuláris Wurtz-reakció)<br />
vagy M = Zn/EtOH/<br />
• alkének karbén addíciója<br />
CHCl 3<br />
NaOH<br />
- HCl<br />
-elimináció<br />
: CCl 2<br />
R 1 R 2 R 1 R 2<br />
Cl<br />
Cl
<strong>Alkének</strong>, di- és poliének <strong>kötésrendszere</strong>, gátolt<br />
rotáció. <strong>Alkének</strong> fizikai és kémiai tulajdonságai.<br />
Elektrofil és gyökös addíciós reakciók.<br />
Markovnyikov-szabály és értelmezése. Anti-<br />
Markovnyikov orientáció. Polimerizáció és<br />
típusai. Allil helyzetű szubsztitúció. -kötés<br />
felszakadásával, illetve lánchasadással járó<br />
oxidációs reakciók. Konjugált diének addíciós<br />
reakciói, az 1,2- és 1,4-addíció és értelmezése.<br />
Diels-Alder cikloaddíció. <strong>Alkének</strong> és diének<br />
előállítása.
<strong>Alkének</strong> (olefinek) és csoportosításuk<br />
Egy vagy több kettőskötést tartalmazó nyílt láncú vagy gyűrűs szénhidrogének.<br />
Általános képlet: C n H 2n , C n H 2n-2 (dién vagy cikloalkén), …<br />
Kettőskötések száma alapján: monoolefin (alkén), dién, trién, polién<br />
Diének csoportosítása:<br />
C C C<br />
kumulált dién<br />
C<br />
penta-2,3-dién<br />
C C<br />
C C<br />
konjugált dién<br />
penta-1,3-dién<br />
C C<br />
(CH 2 ) n<br />
C C<br />
izolált dién (n > 0)<br />
penta-1,4-dién<br />
<strong>Alkének</strong> <strong>kötésrendszere</strong><br />
Legegyszerűbb: + modell<br />
Alap: sp 2 hibridállapotú pillér szénatomok<br />
-váz a hibrid (sp 2 ) AO-kból, a -kötés a p z AO-k<br />
oldalirányú átlapolásával (maximális átfedés =<br />
energiaminimum feltétele: párhuzamos p z AO-k)<br />
Következmény: erősebb, rövidebb kötés<br />
d C=C = 0.134 nm ↔ d C-C = 0.154 nm<br />
E C=C = 610-630 kJ/mól ↔ E C-C = 345-355 kJ/mól<br />
DE! E + < E 2 (690-710 kJ/mól) -kötés gyengébb, ok: kisebb átfedés<br />
A -váz geometriája alapvetően síktrigonális (kötésszög = 120 o ), ezt a szubsztituensek<br />
torzíthatják.<br />
Kettőskötés megjelenésének következménye: gátolt rotáció (az<br />
elfordulás a -kötés gyengülésével, megszűnésével jár!)<br />
A kötéshasítás (izomerizáció) hőközléssel vagy UV fénnyel kiváltható
<strong>Alkének</strong> <strong>kötésrendszere</strong> <strong>2.</strong><br />
Gátolt rotáció következménye: diasztereomerek („geometriai izomerek”) létezése<br />
H H H Et<br />
1<br />
Cl<br />
H<br />
2 1<br />
Cl<br />
Et<br />
1<br />
Me<br />
Et<br />
Me<br />
H<br />
Me<br />
Et<br />
2 1<br />
2<br />
Me<br />
H<br />
2<br />
cisz (Z)<br />
transz (E)<br />
E<br />
Z<br />
Konfigurációjuk megadása: cisz/transz (legfeljebb 1,2-diszubsztituált rendszerekre!)<br />
Általánosan: E (Entgegen = szemben)/Z (Zusammen = együtt) – mindig alkalmazható<br />
Alap: adott szénen levő szubsztituensek rangsorolása a CIP konvenció szerint<br />
<strong>Alkének</strong> fizikai sajátságai<br />
Olvadáspont, forráspont: erős hasonlóság az alkánokhoz – gyenge indukált dipól-indukált<br />
dipól, vagy dipól-dipól kölcsönhatások (alacsony op., fp.)<br />
Dipólmomentum megjelenése – geometriától függően!<br />
Oldékonyság: vízben és erősen poláros oldószerekben gyenge, apoláros oldószerekben<br />
korlátlan vagy jó
<strong>Alkének</strong> stabilitása<br />
Alkánokhoz képest kisebb termodinamikai stabilitás (ld. képződéshő, képződési<br />
szabadentalpia) – ok: két szénatom közötti nagy elektronsűrűség destabilizáló hatása<br />
Különböző szerkezetű alkének stabilitásának összehasonlítása
<strong>Alkének</strong> kémiai sajátságai<br />
Kiindulási pont: -elektronpár<br />
lazábban kötött, nagy<br />
elektronsűrűséget jelent támadás<br />
elektronhiányos részecskékkel<br />
(elektrofil vagy gyök)<br />
C C<br />
E<br />
R<br />
E<br />
C C<br />
karbéniumion<br />
R<br />
C C<br />
E<br />
vagy C C<br />
"nemklasszikus" kation<br />
gyök<br />
Kérdés: a keletkező intermedier további sorsa - addíció vagy elimináció<br />
E<br />
C C<br />
- X<br />
E<br />
C C<br />
X<br />
:Nu<br />
E Nu<br />
C C<br />
R<br />
C C<br />
- X<br />
R<br />
C C<br />
X<br />
R 1<br />
R R 1<br />
C C<br />
Kötési energiák figyelembevételével (vö. E + < E 2 , a -<br />
kötés kisebb energiát képvisel) az addíció preferált!<br />
Megjegyzés: ez mindaddig igaz, amíg a reakciót elsődlegesen az<br />
entalpiatényező vezérli. Az addíció mólszámcsökkenéssel járó,<br />
entrópia oldalról kedvezőtlen folyamat magasabb hőmérsékleten az<br />
entrópiatag felülírhatja az addíciós folyamat dominanciáját<br />
<strong>Alkének</strong> legfontosabb reakciói:<br />
1. Ad E , Ad R<br />
<strong>2.</strong> allil-helyzetű szubsztitúció<br />
3. C=C kötés hasadásával járó reakciók
<strong>Alkének</strong> kémiai sajátságai <strong>2.</strong><br />
1. <strong>Alkének</strong> elektrofil addíciója (Ad E )<br />
C C<br />
E<br />
E<br />
C C<br />
vagy<br />
E<br />
C C<br />
:Nu<br />
E Nu<br />
C C<br />
Az intermedier jellegét az<br />
elektrofil mérete dönti el!<br />
karbéniumion<br />
"nemklasszikus" kation<br />
1.1. Halogénezés – oldatfázisban (gyökiniciálás nélkül!)<br />
Hlg<br />
Hlg<br />
C C<br />
H 2 C CH 2<br />
Br 2<br />
CCl 4 vagy CH 3 COOH<br />
vagy H 2 O<br />
Hlg<br />
Hlg <br />
C C<br />
-komplex<br />
- :Hlg<br />
BrH 2 C CH 2 Br<br />
Hlg<br />
C C<br />
halóniumion<br />
-komplex)<br />
:Hlg<br />
Hlg<br />
Hlg<br />
Hlg = Cl, Br<br />
A nukleofil támadása térszerkezeti okok miatt csak hátoldalról történhet sztereoszelektív<br />
reakció, a két halogén antiperiplanáris helyzetben („transz-addíció”)<br />
Megjegyzés: ez a C-C kötés szabad rotációja miatt gyűrűs rendszereknél (vagy speciális szerkezeti feltételek<br />
esetén) észlelhető
<strong>Alkének</strong> kémiai sajátságai 3.<br />
Az ionos jelleget bizonyítja az oldószernek, illetve a kettőskötéshez kapcsolódó<br />
szubsztituenseknek a reakciósebességre gyakorolt hatása<br />
Az ionos jelleget ÉS az intermedier szerkezetét bizonyítja: Francis-kísérlet (1925)<br />
Különböző halogenidionok kompetíciója miatt termékelegy!<br />
1.<strong>2.</strong> További, „nemklasszikus kation” intermedieren keresztül végbemenő addíciók<br />
Oximerkurálás<br />
OH<br />
1. Hg(OAc) 2 /THF-H 2 O<br />
R<br />
<strong>2.</strong> NaBH 4 /OH<br />
Lehetőség alkoholok előállítására alkénekből, savérzékeny R csoportok esetén is<br />
alkalmazható<br />
Eltérő rendűségű pilérszeneket tartalmazó alkének körében regioszelektív, a nagyobb<br />
rendűségű alkohol képződik!<br />
Hipohalogénessav addíció<br />
R<br />
R<br />
HOHlg/H<br />
R<br />
OH<br />
<br />
Hlg HO Hlg<br />
Támadó elektrofil: Hlg<br />
Eltérő rendűségű pillérszeneket tartalmazó alkének körében regioszelektív, a<br />
hidroxilcsoport a magasabb rendű szénre kerül
<strong>Alkének</strong> kémiai sajátságai 4.<br />
1.3. HX addíció<br />
Indítólépés: kisméretű elektrofil támadása klasszikus karbéniumion képződik. A<br />
nukleofiltől függően változatos termékek<br />
Savkatalizált vízaddíció, klasszikus alkénből kiinduló alkoholszintézis<br />
Regioszelektivitás (orientáció) eltérő rendűségű pillérszeneket tartalmazó nemszimmetrikus<br />
alkének addíciójánál<br />
Elvileg két termék, gyakorlatban az egyik dominál<br />
HBr<br />
Br<br />
H<br />
+<br />
H<br />
Br<br />
2-metilpropén<br />
2-bróm-2-metilpropán<br />
99%<br />
1-bróm-2-metilpropán<br />
1%
<strong>Alkének</strong> kémiai sajátságai 5.<br />
Regioszelektivitás értelmezése<br />
Felhasznált fogalmak:<br />
Kompetitív reakciók, Hammond elv,<br />
karbokationok stabilitási sora (3 o > 2 o > 1 o )<br />
Markovnyikov-szabály: a HX addíció kitüntetetten<br />
a stabilabb kationon keresztül megy végbe<br />
Energiaprofil<br />
G<br />
‡ 1<br />
‡ 2<br />
‡ 3<br />
‡ 4<br />
H 3 C H C CH 3<br />
H 3 C CH 2 CH 2<br />
CH 3 CHHlgCH 3<br />
CH 3 CH=CH 2<br />
+ HHlg<br />
CH 3 CH 2 CH 2 Hlg
<strong>Alkének</strong> kémiai sajátságai 6.<br />
1.4 Kationos polimerizáció<br />
Indító HX (vagy Lewis-sav) csak katalitikus mennyiségben kevés X miatt nukleofilként<br />
egy alkén -elektronpárja támad („menekülési útvonal”) láncnövekedés<br />
Etén esetén kis gyakorlati jelentőség, elektronküldő R csoportoknál gyakori!<br />
1.5. Hidroborálás<br />
R<br />
1. BH 3 /THF<br />
<strong>2.</strong> H 2 O 2 /:OH<br />
R<br />
OH<br />
Eltérő rendűségű pillérszeneket tartalmazó alkének körében regioszelektív, az alacsonyabb<br />
rendűségű alkohol képződik! Lehetőség a korábbi két alkoholszintézis izomer termékei<br />
előállítására.<br />
A Markovnyikov-orientáció csak látszólag sérül, más az elektrofil species
<strong>Alkének</strong> kémiai sajátságai 7.<br />
<strong>2.</strong> <strong>Alkének</strong> gyökös addíciója (Ad R )<br />
Általános séma<br />
Az indító •X újratermelődik<br />
láncreakció<br />
C C<br />
X<br />
X<br />
C C<br />
Y X<br />
Y X<br />
C C<br />
+ X<br />
De! a láncindító •X eredete az adott reakciótól és a körülményektől függ<br />
<strong>2.</strong>1. Halogénezés – gázfázisban (magas hőmérsékleten vagy UV fény jelenlétében)<br />
Hlg Hlg h vagy T 2 Hlg<br />
C C<br />
Hlg<br />
Hlg<br />
C C<br />
Hlg<br />
Hlg<br />
Hlg Hlg<br />
C C<br />
+ Hlg<br />
Hlg = Cl, Br<br />
Gyakorlati felhasználás: Hlg = Cl, Br<br />
Hlg F Cl Br I<br />
H (kJ/mól) -544 -178 -95 +16<br />
<strong>2.</strong><strong>2.</strong> Gyökös HX addíció (X = Br, I, apoláros oldószerekben)!
<strong>Alkének</strong> kémiai sajátságai 8.<br />
Regioszelektivitás (orientáció) eltérő rendűségű pillérszeneket hordozó nemszimmetrikus<br />
alkének Ad R addíciójánál – elvileg két termék, gyakorlatban az egyik dominál<br />
HBr<br />
peroxidok<br />
túlnyomórészt (kizárólag) anti-Markovnyikov<br />
orientációjú termék<br />
A regioszelektivitás értelmezésénél felhasznált<br />
fogalmak (itt is…):<br />
kompetitív reakciók, Hammond elv, gyökök<br />
stabilitási sora (3 o > 2 o > 1 o )<br />
A fordított regioszelektivitás oka: más a támadó<br />
elektronhiányos részecske!<br />
H<br />
Br<br />
Br<br />
H<br />
G<br />
‡ 1<br />
‡ 2<br />
‡ 3<br />
‡ 4<br />
H 3 C H C CH 2<br />
Hlg<br />
H 3 C H C CH 2<br />
Hlg<br />
CH 3 CH=CH 2<br />
+ HHlg<br />
CH 3 CH 2 CH 2 Hlg CH 3 CHHlgCH 3
<strong>Alkének</strong> kémiai sajátságai 9.<br />
<strong>2.</strong>3. Gyökös polimerizáció<br />
R<br />
gyökös iniciálás<br />
R<br />
R<br />
R<br />
Értelmezés:<br />
n<br />
Elemi lépések:<br />
Tipikus iniciátorok – peroxidok<br />
Jelentőség: az iparban leggyakrabban alkalmazott polimerizációs eljárás<br />
R = H (polietilén), Cl (PVC), OAc (polivinilacetát, polivinilalkoholok alapanyaga; lakk és<br />
festékipar), COOQ (poliakrilátok)<br />
Létezik anionos polimerizáció is (erősen elektronszívó R esetén)
<strong>Alkének</strong> kémiai sajátságai 10.<br />
3. <strong>Alkének</strong> katalitikus hidrogénezése<br />
H 2 / Pd-C vagy Pt<br />
vagy PtO 2 vagy Raney-Ni<br />
Me<br />
Me<br />
Me Me<br />
H 2 /kat.<br />
H<br />
H<br />
1,2-cisz-1,2-dimetilciklohexán<br />
Kemiszorpció a katalizátor felületen -kötés és H-H kötés fellazulása<br />
Általában cisz-addíció – magyarázat: „négycentrumos” modell<br />
4. <strong>Alkének</strong> oxidációs reakciói<br />
4.1 Csak -kötés hasadással járó folyamatok<br />
4.1.1. Hidroxilezés (hidroxilálás)<br />
R<br />
R 1 KMnO 4<br />
pH= 7, RT<br />
RT = "room temperature"<br />
OH<br />
R 1<br />
R<br />
OH<br />
vicinális diol<br />
KMnO 4<br />
pH= 7, RT<br />
OH<br />
OH<br />
1,2-cisz-diol<br />
Sztereoszelektív cisz-addíció<br />
Alkalmas kettős kötés kimutatására (Baeyer-próba)
<strong>Alkének</strong> kémiai sajátságai 11.<br />
4.1.<strong>2.</strong> Epoxidálás<br />
Alapja: -kötés elektrongazdag centrum jellege <br />
lehetőség elektronban szegény oxigénnel való<br />
támadásra.<br />
Tipikus epoxidálószerek: peroxikarbonsavak<br />
Iparban: O 2 /Ag<br />
C C<br />
<br />
O<br />
H O<br />
O<br />
R<br />
O<br />
C C<br />
Gyakorlati jelentőség: az epoxidok értékes<br />
intermedierek, lehetőség nukleofilekkel gyűrűnyitásra<br />
O<br />
C C<br />
H Nu<br />
HO<br />
C C<br />
Nu<br />
4.<strong>2.</strong> + kötés felhasadásával (lánchasadással) járó oxidációs reakciók<br />
R<br />
R 1<br />
KMnO 4<br />
H vagy <br />
R<br />
O<br />
OH<br />
+<br />
HO<br />
O<br />
R 1<br />
COOH<br />
COOH<br />
adipinsav<br />
Gyakorlati jelentőség: speciális szerkezetű alkének esetében vagy nagy szénatomszámú<br />
zsírsavkeverékek előállításában<br />
5. Allil-helyzetű szubsztitúció<br />
Magas hőmérsékleten (> 350 o C), gázfázisban Cl 2 (Br 2 ) jelenlétében nem addíció megy végbe!<br />
C C<br />
C<br />
H<br />
allil helyzet<br />
H 2 C CH CH 2<br />
allil csoport<br />
H 2 C CH CH 3<br />
Cl 2<br />
350-500 o C<br />
H 2 C CH CH 2 Cl
<strong>Alkének</strong> kémiai sajátságai 1<strong>2.</strong><br />
H 2 C CH CH 3<br />
Cl<br />
-HCl<br />
Gyökös mechanizmusú láncreakció (S R )<br />
Cl 2<br />
H 2 C CH CH 2<br />
H 2 C CH CH 2 Cl + Cl<br />
A szubsztitúció addícióval szembeni kedvezményezettségének oka: a magas hőmérséklet<br />
miatt az entrópiatényező fontossá válik, túlkompenzálja az entalpiatényezőt<br />
Addíció<br />
Szubsztitúció<br />
T ( o C) G o (kJ/mól) Termékarány G o (kJ/mól)<br />
227 -118 74 26 -116<br />
327 -105 22 78 -116<br />
527 -182 1 99 -118<br />
A mólszámcsökkenéssel<br />
járó addíció entrópia<br />
oldalról kedvezőtlen!<br />
DE!<br />
Cl<br />
Cl 2<br />
Cl 2<br />
Cl<br />
Az allil helyzet kitüntetettségének oka – allil gyök szerkezete, extra stabilitása<br />
E<br />
<br />
<br />
A gyökös centrum is sp 2 hibridállapotú lehetőség a 3 p z<br />
orbitál oldalirányú átlapolására, tricentrumos MO kialakítására<br />
elektrondelokalizáció (energianyereség)<br />
Szemléltetés határszerkezeti formákkal:<br />
<br />
H 2 C CH CH 2 CH 2<br />
H 2 C<br />
CH
Diének <strong>kötésrendszere</strong><br />
Izolált diének – szeparált + kötések, nincsen lehetőség kölcsönhatásra<br />
Kumulált diének – 2 C(sp 2 ) + C(sp) speciális geometria, egymásra<br />
merőleges -kötések a -kötések között nincsen kölcsönhatás, de<br />
a szenek körül nagy az elektronsűrűség erős rövid kötések, de<br />
nagy energiájú, destabilizált molekula<br />
C C C<br />
0.134 nm<br />
H 2 C CH 2<br />
0.131 nm<br />
H 2 C C CH 2<br />
H 2 C C C CH 2<br />
0.128 nm<br />
Következmény: nagy reaktivitás,<br />
fokozott addíciós készség, hajlam az<br />
átrendeződésre<br />
Konjugált diének – lehetőség a 4 p z orbitál oldalirányú átlapolására, négycentrumos MO<br />
kialakítására konjugálódó -kötések, elektrondelokalizáció (energianyereség)<br />
E<br />
<br />
<br />
megnyúló, gyengülő kettőskötések<br />
(kötésrend < 2), erősödő, rövidülő<br />
egyes kötések (kötésrend >1)<br />
0.136 nm<br />
0.147 nm<br />
<br />
<br />
Szemléltetés határszerkezeti formákkal:<br />
ld. még „kémiai kötés” fejezet<br />
H 3 C C<br />
H<br />
C<br />
H<br />
CH 2<br />
H 2 C C<br />
H<br />
C<br />
H<br />
CH 2 H 2 C C<br />
H<br />
C<br />
H<br />
CH 2
Konjugált diének legfontosabb reakciói<br />
Az egyszerű alkénekhez képest fokozott reakciókészség, könnyebb (gyorsabb) addíciók.<br />
Ok: elektrofil támadáskor allil-típusú stabil kationok képződnek.<br />
Teljes addíciók<br />
Br<br />
Br<br />
2 ekv. Br 2 2 ekv. HBr<br />
H<br />
Br<br />
Br<br />
Br<br />
Br<br />
H<br />
Részleges addíciók – csak egy<br />
ekvivalensnyi reagens addicionálódik<br />
Az 1,2- és 1,4-termék megjelenésének értelmezése<br />
E E E<br />
Br<br />
:Nu<br />
:Nu<br />
E<br />
E<br />
Br<br />
Br<br />
Nu<br />
1,2-termék<br />
Nu<br />
1,4-termék
Konjugált diének legfontosabb reakciói <strong>2.</strong><br />
Az 1,2-/1,4-addíció aránya<br />
H<br />
H<br />
a reakcióhőmérséklet emelkedésével egyre<br />
inkább az 1,4-addíció válik dominálóvá<br />
HBr<br />
Br<br />
+<br />
90% 10%<br />
Br<br />
Értelmezés: kinetikai kontra termodinamikai<br />
kontroll<br />
az 1,4-addukt diszubsztituált etén stabilabb<br />
az 1,2-addukthoz tartozó intermedier kation<br />
alacsonyabb energiájú<br />
Br 2<br />
Br<br />
Br<br />
+<br />
Br<br />
54% 46%<br />
Br<br />
G<br />
kinetikai kontroll<br />
termodinamikai kontroll<br />
‡ 1<br />
‡ 2<br />
<br />
H<br />
H<br />
H<br />
H<br />
H<br />
Br<br />
Br
Konjugált diének legfontosabb reakciói 3.<br />
Konjugált diének polimerizációs reakciói<br />
Gyakorlati jelentőség: gumi és műgumi gyártás – általában gyökös mechanizmus<br />
Buta-1,3-dién és 2-klórbuta-1,3-dién hasonlóan polimerizálható
Konjugált diének legfontosabb reakciói 4.<br />
Konjugált diének Diels-Alder-reakciója (1928, Nobel-díj: 1950)<br />
+<br />
X<br />
X<br />
X<br />
dién<br />
Y<br />
dienofil<br />
Y<br />
Y<br />
Diels<br />
Alder<br />
ún. periciklusos reakció (egyetlen TS, elektronok egyidejű vándorlása zárt gyűrűben)<br />
gyors reakció, ha X, Y elektronszívó csoport<br />
Néhány gyakori dienofil<br />
Sztereokémiailag kötött reakció<br />
egyidejű kötésképződés, az exo- és endotermékek<br />
közül az endo képződése<br />
kedvezményezett
<strong>Alkének</strong> előállítása<br />
1. 1,2-elimináció (-elimináció)<br />
Feltétel: X = jó távozó csoport, pl. Hlg, OH + H , NR 3<br />
1.1 Alkilhalogenidek bázis-indukált eliminációja<br />
H<br />
R 4<br />
R 4<br />
H<br />
R 4<br />
R R 1 2 X<br />
R3 - HX<br />
R 1 R 3<br />
R 1 R 3 Leggyakoribb bázisok: alkálihidroxidok (Na/KOH),<br />
R 2<br />
R 4<br />
R R 1 2 Hlg<br />
R3 - HHlg<br />
R 2<br />
alkoholok fémsói (tBuOK), tercier aminok (Et 3 N)<br />
Nemszimmetrikus kiindulási vegyület esetében a két lehetséges termék közül a több<br />
alkilcsoportot tartalmazó (termodinamikailag stabilabb) alkén képződése kedvezményezett.<br />
Zajcev-szabály<br />
Br<br />
1.2 Alkoholok savkatalizált dehidratációja<br />
Dehidratáló reagensek: cc. H 2 SO 4 , KHSO 4 , H 3 PO 4 , AlCl 3 ,<br />
ZnCl 2 , Al 2 O 3 /<br />
Jellemzően Zajcev termékek keletkeznek<br />
H<br />
R 4<br />
H /<br />
R R 1 2 OH<br />
R3 - H 2 O<br />
R 1 R 3<br />
R 2<br />
R 4<br />
<strong>2.</strong> 1,2-Dihalogénalkánok dehalogénezése<br />
Reagensek:<br />
• Zn(Mg)/ROH/<br />
• „soft” nukleofilek (I , SH , S 2 , stb.)<br />
Hlg<br />
R 1 R4<br />
R R 2 Hlg<br />
- Hlg 2 R 3<br />
R 4<br />
R 2
<strong>Alkének</strong> előállítása <strong>2.</strong><br />
3. Alkinek parciális redukciója<br />
R 1 R 2<br />
H<br />
H<br />
H 2<br />
mérgezett<br />
katalizátor<br />
R 1 R 2<br />
Na, Li, Ca<br />
csf. NH 3<br />
R 1 R 2<br />
H<br />
H<br />
4. Wittig-reakció<br />
ilid = Wittig<br />
reagens<br />
ilid generálás: RR’CHHlg +<br />
PPh 3 majd bázis<br />
Nobel-díj: 1979<br />
A legnagyobb teljesítőképességű alkénszintézis, alifás és aromás aldehidek és ketonok<br />
egyaránt reagálnak.<br />
Iparilag fontos diének előállítása<br />
1. Katalitikus dehidrogénezés<br />
Cr 2 O 3 /Al 2 O 3<br />
550-650 o C<br />
<strong>2.</strong> Etanol dehidratációja és dimerizációja<br />
Al 2 O 3 /ZnO<br />
OH + HO<br />
400-500 o C<br />
Cr 2 O 3 /Al 2 O 3<br />
550-650 o C<br />
izoprén<br />
Alapanyag: erjesztéses vagy petrolkémiai úton nyert etanol
<strong>Alkének</strong> előállítása 3.<br />
3. Acetilén-bázisú izopréngyártás<br />
O + HC CH<br />
KOH<br />
csf. NH 3<br />
OH<br />
H 2<br />
kat.<br />
OH<br />
Al 2 O 3<br />
200-300 o C<br />
Hasonló elven működő eljárást korábban butadiénre is kifejleszettek, de ma gazdaságtalan<br />
Megjegyzés: acetilén-bázisú eljárások a XX. szd. első felében széles körben elterjedtek<br />
voltak (C → CaC 2 → HC≡CH) (vö. szénbázisú szerves alapanyaggyártás ↔ petrolkémia)