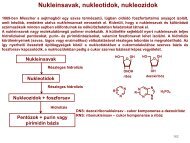
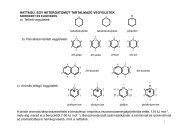
Nukleofil elimináció 2. - Szerves Kémiai Tanszék
Nukleofil elimináció 2. - Szerves Kémiai Tanszék
Nukleofil elimináció 2. - Szerves Kémiai Tanszék
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Szerves</strong> Kémia 1. (TKBE0301)<br />
előadási ábraanyag<br />
(4. rész)<br />
Patonay Tamás
Szénhidrogének halogénszármazékainak<br />
kötésrendszere, fizikai tulajdonságaik. A C-Hlg<br />
kötés erősségét befolyásoló tényezők, kapcsolatuk<br />
a reakciókészséggel. Csökkent, normál és fokozott<br />
reakciókészségű halogenidek. <strong>Nukleofil</strong><br />
szubsztitúció és alapmechanizmusai (S N 1 és S N 2),<br />
alkalmazásuk. <strong>Nukleofil</strong> szubsztitúciót befolyásoló<br />
tényezők. Eliminációs reakciók, - és -<strong>elimináció</strong>,<br />
-<strong>elimináció</strong> alapmechanizmusai (E1, E2 és E1cB).<br />
Szubsztitúció és <strong>elimináció</strong> részesedésének<br />
befolyásolása. Halogénvegyületek reakciója<br />
fémekkel. Alifás és aromás halogénvegyületek<br />
előállítása.
C-Hlg kötésű vegyületek csoportosítása<br />
- a halogén minősége szerint<br />
- a halogének száma szerint<br />
dihalogenidek esetében:<br />
C<br />
Hlg Hlg<br />
geminális<br />
- a szénhidrogén váz jellege szerint: • alifás (telített, telítetlen)<br />
• aromás<br />
- a halogént hordozó szén pillératom rendűsége szerint<br />
Hlg<br />
C C<br />
Hlg<br />
vicinális<br />
Kiemelt fontosságú az - és a -szénatom hibridállapota reaktivitás<br />
Hlg<br />
(C) n<br />
diszjunkt<br />
Hlg<br />
n 1<br />
C<br />
C<br />
C<br />
C Hlg C Hlg C Hlg<br />
H<br />
C<br />
C<br />
H<br />
H<br />
C<br />
primer szekunder tercier<br />
Hlg Ar Hlg<br />
vinil-halogenid<br />
aril-halogenid<br />
Hlg<br />
allil-halogenid<br />
Ar<br />
Hlg<br />
benzil-halogenid<br />
Ar<br />
(C) n<br />
Hlg<br />
aralkil-halogenid<br />
n 2<br />
Elnevezésük<br />
• triviális nevek: pl. kloroform, jodoform, fluotan<br />
• szubsztitúciós nomenklatúra – halogén megnevezése csak előtagként!<br />
• csoportfunkciós nomenklatúra: szénhidrogén csoport + halogenid (fluorid, klorid, bromid,<br />
jodid) utótag – feltéve, hogy nincsen magasabb prioritású funkciós csoport<br />
Cl<br />
2-klórpentán<br />
(1-metilbutil)-klorid<br />
F<br />
fluorciklohexán<br />
ciklohexil-fluorid<br />
Br<br />
1-brómbut-2-én<br />
(but-2-en-1-il)-bromid<br />
CH 2 Cl 2<br />
diklórmetán<br />
metilén-klorid
övidülő kötéstáv<br />
C-Hlg kötésű vegyületek kötésrendszere<br />
Tipikusan EN(Hlg) > EN(C) polarizált<br />
heteronukleáris -kötés, parciális pozitív töltés a<br />
szénatomon (-I effektus)<br />
De! ha a pillérszénatom hibridállapota sp 2 vagy<br />
sp +M effektus is fellép. Következmény:<br />
rövidülő, erősödő kötések, növekvő kötésrend<br />
C-Hlg kötéstáv függ: halogén minősége, szénatom hibridállapota<br />
d C-Hlg<br />
(nm)<br />
F Cl Br I<br />
C<br />
C Hlg<br />
C Hlg<br />
- I effektus +M effektus<br />
C<br />
C Hlg<br />
C Hlg<br />
0.139 0.178 0.195 0.214<br />
C Hlg<br />
0.133 0.172 0.188 0.210<br />
növekvő kötéstáv<br />
C-Hlg kötési energia függ: halogén minősége, szénatom hibridállapota<br />
Átlagos C-Hlg kötési energiák<br />
(kJ/mól)<br />
C-F 488<br />
C-Cl 326<br />
C-Br 278<br />
C-I 210 (becsült)<br />
Ok: gyengébb átfedés,<br />
kisebb töltésszétválás<br />
C-Hlg disszociációenergia (kJ/mól)<br />
Homolitikus<br />
Heterolitikus<br />
F Br F Br<br />
MeCH 2<br />
-Hlg 448 282 920 770<br />
PhCH 2<br />
Hlg 403 229 820 657<br />
CH 2<br />
=CH-Hlg 497 320 1004 837
C-Hlg kötésű vegyületek kötésrendszere <strong>2.</strong><br />
Látható tendenciák:<br />
1. aril/vinil-halogenidek erősődő kötése (vö. +M effektus)<br />
<strong>2.</strong> allil/benzil-halogenidek gyengülő kötése – a kötéshasadás során képződő gyök/kation<br />
nagyobb stabilitása, alacsonyabb energiaállapota már itt is érződik<br />
3. homolitikus kötéshasadás kisebb energiát igényel<br />
DE!! Ez gázfázisra igaz, oldatokban a szolvatációs energia felülírhatja<br />
Várható következmény:<br />
• aril/vinil-halogenidek reakciókészsége kisebb az egyszerű alkil-halogenidekénél<br />
• allil/benzil-halogenidek reakciókészsége nagyobb az egyszerű alkil-halogenidekénél<br />
Alapállapotú kötéspolarizáció következménye: dipólusmomentum megjelenése<br />
Me-F: 1.81 D Me-Cl: 1.87 D Me-Br: 1.80 D<br />
A tényleges dipólusmomentumot két tényező alakítja ki: töltésszétválás értéke (EN<br />
különbség) és a kötéshossz<br />
DE! elemi dipólusmomentumok vektorjellegéből<br />
Következően az eredő lehet nulla is!<br />
Mért dipólusmomentumok sajátos menete<br />
CH 3<br />
-Br CH 3<br />
CH 2<br />
-Br CH 3<br />
CH 2<br />
CH 2<br />
-Br<br />
[D] 1.80 1.88 1.92<br />
Cl<br />
Cl<br />
C<br />
Cl<br />
Cl<br />
Cl<br />
" <br />
C C Hlg<br />
C C<br />
"'<br />
'<br />
H<br />
C C<br />
H<br />
Cl<br />
= 0<br />
<br />
C<br />
<br />
Hlg<br />
Ok: töltésszétválás végigvonul a láncon.<br />
Fontos tanúság a későbbiekre nézve: elektronszívó csoportok nemcsak az -, hanem<br />
csökkenő mértékben a - és a -szénatom körül is csökkentik az elektronsűrűséget!!
C-Hlg kötésű vegyületek fizikai sajátságai<br />
Olvadáspont és forráspont – a halmazt összetartó erők: dipól-dipól kölcsönhatások<br />
Emiatt op, fp nagyobb, mint az azonos szénatomszámú alkánok, alkének esetében<br />
R-Hlg forráspont ( o C) R-H ( o C)<br />
Hlg F Cl Br<br />
Me-Hlg -78 -24 4 -162<br />
Et-Hlg -32 12 38 -89<br />
Bu-Hlg 32 79 102 -1<br />
Forráspont nő:<br />
• halogén minőségének változásával<br />
(F I sorban)<br />
• szénatomszám növekedésével<br />
• halogénszám növekedésével<br />
Sűrűség – nő a F I sorban, a halogénszám növekedéssel, de csökken a szénlánc<br />
méretének növekedésével<br />
d(Me-F) = 0.877 g/cm 3 , d(Pr-F) = 0.779 g/cm 3<br />
d(Me-F) = 0.877 g/cm 3 , d(Me-Br) = 1.732 g/cm 3<br />
d(Me-Cl) = 0.991 g/cm 3 , d(CHCl 3 ) = 1.489 g/cm 3 (de! d(CHBr 3 ) = <strong>2.</strong>890 g/cm 3<br />
Oldékonyság<br />
Jellemző: kis vízoldékonyság (vö. H-hidak erősebbek, mint a dipól-dipól kölcsönhatások).<br />
Kiválóan oldják a kevésbé poláros szerves anyagokat, zsírokat.<br />
jó extrahálószerek<br />
jó tisztítószerek<br />
biológiai lipid-lipid rendszerek módosítása, jó narkotizáló hatás (pl. fluotan:<br />
CHClBr-CF 3 )
C-Hlg kötésű vegyületek kémiai sajátságai<br />
A kötésrendszerből közvetlenül levezethető reakciók:<br />
1. <strong>Nukleofil</strong> szubsztitúció (S N )<br />
<strong>2.</strong> <strong>Nukleofil</strong> <strong>elimináció</strong> (E N )<br />
További reakciók:<br />
3. -<strong>elimináció</strong><br />
4. Reakció fémekkel<br />
5. Reduktív dehalogénezés<br />
1. <strong>Nukleofil</strong> szubsztitúció (alifás szénatomon)<br />
Általánosan:<br />
Jelen esetben:<br />
A B + :C :A + B C<br />
Hlg R + :Nu :Hlg + R Nu
<strong>Nukleofil</strong> szubsztitúció <strong>2.</strong><br />
Reakció O-nukleofilekkel<br />
:OR 1<br />
:OH<br />
R OR 1 R Hlg<br />
R<br />
éter<br />
OH/<br />
H 2 O/<br />
alkoholízis<br />
hidrolízis<br />
R 1 COO: R 1 COOH/<br />
R OCOR 1<br />
karbonsavészter<br />
R OH<br />
alkohol<br />
észterhasítás<br />
(észterhidrolízis)<br />
R Hlg :OR1 R OR 1<br />
Williamson-féle éterszintézis<br />
Megjegyzés: a karbonsavészteren<br />
keresztülhaladó kétlépéses alkohol<br />
előállítás preparatív szempontból<br />
gyakran előnyösebb (konkurens<br />
<strong>elimináció</strong> hiánya!)<br />
Szolvolízis: az S N folyamatban az oldószer szerepel nukleofilként (gyengébb nukleofil, de<br />
nagy feleslegben!)<br />
Reakció S-nukleofilekkel<br />
tioéter<br />
:SR 1<br />
R SR 1 R 1 COS:<br />
:SH<br />
R Hlg<br />
R Hlg R SH<br />
tioalkohol (tiol)<br />
R<br />
S R<br />
szekunder reakció<br />
elõnytelen!<br />
R SCOR 1<br />
karbonsavtiolészter<br />
észterhasítás<br />
(észterhidrolízis)<br />
R Hlg<br />
:SCN<br />
R S C N<br />
tiocianát<br />
R N C S<br />
izotiocianát
<strong>Nukleofil</strong> szubsztitúció 3.<br />
Reakció N-nukleofilekkel<br />
R Hlg<br />
R 1 R 2 NH<br />
R NHR 1 R 2<br />
ammonolízis<br />
Hlg:<br />
:B<br />
R N<br />
R 1<br />
R 2<br />
amin<br />
A bázis (:B) lehet az amin reagens<br />
feleslege is.<br />
Szintetikusan kevésbé alkalmazható reakció, keveréktermék képződése (ld. később)<br />
O<br />
R Hlg<br />
N:<br />
O<br />
K<br />
O<br />
N<br />
O<br />
O<br />
R R NH 2 + NH<br />
primer amin<br />
O<br />
Gabriel-szintézis<br />
Reakció C-nukleofilekkel<br />
R Hlg<br />
:CN<br />
R C N<br />
nitril (alkilcianid)<br />
R N=C:<br />
izonitril<br />
R 1 C C:<br />
R 1 C C R<br />
R Hlg<br />
C-C kötés létrehozás!! Jelentőség:<br />
Újabb példa az ambidens nukleofilre, a termékarány erősen függ<br />
a reakciókörülményektől (Kornblum)<br />
Z 1<br />
HCZ 2 Z 1<br />
R<br />
CH<br />
Z 2<br />
Z 1 ,Z 2 = elektronszívó, rezonanciastabilizációra<br />
képes csoport (ld.<br />
később – malonészter-, acetecetészterszintézis)<br />
lánchosszabbítás, szénlánc kiépítése
<strong>Nukleofil</strong> szubsztitúció 4.<br />
Reakció Hlg-nukleofilekkel<br />
Alapreakció:<br />
R Hlg + :Hlg 1<br />
R Hlg 1 + :Hlg<br />
Probléma: hasonló reaktivitás, hasonló nukleofilicitás egyensúlyi reakció, keverék.<br />
Csekély szintetikus jelentőség.<br />
Gyakorlati alkalmazhatóság kritériuma: irreverzibilitás (oldékonysági tényezők segítsége)<br />
Oldható!<br />
R Cl(Br)<br />
Ag-F<br />
R F + Ag-Cl(Br)<br />
Oldhatatlan!<br />
Oldható!<br />
R Cl(Br)<br />
K-I<br />
Me 2 CO/<br />
R<br />
I + K-Cl(Br)<br />
Oldhatatlan!<br />
Finkelstein-reakció<br />
Alifás (sp 3 ) szénatomon lejátszódó nukleofil reakciók mechanizmusai<br />
1. S N 2 mechanizmus<br />
R<br />
R 1<br />
R 2<br />
C Hlg<br />
:Nu<br />
Nu<br />
R 1<br />
R<br />
C<br />
R 2<br />
Hlg<br />
sp 2 -szerű szénatom<br />
Másodrendű kinetika: r = d[R-Hlg]/dt = k [R-Hlg] [Nu]<br />
Bimolekulás folyamat<br />
Koncertikus (szinkron) folyamat (egyidejű kötéshasadás<br />
és képződés!<br />
Nu<br />
C<br />
R<br />
R 2R1<br />
MeI + MeSH<br />
Me 2 S + HI
<strong>Nukleofil</strong> szubsztitúció 5.<br />
R<br />
R 1<br />
R 2<br />
C Hlg<br />
:Nu<br />
Nu<br />
R<br />
C<br />
R 1 R 2<br />
Hlg<br />
Nu<br />
C<br />
R<br />
R 2R1<br />
Egyetlen átmeneti állapot! Következmény:<br />
sztereokémiailag kötött folyamat<br />
Hátoldali támadás Királis, nem-racém szubsztrátoknál<br />
a konfiguráció ellentétesre változik (Walden-inverzió)<br />
<strong>2.</strong> S N 1 mechanizmus<br />
R Hlg<br />
- :Hlg<br />
lassú,<br />
sebességmeghatározó<br />
R<br />
karbokation<br />
(karbéniumion)<br />
intermedier<br />
:Nu<br />
R Nu<br />
gyors lépés<br />
Elsőrendű kinetika: r = d[R-Hlg]/dt = k [R-Hlg]<br />
monomolekulás folyamat<br />
kétlépéses folyamat
<strong>Nukleofil</strong> szubsztitúció 6.<br />
S N 1 reakció sztereokémiája<br />
A nukleofil szubsztitúciót befolyásoló tényezők – „mindenki, aki arra jár…”<br />
Hlg R + :Nu :Hlg + R Nu<br />
oldószer<br />
hõmérséklet<br />
1. Távozó csoport (halogén minősége) - I > Br > Cl > F<br />
<strong>2.</strong> Alkil (R) csoport jellege<br />
3. <strong>Nukleofil</strong>icitás (nukleofil erő)<br />
4. Oldószerhatás<br />
5. Elektrofil katalízis (Ag ionok reakciómechanizmust módosító hatása)<br />
6. Szomszédcsoport hatás (a távozócsoporthoz képest -helyzetű szubsztituens<br />
részvétele a reakcióban)
<strong>Nukleofil</strong> szubsztitúció 7.<br />
Alkil csoport szerkezetének szerepe a mechanizmusban<br />
S R<br />
R<br />
N 2 R S N 1<br />
:Nu<br />
C Hlg<br />
Nu C Hlg Nu C<br />
R 1<br />
R Hlg - :Hlg R<br />
R 2R1<br />
R 2<br />
R 1<br />
R 2<br />
:Nu<br />
R<br />
Nu<br />
Lehetséges kiindulási pont: kötési energiák, disszociációs energiák (ld. korábban)<br />
S N 1 mechanizmusnak kedvez: alkilkation (karbéniumion) növekvő stabilitása<br />
a kationt stabilizáló tényezők (elektronküldés, mezomeriastabilizált rendszerek) S N 1<br />
mechanizmus érvényesülését eredményezik 3 0 szénatomot tartalmazó szubsztrát,<br />
benzil, allil rendszerek<br />
R Br<br />
EtOH<br />
<br />
R OEt<br />
R Me MeCH 2 Me 2 CH Me 3 C CH 2 =CH-CH 2 PhCH 2<br />
k rel 1 1.7 45 10 8 4x10 6 4x10 6<br />
S N 2 mechanizmusnak kedvez: könnyebb hátoldali támadás, kisebb sztérikus gátlás (kisebb<br />
méretű nukleofil, alacsonyabb rendű szénatom<br />
:Nu<br />
R<br />
R 1<br />
R 2<br />
C Hlg<br />
R Br<br />
KI<br />
Me 2 CO/RT R OEt<br />
R Me MeCH 2 Me 2 CH ciklohexil<br />
k rel 1 1.25x10 -2 10 -4 5x10 -6<br />
-szénatom<br />
szubsztituáltságának<br />
hatása<br />
R Me MeCH 2 MeCH 2 CH 2 Me 2 CHCH 2 Me 3 CCH 2<br />
k rel 1 6x10 -1 2x10 -2 2x10 -3 2x10 -4
<strong>Nukleofil</strong> <strong>elimináció</strong><br />
Alap: szénláncon<br />
végigvonuló polarizáció,<br />
savas -hidrogén<br />
Következmény: <strong>elimináció</strong> a szubsztitúció konkurens folyamata, a kötéshasadások/<br />
kötésképződések (3 kötés!) időrendisége alapján három lehetséges mechanizmus!<br />
1. E2 mechanizmus<br />
G<br />
‡<br />
R-Hlg + Nu<br />
Jellemző: teljesen szinkron folyamat, egyetlen TS,<br />
folytonos elektronátmenet, a szénatomokon nincsen<br />
számottevő töltés.<br />
Másodrendű kinetika, bimolekulás reakció<br />
r = - d[RHlg]dt = k[RHlg][Nu]<br />
alkén + HNu
<strong>Nukleofil</strong> <strong>elimináció</strong> <strong>2.</strong><br />
Reakció során: 2 db sp 3 AO 2 db p z (-kötés).<br />
Minimális energiabefektetés feltétele: mindvégig<br />
maximális átfedés azonos síkban elhelyezkedő atomok<br />
(C-Hlg / C-C / C-H és Nu…H)<br />
További feltétel: atomok minimális mértékű<br />
helyváltoztatása antiperiplanáris helyzetű Hlg és H<br />
atomok kihasadása (anti-<strong>elimináció</strong>) -<br />
DIASZTEREOSZELEKTIVITÁS<br />
További szempont: <strong>elimináció</strong> nemszimmetrikus, eltérő rendűségű - és ’-<br />
szénatomokat tartalmazó alkilhalogenidekből<br />
Zajcev szabály: a hidrogén úgy hasad ki, hogy a nagyobb termodinamikai<br />
stabilitású (több alkilcsoportot hordozó) alkén keletkezik<br />
C<br />
H 2 C<br />
C<br />
CH<br />
CH<br />
C<br />
Hlg<br />
C<br />
C<br />
C<br />
C<br />
H 2 C<br />
C<br />
H<br />
C<br />
C<br />
HC<br />
C<br />
H<br />
CH<br />
C<br />
Kedvezményezett<br />
termék (Zajcevtermék)<br />
Hofmanntermék
<strong>Nukleofil</strong> <strong>elimináció</strong> 3.<br />
<strong>2.</strong> E1 mechanizmus<br />
:B<br />
C<br />
H<br />
C<br />
C<br />
C<br />
gyors lépés<br />
(protonlehasadás)<br />
Jellemző: kétlépéses folyamat, karbokation (karbéniumion) intermedier.<br />
Elsőrendű kinetika, monomolekulás folyamat<br />
r = - d[RHlg]dt = k[RHlg]<br />
C<br />
H<br />
C<br />
Hlg C C<br />
H<br />
+ Hlg:<br />
lassú,<br />
sebességmeghatározó<br />
lépés<br />
G ‡ ‡ 1<br />
‡ 2<br />
R-Hlg + Nu<br />
alkén + HNu<br />
S N 1 folyamat konkurrens reakciója, a termékarány nagyban független a távozó<br />
csoporttól és a nukleofiltől - a Zajcev szabály általában érvényesül<br />
<br />
R <br />
3. E1cB mechanizmus Jellemző: kétlépéses<br />
folyamat, karbanion<br />
intermedier.<br />
Elsőrendű kinetika,<br />
sebességmeghatározó<br />
a :Hlg kihasadás,<br />
monomolekulás<br />
folyamat
<strong>Nukleofil</strong> <strong>elimináció</strong> 4.<br />
3. -<strong>elimináció</strong> - karbénképződés<br />
Speciális, ritka<br />
reakció<br />
Karbének: elektrohiányos (elektronszextettes!) reaktív intermedierek – nukleofil partnert<br />
keresnek.<br />
4. Reakció fémekkel, reduktív dehalogénezés<br />
Halogén-fém kicserélődési reakció – SET mechanizmus („single electron transfer” - egy<br />
elektron átadás)<br />
R Hlg<br />
M<br />
- M<br />
R Hlg<br />
R R<br />
R<br />
R + M + Hlg:<br />
M<br />
R-M<br />
fémorganikus vegyület<br />
Bizonyos fémeknél (Mg, Zn)<br />
beékelődési reakció R-M-Hlg<br />
(ld. később)
Aromás halogenidek szubsztitúciós reakciói<br />
Kiindulási pont: a halogén +M effektusa miatt csökkent reakciókészség (ld. korábban).<br />
Sem S N 1, sem S N 2 nem játszódhat le! Reakció csak erőteljes körülmények között, eltérő<br />
mechanizmusok szerint.<br />
Cl<br />
NaOH<br />
300 o C<br />
OH<br />
Mechanizmusok:<br />
1. Eliminációs-addíciós mechanizmus<br />
Br<br />
NH 2<br />
Nincsen gyakorlati jelentőség<br />
NaNH 2<br />
– drága, környezetszennyező<br />
csf. NH 3<br />
<strong>2.</strong> Addíciós-<strong>elimináció</strong>s mechanizmus<br />
2,4,6-helyzetű elektronszívó<br />
ÉS rezonanciastabilizációra<br />
képes szubsztituensek<br />
jelenlétében!!<br />
Legjobb távozó csoport: F
C-Hlg kötésű vegyületek előállítása<br />
1. Alkil-halogenidek szintézise<br />
1.1. Alkánok gyökös halogénezése<br />
R H<br />
Hlg 2 /h<br />
S R<br />
R Hlg<br />
Hátrány: keveréktermék, nem irányítható! (Hlg = Cl, Br)<br />
1.<strong>2.</strong> Alkének, alkinek Hlg 2 vagy HHlg addíciója (gyökös vagy elektrofil addíciós mechanizmus<br />
szerint)<br />
Hlg<br />
Hlg Hlg<br />
R 1 R 1<br />
HHlg<br />
R<br />
R<br />
Csekély gyakorlati<br />
HHlg<br />
R 1 HC CH R<br />
R 1 jelentőség –<br />
C C R<br />
Hlg<br />
Hlg 2<br />
Hlg<br />
R 1<br />
Hlg<br />
Hlg regioszelektivitási<br />
2<br />
R<br />
R<br />
1<br />
problémák!<br />
R<br />
Hlg<br />
Hlg Hlg<br />
Reakciókészség függ a HHlg minőségétől: HI > HBr > HCl >> HF<br />
1.3. Alkoholok hidroxilcsoportjának cseréje halogénekkel<br />
R OH halogénezõszer<br />
R Hlg<br />
Tipikusan: Hlg = Cl, Br Reagensek: szervetlen<br />
savkloridok (SOHlg 2 , SO 2 Hlg 2 , POHlg 3 , PHlg 3 , PHlg 5 ),<br />
ClSO 2 OH, SF 4<br />
DE! Tercier alkoholok esetében a HHlgekkel<br />
való reakció is elegendő a<br />
cseréhez.<br />
Ok: tercier kation nagy stabilitása<br />
C<br />
C C OH<br />
C<br />
H<br />
C<br />
C C OH 2<br />
C<br />
- H 2 O<br />
C<br />
C C<br />
C<br />
Hlg:
C-Hlg kötésű vegyületek előállítása <strong>2.</strong><br />
1.4. Alkil-halogenidek egymásba alakítása<br />
R Cl(Br)<br />
Ag-F<br />
<strong>2.</strong> Benzil-halogenidek szintézise<br />
Ar<br />
Egyértelmű (nagy<br />
regioszelektivitású) reakció<br />
(ok: benzilgyök stabilitása)<br />
K-I<br />
R F + Ag-Cl(Br) R Cl(Br)<br />
R I + K-Cl(Br) ld. korábban<br />
Me 2 CO/<br />
R<br />
Hlg 2 /h<br />
Hlg<br />
S R Ar R<br />
halogénezõszer<br />
R<br />
OH<br />
Ar<br />
Megnövekedett reaktivitás (ok:<br />
benzilkation stabilitása)<br />
valamennyi korábban említett<br />
reagens használható<br />
A cc. HHlg itt is hatékony<br />
reagens, ok: benzilkation<br />
stabilitása<br />
R<br />
CH OH<br />
Ar<br />
H<br />
R<br />
CH OH 2<br />
Ar<br />
- H 2 O<br />
R<br />
CH<br />
Ar<br />
Hlg:<br />
R<br />
CH Hlg<br />
Ar<br />
Aromás vegyületek klórmetilezése<br />
Az aromás S E újabb példája, elsősorban aktiváló szubsztituens jelenlétében!
C-Hlg kötésű vegyületek előállítása 3.<br />
3. Aromás halogenidek szintézise<br />
3.1. Aromás vegyületek S E mechanizmusú halogénezése<br />
G<br />
Hlg 2 / Lewis sav<br />
S E<br />
G<br />
Hlg<br />
Problémák:<br />
1. Hlg = Cl, Br<br />
<strong>2.</strong> Irányítás, erősen elektronszívó G esetén<br />
csökkent reakciókészség<br />
3.<strong>2.</strong> Aromás diazóniumsók szubsztitúciós reakciója<br />
I<br />
NO 2<br />
N 2 X:<br />
KI/H 2 O/<br />
G<br />
Hlg<br />
Cu 2 Hlg 2<br />
Hlg = Cl, Br<br />
G<br />
G<br />
1. HBF 4<br />
<strong>2.</strong> <br />
G<br />
F<br />
Sandmeyer-reakció<br />
G<br />
Előny: aromás nitrovegyületek előállítása általában könnyű, halogén beépülésének helye<br />
egyértelmű, bármelyik halogén atom beépíthető
Fémorganikus vegyületek kémiájának alapjai.<br />
Kötésrendszerük, az „umpolung” fogalma.<br />
Karbanionok, mint bázisok és C-nukleofilek.<br />
Jelentőségük C-C kötés kiépítésében. Grignardvegyületek<br />
és alkalmazásuk. Fémorganikus<br />
vegyületek előállítása és egymásba alakítása,<br />
transzmetallálás.
Fémorganikus vegyületek kötésrendszere<br />
Fémorganikus vegyület: közvetlen szén-fém kötés<br />
(tipikusan s- és d-mező + néhány a p-mezőből)<br />
Alapvető: EN M < EN C polarizált heteronukleáris<br />
kötés, töltésfelesleg a szénatomon! A kötés<br />
kovalens/ionos jellege a fém minőségétől függ.<br />
A reaktivitás nagyjából arányos a C-M kötés<br />
polarizáltságával!<br />
<br />
R M R M R: + M<br />
Fémorganikus vegyületek =<br />
karbanion ekvivalensek!!<br />
A többi heteroatom esetében:<br />
<br />
R<br />
<br />
X<br />
A C-M kötés polarizáltsága ellentétes a többi heteronukleáris C-X kötés polarizáltságával<br />
„umpolung” (átpolarizálás)<br />
Alapvető reakciók a kötésrendszer/elektroneltolódások alapján elektrofilek,<br />
elektronhiányos reagensek támadása<br />
• proton, mint elektronhiányos részecske (fémorganikus vegyület = bázis)<br />
<br />
M<br />
R<br />
<br />
<br />
H<br />
<br />
A<br />
R H + M A<br />
általában előnytelen, elkerülendő reakció<br />
• tetszőleges elektrofil (E ) támadása C-E kötés kiépülése. Elsődleges jelentőség:<br />
reakció C elektrofilekkel C-C kötés kiépítése, szénváz kialakítás szintézisekben!!<br />
<br />
M<br />
R<br />
<br />
E Nu: R E + M Nu<br />
<br />
M<br />
R<br />
<br />
E R E + M<br />
A fémorganikus vegyületek szintetikus alkalmazása rohamosan bővül, napjaink szerves<br />
kémiája!!!
Fémorganikus vegyületekkel végzett reakciók körülményei<br />
1. Aktív hidrogénnel rendelkező reagensek,<br />
oldószerek nem jönnek számításba inert,<br />
abszolút oldószerek szükségessége, savas<br />
hidrogént nem tartalmazó szubsztrátok!!<br />
<br />
M<br />
R<br />
<br />
<br />
H<br />
<br />
A<br />
R H + M A<br />
Tipikus oldószerek: éterek (Et 2 O, THF, dioxán), (ciklo)alkánok (hexán, ciklohexán)<br />
<strong>2.</strong> Szén-dioxid, mint elektrofil inert atmoszféra<br />
(N 2 , Ar) a reakciók végrehajtása során<br />
<br />
M<br />
R<br />
<br />
<br />
O C O<br />
O:<br />
R C<br />
O<br />
M<br />
3. Oxigén, mint elektronhiányos és reaktív<br />
molekula inert atmoszféra; reaktívabb<br />
fémorganikus vegyületeknél levegőn spontán<br />
öngyulladás!)<br />
Alapállapotú (triplett) oxigén MO diagramja –<br />
biradikál szerkezet<br />
A research student in the University of California died<br />
from her injuries sustained in a laboratory fire. She<br />
was drawing tert-butyl lithium from a bottle into a<br />
syringe when the plunger came out of the syringe<br />
barrel. The chemical, which ignites spontaneously in<br />
air, splashed onto her clothes and set them on fire.<br />
She suffered 40% burns and died later in hospital of<br />
the injuries.<br />
(http://www.liv.ac.uk/safety/SAFETY_ALERT_002_tertbutyl_lithium_fatality.pdf
Grignard-vegyületek szerkezete és kémiája<br />
Előállítás: Mg beékelődése a C-Hlg kötésbe!<br />
R Hlg<br />
Mg<br />
R 1 2O<br />
R Mg Hlg<br />
DE! a Grignard-vegyület szerkezete ennél bonyolultabb!<br />
A fémorganikus vegyületek jellemző sajátsága:<br />
asszociátumok képződése – oligomerek, polimerek<br />
V. Grignard<br />
Nobel-díj: 1912<br />
"for the discovery of the so-called<br />
Grignard reagent, which in recent<br />
years has greatly advanced the<br />
progress of organic chemistry"<br />
R<br />
Mg<br />
R R R<br />
Mg Mg Mg<br />
Hlg Hlg Hlg<br />
De ez így még instabil…<br />
R 1 R 1 R 1<br />
O<br />
R 1 R R<br />
O<br />
1 O<br />
1 R 1 R<br />
O<br />
1<br />
R<br />
Mg<br />
R R R<br />
Mg Mg Mg<br />
Hlg Hlg Hlg<br />
O<br />
R 1 R 1 O<br />
R 1 R 1 R 1 O<br />
R 1<br />
R 1 O R 1<br />
Az éter típusú oldószer beépül az asszociátumba,<br />
stabilizáló hatás!<br />
<br />
R MgHlg R: + MgHlg<br />
A Grignard-vegyület karbanion ekvivalens (bázis vagy<br />
C-nukleofil)<br />
PhMgBr.2Et 2 O
Grignard-vegyületek szerkezete és kémiája <strong>2.</strong><br />
1. Grignard-vegyület, mint bázis<br />
Hlg<br />
<br />
Mg<br />
R<br />
C-H savak esetében: új fémorganikus vegyületek előállítása<br />
Példa:<br />
<br />
<br />
Hlg<br />
H<br />
<br />
Mg<br />
<br />
A<br />
R<br />
<br />
<br />
H<br />
R H + MgHlgA<br />
C<br />
Felhasználási lehetőségek:<br />
• „aktív”hidrogén meghatározás<br />
• reduktív dehalogénezés enyhe<br />
körülmények között<br />
C R 1 HlgMg C C R 1 + R H<br />
Általában azonban elkerülendő mellékreakció!!<br />
<strong>2.</strong> Grignard-vegyület, mint C-nukleofil – elsődlegesen C-elektrofilekkel szemben<br />
<strong>2.</strong>1. Reakció sp 3 szénatomot tartalmazó C-elektrofilekkel – S N reakció!!<br />
<br />
Hlg Mg R R 1<br />
Igazán hatékony C-C kötés kiépítés, csak<br />
Hlg R R 1 + MgHlg 2<br />
akkor ha R 1 = benzil, allil<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
<br />
H 2 C<br />
O<br />
R<br />
O: MgHlg H<br />
R<br />
OH<br />
etilén-oxid<br />
primer alkohol<br />
Formálisan S N (C-O kötéshasadás a Nu támadás hatására), gyakorlatilag Ad N<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
<br />
HC<br />
OEt<br />
OEt<br />
OEt<br />
- :OEt<br />
H<br />
R<br />
acetál<br />
OEt<br />
OEt<br />
H 2 O/H<br />
H<br />
O<br />
R<br />
aldehid
Grignard-vegyületek szerkezete és kémiája 3.<br />
<strong>2.</strong><strong>2.</strong> Reakció sp 2 szénatomot tartalmazó C-elektrofilekkel – Ad N reakció!!<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
R 1<br />
R 2<br />
<br />
C<br />
O<br />
O: MgHlg<br />
R<br />
H 2 O/H OH<br />
R 2 C<br />
R<br />
C<br />
R 2<br />
R 1<br />
R 1<br />
R 1 = R 2 = H (formaldehid) 1 o alkohol<br />
R 1 = alkil/aril; R 2 = H (aldehid) 2 o alkohol<br />
R 1 = R 2 = alkil/aril (keton) 3 o alkohol<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
R 1<br />
<br />
C<br />
EtO<br />
O<br />
R<br />
EtO<br />
O:<br />
C<br />
R 1<br />
- :OEt<br />
Reakcióképes intermedier<br />
Aldehidek, ketonok így NEM szintetizálhatók!<br />
R RMgHlg R<br />
OH<br />
C O<br />
C<br />
R<br />
R 1<br />
R 1<br />
szekunder vagy<br />
tercier alkohol<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
R 1<br />
<br />
C NR 3<br />
R 2<br />
NR 3 MgHlg<br />
R<br />
H 2 O/H NHR<br />
R 2 C<br />
R<br />
C<br />
R 2<br />
<strong>2.</strong>3. Reakció sp szénatomot tartalmazó C-elektrofilekkel – Ad N reakció!!<br />
R 1<br />
R 1<br />
szekunder amin<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
<br />
O C O<br />
O:<br />
R C<br />
O<br />
MgHlg<br />
H 2 O/H<br />
R COOH<br />
karbonsav
Grignard-vegyületek szerkezete és kémiája 4.<br />
<strong>2.</strong>3. Reakció sp szénatomot tartalmazó C-elektrofilekkel – Ad N reakció!!<br />
Hlg<br />
<br />
Mg<br />
R<br />
<br />
<br />
R 1 C<br />
N<br />
R 1<br />
C<br />
R<br />
H 2 O/H<br />
N: MgHlg<br />
Fémorganikus vegyületek előállítása<br />
Általában R-Hlg vegyületekből<br />
Hlg-fém csere (reduktív helyettesítés)<br />
Példák:<br />
R 1<br />
C<br />
R<br />
NH<br />
H 2O/H<br />
R 1<br />
C<br />
R<br />
O<br />
keton<br />
R Hlg + 2 M R M + M Hlg Bu Br + 2 Li Bu Li + Li Br<br />
R Hlg<br />
R 1 M + R M R 1 Hlg +<br />
Et Cl + Pb(Na) PbEt 4 + NaCl<br />
Ph Br<br />
+ Bu Li Ph Li + Bu Br<br />
BuLi<br />
Esetenként fém-fém csere (transzmetallálás)<br />
R M + M 1 R M 1 + M<br />
Me 2 Hg + 2 Na 2 MeNa + Hg<br />
M 1 mindig elektropozitívabb!<br />
Viszonylag erősebb C-H savak esetében hidrogén-fém csere (metallálás)<br />
R H<br />
+ R 1 M R M + R 1 H<br />
Ph H + Et Na Ph Na + Et H