Télécharger la version imprimée du Répertoire vétérinaire 2013
Télécharger la version imprimée du Répertoire vétérinaire 2013
Télécharger la version imprimée du Répertoire vétérinaire 2013
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
TABLE DES MATIÈRESVTABLE DES MATIÈRESAvant - propos . .............................................XVIntro<strong>du</strong>ction ................................................XVIIAdresses utiles. .............................................XIX1 Médicaments anti-infectieux ............................. 11.1 Antibactériens ............................................. 11.1.1 Antibiotiques bêta-<strong>la</strong>ctames. ................................. 31.1.1.1 Pénicillines ............................................. 3Pénicillines naturelles. ................................... 4Aminopénicillines ....................................... 5Aminopénicillines associées à un inhibiteur des bêta-<strong>la</strong>ctamases . 81.1.1.2 Céphalosporines. ....................................... 10Premier groupe: céphalosporines surtoutactives contre les GRAM+ ............................... 11Deuxième groupe: céphalosporines à spectre é<strong>la</strong>rgi. .......... 121.1.2 Aminosides ............................................. 141.1.2.1 Gentamicine ........................................... 151.1.2.2 Paromomycine ......................................... 151.1.2.3 Spectinomycine ........................................ 151.1.3 Florfénicol. .............................................. 161.1.4 Tétracyclines. ............................................ 171.1.4.1 Chlortétracycline. ....................................... 181.1.4.2 Doxycycline ........................................... 181.1.4.3 Oxytétracycline. ........................................ 201.1.5 Macrolides - Lincosamides et Pleuromutilines. .................. 211.1.5.1 Macrolides ............................................ 21Gamithromycine. ...................................... 22Tildipirosine .......................................... 22Tilmicosine ........................................... 22Tu<strong>la</strong>thromycine. ....................................... 23Tylosine ............................................. 23Tylvalosine ........................................... 241.1.5.2 Lincosamides .......................................... 24Clindamycine ......................................... 25Lincomycine. ......................................... 261.1.5.3 Pleuromutilines ......................................... 26Tiamuline ............................................ 27Valnémuline .......................................... 281.1.6 Antimicrobiens Peptidiques ................................ 281.1.6.1 Polymyxines ........................................... 281.1.6.2 Bacitracine ............................................ 291.1.7 Sulfamidés et Triméthoprime ................................ 291.1.7.1 Triméthoprime. ......................................... 301.1.7.2 Sulfamidés associés au triméthoprime ...................... 301.1.8 Fluoroquinolones ......................................... 311.1.8.1 Danofloxacine. ......................................... 331.1.8.2 Difloxacine ............................................ 331.1.8.3 Enrofloxacine .......................................... 331.1.8.4 Fluméquine. ........................................... 361.1.8.5 Ibafloxacine ........................................... 371.1.8.6 Marbofloxacine. ........................................ 37
TABLE DES MATIÈRESVII1.3.3 Médicaments à usage transdermique actifs contre les ecto- etles endoparasites ......................................... 581.3.3.1 Lactones macrocycliques (LM). ............................ 581.3.3.2 Associations ........................................... 60Imidaclopride + moxidectine ............................. 60Ivermectine + closantel . ................................ 611.3.4 Médicaments injectables et à usage oral contenant des substancesantiparasitaires actives contre les ecto- et les endoparasites ....... 611.3.4.1 Lactones macrocycliques. ................................ 61Doramectine. ......................................... 61Ivermectine .......................................... 62Moxidectine .......................................... 631.3.4.2 Associations ........................................... 63Ivermectine + clorsulon . ................................ 63Ivermectine + closantel . ................................ 64Mébendazole + closantel. ............................... 64Moxidectine + praziquantel . ............................. 64Ivermectine + praziquantel. .............................. 651.3.5 Médicaments injectables et à usage oral contenant des substancesantiparasitaires actives contre les ectoparasites ................. 651.3.5.1 Régu<strong>la</strong>teurs de croissance ................................ 65Lufénurone ........................................... 651.3.5.2 Spinosad. ............................................. 661.3.6 Médicaments à usage topique contenant des substancesantiparasitaires actives contre les ectoparasites ................. 672 Médicaments <strong>du</strong> système hormonal. .................... 692.1 Hormones sexuelles et autres médicaments <strong>du</strong> systèmerepro<strong>du</strong>cteur. ............................................. 692.1.1 Œstrogènes ............................................. 692.1.2 Progestagènes ........................................... 692.1.2.1 Progestérone et dérivés de <strong>la</strong> progestérone .................. 71Delmadinone acétate ................................... 71Mégestrol acétate ..................................... 71Médroxyprogestérone acétate. ........................... 71Proligestone .......................................... 71Progestérone ......................................... 712.1.2.2 Dérivés d’androgènes à activité progestative ................. 712.1.3 Médicaments en cas d’hypertrophie bénigne de <strong>la</strong> prostate ........ 722.1.3.1 Osatérone ............................................. 722.1.3.2 Delmadinone acétate .................................... 732.1.4 Stéroïdes anabolisants ..................................... 732.1.4.1 Nandrolone ............................................ 732.1.5 Gonadotrophines et médicaments agissant sur leur libération ...... 742.1.5.1 Gonadotrophine chorionique (hCG) ......................... 772.1.5.2 Gonadotrophine sérique (PMSG ou eCG) .................... 772.1.5.3 GnRH : buséréline, desloréline, gonadoréline, peforéline ........ 772.1.5.4 Lyophilisat de pFSH et pLH ............................... 782.1.5.5 Combinaison de PMSG (eCG) et d’hCG ..................... 782.1.6 Tocolytiques ............................................. 782.1.6.1 Clenbutérol ............................................ 792.1.7 Ocytociques ............................................. 792.1.8 Prostag<strong>la</strong>ndines .......................................... 812.1.8.1 Alfaprostol ............................................ 832.1.8.2 Cloprosténol ........................................... 832.1.8.3 Dinoprost ............................................. 832.1.9 Médicaments agissant sur <strong>la</strong> libération de <strong>la</strong> pro<strong>la</strong>ctine. ........... 832.1.9.1 Cabergoline ........................................... 842.1.9.2 Métergoline. ........................................... 85
VIIITABLE DES MATIÈRES2.1.10 Antiprogestagènes ....................................... 852.1.10.1 Aglépristone . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 862.2 Hormones cortico-surrénales ................................ 862.2.1 Dexaméthasone .......................................... 892.2.2 Méthylprednisolone ....................................... 902.2.3 Prednisolone. ............................................ 902.3 Médicament utilisé en cas d’hypercorticisme chez le chien(ma<strong>la</strong>die de Cushing) ....................................... 912.3.1 Trilostane ............................................... 912.4 Médicaments contre le dysfonctionnement <strong>du</strong> lobe intermédiaire del’hypophyse chez le cheval (ma<strong>la</strong>die de Cushing) ............... 922.4.1 Pergolide ............................................... 922.5 Médicaments de <strong>la</strong> thyroïde ................................. 942.5.1 Hormone thyroïdienne ..................................... 942.5.1.1 Lévothyroxine .......................................... 942.5.2 Médicament antithyroïdien .................................. 952.5.2.1 Méthimazole (thiamazole). ................................ 962.6 Insuline .................................................. 963 Analgésiques, antipyrétiques et anti-inf<strong>la</strong>mmatoires. ... 993.1 Anti-inf<strong>la</strong>mmatoires non stéroïdiens (AINS) .................... 993.1.1 Salicy<strong>la</strong>tes. ............................................. 1003.1.1.1 Salicy<strong>la</strong>te de sodium ................................... 1013.1.1.2 Acide acétylsalicylique .................................. 1013.1.2 Dérivés de <strong>la</strong> pyrazolone. .................................. 1013.1.2.1 Phénylbutazone ....................................... 1023.1.2.2 Métamizole (dipyrone) .................................. 1023.1.3 Dérivés de l’acide nicotinergique et phénamates ............... 1023.1.3.1 Acide tolfénamique. .................................... 1033.1.3.2 Flunixine ............................................. 1033.1.4 Dérivés de l’acide arylpropionique ........................... 1043.1.4.1 Carprofène ........................................... 1053.1.4.2 Kétoprofène .......................................... 1063.1.5 Groupe des oxicams ..................................... 1073.1.6 Groupe des coxibs ....................................... 1103.1.6.1 Cimicoxib ............................................ 1113.1.6.2 Firocoxib. ............................................ 1113.1.6.3 Mavacoxib ........................................... 1123.1.6.4 Robénacoxib ......................................... 1123.1.7 Associations d’un AINS avec d’autres substances actives ........ 1123.2 Analgésiques et antipyrétiques ............................. 1133.2.1 Paracétamol ........................................... 1133.3 Analgésiques opioïdes. .................................... 1133.3.1 Buprénorphine .......................................... 1133.3.2 Butorphanol ............................................ 1153.3.3 Fentanyl ............................................... 1173.3.4 Méthadone ............................................. 1194 Médicaments <strong>du</strong> système gastro-intestinal . ........... 1214.1 Inhibiteur de <strong>la</strong> sécrétion acide gastrique ..................... 1214.1.1 Oméprazole ............................................ 1214.2 Antispasmodiques digestifs ................................ 1224.2.1 Association hyoscine + métamizole .......................... 122
TABLE DES MATIÈRESIX4.3 Antiémétiques ........................................... 1234.3.1 Maropitant ............................................. 1234.3.2 Métoclopramide ......................................... 1244.4 Médicaments utilisés en cas d’obésité ....................... 1254.4.1 Inhibiteurs de <strong>la</strong> protéine microsomiale de transfert des triglycérides 1254.4.1.1 Dirlotapide ........................................... 1264.5 Antidiarrhéiques contenant des agents anti-infectieux. ......... 1264.5.1 Aminosides. ............................................ 1264.5.1.1 Paromomycine ........................................ 1274.5.1.2 Apramycine. .......................................... 1274.5.1.3 Spectinomycine ....................................... 1274.5.2 Polymyxines ............................................ 1275 Médicaments agissant sur le métabolisme. ............ 1295.1 Médicaments réhydratants ................................. 1295.1.1 Réhydratants à administrer par voie orale ..................... 1295.1.2 Réhydratants à administrer par voie parentérale ................ 1305.2 Glucose ................................................. 1305.3 Vitamines ............................................... 1315.3.1 Vitamine B ............................................. 1315.3.2 Vitamine D ............................................. 1325.3.3 Association vitamine A + vitamine D3 + vitamine E .............. 1325.4 Minéraux ................................................ 1335.4.1 Fer ................................................... 1335.4.2 Sélénium. .............................................. 1345.4.3 Association calcium + magnésium. . . . . . . . . . . . . . . . . . . . . . . . . . . .1345.4.4 Associations calcium + magnésium + autres ................... 1355.5 Vitamines + minéraux ..................................... 1355.5.1 Association vitamine E + sélénium ........................... 1355.6 Vitamines + minéraux + toniques ............................ 1366 Médicaments agissant sur le système locomoteur. .... 1376.1 Acide hyaluronique ....................................... 1376.2 Polysulfate de pentosane sodique .......................... 1386.3 Dibotermine alpha (rhBMP-2), protéine ostéogénique. .......... 1397 Médicaments <strong>du</strong> système respiratoire ................. 1417.1 Bronchodi<strong>la</strong>tateurs ....................................... 1417.1.1 Agonistes bêta-2-adrénergiques ............................ 1417.1.1.1 Clenbutérol ........................................... 1417.2 Antihistaminiques ........................................ 1428 Médicaments cardio-vascu<strong>la</strong>ires ....................... 1438.1 Médicaments utilisés dans l’insuffisance cardiaque ............ 1438.1.1 Inhibiteurs de l’Enzyme de Con<strong>version</strong> de l’Angiotensine (IECA). ... 1438.1.1.1 Bénazépril. ........................................... 1448.1.1.2 Ena<strong>la</strong>pril ............................................. 1458.1.1.3 Imidapril ............................................. 146
XTABLE DES MATIÈRES8.1.1.4 Ramipril. ............................................. 1468.1.2 Antagoniste de l’aldostérone ............................... 1468.1.2.1 Spirono<strong>la</strong>ctone ........................................ 1468.1.3 Association d’un IECA et d’un antagoniste de l’aldostérone ....... 1488.1.3.1 Bénazépril + spirono<strong>la</strong>ctone. ............................. 1488.1.4 Inodi<strong>la</strong>tateurs ........................................... 1488.1.4.1 Pimobendane ......................................... 1488.2 Vasodi<strong>la</strong>tateurs périphériques et cérébraux ................... 1498.2.1 Inhibiteurs de phosphodiestérases. .......................... 1498.2.1.1 Propentofylline ........................................ 1498.3 Diurétiques .............................................. 1508.3.1 Diurétiques de l’anse ..................................... 1508.3.1.1 Furosémide. .......................................... 1509 Médicaments <strong>du</strong> système uro-génital . ................. 1539.1 Médicaments ayant comme indication l’incontinenceurinaire chez <strong>la</strong> chienne ovario-hystérectomisée .............. 1539.1.1 Phénylpropano<strong>la</strong>mine (PPA) ................................ 1539.1.2 Œstriol ................................................ 1549.1.3 Ephédrine .............................................. 15510 Médicaments <strong>du</strong> système nerveuxcentral et périphérique ................................. 15710.1 Anesthésiques généraux injectables ......................... 15710.1.1 Anesthésiques injectables: les barbituriques. .................. 15710.1.1.1 Pentobarbital ......................................... 15910.1.2 Anesthésiques injectables non barbituriques .................. 15910.1.2.1 Anesthésiques dissociatifs ............................... 159Kétamine . .......................................... 161Tilétamine + zo<strong>la</strong>zépam ................................ 16210.1.2.2 Propofol ............................................. 16210.1.2.3 Stéroïdes neuroactifs . .................................. 163Alfaxalone .......................................... 16310.2 Anesthésiques généraux vo<strong>la</strong>tils . ........................... 16410.2.1 Isoflurane. ............................................. 16410.3 Agents utilisés pour l’euthanasie ............................ 16610.3.1 Barbituriques ........................................... 16610.3.2 Association ............................................ 16610.4 Anesthésiques locaux ..................................... 16710.4.1 Procaïne ............................................... 16910.4.2 Associations avec un vasoconstricteur ....................... 16910.5 Neuroleptiques ........................................... 17010.5.1 Phénothiazines .......................................... 17110.5.1.1 Acépromazine. ........................................ 17110.5.2 Dérivés de <strong>la</strong> butyrophénone. .............................. 17210.5.2.1 Azapérone. ........................................... 17210.6 Benzodiazépines ......................................... 17310.6.1 Zo<strong>la</strong>zépam ............................................. 17410.7 Les agonistes alpha-2-adrénergiques et leurs antagonistes ..... 17510.7.1 Les agonistes alpha-2-adrénergiques ........................ 17510.7.1.1 Détomidine ........................................... 17710.7.1.2 Dexmédétomidine ..................................... 177
TABLE DES MATIÈRESXI10.7.1.3 Médétomidine. ........................................ 17710.7.1.4 Romifidine. ........................................... 17810.7.1.5 Xy<strong>la</strong>zine. ............................................. 17810.7.2 Les antagonistes alpha-2-adrénergiques ..................... 17910.7.2.1 Atipamézole .......................................... 17910.8 Myore<strong>la</strong>xants ............................................ 18010.8.1 Guaïfénésine. ........................................... 18010.9 Antidépresseurs .......................................... 18110.9.1 Antidépresseurs tricycliques ............................... 18110.9.1.1 Clomipramine ......................................... 18110.9.2 Inhibiteurs sélectifs de <strong>la</strong> recapture de <strong>la</strong> sérotonine ............ 18210.9.2.1 Fluoxétine ............................................ 18210.9.3 Inhibiteurs des monoamines oxydases (IMAO) . . . . . . . . . . . . . . . . . 18310.9.3.1 Sélégiline ............................................ 18310.10 Médicaments antiépileptiques . ............................. 18410.10.1 Phénobarbital ........................................... 18410.10.2 Bromure de potassium. ................................... 18611 Médicaments pour <strong>la</strong> peau ............................. 18911.1 Médicaments administrés par voie systémique pour le traitementsymptomatique de <strong>la</strong> dermatite atopique . .................... 18911.1.1 Glucocorticoïdes ........................................ 18911.1.2 Ciclosporine ........................................... 18912 Médicaments à usage externe. ......................... 19112.1 Médicaments à usage dermatologique . . . . . . . . . . . . . . . . . . . . . . . 19112.1.1 Antiseptiques. .......................................... 19112.1.1.1 Antiseptiques utilisés sur <strong>la</strong> peau .......................... 19112.1.1.2 Solution de trempage des trayons ......................... 192Chlorhexidine ........................................ 192Iode ............................................... 192Chlorite + acide <strong>la</strong>ctique ............................... 19312.1.2 Antibiotiques ........................................... 19412.1.3 Substances antiparasitaires à usage topique, actives contreles ectoparasites . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 19412.1.3.1 Organophosphorés et carbamates. ........................ 195Dimpy<strong>la</strong>te ........................................... 196Phoxime ............................................ 196Propoxur ........................................... 19612.1.3.2 Pyréthrinoïdes. ........................................ 196Deltaméthrine. ....................................... 197Fluméthrine ......................................... 198Perméthrine . ........................................ 19812.1.3.3 Fipronil .............................................. 19812.1.3.4 Pyriprole . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 20012.1.3.5 Imidaclopride . ........................................ 20112.1.3.6 Métaflumizone ........................................ 20112.1.3.7 Amitraz . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 20212.1.3.8 Indoxacarbe . ......................................... 20312.1.3.9 Associations .......................................... 204Propoxur + fluméthrine ................................ 204Imidaclopride + perméthrine . ........................... 204Imidaclopride + fluméthrine ............................. 205Fipronil + (S)-méthoprène .............................. 205Fipronil, (S)-méthoprène + amitraz ....................... 206Indoxacarbe + perméthrine . ............................ 207Métaflumizone + amitraz . .............................. 208
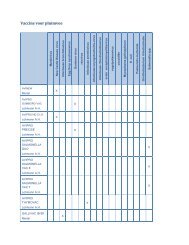
XIITABLE DES MATIÈRES12.1.4 Médicament antiparasitaire pour abeilles ..................... 20812.1.4.1 Thymol .............................................. 20812.1.5 Antifongiques .......................................... 20912.1.6 Glucocorticoïdes ........................................ 20912.1.6.1 Hydrocortisone acéponate ............................... 20912.1.7 Préparation cicatrisante. .................................. 21012.1.7.1 Kétansérine. .......................................... 21012.1.8 Associations ........................................... 21012.2 Médicaments à usage ophtalmologique ...................... 21112.2.1 Préparations contenant au moins un antimicrobien ............. 21112.2.1.1 Gentamicine .......................................... 21112.2.2 Médicaments utilisés contre <strong>la</strong> kératoconjonctivite sèche ........ 21112.2.2.1 Ciclosporine .......................................... 21112.3 Médicaments à usage otique . .............................. 21112.4 Médicaments à usage gynécologique . . . . . . . . . . . . . . . . . . . . . . . . 21312.5 Médicaments à usage intramammaire ....................... 21312.5.1 Traitement des mammites ................................. 21412.5.1.1 Cloxacilline ........................................... 21412.5.1.2 Céphalosporines: premier groupe ......................... 21412.5.1.3 Céphalosporines: deuxième groupe. ....................... 21512.5.1.4 Céphalosporines: troisième groupe . . . . . . . . . . . . . . . . . . . . . . . . 21512.5.1.5 Pirlimycine ........................................... 21512.5.1.6 Associations .......................................... 21512.5.2 Préparations utilisées au cours <strong>du</strong> tarissement et contenantun antimicrobien . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21612.5.2.1 Cloxacilline ........................................... 21612.5.2.2 Céphalosporines surtout actives contre les GRAM+ ........... 21612.5.2.3 Céphalosporines dont le spectre est é<strong>la</strong>rgi .................. 21612.5.2.4 Rifaximine. ........................................... 21612.5.2.5 Associations .......................................... 21712.5.3 Préparations utilisées au cours <strong>du</strong> tarissement et ne contenant pasd’antimicrobien . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21712.5.3.1 Sous nitrate de bismuth ................................. 21713 Médicaments agissant sur l’immunité .................. 21913.1 Vaccins ................................................. 21913.1.1 Vaccins pour le cheval .................................... 21913.1.1.1 Vaccination contre les ma<strong>la</strong>dies virales . .................... 219Grippe équine ....................................... 219Rhinopneumonie . .................................... 221Virus de <strong>la</strong> fièvre <strong>du</strong> Nil occidental (West Nile). .............. 22113.1.1.2 Vaccination contre les ma<strong>la</strong>dies bactériennes ................ 222Tétanos. ............................................ 222Tableau récapitu<strong>la</strong>tif des vaccins pour le cheval . ............... 22413.1.2 Vaccins pour les ruminants. ................................ 22413.1.2.1 Vaccins contre les ma<strong>la</strong>dies virales chez les bovins ........... 224Les vaccins contre les ma<strong>la</strong>dies respiratoires des bovins. ..... 224Vaccins contre les diarrhées virales bovines ................ 228Vaccins contre les diarrhées néonatales d’origine virale ....... 229Vaccination contre <strong>la</strong> fièvre catarrhale ovine (bluetongue). ..... 23013.1.2.2 Vaccins bactériens pour ruminants (bovins et ovins) ........... 231Vaccins colibacil<strong>la</strong>ires ................................. 231Vaccins anti-clostridiens ............................... 232Vaccin contre le piétin . ................................ 234Vaccins contre les ma<strong>la</strong>dies respiratoires d’origine bactérienne -Mannheimia haemolytica . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 234Vaccin contre les mammites causées par E. coli et S. aureus . . 235
TABLE DES MATIÈRESXIIIVaccination contre <strong>la</strong> fièvre Q (Coxiel<strong>la</strong> burnetii) . ............ 23513.1.2.3 Vaccins antiparasitaires pour ruminants. .................... 236Vaccin contre <strong>la</strong> bronchite vermineuse (Dictyocaulus viviparus) . 236Tableau récapitu<strong>la</strong>tif des vaccins pour bovins .................. 237Tableau récapitu<strong>la</strong>tif des vaccins pour ovins et/ou chèvres. ....... 23913.1.3 Vaccins pour le porc. ..................................... 23913.1.3.1 Vaccination contre les ma<strong>la</strong>dies virales <strong>du</strong> porc .............. 239Parvovirose ......................................... 240Grippe porcine (Influenza) . ............................. 241Syndrome dysgénésique et respiratoire porcin (SDRP). ....... 241Circovirus porcin . .................................... 24213.1.3.2 Vaccination contre les ma<strong>la</strong>dies bactériennes chez le porc. ..... 243Pleuropneumonie contagieuse (infections par Actinobacillus pleuropneumoniae)....................................... 243Pneumonie enzootique (infections à Mycop<strong>la</strong>smahyopneumoniae). ..................................... 244Ma<strong>la</strong>die de Glässer (infections à Haemophilus parasuis). ...... 246Rhinite atrophique . ................................... 247Diarrhée néonatale causée par les souches E. coli entérotoxigènes . 248Entéropathie proliférative porcine (EPP)(infections à Lawsonia intracellu<strong>la</strong>ris). ..................... 249Rouget <strong>du</strong> porc ...................................... 250Tableau récapitu<strong>la</strong>tif des vaccins pour le porc. ................. 25213.1.4 Vaccination des <strong>la</strong>pins .................................... 25413.1.4.1 Vaccin combiné contre <strong>la</strong> myxomatose et <strong>la</strong> ma<strong>la</strong>die hémorragiquevirale ................................................ 254Tableau récapitu<strong>la</strong>tif des vaccins pour le <strong>la</strong>pin. ................. 25513.1.5 Vaccination des poules. ................................... 25513.1.5.1 Vaccins contre <strong>la</strong> ma<strong>la</strong>die de Marek. ....................... 25513.1.5.2 Vaccins contre <strong>la</strong> ma<strong>la</strong>die de Newcastle . ................... 25513.1.5.3 Vaccins contre <strong>la</strong> bronchite infectieuse . .................... 25613.1.5.4 Vaccins contre <strong>la</strong> ma<strong>la</strong>die de Gumboro . . . . . . . . . . . . . . . . . . . . . 25613.1.5.5 Vaccins contre l’encéphalomyélite aviaire . .................. 25713.1.5.6 Vaccins contre l’arthrite <strong>du</strong>e aux réovirus ................... 25713.1.5.7 Vaccins contre l’anémie infectieuse virale . .................. 25713.1.5.8 Vaccins contre le syndrome de <strong>la</strong> chute de ponte ............. 25713.1.5.9 Vaccins contre <strong>la</strong> <strong>la</strong>ryngotrachéite infectieuse ................ 25713.1.5.10 Vaccin contre <strong>la</strong> variole aviaire ............................ 25713.1.5.11 Vaccin contre <strong>la</strong> rhinotrachéite ............................ 25713.1.5.12 Vaccins utilisés dans <strong>la</strong> prévention de <strong>la</strong> coccidiose . .......... 25813.1.5.13 Vaccins contre <strong>la</strong> salmonellose ........................... 25813.1.5.14 Vaccins contre d’autres infections bactériennes . ............. 25813.1.6 Vaccination des dindes, pintades, faisans, perdreaux et cailles. .... 25813.1.6.1 Vaccination contre <strong>la</strong> ma<strong>la</strong>die de Newcastle . ................ 25813.1.6.2 Vaccin contre <strong>la</strong> rhinotrachéite aviaire infectieuse ............ 25913.1.7 Vaccination des pigeons. .................................. 26013.1.7.1 Vaccins contre <strong>la</strong> ma<strong>la</strong>die de Newcastle (Paramyxovirose) ...... 26013.1.8 Vaccination des canaris et des pinsons ....................... 26013.1.8.1 Vaccin contre <strong>la</strong> variole <strong>du</strong> canari. ......................... 26013.1.9 Liste des spécialités disponibles ............................ 260Vaccins antiviraux pour vo<strong>la</strong>ille . ......................... 260Vaccins antiparasitaires pour vo<strong>la</strong>ille ...................... 265Vaccins antibactériens pour vo<strong>la</strong>ille. ...................... 266Vaccins pour pigeons. ................................. 267Vaccin pour canaris et pinsons . ......................... 267Tableau récapitu<strong>la</strong>tif des vaccins pour <strong>la</strong> vo<strong>la</strong>ille ................ 267Tableau récapitu<strong>la</strong>tif des vaccins pour pigeons ................. 270Tableau récapitu<strong>la</strong>tif des vaccins pour canaris et pinsons. ........ 27013.1.10 Vaccins pour le chien ..................................... 271
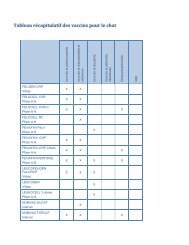
XIVTABLE DES MATIÈRES13.1.10.1 Vaccins contre les ma<strong>la</strong>dies virales <strong>du</strong> chien ................. 271Hépatite infectieuse canine . ............................ 271Parvovirose ......................................... 273Ma<strong>la</strong>die de Carré . .................................... 275L’herpèsvirose canine ................................. 277Infections virales associées à <strong>la</strong> toux de chenil .............. 277Vaccination <strong>du</strong> chiot avec les vaccins multivalents ........... 27913.1.10.2 Vaccins bactériens pour le chien . ......................... 279Bordetel<strong>la</strong> bronchiseptica .............................. 279Leptospira Canico<strong>la</strong>/Icterohaemorrhagiae .................. 28013.1.10.3 Vaccins antiparasitaires pour le chien ...................... 281Leishmania infantum .................................. 281Tableau récapitu<strong>la</strong>tif des vaccins pour le chien . ................ 28213.1.11 Vaccins pour le chat ..................................... 28413.1.11.1 Vaccination contre les ma<strong>la</strong>dies virales <strong>du</strong> chat. .............. 284Panleucopénie féline . ................................. 284Vaccins contre le coryza félin. ........................... 287Virus de <strong>la</strong> leucose féline ............................... 290Vaccin contre <strong>la</strong> péritonite infectieuse féline . ............... 29213.1.11.2 Vaccins bactériens pour le chat ........................... 293Ch<strong>la</strong>mydophi<strong>la</strong> felis . .................................. 293Tableau récapitu<strong>la</strong>tif des vaccins pour le chat .................. 29513.1.12 Vaccins antirabiques. ..................................... 29613.2 Immunocastration . ....................................... 29813.2.1 Vaccin anti-GnRF ....................................... 29813.3 Immunoglobulines et sérums . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 29913.3.1 Immunoglobulines et sérums utilisés chez le bovin . . . . . . . . . . . . . . 29913.3.2 Sérum antitétanique ...................................... 29913.4 Immunomo<strong>du</strong><strong>la</strong>teurs . ..................................... 30013.4.1 Interféron .............................................. 30014 Médicaments antitumoraux ............................ 30114.1 Inhibiteurs des tyrosine kinases ............................. 30114.1.1 Masitinib ............................................... 30214.1.2 Tocéranib .............................................. 302Liste des prémé<strong>la</strong>nges médicamenteux . .................. 303INDEX . ..................................................... 305
AVANT-PROPOSXVAVANT - PROPOSLe C.B.I.P.Le Centre Belge d’Information Pharmacothérapeutique (C.B.I.P.) est une associationsans but lucratif (a.s.b.l.) fondée en 1970 à l’initiative des professeurs depharmacologie humaine des universités belges. Les statuts furent publiés dansle Moniteur Belge le 25 février 1971 et le Centre fut agréé par arrêté royal le 28février 1974. Actuellement, le C.B.I.P. est subsidié par l’Agence Fédérale desMédicaments et des Pro<strong>du</strong>its de Santé (AFMPS).L’objectif <strong>du</strong> Centre est d’assurer <strong>la</strong> formation continue ainsi que <strong>la</strong> mise à jourdes connaissances dans le domaine de <strong>la</strong> pharmacothérapie des médecins, despharmaciens et dentistes, et depuis 1998, des médecins vétérinaires.Activités vétérinairesDepuis 1999, le C.B.I.P. publie annuellement le Répertoire Commenté desMédicaments à Usage Vétérinaire. D’abord édité sous forme de cahiers consacrésaux c<strong>la</strong>sses pharmacothérapeutiques les plus importantes, le répertoire aensuite évolué vers une <strong>version</strong> complète en 2002. Tous les médicaments vétérinairescommercialisés en Belgique y sont rassemblés et commentés par c<strong>la</strong>ssespharmacologiques. Depuis, une édition mise à jour est publiée annuellement etdistribuée aux médecins vétérinaires, pharmaciens et étudiants en médecine vétérinaireet pharmacie.L’objectif de ce répertoire est de promouvoir l’usage rationnel des médicamentsbasé sur les preuves scientifiques justifiant leur qualité, leur efficacité et leur innocuitépour les animaux, les consommateurs de pro<strong>du</strong>its alimentaires d’origineanimale et l’environnement. Les médicaments vétérinaires commercialisés enBelgique sont répertoriés et rassemblés par c<strong>la</strong>sse de médicaments. Un commentaireprécède chaque chapitre afin de donner aux professionnels un aperçudes avantages et des inconvénients de chacun des groupes. Les détails re<strong>la</strong>tifsaux médicaments sont accessibles dans les notices scientifiques, appeléesmaintenant « Résumés des Caractéristiques <strong>du</strong> Pro<strong>du</strong>it (RCP) », éditées par lestitu<strong>la</strong>ires d’enregistrement.En 2001, <strong>la</strong> section vétérinaire <strong>du</strong> C.B.I.P. a é<strong>la</strong>rgi ses activités en publiant lesFolia Veterinaria et en diffusant ses informations en ligne via un site Web: www.cbip-vet.be.Les Folia Veterinaria paraissent trois fois par an et regroupent des articlesd’information générale sur le médicament vétérinaire et <strong>la</strong> pharmacothérapie,des analyses plus ciblées sur un groupe pharmacothérapeutique, voire une nouvellemolécule, et des points d’actualité. Les preuves scientifiques nécessaires àl’évaluation <strong>du</strong> rapport bénéfice/risque qui sous-tend l’usage rationnel des médicamentsy sont discutées.Le site Web <strong>du</strong> C.B.I.P. vétérinaire est mis à jour quotidiennement et reprendl’ensemble des informations contenues dans les publications énuméréesci-dessus.Coordinateur <strong>du</strong> projetPr P. Gustin (ULg)
XVIAVANT-PROPOSBureau de rédaction et col<strong>la</strong>borateursP. Bols (UA) - E. C<strong>la</strong>erebout (UG) - A. De Rick (UG) - P.V. Drion (ULg) - P. Gustin(ULg) - A. Houvenaghel (UA) - L. Laurier (FAGG) - B. Losson (ULg) - J. Mainil (ULg) -G. Sommereyns (CBIP) - E. Thiry (ULg)Col<strong>la</strong>borateurs contribuant ou ayant contribué activement à l’é<strong>la</strong>boration <strong>du</strong>Répertoire et des FoliaG. André-Fontaine (Ecole Nat. Vét. de Nantes) - J. F. Beckers (ULg) – M. Becker(ULg) - P. Bols (UA) - P. Butaye (CODA-CERVA) - C. Cambier (ULg) - B. Catry(WIV-ISP) - E. C<strong>la</strong>erebout (UG) - C. Clercx (ULg) - E. Cox (UG) - S. Croubels (UG) -A. Cuisenaire (ULg) - C. Cuvelier (ULg) - S. Daminet (UG) - M. De Becker (ULg) –E. Cheu (Ulg) - A. De Kruif (UG) - A. De Rick (UG) - M. Debackere - A. Decostere -A. De<strong>la</strong>unois - P. Deprez (UG) - L. Devriese (UG) - A. Dhem - K. Dierick (WIV-ISP) -P.V. Drion (ULg) - F. Gasthuys (UG) - P. Gustin (ULg) - F. Haesebroeck (UG) -J. Hamoir (ULg) - C. Hansen (ULg) - A. Houvenaghel (UA) - L. Janssen (ULg) –F. Klein (AFMPS-FAGG) - L. Laurier (AFMPS-FAGG) - P. Lekeux (ULg) - A. Linden(ULg) – A. Lloret (UAB, Universitat Autònoma de Barcelona) - B. Losson (ULg) -G. Maghuin-Rogister (ULg) - J. Mainil (ULg) - D. Marlier (ULg) - K. McEntee(ULB) - G. Meulemans (CODA-CERVA) - B. Mignon (ULg) - B. Muylkens (ULg) -H. Nauwynck (UG) - L. Okerman (UG) - C. Onclinx (ULg) - F. Pasmans (UG) -P.P. Pastoret (ULg) - D. Peeters (Ulg) - F. Péters (ULg) - M. Pensaert (UG) - I.Polis (UG) -D. Serteyn (ULg) - G. Sommereyns (CBIP-BCFI) - E. Thiry (ULg) - C. Tobback(Centre Antipoisons Belge) - B. Urbain (AFMPS-FAGG) - S. Vandenabeele (UG) -K. Vandermeulen (UG) - L. Van Ham (UG) - K. Van Reeth (UG) - J. Vercruysse (UG) -J. Verstegen (ULg) - A. Zico<strong>la</strong> (ULg)
INTRODUCTIONXVIIINTRODUCTIONCommentaire pharmacothérapeutiqueLes données <strong>du</strong> groupe pharmacothérapeutique sont présentées de manièrestandardisée. Les rubriques prennent en compte, autant que possible, lesRésumés des Caractéristiques <strong>du</strong> Pro<strong>du</strong>it (RCP) des médicaments vétérinairesactuellement commercialisés en Belgique. S’agissant de commentaires généraux,il est impossible d’intégrer toutes les particu<strong>la</strong>rités de chaque médicament. Deuxmédicaments appartenant à un même groupe pharmacothérapeutique peuventavoir des indications différentes. La consultation <strong>du</strong> RCP reste donc essentielle. Ilse peut aussi que des données de <strong>la</strong> littérature, non mentionnées dans les RCP,soient intégrées dans le commentaire.L’usager <strong>du</strong> répertoire tiendra compte aussi <strong>du</strong> fait que l’information de certainesrubriques ne peut pas être exhaustive. Seules les données les plus pertinentessont ainsi reprises dans les rubriques Interactions et Effets indésirables. Lesinteractions et les effets indésirables rares, particuliers à un médicament ou, par <strong>la</strong>force des choses, non encore décrits, ne sont pas signalés.Indications: il s’agit des indications reprises dans le RCP des médicamentscommercialisés, les usages « hors notice » (RCP) n’étant pas traités à ce niveau.Dans le chapitre des médicaments antimicrobiens, cette rubrique est complétéepar le spectre d’activité et <strong>la</strong> résistance.Pharmacodynamie: description de l’action et des effets de <strong>la</strong> substance active.Pharmacocinétique: résumé <strong>du</strong> parcours d’un principe actif, et de ses métabolitesle cas échéant, dans l’organisme de l’animal cible.Contre-indications: généralement énumérées dans le RCP.Effets indésirables: effets indésirables les plus importants.Interactions: les interactions les plus importantes entre les médicaments ou entreceux-ci et d’autres substances issues de l’alimentation par exemple, et parfoisles influences de <strong>la</strong> substance active sur les résultats des tests de biologie et debiochimie clinique.Précautions particulières/Risques pour l’homme: mesures particulières à prendreen compte ou remarques utiles. Dans certains cas, les risques pour l’hommeliés à <strong>la</strong> manipu<strong>la</strong>tion, à l’ingestion accidentelle ou à l’injection <strong>du</strong> médicament ouau contact avec l’animal traité, sont signalés.Repro<strong>du</strong>ction et <strong>la</strong>ctation: les données sont parfois insuffisantes pour autoriserl’administration d’un médicament à un animal destiné à <strong>la</strong> repro<strong>du</strong>ction ou à unanimal gestant ou al<strong>la</strong>itant.LMR : Limite Maximale de Rési<strong>du</strong>s de chaque substance active (ou association desubstances actives): voir aussi couverture intérieure. Cette information est donnéepour tous les médicaments, qu’ils soient destinés à des animaux pro<strong>du</strong>cteurs dedenrées alimentaires ou non.Médicaments vétérinairesCette édition reprend tous les médicaments à usage vétérinaire commercialisés enBelgique au 31 mars <strong>2013</strong>.Pour chaque médicament vétérinaire, les rubriques suivantes sont reprises:
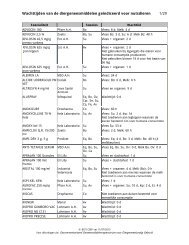
XVIIIINTRODUCTIONMEDICAMENT A USAGE VETERINAIRE (titu<strong>la</strong>ire de l’enregistrement)Enumération qualitative et quantitative des substances actives.Lorsque <strong>la</strong> substance active <strong>du</strong> médicament est un composé, le sel oul’ester <strong>du</strong> composé est p<strong>la</strong>cé entre parenthèses. La posologie mentionne<strong>la</strong> quantité de <strong>la</strong> base active. Toutefois, si <strong>la</strong> posologie ne reprend pas<strong>la</strong> base active mais <strong>la</strong> quantité <strong>du</strong> composé à base <strong>du</strong> sel ou de l’ester,ces derniers ne sont pas p<strong>la</strong>cés entre parenthèses. En règle générale,sauf si mentionné différemment, <strong>la</strong> posologie exprime <strong>la</strong> quantité desubstance(s) active(s) par kg de poids vif ou par animal, et non <strong>la</strong> quantitéde médicament.Forme pharmaceutique, mode d’administrationPosol: espèce cible et posologie pour cette espèceTemps d’attente (Viande, Lait, Oeuf, Miel)Embal<strong>la</strong>geDélivranceR/ : ces médicaments ne sont pas de délivrance libre mais peuvent être livréspar le médecin vétérinaire ou par le pharmacien d’officine sur présentationd’une prescription médicale.R/i : <strong>la</strong> prescription de vaccins et d’antisérums contre les ma<strong>la</strong>diesréglementées (ma<strong>la</strong>dies mentionnées dans le chapitre III de <strong>la</strong> loi re<strong>la</strong>tive à <strong>la</strong>santé des animaux <strong>du</strong> 24 mars 1987) est interdite (AR <strong>du</strong> 5 nov 2002).Voir aussi Circu<strong>la</strong>ire ministérielle <strong>du</strong> 1er mars 2004 et Folia Veterinaria 2004,n° 1.R/par: signifie qu’une firme importe à partir d’un Etat membre de l’Unioneuropéenne un médicament commercialisé en Belgique mais aussi dans cetautre Etat membre. Pour plus d’informations, voir www.afmps.be, cliquersur “Usage vétérinaire” puis sur “Importation parallèle” dans <strong>la</strong> rubrique“Procé<strong>du</strong>res d’autorisation de mise sur le marché”.R/premix : <strong>la</strong> délivrance de prémé<strong>la</strong>nges pour aliments médicamenteux estréglée par l’AR <strong>du</strong> 21 déc 2006 portant exécution de <strong>la</strong> loi <strong>du</strong> 21 juin 1983.R/psych : <strong>la</strong> prescription et <strong>la</strong> délivrance de médicaments stupéfiants et decertaines substances psychotropes sont réglées par respectivement l’AR <strong>du</strong>31 déc 1930 et l’AR <strong>du</strong> 22 janv 1998. Voir pour plus d’information le FoliaVeterinaria 2008 n° 2.Remarque: commentaire formulé par le comité de rédaction <strong>du</strong> CBIP (voir plusloin, «Temps d’attente»)Remarques importantes- Temps d’attenteDepuis le 1er janvier 2000, <strong>la</strong> légis<strong>la</strong>tion de l’Union européenne (le Règlement (CE)n° 470/2009 et le Règlement (UE) n° 37/2010, qui remp<strong>la</strong>ce le Règlement (CEE) n°2377/90) interdit l’administration aux animaux pro<strong>du</strong>cteurs de denrées alimentairesdes substance actives pour lesquelles aucune LMR n’a été fixée.Les temps d’attente sont ceux indiqués dans les notices scientifiques validées. Cestemps d’attente étant susceptibles d’être modifiés soit en fonction de l’évolution desdonnées scientifiques, soit par des lignes directrices européennes, il est conseilléaux utilisateurs de prendre contact avec les titu<strong>la</strong>ires de l’Autorisation de Mise surle Marché pour prendre connaissance des modifications éventuelles. Par ailleurs,les données disponibles sur le site Web <strong>du</strong> CBIP vétérinaire sont régulièrementactualisées en fonction des informations transmises par l’Agence Fédérale desMédicaments et des Pro<strong>du</strong>its de Santé (AFMPS). Une liste des temps d’attentede tous les médicaments indiqués chez les animaux pro<strong>du</strong>cteurs de denréesalimentaires, est disponible sur le site www.cbip-vet.be, sous <strong>la</strong> rubrique « Tempsd’attente » (www.cbip-vet.be/fr/WTlisteFR.pdf).- Les prémé<strong>la</strong>nges médicamenteuxLa livraison de prémé<strong>la</strong>nges médicamenteux est différente de celle des autresmédicaments vétérinaires. Une liste de tous les prémé<strong>la</strong>nges médicamenteuxcommercialisés en Belgique est reprise à <strong>la</strong> fin de cet ouvrage (p. 303).
ADRESSES UTILESXIXADRESSES UTILESCentre Belge d’Information Pharmacothérapeutique - CBIPc/o Campus Heymans Bloc B, 1er étageDe Pinte<strong>la</strong>an 1859000 GentE-mail: cbip.vet@afmps.beSite Web médicaments à usage vétérinairewww.cbip-vet.be ou www.bcfi-vet.beSite Web médicaments à usage humainwww.cbip.be ou www.bcfi.beAgence Fédérale des Médicaments et des Pro<strong>du</strong>its de Santé - AFMPSEurostation IIP<strong>la</strong>ce Victor Horta, 40 bte 40B- 1060 Bruxelles02 524 71 11www.afmps.beCentre Belge de Pharmacovigi<strong>la</strong>nce pour les médicaments à usageVétérinaire – CBPVP<strong>la</strong>ce Victor Horta 40, bte 40B-1060 BruxellesTél: 02 524 81 26Tél: 02 524 81 29E-mail: adversedrugreactions_vet@afmps.beEuropean Medecines Agency - EMA7 Westferry Circus Canary WharfLondon E14 4HBTél: (44-20) 74 18 84 00Fax: (44-20) 74 18 84 16www.ema.europa.euE-mail: info@ema.europa.euAgence Fédérale pour <strong>la</strong> Sécurité de <strong>la</strong> Chaîne alimentaire – AFSCACentre administratif BotaniqueBoulevard <strong>du</strong> Jardin Botanique 551000 Bruxelleswww.favv.beE-mail: info@afsca.beAssociation Régionale de Santé et d’Identification Animales - a.s.b.l.Siège socialAllée des Artisans 25590 CineyE-mail : arsia@arsia.bewww.arsia.beDierengezondheidszorg V<strong>la</strong>anderen - v.z.w.www.dgz.beDrongenDeinse Horsweg 19031 DrongenLierHagenbroeksesteenweg 1672500 Lier
XXADRESSES UTILESTorhoutIn<strong>du</strong>strie<strong>la</strong>an 298820 TorhoutDiestE<strong>du</strong>ard Robeyns<strong>la</strong>an 293290 DiestFaculté de Médecine Vétérinaire, Université de LiègeBd de Colonster B414000 Liègewww.fmv.ulg.ac.beFaculteit Diergeneeskunde, Universiteit GentSalibury<strong>la</strong>an 1339820 Merelbekehttp://www.ugent.be/diCentre antipoisonsc/o Hôpital Militaire Reine AstridRue Bruyn 11120 BruxellesPermanence médicale :Tél (urgences): 070 245 245E-mail: medical.team@poisoncentre.beAdministration :Secrétariat:Tél 02 264 96 36Fax 02 264 96 46E-mail : info@poisoncentre.bewww.poisoncentre.beNotices de tous les médicaments (à usage humain et à usage vétérinaire)autorisés sur le marché belge:www.afmps.beNotices des médicaments vétérinaires enregistrés selon <strong>la</strong> procé<strong>du</strong>re centrale:www.ema.europa.euNotices des médicaments vétérinaires enregistrés selon <strong>la</strong> procé<strong>du</strong>re dereconnaissance mutuelle:www.hma.eu/vmri.html
1 MEDICAMENTS ANTIBACTÉRIENS11. MÉDICAMENTS ANTI-INFECTIEUX1.1 AntibactériensLes antibactériens repris dans ce chapitre sont destinés à être administrés par voieorale ou parentérale. Les médicaments contenant des principes actifs peu résorbéspar le tube digestif ou associés à des principes actifs spécifiquement utilisés pourle traitement des ma<strong>la</strong>dies gastro-intestinales, sont c<strong>la</strong>ssés dans le chapitre consacréaux médicaments <strong>du</strong> tube digestif (voir point 4.5 Antidiarrhéiques contenantdes agents anti-infectieux). Les préparations topiques destinées à être utilisées auniveau ocu<strong>la</strong>ire, mammaire, gynécologique ou otique sont également reprises dansles chapitres correspondants (voir 12. Médicaments à usage externe).Un aperçu global des principales bactéries rencontrées en médecine vétérinairea été publié dans le Folia Veterinaria 2002, n° 1. Tous les textes traitant des antibactérienspubliés antérieurement dans les Folia Veterinaria sont disponibles enligne (www.cbip-vet.be).Les critères de choix des principes actifs et des médicaments qui les contiennentreposent sur un ensemble de paramètres, brièvement rappelés ci-dessous.• Pharmacodynamie (PD) et pharmacocinétique (PK)Bactéricides versus bactériostatiquesLes antibactériens bloquent le développement des bactéries sensibles en interférantavec des cibles molécu<strong>la</strong>ires si possible propres aux agents infectieux. L’arrêt<strong>du</strong> développement peut être temporaire dans le cas des bactériostatiques oudéfinitif pour les bactéricides. Lorsque les défenses immunitaires sont normales,aucun argument ne p<strong>la</strong>ide en faveur de l’une ou l’autre de ces deux catégories. Lasupériorité des antimicrobiens bactéricides n’est considérée en clinique que dansles infections les plus graves comme par exemple les méningites et les bactériémieset chez les patients neutropéniques ou immunodéprimés.Modèles PK/PDLa mise en parallèle de <strong>la</strong> pharmacocinétique (PK) des médicaments anti-infectieuxet de leur pharmacodynamie (PD), évaluée par les Concentrations MinimalesInhibitrices (CMI), a permis le développement de modèle « PK/PD » permettantd’optimaliser les posologies au moment de <strong>la</strong> mise sur le marché des médicaments.Malgré <strong>la</strong> complexité de cette approche, certaines règles de bases s’endégagent, utilisables par le praticien.A l’exception de certaines catégories d’antimicrobiens comme les fluoroquinoloneset les céphalosporines de dernières générations pour lesquelles un antibiogrammeest requis pour justifier leur usage, on ne peut pas systématiquements’appuyer sur l’identification <strong>du</strong> germe causal et <strong>la</strong> détermination de sa sensibilité.Le choix doit dans ce cas être guidé par <strong>la</strong> nature des germes les plus susceptiblesd’être rencontrés et leur sensibilité <strong>la</strong> plus probable tenant compte des donnéesépidémiologiques les plus pertinentes. Lorsque c’est possible, le recoursà des examens microscopiques de frottis ou de prélèvement réalisés au niveaudes sites infectieux peut fournir des indications sur les agents étiologiques en jeu(coques, bâtonnets, infections multifactorielles, gram+/-). En cas d’échec thérapeutiqueou lorsqu’une thérapie d’urgence doit être confirmée, l’isolement desgermes en cause et l’identification de leurs sensibilités doivent être réalisés pourorienter le suivi thérapeutique. Dans certaines exploitations confrontées à desproblèmes infectieux récurrents et les cliniques, les résistances locales doiventêtre connues grâce à <strong>la</strong> mise en p<strong>la</strong>ce de p<strong>la</strong>ns d’épidémiosurveil<strong>la</strong>nce. Dans tousles cas, le choix se portera si possible sur l’antimicrobien dont le spectre est leplus étroit possible.Il tombe sous le sens que pour être efficace, un antimicrobien doit atteindre desconcentrations supérieures aux CMI au niveau des sites infectieux. Sur le p<strong>la</strong>ncinétique, ceci suppose une biodisponibilité (absorption) ainsi qu’une diffusionoptimales <strong>du</strong> principe actif sélectionné. Il est, à ce stade, capital de rappeler que
2 1 MEDICAMENTS ANTIBACTÉRIENS<strong>la</strong> pharmacocinétique <strong>du</strong> principe actif est aussi fortement influencée par <strong>la</strong> formegalénique <strong>du</strong> médicament. De ce point de vue, le choix thérapeutique doit doncd’abord se porter sur un principe actif en fonction de ses propriétés pharmacocinétiquesgénérales. Il convient ensuite de choisir une préparation adéquate enfonction de <strong>la</strong> cinétique propre à chacune.Il est évident qu’un médicament donnant lieu à des concentrations tissu<strong>la</strong>ires inférieuresaux CMI au niveau <strong>du</strong> site infectieux sera inefficace. Vu l’évolution desCMI au cours des décennies, il n’est pas impossible que des posologies efficacesdans le passé, soient devenues obsolètes. Il est donc indispensable d’actualiserces données et de les intégrer dans <strong>la</strong> prise de décision thérapeutique. Les <strong>la</strong>boratoirespharmaceutiques sont tenus de prendre en compte ces changementslors de l’actualisation de leurs dossiers d’enregistrement. Dans le même temps,les vétérinaires praticiens, informés de cette évolution globale et prenant aussien compte des données locales de sensibilité, peuvent au moins s’assurer queles médicaments mis sur le marché permettent d’atteindre des concentrations aumoins supérieures aux CMI au niveau sérique ou mieux au niveau des sites infectieux.De ce point de vue, <strong>la</strong> qualité des informations contenues dans les RCP estcapitale pour opérer un choix thérapeutique raisonné et éliminer les préparationsdevenues obsolètes.Le dépassement des CMI au niveau des sites infectieux n’est pas une conditionsuffisante pour garantir une efficacité optimale. Le temps pendant lequel lesconcentrations sont supérieures aux CMI est primordial pour beaucoup d’antibiotiques.Cette <strong>du</strong>rée dépend de <strong>la</strong> dose administrée et de l’intervalle d’administration,propre à chaque médicament. Si <strong>la</strong> concentration descend sous <strong>la</strong> CMI, <strong>la</strong>multiplication bactérienne reprend le plus souvent. Pour les antibiotiques concentration-dépendants,il est crucial d’assurer un pic de concentration très élevé parrapport au CMI. L’intervalle d’administration peut jouer un rôle moins déterminantdans le cas des antibiotiques temps-dépendants si l’on peut compter sur un effetpost-antibiotique comme pour les fluoroquinolones par exemple. Les implicationspratiques de ces nouvelles approches ont été discutées dans le Folia Veterinaria2012 n° 2.Les voies de métabolisation et d’élimination des antimicrobiens sont décritesdans les notices. Elles peuvent influencer le choix de certains principes actifs.Ainsi, des concentrations urinaires importantes contribuent à l’efficacité vis-à-visdes infections <strong>du</strong> tractus urinaire. De <strong>la</strong> même manière, un cycle entéro-hépatiquede formes actives peut être utile pour assurer une action systémique et locale decertains agents antimicrobiens. Les insuffisances hépatiques et rénales peuventmodifier <strong>la</strong> cinétique de certains principes actifs en ayant pour conséquencepossible une augmentation de leur toxicité ou une ré<strong>du</strong>ction de leur efficacité.Une ré<strong>du</strong>ction de <strong>la</strong> c<strong>la</strong>irance rénale ou hépatique peut aussi aboutir à prolongerle temps d’attente. En cas de suspicion d’insuffisance hépatique ou rénale, ilconvient donc de choisir des antimicrobiens dont <strong>la</strong> cinétique ne soit pas influencéepar ces anomalies cinétiques.Les associations d’antimicrobiens augmentent <strong>la</strong> probabilité d’émergence denouvelles résistances et sont le plus souvent inutiles et peuvent même s’avérernéfastes à l’efficacité <strong>du</strong> traitement. Elles peuvent être justifiées par des synergiesentre antimicrobiens en cas de résistance aux monothérapies ou en cas d’infectionsmultifactorielles.• RésistanceLorsque les concentrations d’un antibactérien sont inférieures ou à peine supérieuresaux CMI, seuls les micro-organismes les plus sensibles sont éliminés tandisque ceux qui le sont moins, c’est-à-dire dotés d’une résistance partielle, continuerontde se développer. Ces résistances partielles sont surmontables en modifiantles posologies. Ces adaptations, envisageables chez les animaux de compagnie,ne sont pas recommandables chez les espèces destinées à <strong>la</strong> consommationhumaine puisque les modifications posologiques invalident le temps d’attente.Quoiqu’il en soit, le lien direct entre l’usage des antimicrobiens et l’émergence desrésistances impose de limiter l’usage de ces substances.
1 MEDICAMENTS ANTIBACTÉRIENS3• Positionnement des antimicrobiensLes antimicrobiens ont une importance cruciale dans les infections graves maisapportent un bénéfice marginal voire nul dans les infections évoluant spontanémentde façon favorable. Il est essentiel de ne pas instaurer une antibiothérapie à<strong>la</strong> moindre suspicion.Le vétérinaire doit se référer aux analyses risques/bénéfices disponibles dans <strong>la</strong>littérature pour certaines pathologies infectieuses animales et évaluer au cas parcas l’intérêt réel de <strong>la</strong> thérapie qu’il souhaite mettre en p<strong>la</strong>ce avant de prendreune décision.En cas d’infection grave aiguë, une antibiothérapie doit être instaurée le plus rapidementpossible en outrepassant parfois les règles imposant <strong>la</strong> réalisation d’unantibiogramme préa<strong>la</strong>blement au traitement si des éléments concrets permettentde considérer qu’aucune alternative thérapeutique n’existe.Les traitements prophy<strong>la</strong>ctiques et métaphy<strong>la</strong>ctiques ne peuvent être justifiés quedans certains cas précis dont il convient de s’informer dans <strong>la</strong> littérature et dansle cadre de <strong>la</strong> formation continue.• Précautions particulières d’emploi, effets indésirables et contre-indicationsLes effets indésirables et les contre-indications propres à chaque antimicrobiensont répertoriés dans les notices.Le choix des agents antimicrobiens se fera aussi en tenant compte de <strong>la</strong> sensibilitéindivi<strong>du</strong>elle liée à un état physiologique ou pathologique particulier.• Santé publiqueLe respect des posologies validées pour des indications précises permet de minimiserl’émergence des résistances.Le respect des temps d’attente est une contrainte légale permettant d’assurer l’absencede concentrations actives d’antimicrobiens dans les denrées alimentaires.Dans <strong>la</strong> mesure <strong>du</strong> possible, les préparations associées à des temps d’attentelongs et donnant lieu à des contaminations prolongées des sites d’injectionsdoivent être considérées comme des second choix.1.1.1 Antibiotiques bêta-<strong>la</strong>ctamesLes bêta-<strong>la</strong>ctamines sont des antibiotiques bactéricides pour lesquels deuxfamilles sont représentées dans le secteur vétérinaire: les pénicillines et lescéphalosporines.1.1.1.1 Pénicillinestaines souches de Staphylococcus aureus,pro<strong>du</strong>ctrices de bêta-<strong>la</strong>ctamasesIndications - spectre d’activité - (ou pénicillinases) extracellu<strong>la</strong>ires.résistancesDiverses bactéries GRAM- peuventTrois groupes de pénicillines sont utilisésen médecine vétérinaire: 1) les vis-à-vis des aminopénicillines.également acquérir des résistancespénicillines naturelles: les benzylpénicillines(pénicilline G) et <strong>la</strong> phénoxy-Les pénicillines, tout comme les cé-Pharmacodynamieméthylpénicilline (pénicilline V) dont phalosporines, possèdent un noyaule spectre est essentiellement limité bêta-<strong>la</strong>ctame qui leur confère une activitéantibactérienne. On les regroupeaux bactéries GRAM+ et à certainesanaérobies, 2) les aminopénicillines, sous le terme de bêta-<strong>la</strong>ctamines. Ellesdont le spectre est é<strong>la</strong>rgi à certaines agissent en inhibant <strong>la</strong> synthèse desbactéries GRAM- et 3) les pénicillines peptidoglycans de <strong>la</strong> paroi des bactéries.Leur effet bactéricide s’exercedites « résistantes aux pénicillinases »comme p. ex. <strong>la</strong> cloxacilline (voir 12.5. uniquement sur les germes en croissancechez lesquels <strong>la</strong> synthèse desMédicaments à usage intramammaire).Des résistances acquises aux pénicillinesexistent cependant chez certainespeptidoglycans est <strong>la</strong> plus intense.bactéries GRAM+, notamment cer-
4 1 MEDICAMENTS ANTIBACTÉRIENSPharmacocinétiqueLa cinétique est très spécifique à chacunede ces substances. Elle varied’une espèce à l’autre et est fortementinfluencée par <strong>la</strong> forme galénique desmédicaments. Par conséquent, il estvivement conseillé d’utiliser des préparationspour lesquelles les profilspharmacocinétiques ont été optimaliséset décrits dans le Résumé desCaractéristiques <strong>du</strong> Pro<strong>du</strong>it (RCP).Leur mise en parallèle avec le niveaude sensibilité des germes visés peutêtre très utile pour le choix d’un antimicrobienet d’une forme pharmaceutiqueparticulière. Ces substancesdont <strong>la</strong> plupart sont éliminées par lesreins grâce à un mécanisme de filtrationgloméru<strong>la</strong>ire et de sécrétiontubu<strong>la</strong>ire active ont une demi-vie d’éliminationproche de 1 heure quelle quesoit l’espèce.Contre-indicationsLes bêta-<strong>la</strong>ctamines sont à proscrirechez le <strong>la</strong>pin, le chinchil<strong>la</strong>, le cobayeet le hamster, car elles provoquent,chez ces espèces, une dérive de<strong>la</strong> flore caecale qui peut être fatale.L’hypersensibilité est aussi une contreindicationmajeure.Effets indésirablesLes pénicillines ont une très faible toxicité,même à des posologies <strong>la</strong>rgementsupérieures aux doses recommandées.Des réactions croisées d’hypersensibilitéplus ou moins sévères, comme del’urticaire, des œdèmes, voire un chocanaphy<strong>la</strong>ctique, peuvent toutefois êtreobservées. Les autres effets toxiquesdépendent de <strong>la</strong> nature chimique <strong>du</strong>principe actif utilisé. Dans le cas dessels potassiques, les effets indésirablessont liés, en cas de surdosage, au potassium,responsable d’arrêt cardiaque.La procaïne, entrant dans <strong>la</strong> compositionde certaines préparations à basede pénicilline (pénicilline-procaïne),peut in<strong>du</strong>ire des symptômes nerveuxcentraux. Le cheval est particulièrementsensible à <strong>la</strong> procaïne.InteractionsDes synergies ou des interactionsadditives ont été constatées contrecertaines bactéries lors d’associationavec d’autres antibiotiques bactéricides,comme les aminoglycosides.On évitera les associations avecdes antibiotiques bactériostatiques,comme les tétracyclines ou les phénicolés(florfénicol).Précautions particulièresLe cheval est particulièrement sensibleà <strong>la</strong> procaïne présente dans <strong>la</strong> compositionde certaines préparations à basede pénicilline (pénicilline-procaïne).Une attention toute particulière doitdonc être portée au respect des posologieset aux conditions de conservationdes préparations injectables. (Voiraussi Folia Veterinaria 2008 n° 1)Repro<strong>du</strong>ction et <strong>la</strong>ctationLes pénicillines pénètrent le p<strong>la</strong>centaen quantité variable selon les espècesanimales et le type de molécules.Leur sécurité <strong>du</strong>rant <strong>la</strong> gestation étantconsidérée comme très élevée et aucuneffet tératogène n’ayant été décrit,leur administration au cours de <strong>la</strong> gestationest envisageable. La pénicillineest excrétée par le <strong>la</strong>it et peut engendrerde <strong>la</strong> diarrhée, de <strong>la</strong> candidoseou des réactions allergiques chez lesanimaux al<strong>la</strong>ités.Pénicillines naturellesLes médicaments à usage vétérinairecontiennent de <strong>la</strong> benzylpénicillineprocaïne ou de <strong>la</strong> phénoxyméthylpénicilline.Un ester lipophile (pénéthamate)est également disponible pour letraitement des mammites.Indications - spectre d’activité- résistancesLes benzylpénicillines sont, a priori,actives contre beaucoup de bactériesGRAM+ aérobies et anaérobies, ycompris tous les streptocoques bêtahémolytiqueset le genre Clostridium,ainsi que contre certaines bactériesGRAM- (Haemophilus, Pasteurel<strong>la</strong>,Actinobacillus, Mannheimia,Fusobacterium…). Elles sont cependantsensibles aux bêta-<strong>la</strong>ctamasespro<strong>du</strong>ites par certains staphylocoques.Le médicament à base de phénoxyméthylpénicillineest enregistrépour <strong>la</strong> prévention de mortalité chezles poules souffrant d’une entéritenécrosante causée par Clostridiumperfringens.PharmacodynamieVoir 1.1.1.1.PharmacocinétiqueRapidement détruits au niveau del’estomac, <strong>la</strong> benzylpénicilline et lepénéthamate sont administrés uniquementpar voie parentérale. La formecristalline, en suspension aqueuse ouhuileuse, permet d’en ralentir l’absorption.Après son administration par voie
1 MEDICAMENTS ANTIBACTÉRIENS5orale, <strong>la</strong> phénoxyméthylpénicillineéchappe en grande partie à <strong>la</strong> destructionpar les sucs gastriques et ce,grâce à sa stabilité à un faible pH. Sabiodisponibilité est d’environ 70 %.Les pénicillines diffusent bien dansles tissus très vascu<strong>la</strong>risés mais leurdistribution se limite au compartimentextracellu<strong>la</strong>ire. Elles traversent difficilementles barrières biologiques, sauflors d’inf<strong>la</strong>mmation. La concentrationde <strong>la</strong> benzylpénicilline dans le <strong>la</strong>it représente20 % de <strong>la</strong> concentration sérique.Des concentrations importantespeuvent être atteintes dans le foie,les poumons, les reins et les urines.L’élimination se fait essentiellementpar voie rénale. Le pénéthamate, <strong>du</strong>fait de sa liposolubilité, se concentredans le <strong>la</strong>it où le principe actif atteintdes concentrations efficaces.Contre-indications - EffetsindésirablesVoir 1.1.1.1.InteractionsVoir aussi 1.1.1.1. Le contact dessolutions contenant de <strong>la</strong> phénoxyméthylpénicillineavec des métaux(systèmes d’eau de boisson) a uneincidence indésirable sur <strong>la</strong> stabilité de<strong>la</strong> phénoxyméthylpénicilline.Précautions particulières -Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir 1.1.1.1.LMR benzylpenicilline procaïne, pénéthamateet phénoxyméthylpénicilline:DEPOSIL (Eurovet)benzylpénicilline procaïne: 300.000 UI/mlsuspension injectable im (Bo, Su, Ov, Ca), sc(Ca, Fe)Posologie:<strong>du</strong>rée <strong>du</strong> traitement: min 3 - 4 jBo: 12 mg/kg pjSu, Ov: 15 mg/kg pjCa, Fe: 30 mg/kg pjViande: Bo, Su: 5 j , Ov: 4 j, Lait: Bo: 11 jNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/DUPHAPEN (Pfizer A.H.)benzylpénicilline procaïne: 300 mg/mlsuspension injectable imPosologie:Bo, Su, Ov: 10 mg/kg pj (3-5 j)Viande: Bo, Su, Ov: 6 j, Lait: Bo: 96 hNe pas utiliser chez les ovins dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/PENI-kel 300.000 UI/ml (Ke<strong>la</strong> Laboratoria)benzylpénicilline procaïne: 300.000 UI/mlsuspension injectable imPosologie:Bo, Su: 21.000/kg pj (Bo max 5 j,Su max 3 j)Viande: Bo: 9 j, Su: 5 j, Lait: 7,5 j (15 traites)f<strong>la</strong>con 100 ml, 250 mlR/MAMMYZINE 5 g (Boehringer Ingelheim)pénéthamate iodhydrate: 5 g (pour une suspensionde 333 mg/ml)poudre et solvant pour suspension injectable imPosologie:Bo: 1er jour: 15 mg/kg, 2e et 3e jour:7,5 mg/kgViande: 8 j, Lait: 4 j10 f<strong>la</strong>cons de poudre (5 g) + 10 f<strong>la</strong>cons desolvant (15 ml)R/MAMMYZINE 10 g (Boehringer Ingelheim)pénéthamate iodhydrate: 10 g (pour une suspensionde 333 mg/ml)poudre et solvant pour suspension injectable imPosologie:Bo: 1er jour: 15 mg/kg, 2e et 3e jour:7,5 mg/kgViande: 8 j, Lait: 4 j10 f<strong>la</strong>cons de poudre (10 g) + 10 f<strong>la</strong>cons desolvant (30 ml)R/PHENOXYPEN WSP (Dopharma Research)phénoxyméthylpénicilline (potassium): 293 mg/gpoudre po avec l’eau de boissonPosologie:poule: 13,5 - 20 mg/kg pj (5 j)Viande: 2 jOeufs: 0 jpoudre (combibus) 1 kgR/AminopénicillinesIndications - spectre d’activité -résistancesL’activité bactéricide de l’amoxicillineet de l’ampicilline vis-à-vis desbactéries GRAM+ est plus faible quecelle de <strong>la</strong> benzylpénicilline, mais leurspectre s’étend à plus de bactériesGRAM-, telles que diverses entérobactériescomme E. coli, Salmonel<strong>la</strong>,Proteus, etc. Les aminopénicillinesrestent inactives contre les souchespro<strong>du</strong>ctrices de pénicillinases.PharmacodynamieVoir 1.1.1.1.PharmacocinétiqueElles sont administrées par voie oraleou parentérale. L’intervalle de dosagevarie entre 6 et 48h. D’une manièregénérale, les préparations caractériséespar une vitesse d’absorptionassez lente au niveau <strong>du</strong> site d’injectiondonnent lieu à des concentrationssériques basses. Leur emploi devraitdonc se limiter au traitement des infectionsprovoquées par les germes
6 1 MEDICAMENTS ANTIBACTÉRIENSles plus sensibles. La distribution tissu<strong>la</strong>iredes aminopénicillines s’adressesurtout aux organes bien vascu<strong>la</strong>risésmais se limite aux liquides interstitiels.Elles sont principalement éliminéespar les urines. Les concentrations lesplus fortes sont détectées dans l’urine,<strong>la</strong> bile et les poumons.Contre-indicationsL’administration orale est contre-indiquéechez le cheval a<strong>du</strong>lte.Effets indésirablesLa toxicité des aminopénicillines estidentique à celle des autres pénicillines.Des diarrhées bénignes ontégalement été observées chez les carnivoreset le veau à <strong>la</strong> suite d’administrationsorales.Interactions - Précautions particulières- Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir 1.1.1.1.- AmpicillineLMR ampicilline: ALBIPEN LA (MSD A.H.)ampicilline (anhydre): 100 mg/mlsuspension injectable imPosologie:Su: 30 mg/kgrépéter le traitement après 48 hViande: 24 jf<strong>la</strong>con 200 mlR/AMPI-DRY 3 g, 5 g (Prodivet)ampicilline anhydre (sodique): 3 g, 5 gpoudre pour solution injectable ivPosologie:Eq: 30 mg/kg à 6 h d’intervalle (max 5 j)Bo, veau: 25 mg/kg PV à 6 h d’intervalle(max 5 j)Viande: Eq: 4 j, Bo: 3 j, Lait: Bo: 48 h (4 traites)f<strong>la</strong>con 3 g, 5 gR/- AmoxicillineLMR amoxicilline: AMOXICURE (Oropharma)amoxicilline (trihydrate): 300 mg/gpoudre po dans l’eau de boissonPosologie:pigeon: 150 mg/kg (5 j) ou 1 dose/l d’eauViande: 60 hpoudre 120 g (boîte)R/AMOXIVAL VET 200 mg compr chien (Sogeval Lab)amoxicilline (trihydrate): 200 mgcomprimé poPosologie:Ca: 2 x pj 10 mg/kg (5 j, ou plus en fonctionde <strong>la</strong> réponse clinique)de préférence en dehors des repascompr 200R/AMOXIVAL VET 400 mg compr chien (Sogeval Lab)amoxicilline (trihydrate): 400 mgcomprimé poPosologie:Ca: 2 x pj 10 mg/kg (5 j, ou plus en fonctionde <strong>la</strong> réponse clinique)de préférence en dehors des repascompr 200R/AMOXYCILLINE 70 % Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)amoxicilline (trihydrate): 700 mg/gpoudre po avec l’eau de boisson (Su, Av) ouavec l’alimentation (Su)Posologie:Su: 10 - 20 mg/kg pj (4 - 5 j)poule: 14 mg/kg pj (5 j)Viande: Su: 2 j, poule: 1 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainepoudre 1 kgR/AMOXY-kel 15 (Ke<strong>la</strong> Laboratoria)amoxicilline (trihydrate): 150 mg/mlsuspension injectable imPosologie:Su: 7 - 15 mg/kg pj (3 j)Viande Su: 53 jf<strong>la</strong>con 250 mlR/CLAMOXYL compr appétents 40 mg (Pfizer A.H.)amoxicilline (trihydrate): 40 mgcomprimé appétent poPosologie:Ca, Fe: 2 x pj 4 - 10 mg/kgcompr 10, 100R/CLAMOXYL compr appétents 200 mg (Pfizer A.H.)amoxicilline (trihydrate): 200 mgcomprimé appétent poPosologie:Ca, Fe: 2 x pj 4 - 10 mg/kgcompr 10, 100R/CLAMOXYL LA (Pfizer A.H.)amoxicilline (trihydrate): 150 mg/mlsuspension injectable im, scPosologie:Su, Ov, Ca, Fe: 15 mg/kgrépéter après 24 h (GRAM-) ou 48 h(GRAM+)Viande: Su: 42 j, Ov: 21 j, Lait: Ov: 96 hf<strong>la</strong>con 250 mlR/CLAMOXYL Ready To Use (Pfizer A.H.)amoxicilline (trihydrate): 150 mg/mlsuspension injectable im (Bo, Su, Ov, Ca, Fe),sc (Ca, Fe)Posologie:Bo, Su, Ov, Ca, Fe: 7 mg/kg pj (3 - 5 j)Viande: Bo: 25 j, Su: 26 j, Ov: 53 j - Lait: Bo:144 hf<strong>la</strong>con 6 x 100 mlR/
1 MEDICAMENTS ANTIBACTÉRIENS7DOKAMOX 100 mg/g premix (Sogeval Lab)amoxicilline (trihydrate): 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 20 mg/kg pj (5 j)Viande et abats: 5 jprém méd 25 kgR/premixDOKAMOX 80% (Emdoka)amoxicilline (trihydrate): 800 mg/gpoudre po dans l’eau de boisson, dans le <strong>la</strong>itPosologie:veau, Su, poulet: 2 x pj 10 mg/kg (3 - 5 j)Viande: veau: 4 j , Su: 3 j , vo<strong>la</strong>ille: 1 jNe pas utiliser chez des poules pondeusesdont les œufs sont destinés à <strong>la</strong> consommationhumaine.poudre 1000 gR/DUPHAMOX LA (Pfizer A.H.)amoxicilline trihydrate: 150 mg/mlsuspension injectable imPosologie:Bo, Su, Ov: 15 mg/kg pjPeut être répété après 48 hViande: Bo: 23 j, Su, Ov: 21 j, Lait: Bo: 84 hNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/LONGAMOX (Vétoquinol)amoxicilline (trihydrate): 150 mg/mlsuspension injectable imPosologie:Bo, Su, Ov: 2 x 15 mg/kg à 48 h d’intervalleViande: Bo: 50 j , Su: 50 j , Ov: 50 j, Lait: Bo: 3 jNe pas administrer aux moutons dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/MOXAJECT 15 % (VMD)amoxicilline (trihydrate): 150 mg/mlsuspension injectable imPosologie:Bo, Su: 15 mg/kg pj (3-5 j)Viande: Bo: 110 j , Su: 93 jNe pas utiliser chez les animaux pro<strong>du</strong>cteurs de<strong>la</strong>it destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/MOXAPULVIS 50 % (VMD)amoxicilline (trihydrate): 500 mg/gpoudre po dans l’eau de boissonPosologie:Su: 2 x pj 20 mg/kg (3-5 j)Viande: 2 jpoudre 1 kgR/OCTACILLIN pour porcs (Eurovet A.H.)amoxicilline (trihydrate): 697 mgpoudre dans l’eau de boisson poPosologie:Su: 14 mg/kg (3 - 5 j)Viande et abats: 2 jpoudre 500 g, 1 kgR/OCTACILLIN pour vo<strong>la</strong>ille (Eurovet A.H.)amoxicilline (trihydrate): 697 mg/gpoudre dans l’eau de boisson poPosologie:poulet: 10 - 20 mg poudre/kg pj (3 - 5 j)Viande: 24 hNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainepoudre 500 gR/ORIGIN (MSD A.H.)amoxicilline (trihydrate): 800 mg/gpoudre po avec l’eau de boissonPosologie:Su: 14 mg/kg (20 mg de poudre/kg) pj(3 - 5 j)poule: 7 - 14 mg/kg (10 - 20 mg de poudre/kg)pj (3 - 5 j)Viande: Su: 48 h, poule: 24 hNe pas administrer aux poules dont les œufssont destinés à <strong>la</strong> consommation humainepot 1 kgR/RHEMOX premix (In<strong>du</strong>strial Veterinaria)amoxicilline (trihydrate): 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su (sevrés): 15 mg amox/kg PV pj (15 j)Viande: 4 jprém méd 24 kgR/premixSURAMOX 5% premix (Virbac)amoxicilline (trihydrate): 5 g/100 gprémé<strong>la</strong>nge médicamenteux poPosologie:porcelet: 15 mg/kg (14 j)Viande: 4 jsac 25 kgR/premixSURAMOX 50% (Virbac)amoxicilline (trihydrate): 500 mgpoudre po avec l’aliment liquidePosologie:Su (sevrés): 20 mg/kg pj (5 j)Viande: 14 jpoudre 1 kgR/VETRIMOXIN 150 mg (Ceva Santé Animale)amoxicilline (trihydrate): 150 mgcomprimé poPosologie:Ca: 2 x pj 10 mg/kg (5 j)compr 500R/VETRIMOXIN 450 mg (Ceva Santé Animale)amoxicilline (trihydrate): 450 mgcomprimé poPosologie:Ca: 2 x pj 10 mg/kg (5 j)compr 20 x 8R/
8 1 MEDICAMENTS ANTIBACTÉRIENSVETRIMOXIN LA (Ceva Santé Animale)amoxicilline (trihydrate): 150 mg/mlsuspension injectable imPosologie:Bo: 15 mg/kg (répéter après 48 h)Su: 15 mg/kg pj (2 j)porcelet: 15 mg/kg pj (3 j)Viande et abats: Bo: 16 j, Su: 24 j,Lait: 6 traites (72 h)f<strong>la</strong>con 250 mlR/Aminopénicillines associées à uninhibiteur des bêta-<strong>la</strong>ctamasesIndications - spectre d’activité- résistancesL’association d’amoxicilline à un inhibiteurdes bêta-<strong>la</strong>ctamases commel’acide c<strong>la</strong>vu<strong>la</strong>nique se justifie par l’extension<strong>du</strong> spectre à des pathogènesimportants comme les staphylocoqueset certains germes GRAM- pro<strong>du</strong>cteursde bêta-<strong>la</strong>ctamases. Le recoursà l’association n’est indiqué que si <strong>la</strong>présence de germes résistants à uneaminopénicilline <strong>du</strong> fait de <strong>la</strong> pro<strong>du</strong>ctiond’une bêta-<strong>la</strong>ctamase est démontréeou suspectée.PharmacodynamieL’acide c<strong>la</strong>vu<strong>la</strong>nique est un inhibiteurdes bêta-<strong>la</strong>ctamases.PharmacocinétiqueLa pharmacocinétique de l’amoxicillinene semble pas être modifiée par <strong>la</strong>présence de l’acide c<strong>la</strong>vu<strong>la</strong>nique.Contre-indicationsVoir 1.1.1.1.Effets indésirablesUne intolérance intestinale peut parfoisse manifester.Interactions - PrécautionsparticulièresVoir 1.1.1.1.Repro<strong>du</strong>ction et <strong>la</strong>ctationTout comme l’amoxicilline, l’acide c<strong>la</strong>vu<strong>la</strong>niquediffuse à travers le p<strong>la</strong>centaet est excrété dans le <strong>la</strong>it. Aucun effettératogène n’a été observé.LMR amoxicilline et acidec<strong>la</strong>vu<strong>la</strong>nique: AMOXICLAV-VMD 50 mg (VMD)amoxicilline: 40 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mgcomprimé poPosologie:Ca, Fe: 2 x pj 10 mg d’amox/kg + 2,5 mgd’ac c<strong>la</strong>v/kg (5-7 j, ou plus longtemps sinécessaire)dose peut être doublée si nécessairecompr 10R/AMOXICLAV-VMD 250 mg (VMD)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé poPosologie:Ca: 2 x pj 10 mg d’amox/kg + 2,5 mg d’acc<strong>la</strong>v/kg (5-7 j, ou plus longtemps sinécessaire)dose peut être doublée si nécessairecompr 10R/AMOXICLAV-VMD 500 mg (VMD)amoxicilline: 400 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mgcomprimé poPosologie:Ca: 2 x pj 10 mg d’amox/kg + 2,5 mg d’acc<strong>la</strong>v/kg (5-7 j, ou plus longtemps sinécessaire)dose peut être doublée si nécessairecompr 2R/CLAVASEPTIN 50 mg (Vétoquinol)amoxicilline (trihydrate): 40 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mgcomprimé poPosologie:Ca, Fe: 2 x pj 10 mg d’amox/kg + 2.5 mgd’ac c<strong>la</strong>v/kg (7 j)le traitement pourra être prolongé de 7 j sinécessaire chez les Fecompr 10, 100R/CLAVASEPTIN 250 mg (Vétoquinol)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé poPosologie:Ca: 2 x pj 10 mg d’amox/kg + 2.5 mg d’acc<strong>la</strong>v/kg (7 j)compr 10, 100R/CLAVASEPTIN 500 mg (Vétoquinol)amoxicilline (trihydrate): 400 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mgcomprimé poPosologie:Ca: 2 x pj 10 mg d’amox/kg + 2.5 mg d’acc<strong>la</strong>v/kg (7 j)compr 10, 100R/CLAVOBAY 50 mg compr (Norbrook Lab)amoxicilline (trihydrate): 40 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mgcomprimé po avec l’alimentationPosologie:Ca, Fe: 2 x pj 12,5 mg/kg (5 - 7 j)compr 100R/CLAVOBAY 250 mg compr (Norbrook Lab)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé po avec l’alimentationPosologie:Ca: 2 x pj 12,5 mg/kg (5 - 7 j)compr 100R/
1 MEDICAMENTS ANTIBACTÉRIENS9CLAVOBAY compr appétents 500 mg (Norbrook Lab)amoxicilline (trihydrate): 400 mg/compracide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mg/comprcomprimé appétent po avec l’alimentationPosologie:Ca: 2 x pj 12,5 mg/kg (5 - 7 j)compr 100R/CLAVUBACTIN 50/12,5 (Le Vet)amoxicilline (trihydrate): 50 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 12,5 mgcomprimé poPosologie:Ca, Fe: 12,5 mg/kg 2 x pj (doubler éventuellement<strong>la</strong> dose), (5 - 10 j) (infect. cut. chron.:10 - 30 j, pyodermite profonde: 6 - 8 sem,cystite chron.: 10 - 28 j)compr 10, 100R/CLAVUBACTIN 250/62,5 (Le Vet)amoxicilline (trihydrate): 250 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 62,5 mgcomprimé poPosologie:Ca: 12,5 mg/kg 2 x pj (doubler éventuellement<strong>la</strong> dose) (5 - 10 j) (infect. cut. chron.:10 - 30 j, pyodermite profonde: 6 - 8 sem,cystite chron.: 10 - 28 j)compr 10, 100R/CLAVUBACTIN 500/125 (Le Vet)amoxicilline (trihydrate): 500 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 125 mgcomprimé poPosologie:Ca: 12,5 mg/kg 2 x pj (doubler éventuellement<strong>la</strong> dose), (5 - 10 j) (infect. cut. chron.:10 - 30 j, pyodermite profonde: 6 - 8 sem,cystite chron.: 10 - 28 j)compr 10, 100R/KESIUM 50 mg/12,5 mg compr à croquer chiens,chats (Sogeval)amoxicilline (trihydrate): 50 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 12,5 mgcomprimé à croquer poPosologie:Ca, Fe: 12,5 mg/kg 2 x pj (5-7 j, ou pluslongtemps si nécessaire) (dose peut êtredoublée si nécessaire)compr 10, 100R/KESIUM 200 mg/50 mg compr à croquer chiens(Sogeval)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé à croquer poPosologie:Ca: 12,5 mg/kg 2 x pj (5-7 j, ou plus longtempssi nécessaire) (dose peut être doubléesi nécessaire)compr 8, 96R/KESIUM 400 mg/100 mg compr à croquer chiens(Sogeval)amoxicilline (trihydrate): 400 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mgcomprimé à croquer poPosologie:Ca: 12,5 mg/kg 2 x pj (5-7 j, ou plus longtempssi nécessaire) (dose peut être doubléesi nécessaire)compr 12, 96R/NOROCLAV 50 mg (Norbrook Lab)amoxicilline (trihydrate): 40 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mgcomprimé po avec l’alimentationPosologie:Ca, Fe: 12,5 mg actif/kg 2 x pj (5 - 7 j, ouplus longtemps dans les cas chroniques)compr 20, 100, 500R/NOROCLAV 250 mg (Norbrook Lab)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé po avec l’alimentationPosologie:Ca: 12,5 mg actif/kg 2 x pj (5 - 7 j, ou pluslongtemps dans les cas chroniques)compr 4 x 5, 10 x 5, 50 x 5R/NOROCLAV 500 mg compr appétents chiens(Norbrook Lab)amoxicilline (trihydrate): 400 mg/compracide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mg/comprcomprimé appétent po avec l’alimentationPosologie:Ca: 12.5 mg actif/kg 2 x pj (5 - 7 j, ou pluslongtemps dans les cas chroniques)compr 25, 100R/NOROCLAV inj (Norbrook Lab)amoxicilline (trihydrate): 140 mg/m<strong>la</strong>cide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 35 mg/mlsuspension injectable im (Bo), sc (Ca)Posologie:Bo, Ca: 8,75 mg/kg pj (3 - 5 j)Viande et abats: 42 j, Lait: 60 h (5 traites)f<strong>la</strong>con 50 ml, 100 mlR/SYNULOX 500 mg bolus (Pfizer A.H.)amoxicilline (trihydrate): 400 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mgcomprimé poPosologie:veau: 2 x pj 6,25 à 12,5 mg/kgne pas admin aux animaux ruminantsViande: 10 jcompr 20R/SYNULOX compr appétents 50 mg (Pfizer A.H.)amoxicilline (trihydrate): 40 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mgcomprimé appétent poPosologie:Ca, Fe: 2 x pj 12,5 mg/kg (5 - 7 j)<strong>la</strong> dose peut être doubléecompr 10, 100R/
10 1 MEDICAMENTS ANTIBACTÉRIENSSYNULOX compr appétents 250 mg (Pfizer A.H.)amoxicilline (trihydrate): 200 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 50 mgcomprimé appétent poPosologie:Ca: 2 x pj 12,5 mg/kg (5 - 7 j)<strong>la</strong> dose peut être doubléecompr 10, 100R/SYNULOX compr appétents 500 mg (Pfizer A.H.)amoxicilline (trihydrate): 400 mgacide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 100 mgcomprimé appétent poPosologie:Ca: 2 x pj 12,5 mg/kg (5 - 7 j)<strong>la</strong> dose peut être doubléecompr 10, 100R/SYNULOX gouttes appétentes (Pfizer A.H.)amoxicilline (trihydrate): 40 mg/m<strong>la</strong>cide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 10 mg/mlpoudre poPosologie:Ca, Fe: 2 x pj 12,5 mg/kg (5 - 7 j)<strong>la</strong> dose peut être doubléef<strong>la</strong>con 15 mlR/SYNULOX READY TO USE (Pfizer A.H.)amoxicilline (trihydrate): 140 mg/m<strong>la</strong>cide c<strong>la</strong>vu<strong>la</strong>nique (potassium): 35 mg/mlsuspension injectable scPosologie:Ca, Fe: 8,75 mg/kg pj pendant 3 - 5 jf<strong>la</strong>con 12 x 50 mlR/1.1.1.2 CéphalosporinesTraditionnellement, les céphalosporinessont c<strong>la</strong>ssées par «générations»,de <strong>la</strong> première à <strong>la</strong> quatrième, quicorrespondent à une chronologie demise sur le marché et, dans une certainemesure, à leur spectre d’activité.Actuellement, il est cependant plusjudicieux de les c<strong>la</strong>sser en fonction deleurs propriétés cinétiques et de leurspectre d’activité.L’administration de médicamentsà usage systémique contenant descéphalosporines de 3 e ou 4 e génération(cefquinome, ceftiofur), destinés àdes animaux pro<strong>du</strong>cteurs d’aliments,fait l’objet d’importantes restrictions.Voir pour plus d’informations le FoliaVeterinaria 2012 n° 2.Indications - spectre d’activité -résistances- Les céphalosporines <strong>du</strong> premiergroupe, comme <strong>la</strong> céfalexine, ont unspectre proche de celui des benzylpénicillines.Elles sont donc essentiellementactives sur les GRAM+ maisaussi sur les staphylocoques pro<strong>du</strong>cteursde pénicillinases, et quelquesbactéries GRAM- (pas les entérobactéries,ni Pseudomonas aeruginosa parexemple).- Celles <strong>du</strong> deuxième groupe, comprenantle ceftiofur, <strong>la</strong> cefquinome et <strong>la</strong>céfovécine, ont un spectre d’activitéproche de celui des aminopénicillines,é<strong>la</strong>rgi à de nombreux GRAM- (entérobactériespar exemple) y compris lessouches sécrétrices de bêta-<strong>la</strong>ctamases,mais restent inactives contrePseudomonas aeruginosa.- Les céphalosporines <strong>du</strong> troisièmegroupe ont un spectre d’activitévariable mais englobent uneactivité contre Pseudomonas aeruginosa(voir 12.5. Médicaments à usageintra-mammaire).- Les céphalosporines <strong>du</strong> quatrièmegroupe ne comprennent pas de principeactif à usage vétérinaire.D’une manière générale, l’é<strong>la</strong>rgissement<strong>du</strong> spectre s’accompagne d’uneactivité moins marquée vis-à-vis desGRAM+. Pour plus d’information sur <strong>la</strong>résistance contre les céphalosporines,voir Folia Veterinaria 2009 n° 1.Afin de favoriser l’usage rationnel descéphalosporines de 3 e ou de 4 e génération(cefquinome, ceftiofur) à usagesystémique chez les animaux pro<strong>du</strong>cteursd’aliments et de préserver ainsil’efficacité de ces médicaments aussibien en médecine vétérinaire qu’enmédecine humaine, quelques restrictionset mises en garde majeures ontété imposées au niveau européen. LesRCP des médicaments concernés ontdû être adaptés (Folia Veterinaria 2012n° 2). Le recours à l’antibiogrammedevrait être systématiquement appliquéavant <strong>la</strong> mise en p<strong>la</strong>ce de cestraitements.PharmacodynamieLes céphalosporines possèdent uncycle dihydrothiazine attaché au noyaubêta-<strong>la</strong>ctame, qui augmente leur résistanceaux bêta-<strong>la</strong>ctamases. Leur mécanismed’action est semb<strong>la</strong>ble à celuides pénicillines. Voir 1.1.1.1.PharmacocinétiqueLa céfalexine est utilisée par voieorale ou parentérale. Sa biodisponibilitéorale, indépendante <strong>du</strong> repas, etsa distribution tissu<strong>la</strong>ire sont comparablesà celles des aminopénicillines.Le ceftiofur et <strong>la</strong> cefquinome sontutilisés par voie parentérale, sont rapidementrésorbés après injection IM ouSC et sont éliminés majoritairementpar voie urinaire et secondairement parvoie biliaire.
1 MEDICAMENTS ANTIBACTÉRIENS11La céfovécine se différencie desautres céphalosporines par sa forteliaison aux protéines et sa longue demivied’élimination avec une longue <strong>du</strong>réed’action chez le chien et le chat. Lacéfovécine est principalement excrétéesous sa forme active inchangéedans les urines.Contre-indicationsLa toxicité de <strong>la</strong> céfalexine est trèsfaible, mais des réactions allergiques,parfois croisées avec les pénicillines,sont rarement observées. Chez lescarnivores, l’administration orale peutparfois provoquer des vomissementset de <strong>la</strong> diarrhée.Effets indésirables – Interactions -Précautions particulières -Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir 1.1.1.1.Premier groupe: céphalosporinessurtout actives contre les GRAM+LMR céfalexine: CEFALEXINE Ke<strong>la</strong> 50 mg (Ke<strong>la</strong> Laboratoria)céfalexine (monohydrate): 50 mg/comprcomprimé poPosologie:Ca: 2 x pj 10 - 15 mg/kg (5 j, peut êtreprolongé)Dose peut être doubléecompr 20R/CEFALEXINE Ke<strong>la</strong> 250 mg (Ke<strong>la</strong> Laboratoria)céfalexine (monohydrate): 250 mg/comprcomprimé poPosologie:Ca: 2 x pj 10 - 15 mg/kg (5 j, peut êtreprolongé)Dose peut être doubléecompr 10, 100R/CEFASEPTIN Forte (Vétoquinol)céfalexine (monohydrate): 600 mgcomprimé poPosologie:Ca: 2 x pj 25 mg/kg (1 à 3 sem)compr 30 et 200R/CEFASEPTIN Mite (Vétoquinol)céfalexine (monohydrate): 120 mgcomprimé poPosologie:Ca, Fe: 2 x pj 25 mg/kg (1 à 3 sem)compr 30 et 150R/CEPHACARE FLAVOUR 250 mg (Animalcare)céfalexine (monohydrate): 250 mgcomprimé poPosologie:Ca: 2 x pj 15 mg/kg (5 j)La dose peut être doublée, le traitementpeut être prolongécompr 100R/CEPHACARE FLAVOUR 500 mg (Animalcare)céfalexine (monohydrate): 500 mgcomprimé poPosologie:Ca: 2 x pj 15 mg/kg (5 j)La dose peut être doublée, le traitementpeut être prolongécompr 100R/CEPOREX 50 mg (MSD A.H.)céfalexine: 50 mgcomprimé poPosologie:Ca, Fe: 2 x pj 10 - 15 mg/kg (5 j)La dose peut être doublée, le traitementpeut être prolongécompr 20R/CEPOREX 250 mg (MSD A.H.)céfalexine: 250 mgcomprimé poPosologie:Ca: 2 x pj 10 - 15 mg/kg (5 j)La dose peut être doublée, le traitementpeut être prolongécompr 10R/CEPOREX inj (MSD A.H.)céfalexine (sodique): 180 mg/mlsuspension injectable sc, imPosologie:Bo: 7 mg/kg pj (5 j)Ca, Fe: 10 mg/kg pj (5 j)Viande: Bo: 19 j, Lait: 0 jf<strong>la</strong>con 100 mlR/KEFAVET VET 250 mg, 500 mg (Orion Corp)céfalexine (monohydrate): 250 mg ou 500 mgcomprimé enrobé poPosologie:Ca:infect. voies urin.: 2 x pj 15 mg/kg (14 j)infect. sévères de <strong>la</strong> peau: 2 x pj 25 - 30 mg/kg(min 3 sem, éventuellement 4 - 6 sem encas de pyodermite prof.)compr 14 x 250 mg, 14 ou 70 x 500 mgR/RILEXINE 75 (Virbac)céfalexine (monohydrate): 75 mgcomprimé poPosologie:Ca, Fe: 2 x pj 15 mg/kg (5 j)compr 14, 210R/RILEXINE 300 (Virbac)céfalexine (monohydrate): 300 mgcomprimé poPosologie:Ca: 2 x pj 15 mg/kg (5 j)compr 14, 210R/RILEXINE 600 (Virbac)céfalexine (monohydrate): 600 mgcomprimé poPosologie:Ca: 2 x pj 15 mg/kg (5 j)compr 14, 210R/
12 1 MEDICAMENTS ANTIBACTÉRIENSTHERIOS 75 mg compr à croquer chats (Sogeval Lab)céfalexine (monohydrate): 75 mg/comprcomprimé à croquer poPosologie:Fe: 15 mg/kg 2 x pj (p<strong>la</strong>ies et abcès: 5 j,infect voies urinaires: 10 à 14 j, pyodermie:min 14 j et poursuivre le traitement pendant10 j après <strong>la</strong> disparition des lésions)compr 20, 100R/THERIOS 300 mg compr appétents chiens(Sogeval Lab)céfalexine (monohydrate): 300 mg/comprcomprimé appétent poPosologie:Ca: 2 x pj 15 mg/kg (14 j en cas d’infectvoies urinaires, min 15 j en cas de dermatiteinfect superf, min 28 j en cas de dermatiteinfect profonde)(<strong>la</strong> dose peut être doublée)compr 10, 200R/THERIOS 750 mg compr appétents chiens(Sogeval Lab)céfalexine (monohydrate): 750 mg/comprcomprimé appétent poPosologie:Ca: 2 x pj 15 mg/kg (14 j en cas d’infectvoies urinaires, min 15 j en cas de dermatiteinfect superf, min 28 j en cas de dermatiteinfect profonde)(<strong>la</strong> dose peut être doublée)compr 10, 200R/Deuxième groupe: céphalosporinesà spectre é<strong>la</strong>rgiLMR céfovécine, cefquinome,ceftiofur: CEFENIL (Norbrook Lab)ceftiofur (sodique): 1 g ou 4 gsolution reconstituée contient 50 mg ceftiofur/mlpoudre et solvant pour solution injectable imPosologie:Bo: 1 mg/kg pj (panaris interdigité: 3 j ouma<strong>la</strong>die resp: 3-5 j)Su: 3 mg/kg pj pendant 3 j (ma<strong>la</strong>die resp)Viande: Bo: 2 j, Su: 2 j, Lait: Bo: 0 h1 x, 6 x, 12 x f<strong>la</strong>cons avec poudre (1g ou 4 g) etf<strong>la</strong>con avec solvant (20 ml, 80 ml)R/CEFFECT 25 mg/ml (Emdoka)cefquinome (sulfate): 25 mg/mlsuspension injectable imPosologie:Bo: 1 mg/kg pj (2 - 5 j)veau: 2 mg/kg pj (3 - 5 j)Su: 2 mg/kg pj (2 - 3 j)porcelet: 2 mg/kg pj (5 j)Viande et abats: Bo: 5 j, Su: 3 j, Lait: Bo: 24 hf<strong>la</strong>con 100 mlR/CEFTIOCYL 50 mg/ml susp inj bovin et porc(Vétoquinol)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable sc (Bo), im (Su)Posologie:Su: 3 mg/kg pj (3 j)Bo:- infec resp: 1 mg/kg (3 - 5 j)- panaris interdigité: 1 mg/kg (3 j)- métrite puerpuérale aigüe: 1 mg/kg (5 j)Viande Bo: 8 j, Lait Bo: 0 h, Viande Su: 6 jf<strong>la</strong>con 100 mlR/CEFTIOSAN 50 mg/ml susp inj porc, bovin(Alfasan)ceftiofur: 50 mg/mlsuspension injectable sc (Bo), im (Su)Posologie:Bo:- infect resp bactér: 1 mg/kg pj (3 à 5 j)- nécrobacillose interdigitale aiguë:1 mg/kg pj (3 j)- métrite post-partum aiguë (< 10 j aprèsvê<strong>la</strong>ge): 1 mg/kg pj (5 j)Su:- infect resp bactér: 3 mg/kg pj (3 j)Viande et abats: Bo: 8 j, Su: 8 j, Lait: 0 hf<strong>la</strong>con 100 ml, 250 mlR/CEVAXEL 50 mg/ml (Ceva Santé Animale)ceftiofur (sodium): 50 mg/ml de solpoudre et solvant pour solution injectable imPosologie:Bo:infect resp: 1 mg/kg pj (3 - 5 j)panaris interdigité: 1 mg/kg pj (3 j)Su: 3 mg/kg pj (3 j)Viande et abats: Bo: 2 j, Su: 2 j, Lait: 0 jf<strong>la</strong>con 4 g de poudre + 80 ml de diluantR/CEVAXEL RTU 50 mg/ml (Ceva Santé Animale)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable sc (Bo), im (Su)Posologie:Bo:infect resp: 1 mg/kg pj (3-5 j)panaris interdigité: 1 mg/kg pj (3 j)métrite post-partum aiguë: 1 mg/kg pj (5 j)(dans les 10 j suivant le vê<strong>la</strong>ge)Su: 3 mg/kg pj (3 j)Viande et abats: Bo: 8 j, Su: 5 j, Lait Bo: 0 hf<strong>la</strong>con 100 mlR/COBACTAN 2,5% (MSD A.H.)cefquinome (sulfate): 25 mg/mlsuspension injectable imPosologie:Bo: 1 mg/kg pj (3 - 5 j) ( 2 j en cas demammite E. coli)veau: 2 mg/kg pj (3 - 5 j)Su: 2 mg/kg pj (3 j) (2 j en cas de MMA)porcelet: 2 mg/kg pj (5 j)Viande: Bo: 5 j, Su: 3 j, Lait: 24 hf<strong>la</strong>con 100 mlR/
1 MEDICAMENTS ANTIBACTÉRIENS13COBACTAN 4,5% (MSD A.H.)cefquinome (sulfate): 45 mg/mlpoudre et solvant pour solution injectable im(Eq, Bo), iv (Eq)Posologie:Eq: 1 x 1 mg/kg pj (5 - 10 j, cesser le traitement2 j après disparition des signescliniques)pou<strong>la</strong>in: 2 x 1 mg/kg pj (6 - 14 j, cesser letraitement 3 j après disparition des signescliniques)Bo: 1 x 1 mg/kg pj (3 - 5 j) ( 2 j en cas demammite E. coli)veau: 1 x 2 mg/kg pj (3 - 5 j)Viande: Eq: 4 j, Bo: 2 j, Lait: Bo: 36 h (3 traites)Ne pas administrer aux Eq <strong>la</strong>ctants dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 30 ml, 100 mlR/COBACTAN LA 7,5% (MSD A.H.)cefquinome (sulfate): 75 mg/mlsuspension injectable scPosologie:Bo: 2 x 2,5 mg/kg à 48 h d’intervalleViande, abats: 13 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine (en périodede <strong>la</strong>ctation et de tarissement) ni dans les 2 mprécédant <strong>la</strong> première mise bas des Bo dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/CONVENIA (Pfizer A.H.)céfovecine (sodique): 852 mg/f<strong>la</strong>conpoudre lyophilisée pour solution injectable scPosologie:Après reconstitution: 80 mg/ml de céfovecinedans <strong>la</strong> solCa, Fe (âge > 8 sem):infect. peau, tissus mous: 1 x 8 mg/kg (peutêtre répété jusqu’à 3 x chez le Ca et 1 xchez le Fe à 14 j d’intervalle)infect. urin.: 1 x 8 mg/kgCa: infect de <strong>la</strong> gencive + des tissus parodontaux:1 x 8 mg/kg1 f<strong>la</strong>con de poudre + 1 f<strong>la</strong>con de solvant (10 ml)R/EFICUR 50 mg/ml (Hipra Lab)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable sc (Bo), im (Su)Posologie:Bo:- infect resp: 1 mg/kg pj sc (3 - 5 j)- nécrobacillose interdigit aiguë:1 mg/kg pj sc (3 j)- métrite post-partum dans les 10 j aprèsmise bas: 1 mg/kg pj sc (5 j) (thérapie desoutien complémentaire peut être requise)Su: 3 mg/kg pj im (3 j)Viande et abats: Bo: 8 j, Su: 5 jLait: 0 jf<strong>la</strong>con 100 ml, 250 mlR/EXCENEL (Pfizer A.H.)ceftiofur (sodique): 1 g , 4 gpoudre pour solution injectable im (Bo, Su)Posologie:Bo: 1 mg/kg/24h (infect. resp.: 3 - 5 j, nécrobaccilloseinterdigit.: 3 j)Su: 3 mg/kg/24h (3 j)Viande: Bo: 48 h, Su: 48 h, Lait: 0 hpoudre 1 g, 4 gR/EXCENEL RTU (Pfizer A.H.)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable im (Su), sc (Bo)Posologie:Bo: 1 mg/kg pj (3 - 5 j)Su: 3 mg/kg pj (3 j)Viande: Bo: 8 j, Su: 5 j, Lait: 0 jf<strong>la</strong>con 100 mlR/NAXCEL bovins (Pfizer A.H.)ceftiofur: 200 mg/mlsuspension injectable scPosologie:Bo: 1 x 6,6 mg/kgViande: Bo: 9 j, Lait: Bo: 0 jf<strong>la</strong>con 100 mlR/NAXCEL porcs (Pfizer A.H.)ceftiofur: 100 mg/mlsuspension injectable imPosologie:Su: 1 x 5 mg/kgViande: 71 jf<strong>la</strong>con 100 mlR/READYCEF 50 mg/ml (Lab Calier)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable im (Su), sc (Bo)Posologie:Bo:- infect resp: 1 mg/kg pj (3 à 5 j)- nécrobacillose interdigit aiguë:1 mg/kg pj (3 j)- métrite post-partum aiguë: 1 mg/kg pj (5 j)dans les 10 j après le vê<strong>la</strong>geSu: 3 mg/kg pj (3 j)Viande et abats: Su: 5 j, Bo: 8 jLait: 0 jf<strong>la</strong>con 100 mlR/TRULEVA RTU (Continental Farmacéutica S.L.)ceftiofur (chlorhydrate): 50 mg/mlsuspension injectable sc (Bo), im (Su)Posologie:Bo:infec resp: 1 mg/kg pj (3-5 j)nécrose interdigitée: 1 mg/kg pj (3 j)métrite puerpérale: 1 mg/kg pj (5 j)Su: 3 mg/kg pj (3 j)Viande et abats: Bo: 8 j, Su: 5 j, <strong>la</strong>it: Bo: 0 jf<strong>la</strong>con 100 mlR/
14 1 MEDICAMENTS ANTIBACTÉRIENS1.1.2 AminosidesAminosides utilisés en cas de diarrhée : voir chapitre 4.5.1.Indications - spectre d’activité - résistancesLeur action bactéricide s’exerce surtout sur les bactéries aérobies GRAM- ainsique sur certains mycop<strong>la</strong>smes et mycobactéries. Leur efficacité diminue en milieuanaérobie, acide et/ou purulent.Les aminosides comprennent les principes actifs suivants:- La streptomycine (non commercialisée en Belgique) possède un spectre d’activitééten<strong>du</strong> aux mycobactéries ainsi qu’à certains mycop<strong>la</strong>smes et staphylocoques,mais elle est inactive contre les genres Pseudomonas et Proteus.- Les néomycines regroupent <strong>la</strong> néomycine (voir chapitre 1.1.9 Associations,chapitre 12.5.1.6 Associations utilisées en cas de mammite), <strong>la</strong> kanamycine (voir12.5.1.6 Associations pour le traitement des mammites) et <strong>la</strong> paromomycine.Elles sont plus actives que <strong>la</strong> streptomycine sur les staphylocoques et dans unemoindre mesure sur les streptocoques. De nombreux pseudomonas sont sensiblesà <strong>la</strong> néomycine, mais pas Pseudomonas aeruginosa.- La gentamicine et l’apramycine (voir chapitre 4.5. Antidiarrhéiques contenantdes agents anti-infectieux) sont les aminosides les plus actifs. Leur spectres’étend à de nombreuses bactéries GRAM+, GRAM- (E. coli et les salmonellesnotamment), aux mycop<strong>la</strong>smes et à Pseudomonas aeruginosa.- Le spectre d’action de <strong>la</strong> spectinomycine (voir aussi chapitre 4.5. Antidiarrhéiquescontenant des agents anti-infectieux) se rapproche de celui de <strong>la</strong> streptomycine.Les pseudomonas y sont résistants. La spectinomycine est utilisée pour le traitementdes infections par les mycop<strong>la</strong>smes et certaines bactéries GRAM- commeles germes coliformes, les salmonelles et les pasteurelles. Elle est également utiliséeen association avec <strong>la</strong> lincomycine.PharmacodynamieLes aminosides ou aminoglycosides sont des antibiotiques à effet bactéricide qui,après pénétration à travers <strong>la</strong> paroi bactérienne, interfèrent avec <strong>la</strong> sous-unité 30S des ribosomes pour inhiber <strong>la</strong> synthèse protéique.PharmacocinétiqueLes aminosides sont utilisés per os ou par voie parentérale. Leur absorption esttrès faible si le tube digestif est intact, mais <strong>la</strong> voie orale peut être conseilléeen cas d’infection localisée <strong>du</strong> tube digestif par des GRAM-. Les préparations àusage oral sont répertoriées dans le chapitre des médicaments <strong>du</strong> tube digestif(4.5.1.). Après une administration parentérale, <strong>la</strong> distribution des aminosides selimite aux fluides extracellu<strong>la</strong>ires. Les aminosides franchissent difficilement lesbarrières biologiques et n’atteignent que de faibles concentrations dans le <strong>la</strong>it, lessécrétions bronchiques ou le liquide cérébrospinal. Ils sont éliminés par filtrationgloméru<strong>la</strong>ire. L’insuffisance rénale et <strong>la</strong> déshydratation provoquent une augmentationdes concentrations sériques <strong>du</strong> fait de l’impact de ces pathologies sur <strong>la</strong>c<strong>la</strong>irance et le volume de distribution. En cas d’obésité, une posologie rapportéeau poids corporel réel aboutit au même résultat. Vu <strong>la</strong> faible marge de sécurité, lesélévations de concentrentions sont rapidement associées à des signes toxiques.Effets indésirablesTous les aminosides peuvent causer, à des degrés variables, de l’ototoxicité, particulièrementchez le chat, et de <strong>la</strong> néphrotoxicité. Les jeunes animaux sont plussensibles. Les aminosides peuvent également pro<strong>du</strong>ire un blocage neuromuscu<strong>la</strong>ireal<strong>la</strong>nt jusqu’à <strong>la</strong> paralysie et l’apnée, surtout lors d’anesthésie et en cas d’associationavec des myore<strong>la</strong>xants. Ce blocage peut être levé par l’administrationde néostigmine ou de gluconate de calcium. L’administration IV peut égalementdonner lieu à un effet cardiodépresseur consécutif à l’hypocalcémie. La spectinomycine,un aminocyclitol, de structure chimique différente des aminosides, nesemble pas aussi toxique.InteractionsLa combinaison avec les diurétiques (furosémide, mannitol) accroît <strong>la</strong> néphrotoxicitédes aminosides. L’ototoxicité est aggravée par l’administration de diurétiquescomme le furosémide. De <strong>la</strong> synergie avec des antibiotiques bactéricides,comme les bêta-<strong>la</strong>ctamines, existe vis-à-vis de certaines bactéries (voir 1.1.9Associations).
1 MEDICAMENTS ANTIBACTÉRIENS15Précautions particulièresUne surveil<strong>la</strong>nce de <strong>la</strong> fonction rénale est conseillée. La marge de sécurité étantfaible, il est indispensable de diminuer <strong>la</strong> posologie des aminosides chez les patientsobèses, déshydratés ou atteints de troubles rénaux. L’administration IV peutégalement donner lieu à un effet cardiodépresseur consécutif à l’hypocalcémie.La néomycine, en raison de sa toxicité très prononcée, devrait être réservée auxtraitements oraux des infections digestives ou à un usage local. La plus grandeprudence s’impose lorsque cet antibiotique est administré par voie parentérale,d’autant plus que des alternatives thérapeutiques existent au sein de ce groupepharmacothérapeutique.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes aminosides diffusent à travers le p<strong>la</strong>centa et dans de rares cas, peuventengendrer des symptômes neurologiques (toxicité <strong>du</strong> nerf crânien VIII) ounéphrologiques chez le fœtus. Les quantités excrétées dans le <strong>la</strong>it semblent minimaleset le risque pour les animaux al<strong>la</strong>ités semble donc minime.1.1.2.1 Gentamicine1.1.2.3 SpectinomycineLMR gentamicine: GENTA-kel 5 % (Ke<strong>la</strong> Laboratoria)gentamicine (sulfate): 50 mg/mlsolution injectable imPosologie:veau: 2 - 3 mg/kg pj (3 j)Viande: 155 jf<strong>la</strong>con 100 mlR/GENTAVETO-5 (VMD)gentamicine (sulfate): 50 mg/mlsolution injectable imPosologie:Su (porcelet): 2 x 5 mg/kg pj (5 j)Viande: 146 jf<strong>la</strong>con 100 mlR/1.1.2.2 ParomomycineLMR spectinomycine: SPECTAM SCOUR-HALT (Ceva Santé Animale)spectinomycine (chlorhydrate) : 50 mg/mlsolution poPosologie:porcelet: posologie de base:20 mg/kg/12 h (3 j)Viande: 12 jf<strong>la</strong>con 100 mlR/LMR paromomycine: GABBROVET (Ceva Santé Animale)paromomycine sulfate: 175.000 UI/mlsolution injectable imPosologie:Su (< 50 kg): 14 mg/kg pj (3-5 j)Viande: Su: 16 jf<strong>la</strong>con 100 mlR/GABBROVET 70 (Ceva Santé Animale)paromomycine sulfate: 100 mg/gpoudre po dans le <strong>la</strong>it ou l’eau de boissonPosologie:veau (non ruminant): 25 - 50 mg/kgpj (3 - 5 j) (<strong>la</strong>it)Su: 25 - 40 mg/kg pj (3 - 5 j) (eau deboisson)Viande: veau (non ruminant): 20 j, Su: 2 jpoudre 1 kgR/
16 1 MEDICAMENTS ANTIBACTÉRIENS1.1.3 FlorfénicolLe florfénicol est un analogue <strong>du</strong> chloramphénicol. Son principal avantage estqu’il ne provoque pas de dépression mé<strong>du</strong>l<strong>la</strong>ire irréversible chez l’homme. Pourcette raison, il peut être utilisé chez les animaux destinés à <strong>la</strong> consommationhumaine, contrairement au chloramphénicol.Indications - spectre d’activité - résistancesC’est un antibiotique bactériostatique à très <strong>la</strong>rge spectre, actif contre <strong>la</strong> plupartdes bactéries GRAM+ et – , aérobies et anaérobies (les genres Proteus etPseudomonas sont naturellement résistants), les rickettsies, les ch<strong>la</strong>mydies, ainsique certains mycop<strong>la</strong>smes. Des résistances sont apparues chez certaines entérobactéries.En règle générale, les résistances au florfénicol sont croisées aveccelles au chloramphénicol, tandis que l’inverse n’est pas toujours vrai.L’usage <strong>du</strong> florfénicol est à réserver aux infections graves.PharmacodynamieLe florfénicol est un puissant inhibiteur de <strong>la</strong> synthèse protéique bactérienne. Il selie de manière irréversible à <strong>la</strong> sous-unité 50 S des ribosomes.PharmacocinétiqueLe florfénicol se distribue dans tout l’organisme, y compris le système nerveuxcentral et l’humeur aqueuse, et traverse bien les barrières biologiques. Il est enpartie métabolisé au niveau <strong>du</strong> foie et éliminé sous forme active par les reins.Contre-indicationsL’administration intraveineuse ou l’administration à des verrats ou des taureauxde repro<strong>du</strong>ction est contre-indiquée.Effets indésirablesRéaction sur le site d’injection.InteractionsAucune interaction spécifique connue.Précautions particulièresL’usage <strong>du</strong> florfénicol est à réserver aux infections graves.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas administrer aux taureaux et verrats destinés à <strong>la</strong> repro<strong>du</strong>ction. Aucun effetembryo- ou fœtotoxique n’a été observé chez les animaux de <strong>la</strong>bo. L’administrationchez des espèces cibles en période de gestation ou de <strong>la</strong>ctation n’a pas été étudiée.LMR florfénicol: COLFEN 300 mg/ml sol inj bovins, porcins (Pfizer A.H.)florfénicol: 300 mg/mlsolution injectable im (Bo, Su), sc (Bo)Posologie:Bo:- traitement: 20 mg/kg (im) (repéter après 48 h)ou 1 x 40 mg/kg (sc)- prévention: 1 x 40 mg/kg (sc)Su: 15 mg/kg (im) (repéter après 48 h)Viande: Bo: 30 j (im) ou 44 j (sc), Su: 18 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/FENFLOR 300 mg/ml sol inj bovins (KRKA)florfénicol: 300 mg/mlsolution injectable imPosologie:Bo traitement:2 x 20 mg/kg (im), à 48 h d’intervalle1 x 40 mg/kg (sc)Bo prévention:1 x 40 mg/kg (sc)Viande et abats Bo: 30 j (im) ou 44 j (sc)Lait Bo: ne pas utiliser chez les animaux dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/FENFLOR 300 mg/ml sol inj porcs (KRKA)florfénicol: 300 mg/mlsolution injectable imPosologie:Su (PV > 2 kg):2 x 15 mg/kg à 48 h d’intervalleViande: 18 jf<strong>la</strong>con 250 mlR/FLORFENIKEL 300 mg/ml (Ke<strong>la</strong> Laboratoria)florfenicol: 300 mg/mlsolution injectable imPosologie:Su (PV > 2 kg):2 x 15 mg/kg à 48 h d’intervalleViande et abats: 18 jf<strong>la</strong>con 100 ml, 250 mlR/FLORGANE 300 mg/ml susp inj bovins (Emdoka)florfénicol: 300 mg/mlsuspension injectable imPosologie:Bo: 1 x 30 mg/kgViande et abats: Bo: 37 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/
1 MEDICAMENTS ANTIBACTÉRIENS17FLORKEM 300 mg/ml sol inj bovins et porcins(Ceva Santé Animale)florfénicol: 300 mg/mlsolution injectable imPosologie:Bo: 2 x 20 mg/kg à 48 h d’intervalleSu (PV > 2 kg):2 x 15 mg/kg à 48 h d’intervalleViande et abats: Bo: 37 j, Su: 18 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/KEFLORIL 300 mg/ml sol inj bovins et porcs(Vétoquinol)florfénicol: 300 mg/mlsolution injectable im, scPosologie:Bo traitement:(im) 2 x 20 mg/kg à 48 h d’intervalle(sc) 1 x 40 mg/kgBo prévention:(sc) 1 x 40 mg/kgSu: 2 x 15 mg/kg (im) à 48 h d’intervalleBo Viande: 30 j (im), 44 j (sc), Su: Viande: 18 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 et 250 mlR/NUFLOR sol inj 300 mg/ml (MSD A.H.)florfénicol: 300 mg/mlsolution injectable im, scPosologie:- traitementBo ( im): 20 mg/kg (2 x à 48 h d’intervalle)Bo (sc): 40 mg/kg (1 x)- préventionBo (sc): 40 mg/kg (1 x)Viande: 30 j (im), 44 j (sc)Ne pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineNe pas administrer aux taureaux de repro<strong>du</strong>ctiona<strong>du</strong>ltesf<strong>la</strong>con 100 ml, 250 mlR/SELECTAN (Hipra Lab)florfénicol: 300 mg/mlsuspension injectable imPosologie:Bo: 20 mg/kg (2 x à 48 h d’intervalle)Su, porcelet (PV > 2 kg):15 mg/kg 2 x à 48 h d’intervallene pas admin aux taureaux destinés à <strong>la</strong>repro<strong>du</strong>ctionViande: Bo: 30 j, Su: 18 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/SELECTAN oral (Hipra Lab)florfénicol: 23 mg/mlsolution po dans l’eau de boissonPosologie:Su: 10 mg/kg pj (5 j)Viande et abats: 20 jbaril 5 lR/SHOTAFLOR 300 mg/ml sol inj bovins (Virbac)florfénicol: 300 mg/mlsolution injectable im, scPosologie:Bo traitement:2 x 20 mg/kg (im), à 48 h d’intervalle1 x 40 mg/kg (sc)Bo prévention:1 x 40 mg/kg (sc)Viande et abats: 30 j (im), 44 j (sc)Ne pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/SHOTAFLOR 300 mg/ml sol inj porcs (Virbac)florfénicol: 300 mg/mlsolution injectable imPosologie:Su (>2 kg): 2 x 15 mg/kg à 48 h d’intervalleViande: 18 jf<strong>la</strong>con 250 mlR/1.1.4 TétracyclinesIndications - spectre d’activité - résistancesLes tétracyclines sont des antibiotiques bactériostatiques dont le spectred’activité s’étend à de nombreuses bactéries GRAM+ et GRAM-, aérobies etanaérobies, aux mycop<strong>la</strong>smes, aux ch<strong>la</strong>mydies, aux rickettsies et à certainsprotozoaires (babésiose, theilériose). Des résistances se sont cependant développéeschez de nombreuses bactéries aérobies et anaérobies. Les mycobactéries,et les genres Proteus et Pseudomonas sont naturellement résistants.PharmacodynamieLes tétracyclines agissent par inhibition de <strong>la</strong> synthèse protéique en interférantavec <strong>la</strong> sous-unité 30 S ribosomale. Leur effet bactériostatique est optimal enmilieu acide.PharmacocinétiqueLes tétracyclines sont des substances amphotères faiblement solubles dans l’eauà pH 7. Elles sont disponibles sous forme orale et parentérale. Des préparations«long acting» (LA) à base d’oxytétracycline sont disponibles. La biodisponibilitéorale des tétracyclines est bonne chez le chien et le chat, mais varie fortementselon <strong>la</strong> forme galénique et le type de molécule. Elle est faible chez le porc et <strong>la</strong>vo<strong>la</strong>ille. Sauf pour <strong>la</strong> doxycycline, l’absorption orale diminue avec le repas, notammentà base de <strong>la</strong>it. Les tétracyclines sont également ché<strong>la</strong>tées par les ionsdivalents présents, par exemple, dans les antiacides. La qualité de l’eau de boissonet les matériaux des auges et des abreuvoirs peuvent fortement influencer <strong>la</strong>
18 1 MEDICAMENTS ANTIBACTÉRIENSbiodisponibilité. Leur forte liposolubilité leur permet de bien diffuser à travers lesbarrières biologiques et atteindre des concentrations efficaces, y compris dansles milieux intracellu<strong>la</strong>ires, notamment dans le p<strong>la</strong>centa, les g<strong>la</strong>ndes mammaires,les sécrétions bronchiques et les liquides d’ascite. Seules les plus liposolubles,comme <strong>la</strong> minocycline (non disponible sur le marché belge) et <strong>la</strong> doxycycline,atteignent des concentrations efficaces dans <strong>la</strong> prostate, <strong>la</strong> salive, les <strong>la</strong>rmes. Laliaison aux protéines de ces molécules limite leur diffusion dans le liquide céphalo-rachidien.L’oxytétracycline est éliminée par filtration gloméru<strong>la</strong>ire sous formeactive et accessoirement, par <strong>la</strong> bile. Le cycle entéro-hépatique prolonge <strong>la</strong> demivied’élimination. Il peut aussi être à l’origine d’une dérive de <strong>la</strong> flore intestinale. Ladoxycycline, très liposoluble, est essentiellement éliminée par voie digestive aprèspassage <strong>du</strong> sang vers <strong>la</strong> lumière intestinale et dans une moindre mesure par <strong>la</strong>bile. L’élimination de <strong>la</strong> doxycycline est indépendante de <strong>la</strong> filtration gloméru<strong>la</strong>irece qui permet son utilisation en cas de troubles rénaux.Contre-indicationsLeur emploi est à éviter chez le cheval, car elles peuvent in<strong>du</strong>ire, même par voieparentérale, une dérive de <strong>la</strong> flore intestinale.Effets indésirablesLes tétracyclines sont des antibiotiques re<strong>la</strong>tivement peu toxiques. Elles peuventprovoquer des vomissements et de <strong>la</strong> diarrhée lors d’administration orale ou deslésions tissu<strong>la</strong>ires à l’endroit d’injection, surtout avec les formes à action longue.Cette caractéristique pose le problème de <strong>la</strong> rémanence des rési<strong>du</strong>s au niveau <strong>du</strong>site d’injection. De plus, ces formes «long acting» peuvent contenir de <strong>la</strong> pyrrolidone,parfois à l’origine de réactions anaphy<strong>la</strong>ctiques. La capacité des tétracyclinesà fixer le calcium est responsable de dépôts au niveau des os et des dentsen croissance, donnant à celles-ci une coloration jaune. Des troubles cardiovascu<strong>la</strong>ireset de l’hypocalcémie ont été décrits. L’administration intraveineuseaugmente les risques de toxicité. A fortes doses, elles in<strong>du</strong>isent également unedégénérescence rénale et hépatique. La dose doit être diminuée chez les veauxde moins de 4 semaines. Des lésions <strong>du</strong> myocarde qui pourraient être liées àl’usage de <strong>la</strong> doxycycline chez le veau ont été rapportées. Bien que davantaged’études soient nécessaires à ce sujet, <strong>la</strong> plus grande prudence s’impose dans cedomaine, à commencer par le respect de <strong>la</strong> posologie. (Voir aussi Folia Veterinaria2012, n° 2)InteractionsLes tétracyclines administrées par voie orale sont ché<strong>la</strong>tées par les ions divalents,présents par exemple dans les antiacides, ou par des pro<strong>du</strong>its contenant<strong>du</strong> fer et administrés par voie orale. Le bicarbonate de soude, le kaolin et <strong>la</strong> pectinepeuvent également diminuer l’absorption des tétracyclines. Les tétracyclinespeuvent augmenter <strong>la</strong> biodisponibilité de <strong>la</strong> digoxine. La dose d’insuline doit éventuellementêtre adaptée.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’administration des tétracyclines pendant <strong>la</strong> gestation peut con<strong>du</strong>ire à une colorationdes dents et retarder le développement squelettique. Les tétracyclines sontsécrétées dans le <strong>la</strong>it.1.1.4.1 Chlortétracycline1.1.4.2 DoxycyclineLMR chlortétracycline : AUROFAC 250 mg/g premix (Pfizer A.H.)chlorhydrate de chlortétracycline: 250 mg/gprémé<strong>la</strong>nge médicamenteux poPosologieSu: 10 - 20 mg/kg pj (5 - 7 j)poulet de chair: 20 - 30 mg/kg pj (5 - 7 j)poule pondeuse: 20 - 25 mg/kg pj (5 - 7 j)Viande et abats: Su: 10 j, poulet: 2 j, Œufs: 4 jprém méd 20 kgR/premixLMR doxycycline: CENTIDOX 100% (Eurovet A.H.)hyc<strong>la</strong>te de doxycycline: 1000 mg/gpoudre po dans le <strong>la</strong>it (ou l’aliment d’al<strong>la</strong>itement),dans l’eau de boissonPosologie:veau: 10 mg/kg pj (5 j)porc: 10 mg/kg pj (5 j)Viande et abats: veau: 16 j, Su: 8 jsac 1 kgR/
1 MEDICAMENTS ANTIBACTÉRIENS19DOXYCYCLINE 75 % Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)doxycycline (hyc<strong>la</strong>te): 750 mg/gpoudre po dans l’eau de boisson, dansl’alimentationPosologie:Su: 10,5 mg/kg pj (5 j)Viande: 5 jpoudre 1 kgR/DOXYLIN 50% WSP (Dopharma Research)hyc<strong>la</strong>te de doxycycline: 500 mg/gpoudre pour solution poPosologie:veau (non ruminant): 10 mg/kg pj (3 - 5 j),réparti sur 2 repasSu: 10 mg/kg pj (3 - 5 j), dans l’eau deboisson ou par-dessus l’alimentpoule: 25 mg/kg pj (3 - 5 j), dans l’eau deboissonViande et abats: veau: 7 j, Su: 8 j, poule: 5 jNe pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainecontainer 1000 gR/DOXYPREX 100 mg/g premix (In<strong>du</strong>strialVeterinaria)doxycycline (hyc<strong>la</strong>te): 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 10 mg/kg PV pj (7 j)Viande et abats: 7 jsac 25 kgR/premixDOXYRAL 10% premix (Emdoka)doxycycline (hyc<strong>la</strong>te): 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 10 mg/kg pj (7 j)Viande et abats: 7 jprém méd 25 kgR/premixDOXYRAL 50% (Emdoka)doxycycline (hyc<strong>la</strong>te): 500 mg/gpoudre po dans l’eau de boisson, le <strong>la</strong>it,l’alimentationPosologie:veau: 10 mg/kg pj (max 3 j)Su: 10 mg/kg pj (max 5 j)Viande: veau: 10 j, Su: 5 jpoudre 1000 gR/DOXYRAL 80% (Emdoka)doxycycline (hyc<strong>la</strong>te): 800 mg/gpoudre po dans l’eau de boisson, le <strong>la</strong>itPosologie:veau: 10 mg/kg pj (max 3 j)Su: 10 mg/kg pj (max 5 j)Viande: veau: 10 j, Su: 5 jpoudre 1000 gR/DOXYVETO 50 % pulvis (VMD)doxycycline (hyc<strong>la</strong>te): 500 mg/gpoudre po dans le <strong>la</strong>it, dans l’eau de boissonPosologie:veau, porcelet: 10 mg/kg pj (3 - 5 j)ne pas admin aux veaux ruminantsViande: veau: 12 j , porcelet: 5 jpoudre 1 kg, 2 kgR/HYDRODOXX 500 mg/g (Huvepharma)doxycycline (hyc<strong>la</strong>te): 500 mg/gpoudre pour solution po dans l’eau de boissonPosologie:porc d’engraissement: 10 mg/kg pj (5 j)poulet de chair: 20 mg/kg pj (3 - 5 j)Viande: Su: 6 j, poulet: 6 jNe pas administrer aux poules dont les œufssont destinés à <strong>la</strong> consommation humaine oudans les 4 sem avant le début de <strong>la</strong> périodede pontesac 1 kgR/ORNICURE 7,5% (Oropharma)hyc<strong>la</strong>te de doxycycline: 75 mg/gpoudre po dans l’eau de boissonPosologie:pigeon, oiseau:15 mg/kg pj (5 j) (ornithose,psittacose: 3 - 4 sem)Ne pas administrer aux pigeons destinés à <strong>la</strong>consommation humainepoudre 8 x 4 g, 24 x 4 g (sachets)R/RONAXAN 20 mg (Merial)doxycycline (hyc<strong>la</strong>te): 20 mgcomprimé poPosologie:Ca, Fe: 10 mg/kg pj (3 - 5 j ou 10 j pour lesformes chroniques)compr 2 x 10R/RONAXAN 100 mg (Merial)doxycycline (hyc<strong>la</strong>te): 100 mgcomprimé poPosologie:Ca: 10 mg/kg pj (3 - 5 j ou 10 j pour lesformes chroniques)compr 10R/SOLUDOX 15 % (Eurovet)hyc<strong>la</strong>te de doxycycline: 150 mg/gpoudre po dans l’eau de boissonPosologie:Su: 12,5 mg/kg pj (3-5 j)poulet: 20 mg/kg pj (3-5 j)pigeon, oiseau: 10 - 20 mg/kg pj (3-5 j,infect Ch<strong>la</strong>mydia: 30-45 j)oiseaux recevant des coquilles pulvérisées:traiter 2 x pj ou doubler <strong>la</strong> doseViande: Su: 12 j, vo<strong>la</strong>ille: 9 jNe pas administrer aux poulets dont les œufssont destinés à <strong>la</strong> consommation humaineNe pas administrer aux pigeons qui sontdestinés à <strong>la</strong> consommation humainepoudre 10 x 100 gR/SOLUDOX 500 mg/g poudre porcs et poulets (Eurovet)hyc<strong>la</strong>te de doxycycline: 500 mg/gpoudre po dans l’eau de boissonPosologie:Su: 12,5 mg/kg PV pj (4 j, si nécessairejusqu’à 8 j max)poulet:- infect P. multocida: 10 mg/kg PV pj (3-4 j)- infect O. rhinotracheale: 20 mg/kg PV pj(3-4 j)Viande: Su: 5 j, poule: 3 j (si dose de 10 mg/kg),12 j (si dose > 10 mg/kg et < 20 mg/kg)Ne pas administrer aux poules dont les oeufssont destinés à <strong>la</strong> consommation humaineboite 1000 gR/
20 1 MEDICAMENTS ANTIBACTÉRIENS1.1.4.3 OxytétracyclineLMR oxytétracycline: BAXYL LA (Prodivet)oxytétracycline (dihydrate): 200 mg/mlsolution injectable imPosologie:Bo, veau, Su: 20 mg/kgViande: Bo: 35 j, Su: 14 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/CITROXY 50 % (Dopharma Research)oxytétracycline chlorhydrate: 500 mg/gpoudre po dans l’eau de boissonPosologie:porcelet: 20 - 40 mg/kg pj (3 - 7 j)Viande: 15 jpoudre 1 kgR/CYCLOSOL 200 LA (Eurovet)oxytétracycline (dihydrate): 200 mg/mlsolution injectable imPosologie:Bo, Su: 20 mg/kg (peut être répété après 3 j)Viande: Bo: 46 j, Su: 28 jNe pas administrer aux bovins dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/DUPHACYCLINE 100 (Pfizer A.H.)oxytétracycline (chlorhydrate): 100 mg/mlsolution injectable imPosologie:Bo, Su, Ov: 10 mg/kg pj (5 j)Viande: Bo: 23 j, Su, Ov: 18 j, Lait: Bo: 5 jNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/DUPHACYCLINE 30 % LA (Pfizer A.H.)oxytétracycline (dihydrate): 300 mg/mlsolution pour injection imPosologie:Bo, Su: 30 mg/kg, 20 mg/kgViande: Bo: 35 j, Su: 18 j (20 mg/kg) - 21 j(30 mg/kg), Lait: 10 jf<strong>la</strong>con 250 mlR/DUPHACYCLINE LA (Pfizer A.H.)oxytétracycline (dihydrate): 200 mg/mlsolution injectable imPosologie:Bo, Su, Ov: 20 mg/kgViande, abats: Bo: 29 j, Su: 18 j, Ov: 10 j,Lait Bo: 10 j, Ov: 7 jf<strong>la</strong>con 250 mlR/ENGEMYCINE 10 % LA (MSD A.H.)oxytétracycline (chlorhydrate): 100 mg/mlsolution injectable imPosologie:Bo: 10 mg/kgveau, Su, porcelet, Ov, agneau: 20 mg/kgpeut être répété après 48 hViande: Bo: 28 j, Su: 11 j, Ov: 18 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/FEEDMIX OXY 10% (Dopharma Research)oxytétracycline HCI: 100 mgprémé<strong>la</strong>nge médicamenteux po avecl’alimentationPosologie:Su: 15 - 40 mg/kg PV pj (5 - 7 j)Viande: 5 jprém méd 5 kgR/premixOXY-kel 20 % LA (Ke<strong>la</strong> Laboratoria)oxytétracycline (chlorhydrate): 200 mg/mlsolution injectable imPosologie:Bo: 20 mg/kg (répéter éventuellement après72 h)Viande: 53 jNe pas administrer aux bovins dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/OXYTETRACYCLINE 80% Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)oxytétracycline (chlorhydrate): 800 mg/gpoudre po dans l’eau de boisson, dans le <strong>la</strong>itPosologie:veau: 2 x pj 20 mg/kg (3 - 5 j)Su: 50 mg/kg pj (4 - max 6 j)Viande: Su: 3 j, veau: 7 jpoudre 1 kgR/RETARDOXI 20 % L.A. (VMD)oxytétracycline (dihydrate): 200 mg/mlsolution injectable imPosologie:Bo, Su: 20 mg/kgsi nécessaire, répéter après 72 hViande: Bo: 46 j, Su: 31 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/TENASAN LA (Ceva Santé Animale)oxytétracycline: 200 mg/mlsolution injectable imPosologie:Bo*, Su, Ov*: 20 mg/kg (répéter si nécessaireaprès 3 j (Bo, Ov) ou 2 j (Su))*(non en <strong>la</strong>ctation)Viande: Bo: 35 j, Su, Ov: 19 jNe pas utiliser chez les animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/TERRAMYCINE 100 (Pfizer A.H.)oxytétracycline chlorhydrate: 100 mg/mlsolution injectable imPosologie:Su: 10 mg/kg pj (5 j)Viande: 24 jf<strong>la</strong>con 250 mlR/TERRAMYCINE LA (Pfizer A.H.)oxytétracycline (dihydrate): 200 mg/mlsolution injectable imPosologie:Bo, Su, Ov: 20 mg/kgViande: Bo: 25 j, Ov, Su: 21 j, Lait Bo, Ov: 7 jf<strong>la</strong>con 250 mlR/
1 MEDICAMENTS ANTIBACTÉRIENS211.1.5 Macrolides - Lincosamides et PleuromutilinesLes macrolides, les lincosamides et les streptogramines forment ensemble ungroupe appelé “antibiotiques MLS”, auquel se rattachent les pleuromutilines àusage strictement vétérinaire.A l’exception de <strong>la</strong> virginiamycine non commercialisée actuellement en médecinevétérinaire et exclusivement à usage topique, les streptogramines ne s’emploientpas en thérapeutique. Ces molécules, bien que structurellement distinctes, possèdentde nombreuses propriétés communes justifiant leur regroupement. En effet,toutes sont des antibiotiques bactéricides ou bactériostatiques selon <strong>la</strong> dose,agissant au niveau de <strong>la</strong> sous-unité 50 S ribosomale, caractérisés par une forteliposolubilité et une très bonne distribution tissu<strong>la</strong>ire et intracellu<strong>la</strong>ire.1.1.5.1 Macrolidesest indiquée pour le traitement despathologies respiratoires associées àIndications - spectre d’activité Mannheimia haemolytica, Pasteurel<strong>la</strong>- résistancesmultocida et Histophilus somni chezLa spiramycine, <strong>la</strong> tylosine, <strong>la</strong> tilmicosineet les molécules plus récentes pleuropneumoniae, Pasteurel<strong>la</strong> multo-les bovins viandeux et à Actinobacillustelles que <strong>la</strong> tu<strong>la</strong>thromycine, <strong>la</strong> tylvalosine(acéthylisovaléryltylosine) et <strong>la</strong> chez le porc. La gamithromycine estcida et Mycop<strong>la</strong>sma hyopneumoniaegamithromycine sont des macrolides rapidement résorbée et a une longueutilisés par voie orale ou parentérale <strong>du</strong>rée d’action sur le poumon. Cettechez les animaux. Ces antibiotiques substance est enregistrée pour le traitementet <strong>la</strong> prévention des ma<strong>la</strong>diessont actifs contre diverses bactériesaérobies et anaérobies GRAM+ respiratoires bovines associées à des(Rhodococcus equi, Bacillus, Corynebacterium,Erysipelothrix rhusiopathiae, haemolytica, Pasteurel<strong>la</strong> multocida etpathogènes bactériens (MannheimiaListeria, Staphylococcus, Streptococcus, Histophilus somni). La tildipirosine estActinomyces, Clostridium) et quelques indiquée dans le traitement des ma<strong>la</strong>diesrespiratoires porcines associéesbactéries GRAM- (Leptospira, Cam pylobacter,Actinobacillus, Bacteroides). à Actinobacillus pleuropneumoniae,Les entérobactéries, les pseudomonades,les mycobactéries et les chiseptica et Haemophilus parasuis.Pasteurel<strong>la</strong> multocida, Bordetel<strong>la</strong> bron-ch<strong>la</strong>mydies sont naturellement résistantes.Des résistances acquises croi-Les macrolides agissent au niveauPharmacodynamiesées avec les lincosamides ont été de <strong>la</strong> sous-unité 50 S ribosomale etobservées.inhibent ainsi <strong>la</strong> synthèse protéique <strong>du</strong>La spiramycine se concentre fortementdans les tissus et peut être dipirosine se distinguent de beaucouppathogène. La tu<strong>la</strong>thromycine et <strong>la</strong> til-utilisée comme traitement alternatifaux pénicillines chez les animaux <strong>du</strong>rée d’action en partie expliquée pard’autres macrolides par leur longueallergiques à celles-ci ou en cas leurs groupes aminés (sous-c<strong>la</strong>sse desd’infections causées par des germes triamilides).résistants. La spiramycine est c<strong>la</strong>ssiquementassociée au métronidazole Les propriétés cinétiques des macro-Pharmacocinétiquechez les carnivores domestiques (voir lides sont semb<strong>la</strong>bles à celles des1.1.9 Associations). La tylosine est lincosamides (voir 1.1.5.2). Elles sesurtout employée dans les infections concentrent dans les milieux plusà mycop<strong>la</strong>smes chez les ruminants, acides que le p<strong>la</strong>sma et atteignentle porc et <strong>la</strong> vo<strong>la</strong>ille. La tylvalosine des concentrations particulièrement(acétylisovaléryltylosine) est enregistréepour le traitement et <strong>la</strong> prévention aussi dans <strong>la</strong> bile, les fluides prosta-importantes dans les poumons maisde <strong>la</strong> pneumonie enzootique porcine tiques, pleuraux et péritonéaux. La résorptiondes macrolides est bonne et<strong>du</strong>e à Mycop<strong>la</strong>sma hyopneumoniae,ainsi que pour le traitement d’infectionsà Brachyspira hyodysenterica et qu’au niveau des sites d’injection. Lesrapide, aussi bien au niveau intestinalLawsonia intracellu<strong>la</strong>ris chez le porc. macrolides ont une bonne distributionLa tilmicosine est utilisée pour traiter tissu<strong>la</strong>ire, en particulier vers les poumons.L’élimination se fait principale-les pneumonies des ovins, des porcset des bovins. La tu<strong>la</strong>thromycine ment par les fèces.
22 1 MEDICAMENTS ANTIBACTÉRIENSContre-indicationsNe pas administrer par voie intra veineuse.Effets indésirablesTous les macrolides sont irritants, cequi peut provoquer, à des degrés divers,de <strong>la</strong> douleur lors d’injection IMou des phlébites en cas d’injection IV.Leur effet stimu<strong>la</strong>nt sur le muscle lissepeut in<strong>du</strong>ire de <strong>la</strong> diarrhée, qui restebénigne chez <strong>la</strong> plupart des espèces,sauf chez le cheval et le <strong>la</strong>pin. Des casde mortalité liés à <strong>la</strong> cardio-toxicitéde <strong>la</strong> tilmicosine ont été décrits chezl’homme suite à une auto-injection.InteractionsPour éviter une résistance croisée, nepas administrer simultanément avecd’autres antibactériens ayant un moded’action simi<strong>la</strong>ire, tels que les autresmacrolides ou les lincosamides.Précautions particulières/ Risquespour l’hommeUne attention particulière est recommandéeafin d’éviter toute auto-injectionaccidentelle. Des étudestoxicologiques chez des animaux de<strong>la</strong>boratoire ont révélé des effets cardiovascu<strong>la</strong>iresaprès administration intramuscu<strong>la</strong>iredes différents macrolides.En cas d’auto-injection accidentelle,demandez immédiatement conseil àun médecin et montrez-lui <strong>la</strong> notice oul’étiquetage. N’utilisez pas de seringuesautomatiques dépourvues d’unsystème de protection complémentaire(voir Folia Veterinaria 2006 nr° 2).Les macrolides peuvent entraîner unesensibilisation par contact cutané eten cas d’exposition ocu<strong>la</strong>ire.Repro<strong>du</strong>ction et <strong>la</strong>ctationEn raison <strong>du</strong> manque de donnéesdisponibles, il est conseillé de ne pasutiliser ces substances pendant <strong>la</strong> gestationou <strong>la</strong> <strong>la</strong>ctation sauf si les bénéficess’avèrent plus importants que lesrisques.GamithromycineLMR gamithromycine: ZACTRAN (Merial)gamithromycine: 150 mg/mlsolution injectable scPosologie:Bo: 1 x 6 mg/kgViande Bo: 64 jNe pas utiliser chez les animaux en <strong>la</strong>ctationdont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaine, ni chez les animaux gravides dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humaine aucours des 2 mois précédant <strong>la</strong> mise basf<strong>la</strong>con 100 mlR/TildipirosineLMR tildipirosine ZUPREVO bovin (MSD A.H.)tildipirosine: 180 mg/mlsolution injectable scPosologie:Bo: 1 x 4 mg/kgViande Bo: 47 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, ni auxanimaux gravides au cours des 2 m précédant<strong>la</strong> mise basf<strong>la</strong>con 50 mlR/ZUPREVO porc (MSD A.H.)tildipirosine: 40 mg/mlsolution injectable imPosologie:Su (âge > 4 sem): 1 x 4 mg/kgViande: Su: 9 jf<strong>la</strong>con 100 ml, 250 mlR/TilmicosineLMR tilmicosine: HYMATIL 300 mg/ml (In<strong>du</strong>strial Veterinaria)tilmicosine: 300 mg/mlsolution injectable scPosologie:Bo: 1 x 10 mg/kgViande et abats: 77 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/MICOTIL (Eli Lilly)tilmicosine: 300 mg/mlsolution injectable scPosologie:jeune bovin, Ov (> 15 kg): 1 x 10 mg/kgViande: jeune bovin: 60 j , Ov: 42 j, Lait: Ov: 15 jNe pas utiliser chez les bovins pro<strong>du</strong>cteurs de<strong>la</strong>it destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 mlR/PULMOTIL 100 Granules (Eli Lilly)tilmicosine (phosphate): 100 g/kggranulés po avec l’alimentPosologie:Su: 8 - 16 mg/kg PV pj (15 - 21 j)<strong>la</strong>pin: 12 mg/kg PV pj (7 j)Viande: Su: 21 j, <strong>la</strong>pin: 4 jgran 2 kgR/PULMOTIL 200 Vet Premix (Eli Lilly)tilmicosine (phosphate): 200 g/kgprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 8 - 16 mg/kg PV pj (15 - 21 j)<strong>la</strong>pin: 12 mg/kg PV pj (7 j)Viande: Su: 21 j, <strong>la</strong>pin: 4 jprém méd 10 kgR/premix
1 MEDICAMENTS ANTIBACTÉRIENS23PULMOTIL AC (Eli Lilly)tilmicosine (phosphate): 250 mg/mlsolution po dans l’eau de boisson, le <strong>la</strong>itartificielPosologie:veau: 2 x pj 12,5 mg/kg (3 - 5 j)Su: 15 - 20 mg/kg pj (5 j)poulet: 15 - 20 mg/kg pj (3 j)dinde: 10 - 27 mg/kg (3 j)Viande: veau: 42 j, Su: 14 j, dinde: 19 j, poulet:12 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumaineNe pas utiliser dans les 14 jours précédant ledébut de <strong>la</strong> ponteNe pas utiliser chez les animaux al<strong>la</strong>itantsf<strong>la</strong>con 960 mlR/TILMI-KEL (Ke<strong>la</strong> Laboratoria)tilmicosine: 300 mg/mlsolution injectable scPosologie:Bo: 1 x 10 mg/kgViande et abats: 77 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 ml, 100 mlR/TILMODIL (Emdoka)tilmicosine: 300 mg/mlsolution injectable scPosologie:Bo, Ov (PV > 15kg): 1 x 5 of 10 mg/kgViande (abats): Bo: 60 j, Ov: 42 j, Lait: Ov: 15 j(360 h)Ne pas utiliser chez les bovins pro<strong>du</strong>isant <strong>du</strong><strong>la</strong>it destiné à <strong>la</strong> consommation humaine. Ne pasutiliser chez des génisses <strong>la</strong>itières gestantes oudes vaches <strong>la</strong>itières en tarissement pendant <strong>la</strong>période de 60 jours avant <strong>la</strong> mise-bas.f<strong>la</strong>con 50 ml, 100 mlR/TILMOVET 100 mg/g gran porcs (Huvepharma)tilmicosine: 100 mg/ggranulés po avec l’alimentationPosologie:porc d’engraissement (sevré):1 x pj 16 mg/kg PV (15 j)Viande et abats: 21 jsac 1 kgR/TILMOVET 200 g/kg premix (Huvepharma)tilmicosine: 200 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 16 mg/kg PV pj (15 j)Viande et abats: 21 jprém méd 20 kgR/premixTILMOVET 250 mg/ml (Huvepharma)tilmicosine: 250 mg/mlsolution poPosologie:veau: 2 x 12,5 mg/kg pj (3-5 j)Su 15 - 20 mg/kg (5 j)poules: 15 - 20 mg/kg (3 j)dinde: 10 - 27 mg/kg (3 j)Bo: 42 j, Su: 14 j, poule: 12 j, dinde: 19 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainef<strong>la</strong>con 960 mlR/Tu<strong>la</strong>thromycineLMR tu<strong>la</strong>thromycine: DRAXXIN (Pfizer A.H.)tu<strong>la</strong>thromycine: 100 mg/mlsolution injectable sc (Bo), im (Su)Posologie:Bo, Su: 2,5 mg/kg (1 x)Viande Bo: 49 j, Su: 33 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineou chez les animaux gravides dans les 2 mprécédant le vê<strong>la</strong>gef<strong>la</strong>con 50 ml, 100 mlR/TylosineLMR tylosine: PHARMASIN 100% w/w gran (Huvepharma)tylosine (tartrate): 1 g/1,1 ggranules po avec l’eau de boissonPosologie:veau: 2 x pj 10 - 20 mg/kg (7 - 14 j)Su:pneum enzoot: 20 mg/kg pj (10 j)iléite: 5 - 10 mg/kg pj (7 j)poule:ma<strong>la</strong>dies chroniques resp:75 - 100 mg/kg pj (3 - 5 j)entérite nécrot: 20 mg/kg pj (3 j)dinde: 75 - 100 mg/kg pj (3 - 5 j)Viande et abats: veau: 12 j, Su: 1 j, poule: 1 j,dinde: 2 jOeuf: poule, dinde: 0 jgran 1,1 kgR/PHARMASIN 250 mg/g gran po porcs(Huvepharma)tylosine phosphate: 250 mg/ggranulés poPosologie:Su: 1 x pj 5 mg/kg PV (3 sem)Viande: Su: 0 jsac 1 kg, 5 kgR/PHARMASIN 250 mg/g premix (Huvepharma)tylosine phosphate: 250 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:- Su traitement et prévention:L. intracellu<strong>la</strong>ris: 4 - 5 mg/kg PV (3 sem)B. hyodysenteriae: 4 - 5 mg/kg PV (4 - 5sem) ou 8 - 10 mg/kg PV (8 j), suivi par4 - 5 mg/kg PV jusqu’à fin de période à risque- poulet traitement et prévention:M. gallisepticum/synoviae: 127 mg/kg PV(5 premiers j de vie), répéter à l’âge de3 - 4 semCl. perfringens: 10 - 20 mg/kg PV (7 j)Viande et abats: Su: 0 j, Av: 1 jNe pas utiliser chez les poules pondeuses dontles œufs sont destinés à <strong>la</strong> consommationhumaineprém méd 20 kgR/premix
24 1 MEDICAMENTS ANTIBACTÉRIENSTYLAN 100 Granules (Eli Lilly)tylosine (phosphate): 100 mg/ggranules po avec l’alimentationPosologie:- Su:dysenterie: 4 - 5 mg/kg PV pj (4 sem)L. intracellu<strong>la</strong>ris et infect resp:4 - 5 mg/kg PV pj (21 j)- poule de chair, poule d’élevage:CRD: 92 - 127 mg/kg PV pj (pendant lespremiers 5 j de <strong>la</strong> vie), ensuite à l’âge de3 - 4 sem: 67 - 92 mg/kg PV pj (2 j)- poule:entérite nécrot: 20 mg/kg pj (7 j)Viande: Su: 0 j, poule: 1 jNe pas administrer aux poules dont les oeufssont destinés à <strong>la</strong> consommation humainegran 1 kgR/TYLAN 200 (Eli Lilly)tylosine: 200 mg/mlsolution injectable im, iv (Bo, veau), im (Su)Posologie:Bo, veau: 5 - 10 mg/kg pj (max 5 j)Su: 5 - 10 mg/kg pj (max 3 j)Viande: Bo: 28 j, Su: 8 j, Lait: 4 jf<strong>la</strong>con 100 ml, 250 mlR/TYLAN 250 Vet Premix (Eli Lilly)tylosine (phospahte): 250 g/kgprémé<strong>la</strong>nge médicamenteux poPosologie:Su:- dysenterie: 4 - 5 mg/kg PV pj (4 - 5 sem)- L. intracellu<strong>la</strong>ris, infect. resp.:4 - 5 mg/kg PV pj (21 j)Av: poulet de chair, poule-mère:- CRD: 92 - 127 mg/kg PV pj (les 5 1ers jde vie), suivi par 67 - 92 mg/kg PV pj (2 j) àl’âge de 3 - 4 sem- entérite nécrot.: 20 mg/kg PV pj (7 j)Viande: Su: 0 j, poule: 1 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainesac 25 kgR/premixTYLAN soluble (Eli Lilly)tylosine (tartrate): 1000 g/sacpoudre soluble po dans l’eau de boisson, dansle <strong>la</strong>itPosologie:- veau non ruminant: 2 x pj 1 g de poudredans <strong>du</strong> <strong>la</strong>it artificiel ou l’eau de boisson(7 - 14 j)- Su: dysenterie: 0,25 g de poudre/l d’eau(3 - 10 j)L. intracellu<strong>la</strong>ris: 5 mg/kg PV pj (7 j)- poule: CRD: 0,5 g de poudre/l d’eau (2-5 j)entérite nécrot.: 24 mg/kg PV (3 j)- dinde: 0,5 g de poudre/l d’eau (2 - 5 j)Viande: veau: 13 j, Su, poules, dinde: 1 j,Oeuf: 0 jpoudre 1000 g/sacR/TYLO-kel 20 % (Ke<strong>la</strong> Laboratoria)tylosine (tartrate): 200 mg/mlsolution injectable im, sc, ivPosologie:Bo: 2,5 - 10 mg/kg pj (1 - 3 j)Viande: 29 j, Lait: 6 jf<strong>la</strong>con 100 mlR/TYLOSINE 75 % Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)tylosine (tartrate): 750.000 UI/g (750 mg/g)poudre po dans l’eau de boissonPosologie:Su: 30 - 60 mg/kg pj (3 - max 10 j)poule: 90 - 150 mg/kg pj (2 - 5 j)Viande: Su, poule: 1 jNe pas administrer aux poules dont les oeufssont destinés à <strong>la</strong> consommation humainepoudre 133 g, 1333 gR/TYLOVETO-20 (VMD)tylosine (tartrate): 200 mg/mlsolution injectable imPosologie:Bo: 2 x pj 20 mg/kg (max 5 j)Viande Bo: 49 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/TylvalosineLMR tylvalosine: AIVLOSIN 42,5 mg/g prém méd porcs (Eco A.H.)tylvalosine (tartrate): 42,5 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su:- prévention, traitement pneum enzoot:2,125 mg/kg pj (7 j)- traitement entéropathie prolif:4,25 mg/kg pj (10 j)- prévention, traitement dysenterie:4,25 mg/kg pj (10 j)Viande et abats: 2 jprém méd 20 kgR/premixAIVLOSIN 625 mg/g gran porcs (Eco A.H.)tylvalosine (tartrate): 625 mg/ggranulés po dans l’eau de boissonPosologie:Su: 5 mg/kg PV pj (5 j)Viande et abats : 1 jgran 40 g, 160 gR/AIVLOSIN 625 mg/g gran poulets (Eco A.H.)tylvalosine (tartrate): 625 mg/ggranulés po dans l’eau de boissonPosologie:poulet: M. gallisepticum:- thérapie: 25 mg/kg PV pj (3 j)- prévention (âge 1 j): 25 mg/kg PV pj (3 j),répéter 1 x en période de risqueViande et abats : 2 jNe pas utiliser chez les poules dont les œufssont destinés à <strong>la</strong> consommation humaineNe pas utiliser dans les 14 j précédant le débutde <strong>la</strong> pontegran 40 g, 400 gR/1.1.5.2 LincosamidesIndications - spectre d’activité -résistancesCe groupe comprend <strong>la</strong> lincomycine et<strong>la</strong> clindamycine. Ces deux substancessont surtout actives contre les bactériesGRAM+ aérobies et anaérobies
1 MEDICAMENTS ANTIBACTÉRIENS25et les mycop<strong>la</strong>smes, mais de nombreusesbactéries GRAM- y sont naturellementrésistantes. Des résistancesacquises sont aussi signalées. La clindamycineest particulièrement activecontre les bactéries anaérobies et agitégalement contre les toxop<strong>la</strong>smes.Les lincosamides restent intéressantesà utiliser dans le traitement desinfections situées dans des territoiresdifficilement accessibles sur le p<strong>la</strong>ncinétique (abcès, prostatite, arthrite,ostéomyélite, pyodermites...) et provoquéespar des bactéries GRAM+,notamment anaérobies.PharmacodynamieLes lincosamides agissent au niveaude <strong>la</strong> sous-unité 50 S ribosomale.PharmacocinétiqueLa lincomycine et surtout <strong>la</strong> clindamycinesont bien absorbées par voieorale chez les monogastriques. Cetteabsorption est cependant ralentie par<strong>la</strong> prise de nourriture et de kaolin. Leslincosamides sont surtout métaboliséspar le foie et éliminés dans unemoindre mesure par voie rénale, sousforme active. Ils traversent bien lesbarrières cellu<strong>la</strong>ires et atteignent desconcentrations tissu<strong>la</strong>ires supérieuresaux concentrations p<strong>la</strong>smatiques, particulièrementau niveau <strong>du</strong> foie, desreins, des poumons, des os, des articu<strong>la</strong>tions,<strong>du</strong> système nerveux central,de <strong>la</strong> prostate et <strong>du</strong> tissu mammaire.Le caractère basique de ces moléculescontribue à leur concentration dansces compartiments. Les concentrationsdans le liquide céphalo-rachidienrestent faibles. La clindamycine diffusesuffisamment au niveau <strong>du</strong> tissuosseux pour atteindre des concentrationsefficaces en cas d’ostéomyélite.De plus, elle peut se concentrer dansles macrophages.Contre-indicationsLes lincosamides sont à proscrire chezles <strong>la</strong>pins, cobayes et hamsters, chevauxet ruminants.Effets indésirablesLe principal effet toxique des lincosamidesest <strong>la</strong> propension à in<strong>du</strong>ire unediarrhée sévère, parfois mortelle, chezl’homme et les herbivores. Chez <strong>la</strong> vache<strong>la</strong>itière, cette diarrhée peut s’accompagnerd’acétonémie et d’une chute de<strong>la</strong> pro<strong>du</strong>ction. Chez les carnivores, leslincosamides sont bien tolérés. D’autreseffets toxiques moins fréquents incluentun blocage neuromuscu<strong>la</strong>ire avec paralysiepost-anesthésique, une dépressioncardiaque après injection IV troprapide, des allergies et une dégénérescencehépatique modérée.InteractionsLes lincosamides antagonisent <strong>du</strong>chloramphénicol et des macrolides.L’absorption de <strong>la</strong> lincomycine estré<strong>du</strong>ite par l’administration de kaolin.L’administration simultanée avec desinhibiteurs neuromuscu<strong>la</strong>ires doit êtreenvisagée avec prudence.Repro<strong>du</strong>ction et <strong>la</strong>ctationEn raison <strong>du</strong> manque de donnéesdisponibles, il est conseillé de ne pasutiliser ces substances pendant <strong>la</strong> gestationou <strong>la</strong> <strong>la</strong>ctation sauf si les bénéficess’avèrent plus importants que lesrisques.ClindamycineLMR clindamycine: ANTIROBE 25 mg (Pfizer A.H.)clindamycine (chlorhydrate): 25 mgcapsule poPosologie:Ca:ostéomyélite: 2 x pj 11 mg/kg (min 28 j)pyodermite superfic:2 x pj 5,5 mg/kg (3 sem)Ca, Fe:p<strong>la</strong>ie infect, abcès: 2 x pj 5,5 mg/kg (7 j ou10 j en cas d’infect. cavité buccale)prévention en chirurgie dentaire: traiter 5 javant, jusqu’à 5 j après l’interventioncaps 16, 80R/ANTIROBE 75 mg (Pfizer A.H.)clindamycine (chlorhydrate): 75 mgcapsule poPosologie:Ca: p<strong>la</strong>ie infect, abcès: 2 x pj 5,5 mg/kg(7 j ou 10 j en cas d’infect cavité buccale)prévention en chirurgie dentaire: traiter 5 javant, jusqu’à 5 j après l’interventionpyodermite superfic:2 x pj 5,5 mg/kg (3 sem)ostéomyélite: 2 x pj 11 mg/kg (min 28 j)caps 16, 80R/ANTIROBE 150 mg (Pfizer A.H.)clindamycine (chlorhydrate): 150 mgcapsule poPosologie:Ca:p<strong>la</strong>ie infect, abcès: 2 x pj 5,5 mg/kg(7 j ou 10 j en cas d’infect cavité buccale)prévention en chirurgie dentaire: traiter 5 javant, jusqu’à 5 j après l’interventionpyodermite superfic:2 x pj 5,5 mg/kg (3 sem)ostéomyélite: 2 x pj 11 mg/kg (min 28 j)caps 16, 80R/
26 1 MEDICAMENTS ANTIBACTÉRIENSANTIROBE 300 mg (Pfizer A.H.)clindamycine (chlorhydrate): 300 mgcapsule poPosologie:Ca: p<strong>la</strong>ie infect, abcès: 2 x pj 5,5 mg/kg(7 j ou 10 j en cas d’infect cavité buccale)prévention en chirurgie dentaire: traiter 5 javant, jusqu’à 5 j après l’interventionpyodermite superfic:2 x pj 5,5 mg/kg (3 sem)ostéomyélite: 2 x pj 11 mg/kg (min 28 j)caps 16, 80R/CLINDABUC 200 (Ceva Santé Animale)clindamycine (chlorhydrate): 200 mgcomprimé poPosologie:Ca: 2 x pj 5,5 mg/kg (min 7 j, max 28 j)compr 1 x 10, 25 x 10R/CLINDAMYCINE Ke<strong>la</strong> 100 mg (Ke<strong>la</strong> Laboratoria)clindamycine (chlorhydrate): 100 mgcomprimé poPosologie:Ca:- p<strong>la</strong>ie infectée, abcès: 2 x pj 5,5 mg/kg (7 j)- infect. buccale ou dentaire:2 x pj 5,5 mg/kg (10 j, max 28 j)- admin préventive en cas de chirurgiedentaire: 2 x 5,5 mg/kg (5 j avant et 5 j aprèsl’intervention)- ostéomyélite: 2 x pj 11 mg/kg (28 j)compr 2 x 10, 8 x 10R/CLINDAMYCINE Ke<strong>la</strong> 200 mg (Ke<strong>la</strong> Laboratoria)clindamycine (chlorhydrate): 200 mgcomprimé poPosologie:Ca:- p<strong>la</strong>ie infectée, abcès: 2 x pj 5,5 mg/kg (7 j)- infect. buccale ou dentaire:2 x pj 5,5 mg/kg (10 j, max 28 j)- admin préventive en cas de chirurgiedentaire: 2 x 5,5 mg/kg (5 j avant et 5 j aprèsl’intervention)- ostéomyélite: 2 x pj 11 mg/kg (28 j)compr 2 x 10, 8 x 10R/LincomycineLMR lincomycine: LINCOCIN 100 mg/ml (Pfizer A.H.)lincomycine (chlorhydrate): 100 mg/mlsolution injectable im (Su) , im, iv (Ca, Fe)Posologie:Su: 10 mg/kg pj (3 j)Ca, Fe: 20 mg/kg 1 x pj ou 10 mg/kg 2 x pjCa, Fe (iv): 10 - 20 mg/kg 1 ou 2 x pjViande: Su: 4 jf<strong>la</strong>con 100 ml, 250 mlR/LINCOCIN 40 % (Pfizer A.H.)lincomycine (chlorhydrate): 400 mg/gpoudre po dans l’eau de boissonPosologie:Su: 6 mg/kg pj (max 10 j)poulets d’engraissement: 5 mg/kg pj (7 j)Viande: Su: 1 j, poulets d’engraissement : 5 jNe pas administrer aux poules pondeuses dontles œufs sont destinés à <strong>la</strong> consommationhumainepoudre 150 g, 1.5 kgR/LINCOMYCINE 40 %-VMD pulvis (VMD)lincomycine (chlorhydrate): 400 mg/gpoudre po dans l’eau de boissonPosologie:Su: 10 mg/kg pj (5, max 10 j)Viande: 1 jpoudre 150 g, 1.5 kgR/LINCOMYCINE-VMD inj (VMD)lincomycine (chlorhydrate): 100 mg/mlsolution injectable imPosologie:Su: 10 mg/kg pj (3 - 7 j)Viande et abats: 3 jf<strong>la</strong>con 100, 250 mlR/1.1.5.3 PleuromutilinesIndications – spectre d’activité -résistancesCes antibiotiques ne sont pas utiliséschez l’humain. Leur spectre d’actionest comparable à celui de <strong>la</strong> tylosine,mais leur activité contre les mycop<strong>la</strong>smeset les bactéries anaérobiesest cependant plus élevée. L’efficacitécontre les entérobactéries est plutôtnégligeable. Etant donné sa toxicitéchez d’autres espèces animales, <strong>la</strong>tiamuline n’est utilisée que chez <strong>la</strong>vo<strong>la</strong>ille et le porc dans le traitementde ma<strong>la</strong>dies respiratoires causéespar des mycop<strong>la</strong>smes, et chez le porcégalement dans le traitement de <strong>la</strong>dysenterie à spirochètes anaérobies(Brachyspira hyodysenteriae). La valnémulineest enregistrée pour le traitementde <strong>la</strong> dysenterie à spirochètesanaérobies (Brachyspira hyodysenteriae)et de <strong>la</strong> pneumonie enzootique àmycop<strong>la</strong>smes (Mycop<strong>la</strong>sma hyopneumoniae)chez le porc.PharmacodynamieLa tiamuline et <strong>la</strong> valnémuline sontdes dérivés semi-synthétiques de <strong>la</strong>pleuromutiline. Comme pour le groupeMLS, leur action antibiotique reposesur l’inhibition de <strong>la</strong> synthèse protéiqueau niveau de l’unité 50 S desribosomes.PharmacocinétiqueLeurs propriétés pharmacocinétiques sontcomparables à celles des macrolides.
1 MEDICAMENTS ANTIBACTÉRIENS27Contre-indicationsEtant donné sa toxicité chez d’autresespèces animales, <strong>la</strong> tiamuline n’estutilisée que chez <strong>la</strong> vo<strong>la</strong>ille et le porc.Effets indésirablesLa notice mentionne des études épidémiologiquesqui ont démontré que lesespèces porcines des races LandraceSuédois et Landrace Danois ainsi queleurs croisements (en particulier lesjeunes animaux) pourraient être plussensibles aux effets indésirables de <strong>la</strong>valnémuline (fièvre, anorexie, ataxie,troubles de coordination, érythème,œdème,… et jusqu’à 1% de mortalité).InteractionsOn n’administrera pas <strong>la</strong> tiamuline et<strong>la</strong> valnémuline simultanément à desantibiotiques ionophores (monensine,salinomycine, narasine).Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas administrer aux animaux pendant<strong>la</strong> gestation ou <strong>la</strong> <strong>la</strong>ctation.TiamulineLMR tiamuline: TIAMUTIN 10% (VMD)tiamuline: 100 mg/mlsolution injectable imPosologie:Su: 8 mg/kg pj (1 - 2 j)Viande: 14 jf<strong>la</strong>con 100 mlR/TIAMUTIN 10% prém méd (VMD)tiamuline fumarate: 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su:traitement dysenterie (B. hyodysenteriae),colite (B. pilosicoli): 5 - 10 mg/kg pj (7 – 10 j)prévention dysenterie (B. hyodysenteriae):2 mg/kg pj (2 - 4 sem)traitement iléite (L. intracellu<strong>la</strong>ris):7,5 mg/kg pj (10 - 14 j)traitement pneum enzoot (M. hyopneumoniae):5 - 10 mg/kg pj (7-10 j)poulet:traitement, prévention affections resp chron(M. gallisepticum), infect sac aérien, synovite:25 mg/kg pj (3 - 5 j)dinde:traitement, prévention sinusite contagieuse,infect sac aérien (M. gallisepticum, M. synoviaeet M. meleagridis): 40 mg/kg pj (3 – 5 j)<strong>la</strong>pin:traitement, prévention entérocolite épizoot:3 mg/kg pj (traiter jusqu’à 2 - 3 j aprèsdisparition signes cliniques, prévention 3 - 4sem après sevrage)Viande: Su: 2 j (dysenterie), 5 j (pneum enzoot),poule: 1 j, dinde: 4 j, <strong>la</strong>pin: 0 j, Œuf poule: 0 jprém méd 5 kgR/premixTIAMUTIN soluble (VMD)tiamuline fumarate: 450 mg/ggranules poPosologie:Su:- dysenterie par B. hyodysenteriae:8,8 mg/kg PV pj (5 j)- pneum enzoot par M. hyopneumoniae:15 - 20 mg/kg PV pj (5 j)poule et dinde: 25 mg/kg PV pj (3 à 5 j)Viande: Su: 5 j, poule: 3 j, dinde: 5 j, Oeuf:poule: 0 jgran 1 kgR/VETMULIN 100 g/kg premix (Huvepharma)fumarate d’hydrogène de tiamuline: 100 g/kgprémé<strong>la</strong>nge médicamenteux poPosologie:Su:dysenterie: 8,8 mg/kg (7 - 10 j)Viande: 7 jprém méd 1 kg, 20 kgR/premixVETMULIN 100 mg/g gran oraux porcs(Huvepharma)hydrogénofumarate de tiamuline: 100 mg/ggranulés poPosologie:Su:dysenterie: 8,8 mg/kg (7 - 10 j)Viande et abats: 7 jsac 1 kgR/VETMULIN 162 mg/ml sol inj porcs (Huvepharma)tiamuline: 162 mg/mlsolution injectable imPosologie:Su:- dysenterie: 1 x 8.1 mg/kg, suivi par de <strong>la</strong>tiamuline dans l’eau de boisson oul’alimentation- pneum enzoot ou arthrite mycop<strong>la</strong>smale:12.1 mg/kg pj (3 j), si nécessaire adminensuite de <strong>la</strong> tiamuline par voie oraleViande et abats: 21 jf<strong>la</strong>con 100 mlR/VETMULIN 450 mg/g (Huvepharma)fumarate d’hydrogène de tiamuline: 450 mg/ggranulés po dans l’eau de boissonPosologie:Su:dysenterie: 8,8 mg/kg (5 j)pneum enzoot: 15 - 20 mg/kg (5 j)Viande: 5 jgran 1 kgR/
28 1 MEDICAMENTS ANTIBACTÉRIENSValnémulineLMR valnémuline: ECONOR 10 % (Novartis)valnémuline (chlorhydrate): 100 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: traitement dysenterie:3 - 4 mg/kg (7 j - 4 sem)prévention dysenterie:1 - 1,5 mg/kg (7 j - 4 sem)entéropathie proliférative:3 - 4 mg/kg (2 sem)prévention colite: 1 - 1,5 mg/kg (4 sem)prévention pneum. enzoot.:10 - 12 mg/kg (3 sem)Viande: 1 jprém méd 1 kgR/premix1.1.6 Antimicrobiens Peptidiques1.1.6.1 PolymyxinesPour les formes orales, voir chapitre 4.5.2.Indications - spectre d’activité -résistancesLa colistine ou polymyxine E est unantibiotique bactéricide qui agit contreles bactéries GRAM-. Les bactériesGRAM+ sont résistantes, de mêmeque les genres Proteus et Serratia.Certaines souches de Pseudomonasaeruginosa peuvent être résistantes.L’activité de <strong>la</strong> colistine vis-à-vis de cegerme est également diminuée en présencede calcium. Sa capacité à complexerles toxines bactériennes est àsouligner. La colistine est disponiblesous forme orale pour le traitementdes infections digestives à bactériesGRAM- (voir chapitre 4.5.2), ou sousforme de solution injectable. Les donnéesrécentes issues de <strong>la</strong> médecinehumaine imposent de ne plus considérerces antibiotiques comme des principesactifs de première ligne.PharmacodynamieLa colistine se lie aux phospholipidesde manière à désorganiser les membranesdes bactéries GRAM-.PharmacocinétiqueLa colistine est très lentement et faiblementabsorbée per os. Elle diffusetrès peu à travers les membranesbiologiques et n’atteint que de faiblesconcentrations dans le <strong>la</strong>it et les fluidesintracellu<strong>la</strong>ires. Elle est excrétée sousforme active dans les urines.Contre-indicationsLes polymyxines sont hautementnéphrotoxiques et sont à proscrire parvoie systémique chez les insuffisantsrénaux.Effets indésirablesElles provoquent, comme les aminosides,un blocage neuromuscu<strong>la</strong>ireinsensible à <strong>la</strong> néostigmine ou aucalcium. De l’apathie et des insuffisancesrespiratoires ont égalementété décrites chez le chien et chez leveau. Les polymyxines sont hautementnéphrotoxiques.InteractionsEffets synergiques avec les substancesantimicrobiennes qui portentatteinte à l’intégrité de <strong>la</strong> membranep<strong>la</strong>smatique, telles que les sulfamidéset le triméthoprime.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucun effet tératogène n’a été observélors d’administration orale chezle rat, ni aucune influence sur <strong>la</strong> fertilité.Il existe cependant des indicesde fœtotoxicité lors d’administrationparentérale.LMR colistine: COLISTINE SULFATE 1 MIO UI/ml (VMD)colistine sulfate: 1.000.000 UI/mlsolution injectable imPosologie:veau: 2 x pj 50.000 UI/kg (3 j)Viande: veau: 62 jf<strong>la</strong>con 40 mlR/
1 MEDICAMENTS ANTIBACTÉRIENS29COLIVET “S” (Prodivet)colistine (sulfate): 2,5 mg/mlsolution injectable imPosologie:porcelet: 2,5 mg/kg pj (3 - 5 j)Viande: 21 jf<strong>la</strong>con 100 mlR/COLIVET “S” FORTE (Prodivet)colistine (sulfate): 20 mg/mlsolution injectable imPosologie:veau, Su: 2,5 mg/kg pj (3 - 5 j)Viande veau: 26 j, Su: 21 jf<strong>la</strong>con 100 mlR/1.1.6.2 BacitracineIndicationsDiminution des signes cliniques et desdécès causés par l’entérocolite liée àdes infections à Clostridium perfringenssensibles à <strong>la</strong> bacitracine, chezles <strong>la</strong>pins d’élevage.PharmacodynamieLa bacitracine est un complexe de sixantibiotiques polypeptidiques analoguesqui inhibent <strong>la</strong> synthèse de <strong>la</strong>paroi cellu<strong>la</strong>ire. Le spectre anti-bactérieninclut les bactéries Gram positivesaérobies et anaérobies.PharmacocinétiqueAprès administration par voie orale ouapplication locale sur <strong>la</strong> peau et les muqueuses,<strong>la</strong> bacitracine est très peu résorbée.Après une administration par voieintramuscu<strong>la</strong>ire, <strong>la</strong> bacitracine montre unebonne distribution tissu<strong>la</strong>ire et est principalementexcrétée par les urines.Contre-indicationsL’insuffisance rénale est contre-indiquéeen cas d’administration parentérale.Effets indésirablesLa bacitracine est néphrotoxique. Sonutilisation par voie parentérale estdonc très limitée.InteractionsUne synergie est observée avec lespénicillines, les aminosides et lespolymyxines.Précautions particulières/Risquespour l’hommeLa bacitracine peut causer des réactionsd’hypersensibilité en cas d’inha<strong>la</strong>tionou de contact avec <strong>la</strong> peau. Il estrecommandé de porter des vêtementsde protection, des lunettes de sécurité,des gants et un masque anti-poussièrelors de <strong>la</strong> préparation de <strong>la</strong> solution.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucun effet tératogène ou embryotoxiquen’a été observé chez le rat encas de dose thérapeutique. L’innocuité<strong>du</strong> pro<strong>du</strong>it n’a cependant pas été établiechez les <strong>la</strong>pins gestants ou en<strong>la</strong>ctation. L’usage n’en est pas recommandéchez ces animaux.LMR bacitracine: BACIVET S (Pfizer A.H.)bacitracine zinc: 4200 UI/gpoudre po dans l’eau de boissonPosologie:<strong>la</strong>pin: 420 UI/kg PV pj (14 j, éventuellement+ 7 j)Viande et abats: 2 jsachet 10 x 100 gR/1.1.7 Sulfamidés et TriméthoprimeIndications - spectre d’activité - résistancesLes sulfamidés sont des substances bactériostatiques dont le spectre comprendles bactéries GRAM+ et GRAM- aérobies et anaérobies, les ch<strong>la</strong>mydies, les toxop<strong>la</strong>smeset les coccidies. Les pseudomonades, les mycop<strong>la</strong>smes et les spirochètessont naturellement résistants. Les sulfamidés sont surtout utilisés dans le traitementdes coccidioses (vo<strong>la</strong>ille, ruminants) ou des infections urinaires et digestives chez lescarnivores. Les résistances acquises assez fréquentes limitent cependant leur usageclinique. Le triméthoprime est aussi une substance bactériostatique active contreles bactéries GRAM- et +, mais pas contre les bactéries anaérobies. Les pseudomonades,les mycop<strong>la</strong>smes et les ch<strong>la</strong>mydies sont aussi naturellement résistants.Actuellement, les sulfamidés sont souvent associés au triméthoprime en raisond’effets synergiques. Ces combinaisons, souvent dans un rapport de 5/1, deviennentbactéricides.PharmacodynamieLes sulfamidés agissent par inhibition compétitive de l’incorporation de l’acidepara-aminobenzoïque (PABA) dans <strong>la</strong> chaîne de synthèse d’acide folique parl’enzyme dihydroptéroate synthétase. Le maintien de concentrations effectivespendant toute <strong>la</strong> <strong>du</strong>rée <strong>du</strong> traitement est indispensable. La présence d’un excèsde PABA, dans les tissus nécrosés, le pus et certaines préparations pharmaceutiques,peut donc entraver leur action. Le triméthoprime est une substance
30 1 MEDICAMENTS ANTIBACTÉRIENSbactériostatique inhibant aussi <strong>la</strong> synthèse de l’acide folique, dont <strong>la</strong> cible enzymatique,l’enzyme dihydrofo<strong>la</strong>te ré<strong>du</strong>ctase, est différente de celle des sulfamidés.Cette double activité sur deux enzymes différents d’une même chaîne métaboliqueest à <strong>la</strong> base de <strong>la</strong> synergie entre les sulfamidés et le triméthoprime.PharmacocinétiqueLes sulfamidés sont des acides faibles. Ils sont en général bien absorbés par voieorale et se distribuent <strong>la</strong>rgement dans tous les tissus, y compris dans le liquidecéphalo-rachidien et synovial. La distribution tissu<strong>la</strong>ire est cependant variable d’unemolécule à l’autre. Le volume de distribution de <strong>la</strong> sulfadiadiazine est assez faibleen comparaison d’autres sulfamidés. Leur concentration dans le <strong>la</strong>it est souventtrop faible pour le traitement de <strong>la</strong> mammite. Leur élimination rénale est facilitée àpH alcalin. La cristallurie peut être ré<strong>du</strong>ite grâce à un apport hydrique adéquat et àl’alcalinisation des urines. La diffusion tissu<strong>la</strong>ire <strong>du</strong> triméthoprime est bonne, notammentdans <strong>la</strong> prostate. Il est en partie métabolisé par le foie et éliminé par les reins.Contre-indicationsPathologies hépatiques, troubles sanguins et hypersensibilité.Effets indésirablesLes sulfamidés peuvent provoquer des troubles rénaux (hématurie, cristallurie, blocage),des troubles de l’hématopoïèse (thrombocytopénie, anémie), des allergies,de <strong>la</strong> kératoconjonctivite sèche et des réactions idiosyncrasiques en particulierchez les chiens Dobermann pinscher, les Schnauzers nains, les chiens Samoyèdeset quelques autres races à pe<strong>la</strong>ge b<strong>la</strong>nc (fièvre, urticaire, polyarthrite,...).InteractionsL’élimination des sulfamidés peut être ralentie par interaction avec d’autres médicaments(phénylbutazone, antibiotiques ionophores, hormones androgènes).Précautions particulièresUtiliser ces substances avec précaution chez les chiens dont l’anamnèse révèleune urolithiase.Repro<strong>du</strong>ction et <strong>la</strong>ctationA doses élevées, des effets tératogènes ont été observés chez les animaux de<strong>la</strong>boratoire.1.1.7.1 TriméthoprimeLMR triméthoprime: THERAPRIM pot (Oropharma)triméthoprime: 80 mg/gpoudre po dans l’eau de boissonPosologie:pigeon, oiseau d’ornement:20 mg/kg ou 400 mg/2 l d’eau (5 j)Ne pas administrer aux pigeons destinés à <strong>la</strong>consommation humainepoudre 120 g (boîte)R/THERAPRIM sachet (Oropharma)triméthoprime: 400 mg/5 gpoudre po dans l’eau de boissonPosologie:pigeon, oiseau d’ornement:20 mg/kg ou 400 mg/2 l d’eau (5 j)Ne pas administrer aux pigeons destinés à <strong>la</strong>consommation humainepoudre 8 x 5 gR/1.1.7.2 Sulfamidés associés autriméthoprimeLMR sulfamidés + triméthoprime : BORGAL 24 % (Virbac)sulfadoxine: 200 mg/mltriméthoprime: 40 mg/mlsolution injectable im, iv, sc (Bo, Su) - iv (Eq)Posologie:Eq, pou<strong>la</strong>in, Bo, veau, Su, porcelet:2,5 mg de T + 12,5 mg de S/kgViande: Eq, Bo, Su: 10 j, Lait: Bo: 4 j (96 h)f<strong>la</strong>con 100 mlR/COSUMIX PLUS (VMD)sulfachlorpyridazine sodique: 100 mg/gtriméthoprime: 20 mg/gpoudre po dans l’eau de boissonPosologie:vo<strong>la</strong>ille: 24 mg/kg pj (3 - 6 j)Viande: vo<strong>la</strong>ille: 7 jNe pas administrer aux poules pondeuses dont lesoeufs sont destinés à <strong>la</strong> consommation humainepoudre 500 g, 2 kgR/
1 MEDICAMENTS ANTIBACTÉRIENS31DOFATRIM-JECT (Dopharma Research)triméthoprime: 40 mg/mlsulfadoxine: 200 mg/mlsolution injectable iv, im, scPosologie:Bo, Su: 15 mg/kgEn cas d’infect. graves et si PV < 200 kg:25 mg/kgViande: 8 j, Lait: 2 jf<strong>la</strong>con 100 ml, 250 mlR/DUPHATROXIM (Pfizer A.H.)sulfadiazine: 200 mg/mltriméthoprime: 40 mg/mlsolution injectable im, ivPosologie:Bo, Su: 12,5 mg de S/kg + 2,5 mgde T/kg pj(1 ml/16 kg pj) (5 j)Viande: Bo: 8 j, Su: 20 j, Lait: 48 hf<strong>la</strong>con 100 ml, 250 mlR/EMDOTRIM 10% sol (Emdoka)sulfadiazine: 83,3 mg/mltriméthoprime: 16,7 mg/mlsolution poPosologie:poule: 33,3 mg de S/kg pj + 6,7 mgde T/kg pj (4 - 6 j)Viande: 3 j, Oeuf: ne pas administrer aux poulesdont les oeufs sont destinés à <strong>la</strong> consommationhumainef<strong>la</strong>con 100 ml, 1000 ml, 5000 mlR/EMDOTRIM 60% MIX (Emdoka)triméthoprime: 100 mg/gsulfadiazine (sodique): 500 mg/gpoudre po dans l’eau de boissonPosologie:Su (porcelet, porcelet sevré):30 mg actif/kg pj (en 2 prises) (5 j)Viande et abats: Su: 10 jpoudre 500 g, 1 kg, 2 kgR/EQUIBACTIN vet (Le vet)sulfadiazine: 333,3 mg/gtriméthoprime: 66,7 mg/gpâte poPosologie:Eq: 5 mg de T/kg + 25 mg de S/kg pj (5 j)Viande et abats: 14 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineseringue 45 gR/LIDOPRIM S (Prodivet)sulfaméthoxazole: 200 mg/mltriméthoprime: 40 mg/mlsolution injectable imPosologie:veau, porcelet: 25 mg de S/kg + 5 mgde T/kg pj (3 - 5 j)Viande: veau: 24 j, porcelet: 4 jf<strong>la</strong>con 250 mlR/METHOXASOL 20/100 mg/ml sol buv porcs,poulets (Eurovet A.H.)sulfaméthoxazole: 100 mg/mltriméthroprime: 20 mg/mlsolution po dans l’eau de boissonPosologie:Su: 25 mg/kg (3-4 j)poulets de chair: 33 mg/ml (3-4 j)Viande: Su: 5 j, Av: 6 jNe pas administrer aux poules pondeuses dontles œufs sont destinés à <strong>la</strong> consommationhumainef<strong>la</strong>con 1 l, 5 lR/TRIMAZIN 30 % (Ke<strong>la</strong> Laboratoria)sulfadiazine (sodique): 250 mg/gtriméthoprime: 50 mg/gpoudre po dans l’alimentation ou dans l’eau deboisson (Su)Posologie:Su: 25 mg de S/kg + 5 mg de T/kg (en 2prises pj) (3 - 5 j)Viande: Su: 12 jpoudre 1 kgR/TRIMAZIN 90 % (Ke<strong>la</strong> Laboratoria)sulfadiazine (sodique): 750 mg/gtriméthoprime: 150 mg/gpoudre po avec l’alimentation, dans l’eau deboissonPosologie:Su: 25 mg de S/kg + 5 mg de T/kg (en 2prises pj) (3 - 5 j)Viande: 12 jpoudre 1 kgR/TUCOPRIM poudre (Pfizer A.H.)sulfadiazine: 12,5 % (w/w)triméthoprime: 2,5 % (w/w)prémé<strong>la</strong>nge médicamenteux poPosologie:activité combinée de S/T: Su:15 - 30 mg/kg pj (5 j, truie: 3 j avant <strong>la</strong> misebas jusqu’à 2 j après)poule non pondeuse: 25 - 30 mg/kg pj (10 j)Viande: Su: 5 j , poulet: 24 hNe pas administrer aux poules dont les oeufssont destinés à <strong>la</strong> consommation humaineprém méd 25 kgR/premix1.1.8 FluoroquinolonesLes fluoroquinolones dérivent des quinolones et s’en distinguent notamment parl’ajout d’un atome de fluor. Les quinolones et les fluoroquinolones diffèrent aussipar leurs spectres respectifs d’activité et leurs propriétés pharmacocinétiques.Ce groupe comprend <strong>la</strong> fluméquine, une ancienne fluoroquinolone utilisée dansle traitement des infections digestives chez les animaux de rente, et des dérivésplus récemment développés: l’enrofloxacine, <strong>la</strong> marbofloxacine, <strong>la</strong> danofloxacine,<strong>la</strong> difloxacine, l’ibafloxacine et <strong>la</strong> pradofloxacine. Ce sont des substancesd’origine purement synthétique.
32 1 MEDICAMENTS ANTIBACTÉRIENSIndications - spectre d’activité – résistancesLes fluoroquinolones ont une activité bactéricide. Elles sont actives contre lesaérobies GRAM- (y compris Pseudomonas aeruginosa), les mycop<strong>la</strong>smes et lesrickettsies, mais peu actives contre les bactéries anaérobies à l’exception de <strong>la</strong>pradofloxacine. Leur activité vis-à-vis des GRAM+ est variable, mais reste modérée.Les fluoroquinolones les plus récentes utilisées en médecine humaine sontplus actives sur les bactéries Gram+ et sur les bactéries anaérobies. Les résistancessont avant tout <strong>la</strong> conséquence de mutations dans les gènes qui codentpour les topoïsomérases bactériennes, mais aussi parfois de l’existence de systèmed’efflux visant à extraire l’antibiotique des corps bactériens. En revanche, lesschémas posologiques récents basés sur l’utilisation systémique de fortes dosesd’antibiotiques pendant un temps re<strong>la</strong>tivement court assurent une efficacité optimaleet limitent probablement l’émergence de résistance. L’émergence récente demécanismes de résistances à bas niveau ou subcliniques (mécanismes Qnr parexemple) renforce <strong>la</strong> nécessité <strong>du</strong> strict respect <strong>du</strong> schéma posologique.Pour plus d’informations sur <strong>la</strong> résistance chez les fluoroquinolones, voir FoliaVeterinaria 2004 n°3 et 2008 n°3.PharmacodynamieLes fluoroquinolones agissent par inhibition des protéines (topoïsomérases) quistabilisent <strong>la</strong> structure tridimensionnelle de l’ADN bactérien, dont l’ADN gyrase.PharmacocinétiqueLes fluoroquinolones sont rapidement et complètement absorbées (80 - 100 %)oralement chez les monogastriques. Des concentrations sériques maximalessont atteintes environ 1 heure après l’ingestion. L’absorption orale diminue enprésence d’aluminium ou de magnésium présents dans les préparations antiacides.Chez les ruminants, <strong>la</strong> biodisponibilité orale est plus faible. Du fait de leurcaractère liposoluble, <strong>la</strong> distribution tissu<strong>la</strong>ire des fluoroquinolones est <strong>la</strong>rge; ellespénètrent bien au niveau des sécrétions bronchiques, des os et des carti<strong>la</strong>gesainsi que de <strong>la</strong> prostate. Leur concentration élevée dans les macrophages et lesneutrophiles contribue à concentrer l’antibiotique au niveau des sites entreprispar une vive réaction inf<strong>la</strong>mmatoire. Elles sont partiellement métabolisées par lefoie et excrétées sous forme active par <strong>la</strong> bile et les urines. Les concentrationsurinaires peuvent être jusqu’à 10 fois supérieures à celles <strong>du</strong> p<strong>la</strong>sma.Contre-indicationsL’usage des fluoroquinolones chez des animaux présentant des troubles articu<strong>la</strong>iresou de <strong>la</strong> croissance doit se faire avec <strong>la</strong> plus grande prudence si d’autressolutions thérapeutiques ne sont pas envisageables.Effets indésirablesLes fluoroquinolones sont peu toxiques. Leur principal effet indésirable estl’érosion des carti<strong>la</strong>ges chez les chiens en croissance. Pour cette raison, il estconseillé de consulter <strong>la</strong> rubrique « contre-indications » dans les notices re<strong>la</strong>tivesà chaque spécialité afin de tenir compte des particu<strong>la</strong>rités de chaque antibiotique.En général, l’administration de fluoroquinolones chez les chiens de moins d’unan ou de moins de 18 mois pour les grandes races est déconseillée. Dans le casde <strong>la</strong> marbofloxacine, le dé<strong>la</strong>i signalé dans <strong>la</strong> notice est plus court. Des troublesdigestifs, notamment des nausées et des diarrhées, et des signes nerveux ont étédécrits à très fortes doses. Des effets toxiques au niveau de <strong>la</strong> rétine con<strong>du</strong>isantà <strong>la</strong> cécité ont été observés chez le chat lors de surdosages avec l’enrofloxacine.InteractionsLa c<strong>la</strong>irance hépatique d’autres médicaments métabolisés par le foie (théophylline)peut être ré<strong>du</strong>ite par l’administration des quinolones.Précautions particulièresL’administration orale de fluoroquinolones chez les espèces animales de rentepose de manière particulièrement aiguë le problème de l’émergence de bactériesrésistantes dans <strong>la</strong> flore bactérienne digestive et de l’impact de cette pratique surle transfert de ces popu<strong>la</strong>tions bactériennes chez l’homme. Pour cette raison, lesfluoroquinolones sont des antimicrobiens de deuxième ligne qui ne devraient êtreadministrés qu’après l’identification <strong>du</strong> germe et <strong>la</strong> détermination de sa sensibilité,chaque fois que ce<strong>la</strong> est possible, chez les animaux ma<strong>la</strong>des ou au sein destroupeaux. Par ailleurs, les fluoroquinolones devraient être réservées au traitementdes ma<strong>la</strong>dies infectieuses peu sensibles ou suspectées répondre faiblement aux
1 MEDICAMENTS ANTIBACTÉRIENS33autres antibiotiques. Cette suspicion doit pouvoir se justifier par des informationsscientifiques ou des données cliniques avérées.Il est conseillé de ne pas utiliser les fluoroquinolones chez les animaux atteints detroubles <strong>du</strong> système nerveux central (SNC) comme l’épilepsie, ces antibiotiquesétant susceptibles d’in<strong>du</strong>ire des convulsions chez les animaux prédisposés.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de <strong>la</strong> plupart des fluoroquinolones en période de gestation ou de <strong>la</strong>ctationn’est pas établie. Des malformations liées à l’administration de fluoroquinolonesont été observées chez certaines espèces de <strong>la</strong>boratoire. L’ibafloxacinepeut être administrée aux chiennes en gestation, mais son innocuité n’a pas étéétablie chez les chattes en gestation, ni chez les chiennes et chattes en <strong>la</strong>ctationni chez les animaux repro<strong>du</strong>cteurs mâles.1.1.8.1 Danofloxacine1.1.8.3 EnrofloxacineLMR danofloxacine: ADVOCIN 180 (Pfizer A.H.)danofloxacine: 180 mg/mlsolution injectable sc, ivPosologie:Bo: 1 x 6 mg/kg (peut être répété après48 h)Viande: 8 j, Lait: 4 jf<strong>la</strong>con 50 ml, 100 mlR/ADVOCIN 2,5 % (Pfizer A.H.)danofloxacine (mési<strong>la</strong>te): 25 mg/mlsolution injectable im, sc, ivPosologie:Bo (im, sc ou iv): 1,25 mg/kg pj (3 j, peutêtre prolongé de 2 j si nécessaire)Su (im): 1,25 mg/kg pj (3 j)Viande Bo: 3 j, Su: 6 j, Lait Bo: 48 hf<strong>la</strong>con 100 mlR/1.1.8.2 DifloxacineLMR difloxacine: DICURAL 100 mg/ml sol orale (Pfizer A.H.)difloxacine (chlorhydrate): 100 mg/mlsolution po dans l’eau de boissonPosologie:poule, dinde (< 2 kg): 10 mg/kg pjViande: 24 hOeuf: ne pas administrer aux Av dont les oeufssont destinés à <strong>la</strong> consommation humainef<strong>la</strong>con 1000 mlR/DICURAL 50 mg/ml sol inj (Pfizer A.H.)difloxacine: 50 mg/mlsolution injectable scPosologie:Bo: 2,5 - 5 mg/kg pj (3-5 j)Ca: 5 mg/kgViande: Bo: 46 jf<strong>la</strong>con 50 mlR/LMR enrofloxacine: BAYTRIL 0,5 % sol orale (Bayer)enrofloxacine: 5 mg/mlsolution poPosologie:porcelet:< 3 kg PV: 5 mg/animal (3 j)de 3 à 10 kg PV: 15 mg/animal (3 j)Viande: 7 jf<strong>la</strong>con 100 mlR/BAYTRIL 10% sol inj (Bayer)enrofloxacine: 100 mg/mlsolution injectable ivPosologie:Bo: 5 mg/kg pj (2 j) avec 24 h d’intervalleViande: 7 j, Lait: 3 jf<strong>la</strong>con 100 mlR/BAYTRIL 10% sol orale (Bayer)enrofloxacine: 100 mg/mlsolution po dans l’eau de boissonPosologie:poule, dinde: 10 mg/kg (3 j ou 5 j en cas desalmonellose et pasteurellose)Viande: poule, dinde: 3 jNe pas administrer aux poules pondeusesdont les oeufs sont destinés à <strong>la</strong> consommationhumaine. Ne pas administrer aux futurespondeuses pendant les 14 j précédant le débutde <strong>la</strong> ponte.f<strong>la</strong>con 100 ml, 1000 mlR/BAYTRIL 100 (Bayer)enrofloxacine: 100 mg/mlsolution injectable scPosologie:Bo hors de <strong>la</strong>ctation: 1 x 7,5 mg/kg (sc)Bo en <strong>la</strong>ctation: 5 mg/kg (iv), répéter après24 hViande: Bo hors <strong>la</strong>ctation: 14 j, Bo en <strong>la</strong>ctation:7 j, Lait: 3 jf<strong>la</strong>con 100 mlR/BAYTRIL 2,5 % sol inj (Bayer)enrofloxacine: 25 mg/mlsolution injectable scPosologie:Ca, Fe: 5 mg/kg pj (5 - 10 j)f<strong>la</strong>con 50 mlR/
34 1 MEDICAMENTS ANTIBACTÉRIENSBAYTRIL 2,5 % sol orale (Bayer)enrofloxacine: 25 mg/mlsolution poPosologie:veau: 2,5 - 5 mg/kg pj (3 - 5 j)Viande: 7 jf<strong>la</strong>con 500 mlR/BAYTRIL 5 % sol inj (Bayer)enrofloxacine: 50 mg/mlsolution injectable sc (veau), iv (Bo, veau), im(Su)Posologie:- Bo, veau:dose recommandée: 2,5 mg/kg pj (3 j)troubles resp. graves: 5 mg/kg pj (3 j)salmonellose: 5 mg/kg pj (5 j)- Su:dose recommandée: 2,5 mg/kg pj (3 j)troubles resp. graves: 5 mg/kg pjViande: Bo: 7 j (iv), 12 j (sc), Su: 10 j, Lait: 3 j (iv)Ne pas administrer par voie sc chez les Bo en<strong>la</strong>ctationf<strong>la</strong>con 100 mlR/BAYTRIL FLAVOUR 25 mg/ml (Bayer)enrofloxacine: 25 mg/mlsuspension poPosologie:Fe: 1 x 5 mg/kg pj (5 - 10 j)f<strong>la</strong>con 8,5 mlR/BAYTRIL FLAVOUR 15 mg compr (Bayer)enrofloxacine: 15 mgcomprimé poPosologie:Ca, Fe: 5 mg/kg pj (5 - 10 j)compr 10, 10 x 10R/BAYTRIL FLAVOUR 50 mg compr (Bayer)enrofloxacine: 50 mgcomprimé poPosologie:Ca: 5 mg/kg pj (5 - 10 j)compr 10, 10 x 10R/BAYTRIL FLAVOUR 150 mg compr (Bayer)enrofloxacine: 150 mgcomprimé poPosologie:Ca: 5 mg/kg pj (5 - 10 j)compr 10, 10 x 10R/BAYTRIL FLAVOUR 250 mg compr (Bayer)enrofloxacine: 50 mgcomprimé poPosologie:Ca: 5 mg/kg pj (5 - 10 j)compr 12R/BAYTRIL MAX (Bayer)enrofloxacine: 100 mg/mlsolution injectable sc (Bo), iv (Bo), im (Su)Posologie:Bo:infect resp: 1 x 7,5 mg/kg sc (infect chronou grave: répéter après 48 h)mammite colibacil<strong>la</strong>ire: 5 mg/kg iv (2 - 3 j)Su:resp infect: 1 x 7,5 mg/kg im (infect chronou grave: répéter après 48 h)Viande: Bo (sc): 14 j, Bo (iv): 7 j, Su: 12 j,Lait: 3 jf<strong>la</strong>con 100 mlR/BAYTRIL pigeon/rabbit (Bayer)enrofloxacine: 25 mg/mlsolution poPosologie:pigeon: 200 ppm d’enroflox dans l’eau deboisson (5 j), soit 8 ml de pro<strong>du</strong>it/l d’eau<strong>la</strong>pin: 1 x 5 mg enroflox/kg pj (5 j)Viande: <strong>la</strong>pin: 3 j - Ne pas administrer auxpigeons destinés à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/BAYTRIL piglet (Bayer)enrofloxacine: 25 mg/mlsolution injectable imPosologie:Su: 1 x pj 2,5 mg/kg (3 j), en cas d’infectresp graves: 5 mg/kgViande et abats: 10 jf<strong>la</strong>con 100 mlR/BAYTRIL swine (Bayer)enrofloxacine: 100 mg/mlsolution injectable imPosologie:Su: 1 x pj 2,5 mg/kg (3 j), en cas d’infectresp graves: 1 x pj 5 mg/kg (3 - 5 j)Viande et abats: 14 jf<strong>la</strong>con 100 mlR/COLMYC 100 mg/ml (S.P. Veterinaria)enrofloxacine: 100 mg/mlsolution injectable sc (Bo), im (Su)Posologie:Bo: 2,5 mg/kg pj (5 j) scSu: 2,5 mg/kg pj (3 j) imViande et abats: Bo (sc): 14 j, Su (im): 10 j,Lait: 96 hf<strong>la</strong>con 100, 250 mlR/DORAFLOX 25 mg/ml (Vetpharma A.H.)enrofloxacine: 25 mg/mlsolution po avec le <strong>la</strong>it, l’eau de boissonPosologie:veau (non ruminant): 5 mg/kg pj (5 j)Viande et abats: veau: 11 jf<strong>la</strong>con 1 lR/
1 MEDICAMENTS ANTIBACTÉRIENS35DORAFLOX 100 mg/ml (Vetpharma A.H.)enrofloxacine: 100 mg/mlsolution injectable sc, imPosologie:Bo: infect resp, digestives:2,5 mg/kg pj (3 j) scinfect resp compliquées: 5 mg/kg (5 j)Su: infect resp, digestives:2,5 mg/kg pj (3 j) iminfect resp compliquées: 5 mg/kg (5 j)Viande et abats: Bo (sc): 13 j, Su (im): 10 j, Lait:Bo (sc): 84 hf<strong>la</strong>con 100 ml, 250 mlR/ENRO-K 10% (Karizoo Lab)enrofloxacine: 100 mg/mlsolution po avec l’eau de boissonPosologie:poule, dinde: 10 mg/kg pj (min 3 j, en cas desalmonellose: 5 j)Viande et abats: poule: 4 j, dinde: 4 jNe pas utiliser chez les poules pro<strong>du</strong>ctricesdont les œufs sont destinés à <strong>la</strong> consommationhumaineNe pas utiliser dans les 4 sem précédant ledébut de <strong>la</strong> pontef<strong>la</strong>con 1 lR/ENROSHORT 100 mg/ml (Eurovet A.H.)enrofloxacine: 100 mg/mlsolution poPosologie:poule, dinde: 10 mg/kg pj (min 3 j, salmonellose:5 j)Viande et abats: 3 j, ne pas administrer auxoiseaux pondeurs dont les œufs sont destinés à<strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 1 lR/ENROVETO 100 mg/ml (Vetpharma A.H.)enrofloxacine: 100 mg/mlsolution po dans l’eau de boissonPosologie:poulet, dinde: 10 mg/kg PV pj (5 j)Viande et abats: poulet, dinde: 4 jNe pas utiliser chez les oiseaux dans les 4 semprécédant le début de <strong>la</strong> ponte si les oeufs sontdestinés à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/ENROX FLAVOUR 15 mg (KRKA)enrofloxacine: 15 mgcomprimé poPosologie:Ca (âge > 1 an ou 18 m), Fe (âge > 8 sem):1 x pj 5 mg/kg ou 2 x pj moitié de <strong>la</strong> dose(5 à 10 j), avec ou sans nourriturecompr 100R/ENROX FLAVOUR 50 mg, 150 mg (KRKA)enrofloxacine: 50 mg ou 150 mgcomprimé poPosologie:Ca (âge > 1 an ou 18 m), Fe (âge > 8 sem):1 x pj 5 mg/kg ou 2 x pj moitié de <strong>la</strong> dose(5 à 10 j), avec ou sans nourriturecompr 100R/ENROXIL MAX 100 mg/ml sol inj (KRKA)enrofloxacine: 100 mg/mlsolution injectable scPosologie:Bo: 7,5 mg/kgViande et abats: 14 j, Lait: 84 hf<strong>la</strong>con 100 mlR/FENOFLOX 50 mg/ml sol inj pour bovins, porcs,chiens et chats (Chanelle Pharmaceuticals)enrofloxacine: 50 mg/mlsolution injectable sc (Bo, Ca, Fe), im (Su)Posologie:Bo, Su: 2.5 mg/kg pj (3 j)infect resp grave: 5 mg/kg pj (5 j)Ca, Fe: 5 mg/kg pj (5 j)Viande + abats: Bo: 14 j, Su: 10 jNe pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/FENOFLOX 100 mg/ml sol inj pour bovins et porcs(Chanelle Pharmaceuticals)enrofloxacine: 100 mg/mlsolution injectable sc, iv (Bo), im (Su)Posologie:Bo, Su: 2.5 mg/kg pj (3 j)infect resp grave: 5 mg/kg pj (5 j)Bo mammite (iv): 5 mg/kg pj (2 j)Viande + abats: Bo (sc): 10 j, Bo (iv): 4 j, Su: 10 jLait: Bo (sc): 84 h (7 traites), Bo (iv): 72 h (6traites)f<strong>la</strong>con 250 mlR/FLOXABACTIN 15 mg chat et chien (Le Vet)enrofloxacine: 15 mg/comprcomprimé poPosologie:Ca (âge > 12 - 18 m selon race):5 mg/kg PV pj (10 j dans infect urin basses,15 j dans infect urin hautes et infect urinbasses associées à prostatite, jusqu’à 21 jdans pyodermite superfic, jusqu’à 49 j danspyodermite prof)Fe (âge > 3 m, PV > 1 kg):5 mg/kg PV pj (5 - 10 j)compr 100R/FLOXABACTIN 50 mg chien (Le Vet)enrofloxacine: 50 mg/comprcomprimé poPosologie:Ca (âge > 12 - 18 m selon race):5 mg/kg PV pj (10 j dans infect urin basses,15 j dans infect urin hautes et infect urinbasses associées à prostatite, jusqu’à 21 jdans pyodermite superfic, jusqu’à 49 j danspyodermite prof)compr 100R/FLOXABACTIN 150 mg chien (Le Vet)enrofloxacine: 150 mg/comprcomprimé poPosologie:Ca (âge > 12 - 18 m selon race):5 mg/kg PV pj (10 j dans infect urin basses,15 j dans infect urin hautes et infect urinbasses associées à prostatite, jusqu’à 21 jdans pyodermite superfic, jusqu’à 49 j danspyodermite prof)compr 100R/
36 1 MEDICAMENTS ANTIBACTÉRIENSFLOXADIL 50 mg/ml sol inj (Emdoka)enrofloxacine: 50 mg/mlsolution injectable sc, iv (Bo), im (Su)Posologie:Bo:dose recommandée: 2,5 mg/kg pj (3 j)infect resp graves, salmonellose: 5 mg/kg (3 j)(salmonellose chez le veau: 5 j)Su:dose recommandée: 2,5 mg/kg pj (3 j)infect. resp. sévères: 5 mg/kgViande: Bo: 7 j (iv), 12 j (sc), Su: 10 jLait: 3 j (iv), ne pas administrer par voie sc chezles Bo en <strong>la</strong>ctationf<strong>la</strong>con 100 ml, 250 mlR/FLOXADIL 100 mg/ml sol inj (Emdoka)enrofloxacine: 100 mg/mlsolution injectable sc, iv (Bo), im (Su)Posologie:Bo:dose recommandée: 2,5 mg/kg pj (5 j)infect resp graves: 5 mg/kg pj (5 j)Su: 2,5 mg/kg pj (3 j) ( 1 - 2 j en cas desyndr MMA)Viande: Bo: 7 j (iv), 14 j (sc), Su: 9 j (im),Lait: 3 j (iv), 5 j (sc)f<strong>la</strong>con 100 ml, 250 mlR/FLOXAMAX 100 mg/ml sol po (S.P. Veterinaria)enrofloxacine: 100 mg/mlsolution po dans l’eau de boissonPosologie:poule, dinde: 10 mg/kg (3 j, salmonellose oupasteurellose: 5 j)Viande et abats: 3 jNe pas utiliser chez les poules pondeuses dontles œufs sont destinés à <strong>la</strong> consommation humaineni chez les poules pondeuses d’élevageendéans les 14 j avant le début de <strong>la</strong> pontef<strong>la</strong>con 1 l, 5 lR/SPECTRON 100 mg/ml (Hipra Lab)enrofloxacine: 100 mg/mlsolution po dans l’eau de boissonPosologie:poulet, dinde: 10 mg/kg pj (3 j, salmonellose:5 j)Viande et abats: 3 jNe pas administrer aux animaux dont les œufssont destinés à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/UNISOL 100 mg/ml sol buvable (Vetpharma A.H.)enrofloxacine: 100 mg/mlsolution po avec l’eau de boissonPosologie:poule, dinde: 10 mg/kg pj (3-5 j)Viande: poule, dinde: 4 jNe pas utiliser chez les poules dont les œufssont destinés à <strong>la</strong> consommation humaine nidans un dé<strong>la</strong>i de 4 sem avant le début de pontef<strong>la</strong>con 1 lR/XEDEN 15 mg compr chats (Sogeval Lab)enrofloxacine: 15 mgcomprimé poPosologie:Fe: 1 x 5 mg/kg pj (5 - 10 j)compr 12, 120R/XEDEN 50 mg compr chiens (Sogeval Lab)enrofloxacine: 50 mgcomprimé poPosologie:Ca: 5 mg/kg 1 x pj (10 j infect voies urinbasses, 15 j infect voies urin hautes et infectvoies urin basses liées à prostatite, 21 jmax pyodermites superfic selon réponseclinique, 49 j max pyodermites prof selonréponse clinique)compr 10, 100R/XEDEN 150 mg compr chiens (Sogeval Lab)enrofloxacine: 150 mgcomprimé poPosologie:Ca: 5 mg/kg 1 x pj (10 j infect voies urinbasses, 15 j infect voies urin hautes et infectvoies urin basses liées à prostatite, 21 jmax pyodermites superfic selon réponseclinique, 49 j max pyodermites prof selonréponse clinique)compr 12, 120R/XEDEN 200 mg compr chiens (Sogeval Lab)enrofloxacine: 200 mgcomprimé poPosologie:Ca: 5 mg/kg 1 x pj (10 j infect voies urinbasses, 15 j infect voies urin hautes et infectvoies urin basses liées à prostatite, 21 jmax pyodermites superfic selon réponseclinique, 49 j max pyodermites prof selonréponse clinique)compr 12, 120R/1.1.8.4 FluméquineLMR fluméquine: ENTERFLUME 50 % (Dopharma Research)fluméquine: 500 mg/gpoudre po dans l’eau de boisson, le <strong>la</strong>itPosologie:veau non ruminant: 2 x pj 5 - 10 mg/kg(3 - 5 j)vo<strong>la</strong>ille: 10 mg/kg pj (3 - 5 j)Viande: veau: 4 j, vo<strong>la</strong>ille: 2 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainepoudre 1 kgR/FLUMIQUIL 50 % (Ceva Santé Animale)fluméquine: 500 mg/gpoudre po dans l’eau de boisson ou le <strong>la</strong>itPosologie:veau (non ruminant), poulet de chair:12 mg/kg PV pj (3 - 5 j)Su: 15 mg/kg PV pj (3 - 5 j)Viande: veau: 6 j, Su: 1 j, vo<strong>la</strong>ille: 2 jNe pas administrer aux poules dont les oeufssont destinés à <strong>la</strong> consommation humainepoudre 1 kgR/
1 MEDICAMENTS ANTIBACTÉRIENS371.1.8.5 IbafloxacineLMR ibafloxacine: IBAFLIN 3 % gel oral (MSD A.H.)ibafloxacine: 30 mg/ggel poPosologie:Ca, Fe: 15 mg/kg pj (pendant repas)applic 1 x 15 mlR/1.1.8.6 MarbofloxacineLMR marbofloxacine: FORCYL 160 mg/ml (Vétoquinol)marbofloxacine: 160 mg/mlsolution injectable imPosologie:Bo: 1 x 10 mg/kgViande (abats): 5 jLait: 48 hf<strong>la</strong>con 100 mlR/MARBIFLOX 20 mg/ml (KRKA)marbofloxacine: 20 mg/mlsolution injectable sc, iv (Bo), im (Bo, Su)Posologie:veau: 2 mg/kg pj (3-5 j) (im, sc, 1e inj peutégalement par voie iv)Su: 2 mg/kg pj (3-5 j) (im)Viande et abats: veau: 6 j, Su: 4 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/MARBIFLOX 100 mg/ml (KRKA)marbofloxacine: 100 mg/mlsolution injectable sc, iv (Bo), im (Bo, Su)Posologie:Bo: inf resp: 1 x 8 mg/kg (im)Bo: mammites: 2 mg/kg pj (3 j) (im, sc, 1e injpeut également par voie iv)Su: 2 mg/kg pj (3 j) (im)Viande et abats: Bo: 3 j (1 x 8 mg/kg), 6 j(2 mg/kg, 3 j), Su: 4 j, Lait: Bo: 72 h (1 x 8 mg/kg),36 h (2 mg/kg, 3 j)f<strong>la</strong>con 100 mlR/MARBOCYL 2% (Vétoquinol)marbofloxacine: 20 mg/mlsolution injectable sc, iv (Bo), im (Bo, Su)Posologie:veau, Su: 2 mg/kg pj (3 - 5 j)Viande: veau: 6 j, Su: 4 jf<strong>la</strong>con 100 mlR/MARBOCYL 10 % (Vétoquinol)marbofloxacine: 100 mg/mlsolution injectable iv, sc, (Bo), im (Bo, Su)Posologie:Bo: 2 mg/kg pj (3 - 5 j)Su (truie): 2 mg/kg pj (3 j)Viande: Bo: 6 j , Su: 4 j, Lait: 36 hf<strong>la</strong>con 50 ml, 100 mlR/MARBOCYL bolus (Vétoquinol)marbofloxacine: 50 mgcomprimé poPosologie:veau: 1 mg/kg pj (3 j)Viande: 6 jcompr 24, 96R/MARBOCYL P 5 mg (Vétoquinol)marbofloxacine: 5 mgcomprimé appétent poPosologie:Ca, Fe: 2 mg/kg pj (<strong>du</strong>rée dépend del’indication)compr 10, 100R/MARBOCYL P 20 mg (Vétoquinol)marbofloxacine: 20 mgcomprimé appétent poPosologie:Ca: 2 mg/kg pj (<strong>du</strong>rée dépend del’indication)compr 10, 100R/MARBOCYL P 80 mg (Vétoquinol)marbofloxacine: 80 mgcomprimé appétent poPosologie:Ca: 2 mg/kg pj (<strong>du</strong>rée dépend del’indication)compr 12, 72R/MARBOX 100 mg/ml sol inj bovins et porcs(Ceva Santé Animale)marbofloxacine: 100 mg/mlsolution injectable im (Bo, Su), sc (Bo)Posologie:Bo:- infect resp: 1 x 8 mg/kg (im)- mammite aiguë: 1 x pj 2 mg/kg sc (3 j),1e inj peut aussi être administrée par voie ivtruie: 1 x pj 2 mg/kg im (3 j)Viande et abats:Bo (im) 3 j, Bo (sc): 6 j, Su (im): 4 jLait: Bo (im): 72 h, Bo (sc): 36 hf<strong>la</strong>con 100 mlR/MARFLOQUIN 20 mg/ml (KRKA)marbofloxacine: 20 mg/mlsolution injectable im (Bo, Su), sc (Bo)Posologie:veau: 1 x 2 mg/kg pj (3 - 5 j), 1e injégalement possible par voie ivSu: 1 x 2 mg/kg pj (3 - 5 j)Viande et abats: veau: 6 j, Su: 4 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/
38 1 MEDICAMENTS ANTIBACTÉRIENSMARFLOQUIN 100 mg/ml (KRKA)marbofloxacine: 100 mg/mlsolution injectable im (Bo, Su), sc (Bo)Posologie:Bo:- infection resp: 1 x 8 mg/kg im- mammite aiguë: 2 mg/kg pj im ou sc (3 j),<strong>la</strong> 1e inj peut aussi se faire en ivSu (truie): 2 mg/kg pj im (3 j)Viande et abats: Bo (im, 1 x 8 mg/kg): 3 j,Bo (im ou sc, 2 mg/kg pj): 6 j, Su: 4 jLait: Bo (im, 1 x 8 mg/kg): 72 h, Bo (im ou sc,2 mg/kg pj): 36 hf<strong>la</strong>con 100 mlR/UBIFLOX 20 mg/ml (KRKA)marbofloxacine: 20 mg/mlsolution injectable im (Bo, Su), sc (Bo)Posologie:veau (PV < 100 kg)Su: 2 mg/kg pj, 3-5 jViande Bo: 6 j, Su: 4 jf<strong>la</strong>con 100 mlR/UBIFLOX 100 mg/ml (KRKA)marbofloxacine: 100 mg/mlsolution injectable sc, iv (Bo), im (Bo, Su)Posologie:Bo: 1 x 8 mg/kg (im)Bo: 2 mg/kg pj (3-5 j) (im, sc, iv)Su: 2 mg/kg pj (3 j)Viande: Bo (1x8 mg/kg): 3 j, Bo (2 mg/kg): 6 j,Su: 4 j,Lait: Bo (1x8 mg/kg): 72 h, Bo (2 mg/kg): 36 hf<strong>la</strong>con 100 mlR/1.1.8.7 PradofloxacineLMR pradofloxacine: VERAFLOX 25 mg/ml susp po chats (Bayer)pradofloxacine: 25 mg/mlsuspension poPosologie:Fe: 5 mg/kg 1 x pj (5 - 7 j selon l’indication)f<strong>la</strong>con 15 mlR/VERAFLOX 15 mg (Bayer)pradofloxacine: 15 mgcomprimé poPosologie:Ca: 1 x 3 mg/kg pj (7 - 35 j, selonl’indication)Fe: 1 x 3 mg/kg pj (5 j)compr 7 ou 70R/VERAFLOX 60 mg (Bayer)pradofloxacine: 60 mgcomprimé poPosologie:Ca: 1 x 3 mg/kg pj (7 - 35 j, selonl’indication)compr 7 ou 70R/VERAFLOX 120 mg (Bayer)pradofloxacine: 120 mgcomprimé poPosologie:Ca: 1 x 3 mg/kg pj (7 - 35 j, selonl’indication)compr 7 ou 70R/1.1.9 Associations à base d’antibiotiquesL’association de deux ou plusieurs antibiotiques devrait toujours pouvoir être justifiéepar des synergies permettant, in fine, d’éviter l’émergence de résistancesupplémentaire. Le simple é<strong>la</strong>rgissement <strong>du</strong> spectre, parfois nécessaire en casd’infection multiple, ne peut justifier le recours systématique à ces associations.L’identification des germes en cause devrait permettre un choix plus spécifiquedes antibiotiques. Le fait de l’association en proportion fixe pose souvent le problèmede <strong>la</strong> disparité pharmacocinétique des principes actifs. L’association de<strong>la</strong> lincomycine et de <strong>la</strong> spectinomycine est courante et exerce des effets additifsou synergiques, permettant d’améliorer leur activité contre les mycop<strong>la</strong>smes.La synergie, par désorganisation de <strong>la</strong> paroi bactérienne, entre les pénicillineset les aminosides contre les bactéries GRAM+ est connue depuis longtemps.Les polymyxines, en désorganisant les membranes, agissent en synergie avecles sulfamidés et le triméthoprime contre certaines entérobactéries résistanteset les pseudomonades. Le métronidazole trouve sa p<strong>la</strong>ce dans certaines associations<strong>du</strong> fait de son activité importante vis-à-vis des germes anaérobiques etcertains protozoaires mais son effet tératogène potentiel doit être pris en compte.Une association comprenant un AINS et un antibiotique est également disponible.
1 MEDICAMENTS ANTIBACTÉRIENS391.1.9.1 Pénicilline + aminosideLMR benzylpénicilline procaïne +néomycine: NEOPEN (MSD A.H.)benzylpénicilline procaïne: 200.000 UI/ml(200 mg/ml)néomycine (sulfate): 100 mg/mlsuspension injectable im, scPosologie:a<strong>du</strong>ltes et jeunes:Bo, Su, Ov: 10.000 UI de BPP/kg + 5 mgde N/kgporcelet, agneau, Ca, Fe:20.000 UI de BPP/kg + 10 mg de N/kgViande et abats: Bo: 89 j, Su: 45 j, Ov: 56 j,Lait: Bo: 3,5 jNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/1.1.9.2 Lincomycine +spectinomycineLMR lincomycine + spectinomycine: EMDACTILIN 150 (Emdoka)lincomycine (chlorhydrate monohydrate):50 mg/mlspectinomycine (chlorhydrate pentahydrate):100 mg/mlsolution injectable imPosologie:veau: 2 x 15 mg/kg le 1er j, ensuite 1 x pj(1 - 4 j)Su: 15 mg/kg pj (3-7 j)Viande: Bo: 24 jSu: 16 jf<strong>la</strong>con 100 ml, 250 mlR/LINCOMYCINE-SPECTINOMYCINE-VMD inj (VMD)lincomycine (chlorhydrate): 50 mg/mlspectinomycine (chlorhydrate): 100 mg/mlsolution injectable imPosologie:Su: 5 mg de L/kg + 10 mg de S/kg pj (3-7 j)Viande et abats: 14 jf<strong>la</strong>con 100, 250 mlR/LINCOMYCINE-SPECTINOMYCINE-VMD pulvis(VMD)lincomycine (chlorhydrate): 222 mg/gspectinomycine (chlorhydrate): 444 mg/gpoudre po dans l’eau de boissonPosologie:Su: 2,33 mg de L/kg + 4,66 mg de S/kg pj(150 poudre/1500 l d’eau) (7 j)Viande: 2 jpoudre 150 g, 1.5 kgR/LINCO-SPECTIN (Pfizer A.H.)lincomycine (chlorhydrate): 50 mg/mlspectinomycine (sulfate): 100 mg/mlsolution injectable imPosologie:Su, Ov: 15 mg/kg pj (Su: 3-7 j, Ov: 3 j)Viande et abats Su: 12 j, Ov: 15 jNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/LINCO-SPECTIN 100 (Pfizer A.H.)lincomycine (chlorhydrate): 33,3 g/150gspectinomycine (sulfate): 66,7 g/150gpoudre po dans l’eau de boissonPosologie:Su: 10 mg actif/kg pj (4 - 7 j) (7 j en casd’iléite)poule:MRC: 150 g de poudre/150 l d’eau (3 - 7 j)coryza: 150 g de poudre/200 l d’eau (3 - 7 j)Viande: Su: 0 j , Av: 5 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainepoudre 150 g, 1.5 kgR/LINCO-SPECTIN 22 + 22 premix (Pfizer A.H.)lincomycine (chlorhydrate): 22 g/kgspectinomycine (sulfate): 22 g/kgprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 2 mg/kg PV de L + 2 mg/kg PV de S(21 j)Viande: 2 jprém méd 25 kgR/premixLINCO-SPECTIN 44 (Pfizer A.H.)lincomycine (chlorhydrate): 22 g/kgspectinomycine (sulfate): 22 g/kgpoudre poPosologie:Su: 3 - 6 mg/kg PV pj (21 j) ou 0,2 kg depoudre/100 kg d’alimentsViande: 0 jpoudre 1 kgR/SPECTOLIPHEN 100 (Ke<strong>la</strong> Laboratoria)lincomycine (chlorhydrate): 222 mg/gspectinomycine (sulfate): 444 mg/gpoudre po dans l’eau de boissonPosologie:Su: 150 g de poudre/1600 l d’eau pj (1 sem)Av préventif:- âge 3 à 5 j: 150 g de poudre/200 l d’eau pj- âge 4 sem ou en cas de stress: 150 gde poudre/200 l d’eau pendant 12 h (PVtotal de 2000 kg) (1 à 3 j)Av curatif: 150 g de poudre/160 l d’eau pj(5 à 10 j)Viande: Su: 8 j, Av: 3 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumainepoudre 150 g, 1.5 kgR/
40 1 MEDICAMENTS ANTIMYCOTIQUES1.1.9.3 Aminopénicilline +polymyxineLMR amoxicilline + colistine: POTENCIL (Virbac)colistine (sulfate): 250.000 UI/m<strong>la</strong>moxicilline (trihydrate): 100 mg/mlsuspension injectable imPosologie:veau: 25.000 UI de C/kg + 10 mg d’A/kgpj (3 j)Viande: 57 jf<strong>la</strong>con 100 mlR/1.1.9.4 Métronidazole +spiramycineLMR métronidazole + spiramycine: STOMORGYL 10 kg (Merial)métronidazole: 125 mgspiramycine: 750.000 UIcomprimé poPosologie:Ca: 12,5 mg de M/kg + 75000 UI de S/kgpj (6-10 j)cas graves ou tenaces:Ca: 16,7 mg de M/kg + 100000 UI de S/kgpj (3 - 5 j)compr 2 x 10R/STOMORGYL P.A. (Merial)métronidazole: 16,67 mgspiramycine: 100.000 UIcomprimé poPosologie:Ca, Fe: 8,33 - 16,67 mg de M/kg +50 000 - 100 000 UI de S/kg pj (6 - 10 j)compr 3 x 10R/1.1.9.5 Florfénicol + flunixineLMR florfénicol + flunixine: RESFLOR 300 bovins (MSD A.H.)florfénicol: 300 mg/mlflunixine (méglumine): 16,5 mg/mlsolution injectable scPosologie:Bo: 1 x 40 mg de flor/kg + 2,2 mg de flun/kgViande: 46 jNe pas utiliser chez les Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, ni chez lesBo en <strong>la</strong>ctation ou en période de tarissement nichez les futurs Bo pro<strong>du</strong>cteurs de <strong>la</strong>it destinéà <strong>la</strong> consommation dans les 2 m précédant <strong>la</strong>mise-basf<strong>la</strong>con 100 ml, 250 mlR/1.2 Médicaments antimycotiques1.2.1 ItraconazoleIndicationsL’itraconazole est un triazole synthétique à <strong>la</strong>rge spectre, actif contre les mycoses,en particulier celles provoquées par les dermatophytes.PharmacodynamieLes triazoles interfèrent, comme les imidazolés, avec <strong>la</strong> synthèse de l’ergostéroldépendante <strong>du</strong> cytochrome P450, et altèrent ainsi <strong>la</strong> membrane fongique. Leuraction est fongistatique.PharmacocinétiqueL’itraconazole est bien résorbé oralement et se lie facilement aux protéines p<strong>la</strong>smatiques.Des concentrations cutanées importantes et soutenues sont enregistréesen cours de traitement. L’élimination se fait principalement par les fèces.Effets indésirablesPar rapport aux autres molécules de ce groupe pharmacothérapeutique, l’itraconazoleinteragit peu avec le cytochrome P450, ce qui explique <strong>la</strong> bonne tolérancechez les espèces cibles. Les effets indésirables les plus fréquents sont les suivants: vomissements, diarrhée, anorexie, ptyalisme, dépression et apathie. Ceseffets sont généralement bénins et de nature passagère. Les chats dont l’état desanté général est mauvais ou qui souffrent de ma<strong>la</strong>dies concomitantes sont plussensibles aux effets indésirables et doivent être suivis de près <strong>du</strong>rant un traitementavec l’itraconazole.InteractionsLes concentrations p<strong>la</strong>smatiques de certains médicaments peuvent être modifiéesen raison de l’interaction possible entre l’itraconazole et le cytochrome P450.Précautions particulièresLes chats dont l’état de santé général est mauvais ou qui souffrent de ma<strong>la</strong>dies
1 MEDICAMENTS ANTIMYCOTIQUES41concomitantes sont plus sensibles aux effets indésirables et doivent être suivisde près <strong>du</strong>rant un traitement avec l’itraconazole. Les chats atteints d’insuffisancecardiaque doivent également être surveillés.Repro<strong>du</strong>ction et <strong>la</strong>ctationIl est déconseillé d’utiliser ce médicament chez les animaux en gestation ou en<strong>la</strong>ctation.LMR itraconazole : ITRAFUNGOL (Eli Lilly)itraconazole: 10 mg/mlsolution poPosologie:Fe: 5 mg/kg pj (7 j)3 x en alternant avec 7 j d’intervalle sanstraitementf<strong>la</strong>con et seringue 52 mlR/1.2.2 KétoconazoleIndications – spectre d’activité - résistanceLe kétoconazole, un dérivé de l’imidazole-dioxo<strong>la</strong>ne, exerce une activité contre lesdermatophytes, les levures et d’autres champignons pathogènes. La préparationest indiquée dans le traitement de dermatomycoses provoquées par Microsporumet Trichophyton spp., dans le traitement de mycoses superficielles ou profondesprovoquées par des levures telles que Candida, Cryptococcus et Ma<strong>la</strong>ssezia, etdans le traitement de mycoses systémiques telles que l’histop<strong>la</strong>smose et <strong>la</strong> coccidioïdomycose.Une résistance contre Candida albicans a été décrite.PharmacodynamieLe kétoconazole bloque <strong>la</strong> synthèse de l’ergostérol en inhibant le cytochromeP450. Ce déficit en ergostérol affecte <strong>la</strong> paroi cellu<strong>la</strong>ire des levures et des champignonset en augmente <strong>la</strong> perméabilité. L’action est fongistatique à doses normaleset fongicide à doses élevées. L’action inhibitrice <strong>du</strong> kétoconazole sur lesenzymes hépatiques P450 in<strong>du</strong>it également l’inhibition de <strong>la</strong> synthèse des stéroïdes,telle que <strong>la</strong> synthèse de cortisol, de testostérone et d’estradiol. Les indicationsliées à cette action ne figurent pas parmi les indications <strong>du</strong> médicamentmentionné ci-dessous.PharmacocinétiqueLe kétoconazole est bien résorbé lorsqu’il est administré avec l’alimentation.L’absorption varie cependant beaucoup d’un indivi<strong>du</strong> à l’autre. Il a une bonnedistribution tissu<strong>la</strong>ire et un temps de demi-vie assez long. Il est métabolisé endifférents métabolites inactifs. L’excrétion se fait principalement par <strong>la</strong> bile et letractus gastro-intestinal, un petit pourcentage est excrété par l’urine. Le kétoconazolese lie majoritairement à <strong>la</strong> fraction albumine des protéines p<strong>la</strong>smatiques.Contre-indicationsLésions hépatiques.Effets indésirablesLe traitement doit être adapté si l’un des effets indésirables suivants est observé:anorexie, vomissements, diarrhée, toxicité hépatique.InteractionsNe pas administrer simultanément (au moins 2 heures d’intervalle) avec des antiacides,des antagonistes H2, des inhibiteurs de <strong>la</strong> pompe à protons et/ou desantihistaminiques, qui diminuent l’absorption <strong>du</strong> kétoconazole. Le kétoconazolepeut inhiber le métabolisme des médicaments qui sont métabolisés par certainesenzymes hépatiques CYP450, principalement de <strong>la</strong> famille CYP3A. Ceci peut résulteren un renforcement ou une prolongation de leur action ainsi que de leurs effetsindésirables. L’action inhibitrice <strong>du</strong> kétoconazole sur les enzymes P450 in<strong>du</strong>itégalement l’inhibition de <strong>la</strong> synthèse des stéroïdes. Lorsque le kétoconazole estadministré en même temps que <strong>la</strong> cyclosporine ou des <strong>la</strong>ctones macrocycliques,<strong>la</strong> posologie de ces derniers doit être ré<strong>du</strong>ite. Le kétoconazole inhiberait les glycoprotéinesP, ce qui peut augmenter <strong>la</strong> toxicité des <strong>la</strong>ctones macrocycliques tellesque l’ivermectine.
42 1 MEDICAMENTS ANTIPARASITAIRESPrécautions particulièresLe kétoconazole est administré de préférence pendant le repas. Son utilisation estdéconseillée chez les animaux avant l’âge <strong>du</strong> sevrage.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas administrer à des animaux en gestation. Le kétoconazole est excrété dansle <strong>la</strong>it.LMR kétoconazole : KETOFUNGOL 200 mg (Eli Lilly)kétoconazole: 200 mgcomprimé poPosologie:Ca (sevré):dermatophytoses et mycoses provoquéespar des levures:10 mg/kg pj (min 20 j)mycoses systémiques: 10 - 30 mg/kg pj(éventuellement en 2 doses pj) (min 3 m)compr 6 x 10R/1.3 Médicaments antiparasitairesCe chapitre rassemble toutes les préparations antiparasitaires exerçant uneaction systémique sur les endo- et les ectoparasites, en distinguant les voiesd’administration. Celles agissant sous forme topique sur les ectoparasites sonttraitées séparément dans le chapitre des médicaments dermatologiques à usageexterne (Voir aussi 12.13.).Les médicaments repris dans les rubriques qui suivent sont présentés par famillepharmacologique et non en fonction de leur spectre. Les principaux parasites rencontrésen médecine vétérinaire sont repris dans le Folia Veterinaria. Ces donnéespeuvent également être consultées sur le site: www.cbip-vet.be. Contrairement auxsubstances antimicrobiennes, les médicaments antiparasitaires sont utilisés à <strong>la</strong>fois à titre prophy<strong>la</strong>ctique et curatif pour contrôler l’impact négatif des parasitosessur les pro<strong>du</strong>ctions animales et prévenir les infestations chez les animaux de compagnie.Cette approche, ren<strong>du</strong>e nécessaire par les conditions d’élevage et de détentiondes animaux ainsi que par les contraintes économiques, est possible <strong>du</strong> faitd’une plus faible aptitude de certains parasites à développer rapidement un certainniveau de résistance aux antiparasitaires en comparaison avec le développementde <strong>la</strong> résistance des germes aux antimicrobiens. La résistance aux antiparasitairespeut cependant poser des problèmes importants également abordés sur le sitewww.cbip-vet.be (voir aussi Folia Veterinaria 2006 n° 3, 2009 n o 1 et 2009 n o 3).1.3.1 Médicaments injectables et à usage oral contenant des substancesantiparasitaires actives contre les endoparasitesNombreuses sont les préparations contenant des principes actifs insuffisammentrésorbés par voie digestive mais exerçant une action efficace contre les endoparasites<strong>du</strong> tube digestif. Ceci ne signifie pas que l’absorption soit suffisamment faiblepour éviter certains effets indésirables généraux et <strong>la</strong> présence de rési<strong>du</strong>s. Le lecteurconsultera les RCP (notices scientifiques) de chaque médicament pour prendreconnaissance de leur spectre exact qui dépend de <strong>la</strong> nature <strong>du</strong> principe actif, de<strong>la</strong> composition de <strong>la</strong> préparation, de <strong>la</strong> posologie et bien enten<strong>du</strong> de l’hôte ciblé.1.3.1.1 Benzimidazoles etprobenzimidazolesIndicationsLes benzimidazoles sont reconnuscomme étant essentiellement nématocides(excepté le tric<strong>la</strong>bendazole, voirchapitre 1.3.1.2). Toutefois, une actioncontre les trématodes et les cestodesest attribuée à certains composés, enfonction des doses utilisées. Le fenbendazoleest également actif contreGiardia. Il est par conséquent conseilléde se référer aux notices de chaquemédicament pour connaître le spectred’action et les espèces de destination.
1 MEDICAMENTS ANTIPARASITAIRES43PharmacodynamieIls agissent en perturbant différentsprocessus biologiques <strong>du</strong> parasitedont <strong>la</strong> polymérisation des microtubuleset le métabolisme énergétique.Certains vers, comme Haemonchuscontortus et les petits strongles(Cyathostominae) chez les chevauxont développé des mécanismes de résistancevis-à-vis des benzimidazoles.PharmacocinétiqueL’absorption intestinale de ces composésdépend de leur solubilité dansl’eau, souvent faible. Leurs concentrationsp<strong>la</strong>smatiques ne reflètent doncpas toujours les doses administréesper os. Les substances à meilleurerésorption (p. ex. oxfendazole et fenbendazole)peuvent être utilisées pourle traitement des verminoses respiratoires.Leur métabolisation et leur éliminationvarient aussi d’un composéà l’autre ; l’élimination biliaire, fécaleet urinaire se combinant différemmentselon les composés. Il en résulte destemps d’attente variables selon les préparationset les principes actifs. Uneadministration unique de benzimidazoleschez les carnivores ne s’avérantpas (suffisamment) effective contretous les nématodes, même à dosesplus élevées, ils sont administrés <strong>du</strong>ranttrois à cinq jours consécutifs chezces espèces. Les probenzimidazoles(fébantel) sont métabolisés en benzimidazoles.Ils ont une marge de sécuritétrès élevée.Contre-indicationsLa gestation peut constituer unecontre-indication, voir plus loin.Effets indésirablesL’utilisation raisonnée des benzimidazolesprésente normalement peu derisques. Cependant, certains effets indésirables,comme de l’anorexie, des nausées,des vomissements, de <strong>la</strong> diarrhée,peuvent se manifester occasionnellement,même à doses thérapeutiques.InteractionsL’utilisation simultanée de fenbendazoleou d’oxfendazole avec des fasciolicidesde type bromsa<strong>la</strong>n (dibromsa<strong>la</strong>n,tribromsa<strong>la</strong>n; ces molécules ne sont enréalité pas enregistrées comme médicamentsen Belgique) provoque de <strong>la</strong>mortalité chez les moutons et l’avortementchez les bovins.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’emploi des benzimidazoles et desprobenzimidazoles pendant <strong>la</strong> gestationdoit se faire avec précaution vules effets tératogènes potentiels decertains d’entre eux se manifestantsurtout pendant le premier tiers de <strong>la</strong>gestation chez certaines espèces. Ilest conseillé de se référer aux notices.AlbendazoleLMR albendazole: VALBAZEN 1,9 % (Eli Lilly)albendazole: 19 g/lsuspension poPosologie:Ov: nématodes, cestodes: 3,8 mg/kgFascio<strong>la</strong>: 5 mg/kg (7,5 mg/kg en cas derisque d’infect élevé)ne pas admin pendant le 1er m de <strong>la</strong>gestationViande: 5 j, Lait: 4 jf<strong>la</strong>con 1 lR/VALBAZEN 10 % (Eli Lilly)albendazole: 100 g/lsuspension poPosologie:Bo: nématodes, cestodes: 7,5 mg/kgnématodes, cestodes, Fascio<strong>la</strong>: 15 mg/kgne pas admin pendant les 3 premiers m de<strong>la</strong> gestationViande: 5 j, Lait: 84 hf<strong>la</strong>con 1 lR/VALBAZEN boli (Eli Lilly)albendazole: 200 mgcomprimé (bolus) poPosologie:Ov: nématodes, cestodes: 3,8 mg/kgFascio<strong>la</strong>: 5 mg/kg (7,5 mg/kg en cas derisque d’infect élevé)ne pas admin pendant le 1er m de <strong>la</strong>gestationViande: 14 j, Lait: 4 jcompr 50R/FébantelLMR fébantel : AVICAS (Oropharma)fébantel: 15 mgcomprimé poPosologie:pigeon: 30 mg/kg ou 1 compr/pigeon(répéter après 8 j)Ne pas administrer aux pigeons destinés à<strong>la</strong> consommation humainecompr 40RINTAL 10 % gran (Bayer)fébantel: 10 g/100 ggranules po avec l’alimentationPosologie:Eq: 6 mg/kgBo: 7,5 mg/kgSu, Ov: 5 mg/kg(animaux sauvages: voir notice)Viande: 14 j, Lait: 4 jgran 250 gR/
44 1 MEDICAMENTS ANTIPARASITAIRESRINTAL pellets (Bayer)fébantel: 1,9 g/100 gpellets poPosologie:Eq: 6 mg/kgBo: 7,5 mg/kgSu, Ov: 5 mg/kgViande: Bo: 9 j, Su: 17 j, Ov: 14 j, Lait: 7 jNe pas administrer aux Eq destinés à <strong>la</strong>consommation humainepellets 2 kg, 10 kgR/FenbendazoleLMR fenbendazole: PANACUR 4% poudre (MSD A.H.)fenbendazole: 40 mg/gpoudre po avec l’alimentationPosologie:Su: 5 mg/kg (administré en une fois, ouréparti sur une période de 5-15 j)Viande: 5 jpoudre 2 kgR/PANACUR 4% premix (MSD A.H.)fenbendazole: 40 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 5 mg/kg (administré en une fois, ouréparti sur une période de 5-15 j)Viande: 5 jprém méd 25 kgR/premixPANACUR AQUASOL (MSD A.H.)fenbendazole: 200 mg/mlsuspension po dans l’eau de boissonPosologie:Su: 2,5 mg/kg pj (2 j)Viande + abats: 4 jf<strong>la</strong>con 1 lR/PANACUR boli 250 mg (MSD A.H.)fenbendazole: 250 mg/boluscomprimé (bolus) poPosologie:Ov: 5 mg/kg (Moniezia spp: 10 mg/kg)Viande: 14 j, Lait: 4 jcompr 5 x 10R/PANACUR compr 250 mg (MSD A.H.)fenbendazole: 250 mgcomprimé poPosologie:- infect. cliniques Ca, Fe, chiot, chaton:50 mg/kg pj (3 x)- traitement de routine Ca:100 mg/kg (1 x)compr 10PANACUR compr 500 mg (MSD A.H.)fenbendazole: 500 mgcomprimé poPosologie:Ca: 50 mg/kg pj (3 j)compr 10PANACUR EQUINE GUARD (MSD A.H.)fenbendazole: 100 mg/mlsuspension poPosologie:Eq: 7,5 mg/kg pj (5 j)Viande: 5 jf<strong>la</strong>con 225 mlR/PANACUR pâte (MSD A.H.)fenbendazole: 187,5 mg/gpâte poPosologie:Eq, âne: 7,5 mg/kgpou<strong>la</strong>in (âge 2 - 3 sem) (Strongyloideswesteri): 50 mg/kgViande: 14 japplic 1 x 24 g, 10 x 24 gR/PANACUR PUPPY (MSD A.H.)fenbendazole: 100 mg/mlsuspension poPosologie:Ca, chiot: 50 mg/kg pj (3 j), (Oslerus osleri:2 x 8 j avec 8 j d’intervalle)f<strong>la</strong>con 100 mlPANACUR SR bolus (MSD A.H.)fenbendazole: 12 gbolus poPosologie:veau ruminant (100 - 300 kg PV, âge > 3-4 m):1 bolus/animalViande: 200 j, Ne pas administrer aux vachesdont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaine ou aux génisses, 200 j avant le vê<strong>la</strong>gebolus 10R/PANACUR susp 2,5 % (MSD A.H.)fenbendazole: 25 mg/mlsuspension poPosologie:Ov: 5 mg/kg (Moniezia spp: 10 mg/kg)Viande: 14 j, Ne pas administrer aux Ov dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/PANACUR susp 10 % (MSD A.H.)fenbendazole: 100 mg/mlsuspension poPosologie:Eq, Bo: 7,5 mg/kgpou<strong>la</strong>in (Strongyloides Westeri): 50 mg/kgViande: 14 j, Lait: 4 jf<strong>la</strong>con 1 lR/ZEROFEN vet 4 % (Chanelle Pharmaceuticals)fenbendazole: 40 mg/gpoudre po avec l’alimentationPosologie:Su (après le sevrage): 1 x 5 mg/kgViande: 21 jpoudre 500 g, 1 kg, 2.5 kgR/
1 MEDICAMENTS ANTIPARASITAIRES45FlubendazoleLMR flubendazole : FLUBENOL 220 mg (Janssen Pharmaceutica)flubendazole: 220 mgcomprimé à croquer poPosologie:Ca: 22 mg/kg pj (2 - 3 j)compr 2 x 3, 60 x 3FLUBENOL 5% prém méd (Eli Lilly)flubendazole: 50 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:porcelet, porc de chair:30 ppm (5 j, contamination sévère par T.suis10 j)contamination A. suum: 30 ppm (5 j) ou 21,4ppm (7 j) ou 15 ppm (10 j)porc reprod: 30 ppm (10 j)traitement indivi<strong>du</strong>el: 1 x 5 mg/kg PVpoule, oie: 30 ppm (7 j)dinde: 20 ppm (7 j), faisan: 60 ppm (7 j)Viande: Su: 5 j, poule, dinde, oie: 1 j, faisan: 5 jOeuf: 0 jprém méd 12 kgR/premixFLUBENOL 5% poudre (Eli Lilly)flubendazole: 50 mg/gpoudre po avec l’alimentationPosologie:porcelet, porc de chair: 1 mg/kg pj (5 j, encas d’infection sévère à T. suis: 10 j)porc reprod: 0,5 mg/kg pj (10 j)dindon: 0,95 mg/kg pj (7 j)poule, oie: 1,43 mg/kg pj (7 j)faisan: 2,86 mg/kg pj (7 j)Viande: Su: 5 j, poule, dinde, oie: 1 j, faisan: 5 jOeuf: 0 jpoudre 600 g, 2 kgR/FLUBENOL KH (Eli Lilly)flubendazole: 44 mg/mlpâte poPosologie:Ca, Fe: 22 mg/kg pj (2 - 3 j)applic 7,8 mlSOLUBENOL 100 mg/g (Eli Lilly)flubendazole: 100 mg/gémulsion po dans l’eau de boissonPosologie:Su:porc de chair, porcelet, truie gestanteAscaris suum, stades a<strong>du</strong>lte + <strong>la</strong>rvaire:1 mg/kg pj (5 j)porc de chair, porcelet:Ascaris suum, stade a<strong>du</strong>lte: 2,5 mg/kg pj(2 j)poule: 1,43 mg/kg pj (7 j)Viande: Su, Av: 4 j, Oeuf: 0 jsachet 5 x 500 gR/MébendazoleLMR mébendazole : TELMIN KH (Eli Lilly)mébendazole: 100 mgcomprimé poPosologie:- ascarides:chiot, chaton: 2 x pj 50 mg/animal (2 j)animal a<strong>du</strong>lte: 2 x pj 100 mg/animal (2 j)- plusieurs espèces de vers:Ca, Fe (< 2 kg PV): 2 x pj 50 mg/animal (5 j)Ca, Fe (> 2 kg PV): 2 x pj 100 mg/animal (5 j)compr 10TELMIN pâte (Eli Lilly)mébendazole: 200 mg/gpâte poPosologie:Eq, poney: 8,8 mg/kgViande: 28 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 20 gR/OxfendazoleLMR oxfendazole: DOLTHENE (Merial)oxfendazole: 22,65 mg/mlsuspension poPosologie:Ca: 11,3 mg/kg pj (3 j)f<strong>la</strong>con 20 ml, 50 ml, 100 mlFENDOV 750 (Pfizer A.H.)oxfendazole: 5 x 750 mg/bolusbolus poPosologie:Bo ruminant (100 - 250 kg PV, âge > 4 m):1 bolus/animalViande: 7 mNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineboli 3 x 4R/FENDOV 1250 (Pfizer A.H.)oxfendazole: 5 x 1.250 mg/bolusbolus poPosologie:Bo ruminant (250 - 500 kg PV):1 bolus/animalViande: 7 mNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineboli 3 x 4R/1.3.1.2 Tric<strong>la</strong>bendazoleIndicationsLe tric<strong>la</strong>bendazole appartient augroupe des benzimidazoles mais il sedistingue par son activité plus puissantecontre les stades immatures etmatures de Fascio<strong>la</strong> hepatica et deFascio<strong>la</strong> gigantica.
46 1 MEDICAMENTS ANTIPARASITAIRESPharmacodynamieLe mécanisme d’action <strong>du</strong> tric<strong>la</strong>bendazolediffère de celui des autres benzimidazoles.Le tric<strong>la</strong>bendazole inhibe<strong>la</strong> synthèse protéique au niveau <strong>du</strong>tégument <strong>du</strong> parasite.PharmacocinétiqueAprès administration orale, le tric<strong>la</strong>bendazolesubit un important effetde premier passage hépatique et estrapidement oxydé en sulfoxyde et ensulfone. Le sulfoxyde est supposé être<strong>la</strong> fraction active. Seule une quantitéminime de tric<strong>la</strong>bendazole atteint lep<strong>la</strong>sma. Contrairement aux autresbenzimidazoles, les métabolites <strong>du</strong>tric<strong>la</strong>bendazole se lient très bien avecl’albumine, ce qui entraîne une demivieet un temps d’attente longs. Lamajeure partie de <strong>la</strong> dose orale estexcrétée par les fèces après 6 à 10jours, sous une forme inchangée, nonabsorbée ou de métabolites.Contre-indicationsLe tric<strong>la</strong>bendazole ne peut pas êtreadministré aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine.Effets indésirablesOn n’observe pas d’effets indésirablesnotables en cas d’administration oralede doses normales.InteractionsAucune interaction connue.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’usage en période de gestation et de<strong>la</strong>ctation n’est pas déconseillé.LMR tric<strong>la</strong>bendazole : Médicaments à base de tric<strong>la</strong>bendazole: voir chapitre 1.3.1.10. et 1.3.2.2.1.3.1.3 ImidazothiazolésIndicationsL’examen des notices est conseillépour évaluer le spectre de chaquemédicament mais l’activité contre lesnématodes gastro-intestinaux et respiratoiresest bien connue.PharmacodynamieLe lévamisole, l’isomère L ou lévogyre<strong>du</strong> tétramisole qui est un mé<strong>la</strong>nge racémiquedes deux isomères (L/D tétramisole)possède un spectre d’actiontrès <strong>la</strong>rge et présente moins d’effetsindésirables que l’isomère D. Le lévamisoleexerce une action paralysanteréversible aboutissant à des contractionsmuscu<strong>la</strong>ires. L’action nicotiniqueet muscarinique a été identifiée. De <strong>la</strong>résistance a été observée. Ce derniersujet a fait l’objet d’une analyse dansle Folia Veterinaria 2006 n°3.PharmacocinétiqueLe lévamisole est rapidement résorbépar le tube digestif, métabolisé auniveau <strong>du</strong> foie et <strong>la</strong>rgement éliminé,par les urines et les fèces au coursdes 48 heures suivant l’administration.Les formes à libération contrôlée permettentde prolonger <strong>la</strong> <strong>du</strong>rée de l’efficacité.Son excellente absorption parvoie transcutanée et intramuscu<strong>la</strong>irejustifie les diverses formes galéniquesproposées.Contre-indicationsIl est important de souligner que <strong>la</strong>chèvre, le chat, le chien et le chevalsont sensibles aux effets indésirables<strong>du</strong> lévamisole. Le lévamisole n’est pasenregistré pour ces espèces cibles. Ilest préférable de ne pas traiter les animauxaffaiblis ou souffrant de pathologiesrénales ou hépatiques avec <strong>du</strong>lévamisole.Effets indésirablesLe lévamisole semble avoir peu d’effetsindésirables aux doses recommandées.Des nausées, des vomissements,de <strong>la</strong> salivation, de l’anorexie,des douleurs abdominales peuventêtre observés. Ces symptômes disparaissentspontanément. L’atropinepeut éventuellement tenir lieu d’antidote(Voir Folia Veterinaria 2005 n°3).InteractionsL’action toxique <strong>du</strong> lévamisole est renforcéepar les substances nicotinergiques(p.ex. le pyrantel, le morantel)et par les inhibiteurs de <strong>la</strong> cholineestérase(p.ex. les organophosphorés,<strong>la</strong> néostigmine). L’utilisation simultanéeavec le chloramphénicol a déjà aboutià de <strong>la</strong> mortalité. L’utilisation simultanéeavec le lévamisole inhibe l’actionanalgésique et anti-inf<strong>la</strong>mmatoire de<strong>la</strong> phénylbutazone et augmente sonhépatotoxicité. La pipérazine antagonisel’action <strong>du</strong> lévamisole. In vitro, lelévamisole est incompatible avec <strong>la</strong>néomycine, les sulfamides, les tétracyclineset <strong>la</strong> phénylbutazone.Précautions particulièresIl est préférable d’éviter l’administrationde lévamisole <strong>du</strong>rant les situationsde stress (vaccination, écornage,castration).Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation pendant <strong>la</strong> gestation ou <strong>la</strong><strong>la</strong>ctation est déconseillée.
1 MEDICAMENTS ANTIPARASITAIRES47LévamisoleLMR lévamisole : CODIVERM 100 (Ke<strong>la</strong> Laboratoria)lévamisole (chlorhydrate): 100 mg/mlsolution injectable sc (Bo), im (Su)Posologie:Bo, Su: 8 mg/kgViande: Bo: 28 j, Su: 18 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/LEVAMISOLE 7,5 % (Ke<strong>la</strong> Laboratoria)lévamisole chlorhydrate: 75 mg/mlsolution injectable scPosologie:Ov: 7,5 mg/kgViande: 14 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 500 mlR/LEVAMISOLE HYDROCHLORIDE 80 % Ke<strong>la</strong> (Ke<strong>la</strong>Laboratoria)lévamisole chlorhydrate: 800 mg/gpoudre po dans l’eau de boissonPosologie:Su: 8 mg/kg ou 10 mg poudre/kgViande: 10 jsachet 10 x 100 gR/LEVAVETO 75 % (VMD)levamisole (chlorhydrate): 750 mg/gpoudre pour solution poPosologie:Su: 1 x 10 mg/kgViande et abats: 12 jsac 1 kgR/QUADROSOL 10 % (Prodivet)lévamisole (chlorhydrate): 100 mg/mlsolution injectable imPosologie:jeunes et a<strong>du</strong>ltes:Bo, Su: 5 mg/kgViande: Bo: 32 j, Su: 34 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/1.3.1.4 Dérivés d’aminoacétonitrile(AAD)MonépantelIndicationIl s’agit d’un anthelminthique à <strong>la</strong>rgespectre, utilisé dans le traitement et<strong>la</strong> prévention des infections gastrointestinalesà nématodes (4e stade<strong>la</strong>rvaire et formes a<strong>du</strong>ltes) chez lesovins, incluant les agneaux âgés deplus de 2 semaines et pesant plus de10 kg. L’utilisation chez les brebis dontle <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaine n’est pas autorisée. Le médicamentest efficace contre les souchesrésistantes aux benzimidazoles, au lévamisole,au morantel, aux salicy<strong>la</strong>nilideset aux <strong>la</strong>ctones macrocycliques.PharmacodynamieLe monépantel est un dérivé d’aminoacétonitrile(AAD). Il s’agit de <strong>la</strong> premièremolécule d’une nouvelle c<strong>la</strong>ssed’anthelminthiques. Il agit sur <strong>la</strong> sousunitéHco-MPTL-1 <strong>du</strong> récepteur nicotiniqueà l’acétylcholine spécifique desnématodes.PharmacocinétiqueAprès administration orale, le monépantelest rapidement absorbé etoxydé en métabolite sulfone. Lesconcentrations p<strong>la</strong>smatiques maximalessont atteintes en un jour. Lademi-vie d’élimination est d’environcinq jours. L’excrétion s’effectue principalementpar les selles, mais aussipar les urines. La prise d’aliments ou lejeûne avant ou peu après le traitementn’a pas d’impact sur l’efficacité.Contre-indicationsL’innocuité <strong>du</strong> pro<strong>du</strong>it n’est pas établiechez les ovins pesant moins de 10 kgou âgés de moins de 2 semaines.Effets indésirablesAucun effet indésirable connu.InteractionsAucune interaction connue.Précautions particulières/Risquespour l’hommeAfin d’éviter le développement de résistance,il est conseillé de vérifier l’efficacité<strong>du</strong> traitement (aspect clinique,nombre d’oeufs dans les matièresfécales). Le mauvais fonctionnement<strong>du</strong> dispositif d’administration ou <strong>la</strong>sous-estimation <strong>du</strong> poids vif peutentraîner des sous-dosages qui augmententle risque de développementde résistance.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe médicament vétérinaire peut êtreutilisé chez les ovins de repro<strong>du</strong>ction,y compris les brebis gestanteset al<strong>la</strong>itantes, à condition que le <strong>la</strong>itne soit pas destiné à <strong>la</strong> consommationhumaine.
48 1 MEDICAMENTS ANTIPARASITAIRESLMR monépantel: ZOLVIX 25 mg/ml sol po ovins (Novartis)monépantel: 25 mg/mlsolution poPosologie:Ov (PV > 10 kg, âge > 2 sem): 2,5 mg/kgViande Ov: 7 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/1.3.1.5 TétrahydropyrimidinesIndicationsL’embonate de pyrantel est utilisécomme nématocide chez les chevaux,les chiens et les chats. L’oxantel estindiqué chez le chien dans le traitementdes infestations par des nématodes(dont Trichuris spp) et descestodes. L’oxantel est commercialisésous forme d’association (voir chapitre1.3.1.10 Associations).PharmacodynamieLe pyrantel est un antagoniste desrécepteurs à acétylcholine. L’activitésur les nématodes <strong>du</strong> tube digestif expliqueles contractions muscu<strong>la</strong>ires (effet“nicotine-like”) ainsi que l’inhibitionde <strong>la</strong> fumarate ré<strong>du</strong>ctase. L’oxantel(voir 1.3.1.10 Associations) étant trèsfaiblement résorbé, <strong>la</strong> concentrationen est élevée au niveau <strong>du</strong> colôn etson action vis-à-vis de Trichuris spps’en trouve améliorée.PharmacocinétiqueL’embonate de pyrantel est faiblementabsorbé par le tube digestif.Effets indésirablesCeux-ci sont très rares (vomissementschez les petits animaux).InteractionsLa toxicité augmente en cas d’usagesimultané avec des substances cholinergiques: lévamisole, morantel etorganophosphorés. Le pyrantel et <strong>la</strong>pipérazine ont un effet antagoniste.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa marge de sécurité de ces composésadministrés par voie orale est trèsimportante y compris chez les jeunessujets, les animaux débilités ainsique chez les femelles gestantes et en<strong>la</strong>ctation.PyrantelLMR pyrantel: CATMINTH (Pfizer A.H.)pyrantel (embonate): 40 mg/gpâte poPosologie:Fe: 20 mg/kgseringue 1 x 3 gDOGMINTH (Pfizer A.H.)pyrantel (embonate): 7,5 mg/gpâte poPosologie:Ca: 1 x 5 mg/kgtube 24 gHORSEMINTH (Pfizer A.H.)pyrantel (embonate): 152,3 mg/gpâte poPosologie:Eq: 6,6 mg/kgTemps d’attente: 0 jseringue 26 g1.3.1.6 QuinolinesIndicationsCette c<strong>la</strong>sse comprend le praziquantel.Son activité se limite essentiellementaux cestodes.PharmacodynamieLe praziquantel provoque un accroissementde l’activité muscu<strong>la</strong>ire et desdommages au niveau des téguments<strong>du</strong> ver, aboutissant à <strong>la</strong> destruction <strong>du</strong>parasite.PharmacocinétiqueLe praziquantel est rapidement absorbéaussi bien par voie orale que parentéraleet se distribue <strong>la</strong>rgement danstout l’organisme. Le praziquantel subitun effet de premier passage important.Chez les rats, il a été démontré que lepraziquantel traverse <strong>la</strong> barrière hémato-méningéeet, à un degré minime, <strong>la</strong>barrière p<strong>la</strong>centaire. Il est métabolisépar le foie avant d’être éliminé, principalementdans les urines, sous formede métabolites inactifs.Contre-indicationsCertaines publications déconseillentl’administration de ces pro<strong>du</strong>its auxjeunes animaux (chiots âgés de moinsde 4 semaines et chatons âgés demoins de 6 semaines).Effets indésirablesEn général bien toléré; de <strong>la</strong> douleurabdominale, des nausées, des vomissementset de <strong>la</strong> diarrhée chez leschiens et les chats ont cependant étésignalés dans <strong>la</strong> littérature médicale.Ces manifestations sont souvent transitoireset dépendent de <strong>la</strong> dose. Ellesapparaissent un peu plus fréquem-
1 MEDICAMENTS ANTIPARASITAIRES49ment lors d’administrations parentérales.D’autres effets indésirablesencore plus rares, peuvent aussi êtreobservés comme de <strong>la</strong> fièvre, <strong>du</strong> prurit,des douleurs articu<strong>la</strong>ires ou muscu<strong>la</strong>ires.L’injection sous-cutanée peutêtre douloureuse.InteractionsLa demi-vie <strong>du</strong> praziquantel peut êtreaugmentée lors de ma<strong>la</strong>dies hépatiqueset d’administration simultanéeavec des substances inhibant l’activité<strong>du</strong> cytochrome P450 comme <strong>la</strong> cimétidine.Les in<strong>du</strong>cteurs <strong>du</strong> cytochromeont l’effet inverse, le phénobarbital parexemple.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation pendant <strong>la</strong> gestation ou <strong>la</strong><strong>la</strong>ctation est sûre.PraziquantelLMR praziquantel : Médicaments à base de praziquantel:voir chapitre 1.3.1.10. Associations.1.3.1.7 Dérivés phénoliques etsalicy<strong>la</strong>nilidesIndicationsLes dérivés phénoliques et salicy<strong>la</strong>nilidessont surtout utilisés contre lestrématodes. Ces molécules agissentplus efficacement sur les douvesa<strong>du</strong>ltes que sur les formes immatures.Certaines de ces molécules peuventégalement être utilisées contre d’autresparasites (arthropodes, nématodes). Ilest conseillé de se référer aux noticesde chaque médicament pour connaîtreleur spectre d’action exact.PharmacodynamieLeur mode d’action principal est ledécoup<strong>la</strong>ge de <strong>la</strong> phosphory<strong>la</strong>tionoxydative.PharmacocinétiqueLe closantel est très peu métaboliséet excrété très lentement, principalementpar les fèces. Le nitroxinil estprésent en grandes concentrationsdans les voies biliaires, il se caractérisepar une grande liaison protéiqueet une métabolisation très lente, et estprincipalement excrété par les fèces.La demi-vie de l’oxyclozanide estbeaucoup plus courte en comparaisonavec les deux substances précitées.L’oxyclozanide est excrété principalementpar les fèces.Contre-indicationsL’administration aux animaux dontle <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaine est contre-indiquée (àl’exception des bovins dans le cas del’oxyclozanide).Effets indésirablesLeur toxicité peut être considéréecomme peu élevée aux doses recommandéesmais peut néanmoinsapparaître lors de surdosage et, pourcertains dérivés, lors d’utilisation chezdes animaux gestants, stressés, enmauvaise condition ou fortement infestés.Elle peut notamment se manifesterpar une diminution d’appétit,des selles molles, de l’hyperpnée, del’hyperthermie liée à leur effet inhibiteurdes phosphory<strong>la</strong>tions oxydatives,des convulsions et de <strong>la</strong> tachycardie.InteractionsAucune interaction connue.Précautions particulièresNoter que le temps d’attente après utilisationde ces substances est long àtrès long, sauf pour l’oxyclozanide quia un dé<strong>la</strong>i d’attente assez court pour <strong>la</strong>viande et pour le <strong>la</strong>it.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucun effet négatif n’a été constatépour l’instant lors de l’administrationde doses thérapeutiques en périodede gestation ou de <strong>la</strong>ctation.ClosantelLMR closantel : FLUKIVER 5% sol inj (Eli Lilly)closantel (sodique): 50 mg/mlsolution injectable scPosologie:Bo: selon l’espèce de ver:2,5 ou 5 mg/kgViande: 11 semNe pas donner aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 4 x 250 mlR/NitroxinilLMR nitroxinil : DOVENIX (Merial)nitroxinil: 250 mg/mlsolution injectable scPosologie:Bo, Ov: 10 mg/kgViande: Bo: 60 j, Ov: 50 jNe pas administrer aux Bo et Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/
50 1 MEDICAMENTS ANTIPARASITAIRESOxyclozanideLMR oxyclozanide: ZANIL (MSD A.H.)oxyclozanide: 34 mg/mlsolution poPosologie:Bo: 10 mg/kg, max 100 mlViande: 10 j, Lait: 60 hbidon 5 lR/1.3.1.8 AnticoccidiensIndicationsLes sulfamidés, l’amprolium et lestriazines (dic<strong>la</strong>zuril et toltrazuril) reprisci-dessous sont particulièrement indiquéscontre les coccidies. Les sulfamidésont déjà été envisagés dans lechapitre 1.1.7.PharmacodynamieLes sulfamidés sont actifs contreEimeria spp. aussi bien dans le côlonque dans l’intestin grêle. Ils présententcependant une efficacitémoindre contre E. tenel<strong>la</strong> (caecum).L’amprolium, un analogue de <strong>la</strong> thiamine,inhibe le transport de <strong>la</strong> thiaminedans les espèces d’Eimeria, perturbantainsi <strong>la</strong> synthèse de glucides.L’efficacité de l’amprolium peut êtreré<strong>du</strong>ite par l’administration concomitantede pro<strong>du</strong>its contenant descomplexes de vitamines B. Le médicamentà base d’amprolium est indiquédans le traitement des coccidioseschez les poulets et les dindes. Le toltrazuril,utilisé chez <strong>la</strong> vo<strong>la</strong>ille et leporc, est actif contre différents stadesintracellu<strong>la</strong>ires <strong>du</strong> cycle de Eimeria etIsospora. Le dic<strong>la</strong>zuril, utilisé chez lesovins et les bovins, est également actifcontre différents stades intracellu<strong>la</strong>iresd’Eimeria.PharmacocinétiqueL’amprolium est faiblement absorbéaprès administration orale chez lespoules et les dindes. Il est éliminé principalementpar les fécès. Après administrationorale, le dic<strong>la</strong>zuril est peurésorbé chez les ovins. L’absorptiondiminue avec l’âge des agneaux. Lamétabolisation est vraisemb<strong>la</strong>blementminime, l’excrétion a lieu principalementpar les fèces. Après administrationorale, le toltrazuril est absorbélentement. La biodisponibilité est de≥ 70 %. L’excrétion <strong>du</strong> toltrazuril estlente et se fait surtout par les fèces. Sademi-vie est d’environ 3 jours.Effets indésirablesEn général, l’usage des triazines estsûr. Des vomissements et des fientesmolles peuvent apparaître. Voir aussile chapitre 1.1.7. pour les effets indésirablesdes sulfamidés.Précautions particulièresL’usage alterné d’anticoccidiens possédantdes mécanismes d’action différentspeut prévenir l’apparition de résistance.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de l’amprolium n’a pas étéétudiée chez les poules pondeuses.AmproliumLMR amprolium : COCCIBAL 200 mg/ml (SP Veterinaria)amprolium (chlorhydrate): 200 mg/mlsolution po dans l’eau de boissonPosologie:poulets (poulets de chair, poulettes, poulespondeuses et repro<strong>du</strong>cteurs) et dindes:20 mg/kg pj (5 - 7 j)Lait: 0 j, Œufs: 0 jf<strong>la</strong>con 1 l, 5 lR/EIMERYL 200 mg/ml sol poulet et dinde (GlobalVet health)amprolium (chlorhydrate): 200 mg/mlsolution po dans l’eau de boissonPosologie:poulet (poulet de chair, poulette, poule pondeuseet poulet repro<strong>du</strong>cteur), dinde:20 mg/kg pj (5 - 7 j)Viande: 0 j, Oeuf: 0 jf<strong>la</strong>con 1 l, 5 lR/Dic<strong>la</strong>zurilLMR dic<strong>la</strong>zuril : VECOXAN 2,5 mg/ml (Eli Lilly)dic<strong>la</strong>zuril: 2,5 mg/mlsuspension poPosologie:veau ou agneau: 1 x 1 mg/kgTemps d’attente veau ou agneau: 0 jf<strong>la</strong>con 200 ml, 1 l, 5 lR/ToltrazurilLMR toltrazuril : BAYCOX 2,5 % sol orale (Bayer)toltrazuril: 25 g/lsolution po dans l’eau de boissonPosologie:poule, dindon (< 16 sem): 7 mg/kg pj (2 j)Viande: poule: 14 j, dindon: 16 jNe pas administrer aux poules pondeusesdont les oeufs sont destinés à <strong>la</strong> consommationhumaine, ne pas administrer aux poulesrepro<strong>du</strong>ctricesf<strong>la</strong>con 100 ml, 1 l, 5 lR/
1 MEDICAMENTS ANTIPARASITAIRES51BAYCOX 50 mg/ml susp orale (Bayer)toltrazuril: 50 mg/mlsuspension poPosologie:Su (âge 3 - 5 j): 1 x 20 mg/kgViande et abats: 77 jf<strong>la</strong>con 250 ml, 1 lR/BAYCOX bovis (Bayer)toltrazuril: 50 mg/mlsuspension poPosologie:veau < 80 kg PV:1 x 15 mg/kgViande et abats: 63 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100, 250 et 1000 mlR/BAYCOX sheep (Bayer)toltrazuril: 50 mg/mlsuspension poPosologie:agneau: 1 x 20 mg/kgViande et abats agneau: 42 jNe pas administrer aux Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/CEVAZURIL (Ceva Santé Animale)toltrazuril: 50 mg/mlsuspension poPosologie:porcelet (âge 3 - 5 j): 1 x 20 mg/kgViande: 77 jf<strong>la</strong>con 1000 mlR/DOZURIL 25 mg/ml (Dopharma Research)toltrazuril: 25 mg/mlsolution po dans l’eau de boissonPosologie:Av: 7 mg/kg pj (2 j), à administrer soit continuellementsur 48 h, soit sur 8 h pj pendant2 j consécutifsViande et abats: 16 jNe pas utiliser chez les Av dont les œufs sontdestinés à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/DOZURIL PIG 50 mg/ml susp po porcs (LavetPharmaceuticals Ltd)toltrazuril: 50 mg/mlsuspension poPosologie:Su (âge 3 - 5 j): 1 x 20 mg/kgViande et abats: 77 jf<strong>la</strong>con 250 ml et 1 lR/TOLTAROX 50 mg/ml susp po porc (KRKA)toltrazuril: 50 mg/mlsuspension poPosologie:porcelet (âge 3 - 5 j): 1 x 20 mg/kgViande et abats: 77 jf<strong>la</strong>con 250 ml, 1 lR/TOLTRANIL 50 mg/ml susp po porc (KRKA)toltrazuril: 50 mg/mlsuspension poPosologie:porcelet (âge 3 - 5 j): 1 x 20 mg/kgViande et abats: 77 jf<strong>la</strong>con 250 mlR/TRATOL 50 mg/ml (KRKA)toltrazuril: 50 mg/mlsuspension poPosologie:Su (âge 3 - 5 j): 20 mg/kgViande: 77 jf<strong>la</strong>con 250 ml, 1 lR/SulfamidésLMR sulfamidés : COXI PLUS (Oropharma)sulfadiméthoxine sodique: 250 mg/gpoudre po dans l’eau de boissonPosologie:pigeon: 50 mg/kg ou 1 dose/2 l d’eau (5 j)Ne pas administrer aux Co destinés à <strong>la</strong>consommation humainepoudre 8 x 4 g (sachets), 120 g (pot)R/ESB 3 30% (Novartis)sulfaclozine sodique (monohydrate): 30 g/100 gpoudre po dans l’eau de boissonPosologie:poule, dindon: 50 - 100 mg/kg pj (3 j, répéteréventuellement après 2 j)pigeon: 60 mg/kg pj (6 j)Viande: poule: 18 j, dindon: 28 jNe pas administrer aux poules pondeuses dontles oeufs sont destinés à <strong>la</strong> consommationhumaineNe pas administrer aux Co destinés à <strong>la</strong>consommation humainepoudre 250 gR/1.3.1.9 Pro<strong>du</strong>its actifssur d’autres protozoairesIndicationsCertains dérivés imidazolés sont préconiséschez le pigeon pour lutter contre<strong>la</strong> trichomonose. L’halofuginone estactive contre les formes libres (sporozoïteet mérozoïte) de Cryptosporidiumparvum et reste le médicament depremier choix dans le traitement decette affection malgré une marge desécurité étroite. D’autres indicationssont décrites dans <strong>la</strong> littérature scientifique,mais elles ne sont pas reprisesdans les notices des médicamentsenregistrés.PharmacodynamieLes nitroimidazoles possèdent, àl’exemple des nitrofuranes, une structureen anneau avec un groupe azoté.La ré<strong>du</strong>ction <strong>du</strong> groupement azotés’opère dans le parasite, formant ainsi
52 1 MEDICAMENTS ANTIPARASITAIRESdes radicaux libres endommageantles macromolécules <strong>du</strong> parasite.L’halofuginone entraverait le métabolisme<strong>du</strong> parasite à différents endroits.PharmacocinétiqueAucune donnée connue pour les imidazolés.La biodisponibilité de l’halofuginoneaprès administration oraleest de plus de 80%. L’halofuginonea une bonne diffusion tissu<strong>la</strong>ire, lesconcentrations tissu<strong>la</strong>ires dépassantles concentrations p<strong>la</strong>smatiques. Laconcentration maximale dans le p<strong>la</strong>smaest atteinte lentement (veau aprèsadministration po: > 11 h). Chez leveau, l’excrétion aurait principalementlieu via les urines.Contre-indicationLe titu<strong>la</strong>ire d’enregistrement <strong>du</strong>médicament à base d’halofuginonedéconseille l’administration aux animauxdont l’estomac est vide ou quisouffrent de diarrhée depuis plus de24 h.Effets indésirablesRonidazole: de légers effets indésirablesgastro-intestinaux ont étéobservés après multiplication par 4de <strong>la</strong> dose normale. La marge thérapeutiquede l’halofuginone est étroite:un doublement de <strong>la</strong> dose peut déjàengendrer des effets indésirablesgastro-intestinaux (diarrhée, anorexie,apathie, déshydratation) suivis éventuellementde mortalité lorsque <strong>la</strong> dosedépasse 5 mg/kg. L’administration<strong>du</strong> pro<strong>du</strong>it avec suffisamment d’eaupourrait ré<strong>du</strong>ire le risque d’effetsindésirables.Précautions particulièresLes imidazoles sont mutagènes dansles bactéries et carcinogènes chez <strong>la</strong>souris et le rat. Leur usage chez lesanimaux pro<strong>du</strong>cteurs de denrées alimentairesn’est donc plus permis.L’halofuginone irrite <strong>la</strong> peau et lesyeux. Etant toxique pour les poissonset les organismes aquatiques, on doitveiller à ce qu’il ne se retrouve pasdans les cours d’eau.Repro<strong>du</strong>ction et <strong>la</strong>ctationHalofuginone: le médicament est indiquéchez les nouveau-nés. La noticedéconseille l’utilisation <strong>du</strong> carnidazoleen période de couvage. Selon lesnotices des médicaments à base deronidazole, son usage est inoffensif enpériode d’élevage.CarnidazoleLMR carnidazole : SPARTRIX (Eli Lilly)carnidazole: 10 mgcomprimé poPosologie:pigeon: 10 mg/animalNe pas administrer aux pigeons destinés à <strong>la</strong>consommation humainecompr 50R/HalofuginoneLMR halofuginone : HALOCUR (MSD A.H.)halofuginone (<strong>la</strong>ctate): 0,50 mg/mlsolution po après les repasPosologie:veau (nouveau-né): 0,1 mg/kg pj (7 j)Viande: 13 jf<strong>la</strong>con 490 mlR/RonidazoleLMR ronidazole : TRICHO PLUS (Oropharma)ronidazole: 200 mg/dosepoudre po dans l’eau de boissonPosologie:pigeon, oiseau d’ornement: 10 mg/kg(5 - 7 j)Ne pas administrer aux pigeons destinés à <strong>la</strong>consommation humainepoudre 8 x 4 g, 30 x 4 g (sachets)R/TRICHOCURE (Oropharma)ronidazole: 5 mgcomprimé poPosologie:pigeon: 10 mg/kg ou 1 compr/pigeonNe pas administrer aux pigeons destinés à <strong>la</strong>consommation humainecompr 40R/1.3.1.10 AssociationsLes associations médicamenteusesont pour principal avantage d’é<strong>la</strong>rgirle spectre antiparasitaire. Il est doncpossible de traiter les animaux en uneseule administration contre plusieursparasites. Les principaux inconvénientssont l’utilisation conjointe de deux moléculesdotées de dé<strong>la</strong>is d’attente trèsdifférents et le traitement concomitantd’espèces parasitaires tout à fait différenteset dont l’épidémiologie diffère.Il peut en résulter une administration àun moment inadéquat de l’année. Lessubstances présentes dans les asso-
1 MEDICAMENTS ANTIPARASITAIRES53ciations reprises ci-dessous ont déjàété commentées précédemment.Moxidectine + tric<strong>la</strong>bendazoleLMR moxidectine + tric<strong>la</strong>bendazole : CYDECTIN TRICLAMOX ovins (Pfizer A.H.)moxidectine: 1 mg/mltric<strong>la</strong>bendazole: 50 mg/mlsolution poPosologie:Ov: 0,2 mg de M/kg + 10 mg de T/kgViande: 31 jNe pas administrer aux Ov dont le <strong>la</strong>it est destinéà <strong>la</strong> consommation humaine ni aux brebisgravides pro<strong>du</strong>ctrices de <strong>la</strong>it au cours des 2 mprécédant <strong>la</strong> mise basf<strong>la</strong>con 1 lR/Milbémycine + praziquantelLMR milbémycine + praziquantel : MILBEMAX petits chats et chatons (Novartis)milbémycine oxime: 4 mgpraziquantel: 10 mgcomprimé poPosologie:Fe (PV > 0,5 kg et âge > 6 sem):1 x 2 mg de M/kg + 5 mg de P/kg (avec ouaprès le repas)compr 2 x 10MILBEMAX chats (Novartis)milbémycine oxime: 16 mgpraziquantel: 40 mgcomprimé poPosologie:Fe (PV > 2 kg): 1 x 2 mg de M/kg +5 mg de P/kg (avec ou après le repas)compr 2 x 10MILBEMAX petits chiens et chiots (Novartis)milbémycine oxime: 2,5 mgpraziquantel: 25 mgcomprimé poPosologie:Ca (PV > 0,5 kg et âge > 2 sem):1 x 0,5 mg de M/kg + 5 mg de P/kg (avecou après le repas)compr 5 x 10R/MILBEMAX chiens (Novartis)milbémycine oxime: 12,5 mgpraziquantel: 125 mgcomprimé poPosologie:Ca (PV > 5 kg): 1 x 0,5 mg de M/kg +5 mg de P/kg (avec ou après le repas)compr 5 x 10R/MILBEMAX compr à croquer petits chiens et chiots(Novartis)milbémycine oxime: 2,5 mg/comprpraziquantel: 25 mg/comprcomprimé à croquer poPosologie:Ca (PV > 1 kg): 1 x 0,5 mg de M/kg +5 mg de P/kg (avec ou après le repas)compr 12 x 4R/MILBEMAX compr à croquer chiens (Novartis)milbémycine oxime: 12,5 mg/comprpraziquantel: 125 mg/comprcomprimé à croquer poPosologie:Ca (PV > 5 kg): 1 x 0,5 mg de M/kg + 5 mgde P/kg (avec ou après le repas)compr 12 x 4R/Praziquantel + pyrantel embonateLMR praziquantel + pyrantel : DRONTAL CAT (Bayer)pyrantel embonate: 230 mgpraziquantel: 20 mgcomprimé poPosologie:Fe (âge > 3 sem): 5 mg de praz/kg +57,5 mg de pyr emb/kgcompr 2, 24Praziquantel + fenbendazoleLMR praziquantel + fenbendazole : CANIQUANTEL PLUS (Fendigo)praziquantel: 50 mgfenbendazole: 500 mgcomprimé poPosologie:Ca, Fe: 5 mg de P/kg + 50 mg de F/kgcompr 6, 100R/PARAZAN (Prodivet)praziquantel: 50 mgfenbendazole: 500 mgcomprimé poPosologie:Ca, Fe: 5 mg de P/kg + 50 mg de F/kg pj(2 j, 3 j en cas d’ankylostomes, trichures)compr 2, 6, 100VEPRAFEN (Ceva Santé Animale)fenbendazole: 500 mgpraziquantel: 50 mgcomprimé poPosologie:Ca, Fe: 5 mg de P/kg + 50 mg de F/kgcompr 6, 100ZANTEL (Chanelle Pharmaceuticals)praziquantel: 50 mgfenbendazole: 500 mgcomprimé poPosologie:Ca (âge > 2 sem): 5 mg de P/kg +50 mg de F/kg pj (2 j)compr 100R/
54 1 MEDICAMENTS ANTIPARASITAIRESPyrantel embonate + fébantel +praziquantelLMR pyrantel + fébantel +praziquantel: ANTHELMEX compr à croquer chiens (LavetPharmaceuticals)fébantel: 150 mgpyrantel (embonate): 50 mgpraziquantel: 50 mgcomprimé à croquer poPosologie:Ca (PV < 30 kg): 1 x 15 mg de féb + 5 mg depyr (emb) + 5 mg de praz/kgcompr 2, 8, 104ANTHELMEX FORTE compr à croquer chiens(Lavet Pharmaceuticals)fébantel: 525 mgpyrantel (embonate): 175 mgpraziquantel: 175 mgcomprimé à croquer poPosologie:Ca (PV > 17,5 kg): 1 x 15 mg de féb + 5 mgde pyr (emb) + 5 mg de praz/kgcompr 2, 48CAZITEL PLUS compr chien (ChanellePharmaceuticals)praziquantel: 50 mgpyrantel (embonate): 50 mgfébantel: 150 mgcomprimé poPosologie:Ca: 15 mg de féb/kg + 5 mg de pyr/kg +5 mg de praz/kg (1 compr/10 kg PV)compr 1 x 2, 13 x 8CESTEM compr appétents chiens moyens et petitschiens (Ceva Santé Animale)fébantel: 150 mgpyrantel (embonate): 50 mgpraziquantel: 50 mgcomprimé poPosologie:Ca, chiot (PV min 3 kg):15 mg de féb/kg + 5 mg de pyr/kg +5 mg de praz/kgchiot (âge 2 -12 sem): traiter toutes les 2 semCa al<strong>la</strong>itantes: 2 sem après <strong>la</strong> parturition,ensuite toutes les 2 sem jusqu’au sevrageCa (âge > 12 sem): traiter tous les 3 mcompr 1 x 2, 52 x 2CESTEM compr appétents grands chiens(Ceva Santé Animale)fébantel: 525 mgpyrantel (embonate): 175 mgpraziquantel: 175 mgcomprimé poPosologie:Ca, chiot: PV > 17,5 kg15 mg de féb/kg + 5 mg de pyr/kg + 5 mgde praz/kgchiot (âge 2 -12 sem): traiter toutes les 2 semCa al<strong>la</strong>itantes: 2 sem après <strong>la</strong> parturition,ensuite toutes les 2 sem jusqu’au sevrageCa (âge > 12 sem): traiter tous les 3 mcompr 1 x 2, 24 x 2DRONTAL DOG FLAVOUR (Bayer)pyrantel embonate: 144 mgpraziquantel: 50 mgfébantel: 150 mgcomprimé poPosologie:Ca: 14,4 mg de pyr emb/kg + 5 mgde praz/kg + 15 mg de féb/kgnématodes et cestodes: 1 j, Giardia: 3 jcompr 2, 6, 104DRONTAL LARGE DOG FLAVOUR (Bayer)fébantel: 525 mgpyrantel embonate: 504 mgpraziquantel: 175 mgcomprimé poPosologie:Ca: 15 mg de féb/kg + 14,4 mg de pyr emb/kg+ 5 mg de praz/kg (soit 1 compr/35 kg)nématodes et cestodes: 1 j, Giardia: 3 jcompr 2, 24ENDOGARD PLUS FLAVOUR (KRKA)praziquantel: 50 mgpyrantel embonate: 144 mgfébantel: 150 mgcomprimé poPosologie:Ca (petite à moyenne taille): 15 mg de féb/kg + 14,4 mg de pyr/kg + 5 mg de praz/kg,à admin à partir de l’âge de 2 sem toutes les2 sem jusqu’à l’âge de 12 sem, ensuite tousles 3 m (traiter simultanément chienne etchiots) (Toxocara: admin 2 sem après misebas aux chiennes al<strong>la</strong>itantes, puis répétertoutes les 2 sem jusqu’au sevrage, forteinfest vers ronds: répéter dose après 14 j,contrôle de routine:1 dose tous les 3 m)compr 30, 100ENDOGARD PLUS XL (KRKA)praziquantel: 175 mgpyrantel embonate: 504 mgfébantel: 525 mgcomprimé poPosologie:Ca (grande à très grande taille): 15 mg deféb/kg + 14,4 mg de pyr/kg + 5 mg de praz/kg(Toxocara: admin 2 sem après mise bas auxchiennes al<strong>la</strong>itantes, puis répéter toutes les2 sem jusqu’au sevrage, forte infest versronds: répéter dose après 14 j, contrôle deroutine:1 dose tous les 3 m)compr 10PRAZITEL PLUS (Chanelle Pharmaceuticals)praziquantel: 50 mgpyrantel (embonate): 50 mgfébantel: 150 mgcomprimé poPosologie:Ca: 15 mg de féb/kg + 5 mg de pyr/kg +5 mg de praz/kgcompr 24, 104R/
1 MEDICAMENTS ANTIPARASITAIRES55Pyrantel embonate + oxantel +praziquantelLMR pyrantel + oxantel +praziquantel : DOLPAC compr petits chiens (Vétoquinol)oxantel (embonate): 40,06 mgpyrantel (embonate): 9,99 mgpraziquantel: 10,00 mgcomprimé poPosologie:Ca: 1 x 20 mg/kg d’ox + 5 mg/kg de pyr +5 mg/kg de praz (= 1 compr/2 kg)clinic pack compr 60R/DOLPAC compr chiens moyens (Vétoquinol)oxantel (embonate): 200,28 mgpyrantel (embonate): 49,94 mgpraziquantel: 50,00 mgcomprimé poPosologie:Ca: 1 x 20 mg/kg d’ox + 5 mg/kg de pyr +5 mg/kg de praz (= 1 compr/10 kg)clinic pack compr 60R/DOLPAC compr grands chiens (Vétoquinol)oxantel (embonate): 500,70 mgpyrantel (embonate): 124,85 mgpraziquantel: 125,00 mgcomprimé poPosologie:Ca: 1 x 20 mg/kg d’ox + 5 mg/kg de pyr +5 mg/kg de praz (= 1 compr/25 kg)clinic pack compr 60R/Pyrantel embonate + fébantelLMR pyrantel + fébantel : DRONTAL PUP (Bayer)pyrantel embonate: 14,4 mg/mlfébantel: 15 mg/mlsuspension poPosologie:chiot, jeune chien: 15 mg de féb/kg +14,4 mg de pyr emb/kgf<strong>la</strong>con 50 mlEmodepside + praziquantelIndicationsCette combinaison est active contreles vers ronds (ascaris et ankylostomes)et les vers p<strong>la</strong>ts.Praziquantel: voir chapitre 1.3.1.6.(pour le pro<strong>du</strong>it indiqué chez le chat,voir chapitre 1.3.2.2)PharmacodynamieL’emodepside est un composé semisynthétiqueappartenant à <strong>la</strong> nouvellec<strong>la</strong>sse des depsipeptides. Il est actifcontre les vers ronds et agit au niveaudes jonctions neuromuscu<strong>la</strong>ires en stimu<strong>la</strong>ntles récepteurs présynaptiquesde <strong>la</strong> famille de <strong>la</strong> sécrétine, entraînant<strong>la</strong> paralysie et <strong>la</strong> mort des parasites.PharmacocinétiqueLes concentrations maximales des deuxprincipes actifs sont atteintes 2 heuresaprès l’administration. Ils sont ensuiteéliminés <strong>du</strong> p<strong>la</strong>sma avec un temps dedemi-vie entre 1.4 à 1.7 heures. Aprèsadministration orale chez le rat, l’emodepsideest distribué dans tous lesorganes. Les concentrations les plusimportantes sont retrouvées dans letissu adipeux. L’emodepside non métaboliséeet des dérivés hydroxylés sontles principaux pro<strong>du</strong>its d’excrétion.L’excrétion de l’emodepside n’a pasété étudiée chez les chiens. Des étudesréalisées chez différentes espècesrévèlent que le praziquantel est rapidementmétabolisé dans le foie. Il estprincipalement éliminé par voie rénale.Contre-indicationsNe pas administrer aux chiens demoins de 12 semaines ou pesantmoins de 1 kg.Effets indésirablesDes troubles digestifs et des troublesneurologiques ont été observés dansde très rares cas. Le non respect desconditions de jeûne tendait à être unecaractéristique de ces cas. Les signesneurologiques observés peuvent êtreplus sévères chez les colleys et lesautres races présentant une mutationmdr1.InteractionsL’emodepside étant un substrat pour <strong>la</strong>glycoprotéine P, des interactions pourraientapparaître avec d’autres substancesfonctionnant comme substratsou inhibiteurs de <strong>la</strong> glycoprotéine P,par exemple, l’ivermectine et d’autres<strong>la</strong>ctones macrocycliques antiparasitaires,l’érythromycine, <strong>la</strong> prednisoloneou <strong>la</strong> ciclosporine. Les conséquencescliniques potentielles de telles interactionsn’ont pas été évaluées.Précautions particulièresAdministrer les pro<strong>du</strong>its par voie oraleuniquement à des chiens à jeun.Aucune nourriture ne doit être donnéedans les 4 heures qui suivent l’administration<strong>du</strong> traitement.Des études réalisées chez les rats etles <strong>la</strong>pins révèlent que l’emodepsidepeut interférer avec le développementembryo-fœtal. En conséquence, lesfemmes enceintes ou susceptibles del’être doivent éviter les contacts avecle pro<strong>du</strong>it ou porter des gants jetableslors de son application.
56 1 MEDICAMENTS ANTIPARASITAIRESRepro<strong>du</strong>ction et <strong>la</strong>ctationLe médicament peut être administréen période de gestation et de <strong>la</strong>ctation.LMR emodepside + praziquantel: PROFENDER compr à lib modif petits chiens(Bayer HealthCare)emodepside: 3 mg/comprpraziquantel: 15 mg/comprcomprimé poPosologie:Ca (âge > 12 sem, PV: 1 - 6 kg):min 1 mg d’E/kg + 5 mg de P/kg(soit 1 compr/3 kg)compr 24R/PROFENDER compr à lib modif chiens moyens(Bayer HealthCare)emodepside: 10 mg/comprpraziquantel: 50 mg/comprcomprimé poPosologie:Ca (âge > 12 sem, PV: 6 - 20 kg):min 1 mg d’E/kg + 5 mg de P/kg(soit 1 compr/10 kg)compr 24, 102R/PROFENDER compr à lib modif grands chiens(Bayer HealthCare)emodepside: 30 mg/comprpraziquantel: 150 mg/comprcomprimé poPosologie:Ca (âge > 12 sem, PV: 20 - 60 kg):min 1 mg d’E/kg + 5 mg de P/kg(soit 1 compr/30 kg)compr 24R/Emodepside + toltrazurilL’administration de cette spécialitén’est pas recommandée chez les chiensColley.LMR emodepside + toltrazuril: PROCOX (Bayer)émodepside: 0,9 mg/mltoltrazuril: 18 mg/mlsuspension poPosologie:Ca (âge > 2 sem, PV > 0,4 kg):1 x 0,45 mg d'E/kg + 9 mg de T/kgf<strong>la</strong>con 20 mlR/1.3.2 Médicaments à usage transdermique actifs contre les endoparasitesL’application cutanée n’exclut pas <strong>la</strong> possibilité d’une action systémique qui peutaussi donner lieu à des effets indésirables généraux et à des intoxications. Il fautparticulièrement insister sur les modalités d’emploi pour ce type de préparations.1.3.2.1 Imidazothiazolés1.3.2.2 AssociationCommentaire : voir chapitre 1.3.1.3.Moxidectine + tric<strong>la</strong>bendazoleLMR lévamisole : Moxidectine: voir chapitre 1.3.3.,tric<strong>la</strong>bendazole: voir chapitre 13.1.2.QUADROSOL pour-on (Prodivet)lévamisole: 200 mg/mlsolution à usage externe (transcutané)Posologie:Bo, veau:10 mg/kg (max 6.000 mg/animal)Viande: 42 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 500 mlR/LMR moxidectine + tric<strong>la</strong>bendazole: CYDECTIN TRICLAMOX BOVINS (Pfizer)moxidectine: 5 mg/mltric<strong>la</strong>bendazole: 200 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 0,5 mg de mox/kg + 20 mg de tri/kgViande: Bo: 143 jNe pas administrer aux Bo en <strong>la</strong>ctation ougestation dont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaineLes animaux traités doivent être gardés séparésdes animaux non traités pendant toute <strong>la</strong>période de retrait (contamination par léchage)f<strong>la</strong>con 1 l, 2.5 l, 5 lR/Emodepside + praziquantelIndicationsCette combinaison est active contre lesvers ronds (ascaris et ankylostomes) etles vers p<strong>la</strong>ts.Praziquantel: voir chapitre 1.3.1.6.(pour le pro<strong>du</strong>it indiqué chez le chien,voir chapitre 1.3.1.10.)
1 MEDICAMENTS ANTIPARASITAIRES57PharmacodynamieL’emodepside est un composé semisynthétiqueappartenant à <strong>la</strong> nouvellec<strong>la</strong>sse des depsipeptides. Il est actifcontre les vers ronds et agit au niveaudes jonctions neuromuscu<strong>la</strong>ires en stimu<strong>la</strong>ntles récepteurs présynaptiquesde <strong>la</strong> famille de <strong>la</strong> sécrétine, entraînant<strong>la</strong> paralysie et <strong>la</strong> mort des parasites.PharmacocinétiqueAprès application cutanée de ce pro<strong>du</strong>itchez les chats, on observe desconcentrations sériques maximales3,2 ± 2,7 jours après application pourl’emodepside, et 18,7 ± 47 heuresaprès application pour le praziquantel.Les deux principes actifs sontensuite lentement éliminés (t1/2 = 9,2± 3,9 jours pour l’emodepside et 4,1 ±1,5 jours pour le praziquantel). Aprèsadministration orale chez le rat, l’emodepsideest distribué dans tous lesorganes. Les concentrations les plusimportantes sont retrouvées dans letissu adipeux. L’emodepside et sesmétabolites sont éliminés essentiellementpar voie fécale. Des études réaliséeschez différentes espèces révèlentque le praziquantel est rapidementmétabolisé dans le foie. Il est principalementéliminé par voie rénale.Contre-indicationsNe pas administrer aux animaux demoins de 8 semaines ou pesant moinsde 0,5 kg.InteractionsL’emodepside étant un substrat pour <strong>la</strong>glycoprotéine P, des interactions pourraientapparaître avec d’autres substancesfonctionnant comme substratsou inhibiteurs de <strong>la</strong> glycoprotéine P,par exemple, l’ivermectine et d’autres<strong>la</strong>ctones macrocycliques antiparasitaires,l’érythromycine, <strong>la</strong> prednisoloneou <strong>la</strong> ciclosporine. Les conséquencescliniques potentielles de telles interactionsn’ont pas été évaluées.Précautions particulièresLe pro<strong>du</strong>it est appliqué par voie transcutanée.Il faut éviter que le chat traitéou les autres chats <strong>du</strong> foyer lèchentle site d’application tant qu’il esthumide, et tenir les enfants à l’écart.Des études réalisées chez les rats etles <strong>la</strong>pins révèlent que l’emodepsidepeut interférer avec le développementembryo-fœtal. En conséquence, lesfemmes enceintes ou susceptibles del’être doivent éviter les contacts avecle pro<strong>du</strong>it ou porter des gants jetableslors de son application.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe médicament peut être administréen période de gestation et de <strong>la</strong>ctation.LMR emodepside + praziquantel: PROFENDER SPOT-on pour chats f<strong>la</strong>con multidoses(Bayer HealthCare)emodepside: 21,4 mg/mlpraziquantel: 85,8 mg/mlsolution pour usage externe (transcutané)Posologie:Fe (âge > 8 sem, PV: 0,5 kg):min 3 mg d’E/kg + 12 mg de P/kg(soit 0,14 ml sol/kg)f<strong>la</strong>con 14 mlR/PROFENDER SPOT-ON sol petits chats(Bayer HealthCare)emodepside: 7,5 mg/pipettepraziquantel: 30 mg/pipettesolution pour usage externe (transcutané)Posologie:Fe (âge > 8 sem, PV: 0,5 - 2,5 kg):min 3 mg d’E/kg + 12 mg de P/kg(soit 0,14 ml sol/kg)pipette 2 x 0,35 ml20 x 0,35 mlR/PROFENDER SPOT-ON sol chats moyens(Bayer HealthCare)emodepside: 15 mg/pipettepraziquantel: 60 mg/pipettesolution pour usage externe (transcutané)Posologie:Fe (âge > 8 sem, PV: 2,5 - 5 kg):min 3 mg d’E/kg + 12 mg de P/kg(soit 0,14 ml sol/kg)pipette 2 x 0,70 ml4 x 0,70 ml20 x 0,70 mlR/PROFENDER SPOT-ON sol grands chats(Bayer HealthCare)emodepside: 24 mg/pipettepraziquantel: 96 mg/pipettesolution pour usage externe (transcutané)Posologie:Fe (âge > 8 sem, PV: 5 - 8 kg):min 3 mg d’E/kg + 12 mg de P/kg(soit 0,14 ml sol/kg)Fe (PV > 8 kg):utiliser combinaison appropriée de pipettespipette 2 x 1,12 ml20 x 1,12 mlR/
58 1 MEDICAMENTS ANTIPARASITAIRES1.3.3 Médicaments à usage transdermique actifs contre les ecto- etles endoparasites1.3.3.1 Lactones macrocycliques(LM)Les <strong>la</strong>ctones macrocycliques rassemblentdifférentes molécules synthétiséespar des Streptomyces. Ellessont c<strong>la</strong>ssées en deux groupes : lesavermectines avec l’ivermectine, <strong>la</strong>doramectine, l’éprinomectine et <strong>la</strong> sé<strong>la</strong>mectine,et les milbémycines avec <strong>la</strong>moxidectine et <strong>la</strong> milbémycine oxime.IndicationsElles sont essentiellement utiliséespour lutter contre les nématodes etcertains arthropodes chez les bovinset les carnivores domestiques. Les trématodeset les cestodes sont naturellementrésistants. L’efficacité des LMapproche 100 % pour <strong>la</strong> plupart desparasites sensibles, aussi bien contreles formes matures qu’immatures,sous forme de <strong>la</strong>rves hypobiotiques.Nematodirus et Psoroptes sont considéréscomme étant les “dose limitinggenera”. La formu<strong>la</strong>tion topique estmoins active contre <strong>la</strong> gale psoroptique.En Europe, seuls quelques casde résistance ont été mentionnéschez des ruminants (Haemonchuscontortus, Te<strong>la</strong>dorsagia circumcincta,Cooperia oncophora). Chez le pou<strong>la</strong>in,des résistances sont suspectées chezParascaris equorum. (Voir aussi FoliaVeterinaria 2006, n° 3 et 2009, n° 1)PharmacodynamieLes <strong>la</strong>ctones macrocycliques (LM) activentles canaux chlorures glutamatedépendants(GluCl) présents dans lescellules nerveuses ou muscu<strong>la</strong>ires desinvertébrés. La membrane cellu<strong>la</strong>iredevient ainsi plus perméable aux ionschlorure, entrainant une hyperpo<strong>la</strong>risationde <strong>la</strong> cellule nerveuse ou muscu<strong>la</strong>ire,qui con<strong>du</strong>it en fin de compte àune paralysie f<strong>la</strong>sque <strong>du</strong> parasite. Chezles mammifères, les canaux GluCl sontabsents. Les LM sont donc pourvusd’une marge de sécurité re<strong>la</strong>tivementélevée chez ces espèces. Dans <strong>la</strong> littératurerécente, ce mécanisme d’actiondes LM est considéré comme étantle plus important. Dans des concentrationsplus élevées, ces moléculespeuvent également interagir avec lescanaux chlorures GABA-dépendants.La stimu<strong>la</strong>tion de ces récepteurs GABA(acide gamma aminobutyrique) provoqueégalement une hyperpo<strong>la</strong>risationprolongée des cellules nerveuseset une paralysie f<strong>la</strong>sque <strong>du</strong> parasite.La présence de GABA dans le cerveaudes mammifères explique les effets indésirablestoxiques des LM. Les tiquesne sont pas immédiatement tuées parles LM, mais ces molécules entraventdivers processus biologiques tels que<strong>la</strong> pro<strong>du</strong>ction d’œufs et le processusde desquamation.PharmacocinétiqueAprès une phase d’absorption plusou moins lente selon <strong>la</strong> voie d’administrationchoisie, ces substancessont essentiellement stockées auniveau des tissus adipeux et <strong>du</strong> foie;en revanche, de faibles taux sontretrouvés dans le système nerveuxcentral malgré leur forte liposolubilité.L’élimination dans les matières fécalesest <strong>la</strong> voie <strong>la</strong> plus importante mais lesvoies urinaire et <strong>la</strong>ctée ne sont pas ànégliger. L’éprinomectine présente uncoefficient de partage <strong>la</strong>it/p<strong>la</strong>sma trèsparticulier. Le pro<strong>du</strong>it ne passe pratiquementpas dans le <strong>la</strong>it et le dé<strong>la</strong>id’attente chez <strong>la</strong> vache <strong>la</strong>itière est parconséquent nul. De même, <strong>la</strong> formepour-on à base de moxidectine a untemps d’attente de zéro jour pour le <strong>la</strong>itdes bovins ; contrairement aux autresmédicaments à base de moxidectineadministrés per os ou par injection.Une métabolisation partielle intervientégalement.Contre-indicationsCertaines races canines sont particulièrementsensibles aux effets indésirablesde ces substances. Voir aussi«Effets indésirables».Effets indésirablesL’utilisation de LM chez des mammifèresen bonne santé ne semblepas présenter de risques importants.Néanmoins, des signes d’ataxie, deléthargie, de mydriase, d’hypothermie,de tremblements, le coma et des casde mortalité peuvent être observéslors de surdosages importants. Uneapplication topique n’exclut pas <strong>la</strong>possibilité d’une action systémiquequi peut donner lieu à des effets indésirablesgénéraux et à des intoxications.Il faut particulièrement insistersur les modalités d’emploi pour cetype de préparation. L’espèce canine,spécialement les races dites ang<strong>la</strong>ises
1 MEDICAMENTS ANTIPARASITAIRES59(collie, bobtail) semble être beaucoupplus sensible et peut développer dessignes cliniques très sérieux, même àdoses thérapeutiques ou infra-thérapeutiques(voir aussi Folia Veterinaria2010 n° 2). Les formu<strong>la</strong>tions topiquesà base de sé<strong>la</strong>mectine ou de moxidectineou <strong>la</strong> milbémycine oxime à usageoral, enregistrées pour cette espèce,sont inoffensives si <strong>la</strong> dose est respectée.Chez le cheval et le chien infestéspar respectivement des microfi<strong>la</strong>iresd’Onchocerca ou de « ver cardiaque »(dirofi<strong>la</strong>riose), des réactions d’hypersensibilitépeuvent apparaître suite à <strong>la</strong>nécrose d’un grand nombre de parasites.Le traitement de bovins infestéspar Hypoderma bovis peut engendrerde graves effets indésirables lorsquele parasite est à proximité <strong>du</strong> canalrachidien (paralysie) ou de l’œsophage(tympanisme). On évitera de traitercette espèce <strong>du</strong>rant <strong>la</strong> période situéeentre début décembre et début mars.InteractionsL’utilisation simultanée avec des benzodiazépinesaugmente <strong>la</strong> toxicité dechaque principe actif.Précautions particulièresIl convient de prendre les mesuresnécessaires pour éviter l’éliminationde ces molécules dans le milieu extérieur.Des mesures spécifiques sontdécrites à cet égard dans les RCP desmédicaments. En effet, les LM ont uneaction létale sur certains arthropodesinféodés aux bouses qui en assurenten partie <strong>la</strong> dégradation (bousiers etcertaines espèces de mouches, parexemple). Ces composés sont dangereuxpour les poissons et les organismesaquatiques dont le milieu peutêtre contaminé par l’élimination def<strong>la</strong>cons usagés ou par les rési<strong>du</strong>s issusd’animaux traités.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune malformation fœtale n’a étéobservée dans les études de repro<strong>du</strong>ctionmenées chez différents animauxde compagnie. L’administration esttoutefois déconseillée dans certainsRCP. A l’exception de l’éprinomectine,ces substances sont excrétées enfaibles concentrations via le <strong>la</strong>it.DoramectineLMR doramectine : DECTOMAX pour-on (Eli Lilly)doramectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 1 x 0,5 mg/kgViande: 35 jNe pas administrer aux vaches <strong>la</strong>itières dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humaine, nichez les vaches en période de tarissement ouchez les génisses <strong>la</strong>itières gravides dans les60 j avant le vê<strong>la</strong>gef<strong>la</strong>con 1 l et 3 lR/DECTOMAX pour-on (Wirtz Farma)doramectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 1 x 0,5 mg/kgViande: 35 j, Ne pas administrer aux vaches<strong>la</strong>itières pendant <strong>la</strong> pro<strong>du</strong>ction, le tarissementou aux génisses 60 j avant le vê<strong>la</strong>gef<strong>la</strong>con 1 lR/parEprinomectineLMR éprinomectine : EPRINEX pour-on (Merial)éprinomectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 1 x 0,5 mg/kgViande: 15 j, Lait: 0 jf<strong>la</strong>con 1 l, 2.5 l, 5 lR/IvermectineLMR ivermectine: ECOMECTIN CATTLE pour-on (Eco A.H.)ivermectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 500 mcg/kg (1 ml/10 kg)Viande: 31 jNe pas administrer aux animaux dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humaine ni enpériode de tarissement ni aux génisses dans les60 j avant <strong>la</strong> mise basf<strong>la</strong>con 1 l, 2.5 l, 5 lR/IVOMEC pour-on (Merial)ivermectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo, veau: 0,5 mg/kgViande: 15 jNe pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ou 60 javant le vê<strong>la</strong>gef<strong>la</strong>con 250 ml, 1 lR/
60 1 MEDICAMENTS ANTIPARASITAIRESNOROMECTIN pour-on (Norbrook Lab)ivermectine: 0,5 % w/vsolution à usage cutanéPosologie:Bo: 500 mcg/kgViande: 28 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ni dans les60 j avant <strong>la</strong> mise basf<strong>la</strong>con 250 ml, 1 l, 2,5 lR/TOPIMEC pour-on sol 0,5 % (Chanelle A.H.)ivermectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 500 mcg/kg (min 28 j entre 2traitements)Viande: 28 j, Ne pas administrer aux animauxdont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaine ni en période de tarissement ni auxgénisses dans les 60 j avant <strong>la</strong> mise basf<strong>la</strong>con 1 l et 2,5 lR/VIRBAMEC pour-on (Virbac)ivermectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 0,5 mg/kgViande: 28 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ou 60 javant le vê<strong>la</strong>gef<strong>la</strong>con 1 l, 2.5 l, 5 lR/MoxidectineLMR moxidectine : CYDECTIN 0,5 % pour-on bovins (Pfizer A.H.)moxidectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 0,5 mg/kg (1 ml/10 kg)Viande: 14 j, Lait: 0 jf<strong>la</strong>con 500 ml, 1 l, 2.5 l, 5 lR/CYDECTIN 0,5 % pour-on bovins (Wirtz Farma)moxidectine: 5 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 0,5 mg/kg (1 ml/10 kg)Viande: 14 j, Lait: 0 jf<strong>la</strong>con 1 lR/parSé<strong>la</strong>mectineLMR sé<strong>la</strong>mectine: STRONGHOLD 15 mg, 30 mg, 45 mg, 60 mg,120 mg, 240 mg (Pfizer A.H.)sé<strong>la</strong>mectine: 15 mg, 30 mg, 45 mg, 60 mg,120 mg, 240 mgsolution à usage externe (transcutané)Posologie:Ca, Fe (> 6 sem): 6 mg/kgtube3 ou 15 x 15 mg/0,25 ml3 ou 6 x 30 mg/0,25 ml3 ou 6 x 45 mg/0,75 ml3 ou 6 x 60 mg/0,5 ml3 ou 6 x 120 mg/1 ml3 ou 6 x 240 mg/2 mlR/1.3.3.2 AssociationImidaclopride + moxidectineMoxidectine: voir chapitre 1.3.3.1 etimidaclopride: voir chapitre 12.1.3.5IndicationsCe pro<strong>du</strong>it est indiqué chez le chien,le chat et le furet pour <strong>la</strong> prévention etle traitement d’infestations parasitairesmixtes : puces (Ca, Fe, furet), gale desoreilles (Ca, Fe), poux broyeurs (Ca),gale sarcoptique et démodécie (Ca),dirofi<strong>la</strong>riose (Ca, Fe, furet) et certainsnématodes gastro-intestinaux (Ca, Fe).La fréquence des doses à administrerdépend <strong>du</strong> type de parasite.PharmacocinétiqueAprès application cutanée, l’imidaclopridese répartit rapidement sur <strong>la</strong>peau de l’animal, tandis que <strong>la</strong> moxidectineest absorbée par voie cutanée.Contre-indicationsNe pas utiliser chez les chiens âgés demoins de 7 semaines et les chats âgésde moins de 9 semaines.Effets indésirablesDu prurit et de rares cas de séborrhée,d’érythème et de vomissementpeuvent survenir chez les animauxtraités. Le léchage de l’endroit où lepro<strong>du</strong>it a été appliqué peut engendrerde <strong>la</strong> salivation, des symptômes neurologiques,une respiration anormaleet des vomissements.Précautions particulièresLes animaux traités ne doivent paspouvoir lécher l’endroit où le pro<strong>du</strong>ita été appliqué (sur eux-mêmes ousur les autres animaux). Le traitementde chiens et de chats pesant moinsd’1 kg ou de furets pesant moins de0,8 kg doit être basé sur une évaluation<strong>du</strong> rapport bénéfice/risque.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it pendant <strong>la</strong> périodede <strong>la</strong>ctation ou de gestation n’apas été démontrée.LMR imidaclopride + moxidectine: ADVOCATE SPOT-ON sol petits chats et furets(Bayer HealthCare)moxidectine: 4 mgimidaclopride: 40 mgsolution à usage cutanéPosologie:Fe (âge > 9 sem , PV jusqu’à 4 kg):10 mg d’I/kg + 1 mg de M/kgfuret (PV > 800 g):10 mg d'I/kg + 1 mg de M/kgpipette 3 x 0,4 ml, 21 x 0,4 mlR/
1 MEDICAMENTS ANTIPARASITAIRES61ADVOCATE SPOT-ON sol grands chats(Bayer HealthCare)moxidectine: 8 mgimidaclopride: 80 mgsolution à usage cutanéPosologie:Fe (âge > 9 sem , PV > 4 - 8 kg):10 - 20 mg d’I/kg + 1 - 2 mg de M/kgFe (PV > 8 kg): combinaison appropriée depipettespipette 3 x 0,8 ml, 21 x 0,8 mlR/ADVOCATE SPOT-ON sol petits chiens(Bayer HealthCare)moxidectine: 10 mgimidaclopride: 40 mgsolution à usage cutanéPosologie:Ca (âge > 7 sem, PV jusqu’à 4 kg):10 mg d’I/kg + 2,5 mg de M/kgpipette 3 x 0,4 ml, 21 x 0,4 mlR/ADVOCATE SPOT-ON sol chiens moyens(Bayer HealthCare)moxidectine: 25 mgimidaclopride: 100 mgsolution à usage cutanéPosologie:Ca (âge > 7 sem, PV > 4 - 10 kg):10 - 25 mg d'I/kg + 2,5 - 6,25 mg de M/kgpipette 3 x 1 ml, 21 x 1 mlR/ADVOCATE SPOT-ON sol grands chiens(Bayer HealthCare)moxidectine: 62,5 mgimidaclopride: 250 mgsolution à usage cutanéPosologie:Ca (âge > 7 sem, PV > 10 - 25 kg):10 - 25 mg d’I/kg + 2,5 - 6,25 mg de M/kgpipette 3 x 2,5 ml, 21 x 2,5 mlR/ADVOCATE SPOT-ON sol très grands chiens(Bayer HealthCare)moxidectine: 100 mgimidaclopride: 400 mgsolution à usage cutanéPosologie:Ca (âge > 7 sem, PV > 25 - 40 kg):10 - 16 mg d’I/kg + 2,5 - 4 mg de M/kgCa (PV > 40 kg):combinaison appropriée de pipettespipette 3 x 4 ml, 21 x 4 mlR/Ivermectine + closantelLMR ivermectine + closantel : CLOSAMECTIN pour-on bovins (Norbrook Lab)ivermectine: 5 mg/mlclosantel (sodium dihydrate): 200 mg/mlsolution à usage externe (transcutané)Posologie:Bo: 500 mcg d’I/kg + 20 mg de C/kgViande et abats: 28 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, y comprisles animaux gestants destinés à pro<strong>du</strong>ire <strong>du</strong> <strong>la</strong>itpour <strong>la</strong> consommation humainef<strong>la</strong>con 1 l, 2.5 lR/1.3.4 Médicaments injectables et à usage oral contenant des substancesantiparasitaires actives contre les ecto- et les endoparasites1.3.4.1 Lactones macrocycliquesVoir 1.3.3.1. Les formu<strong>la</strong>tions injectablesne sont pas indiquées pour letraitement de <strong>la</strong> gale chorioptique.L’absorption lente <strong>du</strong> principe actifimplique une présence prolongée decelui-ci au niveau <strong>du</strong> site d’injection.Il faut noter que l’usage de ces substanceschez des animaux qui ne sontpas repris parmi les espèces ciblesmentionnées dans <strong>la</strong> notice, représenteun risque, parfois majeur, particulièrementchez les chiens, parmilesquels certains indivi<strong>du</strong>s peuventmontrer une sensibilité importante.Rappelons aussi le risque environnementalque peuvent représenter cesprincipes actifs rejetés dans les matièresfécales. Ceci est également va<strong>la</strong>blepour les formu<strong>la</strong>tions «pour-on».DoramectineLMR doramectine : DECTOMAX 10 mg/ml sol inj porc (Eli Lilly)doramectine: 10 mg/mlsolution injectable imPosologie:Su: 0,3 mg/kgViande + abats: 56 jf<strong>la</strong>con 200, 500 mlR/DECTOMAX sol inj (Eli Lilly)doramectine: 10 mg/mlsolution injectable sc (Bo), im (Ov)Posologie:Bo, Ov: 1 x 0,2 mg/kgViande et abats: Bo: 56 j, Ov: 70 jNe pas administrer aux Bo ou Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, ni 60 j (Bo)ou 70 j (Ov) avant <strong>la</strong> mise basf<strong>la</strong>con 50 ml, 200 ml, 500 mlR/
62 1 MEDICAMENTS ANTIPARASITAIRESDECTOMAX sol inj (Wirtz)doramectine: 10 mg/mlsolution injectable sc (Bo), im (Ov)Posologie:Bo, Ov: 1 x 0,2 mg/kgViande et abats: Bo: 56 j, Ov: 70 jNe pas administrer aux Bo ou Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, ni 60 j (Bo)ou 70 j (Ov) avant <strong>la</strong> mise basf<strong>la</strong>con 200 mlR/parIvermectineLMR ivermectine : BOVIMEC B (Cross Vetpharm Group)ivermectine: 10 mg/mlsolution injectable scPosologie:Bo: 200 mcg/kgViande: 49 jNe pas utiliser chez les vaches <strong>la</strong>itières, <strong>du</strong>rant<strong>la</strong> <strong>la</strong>ctation ou le tarissement, lorsque le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineNe pas utiliser chez les génisses gestantesdans les 60 j précédant le vê<strong>la</strong>gef<strong>la</strong>con 500 mlR/ECOMECTIN 6 mg/g poudre (Eco A.H.)ivermectine: 6 mg/gpoudre poPosologie:Su: 0,1 mg/kg PV pj (7 j)Viande: 12 jpoudre 333 gR/ECOMECTIN 6 mg/g premix (Eco A.H.)ivermectine: 6 mg/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 0,1 mg/kg PV pj (7 j)Viande: 12 jprém méd 5 kgR/premixECOMECTIN 10 mg/ml (Eco A.H.)ivermectine: 10 mg/mlsolution injectable scPosologie:Bo, Ov: 1 x 200 mcg/kgSu: 1 x 300 mcg/kgOv (Psoroptes ovis): 2 x 200 mcg/kg à 7 jd’intervalleViande: Bo: 49 j, Ov: 42 j , Su: 28 jNe pas administrer aux Ov ou Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ou dansles 60 j avant <strong>la</strong> mise basf<strong>la</strong>con 200 ml, 500 mlR/EQVALAN (Merial)ivermectine: 18,7 mg/gpâte poPosologie:Eq, pou<strong>la</strong>in: 0,2 mg/kgViande: 16 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 20 x 6,42 gR/ERAQUELL (Virbac)ivermectine: 18,7 mg/gpâte poPosologie:Eq: 1 x 200 mcg/kg (intervalle de 30 j minentre 2 admin)Viande: 30 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainepâte 1 ou 48 x 7,49 gR/ERAQUELL TABS (Virbac)ivermectine: 20 mg/comprcomprimé à croquer poPosologie:Eq (âge > 2 sem): 200 mcg/kgViande et abats: 35 jcompr 1 x 8R/FUREXEL IVERMECTINE (Merial)ivermectine: 1,87 g/100 gpâte poPosologie:Eq, pou<strong>la</strong>in: 0,2 mg/kgViande: 14 jNe pas utiliser chez les juments pro<strong>du</strong>isant <strong>du</strong><strong>la</strong>it pour <strong>la</strong> consommation humaineapplic 6,42 gR/IVERMAX 18,7 mg/g pâte orale chevaux (Eco A.H.)ivermectine: 18,7 mg/gpâte poPosologie:Eq: 200 mcg/kgViande: 34 jLait: ne pas administrer aux juments dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humaineseringue 7,49 gR/IVOMEC 1 % (Merial)ivermectine: 10 mg/mlsolution injectable scPosologie:Bo, veau, Ov, agneau: 0,2 mg/kgTraitement Psoroptes: 2 inj à 7 j d’intervalleViande: Bo: 49 j, Ov: 22 jNe pas administrer aux Bo ou Ov dans les 60 javant <strong>la</strong> parturition, si le <strong>la</strong>it est destiné à <strong>la</strong>consommation humainef<strong>la</strong>con 50 ml, 200 mlR/IVOMEC poudre orale 0,6 % (Merial)ivermectine: 0,6 %poudre po avec l’alimentationPosologie:Su (< 100 kg PV): 0,1 mg/kg pj (7 j)Viande: 12 jpoudre 333 gR/IVOMEC V/P (Merial)ivermectine: 10 mg/mlsolution injectable scPosologie:Su, porcelet: 0,3 mg/kgViande: 14 jf<strong>la</strong>con 200 mlR/
1 MEDICAMENTS ANTIPARASITAIRES63MAXIMEC pâte orale chevaux, 18.7 mg/g (CrossVetpharm Group)ivermectine: 18,7 mg/gpâte poPosologie:Eq: 0,2 mg/kgViande: 21 jNe pas administrer aux juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 6,42 gR/NOROMECTIN 1,87% oral paste for horses(Norbrook Lab)ivermectine: 18,7 mg/gpâte poPosologie:Eq: 1 x 200 mcg/kgViande: 34 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineseringue 1 ou 10 x 7,49 gR/NOROMECTIN inj (Norbrook Lab)ivermectine: 1,0 % g/vsolution injectable scPosologie:Bo: 200 mcg/kgSu: 300 mcg/kgViande: Bo: 49 j, Su: 18 jNe pas administrer aux Bo pendant <strong>la</strong> <strong>la</strong>ctationou le tarissement si le <strong>la</strong>it est destiné à <strong>la</strong>consommation humaine ou aux génisses dansles 60 j avant <strong>la</strong> mise basf<strong>la</strong>con 50 ml, 250 ml, 500 ml, 1 lR/NOROMECTIN premix (Norbrook Lab)ivermectine: 0.6g/100gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 0,1 mg/kg pj (7 j)Viande et abats: 12 jsac 5 kgR/premixPORCIMEC P (Cross Vetpharm Group)ivermectine: 10 mg/mlsolution injectable scPosologie:Su: 300 mcg/kgViande: 28 jf<strong>la</strong>con 500 mlR/VIRBAMEC 1% (Virbac de Portugal Lab.)ivermectine: 10 mg/mlsolution injectable scPosologie:Bo, Ov: 0,2 mg/kgSu: 0,3 mg/kgViande: Bo: 49 j, Su: 35 j, Ov: 45 jNe pas administrer aux Bo et Ov dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 ml, 200 ml, 500 ml, 1 lR/MoxidectineLMR moxidectine : CYDECTIN 0,1 % sol orale ovins (Pfizer A.H.)moxidectine: 1 mg/mlsolution poPosologie:Ov: 200 mcg/kg (1 ml/5 kg)Viande: 14 j, Lait: 5 jf<strong>la</strong>con 1 lR/CYDECTIN 1 % (Pfizer A.H.)moxidectine: 10 mg/mlsolution injectable scPosologie:Bo, veau (> 8 sem):0,2 mg/kg (1 ml/50 kg)Viande: 65 jNe pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, à l’usagein<strong>du</strong>striel ou 60 j avant le vê<strong>la</strong>gef<strong>la</strong>con 50 ml, 200 ml, 500 mlR/CYDECTIN 10% LA (Pfizer A.H.)moxidectine: 100 mg/mlsolution injectable sc dans l’oreillePosologie:Bo (> 100 kg et < 500 kg): 1 mg/kgViande: 108 jNe pas administrer aux Bo dont le <strong>la</strong>it est destinéà <strong>la</strong> consommation humaine ou à un usagein<strong>du</strong>striel ni dans les 80 j précédant le vê<strong>la</strong>gef<strong>la</strong>con 50 ml, 200 mlR/EQUEST gel oral (Pfizer A.H.)moxidectine: 18,92 mg/ggel poPosologie:Eq, poney (âge > 4 m): 1 x 400 mcg/kgViande: 32 japplic 12,2 gR/1.3.4.2 AssociationsIvermectine + clorsulonLes associations thérapeutiques é<strong>la</strong>rgissentle spectre déjà très <strong>la</strong>rge. Ilfaut être conscient que l’ivermectineet les autres <strong>la</strong>ctones macrocycliquesne peuvent être utilisées contre l’hypodermede début décembre à débutmars.Ivermectine: voir chapitres 1.3.3.1 et1.3.4.1IndicationsLe clorsulon n’est actif que sur lesdouves <strong>du</strong> foie a<strong>du</strong>ltes.PharmacodynamieLe clorsulon inhibe les enzymes de <strong>la</strong>glycolyse chez le parasite. Il est inactifcontre les stades immatures de <strong>la</strong>douve <strong>du</strong> foie.
64 1 MEDICAMENTS ANTIPARASITAIRESPharmacocinétiqueLe clorsulon est rapidement résorbéaprès administration orale (tmax Bo =4 h).Effets indésirablesL’usage oral <strong>du</strong> clorsulon chez lesovins et les bovins est sûr. Un usagenormal ne devrait pas engendrer d’effetssecondaires.InteractionsAucune interaction connue.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’usage de clorsulon chez les animauxgestants ou al<strong>la</strong>itants est considérécomme sûr.LMR ivermectine + clorsulon : IVOMEC F (Merial)ivermectine: 10 mg/mlclorsulon: 100 mg/mlsolution injectable scPosologie:Bo, veau:0,2 mg d’I/kg + 2 mg de C/kgViande: 66 jNe pas administrer aux vaches dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ou 60 javant le vê<strong>la</strong>gef<strong>la</strong>con 50 ml, 200 ml, 500 mlR/LEVATUM SUPER (Chanelle)ivermectine: 10 mg/mlclorsulon: 100 mg/mlsolution injectable scPosologie:Bo: 200 mcg d’I + 2 mg de C/kgViande et abats : 66 jLait: ne pas utiliser chez les animaux dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humaineNe pas utiliser chez les vaches <strong>la</strong>itières hors<strong>la</strong>ctation, y compris chez les génisses gestantes,dans les 60 j précédant <strong>la</strong> mise-bascontainer 250 ml, 500 mlR/VIRBAMEC F (Virbac)ivermectine: 10 mg/mlclorsulon: 100 mg/mlsolution injectable scPosologie:Bo: 1 x 0,2 mg d’I + 2 mg de C/kgViande: 66 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine ou auxgénisses dans les 60 j avant le vê<strong>la</strong>gef<strong>la</strong>con 200 ml, 500 mlR/Ivermectine + closantelLes associations sont utilisées pouré<strong>la</strong>rgir un spectre d’action déjà <strong>la</strong>rge.Rappelons que l’ivermectine et les autres<strong>la</strong>ctones macrocycliques ne peuventpas être utilisées contre Hypodermaentre début décembre et début mars.Ivermectine, voir chapitres 1.3.3.1 et1.3.4.1; closantel, voir chapitre 1.3.1.7.LMR ivermectine + closantel : CLOSAMECTIN sol inj bovins (Norbrook Lab)ivermectine: 5 mg/mlclosantel (sodium dihydrate): 125 mg/mlsolution injectable scPosologie:Bo: 200 mcg d’I/kg + 5 mg de C/kgViande et abats: 49 jNe pas administrer aux animaux dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humaine, ni enpériode de tarissement ni aux Bo dans les 60 javant <strong>la</strong> mise basf<strong>la</strong>con 100 ml, 250 ml, 500 mlR/CLOSAMECTIN sol inj ovins (Norbrook Lab)ivermectine: 5 mg/mlclosantel (sodium dihydrate): 125 mg/mlsolution injectable scPosologie:Ov: 200 mcg d’I/kg + 5 mg de C/kg (en casde gale, administrer 2e inject avec ivermectineseulement, dans les 7 j après 1e inject)Viande et abats: 28 jLait: ne pas administrer aux animaux dont le <strong>la</strong>itest destiné à <strong>la</strong> consommation humaine, y comprisles animaux gestants destinés à pro<strong>du</strong>ire<strong>du</strong> <strong>la</strong>it pour <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/Mébendazole + closantelLMR closantel + mébendazole : FLUKIVER COMBI (Eli Lilly)closantel (dihydrate de sodium): 50 mg/mlmébendazole: 75 mg/mlsuspension poPosologie:mouton, agneau: 10 mg de C/kg + 15 mgde M/kgViande et abats: 65 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/Moxidectine + praziquantelMoxidectine, voir chapitres 1.3.3.1et 1.3.4.1; praziquantel, voir chapitre1.3.1.6.Pour le traitement d’infestations avecdes cestodes, des nématodes et desarthropodes.LMR moxidectine + praziquantel : EQUEST PRAMOX (Pfizer A.H.)moxidectine: 19,5 mg/gpraziquantel: 121,8 mg/ggel poPosologie:Eq (âge > 6,5 m): 400 mcg de mox/kg + 2,5 mgde praz/kgViande: 64 j, Lait: ne pas administrer aux Eq<strong>la</strong>ctants dont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaineapplic 11.8 g (10 ou 20 par boîte)R/
1 MEDICAMENTS ANTIPARASITAIRES65Ivermectine + praziquantelIvermectine : voir chapitres 1.3.3.1 et1.3.4.1; praziquantel : voir chapitre1.3.1.6.Cette association ajoute au spectred’activité de l’ivermectine une activitécontre les cestodes.LMR ivermectine + praziquantel : EQUIMAX (Virbac)ivermectine: 18,7 mg/gpraziquantel: 140,30 mg/ggel poPosologie:Eq (âge > 2 sem): 1 x 200 mcg d’I/kg + 1,5 mgde P/kgViande: 35 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 1 ou 48 x 7,49 gR/EQUIMAX tabs (Virbac)ivermectine: 20 mg/comprpraziquantel: 150 mg/comprcomprimé à croquer poPosologie:Eq: 200 mcg d’I/kg + 1.5 mg de P/kgViande: 35 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainecompr 1x 8R/EQVALAN DUO (Merial)ivermectine: 15,5 mg/gpraziquantel: 77,5 mg/gpâte poPosologie:Eq: 1 x 200 mcg d’I/kg + 1 mg de P/kgViande: 30 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 20 x 7,74 gR/1.3.5 Médicaments injectables et à usage oral contenant des substancesantiparasitaires actives contre les ectoparasites1.3.5.1 Régu<strong>la</strong>teurs de croissanceLufénuroneIndicationsLes régu<strong>la</strong>teurs de croissance n’ontaucun effet sur <strong>la</strong> puce a<strong>du</strong>lte maisbien sur les œufs de celle-ci. Le lufénuronesous forme injectable a une <strong>du</strong>réed’activité de 6 mois. Il est conseilléde commencer le traitement un moisavant <strong>la</strong> saison des puces puis de traiterl’animal en fonction des dé<strong>la</strong>is indiquésdans <strong>la</strong> notice.PharmacodynamieCertaines substances sont capablesd’interférer avec le développement desformes <strong>la</strong>rvaires immatures. On trouvedans cette catégorie des inhibiteursde <strong>la</strong> synthèse de chitine comme lelufénurone appartenant à <strong>la</strong> famille desbenzoylurées et actif contre les puces.Il inhibe <strong>la</strong> synthèse de l’exosqueletteconstitué de chitine. La pro<strong>du</strong>ctiond’œufs de <strong>la</strong> puce n’est pas influencéeen soi, mais le lufénurone ingéré par lespuces femelles pendant le repas sanguindans l’animal traité endommagede manière transovarienne les œufs endéveloppement. Le lufénurone qui seretrouve en abondance dans les fècesde <strong>la</strong> puce, est ingéré par <strong>la</strong> <strong>la</strong>rve avecdes conséquences néfastes pour leparasite.PharmacocinétiqueAprès injection sous-cutanée chez lechat, les taux p<strong>la</strong>smatiques actifs sontatteints après 21 jours. Le lufénurone,non métabolisé, est excrété par <strong>la</strong> bile.Contre-indicationsNe pas administrer les formules injectablesde lufénurone aux chiens (réactionvis-à-vis de l’adjuvant).Effets indésirablesLe lufénurone est bien toléré. Dansde rares cas, de <strong>la</strong> léthargie survientaprès injection. Un gonflement local etmomentané peut apparaître au niveau<strong>du</strong> site d’injection.InteractionsLe lufénurone peut être combiné avecd’autres insecticides (a<strong>du</strong>lticides).Repro<strong>du</strong>ction et <strong>la</strong>ctationLe lufénurone peut être administré auxfemelles gestantes ou al<strong>la</strong>itantes. Dansce dernier cas, les chiots et les chatonssont protégés via le <strong>la</strong>it de leurmère traitée.LMR lufénurone : PROGRAM 40 (Novartis)lufénurone: 40 mgsuspension injectable scPosologie:Fe (< 4 kg PV): 10 mg/kgpuces: 6 mseringue 0,4 mlR/
66 1 MEDICAMENTS ANTIPARASITAIRESPROGRAM 80 (Novartis)lufénurone: 80 mgsuspension injectable scPosologie:Fe (> 4 kg PV): 10 mg/kgpuces: 6 mseringue 0,8 mlR/1.3.5.2 SpinosadIndications – spectre d’activité -résistanceTraitement et prévention des infestationspar les puces (Ctenocephalidesfelis) chez le chien. Le médicament doitêtre administré pendant ou immédiatementaprès l’ingestion de nourriture.PharmacodynamieLe spinosad est principalement composé(90 %) de spinosyne A et despinosyne D. Ces spinosynes sontingérées par <strong>la</strong> puce a<strong>du</strong>lte pendantle repas sanguin. La spinosyne activeles récepteurs de l’acétylcholine despuces, entraînant ainsi des contractionset des tremblements muscu<strong>la</strong>ires,<strong>la</strong> prostration, <strong>la</strong> paralysie et<strong>la</strong> mort rapide des puces. Toutes lespuces meurent après 4 heures environ.PharmacocinétiqueLes spinosynes A et D sont rapidementabsorbées et <strong>la</strong>rgement distribuéeschez les chiens. La biodisponibilitéorale est d’environ 70 %. Le Tmax desspinosynes A et D est compris entre 2et 4 heures et <strong>la</strong> demi-vie d’éliminationmoyenne est comprise entre respectivement127,5 et 162,6 heures et 101,3et 131,9 heures. L’aire sous <strong>la</strong> courbe(AUC) et les valeurs de Cmax sont plusfaibles chez les chiens à jeun et augmententquasi linéairement en fonctiondes doses administrées au-delà desdoses thérapeutiques. Par conséquent,il est recommandé d’administrerle pro<strong>du</strong>it pendant les repas. Lesprincipaux métabolites biliaires, fécauxet urinaires chez les rats et les chiensont été identifiés sous <strong>la</strong> forme de spinosynesdéméthylées ou conjuguéesau glutathion. L’élimination s’effectueessentiellement par <strong>la</strong> bile et les fèces,et dans une moindre mesure par lesurines. Chez les chiennes al<strong>la</strong>itantes,le spinosad est excrété dans le colostrumou le <strong>la</strong>it.Contre-indicationsNe pas administrer aux chiens âgés demoins de 14 semaines ou aux chienspesant moins de 3,9 kg.Effets indésirablesLes vomissements représentent l’effetindésirable le plus fréquemmentobservé et surviennent généralementdans les 48 heures suivant l’administration.L’incidence de vomissementss’élève à 5 % environ, et augmente encas de surdosage. Les vomissementsétant transitoires, ils ne nécessitentgénéralement pas de traitement symptomatique.D’autres effets indésirablesont également été rapportés dans detrès rares cas : léthargie, anorexie,diarrhée, ataxie et convulsions.InteractionsLe spinosad étant un substrat de <strong>la</strong>glycoprotéine P ou PGP, il est doncsusceptible d’interagir avec d’autressubstrats, in<strong>du</strong>cteurs ou inhibiteurs de<strong>la</strong> PGP, tels que <strong>la</strong> doxorubicine (cytostatiqueà usage humain), <strong>la</strong> digoxine,<strong>la</strong> ciclosporine, <strong>la</strong> dexaméthasone.L’utilisation concomitante avec del’ivermectine peut entraîner des symptômesnerveux (tremblements, ataxie,convulsions, salivation, mydriase,cécité).Précautions particulièresAdministrer le médicament avec l’alimentationou immédiatement après lerepas. La prudence est recommandéeen cas d’utilisation chez des chiensépileptiques.Repro<strong>du</strong>ction et <strong>la</strong>ctationOn n’a pas observé d’effets tératogènes,foetotoxiques ou maternotoxiqueschez les animaux de<strong>la</strong>boratoire. On n’a pas constaté d’effetssur <strong>la</strong> repro<strong>du</strong>ction chez les mâleset les femelles. L’innocuité <strong>du</strong> spinosadn’a pas été suffisamment étudiéechez les chiens. Le spinosad étantexcrété dans le colostrum et le <strong>la</strong>it etson innocuité pour les chiots al<strong>la</strong>itésn’ayant pas été établie avec certitude,le médicament ne doit être utilisé chezles chiennes al<strong>la</strong>itantes qu’après évaluationbénéfice/risque.LMR spinosad COMFORTIS 270 mg compr à croquer chien etchat (Eli Lilly)spinosad: 270 mgcomprimé à croquer poPosologie:Ca (âge > 14 sem): 45-70 mg/kgFe (âge > 14 sem): 50-75 mg/kgcompr 6R/
1 MÉDICAMENTS ANTIPARASITAIRES 67COMFORTIS 425 mg compr à croquer chien etchat (Eli Lilly)spinosad: 425 mgcomprimé à croquer poPosologie:Ca (âge > 14 sem): 45-70 mg/kgFe (âge > 14 sem): 50-75 mg/kgcompr 6R/COMFORTIS 665 mg compr à croquer chien(Eli Lilly)spinosad: 665 mgcomprimé à croquer poPosologie:Ca (âge > 14 sem): 45-70 mg/kgcompr 6R/COMFORTIS 1040 mg compr à croquer chien(Eli Lilly)spinosad: 1040 mgcomprimé à croquer poPosologie:Ca (âge > 14 sem): 45-70 mg/kgcompr 6R/COMFORTIS 1620 mg compr à croquer chien(Eli Lilly)spinosad: 1620 mgcomprimé à croquer poPosologie:Ca (âge > 14 sem): 45-70 mg/kgcompr 6R/1.3.6 Médicaments à usage topique contenant des substances antiparasitairesactives contre les ectoparasitesLes préparations c<strong>la</strong>ssées dans cette rubrique sont utilisées pour le traitementlocal des ectoparasites intoxiqués suite à un contact direct avec <strong>la</strong> substanceactive. Par conséquent, elles sont reprises dans le chapitre des médicaments àusage dermatologique (voir chapitre 12.1.3).
2 MÉDICAMENTS DU SYSTÈME HORMONAL 692. MÉDICAMENTS DU SYSTÈME HORMONALL’utilisation de ces substances chez les animaux pro<strong>du</strong>cteurs de denrées alimentairesest fixée par <strong>la</strong> Loi <strong>du</strong> 15 juillet 1985 re<strong>la</strong>tive à l’utilisation de substancesà effet hormonal, à effet antihormonal, à effet beta-adrénergique ou à effetstimu<strong>la</strong>teur de pro<strong>du</strong>ction chez les animaux. L’interdiction de ces substancesest érigée en principe de base. L’usage de certaines substances chez quelquesespèces animales pour des indications précises est autorisé par dérogation. Danscette loi, une distinction est faite entre le traitement thérapeutique et le traitementzootechnique.2.1 Hormones sexuelles et autres médicaments<strong>du</strong> système repro<strong>du</strong>cteur2.1.1 ŒstrogènesLes œstrogènes naturels, l’œstrone, l’œstradiol, et l’œstriol sont, suivant lesespèces, synthétisés au niveau des ovaires, des testicules, des surrénales et <strong>du</strong>p<strong>la</strong>centa. Il existe aussi des composés synthétiques, comme le valérate ou cypionated’œstradiol, le DES (diethyl stilbœstrol) et d’autres encore. En Belgique,un seul médicament à base d’œstrogènes est enregistré pour le traitement del’incontinence urinaire chez <strong>la</strong> chienne ovario-hystérectomisée (voir chapitre 9.1).2.1.2 ProgestagènesLes molécules possédant une activité progestative sont soit d’origine naturelle,comme <strong>la</strong> progestérone, soit d’origine synthétique, dérivées de <strong>la</strong> progestéroneou de <strong>la</strong> 17-hydroxyprogestérone. Enfin, certaines proviennent de <strong>la</strong> testostéroneou de <strong>la</strong> nortestostérone, auxquelles des radicaux substitués confèrent une activitéhautement progestative (altrénogest).IndicationsChevauxLes indications pour l’administration d’altrénogest (allyl-trenbolone) dans cetteespèce animale sont <strong>la</strong> synchronisation et l’in<strong>du</strong>ction des chaleurs.BovinsUne spirale vaginale contenant de <strong>la</strong> progestérone peut être administrée chez lesvaches cyclées pour <strong>la</strong> synchronisation de l’œstrus. La spirale peut être p<strong>la</strong>cée 35jours minimum après le vê<strong>la</strong>ge puis retirée après 7 jours. Afin de garantir l’in<strong>du</strong>ction del’œstrus chez tous les animaux traités, le traitement de progestérone doit être accompagnéd’une injection de prostag<strong>la</strong>ndine 24 heures avant l’enlèvement de <strong>la</strong> spirale.PorcsLes indications reconnues pour l’altrénogest dans cette espèce animale sont:- <strong>la</strong> synchronisation de l’œstrus chez les cochettes cyclées. L’administrationd’altrénogest dans l’alimentation, pendant 18 jours, aboutit, 5 à 6 jours aprèsl’arrêt <strong>du</strong> traitement, à des chaleurs fertiles.- <strong>la</strong> synchronisation de l’œstrus chez des truies primipares. Si l’altrénogest estadministré via l’alimentation <strong>du</strong>rant trois jours à partir <strong>du</strong> sevrage, des chaleursfertiles se pro<strong>du</strong>isent quelques jours après l’arrêt <strong>du</strong> traitement. A <strong>la</strong> mise bas quisuivra, le nombre de jeunes nés vivants peut également être augmenté.Petits ruminantsAucun médicament n’est disponible.CarnivoresLes indications sont :- <strong>la</strong> prévention et <strong>la</strong> suppression de l’œstrus. Il est recommandé de pratiquer <strong>la</strong>suppression de l’œstrus <strong>du</strong>rant les 2 ou 3 premiers jours des chaleurs ; <strong>la</strong> préventionde l’œstrus devant débuter <strong>du</strong>rant l’anœstrus et au plus tard un moisavant <strong>la</strong> date présumée des chaleurs.
702 MÉDICAMENTS DU SYSTÈME HORMONAL- le traitement de l’hypertrophie prostatique. Les progestagènes à activité anti-androgéniquecomme l’acétate de delmadinone sont capables d’in<strong>du</strong>ire une involutionrapide de <strong>la</strong> g<strong>la</strong>nde prostatique. Idéalement, leur emploi sera limité à uneou deux administrations suivies par l’utilisation à long terme d’un inhibiteur de <strong>la</strong>5-alpha-ré<strong>du</strong>ctase, chez les animaux de repro<strong>du</strong>ction pour lesquels <strong>la</strong> castrationn’est pas envisageable. Ce type d’inhibiteur inhibe les effets de <strong>la</strong> testostérone sur<strong>la</strong> prostate tout en conservant une libido et un comportement repro<strong>du</strong>cteur normal.Lorsque les progestagènes sont utilisés chez le mâle pour cette indication, defortes doses doivent être administrées si un effet significatif est recherché.- l’hypersexualité et certaines formes d’agressivité vu l’activité anti-androgéniquemarquée de l’acétate de delmadinone. (Voir aussi Folia Veterinaria 2007, n°1 et2010, n°3).PharmacodynamieLa progestérone est naturellement pro<strong>du</strong>ite au niveau <strong>du</strong> corps jaune mais aussides testicules et <strong>du</strong> p<strong>la</strong>centa chez certaines espèces. En prévenant <strong>la</strong> libérationde GnRH, les progestagènes empêchent l’ovu<strong>la</strong>tion. Ils stimulent également <strong>la</strong>prolifération de l’endomètre et inhibent les contractions de l’utérus.PharmacocinétiqueAdministrée per os, cette molécule naturelle subit, comme les œstrogènes naturels,un effet de premier passage hépatique important. La biodisponibilité desmolécules de synthèse est habituellement meilleure. L’administration parentéraleet vaginale est également possible. La progestérone se lie à différentes protéinesp<strong>la</strong>smatiques telles que l’albumine et <strong>la</strong> transcortine. L’importance de cette liaisonà des protéines transporteuses est variable d’une espèce à l’autre.Contre-indicationsLes progestagènes ne sont pas, de manière générale, administrés <strong>du</strong>rant <strong>la</strong>gestation mais ils peuvent parfois s’avérer utiles pour <strong>la</strong> prévention des mises basprématurées en supportant l’effet lutéal. Les progestatifs dérivés de molécules àpropriétés androgéniques ou anti-androgéniques sont contre-indiqués pendant<strong>la</strong> gestation. Administrés erronément <strong>du</strong>rant celle-ci, ils peuvent in<strong>du</strong>ire de <strong>la</strong>cryptorchidie chez les nouveau-nés, des anomalies de <strong>la</strong> différenciation sexuelle,des troubles <strong>du</strong> développement pondéral, ainsi qu’un retard voire une inhibitiontotale de <strong>la</strong> mise bas chez <strong>la</strong> mère. L’emploi des progestagènes injectables et delongue <strong>du</strong>rée d’action est, pour ces raisons, à proscrire <strong>du</strong>rant <strong>la</strong> gestation.Effets indésirablesLes progestagènes, généralement utilisés à des doses pharmacologiquescon<strong>du</strong>isant à des concentrations sériques supérieures aux taux physiologiques,in<strong>du</strong>isent des effets indésirables plus ou moins importants selon l’espèce animaleet les molécules utilisées, notamment liés à leurs effets sur le cortex surrénalien,le pancréas et l’utérus. Ainsi, ils peuvent provoquer de <strong>la</strong> prise de poids, une intoléranceau glucose, <strong>du</strong> diabète sucré et de l’hyperadrénocorticisme. Leur usageest déconseillé dans certains états pathologiques et physiologiques comme lediabète sucré, les tumeurs hormono-dépendantes et les infections de l’appareilrepro<strong>du</strong>cteur. Vu l’effet prédisposant de ces molécules aux infections utérineset aux pathologies tumorales, notamment au niveau mammaire, l’administrationrépétée et à long terme, comme celle mise en p<strong>la</strong>ce dans <strong>la</strong> prévention del’œstrus chez les petits animaux, doit se faire avec <strong>la</strong> prudence requise (voirFolia Veterinaria 2007 n° 1). Chez le mâle, l’utilisation répétée de fortes doses deprogestagènes pourrait compromettre <strong>la</strong> fertilité et le comportement repro<strong>du</strong>cteur.Enfin, lors d’utilisation continue, des cas de gynécomastie, de tumeur mammaireet d’apparition de sécrétions <strong>la</strong>ctées ont été décrits.InteractionsL’usage simultané de progestagènes avec des glucocorticoïdes peut aggraver <strong>la</strong>suppression adrénocorticale et le diabète sucré.Précautions particulières/Risques pour l’hommeLa notice d’un médicament à base d’allyl trenbolone (altrénogest) mentionne lesrisques de manipu<strong>la</strong>tion d’un tel médicament : les femmes enceintes ou en mesurede l’être, les personnes souffrant de tumeurs progestérone-dépendantes ou dema<strong>la</strong>dies thrombo-emboliques ne doivent pas manipuler ni administrer ce pro<strong>du</strong>it.Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir Contre-indications.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 712.1.2.1 Progestérone et dérivés de<strong>la</strong> progestéroneDelmadinone acétateLMR delmadinone acétate: TARDAK (Pfizer A.H.)delmadinone acétate: 10 mg/mlsuspension injectable sc, imPosologie:Ca, Fe: 1 - 2 mg/kgCa, Fe: mâle:- (< 10 kg PV): 1,5 - 2 mg/kg- (10 - 20 kg PV): 1 - 1,5 mg/kg- (> 20 kg PV): 1 mg/kgf<strong>la</strong>con 10 mlR/Mégestrol acétateLMR mégestrol acétate: CHRONOPIL (Ceva Santé Animale)mégestrol acétate: 2 mgcomprimé poPosologie:Fe: 2 mg/sem (max 12 m)compr 30R/MEGECAT (Vétoquinol)mégestrol acétate: 5 mgcomprimé poPosologie:Fe: 5 mg/14 j (max 12 m)compr 18R/Médroxyprogestérone acétateLMR médroxyprogestérone: DEPO-PROMONE 50 mg/ml (Pfizer A.H.)médroxyprogestérone acétate: 50 mg/mlsuspension stérile injectable scPosologie:Ca:- (< 45 kg PV): 50 mg- (> 45 kg PV): 75 - 100 mgFe: 50 mgf<strong>la</strong>con 5 mlR/SUPPRESTRAL (Vétoquinol)médroxyprogestérone acétate: 50 mg/mlsuspension injectable sc, imPosologie:Ca: 50 - 100 mgFe: 50 mgf<strong>la</strong>con 5 mlR/ProligestoneLMR proligestone : DELVOSTERON (MSD A.H.)proligestone: 100 mg/mlsuspension injectable scPosologie:Ca:(< 5 kg PV): 30 mg/kg(5 - 10 kg PV): 30-25 mg/kg(10 - 20 kg PV): 25-17,5 mg/kg(20 - 30 kg PV): 17,5-15 mg/kg(30 - 40 kg PV): 15-12 mg/kg(> 45 kg PV): 12 mg/kgFe: 30 mg/kgf<strong>la</strong>con 20 mlR/ProgestéroneLMR progestérone: CIDR (Pfizer A.H.)progestérone: 1,38 mgdispositif à usage intravaginalPosologie:Bo: 1,38 g/animal (7 j)Viande: 0 j, Lait: 0 jLe <strong>la</strong>it peut être utilisé pour <strong>la</strong> consommationhumaine pendant le traitementapplic 10R/PRID DELTA (Ceva Santé Animale)progestérone: 1,55 g/dispositifdispositif à usage intravaginalPosologie:Bo (min 35 j après le vê<strong>la</strong>ge):1,55 g/animal (7 j)admin une prostag<strong>la</strong>ndine 24 h avant l’enlèvement<strong>du</strong> dispositif chez les Bo cyclées,chez les Bo non cyclées injecter aussi del’eCG (ou bien PMSG) lors <strong>du</strong> retrait <strong>du</strong>dispositifViande et abats: 0 j, Lait: 0 j, Viande et <strong>la</strong>itpeuvent être délivrés pour <strong>la</strong> consommationhumaine <strong>du</strong>rant <strong>la</strong> période de traitementdispositif 10 x 1R/2.1.2.2 Dérivés d’androgènes àactivité progestativeLMR altrénogest: ALTRESYN 4 mg/ml (Ceva Santé Animale)altrénogest: 4 mg/mlsolution poPosologie:Su (truie nullipare cyclée):20 mg/animal pj (18 j)Viande et abats: 9 jf<strong>la</strong>con 540 ml, 1080 mlR/
722 MÉDICAMENTS DU SYSTÈME HORMONALREGUMATE 4 mg/ml sol po porcs (MSD A.H.)altrénogest: 4 mg/mlsolution po avec l’alimentationPosologie:Su:- truie primipare: 5 ml pj (3 j)- cochette cyclée: 5 ml pj (18 j)Viande: 9 jf<strong>la</strong>con 360 ml, 1 lR/VIRBAGEST (Virbac)altrénogest: 4 mg/mlsolution po avec l’alimentationPosologie:cochette cyclée:20 mg d’altrénogest/animal pj (18 j)Viande et abats: 9 jf<strong>la</strong>con 450 ml, 900 mlR/REGUMATE EQUINE (MSD A.H.)altrénogest: 2,20 mg/mlsolution po (avec l’alimentation)Posologie:Eq: 0,044 mg/kg pj (10 j)Viande et abats: 9 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 150 mlR/2.1.3 Médicaments en cas d’hypertrophie bénigne de <strong>la</strong> prostate2.1.3.1 OsatéroneIndicationsL’osatérone, stéroïde anti-androgène,est indiquée dans le traitement del’hyperp<strong>la</strong>sie bénigne de <strong>la</strong> prostate(HBP) chez les chiens mâles, visant àré<strong>du</strong>ire le volume de <strong>la</strong> prostate et de<strong>la</strong> sorte, les symptômes cliniques quiy sont liés.PharmacodynamieL’acétate d’osatérone, ainsi que sonmétabolite pharmacologiquement actif,ont une activité progestative et anti-androgènepuissante. Ils inhibent leseffets in<strong>du</strong>its par un excès de testostérone,empêchent de façon compétitive<strong>la</strong> fixation des androgènes à leursrécepteurs prostatiques et bloquentle passage de <strong>la</strong> testostérone dans <strong>la</strong>prostate. L’acétate d’osatérone a égalementune activité glucocorticoïde.PharmacocinétiqueAprès une administration orale avec <strong>la</strong>nourriture, l’acétate d’osatérone est rapidementabsorbé (Tmax environ 2 h) etsubit une première métabolisation dansle foie. L’acétate d’osatérone est transforméen un métabolite pharmacologiquementactif. L’acétate d’osatéroneet son métabolite se fixent à l’albuminep<strong>la</strong>smatique (respectivement environ90% et 80%). Cette fixation est réversibleet n’est pas affectée par d’autressubstances connues pour leur fixationspécifique à l’albumine. L’osatéroneest principalement éliminée via lesfèces par le biais de l’excrétion biliaire(60%) et, dans une moindre mesure, vial’urine (25%). L’élimination est lente (T½80 h). Après une administration répétéed’actétate d’osatérone à raison de 0,25mg/kg/jour pendant 7 jours, le facteurd’accumu<strong>la</strong>tion est environ de 3-4 sansqu’il y ait un changement dans le tauxd’absorption ou d’élimination. Quinzejours après <strong>la</strong> dernière administration, <strong>la</strong>concentration moyenne dans le p<strong>la</strong>smaest d’environ 6,5 µg/l.Contre-indicationsChiens stressés ou présentant unhypoadrénocorticisme, et chiens souffrantde troubles hépatiques : voir« Précautions particulières ».Effets indésirablesUne augmentation passagère de l’appétitest très fréquente. Des changementspassagers <strong>du</strong> comportementtels qu’une augmentation ou unebaisse de l’activité, ou un comportementplus social, sont courants.D’autres réactions, tels que des vomissementset/ou de <strong>la</strong> diarrhée transitoires,de <strong>la</strong> polyurie/polydipsie, de <strong>la</strong>léthargie, ou un syndrome de féminisation,y compris une hyperp<strong>la</strong>sie de<strong>la</strong> g<strong>la</strong>nde mammaire, se pro<strong>du</strong>isentrarement.Une baisse transitoire <strong>du</strong> cortisolp<strong>la</strong>smatique survient chez <strong>la</strong> plupartdes animaux traités. Dans les essaiscliniques, le traitement avec ce médicamentn’a pas été interrompu et tousles chiens se sont rétablis sans aucuntraitement spécifique.InteractionsChez les chiens présentant uneHBP associée à une prostatite, il est
2 MÉDICAMENTS DU SYSTÈME HORMONAL 73possible d’administrer ce pro<strong>du</strong>itsimultanément avec des pro<strong>du</strong>itsantibactériens.Précautions particulières/Risquespour l’hommeA utiliser avec précaution chez leschiens ayant des antécédents de ma<strong>la</strong>diehépatique étant donné que l’utilisation<strong>du</strong> pro<strong>du</strong>it chez ces chiens n’apas été étudiée de manière approfondieet que le traitement de certains chienssouffrant de troubles hépatiques a entraîné,au cours des essais cliniques,une augmentation réversible de l’ALTet de l’ALP. La concentration <strong>du</strong> cortisoldans le p<strong>la</strong>sma peut diminuer defaçon transitoire et jusqu’à quelquessemaines après l’administration <strong>du</strong>médicament. Il convient de bien surveillerles chiens stressés, notammentaprès une intervention chirurgicale, ouceux atteints d’hypoadrénocorticisme.La réponse normale à un test de stimu<strong>la</strong>tionà l’ACTH peut également êtresupprimée pendant plusieurs semainesaprès l’administration d’osatérone.Chez des animaux de <strong>la</strong>boratoire femelles,l’acétate d’osatérone a causédes effets indésirables sérieux sur lesfonctions repro<strong>du</strong>ctives. Les femmesen âge d’avoir des enfants doiventdonc éviter tout contact avec ce pro<strong>du</strong>itou porter des gants jetables lorsde l’administration.Repro<strong>du</strong>ction et <strong>la</strong>ctationCertaines études cliniques chez leschiens mâles ont montré une ré<strong>du</strong>ction<strong>du</strong> nombre de spermatozoïdes,sans influence négative sur <strong>la</strong> qualité<strong>du</strong> sperme. D’autres études n’ont enrevanche constaté aucun changementdans <strong>la</strong> qualité <strong>du</strong> sperme.LMR osatérone: YPOZANE 1,875 mg, 3,75 mg, 7,5 mg et 15 mg(Virbac)osatérone (acétate):1,875 mg, 3,75 mg, 7,5 mg ou 15 mgcomprimé poPosologie:Ca (mâle): 1 x 0,25 - 0,5 mg/kg pj (7 j)compr 7R/2.1.3.2 Delmadinone acétateL’acétate de delmadinone est indiquédans le traitement de l’hypertrophieprostatique. Les progestagènesà activité anti-androgénique commel’acétate de delmadinone sont capablesd’in<strong>du</strong>ire une involution rapidede <strong>la</strong> g<strong>la</strong>nde prostatique. Idéalement,leur usage sera limité à une ou deuxadministrations suivies par l’utilisationà long terme d’un inhibiteur de<strong>la</strong> 5-alpha-ré<strong>du</strong>ctase, chez les animauxrepro<strong>du</strong>cteurs chez lesquels <strong>la</strong>castration n’est pas envisageable. Cetype d’inhibiteur inhibe les effets de<strong>la</strong> testostérone sur <strong>la</strong> prostate tout enconservant une libido et un comportementrepro<strong>du</strong>cteur normal. Lorsqueles progestagènes sont utilisés chezle mâle pour cette indication, de fortesdoses doivent être administrées si uneffet significatif est recherché. Voiraussi chapitre 2.1.2.LMR delmadinone acétate: TARDAK (Pfizer A.H.)delmadinone acétate: 10 mg/mlsuspension injectable sc, imPosologie:Ca, Fe: 1 - 2 mg/kgCa, Fe: mâle:- (< 10 kg PV): 1,5 - 2 mg/kg- (10 - 20 kg PV): 1 - 1,5 mg/kg- (> 20 kg PV): 1 mg/kgf<strong>la</strong>con 10 mlR/2.1.4 Stéroïdes anabolisants2.1.4.1 NandroloneIndicationsElle est utilisée dans les situations cliniquescaractérisées par un bi<strong>la</strong>n azoténégatif, par exemple des ma<strong>la</strong>diesdébilitantes, des traumatismes et desinterventions chirurgicales.PharmacodynamieLa nandrolone est un stéroïde anabolisantpossédant une faible activité virilisanteet une forte activité anabolisante.PharmacocinétiqueLes stéroïdes anabolisants exogènessont re<strong>la</strong>tivement résistants à <strong>la</strong> biotransformationhépatique. L’éliminations’étend sur plusieurs semaines.Contre-indicationsNe pas administrer aux animaux souffrantde pathologies hépatiques oud’hyperp<strong>la</strong>sie de <strong>la</strong> prostate, aux animauxgestants, repro<strong>du</strong>cteurs ou auxjeunes animaux.
742 MÉDICAMENTS DU SYSTÈME HORMONALEffets indésirablesRétention d’électrolytes (Na, Cl, K, Ca,P) et d’eau, hépatoxicité, troubles de<strong>la</strong> fertilité, anomalies fœtales comme<strong>la</strong> masculinisation, troubles <strong>du</strong> comportement,inhibition des p<strong>la</strong>ques decroissance chez les jeunes animaux.InteractionsDes interactions positives et négativessont décrites respectivement avec lesanticoagu<strong>la</strong>nts et l’insuline. Des adaptationsposologiques et une surveil<strong>la</strong>ncedes pathologies traitées avecces molécules est nécessaire.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation en période de gestationn’est pas recommandée. Aucune donnéen’est connue sur une éliminationéventuelle via le <strong>la</strong>it.LMR nandrolone: LAURABOLIN (MSD A.H.)nandrolone <strong>la</strong>urinate: 25 mg/mlsolution injectable sc, imPosologie:Ca, Fe: 1 mg/kg (max. 25 mg)f<strong>la</strong>con 5 mlR/2.1.5 Gonadotrophines et médicaments agissant sur leur libérationLa stimu<strong>la</strong>tion des gonades mâles et femelles repose sur <strong>la</strong> gonadolibérine d’originehypotha<strong>la</strong>mique ou ses dérivés (GnRH ou Gonadotropin Releasing Hormone,buséréline, gonadoréline, desloréline, peforéline) et sur les hormones gonadotropesou gonadotrophines sécrétées par l’antéhypophyse, à savoir: l’hormonelutéinisante ou LH et l’hormone folliculostimu<strong>la</strong>nte, encore appelée FSH. Deuxautres gonadotrophines, mais d’origine p<strong>la</strong>centaire, sont enregistrées en médecinevétérinaire: <strong>la</strong> PMSG (Pregnant Mare Serum Gonadotropin), maintenant appeléeeCG (equine Chorionic Gonadotropin) et l’hCG (human Chorionic Gonadotropin).IndicationsChevaux- Stimu<strong>la</strong>tion de <strong>la</strong> croissance follicu<strong>la</strong>ire et de l’ovu<strong>la</strong>tion. L’administration d’hCGà des juments en œstrus et chez lesquelles un des deux ovaires présente unfollicule d’au moins trois centimètres de diamètre aboutit, dans <strong>la</strong> plupart descas, à une ovu<strong>la</strong>tion dans les 48 heures. L’administration d’hCG paraît alorsraisonnable si on soupçonne que l’œstrus et <strong>la</strong> croissance d’un follicule serontanormalement longs ou si on ne désire inséminer une jument qu’une seule foisau cours de ce cycle. L’administration de GnRH donne de moins bons résultatsque l’hCG pour cette indication. Le manque d’information concernant le recoursà <strong>la</strong> PMSG chez <strong>la</strong> jument pour cette indication ne permet pas de recommanderson usage.BovinsChez le bovin, l’administration d’hCG et de GnRH est possible pour les mêmesindications. Les deux substances donnent des résultats comparables.- Traitement des follicules ovariens kystiques. L’administration de l’hCG aussi bienque de <strong>la</strong> GnRH provoque <strong>la</strong> lutéinisation <strong>du</strong> ou des kystes ou l’ovu<strong>la</strong>tion. Si letraitement réussit, un œstrus apparaît après 17 à 24 jours (reprise <strong>du</strong> cycle aprèslutéolyse <strong>du</strong> (des) corps jaune(s) in<strong>du</strong>its). Les deux pro<strong>du</strong>its agissent aussi biensur les kystes follicu<strong>la</strong>ires que sur les lutéinisés.- In<strong>du</strong>ction de l’ovu<strong>la</strong>tion. Le recours à l’hCG ou à <strong>la</strong> GnRH, chez <strong>la</strong> vache enœstrus, permet le plus souvent l’ovu<strong>la</strong>tion dans les 24 heures. Cependant, étantdonné que les ovu<strong>la</strong>tions tardives (retardées) surviennent re<strong>la</strong>tivement rarementchez les bovins et qu’en outre, il n’est pas possible de savoir quelles vaches vontovuler tardivement, l’emploi de l’hCG ou de <strong>la</strong> GnRH ne doit pas être encouragépour une telle indication. Il est apparu également qu’une ovu<strong>la</strong>tion tardivesurvient plus ou moins au hasard et qu’elle peut ne plus survenir au cours del’œstrus suivant.- Augmentation de <strong>la</strong> probabilité d’une gestation après une insémination.Beaucoup d’expériences ont été réalisées avec l’hCG et <strong>la</strong> GnRH, administréesà différents moments après l’insémination, en vue d’augmenter le pourcentagede gestations chez les vaches traitées. Les résultats divergents de ces expériencesne permettent pas de conclure formellement à l’efficacité d’un tel traitement.Il est en tout cas certain qu’administrer ces substances à des vaches
2 MÉDICAMENTS DU SYSTÈME HORMONAL 75inséminées une ou deux fois suite à des chaleurs survenues après le part n’a pasde sens. L’utilité <strong>du</strong> traitement des vaches en « repeat breeding » par de l’hCGou de <strong>la</strong> GnRH n’est pas c<strong>la</strong>ire.La PMSG (eCG) est indiquée dans les cas suivants:- In<strong>du</strong>ction d’une superovu<strong>la</strong>tion. Dans le cadre des transp<strong>la</strong>ntations d’embryons,<strong>la</strong> PMSG (eCG) stimule le développement follicu<strong>la</strong>ire. Si ce pro<strong>du</strong>it est administréau bon moment, l’ovu<strong>la</strong>tion de plusieurs follicules est possible. Si l’animal ainsitraité est inséminé, il est possible de récupérer les embryons après 7 jours.La combinaison de FSH et de LH peut également être utilisée dans le cadrede l’in<strong>du</strong>ction d’une superovu<strong>la</strong>tion chez le bovin. Pour y parvenir, les animauxdoivent être traités deux fois par jour, pendant 4 jours, avec des doses décroissantes,respectant ainsi <strong>la</strong> physiologie.PorcsLes indications pour lesquelles l’usage de l’association d’hCG et de PMSG estreconnu chez le porc sont:- l’in<strong>du</strong>ction de l’œstrus chez <strong>la</strong> truie après le sevrage des porcelets. Cette associationstimule le développement des follicules ovariens. Dans <strong>la</strong> plupart descas, l’œstrus survient 3 à 7 jours après le traitement.- l’anœstrus. L’absence d’œstrus survient surtout chez <strong>la</strong> truie primipare. Uneinjection combinée d’hCG et de PMSG (eCG) in<strong>du</strong>it un œstrus fertile chez <strong>la</strong>plupart des animaux, après quelques jours.- <strong>la</strong> synchronisation de l’œstrus. Cette indication est moins évidente parce que ledegré de synchronisation obtenu est souvent faible.- l’in<strong>du</strong>ction de l’oestrus chez les cochettes après synchronisation avec un progestagène.L’insémination artificielle peut être réalisée 30 à 33 heures aprèsl’administration.- <strong>la</strong> subfertilité et le nombre ré<strong>du</strong>it de porcelets par portée. Chez les truies présentantun taux d’ovu<strong>la</strong>tion insuffisant con<strong>du</strong>isant à des portées ré<strong>du</strong>ites, untraitement combiné d’hCG et de PMSG peut être efficace.La PMSG à une dose plus élevée est indiquée dans les cas où <strong>la</strong> combinaisond’hCG et de PMSG donne des résultats insuffisants. La PMSG peut égalementêtre utilisée chez <strong>la</strong> truie pour in<strong>du</strong>ire l’œstrus et pour traiter l’anœstrus chez lescochettes cyclées ou les truies primipares. L’hCG a été également utilisée chez <strong>la</strong>truie en cas de dysga<strong>la</strong>xie post-partum. Les résultats obtenus avec cette thérapeutiquedemandent cependant à être confirmés.Petits ruminantsChez <strong>la</strong> brebis et chez <strong>la</strong> chèvre, l’hCG peut être utilisé pendant l’œstrus pourobtenir une ovu<strong>la</strong>tion, mais l’efficacité n’est pas c<strong>la</strong>irement établie.La PMSG (eCG) peut être administrée dans les cas suivants, pour:- augmenter <strong>la</strong> fertilité et <strong>la</strong> taille de <strong>la</strong> portée après un traitement aux progestagènes.L’administration de <strong>la</strong> PMSG au moment où l’éponge vaginale est retiréedonne de meilleurs pourcentages de gravidité et des portées plus nombreuses.- in<strong>du</strong>ire l’œstrus chez les brebis et les chèvres en anœstrus. Il est possiblequ’aussitôt après <strong>la</strong> stimu<strong>la</strong>tion de l’activité follicu<strong>la</strong>ire ovarienne, l’animal entreen œstrus. Les résultats obtenus avec cette thérapeutique demandent encoreà être confirmés.Carnivores- in<strong>du</strong>ction de l’ovu<strong>la</strong>tion. L’utilisation de l’hCG est à conseiller lors de nymphomanied’origine ovarienne, lors de vagues follicu<strong>la</strong>ires successives et rapprochéesou en présence de follicules kystiques. Cette indication est particulièrement évidentechez <strong>la</strong> chatte et <strong>la</strong> furette, deux espèces à ovu<strong>la</strong>tion provoquée.- détection de <strong>la</strong> présence d’un ovaire rémanent ou d’un testicule intra-abdominal.L’injection d’hCG peut permettre <strong>la</strong> mise en évidence de <strong>la</strong> persistance ou de<strong>la</strong> présence d’une gonade intra-abdominale, après une épreuve dynamique aucours de <strong>la</strong>quelle les taux d’œstrogène ou de testostérone sont mesurés. Lesrésultats de ce test dynamique doivent être interprétés avec prudence.- puberté retardée au-delà de 2 ans et anœstrus prolongé correspondant à un intervallede plus de deux cycles normaux sans chaleurs. L’eCG permet d’in<strong>du</strong>ireles chaleurs chez <strong>la</strong> chienne. Le recours à l’association d’une faible dose d’œstrogènesqui était auparavant recommandé n’est plus admissible actuellement
762 MÉDICAMENTS DU SYSTÈME HORMONALvu les risques liés à l’utilisation de ces hormones chez <strong>la</strong> chienne. Chez le chat,l’administration d’une dose d’eCG est effective à cet égard.Animaux de sexe masculin- Stimu<strong>la</strong>tion des cellules de Leydig. La pro<strong>du</strong>ction de testostérone, <strong>la</strong> libido ainsique <strong>la</strong> fertilité des animaux traités par de l’hCG pourraient être améliorées. Parailleurs, certains essais ont été rapportés concernant l’administration de l’hCGchez le chiot présentant une cryptorchidie complète ou uni<strong>la</strong>térale rapidementaprès <strong>la</strong> naissance, vu l’implication de <strong>la</strong> testostérone dans une des phases demigration testicu<strong>la</strong>ire (résultats aléatoires et controversés).- La desloréline est un analogue synthétique de <strong>la</strong> GnRH qui est administré auxchiens mâles ou aux furets mâles. Elle inhibe <strong>la</strong> synthèse et <strong>la</strong> libération de FSHet de LH, lorsqu’elle est administrée en dose continue faible. L’administration dedesloréline, sous forme d’imp<strong>la</strong>nt, à des chiens mâles a<strong>du</strong>ltes en bonne santéprovoque une infertilité transitoire et réversible. Celle-ci apparaît à partir de 8semaines après le premier traitement et se prolonge minimum 6 mois ou mêmeminimum 12 mois aux doses plus élevées. Chez un petit nombre d’animaux,l’infertilité n’a été obtenue qu’après 12 semaines, mais dans <strong>la</strong> plupart des cas,ces animaux n’ont pas été capables d’engendrer une progéniture. Chez les furets,l’infertilité est obtenue entre 5 et 14 semaines après le traitement initial et<strong>du</strong>re 16 mois. La réversibilité des effets et <strong>la</strong> capacité des furets mâles traités àengendrer une progéniture par <strong>la</strong> suite, n’ont pas été étudiées. (Voir aussi FoliaVeterinaria 2010 n° 3)PharmacodynamieLa GnRH est un décapeptide hypotha<strong>la</strong>mique stimu<strong>la</strong>nt <strong>la</strong> libération des gonadotrophineshypophysaires. Les dérivés synthétiques, <strong>la</strong> gonadoréline et <strong>la</strong> buséréline,ont des propriétés semb<strong>la</strong>bles. La LH et <strong>la</strong> FSH agissent au niveau descellules ovariques et testicu<strong>la</strong>ires en mo<strong>du</strong><strong>la</strong>nt <strong>la</strong> gamétogénèse et <strong>la</strong> pro<strong>du</strong>ctionde stéroïdes gonadiques. L’hCG et l’eCG sont respectivement sécrétées par <strong>la</strong>femme enceinte et <strong>la</strong> jument <strong>du</strong>rant <strong>la</strong> gestation, et ont une action gonadotrope.L’hCG possède exclusivement une action LH tandis que l’eCG a une action FSHet LH variant selon les espèces mais uniquement LH chez l’espèce source.PharmacocinétiqueLes GnRH, synthétiques ou naturelles, sont caractérisées par une demi-vie trèscourte. Leur activité se manifeste rapidement. Les concentrations p<strong>la</strong>smatiquesmaximales de LH et de FSH sont atteintes respectivement 0.5 h et 2 h après uneinjection intraveineuse et intramuscu<strong>la</strong>ire. Les demi-vies de <strong>la</strong> FSH et de <strong>la</strong> LHsont un peu plus longues. Ces hormones sont principalement décomposées dansle foie puis éliminées par les reins.Contre-indicationsIl est conseillé de ne pas administrer de GnRH chez les bovins chez lesquels lerisque de contamination bactérienne de l’utérus est élevé, en particulier pendantles 14 à 18 jours suivant <strong>la</strong> mise bas. L’ovu<strong>la</strong>tion suivie de <strong>la</strong> formation <strong>du</strong> corpsjaune et de <strong>la</strong> pro<strong>du</strong>ction de progestagènes stimule <strong>la</strong> croissance bactériennedans l’utérus et peut in<strong>du</strong>ire une endométrite sévère.Effets indésirablesL’effet indésirable potentiel, lors de l’administration intraveineuse ou intramuscu<strong>la</strong>irede gonadotrophines, est une réaction allergique qui doit être traitée avecde l’adrénaline et des corticoïdes. Les gonadotrophines peuvent augmenter lenombre d’ovu<strong>la</strong>tions se compliquant parfois de kystes ovariens. Le respect desposologies recommandées est capital pour obtenir les effets souhaités et éviterles conséquences indésirables. Il est cependant important de noter que dans plusieursespèces, les doses utilisées sont tout simplement empiriques et qu’uneprudence extrême paraît nécessaire quant à leur emploi.InteractionsAucune interaction connue.Précautions particulièresL’utilisation répétée et abusive de ces hormones peut in<strong>du</strong>ire une immunisationcontre les gonadotrophines exogènes mais aussi, indirectement, par réactioncroisée, contre les gonadotrophines endogènes. Cette réaction peut aboutir àune ré<strong>du</strong>ction de l’efficacité des traitements ultérieurs et même à de l’infertilité.L’utilisation répétée de ces molécules se fera donc avec prudence. L’administration
2 MÉDICAMENTS DU SYSTÈME HORMONAL 77de gonadolibérines, <strong>du</strong> fait de leur faible poids molécu<strong>la</strong>ire et de leur structureproche <strong>du</strong> GnRH endogène, ne présente pas ce même inconvénient et sera doncpréférée lorsque <strong>la</strong> prudence s’impose ou que de nombreuses injections sont envisagées.Cependant, une désensibilisation des récepteurs hypophysaires et uneinhibition subséquente de <strong>la</strong> réponse à <strong>la</strong> GnRH peut s’observer suite à l’administrationfréquente et rapprochée (quelques heures) de cette hormone.Repro<strong>du</strong>ction et <strong>la</strong>ctationIl est déconseillé d’administrer ces molécules lors de <strong>la</strong> gestation.2.1.5.1 Gonadotrophinechorionique (hCG)LMR gonadotrophine chorionique: CHORULON (MSD A.H.)gonadotrophine chorionique (hCG):1.500 UI/5 mllyophilisat et solution injectable im, ivPosologie:Eq: in<strong>du</strong>ction ovu<strong>la</strong>tion: 1500 - 3000 UI (iv)anœstrus: 1500 - 3000 UI (im, iv)répéter éventuellement après 48 hBo: in<strong>du</strong>ction ovu<strong>la</strong>tion: 1500 UI (im, iv)syndr kyste ovarien: 3000 UI (iv)Ca: anoestrus: 500 UI pj (les 10 premiersj des chaleurs ) (iv, im), après traitementpréa<strong>la</strong>ble au PMSGovu<strong>la</strong>tion tardive, chaleurs prolongées:100 - 500 UI pj (im) (jusqu’à disparition despertes vaginales)cryptorchidie: 2 x/sem 100 - 500 UI (im)(6 sem)libido insuffisante: 100 - 500 UI (im) (6 - 12havant l’accouplement)Temps d’attente: 0 jlyophilisat 5 x 1.500 UI + 5 x 5 ml solvantR/2.1.5.2 Gonadotrophine sérique(PMSG ou eCG)LMR gonadotrophine sérique: FOLLIGON (MSD A.H.)gonadotrophine sérique (PMSG): 1.000 UIlyophilisat et solvant injectable sc, imPosologie:Eq: anoestrus, in<strong>du</strong>ction oestrus:1.000 - 2.000 UIBo (im): superovu<strong>la</strong>tion: 1500 - 3000 UIanoestrus: 500 - 1000 UIstimu<strong>la</strong>tion fertilité (après progestagènes):300 - 750 UISu: anaoestrus : 200 - 800 UI (avec HCG)Ov, Capr: in<strong>du</strong>ction ou synchronisationde l’oestrus (après progestagènes):400 - 700 UICa: anoestrus, in<strong>du</strong>ction oestrus: 500 UI ou20 UI/kg pj (10 j) (hCG au j 10)<strong>la</strong>pin (im, sc): anoestrus, in<strong>du</strong>ction oestrus,superovu<strong>la</strong>tion: 40 UITemps d’attente: 0 jlyophilisat 1.000 UI + 1 f<strong>la</strong>con de solvantR/SYNCROSTIM 500 IU (Ceva Santé Animale)gonadotropine sérique équine (eCG): 500 UIlyophilisat pour solution injectable imPosologie:Bo, Ov: 1 x 500 UI/animalViande et abats: 0 j, Lait: 0 j5 f<strong>la</strong>cons de lyophilisat + 10 ml de solvantR/2.1.5.3 GnRH : buséréline,desloréline, gonadoréline,peforélineLMR buséréline, desloréline,gonadoréline, peforéline: MAPRELIN (Veyx-Pharma)péforéline : 75 mcg/mlsolution injectable imPosologie:truie primipare: 24 h après le sevrage37,5 mcg/animaltruie multipare : 24 h après le sevrage150 mcgcochette: 48 h après l’arrêt <strong>du</strong> traitementdestiné à inhiber le cycle: 150 mcgViande et abats: 0 jf<strong>la</strong>con 50 mlR/OVARELIN (Ceva Santé Animale)gonadoréline (diacétate): 50 mcg/mlsolution injectable imPosologie:Bo: 100 mcg/animalViande et abats: 0 j, Lait: 0 hf<strong>la</strong>con 10 mlR/RECEPTAL (MSD A.H.)buséréline acétate: 4,2 mg/mlsolution injectable iv, im, scPosologie:Eq: 5 - 10 mlBo: 2,5 - 5 mlSu (cochette): 2,5 ml/animal<strong>la</strong>pin: 0,2 mlViande: Eq, Bo, <strong>la</strong>pin: 0 j, Lait: Bo: 0 jf<strong>la</strong>con 5 x 10 mlR/SUPRELORIN 4,7 mg imp<strong>la</strong>nt chiens (Virbac)desloréline (acétate): 4,7 mgimp<strong>la</strong>nt scPosologie:Ca (mâle): 1 imp<strong>la</strong>nt/animal (répéter tousles 6 m)l’infertilité apparaît 6 sem après le traitementinitial et <strong>du</strong>re min 6 mimp<strong>la</strong>nt 2, 5R/
782 MÉDICAMENTS DU SYSTÈME HORMONALSUPRELORIN 9,4 mg imp<strong>la</strong>nt chiens, furets(Virbac)desloréline (acétate): 9,4 mgimp<strong>la</strong>nt scPosologie:- Ca (mâle): 1 imp<strong>la</strong>nt/animal/12 ml’infertilité apparaît à partir de 8 sem après letraitement initial et <strong>du</strong>re min 12 m- furet (mâle): 1 imp<strong>la</strong>nt/animal/16 ml’infertilité apparaît entre 5 et 14 sem aprèsle traitement initial et <strong>du</strong>re min 16 mimp<strong>la</strong>nt 2R/VETERELIN 0,004 mg/ml (Lab Calier)buseréline: 0,004 mg/mlsolution injectable sc, im, ivPosologie:Eq: 10 ml de pro<strong>du</strong>it/animal im (iv, sc)Bo: 2.5 - 5 ml de pro<strong>du</strong>it/animal im (iv, sc)Su: 2.5 ml de pro<strong>du</strong>it/animal im (iv)<strong>la</strong>pin: 0.2 ml de pro<strong>du</strong>it/animal im (iv, sc)Viande et abats: 0 j, Lait: 0 jf<strong>la</strong>con 5 x 10 mlR/2.1.5.4 Lyophilisat de pFSH et pLHLMR follitropine + lutropine: PLUSET (Lab Calier)hormone folliculostimu<strong>la</strong>nte porcine (FSHp):500 UI/f<strong>la</strong>conhormone lutéinisante porcine (LHp): 500 UI/f<strong>la</strong>conpoudre et solvant pour solution injectable imPosologie:Bo (femelles sexuellement matures): dosetotale de 800 à 1000 UI en doses décroissantes,en 4 - 5 jViande: 0 j, Lait: 0 j2 f<strong>la</strong>cons de pro<strong>du</strong>it lyophilisé + 1 x 21 ml desolvantR/STIMUFOL (Reprobiol)follitropine: 0,5 mglutropine: 0,1 mglyophilisat et solution injectable imPosologie:<strong>la</strong> dose sera répartie sur 4 j (2 injections pj)Bo: 0,45 - 0,5 mg pFSHgénisse: 0,32 - 0,36 mg pFSHTemps d’attente: 0 jf<strong>la</strong>con lyophilisat + 10 ml solvantR/2.1.5.5 Combinaison de PMSG(eCG) et d’hCGLMR gonadotrophine chorionique +gonadotrophine sérique: FERTIPIG (Ceva Santé Animale)gonadotropine sérique équine (PMSG): 80 UI/mlgonadotropine chorionique humaine (hCG):40 UI/mllyophilisat pour solution injectable imPosologie:truie: 400 UI de PMSG + 200 UI d’hCG paranimal dans les 24 h suivant le sevrageTemps d’attente: 0 jf<strong>la</strong>con 1 x 10 ml de lyophilisat + 1 x 25 ml desolvant (5 doses)R/GESTAVET 600 (Hipra Lab)gonadotrophine sérique (PMSG): 400 UIgonadotrophine chorionique (hCG): 200 UIpoudre et solution injectable imPosologie:truie: 400 UI de PMSG + 200 UI d'hCG(0 à 2 j après le sevrage)Viande et abats: 0 j10 f<strong>la</strong>cons de poudre + 10 f<strong>la</strong>cons de solvant(5 ml/f<strong>la</strong>con)R/GESTAVET 3000 (Hipra Lab)gonadotrophine sérique (PMSG): 2000 UIgonadotrophine chorionique (hCG): 1000 UIpoudre et solution injectable imPosologie:truie: 400 UI de PMSG + 200 UI d'hCG (0 à2 j après le sevrage)Viande et abats: 0 j10 f<strong>la</strong>cons de poudre + 10 f<strong>la</strong>cons de solvant(25 ml/f<strong>la</strong>con)R/PG-600 (MSD A.H.)gonadotrophine chorionique (hCG): 200 UI/dosegonadotrophine sérique (PMSG): 400 UI/doselyophilisat et solvant injectable sc, imPosologie:Su: min 1 dose (5 ml)/animalViande: 0 jf<strong>la</strong>con 1 x 5 doses + 1 f<strong>la</strong>con de solvant (25 ml)5 x 1 dose + 5 f<strong>la</strong>cons de solvant (5 ml)R/2.1.6 TocolytiquesIndicationsBovinsChez le bovin, les tocolytiques sont utilisés:- pour retarder le part. Si les tocolytiques sont administrés au début de l’ouverture<strong>du</strong> col, le part peut être retardé de 4 à 8 heures sans conséquence dommageablepour le veau et <strong>la</strong> vache.- pour ré<strong>du</strong>ire <strong>la</strong> tonicité <strong>du</strong> myomètre susceptible d’entraver le bon déroulementde manœuvres obstétricales diverses comme <strong>la</strong> césarienne, <strong>la</strong> fœtotomie, <strong>la</strong>correction d’une dystocie. En administrant un tocolytique au début de l’opération,l’utérus sera relâché au moment où il doit être sorti de l’abdomen. Lamanipu<strong>la</strong>tion de l’utérus peut s’en trouver facilitée. Après l’intervention, l’action<strong>du</strong> tocolytique doit être antagonisée par l’administration d’oxytocine.- lors d’une intervention obstétricale telle qu’une fœtotomie ou un repositionnement,
2 MÉDICAMENTS DU SYSTÈME HORMONAL 79au cours de <strong>la</strong>quelle un relâchement de l’utérus est nécessaire. Après l’intervention,l’action <strong>du</strong> tocolytique peut être supprimée par administration d’oxytocine.- pour l’inhibition des contractions utérines indésirables pouvant apparaître en finde gestation, en combinaison avec une anesthésie épi<strong>du</strong>rale.PharmacodynamieLe clenbutérol (agonistes bêta2-adrénergiques) permet <strong>la</strong> re<strong>la</strong>xation <strong>du</strong> myomètre.PharmacocinétiqueLe clenbutérol a une bonne distribution et diffuse à travers le p<strong>la</strong>centa chez lesbovins. Les concentrations p<strong>la</strong>smatiques maximales sont atteintes 0.5 à 3 heuresaprès l’administration parentérale. L’activité tocolytique se manifeste 20 min aprèsl’administration intramuscu<strong>la</strong>ire ou immédiatement après injection intraveineuse.L’excrétion <strong>du</strong> clenbutérol, non métabolisé, se fait principalement par voie rénale.Contre-indicationsL’utilisation <strong>du</strong> clenbutérol en dehors de ces indications.Effets indésirablesDe rares cas de polypnée, de sudation, de tremblements et de tachycardie sontdécrits.InteractionsLe clenbutérol ne sera en tout cas pas administré conjointement à des substancessympathicomimétiques ou vasodi<strong>la</strong>tatrices.Précautions particulièresL’effet vasodi<strong>la</strong>tateur <strong>du</strong> clenbutérol peut prédisposer l’animal aux hémorragies.Repro<strong>du</strong>ction et <strong>la</strong>ctationDes études de toxicité de clenbutérol chez le rat ont montré un accroissementde <strong>la</strong> mortalité fœtale et néonatale après l’administration répétée de clenbutérolà l’animal mère.2.1.6.1 ClenbutérolLMR clenbutérol : PLANIPART (Boehringer Ingelheim)clenbutérol (chlorhydrate): 0,03 mg/mlsolution injectable im, ivPosologie:Bo: 0,8 mcg/kg (0,3 mg/animal)Viande: Bo: 6 j, Lait: Bo: 5 traites ou 60 hf<strong>la</strong>con 50 mlR/2.1.7 OcytociquesIndicationsL’oxytocine peut être administrée pour les indications suivantes reposant sur <strong>la</strong>stimu<strong>la</strong>tion <strong>du</strong> myomètre ou de l’éjection <strong>la</strong>ctée:Chevaux- In<strong>du</strong>ction <strong>du</strong> part. Une injection d’oxytocine suffit si <strong>la</strong> jument est à terme. Lepart suit une à deux heures après l’injection.- Expulsion de l’arrière-faix. Si l’expulsion de l’arrière-faix tarde plus de deuxheures, l’oxytocine est indiquée. Cette substance peut être administrée par injectionou mieux, par infusion qui donne de meilleurs résultats. Si un seul traitementest insuffisant, il peut être renouvelé jusqu’à deux fois à une heure d’intervalle àchaque fois. Chez le cheval, l’injection d’un bolus d’oxytocine peut provoquer descoliques.- Traitement de l’endométrite chronique ou d’une endométrite provoquée par unaccouplement ou une insémination. Dans de tels cas, une quantité appréciablede pus s’accumule dans l’utérus. Le <strong>la</strong>vage de <strong>la</strong> matrice s’impose et <strong>la</strong> jumentdevra recevoir de l’oxytocine par voie intramuscu<strong>la</strong>ire 3 à 5 fois par jour pendant2 à 4 jours. Si <strong>la</strong> quantité de liquide à éliminer est limitée, le traitement à l’oxytocinepeut être ramené à 2 injections par jour pendant 1 à 3 jours.Bovins et petits ruminants- Renforcement des contractions utérines chez <strong>la</strong> vache en cas de fièvre de <strong>la</strong>it
802 MÉDICAMENTS DU SYSTÈME HORMONALet lors de cas bien définis, comme <strong>la</strong> hernie ventrale. Toutefois, si <strong>la</strong> fièvre de<strong>la</strong>it est traitée de manière appropriée, un traitement complémentaire avec del’oxytocine n’est pas nécessaire. Des contractions myométriales insuffisantespeuvent aussi être <strong>la</strong> conséquence de ma<strong>la</strong>dies systémiques graves qu’un examenclinique adéquat doit d’abord permettre d’identifier.- Inhibition de l’atonie utérine in<strong>du</strong>ite par des tocolytiques en phase post-chirurgicalede l’hystérotomie.- Favoriser l’involution utérine au cours des pathologies de l’utérus en phase postpartum: saignements intra-utérins, utérus repositionné après in<strong>version</strong> et pro<strong>la</strong>psusou après une mise bas difficile comme <strong>la</strong> fœtotomie.- Favoriser l’élimination <strong>du</strong> <strong>la</strong>it en cas de mammite.Rétention de <strong>la</strong>it : différentes causes sont évoquées (angoisse, douleurs…). Sil’oxytocine est administrée juste avant <strong>la</strong> traite, l’élimination <strong>du</strong> <strong>la</strong>it a lieu immédiatementaprès administration. Chez certains bovins, quelques traitements suffisent; chez d’autres, l’oxytocine doit être administrée pendant parfois plusieursmois, systématiquement avant <strong>la</strong> traite.Porcs- Faiblesse <strong>du</strong> travail surtout rencontrée chez de vieilles truies, par suite d’une atonieutérine. Une injection d’oxytocine permet de hâter l’expulsion des derniersporcelets et de l’arrière-faix.- Syndrome mammite-métrite-aga<strong>la</strong>ctie (MMA). Cette indication trouve souventson origine dans une mastite. La métrite et l’aga<strong>la</strong>ctie sont des épiphénomènes.Le traitement comprend des antibiotiques et de l’oxytocine avec, éventuellement,des corticoïdes.CarnivoresLes indications pour l’utilisation de l’oxytocine sont semb<strong>la</strong>bles à celles citées chezles grandes espèces à savoir : l’inertie utérine primaire ou secondaire, le traitementadjuvant d’un retard à l’involution utérine, des pertes hémorragiques post-partum,etc. Néanmoins, il faut insister sur l’identification de <strong>la</strong> cause de l’atonie ou despertes de sang avant toute administration. L’injection en cas d’atonie provoquéepar une dystocie par malposition peut in<strong>du</strong>ire une rupture utérine. En phase postpartum,l’efficacité de l’oxytocine se maintient pendant une période maximale de 48à 72 h après le part. Il faut toujours veiller à utiliser de faibles doses d’oxytocine, unsurdosage pouvant in<strong>du</strong>ire une atonie par désensibilisation des récepteurs.PharmacodynamieL’oxytocine, hormone synthétisée par l’hypotha<strong>la</strong>mus et stockée au niveau de <strong>la</strong>neuro-hypophyse, agit sur <strong>la</strong> muscu<strong>la</strong>ture utérine, préa<strong>la</strong>blement sensibilisée parles œstrogènes, en stimu<strong>la</strong>nt les contractions myométriales. Un deuxième effet,non négligeable, est aussi observé sur les cellules myoépithéliales des acini mammairesen permettant l’éjection <strong>du</strong> <strong>la</strong>it sans effet propre sur sa synthèse.PharmacocinétiqueL’effet se manifeste immédiatement après une administration intraveineuse, oubien 2 à 3 minutes après une administration intramuscu<strong>la</strong>ire. L’oxytocine est rapidementmétabolisée dans le foie. Seul un petit pourcentage d’oxytocine nonmétabolisée est excrété par voie rénale.Contre-indicationsDystocie <strong>du</strong>e à une position anormale <strong>du</strong> fœtus, col utérin incomplètement ouvert,taille excessive <strong>du</strong> fœtus.Effets indésirablesEn cas de surdosage ou lorsque les dé<strong>la</strong>is ne sont pas respectés lors d’administrationsmultiples, des contractions utérines exagérées, mais pouvant êtrecontrôlées par les agonistes bêta2-adrénergiques, peuvent se pro<strong>du</strong>ire. Une atoniesecondaire peut aussi survenir. En outre, de l’hypertension et des aggravationsd’insuffisances cardiaques ont parfois été observées.InteractionsL’usage simultané avec des sympaticomimétiques peut engendrer de l’hypertension.Précautions particulièresEn cas d’usage pré-partum, on vérifiera d’abord que <strong>la</strong> re<strong>la</strong>xation <strong>du</strong> col utérinsoit complète, et <strong>la</strong> position fœtale normale. L’hypocalcémie ou l’hypoglycémiedoivent être corrigées avant l’administration d’oxytocine.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 81Repro<strong>du</strong>ction et <strong>la</strong>ctationLorsque l’oxytocine est utilisée dans le cadre des indications mentionnées, aucuneanomalie fœtale n’apparaît. L’oxytocine est excrétée en petites quantitésdans le <strong>la</strong>it, sans pour autant influencer l’animal al<strong>la</strong>ité.LMR oxytocine : LONGACTON (VetCom-pharma)carbétocine: 0,07 mg/mlsolution injectable im, ivPosologie:Bo: 0,21 - 0,35 mg/animalSu: 0,105 - 0,21 mg/animalraccourcissement de <strong>la</strong> parturition, Su:0,07 mg/animalViande: Bo, Su: 0 j, Lait: Bo: 0 jf<strong>la</strong>con 1 x 50 mlR/OXYTOCINE 10 UI/ml (VMD)oxytocine: 10 UI/mlsolution injectable iv, im (Eq, Bo, Su, Fe), im(Ov, Capr, Ca)Posologie:selon l’indic et le mode d’admin:Eq: 10 - 75 UIBo: 10 - 30 UIOv, Capr: 10 - 15 UISu: 5 - 40 UICa: 0,5 -1 UI/kg, max 10 UIFe: 2 - 5 UIViande: 0 j, Lait: 0 jf<strong>la</strong>con 50 ml, 100 mlR/2.1.8 Prostag<strong>la</strong>ndinesOXYTOCINE KELA 10 UI (Ke<strong>la</strong> Laboratoria)oxytocine: 10 UI/mlsolution injectable sc (Ca, Fe), iv, im (Eq, Bo,Su, Ov, Capr, Ca, Fe)Posologie:selon l’indic et le mode d’admin:Eq: 10 - 50 UI/500 kgBo: 30 - 60 UI/500 kgOv, Capr: 10 UI/50 kgSu: 10 - 20 UI/200 kgCa, Fe: 0,5 - 1 UI/kgViande: 0 j, Lait: 0 jf<strong>la</strong>con 50 ml, 100 mlR/OXYTOCINE PRODIVET (Prodivet)oxytocine synth.: 10 UI/mlsolution injectable iv (lente), imPosologie:Eq: 10 - 20 UIBo: 30 - 60 UISu: 20 - 40 UIOv, Capr: 10 - 15 UICa: 5 - 10 UIFe: 3 - 5 UITemps d’attente: 0 jf<strong>la</strong>con 50 ml, 100 mlR/IndicationsLes prostag<strong>la</strong>ndines (PG) peuvent être particulièrement utiles dans les situationsoù le corps jaune doit entrer en régression.ChevauxLes PG sont indiquées chez <strong>la</strong> jument pour in<strong>du</strong>ire l’œstrus :- chez une jument qui n’a pas été vue en chaleur et chez <strong>la</strong>quelle un des ovairesprésente un corps jaune présent depuis au moins 6 jours. Un œstrus fertile doitse pro<strong>du</strong>ire après 3 à 4 jours. Il peut s’agir de juments chez lesquelles les chaleurssont passées inaperçues (subœstrus), de juments porteuses d’un embryonmort ou, enfin, de juments présentant un corps jaune persistant (<strong>la</strong>ctation, pyomètreet lorsque <strong>la</strong> mort fœtale est survenue après le 40ème jour de gestation).Si une mort fœtale survient, l’action des PG est alors très variable sinon insuffisante,par suite de <strong>la</strong> présence des cupules endométriales à l’origine de sécrétionde PMSG à effet LH chez <strong>la</strong> jument.- en cas d’un avortement avant le 40ème jour de gravidité. Les PG provoquentalors <strong>la</strong> régression <strong>du</strong> corps gestatif, provoquant ainsi <strong>la</strong> mort embryonnaire.L’œstrus apparaît 3 à 4 jours plus tard.BovinsLes PG peuvent être utilisées chez les bovidés pour les indications suivantes:- traitement <strong>du</strong> subœstrus: les vaches cyclées, chez lesquelles aucune chaleurn’est observée (subœstrus), réagissent à l’administration de PG par l’apparitionde chaleurs 3 à 7 jours plus tard à condition qu’au moment de leur administration,un corps jaune vieux d’au moins 6 jours soit présent. L’intensité deschaleurs est très variable.- synchronisation de l’œstrus. Il est possible d’obtenir une synchronisation del’œstrus avec des PG à condition que les animaux traités soient cyclés. Deuxinjections de PG administrées à 11 - 12 jours d’intervalle assurent <strong>la</strong> synchronisationdes chaleurs. La fertilité de <strong>la</strong> phase œstrale in<strong>du</strong>ite est basse chez lesvaches et normale chez les génisses.- traitement d’un pyomètre ou d’une endométrite purulente. Etant donné qu’un
822 MÉDICAMENTS DU SYSTÈME HORMONALcorps jaune persistant est toujours associé à un pyomètre, de tels animaux neprésentent pas de chaleurs et <strong>du</strong> pus s’accumule dans l’utérus. Les PG entraînent<strong>la</strong> régression <strong>du</strong> corps jaune à <strong>la</strong> suite de <strong>la</strong>quelle les chaleurs peuventsurvenir. Les contractions associées <strong>du</strong> myomètre vont vider l’utérus. Commeun pyomètre a tendance à récidiver, il est recommandé de traiter deux fois lesanimaux avec des PG, à 14 jours d’intervalle. L’endométrite purulente étant lepremier stade <strong>du</strong> pyomètre, il est recommandé de traiter ces animaux (2 fois)avec des PG.- provoquer un avortement. Si une vache est saillie de manière non souhaitée, lesPG peuvent facilement mettre un terme à <strong>la</strong> gestation, <strong>du</strong> 6ème jour minimumau 80ème jour après <strong>la</strong> fécondation. Après le 80ème jour, <strong>la</strong> chance d’obtenir unavortement par une seule injection de PG est de plus en plus limitée. Au coursdes 4ème et 5ème mois de <strong>la</strong> gravidité, un avortement n’est possible que parl’administration répétée de PG, 3 ou 4 fois, à quelques jours d’intervalle.- in<strong>du</strong>ction <strong>du</strong> part. Chez les bovins, l’in<strong>du</strong>ction <strong>du</strong> part avec des PG est possibleà partir <strong>du</strong> 250ème jour de <strong>la</strong> gravidité. Entre le 250ème et le 260ème jour, lerisque de mortalité <strong>du</strong> veau est élevé de même que <strong>la</strong> rétention d’arrière-faix.Le risque diminue après le 270ème jour. L’in<strong>du</strong>ction <strong>du</strong> part peut également êtresouhaitée en cas d’accouchement retardé, d’un œdème grave <strong>du</strong> pis ou d’unhydral<strong>la</strong>ntoïs, ou de ma<strong>la</strong>dies graves pour <strong>la</strong> vache.- traitement d’une vache avec un fœtus momifié. Un corps jaune persistant estprésent lorsque le fœtus est momifié. Ce dernier peut être expulsé par l’administrationde PG. Une seule injection de PG peut parfois s’avérer insuffisante. Il estalors nécessaire de recourir à une seconde injection quelques jours plus tard.Il est recommandé de combiner l’injection avec des œstrogènes, ce qui a poureffet de relâcher le col utérin et de faciliter l’expulsion.PorcsLes PG sont indiquées chez <strong>la</strong> truie pour:- l’in<strong>du</strong>ction <strong>du</strong> part. De nombreuses raisons peuvent être invoquées pour in<strong>du</strong>irele part chez <strong>la</strong> truie. Les plus importantes sont le regroupement des mises baset <strong>la</strong> possibilité de répartir les porcelets entre les mères. L’injection de PG nedoit pas être effectuée trop tôt, soit plus de 2 jours avant <strong>la</strong> fin de <strong>la</strong> <strong>du</strong>réemoyenne de <strong>la</strong> gestation, pour éviter que les chances de survie des porcelets nediminuent. La parturition survient 24 à 40 heures après l’administration de PG.Si on donne de l’oxytocine 20 à 24 heures après l’injection de PG, <strong>la</strong> parturitionsurvient quelques heures après l’injection d’oxytocine.- l’expulsion d’une portée de porcelets momifiés. Si <strong>la</strong> truie n’a pas mis bas à<strong>la</strong> date pressentie, et que l’examen clinique confirme <strong>la</strong> présence de porceletsmomifiés, les porcelets momifiés sont expulsés après un ou deux jours suite àl’administration de PG. Il convient essentiellement de s’assurer qu’il n’y a pas eud’erreur en calcu<strong>la</strong>nt <strong>la</strong> date <strong>du</strong> part.PharmacodynamieLa prostag<strong>la</strong>ndine F2alpha est notamment sécrétée dans le sang par l’endomètreen fin de cycle ou de gestation. Elle se trouve également dans d’autres fluidescorporels comme le sperme et le corps jaune. Des composés synthétiques sontdisponibles. Ces substances possèdent une activité lutéolytique et une actionstimu<strong>la</strong>nte sur les fibres muscu<strong>la</strong>ires lisses, notamment myométriales. La lyse <strong>du</strong>corps jaune est <strong>la</strong> conséquence d’une vasoconstriction locale suivie d’une lysedes cellules lutéales. Le spectre d’action des prostag<strong>la</strong>ndines est re<strong>la</strong>tivement<strong>la</strong>rge mais varie fortement d’une espèce à l’autre.PharmacocinétiqueCes substances sont caractérisées par une métabolisation rapide au niveau despoumons, <strong>du</strong> foie, des reins et d’autres organes. Elles sont principalement excrétéespar voie rénale. La demi-vie est de quelques minutes.Contre-indicationsGestation souhaitée, administration intraveineuse, administration à des animauxplus âgés, administration à des animaux souffrant de ma<strong>la</strong>dies cardio-vascu<strong>la</strong>ires,gastro-intestinales ou respiratoires.Effets indésirablesL’efficacité et l’importance des effets indésirables varient très fortement en fonctionde <strong>la</strong> dose, de <strong>la</strong> nature de <strong>la</strong> molécule utilisée, de l’espèce cible et de <strong>la</strong> sensibilité
2 MÉDICAMENTS DU SYSTÈME HORMONAL 83indivi<strong>du</strong>elle. Les effets indésirables, qui sont habituellement moins prononcés avecles dérivés synthétiques, sont: <strong>la</strong> diarrhée, les vomissements, <strong>la</strong> sudation, <strong>du</strong> ptyalisme,de <strong>la</strong> tachypnée, des avortements et des spasmes des muscles lisses.InteractionsL’activité de l’oxytocine peut être renforcée par les prostag<strong>la</strong>ndines.Précautions particulières/Risques pour l’hommeL’administration de ces composés par des personnes asthmatiques ou ayant desdifficultés respiratoires, ou par des femmes enceintes ou désireuses de le devenir,doit se faire avec <strong>la</strong> plus grande prudence. La possibilité d’une absorption transcutanéene doit pas être écartée.Repro<strong>du</strong>ction et <strong>la</strong>ctationCes pro<strong>du</strong>its ne doivent pas être administrés lors d’une gestation désirée.2.1.8.1 AlfaprostolLMR alfaprostol: GABBROSTIM (Ceva Santé Animale)alfaprostol: 2 mg/mlsolution injectable imPosologie:Eq: 3 mg/animalBo, génisse: 1,5 mg/100 kg (max8 mg/animal)Su: 2 mg/animalViande: 24 h, Lait: 24 hf<strong>la</strong>con 20 mlR/2.1.8.2 CloprosténolLMR cloprosténol : CYCLIX Bovine (Virbac)cloprosténol sodique: 0,263 mg/mlsolution injectable imPosologie:Bo: toutes indic: 2 ml/animalsynchronisation de l’oestrus:2 x 2 ml/animal à 11 j d’intervalleViande: 2 j, Lait: 0 jf<strong>la</strong>con 20 mlR/CYCLIX Porcine (Virbac)cloprosténol sodique: 0,092 mg/mlsolution injectable imPosologie:Su: 2 ml/animalViande: 2 jf<strong>la</strong>con 20 mlR/DALMAZIN 75 mcg/ml (Fatro)d-cloprosténol: 75 mcg/mlsolution injectable imPosologie:Bo: 150 mcg/animalSu: 75 mcg/animal (répéter après 6 h)Viande: Bo: 0 j, Su: 1 j, Lait: 0 jf<strong>la</strong>con 1 x 10 ml, 5 x 20 mlR/ESTRUMATE (MSD A.H.)cloprosténol sodique: 0,263 mg/mlsolution injectable imPosologie:Bo: 2 ml/animal- suboestrus: éventuellement 2e inject (2 ml)après 11 j- pyomètres: éventuellement 2e inject (2 ml)après 10 - 14 j- régu<strong>la</strong>tion d’oestrus: 2 x 2 ml/animal à 11 jd’intervalleViande: 24 h, Lait: 0 jf<strong>la</strong>con 10 ml, 20 mlR/PLANATE (MSD A.H.)cloprosténol (sodique): 0,092 mg/mlsolution injectable imPosologie:Su: 2 ml/animalViande: 24 hf<strong>la</strong>con 20 mlR/2.1.8.3 DinoprostLMR dinoprost : DINOLYTIC (Pfizer A.H.)dinoprost (trométhamine): 5 mg/mlsolution injectable sc, imPosologie:Eq: 5 mg/animalBo: 25 mg/animalSu: 10 mg/animalViande: 0 j, Lait: 0 jf<strong>la</strong>con 5 x 10 ml, 30 mlR/ENZAPROST (Ceva Santé Animale)dinoprost (trométamol): 5 mg/mlsolution injectable imPosologie:Bo: 25 mg/animalSu: 10 mg/animalViande: Bo: 3 j, Su: 2 j, Lait: Bo: 0 hf<strong>la</strong>con 50 ml, 10 x 5 mlR/2.1.9 Médicaments agissant sur <strong>la</strong> libération de <strong>la</strong> pro<strong>la</strong>ctineIndicationsCarnivores- Arrêt de <strong>la</strong> <strong>la</strong>ctation faisant suite à un sevrage précoce, à des avortements, à <strong>la</strong>pseudogestation et au retrait immédiat de <strong>la</strong> portée après <strong>la</strong> parturition.
842 MÉDICAMENTS DU SYSTÈME HORMONALPharmacodynamieLa pro<strong>la</strong>ctine est une hormone hypophysaire dont les concentrations sanguinesvarient en fonction <strong>du</strong> sexe et <strong>du</strong> stade physiologique et physiopathologique del’indivi<strong>du</strong>. La libération de cette hormone est stimulée par <strong>la</strong> pro<strong>la</strong>ctolibérine etinhibée par <strong>la</strong> dopamine. Le tonus dopaminergique inhibiteur est continu, assurantl’inhibition de <strong>la</strong> libération d’une hormone par ailleurs à synthèse constante.Le contrôle de ce tonus permet en conséquence de mo<strong>du</strong>ler <strong>la</strong> sécrétion de pro<strong>la</strong>ctine.Les rôles de cette hormone sont nombreux. Le renforcement de l’actiondopaminergique par le biais de l’utilisation d’agonistes spécifiques des récepteursD2, comme <strong>la</strong> cabergoline et <strong>la</strong> bromocryptine ou en stimu<strong>la</strong>nt <strong>la</strong> libération dedopamine dans l’hypotha<strong>la</strong>mus, par des substances antisérotoninergiques, telleque <strong>la</strong> métergoline aboutit à une inhibition de <strong>la</strong> sécrétion de pro<strong>la</strong>ctine. La g<strong>la</strong>ndemammaire est l’organe cible principal de <strong>la</strong> pro<strong>la</strong>ctine chez les mammifères, notammentlors <strong>du</strong> déclenchement de <strong>la</strong> <strong>la</strong>ctation au moment <strong>du</strong> part. Néanmoins,d’autres tissus comme le foie, les ovaires, les testicules, <strong>la</strong> prostate et l’hypotha<strong>la</strong>mussubissent également l’influence de <strong>la</strong> pro<strong>la</strong>ctine.PharmacocinétiqueLa cabergoline est résorbée à 80% après administration orale, sa demi-vie estde 17 à 24 h. La <strong>du</strong>rée d’action maximale débute 18 à 24 h après ingestion orale.La métergoline a une demi-vie d’environ 4 h, <strong>la</strong> <strong>du</strong>rée d’action maximale débuteenviron 2 à 4 h après ingestion orale.Contre-indicationsIl n’y a pas de contre-indication majeure à l’utilisation des antipro<strong>la</strong>ctiniques hormisune gestation souhaitée.Effets indésirablesCertains effets indésirables comme de <strong>la</strong> somnolence, de l’anorexie, des vomissementspeuvent parfois être observés. L’administration <strong>du</strong> médicament avecl’alimentation peut prévenir les vomissements. Lorsque l’administration d’unantiémétique est nécessaire, celui-ci ne doit pas avoir d’effet pro<strong>la</strong>ctotrope. Lemétoclopramide est donc à exclure. Les symptômes psychotiques, liés à <strong>la</strong> stimu<strong>la</strong>tiondes récepteurs dopaminergiques centraux, sont rares aux posologiesrecommandées. Les neuroleptiques qui ont des propriétés antidopaminergiques,notamment <strong>la</strong> métopimazine, peuvent être utilisés pour atténuer les effets indésirables.L’utilisation de <strong>la</strong> métergoline peut causer des troubles de comportementliés à son action antisérotoninergique centrale. Ces troubles disparaissent aprèsré<strong>du</strong>ction de <strong>la</strong> dose ou après l’arrêt <strong>du</strong> traitement. L’utilisation de <strong>la</strong> cabergolinepourrait engendrer des changements de couleur <strong>du</strong> poil.InteractionsCes médicaments pouvant être hypotenseurs, l’administration simultanée avecd’autres substances partageant les mêmes propriétés devra se faire avec précaution.Les antagonistes de <strong>la</strong> dopamine (métoclopramide, phénothiazines) ne sontpas recommandés étant donné leurs effets pro<strong>la</strong>ctotropes marqués.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser pendant <strong>la</strong> gestation (avortement).2.1.9.1 CabergolineLMR cabergoline : GALASTOP (Ceva Santé Animale)cabergoline: 0,05 mg/mlsolution poPosologie:Ca, Fe: 0,1 ml/kg pj (4 - 6 j)recommencer le traitement en cas derechutef<strong>la</strong>con 7 ml, 15 ml, 24 mlR/KELACTIN 50 mcg/ml (Ke<strong>la</strong> Laboratoria)cabergoline: 50 mcg/mlsolution poPosologie:Ca, Fe: 5 mcg/kg pj (4 - 6 j)f<strong>la</strong>con 7 ml, 15 ml, 24 mlR/
2 MÉDICAMENTS DU SYSTÈME HORMONAL 852.1.9.2 MétergolineLMR métergoline : CONTRALAC 0,5 (Virbac)métergoline: 0,5 mgcomprimé poPosologie:Ca: 0,2 mg/kg pj (en 2 prises) (4 j)caps 16R/CONTRALAC 2 (Virbac)métergoline: 2 mgcomprimé poPosologie:Ca: 0,2 mg/kg pj (en 2 prises) (4 j)caps 16R/2.1.10 AntiprogestagènesIndicationsCarnivores:Les indications thérapeutiques de l’aglépristone sont l’empêchement de <strong>la</strong> nidationet l’interruption de <strong>la</strong> gestation chez les chiennes jusqu’au 45ème jour aprèsune saillie non désirée. Lorsque le traitement est mis en œuvre avant <strong>la</strong> nidationde l’embryon au niveau de l’endomètre, par exemple au lendemain de <strong>la</strong> saillie,l’aglépristone empêche <strong>la</strong> nidation et provoque <strong>la</strong> résorption embryonnaire.Chez <strong>la</strong> chienne confirmée gestante, le traitement entraîne l’avortement dans unintervalle de 3 à 7 jours. Cet avortement peut s’accompagner des signes physiologiquesqui précèdent une mise bas normale (légère anorexie, gonflementdes mamelles, chute de <strong>la</strong> température corporelle, …). Chez certaines chiennes(5%), l’avortement peut être incomplet et un examen clinique de contrôle est doncrecommandé afin de confirmer <strong>la</strong> vacuité utérine. Ce contrôle doit être effectuéenviron 10 jours après le traitement. Le prochain œstrus peut apparaître 1 à 3mois plus tôt que prévu. La fertilité lors des périodes d’œstrus suivantes ne seraitpas modifiée. Dans tous les cas, un monitoring de l’animal traité doit être mis enœuvre pour éviter toute complication liée à l’interruption de gestation.PharmacodynamieL’aglépristone est un stéroïde de synthèse dont l’action antiprogestagène s’exerce parliaison aux récepteurs endométriaux à <strong>la</strong> progestérone mais sans activer cependantde réponse biologique. In vitro, l’affinité de l’aglépristone pour les récepteurs progestéroniquesest trois fois plus élevée que pour <strong>la</strong> progestérone naturelle qui prépare etmaintient <strong>la</strong> gestation. Il est à noter que <strong>du</strong>rant le traitement, <strong>la</strong> progestéronémie resteà des taux physiologiques avant de s’effondrer suite à l’interruption de gestation.PharmacocinétiqueLe traitement consiste en deux injections par voie sous-cutanée à 24h d’intervalle.La concentration maximale d’aglépristone dans le p<strong>la</strong>sma est atteinte environ 2,5jours après <strong>la</strong> seconde injection. L’excrétion de <strong>la</strong> molécule se fait de manière trèslente et principalement par les fèces. 60% de <strong>la</strong> dose administrée est éliminé dansles 10 premiers jours, et 80% dans un intervalle de 24 jours.Contre-indicationsIl est préférable de ne pas traiter avec le pro<strong>du</strong>it ci-dessous:- les animaux souffrant de ma<strong>la</strong>dies hépatiques ou rénales,- les animaux souffrant <strong>du</strong> diabète mellitus,- les animaux souffrant d’hypoadrénocorticisme,- les animaux en mauvais état de santé général.Effets indésirables- Brève réaction locale possible après injection <strong>du</strong> médicament.- L’avortement peut s’accompagner des symptômes apparaissant lors d’unemise bas normale.- Infections de l’utérus.- Raccourcissement de 1 à 3 mois de l’intervalle précédant les prochaineschaleurs.- Modifications hématologiques et biochimiques de nature passagère.
862 MÉDICAMENTS DU SYSTÈME HORMONALInteractionsDes interactions avec le kétoconazole, l’itraconazole ou l’érythromycine sont possibles.L’aglépristone ayant une action anti-glucocorticoïde, il pourrait influencerun traitement à base de glucocorticoïdes.Précautions particulières/Risques pour l’hommeCe médicament contenant un excipient huileux, l’injection accidentelle <strong>du</strong> médicamentchez l’homme peut provoquer une irritation au niveau <strong>du</strong> site d’injection.Une (auto-) injection accidentelle peut représenter un réel danger chez <strong>la</strong> femmeenceinte. Dans les deux cas, il est indispensable de consulter un médecin.Repro<strong>du</strong>ction et <strong>la</strong>ctationCe médicament n’est pas destiné à être administré aux animaux gestants ou <strong>la</strong>ctants(sauf en cas d’interruption de gestation souhaitée). Le traitement n’a généralementpas d’influence sur <strong>la</strong> fertilité lors des manifestations œstrales suivantes.Il a été démontré que l’intervalle interœstrus était ré<strong>du</strong>it significativement aprèstraitement à l’aglépristone.2.1.10.1 AglépristoneLMR aglépristone : ALIZIN 30 mg/ml (Virbac)aglépristone: 30 mg/mlsolution injectable scPosologie:Ca: 2 x 10 mg/kg à 24 h d’intervallef<strong>la</strong>con 10 mlR/2.2 Hormones cortico-surrénalesLes préparations reprises dans ce chapitre et contenant des glucocorticoïdes desynthèse sont destinées à un usage systémique. Rappelons que l’utilisation deces substances chez les animaux pro<strong>du</strong>cteurs de denrées alimentaires et chezle pigeon est soumise à une légis<strong>la</strong>tion stricte et spécifique. Les glucocorticoïdesdisponibles ne diffèrent entre eux que par l’activité anti-inf<strong>la</strong>mmatoire et métaboliquepar unité de poids (puissance), par leur pouvoir minéralocorticoïde et parleur <strong>du</strong>rée d’action.Les glucocorticoïdes sont également abordés dans les chapitres (11.1.1.) 12.1.6,12.1.8 et 12.3.IndicationsLes indications générales des glucocorticoïdes sont les suivantes:- traitement symptomatique des ma<strong>la</strong>dies dans lesquelles des processus immunitairesou inf<strong>la</strong>mmatoires, aigus ou chroniques, sont en cause,- immunosuppression,- insuffisance surrénalienne.Les circonstances cliniques déterminent le choix <strong>du</strong> principe actif, de <strong>la</strong> forme galéniqueet de <strong>la</strong> posologie, qui peut être très variable selon les cas. Par exemple,<strong>la</strong> prednisolone sous forme soluble est parfois préconisée jusqu’à 20 fois <strong>la</strong> doseanti-inf<strong>la</strong>mmatoire normalement utilisée, pour contrôler les œdèmes inf<strong>la</strong>mmatoiresaigus <strong>du</strong> système nerveux central, mais pendant une période très limitée. En casde choc anaphy<strong>la</strong>ctique, des doses massives de glucocorticoïdes doivent êtreadministrées de manière ponctuelle, par voie intraveineuse. Les pathologies inf<strong>la</strong>mmatoireschroniques impliquent parfois des traitements de longue <strong>du</strong>rée mais desposologies les plus faibles possibles. L’immunosuppression nécessite d’adapterles doses, souvent élevées, en fonction de <strong>la</strong> réponse <strong>du</strong> patient. Les traitementsde substitution préconisés dans les cas d’insuffisance surrénalienne nécessitent lerecours à l’hydrocortisone, disponible sous forme de médicament à usage humain,à <strong>la</strong>quelle on peut associer un minéralocorticoïde comme <strong>la</strong> fluorocortisone.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 87PharmacodynamieLes glucocorticoïdes agissent au niveau de <strong>la</strong> plupart des systèmes et influencentun très grand nombre de fonctions physiologiques. Ceci entraîne, hormis denombreux effets indésirables décrits plus loin, un certain nombre d’effets thérapeutiquesintéressants. Les glucocorticoïdes disponibles en Belgique diffèrent en<strong>du</strong>rée d’action et en puissance. L’activité minéralocorticoïde de <strong>la</strong> prednisolone estmoindre que celle de <strong>la</strong> cortisone. Elle est encore moins prononcée pour les autressubstances synthétiques. Cette activité peut être responsable de rétention sodée.La <strong>du</strong>rée d’action des glucocorticoïdes de synthèse est plus longue que celle del’hydrocortisone. Ajoutons que <strong>la</strong> forme galénique est également déterminante àcet égard et que certaines préparations peuvent agir pendant plusieurs semaines.PharmacocinétiquePour éviter l’apparition d’effets indésirables, divers critères doivent orienter lechoix de <strong>la</strong> thérapie à mettre en p<strong>la</strong>ce. Le premier critère de choix porte sur <strong>la</strong>forme galénique. En ce qui concerne les formes administrables par voie parentérale,il faut distinguer les solutions des suspensions microcristallines. L’avantagedes solutions est de pouvoir être administrées par voie intraveineuse afin d’in<strong>du</strong>ireun effet immédiat ou rapide. La cinétique est celle <strong>du</strong> principe actif. Il s’agit despréparations idéales pour les traitements d’urgence, y compris celui <strong>du</strong> choc.On distingue c<strong>la</strong>ssiquement: les glucocorticoïdes à <strong>du</strong>rée d’action courte (< 12 h): hydrocortisone les glucocorticoïdes à <strong>du</strong>rée d’action moyenne (12 - 36 h): prednisolone les glucocorticoïdes à <strong>du</strong>rée d’action longue (> 36 h): dexaméthasoneD’une manière générale, il est à noter que les <strong>du</strong>rées d’action réelles des médicamentspeuvent être plus longues que celle mentionnées dans les notices (RCP),le plus souvent déterminées en fonction de paramètres cinétiques. Ces derniersne sont pas toujours prédictifs des effets qui peuvent se prolonger après <strong>la</strong> disparition<strong>du</strong> corticoïde au niveau sérique. Des informations précises peuvent êtredemandées aux titu<strong>la</strong>ires d’enregistrement à ce sujet. Les suspensions sont despréparations injectables par voie sous-cutanée, qui se caractérisent par uneabsorption parfois très lente. Ces préparations sont à proscrire pour <strong>la</strong> thérapiede substitution et devraient être évitées pour les traitements continus des affectionschroniques. La répétition des injections, couplée à <strong>la</strong> difficulté de contrôlede <strong>la</strong> cinétique, peut aboutir à des effets indésirables. Les suspensions devraienttoujours être réservées à des traitements uniques lorsque des effets transitoiressont souhaités. Si les administrations doivent être répétées quelques fois, ellesdoivent être suffisamment espacées pour éviter le phénomène de bio-accumu<strong>la</strong>tion.Il n’en reste pas moins que, dans certaines pathologies, l’usage continud’anti-inf<strong>la</strong>mmatoires stéroïdiens ne peut être évité comme par exemple, pour lesthérapies substitutives, immunosuppressives, le traitement symptomatique desinf<strong>la</strong>mmations chroniques et des ma<strong>la</strong>dies d’origine allergique. Dans tous ces cas,une thérapie orale doit être instaurée selon un schéma posologique qui visera àrechercher <strong>la</strong> plus petite dose efficace, par ailleurs très variable selon l’objectifthérapeutique. L’administration alternée, un jour sur deux, diminue davantageencore le risque d’une insuffisance surrénalienne. Avec un tel schéma, on perdcependant dans certaines affections l’effet voulu, le jour où le glucocorticoïden’est pas administré. Cette posologie doit être régulièrement évaluée et ajustéeen fonction de l’état clinique <strong>du</strong> patient. La combinaison d’anti-inf<strong>la</strong>mmatoiresstéroïdiens à d’autres anti-inf<strong>la</strong>mmatoires comme les antihistaminiques, les huilesessentielles et les thérapies de désensibilisation peuvent être utiles en dermatologie.Le risque accru d’infections doit éventuellement être contrôlé par uneantibiothérapie faisant idéalement appel à des bactéricides.Contre-indicationsLes contre-indications découlent des effets indésirables (voir ci-dessous).Effets indésirablesL’usage inadéquat de ces substances in<strong>du</strong>it des effets indésirables graves, parfoismortels. Chez les carnivores, les intoxications par les anti-inf<strong>la</strong>mmatoiresreprésentent une part importante de <strong>la</strong> pharmacovigi<strong>la</strong>nce. L’usage de doses élevéeset <strong>la</strong> prolongation des traitements sont des facteurs de risque majeurs pourl’in<strong>du</strong>ction des effets indésirables. Le tableau clinique associé à un surdosage estcelui <strong>du</strong> syndrome de Cushing, qualifié dans ce cas, d’iatrogène:
882 MÉDICAMENTS DU SYSTÈME HORMONAL- rétention hydro-sodée. Elle peut être évitée par l’utilisation de corticoïdes auxpropriétés minéralocorticoïdes moins prononcées;- faiblesse muscu<strong>la</strong>ire et troubles <strong>du</strong> rythme cardiaque liés à l’hypokaliémie;- hyperglycémie. Les glucocorticoïdes peuvent aggraver ou déclencher un diabètesucré;- effet catabolique (fonte muscu<strong>la</strong>ire);- redistribution des graisses;- polyurie, polydipsie, polyphagie;- ostéoporose (fracture spontanée);- fragilisation tendineuse et ligamentaire;- ulcère de <strong>la</strong> cornée;- immunosuppression et altération de <strong>la</strong> formule sanguine. Une résistanceamoindrie aux agents infectieux peut être constatée ainsi qu’une réactivationde certaines pathologies virales;- ulcère gastrique (synergie avec les anti-inf<strong>la</strong>mmatoires non stéroïdiens);- g<strong>la</strong>ucome;- avortement;- tératogenèse;- érosion des surfaces articu<strong>la</strong>ires, avec risque de lésions articu<strong>la</strong>ires;- inhibition de l’axe hypotha<strong>la</strong>mo-hypophyso-surrénalien. Une insuffisance surrénaliennepeut se manifester à l’arrêt <strong>du</strong> traitement ou lors d’un stress intense,par exemple chirurgical, traumatique ou infectieux. Après un traitement prolongé,<strong>la</strong> ré<strong>du</strong>ction progressive de <strong>la</strong> posologie est <strong>la</strong> règle générale pour éviterce type de problème.- retard de cicatrisation;- atrophie cutanée. L’application topique de corticoïdes très puissants représenteun risque particulier à cet égard.InteractionsDe nombreuses interactions des glucocorticoïdes avec d’autres médicamentssont connues, dont voici les plus importantes:- l’administration simultanée avec des AINS augmente les risques d’érosionsgastriques,- de l’hypokaliémie peut apparaître en cas d’usage concomitant avec des diurétiquesqui ne sont pas des diurétiques d’épargne potassique (à l’exemple <strong>du</strong>furosémide),- ils accroissent le risque d’une action toxique des glycosides digitaliques,- les besoins en insuline peuvent augmenter,- les vaccinations doivent être postposées.Précautions particulièresLe caractère symptomatique de <strong>la</strong> corticothérapie ne doit jamais être oublié. Lemédecin vétérinaire doit tout mettre en œuvre pour rechercher l’étiologie de l’affectionet mettre en p<strong>la</strong>ce, si possible, un traitement étiologique. La dose utiliséedoit être aussi basse que possible, et <strong>la</strong> <strong>du</strong>rée de traitement aussi courte quepossible. Après un usage prolongé, l’arrêt de <strong>la</strong> thérapie se fait progressivement.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation pendant <strong>la</strong> gestation n’est pas sûre. Chez les grands animaux, l’administrationde glucocorticoïdes en fin de gestation peut provoquer un avortementou une mise bas précoce.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 892.2.1 DexaméthasoneDurée d’action longue (> 36 h), pas d’activité minéralocorticoïde. Puissance30 fois plus élevée que celle de <strong>la</strong> cortisone.LMR dexaméthasone: RAPIDEXON 2 mg/ml sol inj (Eurovet A.H.)dexaméthasone (phosphate sodique): 2 mg/mlDEXA 0,2 % (Ke<strong>la</strong> Laboratoria)solution injectable im (Eq, Bo, Su, Ca, Fe), iv,iartic, intrabursale, locale (Eq)dexaméthasone (phosphate sodique): 2 mg/mlPosologie:solution injectable im , ivinf<strong>la</strong>mmation, allergie:Posologie:Eq, Bo, Su: 0,06 mg/kg (toutes les 24 - 48 h)Bo: 1 x 0,02 - 0,04 mg/kgCa, Fe: 0,1 mg/kg (toutes les 24 - 48 h)Viande: 21 j, Lait: 84 h (7 traites)Bo: cétose prim: 0,02 - 0,04 mg/kg (peutf<strong>la</strong>con 100 mlêtre répété après 48 h)R/Bo: in<strong>du</strong>ction mise bas: 0,04 mg/kg (peutêtre répété après 48 - 72 h)Eq: arthrite, bursite, ténosynovite: inj locale1 - 5 mlViande: Eq: 11 j, Bo: 7 j, Su: 2 j, Lait: 72 hf<strong>la</strong>con 25 ml, 50 ml, 100 mlR/DEXAFORT (MSD A.H.)dexaméthasone (phosphate sodique): 1 mg/mldexaméthasone (phénylpropionate): 2 mg/mlsuspension injectable im (Bo, Ca), sc (Ca)Posologie:Bo: 0,06 mg/kgCa: 0,3 mg/kgViande: 63 j, Lait: 14 traitesf<strong>la</strong>con 50 mlR/DEXA-JECT 2 mg/ml (Dopharma)dexaméthasone (phosphate de disodium):2 mg/mlsolution injectable iv (Eq), im (Eq, Bo, Su, Ca,Fe), iartic (Eq)Posologie:- inf<strong>la</strong>mmation ou allergie:Eq, Bo, Su: 0,06 mg/kgCa, Fe: 0,1 mg/kgpeut être répété à 24-48 h d’intervalle- acétonémie: Bo: 0,02 à 0,04 mg/kg, dosepeut être répétée après 48 h- in<strong>du</strong>ction parturition: Bo: 1 x 0,04 mg/kg,dose peut être répétée après 48-72 h- arthrite, bursite ou ténosynovite: Eq (iartic):1-5 mlViande et abats: Eq: 12 j, Bo: 8 j, Su: 2 jLait: Bo: 72 h, ne pas administrer aux Eq dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 ml, 100 mlR/DEXAMETHASONE 0,5 % Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)dexaméthasone: 5 mg/mlsuspension injectable imPosologie:Ca: 0,1 - 0,4 mg/kg, répéter si nécessaireaprès 2 jf<strong>la</strong>con 50 mlR/VETODEXIN 0,2 % (VMD)dexaméthasone (phosphate sodique): 2 mg/mlsolution injectable imPosologie:Bo: acétonémie: 10 - 20 mg pjin<strong>du</strong>ction mise bas: 20 mgCa: allergie: 0,1 - 0,4 mg/kg pjViande: 16 j, Lait: 3 jf<strong>la</strong>con 50 ml, 100 mlR/VOREN (Boehringer Ingelheim)dexaméthasone-21-isonicotinate: 1 mg/mlsuspension injectable im, scPosologie:Ca, Fe: 0,05 - 0,1 mg/kgf<strong>la</strong>con 50 mlR/
902 MÉDICAMENTS DU SYSTÈME HORMONAL2.2.2 MéthylprednisoloneDurée d’action moyenne (12 – 36 h), activité minéralocorticoïde négligeable.Puissance 6 fois plus élevée que celle de <strong>la</strong> cortisone.LMR méthylprednisolone : MODERIN compr 4 mg (Pfizer A.H.)méthylprednisolone: 4 mgcomprimé poPosologie:Ca, Fe:- (1 - 5 kg PV): 1 mg- (5 - 9 kg PV): 2 mg- (9 - 18 kg PV): 2 - 4 mg- (18 - 36 kg PV): 4 - 8 mgcompr 30, 10 x 10R/MODERIN compr 16 mg (Pfizer A.H.)méthylprednisolone: 16 mgcomprimé poPosologie:Ca, Fe:- (1 - 5 kg PV): 1 mg- (5 - 9 kg PV): 2 mg- (9 - 18 kg PV): 2 - 4 mg- (18 - 36 kg PV): 4 - 8 mgcompr 30, 10 x 10R/PREDNISOLONE 2,5 % (VMD)prednisolone: 25 mg/mlsolution injectable imPosologie:Ca (PV > 3 kg) dose de départ:0,5 - 2,5 mg/kgdiminuer jusqu’à dose d’entretien effectivef<strong>la</strong>con 50 mlR/PREDNISOLONE 5 mg Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)prednisolone: 5 mgcomprimé poPosologie:Ca: affection inf<strong>la</strong>mmatoire, allergique:- dose d‘attaque: 0,5 - 1 mg/kg pj (en 2prises) (3 - 7 j), puis 1 mg/kg pj en 1 prise(7 j), ensuite ré<strong>du</strong>ire <strong>la</strong> dose de moitié tousles 5 – 7 j- dose d‘entretien: 1 mg/kg/2 jré<strong>du</strong>ire <strong>la</strong> dose progressivement jusqu‘à <strong>la</strong>dose minimale effectivema<strong>la</strong>die auto-immune: 2 – 6 mg/kg pj (en2 prises), puis ré<strong>du</strong>ire progressivementjusqu‘à dose effective/2 jcompr 30, 100R/MODERIN compr 32 mg (Pfizer A.H.)méthylprednisolone: 32 mgcomprimé poPosologie:Ca, Fe:- (1 - 5 kg PV): 1 mg- (5 - 9 kg PV): 2 mg- (9 - 18 kg PV): 2 - 4 mg- (18 - 36 kg PV): 4 - 8 mgcompr 30, 20 x 10R/MODERIN LA 40 mg/ml (Pfizer A.H.)méthylprednisolone acétate: 40 mg/mlsuspension injectable im, iarticPosologie:- admin systémique:Ca: 0,5 - 2 mg/kg PVFe: 2 - 5 mg/kg PV- admin locale:Ca: 0,5 - 2 mg/kg PV (iartic)f<strong>la</strong>con 5 mlR/2.2.3 PrednisoloneDurée d’action moyenne (12 – 36 h), activité minéralocorticoïde modéréevoire faible. Puissance 5 fois plus élevée que celle de <strong>la</strong> cortisone.LMR prednisolone: PREDNISOLONE 20 mg Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)prednisolone: 20 mgPREDNISOLONE 1 % (VMD)comprimé poPosologie:prednisolone: 10 mg/mlCa: affection inf<strong>la</strong>mmatoire, allergique:solution injectable im, iartic, périartic- dose d‘attaque: 0,5 - 1 mg/kg pj (en 2Posologie:prises) (3 - 7 j), puis 1 mg/kg pj en 1 priseCa: 0,5 - 2,5 mg/kg(7 j), ensuite ré<strong>du</strong>ire <strong>la</strong> dose de moitié tousdiminuer jusqu’à dose d’entretien effectiveles 5 – 7 jf<strong>la</strong>con 100 ml- dose d‘entretien: 1 mg/kg/2 jR/ré<strong>du</strong>ire <strong>la</strong> dose progressivement jusqu‘à <strong>la</strong>dose minimale effectivema<strong>la</strong>die auto-immune: 2 – 6 mg/kg pj (en2 prises), puis ré<strong>du</strong>ire progressivementjusqu‘à dose effective/2 jcompr 30, 100R/SOLU-DELTA-CORTEF 500 mg (Pfizer A.H.)prednisolone (succinate sodique): 500 mg/10 mlsolution stérile injectable im, ivPosologie:Bo (hors <strong>la</strong>ctation): max 1 mg/kg (iv)Ca (choc): 5 - 10 mg/kg (iv)Ca: 0,5 - 2 mg/kg (im)Viande: 1 jf<strong>la</strong>con 10 mlR/
2 MÉDICAMENTS DU SYSTÈME HORMONAL 912.3 Médicament utilisé en cas d’hypercorticismechez le chien (ma<strong>la</strong>die de Cushing)2.3.1 TrilostaneIndicationsTraitement de l’hypercorticisme d’origine hypophysaire (ma<strong>la</strong>die de Cushing) oud’origine surrénalienne (syndrome de Cushing primaire) chez le chien.PharmacodynamieLe trilostane inhibe l’enzyme 3-bêta-hydroxystéroïde-déhydrogénase et donc <strong>la</strong>synthèse de différentes hormones stéroïdiennes telles que le cortisol et l’aldostérone.L’inhibition est réversible et dose-dépendante. L’effet <strong>du</strong> trilostane sur <strong>la</strong>stéroïdogénèse gonadique n’est important qu’à haute dose.PharmacocinétiqueChez le chien, l’absorption <strong>du</strong> trilostane après administration orale est bonne bienque variable. La concentration sérique maximale est atteinte après 1.5 – 2 h. Lanotice conseille d’administrer le médicament avec l’alimentation. L’action <strong>du</strong> trilostaneest de courte <strong>du</strong>rée ; certaines publications y voient l’explication de l’absencede réaction chez certains chiens après l’administration de <strong>la</strong> dose uniquerecommandée par jour. Le trilostane est métabolisé par le foie, entre autres enkétotrilostane actif. L’index thérapeutique <strong>du</strong> trilostane dépasse celui <strong>du</strong> mitotane.La dose d’attaque sera ajustée en fonction des résultats des tests de stimu<strong>la</strong>tionde l’ACTH effectués régulièrement (10 jours, 4 semaines et 12 semaines après ledébut de <strong>la</strong> thérapie, ensuite tous les 3 mois). La dose initiale mentionnée dans <strong>la</strong>notice est plus élevée que <strong>la</strong> dose initiale recommandée par le Vetoryl ConsensusMeeting (Amsterdam) (voir Folia Veterinaria 2008 n° 1).Contre-indicationsNe pas utiliser chez les chiens atteints d’une ma<strong>la</strong>die hépatique primaire et/ousouffrant d’insuffisance rénale ; ni chez les chiens pesant moins de 3 kg.Effets indésirablesLe trilostane est re<strong>la</strong>tivement bien toléré par le chien. Les effets indésirables sontassez rares. Des symptômes associés à une insuffisance surrénalienne iatrogènetels qu’une faiblesse, une léthargie, une anorexie, des vomissements ou des diarrhéespeuvent être observés. Ces signes disparaissent généralement à l’arrêt <strong>du</strong>traitement. Une crise addissonienne aiguë (choc) peut aussi se pro<strong>du</strong>ire. Quelquesrares cas isolés de nécrose de <strong>la</strong> g<strong>la</strong>nde surrénale ont été observés chez deschiens traités, pouvant aboutir à une insuffisance surrénalienne. Une insuffisancerénale subclinique peut évoluer vers une insuffisance clinique suite à un traitementau trilostane. Une polyarthrite subclinique peut être révélée et évoluer versune arthrite symptomatique en raison de <strong>la</strong> ré<strong>du</strong>ction des quantités circu<strong>la</strong>ntesde corticostéroïdes endogènes. Il existe quelques descriptions de morts subitessous traitement. D’autres effets indésirables de faible intensité et rares commeune ataxie, une hypersalivation, de l’œdème, des tremblements muscu<strong>la</strong>ires etdes altérations cutanées peuvent apparaître.InteractionsOn évitera l’usage simultané avec des diurétiques d’épargne potassique (comme <strong>la</strong>spirono<strong>la</strong>ctone par exemple), le trilostane pouvant provoquer une hyperkaliémie enraison de son action inhibitrice sur <strong>la</strong> synthèse de l’aldostérone. L’activité des IECApeut être renforcée. D’autres molécules diminuant le taux de cortisol (le mitotane, lekétoconazole, l’aminoglutéthimide) renforcent l’action <strong>du</strong> trilostane, pouvant engendrerainsi de l’hypoadrénocorticisme (voir aussi « Précautions particulières »).Précautions particulières/Risques pour l’hommeEtant donné que l’hypercorticisme touche principalement les chiens âgés, il est importantde vérifier l’absence de ma<strong>la</strong>die hépatique primaire ou d’insuffisance rénaleavant et pendant le traitement (voir « Contre-indications »). La présence simultanéed’un diabète sucré requiert un traitement spécifique. En cas de traitement préa<strong>la</strong>bleau mitotane, <strong>la</strong> notice conseille de respecter un intervalle d’au moins un mois entrel’arrêt <strong>du</strong> mitotane et le début <strong>du</strong> traitement avec le trilostane. Les chiens pouvantêtre plus sensibles aux effets <strong>du</strong> trilostane après un traitement au mitotane,
922 MÉDICAMENTS DU SYSTÈME HORMONALune étroite surveil<strong>la</strong>nce de <strong>la</strong> fonction surrénalienne est conseillée. Chez les chiensatteints d’une anémie préexistante, une ré<strong>du</strong>ction supplémentaire de l’hématocriteet de l’hémoglobine pourrait survenir. Le trilostane peut entraîner une diminution de<strong>la</strong> synthèse de testostérone et a des propriétés anti-progestérone. Les femmes enceintesou susceptibles de l’être doivent éviter de manipuler les gélules. Le contenudes gélules peut provoquer des irritations et une hypersensibilité cutanées et ocu<strong>la</strong>ires.Il ne faut donc pas fractionner ni ouvrir les gélules.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser chez les chiennes gestantes ou al<strong>la</strong>itantes ou chez les animauxdestinés à <strong>la</strong> repro<strong>du</strong>ction.LMR trilostane : VETORYL 10 mg (Dechra)trilostane: 10 mgcapsules po avec l’alimentationPosologie:Ca: dose d’attaque: 1 x 6 mg/kg pjadapter ensuite <strong>la</strong> dose en fonction de <strong>la</strong>réactioncaps 3 x 10R/VETORYL 30 mg (Dechra)trilostane: 30 mgcapsules po avec l’alimentationPosologie:Ca: dose d’attaque: 1 x 6 mg/kg pjadapter ensuite <strong>la</strong> dose en fonction de <strong>la</strong>réactioncaps 3 x 10R/VETORYL 60 mg (Dechra)trilostane: 60 mgcapsules po avec l’alimentationPosologie:Ca: dose d’attaque: 1 x 6 mg/kg pjadapter ensuite <strong>la</strong> dose en fonction de <strong>la</strong>réactioncaps 3 x 10R/2.4 Médicaments contre le dysfonctionnement<strong>du</strong> lobe intermédiaire de l’hypophyse chez lecheval (ma<strong>la</strong>die de Cushing)2.4.1 PergolideIndicationTraitement symptomatique des signes cliniques associés au “Dysfonctionnement<strong>du</strong> Lobe Intermédiaire de l’Hypophyse » (Pituitary Pars Intermedia Dysfunction -PPID) (ma<strong>la</strong>die de Cushing chez le cheval).PharmacodynamieLe pergolide, un dérivé synthétique de l’ergot de seigle, est un puissant agonistedes récepteurs de <strong>la</strong> dopamine. Il diminue, au niveau de <strong>la</strong> pars intermedia, lestaux p<strong>la</strong>smatiques d’ACTH, de MSH et des autres peptides précurseurs des hormonespolypetitidiques (pro-opiomé<strong>la</strong>nocortine). Comme les autres agonistesdopaminergiques, le pergolide inhibe <strong>la</strong> sécrétion de pro<strong>la</strong>ctine. Aux doses thérapeutiques,le pergolide a peu ou pas d’effet sur les voies noradrénergiques,adrénergiques ou sérotoninergiques.PharmacocinétiqueLes études pharmacocinétiques disponibles chez le cheval indiquent que le pergolideest rapidement absorbé et qu’il semble très rapidement éliminé. Néanmoins,les données révèlent surtout une grande variabilité, en partie <strong>du</strong>e à des aspectsméthodologiques.Effets indésirablesSudation, perte d’appétit, anorexie et léthargie transitoires, signes légers affectantle système nerveux central (légères dépression et ataxie par exemple), diarrhée etcoliques. Si des signes d’intolérance apparaissent, le traitement devra être arrêtépendant 2 à 3 jours et réinstauré à demi-dose. La dose journalière totale pourraensuite être ajustée en l’augmentant de 0,5 mg toutes les 2 à 4 semaines jusqu’àobtention de l’effet clinique souhaité.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 93Contre-indicationsNe pas administrer en même temps que des antagonistes de <strong>la</strong> dopamine, telsque les neuroleptiques comme l’acépromazine <strong>du</strong> groupe des phénothiazines, <strong>la</strong>dompéridone ou le métoclopramide; ces molécules étant susceptibles de ré<strong>du</strong>irel’efficacité <strong>du</strong> pergolide.InteractionsL’administration concomitante d’autres médicaments affectant <strong>la</strong> liaison aux protéinesp<strong>la</strong>smatiques peut accroître <strong>la</strong> toxicité <strong>du</strong> médicament. La combinaisonavec des antagonistes de <strong>la</strong> dopamine est contre-indiquée.Précautions particulières/Risques pour l’hommeDe nombreuses précautions d’usage sont décrites dans le RCP de ce médicament.Parmi les plus importantes, on peut noter que :- ce pro<strong>du</strong>it peut causer une irritation ocu<strong>la</strong>ire, olfactive ou des maux de tête aprèsdécoupe <strong>du</strong> comprimé qui ne pourra en aucun cas être écrasé.- il est impératif de minimiser les risques d’exposition lors de <strong>la</strong> section des compriméset d’éviter tout contact avec les yeux et l’inha<strong>la</strong>tion lors de <strong>la</strong> manipu<strong>la</strong>tiondes comprimés et de se <strong>la</strong>ver les mains après utilisation.- les femmes enceintes ou en période d’al<strong>la</strong>itement doivent porter des gants pouradministrer le pro<strong>du</strong>it.- en cas de contact avec <strong>la</strong> peau, il est impératif de <strong>la</strong>ver à l’eau <strong>la</strong> partie exposée.En cas d’exposition ocu<strong>la</strong>ire au pergolide, rincer immédiatement l’œil atteintavec de l’eau et demander conseil à un médecin. En cas d’irritation nasale, respirerde l’air frais et demander conseil à un médecin si des difficultés respiratoiresapparaissent.- les enfants ne doivent pas être mis en contact <strong>du</strong> médicament. Une ingestionaccidentelle peut causer des effets indésirables, spécialement chez les enfants.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie chez les juments gravides. Des étudesde <strong>la</strong>boratoire sur souris et <strong>la</strong>pins n’ont pas mis en évidence d’effets tératogènes.Une ré<strong>du</strong>ction de <strong>la</strong> fertilité a été observée chez les souris à partir de 5,6 mg/kgpar jour.L’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie chez les juments en <strong>la</strong>ctation. Chez lessouris, une ré<strong>du</strong>ction <strong>du</strong> poids corporel et des taux de survie de <strong>la</strong> descendanceont été attribués à l’inhibition pharmacologique de <strong>la</strong> sécrétion de pro<strong>la</strong>ctine, entraînantune chute de <strong>la</strong>ctation.L’extrapo<strong>la</strong>tion de ces données au cheval sont hasardeuses.LMR pergolide: PRASCEND 1 mg (Boehringer IngelheimVetmedica)pergolide (mési<strong>la</strong>te): 1 mgcomprimé poPosologie:Eq (âge > 2 ans): dose initiale: 2 mcg/kg pjadapter ensuite <strong>la</strong> dose en fonction de <strong>la</strong>réponse cliniqueNe pas administrer aux chevaux destinés à <strong>la</strong>consommation humaineNe pas administrer aux juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainecompr 60, 160R/
942 MÉDICAMENTS DU SYSTÈME HORMONAL2.5 Médicaments de <strong>la</strong> thyroïde2.5.1 Hormone thyroïdienneIndicationHypothyroïdie chez le chien.PharmacodynamieLa lévothyroxine (L-thyroxine, L-T4) agit comme précurseur de <strong>la</strong> liothyronine ouT3 (tri-iodothyronine), <strong>la</strong> forme biologique active de l’hormone thyroïdienne.PharmacocinétiqueLa lévothyroxine (L-thyroxine, L-T4) est administrée par voie orale. La résorptionvarie de 10 à 50 % et <strong>la</strong> demi-vie d’élimination est de 12 à 16 heures (l’action <strong>du</strong>replus longtemps) chez le chien. La métabolisation siège principalement dans le foieet l’excrétion s’effectue par <strong>la</strong> bile et les urines.Contre-indications- Infarctus <strong>du</strong> myocarde aigu.- Thyrotoxicose.- Hypoadrénocorticisme non traité.Effets indésirablesDes effets indésirables apparaissent en cas de surdosage.Interactions- La lévothyroxine renforce l’action de l’adrénaline et de <strong>la</strong> noradrénaline, ainsique celle d’autres catécho<strong>la</strong>mines et sympaticomimétiques.- En accélérant <strong>la</strong> dégradation des facteurs de coagu<strong>la</strong>tion vitamineK-dépendants, elle renforce l’action des anticoagu<strong>la</strong>nts tels que <strong>la</strong> warfarine.- Les besoins en insuline pouvant être modifiés, un suivi précis est nécessaire.- Les œstrogènes augmentent les besoins en lévothyroxine.- Les effets thérapeutiques de <strong>la</strong> digoxine et de <strong>la</strong> digitoxine peuvent diminuer.- L’usage simultané de <strong>la</strong> kétamine peut engendrer de <strong>la</strong> tachycardie.Précautions particulièresUn usage prudent et une posologie initiale ré<strong>du</strong>ite sont conseillés chez:- les animaux âgés,- les animaux souffrant de ma<strong>la</strong>dies cardiaques,- les animaux souffrant <strong>du</strong> diabète sucré,- les animaux souffrant d’hypoadrénocorticisme.Chez le chien, l’absorption de <strong>la</strong> lévothyroxine est influencée par <strong>la</strong> présence del’alimentation. Le moment <strong>du</strong> traitement et celui de l’alimentation doivent doncêtre standardisés.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune influence sur le fœtus ou les animaux al<strong>la</strong>ités n’a été constatée.2.5.1.1 LévothyroxineFORTHYRON f<strong>la</strong>voured 400 mcg compr chien(Eurovet A.H.)lévothyroxine sodique: 400 mcgLMR lévothyroxine : comprimés poPosologie:Ca: 10 mcg/kg/12 hadapter dose aux besoinscompr 250R/FORTHYRON f<strong>la</strong>voured 200 mcg compr chien(Eurovet A.H.)lévothyroxine sodique: 200 mcgcomprimé poPosologie:Ca: 10 mcg/kg/12 hadapter dose aux besoinscompr 250R/LEVENTA (MSD A.H.)lévothyroxine sodique (multihydrate): 1 mg/mlsolution poPosologie:Ca: dose d’attaque: 20 mcg/kg pjajuster <strong>la</strong> dose 4 sem plus tard(<strong>la</strong> dose d’entretien se situe généralemententre 10 et 40 mcg/kg pj)f<strong>la</strong>con 1 x 30 mlR/
2 MÉDICAMENTS DU SYSTÈME HORMONAL 952.5.2 Médicament antithyroïdienIndicationLe méthimazole, <strong>la</strong> préparation à usage vétérinaire commercialisée actuellement,est utilisé chez le chat dans le traitement de l’hyperthyroïdie.PharmacodynamieLe méthimazole appartient au groupe des thionamides. Ces derniers inhibent <strong>la</strong>fixation de l’iode sur <strong>la</strong> tyrosine dans <strong>la</strong> g<strong>la</strong>nde thyroïde en se liant à <strong>la</strong> peroxidasede <strong>la</strong> thyroïde et diminuent ainsi <strong>la</strong> synthèse des hormones thyroïdiennes. Lesthionamides n’influencent pas les hormones thyroïdiennes déjà synthétisées nileur libération. L’effet clinique n’est donc perceptible qu’à partir <strong>du</strong> moment oùle stock pré-formé en hormones thyroïdiennes est épuisé et que <strong>la</strong> concentrationp<strong>la</strong>smatique des hormones diminue.PharmacocinétiqueLe méthimazole est oralement bien absorbé (biodisponibilité supérieure à 75%).La molécule est rapidement métabolisée, principalement par le foie. Elle est éliminéepar voie rénale.Contre-indications- Ma<strong>la</strong>dies hépatiques.- Anomalies auto-immunitaires.Effets indésirablesIl est conseillé de traiter le chat souffrant d’hyperthyroïdie deux fois par jour. Cecidiminuerait le risque d’apparition d’effets indésirables tels que des vomissementsou de l’anorexie. Les effets indésirables sont généralement légers et transitoires.Les effets indésirables plus graves sont généralement réversibles dès l’arrêt <strong>du</strong>traitement. A des doses quotidiennes de 5 à 15 mg par chat, les effets secondairescliniques étaient les suivants: vomissements, inappétence/anorexie, léthargie,prurit sérieux et excoriations de <strong>la</strong> tête et <strong>du</strong> cou, syndrome hémorragiqueet ictère liés à une hépatopathie, et troubles hématologiques (éosinophilie, lymphocytose,neutropénie, lymphopénie, légère leucopénie, agranulocytose, thrombocytopénieou anémie hémolytique). Ces effets indésirables disparaissaientdans les 7 à 45 jours suivant l’arrêt <strong>du</strong> traitement. Une leucopénie ou une anémiehémolytique peuvent se manifester. Il convient d’effectuer une prise de sangpour examens hématologiques et biochimiques chez les animaux qui deviennentsouffrants pendant le traitement, en particulier lorsqu’ils présentent de <strong>la</strong> fièvre.En cas d’effets secondaires immunologiques (anémie, thrombocytopénie, anticorpssériques antinucléaires), il convient d’arrêter immédiatement le traitementet d’envisager un traitement alternatif.InteractionsLe phénobarbital peut ré<strong>du</strong>ire l’efficacité clinique <strong>du</strong> méthimazole. Le méthimazolepeut ré<strong>du</strong>ire l’oxydation hépatique des benzimidazoles et entraîner ainsil’augmentation de <strong>la</strong> concentration p<strong>la</strong>smatique de ces substances. Le méthimazolea un effet immunomo<strong>du</strong><strong>la</strong>teur.Précautions particulières/Risques pour l’hommeIl faut veiller à contrôler régulièrement le taux en hormone thyroïdienne dans lesang et à adapter <strong>la</strong> dose de méthimazole. Les comprimés ne doivent pas êtrefractionnés. L’objectif est de parvenir à <strong>la</strong> plus faible dose possible. La leucopénieou l’anémie hémolytique sont également dépistées par des analyses desang. Le méthimazole pouvant ré<strong>du</strong>ire le taux de filtration gloméru<strong>la</strong>ire, il convientde surveiller étroitement <strong>la</strong> fonction rénale chez les animaux présentant des problèmesrénaux. En raison de l’action tératogène suspectée <strong>du</strong> méthimazole chezl’homme, les femmes en âge de procréer doivent porter des gants lors de <strong>la</strong> manipu<strong>la</strong>tionde <strong>la</strong> litière des chats traités.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe méthimazole diffuse à travers le p<strong>la</strong>centa et peut causer de l’hypothyroïdiechez les chatons. Ne pas administrer aux chattes en gestation ou en <strong>la</strong>ctation.
962 MÉDICAMENTS DU SYSTÈME HORMONAL2.5.2.1 Méthimazole (thiamazole)LMR méthimazole : FELIMAZOLE 2,5 mg (Dechra)thiamazole (méthimazole): 2,5 mgcomprimé enrobé poPosologie:Fe: 2 x pj 2,5 mg (adapter <strong>la</strong> dose après3 sem, max 20 mg pj)compr 100R/FELIMAZOLE 5 mg (Dechra)thiamazole (méthimazole): 5 mgcomprimé enrobé poPosologie:Fe: 2 x pj 2,5 mg (adapter <strong>la</strong> dose après3 sem, max 20 mg pj)compr 100R/2.6 InsulineIndicationsTraitement <strong>du</strong> diabète sucré insulino-dépendant chez le chien et le chat.PharmacodynamieL’insuline permet <strong>la</strong> pénétration et l’utilisation <strong>du</strong> glucose dans les cellules et stimulele métabolisme des glucides.PharmacocinétiqueL’insuline, hormone polypeptidique, n’est active que par voie parentérale (SC ouIM). La seule préparation à usage vétérinaire sur le marché en Belgique contientde l’insuline purifiée de porc dont <strong>la</strong> structure est identique à l’insuline de chien.Elle contient 40 UI/ml, en partie sous forme amorphe, en partie sous forme cristallineconditionnant l’action prolongée. La <strong>du</strong>rée d’action totale varie de 14 à 24heures (premier pic p<strong>la</strong>smatique après environ 4 heures; deuxième pic après environ12 heures). La posologie dépend de <strong>la</strong> glucosurie et de <strong>la</strong> glycémie et doit êtreadaptée au cas par cas (dose d’attaque et dose d’entretien: voir le RCP).Contre-indicationsAucune.Effets indésirables- Hypoglycémie suite à un surdosage.- L’insuline porcine n’engendre que très rarement des réactions d’hypersensibilité.InteractionsLes médicaments renforçant l’action hypoglycémique de l’insuline sont: les inhibiteursde l’enzyme de con<strong>version</strong> de l’angiotensine (p.ex. l’éna<strong>la</strong>pril), les stéroïdesanabolisants, les bêta-bloquants (p. ex. le propranolol), <strong>la</strong> phénylbutazone, lessulfamidés, les tétracyclines, les inhibiteurs de monoamine oxydase, <strong>la</strong> guanéthidine,l’aspirine et d’autres salicy<strong>la</strong>tes. Les médicaments inhibant l’action hypoglycémiquede l’insuline sont: <strong>la</strong> dextrothyroxine, le diltiazem (hypotensif), <strong>la</strong>dobutamine, l’épinéphrine, les associations œstroprogestatives, le furosémide, lesglucocorticoïdes, les dérivés de <strong>la</strong> phénothiazine et les diurétiques thiazidiques.Précautions particulièresL’insuline peut influencer <strong>la</strong> teneur en potassium dans le sérum; le traitementsimultané avec des glycosides cardiotoniques doit être suivi avec précaution.Surtout lorsque des diurétiques sont également associés.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune influence négative de l’insuline porcine sur le fœtus ou les chiots al<strong>la</strong>itésn’est connue.
2 MÉDICAMENTS DU SYSTÈME HORMONAL 97LMR insuline : CANINSULIN (MSD A.H.)insuline: 40 UI/mlsuspension injectable sc, imPosologie:Ca (1 x pj):- dose initiale: 1 UI/kg + :(< 10 kg PV): 1 UI(+/- 10 kg PV): 2 UI(12 - 20 kg PV): 3 UI(> 20 kg PV): 4 UI- dose d’entretien: déterminée selon les tauxp<strong>la</strong>smatiques de glucoseFe (2 x pj à 12 h d’intervalle):- dose initiale: 0,25 - 0,5 UI/kg selon les tauxp<strong>la</strong>smatiques de glucose- dose d’entretien: déterminée selon les tauxp<strong>la</strong>smatiques de glucosef<strong>la</strong>con 10 x 2,5 mlcartouche 10 x 2,7 mlR/
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 993. ANALGÉSIQUES, ANTIPYRÉTIQUES ETANTI-INFLAMMATOIRES3.1 Anti-inf<strong>la</strong>mmatoires non stéroïdiens (AINS)Ces substances partagent des propriétés analgésiques, antipyrétiques et antiinf<strong>la</strong>mmatoires.A l’opposé des analgésiques <strong>du</strong> groupe des narcotiques, ellesn’ont aucun effet psychotrope. Ces médicaments exercent uniquement des effetssymptomatiques. Leur administration ne dispense pas de rechercher <strong>la</strong> cause de<strong>la</strong> ma<strong>la</strong>die ni de recourir au traitement étiologique. Les AINS appartiennent à différentesc<strong>la</strong>sses chimiques ce qui explique les différences au p<strong>la</strong>n pharmacodynamiqueet pharmacocinétique détaillées dans les résumés des caractéristiquesdes pro<strong>du</strong>its (RCP) de chaque médicament.IndicationsEn médecine vétérinaire, les AINS sont particulièrement utilisés pour leurs propriétésanti-inf<strong>la</strong>mmatoires et analgésiques dans les affections de l’appareil locomoteurou pour contrôler les douleurs d’origine viscérale (colique) et dans certainscas particuliers, chirurgicale. En effet, dans ce dernier cas, seules quelques préparationspossèdent cette indication.PharmacodynamieLe mécanisme d’action commun de toutes ces substances rendant compte deleurs trois propriétés pharmacodynamiques de base repose sur le ralentissementde <strong>la</strong> synthèse des prostanoïdes (thromboxanes, prostacyclines et prostag<strong>la</strong>ndines)décou<strong>la</strong>nt de l’inhibition de l’enzyme cyclo-oxygénase, dont deux isoformesont été identifiées (COX1 et COX 2). COX 1 est responsable de <strong>la</strong> synthèse deprostag<strong>la</strong>ndines exerçant des actions physiologiques comme <strong>la</strong> régu<strong>la</strong>tion de <strong>la</strong>perfusion rénale et <strong>la</strong> protection de <strong>la</strong> muqueuse gastro-intestinale via <strong>la</strong> mo<strong>du</strong><strong>la</strong>tionde <strong>la</strong> sécrétion d’acide chlorhydrique et <strong>la</strong> pro<strong>du</strong>ction de mucus. La synthèsedes prostag<strong>la</strong>ndines, impliquées dans les processus inf<strong>la</strong>mmatoires, est surtoutsous <strong>la</strong> dépendance de COX 2. La plupart des AINS inhibent les deux variétés de<strong>la</strong> cyclo-oxygénase. Des inhibiteurs sélectifs de COX 2 ouvrent de nouvelles perspectives,notamment en ce qui concerne <strong>la</strong> tolérance gastro-intestinale. Un effetantipyrétique important est obtenu lorsqu’une action centrale prédomine. C’estle cas <strong>du</strong> paracétamol connu pour ses propriétés antipyrétiques et antalgiques.L’effet anti-inf<strong>la</strong>mmatoire résulte avant tout d’une action périphérique. L’inhibitionde l’activité de <strong>la</strong> cyclo-oxygénase peut être irréversible (salicylés et pyrazolones)ou réversible (ibuprofène et piroxicam). Les autres mécanismes d’action des AINSsont multiples et restent encore mal identifiés. Le découp<strong>la</strong>ge des phosphory<strong>la</strong>tionsoxydatives, l’acéty<strong>la</strong>tion d’enzymes, <strong>la</strong> capture de radicaux libres réactifset l’inhibition de l’activation, au sens <strong>la</strong>rge, des polynucléaires neutrophiles sontcités. Inhibition de <strong>la</strong> synthèse des leucotriènes.PharmacocinétiqueIls peuvent être administrés aussi bien par voie orale que par voie parentérale. Lesprincipaux AINS étant des acides faibles, <strong>la</strong> résorption est beaucoup plus rapidechez les carnivores que chez les herbivores lors d’administration orale. Le plussouvent, <strong>la</strong> liaison à l’albumine est importante, limitant <strong>la</strong> diffusion tissu<strong>la</strong>ire saufdans les exsudats. La biotransformation (conjugaison dans le foie), le degré derecyc<strong>la</strong>ge entéro-hépatique et l’excrétion des molécules (bile, urine) dépendentde <strong>la</strong> substance en cause et de l’espèce animale. Il est dès lors très important delimiter l’usage aux espèces recommandées et, pour les animaux pro<strong>du</strong>cteurs dedenrées alimentaires, de respecter scrupuleusement les temps d’attente. La plupartdes AINS sont métabolisés par glucuronoconjugaison hépatique. Le déficitd’enzyme glucuronyltransférase chez le chat prolonge <strong>la</strong> demi-vie de ces substances.D’autres AINS tels que le piroxicam ou le méloxicam sont principalementmétabolisés par oxydation. L’activité anti-inf<strong>la</strong>mmatoire et analgésique des AINSest souvent plus longue que ne le <strong>la</strong>isse présumer leur demi-vie sérique. Cecis’explique probablement par leur forte liaison aux protéines, qui permet aux AINSde persister plus longtemps dans les tissus inf<strong>la</strong>mmatoires que dans le p<strong>la</strong>sma.
1003 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESChez une même espèce, <strong>la</strong> demi-vie d’élimination est très variable d’une moléculeà l’autre.Contre-indicationsLa plupart des AINS ne peuvent pas être administrés au chat. Leur usage estcontre-indiqué en cas de problèmes rénaux ou gastro-intestinaux, de problèmesde coagu<strong>la</strong>tion ainsi qu’en cas de gestation ou d’accouchement imminent <strong>du</strong> faitde l’intervention des prostag<strong>la</strong>ndines dans ce processus. La cirrhose hépatique,le jeune âge et <strong>la</strong> vieillesse sont également des facteurs de risque supplémentaires<strong>du</strong> fait d’une clearance moins bonne.Effets indésirablesIl faut néanmoins garder en mémoire que <strong>la</strong> sensibilité particulière des indivi<strong>du</strong>simpose <strong>la</strong> plus grande prudence lors de l’usage de ces médicaments afin d’évitertout accident hémorragique. L’effet ulcérogène sur <strong>la</strong> muqueuse gastro-intestinale,<strong>la</strong> néphrotoxicité et l’allongement <strong>du</strong> temps de saignement représententles principaux effets indésirables des AINS, surtout au cours de traitements delongue <strong>du</strong>rée et lorsque des posologies élevées sont utilisées. Après injectionintramuscu<strong>la</strong>ire ou sous-cutanée, certains AINS peuvent provoquer des réactionstissu<strong>la</strong>ires douloureuses. La fermeture précoce <strong>du</strong> canal artériel et des hémorragieschez le fœtus sont des risques à prendre en compte. Les AINS peuventprovoquer une insuffisance rénale aiguë surtout en présence d’insuffisance cardiaque,de problèmes hépatiques accompagnés d’ascite, de déplétion volémiquepar les diurétiques notamment, de restriction sodée, de syndrome néphrotique.Une hyperkaliémie peut survenir chez les animaux traités par des diurétiqueshyperkaliémiants ou des inhibiteurs de l’enzyme de con<strong>version</strong>. Des réactionscutanées sont possibles.InteractionsL’association de plusieurs AINS ou d’un AINS avec des corticoïdes n’est pas souhaitablesur le p<strong>la</strong>n scientifique : <strong>du</strong> fait de l’action synergique vis-à-vis de l’inhibitionde <strong>la</strong> synthèse des prostanoïdes, ils renforcent mutuellement, en cas d’usagesimultané, leur toxicité. En raison de leur liaison protéique importante, les AINSne peuvent être administrés en même temps que des anticoagu<strong>la</strong>nts. Ils peuventantagoniser les effets des diurétiques. Les AINS peuvent modifier <strong>la</strong> métabolisationhépatique de certaines molécules par in<strong>du</strong>ction ou inhibition de certainesenzymes hépatiques. L’utilisation concomitante d’AINS et d’IECA, éventuellementassociés à des diurétiques, peut engendrer des effets indésirables rénaux enré<strong>du</strong>isant <strong>la</strong> filtration gloméru<strong>la</strong>ire. L’utilisation concomitante d’inhibiteurs de <strong>la</strong>pompe à protons (oméprazole, misoprostol) permet de prévenir les effets indésirablesgastro-intestinaux liés aux AINS.Précautions particulièresEn cas de thérapie prolongée, les paramètres hématologiques et biochimiquesdoivent être contrôlés. Le médecin vétérinaire doit encourager les propriétairesà rapporter sans dé<strong>la</strong>i les effets indésirables (troubles gastro-intestinaux, appétitmodifié, etc.). Etant donné son action inhibitrice sur l’agrégation des thrombocytes,l’acide tolfénamique est déconseillé en pré-chirurgie.Repro<strong>du</strong>ction et <strong>la</strong>ctationPour <strong>la</strong> plupart des AINS, aucun essai n’a été effectué sur les espèces ciblesconcernées. Chez les animaux de <strong>la</strong>boratoire, une ré<strong>du</strong>ction de <strong>la</strong> portée, unemortalité néonatale accrue et un nombre plus élevé de mort-nés ont été observés.La règle veut donc que l’on n’administre pas d’AINS, par précaution, chez lesanimaux gestants ou en <strong>la</strong>ctation, sauf si les bénéfices <strong>du</strong> traitement suppléentles risques.3.1.1 Salicy<strong>la</strong>tesIndicationsLes salicy<strong>la</strong>tes ont un effet analgésique, antipyrétique et antiphlogistique aussibien au niveau périphérique que central, et inhibent l’agrégation p<strong>la</strong>quettaire. Lesnotices des médicaments mentionnent comme indications le traitement d’appointde <strong>la</strong> fièvre en cas de ma<strong>la</strong>die respiratoire chez les bovins, les veaux ou les porcset le traitement de l’inf<strong>la</strong>mmation chez les porcs.
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 101PharmacodynamieLe salicy<strong>la</strong>te de sodium inhibe <strong>la</strong> cyclo-oxygénase, ré<strong>du</strong>isant ainsi <strong>la</strong> pro<strong>du</strong>ctionde prostag<strong>la</strong>ndine. Cette inhibition est réversible dans <strong>la</strong> plupart des cellules, l’inhibitionde cette enzyme dans les thrombocytes est cependant irréversible. Voiraussi 3.1.PharmacocinétiqueLe salicy<strong>la</strong>te de sodium administré par voie orale est rapidement absorbé au niveaude l’estomac et de <strong>la</strong> partie antérieure de l’intestin grêle. Le salicy<strong>la</strong>te desodium a une très bonne répartition tissu<strong>la</strong>ire. Les valeurs <strong>du</strong> volume de distributionsont plus élevées chez les nouveau-nés. La demi-vie est plus longue chezles animaux très jeunes (âgés de 7 à 14 jours). Le salicy<strong>la</strong>te de sodium est principalementmétabolisé dans le foie et éliminé par l’urine, un pH élevé augmentel’élimination.Contre-indicationsIl est déconseillé d’administrer ce médicament à de jeunes animaux (veaux < 2sem ou porcelets < 4 sem). Voir aussi 3.1Effets indésirablesVoir 3.1.InteractionsVoir 3.1.Précautions particulièresVoir 3.1.Repro<strong>du</strong>ction et <strong>la</strong>ctationVu les effets tératogènes et fœtotoxiques possibles chez les rats, l’administrationn’est pas recommandée en période de gestation ou de <strong>la</strong>ctation. Voir aussi 3.1.3.1.1.1 Salicy<strong>la</strong>te de sodium3.1.1.2 Acide acétylsalicyliqueLMR salicy<strong>la</strong>te de sodium: SODIUM SALICYL 80% WSP (DopharmaResearch)salicy<strong>la</strong>te de sodium: 800 mg/gpoudre pour solution po dans le <strong>la</strong>it de substitutionet/ou dans l’eau de boissonPosologie:Bo (âge > 2 sem): 1 x 40 mg/kg PV pj(1 - 3 j)Su (âge > 4 sem): 35 mg/kg PV pj (3 - 5 j)Viande et abats: Bo, Su: 0 jboîte 1 kgseau 1 kg, 5 kgR/LMR acide acétylsalicylique: ASPI-KEL 65% (Ke<strong>la</strong> Laboratoria)acide acétylsalicylique: 650 mg/gpoudre pour solution po avec l’eau de boissonPosologie:porc à l’engrais (âge > 2,5 m):50 mg/kg PV pj (max 10 j)Viande: 1 jsac 1 kgR/SOLACYL 100% (Eurovet A.H.)salicy<strong>la</strong>te de sodium: 1000 mg/gpoudre po (dans l’eau de boisson, le <strong>la</strong>it)Posologie:veau (âge > 2 sem): 40 mg/kg 1 x pj (1 - 3 j)Su (âge > 4 sem): 35 mg/kg pj (3 - 5 j)Viande: Bo: 0 j, Su: 0 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainesac 1 kgR/3.1.2 Dérivés de <strong>la</strong> pyrazoloneIndicationsLe métamizole (dipyrone) a surtout un effet analgésique et spasmolytique. La phénylbutazonea en plus une action anti-inf<strong>la</strong>mmatoire.PharmacodynamieVoir 3.1.PharmacocinétiqueLa phénylbutazone a une forte liaison avec les albumines p<strong>la</strong>smatiques (97-99 %).Le temps de demi-vie d’élimination de <strong>la</strong> phénylbutazone varie fortement avec
1023 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESl’espèce animale.Contre-indicationsVoir 3.1. Sont contre-indiqués : les anomalies hématologiques et mé<strong>du</strong>l<strong>la</strong>ires existantes,les pathologies rénales et les ulcères gastro-intestinaux.Chez le chat, <strong>la</strong> phénylbutazone est toxique pour <strong>la</strong> moelle osseuse.Effets indésirablesVoir 3.1.InteractionsVoir 3.1. La phénylbutazone stimule <strong>la</strong> dégradation microsomiale hépatiqued’autres molécules telles que <strong>la</strong> digoxine, influençant leur <strong>du</strong>rée d’action. D’autresin<strong>du</strong>cteurs enzymatiques tels que les barbituriques et les corticostéroïdes accélèrentquant à eux <strong>la</strong> dégradation hépatique de <strong>la</strong> phénylbutazone. Des interférencessont possibles entre <strong>la</strong> phénylbutazone et les tests de fonction thyroïdienne.En association avec des neuroleptiques (phénothiazines), le métamizole peutin<strong>du</strong>ire de l’hypothermie.Précautions particulièresLa phénylbutazone irritant les tissus, elle ne peut donc pas être injectée par voiesous-cutanée ni intramuscu<strong>la</strong>ire. Voir aussi 3.1.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucun effet tératogène direct n’est connu pour <strong>la</strong> phénylbutazone. Chez le <strong>la</strong>pincependant, une ré<strong>du</strong>ction de <strong>la</strong> portée, une mortalité néonatale accrue et unnombre accru de mort-nés ont été observés.Voir aussi 3.1.3.1.2.1 Phénylbutazone3.1.2.2 Métamizole (dipyrone)LMR phénylbutazone: FENYLBUTAZON 20 % (VMD)phénylbutazone: 200 mg/mlsolution injectable ivPosologie:Ca: 2 - 3 x pj 15 mg/kg (max 2 j)Eq: 1 x pj 4,4 mg/kg (max 5 j)Ne pas administrer aux Eq destinés à <strong>la</strong>consommation humainef<strong>la</strong>con 100 mlR/LMR métamizole: VETALGIN (MSD A.H.)métamizole sodique monohydrate: 500 mg/mlsolution injectable im, ivPosologie:Eq: 1 x 40 - 50 mg/kg (iv)Bo: 1 x 40 mg/kg (im, iv)Su: 1 x 15 - 50 mg/kg (im)Viande: Eq: 7 j, Bo: 12 j, Su: 3 j,Lait: Bo: 2 j (4 traites)f<strong>la</strong>con 100 mlR/3.1.3 Dérivés de l’acide nicotinergique et phénamatesIndicationsLa flunixine méglumine et l’acide tolfénamique sont des anti-inf<strong>la</strong>mmatoires etdes analgésiques particulièrement puissants contre les douleurs viscérales. Laflunixine a une action anti-inf<strong>la</strong>mmatoire, en particulier vis-à-vis de celle in<strong>du</strong>itepar les endotoxines de E. Coli. La tolfénamine peut être administrée aux chats(contrairement à <strong>la</strong> flunixine et à de nombreux autres AINS).PharmacodynamieVoir 3.1.PharmacocinétiqueEn dépit de <strong>la</strong> demi-vie d’élimination courte (1,5 à 2,5 heures chez le cheval etenviron 4 heures chez le chien), le temps d’action de <strong>la</strong> flunixine méglumine estsuffisamment long pour qu’une seule administration par 24 heures soit suffisante.Il est conseillé de ré<strong>du</strong>ire <strong>la</strong> <strong>du</strong>rée d’administration à 5 jours consécutifs. L’acidetolfénamique se lie fortement aux albumines p<strong>la</strong>smatiques (> 97 % chez les bovins,92 % chez le chien; 87 % chez le cheval). Dans le dosage recommandéet en fonction <strong>du</strong> mode d’administration, le temps de demi-vie d’élimination estde 8 à 15 heures chez le bovin, de 3 à 5 heures chez le porc et de 5 à 7 heureschez le chien. La biodisponibilité de l’acide tolfénamique peut être augmentée parl’administration avec l’alimentation, le cycle entéro-hépatique étant ainsi stimulé.Contre-indicationsVoir 3.1. La flunixine ne peut être administrée à des chats.
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 103Effets indésirablesLa flunixine et l’acide tolfénamique sont, en comparaison avec d’autres AINS,re<strong>la</strong>tivement sûrs d’usage, même si les effets indésirables c<strong>la</strong>ssiques peuventapparaître, en particulier lors de dosages plus élevés ou de traitements prolongés.Voir 3.1.Interactions - Précautions particulièresVoir 3.1.Repro<strong>du</strong>ction et <strong>la</strong>ctationIl est déconseillé d’utiliser <strong>la</strong> flunixine chez les animaux gestants ou en <strong>la</strong>ctation(absence d’études de sécurité).3.1.3.1 Acide tolfénamique3.1.3.2 FlunixineLMR acide tolfénamique: TOLFEDINE 4 % (Vétoquinol)acide tolfénamique: 40 mg/mlsolution injectable sc, imPosologie:Ca, Fe: 4 mg/kg pj (max 10 j)douleur post-opératoire: injecter 1 h avantin<strong>du</strong>ction de l’anesthésief<strong>la</strong>con 10 ml, 30 mlR/TOLFEDINE 6 mg (Vétoquinol)acide tolfénamique: 6 mgcomprimé poPosologie:Ca, Fe: 3 - 6 mg/kg pj (en 2 prises) (3 - 5 j)compr 20, 100R/TOLFEDINE 60 mg (Vétoquinol)acide tolfénamique: 60 mgcomprimé poPosologie:Ca: 3 - 6 mg/kg pj (en 2 prises) (3 - 5 j)compr 16, 96R/TOLFINE (Vétoquinol)acide tolfénamique: 40 mg/mlsolution injectable im (Bo, Su), iv (Bo)Posologie:Bo:- pathologie resp.: 2 mg/kg (im) (peut êtrerépété après 48 h)- mammite: 4 mg/kg (iv)Su: 2 mg/kgViande: Bo: 14 j (im), 7 j (iv), Su: 16 j, Lait: Bo(iv, im): 0 jf<strong>la</strong>con 100 ml, 250 mlR/LMR flunixine: CRONYXIN 50 mg/ml sol inj bovins, chevaux,porcs (Cross Vetpharm Group)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su)Posologie:Bo: 1,1 - 2,2 mg/kg iv, répéter si nécessaireà 24 h d’intervalle (max 3 j)Eq:- troubles musculosquelett: 1,1 mg flunixine/kgiv, à 24 h d’intervalle (max 5 j)- colique: 1,1 mg flunixine/kg iv, traitementpeut être répété 1 ou 2 xSu (PV > 6 kg): 1 x 2,2 mg/kg im, commetraitement adjuvant à une antibiothérapieViande et abats: Eq: 28 j, Bo: 10 j, Su: 24 jLait: Bo: 48 h, Eq: ne pas administrer aux Eqdont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumainef<strong>la</strong>con 100 mlR/EMDOFLUXIN 50 (Emdoka)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su, Bo < 200kg PV), sc (Ca)Posologie:Eq: 1,1 mg/kg pj (max 5 j), colique: répéteréventuellement 1 à 2 x à 1 h d’intervalleBo: 1,1 mg/kg pj (max 3 j)veau (PV < 200 kg): 1,1 - 2,2 mg/kg pj(max 5 j)Su: 1,1 - 2,2 mg/kg/12 h (1 - 3 x)Ca: 1 - 2 mg/kg pj (max 5 j)Viande: Eq: 10 j, Bo: 3 j (iv), veau (< 200 kg) (im):12 j, Su: 24 j, Lait: Bo: 24 hf<strong>la</strong>con 50, 100 ou 250 mlR/FINADYNE 50 mg/ml sol inj (MSD A.H.)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su)Posologie:Eq, pou<strong>la</strong>in:- squelette et muscles: 1,1 mg/kg pj (3 - 5 j)- colique: 1,1 mg/kg (1 - 3 x, à 1 hd’intervalle)Bo, veau: 1,1 - 2,2 mg/kg pj (1 - 3 j)Su, porcelet:- squelette et muscles - MMA: 1,1 - 2,2mg/kg pj (1 - 2 x avec 12 h d’intervalle),max 3 inj- troubles resp.: 1 x 2,2 mg/kgViande: Eq: 4 j, Bo: 3 j, Su: 24 j, Lait: 24 hf<strong>la</strong>con 100 mlR/
1043 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESFINADYNE CHEVAUX 50 mg/g pâte (MSD A.H.)flunixine (méglumine): 50 mg/gpâte poPosologie:Eq (âge > 72 h):1,1 mg/kg pj = 1 seringue de 10 g/454 kgpj (max 5 j)entre 2 traitements, observer intervalle de5 - 7 jViande: 7 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineNe pas administrer aux Eq de compétitionapplic 6 x 10 gR/FLUNIVETO (Norbrook Lab)flunixine (méglumine): 50 mg/mlsolution injectable ivPosologie:Eq: 1,1 mg/kg pj (5 j max)Bo: 2,2 mg/kg pj (3 j max)Viande: Eq: 28 j, Bo: 14 j, Lait: Bo: 48 hNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/FLURAZIN 50 mg/ml (CEVA Santé Animale)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su)Posologie:Eq: 1 mg/kg pj (max 5 j)Bo: 1 - 2 mg/kg pj (max 3 j)Su: 2.2 mg/kg, en association avec thérapieantimicrob appropriéeViande et abats: Eq: 28 j, Bo: 7 j, Su: 24 j,Lait: 24 hf<strong>la</strong>con 100 mlR/FLUVEX 50 mg/ml sol inj bovins, porcs, chevaux(S.P. Veterinaria)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su)Posologie:Bo: 2,2 mg/kgEq:- ma<strong>la</strong>dies musculo-squelet: 1 x 1,1 mg/kgpj (max 5 j)- douleurs viscérales (coliques): 1,1 mg/kg(peut être répété)Su: syndrome MMA: 2,2 mg/kg, 1 of 2 x à12 h d’intervalle en fonction de <strong>la</strong> réponsecliniqueViande et abats: Eq: 28 j, Bo: 14 j, Su: 28 j,Lait: Bo: 2 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/MEFLOSYL 5 % inj (Pfizer A.H.)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), im (Su)Posologie:Eq: 1,11 mg/kg pj (max 5 j), colique:1,11 mg/kg/h (1 - 3 x)Bo: 1,11 - 2,22 mg/kg pj (max 3 j)Su: 1,11 - 2,22 mg/kg pj (1 - 2 inj toutes les12 h, max 3 inj)Viande: Eq: 4 j, Bo: 3 j, Su: 24 j,Lait: Eq, Bo: 24 hf<strong>la</strong>con 50 ml, 100 mlR/NIGLUMINE (Lab Calier)flunixine (méglumine): 50 mg/mlsolution injectable iv (Eq, Bo), Su (im)Posologie:Eq: 1,1 mg/kg pj (5 j)Bo: 2,2 mg/kg pj (3 j)Su: jusqu’à 2 x 2,2 mg/kg à 12 h d’intervalleViande et abats: Eq: 28 j, Bo: 4 j, Su: 28 j,Lait: 24 hNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/3.1.4 Dérivés de l’acide arylpropioniqueIndicationsLe carprofène et le kétoprofène sont indiqués comme antipyrétiques, antiphlogistiqueset comme analgésiques, en cas d’infections respiratoires, dans lesaffections de l’appareil locomoteur, dans les coliques et en cas de douleurs postopératoiresassociées à <strong>la</strong> chirurgie des tissus mous ou à <strong>la</strong> chirurgie orthopédique.Aux posologies recommandées, il semble que le temps de saignement nesoit pas altéré, ce qui ouvre le champ de l’analgésie des douleurs d’origine chirurgicaleà cette molécule. La plus grande prudence est néanmoins recommandéevu les sensibilités indivi<strong>du</strong>elles assez variables dans ce domaine.PharmacodynamieIl s’agit de mé<strong>la</strong>nges racémiques dans lesquels les deux énantiomères participentà l’activité thérapeutique <strong>du</strong> mé<strong>la</strong>nge. Le carprofène est plutôt un inhibiteur faiblede COX, ce qui explique en partie son profil d’effets indésirables plus favorable.PharmacocinétiqueUne résorption rapide et une grande biodisponibilité (70 à 100 % suivant <strong>la</strong> substanceet l’espèce animale considérée) sont observées suite à une administrationorale. La demi-vie <strong>du</strong> carprofène, administré par voie orale, est de 8 heures chezle chien. En cas d’administration intraveineuse, <strong>la</strong> demi-vie p<strong>la</strong>smatique <strong>du</strong> kétoprofèneest de 2,7 heures chez le bovin et d’une heure seulement, chez le cheval.Le carprofène est principalement métabolisé au niveau <strong>du</strong> foie et excrété par les
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 105fèces. Le kétoprofène est quant à lui principalement éliminé par voie rénale.Contre-indicationsVoir 3.1.Effets indésirablesCes molécules sont généralement bien tolérées. Des effets indésirables graves,caractéristiques aux AINS, peuvent néanmoins apparaître. Voir aussi 3.1.InteractionsVoir aussi 3.1. Des interférences sont possibles entre le carprofène et les teststhyroïdiens. Le kétoprofène peut in<strong>du</strong>ire des résultats faussement positifs de glycémie,de bilirubinémie et de fer p<strong>la</strong>smatique, en fonction des tests de <strong>la</strong>boratoireet des réactifs utilisés.Précautions particulièresEn ce qui concerne le carprofène, certains auteurs recommandent un usage prudentchez les patients âgés et ceux souffrant de ma<strong>la</strong>dies chroniques (insuffisancesrénales ou hépatiques, ou « inf<strong>la</strong>mmatory bowel disease »).Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune étude de sécurité n’étant connue pour le carprofène ou le kétoprofène,leur utilisation chez les animaux gestants ou en <strong>la</strong>ctation est déconseillée.3.1.4.1 CarprofèneLMR carprofène : CARPRODYL F 20 mg (Ceva Santé Animale)carprofène: 20 mgcomprimé poPosologie:Ca (âge > 4 m): 4 mg/kg pj (peut être répartisur 2 prises)diminuer <strong>la</strong> dose selon l’effet cliniquecompr 10 x 10R/CARPRODYL F 50 mg (Ceva Santé Animale)carprofène: 50 mgcomprimé poPosologie:Ca (âge > 4 m): 4 mg/kg pj (peut être répartisur 2 prises)diminuer <strong>la</strong> dose selon l’effet cliniquecompr 20 x 5R/CARPRODYL F 100 mg (Ceva Santé Animale)carprofène: 100 mgcomprimé poPosologie:Ca (âge > 4 m): 4 mg/kg pj (peut être répartisur 2 prises)diminuer <strong>la</strong> dose selon l’effet cliniquecompr 20 x 5R/DOLAGIS 50 mg compr chiens (Sogeval Lab)carprofène: 50 mg/comprcomprimé poPosologie:Ca: 4 mg/kg pjcompr 20, 100R/DOLAGIS 120 mg compr à croquer chiens(Sogeval Lab)carprofène: 120 mg/comprcomprimé à croquer poPosologie:Ca: 4 mg/kg pjcompr 12, 120R/NOROCARP 20 mg, 50 mg compr (Norbrook Lab)carprofène: 20 mg, 50 mgcomprimé poPosologie:Ca (âge > 4 m): 4 mg/kg pj (éventuellementréparti en 2 prises)compr 20 mg: 10 x 10compr 50 mg: 10 x 10, 50 x 10R/NOROCARP 100 mg compr (Norbrook Lab)carprofène: 100 mgcomprimé poPosologie:Ca (âge > 4 m): 4 mg/kg pjcompr 100R/NOROCARP 20 mg compr appétents pour chiens(Norbrook <strong>la</strong>b)carprofène: 20 mgcomprimé appétent poPosologie:Ca (âge > 4 m):dose initiale: 4 mg/kg pjdose d‘entretien: 2 mg/kg pjcompr 2 x 10, 10 x 10R/NOROCARP 50 mg compr appétents pour chiens(Norbrook <strong>la</strong>b)carprofène: 50 mgcomprimé appétent poPosologie:Ca (âge > 4 m): 4 mg/kg pjcompr 2 x 10, 10 x 10R/NOROCARP 100 mg compr appétents pour chiens(Norbrook <strong>la</strong>b)carprofène: 100 mgcomprimé appétent poPosologie:Ca (âge > 4 m):dose initiale: 4 mg/kg pjdose d‘entretien: 2 mg/kg pjcompr 2 x 10, 10 x 10R/
1063 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESNOROCARP 50 mg/ml sol inj (Norbrook Lab)carprofène: 50 mg/mlsolution injectable sc, ivPosologie:Bo: 1,4 mg/kgViande et abats: 21 j, Lait: 0 hf<strong>la</strong>con 50 mlR/RIMADYL 20 mg compr appétents (Pfizer A.H.)carprofène: 20 mgcomprimé appétent poPosologie:Ca: 2 x pj 2 mg/kg (7 j), ensuite 2 mg/kg pjcompr 20, 100R/RIMADYL 50 mg compr appétents (Pfizer A.H.)carprofène: 50 mgcomprimé appétent poPosologie:Ca: 2 x pj 2 mg/kg (7 j), ensuite 2 mg/kg pjcompr 20, 100R/RIMADYL 100 mg compr appétents (Pfizer A.H.)carprofène: 100 mgcomprimé appétent poPosologie:Ca: 2 x pj 2 mg/kg (7 j), ensuite 2 mg/kg pjcompr 20, 100R/RIMADYL bovins 50 mg/ml (Pfizer A.H.)carprofène: 50 mg/mlsolution injectable sc, ivPosologie:Bo: 1,4 mg/kgViande: 21 j, Lait: 0 hf<strong>la</strong>con 50 mlR/RIMADYL sol inj (Pfizer A.H.)carprofène: 50 mg/mlsolution injectable iv, scPosologie:Ca: 4 mg/kg (peut être suivi par unethérapie po)Fe: 4 mg/kgf<strong>la</strong>con 20 mlR/RIMIFIN 20 mg, 50 mg, 100 mg (ChanellePharmaceuticals)carprofène: 20, 50 ou 100 mgcomprimé poPosologie:Ca: 2 à 4 mg/kg pjcompr 10 x 100R/3.1.4.2 KétoprofèneLMR kétoprofène: ARISTAL 100 mg/ml (In<strong>du</strong>strial Veterinaria)kétoprofène: 100 mg/mlsolution injectable im (Bo, Su), iv (Bo, Eq)Posologie:Bo: 3 mg/kg 1 x pj (max 3 j)Su: 1 x 3 mg/kgEq: 2,2 mg/kg 1 x pj (3 - 5 j), en cas decoliques ne pas répéter le traitement sansréévaluation clinique de l’animalViande et abats: 4 j, Lait (Bo): 0 hNe pas utiliser chez les juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 ml, 250 mlR/COXOFEN 100 mg/ml (Vetpharma A.H.)kétoprofène: 100 mg/mlsolution injectable iv, imPosologie:Eq: 1 x pj 2,2 mg/kg (3 à 5 j) (iv)Bo: 1 x pj 3 mg/kg (max 3 j) (iv, im)Su: 1 x 3 mg/kg (im)Viande et abats: 4 j, Lait: Bo: 0 hNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/KELAPROFEN 100 mg/ml (Ke<strong>la</strong> Laboratoria)kétoprofène: 100 mg/mlsolution injectable iv, imPosologie:Eq:- troubles musculo-squel: 2,2 mg/kg (iv)3-5 j- coliques: 2,2 mg/kg (iv) (peut être répété)Bo: 3 mg/kg (iv, im) (max 3 j)Su: 3 mg/kg (im)Viande: Eq: 1 j, Bo (iv): 1 j, Bo (im): 2 j, Su: 2 jLait: Bo: 0 h, Eq: ne pas administrer aux Eqdont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumainef<strong>la</strong>con 50 ml, 100 ml, 250 mlR/KETOFEN 1 % (Merial)kétoprofène: 10 mg/mlsolution injectable im, iv, sc (Ca), sc (Fe)Posologie:Ca, Fe: 2 mg/kg pj (1 - 3 j)f<strong>la</strong>con 20 mlR/KETOFEN 10 % (Merial)kétoprofène: 100 mg/mlsolution injectable iv (Eq, Bo), im (Bo, Su)Posologie:Eq: 2,2 mg/kg pj (3 - 5 j), colique: 2,2 mg/kg(peut être répété)Bo: 3 mg/kg pj (1 - 3 j)Su: 3 mg/kg pj (3 j)Viande: Eq, Bo, Su: 4 j, Lait: Eq, Bo: 0 jf<strong>la</strong>con 50 ml, 100 mlR/KETOFEN 5 mg (Merial)kétoprofène: 5 mgcomprimé poPosologie:Ca, Fe: 1 mg/kg pj (3 - 5 j)compr 1 x 10R/
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 107KETOFEN 20 mg (Merial)kétoprofène: 20 mgcomprimé poPosologie:Ca: 1 mg/kg pj (3 - 5 j)compr 1 x 10R/KETOPROPIG 100 mg/ml (Labiana Life Sciences)kétoprofène: 100 mg/mlsolution po dans l’eau de boissonPosologie:Su: 3 mg/kg (24 h)Viande: 2 jf<strong>la</strong>con 1 lR/3.1.5 Groupe des oxicamsIndicationsLe méloxicam a des actions antipyrétiques, analgésiques et antiphlogistiquespuissantes. Chez le cheval, le chien et le porc, le méloxicam est indiqué dans lesaffections non infectieuses de l’appareil locomoteur. Chez le cheval, les indicationsreprennent depuis peu aussi le traitement des coliques. Chez le porc, il peutaussi être utilisé en association avec un antibiotique dans le traitement <strong>du</strong> syndromede l’hypoga<strong>la</strong>ctie transitoire post-partum (HTPP). Chez le chien et le chat,le méloxicam peut être administré pour éviter des douleurs d’origine chirurgicale.Chez le bovin, il est utilisé comme thérapie d’appoint dans les infections respiratoires,<strong>la</strong> diarrhée et <strong>la</strong> mastite, en association avec les antibiotiques, ainsi quepour le sou<strong>la</strong>gement de <strong>la</strong> douleur postopératoire suivant l’écornage des veaux.PharmacodynamieVoir 3.1.PharmacocinétiqueLe méloxicam a une excellente biodisponibilité orale, proche de 100 %, indépendantede l’alimentation. La liaison avec les albumines est supérieure à 97 %. Lamétabolisation en métabolites inactifs a lieu dans le foie. Un cycle entéro-hépatiqueefficace prolonge <strong>la</strong> demi-vie d’élimination de <strong>la</strong> molécule qui est d’environ24 heures chez le chien (voie orale) et de 24 à 28 heures chez le veau (voie parentérale).L’excrétion s’effectue via les fèces et l’urine.Contre-indicationsVoir 3.1. Ne pas administrer aux animaux âgés de moins de 6 semaines (cheval,chien, chat) ou de moins d’1 semaine (bovins) ou aux chats pesant moins de 2 kg.Effets indésirablesIl a peu d’effets indésirables, sans doute <strong>du</strong> fait de sa sélectivité re<strong>la</strong>tive pourCOX2. Néanmoins, le méloxicam reste un AINS avec tous les effets indésirablespotentiels re<strong>la</strong>tifs à cette c<strong>la</strong>sse de principes actifs même si <strong>la</strong> marge de sécuritéen ré<strong>du</strong>it <strong>la</strong> probabilité d’apparition. Voir 3.1.InteractionsVoir 3.1.Précautions particulièresLe méloxicam présente une affinité préférentielle vis à vis de l’iso-enzyme COX-2,mais sans être toutefois un inhibiteur sélectif de <strong>la</strong> COX-2 car cette spécificitédisparaît avec des doses plus élevées.Voir 3.1.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe méloxicam diffuse à travers le p<strong>la</strong>centa de rattes gestantes et est excrété dansle <strong>la</strong>it. Le méloxicam est en général déconseillé chez les animaux gestants ou en<strong>la</strong>ctation. La notice de Metacam ® injectable pour bovins et porcins mentionne quece médicament peut être utilisé chez les bovins gestants et les truies gestantesou en <strong>la</strong>ctation.
1083 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESLMR méloxicam: ACTICAM 5 mg/ml (Ecuphar)méloxicam: 5 mg/mlsolution injectable sc (Ca, Fe), iv (Ca)Posologie:(Ca, Fe: âge > 6 sem, Fe: PV > 2 kg)- affection de l’app. locomoteur:Ca: 1 x 0,2 mg/kg- atténuation de <strong>la</strong> douleur post-opératoire:Ca: 1 x 0,2 mg/kg (avant l’opération)Fe: 1 x 0,3 mg/kg (avant l’opération)f<strong>la</strong>con 10 mlR/EMDOCAM 20 mg/ml (Emdoka)méloxicam: 20 mg/mlsolution injectable iv (Eq, Bo), im (Su), sc (Bo)Posologie:Eq (âge > 6 sem): 1 x 0,6 mg/kgBo: 1 x 0,5 mg/kg (traitement diarrhée, âge> 1 sem)Su: 0,4 mg/kg (si nécessaire: 2e inj après24 h)Viande (abats): Eq: 5 j, Bo: 15 j, Su 5 j, Lait:Bo: 5 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 ml, 100 ml, 250 mlR/INFLACAM 1 mg et 2,5 mg compr à croquer chiens(Chanelle)méloxicam: 1 mg ou 2,5 mgcomprimé à croquer poPosologie:Ca (âge > 6 sem, PV > 4 kg):- dose initiale: 1 x 0,2 mg/kg le 1er j- entretien: 0,1 mg/kg 1 x pjcompr 100R/INFLACAM 1,5 mg/ml susp po chiens (Chanelle)méloxicam: 1,5 mg/mlsuspension poPosologie:Ca (âge > 6 sem):- dose initiale: 1 x 0,2 mg/kg le 1er j- entretien: 0,1 mg/kg1 x pj, en cas detraitement prolongé, ajuster éventuellement<strong>la</strong> dose à <strong>la</strong> plus faible dose indivi<strong>du</strong>elleefficacef<strong>la</strong>con 15, 42, 100 et 200 mlR/INFLACAM 15 mg/ml susp po chevaux (Chanelle)méloxicam: 15 mg/mlsuspension poPosologie:Eq (âge > 6 sem): 0,6 mg/kg 1 x pj (max 14 j)Viande + abats: 3 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 et 250 mlR/LOXICOM 1 mg et 2,5 mg compr à croquer chiens(Norbrook Lab)méloxicam: 1 mg ou 2,5 mgcomprimé à croquer poPosologie:Ca (âge > 6 sem, PV > 4 kg):- dose initiale: 1 x 0,2 mg/kg le 1er j- entretien: 0,1 mg/kg 1 x pjdose initiale éventuellement par voieinjectablecompr 10, 100R/LOXICOM 20 mg/ml sol inj bovins, porcins, chevaux(Norbrook Lab)méloxicam: 20 mg/mlsolution injectable iv (Eq, Bo), sc (Bo), im (Su)Posologie:Eq: 1 x 0,6 mg/kg iv, le traitement peut êtrepoursuivi poBo: 1 x 0,5 mg/kg sc ou iv (éventuellementavec antibiothérapie ou réhydratation)Su: 1 x 0,4 mg/kg im (éventuellement avecantibiothérapie) (peut être répété après 24 h)Viande et abats: Eq: 5 j, Bo: 15 j, Su: 5 jLait: Bo: 5 j, ne pas administrer aux Eq dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 ml, 100 ml et 250 mlR/LOXICOM sol inj chien et chat (Norbrook Lab)méloxicam: 5 mg/mlsolution sc (Ca, Fe), iv (Ca)Posologie:- Ca: troubles musculo-squel: 1 x 0,2 mg/kg (sc),traitement peut être poursuivi avecLoxicam® susp oraledouleur postopératoire: 1 x 0,2 mg/kg (sc ouiv) avant <strong>la</strong> chirurgie- Fe: douleur postopératoire: 1 x 0,3 mg/kg(sc) avant <strong>la</strong> chirurgief<strong>la</strong>con 20 mlR/LOXICOM susp orale chat (Norbrook Lab)méloxicam: 0,5 mg/mlsuspension poPosologie:Fe (âge > 6 sem):dose initiale: 1 x 0,1 mg/kg le 1er jdose d’entretien: 1 x 0,05 mg/kg pjf<strong>la</strong>con 5 ml, 15 mlR/LOXICOM susp orale chien (Norbrook Lab)méloxicam: 0,5 mg/ml ou 1,5 mg/mlsuspension poPosologie:Ca: dose d’attaque: 0,2 mg/kg,dose d’entretien: 1 x 0,1 mg/kg pjEn cas d’usage prolongé, administrer <strong>la</strong>dose indivi<strong>du</strong>elle efficace <strong>la</strong> plus faiblef<strong>la</strong>con 15 ml (0,5 mg/ml), 10 ml, 32 ml ou100 ml (1,5 mg/ml)R/MELOVEM (Dopharma Research)méloxicam: 5 mg/mlsolution injectable im, scPosologie:Bo (veaux, jeunes bovins): 1 x 0,5 mg/kgSu: 1 x 0,4 mg/kg (si nécessaire, répeteraprès 24 h)Viande et abats: Bo: 15 j, Su: 5 jNe pas administrer aux Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 109MELOXIDYL 0,5 mg/ml susp po chat (Ceva SantéAnimale)méloxicam: 0,5 mg/mlsuspension poPosologie:Fe (âge > 6 sem):- douleur/inf<strong>la</strong>mmation postopératoires:traitement initial avec inj appropriée deméloxicamentretien après 24 h: 1 x pj 0,05 mg/kg (4 j)- troubles musculo-squelett chroniques:traitement initial: 1 x 0,1 mg/kgentretien: 1 x pj 0,05 mg/kgmax 14 j en l’absence d’améliorationcliniquef<strong>la</strong>con 15 mlR/MELOXIDYL 1,5 mg/ml susp po chiens (CevaSanté Animale)méloxicam: 1,5 mg/mlsuspension po avec l’alimentationPosologie:Ca (âge > 6 sem): dose d’attaque:0,2 mg/kgdose d’entretien (après 24 h d’intervalle):0,1 mg/kg pjmax 10 j en l’absence d’améliorationf<strong>la</strong>con 10 ml, 32 ml, 100 mlR/MELOXIDYL 5 mg/ml sol inj (Ceva Santé Animale)méloxicam: 5 mg/mlsolution injectable sc (Ca, Fe), iv (Ca)Posologie:Ca (âge > 6 sem):- troubles musculo-squel: 1 x 0,2 mg/kg(sc),traitement peut être poursuivi avecMeloxidyl 1,5 mg/ml susp po® après 24 h- douleur postopérat (pendant 24 h):1 x 0,2 mg/kg sc ou iv avant l’interventionFe (âge > 6 sem, PV > 2 kg):douleur postopérat: 1 x 0,3 mg/kg (sc) avantl’interventionf<strong>la</strong>con 10 mlR/MELOXIDYL 20 mg/ml (Ceva Santé Animale)méloxicam: 20 mg/mlsolution injectable sc, im, ivPosologie:Eq (âge > 6 sem) (iv): 1 x 0,6 mg/kgBo (âge > 1 sem) (sc, iv): 1 x 0,5 mg/kgSu (im):1 x 0,4 mg/kg (si nécessaire 2e injaprès 24 h)Viande et abats: Eq: 5 j, Bo 15 j, Su: 5 j, LaitBo: 5 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/MELOXIVET 0,5 mg/ml (Eli Lilly)méloxicam: 0,5 mg/mlsuspension po avec l’alimentationPosologie:Ca:dose d’attaque: 0,2 mg/kg (1 j)dose d’entretien: 0,1 mg/kg pj(<strong>du</strong>rée <strong>du</strong> traitement:max 10 j en l’absence d’améliorationclinique)f<strong>la</strong>con 10 ml, 30 ml, 150 mlR/MELOXIVET 1,5 mg/ml susp po (Eli Lilly)méloxicam: 1,5 mg/mlsuspension po avec l’alimentationPosologie:Ca:dose d’attaque: 0,2 mg/kg (1 j)dose d’entretien: 0,1 mg/kg pj(<strong>du</strong>rée <strong>du</strong> traitement:max 10 j en l’absence d’améliorationclinique)f<strong>la</strong>con 10 ml, 30 ml, 150 mlR/MELOXORAL 0,5 mg/ml susp po chat (Le Vet)méloxicam: 0,5 mg/mlsuspension poPosologie:Fe (âge > 6 sem):dose initiale: 1 x 0,1 mg/kgdose d’entretien:0,05 mg/kg pj à 24 h d’intervalle (max 14 j)f<strong>la</strong>con 5 ml, 10 ml, 25 mlR/MELOXORAL 1,5 mg/ml susp po chien (Le Vet)méloxicam: 1,5 mg/mlsuspension poPosologie:Ca:dose d’attaque: 0,2 mg/kg (1 j)dose d’entretien: 0,1 mg/kg pj(<strong>du</strong>rée <strong>du</strong> traitement:max 10 j en l’absence d’améliorationclinique)f<strong>la</strong>con 10 ml, 25 ml, 50 ml, 125 mlR/METACAM 1 mg compr à croquer chiens(Boehringer Ingelheim Vetmedica)méloxicam: 1 mgcomprimé à croquer po (avec alimentation)Posologie:Ca (âge > 6 sem ou PV < 4 kg):1 x 0,2 mg/kg, après 24 h: 0,1 mg/kgcompr à croquer 7, 84R/METACAM 2,5 mg compr à croquer chiens(Boehringer Ingelheim Vetmedica)méloxicam: 2,5 mgcomprimé à croquer po (avec alimentation)Posologie:Ca (âge > 6 sem):1 x 0,2 mg/kg, après 24 h: 0,1 mg/kgcompr à croquer 7, 84R/METACAM 2 mg/ml sol inj chat (BoehringerIngelheim Vetmedica)méloxicam: 2 mg/mlsolution injectable scPosologie:Fe (âge > 6 sem, PV > 2 kg):1 x 0,2 mg/kgtraitement postopératoire po après 24 h:0,05 mg/kg pj (max 4 x)traitement postopératoire sc:1 x 0,3 mg/kgf<strong>la</strong>con 10 mlR/
1103 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESMETACAM 5 mg/ml sol inj chiens et chats(Boehringer Ingelheim Vetmedica)méloxicam: 5 mg/mlsolution injectable sc (Ca, Fe), iv (Ca)Posologie:(Ca, Fe: âge > 6 sem, Fe: PV > 2 kg)- troubles locomot:Ca: 1 x 0,2 mg/kg, suivi par un traitement po(0,1 mg/kg après 24 h)- douleur postopérat:Ca: 1 x 0,2 mg/kg (avant l’opération)Fe: 1 x 0,3 mg/kg (avant l’opération)f<strong>la</strong>con 20 mlR/METACAM 5 mg/ml sol inj bovins et porcins(Boehringer Ingelheim Vetmedica)méloxicam: 5 mg/mlsolution injectable sc (Bo), iv (Bo), im (Su)Posologie:Bo (âge > 1 sem): 1 x 0,5 mg/kg, en associationà antibiothérapie ou réhydratationorale selon l’indicSu (âge > 2 j): 1 x 0,4 mg/kg, si nécessaire2e dose après 24 hViande: Bo: 15 j, Su: 5 jf<strong>la</strong>con 100 mlR/METACAM 20 mg/ml sol inj bovins, porcs et chevaux(Boehringer Ingelheim Vetmedica)méloxicam: 20 mg/mlsolution injectable iv, scPosologie:Eq (âge > 6 sem): 1 x 0,6 mg/kg suivi par untraitement po 24 h après injBo (veau, jeune bétail, (âge > 1 sem)):1 x 0,5 mg/kgSu: 1 x 0,4 mg/kg, répéter après 24 h sinécessaireViande et abats: Eq: 5 j, Bo: 15 j, Su: 5 jLait: 5 jf<strong>la</strong>con 50 ml, 100 ml, 250 ml, 12 x 20 ml,12 x 100 mlR/METACAM 0,5 mg/ml susp po chats (BoehringerIngelheim Vetmedica)méloxicam: 0,5 mg/mlsuspension po (avec alimentation)Posologie:Fe (âge > 6 sem):dose initiale: 1 x 0,1 - 0,2 mg/kgdose d’entretien:0,05 mg/kg pj à 24 h d’intervalle (max 14 j)f<strong>la</strong>con avec compte-gouttes et seringuedoseuse3 ml, 15 ml, 30 mlR/METACAM 1,5 mg/ml susp po chiens (BoehringerIngelheim Vetmedica)méloxicam: 1,5 mg/mlsuspension po (avec alimentation)Posologie:Ca (âge > 6 sem):1 x 0,2 mg/kg, ensuite 0,1 mg/kg pjf<strong>la</strong>con avec seringue-doseuse10 ml, 32 ml, 100 ml, 180 mlR/METACAM 15 mg/ml susp po chevaux (BoehringerIngelheim Vetmedica)méloxicam: 15 mg/mlsuspension po (éventuellement avec un peud’aliment)Posologie:Eq (âge > 6 sem): 0,6 mg/kg pj (jusqu’à 14 j)admin juste avant le repasViande et abats: 3 jf<strong>la</strong>con 100 mlR/RHEUMOCAM horse 15 mg/ml (ChanellePharmaceuticals)méloxicam: 15 mg/mlsuspension poPosologie:Eq (âge > 6 sem): 0,6 mg/kg pj (max 14 j)Viande Eq: 3 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/RHEUMOCAM susp (Chanelle Pharmaceuticals)méloxicam: 1,5 mg/mlsuspension po avec l’alimentationPosologie:Ca (âge > 6 sem): dose initiale:1 x 0,2 mg/kgdose d’entretien: 0,1 mg/kg/24 hf<strong>la</strong>con 15, 42, 100 ou 200 mlR/3.1.6 Groupe des coxibsIndicationsLe cimicoxib est indiqué dans le traitement de <strong>la</strong> douleur et de l’inf<strong>la</strong>mmationassociées à l’arthrose, et dans <strong>la</strong> gestion de <strong>la</strong> douleur périopératoire causée par<strong>la</strong> chirurgie orthopédique ou des tissus mous, chez les chiens. Le firocoxib et lemavacoxib sont utilisés pour sou<strong>la</strong>ger <strong>la</strong> douleur et l’inf<strong>la</strong>mmation associées àl’arthrose chez le cheval (firocoxib) et le chien (firocoxib, mavacoxib). Le médicamentà base de mavacoxib n’est administré qu’une fois par mois après lesdeux doses initiales à 14 jours d’intervalle. Le robénacoxib est indiqué dans letraitement de <strong>la</strong> douleur et de l’inf<strong>la</strong>mmation associées aux troubles musculosquelettiqueschez le chat ou à l’arthrose chronique chez le chien, et peut égalementêtre utilisé chez le chien dans le traitement de <strong>la</strong> douleur et de l’inf<strong>la</strong>mmationliées à une chirurgie orthopédique ou des tissus mous, et chez le chat, dans letraitement de <strong>la</strong> douleur et de l’inf<strong>la</strong>mmation liées à <strong>la</strong> chirurgie des tissus mous.
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 111PharmacodynamieVoir 3.1 AINS. Les coxibs sont des inhibiteurs sélectifs de l’enzyme cyclooxygenase2 (COX-2).PharmacocinétiqueLes coxibs sont rapidement absorbés après une administration orale. La biodisponibilité<strong>du</strong> firocoxib est d’environ 35% chez le chien et de 80% chez le cheval.Celle <strong>du</strong> robénacoxib est de 49 %. La biodisponibilité n’est que peu influencée par<strong>la</strong> prise d’aliments. La liaison <strong>du</strong> firocoxib aux protéines p<strong>la</strong>smatiques est importante(plus de 90%). Le firocoxib est principalement métabolisé dans le foie, pardésalky<strong>la</strong>tion et glucuronoconjugaison. L’élimination se fait essentiellement par <strong>la</strong>bile. Le mavacoxib présente une longue demi-vie p<strong>la</strong>smatique (jusqu’à plus de 80jours) <strong>du</strong>e à son faible taux d’élimination, d’où une <strong>du</strong>rée d’action de 1 à 2 moisaprès l’administration de <strong>la</strong> deuxième dose.Contre-indicationsLe firocoxib est contre-indiqué chez les animaux gestants ou en <strong>la</strong>ctation, lesjeunes animaux, les animaux présentant un saignement gastro-intestinal, unedyscrasie sanguine (trouble de l’hémostase) ou des troubles hémorragiques.L’usage <strong>du</strong> firocoxib est déconseillé chez les chevaux de moins de 10 semaines.Voir 3.1 AINS.Effets indésirablesLe firocoxib administré à <strong>la</strong> dose recommandée et selon <strong>la</strong> <strong>du</strong>rée de traitement de30 jours est bien toléré chez les chiens a<strong>du</strong>ltes. La marge de sécurité de cette substanceest cependant ré<strong>du</strong>ite, surtout chez les jeunes animaux. Des effets secondaires(hépatiques, gastro-intestinaux et nerveux centraux) peuvent être observésà une dose de 3 à 10 fois supérieure à <strong>la</strong> dose recommandée. Si des effets secondairesapparaissent tels que vomissements, diarrhées permanentes, méléna, pertede poids soudaine, anorexie, léthargie, détérioration de paramètres biochimiqueshépatiques ou rénaux, le traitement doit être interrompu. Des lésions orales peuventoccasionnellement être observées chez le cheval, éventuellement associées à de<strong>la</strong> salivation, un oedème de <strong>la</strong> lèvre et de <strong>la</strong> <strong>la</strong>ngue. Le cimicoxib et le robénacoxibsont associés à des effets indésirables modérés et passagers tels que de <strong>la</strong> diarrhéeet des vomissements. Les principaux effets indésirables <strong>du</strong> mavacoxib sont uneperte d’appétit, de <strong>la</strong> diarrhée et des vomissements. Voir 3.1 AINS.InteractionsVoir 3.1 AINS.Précautions particulièresLa marge de sécurité <strong>du</strong> firocoxib est re<strong>la</strong>tivement ré<strong>du</strong>ite; lors de surdosages de3 à 10 fois <strong>la</strong> dose thérapeutique, des effets secondaires ont été constatés.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’usage de ces substances est contre-indiqué chez les femelles gestantes ou en<strong>la</strong>ctation.3.1.6.1 Cimicoxib3.1.6.2 FirocoxibLMR cimicoxib: CIMALGEX 8 mg, 30 mg, 80 mg compr à croquerchien (Vétoquinol)cimicoxib: 8 mg, 30 mg ou 80 mg/comprcomprimé à croquer poPosologie:Ca (âge > 10 sem): 2 mg/kg pj (3 à 7 j encas de douleur périopératoire, 6 m en casd’arthrose)compr 32 et 144R/LMR firocoxib: EQUIOXX pâte orale pour chevaux (Merial)firocoxib: 8,2 mg/gpâte poPosologie:Eq: 1 x 0,1 mg/kg pj (max 14 j)Viande: 26 jNe pas administrer aux juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineseringue 7,32 gR/
1123 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESEQUIOXX sol inj pour chevaux (Merial)firocoxib: 20 mg/mlsolution injectable ivPosologie:Eq: 1 x 0,09 mg/kg pj, poursuivre éventuellementle traitement avec Equioxx pâteorale® (max 14 j)Viande: 26 jNe pas administrer aux juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 25 mlR/PREVICOX 57 mg compr à croquer chiens (Merial)firocoxib: 57 mgcomprimé poPosologie:Ca (âge min 10 sem, PV min 3 kg):5 mg/kg pjne pas admin aux chiennes gestantes ouen <strong>la</strong>ctationcompr 3 x 10, 18 x 10R/PREVICOX 227 mg compr à croquer chiens(Merial)firocoxib: 227 mgcomprimé poPosologie:Ca (âge min 10 sem, PV min 3 kg):5 mg/kg pjne pas admin aux chiennes gestantes ouen <strong>la</strong>ctationcompr 3 x 10, 18 x 10R/3.1.6.3 MavacoxibLMR mavacoxib: TROCOXIL compr à croquer chien 6 mg, 20 mg, 30mg, 75 mg, 95 mg (Pfizer A.H.)mavacoxib: 6 mg, 20 mg, 30 mg, 75 mg, 95 mgcomprimé poPosologie:Ca (âge > 12 m, PV > 5 kg): 2 mg/kg, justeavant ou pendant repasrépéter après 14 j, ensuite l‘intervalle entreles doses est de 1 m (max 6,5 m)compr 2R/3.1.6.4 RobénacoxibLMR robénacoxib: ONSIOR 5, 10, 20 et 40 mg compr chien (Novartis)robénacoxib: 5, 10, 20 ou 40 mg/comprcomprimé poPosologie:Ca: 1 - 2 mg/kg pjcompr 4 x 7R/ONSIOR 6 mg compr chat (Novartis)robénacoxib: 6 mg/comprcomprimé poPosologie:Fe: 1 - 2,4 mg/kg pj (6 j)compr 5 x 6R/ONSIOR 20 mg/ml sol inj chien et chat (Novartis)robénacoxib: 20 mg/mlsolution injectable scPosologie:Fe, Ca: 2 mg/kg, environ 30 min avantl’interventionf<strong>la</strong>con 20 mlR/3.1.7 Associations d’un AINS avec d’autres substances activesLa première association comprend un antimuscarinique exerçant un effet surles muscles lisses <strong>du</strong> tractus gastro-intestinal et un antalgique <strong>du</strong> groupe despyrazolés.La seconde association, comprenant un AINS (flunixine) et une substance antibiotique(florfénicol), est indiquée dans le traitement de certaines infections respiratoiresassociées à de <strong>la</strong> fièvre chez les bovins.LMR métamizole + butylhyoscinebromure: BUSCOPAN compositum ad us vet (BoehringerIngelheim)métamizole sodique: 500 mg/mlbutylhyoscine bromure: 4 mg/mlsolution injectable iv, scPosologie:Eq: 5 ml/100 kg (iv)veau: 5 ml/50 kg (iv)Ca: 0,5 ml/5 kg (iv, sc)Viande et abats: Eq: 12 j, veau: 15 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/LMR flunixine + florfénicol: RESFLOR 300 bovins (MSD A.H.)florfénicol: 300 mg/mlflunixine (méglumine): 16,5 mg/mlsolution injectable scPosologie:Bo: 1 x 40 mg de flor/kg + 2,2 mg de flun/kgViande: 46 jNe pas utiliser chez les Bo dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine, ni chez lesBo en <strong>la</strong>ctation ou en période de tarissement nichez les futurs Bo pro<strong>du</strong>cteurs de <strong>la</strong>it destinéà <strong>la</strong> consommation dans les 2 m précédant <strong>la</strong>mise-basf<strong>la</strong>con 100 ml, 250 mlR/
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 1133.2 Analgésiques et antipyrétiques3.2.1 ParacétamolIndicationsLe paracétamol est indiqué dans le traitement symptomatique de <strong>la</strong> fièvre et de <strong>la</strong>douleur. Le paracétamol n’a pas d’action anti-inf<strong>la</strong>mmatoire.PharmacodynamieJusqu’à présent, on admettait que le paracétamol (acétaminophène) se liait plusfaiblement aux COX 1. Des études récentes mettent en doute cette hypothèsemais n’identifient pas c<strong>la</strong>irement <strong>la</strong> variante COX liée au paracétamol. L’actionantipyrétique et analgésique <strong>du</strong> paracétamol, dénuée des effets indésirablesgastro-intestinaux c<strong>la</strong>ssiques apparaissant chez d’autres AINS, reste cependantin<strong>du</strong>bitable.PharmacocinétiqueLa biodisponibilité se situe autour de 75%. La métabolisation se fait principalementpar le foie; l’élimination par les reins.Contre-indicationsLe paracétamol est contre-indiqué en cas d’hypersensibilité connue contre leparacétamol et d’insuffisance rénale et hépatique.Effets secondairesVoir 3.1.InteractionsL’administration simultanée avec des substances néphrotoxiques doit être évitée.Précautions particulières - Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir 3.1.LMR paracétamol: PRACETAM 200 mg/g poudre (Sogeval Lab)paracétamol: 200 mg/gpoudre po dans l’eau de boissonPosologie:Su: 30 mg/kg PV (max 5 j)Viande et abats: 0 jsac 10 kgR/PRACETAM 200 mg/ml sol (Sogeval Lab)paracétamol: 200 mg/mlsolution po avec l’eau de boissonPosologie:Su: 30 mg/kg pj (5 j)Viande et abats: 0 jf<strong>la</strong>con 5 lR/3.3 Analgésiques opioïdesLa plupart des analgésiques opioïdes relèvent de <strong>la</strong> légis<strong>la</strong>tion sur les stupéfiantset les substances psychotropes (respectivement AR <strong>du</strong> 31/12/1930 et AR <strong>du</strong>22/01/1998). Ces textes stipulent les conditions de dépôt, d’administration et deprescription (voir Folia veterinaria 2012 n° 2 – Points d’actualité).3.3.1 BuprénorphineIndicationsAnalgésie postopératoire chez les chiens et les chats. Potentialisation des effetssédatifs des agents ayant une action centrale chez les chiens.PharmacodynamieLa buprénorphine est un agoniste partiel des récepteurs morphiniques μ et elle esttrente fois plus puissante que <strong>la</strong> morphine. L’analgésie in<strong>du</strong>ite est dose-dépendante.Contrairement à <strong>la</strong> plupart des morphiniques, <strong>la</strong> buprénorphine présenteun effet sédatif limité lorsqu’elle est utilisée à des doses cliniques. La forte affinitépour les récepteurs μ dans le système nerveux central pourrait expliquer <strong>la</strong> longue<strong>du</strong>rée d’action de <strong>la</strong> buprénorphine. Les effets sur le système cardio-vascu<strong>la</strong>ireprovoquent une chute de <strong>la</strong> tension artérielle et un ralentissement de <strong>la</strong> fréquencecardiaque. Une dépression respiratoire est possible. Les symptômes gastro-intestinauxsont re<strong>la</strong>tivement rares.
1143 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESPharmacocinétiqueLa buprénorphine est rapidement absorbée après injection intramuscu<strong>la</strong>ire.Chez les rats, <strong>la</strong> buprénorphine est <strong>la</strong>rgement distribuée dans le foie, mais on<strong>la</strong> retrouve aussi dans le cerveau, le système gastro-intestinal et le p<strong>la</strong>centa. Labuprénorphine se lie fortement aux protéines p<strong>la</strong>smatiques (96%). Elle diffuse àtravers le p<strong>la</strong>centa dans le <strong>la</strong>it. La buprénorphine est métabolisée dans le foiepar N-désalky<strong>la</strong>tion et glucuroconjugaison. Ses métabolites sont principalementexcrétés par <strong>la</strong> bile (70%) et dans une moindre mesure par l’urine (27%). Les effetsanalgésiques se manifestent après 30 minutes environ, le pic étant habituellementobservé 1h à 1,5 h après l’administration. Des études pharmacocinétiqueset pharmacodynamiques associées ont permis de démontrer une hystérèse marquéeentre <strong>la</strong> concentration p<strong>la</strong>smatique et l’effet analgésique.Contre-indicationsLe pro<strong>du</strong>it ne doit pas être utilisé en pré-opératoire pour une césarienne. On citeégalement comme contre-indications une insuffisance rénale, l’hypothyroïdie, uneinsuffisance adrénocorticale, les animaux gériatriques ou fortement affaiblis.Effets indésirablesDe <strong>la</strong> salivation, de <strong>la</strong> bradycardie, une hypothermie, de l’agitation, une déshydratationet un myosis peuvent survenir chez le chien, et dans de rares cas, unehypertension et une tachycardie. Une mydriase et des signes d’euphorie (chatvenant se frotter, al<strong>la</strong>nt et venant et ronronnant de façon excessive) se pro<strong>du</strong>isentfréquemment chez les chats et disparaissent habituellement dans les 24 heures.La buprénorphine peut provoquer une dépression respiratoire. A moins que lesdoses recommandées ne soient dépassées, on observe rarement de <strong>la</strong> sédationlorsque <strong>la</strong> buprénorphine est utilisée comme analgésique. En cas de surdosage,on peut utiliser des antagonistes morphiniques tels que <strong>la</strong> naloxone ou des stimu<strong>la</strong>ntsrespiratoires tels que le doxapram.InteractionsLa buprénorphine peut provoquer de <strong>la</strong> somnolence, susceptible d’être potentialiséepar d’autres pro<strong>du</strong>its ayant une action centrale, tels que les tranquillisants,les sédatifs et les hypnotiques.Il est conseillé de ne pas utiliser <strong>la</strong> buprénorphine conjointement avec <strong>la</strong> morphineou d’autres analgésiques morphiniques tels que l’étorphine, le fentanyl, <strong>la</strong> péthidine,<strong>la</strong> méthadone, le papaveretum et le butorphanol.La buprénorphine a été utilisée avec succès en association avec l’acépromazine,l’alphaxalone/alphadalone, l’atropine, <strong>la</strong> dexmédétomidine, l’halothane, l’isoflurane,<strong>la</strong> kétamine, <strong>la</strong> médétomidine, le propofol, le sévoflurane, <strong>la</strong> thiopentone et<strong>la</strong> xy<strong>la</strong>zine.L’usage concomitant avec des sédatifs peut augmenter les effets dépresseurs surle rythme cardiaque et <strong>la</strong> respiration.Précautions particulières/Risques pour l’hommeAvant d’instaurer le traitement, il convient d’évaluer le rapport bénéfice/risquechez :- les animaux atteints d’un dysfonctionnement rénal, cardiaque ou hépatique ouen cas de choc,- les animaux ayant une fonction respiratoire altérée ou les animaux recevant desmédicaments susceptibles de provoquer une dépression respiratoire,- les animaux dont <strong>la</strong> fonction hépatique est altérée,- les chats cliniquement affaiblis,- les animaux âgés de moins de 7 semaines.Le profil d’innocuité de <strong>la</strong> buprénorphine administrée de manière prolongée auxchats (plus de 5 jours) n’a pas été étudié. L’effet d’un morphinique sur une blessureà <strong>la</strong> tête dépend de <strong>la</strong> nature et de <strong>la</strong> gravité de cette blessure, ainsi que del’assistance respiratoire apportée. La buprénorphine peut provoquer une dépressionrespiratoire chez l’homme et peut mettre <strong>la</strong> vie des enfants en danger encas d’ingestion accidentelle. En cas d’auto-injection ou d’ingestion accidentelle,il convient de demander immédiatement conseil à un médecin. Après un contactavec l’oeil ou <strong>la</strong> peau, rincez abondamment à l’eau froide.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune étude de toxicité sur <strong>la</strong> repro<strong>du</strong>ction n’a été réalisée sur les espècescibles. Lors de césarienne, le pro<strong>du</strong>it ne doit pas être utilisé en pré-opératoire en
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 115raison <strong>du</strong> risque de dépression respiratoire chez les nouveau-nés. La buprénorphineétant excrétée dans le <strong>la</strong>it, son utilisation n’est pas recommandée pendant<strong>la</strong> <strong>la</strong>ctation.LMR buprénorphine: , VETERGESIC MULTIDOSIS 0,3 mg/ml sol injchiens et chats (Alstoe)buprénorphine: 0,3 mg/mlsolution injectable iv, imPosologie:Ca:- analgésie post-opérat: 10-20 mcg/kg(répéter si nécessaire après 3-4 h avec 10mcg/kg ou après 5-6 h avec 20 mcg/kg),- potentialisation sédation: 10-20 mcg/kgFe: analgésie post-opérat: 10-20 mcg/kg(répéter si nécessaire 1 x après 1-2 h)f<strong>la</strong>con 10 mlR/psych3.3.2 ButorphanolIndicationsAnalgésie de courte <strong>du</strong>rée chez le chien ou le cheval. Analgésie de courte àmoyenne <strong>du</strong>rée chez le chat. Sou<strong>la</strong>gement de <strong>la</strong> douleur associée à des coliquesd’origine gastro-intestinale chez le cheval et sou<strong>la</strong>gement des douleurs viscéralesfaibles à modérées chez le chien et le chat. Sédation en association aveccertains agonistes des récepteurs alpha-2-adrénergiques chez le chien, le chatet le cheval.PharmacodynamieLe tartrate de butorphanol (R(-) énantiomère) est un analgésique à action centrale,agoniste pour les récepteurs opioïdes <strong>du</strong> sous-type kappa et antagoniste pour lesrécepteurs opioïdes <strong>du</strong> sous-type mu. Les récepteurs kappa contrôlent l’analgésie,<strong>la</strong> sédation sans dépression <strong>du</strong> système cardio-pulmonaire et <strong>la</strong> températurecorporelle, alors que les récepteurs mu contrôlent l’analgésie supraspinale, <strong>la</strong> sédation,<strong>la</strong> dépression <strong>du</strong> système cardio-pulmonaire et <strong>la</strong> température corporelle.L’activité agoniste <strong>du</strong> butorphanol est 10 x plus puissante que l’activité antagoniste.L’analgésie survient généralement dans les 15 min. suivant l’administrationintraveineuse et persiste chez le cheval habituellement 15 à 60 minutes et chez lechien, 15 à 30 min. (après une administration unique par voie IV).PharmacocinétiqueLe butorphanol est entièrement résorbé après injection IM. Le volume de distributionest important, avec des concentrations élevées dans le foie, les reins et lesintestins. Le butorphanol passe <strong>la</strong> barrière p<strong>la</strong>centaire et est excrété dans le <strong>la</strong>it.Chez l’homme, environ 80 % de <strong>la</strong> substance se lie aux protéines p<strong>la</strong>smatiques.Le butorphanol est principalement métabolisé dans le foie et excrété dans l’urine.Les métabolites ne sont pas actifs. Chez le cheval aussi bien que chez le chien, lebutorphanol a une c<strong>la</strong>irance importante (en moyenne 1,3 L/h.kg après une administrationIV chez le cheval et environ 3,5 L/h.kg après injection IM chez le chien).Chez le chat, le butorphanol a une clearance plus faible (< 1320 ml/h/kg aprèsadministration par voie SC). Le butorphanol a une demi-vie courte (moyenne < 1 hchez le cheval et < 2 h chez le chien), c’est pourquoi 97 % de <strong>la</strong> dose sera éliminéen moyenne en moins de 5 h chez le cheval (IV) et moins de 10 h chez le chien(IM). La demi-vie chez les chat est re<strong>la</strong>tivement élevée (ca. 6 h), 97 % de <strong>la</strong> doseétant éliminé après environ 30 h.La pharmacocinétique après des doses répétées n’a pas été étudiée.Contre-indicationsNe pas utiliser chez les animaux souffrant de ma<strong>la</strong>dies hépatiques ou rénales,d’hypothyroïdie ou d’hypoadrénocorticisme (ma<strong>la</strong>die d’Addison). La prudence estégalement de mise chez les animaux souffrant d’un traumatisme crânien, d’unepression intracrânienne accrue ou de troubles au niveau <strong>du</strong> système nerveuxcentral. L’association butorphanol/détomidine ne doit pas être utilisée chez leschevaux présentant des troubles <strong>du</strong> rythme cardiaque ou en cas de coliques de
1163 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESstase étant donné que cette association entraîne une ré<strong>du</strong>ction de <strong>la</strong> motilité gastro-intestinale.L’innocuité <strong>du</strong> médicament ci-dessous n’a pas été démontrée chezles chiots et les pou<strong>la</strong>ins.Voir plus loin « Précautions particulières ».Effets indésirablesCheval: excitation locomotrice (marcher), ataxie, ré<strong>du</strong>ction de <strong>la</strong> motilité gastrointestinale,dépression <strong>du</strong> système cardio-vascu<strong>la</strong>ire.Chien: dépression des systèmes respiratoire et cardio-vascu<strong>la</strong>ire, anorexie etdiarrhée, ré<strong>du</strong>ction de <strong>la</strong> motilité gastro-intestinale, douleur locale suite à uneinjection IM.Lors de surdosage apparaît une dépression respiratoire qui peut être traitée par unantagoniste des opioïdes. Chez les chevaux, d’autres signes de surdosage sont:agitation/excitation, tremblements muscu<strong>la</strong>ires, ataxie, hypersalivation, baisse de<strong>la</strong> motilité gastro-intestinale et convulsions.InteractionsL’utilisation concomitante avec d’autres médicaments inhibant le système nerveuxcentral, peut renforcer les effets <strong>du</strong> butorphanol et doit donc être envisagéeavec prudence. La dose doit être ré<strong>du</strong>ite en cas d’utilisation concomitante de cesmédicaments. Moyennant une adaptation de <strong>la</strong> dose, le butorphanol peut êtreutilisé en association avec d’autres sédatifs comme les agonistes des récepteursalpha2-adrénergiques (p. ex. romifidine ou détomidine chez les chevaux, médétomidinechez les chiens). L’association <strong>du</strong> butorphanol et d’alpha2-adrénergiquesdoit être utilisée avec prudence chez les animaux souffrant d’une affection cardiovascu<strong>la</strong>ire.L’utilisation concomitante avec des médicaments anticholinergiquestels que l’atropine p. ex., doit être envisagée. En raison de ses propriétés antagonistesvis-à-vis <strong>du</strong> récepteur mu opiacé, le butorphanol peut supprimer l’effetanalgésique chez les animaux qui ont déjà reçu des agonistes des récepteurs muopiacés purs.Précautions particulièresLe pro<strong>du</strong>it pouvant entraîner une ataxie transitoire et/ou une excitation et afin deprévenir tout risque de blessure chez l’animal traité et chez les personnes administrantle traitement, le lieu où l’injection sera pratiquée devra être choisi avec <strong>la</strong>plus grande attention, en particulier chez le cheval.Chez les animaux souffrant de ma<strong>la</strong>dies respiratoires associées à une pro<strong>du</strong>ctionaccrue de mucus ou chez les animaux traités à l’aide d’expectorants, le butorphanolqui inhibe le réflexe de <strong>la</strong> toux, devra être utilisé par le vétérinaire sur <strong>la</strong> based’une évaluation <strong>du</strong> rapport bénéfice/risque.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa sécurité <strong>du</strong> médicament n’a pas été établie chez les espèces cibles pendant <strong>la</strong>gestation et <strong>la</strong> <strong>la</strong>ctation.L’utilisation <strong>du</strong> butorphanol pendant <strong>la</strong> gestation et <strong>la</strong> <strong>la</strong>ctation n’est pasrecommandée.
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 117LMR butorphanol: BUTOMIDOR 10 mg/ml (Richter Pharma)butorphanol (tartrate): 10 mg/mlsolution injectable iv, im, scPosol:Eq:- analgésie:Eq: 0,1 mg/kg (iv)- sédation/pré-anesthésie:Eq: 0,012 mg de détomidine/kg (iv) + 0,025 mgde butorphanol/kg (iv)Eq: 0,05 mg de romifidine/kg (iv) + 0,02 mgde butorphanol/kg (iv)Eq: 0,5 mg de xy<strong>la</strong>zine/kg (iv) + 0,05 - 0,1 mgde butorphanol/kg (iv)Ca:- analgésie:Ca: 0,1 – 0,4 mg/kg (iv lente, im, sc)- sédation:Ca: 0,1 mg de butorphanol/kg (iv, im) + 0,01 mgde médétomidine/kg (iv, im)- pré-anesthésie :Ca: 0,1 mg de butorphanol/kg (im) + 0,025 mgde médétomidine/kg (im), après 15 min:5 mg de kétamine/kg (im)Fe :- analgésie:Fe: 0,4 mg/kg (sc) ou 0,1 mg/kg (iv)- sédation:Fe: 0,4 mg de butorphanol/kg (sc) + 0,05 mgde médétomidine/kg (sc)- pré-anesthésie:Fe: 0,1 mg de butorphanol/kg (iv) + 0,04 mgde médétomidine/kg (iv) + 1,5 mg dekétamine/kg (iv)Viande: Eq: 0 jf<strong>la</strong>con 10 mlR/DOLOREX (MSD A.H.)butorphanol (tartrate): 10 mg /mlsolution injectable iv, imPosologie:Eq:analgésie: 0,05 - 0,1 mg/kg (iv)sédation: 0,01 - 0,02 mg/kg (administrerd’abord 0,01 - 0,02 mg de détomidine/kg)ou0,02 mg/kg (administrer d’abord 0,05 mg deromifidine/kg) (iv)Ca:analgésie: 0,2 - 0,4 mg/kg (iv)sédation: 0,1-0,2 mg/kg (administrer d’abord0,01 - 0,03 mg de médétomidine/kg) (im)Fe:analgésie: 0,4 mg/kg (sc)Viande: 0 j, Lait: 0 jf<strong>la</strong>con 10 ml, 50 mlR/MORPHASOL 4 mg/ml sol inj chien et chat(aniMedica)butorphanol (tartrate): 4 mg/mlsolution injectable ivPosologie:Ca:analgésie: 0,2 - 0,4 mg/kgsédation: 0,1 - 0,2 mg de butorphanol/kgavec 10 - 30 mcg de médétomidine/kgFe: analgésie: 0,1-0,2 mg/kgf<strong>la</strong>con 10 mlR/MORPHASOL 10 mg/ml sol inj cheval (aniMedica)butorphanol (tartrate): 10 mg/mlsolution injectable ivPosologie:Eq:analgésie: 100 mcg/kgsédation:- 12 mcg de détomidine hydrochloride/kg (iv),suivi dans les 5 min de 25 mcg debutorphanol/kg- 40 - 120 mcg de romifidine/kg, suivi dansles 5 min de 20 mcg de butorphanol/kg- 500 mcg de xy<strong>la</strong>zine/kg, suivi immédiatementde 25 - 50 mcg de butorphanol/kgViande et abats: 0 j, Lait: 0 jf<strong>la</strong>con 20 mlR/3.3.3 FentanylIndicationLe fentanyl, un opiacé très puissant, est indiqué pour le contrôle de <strong>la</strong> douleurau cours d’interventions chirurgicales, orthopédiques et des tissus mous, particulièrementalgogènes chez le chien. Le contrôle de <strong>la</strong> douleur pendant <strong>la</strong> phasepost-opératoire est également visé.PharmacodynamieLe fentanyl est un agoniste sélectif des récepteurs opioïdes μ pro<strong>du</strong>isant une analgésieprofonde lorsqu’il est administré aux doses thérapeutiques.PharmacocinétiqueAprès injection par <strong>la</strong> voie intraveineuse, le fentanyl agit dans les minutes qui suivent.La <strong>du</strong>rée de l’effet analgésique chez les chiens est comprise entre 20 minutes et40 minutes selon que les doses recommandées les plus faibles ou les plus fortessoient utilisées. En raison de <strong>la</strong> redistribution, les concentrations p<strong>la</strong>smatiques diminuentrapidement après injection intraveineuse. Le taux de liaison aux protéinesp<strong>la</strong>smatiques est de 60 %. Le volume de distribution est supérieur à 5 l/kg. La demivied’élimination est re<strong>la</strong>tivement longue et variable (45 minutes à plus de 3 heures).
1183 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESLa c<strong>la</strong>irance p<strong>la</strong>smatique est élevée avec des valeurs al<strong>la</strong>nt de 40 à 80 ml/minutes/kg.Le fentanyl est principalement métabolisé dans le foie. Moins de 8 % de <strong>la</strong> dosetotale administrée sont éliminés sous forme inchangée. En cas d’infusion à débitconstant, <strong>la</strong> compatibilité physico-chimique a été démontrée uniquement pour desdilutions au cinquième (1/5) avec les solutés de perfusion suivants : chlorure desodium 0,9 %, solution de Ringer, et glucose 5 %.Effets indésirablesLes principaux effets indésirables sont <strong>la</strong> sédation, <strong>la</strong> dépression respiratoire et <strong>la</strong>bradycardie. La naloxone (0,01 à 0,04 mg/kg) peut être utilisée pour bloquer leseffets indésirables <strong>du</strong> fentanyl.Contre-indicationsLe fentanyl ne doit pas être administré aux chiens présentant une insuffisance cardiaque,une hypotension, une hypovolémie, une obstruction des voies aériennes,une dépression respiratoire, une hypertension, ou ayant des antécédents d’épilepsie.Ne pas administrer aux animaux présentant un dysfonctionnement hépatiqueou rénal sévère.InteractionsAprès utilisation <strong>du</strong> fentanyl, <strong>la</strong> posologie des anesthésiques doit être adaptée euégard à l’effet d’épargne vis-à-vis des anesthésiques. L’utilisation concomitantede ce pro<strong>du</strong>it avec d’autres morphiniques ou des agonistes alpha-2-adrénergiquesn’a pas été étudiée. Il est à noter que le RCP ne spécifie pas les protocolesd’anesthésie à utiliser, se limitant à signaler que les anesthésiques doivent êtreadministrés en fonction de <strong>la</strong> réponse des animaux. La responsabilité des vétérinairesest donc entièrement engagée.Précautions particulières/Risques pour l’hommeCe médicament vétérinaire doit faire l’objet d’une titration indivi<strong>du</strong>elle afin dedéterminer <strong>la</strong> dose procurant une analgésie adéquate avec le minimum d’effetsindésirables. Les doses d’autres médicaments agissant sur le système nerveuxcentral doivent être ré<strong>du</strong>ites. Le RCP ne contient toutefois aucune informationpratique et concrète à cet égard.Chez l’homme, le fentanyl peut causer des effets indésirables incluant <strong>la</strong> dépressionrespiratoire ou l’apnée, <strong>la</strong> sédation, l’hypotension et le coma, après uncontact cutané ou une auto-injection accidentelle ou volontaire. Le pro<strong>du</strong>it peutcauser des réactions d’hypersensibilité. Eviter tout contact avec les yeux ou <strong>la</strong>peau. Porter des gants imperméables pour manipuler le pro<strong>du</strong>it.Il est déconseillé aux femmes enceintes de manipuler le pro<strong>du</strong>it. En cas d’expositionaccidentelle d’une femme qui al<strong>la</strong>ite, l’al<strong>la</strong>itement doit être suspen<strong>du</strong> pendant24 heures.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes études de <strong>la</strong>boratoire sur les rats n’ont pas mis en évidence d’effets tératogènes,foetotoxiques, ou mutagènes.Le fentanyl traverse <strong>la</strong> barrière hémato-p<strong>la</strong>centaire. L’administration pendant <strong>la</strong>mise-bas peut causer une dépression respiratoire chez les fœtus. L’innocuité <strong>du</strong>médicament vétérinaire chez le chien n’a pas été établie en cas de gravidité oude <strong>la</strong>ctation. L’utilisation <strong>du</strong> pro<strong>du</strong>it n’est pas recommandée pendant <strong>la</strong> gestation.LMR fentanyl: FENTADON 50 mcg/ml (Eurovet)fentanyl (citrate): 50 mcg/mlsolution injectable iv (CRI)Posologie:Ca:- analgésie intra-opérat:5 - 10 mcg/kg (0,1 - 0,2 ml/kg) IV en bolus,puis 12 – 24 mcg/kg/h (0,24 – 0,48 ml/kg/h)IV par CRI- analgésie post-opérat:6 - 10 mcg/kg/h (0,12 - 0,2 ml/kg/h) IV par CRIf<strong>la</strong>con 10 mlR/
3 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRES 1193.3.4 MéthadoneIndicationsLa méthadone est indiquée chez le chien et le chat dans l’analgésie ou dans <strong>la</strong>prémédication en vue d’une anesthésie générale ou d’une neuroleptanalgésie enassociation avec un neuroleptique.PharmacodynamieLa méthadone est un mé<strong>la</strong>nge racémique dans lequel l’isomère D inhibe <strong>la</strong> réabsorptionde <strong>la</strong> norépinéphrine en antagonisant le récepteur NMDA, et l’isomère Lantagonise le récepteur opioïde de type µ. Les sous-types µ1 et µ2 in<strong>du</strong>isent leseffets analgésiques de <strong>la</strong> méthadone, tandis que le sous-type µ2 in<strong>du</strong>it <strong>la</strong> dépressionrespiratoire et l’inhibition de <strong>la</strong> motilité gastro-intestinale. Le sous-type µ1pro<strong>du</strong>it une analgésie supraspinale et les récepteurs µ2 pro<strong>du</strong>isent une analgésiespinale. La méthadone in<strong>du</strong>it une analgésie profonde. Elle peut aussi servir deprémédication et contribuer à <strong>la</strong> pro<strong>du</strong>ction d’une sédation en combinaison avecdes tranquillisants ou des sédatifs. La <strong>du</strong>rée des effets peut varier entre 1,5 et 6,5heures. Les opioïdes pro<strong>du</strong>isent une dépression respiratoire liée à <strong>la</strong> dose. Desdoses très élevées peuvent provoquer des convulsions.PharmacocinétiqueQue ce soit chez le chien ou le chat, <strong>la</strong> méthadone est rapidement absorbéeaprès injection intramuscu<strong>la</strong>ire. La biodisponibilité est élevée chez le chien (90 %en moyenne). Après administration sous-cutanée, <strong>la</strong> méthadone est absorbéeplus lentement ce qui ré<strong>du</strong>it sa biodisponibilité. La méthadone se lie fortementaux protéines et possède un important volume de distribution en raison de sescaractéristiques physico-chimiques (caractère lipophile, base faible). La demi-vied’élimination se situe entre 0,9 et 2,2 h chez le chien, et entre 6 et 15 h chez lechat. Une petite quantité (3 à 4 % chez le chien) de <strong>la</strong> dose administrée est excrétéesous forme inchangée dans l’urine; le reste est métabolisé dans le foie puisexcrété.Contre-indicationsNe pas administrer aux animaux présentant une insuffisance respiratoire progressiveou un dysfonctionnement hépatique ou rénal sévère.Effets indésirablesUne dépression respiratoire peut être observée, ainsi que des réactions légères :halètement, léchage des lèvres, salivation, vocalisation, respiration irrégulière,hypothermie, regard fixe et tremblements. Une miction et une défécation occasionnellespeuvent s’observer <strong>du</strong>rant <strong>la</strong> première heure suivant l’administration.Toutes les réactions étaient de nature passagère.InteractionsLa méthadone peut potentialiser les effets des analgésiques, des inhibiteurs <strong>du</strong>système nerveux central et des substances qui provoquent une dépression respiratoire.La méthadone peut être antagonisée par <strong>la</strong> naloxone.Précautions particulières et risques pour l’hommeL’innocuité de <strong>la</strong> méthadone n’a pas été démontrée chez les chiens de moins de8 semaines ni chez les chats de moins de 5 mois. La prudence s’impose en casd’utilisation chez des animaux âgés ou souffrant d’un traumatisme crânien oud’une pression intracrânienne accrue. La méthadone peut provoquer une dépressionrespiratoire en cas d’auto-injection et même après un contact cutané accidentel.Eviter tout contact avec <strong>la</strong> peau, les yeux et <strong>la</strong> bouche, et porter des gantsimperméables pour manipuler le pro<strong>du</strong>it. La méthadone est susceptible de causer<strong>la</strong> mort fœtale in utero. Il est conseillé aux femmes enceintes de ne pas manipulerle pro<strong>du</strong>it. En cas d’auto-injection accidentelle, il est indispensable de consulterun médecin en lui montrant <strong>la</strong> notice et surtout, de ne pas con<strong>du</strong>ire de véhiculeen raison <strong>du</strong> risque de sédation.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa méthadone diffuse à travers le p<strong>la</strong>centa et peut avoir des effets négatifs sur<strong>la</strong> repro<strong>du</strong>ction. L’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été démontrée chez les chiennesen gestation ou en <strong>la</strong>ctation. L’utilisation <strong>du</strong> pro<strong>du</strong>it est déconseillée pendant <strong>la</strong>gestation.
1203 ANALGÉSIQUES, ANTIPYRÉTIQUES ET ANTI-INFLAMMATOIRESLMR méthadone : COMFORTAN 10 mg/ml (Eurovet A.H.)chlorhydrate de méthadone: 10 mg/mlsolution injectable sc, im ou ivPosologie:Ca (âge > 8 sem): 0,5 - 1 mg/kg (sc, im, iv)Fe (âge > 5 m): 0,3 - 0,6 mg/kg (im)f<strong>la</strong>con 10 mlR/psych
4 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINAL 1214. MÉDICAMENTS DU SYSTÈMEGASTRO-INTESTINAL4.1 Inhibiteur de <strong>la</strong> sécrétion acide gastrique4.1.1 OméprazoleIndicationsL’oméprazole est un inhibiteur de <strong>la</strong> pompe à protons indiqué dans le traitementdes ulcères gastriques chez les chevaux (EGUS, equine gastric ulcer syndrome).D’autres facteurs ulcérogènes sont à prendre en compte dans le traitement ou <strong>la</strong>prévention des ulcères chez les chevaux, notamment, <strong>la</strong> ré<strong>du</strong>ction <strong>du</strong> stress ainsique l’adaptation <strong>du</strong> régime alimentaire et des conditions d’élevage.PharmacodynamieL’oméprazole inhibe <strong>la</strong> sécrétion gastrique acide au niveau des cellules gastriquespariétales en se liant à <strong>la</strong> pompe à protons. Il inhibe autant <strong>la</strong> sécrétion acidebasale que celle apparaissant suite à <strong>la</strong> stimu<strong>la</strong>tion des récepteurs à l’acétylcholine,à l’histamine ou à <strong>la</strong> gastrine.PharmacocinétiqueL’oméprazole est instable en milieu acide. Dès lors, son absorption est très variablelorsque les préparations utilisées ne sont pas gastroprotégées. L’usaged’une pâte peut donc contribuer à l’absence d’efficacité chez certains animaux.Après métabolisation, l’oméprazole est principalement excrété par les reins etdans une moindre proportion par <strong>la</strong> bile. Aucune accumu<strong>la</strong>tion n’a été mise enévidence après administrations répétées.Contre-indicationsHypersensibilité connue à l’oméprazole. Troubles graves de <strong>la</strong> fonction hépatiqueou rénale.Effets indésirablesAucun effet indésirable n’a été observé chez les chevaux a<strong>du</strong>ltes ou chez lespou<strong>la</strong>ins âgés d’au moins 2 mois, lors d’un traitement de 91 jours avec une dosede 20 mg/kg.InteractionsEn cas d’usage simultané, l’oméprazole peut retarder l’élimination de <strong>la</strong> warfarineet de certaines benzodiazépines <strong>du</strong> fait de son action sur le cytochrome P450.Précautions particulièresNe pas administrer aux animaux âgés de moins de 4 semaines ou pesant moinsde 70 kg.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa sécurité de l’oméprazole chez les chevaux gestants ou en <strong>la</strong>ctation n’a pas étéétablie. Son utilisation chez ces animaux est donc déconseillée.LMR oméprazole : GASTROGARD 37% pâte orale chevaux (Merial)oméprazole: 370 mgpâte poPosologie:Eq, pou<strong>la</strong>in (âge > 4 sem et PV > 70 kg),étalon repro<strong>du</strong>cteur:- prévention:1 mg/kg pj- traitement:4 mg/kg pj (28 j), suivi de 1 mg/kg pj (28 j)Viande: 1 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaineapplic 7 x 10 ml (6,16 g)R/
1224 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINAL4.2 Antispasmodiques digestifs4.2.1 Association hyoscine + métamizoleIndicationsCette combinaison peut être administrée chez le jeune veau diarrhéique pour seseffets antispasmodiques. Cependant, l’utilité des antispasmodiques lors de diarrhéereste controversée. Elle peut également être administrée chez le cheval souffrantde coliques, pour ses propriétés antispasmodique et analgésique; ou encorechez le chien, pour lutter contre les spasmes urogénitaux, gastro-intestinaux etbiliaires, <strong>la</strong> diarrhée et les vomissements.PharmacodynamieLe métamizole appartient au groupe des AINS et possède une activité antipyrétiqueet analgésique; son action anti-inf<strong>la</strong>mmatoire ne se manifestant qu’à desposologies plus élevées. Contrairement à <strong>la</strong> plupart des AINS, le métamizole possèdeégalement une activité spasmolytique. L’hyoscine ou scopo<strong>la</strong>mine appartientau groupe des alcaloïdes naturels et exerce en tant qu’anticholinergique uneffet spasmolytique sur <strong>la</strong> muscu<strong>la</strong>ture lisse <strong>du</strong> tractus gastro-intestinal, des voiesbiliaires et des voies urogénitales. En général, les douleurs disparaissent dans les15 minutes après une injection intraveineuse chez le cheval atteint de coliquesgastro-intestinales. L’effet clinique se maintient de 4 à 6 heures en fonction de <strong>la</strong>voie d’administration. Une seule injection est généralement suffisante. La <strong>du</strong>rée etl’intensité des effets pro<strong>du</strong>its con<strong>du</strong>isent à ne pas recommander cette préparationen absence de diagnostic précis.PharmacocinétiqueMétamizole: voir chapitre 3.1.2. La butylhyoscine est rapidement résorbée aprèsinjection intramuscu<strong>la</strong>ire et a une bonne distribution tissu<strong>la</strong>ire, avec des concentrationsplus élevées dans le foie et les reins. Après métabolisation, elle est excrétéepar les urines, et dans une moindre mesure par les fèces.Contre-indicationsLes dérivés de <strong>la</strong> pyrazolone sont contre-indiqués en cas d’insuffisance cardiaque,hépatique ou rénale graves, lors d’affections hématologiques et lors d’ulcèresgastriques. L’utilisation de l’hyoscine est contre-indiquée en cas de g<strong>la</strong>ucome oude constipation.Effets indésirablesLors d’un surdosage, <strong>la</strong> composante pyrazolée in<strong>du</strong>it des troubles neurologiques.Le traitement sera symptomatique. La composante anticholinergique in<strong>du</strong>it quantà elle une symptomatologie parasympathicolytique. L’antidote est <strong>la</strong> néostigmine.InteractionsL’administration simultanée avec des glucocorticoïdes augmente le risque de saignementsgastro-intestinaux. Le métamizole peut ré<strong>du</strong>ire l’activité diurétique <strong>du</strong>furosémide.Les associations avec des neuroleptiques (en particulier les phénothiazines)augmentent le risque d’hypothermie grave. Les antihistaminiques, l’atropine, lesneuroleptiques, les phénothiazines et les antidépresseurs tricycliques peuventrenforcer l’activité de l’hyoscine.Repro<strong>du</strong>ction et <strong>la</strong>ctationVoir 3.1.2 pour le métamizole.La tolérance de <strong>la</strong> butylhyoscine est en général considérée comme bonne en casde gestation. Des études de rési<strong>du</strong>s de <strong>la</strong> butylhyoscine n’ont pas relevé desquantités mesurables dans le <strong>la</strong>it des vaches.
4 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINAL 123LMR métamizole et butylhyoscine : BUSCOPAN compositum ad us vet (BoehringerIngelheim)métamizole sodique: 500 mg/mlbutylhyoscine bromure: 4 mg/mlsolution injectable iv, scPosologie:Eq: 5 ml/100 kg (iv)veau: 5 ml/50 kg (iv)Ca: 0,5 ml/5 kg (iv, sc)Viande et abats: Eq: 12 j, veau: 15 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/4.3 Antiémétiques4.3.1 MaropitantIndicationsChez le chien, les comprimés ainsi que <strong>la</strong> solution injectable à base de maropitantsont indiqués dans <strong>la</strong> prévention et le traitement des vomissements chez lechien. Pour ceux in<strong>du</strong>its par <strong>la</strong> chimiothérapie, l’usage <strong>du</strong> maropitant est plus efficacesi l’administration se fait de manière préventive. Les comprimés sont aussiindiqués dans <strong>la</strong> prévention des vomissements in<strong>du</strong>its par le mal des transports.Le traitement des vomissements se fera en association avec d’autres mesuresd’accompagnement (contrôle diététique, fluidothérapie) et avec le traitement de<strong>la</strong> cause sous-jacente.Chez le chat, <strong>la</strong> solution injectable est indiquée dans le traitement des vomissements,en association avec d’autres mesures d’accompagnement, ou dans <strong>la</strong>prévention des vomissements et pour <strong>la</strong> ré<strong>du</strong>ction des nausées, à l’exception decelles in<strong>du</strong>ites par le mal des transports.PharmacodynamieLe maropitant est un antagoniste sélectif des récepteurs aux neurokinines (NK1)qui agit en inhibant <strong>la</strong> liaison de <strong>la</strong> substance P. La substance P est considéréecomme un des principaux neurotransmetteurs impliqués dans le vomissement.De par son action au niveau <strong>du</strong> centre <strong>du</strong> vomissement, le maropitant est efficacecontre les causes nerveuses et humorales <strong>du</strong> vomissement. Les signes associésaux nausées comme <strong>la</strong> salivation excessive et <strong>la</strong> léthargie peuvent persister pendantle traitement. Le maropitant n’a pas d’activité sédative.PharmacocinétiqueLe maropitant a une pharmacocinétique non linéaire après une administrationorale, et linéaire après injection sous-cutanée. La biodisponibilité orale <strong>du</strong> maropitanta été évaluée à 23,7 % et 37,0 % selon <strong>la</strong> dose. La bio-disponibilité chezle chien et le chat après une injection SC est de 90 % environ. La liaison auxprotéines p<strong>la</strong>smatiques <strong>du</strong> maropitant chez le chien et le chat est supérieure à99 %. La variation interindivi<strong>du</strong>elle de <strong>la</strong> cinétique peut être importante après uneadministration orale. Le maropitant est métabolisé par le cytochrome P450 hépatique.Des concentrations p<strong>la</strong>smatiques effectives sont obtenues après 1 h, aussibien après administration orale qu’après injection SC. Moins de 1% est éliminépar voie rénale.Contre-indicationsL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie chez les chiots âgés de moins de 16semaines (pour les comprimés plus fortement dosés) ou de moins de 8 semaines(pour les comprimés plus faiblement dosés et <strong>la</strong> solution injectable), ni chez leschatons âgés de moins de 16 semaines, ni chez les animaux gestants ou al<strong>la</strong>itants.Effets indésirablesAprès une administration de <strong>la</strong> dose élevée chez le chien (prévention des vomissementsin<strong>du</strong>its par le mal des transports), des vomissements, généralementdans les 2 heures suivant l’administration orale, ont été fréquemment rapportés.
1244 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINALL’injection peut provoquer une douleur au point d’injection, en particulier chez leschats. Le refroidissement de <strong>la</strong> solution injectable (température réfrigérée) peutré<strong>du</strong>ire <strong>la</strong> douleur à l’injection. Dans de très rares cas, des réactions de type anaphy<strong>la</strong>ctiquepeuvent se pro<strong>du</strong>ire.InteractionsLe maropitant ayant des affinités pour les canaux calciques, il ne doit pas êtreutilisé simultanément avec des antagonistes des canaux calciques. Le maropitantest fortement lié aux protéines p<strong>la</strong>smatiques et peut entrer en compétition avecd’autres médicaments à ce niveau.Précautions particulièresIl est recommandé de donner un repas léger avant l’administration des comprimés.Le maropitant ayant des affinités avec les canaux ioniques calciques etpotassiques, il doit être utilisé avec précaution chez les animaux souffrant detroubles cardiaques ou ayant des prédispositions. Le maropitant doit aussi êtreutilisé avec précaution chez les patients souffrant de troubles hépatiques.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie en cas de gestation ou de <strong>la</strong>ctation.LMR maropitant : CERENIA 10 mg/ml (Pfizer A.H.)maropitant (citrate monohydraté): 10 mg/mlsolution injectable scPosologie:Ca, Fe: 1 x pj 1 mg/kg (max 5 j)f<strong>la</strong>con 20 mlR/4.3.2 MétoclopramideCERENIA 16 mg, 24 mg, 60 mg, 160 mg (PfizerA.H.)maropitant (citrate monohydraté):16 mg, 24 mg, 60 mg, 160 mgcomprimé poPosologie:Ca traitement et prévention:1 x pj 2 mg/kg (max 5 j)Ca prévention <strong>du</strong> mal des transports:1 x pj 8 mg/kg (max 2 j)compr 4R/IndicationsTraitement symptomatique des vomissements et de <strong>la</strong> ré<strong>du</strong>ction de <strong>la</strong> motilitégastro-intestinale associée à une gastrite, un spasme pylorique, une néphritechronique et une intolérance digestive à certains médicaments.PharmacodynamieL’action anti-émétique <strong>du</strong> métoclopramide est principalement <strong>du</strong>e à son activitéantagoniste des récepteurs D2 dans le système nerveux central, et prévientles nausées et les vomissements déclenchés par <strong>la</strong> plupart des stimuli. L’effetprokinétique sur le transit gastro-<strong>du</strong>odénal (augmentation <strong>du</strong> tonus et <strong>du</strong> rythmedes contractions de l’estomac, et ouverture <strong>du</strong> pylore) est lié à l’activité muscarinique,l’activité antagoniste des récepteurs D2 et des récepteurs 5-HT4 au niveaugastro-intestinal.PharmacocinétiqueLe métoclopramide est absorbé rapidement et complètement après administrationparentérale. Après administration sous-cutanée aux chiens et aux chats, lesconcentrations maximales sont obtenues après 15 - 30 minutes. Le métoclopramideest distribué rapidement dans <strong>la</strong> plupart des tissus et des fluides et traverse<strong>la</strong> barrière hémato-encéphalique. Le métoclopramide est métabolisé par le foie.L’élimination <strong>du</strong> métoclopramide est rapide. Chez le chien, 65% de <strong>la</strong> dose estéliminé dans les 24 heures (essentiellement par voie urinaire).Contre-indicationsNe pas administrer en cas de perforation ou d’obstruction gastro-intestinale.Eviter l’administration aux animaux atteints d’épilepsie.Effets indésirablesDans de rares cas, des effets extrapyramidaux (agitation, ataxie, positions et/oumouvements anormaux, prostration, tremblements et agressivité, vocalisation)ont été observés. Ces effets sont passagers et disparaissent à l’arrêt <strong>du</strong> traitement.Des réactions allergiques peuvent survenir dans de rares cas.
4 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINAL 125InteractionsEn cas de gastrite, il convient d’éviter l’administration simultanée de médicamentsanticholinergiques qui risquent d’inhiber les effets <strong>du</strong> métoclopramide sur <strong>la</strong> motilitégastro-intestinale. Il n’y a pas de contre-indication à l’utilisation de médicamentsanticholinergiques en cas de diarrhée simultanée si l’effet procinétiquen’est pas recherché. L’administration concomitante <strong>du</strong> métoclopramide avec desneuroleptiques dérivés de <strong>la</strong> phénothiazine (acépromazine) et de butyrophénonesaccroît le risque d’effets extrapyramidaux. Le métoclopramide peut potentialiserl’action des dépresseurs <strong>du</strong> SNC. En cas d’administration simultanée, il estconseillé d’administrer <strong>la</strong> posologie <strong>la</strong> plus basse de métoclopramide afin d’éviterune sédation excessive.Précautions particulièresLa posologie doit être adaptée chez les animaux atteints d’une insuffisance rénaleou hépatique en raison d’une augmentation <strong>du</strong> risque d’effets secondaires. La posologiedoit être respectée scrupuleusement, surtout chez les chats et les chiensde repro<strong>du</strong>ction de petite race.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été évaluée chez les espèces cibles. Les étudeschez des animaux de <strong>la</strong>boratoire n’ont pas révélé d’effets tératogènes ou foetotoxiques.L’utilisation <strong>du</strong>rant <strong>la</strong> gestation ou <strong>la</strong> <strong>la</strong>ctation ne doit se faire qu’aprèsévaluation <strong>du</strong> rapport bénéfice/risque.LMR métoclopramide: EMEPRID 1 mg/ml (Ceva Santé Animale)métoclopramide chlorhydrate: 1 mg/mlsolution poPosologie:Ca, Fe: 0,5 - 1 mg/kg pjf<strong>la</strong>con 125 mlR/EMEPRID 5 mg/ml (Ceva Santé Animale)métoclopramide chlorhydrate: 5 mg/mlsolution poPosologie:Ca, Fe: 0,5 - 1 mg/kg pj (en 2 ou 3injections)f<strong>la</strong>con 10 mlR/VOMEND ANTI-EMETICUM 5 mg/ml (Eurovet A.H.)métoclopramide chlorhydrate (monohydrate):5 mg/mlsolution injectable im, scPosologie:Ca, Fe: 0,5 mg/kg (à répéter toutes les 6 - 8 hsi nécessaire)f<strong>la</strong>con 10 ml, 20 mlR/4.4 Médicaments utilisés en cas d’obésité4.4.1 Inhibiteurs de <strong>la</strong> protéine microsomiale de transfert des triglycéridesIndicationsAide à <strong>la</strong> prise en charge <strong>du</strong> surpoids et de l’obésité des chiens a<strong>du</strong>ltes (en associationavec un régime alimentaire adapté et une augmentation de l’exercice physique)selon un programme de traitement complet.PharmacodynamieLe dirlotapide inhibe <strong>la</strong> protéine microsomale de transfert des triglycérides (PMT).Cette enzyme joue un rôle clé dans l’absorption des lipides au niveau de l’intestingrêle. Son inhibition entraîne une absorption ré<strong>du</strong>ite des lipides alimentaires,une diminution dose-dépendante en cholestérol sérique et en triglycérides et uneprésence accrue de gouttelettes contenant des triglycérides dans les entérocytes.Il est admis que ces effets sont liés à l’inhibition de <strong>la</strong> PMT au niveau des entérocytes.L’accumu<strong>la</strong>tion des triglycérides dans les entérocytes peut être suivie d’uneperte d’appétit. Le dirlotapide n’a aucun effet au niveau central.PharmacocinétiqueAprès administration orale, le dirlotapide est rapidement absorbé. La biodisponibilitéaprès administration orale est de 24 à 41 % pour le dirlotapide lorsqu’ilest administré avec l’alimentation, ou de 22 % lorsqu’il est administré à jeun.L’excrétion <strong>du</strong> dirlotapide se fait principalement par les fèces.
1264 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINALContre-indicationsNe pas utiliser : chez le chien souffrant d’insuffisance hépatique, en cas d’hypersensibilitéau principe actif ou à l’un de ses métabolites, chez <strong>la</strong> chienne enpériode de gestation ou de <strong>la</strong>ctation, chez les chiens en croissance, chez le chiendont le surpoids résulte d’une ma<strong>la</strong>die systémique telle que l’hypothyroïdie oul’hypercorticisme par exemple. Ne pas utiliser chez le chat en raison <strong>du</strong> risque dedéveloppement d’une lipidose hépatique.Effets secondairesDes vomissements parfois accompagnés de diarrhée ont été observés pendantle traitement, mais ces effets sont généralement passagers. Une augmentationlégère et sporadique des ALAT peut être observée sans être associée à des lésionshistopathologiques <strong>du</strong> foie. Dans de très rares cas, une polyphagie peutêtre observée.InteractionsLes interactions entre le dirlotapide et d’autres types de médicaments n’ont pasété étudiées.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation chez le chien destiné à <strong>la</strong> repro<strong>du</strong>ction n’a pas été évaluée. Ne pasutiliser chez <strong>la</strong> chienne en gestation et en <strong>la</strong>ctation.4.4.1.1 DirlotapideLMR dirlotapide : SLENTROL (Pfizer A.H.)dirlotapide: 5 mg/mlsolution poPosologie:Ca:dose initiale: 1 x 0,05 mg/kg pjAprès 2 sem, dose: 0,10 mg/kg pjAdapter ensuite <strong>la</strong> dose mensuellement(voir RCP)<strong>du</strong>rée de traitement max: 12 mdose max: 1 mg/kgf<strong>la</strong>con (et pipette doseuse) 20, 50 et 150 mlR/4.5 Antidiarrhéiques contenant des agentsanti-infectieuxL’utilisation d’antimicrobiens en cas de troubles intestinaux est moins souvent indiquéequ’on ne le pense généralement. Il suffit souvent de traiter les conséquencesde <strong>la</strong> diarrhée (voir le chapitre sur les réhydratants). Si l’on opte néanmoins pourun traitement antimicrobien, on choisira de préférence des médicaments qui nesont pas ou très peu résorbés par le tractus gastro-intestinal. La diarrhée peutégalement être provoquée par certains parasites ou protozoaires (tels que lescoccidies) qui portent atteinte aux muqueuses intestinales.4.5.1 AminosidesLes aminosides ont été précédemment décrits dans le chapitre 1.1.2.Rappelons ici que l’absorption orale est très faible si le tube digestif est intact.Ceci n’empêche pas que des temps d’attente soient attribués à ces préparations<strong>du</strong> fait d’une absorption même très limitée <strong>du</strong> principe actif.
4 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINAL 1274.5.1.1 ParomomycineLMR paromomycine : GABBROVET 70 (Ceva Santé Animale)paromomycine sulfate: 100 mg/gpoudre po dans le <strong>la</strong>it ou l’eau de boissonPosologie:veau (non ruminant): 25 - 50 mg/kg PV pj(3 - 5 j) (<strong>la</strong>it)Su: 25 - 40 mg/kg PV pj (3 - 5 j) (eau deboisson)Viande: veau (non ruminant): 20 j, Su: 2 jpoudre 1 kgR/4.5.1.2 ApramycineLMR apramycine : APRALAN 100 Granules (Eli Lilly)apramycine (sulfate): 100 g/kggranules po avec l’alimentationPosologie:Su: 4 - 8 mg/kg PV (100 ppm) (min 21 j)Viande et abats: 1 jsac 1 kgR/APRALAN 100 Vet Premix (Eli Lilly)apramycine (sulfate): 100 g/kgprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 4 - 8 mg/kg PV (1 kg de prémméd/1.000 kg d’aliment ou 100 ppm) (min21 j)Viande et abats: 1 jprém méd 25 kgR/premix4.5.1.3 SpectinomycineLMR spectinomycine: SPECTAM SCOUR-HALT (Ceva Santé Animale)spectinomycine (chlorhydrate) : 50 mg/mlsolution poPosologie:porcelet: posologie de base:20 mg/kg/12 h (3 j)Viande: 12 jf<strong>la</strong>con 100 mlR/4.5.2 PolymyxinesLes polymyxines ont été traitées précédemment (voir chapitre 1.1.6.1).La capacité de <strong>la</strong> colistine à complexer les toxines bactériennes est à souligner.La colistine est très lentement et faiblement absorbée per os.LMR colistine : COLISTINEMIX 1.200.000 UI/g (Eurovet)colistine sulfate: 1.200.000 UI/gpoudre po dans l’eau de boisson, le <strong>la</strong>itPosologie:veau: 2 x pj 10 g de poudre/250 kg PV(3 - 5 j)Su: 17 - 30 g de poudre/250 kg PVViande: veau: 7 j, Su: 2 jpoudre 1 kgR/COLIPLUS 2 000 000 IU/ml (Divasa-Farmavic)colistine (sulfate): 2000 000 UI/mlsolution poPosologie:veau, Su, agneau: 100.000 UI/kg pj (3 - 5 j)vo<strong>la</strong>ille: 75.000 UI/kg pj (3 - 5 j)Viande et abats: 1 j, Œufs : 0 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 1 lR/COLISTIMAX 1200 pulvis (Ke<strong>la</strong> Laboratoria)colistine sulfate: 1.200.000 UI eq. 50 mg/gpoudre po avec le <strong>la</strong>it ou l’eau de boissonPosologie:veau (non ruminant):2 x 50.000 UI/kg pj (3-5 j)porcelet: 100.000 UI/kg pj (3-5 j)Viande: veau: 1 j, porcelet: 1 jpoudre 1000 gR/COLISTINE EUROVET 400.000 UI/ml (Eurovet)colistine sulfate: 400.000 UI/mlsolution po dans l’eau de boisson, le <strong>la</strong>itPosologie:veau: 80.000 UI/kg pj (en 2 x) (5 - 7 j)Su: 80.000 - 144.000 UI/kg pj (5 - 10 j)vo<strong>la</strong>ille: 60.000 - 80.000 UI/kg pj (3 - 5 j)Viande: 1 j, Oeuf: 0 jf<strong>la</strong>con 1 lR/COLIVET bolus 150 mg (Prodivet)colistine (sulfate): 150 mgcomprimé (bolus) poPosologie:veau: 2,5 mg/kg 2 x pj (3 - 5 j)Viande: veau: 3 jcompr 20, 100R/COLIVET Quick Pump (Prodivet)sulfate de colistine: 8 mg/mlsuspension poPosologie:porcelet: 6,4 mg/kg toutes les 24 h (max 5 j),en cas d’infect grave, traitement peut êtrerépété toutes les 12 h (max 5 j)Temps d’attente: Su: 3 jf<strong>la</strong>con 100 mlR/
1284 MÉDICAMENTS DU SYSTÈME GASTRO-INTESTINALEMDOCOLIN 10% (Emdoka)colistine sulfate: 100 mg/gpoudre po dans le <strong>la</strong>it (veau), dans l’eau deboisson (Su)Posologie:veau: 5 mg/kg pj , à répartir sur deux repas,(3-7 j)Su: 5 mg/kg pjViande: veau, Su: 1 jpoudre 1 kg, 2 kgR/EMDOCOLIN 50% (Emdoka)colistine sulfate: 500 mg/gpoudre po dans le <strong>la</strong>it, dans l’eau de boissonPosologie:veau: 5 mg/kg PV pj (à répartir sur 2 repas)(<strong>la</strong>it) (3 - 7 j)Su: 5 mg/kg PV pj (eau de boisson) (3 - 7 j)Viande: Bo, Su: 1 jpoudre 1 kgR/EMDOCOLIN TABS (Emdoka)colistine (sulfate): 121,56 mgcomprimé poPosologie:veau (non-ruminant): 5 mg/kg pj (3 - 5 j)(veau < 48 h: en 2 prises pj)Viande: 1 jcompr 20, 100R/PROMYCINE 400 IU/mg prém méd (VMD)colistine sulfate: 400.000 UI/gprémé<strong>la</strong>nge médicamenteux poPosologie:Su: 100.000 UI/kg pj (5 j)Viande: 1 jprém méd 25 kgR/premixPROMYCINE BOLUS 3 MIO UI/bolus (VMD)colistine sulfate: 3.000.000 UIcomprimé (bolus) poPosologie:veau: 100.000 UI/kg pj en 2 prisesViande: 1 jcompr 40R/PROMYCINE PULVIS 1.000 UI/mg (VMD)colistine sulfate: 1.000.000 UI/gpoudre po dans l’eau de boissonPosologie:veau, Su: 100.000 UI/kg pj (5 - 7 j)vo<strong>la</strong>ille: 150.000 UI/kg pj (5 - 7 j)Viande: veau: 1 j, Su: 2 j, Av: 0 jNe pas administrer aux Av dont les œufs sontdestinés à <strong>la</strong> consommation humainepoudre 1 kgR/PROMYCINE PULVIS 4.800 IU/mg (VMD)colistine sulfate: 4.800.000 UI/gpoudre po dans l’eau de boisson, dans le <strong>la</strong>itPosologie:veau, Su: 100.000 UI/kg pj (5 - 7 j)vo<strong>la</strong>ille: 150 000 UI/kg pj (5 - 7 j)Viande: veau: 1 j, Su: 2 j, vo<strong>la</strong>ille: 0 jNe pas administrer aux Av dont les œufs sontdestinés à <strong>la</strong> consommation humainepoudre 1 kgR/
5 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISME 1295. MÉDICAMENTS AGISSANTSUR LE MÉTABOLISME5.1 Médicaments réhydratantsIndicationsIls sont utilisés en vue de corriger les troubles hydriques, électrolytiques, acidobasiqueset énergétiques survenant au cours de diverses pathologies, notamment<strong>la</strong> diarrhée néonatale chez le veau. Chez le veau, les réhydratants oraux peuventêtre administrés au seau, au biberon ou à <strong>la</strong> sonde.PharmacodynamieL’apport exogène de potassium permet d’entraver <strong>la</strong> diminution <strong>du</strong> taux de potassiumintracellu<strong>la</strong>ire. Cette diminution peut, en cas d’acidose notamment, êtreaccompagnée d’une hyperkaliémie empêchant un apport direct en potassium, parvoie intraveineuse surtout. Les agents alcalinisants peuvent être apportés sousforme de bicarbonate ou de précurseurs de celui-ci (citrate, propionate, acétate et<strong>la</strong>ctate). Ceux-ci ont pour avantage d’in<strong>du</strong>ire des effets alcalinisants moins brusqueset moins prolongés que le bicarbonate. Cependant, ces précurseurs présentent ledésavantage de devoir être métabolisés au niveau <strong>du</strong> foie et/ou des tissus périphériques.Une combinaison des deux types d’alcalinisants semble donc raisonnable.Le pouvoir alcalinisant des diverses préparations disponibles sur le marché est trèsvariable et peut être pris en compte dans le choix thérapeutique. Le glucose, le<strong>la</strong>ctose ou le <strong>la</strong>ctosérum assurent un certain apport calorique, le plus souvent limitépar rapport aux besoins énergétiques réels de l’animal.PharmacocinétiqueLes médicaments réhydratants seront administrés soit par voie orale, soit par voieparentérale (essentiellement intraveineuse) en fonction de l’état clinique de l’animal.On veillera à respecter le rythme de perfusion recommandé pour couvrir les déficitshydriques, les besoins quotidiens et les pertes à venir. L’absorption intestinalede l’eau dépend essentiellement de l’absorption <strong>du</strong> sodium. Certains composés,comme le glucose et <strong>la</strong> glycine, favorisent l’absorption intestinale <strong>du</strong> sodium.Contre-indicationsLa réhydratation orale chez les animaux souffrant d’iléus est contre-indiquée. Demême, l’apport de liquide à un animal suppose une fonction rénale efficiente, afind’éviter <strong>la</strong> formation d’œdème.InteractionsCertains réhydratants oraux ne doivent pas être administrés simultanément à desaliments médicamenteux contenant des tétracyclines. L’administration simultanéede <strong>la</strong>it de vache et de réhydratants oraux contenant <strong>du</strong> bicarbonate ou <strong>du</strong>citrate peut être contre-indiquée pour des raisons de digestibilité <strong>du</strong> <strong>la</strong>it.5.1.1 Réhydratants à administrer par voie oraleEFFYDRAL (Pfizer A.H.)sodium chlorure: 2,34 gpotassium chlorure: 1,12 gsodium hydrogénocarbonate: 6,72 gacide citrique anhydrique: 3,84 g<strong>la</strong>ctose: 32,44 gglycine: 2,25 gcomprimé effervescent po dans l’eau deboissonPosologie:1 compr/l d’eauveau: 2 x pj 2 - 3 l/animal (2 j, si nécessaire4 j), ensuite 1 - 1,5 l de sol d’Effydral +1 - 1,5 l de <strong>la</strong>it ou de <strong>la</strong>it artificielViande: 0 jcompr 48EUROLECTROL (Eurovet)sodium chlorure: 152 mg/gpotassium chlorure: 17,6 mg/gbicarbonate de soude: 117,6 mg/gglucose: 711,8 mg/gpoudre po dans l’eau de boissonPosologie:Eq, Bo, Su, Ov, Capr, Ca, Fe:25 g de poudre/l d’eau/10 kg PV pj (en3 - 5 x)Temps d’attente: 0 jpoudre 1 kg, 5 kg
1305 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISMELACTOLYTE (Virbac)poudre <strong>la</strong>ctosérum: 76,88 g/90 gsodium acétate anhydre: 4,9 g/90 gsodium propionate anhydre: 1,92 g/90 gsodium chlorure anhydre: 2,92 g/90 gpotassium chlorure anhydre: 0,74 g/90 gmagnésium chlorure anhydre: 0,38 g/90 gphosphate monopotassique anhydre:1,36 g/90 gpoudre po dans l’eau de boissonPosologie:Bo (veau): 2 x pj 90 g de poudre/2 l d’eau(2 - 3 j)Viande: 0 j, Lait: 0 jpoudre 8 x 90 g5.1.2 Réhydratants à administrer par voie parentéraleB.BRAUN VET CARE hypertonique NaCl sol(B. Braun Melsungen)chlorure de sodium: 7,5 g/100 mlsolution pour perfusion ivPosologie:Eq, Bo, Su, Ov, Capr, Ca, Fe: 3 à 5 ml/kg PVen 15 minutes (1 ml/kg/min),suivi d’une perfusion de fluides isotoniquesViande et abats: 0 j, Lait: 0 hf<strong>la</strong>con 10 x 500 mlR/B.BRAUN VET CARE Ringer Lactate Hartmann sol(B. Braun Melsungen)chlorure de sodium: 0,600 g/100 mlchlorure de potassium: 0,040 g/100 mlchlorure de calcium dihydraté: 0,027 g/100 ml(S) <strong>la</strong>ctate de sodium: 0,312 g/100 mlsolution pour perfusion ivPosologie:Eq, Bo, Su, Ov, Capr, Ca, Fe: 5 - 25 ml/kg/h(recommandé: 15 ml/kg/h, à adapter en casde choc)Viande et abats: 0 j, Lait: 0 hf<strong>la</strong>con 10 x 500 ml ou 10 x 1000 mlR/LACTETROL (Eurovet)sodium chlorure: 5,76 mg/mlpotassium chlorure: 0,37 mg/mlcalcium chlorure: 0,37 mg/mlmagnésium chlorure: 0,20 mg/mlsodium <strong>la</strong>ctate: 10,08 mg/mlsolution injectable iv, ip, scPosologie:Eq, Bo, Su, Ov, Capr, Ca, Fe: 30 - 50 ml/kgpj (répéter en cas de nécessité)Temps d’attente: 0 jf<strong>la</strong>con 500 mlR/SOLUTION PHYSIOLOGIQUE (Eurovet)sodium chlorure: 9 mg/mlsolution injectable iv, scPosologie:Eq, Bo, Su, Ca, Fe:dose d’entretien indicative les premières4 - 6 h: 100 - 150 ml/kg PV, les 20 - 24 hsuivantes: 50 - 100 ml/kgTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/5.2 GlucoseIndicationsLes solutions hypertoniques (glucose 300 mg/ml) sont indiquées dans les affectionsliées à un déficit énergétique, telles que l’acétonémie chez <strong>la</strong> vache ou <strong>la</strong>toxémie gravidique chez <strong>la</strong> brebis et <strong>la</strong> chèvre. La solution isotonique (glucose 5g/100 ml) est indiquée dans le traitement de <strong>la</strong> déshydratation, en l’absence d’unétat de choc, chez les bovins, ovins, caprins, porcins, chevaux, chiens et chats.Elle peut également être utilisée pour corriger une hypernatrémie en compensant<strong>la</strong> perte d’eau et contribuer à <strong>la</strong> correction d’une hyperkaliémie en facilitant <strong>la</strong>pro<strong>du</strong>ction d’insuline qui, à son tour, entraîne un mouvement <strong>du</strong> potassium p<strong>la</strong>smatiquevers l’intérieur des cellules.PharmacodynamieLes solutions hypertoniques (300 mg/ml) fournissent environ 3,4 kCal/g de glucose.La solution concentrée à raison de 5 g/100 ml est isotonique au momentde l’administration, évitant ainsi l’hémolyse par choc osmotique. Le glucose étantensuite métabolisé en eau, l’effet final est celui de l’administration d’une solutionhypotonique. La solution isotonique (glucose 5 g/100 ml) fournit environ 4 kcal/gde glucose.PharmacocinétiqueLa perfusion intraveineuse permet une distribution rapide. Les constituants de <strong>la</strong>solution pour perfusion sont métabolisés et excrétés par les mêmes voies quel’eau et le glucose d’origine alimentaire. Si <strong>la</strong> vitesse de perfusion dépasse 0.5 g
5 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISME 131de glucose/kg PV/h, un effet diurétique apparaîtra suite à <strong>la</strong> glucosurie.Contre-indicationsLa solution hypertonique ne peut pas être administrée aux animaux déshydratés.La solution isotonique (glucose 5 g/100 ml) ne convient pas pour <strong>la</strong> correctiond’une déshydratation hypotonique. L’administration sous-cutanée estdéconseillée.Effets indésirablesLorsque l’injection iv n’est pas suffisamment minutieuse, une phlébite et des réactionstissu<strong>la</strong>ires peuvent se pro<strong>du</strong>ire sur le site d’administration.InteractionsNe pas administrer avec d’autres médicaments. On a constaté des incompatibilitésavec certains antibiotiques (tels que les bêta-<strong>la</strong>ctamines, les tétracyclines, <strong>la</strong>sulfadiazine sodique) et l’héparine.Précautions particulièresLa solution hypertonique doit être administrée exclusivement par voie intraveineuse.La solution doit être administrée à <strong>la</strong> température <strong>du</strong> corps. Une perfusionexcessive peut con<strong>du</strong>ire à une hyperhydratation et une hypertension.L’administration excessive de glucose peut entraîner une hyperglycémie, une glycosurieet une polyurie.Repro<strong>du</strong>ction et <strong>la</strong>ctationAucune restriction connue.LMR glucose : GLUCOSE 30 % (Eurovet)dextrose (monohydrate): 300 mg/mlsolution injectable ivPosologie:Bo acétonémie: 0,5 g/kgOv, Capr toxémie gravidique: 5-7 g/kgTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/5.3 VitaminesGLUCOSE 30 % Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)glucose (monohydrate): 300 mg/mlsolution injectable ivPosologie:Bo: 150 - 300 mg/kgTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/GLUCOSE 5 g/100 ml B. BRAUN VET CARE (B.Braun Melsungen)glucose (monohydrate): 5 g/100 mlsolution pour perfusion ivPosologie:bovins, chevaux, ovins, caprins, porcins,chien et chatsViande et abats: 0 j, Lait: 0 hf<strong>la</strong>con 10 x 500 mlR/L’administration de vitamines ne devrait jamais être effectuée de manière systématiquemais devrait toujours être réalisée dans un but thérapeutique bien précis,considérant les besoins journaliers et les apports alimentaires. Il est égalementimportant de rappeler que pour certaines vitamines, le surdosage peut donner lieuà une intoxication; c’est en particulier le cas pour les vitamines A et D.5.3.1 Vitamine BLes vitamines traditionnellement c<strong>la</strong>ssées dans le groupe B interviennent dansdifférents processus métaboliques. Ces vitamines sont essentielles au régime alimentairede <strong>la</strong> plupart de nos animaux domestiques. Les ruminants font exceptionà <strong>la</strong> règle, leur flore ruminale fonctionnant comme source de vitamine B. Le déficiten vitamines <strong>du</strong> groupe B, qui se manifeste généralement sous forme de troublesnerveux et d’affections cutanées, apparaît rarement lorsque l’alimentation est bienéquilibrée. Un apport supplémentaire, par mesure de précaution, pourrait garantirl’ingestion des besoins optimaux, nécessaires pour maintenir une pro<strong>du</strong>ction optimale.Les besoins optimaux varient en fonction des aliments ingérés, <strong>du</strong> stresset de l’état physiologique de l’animal. Une hypovitaminose B1 secondaire peutainsi être in<strong>du</strong>ite par <strong>la</strong> prolifération de <strong>la</strong> flore pro<strong>du</strong>ctrice de thiaminase en casd’acidification <strong>du</strong> rumen ou encore par l’ingestion simultanée d’un taux élevé de
1325 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISMEthiaminase. Les besoins en vitamine B6 sont augmentés dans un régime alimentaireriche en protéines, et sont plus élevés chez les porcs charcutiers que chez lesanimaux de repro<strong>du</strong>ction. L’acide folique a un effet bénéfique sur <strong>la</strong> repro<strong>du</strong>ction,car en empêchant <strong>la</strong> mortalité embryonnaire ou fœtale, il in<strong>du</strong>it une augmentationdes portées. L’utilisation de préparations associant différentes vitamines semblepeu adéquate, même si le risque d’hypervitaminose est re<strong>la</strong>tivement faible pources vitamines hydrosolubles.LMR vit B1 + vit B2 + vit B5 + vit B6 + vit B12: VITAMINE B COMPLEX Ke<strong>la</strong> (Ke<strong>la</strong> Laboratoria)thiamine HCl (vit B1): 10 mg/mlribof<strong>la</strong>vine phosphate de sodium( vit B2):5,4 mg/mlnicotinamide HCl (vit B3): 25 mg/mldexpanthénol (vit B5): 5 mg/mlpyridoxine HCl (vit B6): 4 mg/mlcyano-coba<strong>la</strong>mine (vit B12): 10 mcg/mlsolution injectable imPosologie:Su, admin unique:- (jusqu‘à 10 kg): 1 ml/5 kg- (entre 10 - 50 kg): 1 ml/10 kg- (> 50 kg, cochette, verrat incl), truie en<strong>la</strong>ctation: 0,5 ml/10 kg- truie gestante, verrat a<strong>du</strong>lte: 0,25 ml/10 kgTemps d‘attente: 0 jf<strong>la</strong>con 100 mlR/5.3.2 Vitamine DLa vitamine D est un composé liposoluble indiqué dans <strong>la</strong> prévention et le traitement<strong>du</strong> rachitisme et de l’ostéoma<strong>la</strong>cie, dans le traitement des états hypocalcémiqueset dans <strong>la</strong> prévention de <strong>la</strong> fièvre de <strong>la</strong>it. Le 1,25-dihydroxy D3 régulel’absorption <strong>du</strong> calcium au niveau intestinal ainsi que l’incorporation et <strong>la</strong> mobilisation<strong>du</strong> calcium et <strong>du</strong> phosphore dans les os. On utilise généralement le cholécalciférol(vitamineD3) qui, pour exercer son activité, doit être métabolisé auniveau hépatique en calcifédiol (25-hydroxy D3) et hydroxylé une nouvelle foisdans le rein en calcitriol (1,25-dihydroxy D3). L’intoxication à <strong>la</strong> vitamine D3 peutentraîner des calcifications anarchiques au niveau des tissus mous et en particulierles vaisseaux et les reins. Pour cette raison, on évitera l’administration dedoses excessives et on fera systématiquement attention aux apports calciques.LMR vit D: DUPHAFRAL D3 1000 (Pfizer A.H.)vitamine D3: 1.000.000 UI/mlsolution injectable imPosologie:Bo: 10 ml (8 - 2 j avant <strong>la</strong> mise bas), répéteraprès 8 j si nécessaireTemps d’attente: 0 jf<strong>la</strong>con 10 x 10 mlR/5.3.3 Association vitamine A + vitamine D3 + vitamine EL’effet de <strong>la</strong> vitamine D a été décrit précédemment. La carence en vitamine E (tocophérol),associée ou non à une carence en sélénium, provoque des lésions muscu<strong>la</strong>iresdégénératives et des lésions vascu<strong>la</strong>ires. La carence en vitamine E peutêtre à l’origine de myopathies chez diverses espèces (ex: myopathie dyspnée ouma<strong>la</strong>die <strong>du</strong> muscle b<strong>la</strong>nc chez le veau). La vitamine E possède des propriétés anti-oxydanteset maintient ainsi l’intégrité cellu<strong>la</strong>ire. Elle présente donc une activitéanalogue à celle <strong>du</strong> sélénium. Dans <strong>la</strong> mesure où il n’y a pas de sélénium associéà <strong>la</strong> préparation utilisée, un surdosage en vitamine E reste généralement sansconséquence. En ce qui concerne <strong>la</strong> vitamine A, une carence est associée à une
5 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISME 133baisse des performances zootechniques, à de l’infécondité et à une diminutionde <strong>la</strong> résistance aux infections et aux infestations parasitaires. Chez le jeune, unecarence en vitamine A peut s’accompagner de cécité. Il faut cependant veillerà administrer les complexes contenant les vitamines D et A avec prudence. Eneffet, si l’intoxication à <strong>la</strong> vitamine D peut entraîner des calcifications anarchiquesau niveau des tissus mous, l’hypervitaminose A in<strong>du</strong>it des troubles articu<strong>la</strong>ireset peut avoir des effets tératogènes. Un apport supplémentaire de vitamine A enpériode de gestation n’est donc pas recommandé.LMR vit A + vit D + vit E: DUPHAFRAL AD3E (Pfizer A.H.)vitamine A: 500.000 UI/mlvitamine D3: 50.000 UI/mlvitamine E: 50 mg/mlsolution injectable imPosologie:Eq, Bo: 1 ml/100 kg (max 6 ml/animal)Su, Ov: 1 ml/100 kg (max 2 ml/animal)génisse, jeune Eq: 0,5 ml/100 kg (max 2 ml/animal)veau: 0,5 ml/100 kg (max 1 ml/animal)agneau, porcelet: 0,1 ml/10 kg (max 0,5 ml/animal)(préventif: 1 inj/2 - 3 m)Viande: 8 j, Lait: 0 jf<strong>la</strong>con 50 mlR/5.4 MinérauxVITAMINE A + D3 + E inj (VMD)vitamine A: 50.000 UI/mlvitamine D3: 25.000 UI/mlvitamine E acétate: 20 mg/mlsolution injectable imPosologie:veau: 1 ml/100 kg - max 3 mltruie: 3 ml/100 kg - max 6 mlporcelet: 0,5ml/10 kg - max 2 mlViande et abats: veau, truie, porcelet: 28 jf<strong>la</strong>con 100 mlR/VITAMINE A + D3 + E sol buvable (VMD)vitamine A: 50.000 UI/mlvitamine D3: 25.000 UI/mlvitamine E: 20 mg/mlsolution po avec l’eau de boissonPosologie:Eq, Bo: 20 mlpou<strong>la</strong>in, veau, Su, porcelet: 1 ml/10 kgOv, agneau: 1 ml/6 kgpoule pondeuse: 200 ml/1000 animauxpoule de chair: 100 ml/1000 animauxf<strong>la</strong>con 1 lR/Tout comme l’administration de vitamines, l’administration de minéraux ne devraitjamais être effectuée de manière systématique mais devrait toujours être réaliséedans un but thérapeutique bien précis, considérant les besoins journaliers et lesapports alimentaires. Il est également important de rappeler que pour certainsminéraux, le surdosage peut donner lieu à une intoxication; c’est le cas pour le fer,le cuivre et le calcium.5.4.1 FerLe fer est utilisé dans <strong>la</strong> prévention et le traitement de l’anémie, tout particulièrementchez le porcelet. Le fer est souvent combiné au dextran, pour donner despréparations injectables d’où le fer se libère progressivement. Le fer peut égalementêtre fixé sur un holoside polymérisé (polymaltose). L’injection de fer peutin<strong>du</strong>ire des réactions locales oedémateuses au point d’injection et in<strong>du</strong>ire deschangements de coloration de <strong>la</strong> viande liés à un dépôt d’hémosidérine qui peutpersister jusqu’à l’abattage. Des cas de mortalité de porcelets ont été décrits suiteà l’injection de fer-dextran. Ces cas ont essentiellement été observés chez desporcelets dont les mères avaient reçu une nourriture riche en graisses oxydées etqui étaient prédisposés aux affections muscu<strong>la</strong>ires dégénératives. Un état de déficienceen vitamine E serait responsable de cette sensibilité. De manière générale,le risque de toxicité est plus important pour les préparations injectables que pourles préparations destinées à <strong>la</strong> voie orale. Outre de <strong>la</strong> nécrose hépatique, l’excèsde fer peut causer deux syndromes distincts:- le premier est caractérisé par une dépression sévère, un choc et une acidose,- le second est une réaction de type anaphy<strong>la</strong>ctique.
1345 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISMELMR fer (dextran): FERRAJECT-200 (Eurovet)fer (dextran): 200 mg/mlsolution injectable imPosologie:- préventif:porcelet (âge 3 - 5 j): 1 ml/animal- curatif:veau, porc de chair, porcelet: 1 ml/40 kgTemps d’attente: 0 jf<strong>la</strong>con 100 ml, 250 mlR/FERROHIPRA 200 (Hipra Lab)fer (dextran): 200 mg/mlsolution injectable imPosologie:porcelet:- préventif (âge 1 - 4 j): 100 - 150 mg/animalen 1 dose (peut être répété à l’âge de 2 sem)- curatif: 100 - 200 mg/animal en 1 dose(peut être répété après 10 à 15 j)Temps d’attente: 0 jf<strong>la</strong>con 12 x 250 mlR/UNIFERON 200 mg/ml (Pharmacosmos)fer 3+ (dextran complexe): 200 mg/mlsolution injectable im, (sc)Posologie:porcelet (âge 2 - 5 j): 1 ml/animalTemps d’attente: 0 jf<strong>la</strong>con 12 x 200 mlR/5.4.2 SéléniumLe sélénium est indiqué dans <strong>la</strong> prévention des carences en sélénium. Le séléniumfait partie intégrante des enzymes glutathion peroxydase (GSHPx), qui sontimpliquées dans <strong>la</strong> protection contre le stress oxydatif. Ces enzymes agissenten synergie avec <strong>la</strong> vitamine E et d’autres antioxydants pour l’élimination desperoxydes cytotoxiques et <strong>la</strong> prévention des dommages liés à l’oxydation desmembranes. Dans <strong>la</strong> thyroïde, le sélénium est nécessaire à <strong>la</strong> con<strong>version</strong> de l’hormonethyroïdienne T4 (thyroxine) en T3 (tri-iodothyronine), <strong>la</strong> forme active de cettehormone. Le sélénium intervient comme un cofacteur dans les enzymes iodothyroninedéiodinase à l’origine de cette con<strong>version</strong> de T4 en T3. Voir aussi 5.5.1.Association vitamine E + sélénium.LMR sélénium: SELENATE LA 50 mg/ml (Cross Vetpharm Group)sélénium (sélénate de baryum): 50 mg/mlsuspension injectable scPosologie:Bo: 1 mg de Se/kg (max 1 x/an)Viande et abats: 31 j, Lait: 0 hf<strong>la</strong>con 50 mlR/5.4.3 Association calcium + magnésiumLe calcium est indiqué dans le traitement de <strong>la</strong> fièvre vitu<strong>la</strong>ire et des tétaniesdiverses. Le chlorure de magnésium est associé au calcium dans le traitement desétats hypocalcémiques. Lorsque le magnésium est prédominant dans certainespréparations, il permet le traitement des états hypomagnésémiques, parfois appeléstétanies d’herbage, même si <strong>la</strong> cause de <strong>la</strong> tétanie est plutôt secondaire.Le chlorure joue ici un rôle important : en stimu<strong>la</strong>nt le caractère acidogène del’équilibre électrolytique, il favorise l’absorption <strong>du</strong> calcium aussi bien que <strong>du</strong> magnésium.Le chlorure de calcium, injecté uniquement par voie intraveineuse, estmaintenant remp<strong>la</strong>cé par des complexes organiques de calcium, moins irritants etpouvant être administrés par voie intraveineuse et sous-cutanée. L’administrationtrop rapide de calcium par voie intraveineuse peut in<strong>du</strong>ire une hypotension, desarythmies et un arrêt cardiaque. L’administration concomitante de hautes dosesde vitamine D peut augmenter l’absorption <strong>du</strong> calcium et in<strong>du</strong>ire une hypercalcémie.D’autres substances, d’utilité discutable, sont parfois associées au calciumet au magnésium.
5 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISME 135LMR calcium + magnésium : PARPUMAG 30% (Eurovet)magnésium chlorure: 33,3 mg/mlcalcium gluconate: 298 mg/mlsolution injectable iv (Eq, Bo, Su, Ov), sc (Bo,Ov)Posologie:Eq: 5 ml/10 kgBo, Su, Ov: 10 ml/10 kg(peut être répété après 6 - 8 h)Viande: 0 j, Lait: 0 jf<strong>la</strong>con 500 mlR/5.4.4 Associations calcium + magnésium + autresLMR calcium + magnésium + acideborique: CALCII BOROGLUCONAS (Eurovet)calcium gluconate: 187 mg/mlmagnésium chlorure: 60 mg/m<strong>la</strong>cide boriquesolution injectable ivPosologie:Eq, Bo: 500 ml/animalOv: 1 ml/kgPeut être répété après 6 - 8 hTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/CALCIUMBORO-kel (Ke<strong>la</strong> Laboratoria)calcium (gluconate): 279,24 mg/mlmagnésium (chlorure): 40 mg/m<strong>la</strong>cide borique: 77,05 mg/mlsolution injectable ivPosologie:Bo (500 - 600 kg): 500 ml/animalOv: 1 ml/kgTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/LMR calcium + magnésium +butafosfan: CALPHONE (Bayer)gluconate de calcium: 95 g/500 mlgluceptate de calcium : 22,5 g/500 mlsaccharate de calcium : 5 g/500 ml(11 g de calcium au total)chlorure de magnésium : 30 g/500 mlbutafosfan: 2 g/500 mlsolution pour perfusion iv (Bo, Ca), im, sc (Ca)Posologie:Bo (+/- 500 kg): 250 mlveau (+/- 50 à 100 kg): 30 - 50 mlCa: 2,5 - 10 mlViande: 0 j, Lait: 0 jf<strong>la</strong>con 500 mlR/5.5 Vitamines + minéraux5.5.1 Association vitamine E + séléniumLe sélénium est associé à <strong>la</strong> vitamine E dans de nombreuses préparations injectablescar leurs propriétés sont analogues. La principale indication est <strong>la</strong> préventionde myopathies dégénératives chez les ovins, les bovins et les porcs (ma<strong>la</strong>diedes muscles b<strong>la</strong>ncs ou white muscle disease, cardiopathie muriforme ou mulberryheart disease). La littérature mentionne d’autres indications. Celles-ci nesont cependant pas reprises dans les notices des pro<strong>du</strong>its cités ci-dessous. Lesélénium et <strong>la</strong> vitamine E interviennent tous deux dans le métabolisme cellu<strong>la</strong>ire<strong>du</strong> soufre. La vitamine E est un antioxydant : avec le sélénium, elle protège lesglobules rouges contre l’hémolyse et prévient les effets de <strong>la</strong> peroxydase sur lesacides gras non saturés dans <strong>la</strong> membrane cellu<strong>la</strong>ire. La vitamine E est stockéedans le tissu adipeux. Elle ne passe que très peu <strong>la</strong> barrière p<strong>la</strong>centaire. Chezdiverses espèces animales, il a été démontré que le surdosage en sélénium peutparticiper à un stress oxydatif. Il est important de noter que <strong>la</strong> toxicité <strong>du</strong> séléniumest élevée dans les associations. Des tremblements et de l’incoordination peuventêtre observés après administration unique par voie parentérale. La présence dansl’alimentation de nutriments antioxydants (vitamine E, Se, caroténoïdes, vitamineC, oligo-éléments) peut stimuler l’action antioxydante de <strong>la</strong> vitamine E et <strong>du</strong> Se
1365 MÉDICAMENTS AGISSANT SUR LE MÉTABOLISMEs’ils sont en quantité modérée, ou accélérer le passage vers un stress oxydatifs’ils sont en quantité excessive.LMR vit E + sélénium: ETOSOL-SE (Eurovet)alpha-tocopherylis acetate : 50 mg/mlsélénium sodique anhydr: 0,987 mg/mlsolution injectable scPosologie:veau: 1 ml/10kgViande: veau: 15 jf<strong>la</strong>con 100 mlR/MYOGASTER-E (VMD)vitamine E: 100 mg/mlsélénium sodique: 2 mg/mlsolution injectable imPosologie:prophy<strong>la</strong>ctique:veau, Su, Ov: 1 ml/10 kgcuratif:veau, Su, Ov: 1 ml/5 kgViande: 0 j, Lait: 0 jf<strong>la</strong>con 100 mlR/VITAMINE E + SELENIUM (VMD)alpha-tocophérol acétate: 17 mg/mlsélénium sodique: 1,67 mg/mlémulsion injectable imPosologie:Ru (veau, agneau): 0,2 - 0,25 ml/kgSu: 0,12 ml/kgViande: 14 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 100 mlR/5.6 Vitamines + minéraux + toniquesLes associations multiples devront toujours être administrées de manière raisonnée,tenant compte des besoins de l’animal et des apports journaliers des rationsalimentaires. Idéalement, une complémentation de <strong>la</strong> ration en vitamines et ou enminéraux devrait être ciblée et focalisée uniquement sur les éléments déficients.LMR butafosfan + cyano-coba<strong>la</strong>mine (vit B12): CATOSAL (Bayer)butafosfan: 100 mg/mlcyano-coba<strong>la</strong>mine: 50 mcg/mlsolution injectable iv, im, scPosologie:- affections aiguës:Bo: 5 - 25 ml (iv)veau: 5 - 12 ml (iv)Ca: 0,5 - 5 ml (iv, im, sc)Fe, animaux à fourrure:0,5 - 2,5 ml (iv, im, sc)à renouveler au besoin chaque j- affections chron:dédoubler les doses, à renouveler au besoinà intervalles de 1 - 2 semViande: 0 j, Lait: 0 jf<strong>la</strong>con 100 mlR/
6 MÉDICAMENTS AGISSANT SUR LE SYSTÈME LOCOMOTEUR 1376. MÉDICAMENTS AGISSANT SURLE SYSTÈME LOCOMOTEURCertains médicaments indiqués dans le traitement de troubles locomoteurs sontabordés dans d’autres chapitres:- Médicaments anti-infectieux, voir chapitre 1.1. Pour le traitement de l’arthriteinfectieuse ou de <strong>la</strong> polyarthrite en cas d’infection systémique, plusieurs antibiotiquespeuvent être utilisés, dont le choix reposera sur des tests de sensibilité<strong>du</strong> pathogène.- Glucocorticoïdes, voir chapitre 2.2. Plusieurs glucocorticoïdes ont été enregistréspour le traitement des affections <strong>du</strong> système locomoteur. Ces médicamentsont une efficacité prouvée dans les processus inf<strong>la</strong>mmatoires aigus;en cas d’usage prolongé, ils entravent cependant le rétablissement <strong>du</strong> tissucarti<strong>la</strong>gineux.- Analgésiques utilisés dans les troubles locomoteurs, voir chapitre 3.1.6.1 Acide hyaluroniqueIndicationsL’acide hyaluronique est indiqué pour le traitement symptomatique des affectionsaiguës non infectieuses tendineuses et ostéo-articu<strong>la</strong>ires. En cas de pathologiedégénérative, <strong>la</strong> voie intra-articu<strong>la</strong>ire est conseillée.PharmacodynamieL’acide hyaluronique est un composant <strong>du</strong> carti<strong>la</strong>ge, des tendons et de <strong>la</strong> synovie.Il joue un rôle important au niveau articu<strong>la</strong>ire aussi bien <strong>du</strong> point de vue mécanique,en assurant une viscosité adéquate des tissus et des liquides, que sur lep<strong>la</strong>n anti-inf<strong>la</strong>mmatoire en inhibant <strong>la</strong> migration leucocytaire et l’activation deslymphocytes. Le mécanisme d’action n’est pas c<strong>la</strong>irement identifié. Le but del’apport exogène d’acide hyaluronique est de compenser <strong>la</strong> perte et <strong>la</strong> dépolymérisationen mucopolysaccharides associées aux processus inf<strong>la</strong>mmatoiresostéo-articu<strong>la</strong>ires.PharmacocinétiqueAprès une injection intra-articu<strong>la</strong>ire, l’acide hyaluronique est transporté via lesvaisseaux lymphatiques et métabolisé au niveau <strong>du</strong> foie. La cinétique, en particulier<strong>la</strong> diffusion intra-articu<strong>la</strong>ire, associée à une injection intraveineuse est malconnue.Contre-indicationsL’infection articu<strong>la</strong>ire est une contre-indication.Effets indésirablesLa notice ne mentionne pas d’effets indésirables.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de l’acide hyaluronique n’a pas été établie chez les animaux gestantsou en <strong>la</strong>ctation. Etant donné <strong>la</strong> nature de cette substance, des effets négatifsrestent cependant improbables.LMR hyaluronate: HYONATE (Bayer)hyaluronate sodique: 10 mg/mlsolution injectable iartic, ivPosologie:Eq: 40 mg/animal (iv) (3 x avec 1 semd’intervalle),20 mg/articu<strong>la</strong>tion (iartic) (3 x avec 1 semd’intervalle)Viande: 0 jf<strong>la</strong>con 2 x 2 mlR/
1386 MÉDICAMENTS AGISSANT SUR LE SYSTÈME LOCOMOTEUR6.2 Polysulfate de pentosane sodiqueLe polysulfate de pentosane sodique (NaPPS) est un polysaccharide d’originevégétale (hémicellulose <strong>du</strong> bois de hêtre) et non animale.IndicationsLe médicament vétérinaire actuellement commercialisé est indiqué dans le traitementde l’ostéoarthrose non-infectieuse chez le chien.PharmacodynamieLe NaPPS a des propriétés anti-inf<strong>la</strong>mmatoires et anticoagu<strong>la</strong>ntes, et stimule <strong>la</strong>lipolyse et <strong>la</strong> fibrinolyse. Dans un modèle d’ostéoarthrite chez les chiens, l’administrationde NaPPS aux doses utilisées en thérapeutique a entraîné une ré<strong>du</strong>ction<strong>du</strong> taux de métalloprotéinases dans le carti<strong>la</strong>ge et une augmentation <strong>du</strong> taux del’inhibiteur tissu<strong>la</strong>ire de métalloprotéinase (TIMP), protégeant ainsi le contenu enprotéoglycane et <strong>la</strong> matrice <strong>du</strong> carti<strong>la</strong>ge de <strong>la</strong> dégradation. Chez les chiens souffrantd’ostéoarthrite, l’administration de NaPPS a provoqué une fibrinolyse, une lipolyseet une diminution de l’aggrégabilité p<strong>la</strong>quettaire. Dans les études in vitro et in vivocon<strong>du</strong>ites sur des espèces de <strong>la</strong>boratoire, avec des doses supérieures à celles utiliséesen thérapeutique, les NaPPS ont supprimé certains niveaux de médiateursanti-inf<strong>la</strong>mmatoires et stimulé <strong>la</strong> synthèse hyaluronique par les fibrob<strong>la</strong>stes.PharmacocinétiqueChez le chien, le pic de concentration p<strong>la</strong>smatique est atteint 15 minutes aprèsinjection par voie sc. Le NaPPS se lie aux protéines p<strong>la</strong>smatiques. Le NaPPS seconcentre dans le foie, les reins et le système réticulo-endothélial. On en retrouvede faibles concentrations dans le tissu conjonctif et les muscles. Une désulfatation<strong>du</strong> NaPPS se pro<strong>du</strong>it dans le système hépato-réticulo-endothélial, principalementdans le foie. Une dépolymérisation peut également se pro<strong>du</strong>ire dans lesreins. Quarante-huit heures après l’injection, environ 70 % de <strong>la</strong> dose administréeest éliminée dans l’urine.Contre-indicationsNe pas administrer aux chiens dont le squelette n’a pas atteint <strong>la</strong> maturité. Ne pasadministrer en période péri-opératoire. Ne pas administrer aux chiens souffrantde troubles sévères <strong>du</strong> foie ou des reins ou en cas d’infections déc<strong>la</strong>rées, detroubles sanguins, de troubles de <strong>la</strong> coagu<strong>la</strong>tion, de saignements ou de tumeursmalignes (notamment d’hémangiosarcome). Le traitement de l’arthrose septiqueest contre-indiqué.Effets indésirablesDes vomissements, de <strong>la</strong> diarrhée, une léthargie et une anorexie ont été signaléscomme réactions d’hypersensibilité au PPS. Des hémorragies internes graves,<strong>du</strong>es à une tumeur ou à une anomalie vascu<strong>la</strong>ire, pourraient apparaître. Destroubles de l’hémostase tels que des saignements de nez, des diarrhées hémorragiqueset des hématomes ont été signalés. Des réactions locales telles qu’ungonflement passager ont été observées suite à l’injection.InteractionsLes AINS potentialisent l’activité anticoagu<strong>la</strong>nte <strong>du</strong> NaPPS. Les corticostéroïdesont un effet inhibiteur sur certaines activités <strong>du</strong> NaPPS. L’utilisation concomitante<strong>du</strong> NaPPS et de stéroïdes, d’AINS, d’héparine, de warfarine ou d’autres anticoagu<strong>la</strong>ntsest déconseillée.Repro<strong>du</strong>ction et <strong>la</strong>ctationChez le <strong>la</strong>pin, des études de <strong>la</strong>boratoire ont révélé des effets embryotoxiques.L’innocuité <strong>du</strong> médicament chez <strong>la</strong> chienne en gestation n’ayant pas été étudiée,son utilisation n’est pas recommandée pendant <strong>la</strong> gestation.LMR polysulfate de pentosane sodique: ANARTHRON (Forte Healthcare)polysulfate de pentosane sodiquesolution injectable scPosologie:Ca: 3 mg/kg 4 x à 5 - 7 j d’intervallef<strong>la</strong>con 10 mlR/
6 MÉDICAMENTS AGISSANT SUR LE SYSTÈME LOCOMOTEUR 1396.3 Dibotermine alpha (rhBMP-2), protéineostéogéniqueIndicationsLa dibotermine alpha est une protéine ostéogénique utilisée sous forme d’imp<strong>la</strong>ntcomme adjuvant au traitement standard des fractures diaphysaires chez le chien.PharmacodynamieLa dibotermine alpha (protéine-2 ostéogénique humaine recombinante ourhBMP-2) est une copie de <strong>la</strong> protéine-2 ostéogénique (BMP-2) qui est pro<strong>du</strong>itenaturellement par le corps humain et contribue à <strong>la</strong> néoformation de tissu osseux.L’imp<strong>la</strong>ntation de l’éponge de col<strong>la</strong>gène à base de dibotermine alpha in<strong>du</strong>it <strong>la</strong> formationde tissu osseux au site d’imp<strong>la</strong>ntation ; l’éponge est entièrement résorbée.PharmacocinétiqueLa dibotermine alpha est libérée lentement au départ de l’éponge au niveau <strong>du</strong>site d’imp<strong>la</strong>ntation, puis rapidement éliminée après passage dans <strong>la</strong> circu<strong>la</strong>tionsanguine.Contre-indicationsNe pas utiliser chez les chiens présentant une immaturité <strong>du</strong> squelette, une infectionactive au site de fracture, une fracture pathologique ou une tumeur maligneactive quelconque. Ne pas utiliser chez les chiens allergiques à l’une ou plusieursdes substances contenues dans ce médicament.Effets indésirablesTrès fréquents: boitement, gonflement ferme dans les 3 premières semaines aprèsl’opération qui se résorbe gra<strong>du</strong>ellement, ou gonflement mou qui se résorbe dansles 3 semaines. Pour une description complète des effets indésirables, voir <strong>la</strong>notice.InteractionsAucune étude d’interaction n’a été menée.Précautions particulièresRéaliser <strong>la</strong> ré<strong>du</strong>ction définitive, <strong>la</strong> fixation et l’hémostase de <strong>la</strong> fracture avant d’imp<strong>la</strong>nterl’éponge.N’utiliser que <strong>la</strong> quantité d’éponge nécessaire au recouvrement des lignes de fractureet défauts osseux accessibles. Le pro<strong>du</strong>it n’assure pas <strong>la</strong> stabilité mécaniqueet ne doit pas être utilisé pour remplir un espace en présence de forces de compression.Après imp<strong>la</strong>ntation, recouvrir complètement les éponges par les tissusmous.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> médicament vétérinaire n’a pas été établie chez les chiens repro<strong>du</strong>cteurs,en gestation ou en <strong>la</strong>ctation. Chez ces groupes cibles, le médicament nedoit être utilisé qu’après évaluation <strong>du</strong> rapport bénéfice/risque par le vétérinaire.LMR dibotermine TRUSCIENT 0,66 mg kit pour imp<strong>la</strong>nt pour chiens(Pfizer)dibotermine alpha: 0,66 mgsolution pour imp<strong>la</strong>ntPosologie:Ca: max 2 éponges (2,5 x 5 cm)/animalf<strong>la</strong>con 10 ml de lyophilisat + 10 ml de solvantéponge2 x (2.5 x 5 cm)seringue2 x 3 ml et 1 x 6 mlR/
7 MÉDICAMENTS DU SYSTÈME RESPIRATOIRE 1417. MÉDICAMENTS DU SYSTÈME RESPIRATOIRE7.1 Bronchodi<strong>la</strong>tateurs7.1.1 Agonistes bêta-2-adrénergiques7.1.1.1 ClenbutérolIndicationsL’utilisation <strong>du</strong> clenbutérol pour le traitementdes ma<strong>la</strong>dies respiratoires à composantebronchospastique est permisechez le cheval, qu’il soit destiné ou non à<strong>la</strong> consommation alimentaire. Les allergiesrespiratoires figurent aussi parmi lesindications. Dans l’espèce bovine, l’utilisationde clenbutérol est uniquementautorisée comme substance tocolytique(voir chapitre 2.1.6). Le médecin vétérinairedoit rester attentif aux aspectslégaux re<strong>la</strong>tifs à <strong>la</strong> détention, <strong>la</strong> fournitureet l’administration des préparationscontenant <strong>du</strong> clenbutérol.PharmacodynamieL’effet bronchodi<strong>la</strong>tateur <strong>du</strong> clenbutérolrepose sur son action stimu<strong>la</strong>nte desrécepteurs bêta-2-adrénergiques desvoies aériennes. Le succès thérapeutiquedépend donc de <strong>la</strong> présence d’unbronchospasme et de récepteurs fonctionnels.Vu ses effets stimu<strong>la</strong>nts sur <strong>la</strong>pro<strong>du</strong>ction de mucus et son éliminationpar l’appareil mucociliaire, le clenbutérolest aussi indiqué pour traiter les obstructionsbronchiques causées par <strong>du</strong>mucus. De ce point de vue, il faut resterattentif au fait que, dans ce cas, l’objectifthérapeutique ne peut être atteintqu’à <strong>la</strong> condition que l’intégrité des cellulesciliées de l’épithélium bronchiquereste entière. Dans le cas contraire, lemucus pro<strong>du</strong>it risque de s’accumulerdans les voies aériennes et d’altérer leséchanges gazeux.PharmacocinétiqueElle dépend de <strong>la</strong> voie d’administrationutilisée. L’administration aérogèneainsi que les adaptations posologiquesparfois nécessaires pour obtenir uneréponse thérapeutique suffisante sontdes pratiques hors notice qui, à cetitre, engagent <strong>la</strong> responsabilité <strong>du</strong>médecin vétérinaire.Effets indésirablesDes effets hypotenseurs et tachycardisantspeuvent apparaître de même quedes tremblements et une sudation abondante.Les effets indésirables en casde surdosage étant liés à <strong>la</strong> stimu<strong>la</strong>tiondes récepteurs bêta-2 mais aussi bêta-1-adrénergiques, les bêta-bloquantssont envisageables comme antidote.InteractionsLes corticoïdes potentialisent les effets<strong>du</strong> clenbutérol, notamment l’hypotension.L’usage simultané de cet agonisteet d’anesthésiques locaux oude tout autre agent vasodi<strong>la</strong>tateur oucardiodépresseur peut aussi accroîtrele risque d’hypotension.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’administration doit être suspen<strong>du</strong>equelques jours avant <strong>la</strong> parturition vules effets tocolytiques de <strong>la</strong> molécule.Le clenbutérol peut aussi interféreravec l’action stimu<strong>la</strong>nte de l’oxytocineet des prostag<strong>la</strong>ndines F2 alpha.LMR clenbutérol: VENTIPULMIN gran (Boehringer Ingelheim)clenbutérol chlorhydrate: 0,16 mg/10 ggranules po avec l’alimentationPosologie:Eq: 2 x pj 0,8 mcg/kg (10 - 15 j, en casd’infect chron: min 4 sem)Ne pas administrer chez des Eq destinés à <strong>la</strong>consommation humaine ou chez des Eq dont le<strong>la</strong>it est destiné à <strong>la</strong> consommation humainegran 500 gR/VENTIPULMIN sirop (Boehringer Ingelheim)clenbutérol chlorhydrate: 0,1 ml/4 mlsirop po (pur ou avec l’alimentation)Posologie:Eq: 2 x pj 0,8 mcg/kg (11 j, en cas d’infectchron: min 4 sem)Viande: 28 j (établi pour le traitement de 11 j)Ne pas administrer chez des Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con avec pompe doseuse 355 mlR/VENTIPULMIN sol inj (Boehringer Ingelheim)clenbutérol chlorhydrate: 0,03 mg/mlsolution injectable ivPosologie:Eq: 2 x pj 0,8 mcg/kg (11 j, en cas d’infectchron: min 4 sem)Viande: 28 j (établi pour le traitement de 11 j)Ne pas administrer chez des Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 50 mlR/
1427 MÉDICAMENTS DU SYSTÈME RESPIRATOIRE7.2 AntihistaminiquesSeuls les antagonistes H1 sont abordés dans ce chapitre. Aucun antagonistedes récepteurs H2 des cellules de <strong>la</strong> muqueuse gastrique contrô<strong>la</strong>nt <strong>la</strong> sécrétiond’acide chlorhydrique n’est enregistré malgré l’intérêt de ces substances chez lechien (cimétidine, par exemple).IndicationsLes antihistaminiques antagonistes des récepteurs histaminergiques, ayant unespécificité pour les récepteurs H1 distribués notamment sur les fibres muscu<strong>la</strong>ireslisses des vaisseaux sanguins, les bronches et le tractus gastro-intestinal,sont indiqués dans les réactions allergiques (démangeaisons, œdème, bronchospasme)et dans <strong>la</strong> prévention <strong>du</strong> mal de voyage. Cependant, lors de crise anaphy<strong>la</strong>ctiqueinstallée, ils sont d’un intérêt secondaire par rapport à l’adrénaline etaux corticostéroïdes. Le médicament disponible sur le marché belge est un siroppour le traitement symptomatique des troubles respiratoires chez le chien et lechat dont l’antagoniste H1 (maléate de chlorphénamine) est associé à un dérivéde <strong>la</strong> morphine (dépresseur <strong>du</strong> centre de <strong>la</strong> toux), un expectorant et de l’éphédrine(bronchodi<strong>la</strong>tateur).PharmacodynamieLes antagonistes H1 entrent en compétition avec l’histamine pour les récepteursà l’histamine au niveau des cellules effectrices. La libération de l’histaminen’est pas influencée. Ils ont également des effets antisérotoninergiques etanticholinergiques.PharmacocinétiqueLes antihistaminiques H1 peuvent être administrés par voie orale ou parentérale.Par voie entérale, ils sont généralement bien résorbés chez les monogastriques.Ceci n’est pas toujours le cas chez les ruminants.Contre-indicationsLeur utilisation est contre-indiquée en cas d’hypertrophie de <strong>la</strong> prostate, d’obstructions<strong>du</strong> col vésical, d’insuffisance cardiaque grave, de g<strong>la</strong>ucome à anglefermé et d’obstructions gastro-intestinales.Effets indésirablesLeurs effets indésirables sont plus ou moins prononcés suivant l’indivi<strong>du</strong> (âge,sexe, race, espèce,…) et suivant le type, <strong>la</strong> dose et <strong>la</strong> forme galénique <strong>du</strong> principeactif. A dose thérapeutique, ils in<strong>du</strong>isent de <strong>la</strong> sédation; à forte dose, ilsprovoquent de l’excitation et des convulsions. Dans certains cas, des réactionsallergiques paradoxales ont été observées ainsi que des effets tératogènes.InteractionsL’effet dépresseur sur le système nerveux central de molécules, telles que lesbarbituriques ou les tranquillisants, peut être renforcé par une administration combinéeavec les antihistaminiques. Un renforcement de l’activité des substancesanticholinergiques ainsi qu’une inhibition des effets vasoconstricteurs de l’éphédrinesont possibles.Repro<strong>du</strong>ction et <strong>la</strong>ctationEtant donné le manque de données spécifiques sur l’utilisation chez des animauxen gestation, il est conseillé de ne pas administrer le pro<strong>du</strong>it pendant <strong>la</strong> gestationou l’al<strong>la</strong>itement.LMR guaïfénésine + éphédrine + dextrométhorphane ATUSSIN (Vétoquinol)guaïfénésine: 9 mg/mléphédrine chlorhydrate: 5 mg/mlchlorphénamine maléate: 0,71 mg/mldextrométhorphane bromhydrate: 5 mg/mlsirop poPosologie:Ca: 2 - 3 x pj 1 - 3 ml (1 ml = 30 gtts)(3 sem max)Fe: 2 - 3 x pj 1 ml (3 sem max)<strong>la</strong> dose peut éventuellement être doubléef<strong>la</strong>con 60 mlR/
8 MÉDICAMENTS CARDIO-VASCULAIRES 1438. MÉDICAMENTS CARDIO-VASCULAIRES8.1 Médicaments utilisés dans l’insuffisancecardiaqueOn notera que toutes les c<strong>la</strong>sses thérapeutiques ne sont pas abordées ici enraison de l’absence de médicaments à usage vétérinaire correspondants enregistrésen Belgique. Citons, à titre d’exemple, les glycosides cardiotoniques, lesdérivés nitrés, les sympathicomimétiques. Le lecteur peut consulter le RépertoireCommenté des Médicaments (à usage humain) et <strong>la</strong> littérature vétérinaire pourobtenir des informations à ce sujet. (Voir aussi les Folia Veterinaria 2002 n° 3, 2006n° 2 et 2009 n°3).8.1.1 Inhibiteurs de l’Enzyme de Con<strong>version</strong> de l’Angiotensine (IECA)IndicationsLes IECA sont indiqués chez le chien dans le cas d’une insuffisance cardiaquesymptomatique débutante (grade II selon <strong>la</strong> c<strong>la</strong>ssification NYHA), modérée (gradeIII) ou sévère (grade IV), le plus fréquemment suite à une insuffisance valvu<strong>la</strong>ire(mitrale ou tricuspide) ou une cardiomyopathie di<strong>la</strong>tée. Les IECA en médecine vétérinaireet disponibles sur le marché, à savoir le bénazépril, l’éna<strong>la</strong>pril, l’imidaprilet le ramipril ont une efficacité équivalente, considérant le degré d’inhibition del’enzyme. Certains médicaments à base de bénazépril sont indiqués chez le chatpour ralentir l’insuffisance rénale chronique par ré<strong>du</strong>ction de <strong>la</strong> pression artérielle.PharmacodynamieLes IECA inhibent l’enzyme de con<strong>version</strong> responsable de <strong>la</strong> transformation del’angiotensine I en angiotensine II qui est <strong>la</strong> seule forme active. L’enzyme decon<strong>version</strong> intervient également dans <strong>la</strong> dégradation de <strong>la</strong> bradykinine. Du faitdes effets vasoconstricteurs de l’angiotensine II, les IECA in<strong>du</strong>isent un effet vasodi<strong>la</strong>tateurartériel et veineux. Les IECA inhibent également <strong>la</strong> rétention d’eau et <strong>la</strong>vasoconstriction in<strong>du</strong>ites par <strong>la</strong> vasopressine ainsi que <strong>la</strong> rétention d’eau et desodium et l’élimination de potassium contrôlées par l’aldostérone, deux hormonesstimulées par l’angiotensine II. Ces effets hypotenseurs se font aux dépens d’uneactivation de <strong>la</strong> rénine et d’une accumu<strong>la</strong>tion p<strong>la</strong>smatique de l’angiotensine I.PharmacocinétiqueLes IECA sont des prodrogues qui sont transformées en métabolites actifs auniveau hépatique. La ba<strong>la</strong>nce entre les voies d’élimination biliaire et urinaire diffèred’une molécule à l’autre.Contre-indicationsNe pas utiliser en cas d’hypersensibilité aux IECA.Effets indésirablesLes IECA sont généralement bien tolérés et possèdent une grande marge de sécurité.Les effets indésirables décrits sont: apathie, ataxie, incoordination, anorexie,vomissements et diarrhée. Ceux-ci sont généralement des signes d’hypotensionet/ou d’azotémie. Toutes les substances vasodi<strong>la</strong>tatrices, comme les IECA, ouqui ré<strong>du</strong>isent le volume sanguin, comme les diurétiques, peuvent in<strong>du</strong>ire une azotémiepré-rénale. L’azotémie pré-rénale est <strong>la</strong> conséquence d’une diminution <strong>du</strong>taux de filtration gloméru<strong>la</strong>ire suite à l’hypotension rénale.InteractionsLes IECA peuvent être associés aux autres traitements conventionnels de l’insuffisancecardiaque. L’administration concomitante de diurétiques ou d’autres vasodi<strong>la</strong>tateursaccroît les risques d’hypotension. L’administration de potassium ou dediurétiques d’épargne potassique peut in<strong>du</strong>ire une hyperkaliémie.Précautions particulières/Risques pour l’hommeLa fonction rénale doit être surveillée avant le début <strong>du</strong> traitement et 2 à 7 joursaprès <strong>la</strong> mise en route <strong>du</strong> traitement. Chez les chats atteints d’insuffisance rénalechronique, les IECA peuvent augmenter <strong>la</strong> créatininémie en début de traitement,suite à leur effet thérapeutique hypotenseur. En l’absence d’autres symptômes, il
1448 MÉDICAMENTS CARDIO-VASCULAIRESn’y a pas lieu d’arrêter le traitement. Comme il est d’usage en cas d’insuffisancerénale chronique, il est recommandé de surveiller <strong>la</strong> créatinine p<strong>la</strong>smatique pendantle traitement.Si des symptômes d’hypotension et/ou d’azotémie se manifestent, <strong>la</strong> dose dediurétique et/ou d’IECA doit être ré<strong>du</strong>ite. Les IECA seront utilisés avec prudencechez les animaux montrant une insuffisance rénale, une hypovolémie et/ou unehyponatrémie.Chez <strong>la</strong> femme, les IECA sont contre-indiqués pendant toute <strong>la</strong> période de <strong>la</strong>grossesse, c’est pourquoi les femmes enceintes doivent prendre les précautionsnécessaires pour éviter toute exposition orale accidentelle. Il convient de se <strong>la</strong>verles mains après utilisation. En cas d’ingestion accidentelle par des enfants, onconsultera immédiatement un médecin en lui montrant l’étiquette ou <strong>la</strong> notice.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes IECA peuvent passer <strong>la</strong> barrière p<strong>la</strong>centaire. Ils ne doivent donc pas êtreadministrés <strong>du</strong>rant <strong>la</strong> gestation. Même si, en revanche, le passage dans le <strong>la</strong>itmaternel est re<strong>la</strong>tivement faible, les IECA seront administrés avec prudence chezles chiennes al<strong>la</strong>itantes.8.1.1.1 BénazéprilLMR bénazépril : BANACEP VET 5 mg (Lab Calier)bénazépril (chlorhydrate): 4,6 mgcomprimé poPosologie:Ca (PV > 5 kg):1 x 0,23 mg de bénazépril/kg pjdoubler éventuellement <strong>la</strong> dose quotidienneunique si cliniquement nécessaireFe: 1 x 0,46 mg/kg pjcompr 14, 140R/BENAKOR F 5 mg (Le Vet)bénazépril chlorhydrate: 5 mgcomprimé poPosologie:Ca: 0,25 mg/kg pjdose peut être doubléecompr 28, 98R/BENAKOR F 20 mg (LeVet)bénazépril chlorhydrate: 20 mgcomprimé poPosologie:Ca: 0,25 mg/kg pjdose peut être doubléecompr 28, 98R/BENAZECARE FLAVOUR 5 mg (Animalcare)chlorhydrate de bénazépril: 5 mg/comprcomprimé poPosologie:Ca: 1 x 0,25 mg/kg pj (dose peut êtredoublée)Fe: 1 x 0,5 mg/kg pjcompr 140R/BENAZECARE FLAVOUR 20 mg (Animalcare)chlorhydrate de bénazépril: 20 mg/comprcomprimé poPosologie:Ca: 1 x 0,25 mg/kg (dose peut être doublée)compr 140R/BENEFORTIN FLAVOUR 2,5 mg (LavetPharmaceuticals)bénazépril chlorhydrate: 2,5 mgcomprimé poPosologie:Ca: 0,25 mg/kg pj (avec ou sans nourriture)(dose peut être doublée)Fe: 0,50 mg/kg pj (avec ou sans nourriture)compr 2 x 14R/BENEFORTIN FLAVOUR 5 mg (LavetPharmaceuticals)bénazépril chlorhydrate: 5 mgcomprimé poPosologie:Ca: 0,25 mg/kg pj (avec ou sans nourriture)(dose peut être doublée)compr 2 x 14, 10 x 14R/BENEFORTIN FLAVOUR 20 mg (LavetPharmaceuticals)bénazépril chlorhydrate: 20 mgcomprimé poPosologie:Ca: 0,25 mg/kg pj (avec ou sans nourriture)(dose peut être doublée)compr 4 x 7R/BEXEPRIL 5 mg (Chanelle Pharmaceuticals)bénazépril chlorhydrate: 5 mgcomprimé poPosologie:Ca (PV > 10 kg): 0,25 mg/kg pj (<strong>la</strong> dose peutêtre doublée)compr 2 x 14R/BEXEPRIL 20 mg (Chanelle Pharmaceuticals)bénazépril chlorhydrate: 20 mgcomprimé poPosologie:Ca (PV > 40 kg): 0,25 mg/kg pj (<strong>la</strong> dose peutêtre doublée)compr 2 x 14R/
8 MÉDICAMENTS CARDIO-VASCULAIRES 145FORTEKOR 2,5 (Novartis)bénazépril chlorhydrate: 2,5 mgcomprimé poPosologie:Ca: 0,25 mg/kg pjFe: 0,5 – 1,0 mg/kg pjcompr 2 x 14R/FORTEKOR FLAVOUR 5 (Novartis)bénazépril chlorhydrate: 5 mgcomprimé poPosologie:Ca: 0,25 – 0,5 mg/kg pj (dose peut êtredoublée)compr 2 x 14, 4 x 14R/FORTEKOR FLAVOUR 20 (Novartis)bénazépril chlorhydrate: 20 mgcomprimé poPosologie:Ca: 0,25 – 0,5 mg/kg pj (dose peut êtredoublée)compr 2 x 14R/NELIO 2,5 mg compr chat (Sogeval Lab)bénazépril chlorhydrate: 2,5 mg/comprcomprimé poPosologie:Fe (> 2.5 kg): 1 x 0,5 mg/kg pjcompr 20, 100R/NELIO 5 mg, 20 mg compr chien (Sogeval Lab)bénazépril chlorhydrate: 5 mg ou 20 mgcomprimé poPosologie:Ca (> 2.5 kg): 1 x 0,25 mg/kg pjdose peut être doublée si l‘état clinique lejustifiecompr 10, 100R/PRILBEN VET 5 mg compr pelliculé chien/chat(Chemo Iberica)bénazépril (chlorhydrate): 4,6 mgcomprimé pelliculé po (éventuellement avecl’alimentation)Posologie:Ca (PV > 5 kg): 0,23 mg/kg 1 x pjFe (PV > 2,5 kg): 0,46 mg/kg 1 x pjcompr 1 of 10 x 14R/PRILBEN VET 20 mg compr pelliculé chien (ChemoIberica)bénazépril (chlorhydrate): 18,42 mgcomprimé pelliculé po (éventuellement avecl’alimentation)Posologie:Ca (PV > 20 kg): 0,23 mg/kg 1 x pj (<strong>la</strong> dosepeut être doublée)compr 14R/8.1.1.2 Ena<strong>la</strong>prilLMR éna<strong>la</strong>pril: ENACARD 1 mg (Merial)éna<strong>la</strong>pril maléate: 1 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (éventuellement 2 x pj)compr 4 x 7R/ENACARD 2,5 mg (Merial)éna<strong>la</strong>pril maléate: 2,5 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (éventuellement 2 x pj)compr 4 x 7R/ENACARD 5 mg (Merial)éna<strong>la</strong>pril maléate: 5 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (éventuellement 2 x pj)compr 4 x 7R/ENACARD 10 mg (Merial)éna<strong>la</strong>pril maléate: 10 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (éventuellement 2 x pj)compr 4 x 7R/ENACARD 20 mg (Merial)éna<strong>la</strong>pril maléate: 20 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (éventuellement 2 x pj)compr 4 x 7R/PRILENAL 2,5 mg (Ceva Santé Animale)éna<strong>la</strong>pril (maléate): 1,911 mgcomprimé poPosologie:Ca: 0,38 mg/kg pjAdapter dose en fonction de <strong>la</strong> réponsecliniqueSi pas de réponse clinique dans les 2 semaprès début de <strong>la</strong> thérapie, <strong>la</strong> dose peut êtreadministrée 2 x pjcompr 4 x 7R/PRILENAL 5 mg (Ceva Santé Animale)éna<strong>la</strong>pril (maléate): 3,822 mgcomprimé poPosologie:Ca: 0,38 mg/kg pjAdapter dose en fonction de <strong>la</strong> réponsecliniqueSi pas de réponse clinique dans les 2 semaprès début de <strong>la</strong> thérapie, <strong>la</strong> dose peut êtreadministrée 2 x pjcompr 4 x 7R/
1468 MÉDICAMENTS CARDIO-VASCULAIRESPRILENAL 10 mg (Ceva Santé Animale)éna<strong>la</strong>pril (maléate): 7,645 mgcomprimé poPosologie:Ca: 0,38 mg/kg pjAdapter dose en fonction de <strong>la</strong> réponsecliniqueSi pas de réponse clinique dans les 2 semaprès début de <strong>la</strong> thérapie, <strong>la</strong> dose peut êtreadministrée 2 x pjcompr 4 x 7R/PRILENAL 20 mg (Ceva Santé Animale)éna<strong>la</strong>pril (maléate): 15,289 mgcomprimé poPosologie:Ca: 0,38 mg/kg pjAdapter dose en fonction de <strong>la</strong> réponsecliniqueSi pas de réponse clinique dans les 2 semaprès début de <strong>la</strong> thérapie, <strong>la</strong> dose peut êtreadministrée 2 x pjcompr 4 x 7R/8.1.1.3 ImidaprilLMR imidapril: PRILIUM 75 mg (Vétoquinol)imidapril chlorhydrate: 75 mgpoudre pour solution poPosologie:Ca (PV > 2 kg): 0,25 mg/kg pjf<strong>la</strong>con 30 ml (0,805 g de poudre) et applic (2 ml)R/PRILIUM 150 mg (Vétoquinol)imidapril chlorhydrate: 150 mgpoudre pour solution poPosologie:Ca (PV > 4 kg): 0,25 mg/kg pjf<strong>la</strong>con 30 ml (0,880 g de poudre) et applic (2 ml)R/PRILIUM 300 mg (Vétoquinol)imidapril chlorhydrate: 300 mgpoudre pour solution poPosologie:Ca (PV > 8 kg): 0,25 mg/kg pjf<strong>la</strong>con 30 ml (1,030 g de poudre) et applic (2 ml)R/8.1.1.4 RamiprilLMR ramipril: VASOTOP P 0,625 mg (MSD A.H.)ramipril: 0,625 mgcomprimé poPosologie:Ca: 0,125 mg/kg pjcompr 1 x 28R/VASOTOP P 1,25 mg (MSD A.H.)ramipril: 1,25 mgcomprimé poPosologie:Ca: 0,125 mg/kg pjcompr 1 x 28, 3 x 28R/VASOTOP P 2,5 mg (MSD A.H.)ramipril: 2,5 mgcomprimé poPosologie:Ca: 0,125 mg/kg pjcompr 1 x 28, 3 x 28R/VASOTOP P 5 mg (MSD A.H.)ramipril: 5 mgcomprimé poPosologie:Ca: 0,125 mg/kg pjcompr 1 x 28, 3 x 28R/8.1.2 Antagoniste de l’aldostérone8.1.2.1 Spirono<strong>la</strong>ctoneIndicationsA utiliser en association avec une thérapiec<strong>la</strong>ssique, incluant éventuellementun traitement diurétique, pour letraitement de l’insuffisance cardiaquecongestive <strong>du</strong>e à une valvulopathie,chez les chiens.PharmacodynamieLa spirono<strong>la</strong>ctone et ses métabolitesactifs sont des antagonistes spécifiquesde l’aldostérone, qui se fixentde manière compétitive aux récepteursminéralocorticoïdes situés dansles reins, le coeur et les vaisseaux sanguins.Dans les reins, <strong>la</strong> spirono<strong>la</strong>ctoneinhibe <strong>la</strong> rétention de sodium in<strong>du</strong>itepar l’aldostérone, entraînant ainsi uneaugmentation de l’excrétion <strong>du</strong> sodiumet par conséquent de l’eau. Laspirono<strong>la</strong>ctone est hyperkaliémiante.Par rapport aux diurétiques hypokaliémiantscomme les diurétiques del’anse et les thiazides, le pouvoir diurétiquede <strong>la</strong> spironoloactone est faible.Ces effets rénaux con<strong>du</strong>isent à unediminution <strong>du</strong> volume extracellu<strong>la</strong>ire etpar conséquent à une diminution de <strong>la</strong>précharge cardiaque et de <strong>la</strong> pressionde l’oreillette gauche. Il en résulte uneamélioration de <strong>la</strong> fonction cardiaque.Dans le système cardio-vascu<strong>la</strong>ire,<strong>la</strong> spirono<strong>la</strong>ctone prévient les effetsnéfastes de l’aldostérone. Bien queson mécanisme d’action précis ne soitpas c<strong>la</strong>irement défini, l’aldostéronefavorise <strong>la</strong> fibrose myocardique, leremode<strong>la</strong>ge myocardique et vascu<strong>la</strong>ireet un dysfonctionnement endothélial.Des modèles expérimentaux sur deschiens ont montré qu’une thérapie à
8 MÉDICAMENTS CARDIO-VASCULAIRES 147long terme avec un antagoniste de l’aldostéroneprévient le dysfonctionnementprogressif <strong>du</strong> ventricule gaucheet atténue son remode<strong>la</strong>ge chez leschiens présentant une insuffisancecardiaque chronique. Les résultats desétudes cliniques sur <strong>la</strong> spirono<strong>la</strong>ctonene sont pas univoques, mais on pourraiten conclure de manière généraleque l’association de <strong>la</strong> spirono<strong>la</strong>ctoneaux traitements c<strong>la</strong>ssiquement utiliséspeut avoir un effet positif sur <strong>la</strong> morbidité<strong>du</strong>e à l’insuffisance cardiaque liéeà une valvulopathie. La spirono<strong>la</strong>ctonepeut prévenir les effets de « l’aldosteron-escape» lorsqu’elle est utilisée enassociation aux IECA.PharmacocinétiqueLa prise simultanée d’aliments augmenteconsidérablement <strong>la</strong> biodisponibilitéde <strong>la</strong> spirono<strong>la</strong>ctone. Après uneadministration orale de 2 à 4 mg/kg,l’absorption augmente linéairementavec <strong>la</strong> quantité administrée. La distributionse fait principalement vers letractus gastro-intestinal, les reins, lefoie et les g<strong>la</strong>ndes surrénales. La spirono<strong>la</strong>ctoneest rapidement et complètementmétabolisée par le foie en7-thiométhylespirono<strong>la</strong>ctone et encanrénone, les principaux métabolitesactifs chez le chien. Les Cmax sontatteintes après respectivement 2 et 4heures pour les métabolites primaires,<strong>la</strong> 7-thiométhylespirono<strong>la</strong>ctone et<strong>la</strong> canrénone. Un état d’équilibre estatteint au bout de 2 jours. La spirono<strong>la</strong>ctoneest principalement excrétéesous forme de métabolites. Chez lechien, 70% de <strong>la</strong> dose administrée estretrouvée dans les fèces et 20 % dansl’urine.Contre-indicationsL’utilisation chez des animaux repro<strong>du</strong>cteurs,chez les chiens souffrantd’hypoadrénocorticisme,d’hyperkaliémie ou d’hyponatrémieest contre-indiquée. Ne pas associer<strong>la</strong> spirono<strong>la</strong>ctone aux AINS chez leschiens insuffisants rénaux.Effets secondairesUne atrophie prostatique réversible estsouvent observée chez les mâles noncastrés.InteractionsAucune interaction n’a été constatée<strong>du</strong>rant les études cliniques entre<strong>la</strong> spiro<strong>la</strong>ctone et le furosémide oule pimobendane. La spirono<strong>la</strong>ctoneré<strong>du</strong>it l’élimination de <strong>la</strong> digoxine,augmentant ainsi <strong>la</strong> digoxinémie.L’administration de désoxycorticostéroneou d’AINS avec de <strong>la</strong> spirono<strong>la</strong>ctonepeut con<strong>du</strong>ire à une ré<strong>du</strong>ctionde l’excrétion urinaire <strong>du</strong> sodium. Leschiens traités à <strong>la</strong> fois par de <strong>la</strong> spirono<strong>la</strong>ctoneet un AINS doivent être correctementhydratés. Une surveil<strong>la</strong>ncede leur fonction rénale et <strong>du</strong> taux depotassium p<strong>la</strong>smatique est recommandéeavant l’initiation et pendantle traitement avec <strong>la</strong> thérapie combinée.L’administration concomitantede <strong>la</strong> spirono<strong>la</strong>ctone avec un IECAet d’autres médicaments d’épargne<strong>du</strong> potassium (tels que les bêta-bloquants,les bloqueurs des canauxcalciques, etc…) peut éventuellementcon<strong>du</strong>ire à une hyperkaliémie. La spirono<strong>la</strong>ctonepouvant provoquer à <strong>la</strong>fois une in<strong>du</strong>ction et une inhibitiondes enzymes <strong>du</strong> cytochrome P450,elle peut affecter le métabolisme desautres médicaments métabolisés parces enzymes.Précautions particulières/Risquespour l’hommeLa fonction rénale et le taux de potassiumsérique doivent être évalués avantle début d’un traitement associant <strong>la</strong>spirono<strong>la</strong>ctone à un IECA. Chez leschiens souffrant d’insuffisance rénale,il est recommandé d’effectuer un suivirégulier de <strong>la</strong> fonction rénale et <strong>du</strong> tauxde potassium sérique car il peut y avoirune augmentation <strong>du</strong> risque d’hyperkaliémie.La spirono<strong>la</strong>ctone ayant uneffet anti-androgène, il est recommandéde ne pas utiliser le pro<strong>du</strong>it chez leschiens en croissance. La spirono<strong>la</strong>ctonedoit être utilisée avec précautionchez les chiens présentant un dysfonctionnementhépatique. Le pro<strong>du</strong>itpeut provoquer une sensibilisation de<strong>la</strong> peau chez les personnes sensibles.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser chez les animaux engestation ou en <strong>la</strong>ctation ni chez lesanimaux de repro<strong>du</strong>ction, vu les résultatsobtenus chez les espèces de<strong>la</strong>boratoire (foetotoxicité).LMR spirono<strong>la</strong>ctone: PRILACTONE 10 mg (Ceva Santé Animale)spirono<strong>la</strong>ctone: 10 mgcomprimé po avec l‘alimentationPosologie:Ca: 1 x 2 mg/kg pjcompr 3 x 10R/
1488 MÉDICAMENTS CARDIO-VASCULAIRESPRILACTONE 40 mg (Ceva Santé Animale)spirono<strong>la</strong>ctone: 40 mgcomprimé po avec l‘alimentationPosologie:Ca: 1 x 2 mg/kg pjcompr 3 x 10R/PRILACTONE 80 mg (Ceva Santé Animale)spirono<strong>la</strong>ctone: 40 mgcomprimé po avec l‘alimentationPosologie:Ca: 1 x 2 mg/kg pjcompr 3 x 10R/8.1.3 Association d’un IECA et d’un antagoniste de l’aldostérone8.1.3.1 Bénazépril + spirono<strong>la</strong>ctoneLe bénazépril et <strong>la</strong> spiron<strong>la</strong>ctoneagissent à différents niveaux sur lesystème rénine-angiotensine-aldostérone.Voir commentaires 8.1.1.pour le bénazépril et 8.1.2.1. pour <strong>la</strong>spirono<strong>la</strong>ctone.LMR bénazépril + spirono<strong>la</strong>ctone CARDALIS 2,5 mg/20 mg compr chien (CevaSanté Animale)chlorhydrate de bénazépril: 2,5 mgspirono<strong>la</strong>ctone: 20 mgcomprimé po avec l’alimentationPosologie:Ca: 1 x pj 0,25 mg de bénaz HCl/kg + 2 mgde spir/kgcompr 30R/CARDALIS 5 mg/40 mg compr chien (Ceva SantéAnimale)chlorhydrate de bénazépril: 5 mgspirono<strong>la</strong>ctone: 40 mgcomprimé po avec l’alimentationPosologie:Ca: 1 x pj 0,25 mg de bénaz HCl/kg + 2 mgde spir/kgcompr 30R/CARDALIS 10 mg/80 mg compr chien (CevaSanté Animale)chlorhydrate de bénazépril: 10 mgspirono<strong>la</strong>ctone: 80 mgcomprimé po avec l’alimentationPosologie:Ca: 1 x pj 0,25 mg de bénaz HCl/kg + 2 mgde spir/kgcompr 30R/8.1.4 Inodi<strong>la</strong>tateurs8.1.4.1 PimobendaneIndicationsLe pimobendane est indiqué dans letraitement de l’insuffisance cardiaquesuite à une cardiomyopathie ou àune insuffisance valvu<strong>la</strong>ire, mitrale ettricuspide.PharmacodynamieLe pimobendane est qualifié d’inodi<strong>la</strong>tateuren raison de ses propriétéstonicardiaques et vasodi<strong>la</strong>tatrices.Le pimobendane augmente <strong>la</strong> sensibilitéde <strong>la</strong> troponine pour le calciumintracellu<strong>la</strong>ire dans le myocarde cequi a pour effet d’amplifier <strong>la</strong> contractioncellu<strong>la</strong>ire pour une concentrationcalcique intracellu<strong>la</strong>ire donnée.L’inhibition des phosphodiestérases(PDE III) contribue aussi à son effetinotrope positif. Cet effet n’imposepas d’augmentation de <strong>la</strong> demandeen énergie et en oxygène. Le pimobendaneinhibe <strong>la</strong> phosphodiestérasedans les cellules muscu<strong>la</strong>ires lissesartérielles et veineuses con<strong>du</strong>isant àune augmentation en AMPc intracellu<strong>la</strong>ireresponsable de l’effet vasodi<strong>la</strong>tateur.La combinaison de <strong>la</strong> ré<strong>du</strong>ctionde <strong>la</strong> précharge et de <strong>la</strong> postchargecardiaque et de l’augmentation de <strong>la</strong>contractilité <strong>du</strong> myocarde in<strong>du</strong>isentdes effets hémodynamiques favorablesexploités pour le traitement del’insuffisance cardiaque.PharmacocinétiqueLes effets inotropes positifs <strong>du</strong> pimobendanesont observés pendant 8 à12 heures après l’administration orale.Après une administration orale, <strong>la</strong> biodisponibilité<strong>du</strong> pimobendane est de60 à 63 %. Cette biodisponibilité estconsidérablement ré<strong>du</strong>ite lorsque leprincipe actif est administré pendantou peu de temps après le repas. Laliaison aux protéines p<strong>la</strong>smatiquesest en moyenne de 93 %. La demi-vied’élimination p<strong>la</strong>smatique est d’environ0,4 heure. Le métabolite actifprincipal est éliminé dans le p<strong>la</strong>smaavec une demi-vie d’environ 2 heures.L’élimination se réalise presque exclusivementpar les selles.Contre-indicationsLe pimobendane est contre-indiquéchez les chiens atteints de cardiomyopathiehypertrophique ou dans dessituations cliniques où l’augmentation<strong>du</strong> volume d’éjection systolique ne
8 MÉDICAMENTS CARDIO-VASCULAIRES 149peut avoir lieu pour des raisons fonctionnelleset anatomiques comme <strong>la</strong>sténose aortique par exemple.Effets indésirablesLe pimobendane est généralementbien toléré. Dans de rares cas, un effetchronotrope positif modéré et desvomissements peuvent cependant sepro<strong>du</strong>ire. Ces effets indésirables sontdépendants de <strong>la</strong> dose et peuventêtre évités par une ré<strong>du</strong>ction de <strong>la</strong>posologie.InteractionsLe pimobendane peut être utilisé chezle chien simultanément à d’autrestraitements conventionnels de l’insuffisancecardiaque. L’effet inotrope positif<strong>du</strong> pimobendane est diminué parle vérapamil et le propranolol.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe pimobendane n’est pas recommandéchez les chiennes gestantes oual<strong>la</strong>itantes et ne sera utilisé que si lesavantages thérapeutiques contreba<strong>la</strong>ncentles risques potentiels.LMR pimobendane: CARDISURE APPETENT 1,25 mg (Eurovet A.H.)pimobendane: 1,25 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (en 2 demi-dosages)adapter <strong>la</strong> dose selon l‘effet cliniquecompr 10 x 10R/CARDISURE APPETENT 2,5 mg (Eurovet A.H.)pimobendane: 2,5 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (en 2 demi-dosages)adapter <strong>la</strong> dose selon l‘effet cliniquecompr 10 x 10R/CARDISURE APPETENT 5 mg (Eurovet A.H.)pimobendane: 5 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (en 2 demi-dosages)adapter <strong>la</strong> dose selon l‘effet cliniquecompr 10 x 10R/CARDISURE APPETENT 10 mg (Eurovet A.H.)pimobendane: 10 mgcomprimé poPosologie:Ca: 0,5 mg/kg pj (en 2 demi-dosages)adapter <strong>la</strong> dose selon l‘effet cliniquecompr 10 x 10R/VETMEDIN 1,25 mg (Boehringer Ingelheim)pimobendane: 1,25 mgcomprimé appétent poPosologie:Ca: 2 x 0,25 mg/kg pj 1 h avant l‘alimentation,à 12 h d‘intervallecompr 50, 100R/VETMEDIN 5 mg compr appétents chien(Boehringer Ingelheim)pimobendane: 5 mgcomprimé appétent poPosologie:Ca: 2 x 0,25 mg/kg pj 1 h avant l‘alimentation,à 12 h d‘intervallecompr 50R/VETMEDIN 5 mg gélules (Boehringer Ingelheim)pimobendane: 5 mgcapsule poPosologie:Ca: 2 x 0,25 mg/kg pj 1 h avant l‘alimentation,à 12 h d‘intervallecaps 100R/8.2 Vasodi<strong>la</strong>tateurs périphériques et cérébrauxLes mécanismes d’action des vasodi<strong>la</strong>tateurs sont multiples, ils peuvent êtreutilisés pour des indications très variables. Certains, comme les inhibiteurs del’enzyme de con<strong>version</strong> de l’angiotensine et de phosphodiestérases ont été développésspécialement pour le traitement symptomatique de certaines insuffisancescardiaques (voir chapitre précédent). D’autres sont indiqués dans des pathologiesqui ne sont pas de type cardiaque; ils sont repris dans ce chapitre.8.2.1 Inhibiteurs de phosphodiestérases8.2.1.1 PropentofyllineIndicationsLa propentofylline est indiquée dansles troubles vascu<strong>la</strong>ires cérébraux etpériphériques.PharmacodynamieLa propentofylline, un dérivé de xanthine,est un inhibiteur non sélectifdes phosphodiestérases. Elle a despropriétés vasodi<strong>la</strong>tatrices, améliore
1508 MÉDICAMENTS CARDIO-VASCULAIRES<strong>la</strong> flexibilité des érythrocytes et inhibel’agrégation p<strong>la</strong>quettaire.PharmacocinétiqueChez le chien, le taux p<strong>la</strong>smatiquemaximal est atteint 15 minutes aprèsadministration orale. La demi-vie estde 30 minutes, <strong>la</strong> biodisponibilité d’environ30%. La métabolisation s’effectueau niveau <strong>du</strong> foie. L’éliminationpar voie rénale, sous forme de métabolites,est de 80-90%, le reste étantéliminé par l’intestin.Contre-indicationsL’inhibition non spécifique des phosphodiestérasess’exerce dans denombreux systèmes, aboutissant àdes effets très divers: aux niveaux cardio-vascu<strong>la</strong>ire,<strong>du</strong> système nerveuxcentral, des reins…Effets indésirablesDes vomissements, des réactions allergiquesou des troubles cardiaquespeuvent survenir.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser en période de gestation.LMR propentofylline : KARSIVAN (MSD A.H.)propentofylline: 50 mgcomprimé poPosologie:Ca: 2 x 2,5 mg/kg pj (min 4 - 8 sem)compr 60R/VITOFYLLIN 50 mg compr pelliculés chiens(Animalcare)propentofylline: 50 mgcomprimé pelliculé poPosologie:Ca (PV > 2,5 kg): 6 – 10 mg/kg en 2 prisescompr 56, 140R/VITOFYLLIN 100 mg compr pelliculés chiens(Animalcare)propentofylline: 100 mgcomprimé pelliculé poPosologie:Ca (PV > 5 kg): 6 – 10 mg/kg en 2 prisescompr 56, 140R/8.3 DiurétiquesDe façon générale, <strong>la</strong> c<strong>la</strong>sse pharmacologique des diurétiques comprend:- les diurétiques «cardio-vascu<strong>la</strong>ires», représentés par les dérivés xanthiques,- les diurétiques osmotiques,- les natriurétiques. Ce dernier groupe est représenté par les inhibiteurs de l’anhydrasecarbonique, les thiazides, les diurétiques de l’anse, tous hypokaliémiants,et les diurétiques d’épargne potassique, antagonistes ou non de l’aldostérone.Seul le furosémide, diurétique de l’anse, est abordé dans ce chapitre. La spirono<strong>la</strong>ctone,un diurétique d’épargne potassique, est abordée dans le chapitre 8.1.2.8.3.1 Diurétiques de l’anse8.3.1.1 FurosémideIndicationsLe RCP <strong>du</strong> furosémide précise qu’ilest indiqué dans le traitement desœdèmes, qu’ils soient d’origine cardiaque,rénale ou autre. Le furosémideest également indiqué dans le traitementde l’œdème de <strong>la</strong> mamelle et desextrémités. Il est utilisé aussi pour stimuler<strong>la</strong> diurèse en cas d’insuffisancerénale ou dans certaines intoxications.PharmacodynamieLe furosémide agit principalement sur<strong>la</strong> branche ascendante de l’anse deHenlé en bloquant <strong>la</strong> réabsorption desions chlore et sodium. Il en résulte uneffet diurétique ainsi qu’une excrétionaccrue <strong>du</strong> potassium, <strong>du</strong> calcium, <strong>du</strong>magnésium, des ions phosphates,bicarbonates, hydrogènes et ammoniums.Sur le p<strong>la</strong>n métabolique, lefurosémide peut également in<strong>du</strong>ireune augmentation de <strong>la</strong> glycémie et <strong>du</strong>taux de triglycérides. Contrairementaux thiazides, caractérisés par un effetplus long et plus modéré que celui desdiurétiques de l’anse, le furosémideconserve son action même lors d’unedéficience de <strong>la</strong> fonction rénale.PharmacocinétiqueLe furosémide exerce un effet puissant,rapide, mais de courte <strong>du</strong>rée. Ainsi, sil’action salidiurétique est observéeenviron cinq minutes après l’injectionintraveineuse de furosémide, elle nepersiste que <strong>du</strong>rant trois heures. Ilfaut cependant noter que <strong>la</strong> demi-vie<strong>du</strong> furosémide est prolongée chez lesnouveau-nés et chez les patients souffrantd’insuffisance rénale, hépatique
8 MÉDICAMENTS CARDIO-VASCULAIRES 151ou cardiaque. L’excrétion urinaire estdépendante <strong>du</strong> pH urinaire, ce quipeut expliquer les différences de <strong>du</strong>réed’action et de posologies chez les carnivoreset les herbivores.Contre-indicationsL’utilisation <strong>du</strong> furosémide est contreindiquéeen cas d’hypovolémie, d’hypokaliémie,d’hyponatrémie, de troubles de<strong>la</strong> fonction hépatique ou d’insuffisancerénale.Effets indésirablesLes chats surtout sont très sensiblesaux effets indésirables <strong>du</strong> furosémide.Les effets indésirables les plus communsassociés à l’administration defurosémide sont liés aux troubles de <strong>la</strong>ba<strong>la</strong>nce hydrique et électrolytique et incluentnotamment : déshydratation, hyponatrémie,alcalose hypochlorémique,hypokaliémie, hypomagnésémie ethypocalcémie. Ces troubles sont principalementobservés lors d’administrationprolongée ou en cas de surdosage.L’administration trop rapide de furosémidepar voie intraveineuse peut s’accompagnerd’ototoxicité.InteractionsLe furosémide peut également in<strong>du</strong>ireune augmentation:- de <strong>la</strong> glycémie et <strong>du</strong> taux detriglycérides,- de <strong>la</strong> néphrotoxicité des céphalosporineset de l’ototoxicité desamino glycosides,- de l’action hypotensive de diverscomposés, une attention touteparticulière devant être portée auxinhibiteurs de l’enzyme de con<strong>version</strong>de l’angiotensine. Afin d’éviterune baisse de pression trop forte, <strong>la</strong>dose de furosémide doit être diminuéede 25 à 50 %.- des pertes de potassium (augmentationqui peut, lors de traitementaux digitaliques, potentialiser <strong>la</strong> toxicitéde ces derniers),- de l’activité des anticoagu<strong>la</strong>nts.La réponse aux diurétiques de l’anse estatténuée par l’administration d’AINS.Du fait d’une augmentation <strong>du</strong> volumeurinaire, les concentrations dans l’urined’autres molécules, en particulier acides(furosémide, flunixine, phénylbutazone)sont diminuées (doping!).Précautions particulièresIl faudra veiller à ce qu’un apport hydrosodéadéquat accompagne l’administration<strong>du</strong> diurétique.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’usage raisonné chez des chiennes etchattes en gestation est possible maisdoit être évité dans <strong>la</strong> période précédantde peu <strong>la</strong> mise bas. Le furosémideest excrété par le <strong>la</strong>it ; mais onn’en connaît pas <strong>la</strong> répercussion cliniquechez les jeunes al<strong>la</strong>ités.LMR furosémide : DIMAZON (MSD A.H.)furosémide: 50 mg/mlsolution injectable im, ivPosologie:Eq, Bo: 0,5 - 1 mg/kg(intervalle entre 2 doses: Eq: 6 - 8 h, Bo:12 - 14 h)La dose peut être doubléeCa, Fe: 5 mg/kg, suivi par 1 - 2 mg/kg après6 - 8 hViande: Eq, Bo: 1 j, Lait: Bo: 1 jf<strong>la</strong>con 10 mlR/
9 MÉDICAMENTS DU SYSTÈME URO-GÉNITAL 1539. MÉDICAMENTS DU SYSTÈME URO-GÉNITALLes médicaments en médecine vétérinaire spécifiquement développés pourle traitement <strong>du</strong> tractus uro-génital sont répertoriés et commentés dans diverschapitres. Médicaments ayant pour indication le traitement de l’hypertrophie bénigne de<strong>la</strong> prostate: voir chapitre 2.1.3. Diurétiques: voir chapitre 8.3. Substances antibactériennes à usage gynécologique: voir chapitre 12.4. Substances antibactériennes à usage intramammaire: voir chapitre 12.5.9.1 Médicaments ayant comme indicationl’incontinence urinaire chez <strong>la</strong> chienneovario-hystérectomiséeL’ovario-hystérectomie chez les chiennes augmente l’incidence de l’incontinenceurinaire. Dans le passé, on pensait que cette forme d’incontinence urinaire était<strong>du</strong>e à <strong>la</strong> disparition de l’influence des œstrogènes sur le sphincter vésical, dont lerelâchement provoquait <strong>la</strong> perte urinaire. De nos jours, on admet cependant queles problèmes <strong>du</strong> sphincter ne sont pas tant <strong>du</strong>s à <strong>la</strong> baisse des œstrogènes maisplutôt à l’augmentation des taux de FSH et de LH qui l’accompagne, et qui résultede <strong>la</strong> disparition <strong>du</strong> feedback négatif des œstrogènes. Le traitement médical viseà augmenter <strong>la</strong> pression de clôture <strong>du</strong> sphincter vésical.9.1.1 Phénylpropano<strong>la</strong>mine (PPA)IndicationsTraitement, chez les chiennes ovariectomisées, de l’incontinence urinaire.PharmacodynamieCe sympathicomimétique a comme effet pharmacodynamique de stimuler lesrécepteurs de l’urètre principalement de nature adrénergique. Cette stimu<strong>la</strong>tionengendre un renforcement et une stabilisation de <strong>la</strong> fermeture <strong>du</strong> sphincter urétral.PharmacocinétiqueLa phénylpropano<strong>la</strong>mine est administrée oralement. La biodisponibilité est plusgrande lorsque <strong>la</strong> phénylpropano<strong>la</strong>mine est administrée à jeun.Contre-indicationsTraitement des troubles de comportement caractérisés par une tendance à uriner.Voir aussi Interactions.Effets indésirablesLes effets indésirables des sympathicomimétiques sont nombreux (cardio-vascu<strong>la</strong>ires,gastro-intestinaux) <strong>du</strong> fait de l’excitation <strong>du</strong> système nerveux sympathique.La phénylpropano<strong>la</strong>mine doit être employée avec beaucoup de précaution chezles sujets présentant des affections cardio-vascu<strong>la</strong>ires, une insuffisance rénaleou hépatique, un diabète sucré, de l’hyperadrénocorticisme, un g<strong>la</strong>ucome, del’hyperthyroïdie ou d’autres troubles métaboliques.InteractionsLes sympathicomimétiques augmentent <strong>la</strong> toxicité de <strong>la</strong> PPA. Ne pas administrersimultanément à des antagonistes cholinergiques. Un intervalle de 2 semainesdevrait être observé lorsque l’on veut administrer <strong>la</strong> PPA à des animaux préa<strong>la</strong>blementtraités avec des inhibiteurs des monoamine-oxydases. Combinés à <strong>la</strong> PPA,l’indométhacine (ou d’autres AINS), <strong>la</strong> réserpine et les antidépresseurs tricycliquespeuvent augmenter le risque d’une hausse de tension. Le cyclopropane et lesanesthésiques hydrocarbonés halogénés, administrés simultanément à <strong>la</strong> PPA,augmentent le risque d’arythmies.Précautions particulièresAvant tout traitement, il est nécessaire de s’assurer que l’incontinence n’est pasliée à d’autres facteurs tels qu’une anomalie morphologique ou des troubles decomportement. L’examen clinique reste primordial.
1549 MÉDICAMENTS DU SYSTÈME URO-GÉNITALRepro<strong>du</strong>ction et <strong>la</strong>ctationEtant donné l’indication, l’administration <strong>du</strong>rant <strong>la</strong> gestation ou <strong>la</strong> <strong>la</strong>ctation n’estpas d’application.LMR phénylpropano<strong>la</strong>mine : PROPALIN SIROP CHIEN (Vétoquinol)phénylpropano<strong>la</strong>mine chlorhydrate: 50 mg/mlsirop poPosologie:Ca: 1 mg/kg 3 x pjf<strong>la</strong>con 30 ml (+ seringue de 1,5 ml),100 ml (+ seringue de 1,5 ml)R/9.1.2 ŒstriolIndicationsTraitement de l’incontinence urinaire hormono-dépendante chez des chiennesovario-hystérectomisées.PharmacodynamieMalgré un mécanisme d’action cellu<strong>la</strong>ire et une affinité aux récepteurs identiques,l’action de l’œstriol est plus courte que celle de l’œstradiol. Ceci s’explique parune dissociation plus rapide <strong>du</strong> récepteur et une élimination plus rapide de l’œstriol.Tout en ayant une action courte, l’œstriol n’est pas un œstrogène faible.Ceci pourrait expliquer l’absence d’effets utérotropes. La liaison de l’œstriol avecles récepteurs d’œstrogène présents au niveau des parties distales <strong>du</strong> systèmeurogénital, améliore <strong>la</strong> pression de clôture urétrale et augmente <strong>la</strong> capacité de <strong>la</strong>vessie.PharmacocinétiqueL’œstriol est rapidement résorbé chez le chien après une administration orale.La concentration p<strong>la</strong>smatique maximale est atteinte après 1 heure. Lors d’administrationsrépétées, un état stable apparaît rapidement. Il n’y a pas d’accumu<strong>la</strong>tion.En raison des variations indivi<strong>du</strong>elles importantes des Cmax et desAUC, les doses d’œstriol doivent être définies pour chaque animal séparément.L’élimination, principalement par voie rénale, est rapide.Effets indésirablesDes effets œstrogéniques tels que le gonflement mammaire et vulvaire et/oul’attraction des mâles ainsi que des vomissements ont été observés lors d’administrationde doses élevées. Ces effets secondaires sont réversibles (diminutionde <strong>la</strong> dose). Exceptionnellement, des saignements vaginaux ont été constatés.La ré<strong>du</strong>ction de <strong>la</strong> dose ou l’arrêt <strong>du</strong> traitement résout ce problème. L’œstriol neprésente pas les effets indésirables typiques des autres œstrogènes, tels que <strong>la</strong>suppression de <strong>la</strong> moelle osseuse ou l’in<strong>du</strong>ction de pyomètres. De fortes dosesd’œstrogènes peuvent favoriser des tumeurs des organes cibles comportant desrécepteurs aux œstrogènes comme les g<strong>la</strong>ndes mammaires. En comparaison au17-bêta-œstradiol, l’œstriol n’est pas ou très peu carcinogène.Contre-indicationsL’administration à des femelles non stérilisées est contre-indiquée. Ne pas administreraux animaux souffrant d’un syndrome de polyurie/polydipsie.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe médicament ci-dessous est exclusivement indiqué dans le traitement dechiennes ovario-hystérectomisées.LMR œstriol: INCURIN (MSD A.H.)oestriol: 1 mgcomprimé poPosologie:Ca: 1 compr/animal pj (adapter <strong>la</strong> dose par<strong>la</strong> suite)compr 30R/
9 MÉDICAMENTS DU SYSTÈME URO-GÉNITAL 1559.1.3 EphédrineIndicationL’éphédrine est un sympathicomimétique principalement utilisé dans le traitementde l’incontinence urinaire causée par une hypotonie <strong>du</strong> sphincter de l’urètre chezdes chiennes ovario-hystérectomisées.PharmacodynamieL’éphédrine stimule les récepteurs adrénergiques alpha et bêta ainsi que <strong>la</strong> secrétionde catécho<strong>la</strong>mines des neurones sympathiques. L’éphédrine a égalementdes effets centraux.Elle provoque une contraction <strong>du</strong> sphincter urétral interne et une re<strong>la</strong>xation desmuscles de <strong>la</strong> vessie par action sympathicomimétique des récepteurs adrénergiquespériphériques.PharmacocinétiqueL’éphédrine est rapidement absorbée et <strong>la</strong> biodisponibilité élevée. Elle est <strong>la</strong>rgementdiffusée dans le corps et franchit <strong>la</strong> barrière hémato-encéphalique. Laprincipale voie de métabolisation est <strong>la</strong> déméthy<strong>la</strong>tion en noréphédrine. Avec uneacidité urinaire élevée, 80 à 90% de <strong>la</strong> dose administrée est éliminée dans les48 heures par excrétion urinaire.Contre-indicationsNe pas utiliser chez les chiens atteints de g<strong>la</strong>ucome ni en cas d’hypersensibilitéà l’éphédrine. Le pro<strong>du</strong>it ne doit être utilisé chez les chiens souffrant de ma<strong>la</strong>diescardiovascu<strong>la</strong>ires qu’après une analyse détaillée des risques/bénéfices. Ne pasutiliser chez les chiens pesant moins de 20 kg. Il convient de contrôler régulièrementau cours <strong>du</strong> traitement les animaux souffrant de ma<strong>la</strong>dies cardiovascu<strong>la</strong>ires,d’obstruction urétrale partielle, d’hypertension, de diabète sucré, d’hypercorticisme,d’hyperthyroïdie ou d’autres désordres métaboliques.Effets indésirablesEffets cardiovascu<strong>la</strong>ires (tachycardie, fibril<strong>la</strong>tion auricu<strong>la</strong>ire, stimu<strong>la</strong>tion de l’activitécardiaque et vasoconstriction), stimu<strong>la</strong>tion <strong>du</strong> système nerveux central (insomnie,excitation, anxiété et tremblements muscu<strong>la</strong>ires), halètement, mydriase,cystite, broncho-di<strong>la</strong>tation et diminution de <strong>la</strong> sécrétion de mucus, ré<strong>du</strong>ction de <strong>la</strong>motilité et <strong>du</strong> tonus de <strong>la</strong> paroi intestinale.Les effets indésirables propres à l’action de l’éphédrine apparaissent fréquemment,l’anxiété et les effets cardiovascu<strong>la</strong>ires étant les plus fréquents.InteractionsDes interactions avec d’autres sympathicomimétiques peuvent survenir.L’éphédrine peut stimuler le métabolisme glucocorticoïde. Un emploi concomitantavec les inhibiteurs de <strong>la</strong> monoamine oxydase peut provoquer de l’hypertension.L’éphédrine peut accentuer l’action de pro<strong>du</strong>its de <strong>la</strong> même c<strong>la</strong>sse comme, parexemple, <strong>la</strong> théophylline. Les anesthésiques vo<strong>la</strong>tils peuvent accentuer <strong>la</strong> sensibilité<strong>du</strong> myocarde aux effets cardiovascu<strong>la</strong>ires de l’éphédrine. Un emploi concomitantavec des glucosides cardiaques, de <strong>la</strong> quinine et des antidépresseurstricycliques peut provoquer une arythmie. Des constrictions vascu<strong>la</strong>ires peuventse pro<strong>du</strong>ire après un traitement concomitant avec des alcaloïdes de l’ergot et del’oxytocine. Les substances susceptibles d’augmenter le pH de l’urine peuventprolonger l’excrétion d’éphédrine, alors que les substances diminuant le pH del’urine, peuvent accélérer l’excrétion d’éphédrine.Précautions particulières/Risques pour l’hommeIl est recommandé aux femmes enceintes de porter des gants pour administrerle pro<strong>du</strong>it. La notice insiste également sur les risques en cas d’ingestion orale, enparticulier chez les enfants.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie en cas de gestation ou de <strong>la</strong>ctation. Nepas administrer aux animaux de repro<strong>du</strong>ction.
1569 MÉDICAMENTS DU SYSTÈME URO-GÉNITALLMR éphédrine : ENURACE 10 (Ecuphar)éphédrine chlorhydrate: 10 mg/comprcomprimé poPosologie:Ca (PV de 5 à 20 kg): doser selon effet,dose de départ: 2 mg/kg pj (en 2 prises),max 5 mg/kgcompr 60R/ENURACE 50 (Ecuphar)éphédrine chlorhydrate: 50 mgcomprimé poPosologie:Ca (PV > 20 kg): doser selon effet,dose de départ: 2 mg/kg pj (en 2 prises),max 5 mg/kgcompr 100R/
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 15710. MÉDICAMENTS DU SYSTÈME NERVEUX CENTRALET PÉRIPHÉRIQUE10.1 Anesthésiques généraux injectables10.1.1 Anesthésiques injectables: les barbituriquesLes barbituriques sont des anesthésiques injectables utilisés de longue date. EnBelgique, le pentobarbital n’est enregistré qu’à des fins vétérinaires; le thiopentalet le phénobarbital sont des pro<strong>du</strong>its à usage humain. La substitution de l’acidebarbiturique qui est <strong>la</strong> structure chimique de base de ces composés, a permis <strong>la</strong>synthèse de diverses molécules. Elles diffèrent notamment par leur puissance,leur rapidité d’action et d’élimination, et leur métabolisme ainsi que par leur activitéhypnotique, anticonvulsivante ou anesthésique.Indications- Les barbituriques à action ultracourte comme le méthohexital ne sont plusdisponibles.- Les thiobarbituriques à action courte comme le thiopental, disponible sousforme de poudre soluble à usage humain, sont utilisés pour l’in<strong>du</strong>ction etéventuellement le maintien de l’anesthésie. Le contrôle de <strong>la</strong> prolongation del’anesthésie obtenue par des administrations réitérées et le réveil qui s’ensuitest parfois difficile vu <strong>la</strong> cinétique variable d’un indivi<strong>du</strong> à l’autre, en particulierliée à <strong>la</strong> redistribution dans les graisses corporelles. Les schémas posologiquesdépendent aussi de <strong>la</strong> prémédication éventuelle.- Les barbituriques dont <strong>la</strong> <strong>du</strong>rée d’action est moyenne, comme le pentobarbitalen solution (6% ou 20%), sont utilisés pour le maintien de l’anesthésieou pour l’euthanasie. Les solutions concentrées permettent l’injection de volumesassez faibles mais sont réservées à l’euthanasie (voir chapitre 10.3.1.)- Les barbituriques à action longue (phénobarbital) peuvent être utilisés parvoie orale dans le cadre <strong>du</strong> traitement de fond de l’épilepsie (voir chapitre10.10.1.).PharmacodynamieLe mode d’action des barbituriques n’est pas encore complètement élucidé, maisleur action principale consiste à inhiber les influx nerveux en direction <strong>du</strong> cortexcérébral. Il a été établi qu’ils interagissent avec <strong>la</strong> libération et l’action de différentsneuromédiateurs et notamment de l’acide gamma aminobutyrique (GABA), etqu’ils in<strong>du</strong>isent une diminution de con<strong>du</strong>ctance des canaux ioniques. Leur actionsur le récepteur à <strong>la</strong> glycine justifie leur usage en cas d’intoxication à <strong>la</strong> strychnine.Leur action sur le système nerveux central comprend des effets majoritairementdépresseurs pouvant con<strong>du</strong>ire, lors de surdosage volontaire ou involontaire, aucoma et à <strong>la</strong> mort de l’animal <strong>du</strong> fait de l’inhibition des centres respiratoires. Selon<strong>la</strong> dose administrée, les barbituriques peuvent in<strong>du</strong>ire tous les états de dépression<strong>du</strong> système nerveux central depuis une sédation plus ou moins profonde jusqu’àun stade d’anesthésie générale avancé voire jusqu’à l’euthanasie. Une injectionrapide entraîne une narcose profonde ; une injection lente requiert une augmentationde <strong>la</strong> dose. En revanche, l’analgésie et <strong>la</strong> myore<strong>la</strong>xation sont souvent de qualitémoyenne ou mauvaise. La réponse obtenue dépend de <strong>la</strong> substance active,de l’espèce traitée, de <strong>la</strong> voie d’administration, de <strong>la</strong> posologie et de <strong>la</strong> pharmacocinétiquede <strong>la</strong> molécule.PharmacocinétiqueLes barbituriques subissent un phénomène de redistribution après leur administrationvers les tissus adipeux. Cette caractéristique est responsable de l’effetcumu<strong>la</strong>tif lors d’injections répétées. Une attention particulière doit être accordéeau taux d’albumine p<strong>la</strong>smatique (notamment pour le thiopental dont <strong>la</strong> liaison auxprotéines est importante), et au pH sanguin. Un pH bas augmente <strong>la</strong> proportionde <strong>la</strong> forme active en modifiant le degré d’ionisation <strong>du</strong> principe actif. Lorsque
15810 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEdes barbituriques de type court sont employés, le réveil rapide est lié à <strong>la</strong> redistribution<strong>du</strong> principe actif dans les graisses. En cas d’administrations répétées,<strong>la</strong> bioaccumu<strong>la</strong>tion qui s’instaure impose de ré<strong>du</strong>ire progressivement les dosesinjectées. L’action longue <strong>du</strong> pentobarbital s’explique par sa redistribution lente.Tous les barbituriques passent rapidement les barrières hémato-méningée et p<strong>la</strong>centaire.La liposolubilité, plus ou moins importante selon les molécules, mo<strong>du</strong>lenéanmoins <strong>la</strong> vitesse d’in<strong>du</strong>ction. Les thiobarbituriques sont essentiellementmétabolisés par le foie et d’autres tissus, puis excrétés par voie rénale. Le phénobarbitalest surtout évacué par voie urinaire. Le pentobarbital occupe une positionintermédiaire. L’alcalinisation des urines peut augmenter <strong>la</strong> vitesse d’éliminationdes barbituriques dont <strong>la</strong> forme active est éliminée majoritairement par l’urine.Bien que ceci concerne moins <strong>la</strong> médecine vétérinaire, ces substances in<strong>du</strong>isentégalement une dépendance et de <strong>la</strong> tolérance con<strong>du</strong>isant in fine à l’utilisation dedoses croissantes. L’index thérapeutique reste cependant identique.Contre-indicationsLes barbituriques doivent toujours être utilisés avec précaution, en particulier dansles cas suivants: hypovolémie, anémie, troubles respiratoires et insuffisance hépatiquegrave. Les chats sont plus sensibles à <strong>la</strong> dépression respiratoire. Certainesraces canines telles que le boxer, <strong>du</strong> fait de l’anatomie particulière <strong>du</strong> pharynx,et les lévriers, chez lesquels l’administration de barbituriques à action courte setra<strong>du</strong>it par des effets de longue <strong>du</strong>rée, sont particulièrement sensibles aux effetsdes barbituriques. Le pentobarbital ne peut pas être administré pour le traitementde convulsions causées par une intoxication à <strong>la</strong> lidocaïne.Effets indésirablesCertains effets indésirables non négligeables sont rencontrés spécialement lorsde l’utilisation de doses importantes. Ainsi, le vétérinaire peut s’attendre à unedépression respiratoire et cardiaque dose-dépendante aboutissant, suivant l’indivi<strong>du</strong>et <strong>la</strong> dose utilisée, à un arrêt respiratoire puis cardiaque, précédant parfoisl’arrêt total de l’activité cérébrale. Des effets cardio-vascu<strong>la</strong>ires tels que tachycardie,arythmies, hypotension, diminution de <strong>la</strong> contractilité myocardique peuventaussi apparaître à doses plus faibles, essentiellement chez des patients souffrantd’insuffisance cardiaque congestive ou d’hypotension. Des perturbations rénalescomme l’oligurie et l’anurie peuvent survenir <strong>du</strong> fait d’une hypotension sévère etprolongée. Les barbituriques peuvent aussi diminuer <strong>la</strong> motricité gastro-intestinale.La motricité et <strong>la</strong> coordination muscu<strong>la</strong>ire sont souvent perturbées après <strong>la</strong>levée de l’anesthésie. Le traitement à mettre en p<strong>la</strong>ce en cas d’intoxication pardes barbituriques est purement symptomatique et consiste à maintenir les fonctionsvitales perturbées. La respiration assistée, l’usage de médicaments soutenantles systèmes cardiorespiratoires inhibés, et l’alcalinisation urinaire figurentparmi les mesures couramment employées. L’alcalinisation des urines vise àré<strong>du</strong>ire <strong>la</strong> réabsorption des barbituriques dans les tubuli rénaux.InteractionsEn cas d’usage prolongé de ces substances, l’in<strong>du</strong>ction <strong>du</strong> système microsomalhépatique peut mo<strong>du</strong>ler le métabolisme d’autres médicaments, y compris desbarbituriques. Inversement, les molécules interférant avec le cytochrome P450peuvent modifier <strong>la</strong> biotransformation des barbituriques. A titre d’exemple, l’effetdes barbituriques est renforcé par le chloramphénicol bien connu pour sonaction inhibitrice sur le cytochrome P450. L’activité d’anticoagu<strong>la</strong>nts oraux, desglucocorticoïdes, des bêta-bloquants (propanolol), de <strong>la</strong> théophylline et <strong>du</strong> métronidazoleest inhibée en raison de l’in<strong>du</strong>ction possible <strong>du</strong> cytochrome P450 parles barbituriques. Sur le p<strong>la</strong>n pharmacodynamique, des effets synergiques avecd’autres médicaments agissant sur le système nerveux central sont à prendre encompte (autres anesthésiques, sédatifs, hypnotiques, phénothiazines, antihistaminiques…).Rappelons que le glucose potentialise les effets des barbituriques etpeut engendrer un approfondissement ou une réin<strong>du</strong>ction de l’anesthésie lorsqu’ilest administré <strong>du</strong>rant <strong>la</strong> période de réveil aux oiseaux, aux hamsters, aux <strong>la</strong>pinset, dans une moindre mesure, chez le chien.Précautions particulièresChez les petits animaux de compagnie, l’injection IV <strong>du</strong> premier tiers de <strong>la</strong> dosedoit être re<strong>la</strong>tivement rapide, afin d’éviter <strong>la</strong> phase d’excitation. Ensuite, le barbituriqueest injecté à <strong>la</strong> demande, lentement, progressivement et de manière
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 159discontinue. Chez les grands animaux, <strong>la</strong> dose est généralement administrée parvoie IV sous forme de bolus, ce qui entraine une in<strong>du</strong>ction rapide (« crash-in<strong>du</strong>ction») souvent caractérisée par une apnée. La solution ayant un pH alcalin trèsmarqué, une administration strictement intraveineuse est indispensable. Des dilutionsadaptées (1.25 à 2.5 %) permettent d’éviter les lésions de <strong>la</strong> paroi veineuse.Une administration périveineuse entraîne une nécrose tissu<strong>la</strong>ire.L’administrationpar voie intrapéritonéale est possible chez les espèces plus petites mais elle in<strong>du</strong>itune anesthésie imprévisible (aussi bien en <strong>du</strong>rée qu’en intensité).Repro<strong>du</strong>ction et <strong>la</strong>ctationLes barbituriques sont embryotoxiques et provoquent des anomalies congénitales.De petites quantités sont excrétées par le <strong>la</strong>it et peuvent provoquer de <strong>la</strong>sédation chez les animaux al<strong>la</strong>ités. Les barbituriques engendrent une dépressionrespiratoire chez le fœtus, il est donc déconseillé de les administrer pendant l’exécutiond’une césarienne.10.1.1.1 PentobarbitalLMR pentobarbital : NEMBUTAL (Ceva Santé Animale)pentobarbital sodique: 60 mg/mlsolution injectable iv (ip)Posologie:Ca: 25 à 35 mg/kgFe: 25 mg/kganimal de <strong>la</strong>bo: 25 à 35 mg/kgf<strong>la</strong>con de 100 mlR/psych10.1.2 Anesthésiques injectables non barbituriques10.1.2.1 Anesthésiques dissociatifsParmi les agents dissociatifs utilisésen médecine vétérinaire, il faut citer <strong>la</strong>phencyclidine, <strong>la</strong> tilétamine et <strong>la</strong> kétamine,qui sont toutes trois des dérivéscyclohexy<strong>la</strong>mines. Seules <strong>la</strong> kétamineet <strong>la</strong> tilétamine sont enregistrées enBelgique à usage vétérinaire. La tilétaminepossède une action plus longueet un effet analgésique plus marquéque <strong>la</strong> kétamine.IndicationsLes anesthésiques dissociatifs ontun spectre thérapeutique assez <strong>la</strong>rgeet une toxicité organique faible. Ilspeuvent être administrés par voieintraveineuse ou intramuscu<strong>la</strong>ire et in<strong>du</strong>isentune bonne analgésie périphérique.Leur influence sur <strong>la</strong> respirationétant modérée, ils ne répriment quasimentpas les réflexes de déglutition etde toux. En raison de l’analgésie viscéraleminime et <strong>du</strong> risque de catalepsielié à <strong>la</strong> rigidité muscu<strong>la</strong>ire, il est déconseilléde les utiliser seuls. L’état cataleptiqueapparaît moins fréquemmenten cas d’usage simultané avec desbenzodiazépines. La kétamine est unesolution aqueuse d’un mé<strong>la</strong>nge racémiquedont <strong>la</strong> forme S constitue l’élémentanalgésique actif. La tilétamineest disponible sous forme de poudrelyophilisée (250 mg) en associationavec <strong>du</strong> zo<strong>la</strong>zépam (1:1), un dérivé desbenzodiazépines apportant des effetsmyore<strong>la</strong>xants et anti-convulsivants.Les combinaisons fixes, apparemmentd’usage plus simle, ne permettent pasde mo<strong>du</strong>ler les apports de chaqueprincipe actif en fonction des besoins.La posologie est déterminée en fonction<strong>du</strong> type de prémédication. La posologieest par exemple ré<strong>du</strong>ite en casd’utilisation d’agonistes alpha-2. Outreces indications revendiquées dansles notices des pro<strong>du</strong>its actuellementsur le marché, d’autres sont décritesdans <strong>la</strong> littérature. Elles peuvent êtreexploitables en clinique à conditionque le praticien en prenne l’entièreresponsabilité.PharmacodynamieLes anesthésiques dissociatifs in<strong>du</strong>isent,après une administration IVou IM, une anesthésie caractérisée parun « sommeil » re<strong>la</strong>tivement superficielcombiné à une analgésie somatiqueou périphérique de bonne qualité.L’analgésie viscérale est plus faible.L’utilisation de faibles doses IV de kétamine,en boli ou en infusion, entraîne
16010 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEun effet analgésique périphériquepositif, utile en cas d’usage per- oupostopératoire. La kétamine administréepar voie épi<strong>du</strong>rale provoque unebrève analgésie périphérique del’arrière-train, de bonne qualité. Lesélectro-encéphalogrammes montrentune dissociation entre le tha<strong>la</strong>muset le système limbique. Certaines régionstelles que le tha<strong>la</strong>mus et celle<strong>du</strong> cortex sont déprimées tandis qued’autres, telles que le système limbique,restent activées, donnant ainsiune explication possible aux effets hallucinogènes.Ces caractéristiques sontspécifiques à cette famille d’anesthésiqueset expliquent aussi l’augmentation<strong>du</strong> tonus muscu<strong>la</strong>ire et pourquoiles réflexes pharyngés et <strong>la</strong>ryngés,le tonus maxil<strong>la</strong>ire, des mouvementsocu<strong>la</strong>ires comme le nystagmus et l’ouverturedes paupières sont conservés.Le mécanisme d’action est complexeet repose sur des interactions avecplusieurs récepteurs, telles que l’antagonisation<strong>du</strong> récepteur NMDA (acideN-méthyl-D-aspartique) et des médiateursdans le système nerveux central,en particulier dans le cerveau et dans<strong>la</strong> corne dorsale de <strong>la</strong> moelle épinière.PharmacocinétiqueLa kétamine est disponible sous formede solution injectable à usage intramuscu<strong>la</strong>ire,intraveineux ou sous-cutané.Une administration épi<strong>du</strong>raleest possible mais relève de <strong>la</strong> cascadethérapeutique. La tilétamine estcombinée au zo<strong>la</strong>zépam et disponiblesous forme de poudre lyophilisée (1:1).En raison de sa grande liposolubilité,de son faible poids molécu<strong>la</strong>ire et <strong>du</strong>pKa de 7.5, les effets de <strong>la</strong> kétaminesur le SNC apparaissent rapidement(T max: 10 minutes), mais per<strong>du</strong>renttrois fois moins longtemps que ceuxde <strong>la</strong> tilétamine. Sa demi-vie est d’environ1 à 3 heures suivant les espèces.La kétamine a une grande liposolubilitéet diffuse dans tous les tissus,particulièrement dans le cerveau, lefoie, les poumons et le tissu adipeux.La kétamine traverse également <strong>la</strong>barrière p<strong>la</strong>centaire. La disparition deseffets sur le SNC après l’administrationunique d’un bolus intervient <strong>du</strong> faitd’une redistribution rapide <strong>du</strong> cerveauaux autres tissus. Chez le chien et lecheval, <strong>la</strong> kétamine est métaboliséepar déméthy<strong>la</strong>tion et hydroxy<strong>la</strong>tionau niveau <strong>du</strong> foie. Les métabolites etune partie de <strong>la</strong> forme inchangée sontexcrétés dans les urines. La faible métabolisationhépatique chez le chat expliquel’excrétion rénale de <strong>la</strong> kétaminesous forme inchangée. Administréede manière répétée, <strong>la</strong> kétamine in<strong>du</strong>itune augmentation des enzymesmicrosomales hépatiques, ce qui peutprovoquer de <strong>la</strong> tolérance à plus longterme.Contre-indications- Hypersensibilité connue à <strong>la</strong>kétamine.- Utilisation sans prémédication pourles interventions chirurgicales.- Insuffisance hépatique, rénale oucardiaque.- Pression intracrânienne accrue(traumatisme à <strong>la</strong> tête).- G<strong>la</strong>ucome.- Opération intra-ocu<strong>la</strong>ire prévue.- Patients traités avec desorganophosphorés.- Etant donné que les réflexes dedéglutition et de toux sont conservés,les interventions au <strong>la</strong>rynx, aupharynx ou à <strong>la</strong> trachée sont difficilementréalisables.- Chez l’homme, risque d’hypertensionsévère et de tachycardie chezles patients souffrant d’hyperthyroïdieou chez les patients traités avecune hormone thyroïdienne exogène.La pertinence de cette contre-indicationen médecine vétérinaire resteincertaine, même si dans certainescirconstances (importante haussede pression sanguine), des lésions<strong>du</strong> myocarde ont été observées,e.a. chez le chat après usage de <strong>la</strong>kétamine.Effets indésirablesLa solution ayant un pH bas (3.5), uneadministration IM peut être suivie dedouleurs et de réactions tissu<strong>la</strong>ires. Lesanesthésiques dissociatifs in<strong>du</strong>isentune augmentation <strong>du</strong> débit sanguincérébral et des pressions intracrânienneet intra-ocu<strong>la</strong>ire. Ces effetsjustifient leur contre-indication chezdes animaux présentant une pressionintracrânienne accrue, un traumatismede <strong>la</strong> tête ou de <strong>la</strong> cornée. Des effetshallucinogènes peuvent être observés<strong>du</strong>rant <strong>la</strong> période de réveil, se tra<strong>du</strong>isantpar un comportement anormal, etdes réactions excessives aux stimuli.En raison de <strong>la</strong> stimu<strong>la</strong>tion indirecte<strong>du</strong> système cardio-vascu<strong>la</strong>ire d’originesympathique, l’administration d’anesthésiquesdissociatifs provoque un effetinotrope positif, une augmentation
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 161<strong>du</strong> rythme cardiaque, de <strong>la</strong> pressionsanguine et <strong>du</strong> débit cardiaque, avec,toutefois, une résistance périphériqueconstante. L’accroissement de <strong>la</strong> circu<strong>la</strong>tionsanguine coronarienne aprèsl’administration de <strong>la</strong> kétamine estparfois insuffisant pour compenser <strong>la</strong>consommation accrue en oxygène parle myocarde. Cette combinaison d’effetpourrait être à l’origine de l’apparitionde lésions <strong>du</strong> myocarde chez le chat.La dépression respiratoire est minime.Une apnée et des irrégu<strong>la</strong>rités respiratoiressont cependant possibles. Lesurdosage résulte en une dépressionrespiratoire ou une apnée sévère. Uneaugmentation des sécrétions bronchiqueset salivaires qui deviennentplus visqueuses est observée. L’usaged’agents parasympathicolytiques peuts’avérer utile pour contrôler ces effets.Notons que l’atropine peut renforcerles effets stimu<strong>la</strong>nts sur le systèmecardio-vascu<strong>la</strong>ire.InteractionsDe nombreuses interactions ont étédécrites avec d’autres substancesactives comme les agonistes alpha-2-adrénergiques, les benzodiazépines,les anesthésiques vo<strong>la</strong>tils, lesbarbituriques, <strong>la</strong> guaïfénésine et lesneuroleptiques. Elles sont exploitéesen anesthésiologie; les combinaisonsvariant selon les espèces et le statutphysiologique et physiopathologiquede l’animal. L’utilisation raisonnée debenzodiazépines, d’agonistes alpha-2-adrénergiques ou de phénothiazinesen association avec des anesthésiquesdissociatifs permet de contrôler ou toutau moins de ré<strong>du</strong>ire les effets indésirablessur le système cardio-vascu<strong>la</strong>irenotamment. Les effets vagolytiques etsympathicomimétiques centraux justifientque ces dérivés soient utilisés enassociation avec les agonistes alpha-2-adrénergiques connus pour leurs effetsinverses, notamment au niveau <strong>du</strong>système cardio-vascu<strong>la</strong>ire. On noteraque l’administration d’atipamézole àun animal soumis à l’action combinéede <strong>la</strong> kétamine et d’un agoniste alphaadrénergiquepeut in<strong>du</strong>ire des convulsions,tout particulièrement chez lechien. Une autre association très couranteest l’utilisation de kétamine oude tilétamine avec certains dérivésdes benzodiazépines tels que le zo<strong>la</strong>zépam,le diazépam ou le midazo<strong>la</strong>m,afin d’exploiter l’effet myore<strong>la</strong>xant etanticonvulsivant de ces dernières (voirchapitre 10.6). Les hormones thyroïdiennespeuvent amplifier l’hypertensionet <strong>la</strong> tachycardie in<strong>du</strong>ites par<strong>la</strong> kétamine. Le chloramphénicol estsusceptible de prolonger l’anesthésiechez le chat <strong>du</strong> fait d’une action sur lecytochrome P450.Précautions particulièresLes yeux <strong>du</strong> chat restent ouverts <strong>du</strong>rantl’anesthésie et doivent donc êtreprotégés. Durant l’anesthésie, les stimu<strong>la</strong>tionsauditives intempestivessont à éviter. Des hallucinations ayantété décrites chez l’homme, ces substancessont c<strong>la</strong>ssées parmi les stupéfiants(médicaments psychotropes).On veillera donc à respecter toutes lesprescriptions légales en <strong>la</strong> matière.Repro<strong>du</strong>ction et <strong>la</strong>ctationMême si <strong>la</strong> kétamine passe <strong>la</strong> barrièrep<strong>la</strong>centaire, les effets chez le fœtusrestent acceptables. La kétamine peutêtre administrée <strong>du</strong>rant <strong>la</strong> gestation ou<strong>la</strong> <strong>la</strong>ctation, il faut cependant noter queson usage <strong>du</strong>rant une césarienne in<strong>du</strong>itune anesthésie des nouveau-nés.KétamineLMR kétamine : ANESKETIN (Eurovet)kétamine (chlorhydrate): 100 mg/mlsolution injectable iv, imPosologie:Fe:- seul: 10 - 30 mg/kg (im) ou 2 - 6 mg/kg (iv)- après préméd: 10 - 22 mg/kg (im) ou3 - 8 mg/kg (iv)Ca:- après préméd: 5 - 22 mg/kg (im) ou5 - 10 mg/kg (iv)f<strong>la</strong>con 1 ou 5 x 10 mlR/psychKETAMINE 1000 CEVA (Ceva Santé Animale)kétamine (chlorhydrate): 100 mg/mlsolution injectable imPosologie:Après préméd avec xy<strong>la</strong>zine:Ca: 5 - 10 mg/kgFe: 10 - 20 mg/kgf<strong>la</strong>con 5 x 10 mlR/psych
16210 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUETilétamine + zo<strong>la</strong>zépamZo<strong>la</strong>zépam: voir aussi chapitre 10.6.LMR tilétamine + zo<strong>la</strong>zépam: ZOLETIL 100 (Virbac)tilétamine: 50 mg/mlzo<strong>la</strong>zépam: 50 mg/mlpoudre pour solution injectable im, ivPosologie:préméd: atropinedosage en mg de l’ensemble des substancesactivesCa:examen: 7 - 10 mg/kg (im), 5 mg/kg (iv)petite chirurgie:10 - 15 mg/kg (im), 7,5 mg/kg (iv)chirurgie majeure:15 - 25 mg/kg (im), 10 mg/kg (iv)Fe:examen, petite chirurgie:10 mg/kg (im), 5 mg/kg (iv)chirurgie majeure:15 mg/kg (im), 7,5 mg/kg (iv)animaux sauvages: voir notice spécialef<strong>la</strong>con 500 mg (poudre) + 5 ml (solvant)R/10.1.2.2 PropofolIndicationsLe propofol est un dérivé phénol quine peut être administré que par voieintraveineuse, en tant qu’anesthésiqueà action rapide mais courte. Il estutilisé pour in<strong>du</strong>ire des anesthésiesprolongées avec des agents vo<strong>la</strong>tils oupour l’entretien d’anesthésie de courtevoire de moyenne <strong>du</strong>rée (5 à 30 min enajustant les doses répétées).PharmacodynamieLe mécanisme d’action exact <strong>du</strong>propofol n’est pas encore élucidé.Le propofol interfère avec le neurotransmetteurinhibiteur GABA (acidegamma-aminobutyrique) et fait chuterl’activité métabolique cérébrale. Afaible dose, il est sédatif. Chez <strong>la</strong> plupartdes animaux domestiques, lepropofol administré par voie IV in<strong>du</strong>itune anesthésie rapide et brève, avecune bonne re<strong>la</strong>xation muscu<strong>la</strong>ire maisune analgésie minime. L’administrationd’analgésiques est nécessaire en casd’intervention chirurgicale. Des réactionsdouloureuses peuvent apparaîtreen cas d’administration IV. Le pro<strong>du</strong>itn’irrite toutefois pas ou peu les tissus.La posologie dépend de <strong>la</strong> prémédication(dose plus faible en cas d’usaged’agonistes alpha-2).PharmacocinétiqueLe propofol étant un anesthésiquehautement liposoluble, il est rapidementabsorbé par les tissus, notammentle cerveau. La courte <strong>du</strong>réed’action et le réveil total chez <strong>la</strong> plupartdes espèces sont les conséquencesde <strong>la</strong> redistribution rapide <strong>du</strong> cerveauvers les tissus périphériques et àl’élimination p<strong>la</strong>smatique efficace. Lamétabolisation a lieu dans le foie, maiségalement dans les poumons et lesreins (métabolisation extra-hépatique).L’excrétion se fait principalement parvoie rénale. Le réveil ne dépendant pasou peu de l’activité hépatique et rénale,le propofol peut être administré avecsuccès dans le cas d’insuffisancesde ces systèmes. Un effet cumu<strong>la</strong>tifen cas d’administration continue estnéanmoins possible. Dans ce cas,le rôle des systèmes d’éliminationprend de l’importance pour mettre finà l’anesthésie. Chez <strong>la</strong> plupart desespèces, le propofol in<strong>du</strong>it une anesthésierapide (dans les 30 – 60 sec) etbrève (10 min) avec une bonne myore<strong>la</strong>xationmais une analgésie minime.Chez le chien, le propofol est en grandepartie métabolisé via une hydroxy<strong>la</strong>tionassurée par le cytochrome P450puis via une glucurono-conjugaison.Cette dernière voie étant quasi absentechez le chat, <strong>la</strong> <strong>du</strong>rée d’éliminationet par conséquent le réveil, seront pluslents, surtout après des administrationscontinues ou répétées. Le mêmemécanisme est tenu pour responsable<strong>du</strong> réveil assez lent chez les lévriersaprès l’administration de propofol. Lamétabolisation est moins bien connuechez les autres espèces animales. Vul’existence d’autres voies de métabolisationtelles que les poumons, le propofolpeut être utilisé chez les patientsatteints d’insuffisance rénale et/ouhépatique.Contre-indicationsCe pro<strong>du</strong>it ne doit pas être utilisé pourl’in<strong>du</strong>ction et l’entretien de l’anesthésiegénérale par des doses répétéesqui dépasseraient les limites de <strong>la</strong>dose totale de 24 mg/kg (2,4 ml/kg) depropofol par anesthésie, en raison <strong>du</strong>risque d’effets toxiques <strong>du</strong>s au conservateur,l’alcool benzylique.Hypoprotéinémie, hypovolémie.Les patients en état de choc ou traumatiséssont plus sensibles aux effetsindésirables.Effets indésirablesDes effets indésirables tels que desnausées, des vomissements, del’hypothermie après une perfusionprolongée, des perturbations <strong>du</strong> comportementavec léchage excessif, ont
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 163été observés chez le chien et le chat.Des phases d’excitation peuvent êtreobservées après une administration IVchez le chien et le chat. Des contractionsmuscu<strong>la</strong>ires incontrôlées et desconvulsions chez le chien peuvent êtreobservées <strong>du</strong>rant l’anesthésie, surtouten l’absence d’une bonne prémédication.Au niveau cardio-vascu<strong>la</strong>ire, unedépression dose-dépendante accompagnéed’hypotension, de bradycardieet d’un effet inotrope négatif, comparablesaux effets pro<strong>du</strong>its par les thiobarbituriques,peut se manifester. Unedépression respiratoire et de l’apnéepeuvent également être observées,principalement suite à l’administrationde fortes doses ou d’une injection intraveineusetrop rapide.InteractionsIl a été démontré que cette moléculeest compatible avec de nombreuxagents neurotropes et notammentceux utilisés pour <strong>la</strong> prémédicationet les anesthésiques vo<strong>la</strong>tils ou myore<strong>la</strong>xants.Les molécules interférantavec le cytochrome P450 (p. ex. lechloramphénicol, <strong>la</strong> cimétidine) et lessubstances lipophiles (p. ex. le fentanyl,l’halothane) allongent <strong>la</strong> phasede réveil.Précautions particulièresAvant utilisation, le pro<strong>du</strong>it doit êtreinspecté visuellement pour vérifierl’absence de particules et d’anomaliesde <strong>la</strong> coloration. Il doit être jeté dans lecas contraire.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe propofol passe <strong>la</strong> barrière p<strong>la</strong>centaire.En raison de l’efficacité deconjugaison des enzymes, <strong>la</strong> dépressionchez les nouveau-nés est plutôtminimale. Des données sur l’utilisation<strong>du</strong> propofol chez les chiennes etles chattes al<strong>la</strong>itantes ne sont pasconnues.LMR propofol: PROPOVET MULTIDOSE 10 mg/ml émulsion injchiens, chats (Abbott Laboratories)propofol: 10 mg/mlémulsion injectable ivPosologie:Ca (âge > 5 m):- in<strong>du</strong>ction sans préméd: 6,5 mg/kg- in<strong>du</strong>ction avec un agoniste alpha2:1 mg/kg- in<strong>du</strong>ction sans agoniste alpha2: 4 mg/kgFe (âge > 5 m):- in<strong>du</strong>ction sans préméd: 8 mg/kg- in<strong>du</strong>ction avec un agoniste alpha2:1,2 mg/kg- in<strong>du</strong>ction sans agoniste alpha2: 6 mg/kgCa, Fe: entretien de l’anesth par PropoVet:administrer des doses répétées de 1 mg/kgf<strong>la</strong>con 5 x 20 mlR/10.1.2.3 Stéroïdes neuroactifsAlfaxaloneIndicationsLe médicament est indiqué chez leschiens et les chats comme anesthésiqued’in<strong>du</strong>ction préa<strong>la</strong>blement à uneanesthésie par inha<strong>la</strong>tion, ou commeanesthésique unique d’in<strong>du</strong>ction etd’entretien de l’anesthésie pour <strong>la</strong> réalisationd’examens ou d’interventionschirurgicales.PharmacodynamieL’alfaxalone est une molécule stéroïdeneuroactive possédant les propriétésd’un anesthésique général. Elle provoqueune action hypnotique par soninteraction avec les récepteurs GABA.Aux doses cliniques, l’effet analgésiquede l’alfaxalone est limité.PharmacocinétiqueLe volume de distribution après injectionunique de doses cliniques de 2 et5 mg/kg PV chez le chien et le chat estrespectivement de 2.4 l/kg et 1,8 l/kg.L’alfaxalone est métabolisée dansle foie. Les chiens comme les chatsforment les mêmes cinq métabolitesde Phase I (cytochrome P450) de l’alfaxalone.Les métabolites de Phase II(conjugaison) observés chez le chatsont le sulfate d’alfaxalone et le glucuronided’alfaxalone, tandis que chezle chien, <strong>du</strong> glucuronide d’alfaxalone aété observé. Chez le chat, <strong>la</strong> demi-vied’élimination p<strong>la</strong>smatique moyenne(t1/2) de l’alfaxalone est d’environ 45minutes pour une dose de 5 mg/kg.Chez le chien, <strong>la</strong> demi-vie d’éliminationp<strong>la</strong>smatique moyenne (t1/2) de l’alfaxaloneest d’environ 25 minutes pourune dose de 2 mg/kg. L’élimination
16410 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEde l’alfaxalone chez les chiens etles chats montre une cinétique nonlinéaire (dose-dépendante). Les métabolitessont éliminés, chez le chien etle chat, par voie fécale et rénale.Contre-indicationsNe pas utiliser concomitamment avecd’autres anesthésiques administréspar voie intraveineuse.Effets indésirablesUne apnée post-in<strong>du</strong>ction de naturepassagère peut survenir. C’est pourquoiune intubation endotrachéale etun apport d’oxygène sont nécessaires.Des doses plus élevées peuvent égalementprovoquer une dépressionrespiratoire.InteractionsEn cas d’utilisation simultanée d’autresdépresseurs <strong>du</strong> système nerveux central,on peut s’attendre à une potentialisationdes effets dépresseurs del’alfaxalone. En cas d’utilisation d’unou plusieurs agents de prémédication,<strong>la</strong> dose d’alfaxalone nécessaire peutêtre diminuée. Une prémédicationavec des agonistes des récepteursalpha-2-adrénergiques peut prolonger<strong>la</strong> <strong>du</strong>rée de l’anesthésie de manièredose-dépendante. La <strong>du</strong>rée <strong>du</strong>réveil peut être raccourcie en antagonisantles effets de ces agents deprémédication.En cas d’utilisation de benzodiazépinescomme seuls agents de prémédicationchez les chiens et les chats, <strong>la</strong>qualité de l’anesthésie n’est pas toujoursoptimale.Précautions particulièresL’innocuité <strong>du</strong> pro<strong>du</strong>it chez des animauxâgés de moins de 12 semainesn’a pas été étudiée. Afin d’éviter lerisque d’apnée post-in<strong>du</strong>ction, l’injectionintraveineuse doit être lente.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas étéétablie en période de gestation ou de<strong>la</strong>ctation. Des études sur l’alfaxalonechez des souris, des rats et des <strong>la</strong>pinsen gestation n’ont cependant pasmontré d’effets nuisibles. L’utilisation<strong>du</strong> pro<strong>du</strong>it doit donc faire l’objet d’uneévaluation bénéfice/risque chez lesanimaux en gestation.LMR alfaxalone: ALFAXAN 10 mg/ml (Jurox plc)alfaxalone: 10 mg/mlsolution injectable ivPosologie:Ca: in<strong>du</strong>ction:- sans préméd: 3 mg/kg- avec préméd: 2 mg/kgFe: in<strong>du</strong>ction:- avec ou sans préméd: 5 mg/kgCa: entretien perf:- sans préméd: 8 - 9 mg/kg/h- avec préméd: 6 - 7 mg/kg/hCa: entretien bolus:- sans préméd: 1,3 - 1,5 mg/kg (pour 10min)- avec préméd: 1 - 1,2 mg/kg (pour 10 min)Fe: entretien perf:- sans préméd: 10 - 11 mg/kg/h- avec préméd: 7 - 8 mg/kg/hFe: entretien bolus:- sans préméd: 1,6 - 1,8 mg/kg (pour 10min)- avec préméd: 1,1 - 1,3 mg/kg (pour 10min)f<strong>la</strong>con 10 mlR/10.2 Anesthésiques généraux vo<strong>la</strong>tils10.2.1 IsofluraneIndicationsL’isoflurane est enregistré en Belgique pour être utilisé chez les chevaux, leschiens, les chats, les oiseaux ornementaux, les reptiles ainsi que les petits mammifères(excepté l’in<strong>du</strong>ction au masque chez les <strong>la</strong>pins).PharmacodynamieLe mécanisme d’action exact de l’isoflurane n’est pas encore élucidé. Des changementsréversibles de <strong>la</strong> membrane neuronale dans le cerveau perturbant <strong>la</strong>neurotransmission sont suspectés. L’isoflurane in<strong>du</strong>it <strong>la</strong> perte de conscience maispossède des propriétés analgésiques modérées. Une dépression dose-dépendantedes centres respiratoire et cardio-vascu<strong>la</strong>ire provoque de l’hypotensionet de l’hypoventi<strong>la</strong>tion. L’effet sensibilisant <strong>du</strong> myocarde aux catécho<strong>la</strong>minesest moindre que celui exercé par l’halothane. Une dépression dose-dépendantedes systèmes rénal et hépatique est observée. L’isoflurane passant <strong>la</strong> barrièrep<strong>la</strong>centaire, les fœtus sont également anesthésiés. Les caractéristiques physicochimiquesde <strong>la</strong> molécule expliquent que l’in<strong>du</strong>ction et le réveil se déroulent assez
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 165rapidement. Chez les chevaux, une sédation supplémentaire peut être administréepour un réveil serein.PharmacocinétiqueCet anesthésique est très peu métabolisé (0.2% en moyenne de <strong>la</strong> dose inhalée),l’élimination pulmonaire étant <strong>la</strong> voie principale d’élimination. La concentrationalvéo<strong>la</strong>ire minimale dépend de l’espèce animale et de l’âge, elle s’élève en généralà 1.3 volume%.Contre-indications- Chez le <strong>la</strong>pin, une apnée dangereuse peut se manifester en cas d’in<strong>du</strong>ction aumasque.- Antécédents d’hypersensibilité à l’isoflurane.- Antécédents d’hyperthermie maligne.- Pression cérébro-spinale accrue.- Traumatisme crânien.- Myasthenia gravis.Effets indésirablesUne dépression dose-dépendante des systèmes cardio-vascu<strong>la</strong>ire, respiratoire,rénal et hépatique est observée. De petites quantités de fluoride se forment pendant<strong>la</strong> métabolisation.InteractionsLa prémédication utilisée et les autres anesthésiques administrés peuvent influencerl’intensité de l’anesthésie, qui devra être adaptée en conséquence.Précautions particulièresL’administration de l’isoflurane demande un équipement adéquat (vaporisateurspécifique, appareil d’anesthésie adapté) pourvu d’un système de venti<strong>la</strong>tionefficace afin d’éviter <strong>la</strong> pollution de l’environnement. L’oxygène peut être utilisécomme gaz porteur, seul ou combiné avec <strong>du</strong> protoxyde d’azote ou de l’air comprimé.L’isoflurane peut interagir avec les absorbants secs <strong>du</strong> dioxyde de carboneet provoquer <strong>la</strong> formation de monoxyde de carbone. Eviter donc le dessèchementdes absorbants de dioxyde de carbone.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’utilisation <strong>du</strong> pro<strong>du</strong>it ne doit se faire qu’après évaluation <strong>du</strong> rapport bénéfice/risque. L’isoflurane peut être utilisé lors d’une césarienne, les fœtus ou les nouveau-nésétant également anesthésiés.LMR isoflurane: ISOBA (MSD A.H.)isoflurane 100% w/wliquide pour inha<strong>la</strong>tion par fumigationPosologie:adapter <strong>la</strong> concentration à <strong>la</strong> pré-anesthésie:- Ca: in<strong>du</strong>ction: 2 - 4 %, entretien: 1,5 - 2,5 %- Fe: in<strong>du</strong>ction: 2 - 4 %, entretien: 1,5 - 3 %- Eq: in<strong>du</strong>ction: 3 - 5 %, entretien: 1,5 - 2,5 %- oiseaux de volière: in<strong>du</strong>ction: 3 - 5 %,entretien: habituellement 2 - 3 %, à adapterselon l’espèce/indivi<strong>du</strong>- reptiles: in<strong>du</strong>ction: 2 - 4 %, entretien:généralement 1 - 3 %- petits mammifères (voir notice): in<strong>du</strong>ction:2 - 3 %, entretien: 0,25 - 2 %Viande: Eq: 2 j, Lait: ne pas administrer auxEq dont le <strong>la</strong>it est destiné à <strong>la</strong> consommationhumaineNe pas administrer aux Co destinés à <strong>la</strong>consommationf<strong>la</strong>con 250 mlR/ISOFLO 100% w/w Inha<strong>la</strong>tion Vapeur, liquide(Abbott Lab)isoflurane: 100 %liquide pour inha<strong>la</strong>tionPosologie:Eq, Ca:- in<strong>du</strong>ction: 3 - 5 %- entretien: 1,5 - 2,5 %Fe:- in<strong>du</strong>ction: jusqu’à 4 %- entretien: 1,5 - 3 %rat, souris, hamster, chinchil<strong>la</strong>, gerbil,cobaye, furet:- in<strong>du</strong>ction: 2 - 3 %- entretien: 0,25 - 2 %oiseau de volière:- in<strong>du</strong>ction: 3 - 5 %- entretien: 2 - 3 %reptile:- in<strong>du</strong>ction: 2 - 4 %- entretien: 1 - 3 %Viande: Eq: 2 jf<strong>la</strong>con 250 mlR/
16610 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEISO-VET (Piramal Healthcare UK)isoflurane: 100 %liquide pour inha<strong>la</strong>tionPosologie:Eq, Ca:- in<strong>du</strong>ction: 3 - 5 %- entretien: 1,5 - 2,5 %Fe:- in<strong>du</strong>ction: jusqu’à 4 %- entretien: 1,5 - 3 %rat, souris, hamster, chinchil<strong>la</strong>, gerbil,cobaye, furet:- in<strong>du</strong>ction: 2 - 3 %- entretien: 0,25 - 2 %oiseau de volière:- in<strong>du</strong>ction: 3 - 5 %- entretien: 2 - 3 %reptile:- in<strong>du</strong>ction: 2 - 4 %- entretien: 1 - 3 %Viande + abats: Eq: 2 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/VETFLURANE 1000 mg/g (Virbac)isoflurane: 1000 mg/gliquide pour inha<strong>la</strong>tionPosologie:adapter <strong>la</strong> concentration à <strong>la</strong> pré-anesthésie:- Eq: in<strong>du</strong>ction: 3 - 5 %, entretien: 1,5 - 2,5 %- Ca: in<strong>du</strong>ction: max 5 %, entretien: 1,5 -2,5 %- Fe: in<strong>du</strong>ction: max 4 %, entretien: 1,5 - 3 %- oiseaux de volière: in<strong>du</strong>ction: 3 - 5 %,entretien: habituellement 2 - 3 %, à adapterselon l’espèce/indivi<strong>du</strong>- reptiles: in<strong>du</strong>ction: 2 - 4 %, entretien:généralement 1 - 3 %- petits mammifères (voir notice): in<strong>du</strong>ction:2 - 3 %, entretien: 0,25 - 2 %Viande et abats: Eq: 2 jNe pas utiliser chez les juments dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 mlR/10.3 Agents utilisés pour l’euthanasieLes drogues utilisées pour l’euthanasie peuvent provoquer <strong>la</strong> mort selon deuxmécanismes différents: l’hypoxie in<strong>du</strong>ite par les curarisants par exemple et <strong>la</strong>dépression des centres respiratoire et cardio-vascu<strong>la</strong>ire. Les méthodes doucesin<strong>du</strong>isant un minimum de souffrance et pro<strong>du</strong>isant d’abord l’état d’inconscienceavant <strong>la</strong> mort sont évidemment à privilégier. De ce point de vue, l’euthanasie peutse définir comme une anesthésie dépassée. L’usage des curarisants seuls estéthiquement inacceptable. (Voir aussi Folia Veterinaria 2007 n° 3)10.3.1 BarbituriquesLes effets des préparations reprises dans cette rubrique sont détaillés dans lechapitre consacré à l’usage des barbituriques en anesthésiologie. Les préparationsreprises ci-dessous ne peuvent être utilisées pour l’in<strong>du</strong>ction de l’anesthésievu <strong>la</strong> concentration en principe actif.LMR: les animaux euthanasiés sont impropres à <strong>la</strong> consommationDOLETHAL (Vétoquinol)pentobarbital sodique: 200 mg/mlsolution injectable iv, icardPosologie:Ca, Fe: 200 mg/1,5 kgf<strong>la</strong>con 100 ml, 250 mlR/psychNATRIUM PENTOBARBITAL 20% (Ke<strong>la</strong>Laboratoria)pentobarbital sodique: 200mg/mlsolution injectable iv, icardPosologie:Ca, Fe: 100 - 200 mg/kgf<strong>la</strong>con 100 mlR/psychRELEASE 300 mg/ml sol inj (WDT)pentobarbital sodique: 300 mg/mlsolution injectable iv, (icard sauf chez Av,intrapulmonale ou intrapéritonéale sauf chezEq, poneys, Bo, Su)Posologie:En fonction de l’espèce cibleLes animaux euthanasiés sont impropres à <strong>la</strong>consommationf<strong>la</strong>con 100 mlR/psych10.3.2 AssociationIndicationsT-61 ® est un médicament injectable destiné uniquement à l’euthanasie et necontenant pas de barbiturique mais un mé<strong>la</strong>nge de trois molécules actives.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 167PharmacodynamieL’embutramide est un narcotique à action centrale inhibant le système nerveuxcentral, principalement au niveau des centres respiratoires et circu<strong>la</strong>toires.L’io<strong>du</strong>re de mebenzonium exerce un effet curarisant déprimant les muscles striésy compris respiratoires. Enfin <strong>la</strong> tetracaïne, un anesthésique local inclus dans <strong>la</strong>préparation, permet selon <strong>la</strong> notice une injection indolore. Les effets cardiaquesne sont toutefois pas à exclure.PharmacocinétiqueIl est vivement conseillé d’utiliser ce médicament uniquement par voie intraveineuseou éventuellement par voie intracardiaque chez les animaux anesthésiés,car l’administration par une autre voie ne garantit pas de manière absolue quel’embutramide, responsable de <strong>la</strong> perte de conscience, agisse chronologiquementen premier lieu. Il est pourtant indispensable que cette dépression <strong>du</strong> systèmenerveux central précède le blocage neuromuscu<strong>la</strong>ire sous peine d’imposerune mort par asphyxie d’un animal conscient. Le respect scrupuleux des posologiesest capital de ce point de vue.Précautions particulières/Risques pour l’hommeCes pro<strong>du</strong>its étant également actifs chez l’homme, il convient de prendre toutesles mesures nécessaires pour éviter une auto-injection accidentelle.LMR: les animaux euthanasiés sont impropres à <strong>la</strong> consommation.T 61 (MSD A.H.)embutramide: 200 mg/mlio<strong>du</strong>re de mébézonium: 50 mg/mltétracaïne chlorhydrate: 5 mg/mlsolution injectable iv, icard, ipulmPosologie:Ca:- iv, icard: 0,3 ml/kg- ipulm:- (< 10 kg PV): 0,7 - 1,0 ml/kg- (> 10 kg PV): 10 - 20 ml/animalFe (ipulm):âgé de quelques jours: 1 ml/animal- (âge < 6 m): 3 ml/animal- (âge > 6 m): 5 ml/a,imal- (> 5 kg PV): 10 m/animalvison (ipulm): 0,5 - 1 m/animallEq, Bo (iv): 4 - 6 ml/50 kgautres (oiseau, animal de <strong>la</strong>boratoire) (ipulm):0,5 - 2 ml/animalLes animaux tués ne peuvent pas être destinésà <strong>la</strong> consommation humainef<strong>la</strong>con 50 mlR/10.4 Anesthésiques locauxIndicationsCes substances sont principalement utilisées après infiltration, avant des interventionschirurgicales, généralement après sédation mais également pour desprocédés d’anesthésie locale assurant l’analgésie (thérapeutique ou diagnostique)ou l’arrêt de l’activité motrice. Nombre de ces procédés ont été décrits demanière circonstanciée dans <strong>la</strong> littérature. Les indications peuvent varier selon<strong>la</strong> substance active et sa concentration. Alors que de nombreux anesthésiqueslocaux sont disponibles en médecine humaine, seules <strong>la</strong> procaïne et <strong>la</strong> lidocaïnesont enregistrées en Belgique pour usage vétérinaire. Pour prolonger l’action dessolutions, des substances vasoconstrictrices (telle que l’adrénaline) y sont parfoisajoutées.PharmacodynamieLes anesthésiques locaux sont des esters (procaïne, tétracaïne…) ou des amides(lidocaïne, mépivacaïne…). Leur puissance, leur <strong>du</strong>rée d’action, leur toxicité etleur vitesse de diffusion peuvent varier suivant <strong>la</strong> molécule considérée et l’espèceanimale. De manière générale, ces substances peuvent être subdivisées enpro<strong>du</strong>its à action courte (procaïne), à action moyenne (lidocaïne, mépivacaïne) et
16810 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEà action longue (bupivacaïne, ropivacaïne). L’effet inhibiteur atteint d’abord lesfibres <strong>du</strong> système nerveux autonome puis les fibres sensibles à <strong>la</strong> douleur, aufroid, au chaud, au toucher, et enfin les fibres motrices; et inversement lorsquel’action de l’anesthésique disparaît. Cet arrêt de <strong>la</strong> transmission nerveuse périphériqueprovient d’une inhibition des potentiels d’excitation <strong>du</strong> fait d’un blocagede l’ouverture des canaux sodium. L’un des avantages des anesthésiques locauxréside dans le fait que les effets systémiques sont souvent moins importants queceux des anesthésiques généraux.PharmacocinétiqueLes anesthésiques locaux sont rapidement résorbés et métabolisés. Les esters(procaïne, tétracaïne) sont métabolisés par les estérases p<strong>la</strong>smatiques et hépatiques.Les amides (lidocaïne, mépivacaïne) subissent quant à eux le métabolismehépatique. Tous les anesthésiques locaux sont excrétés par voie rénale aprèsmétabolisation. Les anesthésiques locaux sont souvent associés à un vasoconstricteur,comme l’adrénaline ou <strong>la</strong> noradrénaline, qui permet de diminuer <strong>la</strong> vitessed’absorption et de localiser le médicament au site d’injection, mais également deprolonger son action.Contre-indicationsMyasthenia gravis (procaïne), pathologies cardiaques, hypersensibilité vis-à-visdes anesthésiques locaux. Vu <strong>la</strong> possibilité de nécrose in<strong>du</strong>ite par l’incorporationd’agents vasoconstricteurs, ces associations ne peuvent pas être utilisées pourl’anesthésie des organes à circu<strong>la</strong>tion terminale comme les doigts, les oreilles, lepénis. Ces associations sont également à exclure pour les procédés d’anesthésieintraveineuse, et à éviter chez des animaux hyperten<strong>du</strong>s, hyperthyroïdiens, traitéspar des inhibiteurs de monoamine oxydase ou atteints d’arythmie.Effets indésirablesDes effets indésirables touchant le système cardio-vascu<strong>la</strong>ire, respiratoire et nerveuxpeuvent être observés, surtout si les anesthésiques locaux sont par erreuradministrés par voie intravascu<strong>la</strong>ire ou en cas de surdosage. Ces effets indésirablespeuvent aussi apparaître par suite de résorption excessive de <strong>la</strong> moléculeau niveau <strong>du</strong> site d’injection, surtout chez les jeunes animaux au poids corporelfaible. Au niveau cardio-vascu<strong>la</strong>ire, de <strong>la</strong> bradycardie, une diminution <strong>du</strong> débitcardiaque, des troubles de <strong>la</strong> con<strong>du</strong>ction cardiaque, de <strong>la</strong> vasoconstriction puisde <strong>la</strong> vasodi<strong>la</strong>tation peuvent être observés. Une hypotension marquée suit parfoisleur administration par voie épi<strong>du</strong>rale <strong>du</strong> fait de l’inhibition <strong>du</strong> tonus sympathique.Au niveau nerveux, de <strong>la</strong> sédation ou de l’excitation mais aussi des arrêts respiratoiresont été décrits. Des réactions allergiques sont possibles mais sont plus fréquentesavec les esters. Les réactions croisées entre les esters et les amides sontrares. Les conservateurs tels que les bisulfites peuvent aussi être responsables deréactions (pseudo-) allergiques.InteractionsLa procaïne ne peut pas être administrée simultanément à des sulfamidés, dontl’action est inhibée par l’acide para-aminobenzoïque, le métabolite de <strong>la</strong> procaïne.L’amiodarone augmente le taux p<strong>la</strong>smatique et l’effet pharmacologique de <strong>la</strong> procaïneet de <strong>la</strong> lidocaïne. Ces deux substances interagissent en renforçant mutuellementleur action ainsi que celle d’autres anti-arythmiques, avec, éventuellement,un effet inotrope négatif renforcé. La procaïne peut potentialiser ou prolonger l’actiondes bêta-bloquants, de <strong>la</strong> succinylcholine, des myore<strong>la</strong>xants curarisants, desanticholinergiques et des aminoglycosides. La procaïne inhibe l’action des inhibiteursde <strong>la</strong> cholinestérase tels que <strong>la</strong> néostigmine ou <strong>la</strong> pyridostigmine chez lespatients souffrant de myasthenia gravis. L’hyperkaliémie potentialise l’action de<strong>la</strong> procaïne alors que l’hypokaliémie a l’effet inverse. Tandis que <strong>la</strong> procaïne raccourcitl’action <strong>du</strong> phénobarbitural; <strong>la</strong> phénytoïne raccourcit celle de <strong>la</strong> procaïne.La cimétidine inhibe l’excrétion rénale de <strong>la</strong> procaïne ce qui peut con<strong>du</strong>ire à desconcentrations p<strong>la</strong>smatiques plus élevées et donc à accroître <strong>la</strong> toxicité potentiellede l’anesthésique. La perfusion sanguine ré<strong>du</strong>ite au niveau <strong>du</strong> foie contribueégalement à cet effet. La dose des anesthésiques injectables et vo<strong>la</strong>tils doit êtrediminuée lorsqu’ils sont administrés simultanément à <strong>la</strong> lidocaïne. L’associationde <strong>la</strong> lidocaïne et <strong>du</strong> propanolol ou <strong>du</strong> métoprolol augmente le risque d’apparitiond’extrasystoles (contrairement à l’aténolol). Des doses plus élevées de lidocaïnepeuvent prolonger les phases d’apnée in<strong>du</strong>ites par le chlorure de succinyle.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 169Précautions particulièresLes chats sont particulièrement sensibles aux effets de <strong>la</strong> procaïne et de <strong>la</strong> lidocaïnesur le système nerveux central.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’usage de <strong>la</strong> procaïne en obstétrique est considéré comme inoffensif chez leshumains et les animaux. Pour ce qui est de <strong>la</strong> lidocaïne, des études multigénérationnelleschez le rat n’ont pas démontré d’anomalies ni dans <strong>la</strong> repro<strong>du</strong>ction nichez les nouveau-nés al<strong>la</strong>ités.10.4.1 ProcaïneLMR procaïne: PROCAINE CHLORHYDRATE 4 % (VMD)procaïne chlorhydrate: 40 mg/mlsolution injectable sc, épidPosologie:- anesth locale:Eq, Bo, Su, Ov: 100 - 400 mg- anesth épid sacrée:veau: 100 - 200 mgjeune bovin: 150 - 240 mgvache, taureau: 200 - 300 mgOv: 60 - 100 mg- anesth épid haute:veau: 300 mgjeune bovin: 600 mgtaureau: 800 mgOv: max 300 mgSu: 20 mg/4,5 kg PV- anesth de <strong>la</strong> con<strong>du</strong>ction nerveuse:Eq, Bo, Su, Ov: 200 - 400 mgViande: 0 j, Lait: 0 jf<strong>la</strong>con 250 mlR/10.4.2 Associations avec un vasoconstricteurLMR lidocaïne + epinéphrine(adrénaline): LIGNOCAINE HCL 2% + ADRENALINE TARTRATE(Ke<strong>la</strong> Laboratoria)lidocaïne chlorhydrate: 20 mg/m<strong>la</strong>drénaline tartrate: 0,036 mg/mlsolution injectable im, sc, épidPosologie:anesth épid:Ca, Fe: 1 ml/5 kganesth par infiltration:Eq: max 10 - 100 ml/animalCa: max 0,5 - 15 ml/animalFe: max 0,5 - 5 ml/animalViande et abats: 0 jf<strong>la</strong>con 100 mlR/LMR procaïne + epinéphrine(adrénaline): PROCAINE HCL 4% + ADRENALINE (Ke<strong>la</strong>Laboratoria)procaïne chlorhydrate: 40 mg/m<strong>la</strong>drénaline tartrate: 0,036 mg/mlsolution injectable épid, im, scPosologie:- anesth par infiltration:Eq, Bo, Su: max 600 mgOv: max 400 mg- anesth épi<strong>du</strong>rale:Bo: 40 mg/100 kg PV- anesth de <strong>la</strong> con<strong>du</strong>ction nerveuse:Eq, Bo, Su, Ov: 200 - 400 mgRemarque: Le temps d’attente pour le <strong>la</strong>it n’estpas disponibleViande et abats: Eq, Bo, Su, Ov: 3 jf<strong>la</strong>con 250 mlR/
17010 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEPROCAINE HCL 4% + ADRENALINE (VMD)procaïne chlorhydrate: 40 mg/mlépinéphrine bitartrate: 0,036 mgsolution injectable épid, im, scPosologie:- anesth locale:Eq, Bo, Su, Ov: 100 - 400 mg- anesth épid sacrée:veau: 200 mgjeune bovin: 240 mgvache, taureau: 300 mgOv: 60 - 100 mg- anesth épid haute:veau: 400 - 1350 mgjeune bovin: 750 - 1800 mgvache: 1000 - 2250 mgOv: max 300 mgSu: 20 mg/4,5 kg PV, max 400 mg- anesth de <strong>la</strong> con<strong>du</strong>ction nerveuse:Eq, Bo, Su, Ov: 200 - 400 mgViande: 0 j, Lait: 0 jf<strong>la</strong>con 250 mlR/10.5 NeuroleptiquesLes neuroleptiques ou antipsychotiques, aussi appelés tranquillisants majeurs,ont été regroupés en différentes familles. Seules les phénothiazines et les butyrophénonessont utilisées en médecine vétérinaire.IndicationsEn médecine humaine, les neuroleptiques sont indiqués dans le traitement despsychoses et dans certains syndromes comportant des hallucinations ou del’agitation psychomotrice. En médecine vétérinaire, ces substances sont surtoututilisées pour leurs propriétés sédatives et antiémétiques, notamment dans lecas particulier <strong>du</strong> mal des transports, et leurs propriétés antihistaminiques. Lasédation est lente à apparaître, surtout après une administration orale. Elle estsusceptible d’être interrompue de manière abrupte, par exemple par des stimu<strong>la</strong>tionsauditives, et elle est de qualité moyenne. L’analgésie est absente. Ces substancespeuvent aussi être utiles pour le traitement de l’agressivité et l’inhibitiondes réflexes conditionnés. Les neuroleptiques diminuent les arythmies in<strong>du</strong>itespar l’adrénaline, ce qui fait supposer qu’ils protègent le myocarde.PharmacodynamieLa pharmacologie de ces substances est assez complexe. L’action antagonistevis-à-vis des récepteurs dopaminergiques D2 et des récepteurs sérotoninergiquesrend compte de l’indifférence psychomotrice, de <strong>la</strong> ré<strong>du</strong>ction de l’agressivité etdes troubles psychotiques ainsi que de l’effet antiémétique. La sédation est plutôt<strong>la</strong> résultante des effets antagonistes au niveau des récepteurs alpha-1 adrénergiqueset histaminergiques.PharmacocinétiqueCes substances sont actives par voie parentérale et orale bien que dans ce cas,l’action soit ralentie. Elles subissent un métabolisme hépatique variable selon lesmolécules et les espèces. Une stimu<strong>la</strong>tion <strong>du</strong> système microsomal a été observée.Ces substances sont excrétées par voie rénale.Contre-indicationsLes neuroleptiques ne sont pas des anti-épileptiques, au contraire, ils facilitentl’épilepsie. L’administration prolongée peut con<strong>du</strong>ire à des dyskinésies irréversiblesse manifestant par des mouvements anormaux.Effets indésirablesLes effets indésirables nombreux sont en partie <strong>la</strong> conséquence d’une action inhibitricesur les récepteurs dopaminergiques centraux qui, selon leur localisation,jouent des rôles très variés. Ainsi, les neuroleptiques peuvent in<strong>du</strong>ire des symptômesextrapyramidaux caractérisés par des tremblements, de <strong>la</strong> rigidité et del’akinésie. De l’hyperkinésie est parfois constatée. De <strong>la</strong> ga<strong>la</strong>ctorrhée résultantd’une hyperpro<strong>la</strong>ctinémie est aussi décrite. Une hypotension prolongée, éventuellementcompensée par de <strong>la</strong> tachycardie, peut être observée suite à <strong>la</strong> dépression
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 171des réflexes vasomoteurs contrôlés par l’hypotha<strong>la</strong>mus et le tronc cérébral, aublocage des récepteurs alpha-1 (vasodi<strong>la</strong>tation), à l’effet direct sur les muscleslisses vascu<strong>la</strong>ires périphériques et à une dépression <strong>du</strong> myocarde. L’action inhibitricevis-à-vis des récepteurs muscariniques explique certains effets indésirablescomme <strong>la</strong> sécheresse de <strong>la</strong> bouche et <strong>la</strong> constipation.InteractionsLes effets sédatifs des autres substances agissant en ce sens sur le systèmenerveux central sont amplifiés par les neuroleptiques.Repro<strong>du</strong>ction et <strong>la</strong>ctationDes effets tératogènes ont été décrits.10.5.1 PhénothiazinesLes phénothiazines les plus utilisées en médecine vétérinaire sont l’acépromazineet <strong>la</strong> propionylpromazine. Seule l’acépromazine est disponible en Belgique.10.5.1.1 Acépromazineatteints de défail<strong>la</strong>nces hépatiques, dema<strong>la</strong>dies cardiaques ou débilités. IlIndicationsfaut aussi signaler que leur utilisationMême si elle est active chez toutes chez des animaux sujets à des crisesles espèces cibles, l’acépromazine épileptiformes est soumise à cautionet doit être évitée lors d’atteintesest uniquement commercialisée enBelgique pour in<strong>du</strong>ire <strong>la</strong> sédation (sans nerveuses comme les méningites,propriétés analgésiques) chez le chien les encéphalites et l’intoxication paret le chat.des convulsivants comme <strong>la</strong> strychnine.Certaines races canines tellesPharmacodynamieEn raison de leur action sympathicolytique(alpha-1-antagoniste), cette semblent plus sensibles aux effets desque le boxer ou encore le greyhoundfamille engendre, outre les effets déjà phénothiazines.signalés, des effets cardio-vascu<strong>la</strong>ires Effets indésirablesaboutissant à une vasodi<strong>la</strong>tation périphériqueet une hypotension concotoireprovoque une diminution de <strong>la</strong>Leur influence sur <strong>la</strong> sphère respiramitante.Cette vasodi<strong>la</strong>tation des fréquence respiratoire, sans effetsvaisseaux cutanés provoque aussi une majeurs sur les différents paramètresperte de calories pouvant con<strong>du</strong>ire à sanguins. L’inhibition des récepteursune chute de <strong>la</strong> température corporelle. alpha-1 périphériques in<strong>du</strong>it une accumu<strong>la</strong>tionde sang dans <strong>la</strong> rate seLa bradycardie est <strong>du</strong>e au blocagedes récepteurs dopaminergiques. Elle tra<strong>du</strong>isant par une diminution de l’hématocritechez le cheval et le chien. Unest suivie d’une tachycardie -liée auxeffets anti-muscariniques- et renforcée pro<strong>la</strong>psus <strong>du</strong> pénis peut être observépar un réflexe initié par l’hypotension. chez l’étalon suite à <strong>la</strong> vasodi<strong>la</strong>tationLes phénothiazines peuvent aussi corrigerles troubles <strong>du</strong> rythme, parfois lysie permanente peut en découler. Unin<strong>du</strong>ite. Si celui-ci per<strong>du</strong>re, une para-in<strong>du</strong>its par d’autres molécules comme allongement de l’intervalle QT est décritet des torsades de pointes peuventl’halothane ou les catécho<strong>la</strong>mines.Pharmacocinétiquesurvenir particulièrement en combinaisonavec certains anti-histaminiques.L’acépromazine a un volume de distributionélevé et se lie très facilement En cas de surdosage accidentel, uneaux protéines p<strong>la</strong>smatiques. L’effet hypotension sévère apparaît. Un traitementsymptomatique peut alors êtreclinique optimal est re<strong>la</strong>tivement lentà apparaître (après IV, environ 15 min) instauré, une fluidothérapie intensivemais <strong>du</strong>re longtemps (plus de 8 h). est primordiale. L’adrénaline n’étantAprès métabolisation dans le foie, les pas conseillée, seules <strong>la</strong> noradrénaline,l’éphédrine et <strong>la</strong> phényléphrinemétabolites sont excrétés via l’urine.Contre-indications(activité bêta2 minimale, principalementstimu<strong>la</strong>tion alpha1) peuvent êtreToutes les formes d’hypovolémie etd’état de choc constituent les contreindicationsles plus importantes. Une traitées avec des barbituriques ou desutilisées. Les convulsions peuvent êtreattention particulière doit aussi être accordéelors de l’utilisation de cette fa-benzodiazépines.mille de molécules chez des indivi<strong>du</strong>s
17210 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEInteractionsL’activité des organophophorés et de<strong>la</strong> procaïne est renforcée. D’autressubstances exerçant des effets dépresseurssur le SNC (barbituriques,anesthésiques, etc) renforcent l’actionde l’acépromazine. Des médicamentsutilisés contre <strong>la</strong> diarrhée (pectine,salicy<strong>la</strong>tes de bismuth) et les antiacidespeuvent diminuer <strong>la</strong> résorptionde l’acépromazine administrée oralement.Les phénothiazines bloquentles récepteurs alpha-1-adrénergiques;une administration simultanée avecl’adrénaline peut engendrer une activitébêta accrue accompagnée devasodi<strong>la</strong>tation et d’une augmentation<strong>du</strong> rythme cardiaque. Les concentrationsp<strong>la</strong>smatiques <strong>du</strong> propranolol(bêta-bloquant) et des phénothiazinesaugmentent lorsqu’ils sont administréssimultanément. Les propriétés hypotensivesdes phénothiazines sont renforcéespar les opiacés.Repro<strong>du</strong>ction et <strong>la</strong>ctationMême si l’innocuité des phénothiazinesadministrées aux animaux gestants oual<strong>la</strong>itants n’a pas été démontrée, cesmolécules sont considérées commere<strong>la</strong>tivement inoffensives.LMR acépromazine: ACEPE compr (Eurovet)acépromazine (maléate): 10 mgcomprimé poPosologie:Ca, Fe:1 - 3 mg/kg (avant alimentation)compr 10 x 2R/KALMIVET (Vétoquinol)acépromazine (maléate): 12,5 mg/comprcomprimé poPosologie:Ca: 1,25 - 5 mg/kgFe: 2,5 mg/kgcompr 2 x 104 x 10R/PLACIVET (Ke<strong>la</strong> <strong>la</strong>boratoria)acépromazine (maléate): 20 mg/mlsolution injectable im, ivPosologie:sédation: Ca: 0,5 mg/kg iv ou0,5 - 1 mg/kg imFe: 1 - 2 mg/kg imf<strong>la</strong>con 10 mlR/TRANQUILINE 35 mg/ml (Floris VeterinairePro<strong>du</strong>cten)acépromazine (maléate): 35 mg/mlgel poPosologie:Ca (PV > 17,5 kg):sédation: 1 - 2 mg/kgprémédication: 3 mg/kgf<strong>la</strong>con 10 mlR/10.5.2 Dérivés de <strong>la</strong> butyrophénone10.5.2.1 AzapéroneIndicationsL’azapérone est utilisée chez le porcpour contrôler les effets <strong>du</strong> stress etl’agressivité. Les posologies utiliséesvarient suivant l’indication.PharmacodynamieL’azapérone a des effets anti-adrénergiques,anticholinergiques, antihistaminergiqueset antidopaminergiques.A l’instar des autres neuroleptiques,l’azapérone bloque les récepteurs à <strong>la</strong>dopamine dans le SNC, inhibe <strong>la</strong> libérationet augmente le métabolisme de<strong>la</strong> dopamine. La sédation est moinsprononcée que celle provoquée parles phénothiazines. L’azapérone n’apas d’activité analgésique. Les butyrophénonessont aussi de puissantsantiémétiques agissant directementsur l’aire <strong>du</strong> vomissement (CTZ).PharmacocinétiqueRésorbée rapidement après une administrationIM et dans une moindremesure après administration SC, l’azapéroneest métabolisée dans le foie etexcrétée principalement via l’urine. La<strong>du</strong>rée d’action est de 2 à 3 h chez lesjeunes animaux et de 3 à 4 h chez lesanimaux plus âgés.Contre-indications- Administration par voie intraveineuse(peut provoquer des phasesd’excitation).- Administration dans un environnementfroid (col<strong>la</strong>psuscardio-vascu<strong>la</strong>ire).Effets indésirablesDe l’excitation apparaît parfois aprèsune stimu<strong>la</strong>tion externe peu après l’injection.Des effets cardio-vascu<strong>la</strong>irescaractérisés par une chute de <strong>la</strong> pressionartérielle peuvent être observés etsont probablement <strong>du</strong>s aux propriétésalpha-1 antagonistes. Le rythme etle débit cardiaque ne semblent quepeu modifiés. Les effets sur le systèmerespiratoire sont peu importants.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 173Le dérèglement de <strong>la</strong> régu<strong>la</strong>tion thermiquecentrale, associé à <strong>la</strong> vasodi<strong>la</strong>tation,entraîne une baisse de <strong>la</strong>température corporelle.InteractionsUn effet additif apparaît lorsque l’azapéroneest administrée simultanémentavec d’autres substances exerçant uneffet dépresseur sur le SNC (barbituriques,anesthésiques, …).Précautions particulièresIl faut veiller à ce que l’injection soitfaite strictement par voie intramuscu<strong>la</strong>ireet non dans le tissu graisseuxce qui diminuerait l’efficacité <strong>du</strong> traitement.De plus, il faut veiller à ceque les animaux traités soient isolésafin d’obtenir une sédation de bonnequalité mais également afin d’éviter lecannibalisme.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe pro<strong>du</strong>it peut être administré à desdoses normales aux animaux gestantsou al<strong>la</strong>itants. Lorsque l’azapérone estutilisée pendant une césarienne, lesporcelets sont somnolents, mais il y apeu de dépression respiratoire. L’effetsédatif sur <strong>la</strong> truie peut <strong>du</strong>rer assezlongtemps, ce qui empêche les porceletsde téter ou entraîne l’écrasementde ceux-ci par <strong>la</strong> mère.LMR azapérone: STRESNIL (Eli Lilly)azapérone: 40 mg/mlsolution injectable imPosologie:Su:stress: 0,4 mg/kgtransport porcelet (âge de sevrage):0,4 - 2 mg/kg)transport verrat: 1 mg/kgobstétrique: 2 mg/kgagressivité: 2 mg/kgpréméd: 1 - 2 mg/kgViande: 16 jampoule 100 mlR/10.6 BenzodiazépinesLes benzodiazépines, encore appelées tranquillisants mineurs, contrairement auxneuroleptiques qualifiés de majeurs, sont couramment utilisées en médecine vétérinaire,le plus souvent en ayant recours aux médicaments à usage humain (diazépam,midazo<strong>la</strong>m, climazo<strong>la</strong>m) puisqu’il n’existe qu’une seule préparation à usagevétérinaire contenant une benzodiazépine en association avec un anesthésiquedissociatif sur le marché belge (zo<strong>la</strong>zépam + tilétamine, voir chapitre 10.1.2.1). Lessolutions à base de diazépam contiennent généralement <strong>du</strong> propylène glycol etne peuvent donc pas être mé<strong>la</strong>ngées à des solutions aqueuses. Les benzodiazépinespossèdent des propriétés anxiolytique, sédative, hypnotique, anti-convulsivanteet myore<strong>la</strong>xante. Chez l’homme, une amnésie réversible peut être observée.La nature et les effets obtenus dépendent de <strong>la</strong> molécule, de l’espèce animale etde <strong>la</strong> dose administrée. La très faible toxicité des benzodiazépines les distinguedes autres sédatifs. Leur c<strong>la</strong>ssification se base sur les mécanismes d’action desmolécules, conditionnant leurs effets pharmacologiques et toxiques. Un assezgrand nombre de benzodiazépines existent actuellement, différant entre elles parleur biodisponibilité, leur posologie, leurs indications, leur puissance et leur <strong>du</strong>réed’action. L’extrapo<strong>la</strong>tion des indications et des posologies d’une espèce à l’autren’est pas recommandée en absence de données scientifiques validées.IndicationsEn médecine vétérinaire, les benzodiazépines sont couramment utilisées au coursde <strong>la</strong> prémédication de l’anesthésie <strong>du</strong> fait de leur effet synergique avec les anesthésiqueset toute substance dépressive <strong>du</strong> système nerveux central en général.En outre, certaines d’entre elles sont utilisées comme orexigène dans le cadre <strong>du</strong>traitement symptomatique des anorexies chez certaines espèces comme le chatet le <strong>la</strong>pin ainsi que lors <strong>du</strong> traitement d’urgence de certains syndromes convulsifsou d’épilepsie. L’effet myore<strong>la</strong>xant de certaines molécules peut aussi êtrerecherché, notamment pour éviter l’hypertonie muscu<strong>la</strong>ire liée aux anesthésiquesdissociatifs.PharmacodynamieLes benzodiazépines agissent sur les récepteurs spécifiques aux benzodiazépines,dans le cerveau et <strong>la</strong> moelle épinière. Les effets anxiolytique et myore<strong>la</strong>xantsont dûs à <strong>la</strong> libération accrue de glycine, un neurotransmetteur inhibiteur.L’action anticonvulsivante et anxiolytique des benzodiazépines s’explique par leurmode d’action qui repose sur leur capacité à se lier aux récepteurs GABA et à
17410 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEaugmenter l’affinité de ce dernier pour ce neuromédiateur. L’acide gamma-aminobutyrique(GABA) augmente le transport d’ion chlore vers le milieu intracellu<strong>la</strong>ire,in<strong>du</strong>isant une hyperpo<strong>la</strong>risation de celui-ci et rendant in fine <strong>la</strong> cellule réfractaireà certains stimuli. L’existence de récepteurs spécifiques aux benzodiazépines apermis <strong>la</strong> mise au point d’antagonistes spécifiques appelés flumazénil (Anexate®,Flumazenil B. Braun®, médicaments à usage humain, usage hospitalier) et sarmazénil.Des doses cliniques in<strong>du</strong>isent une myore<strong>la</strong>xation très nette, <strong>du</strong>e à l’interactionau niveau des inter-neurones de <strong>la</strong> moelle épinière.PharmacocinétiquePratiquement, ces molécules peuvent, suivant <strong>la</strong> forme galénique et/ou le médicament,être adminsitrées par voie orale, IM ou IV. Il est préférable de ne pas administrerles solutions non aqueuses par voie IM en raison des réactions tissu<strong>la</strong>ireséventuelles. Par voie orale, <strong>la</strong> biodisponibilité des benzodiazépines est importante.Les benzodiazépines se lient facilement aux protéines et sont métabolisées(par déméthy<strong>la</strong>tion et hydroxy<strong>la</strong>tion) en métabolites actifs, ce qui expliqueles effets prolongés de certaines molécules. Les métabolites sont majoritairementexcrétés par les urines, partiellement par les fèces. Une attention particulière doitêtre apportée au schéma posologique en cas d’insuffisance hépatique ou rénale.Un recyc<strong>la</strong>ge entérohépatique pourrait expliquer <strong>la</strong> réapparition des effets sédatifsaprès 6 à 8 heures. Le midazo<strong>la</strong>m a une demi-vie plus courte que le diazépam, ilest également moins cumu<strong>la</strong>tif.Effets indésirablesLes effets cardio-vascu<strong>la</strong>ires et respiratoires sont habituellement faibles mais présents,rendant cette c<strong>la</strong>sse pharmacologique re<strong>la</strong>tivement sûre sauf chez des animauxdébilités. En effet, excepté une vasodi<strong>la</strong>tation et une hypotension légères,aucune autre manifestation majeure n’est habituellement décrite. Des troublescardiaques (arythmie, dépression) peuvent cependant apparaître après administrationIV de certaines formu<strong>la</strong>tions contenant une solution à base de propylène.Une trombophlébite est parfois observée après l’injection qui peut être douloureuse.Il est préférable de ne pas administrer les solutions à base de propylènepar voie IM en raison des réactions tissu<strong>la</strong>ires éventuelles. L’administration IV debenzodiazépines en monothérapie peut provoquer un état d’excitation ainsi quedes changements de comportement chez les petits animaux de compagnie. Chezle cheval, elle in<strong>du</strong>it un affaiblissement muscu<strong>la</strong>ire qui pourrait expliquer les réactionsde panique observées chez cette espèce. En cas de surdosage accidentel,le flumazénil (Anexate®, Flumazenil B. Braun®, médicaments à usage humain,usage hospitalier) peut être administré en association avec une thérapie de soutienadéquate. Des symptômes de sevrage sont bien connus chez l’homme et enphase expérimentale chez les singes. Aucune donnée n’est disponible concernantcet effet secondaire chez les animaux de compagnie.InteractionsLes benzodiazépines prolongent les effets de <strong>la</strong> plupart des anesthésiques. Lepentobarbital accentue l’affinité <strong>du</strong> diazépam pour les récepteurs aux benzodiazépines.L’érythromycine prolonge et renforce les effets <strong>du</strong> midazo<strong>la</strong>m.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes benzodiazépines traversant <strong>la</strong> barrière p<strong>la</strong>centaire, les nouveau-nés sont euxaussi sous sédation.10.6.1 Zo<strong>la</strong>zépamLMR zo<strong>la</strong>zépam + tilétamine: Voir chapitre 10.1.2.1.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 17510.7 Les agonistes alpha-2-adrénergiques et leursantagonistes10.7.1 Les agonistes alpha-2-adrénergiquesLes agonistes des récepteurs adrénergiques de type alpha-2 sont des substancescouramment utilisées en médecine vétérinaire et plus rarement administrées enmédecine humaine. Différentes molécules dont <strong>la</strong> détomidine, <strong>la</strong> médétomidine,<strong>la</strong> romifidine et <strong>la</strong> xy<strong>la</strong>zine sont disponibles.IndicationsLeurs applications cliniques reposent sur une sédation très profonde, une myore<strong>la</strong>xationtrès marquée et une analgésie viscérale de très bonne qualité. Ils in<strong>du</strong>isentégalement une inhibition de <strong>la</strong> spasticité intestinale et une légère formed’anxiolyse. Ils sont administrés pour des interventions sous sédation ou commeprémédication pour une anesthésie générale, auquel cas <strong>la</strong> dose d’anesthésiquediminue nettement.PharmacodynamieLes agonistes alpha-2-adrénergiques ont une affinité spécifique pour les récepteursalpha-2 adrénergiques, empêchant notamment <strong>la</strong> libération de noradrénalinedans <strong>la</strong> synapse <strong>du</strong> fait de l’activation d’un rétrocontrôle négatif exercé parce type de récepteurs au niveau pré-synaptique dans <strong>la</strong> synapse adrénergique.La stimu<strong>la</strong>tion des récepteurs post-synaptiques con<strong>du</strong>it à des perturbations fonctionnellesde nombreux systèmes. L’affinité différentielle des molécules mises surle marché pour les récepteurs alpha-2-adrénergiques détermine leur puissance indivi<strong>du</strong>elleet, par conséquent, les doses utilisées en clinique. Par exemple, <strong>la</strong> puissancemoindre de <strong>la</strong> xy<strong>la</strong>zine par rapport à celle de <strong>la</strong> médétomidine explique lesdifférences de posologies majeures entre ces deux principes actifs. Le degré despécificité, mesuré par le rapport d’affinité pour les récepteurs alpha-1 et alpha-2varie aussi selon les molécules. La médétomidine est un mé<strong>la</strong>nge racémique; <strong>la</strong>forme « dextrogyre » étant <strong>la</strong> plus active. Les divers signes cliniques ainsi que ledegré de sensibilité différent selon l’espèce s’expliquent en partie par <strong>la</strong> répartitionpré- et post-synaptique, centrale et périphérique des récepteurs chez lesdiverses espèces et par l’affinité variable des molécules. Ainsi, les ruminants sont,en général, très sensibles à ce type de substances, alors que les porcs sont plutôtrésistants. Des antagonistes alpha-2 spécifiques sont disponibles (atipamézole,voir chapitre 10.7.2.). La sédation est provoquée par stimu<strong>la</strong>tion des récepteursalpha-2 dans le locus coerulus ; l’analgésie et <strong>la</strong> myore<strong>la</strong>xation sont in<strong>du</strong>ites parl’action sur des récepteurs centraux, spinaux et périphériques. Une administrationépi<strong>du</strong>rale est également possible et in<strong>du</strong>it une analgésie de l’arrière-train, longueet de bonne qualité et accompagnée d’effets systémiques moins marqués.PharmacocinétiqueLes agonistes alpha-2 sont principalement administrés par voie parentérale, <strong>la</strong>voie IV in<strong>du</strong>isant les effets les plus rapides. Ces molécules sont métabolisées parle foie et éliminées par voie rénale.Contre-indicationsEtant donné leur mécanisme d’action, l’usage simultané avec des sympaticomimétiquestels que l’adrénaline et <strong>la</strong> noradrénaline, n’est pas conseillé. Cessubstances devraient être utilisées chez des animaux en bonne santé, vu les effetsindésirables importants. La décision de les utiliser chez des animaux dont l’état desanté général est mauvais, doit toujours faire l’objet d’une évaluation <strong>du</strong> rapportbénéfice/risque. Ces pro<strong>du</strong>its ne doivent pas être administrés aux animaux souffrantd’une hyperglycémie connue (diabète), de ma<strong>la</strong>dies cardiaques sévères oud’une obstruction au niveau <strong>du</strong> système urinaire (diurèse accrue avec risque derupture vésicale). Chez les animaux souffrant d’une hypertension connue ou d’unedégradation sévère des vaisseaux sanguins, l’hypertension initiale peut in<strong>du</strong>iredes complications (rupture des vaisseaux sanguins).Effets indésirablesLes agonistes alpha-2-adrénergiques provoquent <strong>la</strong> contraction des sphinctersdigestifs et une re<strong>la</strong>xation de <strong>la</strong> muscu<strong>la</strong>ture lisse intestinale, engendrant ainsi
17610 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEune paralysie temporaire de ce système (parfois suivi d’une courte période dediarrhée) et <strong>du</strong> tympanisme chez les herbivores. Il est conseillé de mettre en p<strong>la</strong>ceune période adéquate de jeûne après l’administration de ces pro<strong>du</strong>its, afin d’éviterdes obstructions de l’œsophage ou des coliques chez le cheval. Ils ont une actionémétique chez les carnivores, principalement chez les félins, et provoquent del’hyperglycémie, généralement sans glycosurie, en inhibant <strong>la</strong> pro<strong>du</strong>ction d’insulinepar les cellules bêta <strong>du</strong> pancréas. L’inhibition de l’hormone antidiurétique apour résultat une augmentation de <strong>la</strong> diurèse et <strong>la</strong> pro<strong>du</strong>ction d’une urine fortementdiluée chez toutes les espèces. Les agonistes alpha-2 provoquent descontractions utérines chez les grands espèces animales domestiques, aussi bienchez les animaux non gestants que gestants. Dans ce dernier cas, des avortementssont possibles. Une hypothermie peut être observée, <strong>du</strong>e à une actiondirecte sur le centre de <strong>la</strong> thermorégu<strong>la</strong>tion. Si l’animal est p<strong>la</strong>cé dans un endroitchaud, sa température interne risque d’augmenter dangereusement. Une altérationdes échanges gazeux aboutissant à une diminution de <strong>la</strong> pression partielle enoxygène, variable selon les espèces, peut être in<strong>du</strong>ite. Chez les petits ruminants,un col<strong>la</strong>psus pulmonaire et de l’œdème ont été décrits après administration IV.L’administration intraveineuse provoque une vasoconstriction intense entraînantune hypertension, variable selon les espèces, liée à <strong>la</strong> stimu<strong>la</strong>tion des récepteursvascu<strong>la</strong>ires périphériques. Elle est rapidement remp<strong>la</strong>cée par une hypotensionrésultant <strong>du</strong> renforcement <strong>du</strong> tonus vagal d’origine centrale et de <strong>la</strong> bradycardie.Cette dernière peut être antagonisée par des parasympathicolytiques (atropine,glycopyrro<strong>la</strong>te), mais l’hypertension est ainsi prolongée. Chez le chien, <strong>la</strong> xy<strong>la</strong>zinerenforce <strong>la</strong> sensibilité <strong>du</strong> myocarde aux catécho<strong>la</strong>mines. Les agonistes alpha-2adrénergiques passant <strong>la</strong> barrière p<strong>la</strong>centaire, les fœtus ou les nouveau-nés sontaussi sous sédation. L’altération de <strong>la</strong> perfusion de l’utérus gestant peut con<strong>du</strong>ireà une diminution de l’apport en oxygène chez les fœtus. Chez le cheval, des réactionsde défense sont parfois observées lorsque l’arrière-train est touché, sansdoute en raison d’une sensibilité accrue de <strong>la</strong> peau. L’usage simultané d’opiacésatténue quelque peu celle-ci. En cas de surdosage ou d’intolérance, ces effetspeuvent être inhibés par l’administration d’antagonistes alpha-2-adrénergiquescomme <strong>la</strong> yohimbine (usage humain), <strong>la</strong> to<strong>la</strong>zoline (non disponible en Belgique) oul’atipamézole (voir chapitre 10.7.2) qui a, par ailleurs, une action plus longue que<strong>la</strong> médétomidine.InteractionsL’usage simultané de <strong>la</strong> xy<strong>la</strong>zine avec l’acépromazine augmente le risque d’hypotension.Un effet additif peut être observé lors d’un usage simultané avec d’autresdépresseurs <strong>du</strong> SNC (barbituriques, anesthésiques, …). L’usage simultané parvoie IV d’agonistes alpha-2 avec des sulfamidés peut in<strong>du</strong>ire un col<strong>la</strong>psus cardiovascu<strong>la</strong>irefatal chez le cheval. La combinaison de propofol et de médétomidinepeut causer de l’hypoxémie.Précautions particulières/Risques pour l’hommeLes bovinés, les ovinés et les caprinés sont particulièrement sensibles à l’actionde ces substances. Ces pro<strong>du</strong>its sont également actifs chez l’homme. Voir aussiFolia Veterinaria 2009 n°3.Les agonistes alpha-2 ne peuvent être administrés que par le vétérinaire conformémentà l’art. 12 de <strong>la</strong> loi sur l’exercice de <strong>la</strong> médecine vétérinaire <strong>du</strong> 28/8/1991.Les agonistes alpha-2 ne peuvent pas être fournis au responsable des animaux etne peuvent en aucun cas être présents dans <strong>la</strong> réserve de l’éleveur responsable.Repro<strong>du</strong>ction et <strong>la</strong>ctationVu les effets indésirables rapportés, l’administration de ces pro<strong>du</strong>its <strong>du</strong>rant <strong>la</strong> gestationou <strong>la</strong> <strong>la</strong>ctation requiert toute <strong>la</strong> prudence nécessaire.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 17710.7.1.1 DétomidineLMR détomidine: DETOGESIC 10 mg/ml sol inj chevaux (Vetcare Oy)détomidine chlorhydrate: 10 mg/mlsolution injectable ivPosologie:Eq:sédation légère: 10 - 20 mcg/kgsédation moyenne: 20 - 40 mcg/kgeffet prolongé: 40 - 80 mcg/kgpréméd: 10 - 30 mcg/kgViande et abats: 2 j, Lait: 12 hf<strong>la</strong>con 10 mlR/DETONERVIN 10 mg/ml (Le Vet)détomidine chlorhydrate: 10 mg/mlsolution injectable im, ivPosologie:Eq, Bo:sédation légère:10-20 mcg/kgsédation modérée: 20-40 mcg/kgsédation ou analgésie prolongée: 80 mcg/kgViande: 2 j, Lait: 12 hf<strong>la</strong>con 5 ml, 20 mlR/DOMIDINE 10 mg/ml (Eurovet A.H.)hydrochlorure de détomidine: 10 mg/mlsolution injectable iv, imPosologie:Eq, Bo:- sédation légère: 10 - 20 mcg/kg- sédation modérée: 20 - 40 mcg/kgViande: Eq, Bo: 2 j, Lait: Eq, Bo: 12 hf<strong>la</strong>con 5 ml, 10 ml, 20 mlR/DOMOSEDAN (Orion Corp)hydrochlorure de détomidine: 10 mg/mlsolution injectable im, ivPosologie:selon l’effet désiré:Eq, Bo: 10 - 80 mcg/kgViande: 24 h, Lait: 0 jf<strong>la</strong>con 5 mlR/DOMOSEDAN gel 7,6 mg/ml (Orion Corp)chlorhydrate de détomidine: 7,6 mg/mlgel par voie sublingualePosologie:Eq: 40 mcg/kgViande et abats: 0 j, Lait: 0 hseringue 1 x 3,0 mlR/MEDESEDAN 10 mg/ml (CP-Pharma)détomidine chlorhydrate: 10 mg/mlsolution injectable im, ivPosologie:Eq, Bo: sédation légère: 10 - 20 mcg/kgsédation modérée: 20 - 40 mcg/kgsédation prolongée + analgésie:40 - 80 mcg/kgpréméd: 10 - 30 mcg/kgViande et abats: Eq, Bo: 2 j, Lait : 12 hf<strong>la</strong>con 5 ml, 20 mlR/10.7.1.2 DexmédétomidineLMR dexmédétomidine: DEXDOMITOR 0,1 mg/ml (Orion Corporation)dexmédétomidine hydrochloride: 0,1 mg/mlsolution injectable im, ivPosologie:Ca (> 6 m): 375 mcg/m2 de surf corp (iv),500 mcg/m2 de surf corp (im)Fe (> 5 m): 40 mcg/kg (im)f<strong>la</strong>con 15 mlR/DEXDOMITOR 0,5 mg/ml (Orion Corporation)dexmédétomidine hydrochloride: 0,5 mg/mlsolution injectable im, ivPosologie:Ca ( > 6 m): 375 mcg/m2 de surf corp (iv),500 mcg/m2 de surf corp (im)Fe (> 5 m): 40 mcg/kg (im)f<strong>la</strong>con 10 mlR/10.7.1.3 MédétomidineLMR médétomidine: DOMITOR (Orion Corp)médétomidine chlorhydrate: 1 mg/mlsolution injectable im, iv (Ca), im, iv, sc (Fe)Posologie:Ca:- tranquillisation: 10 - 40 mcg/kg- sédation + analgésie: 40 - 80 mcg/kg- anesth (< 1 h):20 - 40 mcg/kg + 8 - 10 mg de kétamine/kg50 - 60 mcg/kg + 2 - 4 mg de kétamine/kgprolonger l’anesth avec 2 - 4 mg dekétamine/kg- anesth (> 1 h): diminuer dose de l’anesthésiquede 30 - 50 %10 - 40 mcg/kg + halothane10 mcg/kg + pentobarbitalFe:- tranquillisation ou sédation:80 - 150 mcg/kg- anesth:80 mcg/kg + 5 - 7,5 mg de kétamine/kgf<strong>la</strong>con 10 mlR/DORBENE VET 1 mg/ml (Laboratorios Syva)médétomidine chlorhydrate: 1 mg/mlPosologie:Ca:- sédation:750 mcg/m2 de surf corp (iv) ou 1000 mcg/m2de surf corp (im) (20 - 80 mcg/kg)- préméd:10 - 40 mcg/kgFe:- sédation moyenne - profonde:50 - 150 mcg/kg- anesth:80 mcg/kg (avec 2,5 - 7,5 mg de kétamine/kg)f<strong>la</strong>con 10 mlR/
17810 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUEMEDETOR 1mg/ml (CP-Pharma)médétomidine chlorhydrate: 1 mg/mlsolution injectable im (Ca, Fe, iv (Ca)Posologie:Sédatif:Ca: 750 mcg/m2 de surf corp (iv)Ca: 1000 mcg/m2 de surf corp (im)Fe: 50 - 150 mcg/kg (im)anesth avec kétamine:Fe: 80 mcg/kg (im)f<strong>la</strong>con 10 mlR/NARCOSTART 1 mg/ml (Le Vet)médétomidine chlorhydrate: 1 mg/mlsolution injectable im, iv (Ca), im (Fe)Posologie:- Ca:sédation: 750 mcg/m2 de surface corporelle(iv) ou 1000 mcg/m2 de surface corporelle (im)préméd: 10-40 mcg/kg- Fe:sédation: 50-150 mcg/kganesth: 80 mcg/kg + 2,5-7,5 mg dekétamine/kgf<strong>la</strong>con 1 x 10 mlR/SEDATOR (Eurovet A.H.)médétomidine chlorhydrate: 1 mg/mlsolution injectable im (Ca, Fe), iv (Ca)Posologie:Ca:- sédation: 750 mcg/m2 de surf corp (iv) ou1000 mcg/m2 de surf corp (im)- préméd: 10 - 40 mcg/kgFe:- sédation: 50 - 150 mcg/kg- anesth: 80 mcg/kg + kétamine (2,5 - 7,5 mg/kg)- prolongation de l’anesth: avec 40 mcg/kgmédétom + kétamine (2,5 - 3,75 mg/kg) ouavec de <strong>la</strong> kétamine (3 mg/kg)f<strong>la</strong>con 10 ml, 20 mlR/SEDEDORM (Vetpharma A.H.)médétomidine chlorhydrate: 1 mg/mlsolution injectable im, iv, sc (Fe)Posologie:Ca:sédation: 15 - 80 mcg/kg (iv) ou 20 - 100mcg/kg (im)préméd: 10 - 40 mcg/kg (selon les autresanesthésiques utilisés)Fe:sédation: 50 - 150 mcg/kg (iv, im, sc)f<strong>la</strong>con 10 mlR/10.7.1.4 RomifidineLMR romifidine: SEDIVET 10 mg/ml (Boehringer Ingelheim)romifidine chlorhydrate: 10 mg/mlsolution injectable ivPosologie:Eq: selon l’intensité de <strong>la</strong> sédation:0,04 mg/kg0,08 mg/kg0,12 mg/kgViande: 6 jNe pas administrer aux Eq dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 20 mlR/10.7.1.5 Xy<strong>la</strong>zineLMR xy<strong>la</strong>zine: PROXYLAZ 2 % (Prodivet)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable iv, imPosologie:Eq (iv): 0,6 - 1 mg/kgBo: selon l’intensité de <strong>la</strong> sédation0,016 - 0,024 mg/kg (iv) ou 0,05 mg/kg (im)0,034 - 0,05 mg/kg (iv) ou 0,1 mg/kg (im)0,066 - 0,1 mg/kg (iv) ou 0,2 mg/kg (im)0,3 mg/kg (im)Ca (im), Fe (im): 3 mg/kgViande Eq, Bo: 1 j, Lait Bo: 0 jf<strong>la</strong>con 25 ml, 50 mlR/ROMPUN sol 2% (Bayer)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable iv, im, scPosologie:Eq: 0,6-1 mg/kg (iv)Bo: selon l’intensité de <strong>la</strong> sédation:0,05 mg/kg, 0,1 mg/kg, 0,2 mg/kg,0,3 mg/kg (im) ou1,6 - 2,4 mg/100 kg, 3,4 - 5 mg/100 kg,6,6 - 10 mg/100 kg (iv)Ca: 1-3 mg/kg (im, iv)Fe: 2-4 mg/kg (im, sc)Viande: Eq, Bo: 1 j, Lait: 0 jf<strong>la</strong>con 25 mlR/ROMPUN substance sèche (Bayer)xy<strong>la</strong>zine (chlorhydrate): 500 mgpoudre pour solution injectable im, ivPosologie:Eq: (sol 5 % ou 10 %)0,6 - 1mg/kg (iv)1,8 - 3 mg/kg (im)animaux sauvages: voir noticeViande: 1 jNe pas administrer aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine5 x 1 f<strong>la</strong>con 500 mg actif + 1 f<strong>la</strong>con 50 ml desolvantR/SEDAXYL (Ke<strong>la</strong> <strong>la</strong>boratoria)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable im, iv, scPosologie:Bo (im): selon le degré de sédation désiré:0,25 - 1,50 ml/100 kgEq:- iv: 4 ml (3 - 5 ml)/100 kg- im: 10 ml (7,5 - 15 ml)/100 kgCa (im et iv): 0,15 ml/kgFe (im ou sc): 0,15 ml/kgViande: 1 j, Lait: 0 jf<strong>la</strong>con 25 mlR/
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 179SEDAXYLAN (Eurovet A.H.)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable im (Bo, Ca, Fe), iv (Eq, Bo,Ca), sc (Ca, Fe)Posologie:Eq: 0,5 - 1 mg/kg (iv)Bo: 0,05 - 0,2 mg/kg (im) ou0,03 - 0,1 mg/kg (iv)Ca: 1 - 2 mg/kg (im, sc) ou0,7 - 1 mg/kg (iv)Fe: 0,5 - 1 mg/kg (im, sc)Viande: Eq: 1 j, Bo: 1 j, Lait: Bo: 0 jf<strong>la</strong>con 25R/VEXYLAN (Ceva Santé Animale)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable iv, imPosologie:Eq: 0,6 - 1 mg/kg (iv)Bo: 0,05 - 0,3 mg/kg (im),0,016 - 0,1 mg/kg (iv)Ca: 1 - 3 mg/kg (im)Fe: 1 - 2 mg/kg (im)Viande: Eq, Bo: 24 h, Lait: 0 jf<strong>la</strong>con 25 mlR/XYL-M 2% (VMD)xy<strong>la</strong>zine (chlorhydrate): 20 mg/mlsolution injectable iv, im, scPosologie:Eq: 0,6 - 1 mg/kg (iv)Bo:0,016 - 0,1 mg/kg (iv)0,05 - 0,3 mg/kg (im)max 0,3 mg/kgCa:3 mg/kg (im)1 - 1,5 mg/kg (iv)Fe:3 mg/kg (im,sc)0,5 - 1,1 mg/kg (iv)Viande: Eq: 24 h, Bo: 24 h, Lait: 0 jf<strong>la</strong>con 25 mlR/10.7.2 Les antagonistes alpha-2-adrénergiques10.7.2.1 AtipamézoleIndicationsL’atipamézole est le seul agonistealpha-2-adrénergique enregistré enBelgique comme antagoniste deseffets de <strong>la</strong> médétomidine et de <strong>la</strong> dexmédétomidine.L’atipamézole s’utiliseégalement comme antidote d’autresagonistes alpha-2-adrénergiques sansque les schémas posologiques n’aientété validés.PharmacodynamieCette substance est spécifique desrécepteurs alpha-2-adrénergiques.Au niveau pré-synaptique, il s’ensuitune augmentation de <strong>la</strong> libération et<strong>du</strong> turnover de <strong>la</strong> noradrénaline. Cetteaction, combinée au blocage desrécepteurs post-synaptiques, a pourconséquence de faire disparaître tousles effets in<strong>du</strong>its par les agonistesalpha-2-adrénergiques. Vu <strong>la</strong> spécificitéde son action vis-à-vis desrécepteurs alpha-2 adrénergiques,l’administration d’atipamézole à unanimal soumis à l’action combinéede <strong>la</strong> médétomidine et d’une autresubstance psychotrope, peut révélerles effets de cette dernière. Ainsi, encas d’association d’un agoniste alpha-2-adrénergique avec <strong>la</strong> kétamine, l’effetconvulsivant de cette dernière peutêtre démasqué. L’animal est réveilléune dizaine de minutes après l’injection.En cas de surdosage accidente<strong>la</strong>vec d’autres substances <strong>du</strong> mêmegroupe, l’atipamézole s’avère être unbon antidote.PharmacocinétiqueL’atipamézole est excrété par les reinset le foie.Contre-indicationsL’atipamézole ne peut pas être utilisésimultanément avec des substancesqui ont une activité sur le systèmenerveux central ou chez des patientsprésentant une cardiopathie ou unmauvais état général.Effets indésirablesBrève et légère diminution de <strong>la</strong> pressionartérielle après l’administrationchez le chien. Exceptionnellement:hyperactivité, tachycardie, salivation,vomissements.Possibilité d’hypothermie chez le chat.InteractionsIl est déconseillé d’utiliser l’atipamézolesimultanément avec dessubstances qui ont une activité surle système nerveux central ou autonome,autres que les substancesalpha-2-adrénergiques.Précautions particulières/Risquespour l’hommeCe pro<strong>du</strong>it est également actif chezl’homme.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de ce pro<strong>du</strong>it chez les animauxrepro<strong>du</strong>cteurs, gestants ou al<strong>la</strong>itantsn’a pas été démontrée.
18010 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUELMR atipamézole: ALZANE 5 mg/ml (Laboratorios Syva)hydrochlorure d’atipamézole: 5 mg/mlsolution injectable imPosologie:Ca: hydrochlorure d’atipamézole (en mcg) =5 x <strong>la</strong> dose précédente d’hydrochlorure demédétomidine ou 10 x <strong>la</strong> dose d’hydrochlorurede dexmédétomidineFe: hydrochlorure d’atipamézole (en mcg) =2,5 x <strong>la</strong> dose précédente d’hydrochlorure demédétomidine ou 5 x <strong>la</strong> dose d’hydrochlorurede dexmédétomidinef<strong>la</strong>con 1 x 10 mlR/ANTISEDAN (Orion Corp)atipamézole chlorhydrate: 5 mg/mlsolution injectable imPosologie:Ca: <strong>la</strong> dose (en mcg) est égale à:5 x <strong>la</strong> dose de médétomidine administrée (1mg/ml de sol) ou10 x <strong>la</strong> dose de dexmédétomidine (0,5 mg/ml de sol) administrée(ce qui correspond à un même volume quecelui de l’alpha-2-agoniste)Fe: <strong>la</strong> dose (en mcg) est égale à:2,5 x <strong>la</strong> dose de médétomidine (1 mg/ml desol) administrée ou5 x <strong>la</strong> dose de dexmédétomidine (0,5 mg/mlde sol) administrée(ce qui correspond à <strong>la</strong> moitié <strong>du</strong> volume del’alpha-2-agoniste)f<strong>la</strong>con 10 mlR/ATIPAM (Eurovet A.H.)atipamézole chlorhydrate: 5 mg/mlsolution injectable imPosologie:Ca: <strong>la</strong> dose (en mcg) est égale à:5 x <strong>la</strong> dose de médétomidine administrée (1mg/ml de sol) ou10 x <strong>la</strong> dose de dexmédétomidine administrée(0,5 mg/ml de sol)(ce qui correspond à un même volume quecelui de l’alpha-2-agoniste)Fe: <strong>la</strong> dose (en mcg) est égale à:2,5 x <strong>la</strong> dose de médétomidine administrée(1 mg/ml de sol) ou5 x <strong>la</strong> dose de dexmédétomidine administrée(0,5 mg/ml de sol)(ce qui correspond à <strong>la</strong> moitié <strong>du</strong> volume del’alpha-2-agoniste)f<strong>la</strong>con 5 ml, 10 mlR/NARCOSTOP (Le Vet)atipamézole chlorhydrate: 5 mg/mlsolution injectable imPosologie:Ca: <strong>la</strong> dose (en mcg) est égale à:5 x <strong>la</strong> dose de médétomidine administrée (1mg/ml de sol) ou10 x <strong>la</strong> dose de dexmédétomidine (0,5 mg/ml de sol) administrée(ce qui correspond à un même volume quecelui de l’alpha-2-agoniste)Fe: <strong>la</strong> dose (en mcg) est égale à:2,5 x <strong>la</strong> dose de médétomidine (1 mg/ml desol) administrée ou5 x <strong>la</strong> dose de dexmédétomidine (0,5 mg/mlde sol) administrée(ce qui correspond à <strong>la</strong> moitié <strong>du</strong> volume del’alpha-2-agoniste)f<strong>la</strong>con 1 x 10 mlR/REVERTOR 5 mg/ml (CP-Pharma)chlorhydrate d’atipamézole: 5 mg/mlsolution injectable imPosologie:Ca: <strong>la</strong> dose intramuscu<strong>la</strong>ire optimale dechlorhydrate d’atipamézole [en mcg] =5 x <strong>la</strong> dose préa<strong>la</strong>ble de chlorhydrate demédétomidine ou 10 x <strong>la</strong> dose préa<strong>la</strong>ble dechlorhydrate de dexmédétomidineFe: <strong>la</strong> dose intramuscu<strong>la</strong>ire optimale dechlorhydrate d’atipamézole [en mcg] =2,5 x <strong>la</strong> dose préa<strong>la</strong>ble de chlorhydrate demédétomidine ou 5 x <strong>la</strong> dose préa<strong>la</strong>ble dechlorhydrate de dexmédétomidinef<strong>la</strong>con 10 mlR/10.8 Myore<strong>la</strong>xants10.8.1 GuaïfénésineIndicationsLa guaïfénésine, ou guaiacol-glycérine-éther, est une molécule myore<strong>la</strong>xante utiliséechez les équidés.PharmacodynamieLa guaïfénésine exerce une inhibition centrale des réflexes neuromuscu<strong>la</strong>ires, setra<strong>du</strong>isant par une re<strong>la</strong>xation des muscles squelettiques. L’animal reste conscientet ne bénéficie d’aucun effet antalgique, raisons pour lesquelles une prémédicationest indispensable pour in<strong>du</strong>ire un effet sédatif. L’analgésie peut être obtenuepar l’emploi d’analgésiques spécifiques ou d’anesthésiques locaux et généraux.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 181Les effets respiratoires et cardio-vascu<strong>la</strong>ires sont minimes lorsque les posologiesrecommandées sont respectées.PharmacocinétiqueL’effet clinique est perceptible après environ deux minutes. La guaïfénésine estmétabolisée dans le foie et excrétée via l’urine. La guaïfénésine traverse <strong>la</strong> barrièrep<strong>la</strong>centaire.Contre-indicationsLes animaux débilités ou anémiques ne peuvent pas être traités avec <strong>la</strong> guaïfénésine.La notice d’un pro<strong>du</strong>it étranger mentionne l’usage simultané avec de <strong>la</strong>physostigmine comme contre-indication.Effets indésirablesLes effets indésirables sont bénins et de nature passagère (baisse de tension,tachycardie). La solution à 10% pouvant in<strong>du</strong>ire une thrombophlébite, une dilutionadéquate est conseillée. Une administration prolongée entraîne un réveil difficilecaractérisé par de l’ataxie. En cas de surdosage ou chez les animaux présentantune forte acidose, une rigidité muscu<strong>la</strong>ire passagère peut être observée.InteractionsLes autres myore<strong>la</strong>xants (benzodiazépines, bloquants neuromuscu<strong>la</strong>ires) renforcentl’action de <strong>la</strong> guaïfénésine.Précautions particulièresLa fonction respiratoire et cardiaque doit être particulièrement surveillée en casd’association avec d’autres substances. Il est conseillé de se référer à <strong>la</strong> littératurescientifique spécialisée pour utiliser cette substance dans le cadre de protocolesd’anesthésie comme le « Triple drip », associant <strong>la</strong> guaïfénésine à <strong>la</strong> kétamine et àun agoniste alpha-2-adrénergique.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas administrer aux animaux gestants.LMR guaïfénésine: MYORELAX (Eurovet)guaïfénésine: 100 mg/mlsolution pour perfusion ivPosologie:après prémédEq: 60 - 100 mg/kgNe pas administrer aux Eq destinés à <strong>la</strong>consommation humainef<strong>la</strong>con 500 mlR/10.9 Antidépresseurs10.9.1 Antidépresseurs tricycliques10.9.1.1 ClomipramineIndicationsLa clomipramine est utilisée en appointà <strong>la</strong> thérapie comportementale, particulièrementdans le cadre de l’anxiétéde séparation.PharmacodynamieLa clomipramine est une substancecapable d’inhiber <strong>la</strong> recapture de <strong>la</strong> sérotonineet de <strong>la</strong> noradrénaline par lesneurones <strong>du</strong> système nerveux central.PharmacocinétiqueAprès absorption, <strong>la</strong> clomipramine estmétabolisée dans le foie en métaboliteactif. Tous deux se lient très facilementaux protéines p<strong>la</strong>smatiques. La clomipramineest particulièrement lipophile,a une bonne distribution tissu<strong>la</strong>ire etdiffuse à travers <strong>la</strong> barrière hématoméningée,le p<strong>la</strong>centa et vers le <strong>la</strong>it.La métabolisation a lieu dans le foie etles deux tiers de l’excrétion via l’urine,le reste par les fèces. Il faut attendrequelques semaines avant de pouvoirobserver l’effet clinique, les effetsindésirables peuvent cependant semanifester plus tôt.Contre-indications- Troubles cardio-vascu<strong>la</strong>ires etépilepsie.
18210 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE- Usage simultané avec des monoaminesoxydases (p. ex. <strong>la</strong> sélégiline,l’amitraz).- Un usage prudent est conseillé chezles patients souffrant d’hyperthyroïdieet les patients traités avec deshormones thyroïdiennes, en raison<strong>du</strong> risque accru de troubles <strong>du</strong>rythme cardiaque.- En raison de son activité anticholinergique,<strong>la</strong> prudence est égalementde mise chez les patients souffrantde troubles de motilité gastro-intestinale,de rétention urinaire, d’unepression intra-ocu<strong>la</strong>ire accrue et detroubles <strong>du</strong> rythme cardiaque.Effets indésirablesBien que <strong>la</strong> tolérance soit considéréecomme bonne chez le chien, desaccidents liés à des altérations de <strong>la</strong>pression artérielle et des troubles de<strong>la</strong> con<strong>du</strong>ction cardiaque ne sont pasimpossibles, vu <strong>la</strong> pharmacodynamiede cette molécule. Chez l’homme, desnausées et des troubles de l’éjacu<strong>la</strong>tionsont aussi signalés. En cas desurdosage, un syndrome sérotoninergiqueest possible (fièvre, myoclonies,agitation…).Interactions- Inhibiteurs des monoamines oxydases(sélégiline, amitraz). Lessubstances de ce groupe sontconnues pour leurs propriétés inhibitrices<strong>du</strong> cytochrome P450.- Anticholinergiques et moléculesagissant sur le SNC (effet additif).- La cimétidine diminue le métabolismede <strong>la</strong> clomipramine.- Les sympaticomimétiques augmententles risques d’effets cardiaques.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa sécurité de <strong>la</strong> clomipramine chezles animaux gestants ou al<strong>la</strong>itants n’apas été étudiée. Chez les animaux de<strong>la</strong>boratoire, il existe des indices d’effetsembryotoxiques. Il est par conséquentdéconseillé d’administrer cettemolécule aux animaux gestants oual<strong>la</strong>itants.LMR clomipramine: CLOMICALM 5 mg (Novartis)clomipramine chlorhydrate: 5 mgcomprimé poPosologie:Ca: 1 - 2 mg/kg 2 x pjcompr 30R/CLOMICALM 20 mg (Novartis)clomipramine chlorhydrate: 20 mgcomprimé poPosologie:Ca: 1 - 2 mg/kg 2 x pjcompr 30R/CLOMICALM 80 mg (Novartis)clomipramine chlorhydrate: 80 mgcomprimé poPosologie:Ca: 1 - 2 mg/kg 2 x pjcompr 30R/10.9.2 Inhibiteurs sélectifs de <strong>la</strong> recapture de <strong>la</strong> sérotonine10.9.2.1 FluoxétineIndicationsAide à <strong>la</strong> thérapie comportementale,en particulier dans le traitement <strong>du</strong>trouble de l’anxiété de séparation semanifestant par des comportementsinappropriés.PharmacodynamieLa fluoxétine et son métabolite actif,<strong>la</strong> norfluoxétine, sont des inhibiteursextrêmement sélectifs de <strong>la</strong> capture de<strong>la</strong> sérotonine. Suite à cette inhibition,<strong>la</strong> fluoxétine améliore <strong>la</strong> neurotransmissionsérotonergique et pro<strong>du</strong>it deseffets fonctionnels résultant de l’augmentationde l’activation des récepteursde <strong>la</strong> sérotonine. La fluoxétine n’apas d’action sédative et n’a pas d’effet,in vivo et aux doses recommandées,sur <strong>la</strong> capture de <strong>la</strong> catécho<strong>la</strong>mine. Lafluoxétine n’a pas d’affinité significativeavec les récepteurs muscariniques, lesrécepteurs alpha adrénergiques ou lesrécepteurs H1, et n’exerce pas d’effetsdirects sur le coeur.PharmacocinétiqueLa fluoxétine est bien absorbéeaprès administration orale (~72 %).L’absorption n’est pas influencée parl’alimentation. La fluoxétine est métaboliséeen norfluoxétine, métaboliteactif. On observe une accumu<strong>la</strong>tionde <strong>la</strong> fluoxétine et de son métabolite<strong>du</strong>rant les 10 premiers jours suivantl’instauration <strong>du</strong> traitement, puis unétat d’équilibre est atteint. Chez leschiens, l’élimination se fait via l’urine etles selles. En raison de <strong>la</strong> longue demi-viede ce médicament, il n’est pasnécessaire de ré<strong>du</strong>ire progressivementles doses lors de l’arrêt <strong>du</strong> traitement.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 183Contre-indicationsNe pas utiliser chez les chiens pesantmoins de 4 kg ou âgés de moins de6 mois. Ne pas utiliser chez les chiensépileptiques.Effets indésirables- Très fréquents : anorexie, léthargie.- Courants : troubles <strong>du</strong> système urinaire(cystite, incontinence urinaire,rétention urinaire, strangurie), troubles<strong>du</strong> système nerveux central (incoordination,désorientation).- Peu courants : perte de poids/deforme, mydriase.- Rares : convulsions.InteractionsNe pas administrer simultanémentavec:- des médicaments abaissant le seuild’apparition des convulsions, tels quel’acépromazine.- d’autres agents sérotonergiques.- des inhibiteurs de <strong>la</strong> monoamine oxydase(MAOI) tels que <strong>la</strong> sélégiline oul’amitraz.- des amines tricycliques, telles que <strong>la</strong>clomipramine.Des interactions sont possibles avecd’autres médicaments métaboliséspar le système enzymatique P45.Une période sans traitement de 6 semainesdoit être respectée après l’arrêt<strong>du</strong> traitement.Précautions particulièresLe traitement doit être arrêté en cas deconvulsions.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de ce médicament n’ayantpas été établie en cas de gestation etde <strong>la</strong>ctation, son utilisation n’est doncpas recommandée dans ces cas-là. Onn’a pas observé d’effets tératogènes,foetotoxiques ou maternotoxiqueschez les animaux de <strong>la</strong>boratoire. Iln’y a pas eu de tests sur les chiens.Aucun effet sur <strong>la</strong> capacité de repro<strong>du</strong>ctiondes rats mâles et femelles n’aété constaté.LMR fluoxétine : RECONCILE compr à croquer pour chiens (Eli Lilly)fluoxétine (hydrochlorure): 8 mg, 16 mg, 32 mgou 64 mg/comprcomprimé à croquer poPosologie:Ca (PV > 4 kg, âge > 6 m): 1 à 2 mg/kgcompr 30R/10.9.3 Inhibiteurs des monoamines oxydases (IMAO)10.9.3.1 SélégilineIndicationsChez le chien, elle est indiquée pour letraitement des troubles comportementauxd’origine émotionnelle. Cette indication,vague et très <strong>la</strong>rge, ne doit pasdispenser le praticien d’un diagnosticprécis le con<strong>du</strong>isant à une thérapiecomportementale adéquate éventuellementsoutenue par un traitementmédicamenteux.PharmacodynamieL’inhibition de l’activité enzymatiquedes monoamines oxydases de type B(MAO-B), impliquées dans <strong>la</strong> dégradationde <strong>la</strong> dopamine, confère à ces moléculesdes propriétés antidépressives.PharmacocinétiqueAprès administration orale, <strong>la</strong> sélégilineest rapidement absorbée. La biodisponibilitése ré<strong>du</strong>it à 10% chez lechien, en raison d’un effet de premierpassage important. De nature lipophile,<strong>la</strong> sélégiline pénètre rapidementà travers les tissus, et se concentreparticulièrement au niveau <strong>du</strong> cerveau.Elle se lie irréversiblement à l’enzymemonoamine-oxydase. La métabolisationaboutit à trois métabolites actifs;l’excrétion a lieu par voie rénale. L’effetclinique n’est perceptible qu’aprèsquelques jours et il faut parfois attendrejusqu’à 3 mois avant de noterune activité maximale.Contre-indicationsUsage simultané avec des antidépresseurstricycliques (p.ex. <strong>la</strong>clomipramine).Effets indésirablesDes vomissements et une ré<strong>du</strong>ctionde <strong>la</strong> libération de pro<strong>la</strong>ctine sontpossibles.InteractionsDes interactions se manifestent en casd’usage simultané des inhibiteurs demonoamines oxydases (IMAO) avecdes antagonistes alpha-2, de l’amitraz,des anesthésiques, de l’éphédrine, de<strong>la</strong> mépéridine, des molécules opioïdes,des sympaticomimétiques, des antidépresseurstricycliques (clomipramine)et des inhibiteurs sélectifs de <strong>la</strong> recapturede <strong>la</strong> sérotonine (ISRS).
18410 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUERepro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de <strong>la</strong> sélégiline chez lesanimaux gestants ou al<strong>la</strong>itants n’a pasété étudiée. Il est par conséquent déconseilléd’administrer cette moléculeaux animaux gestants ou al<strong>la</strong>itants.Par son action inhibitrice sur les monoaminesoxydases, <strong>la</strong> sélégiline peutinhiber <strong>la</strong> pro<strong>du</strong>ction de pro<strong>la</strong>ctine.LMR sélégiline: SELGIAN 4 mg (Ceva Santé Animale)sélégiline chlorhydrate: 4 mgcomprimé poPosologie:Ca (min 1,5 kg et < 17 kg): 1 x 0,5 mg/kg pj(<strong>du</strong>rée de traitement min: 2 m)compr 3 x 10R/SELGIAN 10 mg (Ceva Santé Animale)sélégiline chlorhydrate: 10 mgcomprimé poPosologie:Ca (min 8 kg et < 37 kg): 1 x 0,5 mg/kg pj(<strong>du</strong>rée de traitement min: 2 m)compr 3 x 10, 10 x 10R/SELGIAN 20 mg (Ceva Santé Animale)sélégiline chlorhydrate: 20 mgcomprimé poPosologie:Ca (min 36 kg): 1 x 0,5 mg/kg pj (<strong>du</strong>rée detraitement min: 2 m)compr 3 x 10R/10.10 Médicaments antiépileptiques10.10.1 PhénobarbitalIndicationPrévention des crises <strong>du</strong>es à l’épilepsie généralisée chez les chiens. (Voir aussiFolia Veterinaria 2008, n° 2).PharmacodynamieLes effets antiépileptiques <strong>du</strong> phénobarbital résultent probablement d’une ré<strong>du</strong>ctionde <strong>la</strong> transmission monosynaptique, in<strong>du</strong>isant vraisemb<strong>la</strong>blement une diminutionde l’excitabilité neuronale et une élévation <strong>du</strong> seuil de stimu<strong>la</strong>tion électriquede l’aire motrice corticale.PharmacocinétiqueAprès administration orale chez le chien, le phénobarbital est rapidement absorbéà partir <strong>du</strong> tube digestif, les concentrations p<strong>la</strong>smatiques maximales sont atteintesdans les 4 à 8 heures. La biodisponibilité est comprise entre 86 et 96 %. Levolume de distribution est de 0,75 l/kg et une concentration sérique à l’équilibreest atteinte 2 à 3 semaines après l’instauration <strong>du</strong> traitement. Environ 45 % de<strong>la</strong> concentration p<strong>la</strong>smatique est lié aux protéines. La métabolisation se fait parhydroxy<strong>la</strong>tion aromatique <strong>du</strong> groupe phényl en position para (p–hydroxyphénobarbital).Environ 25 % <strong>du</strong> médicament est excrété sous forme inchangée dans lesurines. La variabilité interindivi<strong>du</strong>elle de <strong>la</strong> demi-vie d’élimination est importante,al<strong>la</strong>nt de 40 à 90 heures.Contre-indicationsNe pas utiliser chez les animaux souffrant d’insuffisance hépatique sévère, detroubles rénaux ou cardiovascu<strong>la</strong>ires sévères. Ne pas utiliser chez les chiens pesantmoins de 5 kg.Effets indésirables- Ataxie, somnolences, faiblesse et étourdissements peuvent apparaître en débutde traitement. Ces effets disparaissent généralement au cours <strong>du</strong> traitement.- Parfois : hyperexcitabilité paradoxale, en particulier au début d’un premier traitement.Cette hyperexcitabilité n’étant pas liée à un surdosage, il n’y a pas lieude ré<strong>du</strong>ire <strong>la</strong> posologie.- Polyurie, polydipsie et polyphagie peuvent survenir à des concentrationssériques moyennes ou élevées ; ces effets peuvent être atténués en limitantl’absorption d’eau et de nourriture.- L’ataxie et <strong>la</strong> somnolence deviennent souvent problématiques lorsque les tauxsériques atteignent les limites supérieures de l’intervalle thérapeutique. Desconcentrations sériques élevées peuvent être associées à une hépatotoxicité.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 185- Le phénobarbital peut avoir des effets délétères sur les cellules souches de <strong>la</strong>moelle osseuse. Les conséquences sont une pancytopénie immunotoxique et/ou une neutropénie. Ces réactions disparaissent à l’arrêt <strong>du</strong> traitement.- Le traitement des chiens avec le phénobarbital peut entraîner une ré<strong>du</strong>ction destaux sériques de <strong>la</strong> T4 totale ou de <strong>la</strong> T4 libre, sans que ceci indique nécessairementune hypothyroïdie. (Voir Folia Veterinaria 2006, n° 3) Un traitement desubstitution de l’hormone thyroïdienne ne doit être instauré que si l’on observedes signes cliniques de <strong>la</strong> ma<strong>la</strong>die.En cas d’effets indésirables sévères, on conseille de ré<strong>du</strong>ire <strong>la</strong> dose administrée.Interactions- À <strong>la</strong> dose thérapeutique, le phénobarbital est un in<strong>du</strong>cteur des protéines p<strong>la</strong>smatiques(telles que <strong>la</strong> glycoprotéine acide alpha1, GPA), auxquelles se lient lesmédicaments. Il convient donc de prêter une attention particulière aux caractéristiquespharmacocinétiques et aux posologies des médicaments administréssimultanément.- L’administration concomitante de phénobarbital con<strong>du</strong>it à une diminution desconcentrations p<strong>la</strong>smatiques de <strong>la</strong> ciclosporine, des hormones thyroïdiennes etde <strong>la</strong> théophylline. L’efficacité de ces substances s’en trouve ré<strong>du</strong>ite.- La cimétidine et le kétoconazole sont des inhibiteurs des enzymes hépatiques :leur administration concomitante avec le phénobarbital peut provoquer uneaugmentation de <strong>la</strong> concentration sérique <strong>du</strong> phénobarbital.- L’utilisation concomitante de bromure de potassium augmente le risque depancréatite.- L’administration concomitante d’autres médicaments ayant une action dépressivesur le système nerveux central, tels que les analgésiques narcotiques, lesdérivés morphiniques, les phénothiazines, les antihistaminiques, <strong>la</strong> clomipramineet le chloramphénicol, peut ré<strong>du</strong>ire les effets <strong>du</strong> phénobarbital.- L’administration concomitante de phénobarbital peut stimuler le métabolismeet ré<strong>du</strong>ire les effets des antiépileptiques, <strong>du</strong> chloramphénicol, des corticostéroïdes,de <strong>la</strong> doxycycline, des bêta-bloquants et <strong>du</strong> métronidazole.- L’efficacité des contraceptifs oraux peut être atténuée.- Le phénobarbital peut ré<strong>du</strong>ire l’absorption de <strong>la</strong> griséofulvine.- Les principes actifs suivants peuvent abaisser le seuil convulsif : quinolones,bêta–<strong>la</strong>ctamines à doses élevées, théophylline, aminophylline, ciclosporineet propofol. Les médicaments susceptibles de modifier le seuil convulsif nedoivent être utilisés qu’en cas de réelle nécessité et lorsqu’il n’existe aucunealternative plus sûre.Précautions particulièresLes comprimés ne doivent pas être divisés. Chez les petits chiens, contrairementaux recommandations, <strong>la</strong> dose ne peut donc pas être ajustée par paliers de 20 % ;une surveil<strong>la</strong>nce particulière est donc nécessaire chez ces animaux.La prudence est de mise chez les animaux présentant une insuffisance hépatiqueou rénale, une hypovolémie, une anémie, une affection cardiaque ou respiratoire.Le risque d’effets indésirables hépatotoxiques peut être ré<strong>du</strong>it ou différé en utilisant<strong>la</strong> dose efficace <strong>la</strong> plus faible possible. Il est recommandé de surveiller lesparamètres hépatiques en cas de traitement prolongé.L’état clinique de l’animal traité devra être évalué 2 à 3 semaines après l’instauration<strong>du</strong> traitement puis tous les 4 à 6 mois, en mesurant par exemple les enzymeshépatiques et les acides biliaires sériques. Il est important de noter quesuite à une crise, l’hypoxie notamment entraîne une élévation des taux d’enzymeshépatiques.Le phénobarbital peut augmenter l’activité de <strong>la</strong> phosphatase alcaline et des transaminases,sans que ce<strong>la</strong> soit obligatoirement signe d’hépatotoxicité. En cas desuspicion d’hépatotoxicité, il est recommandé d’effectuer des bi<strong>la</strong>ns hépatiques.Si les concentrations en enzymes hépatiques augmentent mais que les concentrationssériques en acides biliaires demeurent dans l’intervalle physiologique, iln’est pas nécessaire de ré<strong>du</strong>ire <strong>la</strong> dose de phénobarbital.Si l’état d’un animal épileptique est stabilisé, il est déconseillé de substituer uneformu<strong>la</strong>tion de phénobarbital par une autre. L’arrêt <strong>du</strong> traitement au phénobarbitaldoit être progressif afin d’éviter une augmentation de <strong>la</strong> fréquence des crises.
18610 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUERepro<strong>du</strong>ction, gestation et <strong>la</strong>ctationLe phénobarbital traverse <strong>la</strong> barrière p<strong>la</strong>centaire et est excrété en faible quantitédans le <strong>la</strong>it maternel. L’innocuité <strong>du</strong> médicament vétérinaire pendant <strong>la</strong> gestationn’a pas été établie chez <strong>la</strong> chienne. Les effets sédatifs indésirables doivent êtreétroitement surveillés chez les chiot al<strong>la</strong>ités. En cas de gravidité ou de <strong>la</strong>ctation, lepro<strong>du</strong>it ne devra être administré qu’après évaluation <strong>du</strong> rapport bénéfice/risque.LMR phénobarbital : PHENOLEPTIL 12,5 mg chien (Le Vet)phénobarbital: 12,5 mgcomprimé poPosologie:Ca (PV < 5 kg):dose initiale: 2 x pj 2,5 mg/kgdose d’entretien: adapter <strong>la</strong> doseindivi<strong>du</strong>ellementcompr 10 x 10, 50 x 10R/PHENOLEPTIL 50 mg chien (Le Vet)phénobarbital: 50 mgcomprimé poPosologie:Ca:dose initiale: 2 x pj 2,5 mg/kgdose d’entretien: adapter <strong>la</strong> doseindivi<strong>du</strong>ellementcompr 10 x 10, 50 x 10R/10.10.2 Bromure de potassiumIndicationsAgent antiépileptique à utiliser en complément <strong>du</strong> phénobarbital dans le contrôledes cas réfractaires d’épilepsie chez le chien. Administrer aux chiens souffrantd’épilepsie réfractaire, lorsque le contrôle des crises n’est pas satisfaisant en dépitd’un traitement au phénobarbital approprié con<strong>du</strong>isant à des concentrationssériques de phénobarbital stables et comprises entre les limites thérapeutiques.La dose doit être déterminée en fonction <strong>du</strong> chien traité et administrée deux foispar jour avec l’alimentation. (Voir aussi Folia Veterinaria 2008, n° 2)PharmacodynamieLe bromure de potassium est en compétition avec le transport <strong>du</strong> chlore à traversles membranes des cellules nerveuses et inhibe le transport <strong>du</strong> sodium,provoquant ainsi l’hyperpo<strong>la</strong>risation des membranes. Celle-ci augmente le seuilépileptogène et prévient <strong>la</strong> propagation des décharges épileptiques. Le bromureagit sur le transport actif à travers <strong>la</strong> membrane des cellules gliales et affecteles mouvements passifs des ions en entrant en compétition avec le chlorure auniveau des canaux anioniques dans les membranes post-synaptiques qui sontactivées par les neurotransmetteurs inhibiteurs. Ce<strong>la</strong> potentialise l’effet <strong>du</strong> neuromédiateurGABA et provoque une activité synergique <strong>du</strong> bromure avec d’autresmédicaments ayant une activité directe ou indirecte sur ce récepteur, tel que lephénobarbital.PharmacocinétiqueLa demi-vie étant d’environ 24 jours chez le chien, les concentrations à l’étatd’équilibre ne sont parfois atteintes qu’après quelques semaines, voire plusieursmois. Le bromure de potassium est bien absorbé par voie orale, avec un pic intervenant1,5 h environ après une prise orale. Le bromure diffuse rapidement, toutcomme l’ion chlore, dans tout l’espace extracellu<strong>la</strong>ire et dans les cellules. Lesmécanismes de diffusion de ces deux ions sont simi<strong>la</strong>ires. Le bromure n’est pasmétabolisé et est excrété principalement par les reins, où il entre en compétitionavec le chlorure pour <strong>la</strong> réabsorption tubu<strong>la</strong>ire. La concentration de chlorure diminueen proportion directe avec l’augmentation de <strong>la</strong> concentration de bromuredans l’organisme.Contre-indicationsLes animaux âgés sont plus sensibles au surdosage que les jeunes.Effets indésirablesUne sédation temporaire peut être observée pendant 3 semaines. D’autres effetsindésirables peuvent apparaître comme l’ataxie, les vomissements, <strong>la</strong> polyurie et<strong>la</strong> polydipsie, <strong>la</strong> polyphagie, des nausées et des réactions cutanées. Parmi leseffets moins fréquents, on cite de l’agressivité et des pancréatites. Dans de nombreuxcas, ces effets indésirables peuvent disparaître après ré<strong>du</strong>ction de <strong>la</strong> dosede phénobarbital de 10 à 25 %. Dans les cas de pancréatite ou de dermatite, untraitement symptomatique peut être requis.
10 MÉDICAMENTS DU SYSTÈME NERVEUX CENTRAL ET PÉRIPHÉRIQUE 187InteractionsUne forte assimi<strong>la</strong>tion d’ions chlore avec l’alimentation (aliments secs avec> 1 % Cl) stimule l’excrétion <strong>du</strong> bromure par l’urine et diminue les concentrationssériques <strong>du</strong> bromure, ce qui pourrait provoquer des crises d’épilepsie. À l’inverse,le passage à un régime alimentaire pauvre en chlorure augmentera les concentrationssériques de bromure, ce qui peut entraîner une intoxication au bromure.L’administration de liquides ou de médicaments contenant <strong>du</strong> chlorure peut ré<strong>du</strong>ireles concentrations sériques de bromure. Les diurétiques de l’anse dont lefurosémide peuvent augmenter l’excrétion <strong>du</strong> bromure et ré<strong>du</strong>ire ainsi les concentrationssériques. Une intoxication au bromure peut être traitée en administrant<strong>du</strong> chlorure de sodium ou un pro<strong>du</strong>it stimu<strong>la</strong>nt l’excrétion <strong>du</strong> chlorure par l’urine.Précautions particulièresEviter l’interruption brutale <strong>du</strong> traitement vu le risque d’in<strong>du</strong>ction des crises. Ilpeut être nécessaire de ré<strong>du</strong>ire <strong>la</strong> dose chez les animaux souffrant d’insuffisancerénale. Une ré<strong>du</strong>ction de <strong>la</strong> prise de chlorure de sodium peut entraîner une intoxicationau bromure. L’administration à un animal à jeun peut entraîner des vomissements.Il n’est pas possible d’administrer avec précision <strong>la</strong> posologie initialerecommandée aux chiens de moins de 11 kg.Risques pour l’hommeCe pro<strong>du</strong>it ne doit pas être manipulé par des femmes enceintes ou qui pourraientl’être, ni par des femmes qui al<strong>la</strong>itent. Les personnes présentant une hypersensibilitéconnue au bromure devraient éviter tout contact avec le médicament vétérinaire.En cas d’irritation de <strong>la</strong> peau ou des yeux, ou en cas d’auto-administrationaccidentelle, demander immédiatement conseil à un médecin et montrer <strong>la</strong> noticeou l’étiquetage.Repro<strong>du</strong>ction et <strong>la</strong>ctationLa sécurité <strong>du</strong> médicament vétérinaire n’a pas été établie en cas de gravidité oude <strong>la</strong>ctation. Le bromure peut traverser le p<strong>la</strong>centa et des cas d’intoxication néonataleau bromure ont été rapportés chez l’homme. Le traitement en période degravidité ou de <strong>la</strong>ctation doit reposer sur une évaluation bénéfice/risque.LMR bromure de potassium : LIBROMIDE 325 mg (Dechra)bromure de potassium: 325 mgcomprimé po avec l’alimentationPosologie:Ca (PV > 11 kg): 2 x 15 mg/kg pjadapter <strong>la</strong> dose en fonction <strong>du</strong> chien traitécompr 100R/
11 MÉDICAMENTS POUR LA PEAU 18911. MÉDICAMENTS POUR LA PEAULes substances actives à usage dermatologique, mais destinées à un usage local,sont traitées dans le chapitre 12. Médicaments à usage externe.11.1 Médicaments administrés par voie systémiquepour le traitement symptomatique de<strong>la</strong> dermatite atopique11.1.1 GlucocorticoïdesVoir chapitre 2.2. et 12.1.6.11.1.2 CiclosporineConcernant l’usage en ophtalmologie, voir chapitre 12.2.2.1.IndicationsLa ciclosporine peut être administrée per os dans le traitement symptomatiquede <strong>la</strong> dermatite atopique. Avant d’initier le traitement, il est impératif d’écarter lesautres causes de dermatoses caractérisées par les mêmes symptômes que ceuxassociés à <strong>la</strong> dermatite atopique.PharmacodynamieLes puissantes propriétés immunomo<strong>du</strong><strong>la</strong>trices de <strong>la</strong> ciclosporine s’expliquentprincipalement par l’inhibition de <strong>la</strong> transcription de gènes codant pour <strong>la</strong> synthèsede cytokines dans les cellules-T activées par un contact antigénique. Lapro<strong>du</strong>ction et <strong>la</strong> sécrétion de plusieurs cytokines sont ainsi réprimées. D’autrescellules impliquées dans les réactions allergiques cutanées comme les mastocytes,les cellules de Langerhans, les éosinophiles et les kératinocytes sont égalementinhibées.PharmacocinétiqueLa biodisponibilité chez le chien est faible et varie fortement en fonction des indivi<strong>du</strong>s.Elle est optimale lorsque <strong>la</strong> ciclosporine est administrée en dehors desrepas. La métabolisation a principalement lieu dans le foie et est dépendante<strong>du</strong> cytochrome P450. Les substances ayant un effet sur ce complexe enzymatiquepeuvent influencer <strong>la</strong> concentration p<strong>la</strong>smatique de <strong>la</strong> ciclosporine (voirInteractions). Les matières fécales représentent <strong>la</strong> voie d’élimination majeure. Lesreins y contribuent également mais dans une moindre mesure. Les propriétéspharmacocinétiques de <strong>la</strong> ciclosporine chez le chien sont analogues à celles de<strong>la</strong> ciclosporine utilisée chez l’homme. La marge de sécurité est cependant plusgrande chez le chien.Contre-indications Hypersensibilité à <strong>la</strong> ciclosporine. L’immunodépression pouvant favoriser le développement de tumeurs malignes,l’usage de cette substance est contre-indiqué chez les animaux présentantde telles pathologies. Troubles hépatiques ou rénaux graves. Chiens âgés de moins de 6 mois ou pesant moins de 2 kg. Les vaccinations <strong>du</strong>rant le traitement sont à éviter surtout avec des vaccinsvivants atténués. Elles doivent avoir lieu 2 semaines avant ou 2 semainesaprès le traitement. Diabète sucré.Effets indésirablesDes vomissements et de <strong>la</strong> diarrhée peuvent survenir chez le chien. Ces effetsindésirables sont généralement de courte <strong>du</strong>rée et apparaissent surtout chez lesraces plus petites. D’autres effets indésirables dépendent de <strong>la</strong> dose administréeet n’apparaissent que rarement lorsque <strong>la</strong> posologie recommandée est respectée.
19011 MÉDICAMENTS POUR LA PEAUL’insuffisance rénale et l’hypertension pouvant apparaître chez l’homme, mêmelorsque les doses sont peu élevées, ne se manifestent pas chez le chien.InteractionsLa ciclosporine augmente <strong>la</strong> concentration p<strong>la</strong>smatique de <strong>la</strong> digoxine. Elle peutégalement augmenter <strong>la</strong> néphrotoxicité des aminoglycosides et <strong>du</strong> triméthoprime.Inversement, plusieurs substances actives peuvent diminuer les concentrationsp<strong>la</strong>smatiques en ciclosporine: les sulfamidés, le triméthoprime, <strong>la</strong> rifampicine, lephénobarbital, l’oméprazole, <strong>la</strong> phénytoïne (anti-arythmique), <strong>la</strong> terbinafine (antimycotique),le probucol (diminue le cholestérol). En revanche, les antifongiques,notamment les dérivés azolés tels que le kétoconazole, le fluconazole, les inhibiteursdes canaux calciques (le vérapamil, le diltiazem), les macrolides (érythromycine),le métoclopramide, les androgènes, l’amiodarone (anti-arythmique)peuvent augmenter les concentrations p<strong>la</strong>smatiques en ciclosporine et accroîtresa toxicité. L’administration simultanée de <strong>la</strong> ciclosporine avec des glucocorticoïdes,de <strong>la</strong> colchicine ou <strong>la</strong> lovastatine peut augmenter <strong>la</strong> toxicité de chacunede ces substances. En inhibant <strong>la</strong> P-glycoprotéine de transport, <strong>la</strong> ciclosporinepeut diminuer l’efflux des <strong>la</strong>ctones macrocycliques (ivermectine, milbémycine) auniveau de <strong>la</strong> barrière hémato-encéphalique et déclencher <strong>la</strong> symptomatologie nerveusetypiquement associée à l’intoxication par ces antiparasitaires.L’efficacité des vaccins peut être influencée.Précautions particulièresVu l’effet immunosuppresseur de <strong>la</strong> ciclosporine, il est déconseillé de vacciner<strong>du</strong>rant le traitement. La ciclosporine n’in<strong>du</strong>it pas de tumeur mais peut con<strong>du</strong>ire àl’augmentation de l’incidence des manifestations cliniques d’affections malignes.Toute lymphadénopathie observée au cours <strong>du</strong> traitement à <strong>la</strong> ciclosporine doitêtre régulièrement contrôlée.Repro<strong>du</strong>ction et <strong>la</strong>ctationIl a été démontré que des doses de 2 à 5 fois plus élevées que <strong>la</strong> normale sontembryo- et fœtotoxiques. La sécurité <strong>du</strong> pro<strong>du</strong>it n’a pas été établie chez les animauxgestants ou en <strong>la</strong>ctation, ni chez les animaux repro<strong>du</strong>cteurs mâles.LMR ciclosporine: ATOPICA 25 mg (Novartis)ciclosporine: 25 mgcapsule poPosologie:Ca (âge > 6 m, PV > 2 kg): 5 mg/kg pj,2 h avant ou après l’alimentationcapsules 15R/ATOPICA 50 mg (Novartis)ciclosporine: 50 mgcapsule poPosologie:Ca (âge > 6 m, PV > 2 kg): 5 mg/kg pj,2 h avant ou après l’alimentationcapsules 15R/ATOPICA 100 mg (Novartis)ciclosporine: 100 mgcapsule poPosologie:Ca (âge > 6 m, PV > 2 kg): 5 mg/kg pj,2 h avant ou après l’alimentationcapsules 15R/ATOPICA 100 mg/ml (Novartis)ciclosporine: 100 mg/mlsolution poPosologie:Fe (âge > 6 m, PV > 2,3 kg): 7 mg/kg pj(ré<strong>du</strong>ire <strong>la</strong> fréquence d’administration enfonction de <strong>la</strong> réponse clinique)f<strong>la</strong>con + distributeur 5 ml, 17 mlR/
12 MÉDICAMENTS À USAGE EXTERNE 19112. MÉDICAMENTS À USAGE EXTERNELorsqu’elles sont administrées par voie systémique, les substances actives dont ilest question dans ce chapitre sont discutées dans un chapitre séparé.12.1 Médicaments à usage dermatologiqueLes médicaments repris dans ce chapitre sont des topiques à usage cutané, utiliséspour traiter et souvent prévenir les infections superficielles d’origine bactérienne,mycosique ou parasitaire. L’idée de prévention des infections aboutitle plus souvent à un usage inconsidéré des antibiotiques et des antiseptiques.D’une manière générale, les associations de plusieurs principes actifs ne sont pasrecommandées et souvent superflues après un diagnostic étiologique. Il faut aussisouligner le risque allergique lié à l’administration cutanée de substances activeset d’excipients.12.1.1 AntiseptiquesLes antiseptiques peuvent tuer des micro-organismes par dénaturation, précipitationou oxydation des protéines. Ils peuvent également perturber les processusenzymatiques dans les micro-organismes ou porter atteinte à l’intégrité de <strong>la</strong> paroicellu<strong>la</strong>ire ou de <strong>la</strong> membrane cellu<strong>la</strong>ire en modifiant <strong>la</strong> tension superficielle. Leurefficacité dépend <strong>du</strong> temps de contact avec le micro-organisme et de <strong>la</strong> concentration<strong>du</strong> désinfectant. La température joue également un rôle essentiel dansl’efficacité des antiseptiques (plus elle est élevée, plus l’efficacité est grande). Laprésence de pus, de nécrose tissu<strong>la</strong>ire, de sang, de rési<strong>du</strong>s de matières fécalesou d’or<strong>du</strong>res peut diminuer considérablement l’action des antiseptiques. Pourque l’application d’antiseptiquessoit utile, il convient donc de rincer autant quepossible <strong>la</strong> surface à traiter. La sensibilité des différentes sortes de micro-organismesaux antiseptiques varie. Les bactéries formant des spores sont difficiles àéliminer ; les halogènes et les aldéhydes possèdent des propriétés sporicides. Lesmycobactéries sont souvent résistantes aux antiseptiques.12.1.1.1 Antiseptiques utilisés sur<strong>la</strong> peau- L’aluminium est utilisé commeastringent pour favoriser <strong>la</strong> cicatrisationdes p<strong>la</strong>ies, que ce soit en casde piétin, d’ecthyma, après des interventionschirurgicales ou en cas detraumatisme.- La chlorhexidine provoque <strong>la</strong> lysebactérienne en augmentant <strong>la</strong> perméabilitémembranaire. Son actionest bactériostatique ou bactéricideet principalement dirigée contre lesbactéries Gram+ et Gram-, mais ellepossède également une activité antimycosiqueet agirait sur certains virus,bien que cette activité soit moins biendocumentée. Après administrationtopique de chlorhexidine, l’absorptionpercutanée n’est pas significative.Ce médicament est indiqué pour <strong>la</strong>désinfection cutanée préopératoirevisant à ré<strong>du</strong>ire <strong>la</strong> contamination microbienne<strong>du</strong> champ opératoire. Uneassociation à base de chlorhexidine+ nitrate de miconazole est disponiblesous forme de shampooingpour le traitement de <strong>la</strong> dermatiteséborrhéique associée à Ma<strong>la</strong>sseziapachydermatis et Staphylococcus intermediuschez le chien. Chez le chat,ce shampooing peut être utilisé en associationavec <strong>la</strong> griséofulvine commetraitement d’appoint de <strong>la</strong> teigne <strong>du</strong>eà Microsporum canis. En Belgique,aucun médicament à base de griséofulvinen’est commercialisé.- Les iodophores sont des solutionsaqueuses d’iode associé à des facteurstensio-actifs comme par exemplele polyvidone. Ils sont actifs contre lesbactéries GRAM- et GRAM+, les mycobactéries,les spores bactériennes(augmentation de <strong>la</strong> concentration et/ou allongement <strong>du</strong> temps de contact),les moisissures et certains virus. Ilssont moins toxiques que les teinturesd’iode et ont une action plus longueaprès administration. L’action desiodophores est entravée par l’eau calcaire,les graisses et l’amidon (rési<strong>du</strong>salimentaires).
19212 MÉDICAMENTS À USAGE EXTERNELMR aluminium: , chlorhexidine: ,polyvidone iodée: ALUSPRAY (Vétoquinol)aluminium (poudre): 3 gsuspension pour appl cutanéePosologie:Eq, Ru, Su, Ca, Fe, vo<strong>la</strong>ille:pulvériser 1 à 2 xTemps d’attente: 0 jspray 220 mlCODITANE 5% (Ke<strong>la</strong> Laboratoria)digluconate de chlorhexidine: 50 mg/mlsolution à diluer pour usage cutanéPosologie:diluer <strong>la</strong> sol (additioner 80 ml de sol + eaupour atteindre 100 ml), nettoyer <strong>la</strong> peaurasée 3 x 3 minViande + abats: 0 j, Lait: 0 jf<strong>la</strong>con 1,5 l, 25 lECUTAN 5% (Ecuphar)digluconate de chlorhexidine: 50 mg/mlsolution à diluer pour application cutanéePosologie:Ca: diluer 1 ml sur 10 ml d’alcool (70%) ou1 ml sur 100 ml d’eaufrotter <strong>la</strong> peau 2 x 3 min avec <strong>la</strong> sol diluéef<strong>la</strong>con 1 l, 10 l, 25 lPOVIDERM dermicum (Ecuphar)povidone iodée: 100 mg/mlsolution pour appl cutanéePosologie:Ca: en<strong>du</strong>ire le champ opératoire pendant ±2 fois 3 minutesf<strong>la</strong>con 250 ml, 500 ml, 5 lPOVIDERM sol (Emdoka)povidone iodée: 30 mg/gsolution pour appl cutanéePosologie:Ca, Lm: éventuellement plusieurs x pjf<strong>la</strong>con 500 ml, 5 lPOVIDERM spray (Emdoka)povidone iodée: 30 mg/gspray pour appl cutanéePosologie:Ca, Lm:vaporiser éventuellement plusieurs x pjspray 200 mlVET-CLEAN (Ecuphar)povidone iodée: 75 mg/mlsolution à usage cutanéPosologie:Ca: environ 5 ml de sol non diluée/dm2 depeau (frotter pendant 2 x 3 min)f<strong>la</strong>con 500 ml, 5 l ou 10 l12.1.1.2 Solution de trempage destrayonsChlorhexidineIndicationsDésinfection des trayons dans le cadred’une stratégie de prévention desmammites chez les vaches <strong>la</strong>itières.PharmacodynamieLa chlorhexidine est un bisbiguanidequi provoque <strong>la</strong> lyse bactérienne enaugmentant <strong>la</strong> perméabilité membranaire.Son action est bactériostatiqueou bactéricide et principalementdirigée contre les bactéries Gram+ etGram-, mais elle possède égalementune activité antimycosique et agiraitsur certains virus, bien que cette activitésoit moins bien documentée.PharmacocinétiqueLa résorption cutanée de <strong>la</strong> chlorhexidinen’est pas significative après applicationtopique.Précautions particulières/Risquespour l’hommeLaisser sécher le pro<strong>du</strong>it avant d’exposerles vaches à des conditions climatiqueshumides, froides ou venteuses.Eviter le contact avec les yeux.Repro<strong>du</strong>ction et <strong>la</strong>ctationPeut être utilisé pendant <strong>la</strong> gestation et<strong>la</strong> <strong>la</strong>ctation.LMR chlorhexidine : KENOCIDIN (CID LINES)chlorhexidine digluconate: 5 mg/gsolution pour trempage des trayonsPosologie:Bo: min 5 ml/animal/traitement, max 2 x pjaprès <strong>la</strong> traiteViande et abats: 0 j, Lait: 0 hfût 10 l, 20 l, 60 l et 200 lKENOCIDIN Spray & Dip (CID LINES)chlorhexidine digluconate: 5 mg/gsolution pour trempage et pulvérisation destrayonsPosologie:Bo: min 5 ml/animal/traitement, max 2 x pjaprès <strong>la</strong> traiteViande et abats: 0 j, Lait: 0 hfût 10 l, 20 l, 60 l et 200 lIodeIndicationsDésinfection des trayons dans le cadrede <strong>la</strong> stratégie de prévention des mammiteschez les bovins <strong>la</strong>itiers.PharmacodynamieL’iode cause une dégradation irréversiblede <strong>la</strong> paroi cellu<strong>la</strong>ire bactérienne.PharmacocinétiqueL’iode couvrant <strong>la</strong> peau interagit rapidementavec <strong>la</strong> matière organiqueprésente, <strong>la</strong>issant très peu d’iodelibre pour une absorption à traversl’épiderme.Contre-indicationsL’utilisation pour le traitement destrayons ayant des lésions cutanéespeut retarder <strong>la</strong> cicatrisation. Il estconseillé d’interrompre le traitementjusqu’à <strong>la</strong> guérison des lésions.
12 MÉDICAMENTS À USAGE EXTERNE 193InteractionsAucune interaction connue. Ne pasmé<strong>la</strong>nger avec d’autres pro<strong>du</strong>itschimiques.Précautions particulières/Risquespour l’hommeEviter le contact avec les yeux. L’iodeest potentiellement allergisant.Repro<strong>du</strong>ction et <strong>la</strong>ctationPeut être utilisé sur les bovins en <strong>la</strong>ctationet en gestation.LMR iode: BLOCKADE 0,25% w/w (DeLaval)iode: 2,5 mg/gsolution pour trempage des trayonsPosologie:vache <strong>la</strong>itière: 5 ml/animal/traitementViande: 0 j, Lait: 0 hfût 10 l, 20 l, 60 l, 200 lBOVIDIP 2% w/v (DeLaval)iode: 20 mg/ml (concentré), 5 mg/ml (sol prêteà l’emploi)solution pour trempage ou pulvérisation destrayonsPosologie:vache <strong>la</strong>itière:5 ml de sol diluée/animal/traitementViande: 0 j, Lait: 0 hfût 5 l, 20 lDIPAL Conc 0,75% w/w (DeLaval)iode: 7,5 mg/g (concentré), 1,5 mg/g (sol prêteà l’emploi)solution pour le trempage ou <strong>la</strong> pulvérisationdes trayonsPosologie:vache <strong>la</strong>itière:5 ml de sol diluée/animal/traitementViande: 0 j, Lait: 0 hfût 5 lKENOSTART (CID LINES)iode: 3 mg/gsolution pour le trempage des trayonsPosologie:Bo: tremper chaque trayon après <strong>la</strong> traiteViande et abats: 0 j, Lait: 0 jf<strong>la</strong>con 10 l, 20 l et 60 lfût 200 lKENOSTART spray & dip (CID LINES)iode: 3 mg/gsolution pour le trempage des trayonsPosologie:Bo: tremper ou vaporiser chaque trayonaprès <strong>la</strong> traiteViande et abats: 0 j, Lait: 0 jf<strong>la</strong>con 10 l, 20 l et 60 lfût 200 lPROACTIVE 0,15 w/w (DeLaval)iode: 1,5 mg/gsolution pour le trempage ou <strong>la</strong> pulvérisationdes trayonsPosologie:vache <strong>la</strong>itière: 5 ml/animal/traitementViande: 0 j, Lait: 0 hfût 10 l, 20 l, 60 l, 200 lPROACTIVE PLUS 0,15% w/w (DeLaval)iode: 1,5 mg/gsolution pour le trempage ou <strong>la</strong> pulvérisationdes trayonsPosologie:vache <strong>la</strong>itière: 5 ml/animal/traitementViande: 0 j, Lait: 0 hfût 20, 60 et 200 lChlorite + acide <strong>la</strong>ctiqueIndicationsSolution pour trempage des trayons utiliséeaprès <strong>la</strong> traite chez <strong>la</strong> vache <strong>la</strong>itièrecomme aide au contrôle des mammitescausées par des pathogènes tels queStaphylococcus aureus, Streptococcusaga<strong>la</strong>ctiae, Streptococcus dysga<strong>la</strong>ctiae,Streptococcus uberis ou Escherichiacoli.PharmacodynamieLa solution contient comme substancesactives de l’acide <strong>la</strong>ctique et<strong>du</strong> chlorite. En préparant <strong>la</strong> solution,le mé<strong>la</strong>nge de chlorite et d’acide <strong>la</strong>ctiqueforme un acide chloreux. Celuicipossède un <strong>la</strong>rge spectre d’activitébactéricide, probablement par actionoxydative. L’adsorption de l’acide<strong>la</strong>ctique sur <strong>la</strong> surface des cellules <strong>du</strong>germe in<strong>du</strong>it <strong>la</strong> fuite d’ions hydrogèneà travers <strong>la</strong> membrane cellu<strong>la</strong>ire, cequi entraîne l’acidification de l’intérieurde <strong>la</strong> cellule et l’inhibition <strong>du</strong> transportdes nutriments. En formant un film sur<strong>la</strong> surface de <strong>la</strong> peau des trayons, <strong>la</strong>solution protège ceux-ci et prévientune contamination. Ce film capturepar ailleurs les rési<strong>du</strong>s d’acide <strong>la</strong>ctique<strong>la</strong>issés par <strong>la</strong> réaction chimique initiale.Contre-indicationsNe pas utiliser sur des trayons présentantune blessure ou une inf<strong>la</strong>mmation.Précautions particulières/Risquespour l’hommeNe pas faire sortir les vaches tant que<strong>la</strong> solution pour trempage n’est pascomplètement sèche, en particulierpar basses températures.Utiliser le pro<strong>du</strong>it dans un local bienventilé (risque d’accumu<strong>la</strong>tion de gazde dioxyde de chlore irritant). Irritantpour les yeux. En cas de contact, rincerles yeux abondamment à l’eau.
19412 MÉDICAMENTS À USAGE EXTERNELMR chlorite de sodium + acide <strong>la</strong>ctique: ALCIDE UDDERGOLD PM VET (Eco<strong>la</strong>b)- concentré Base:chlorite de sodium: 6,4 mg/ml- concentré Activator:acide <strong>la</strong>ctique: 26,4 mg/mlsolution pour le trempage des trayonsPosologie:Bo: tremper chaque trayon après <strong>la</strong> traite(environ 7,5 ml de pro<strong>du</strong>it/animal/traite)Viande: Bo: 0 j, Lait: 0 hf<strong>la</strong>con 2 x 20 l (20 l d’Activator + 20 l de Base)12.1.2 AntibiotiquesLes préparations dermatologiques à base d’antibiotiques existent seulement sous<strong>la</strong> forme de sprays qui contiennent une tétracycline et sont utilisés essentiellementen chirurgie pour <strong>la</strong> désinfection des p<strong>la</strong>ies. Ces sprays sont d’une efficacitélimitée en cas d’infections cutanées graves <strong>du</strong> fait des germes incriminés, dont<strong>la</strong> sensibilité peut être faible, et de leur localisation tissu<strong>la</strong>ire, peu propice à <strong>la</strong>diffusion de l’antibiotique. En outre, les sprays peuvent représenter un risque parrapport à l’émergence des résistances, étant donné l’absence de contrôle desconcentrations en antibiotique au niveau local. Les antiseptiques représententune alternative efficace aux antibiotiques en application topique. Si l’antisepsieest insuffisante, le recours aux antibiotiques administrés par voie systémique doitêtre préféré. Voir aussi chapitre 1.1.4.LMR chlortétracycline: CYCLOSPRAY (Eurovet)chlortétracycline chlorhydrate:min 2,84 g/bombe aérosol de 200 ml etmin 5,68 g/bombe aérosol de 400 mlspray pour appl cutanéePosologie:Bo, Ov, porcelet: p<strong>la</strong>ies : 1 xBo, Ov: ongles/sabots: 1-3 jViande: 0 j, Lait: 0 jspray 200 ml, 400 mlR/LMR oxytétracycline: ENGEMYCIN spray (MSD A.H.)oxytétracycline chlorhydrate: 5 gspray pour appl cutanéePosologie:Bo, Su, Ov: pulvériser 1 - 2 sec jusqu’à ceque <strong>la</strong> zone traitée ait une couleur homogène(2 x pj, 1 - 3 j)Viande: Bo, Su, Ov: 0 j, Lait: Bo, Ov: 0 jEnlever <strong>la</strong> partie colorée de <strong>la</strong> peau chez le porcf<strong>la</strong>con 1 x 200 mlR/NIXAL spray (Norbrook Lab)oxytétracycline chlorhydrate: 32,1 mg/mlspray pour appl cutanéePosologie:OvViande: 0 j, Lait: 0 jspray 140 gR/OXYTEM spray (Emdoka)oxytétracycline chlorhydrate: 5 gspray pour appl cutanéePosologie:Bo, Ca, Fe: vaporiser <strong>du</strong>rant 2-10 secBo: Viande et abats: 0 j, Lait: 0 jf<strong>la</strong>con 200 mlR/12.1.3 Substances antiparasitaires à usage topique, actives contre lesectoparasitesCes préparations, bien qu’ayant une action localisée au niveau de <strong>la</strong> peau justifiantleur p<strong>la</strong>ce dans ce chapitre, peuvent donner lieu à des intoxications en casd’absorption orale ou de surdosage. Le contact avec <strong>la</strong> peau des animaux traités ouavec le pro<strong>du</strong>it lui-même devrait être évité par précaution, surtout chez les enfants.Un grand nombre de pro<strong>du</strong>its pouvant être utilisés dans <strong>la</strong> lutte contre les ectoparasiteschez les animaux sont commercialisés comme biocides. Ces pro<strong>du</strong>itsn’ayant pas le statut de médicament, ils ne sont pas repris dans ce répertoire. Pourplus d’information, consulter le Folia veterinaria 2004 n°2.
12 MÉDICAMENTS À USAGE EXTERNE 195Des informations comme <strong>la</strong> <strong>du</strong>rée d’action, les modalités particulières d’emploi oudes indications spécifiques comme l’allergie aux piqures de puces chez le chien,sont particulières à chaque médicament. Il convient de consulter les RCP pour enprendre connaissance.12.1.3.1 Organophosphorés etcarbamatesIndicationsLes substances reprises ci-dessoussont utilisées contre les puces et lestiques chez les chiens et les chats,et contre les poux rouges chez lespoules.PharmacodynamieLes organophosphorés et les carbamatesagissent en bloquant l’acétylcholinestérasedont le rôle est dedégrader l’acétylcholine (Ach). Cetteinhibition entraîne une accumu<strong>la</strong>tionde ce neuromédiateur au niveausynaptique et con<strong>du</strong>it à une stimu<strong>la</strong>tionexcessive des récepteurs muscariniqueset nicotiniques. Le sulfated’atropine est un antidote.PharmacocinétiqueLa résorption <strong>du</strong> phoxime appliqué sur<strong>la</strong> peau est minime (0,5 à 3 % de <strong>la</strong>dose).Le dimpy<strong>la</strong>te administré par le biaisdes colliers, est libéré plus longuementsous forme de gaz et se distribue surtoute <strong>la</strong> surface corporelle.Le propoxur est libéré par le colliersous forme de poudre microfine etréparti sur le corps de l’animal.Contre-indicationsL’administration aux jeunes animauxou aux animaux débilités est contreindiquée.En fonction de <strong>la</strong> substanceactive, on cite également les contreindicationssuivantes: <strong>la</strong> colique, <strong>la</strong>diarrhée, <strong>la</strong> constipation, l’insuffisancecardiaque, les bronchospasmes oules affections rénales. Le médicamentà base de phoxime ne peut pas êtreadministré aux animaux dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humaine.Effets indésirablesLes effets indésirables apparaissentsuite à l’inhibition de l’acétylcholine estérase.La stimu<strong>la</strong>tion des récepteursmuscariniques in<strong>du</strong>it de <strong>la</strong> salivation,des vomissements, de <strong>la</strong> bradycardie,de l’hypotension, <strong>du</strong> myosis, <strong>du</strong>bronchospasme, de l’hypersécrétiondes muqueuses respiratoires. Cet ensemblede symptômes peut toutefoisêtre perturbé par l’action nicotinique,possible au niveau ganglionnaire,aboutissant à des effets neurovégétatifsinverses comme de <strong>la</strong> mydriase, de<strong>la</strong> tachycardie et de l’hypertension. Lastimu<strong>la</strong>tion des récepteurs nicotiniques<strong>du</strong> système nerveux central expliqueles convulsions alors que les tremblementsmuscu<strong>la</strong>ires sont le résultatd’une action directe sur <strong>la</strong> p<strong>la</strong>que neuromotrice.Les effets neurovégétatifspeuvent être contrôlés par l’atropine(atropinisation). Les tranquillisantspeuvent contribuer à atténuer leseffets centraux. Ils sont d’autant plusintéressants qu’ils peuvent exercer uneffet myore<strong>la</strong>xant. Théoriquement, lestremblements muscu<strong>la</strong>ires peuventêtre inhibés par les paralysants neuromuscu<strong>la</strong>ireshyperpo<strong>la</strong>risants maisleur emploi reste difficile en pratique.L’hyperthermie peut être limitée enaspergeant l’animal d’eau froide.L’emploi des régénérateurs de l’acétylcholinestéraseest envisageable dansles cas d’intoxication aux organophosphorés,à condition d’agir très rapidementaprès l’intoxication.InteractionsL’association d’organophosphorés etde carbamates, ou de ces substancesavec d’autres inhibiteurs de <strong>la</strong> choline-estérase(lévamisole, néostigmine,pyrantel, morantel) accroît leur actiontoxique. Le phoxime peut accroître leseffets indésirables des myore<strong>la</strong>xantsdépo<strong>la</strong>risants. On évitera l’usage deces substances <strong>du</strong>rant les 10 joursprécédant et suivant l’administrationde phoxime. Le phoxime ne doit pasêtre administré simultanément auxphénothiazines. Ajoutons que certainsorganophosphorés, comme les composéssoufrés, peuvent inhiber le cytochromeP450 hépatique et ralentir <strong>la</strong>détoxification d’autres xénobiotiques.Précautions particulières/Risquespour l’hommeLes colliers doivent être enlevés 24 à48 heures avant chaque anesthésie.L’absorption digestive, cutanée etrespiratoire étant possible, les précautionsparticulières d’emploi sont à respecterplus que jamais. Il est conseilléde lire attentivement les notices pourle traitement des jeunes animaux etdes femelles gestantes et al<strong>la</strong>itantes.Eviter le contact avec <strong>la</strong> peau et lesmuqueuses.
19612 MÉDICAMENTS À USAGE EXTERNERepro<strong>du</strong>ction et <strong>la</strong>ctationSelon le titu<strong>la</strong>ire d’enregistrement, lephoxime peut être administré par voietopique chez des animaux dont <strong>la</strong> gestationest presque à terme. L’usage decolliers à base de dimpy<strong>la</strong>te en périodede gestation est déconseillé par le titu<strong>la</strong>ired’enregistrement.Dimpy<strong>la</strong>teLMR dimpy<strong>la</strong>te: PREVENTEF chat (Virbac)dimpy<strong>la</strong>te: 15 g/100 gcollier imprégné à usage cutanéPosologie:Fe (puces: 5 m)collier imprégné 12,5 gPREVENTEF chien (Virbac)dimpy<strong>la</strong>te: 15 g/100 gcollier imprégné à usage cutanéPosologie:Ca (puces: 5 m, tiques: 4 m)collier imprégné 20 gPREVENTEF grand chien (Virbac)dimpy<strong>la</strong>te: 15 g/100 gcollier imprégné à usage cutanéPosologie:Ca (puces: 5 m, tiques: 4 m)collier imprégné 37 gPhoximeLMR phoxime : BYEMITE 500 mg/ml (Bayer)phoxime: 500 mg/mlémulsion à pulvériser pour surfacesPosologie:pulvériser 100 ml d’émulsion/25 l d’eau surles surfaces (pour 1000 p<strong>la</strong>ces de pondeuses)en présence des poules pondeuses(répéter 7 j plus tard)Viande poule pondeuse: 25 j après le 2etraitementOeuf: 12 h (enlever les œufs avant le traitementet les œufs pon<strong>du</strong>s le jour <strong>du</strong> traitement)f<strong>la</strong>con 250 ml, 1000 mlR/SARNACURAN pour-on (Bayer)phoxime: 7,5 g/100 mlsolution à usage cutanéPosologie:Su, porcelet: 4 ml/10 kgViande: 4 semf<strong>la</strong>con 5 x 1 l, 5 lR/SARNACURAN sol (Bayer)phoxime: 500 mg/mlsolution à usage cutanéPosologie:- spray et <strong>la</strong>vage:Su, Ov: 10 ml de pro<strong>du</strong>it/10 l d’eau (1 x)gale: 10 ml de pro<strong>du</strong>it/10 l d’eau ou 20 mlde pro<strong>du</strong>it/10 l d’eau si infestations sévères,2 x à 7 j d’intervalle (Chorioptes, Psoroptes)ou 14 j d’intervalle (Sarcoptes)- dip:Ov: 1 l de pro<strong>du</strong>it/1000 l d’eauViande: Su: 4 sem, Ov: 5 semNe pas administrer aux brebis dont le <strong>la</strong>it estdestiné à <strong>la</strong> consommation humainef<strong>la</strong>con 250 ml, 1 lR/PropoxurLMR propoxur : BOLFO shampoo (Bayer)propoxur: 1,1 mg/mlshampooing à usage cutanéPosologie:Ca (âge > 3 m)f<strong>la</strong>con 250 mlBOLFO spray (Bayer)propoxur: 2,5 mg/mgspray à usage cutanéPosologie:Ca, Fe (âge > 3 m)aérosol 250 mlCOLLIER PROPOXUR petits chiens et chats(Bayer)propoxur: 1,145 gcollier imprégné à usage cutanéPosologie:Ca, Fe (puces: 4 m, tiques: 8 sem)collier imprégné 36 cmCOLLIER PROPOXUR chiens moyens et grands(Bayer)propoxur: 3,854 gcollier imprégné à usage cutanéPosologie:Ca (puces: 4 m, tiques: 8 sem)collier imprégné 66 cm12.1.3.2 PyréthrinoïdesIndicationsLes pyréthrinoïdes sont utilisés, selonles principes actifs et les formu<strong>la</strong>tions,pour lutter contre les diptères, les acarienset les poux chez les bovins et lesovins, et contre les puces et les tiqueschez les chiens.PharmacodynamieLes pyréthrinoïdes sont des liaisonssynthétiques. Leur structure est dérivéedes pyréthrines, insecticidesnaturels issus de <strong>la</strong> fleur <strong>du</strong> pyrèthre,facilement dégradées par <strong>la</strong> lumièreet <strong>la</strong> chaleur. Les pyréthrinoïdes sontdes insecticides synthétiques, moinsphoto sensibles et, par conséquent,plus rémanents et plus puissants.Chez l’insecte, ils ont une action neu-
12 MÉDICAMENTS À USAGE EXTERNE 197rotrope caractérisée par une dépo<strong>la</strong>risationdes centres nerveux via uneinteraction avec les canaux à sodium,les récepteurs GABA et ceux <strong>du</strong> glutamateaboutissant à un effet “knockdown”.PharmacocinétiqueLes pyréthrinoïdes à usage topiquesont à peine résorbés par les animauxà sang chaud. Ils se diffusent rapidementsur <strong>la</strong> surface corporelle. Lorsd’ingestion orale (accidentelle), leurmétabolisation par les estérases sanguineset hépatiques est très rapideet limite leur toxicité chez les mammifères.Ils sont conjugués puis éliminéspar les urines.Contre-indicationsNe pas utiliser chez les jeunes chiens(l’âge mentionné dans les noticesvarie). Ne pas administrer aux chats,surtout les chatons en dessous de sixsemaines, car ils sont particulièrementsensibles vu leur capacité métaboliqueplus faible que celle des autresespèces. (Voir aussi Folia Veterinaria2008 n° 2 et 2010 n° 2)Effets indésirablesLes pyréthrinoïdes sont réputés trèspeu toxiques lorsque les modalitésd’usage sont respectées. Néanmoins,ils peuvent donner lieu à des effetstoxiques chez l’hôte en cas d’ingestionorale (accidentelle). De l’hypersalivation,des vomissements, de l’ataxie,de <strong>la</strong> diarrhée, de l’hyper- ou hypothermie,des symptômes cutanés, commede <strong>la</strong> dépi<strong>la</strong>tion voire de l’érythèmemarqué au site d’application, sont leseffets indésirables les plus courammentobservés en cas d’intoxication.Des réactions d’hypersensibilité nesont pas à exclure. Des fascicu<strong>la</strong>tionsmuscu<strong>la</strong>ires et des convulsionspeuvent apparaître. La mort survient<strong>du</strong> fait de <strong>la</strong> détresse respiratoire. Lescirconstances d’intoxication sont souventliées à une ingestion accidentelleet à un surdosage. En cas d’intoxication,il est utile de <strong>la</strong>ver l’animal et delui administrer des émétisants et <strong>du</strong>charbon activé en cas d’ingestion. Untraitement symptomatique doit êtremis en p<strong>la</strong>ce.InteractionsLeur action peut être potentialisée parle pipéronyle butoxide qui inhibe lemétabolisme microsomal responsablede l’inactivation chez l’insecte. Chez lecheval, <strong>la</strong> perméthrine prolonge parfoisl’action des barbituriques. Associésaux organophosphorés, les pyréthrinoïdesvoient leur action potentialisée.L’administration concomitante de phénothiazinespeut faciliter l’apparitionde crises d’épilepsie.Précautions particulièresLes chats sont très sensibles auxpyréthrinoïdes et pourraient mêmeprésenter des effets indésirables encas de contact étroit avec des chiensvenant d’être traités. Il faut éviter queles chatons ne lèchent un animal traité.(Voir aussi Folia Veterinaria 2008 n° 2et 2010 n° 2) Le respect des noticesquant aux espèces cibles est important.Les poissons sont extrêmementsensibles à ces dérivés. Il est doncconseillé de prendre toutes les précautionsnécessaires lors de l’utilisation enleur présence. Des cas de résistancecontre certains pyréthrinoïdes tels que<strong>la</strong> deltaméthrine ont été rapportéspour certains parasites.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes titu<strong>la</strong>ires d’enregistrement ne déconseillentpas l’usage <strong>du</strong>rant <strong>la</strong> gestationou <strong>la</strong> <strong>la</strong>ctation.DeltaméthrineLMR deltaméthrine : BUTOX PROTECT 7,5 mg/ml (MSD A.H.)deltaméthrine: 7,5 mg/mlsuspension à usage cutanéPosologie:- mouches:Bo:10 ml (PV < 100 kg), 20 ml (100 kg > PV< 300 kg) ou 30 ml (PV > 300 kg)répéter éventuellement toutes les 6-10 sem)- poux et mélophages:Bo, Ov: 10 ml/animal (traiter les brebis 4-6sem avant <strong>la</strong> mise bas)Viande et abats: Bo: 18 j, Ov: 1 jLait: Bo: 0 j, Ov: 12 hf<strong>la</strong>con 1 l et 2,5 lR/SCALIBOR PROTECTORBAND 48 cm (MSD A.H.)deltaméthrine: 0,760 g/collier (48 cm, 19 g)collier imprégné à usage cutanéPosologie:petit chien ou chien moyen (âge > 7 sem)moustiques, tiques, phlébotomes : 5 - 6 mcollier 1SCALIBOR PROTECTORBAND 65 cm (MSD A.H.)deltaméthrine: 1,000 g/collier (65 cm, 25 g)collier imprégné à usage cutanéPosologie:grand chien (âge > 7 sem)moustiques, tiques, phlébotomes : 5 - 6 mcollier 1
19812 MÉDICAMENTS À USAGE EXTERNEFluméthrineLMR fluméthrine : BAYTICOL pour-on 1 % (Bayer)fluméthrine: 10 mg/mlsolution à usage cutanéPosologie:Bo:- acariens de gale, poux:2 mg/kg ou 20 ml/100 kg PV- tiques: 1 mg/kg ou 10 ml/100 kg PV(peut être répété après 14 j)Viande: 5 j, Lait: 8 jf<strong>la</strong>con 1 l, 5 lR/PerméthrineLMR perméthrine : DEFENDOG (Virbac)perméthrine (40:60) technique: 2 g/100 mlsolution à usage cutanéPosologie:Ca (> 3 m): 100 mg/kg (vaporiser 5 x/kg)puces: 60 j, poux: 30 jf<strong>la</strong>con 250 mlEXSPOT spot-on chien (MSD A.H.)perméthrine: 731 mg/mlsolution à usage cutanéPosologie:Ca (âge > 2 sem):- PV < 15 kg: 1 ml- PV > 15 kg et < 30 kg: 2 ml- PV = ou > 30 kg: 3 mlpuces, tiques: 2-4 semampoule 12 x (6 x 1 ml)12.1.3.3 FipronilIndicationsLe fipronil, destiné aux chiens et auxchats, appartient à <strong>la</strong> famille desphénylpyrazolés. Il est actif contreles puces, les tiques et certainsacariens responsables de gales oupseudo-gales.PharmacodynamieIl agit par blocage <strong>du</strong> transfert desions chlore et inhibition <strong>du</strong> complexeGABA, entraînant une hyperstimu<strong>la</strong>tionde l’insecte. Le fipronil est actifprincipalement comme a<strong>du</strong>lticide.PharmacocinétiqueAprès application cutanée, <strong>la</strong> moléculeest peu résorbée et persiste longtempssur <strong>la</strong> peau, ce qui permet d’espacerles administrations (environ 1 mois).Contre-indicationsNe pas administrer Fipronil spot-on®aux chiots et chatons âgés de moinsde 8 semaines ou pesant moins de 2kg (chien) ou de 1 kg (chat). Ne pasutiliser chez les animaux ma<strong>la</strong>des(ma<strong>la</strong>dies systémiques, fièvre …) ouconvalescents. Ne pas administrer aux<strong>la</strong>pins.Effets indésirablesLes risques d’intoxication sont peuimportants. En cas de léchage, unebrève période d’hypersalivation <strong>du</strong>e à<strong>la</strong> nature <strong>du</strong> solvant peut être observée.Parmi les effets indésirables extrêmementrares, des réactions cutanées transitoires(érythème, prurit, alopécie) ontété rapportées. Exceptionnellement, del’hypersalivation, des symptômes neurologiquesréversibles (hyperesthésie,dépression, symptômes nerveux), desvomissements ou des symptômes respiratoiresont été observés après utilisation.Ne pas surdoser. L’utilisation <strong>du</strong>spray chez de jeunes animaux ou desanimaux débilités pourrait avoir desissues fatales par l’inha<strong>la</strong>tion de l’isopropanolutilisé comme solvant.Précautions particulièresIl est important de veiller à ce que lesanimaux ne se lèchent pas entre euxaprès le traitement. Les immersionsdans l’eau (bains, nage) dans les 2jours suivant l’application <strong>du</strong> pro<strong>du</strong>itdevraient être évitées.Repro<strong>du</strong>ction et <strong>la</strong>ctationLe pro<strong>du</strong>it peut être administré pendant<strong>la</strong> gestation et <strong>la</strong> <strong>la</strong>ctation.LMR fipronil: EFFIPRO SPOT-ON 50 mg chats (Virbac)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Fe: 1 pipette/animal (4 sem d’intervalle aumoins) (puces: 5 sem, tiques: 2 sem)pipette 4 ou 24 x 0,5 mlEFFIPRO SPOT-ON 67 mg petits chiens (Virbac)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (2 - 10 kg PV): 1 pipette/animal (4 semd’intervalle au moins)pipette 4 ou 24 x 0,67 mlEFFIPRO SPOT-ON 134 mg chiens moyens(Virbac)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (10 - 20 kg PV): 1 pipette/animal (4 semd‘intervalle au moins) (puces: 8 sem, tiques:4 sem)pipette 4 ou 24 x 1,34 mlEFFIPRO SPOT-ON 268 mg grands chiens (Virbac)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (20 - 40 kg PV): 1 pipette/animal (4 semd‘intervalle au moins) (puces: 8 sem, tiques:4 sem)pipette 4 ou 24 x 2,68 ml
12 MÉDICAMENTS À USAGE EXTERNE 199EFFIPRO SPOT-ON 402 mg très grands chiens(Virbac)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (40 - 60 kg PV): 1 pipette/animal (4 semd‘intervalle au moins) (puces: 8 sem, tiques:4 sem)pipette 4 ou 24 x 4,02 mlEFFIPRO spray 2,5 mg/ml (Virbac)fipronil: 2,5 mg/mlspray à usage cutanéPosologie:Ca, Fe: 7,5 - 15 mg/kg(4 sem d‘intervalle au moins)f<strong>la</strong>con 100 ml, 250 ml, 500 mlELIMINALL 50 spot-on chats (KRKA)fipronil: 50 mg/pipetsolution à usage cutanéPosologie:Fe (âge > 8 sem, PV > 1 kg):1 pipette/animalpuces, tiques: 4 sempipette 3, 6, 30ELIMINALL 67-134-268-402 spot-on chiens(KRKA)fipronil: 67 mg-134 mg-268 mg-402 mg/pipettesolution à usage cutanéPosologie:Ca (âge > 8 sem):PV > 2-10 kg:1 pipette de 67 mg/animal (0,67 ml)PV > 10-20 kg:1 pipette de 134 mg/animal (1,34 ml)PV > 20-40 kg:1 pipette de 268 mg/animal (2,68 ml)PV > 40-60 kg:1 pipette de 402 mg/animal (4,02 ml)PV > 60 kg: 1 pipette de 402 mg + pipetteadaptée au poidspuces – tiques: 4 sempipette 3, 6, 30FIPROSPOT 50 mg (IDT Biologika)fipronil: 50 mgsolution à usage cutanéPosologie:Fe (PV > 1 kg, âge > 8 sem): 5 mg/kgrespecter intervalle de min 4 sem entre 2traitementspuces: 4 sem, tiques: max 1 sempipette 3, 6FIPROSPOT 67 mg (IDT Biologika)fipronil: 67 mgsolution à usage cutanéPosologie:Ca (PV 2 - 10 kg), (PV > 2 kg, âge > 2 m) :6,7 mg/kgrespecter intervalle de min 4 sem entre 2traitementspuces: 6 sem, tiques: 3 - 4 sempipette 3, 6FIPROSPOT 134 mg (IDT Biologika)fipronil: 134 mgsolution à usage cutanéPosologie:Ca (PV 10 - 20 kg): 6,7 mg/kg(min 4 sem entre 2 traitements)puces: 6 sem, tiques: 3 - 4 sempipette 3, 6FIPROSPOT 268 mg (IDT Biologika)fipronil: 268 mgsolution à usage cutanéPosologie:Ca (PV 20 - 40 kg): 6,7 mg/kg(min 4 sem entre 2 traitements)puces: 6 sem, tiques: 3 - 4 sempipette 3, 6FIPROSPOT 402 mg (IDT Biologika)fipronil: 402 mgsolution à usage cutanéPosologie:Ca (PV 40 - 60 kg): 6,7 mg/kg(min 4 sem entre 2 traitements)puces: 6 sem, tiques: 3 - 4 sempipette 3, 6FLEVOX 50 mg sol spot-on chat (Vétoquinol)fipronil: 50 mg/pipette de 0,5 mlsolution à usage cutanéPosologie:Fe (âge > 8 sem, PV > 1 kg):1 pipette de 0,5 ml/animalpuces: 4 sem, tiques: 1 sempipette 36FLEVOX 67 mg sol spot-on chien S (Vétoquinol)fipronil: 67 mg/pipette de 0,67 mlsolution à usage cutanéPosologie:Ca (2 - 10 kg, âge > 8 sem):1 pipette de 0,67 ml/animalpuces: 8 sem, tiques: 3-4 sempipette 36FLEVOX 134 mg sol spot-on chien M (Vétoquinol)fipronil: 134 mg/pipette de 1,34 mlsolution à usage cutanéPosologie:Ca (10 - 20 kg, âge > 8 sem):1 pipette de 1,34 ml/animalpuces: 8 sem, tiques: 3-4 sempipette 36FLEVOX 268 mg sol spot-on chien L (Vétoquinol)fipronil: 268 mg/pipette de 2,68 mlsolution à usage cutanéPosologie:Ca (20 - 40 kg, âge > 8 sem):1 pipette de 2,68 ml/animalpuces: 8 sem, tiques: 3-4 sempipette 36FLEVOX 402 mg sol spot-on chien XL (Vétoquinol)fipronil: 402 mg/pipette de 4,02 mlsolution à usage cutanéPosologie:Ca (40 - 60 kg, âge > 8 sem):1 pipette de 4,02 ml/animalpuces: 8 sem, tiques: 3-4 sempipette 36FRONTLINE spot-on chat (Merial)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Fe (âge > 8 sem, PV > 1 kg):1 pipette/animal (puces: 1 m, tiques: 17 j)pipette 3 ou 6 x 0,5 ml
20012 MÉDICAMENTS À USAGE EXTERNEFRONTLINE spot-on chien 0,67 ml (Merial)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, 2 - 10 kg PV):1 pipette/animal(puces: max 3 m, tiques: 1 m)pipette 3 ou 6 x 0,67 mlFRONTLINE spot-on chien 1,34 ml (Merial)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, 10 kg - 20 kg PV):1 pipette/animal(puces: max 3 m, tiques: 1 m)pipette 3 ou 6 x 1,34 mlFRONTLINE spot-on chien 2,68 ml (Merial)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, 20 kg - 40 kg PV):1 pipette/animal(puces: max 3 m, tiques: 1 m)pipette 3 ou 6 x 2,68 mlFRONTLINE spot-on chien 4,02 ml (Merial)fipronil: 100 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, 40 - 60 kg):1 pipette/animalCa (> 60 kg): 1 pipette (4,02 ml) + pipetteappropriée au restant <strong>du</strong> poids(puces: max 3 m, tiques: 1 m)pipette 3 ou 6 x 4,02 mlFRONTLINE spray (Merial)fipronil: 250 mg/100 mlsolution à usage cutanéPosologie:Ca, Fe: 7,5 - 15 mg/kg (puces: 1 - 3 m,tiques: 3 - 5 sem)f<strong>la</strong>con 100 ml, 250 ml12.1.3.4 PyriproleIndicationsTraitement et prévention des infestationspar les puces (Ctenocephalides canis etC. felis) et/ou par les tiques (Ixodes ricinus,Rhipicephalus sanguineus, Ixodesscapu<strong>la</strong>ris, Dermacentor reticu<strong>la</strong>tus,Dermacentor variabilis, Amblyommaamericanum) chez le chien.PharmacodynamieLe pyriprole est un dérivé de <strong>la</strong> familledes phénylpyrazolés et interagit avecles récepteurs GABA en inhibant lepassage pré- et post-synaptique desions chlorures à travers <strong>la</strong> membranecellu<strong>la</strong>ire. Ce<strong>la</strong> provoque un dérèglement<strong>du</strong> système nerveux central et<strong>la</strong> mort des puces et tiques. L’actioninsecticide intervient principalementaprès ingestion de <strong>la</strong> substance activepar les parasites. Le pyriprole tue lespuces en 24 heures et les tiques en48 heures après leur exposition aupro<strong>du</strong>it. Après traitement, les tiquesse détachent de l’hôte dans les 24 à48 heures après infestation. Quelquestiques peuvent cependant rester fixéessur l’animal. La transmission de ma<strong>la</strong>diesinfectieuses par les tiques nepeut donc pas être totalement exclue.L’efficacité contre les puces et lestiques persiste 4 semaines.PharmacocinétiqueAprès administration cutanée, le pyriproleest distribué dans le pe<strong>la</strong>ge <strong>du</strong>chien en un jour. Il est ensuite stockédans les g<strong>la</strong>ndes sébacées et libéréprogressivement. Le pro<strong>du</strong>it est partiellementrésorbé, métabolisé dans lefoie et excrété par les fèces.Contre-indicationsNe pas utiliser chez les chiots âgés demoins de 8 semaines et/ou chez leschiens pesant moins de 2 kg. Ne pasutiliser chez les animaux ma<strong>la</strong>des ouconvalescents. Ne pas utiliser chez leschats ou les <strong>la</strong>pins.Effets indésirablesUne décoloration de <strong>la</strong> fourrure, del’alopécie ou <strong>du</strong> prurit peuvent apparaîtrelocalement. Une hypersalivationpeut être observée si l’animal lèche<strong>la</strong> zone d’application (sur lui ou surd’autres animaux) immédiatementaprès le traitement.InteractionsAucune interaction connue.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> médicament n’a pas étéétablie chez les femelles gestantes oual<strong>la</strong>itantes, ni chez les animaux repro<strong>du</strong>cteurs.Des études chez des animauxde <strong>la</strong>boratoire n’ont révélé aucuneffet sur <strong>la</strong> repro<strong>du</strong>ction ou le développementfœtal. N’utiliser le médicamentqu’après évaluation <strong>du</strong> rapportbénéfice/risque.LMR pyriprole : PRAC-TIC 56,25 mg sol spot-on très petits chiens(Novartis)pyriprole: 125 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV > 2 kg): 12,5 mg/kg PVpuces - tiques: 4 sempipette (0,45 ml) 1 x 3R/PRAC-TIC 137,5 mg sol spot-on petits chiens(Novartis)pyriprole: 125 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV > 2 kg): 12,5 mg/kg PVpuces - tiques: 4 sempipette (1,1 ml) 1 x 3, 2 x 3R/
12 MÉDICAMENTS À USAGE EXTERNE 201PRAC-TIC 275 mg sol spot-on chiens moyens(Novartis)pyriprole: 125 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV > 2 kg): 12,5 mg/kg PVpuces - tiques: 4 sempipette (2,2 ml) 1 x 3, 2 x 3R/PRAC-TIC 625 mg sol spot-on grands chiens(Novartis)pyriprole: 125 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV > 2 kg): 12,5 mg/kg PVpuces - tiques: 4 sempipette (5,0 ml) 1 x 3, 2 x 3R/12.1.3.5 ImidacloprideIndicationsL’imidaclopride est utilisé dans <strong>la</strong> préventionet le traitement des infestationsde puces et le traitement de pouxbroyeurs (Trichodectes canis) chezles chiens, et dans le traitement despuces chez les chats. L’imidaclopridea une action rapide contre les pucesa<strong>du</strong>ltes.PharmacodynamieL’imidaclopride est une molécule de <strong>la</strong>famille des nitroguanidines qui exerceun effet antagoniste au niveau desrécepteurs nicotiniques post-synaptiquesde <strong>la</strong> puce. Ce principe actifagit rapidement par contact direct <strong>du</strong>parasite avec <strong>la</strong> peau sans dépendrede <strong>la</strong> prise d’un repas sanguin.L’imidaclopride est surtout actif contreles a<strong>du</strong>ltes (a<strong>du</strong>lticide) mais possèdeaussi une activité contre les stades <strong>la</strong>rvairesprésents dans l’environnement(<strong>la</strong>rvicide).PharmacocinétiqueAprès administration topique, l’imidacloprideest distribué dans le sébum,dont il est progressivement excrété.Il n’y a pas d’absorption systémiqueaprès administration locale.Contre-indicationsLes animaux non sevrés de moins de 8semaines ne peuvent être traités avecce pro<strong>du</strong>it.Effets indésirablesCette molécule possède une grandemarge de sécurité et peut s’utiliser encombinaison avec d’autres insecticides.De <strong>la</strong> salivation peut être observéeaprès l’application <strong>du</strong> médicamentquand le pro<strong>du</strong>it est léché par l’animal.InteractionsAucune interaction connue.Repro<strong>du</strong>ction et <strong>la</strong>ctationSelon des études menées chez les ratset les <strong>la</strong>pins, ainsi que des études limitéeschez les chiennes et les chattesen gestation et al<strong>la</strong>itantes en contactavec leur portée, on peut admettre quel’usage <strong>du</strong> pro<strong>du</strong>it est sûr en périodede gestation ou de <strong>la</strong>ctation.LMR imidaclopride: ADVANTAGE 40 chat (Bayer)imidaclopride: 40 mgsolution à usage cutanéPosologie:Fe (> 8 sem):(< 4 kg PV): 1 pipette/animal(puces: 3 - 4 sem)pipette 4 x 0,4 mlADVANTAGE 80 chat (Bayer)imidaclopride: 80 mgsolution à usage cutanéPosologie:Fe (> 8 sem):(> 4 kg PV): 1 pipette/animal(puces: 3 - 4 sem)pipette 4 x 0,8 mlADVANTAGE 40 chien (Bayer)imidaclopride: 40 mgsolution à usage cutanéPosologie:Ca (> 8 sem):(< 4 kg PV): 1 pipette/animal(puces: 4 sem)pipette 4 x 0,4 mlADVANTAGE 100 chien (Bayer)imidaclopride: 100 mgsolution à usage cutanéPosologie:Ca (> 8 sem):(4 - < 10 kg PV): 1 pipette/animal(puces: 4 sem)pipette 4 x 1 mlADVANTAGE 250 chien (Bayer)imidaclopride: 250 mgsolution à usage cutanéPosologie:Ca (> 8 sem):(10 - < 25 kg PV): 1 pipette/animal(puces: 4 sem)pipette 4 x 2,5 mlADVANTAGE 400 chien (Bayer)imidaclopride: 400 mgsolution à usage cutanéPosologie:Ca (> 8 sem):- (25 - < 40 kg PV): 1 pipette/animal- (> 40 kg PV): 2 pipettes/animal(puces: 4 sem)pipette 4 x 4 ml12.1.3.6 MétaflumizoneIndicationsTraitement et prévention des infestationspar les puces (Ctenocephalidescanis et C. felis) chez les chats et leschiens (voir chapitre 12.1.3.9, pour lemédicament destiné aux chiens).
20212 MÉDICAMENTS À USAGE EXTERNEPharmacodynamieLa métaflumizone, insecticide appartenantau groupe des semicarbazones(dérivé de <strong>la</strong> pyrazolone), est un antagonistedes canaux sodiques et interromptle fonctionnement <strong>du</strong> systèmenerveux, provoquant <strong>la</strong> paralysie et <strong>la</strong>mort des insectes. L’action insecticidese déclenche principalement aprèsingestion de <strong>la</strong> substance par le parasite.L’efficacité maximale est atteintedans les 48 heures.PharmacocinétiqueAprès une administration topique, <strong>la</strong>métaflumizone est rapidement distribuéeà <strong>la</strong> surface de <strong>la</strong> peau. Lesconcentrations maximales dans lespoils ont été obtenues en général dansles 1 à 2 jours après le traitement. Laconcentration dans les poils reste élevée,jusqu’à 42 jours au moins après letraitement.Contre-indicationsNe pas administrer aux animaux âgésde moins de 8 semaines. L’utilisationchez les animaux débilités ou ma<strong>la</strong>desdemande une évaluation <strong>du</strong> rapportbénéfice/risque.Effets indésirablesLa métaflumizone possède une toxicitémammifère minime. Une hypersalivationpeut être observée en cas deléchage <strong>du</strong> site d’application.InteractionsAucune interaction connue.Précautions particulières/Risquespour l’hommeEviter tout contact direct avec <strong>la</strong> peau,<strong>la</strong> bouche et les yeux lorsque l’on administrele pro<strong>du</strong>it.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> médicament vétérinairen’a pas été établie pendant <strong>la</strong> gestationet <strong>la</strong> <strong>la</strong>ctation. Des études menées avec<strong>la</strong> métaflumizone chez les rats et/oules <strong>la</strong>pins n’ont montré aucun effet tératogèneou toxique sur le fœtus ou <strong>la</strong>mère. A n’utiliser qu’après évaluation<strong>du</strong> rapport bénéfice/risque (le pro<strong>du</strong>itdestiné aux chiens et associant del’amitraz à <strong>la</strong> métaflumizone, ne peutpas être administré en période de gestationou de <strong>la</strong>ctation en raison de <strong>la</strong>présence d’amitraz).LMR métaflumizone: PROMERIS spot-on chats (Pfizer A.H.)métaflumizone: 200 mg/mlsolution à usage cutanéPosologie:Fe (âge > 8 sem): 40 mg/kg PVpuces: 6 sempipette 3 ou 6 x 0,80 ml ou 1,60 mlR/12.1.3.7 AmitrazIndicationsL’amitraz est potentiellement actifcontre les poux, les tiques, les puceset les agents des gales.PharmacodynamieL’amitraz est un insecticide de <strong>la</strong>famille des formamidines, agissantcomme agoniste des récepteurs d’octopaminedans les synapses excitatrices<strong>du</strong> système nerveux central desinsectes. Cette substance inhiberait<strong>la</strong> monoamine oxydase (MAO) maispossède surtout des propriétés alpha-2-adrénergiques chez les mammifères.PharmacocinétiqueL’absorption transcutanée est lente etpartielle mais peut donner lieu à desinteractions avec d’autres substancesayant des mécanismes d’action comparables,et entraîner des temps d’attentechez les espèces pro<strong>du</strong>ctricesde denrées alimentaires. L’amitraz estrésorbé par voie orale. Il est métabolisé,notamment en 4-amino-3-méthylbenzoïque,avant d’être éliminéessentiellement par voie urinaire.Contre-indicationsL’amitraz est contre-indiqué chezcertaines espèces (chat, cheval), certainesraces (chihuahuas) ainsi quedans certains états physiologiques etpathologiques (gestation, <strong>la</strong>ctation,jeunes animaux, sujets débilités).Effets indésirablesL’amitraz ne provoque habituellementpas d’effets indésirables importantslorsqu’il est administré de façon adéquate.Cependant, on peut noter, dansde rares cas, de <strong>la</strong> somnolence, desvomissements, de l’hypothermie, del’hypotension et de <strong>la</strong> bradycardieexpliqués par son action agoniste surles récepteurs alpha-2-adrénergiques.En cas de surdosage important,les antagonistes de ces récepteurspeuvent être utilement administrés.L’application est contre-indiquée chezles animaux exposés au soleil.
12 MÉDICAMENTS À USAGE EXTERNE 203InteractionsIl est déconseillé d’utiliser l’amitrazavec d’autres alpha-2-agonistes, quipourraient augmenter leur toxicité.L’usage simultané avec d’autres inhibiteursde MAO tels que <strong>la</strong> sélégillinep.ex., ou avec des antidépresseurs telsque <strong>la</strong> clomipramine, est déconseillé.Précautions particulièresA utiliser précautionneusement chezles patients souffrant de diabète,l’action alpha-2-adrénergique pouvantaugmenter les concentrations de glucosep<strong>la</strong>smatique.Repro<strong>du</strong>ction et <strong>la</strong>ctationSelon <strong>la</strong> notice, le pro<strong>du</strong>it peut êtreadministré aux bovins, porcs et ovinsgestants ou al<strong>la</strong>itants. L’utilisationchez des chiennes gestantes ou al<strong>la</strong>itantesest déconseillée.LMR amitraz : TAKTIC (MSD A.H.)amitraz: 125 mg/mlconcentré émulsifiable à usage cutanéPosologie:Bo: 2 ml/l d‘eau (répéter après 7 - 10 j)(spray)Su: 4 ml/l d‘eau (répéter après 7 - 10 j)(spray)Ov: 4 ml/l d‘eau (répéter après 14 j) (parspray ou par immersion)Viande: Bo, Su, Ov: 7 j, Lait: Bo, Ov: 7 jf<strong>la</strong>con 1 l, 5 lR/12.1.3.8 IndoxacarbeIndicationsL’indoxacarbe peut être utilisé dans letraitement et <strong>la</strong> prévention des infestationspar les puces (Ctenocephalidesfelis).PharmacodynamieL’indoxacarbe, appartenant à <strong>la</strong> familledes oxadiazines, est un précurseur(pro-drogue) qui déclenche ses effetspharmacodynamiques après bio-activationpar les enzymes de l’insecte. Lemétabolite de l’indoxacarbe est actifcontre les stades a<strong>du</strong>ltes, <strong>la</strong>rvaires etles œufs des insectes. Chez les puces,l’indoxacarbe a une activité a<strong>du</strong>lticideet agit sur les stades <strong>la</strong>rvaires dansl’environnement immédiat de l’animaltraité. L’indoxacarbe pénètre dans l’insectepar voie orale. La molécule estbio-activée au niveau de l’intestin. Lemétabolite actif bloque les canaux sodiquesau niveau <strong>du</strong> système nerveuxcentral, provoquant un arrêt rapide del’alimentation dans les 4 h suivant letraitement, suivi d’un arrêt de <strong>la</strong> ponte(oviposition), de paralysie et de <strong>la</strong> mortdans les 4 à 48 h.PharmacocinétiqueAprès une application unique <strong>du</strong> pro<strong>du</strong>it(spot-on), l’indoxacarbe peutencore être détecté 4 semaines aprèsle traitement, aussi bien dans <strong>la</strong> peauque dans les poils. Il existe égalementune absorption transcutanée, maiscette absorption n’est pas pertinente<strong>du</strong> point de vue de l’efficacité clinique.L’indoxacarbe absorbé est <strong>la</strong>rgementmétabolisé par le foie en divers métabolites.L’excrétion se fait principalementpar les fèces.Contre-indicationsAucune contre-indication connue.Effets indésirablesUne hypersalivation de courte <strong>du</strong>réepeut être observée si l’animal lèchele site d’application immédiatementaprès le traitement. Une irritation transitoireou une perte de poils au niveau<strong>du</strong> site d’application peut survenir.InteractionsAucune interaction connue.Précautions particulières/Risquespour l’hommeL’innocuité <strong>du</strong> pro<strong>du</strong>it n’a pas été établiechez les chiens et les chats âgésde moins de 8 semaines ou chez leschiens pesant moins de 1,5 kg et chezles chats pesant moins de 0,6 kg.Eviter que le site d’application puisseêtre léché par l’animal traité ou pard’autres animaux.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser chez les femelles gestantesou al<strong>la</strong>itantes ou chez les animauxdestinés à <strong>la</strong> repro<strong>du</strong>ction.LMR indoxacarbe: ACTIVYL 100 mg spot-on sol chats de petite taille(MSD A.H.)indoxacarbe: 99,45 mgsolution à usage cutanéPosologie:Fe (âge > 8 sem, PV: 0,6 - 4 kg):min 25 mg/kgpipette 4R/ACTIVYL 200 mg spot-on sol chats de grande taille(MSD A.H.)indoxacarbe: 195 mg/mlsolution à usage cutanéPosologie:Fe (âge > 8 sem, PV > 4 kg): max 50 mg/kgpipette 4R/
20412 MÉDICAMENTS À USAGE EXTERNEACTIVYL 100 mg spot-on sol chiens de très petitetaille (MSD A.H.)indoxacarbe: 99,45 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV: 1,5 - 6,5 kg):min 15 mg/kgpipette 4R/ACTIVYL 150 mg spot-on sol chiens de petite taille(MSD A.H.)indoxacarbe: 150,15 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV: 6,6 -10 kg):15-23 mg/kgpipette 4R/ACTIVYL 300 mg spot-on sol chiens de taillemoyenne (MSD A.H.)indoxacarbe: 300,30 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV: 10,1 - 20 kg):15-30 mg/kgpipette 4R/ACTIVYL 600 mg spot-on sol chiens de grandetaille (MSD A.H.)indoxacarbe: 600,60 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV: 20,1 kg - 40 kg):15-30 mg/kgpipette 4R/12.1.3.9 AssociationsA l’exception <strong>du</strong> (S)-méthoprène (voirplus loin), les substances actives ontété décrites précédemment.Propoxur + fluméthrineL’association de propoxur et de fluméthrinese justifie par l’action synergiqueentre ces substances. Cetteassociation est utilisée contre lesinfestations par les tiques (Ixodes ricinus,Rhipicephalus sanguineus) etles puces (Ctenocephalides canis,Ctenocephalides felis) chez le chien.Le pro<strong>du</strong>it ne peut pas être utilisé chezle chat !LMR propoxur + fluméthrine : KILTIX petits chiens (Bayer)propoxur: 1 g/10 gfluméthrine: 0,225 g/10 gcollier imprégné à usage cutanéPosologie:Capuces, tiques: max 6 mcollier imprégné 35 cm (12,5 g)KILTIX chiens moyens (Bayer)propoxur: 1 g/10 gfluméthrine: 0,225 g/10 gcollier imprégné à usage cutanéPosologie:Capuces, tiques: max 6 mcollier imprégné 48 cm (30,2 g)KILTIX grands chiens (Bayer)propoxur: 1 g/10 gfluméthrine: 0,225 g/10 gcollier imprégné à usage cutanéPosologie:Capuces, tiques: max 6 mcollier imprégné 66 cm (45,0 g)Imidaclopride + perméthrineDans cette association, l’imidaclopriderenforce l’action de <strong>la</strong> perméthrine.Cette dernière, outre son effetinsecticide (Ctenocephalides canis,Ctenocephalides felis) et acaricide(Rhipicephalus sanguineus, Ixodesricinus et Dermacentor reticu<strong>la</strong>tus),repousse les tiques, les phlébotomes(« moucherons des sables ») et lesmoustiques. Ainsi, le risque de morsurespar ces parasites et de transmissionde ma<strong>la</strong>dies, est fortementdiminué. Il est préférable d’ôter lestiques déjà présentes sur le corps<strong>du</strong> chien au moment <strong>du</strong> traitement.L’action répulsive contre les tiquesphlébotomes est de maximum varie de2 semaines. Contre les moustiques,elle varie de 2 à 4 semaines selonl’espèce. L’action répulsive contre lesmouches d’étable <strong>du</strong>re 4 semaines.LMR imidaclopride + perméthrine : ADVANTIX 40/200 sol spot-on (Bayer)imidaclopride: 40 mg/0,4 mlperméthrine: 200 mg/0,4 mlsolution à usage cutanéPosologie:Ca (1,5 kg < PV < 4 kg) (âge > 7 sem): 0,4 mlpuces: 4 sem, tiques: 3-4 sempipette 4 x 0,4 ml, 6 x 0,4 mlADVANTIX 100/500 sol spot-on chien (Bayer)imidaclopride: 100 mg/1 mlperméthrine: 500 mg/1 mlsolution à usage cutanéPosologie:Ca (4 kg < PV < 10 kg) (âge > 7 sem): 1 mlpuces: 4 sem, tiques: 3-4 sempipette 4 x 1 ml, 6 x 1 mlADVANTIX 250/1250 sol spot-on chien (Bayer)imidaclopride: 250 mg/2,5 mlperméthrine: 1250 mg/2,5 mlsolution à usage cutanéPosologie:Ca (10 kg < PV < 25 kg) (âge > 7 sem):2,5 mlpuces: 4 sem, tiques: 3-4 sempipette 4 x 2,5 ml, 6 x 2,5 ml
12 MÉDICAMENTS À USAGE EXTERNE 205ADVANTIX 400/2000 sol spot-on chien (Bayer)imidaclopride: 400 mg/4 mlperméthrine: 2000 mg/4 mlsolution à usage cutanéPosologie:Ca (25 kg < PV < 40 kg) (âge > 7 sem): 4 mlpuces: 4 sem, tiques: 3-4 sempipette 4 x 4 ml, 6 x 4 mlImidaclopride + fluméthrineIndicationsChien:- Traitement et prévention des infestationspar les puces (Ctenocephalidesfelis) et des infestations par les tiques(Ixodes ricinus, Rhipicephalus sanguineus,Dermacentor reticu<strong>la</strong>tus).- Traitement des infestations par lespoux piqueurs/suceurs (Trichodectescanis).PharmacodynamieL’imidaclopride est actif contre lespuces aux stades a<strong>du</strong>lte et <strong>la</strong>rvaireet contre les poux. La fluméthrine estresponsable de l’activité acaricide <strong>du</strong>pro<strong>du</strong>it.PharmacocinétiqueLes deux principes actifs sont libérésde manière lente et continue, à defaibles concentrations, de <strong>la</strong> matricepolymère <strong>du</strong> collier vers l’animal, et sepropagent sur <strong>la</strong> totalité de <strong>la</strong> surfacecutanée. Des études de surdosage etde cinétique sérique chez les chiensont démontré que l’imidaclopride atteignaittransitoirement <strong>la</strong> circu<strong>la</strong>tionsystémique, tandis que <strong>la</strong> fluméthrinen’était généralement pas mesurable.L’absorption orale des deux principesactifs est faible et n’intervient pas dansl’efficacité clinique.Contre-indicationsNe pas traiter les chiots âgés de moinsde 7 semaines.Effets indésirablesUne légère chute de poils et de légèresréactions cutanées peuventsurvenir sur le site d’application etdisparaissent habituellement en 1 ou2 semaines sans que le collier doiveêtre retiré.Précautions particulièresEviter une exposition prolongée etintense à l’eau ou un shampouinageintensif pour ne pas entraver l’efficacité<strong>du</strong> pro<strong>du</strong>it.Repro<strong>du</strong>ction et <strong>la</strong>ctationCe médicament n’a pas d’effets sur <strong>la</strong>fertilité ou <strong>la</strong> repro<strong>du</strong>ction ni d’effetstératogènes ou fœtotoxiques chez lesanimaux de <strong>la</strong>boratoire. L’innocuité dece médicament n’ayant pas été établiechez le chien <strong>du</strong>rant <strong>la</strong> gestation et <strong>la</strong><strong>la</strong>ctation, son utilisation n’est donc pasrecommandée chez les chiennes engestation ou al<strong>la</strong>itantes.LMR imidaclopride + fluméthrine: SERESTO 1,25 g + 0,56 g collier pour chats (Bayer)imidaclopride: 1,250 gfluméthrine: 0,56 gcollier à usage cutanéPosologie:Fe (âge > 10 sem): 1 collier/animalpuce: 7-8 m, tique: 8 mcollier 38 cmR/SERESTO 1,25 g + 0,56 g collier pour chiensjusqu’à 8 kg (Bayer)imidaclopride: 1,250 gfluméthrine: 0,56 gcollier à usage cutanéPosologie:Ca (âge > 7 sem, PV jusqu’à 8 kg):1 collier/animalpuce: 7-8 m, tique: 8 mcollier 38 cmR/SERESTO 4,50 g + 2,03 g collier pour chiens > 8 kg(Bayer)imidaclopride: 4,50 gfluméthrine: 2,03 gcollier à usage cutanéPosologie:Ca (âge > 7 sem, PV > 8 kg): 1 collier/animalpuce: 7-8 m, tique: 8 mcollier 70 cmR/Fipronil + (S)-méthoprèneIndicationsCe médicament combine le fipronil,a<strong>du</strong>lticide et le (S)-méthoprène, régu<strong>la</strong>teurde croissance à activité ovicideet <strong>la</strong>rvicide. Cette combinaison peutêtre utilisée aussi bien chez les chiensque chez les chats, dans le traitementcontre les infestations par lespuces (Ctenocephalides spp.), tiques(Ixodes ricinus, Dermacentor variabilis,Rhipicephalus sanguineus) et/oupoux. Ce pro<strong>du</strong>it pour les chats estégalement indiqué pour le traitementou <strong>la</strong> prévention des infestations pardes puces (Ctenocephalides spp.) etl’élimination des tiques (Ixodes ricinus)chez les furets.PharmacodynamieLe (S)-méthoprène est un régu<strong>la</strong>teurde croissance des insectes. Il interromptle développement vers le stadea<strong>du</strong>lte de <strong>la</strong> puce.PharmacocinétiqueCes deux substances diffusent rapidementsur <strong>la</strong> surface corporelle.L’absorption systémique est très faible.
20612 MÉDICAMENTS À USAGE EXTERNEContre-indicationsNe pas administrer aux animaux âgésde moins de 8 semaines ou aux chatonspesant moins d’1 kg, ni auxchiens pesant moins de 2 kg. Ne pasadministrer aux furets de moins de 6mois. Ne pas administrer à d’autresanimaux que les espèces cibles.Effets indésirablesLe léchage <strong>du</strong> pro<strong>du</strong>it peut provoquerune salivation excessive passagère.D’autres effets indésirables sont rares.InteractionsAucune interaction connue.Précautions particulièresLe (S)-méthoprène est toxique pour lesorganismes aquatiques (invertébrés etvertébrés).Repro<strong>du</strong>ction et <strong>la</strong>ctationLe médicament ci-dessous peut êtreadministré pendant <strong>la</strong> gestation ou <strong>la</strong><strong>la</strong>ctation chez le chien et le chat. Chezle furet, l’innocuité de ce médicamentn’a pas été démontrée <strong>du</strong>rant <strong>la</strong> gestationet <strong>la</strong> <strong>la</strong>ctation. L’utilisation nedoit se faire qu’après une évaluationbénéfice/risque.LMR fipronil + (S)-méthoprène : FRONTLINE COMBO spot-on chat (Merial)(S)-méthoprène: 60 mgfipronil: 50 mgsolution à usage cutanéPosologie:Fe: (âge > 8 sem) (PV > 1 kg):1 pipette/animal/4 semfuret (âge > 6 m): 1 pipette/animal/4 sempipette 3 x 0,5 ml ou 6 x 0,5 mlR/FRONTLINE COMBO spot-on chien S (Merial)(S)-méthoprène: 60,3 mgfipronil: 67 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem) (2 kg < PV < 10 kg):1 pipette/animal/4 sempipette 3 x 0,67 mlR/FRONTLINE COMBO spot-on chien M (Merial)(S)-méthoprène: 120,6 mgfipronil: 134 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem) (10 kg < PV < 20 kg):1 pipette/animal/4 sempipette 3 x 1,34 mlR/FRONTLINE COMBO spot-on chien L (Merial)(S)-méthoprène: 241,2 mgfipronil: 268 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem) (20 kg < PV < 40 kg):1 pipette/animal/4 sempipette 3 x 2,68 mlR/FRONTLINE COMBO spot-on chien XL (Merial)(S)-méthoprène: 361,8 mgfipronil: 402 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem) (PV > 40 kg):1 pipette/animal/4 sempipette 3 x 4,02 mlR/FRONTLINE COMBO Spot-on Clinic Pack Chat(Merial)fipronil: 50,00 mg(S)-méthoprène: 60,00 mgsolution spot-on à usage cutanéPosologie:Fe: 5 mg de fipr/kg + 6 mg de (S)-méth/kg(1 pipette/animal/4 sem)furet: 1 pipette/animal/4 sempipette 30 x 0,5 mlR/FRONTLINE COMBO Spot-on Clinic Pack Chien S(Merial)fipronil: 67,00 mg(S)-méthoprène: 60,30 mgsolution spot-on à usage cutanéPosologie:Ca (PV 2 - 10 kg): 6,7 mg de fipr/kg + 6 mgde (S)-méth/kg (1 pipette/animal/4 sem)pipette 18 x 0,67 mlR/FRONTLINE COMBO Spot-on Clinic Pack Chien M(Merial)fipronil: 134,00 mg(S)-méthoprène: 120,60 mgsolution spot-on à usage cutanéPosologie:Ca (PV 10 - 20 kg): 6,7 mg de fipr/kg + 6 mgde (S)-méth/kg (1 pipette/animal/4 sem)pipette 18 x 1,34 mlR/FRONTLINE COMBO Spot-on Clinic Pack Chien L(Merial)fipronil: 268,00 mg(S)-méthoprène: 241,20 mgsolution spot-on à usage cutanéPosologie:Ca (PV 20 - 40 kg): 6,7 mg de fipr/kg + 6 mgde (S)-méth/kg (1 pipette/animal/4 sem)pipette 18 x 2,68 mlR/Fipronil, (S)-méthoprène + amitrazIndicationsCette association est utilisée chez lechien dans le traitement et <strong>la</strong> préventiondes infestations par les tiques(Ixodes ricinus, Dermacentor reticu<strong>la</strong>tus,Rhipicephalus sanguineus, Ixodesscapu<strong>la</strong>ris, Dermacentor variabilis,Haemaphysalis elliptica, Haemaphysalislongicornis, Amblyomma americanumet Amblyomma macu<strong>la</strong>tum) etles puces (Ctenocephalides felis etCtenocephalides canis), ainsi que dansle traitement des infestations par lespoux broyeurs. Ce pro<strong>du</strong>it peut entrerdans le cadre d’une stratégie théra-
12 MÉDICAMENTS À USAGE EXTERNE 207peutique de contrôle de <strong>la</strong> dermatiteallergique aux piqûres de puces.PharmacodynamieLe fipronil tue les puces et les tiquesa<strong>du</strong>ltes. L’amitraz tue les tiquesa<strong>du</strong>ltes. L’association de ces deuxmolécules agit sur plusieurs sites <strong>du</strong>système nerveux des tiques et présenteune efficacité synergique, l’éliminationdes tiques étant plus rapideet <strong>la</strong> <strong>du</strong>rée d’action plus longue. Le(S)-méthoprène est un régu<strong>la</strong>teur decroissance de <strong>la</strong> c<strong>la</strong>sse des analoguesde l’hormone juvénile, qui a uneactivité ovicide et <strong>la</strong>rvicide. On n’a pasobservé d’interactions pharmacodynamiqueschez les mammifères entre lefipronil, l’amitraz et le (S)-méthoprène.PharmacocinétiqueLes trois molécules sont bien distribuéessur le pe<strong>la</strong>ge des chienstraités pendant <strong>la</strong> première semainesuivant l’application. Ces moléculeset leurs principaux métabolites sontdétectables pendant au moins 58 joursaprès application. L’absorption systémiquedes molécules de ce pro<strong>du</strong>it esttrès faible.Contre-indicationsNe pas administrer aux animaux ma<strong>la</strong>desou atteints de ma<strong>la</strong>dies systémiquestelles que le diabète. Ne pasutiliser ce pro<strong>du</strong>it chez les <strong>la</strong>pins et leschats.Effets indésirablesRarement: réactions locales tellesqu’une décoloration de <strong>la</strong> peau, uneperte de poils, des démangeaisons. Encas de léchage <strong>du</strong> site d’application :entre autres, hypersalivation, vomissements,hyperglycémie, bradycardie,bradypnée. Ces signes disparaissentdans les 24 heures.InteractionsAucune interaction connue.Précautions particulièresCe pro<strong>du</strong>it peut provoquer une sensibilisationde <strong>la</strong> peau, des réactionsallergiques et de légères irritations del’oeil chez l’homme. Il est toxique pourles organismes aquatiques (vertébréset invertébrés).Repro<strong>du</strong>ction et <strong>la</strong>ctationCe pro<strong>du</strong>it peut être utilisé en cours degestation ou de <strong>la</strong>ctation.LMR fipronil + (S)-méthoprène +amitraz : CERTIFECT 67 mg/60,3 mg/80 mg sol spot-onchiens de 2-10 kg (Merial)fipronil: 67 mgS-méthoprène: 60,3 mgamitraz: 80 mgsolution à usage cutanéPosologie:Ca: 6,7 mg de fipr/kg + 6 mg de (S)-méth/kget 8 mg d’amitr/kg (1 pipette/animal/4 sem)puces: 5 sem, tiques: 5 sempipette 1 ou 3 x 1,07 mlR/CERTIFECT 134 mg/120,6 mg/160 mg sol spot-onchiens de 10-20 kg (Merial)fipronil: 134 mgS-méthoprène: 120,6 mgamitraz: 160 mgsolution à usage cutanéPosologie:Ca: 6,7 mg de fipr/kg + 6 mg de (S)-méth/kget 8 mg d’amitr/kg (1 pipette/animal/4 sem)puces: 5 sem, tiques: 5 sempipette 1 ou 3 x 2,14 mlR/CERTIFECT 268 mg/241,2 mg/320 mg sol spot-onchiens de 20-40 kg (Merial)fipronil: 268 mgS-méthoprène: 241,2 mgamitraz: 320 mgsolution à usage cutanéPosologie:Ca: 6,7 mg de fipr/kg + 6 mg de (S)-méth/kget 8 mg d’amitr/kg (1 pipette/animal/4 sem)puces: 5 sem, tiques: 5 sempipette 1 ou 3 x 4,28 mlR/CERTIFECT 402 mg/361,8 mg/480 mg sol spot-onchiens de 40-60 kg (Merial)fipronil: 402 mgS-méthoprène: 361,8 mgamitraz: 480 mgsolution à usage cutanéPosologie:Ca: 6,7 mg de fipr/kg + 6 mg de (S)-méth/kget 8 mg d’amitr/kg (1 pipette/animal/4 sem)puces: 5 sem, tiques: 5 sempipette 1 ou 3 x 6,42 mlR/Indoxacarbe + perméthrineVoir 12.1.3.8 et 12.1.3.2LMR indoxacarbe + perméthrine: ACTIVYL TICK PLUS spot-on sol chiens de petitetaille (MSD A.H.)indoxacarbe: 150 mgperméthrine: 480 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV 5-10 kg): 15-30 mgd’indox/kg + 48-96 mg de perm/kgpipette 4R/
20812 MÉDICAMENTS À USAGE EXTERNEACTIVYL TICK PLUS spot-on sol chiens de taillemoyenne (MSD A.H.)indoxacarbe: 300 mgperméthrine: 960 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV 10-20 kg): 15-30 mgd’indox/kg + 48-96 mg de perm/kgpipette 4R/ACTIVYL TICK PLUS spot-on sol chiens de grandetaille (MSD A.H.)indoxacarbe: 600 mgperméthrine: 1920 mgsolution à usage cutanéPosologie:Ca (âge > 8 sem, PV 20-40 kg): 15-30 mgd’indox/kg + 48-96 mg de perm/kgpipette 4R/Métaflumizone + amitrazVoir aussi chapitres 12.1.3.6 et12.1.3.7.LMR métaflumizone + amitraz : PROMERIS DUO spot-on chiens (Pfizer A.H.)métaflumizone: 150 mg/m<strong>la</strong>mitraz: 150 mg/mlsolution à usage cutanéPosologie:Ca (âge > 8 sem): 20 mg/kg PVpuces: 6 sem, tiques: 4 sempipette 3 ou 6 x 0,67 ml ou 1,33 ml ou 3,33 mlou 5,33 ml ou 6,66 mlR/12.1.4 Médicament antiparasitaire pour abeilles12.1.4.1 ThymolIndicationLutte contre <strong>la</strong> varroase (Varroa destructor)de l’abeille mellifère.(AR 7 mars 2007, AM 10 août 2007)PharmacodynamieLe thymol est un phénol naturellementprésent dans les fractionsd’huile essentielle d’un grand nombrede p<strong>la</strong>ntes. En s’évaporant de <strong>la</strong> p<strong>la</strong>quette,le thymol sature l’air dans lerucher. Des concentrations de plus de5 microgrammes de thymol par litred’air dans <strong>la</strong> ruche tuent les acariensphorétiques sur les abeilles. Son mécanismed’action n’est pas complètementconnu.PharmacocinétiqueLa pharmacocinétique <strong>du</strong> thymol dansles abeilles n’est pas connue.Le thymol de chaque p<strong>la</strong>quette estsublimé dans le rucher sur une périodede 21 à 28 jours. La sublimation appropriée<strong>du</strong> thymol se pro<strong>du</strong>it à destempératures comprises entre 15°C et30°C.Lorsque les p<strong>la</strong>quettes ont été retirées<strong>du</strong> rucher, le thymol disparaît peuà peu de <strong>la</strong> ruche. Les rési<strong>du</strong>s dans<strong>la</strong> cire des rayons sont rapidementévacués.Contre-indicationsNe pas utiliser lors de températuresjournalières supérieures à 30 °C, cecicauserait une augmentation <strong>du</strong> stresset de <strong>la</strong> mortalité des abeilles et <strong>du</strong>couvain. L’efficacité <strong>du</strong> traitement diminuelors de températures inférieuresà 15 °C. Ne pas traiter pendant <strong>la</strong>miellée. Au printemps suivant, ne pasextraire les rayons de <strong>la</strong> chambre àcouvain qui ont été présents pendantle traitement. Il est conseillé de ne pastraiter plus de deux fois par an.Effets indésirablesLes abeilles peuvent dép<strong>la</strong>cer lesréserves de sucre ou de miel situéesdirectement sous les p<strong>la</strong>quettes. Lecouvain trop proche des p<strong>la</strong>quettespourrait aussi être dép<strong>la</strong>cé par lesabeilles. La quantité de nourritureingérée par les abeilles pourrait êtremoindre lorsque l’alimentation est administréesimultanément au traitement.Lors de températures élevées (> 30 °C)pendant le traitement, on peut constaterune perturbation légère de <strong>la</strong> colonieainsi qu’une légère mortalité <strong>du</strong>couvain et des abeilles. Un surdosageprovoque une mortalité plus élevée(> 20 abeilles devant le trou de vol).Précautions particulièresSi les p<strong>la</strong>quettes sont déposées justeavant ou pendant <strong>la</strong> miellée, les rési<strong>du</strong>sdans le miel peuvent augmenter.Dans un rucher, il est important de traitertoutes les ruches simultanément.Contrôle intégré des organismesnuisiblesL’efficacité peut varier entre les coloniesen fonction des conditionsenvironnementales (température, réinfestationsetc.). C’est pourquoi lemédicament ci-après doit être utilisédans le cadre d’un programme de lutteintégrée au cours <strong>du</strong>quel <strong>la</strong> chute desvarroas doit être régulièrement observée.Les colonies qui ont un taux dechute de varroas de plus d’un indivi<strong>du</strong>par jour deux semaines après le der-
12 MÉDICAMENTS À USAGE EXTERNE 209nier traitement, doivent subir un traitementsupplémentaire en hiver ou auprintemps avec une autre substanceactive contre les varroas.LMR thymol: THYMOVAR (Andermatt Bio Vet)thymol: 15 g/p<strong>la</strong>quettep<strong>la</strong>quette dans <strong>la</strong> ruchePosologie:p<strong>la</strong>cer 2 x 1 à 2 p<strong>la</strong>quettes (selon type deruche) à 3 - 4 sem d’intervalle (max 2 x/an)Miel: 0 jNe pas administrer juste avant et pendant <strong>la</strong>mielléep<strong>la</strong>quette 2 x 512.1.5 AntifongiquesIci aussi, il faut rappeler l’utilité de certains antiseptiques, notamment des iodéscontre <strong>la</strong> teigne. L’énilconazole est tout comme le kétonazole, un dérivé imidazoléà <strong>la</strong>rge spectre actif contre Trichophytum, Microsporum et Aspergillus.LMR énilconazole : IMAVEROL, émulsion (Eli Lilly)énilconazole: 100 mg/mlémulsion pour appl cutanéePosologie:Eq, Bo, Ca: 4 x à 3 - 4 j d’intervalleDé<strong>la</strong>yer <strong>la</strong> solution pour obtenir une émulsionde 0,2 %Viande: 0 j, Lait: 0 jf<strong>la</strong>con 100 ml, 1000 mlR/12.1.6 Glucocorticoïdes12.1.6.1 Hydrocortisone acéponateIndicationsTraitement symptomatique des dermatitesinf<strong>la</strong>mmatoires et prurigineuses<strong>du</strong> chien. Le traitement doit être étayépar des contrôles cliniques réguliers.PharmacodynamieVoir chapitre 2.2 Hormonescortico-surrénales.PharmacocinétiqueL’hydrocortisone acéponate (HCA) (unglucocorticoïde de <strong>la</strong> c<strong>la</strong>sse des diesters)assure, grâce à sa propriété lipophile,une pénétration élevée dans <strong>la</strong>peau associée à une faible biodisponibilitép<strong>la</strong>smatique. L’HCA s’accumuleainsi dans <strong>la</strong> peau. Chez les animauxde <strong>la</strong>boratoire, l’HCA est éliminée de <strong>la</strong>même manière que l’hydrocortisone,par l’urine et les selles.Contre-indicationsNe pas utiliser en cas d’infectionsbactériennes ou d’infestations parasitaires.L’utilisation <strong>du</strong> pro<strong>du</strong>it chez lesjeunes animaux en période de croissanceou chez les animaux souffrant<strong>du</strong> syndrome de Cushing devra êtrebasée sur une évaluation <strong>du</strong> rapportbénéfice/risque.Effets indésirablesL’application locale de l’hydrocortisoneacéponate in<strong>du</strong>it peu d’effetssystémiques secondaires.InteractionsAucune interaction connue.Précautions particulièresL’hydrocortisone acéponate irrite lesyeux.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> médicament vétérinairen’a pas été établie en période de gestationet de <strong>la</strong>ctation. L’absorptionsystémique étant négligeable, il estpeu probable que des effets tératogènes,fœtotoxiques ou délétères pour<strong>la</strong> mère apparaissent à <strong>la</strong> posologierecommandée. L’utilisation ne doit sefaire qu’après une évaluation <strong>du</strong> rapportbénéfice/risque.LMR hydrocortisone acéponate : CORTAVANCE (Virbac)hydrocortisone (acéponate): : 0,584 mg/mlspray à usage cutanéPosologie:Ca: 1,52 mcg/cm2 de peau pj (7 j)f<strong>la</strong>con 76 mlR/
21012 MÉDICAMENTS À USAGE EXTERNE12.1.7 Préparation cicatrisante12.1.7.1 KétansérineIndicationsLa kétansérine est utilisée dans le traitementde p<strong>la</strong>ies, plus particulièrementpour <strong>la</strong> prévention de <strong>la</strong> formation deschéloïdes.PharmacodynamieLes propriétés cicatrisantes de <strong>la</strong>kétansérine reposent sur son effetantisérotoninergique qui aboutit à uneinhibition de <strong>la</strong> vasoconstriction, del’agrégation p<strong>la</strong>quettaire, de <strong>la</strong> libérationde médiateurs et de facteurs decroissance par les p<strong>la</strong>quettes in<strong>du</strong>itespar <strong>la</strong> sérotonine. Une ré<strong>du</strong>ction de <strong>la</strong>perméabilité microvascu<strong>la</strong>ire est aussiobservée. Ces effets permettent unmeilleur approvisionnement en oxygèneau niveau de <strong>la</strong> lésion et uneré<strong>du</strong>ction de <strong>la</strong> croissance de <strong>la</strong> sérotoninesur les myofibrob<strong>la</strong>stes.PharmacocinétiqueSeule une quantité négligeable de kétansérineest résorbée.Précautions particulièresLa préparation ne peut être appliquéetant que l’hémorragie n’est pas jugulée.De même, le traitement doit êtreinstauré après excision chirurgicaledes chéloïdes lorsqu’elles sont déjàformées.LMR kétansérine: VULKETAN (Eli Lilly)kétansérine (tartrate): 2,5 mg/ggel pour appl cutanéePosologie:Eq: 2 x pjTemps d’attente: 0 jgel 75 gR/12.1.8 AssociationsCertaines préparations à usage dermatologique contiennent un ou plusieursantimicrobiens, éventuellement associés à un ou plusieurs composés tels qu’unagent cicatrisant, comme l’oxyde de zinc, un corticoïde ou un antifongique. Cespréparations sont utilisées sous <strong>la</strong> forme de sprays, de poudre, d’onguent ou desuspension à application locale. Les aminosides peuvent être utiles en usage localpour éviter leur toxicité lorsque les germes identifiés ont révélé une sensibilité particulièreà ce groupe d’antibiotiques. Un diagnostic étiologique devrait permettred’éviter ce type d’association qui peut contribuer à l’émergence de résistance,d’hypersensibilité et à ré<strong>du</strong>ire l’immunité locale lorsqu’un corticoïde est présentdans <strong>la</strong> préparation. Des effets systémiques liés à l’usage local d’un corticostéroïdene sont pas à exclure. Si <strong>la</strong> corticothérapie locale a une utilité évidente danscertaines affections cutanées, notamment d’origine allergique et auto-immune,le choix <strong>du</strong> corticoïde, de ses concentrations et de <strong>la</strong> posologie doit pouvoir sefaire indépendamment de <strong>la</strong> présence d’autres composés dont l’utilité et <strong>la</strong> naturedoivent par ailleurs être évaluées.LMR soufre précipité + néomycine +prednisolone : LMR prednisolone + polymyxine B +miconazole nitrate: DOG ECZEMA (Ke<strong>la</strong> Laboratoria)soufre précipité: 5 mg/gnéomycine sulfate: 5.000 UI/gprednisolone: 1 mg/goxyde de zinc: 30 mg/gémulsion pour appl cutanéePosologie:Ca: 2 - 3 x pj (7 j)f<strong>la</strong>con 100 g, 500 gR/SUROLAN (Eli Lilly)prednisolone acétate: 5 mg/mlpolymyxine B sulfate: 0.5293 mg/mlmiconazole nitrate: 23 mg/mlsuspension pour appl cutanée, instill. auricu<strong>la</strong>irePosologie:Ca, Fe: 2 x pj:instill. auricu<strong>la</strong>ire: 3 - 5 gttsappl cutanée: quelques gttsf<strong>la</strong>con 15, 30 mlR/
12 MÉDICAMENTS À USAGE EXTERNE 21112.2 Médicaments à usage ophtalmologique12.2.1 Préparations contenant au moins un antimicrobien12.2.1.1 GentamicineVoir chapitre 1.1.2.LMR gentamicine: CLINAGEL-VET (Ecuphar)gentamicine (sulfate): 3 mg/ggel à usage ophtalmiquePosologie:Ca: 2 - 3 x pj, sous <strong>la</strong> paupière inférieuretube 1 x 4 gR/SOLIGENTAL (Virbac)gentamicine (sulfate): 3.000 UI/mlsolution à usage ophtalmiquePosologie:Ca, Fe: 3 x pj 2 gtts (pendant 8 j)f<strong>la</strong>con 5 mlR/12.2.2 Médicaments utilisés contre <strong>la</strong> kératoconjonctivite sèche12.2.2.1 CiclosporineLa ciclosporine, utilisée pour le traitementde l’atopie, a fait l’objet de commentairesdans le chapitre 11.1.2.IndicationsLa kératoconjonctivite sèche (ma<strong>la</strong>dieinf<strong>la</strong>mmatoire chronique des g<strong>la</strong>ndes<strong>la</strong>crymales caractérisée par une ré<strong>du</strong>ctionde <strong>la</strong> pro<strong>du</strong>ction des <strong>la</strong>rmes) et <strong>la</strong>kératite superficielle chronique chez lechien.PharmacodynamieLa ciclosporine, <strong>du</strong> fait de son effetimmunosuppresseur, empêche <strong>la</strong>dégradation des g<strong>la</strong>ndes <strong>la</strong>crymaleset stimule <strong>la</strong> pro<strong>du</strong>ction <strong>la</strong>crymale.La ciclosporine permet également lecontrôle de <strong>la</strong> kératite pigmentaire quiaccompagne souvent <strong>la</strong> kératoconjonctivitesèche. L’expérience cliniquesuggère que plus de 90 % des chiensrequièrent un traitement à vie.PharmacocinétiqueLa biodisponibilité est minime aprèsune application topique. La demi-viede <strong>la</strong> ciclosporine appliquée localementétant de 8 h, une administration2 x par jour suffit en général pour maîtriserl’affection.Contre-indicationsIl est recommandé de ne pas appliquer<strong>la</strong> ciclosporine lors d’infections ocu<strong>la</strong>iresvirales ou fongiques.Effets indésirablesUne légère irritation ocu<strong>la</strong>ire peut êtreobservée. Si celle-ci persiste, unehyper sensibilité à <strong>la</strong> ciclosporine doitêtre suspectée.InteractionsAucune interaction connue.Précautions particulièresAprès l’instauration <strong>du</strong> traitement,il faut parfois attendre quelques semainespour que le Schirmer-tests’améliore visiblement (3 – 8 sem).Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it chez les animauxgestants ou en <strong>la</strong>ctation n’apas été démontrée par le titu<strong>la</strong>ired’enregistrement.LMR ciclosporine : OPTIMMUNE-CANIS (MSD A.H.)ciclosporine A: 2 mg/gonguent ophtalmiquePosologie:Ca: 1 cm onguent/oeil/12 honguent 3,5 gR/12.3 Médicaments à usage otiqueIndicationsLes gouttes et les crèmes otiques peuvent être utiles dans le traitement d’étatsinf<strong>la</strong>mmatoires ou infectieux <strong>du</strong> con<strong>du</strong>it auditif externe. En raison de <strong>la</strong> multiplicitédes agents pathogènes impliqués dans les otites (surtout chez les carnivores), lespréparations à usage otique contiennent généralement plusieurs principes actifs,dont au moins un antibiotique souvent associé à un corticostéroïde. Un insecti-
21212 MÉDICAMENTS À USAGE EXTERNEcide et un antifongique peuvent y être ajoutés en cas d’otites compliquées par de<strong>la</strong> gale auricu<strong>la</strong>ire ou des mycoses.Contre-indicationsL’administration est à proscrire en cas de perforation <strong>du</strong> tympan. Selon le médicament,l’administration aux animaux gestants, al<strong>la</strong>itants ou repro<strong>du</strong>cteurs est citéecomme contre-indication.Effets indésirablesUne déficience auditive transitoire, en particulier chez les animaux âgés, peut êtreobservée. Des réactions locales sont possibles. Les corticoïdes peuvent provoquerdes effets indésirables locaux et systémiques en cas d’usage chronique.Précautions particulièresLes réserves émises au sujet des associations multiples sont identiques à cellesformulées dans <strong>la</strong> rubrique consacrée aux agents dermatologiques. L’inclusiondes fluoroquinolones dans des préparations le plus souvent utilisées en premièreintention est critiquable sur le p<strong>la</strong>n de <strong>la</strong> sélection des résistances. De telles préparationsdevraient être réservées aux cas impliquant un germe multi-résistant etuniquement sensible aux fluoroquinolones.LMR marbofloxacine + clotrimazole +dexaméthasone : LMR gentamicine + betaméthasone +clotrimazole: AURIZON gttes auric, susp (Vétoquinol)marbofloxacine: 3 mg/mlclotrimazole: 10 mg/mldexaméthasone (acétate): 0,9 mg/mlsuspension instill. auricu<strong>la</strong>irePosologie:Ca: 10 gtts/oreille pj (7 j, répéteréventuellement)f<strong>la</strong>con 10 ml avec pipette, 20 ml avec 2 pipettesR/LMR prednisolone + framycétinesulfate + nystatine + diéthano<strong>la</strong>minefusidate : CANAURAL gttes auric (Dechra VeterinaryPro<strong>du</strong>cts)prednisolone: 2,5 mg/gframycétine sulfate: 5 mg/gnystatine: 100.000 UI/gdiéthano<strong>la</strong>mine fusidate: 5 mg/gsuspension pour instill. auricu<strong>la</strong>irePosologie:Ca, Fe: 2 x pj 5 à 10 gtts/oreille (min 7 j)f<strong>la</strong>con 15 ml, 25 mlR/LMR hydrocortisone + miconazole +gentamicine: EASOTIC (Virbac)acéponate d’hydrocortisone: 1,11 mg/mlnitrate de miconazole: 15,1 mg/mlsulphate de gentamicine: 1505 UI/ mlsuspension pour instill. auricu<strong>la</strong>irePosologie:Ca: 1 x 1 ml par oreille infectée pj (5 j)f<strong>la</strong>con multidose 10 mlR/OTOMAX ear drops susp (MSD A.H.)gentamicine (sulfate): 2640 UI/mlbetaméthasone (valérate): 0,88 mg/mlclotrimazole: 8,80 mg/mlsuspension pour instill. auricu<strong>la</strong>irePosologie:Ca:(< 15 kg PV): 2 x pj 4 gtts (7 j)(> 15 kg PV): 2 x pj 8 gtts (7 j)f<strong>la</strong>con 14 ml, 34 mlR/LMR dexaméthasone + lidocaïne +polymyxine B + néomycine +monosulfiram: OTOSPECTRINE (Ke<strong>la</strong> Laboratoria)dexaméthasone: 1 mg/mllidocaïne (chlorhydrate): 40 mg/mlnéomycine sulfate: 5.000 UI/mlpolymyxine B sulfate: 10.000 UI/mlsulfiram: 50 mg/mlsuspension pour instill. auricu<strong>la</strong>irePosologie:adapter <strong>la</strong> dose en fonction de <strong>la</strong> taille del‘animal et <strong>du</strong> degré d‘inf<strong>la</strong>mmationpetit Ca, Fe (< 5 kg): 3 gtts 1 à 2 x pj (7 j)Ca moyen (5 - 10 kg): 5 gtts 1 à 2 x pj (7 j)grand Ca (> 10 kg): 10 gtts 1 à 2 x pj (7 j)f<strong>la</strong>con 15 mlR/LMR prednisolone + polymyxine B +miconazole nitrate: SUROLAN (Eli Lilly)prednisolone acétate: 5 mg/mlpolymyxine B sulfate: 0.5293 mg/mlmiconazole nitrate: 23 mg/mlsuspension pour appl cutanée, instill. auricu<strong>la</strong>irePosologie:Ca, Fe: 2 x pj:instill. auricu<strong>la</strong>ire: 3 - 5 gttsappl cutanée: quelques gttsf<strong>la</strong>con 15, 30 mlR/
12 MÉDICAMENTS À USAGE EXTERNE 213LMR orbifloxacine + mométasonefuroate + posaconazole : POSATEX (MSD A.H.)orbifloxacine: 8,5 mg/mlmométasone furoate (monohydrate): 0,9 mg/mlposaconazole: 0,9 mg/mlsuspension instill auricu<strong>la</strong>irePosologie:Ca (âge > 4 m):PV < 2 kg: 1 x pj 2 gttes/oreille (7 j)PV 2 - 15 kg: 1 x pj 4 gttes/oreille (7 j)PV > 15 kg: 1 x pj 8 gttes/oreille (7 j)f<strong>la</strong>con 8,8 ml, 17,5 mlR/12.4 Médicaments à usage gynécologiqueIndicationsLes infections utérines ou vaginales des grands animaux peuvent être traitées parvoie locale, en complément ou non d’une antibiothérapie systémique. Le choix de<strong>la</strong> voie d’administration sera notamment déterminé en fonction des germes pathogènesresponsables, <strong>du</strong> stade de l’infection et des circonstances d’apparition.PharmacocinétiqueLes préparations utilisées par voie intra-utérine sont des comprimés (oblets) oudes suspensions huileuses qui diffusent dans les sécrétions génitales et l’endomètre.Leur efficacité pendant <strong>la</strong> période post-partum a été remise en question. Lac<strong>la</strong>ssification des préparations intra-utérines dans <strong>la</strong> catégorie des médicamentsà usage interne ou externe n’est pas c<strong>la</strong>irement établie. Cette voie d’administrationpermet l’in<strong>du</strong>ction d’effets thérapeutiques locaux. La résorption systémiquefaible ne permet pas d’in<strong>du</strong>ire d’effets thérapeutiques systémiques mais <strong>la</strong> présencede rési<strong>du</strong>s dans <strong>la</strong> carcasse ou le <strong>la</strong>it des animaux ne peut être exclue.Ce sont donc des traitements locaux, ce qui justifie leur c<strong>la</strong>ssification dans cetterubrique.Effets indésirablesLes effets indésirables se limitent le plus souvent à quelques réactions locales.LMR chlortétracycline: METRICYCLIN (Ke<strong>la</strong> Laboratoria)chlortétracycline chlorhydrate: 1 gcomprimé (oblet) iuPosologie:Bo:- traitement préventif: 1 g- traitement curatif: 1 - 2 gViande: 10 j, Lait: 4 jcompr 100R/OBLETS GYNECOLOGIQUES (VMD)chlortétracycline chlorhydrate: 1.000 mgcomprimé iuPosologie:Bo: 1.000 mg (1 - 3 j)Viande: 7 j, Lait: 3 jcompr 100R/LMR céfapirine: METRICURE (MSD A.H.)céfapirine (benzathine): 500 mgsuspension iuPosologie:Bo: 500 mg (peut être répété après 7 à 14 j)Viande: 2 j, Lait: 0 happlic 10 x 19 gR/12.5 Médicaments à usage intramammaireIndicationsLes mammites bovines cliniques peuvent être traitées par des applications localesd’antibiotiques dans le canal <strong>du</strong> trayon. Si des symptômes généraux sontobservés, une antibiothérapie systémique peut être mise en p<strong>la</strong>ce. Si l’antibiotiqueadministré par voie systémique ne peut diffuser suffisamment dans le <strong>la</strong>it <strong>du</strong> faitde ses propriétés pharmacocinétiques, son application locale peut, dans ce casprécis, être utile. L’administration locale et systémique de principes actifs faisant
21412 MÉDICAMENTS À USAGE EXTERNEpartie de <strong>la</strong> même famille pharmacologique est à privilégier. Si des antibiotiquesdifférents doivent être appliqués par voie intramammaire, c’est en respectant lesrègles générales d’association et en tenant compte de leur cinétique. Les germesles plus souvent en cause peuvent être des bactéries GRAM+ (staphylocoques,streptocoques, A. pyogenes), des entérobactéries (E. coli), des mycop<strong>la</strong>smes (enparticulier Mycop<strong>la</strong>sma bovis) ou plus rarement des anaérobies. Des résistancesliées à <strong>la</strong> synthèse de bêta-<strong>la</strong>ctamase sont souvent observées. Une thérapie endébut de tarissement (dry cow therapy) doit permettre de compléter l’efficacitédes traitements des mammites cliniques et d’éviter les infections qui peuvent survenirà ce moment.PharmacodynamieLes antibiotiques utilisés par voie intramammaire appartiennent surtout auxgroupes des bêta<strong>la</strong>ctamines et des aminosides. La plupart des antibiotiques utiliséspour le traitement des mammites ont été décrits précédemment (voir chapitre1.1). L’application locale permet généralement d’obtenir une guérison clinique,mais pas toujours bactériologique, les animaux restant porteurs des germes àl’état <strong>la</strong>tent. Ces antibiotiques sont souvent associés entre eux. Un diagnosticétiologique devrait permettre d’éviter le recours automatique à ces associations,parfois utiles <strong>du</strong> fait des synergies possibles et de l’é<strong>la</strong>rgissement <strong>du</strong> spectrelorsque plusieurs germes sont impliqués. Leur usage est controversé <strong>du</strong> fait deleur influence sur <strong>la</strong> santé publique.PharmacocinétiqueLes préparations «dry cow» sont faiblement irritantes et contiennent un ou plusieursantibiotiques bactéricides très actifs, ayant une forte affinité pour le tissumammaire et ses sécrétions. Ce sont des suspensions huileuses qui libèrent lentementleurs principes actifs. Ces préparations ne doivent pas être utilisées enpériode de <strong>la</strong>ctation, car elles exigent un temps d’attente trop long.Remarque : La c<strong>la</strong>ssification des préparations intramammaires dans <strong>la</strong> catégoriedes médicaments à usage interne ou externe n’est pas c<strong>la</strong>irement établie. Cettevoie d’administration permet l’in<strong>du</strong>ction d’effets thérapeutiques locaux. La résorptionsystémique faible ne permet pas d’in<strong>du</strong>ire d’effets thérapeutiques systémiquesmais <strong>la</strong> présence de rési<strong>du</strong>s dans <strong>la</strong> carcasse des animaux ne peut être exclue. Cesont donc des traitements locaux, ce qui justifie leur c<strong>la</strong>ssification dans <strong>la</strong> rubrique.Précautions particulièresL’identification des germes en cause et de leur sensibilité est une recommandationessentielle.Repro<strong>du</strong>ction et <strong>la</strong>ctationLes préparations intramammaires sont suffisamment sûres pour être administréespendant <strong>la</strong> gestation. En raison de leur temps d’attente long, les préparationsdestinées au tarissement ne peuvent pas être administrées pendant <strong>la</strong> <strong>la</strong>ctation.12.5.1 Traitement des mammites12.5.1.1 CloxacillineIndications - spectre d’activité –résistanceLa cloxacilline est surtout utilisée contreles coques gram positifs pro<strong>du</strong>cteursde pénicillinase, dont Staphylococcusspp. Le spectre d’activité de cettepénicilline semi-synthétique et résistanteà <strong>la</strong> pénicillinase est plus ré<strong>du</strong>itque celui de <strong>la</strong> pénicilline naturelle. De<strong>la</strong> résistance a été constatée mais neconstitue pas (encore) de problème enmédecine vétérinaire.Contre-indicationsHypersensibilité connue aux pénicillines.LMR cloxacilline: ORBENIN LA (Pfizer A.H.)cloxacilline: 200 mgsuspension intramammairePosologie:Bo: 1 applic/quart/48 h (3 x)traitement des mammitesViande: 1 j, Lait: 120 happlic 12 x 3 gR/12.5.1.2 Céphalosporines: premiergroupeLa céfazoline et <strong>la</strong> céfalexine, appartenantau premier groupe, sont essentiellementactives contre les GRAM+.Voir chapitre 1.1.1.2.
12 MÉDICAMENTS À USAGE EXTERNE 215LMR céfazoline : CEFOVET <strong>la</strong>ctation (Merial)céfazoline: 300 mgsuspension intramammairePosologie:Bo: 1 applic/quart/12 h (2 x)Traitement des mammitesViande: 24 h, Lait: 8 traitesapplic 2 x 6 gR/LMR céfalexine : RILEXINE 200 <strong>la</strong>ctating cow (Virbac)céfalexine: 200 mgsuspension intramammairePosologie:Bo: 1 applic/quart/12 h (4 x)Traitement des mammitesViande et abats: 4 j, Lait: 4 traitesapplic 12 ou 24 x 10 mlR/12.5.1.3 Céphalosporines: deuxièmegroupeLa cefquinome, <strong>du</strong> deuxième groupe, estactive contre les GRAM+ et les GRAM-,notamment les entérobactéries.Voir chapitre 1.1.1.2.LMR cefquinome: COBACTAN LC (MSD A.H.)cefquinome (sulfate): 75 mgpommade intramammairePosologie:Bo: 1 applic/quart/12 h (3 x)Traitement des mammitesViande: 4 j, Lait: 5 japplic 15 x 8 gR/12.5.1.4 Céphalosporines: troisièmegroupeLa céfopérazone, <strong>du</strong> troisième groupe,a un spectre d’activité très <strong>la</strong>rge,englobant GRAM+ et GRAM-, dontPseudomonas aeruginosa.Voir chapitre 1.1.1.2.LMR céfopérazone: PATHOZONE (Pfizer A.H.)céfopérazone: 250 mgsuspension intramammairePosologie:Bo: 1 applic/quartTraitement des mammitesViande: 2 j, Lait: 96 happlic 10 x 10 mlR/12.5.1.5 PirlimycineLa pirlimycine est un antibiotique <strong>du</strong>groupe des lincosamides exerçantune action sur les germes GRAM+, lesanaérobies et certains mycop<strong>la</strong>smes.La diffusion intracellu<strong>la</strong>ire de cet antibiotiqueest bonne et sa concentrationdans le <strong>la</strong>it reste élevée après une applicationlocale.LMR pirlimycine: PIRSUE 5 mg/ml (Pfizer A.H.)pirlimycine (chlorhydrate): 50 mg/10 mlsolution intramammairePosologie:Bo: 1 applic/quart pj (8 x)Traitement des mammites subcliniquesViande: 23 j, Lait: 5 japplic 24 x 10 mlR/12.5.1.6 AssociationsVoir plus haut.LMR cloxacilline + ampicilline : AMPICLOX Q.R. 75/200 mg (Pfizer A.H.)cloxacilline (monohydrate sodique): 200 mgampicilline (sodique): 75 mgsuspension intramammairePosologie:Bo: 1 applic/quart/12 h (3 x)Traitement des mammitesViande: 2 j, Lait: 60 hboîte 24 x 3 g applicR/LMR céfalexine + kanamycine: UBROLEXIN (Boehringer Ingelheim)céfalexine (monohydrate): 200 mgkanamycine (monosulphate): 100.000 UIsuspension intramammairePosologie:Bo: 2 x 1 applic à 24 h d’intervalleTraitement des mammitesViande: 10 j, Lait: 5 japplic 20 x 10 gR/LMR lincomycine + néomycine : LINCOCIN intramammaire (Pfizer A.H.)lincomycine (chlorhydrate): 330 mgnéomycine (sulfate): 100 mgsolution stérile intramammairePosologie:Bo: 1 applic/quart/12 h (3 x)Traitement des mammitesViande: 3 j, Lait: 84 happlic 24 x 10 mlR/LMR néomycine + benzylpénicillineprocaïne: MASTI-kel (Ke<strong>la</strong> Laboratoria)néomycine sulfate: 500.000 UIbenzylpénicilline procaïne: 300.000 UIonguent intramammairePosologie:Bo: 1 applic/quart/24 h (3 x)Traitement des mammitesViande: 20 j, <strong>la</strong>it: 204 h (17 traites)applic 20 x 10 gR/
21612 MÉDICAMENTS À USAGE EXTERNE12.5.2 Préparations utilisées au cours <strong>du</strong> tarissement et contenant unantimicrobien12.5.2.1 CloxacillineVoir chapitre 12.5.1.1LMR cloxacilline benzathine: DRYCLOXA-kel (Ke<strong>la</strong> Laboratoria)cloxacilline benzathine: 1.000 mgonguent intramammairePosologie:Bo: 1 applic/quarttarisseur: administrer au moins 35 j avantle vê<strong>la</strong>geViande: 10 j, Lait: 12 h après le vê<strong>la</strong>ge (administrationplus de 60 j avant le vê<strong>la</strong>ge) - 60 j aprèsl’administration (administration moins de 60 javant le vê<strong>la</strong>ge)applic 20 x 9 gR/KLOXERATE DC (Pfizer A.H.)cloxacilline (benzathine): 500 mgsuspension intramammairePosologie:Bo: 1 applic/quarttarisseur: admin au moins 7 sem avant levê<strong>la</strong>geViande: 56 j, Lait: 96 h après le vê<strong>la</strong>ge (tarissement> 7 sem) ou 53 j (tarissement < 7 sem)applic 24 x 4,5 g, 120 x 4,5 gR/ORBENIN E.D.C. 600 mg (Pfizer A.H.)cloxacilline: 600 mgsuspension intramammairePosologie:Bo: 1 applic/quarttarisseur: admin au moins 42 j avant levê<strong>la</strong>geViande: 24 h, Lait: 36 h (tarissement min 42 j) ou44 j (tarissement < 42 j)applic 24 x 3,6 g, 60 x 3,6 gR/12.5.2.2 Céphalosporines surtoutactives contre les GRAM+Voir chapitre 1.1.1.2.LMR céfazoline : CEFOVET DC (Merial)céfazoline: 250 mgsuspension intramammairePosologie:Bo: 1 applic/quartViande: 21 j, Lait: 0 j en cas de tarissement demin 6 semEn cas de vê<strong>la</strong>ge précoce: 14 japplic 4 x 3 gR/LMR céfalonium : CEPRAVIN DRY COW (MSD A.H.)céfalonium: 250 mgsuspension intramammairePosologie:Bo: 1 applic/quartViande: 0 j, Lait: 96 h (4 j) en cas de tarissementde min 54 jEn cas de vê<strong>la</strong>ge précoce: 54 j + 96 h (58 j)applic 20 x 3 gR/LMR céfalexine : RILEXINE 500 DC (Virbac)céfalexine (benzathine): 375 mgsuspension intramammairePosologie:Bo: 1 applic/quarttarisseur: admin au moins 2 m avant levê<strong>la</strong>geViande: 4 j, Lait: 0 j. En cas de vê<strong>la</strong>ge précoce:faire un test de recherche d’antibiotiqueapplic 12 ou 60 x 8 gR/12.5.2.3 Céphalosporines dont lespectre est é<strong>la</strong>rgiVoir chapitre 1.1.1.2.LMR cefquinome: VIRBACTAN (Virbac)cefquinome (sulfate): 150 mg/injecteur (3 g)suspension intramammairePosologie:Bo (en période de tarissement):1 injecteur/quartViande: 2 j, Lait: 36 j après traitement (si tarissementcourt < 5 sem), 1 j après mise bas (sitarissement > 5 sem)injecteur 3 g ( 6 x 4 ou 15 x 4)R/12.5.2.4 RifaximineLa rifaximine est un antibiotique de <strong>la</strong>famille des ansamycines. Elle présentele mécanisme d’action des rifamycines,agissant directement au niveaude <strong>la</strong> transcription par interactionavec l’ARN-polymérase, ADN dépendante.Elle empêche ainsi <strong>la</strong> synthèsede l’ARN messager et des protéines.Le spectre englobe en particulier lesprincipaux germes GRAM+ responsablesde mammites, en multiplicationet à l’état quiescent: Staphyloccusaureus, Streptococcus aga<strong>la</strong>ctiae,Streptococcus dysga<strong>la</strong>ctiae,Streptococcus uberis et Actynomycespyogenes. Du fait de l’utilisation des rifamycinesen médecine humaine dansle traitement de <strong>la</strong> tuberculose, leur
12 MÉDICAMENTS À USAGE EXTERNE 217utilisation en médecine vétérinaire està limiter au maximum.LMR rifaximine: FATROX (Fatro)rifaximine: 100 mgpommade intramammairePosologie:Bo: 1 applic/quarttarisseur: admin au moins 4 sem avant levê<strong>la</strong>geViande: 0 j, Lait: 0 h (plus de 4 sem aprèstarissement), 22 traites (moins de 4 sem aprèstarissement)applic 4 x 5 ml, 60 x 5 mlR/12.5.2.5 AssociationsLMR cloxacilline + ampicilline : KLOXERATE DC PLUS (Pfizer A.H.)ampicilline (trihydrate): 250 mgcloxacilline (benzathine): 500 mgsuspension intramammairePosologie:Bo: 1 applic/quarttarisseurViande: 56 j, Lait: 216 h (9 j) (tarissement > 45 j)ou 54 j (tarissement < 45 j)applic 24 x 4,5 g, 120 x 4,5 gR/LMR procaïne benzylpenicilline +dihydrostreptomycine: NAFPENZAL DC (MSD A.H.)procaïne benzylpénicilline G: 300.000 U/injdihydrostreptomycine (sulfate): 100 mg/injnafcilline (sodique): 100 mg/injsuspension intramammairePosologie:Bo: 1 applic/quarttarisseur: admin jusqu‘à max 8 sem avantle vê<strong>la</strong>geViande et abats: 5 sem, Lait: 3 traites, aprèstarissement de min 46 jTarissement plus court: 46 japplic 1 x 20R/LMR pénéthamate + bénéthaminepénicilline + framycétine sulfate : UBROSTAR DRY COW (Boehringer Ingelheimvetmedica)pénéthamate iodhydrate: 100 mgbénéthamine pénicilline: 280 mgframycétine sulfate: 100 mgsuspension intramammairePosologie:Bo: 1 x 1 applicTarisseurViande et abats: 10 jLait: tarissement moins de 35 j: 36 h après levê<strong>la</strong>ge, tarissement moins de 35 j: 37 j après letraitementapplic 60 x 5 mlR/12.5.3 Préparations utilisées au cours <strong>du</strong> tarissement et ne contenant pasd’antimicrobien12.5.3.1 Sous nitrate de bismuthIndicationsLe sous nitrate de bismuth est utiliséau cours <strong>du</strong> tarissement chez lesbovins.PharmacodynamieLe pro<strong>du</strong>it n’a pas d’effet antibactérienen soi, mais forme au niveau <strong>du</strong> canalmammaire une barrière physique iso<strong>la</strong>ntle tissu mammaire de l’environnementextérieur.PharmacocinétiqueLe sous nitrate de bismuth n’est pasrésorbé par le tissu mammaire. Letemps d’attente est donc nul.Contre-indicationsNe pas administrer aux animauxsouffrant de mammite subclinique ouclinique.Effets indésirablesAucun effet secondaire connu.InteractionsNe pas administrer simultanémentavec d’autres médicamentsintramammaires.Précautions particulièresLes mesures d’hygiène d’usagedoivent être respectées lors de l’applicationde <strong>la</strong> préparation dans le canalmammaire.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité <strong>du</strong> pro<strong>du</strong>it permet de l’administrer<strong>du</strong>rant <strong>la</strong> gestation.LMR sous-nitrate de bismuth: ORBESEAL (Pfizer A.H.)subnitrate de bismuth: 2,6 gsuspension intrammmairePosologie:Bo: 1 applic/quarttarisseurViande: 0 j, Lait: 0 japplic 24, 60R/
13 VACCINS POUR LE CHEVAL 21913. MÉDICAMENTS AGISSANT SUR L’IMMUNITÉ13.1 VaccinsLes préparations disponibles en Belgique sont envisagées pour chaque espèce.Les vaccins antirabiques sont repris séparément. De très nombreux vaccins comprenantplusieurs valences, des tableaux récapitu<strong>la</strong>tifs qui reprennent les vaccinspar ordre alphabétique avec les valences correspondantes ont été ajoutés. Voiraussi Folia Veterinaria 2010 n° 1 concernant le début et <strong>la</strong> <strong>du</strong>rée de l’immunité(« Onset Of Immunity » ou « OOI » et « Duration Of Immunity » ou « DOI »). (Voiraussi Folia Veterinaria 2007 n° 2 et 3)13.1.1 Vaccins pour le cheval13.1.1.1 Vaccination contre lesma<strong>la</strong>dies viralesLa grippe équine et <strong>la</strong> rhinopneumoniesont les ma<strong>la</strong>dies virales contre lesquelleson vaccine habituellement lecheval en Belgique. Un vaccin contre<strong>la</strong> fièvre <strong>du</strong> Nil occidental (West Nile)est également disponible.Grippe équineLe virus de <strong>la</strong> grippe équine engendreune infection aiguë de l’épithélium desvoies respiratoires supérieures et despoumons. Fièvre, abattement, anorexieet toux sèche en sont les signescliniques caractéristiques. Seules lesinfections bactériennes secondairespeuvent en général provoquer de <strong>la</strong>mortalité qui reste plutôt rare, mais lesperformances des chevaux peuventêtre amoindries <strong>du</strong>rant de nombreusessemaines. Il existe deux sous-types<strong>du</strong> virus de <strong>la</strong> grippe équine, H7N7(type 1) et H3N8 (type 2), dont lessouches prototypes sont respectivementPrague/56 et Miami/63. Le virusinfluenza A équin de sous-type H7N7n’a plus été associé à un cas cliniquedepuis 1979. Des chevaux ayant occasionnellementencore été trouvésséropositifs, on peut admettre que levirus circule sous forme subclinique ausein de <strong>la</strong> popu<strong>la</strong>tion équine. Quant àl’autre sous-type, H3N8, il circule <strong>la</strong>rgementdans les popu<strong>la</strong>tions de chevauxet engendre fréquemment desépisodes de grippe chez le chevaldans le monde entier.VaccinVaccin contre <strong>la</strong> grippe équine -Vaccins combinés avec l’anatoxinetétaniqueLa plupart des vaccins sont des vaccinsinactivés à base d’un virus completou d’antigènes, hémagglutinine(HA) et neuraminidase (NA), fractionnés.Un vaccin recombinant est préparéà base de 2 vecteurs poxvirus<strong>du</strong> canari exprimant les hémagglutininesde virus H3N8 de <strong>la</strong> lignée américaineet de <strong>la</strong> lignée européenne. Ilscontiennent au minimum un iso<strong>la</strong>t dechaque sous-type et en général égalementun adjuvant (huile, dérivésd’aluminium, carbomère ou Quil A). Lesous-type H3N8 présente une certaine« dérive antigénique » (antigenic drift).De ce fait, des iso<strong>la</strong>ts plus récentsassurent une protection plus <strong>la</strong>rgecontre les souches actuellement circu<strong>la</strong>ntes.C’est pourquoi tous les vaccinscontiennent une ou plusieurs souchesrécentes de virus H3N8, en plus de <strong>la</strong>souche Miami/63 ou s’y substituant.Certains vaccins H3N8 contiennenten plus, à côté d’iso<strong>la</strong>ts de <strong>la</strong> lignéeeuropéenne, un représentant de <strong>la</strong>lignée américaine (Newmarket/1/93).Des adjuvants tels que les carbomères(carbopol) et les saponines (Quil A), oules systèmes de présentation d’antigènes(immune stimu<strong>la</strong>ting complexes,ISCOMS) peuvent é<strong>la</strong>rgir et prolonger<strong>la</strong> réponse en anticorps. Les vaccinsISCOM seraient également en mesurede stimuler <strong>la</strong> réponse immune à médiationcellu<strong>la</strong>ire.ProtectionLa protection est basée sur <strong>la</strong> présenced’anticorps sériques dirigéscontre l’hémagglutinine: il y a unecorré<strong>la</strong>tion très nette entre le taux enanticorps et le degré de protection. Laréponse en anticorps après <strong>la</strong> vaccinationest cependant de courte <strong>du</strong>rée
2<strong>2013</strong> VACCINS POUR LE CHEVALet des revaccinations fréquentes sontnécessaires afin d’assurer un taux enanticorps qualifié de «protecteur».Chez les chevaux à haut risque telsles chevaux de compétition ou despectacle, il est conseillé de procéderà des revaccinations tous les 3 à 4mois. Dans d’autres situations, il suffitde revacciner tous les 6 mois à un an.Même les chevaux bien vaccinés sontsouvent seulement partiellement immunisés.Ils sont alors protégés contre<strong>la</strong> ma<strong>la</strong>die, mais non contre l’infection.Excrétant encore le virus, ils sont unesource d’infection dangereuse pourles animaux sensibles. L’efficacité desvaccins est également déterminée par<strong>la</strong> concentration en antigènes et <strong>la</strong> parentéantigénique entre les souches <strong>du</strong>vaccin et les souches circu<strong>la</strong>ntes.Particu<strong>la</strong>ritésDes directives spécifiques sont envigueur concernant <strong>la</strong> vaccinationdes chevaux de sport participant auxconcours de <strong>la</strong> FEI. La non observationde ces directives peut entraînerl’exclusion <strong>du</strong> droit de participationau concours (http://www.horsesport.org: voir «Veterinary» > «Vaccinations& Health Requirements»). Vaccin contre <strong>la</strong> grippe équineEQUILIS PREQUENZA (MSD A.H.)sous-unités purifiées d’hémagglutinines desvirus influenza équins:A/equine-1/Prague/56: 100 UAA/equine-2/Newmarket/1/93: 50 UAA/equine-2/Newmarket/2/93: 50 UAadjuv: saponine, cholestérol,phosphatidylcholinevaccin injectable imPosologie:Eq (âge > 6 m)- Primovac: 1 dose/animal, répéter après4 sem- Revac: 1 x 1 dose après 5 m, ensuite 1dose/12 mpou<strong>la</strong>in sans imm mat (âge 4 m): 1 dose,suivie d’un protocole de vac completOOI: 2 sem après vac de baseDOI: 5 m après vac de base, 12 m après 1erevacTemps d’attente: 0 jseringues pré-remplies avec aiguilles 10 x 1doseR/PROTEQFLU (Merial)virus canarypox recombiné grippe A/equi-2/Ohio/03 [H3N8] (vCP2242):min 5,3 log10 FAID50/dosevirus canarypox recombiné grippe A/equi-2/Newmarket/2/93 [H3N8] (vCP1533):min 5,3 log10 FAID50/doseadjuv: carbomèrevaccin injectable imPosologie:Primovac:Eq (âge: min 5 - 6 m): 2 x 1 dose (1 ml) avec4 - 6 sem d’intervalleRevac: 5 m après <strong>la</strong> primovac, ensuite 1x/anen cas de risque accru: 1e vac à l’âge de 4 m,puis suivre schéma ci-dessusOOI: 14 j après vac de baseDOI: 5 m après vac de base et 1 an après 3evacTemps d’attente: 0 jf<strong>la</strong>con 10 x 1 doseR/ Vaccins combinés avecl’anatoxine tétaniqueDUVAXYN IE PLUS T (Eli Lilly)virus de <strong>la</strong> grippe équine, inact (par dose):A/Equi-1 Prague (H7N7): 15 mcg HA/1,5 mlA/Equi-2 Newmarket (H3N8): 15 mcg HA/1,5 mlA/Equi-2 Suffolk (H3N8) : 15 mcg HA/1,5 m<strong>la</strong>natoxine tétanique: 15 Lf/1,5 m<strong>la</strong>djuv: hydroxyde d’alminium, carbomère 934 Pvaccin injectable imPosologie:Primovac:Eq (âge > 3 m): 1 dose si risque accrud’infect., puis schéma suivant:Eq (âge > 5 - 6 m): 2 x 1 dose à 4 - 6 semd’intervalleRevac:6 m après primovacet 6 m après 1er rappelensuite 1 dose/anOOI: 2 sem après <strong>la</strong> vac, DOI: 6 mf<strong>la</strong>con 10 x 1 doseR/EQUILIS PREQUENZA TE (MSD A.H.)sous-unités purifiées d’hémagglutinines desvirus influenza équins:A/equine-1/Prague/56: 100 UAA/equine-2/Newmarket/1/93: 50 UAA/equine-2/Newmarket/2/93: 50 UAanatoxine tétanique: 40 EFadjuv: saponine, cholestérol,phosphatidylcholinevaccin injectable imPosologie:Eq (âge > 6 m):Primovac: 1 dose/animal, répéter après4 semRevac:- influenza: 1 dose après 5 m, ensuite 1dose/12 m- tétanos: 1 dose max 17 m après vac debase, suivi par 1 dose/2 anspou<strong>la</strong>in sans imm mat (âge 4 m): 1 dose,suivi d’un protocole de vac completEIV: OOI: 2 sem après vac de base, DOI: 5 maprès vac de base, 12 m après 1e revacTe: OOI: 2 sem après vac de base, DOI: 17 maprès vac de base, 24 m après 1e revacTemps d’attente: 0 jf<strong>la</strong>cons 10 x 1 dose (1 ml)seringues pré-remplies avec aiguilles 10R/
13 VACCINS POUR LE CHEVAL 221PROTEQFLU-TE (Merial)virus canarypox recombiné grippe A/equi-2/Ohio/03 [H3N8] (vCP2242):min 5,3 log10 FAID50/dosevirus canarypox recombiné grippe A/equi-2/Newmarket/2/93 [H3N8] (vCP1533):min 5,3 log10 FAID50/doseanatoxine Clostridium tetani: min 30 UI/doseadjuv: carbomèrevaccin injectable imPosologie:Primovac:Eq (âge: min 5 - 6 m): 2 x 1 dose (1 ml) avec4 - 6 sem d’intervalleRevac: 5 m après <strong>la</strong> primovac, ensuite 1x/anen cas de risque accru: 1e vac à l’âge de 4 m,puis suivre schéma ci-dessusOOI: 14 j après vac de baseDOI: 5 m après vac de base et après <strong>la</strong> primovacet le rappel 5 m plus tard : 1 an pour <strong>la</strong>grippe équine et 2 ans pour le tétanosTemps d’attente: 0 jf<strong>la</strong>con 10 x 1 doseR/RhinopneumonieL’herpèsvirus équin de type 1 (EHV-1)et l’EHV-4 sont présents de manièreenzootique dans <strong>la</strong> popu<strong>la</strong>tion équine.Les deux virus se multiplient d’aborddans le système respiratoire. Ce phénomènepeut entraîner des troublesrespiratoires (rhinopneumonie). C’estsurtout dans le cas <strong>du</strong> EHV-1 que <strong>la</strong>multiplication primaire est suivie d’unevirémie. Le virus se localise dans lesglobules b<strong>la</strong>ncs et se dissémine dansdifférents organes cibles, aussi bienl’utérus que le système nerveux. Cecipeut entraîner des avortements, de<strong>la</strong> mortalité néonatale et des troublesnerveux.VaccinVaccin contre <strong>la</strong> rhinopneumonieCes vaccins inactivés peuvent être utiliséschez les chevaux et les poneysquel que soit leur état physiologique.ProtectionLes vaccins actuellement disponiblespour le contrôle de l’EHV-1 et del’EHV-4 assurent principalement uneprotection clinique contre l’apparitionde troubles respiratoires. La protectioncontre les avortements, <strong>la</strong> mortaliténéonatale ou les troubles nerveux nepeut pas être garantie, car, même enprésence d’anticorps neutralisants,une virémie peut apparaître suite à une(ré-)infection par l’EHV-1 suivie d’unedissémination vers les organes cibles.Les animaux peuvent être vaccinésdès <strong>la</strong> disparition de l’immunité maternelle.Des revaccinations régulièressont conseillées. Vaccin contre <strong>la</strong> rhinopneumonieEQUIP EHV 1,4 (Pfizer A.H.)herpèsvirus équin inact:EHV-1 (438/77): min 10exp 7,3 DICT50/doseEHV-4 (405/76): min 10exp 7,3 DICT50/doseadjuv: carbopolvaccin injectable imPosologie:Primovac:Eq (âge > 5 - 6 m ou > 3 m lorsque risqueélevé d’infect.):2 x 1 dose (1,5 ml) à 4 - 6 sem d’intervalleRevac:1 dose/ 6 mjument: 1 dose au cours des 5e, 7e et 9emois de <strong>la</strong> graviditéOOI: 3 semDOI: 6 mTemps d’attente: 0 jf<strong>la</strong>con 10 x 1 doseR/Virus de <strong>la</strong> fièvre <strong>du</strong> Nil occidental(West Nile)Le virus de <strong>la</strong> fièvre <strong>du</strong> Nil occidentalou virus West Nile est un f<strong>la</strong>vivirus appartenantau sérogroupe de l’encéphalitejaponaise. Il s’agit d’un arbovirus àARN, dont les vecteurs sont des moustiques<strong>du</strong> genre Culex. Les oiseauxjouent le rôle de réservoir. Le virus estcapable d’infecter une très grande diversitéd’animaux, et spécialement lecheval et l’homme qui peuvent développerune ma<strong>la</strong>die de gravité variablejusqu’à une encéphalite mortelle.Le virus peut être intro<strong>du</strong>it dans unenouvelle région par le biais d’oiseauxmigrateurs. Des moustiques contaminéspeuvent infecter les mammifèreset l’homme. L’homme et le cheval sontdes hôtes accidentels. La virémie esttrop faible chez les mammifères etles espèces animales autres que lesoiseaux pour infecter les moustiques :ce virus ne se propage pas parmi cesanimaux, qui sont donc des culs-desacépidémiologiques. Les signescliniques après infection sont principalementobservés chez le cheval, dansseulement 10% des cas infectés. Lessignes peuvent apparaître de manièreaiguë ou gra<strong>du</strong>ellement. Les principauxsignes cliniques tra<strong>du</strong>isent uneméningo-encéphalomyélite descendante: faiblesse muscu<strong>la</strong>ire, incoordination,ataxie, parésie, paralysie desmembres postérieurs, puis des quatremembres, et qui peut évoluer en uneencéphalite fatale.VaccinLe vaccin contient <strong>la</strong> souche VM-2 <strong>du</strong>virus West Nile inactivé, issu d’un iso<strong>la</strong>taméricain qui protège également
22213 VACCINS POUR LE CHEVALcontre les types de virus sauvagesrencontrés en Europe.ProtectionLe vaccin est indiqué dans l’immunisationactive des chevaux de 6 moiset plus contre <strong>la</strong> ma<strong>la</strong>die causée parle virus West Nile, en vue de ré<strong>du</strong>irele nombre de chevaux virémiques. Levaccin diminue et prévient les signescliniques chez les animaux vaccinés.Après <strong>la</strong> vaccination, une légèretuméfaction peut survenir au niveau<strong>du</strong> site d’injection, elle disparait spontanémentaprès 1 à 2 jours. Danscertains cas, de l’hyperthermie semanifeste <strong>du</strong>rant les 2 jours suivant <strong>la</strong>vaccination.Particu<strong>la</strong>ritésL’interférence de <strong>la</strong> vaccination sur <strong>la</strong>surveil<strong>la</strong>nce épidémiologique est faibleétant donné l’absence de particulesvirales vivantes dans le vaccin et untaux d’ARN viral très faible, qui n’estdonc probablement pas détecté parles techniques de PCR. Elle est faiblesi les tests sérologiques sont baséssur <strong>la</strong> détection d’anticorps IgM, présentsen cas d’infections naturellesmais pas en cas de vaccination. Cetteinterférence est néanmoins réelle si lestests sérologiques dépistent les IgG.Cette ma<strong>la</strong>die est à déc<strong>la</strong>ration obligatoire(A.R. <strong>du</strong> 25/04/1988 désignantles ma<strong>la</strong>dies des animaux soumises àl’application <strong>du</strong> chapitre III de <strong>la</strong> loi <strong>du</strong>24 mars 1987).EQUIP WNV (Pfizer A.H.)West Nile Virus inact, souche VM-2: 1,0- 2,2 RPadjuv: huilevaccin injectable imPosologie:Eq (âge > 6 m):Primovac: 2 x 1 dose (1 ml)/animal à 3 - 5sem d’intervalleRevac: 1 dose/an (non validé)OOI: 3 sem après vac de baseDOI: 12 m après vac de baseTemps d’attente: 0 jseringue 5 x 1 doseR/iPROTEQ WEST NILE (Merial)virus canarypox recombiné West Nile(vCP2017): 6.0 à 7.8 log10 CCID50adjuv: carbomèrevaccin injectable imPosologie:Primovac:Eq (âge: min 5 m): 2 x 1 dose (1 ml) à 4 - 6sem d’intervalleRevac: 1x/anOOI: 4 sem après vac de base, DOI: 1 an aprèsvac de base avec 2 injTemps d’attente: 0 jf<strong>la</strong>con 2 x 1 doseR/i13.1.1.2 Vaccination contre lesma<strong>la</strong>dies bactériennesTétanosCette affection est caractérisée par desspasmes toniques des muscles striéssuite à <strong>la</strong> formation d’une exotoxine,<strong>la</strong> tétanospasmine, par <strong>la</strong> bactérieClostridium tetani. Dans un milieu anaérobie,ce germe peut engendrer uneinfection de <strong>la</strong> p<strong>la</strong>ie ou de l’ombilic. Iln’est cependant pas invasif et <strong>la</strong> multiplicationse ré<strong>du</strong>it à <strong>la</strong> p<strong>la</strong>ie. C’est à ceniveau que se forme <strong>la</strong> tétano spasminequi atteint le système nerveux centralpar les fibres nerveuses, les vaisseauxlymphatiques et sanguins. Latoxine agit sur <strong>la</strong> corne ventrale de <strong>la</strong>moelle épinière et au niveau <strong>du</strong> tronccérébral. Elle bloque, au niveau desextrémités nerveuses présynaptiques,l’excrétion de neurotransmetteurs telsque <strong>la</strong> glycine ou l’acide gamma-aminobutyrique, levant ainsi le contrôleexercé par les neurones inhibiteurs etprovoquant les spasmes muscu<strong>la</strong>irescaractéristiques.VaccinVaccin monovalent contre le tétanos- Vaccins combinés avec l’anatoxinetétanique et le virus de <strong>la</strong> grippeéquine.ProtectionLes vaccins à base de l’exotoxine inactivéede C. tetani sont en mesure d’in<strong>du</strong>ireune très bonne protection contrecette affection. Plusieurs schémas devaccination sont proposés. Un animalvacciné pour <strong>la</strong> première fois doit recevoirdeux injections à 4 - 6 semainesd’intervalle. Chez les pou<strong>la</strong>ins issusd’une jument vaccinée, l’immunité maternellepeut interférer avec <strong>la</strong> vaccinationjusqu’à l’âge d’environ 4 – 5 mois.Une troisième vaccination a lieu depréférence six mois voire un an après<strong>la</strong> deuxième. Il est conseillé par <strong>la</strong> suitede répéter <strong>la</strong> vaccination annuellementou tous les trois ans. La revaccinationest également à conseiller chez lesanimaux ayant des p<strong>la</strong>ies suspectes.Lorsqu’une jument gestante reçoitune vaccination de rappel 1 à 3 moisavant <strong>la</strong> mise bas (avec un vaccin dont<strong>la</strong> notice assure l’innocuité lors de <strong>la</strong>gestation), son pou<strong>la</strong>in est protégé parl’immunité colostrale <strong>du</strong>rant 1 à 4 mois.Pour ce qui est des pou<strong>la</strong>ins nouveaunésissus d’une jument non vaccinée,il est recommandé de leur administrer
13 VACCINS POUR LE CHEVAL 223des anticorps contre l’exotoxine deC. tetani (voir chapitre 13.3.2). Vaccin contre le tétanosTETAPUR (Merial)anatoxine tétanique purif (souche IM 1472C):min 30 UI/m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:âge pou<strong>la</strong>ins dont mères vac: 6 mâge pou<strong>la</strong>ins dont mères non vac: 4 m- préventifPrimovac:2 x 1 dose (1 ml) à 1 m d’intervalleRevac:1 an plus tard, puis tous les 3 ansun rappel sera effectué après tout traumatismesuspect- curatif3 x 1 dose (im) à 4 - 5 j d’intervallesimultanément avec <strong>la</strong> 1e dose, et en unautre point, pratiquer une inject de sérumantitétanique par voie imOOI: 15 j après 1e vacDOI: 1 an après 1e vac, 3 ans après revacTemps d’attente: 0 jampoule monodose (1 ml) 10 x 1 doseR/ Vaccins combinant le tétanos etle virus de <strong>la</strong> grippe équineDUVAXYN IE PLUS T (Eli Lilly)virus de <strong>la</strong> grippe équine, inact (par dose):A/Equi-1 Prague (H7N7): 15 mcg HA/1,5 mlA/Equi-2 Newmarket (H3N8): 15 mcg HA/1,5 mlA/Equi-2 Suffolk (H3N8) : 15 mcg HA/1,5 m<strong>la</strong>natoxine tétanique: 15 Lf/1,5 m<strong>la</strong>djuv: hydroxyde d’alminium, carbomère 934 Pvaccin injectable imPosologie:Primovac:Eq (âge > 3 m): 1 dose si risque accrud’infect., puis schéma suivant:Eq (âge > 5 - 6 m): 2 x 1 dose à 4 - 6 semd’intervalleRevac:6 m après primovacet 6 m après 1er rappelensuite 1 dose/anOOI: 2 sem après <strong>la</strong> vac, DOI: 6 mf<strong>la</strong>con 10 x 1 doseR/EQUILIS PREQUENZA TE (MSD A.H.)sous-unités purifiées d’hémagglutinines desvirus influenza équins:A/equine-1/Prague/56: 100 UAA/equine-2/Newmarket/1/93: 50 UAA/equine-2/Newmarket/2/93: 50 UAanatoxine tétanique: 40 EFadjuv: saponine, cholestérol,phosphatidylcholinevaccin injectable imPosologie:Eq (âge > 6 m):Primovac: 1 dose/animal, répéter après4 semRevac:- influenza: 1 dose après 5 m, ensuite 1dose/12 m- tétanos: 1 dose max 17 m après vac debase, suivi par 1 dose/2 anspou<strong>la</strong>in sans imm mat (âge 4 m): 1 dose,suivi d’un protocole de vac completEIV: OOI: 2 sem après vac de base, DOI: 5 maprès vac de base, 12 m après 1e revacTe: OOI: 2 sem après vac de base, DOI: 17 maprès vac de base, 24 m après 1e revacTemps d’attente: 0 jf<strong>la</strong>cons 10 x 1 dose (1 ml)seringues pré-remplies avec aiguilles 10R/PROTEQFLU-TE (Merial)virus canarypox recombiné grippe A/equi-2/Ohio/03 [H3N8] (vCP2242):min 5,3 log10 FAID50/dosevirus canarypox recombiné grippe A/equi-2/Newmarket/2/93 [H3N8] (vCP1533):min 5,3 log10 FAID50/doseanatoxine Clostridium tetani: min 30 UI/doseadjuv: carbomèrevaccin injectable imPosologie:Primovac:Eq (âge: min 5 - 6 m): 2 x 1 dose (1 ml) avec4 - 6 sem d’intervalleRevac: 5 m après <strong>la</strong> primovac, ensuite 1x/anen cas de risque accru: 1e vac à l’âge de 4 m,puis suivre schéma ci-dessusOOI: 14 j après vac de baseDOI: 5 m après vac de base et après <strong>la</strong> primovacet le rappel 5 m plus tard : 1 an pour <strong>la</strong>grippe équine et 2 ans pour le tétanosTemps d’attente: 0 jf<strong>la</strong>con 10 x 1 doseR/
22413 VACCINS POUR LES RUMINANTSTableau récapitu<strong>la</strong>tif des vaccins pour le chevalvirus influenzavirus de <strong>la</strong>rhinopneumonievirus de <strong>la</strong> fièvre <strong>du</strong>Nil occidentaltétanosrageDUVAXYN IE-PLUS-TPfizer A.H.XXEQUILIS PREQUENZAMSD A.H.XEQUILIS PREQUENZA TEMSD A.H.XXEQUIP EHV 1,4Pfizer A.H.XEQUIP WNVPfizer A.H.XNOBIVAC RABIESMSD A.H.XPROTEQFLUMerialXPROTEQFLU-TEMerialXXPROTEQ WEST NILEMerialXRABISINMerialXTETAPURMerialX13.1.2 Vaccins pour les ruminants13.1.2.1 Vaccins contre les ma<strong>la</strong>diesvirales chez les bovinsLes vaccins contre les ma<strong>la</strong>diesrespiratoires des bovinsLes agents pathogènes suivants sontprincipalement responsables de ma<strong>la</strong>diesrespiratoires chez les bovins :- virus respiratoire syncytial bovin(RSB) ;- virus de <strong>la</strong> rhinotrachéite infectieusebovine (IBR) ;- virus para-influenza 3 bovin (PI-3) ;- adénovirus bovins ;- Mannheimia haemolytica.- Histophilus somni.On peut également citer les mycop<strong>la</strong>smesbovins. Le virus de <strong>la</strong> diarrhéevirale bovine (BVD) n’est pas unvirus directement pneumotrope, maisson infection peut être associée à destroubles respiratoires.VaccinVaccins monovalents contre le virusRSB, le virus IBR (voir plus loin), le virusBVD (voir plus loin) et Mannheimiahaemolytica (voir plus loin) - Vaccinsmultivalents contre le virus RSB, levirus PI-3, le virus BVD et Mannheimiahaemolytica.Ces vaccins sont soit atténués, soitinactivés. Un vaccin ne peut être administrépar voie intranasale que si cettevoie est c<strong>la</strong>irement mentionnée dans <strong>la</strong>notice <strong>du</strong> vaccin. Le choix entre vaccinsmonovalents et multivalents doitêtre motivé par <strong>la</strong> situation épidémiologiquede l’exploitation et l’anamnèse
13 VACCINS POUR LES RUMINANTS 225qui permettent de connaître quelsagents pathogènes sont présents.ProtectionDans le cadre de <strong>la</strong> prévention desma<strong>la</strong>dies respiratoires, <strong>la</strong> vaccinationcontre le virus BVD peut être envisagéede deux manières: soit <strong>la</strong> vaccinationdes jeunes animaux à partir del’âge de 3 à 4 mois, soit <strong>la</strong> vaccinationdes génisses et des vaches dans lebut d’empêcher l’apparition d’animauxinfectés persistants immunotolérantsresponsables de <strong>la</strong> circu<strong>la</strong>tion<strong>du</strong> virus BVD. La prévalence élevée deces infections dans le cheptel bovinest responsable de <strong>la</strong> présence d’uneimmunité colostrale chez de nombreuxveaux. Cette immunité maternelle peutinterférer avec <strong>la</strong> vaccination jusqu’àl’âge de 3 à 4 mois. Il est impératif que<strong>la</strong> notice vaccinale mentionne c<strong>la</strong>irement<strong>la</strong> possibilité de protéger en surmontantl’interférence colostrale. Eneffet, <strong>la</strong> plupart des vaccins présententune bonne innocuité chez le veau,même nouveau-né, et peuvent doncêtre injectés sans réaction secondairedéfavorable. Cette indication d’innocuiténe représente en aucune manièreun gage d’efficacité à un âge inférieurà 3 ou 4 mois où l’immunité passivepeut interférer avec le développementd’une réponse vaccinale protectrice.Comme le statut indivi<strong>du</strong>el de chaqueveau vacciné est inconnu et en l’absenced’information sur l’efficacité de<strong>la</strong> vaccination en présence d’anticorpscolostraux, il est nécessaire de répéteren tout ou en partie le protocolede vaccination lorsque l’âge de 3 à 4mois est atteint. En général, un vaccinatténué administré par voie intranasalein<strong>du</strong>it une réponse immune capablede mieux surmonter l’interférencein<strong>du</strong>ite par les anticorps colostraux. Ilest impératif que <strong>la</strong> notice vaccinalementionne c<strong>la</strong>irement <strong>la</strong> possibilité deprotéger en surmontant l’interférencecolostrale. L’apparition de <strong>la</strong> protectionest généralement plus précocelors d’injection intranasale que lorsd’administration parentérale. La <strong>du</strong>réed’immunité est inférieure à un an pourplusieurs vaccins, et en particulierpour les vaccins contre le RSB. Il estdonc recommandé de vacciner les animauxavant <strong>la</strong> période de l’année oùl’incidence maximale de <strong>la</strong> ma<strong>la</strong>die estconstatée, soit, pour les ma<strong>la</strong>dies respiratoires,avant l’automne et l’hiver.Particu<strong>la</strong>ritésLa qualité de <strong>la</strong> protection conféréepar un vaccin dépend de <strong>la</strong> maîtrise<strong>du</strong> protocole de repro<strong>du</strong>ction expérimentalede <strong>la</strong> ma<strong>la</strong>die. Elle est aiséepour le virus IBR et, dans ce cas, lesvaccins peuvent être testés expérimentalementenvers l’infection et <strong>la</strong>ma<strong>la</strong>die telles qu’elles se présententnaturellement. Aussi, on dispose devaccins contre l’IBR dont l’efficacitécontre <strong>la</strong> ma<strong>la</strong>die clinique estde bonne qualité. En revanche, lesmodèles expérimentaux d’infectionspar les virus RSB, PI-3 imitent beaucoupmoins les situations naturelles.Dans tous les cas, les études réaliséesdoivent être conformes aux monographiesde <strong>la</strong> Pharmacopée Européenne,lorsqu’elles existent. En conséquence,les vaccins développés contre ces infectionsvirales peuvent actuellementprésenter des défauts dont les firmespharmaceutiques ne sont pas responsableset qui ne pourront être corrigésque lorsque les connaissances scientifiquesauront progressé. Vaccins contre le virusrespiratoire syncytial bovin (virusRSB)Vaccin combiné contre le virus RSBet le virus PI-3 bovinRISPOVAL RS + PI3 intranasal (Pfizer A.H.)virus att <strong>du</strong> parainfluenza bovin 3 (PI3), soucheRLB 103: 10exp5.0 à 10exp8.6 CCID50/dosevirus syncytial respiratoire bovin (BSRV) att,souche 375: 10exp5.0 à 10exp7.2 CCID50/dosevaccin lyophilisé et solvant inasPosologie:Bo (âge > 9 j): 1 x 1 dose (2 ml)OOI: 5 j (BRSV) - 10 j (PI3V) après vacDOI: 12 semTemps d’attente: 0 jf<strong>la</strong>con 5 doses (lyophilisat) + 10 ml de solvantR/
22613 VACCINS POUR LES RUMINANTSVaccin combiné contre le virus RSBet le virus PI-3 bovin (incluantM. haemolytica)BOVILIS BOVIPAST RSP (MSD A.H.)BRSV inact (souche EV 908): min 10exp 5,5 -max 10exp 6,4 DICT50/5 mlvirus PI-3 inact (souche SF-4 Reisinger): min10exp 7,3 - max 10exp 8,3 DICT50/5 mlMannheimia (Pasteurel<strong>la</strong>) haemolytica inact (A1,souche M4/1): 9 x 10exp 9 cellulesadjuv: hydroxyde d’aluminium, Quil A (saponine)vaccin injectable scPosologie:Primovac:Bo (âge > 2 sem): 2 x 1 dose (5 ml) à 4 semd’intervalleRevac:Bo: 1 dose 2 sem avant période à risqueOOI: 2 sem après vac de base, l’imm humoraleest maxDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/Vaccin combiné contre le virusRSB, le virus bovin PI-3-virus et levirus BVDRISPOVAL 3 BRSV-PI3-BVD (Pfizer A.H.)- lyophilisat:virus PI-3 att (RLB103): min 10 exp5.0 et max10 exp8.6 CCID50virus RSB att (375): min 10 exp5.0 et max10 exp7.2 CCID50- suspension:virus BVD type 1 inact, souches 5960 (cytopathogène)et 6309 (non cytopathogène): in<strong>du</strong>it untitre moyen séroneutralisant chez le cobaye demin 3,0 log2adjuv: Alhydrogel (hydroxyde d’aluminium)vaccin injectable imPosologie:Bo (âge > 12 sem): 2 x 1 dose (4 ml) à 3 - 4sem d’intervalleRevac:tous les 6 m (pour les virus BRS et BVD, <strong>la</strong><strong>du</strong>rée d’immunité <strong>du</strong> virus PI-3 n’est pasconnue)OOI: BRSV, virus PI3 et BVDV de type1: 3 semaprès vacDOI: BRSV et BVDV de type1: 6 m après vac,virus PI3: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 5 doses de lyophilisat + 5 doses desuspensionR/ Vaccins contre <strong>la</strong> rhinotrachéiteinfectieuse bovine (IBR)La légis<strong>la</strong>tion belge impose l’utilisationde vaccins contre l’IBR qui possèdentcomme marqueur sérologiquel’absence de <strong>la</strong> glycoprotéine viraled’enveloppe E (gE). (voir plus loin,“Particu<strong>la</strong>rités”)VaccinLes vaccins marqués, dénommés négatifsenvers gE, immunisent l’animalcontre tous les antigènes <strong>du</strong> virus responsable,soit le BoHV-1, sauf <strong>la</strong> glycoprotéinegE. Un examen sérologiquepermet de différencier les animauxséronégatifs envers gE (animaux vaccinésà l’aide <strong>du</strong> vaccin marqué) desbovins séropositifs (animaux infectésnaturellement). Les vaccins contrel’IBR sont soit vivants atténués, soitinactivés. Les vaccins vivants peuventêtre administrés soit par voie intranasale,soit par voie parentérale. Lesvaccins inactivés sont exclusivementinjectés par voie parentérale.ProtectionLa vaccination contre l’IBR est appliquéedans deux situations épidémiologiquestrès précises: une prévalenceélevée d’animaux séropositifs enversle BoHV-1 et/ou une incidence élevéedes signes cliniques associés à l’infectionpar le BoHV-1. Dans le premier cas,elle est liée à une volonté de contrôler,voire d’éradiquer l’IBR dans <strong>la</strong> ferme.Dans l’autre cas, son objectif est demaîtriser les conséquences cliniquesde l’infection virale. Le protocole devaccination appliqué sera donc différentselon <strong>la</strong> situation rencontrée. Laprotection contre les signes cliniquesest atteinte après primovaccination. Sicelle-ci est effectuée chez des veauxde moins de 3 mois, <strong>la</strong> vaccinationintranasale par un vaccin atténué estrecommandée. L’animal sera revaccinélorsqu’il aura atteint l’âge de 3mois. Des vaccinations répétées serontnécessaires dans une situation decontrôle et d’éradication de l’IBR dansune exploitation. Après <strong>la</strong> primovaccination,des rappels de vaccination seronteffectués tous les 6 mois jusqu’àl’obtention d’un statut où les animauxseront tous séronégatifs envers <strong>la</strong> glycoprotéinegE. A ce moment, le virussauvage ne sera plus présent dansl’exploitation et celle-ci pourra évoluervers un statut complètement négatifenvers l’IBR.Particu<strong>la</strong>ritésDepuis le 5 janvier 2012, tout éleveurde bovins doit disposer d’un statut IBRva<strong>la</strong>ble: I2, I3 ou I4. Les exploitationsqui ne sont pas en mesure de présenterun statut IBR va<strong>la</strong>ble se voient attribuerautomatiquement un statut I1.Dans ce cas, il y a interdiction de pâturageet les bovins ne peuvent qu’êtretransportés à l’abattoir. La vente debétail à d’autres éleveurs n’est plusautorisée. L’AFSCA effectuera descontrôles supplémentaires dans lesexploitations à statut I1.L’IBR clinique est une ma<strong>la</strong>die à déc<strong>la</strong>rationobligatoire. Dès que <strong>la</strong> sus-
13 VACCINS POUR LES RUMINANTS 227picion est confirmée par les résultatsdes analyses, l’AFSCA doit en êtreinformée.Arrêté royal <strong>du</strong> 22 novembre 2006 re<strong>la</strong>tifà <strong>la</strong> lutte contre <strong>la</strong> rhinotrachéiteinfectieuse bovine;Arrêté royal <strong>du</strong> 16 février 2011 modifiantl’arrêté royal <strong>du</strong> 22 novembre 2006re<strong>la</strong>tif à <strong>la</strong> lutte contre <strong>la</strong> rhinotrachéiteinfectieuse bovine.Voir aussi:www.arsia.be/?page_id=406 ouwww.dgz.be/programma/ibr-bestrijdingBOVILIS IBR MARKER INAC (MSD A.H.)herpèsvirus bovin type 1 inact, souche GK/D(gE-): 60 U ELISA pour l’in<strong>du</strong>ction de6,1 - 11,1 log2 U VNadjuv: hydroxyde d’aluminium, phosphated’aluminiumvaccin injectable imPosologie:Bo (âge > 3 m): 2 x 1 dose (2 ml) à 4 semd’intervalleRevac: 1 dose tous les 6 mOOI: 3 sem après vac de baseDOI: 6 m après vac de baseTemps d’attente: 0 jf<strong>la</strong>con 10, 50 dosesR/iBOVILIS IBR MARKER LIVE (MSD A.H.)par dose (2 ml):herpèsvirus bovin type 1 (souche GK/D, gE-négatif):10exp 5,7 - 10 exp7,3 TCID50vaccin lyophilisé et solvant injectableinas (âge 2 sem - 3 m), im, inas (âge > 3 m)Posologie:Primovac:Bo (âge 2 sem - 3 m): 1 dose/animal, répéterà l’âge de 3 - 4 mBo (âge > 3 m): 1 dose/animalRevac:1 dose/6 mOOI: Bo (âge min 3 m, séronég): 4 j (vac inas)ou 14 j (vac im) après vacDOI: Bo (âge 2 sem, séronég): jusqu’à l’âge de3 - 4 m, après revac à l’âge de 3 - 4 m: min 6 mOOI: Bo (âge 3 m, inas, im): 3 sem après vacDOI: min 6 m après 1 vacTemps d’attente: 0 jf<strong>la</strong>con 5, 10, 25 dosesR/iHIPRABOVIS IBR MARKER LIVE (Hipra Lab)par dose (2 ml):- lyophilisat:herpèsvirus bovin de type 1 (BoHV-1) (soucheCEDDEL): 10exp6.3 – 10exp7.3 DICC50vaccin lyophilisé et solvant injectable imPosologie:Bo (âge > 3 m):dose initiale: 2 x 1 dose/animal à 3 semd’intervallerevac: 1 dose/6 mOOI: 21 j après vac de baseDOI: 6 m après vac de baseTemps d’attente: 0 jf<strong>la</strong>con 5 doses, 25 dosesR/iIBRAXION (Merial)virus IBR (gE-négatif): min 0,75 VN U/2 m<strong>la</strong>djuv: paraffine-huile légèrevaccin injectable scPosologie:Bo:Primovac:pas d’imm mat (âge > 2 sem):2 x 1 dose (2 ml) à 21 j d’intervalleimm mat (âge > 3 m): 2 x 1 dose à 21 jd’intervalleRevac: tous les 6 mOOI: 14 j, DOI: 6 mTemps d’attente: 0 jf<strong>la</strong>con 10 dosesR/iRISPOVAL IBR-MARKER INACTIVATUM(Pfizer A.H.)herpèsvirus bovin type 1 inact (Difivac, gE-négatif):titre en anticorps séroneutralisant d’aumoins 1:160 chez les Bo (2 ml)adjuv: hydroxyde d’aluminium, Quil Avaccin injectable scPosologie:Primovac:Bo (âge > 3 m): 2 x 1 dose (2 ml) à 3 - 5 semd’intervalleRevac après primovac avec RISPOVAL IBRMARKER INACTIVATUM:Bo: 1 dose tous les 6 mRevac après primovac avec RISPOVAL IBRMARKER VIVUM:Bo: 1 dose 6 m après <strong>la</strong> primovac, ensuitetous les 12 mOOI: pas d’infoDOI: 6 m après primovac avec Rispoval IBR viv,12 m après révac avec Rispoval IBR inac.Temps d’attente: 0 jf<strong>la</strong>con 10 doses (20 ml)50 doses (100 ml)R/i
22813 VACCINS POUR LES RUMINANTSRISPOVAL IBR-MARKER VIVUM (Pfizer A.H.)herpèsvirus bovin type 1 att (Difivac, gE-négatif):min 10exp 5 CCID50 - max 10exp 7CCID50/dosevaccin lyophilisé et solvant inas, imPosologie:Primovac:Bo (âge 2 sem – 3 m): 1 dose (2 ml) inas,2e dose à l’âge de 3 m (im)Bo avec imm mat: 1 dose supplémentaire(inas ou im) 3 sem après 1e vacBo (âge > 3 m): 1 x 1 dose (im)Bo en gestation: 2 x 1 dose (2 ml) à 3 - 5sem d’intervalle (im)Bo à risque infectieux immédiat: 1 doseinas, 2de dose après 3-5 sem (im)Revac:Bo: 1e revac à l’âge de 6 m, ensuite tous les6 m (RISPOVAL IBR-MARKER VIVUM) ou 12m (RISPOVAL IBR-MARKER INACTIVATUM)OOI: 7 j après 1e dose inas ou 21 j après 1edose imDOI (Bo âge 3 m ou plus): 6 mTemps d’attente: 0 jf<strong>la</strong>con 10 doses (20 ml)50 doses (100 ml)R/iVaccins contre les diarrhées viralesbovines Vaccins contre <strong>la</strong> diarrhée viralebovine – ma<strong>la</strong>die des muqueuses(BVD-MD)Le virus BVD peut exercer son actionpathogène de deux manières différentes.L’infection post-natale est responsablede <strong>la</strong> diarrhée virale bovine,<strong>du</strong> syndrome hémorragique ou de l’intervention<strong>du</strong> virus BVD dans des pathologiesmultifactorielles respiratoiresou digestives. L’infection in utero mèneà <strong>la</strong> mortalité embryonnaire, l’avortement,des anomalies congénitalesou à <strong>la</strong> pro<strong>du</strong>ction de veaux infectéspersistants immunotolérants (IPI). Lesanimaux IPI sont des excréteurs persistantsde virus et sont donc responsablesde <strong>la</strong> circu<strong>la</strong>tion <strong>du</strong> virus dansl’exploitation. Lorsque les animaux IPIsont surinfectés par une souche debiotype cytopathogène de même antigénicitéque <strong>la</strong> souche non cytopathogènequ’ils hébergent, ils développent<strong>la</strong> ma<strong>la</strong>die des muqueuses mortelle.VaccinVaccin monovalent – vaccin combinéLes virus BVD présents dans les vaccinsdoivent être capables d’immuniserl’animal envers un <strong>la</strong>rge spectre desouches virales d’antigénicité variable.La présence de virus BVD de génotypeII en Belgique et dans d’autres payseuropéens, où le génotype I est le plusprévalent, rend également nécessairel’utilisation de vaccins qui puissentprotéger les bovins contre les deuxespèces de virus BVD.ProtectionLa vaccination doit aussi être adaptéeau type d’infection contre lequel ondésire protéger l’animal. La protectioncontre les infections post-natales,principalement les ma<strong>la</strong>dies respiratoires,est obtenue par <strong>la</strong> vaccinationdes jeunes veaux, lorsque l’immunitécolostrale n’interfère plus avec<strong>la</strong> vaccination. La protection contre<strong>la</strong> virémie et plus précisément contrel’infection intra-utérine est obtenuepar <strong>la</strong> vaccination des génisses oudes vaches avant <strong>la</strong> gestation. A ceteffet, <strong>la</strong> notice vaccinale doit indiquer<strong>la</strong> nature de <strong>la</strong> protection conférée :soit contre l’infection post-natale, soitcontre <strong>la</strong> virémie, soit contre l’infectionin utero. L’efficacité de <strong>la</strong> vaccinationdes vaches gestantes pour enrichirle colostrum en anticorps anti-BVDet protéger passivement le veau nouveau-nén’est pas établie.Vaccin monovalentBOVILIS BVD (MSD A.H.)virus BVD inact (C86): eq. à 50 U Elisa in<strong>du</strong>isantmin 4,6 log2 VN Uadjuv: hydroxyde d’aluminium, phosphated’aluminumvaccin injectable imPosologie:Bo (âge > 8 m):Vac indivi<strong>du</strong>elle:Primovac:2 x 1 dose (2 ml) à 4 sem d’intervalle (2e vacau moins 4 sem avant <strong>la</strong> gestation)Revac:1 dose 4 sem avant <strong>la</strong> prochaine gestationVac <strong>du</strong> troupeau:Primovac:Bo (âge > 8 m): 2 x 1 dose à 4 semd’intervalleRevac: 1 dose/6 mOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 10 ml, 20 ml, 50 mlR/
13 VACCINS POUR LES RUMINANTS 229Vaccin combinéRISPOVAL 3 BRSV-PI3-BVD (Pfizer A.H.)- lyophilisat:virus PI-3 att (RLB103): min 10 exp5.0 et max10 exp8.6 CCID50virus RSB att (375): min 10 exp5.0 et max10 exp7.2 CCID50- suspension:virus BVD type 1 inact, souches 5960 (cytopathogène)et 6309 (non cytopathogène): in<strong>du</strong>it untitre moyen séroneutralisant chez le cobaye demin 3,0 log2adjuv: Alhydrogel (hydroxyde d’aluminium)vaccin injectable imPosologie:Bo (âge > 12 sem): 2 x 1 dose (4 ml) à 3 - 4sem d’intervalleRevac:tous les 6 m (pour les virus BRS et BVD, <strong>la</strong><strong>du</strong>rée d’immunité <strong>du</strong> virus PI-3 n’est pasconnue)OOI: BRSV, virus PI3 et BVDV de type1: 3 semaprès vacDOI: BRSV et BVDV de type1: 6 m après vac,virus PI3: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 5 doses de lyophilisat + 5 doses desuspensionR/Vaccins contre les diarrhéesnéonatales d’origine viraleVaccinLes vaccins destinés à <strong>la</strong> protectioncontre les virus responsables de<strong>la</strong> diarrhée néonatale chez le veaucontiennent les deux valences rotaviruset coronavirus. La valence E. coliest souvent associée. La vaccination<strong>du</strong> veau à <strong>la</strong> naissance est théoriquementpossible, car le veau nouveau-néest immunocompétent. Cependant,<strong>la</strong> période d’incubation des diarrhéesvirales est plus courte que le tempsnécessaire à l’in<strong>du</strong>ction de <strong>la</strong> protectionpost-vaccinale et <strong>la</strong> vaccinationen période néonatale n’est pas recommandée.Ces vaccins ont dès lors étédéveloppés pour l’immunisation de <strong>la</strong>mère <strong>du</strong>rant <strong>la</strong> gestation, de manière àconférer au veau une immunité colostralespécifique.ProtectionPour obtenir un colostrum enrichi enanticorps anti-rotavirus et coronavirus,<strong>la</strong> deuxième injection de vaccin ou lerappel de vaccination doit être réaliséaux environs de 2 à 4 semaines avant<strong>la</strong> date prévue de parturition. La vaccinationau moment de <strong>la</strong> parturitionpermet uniquement d’enrichir le <strong>la</strong>it enanticorps spécifiques, mais <strong>la</strong> concentrationen anticorps est 100 fois plusfaible dans le <strong>la</strong>it que dans le colostrum.C’est donc <strong>la</strong> vaccination <strong>du</strong>rant<strong>la</strong> gestation qui est recommandée.Particu<strong>la</strong>ritésLa vaccination contre les diarrhéesnéonatales doit prendre en considérationtrois éléments qui sont tous trèscritiques pour l’efficacité de l’immunisation:1) <strong>la</strong> vaccination appropriéedes mères, 2) l’ingestion d’une quantitésuffisante de colostrum de bonnequalité, suffisamment tôt dans <strong>la</strong> vie<strong>du</strong> veau (un demi-litre à <strong>la</strong> naissanceet deux litres dans les deux premièresheures de <strong>la</strong> vie), et 3) l’hygiène del’élevage des veaux nouveau-nés.Vaccins contre les rotavirus et coronaviruscombinés avec E. coliBOVILIS LACTOVAC (Pfizer A.H.)rotavirus bovin inact (1005/78):10exp 7,4 DICT50/doserotavirus bovin inact (Hol<strong>la</strong>nd):10exp 7,0 DICT50/dosecoronavirus bovin inact (800):10exp 5,8 DICT50/doseE. coli inact F5/F41: min 250 UHA/doseadjuv: hydroxyde d’aluminium, saponinevaccin injectable scPosologie:Primovac:Bo: 2 x 1 dose (5 ml) à 4 - 5 sem d’intervalle(1ère à 6 - 8 sem et 2e à 1 - 3 sem avant <strong>la</strong>mise bas)Revac:Bo: 1 dose 2 - 6 sem avant <strong>la</strong> mise basImmunisation passive <strong>du</strong> veau: donner lecolostrum de <strong>la</strong> vache vaccinée dans lespremières 12 h après <strong>la</strong> naissanceOOI-DOI: pas d’infoViande, Lait: 0 jf<strong>la</strong>con 25 ml (5 doses)R/ROTAVEC CORONA (MSD A.H.)par dose de 2 ml:- 1/4 de dose <strong>du</strong> vaccin:rotavirus bovin inact (souche UK-Compton,sérotype G6 P5): min 7,7 log2/ml d’Ac neutralisantle virus (cobaye)- 1/20 de dose <strong>du</strong> vaccin:coronavirus bovin inact (souche Mebus):min 3,41 log10/ml d’Ac ELISA (cobaye)adhésine E. coli F5 (K99): min 0,64 d’Ac ELISA(OD492) (cobaye)adjuv: huile minérale, hydroxyde d’aluminiumvaccin injectable imPosologie:Bo (gestant): 1 x 1 dose (2 ml) entre 12 - 3sem avant <strong>la</strong> mise basOOI: dès le début de <strong>la</strong> prise de colostrumDOI: veau artificiellement nourri: jusqu’à <strong>la</strong> finde l’administration de colostrum, veau al<strong>la</strong>ité:rotavirus: 7 j, coronavirus: 14 jTemps d’attente: 0 jf<strong>la</strong>con 10 ml, 40 mlR/
23013 VACCINS POUR LES RUMINANTSSCOURGUARD 3 (Pfizer A.H.)- fraction lyophilisée:rotavirus bovin att (Lincoln, groupe A sérotypeG6): 10exp 7 - 10exp8 DICC50/2 mlcoronavirus bovin att (Hansen):10exp 5 - 10 exp 7,5 DICC50/2 ml- fraction liquide:E. coli F5 (K99): 10exp 10 - 2 x 10exp 10germes/2 mlvaccin lyophilisé et solvant injectable imPosologie:Primovac:Bo: 1 x 1 dose 6 - 8 sem sem avant <strong>la</strong> misebas2e dose 3 sem avant <strong>la</strong> mise basRevac:Bo: 1 dose/an 3 sem avant chaque mise basImmunisation passive <strong>du</strong> veau par lecolostrum de <strong>la</strong> vache vaccinée, dans lespremières 6 h après <strong>la</strong> naissance et pendantles 2 premières sem par le <strong>la</strong>it de <strong>la</strong> vachevaccinéeOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 x 1 dose de fraction lyophilisée et25 x 1 dose de fraction liquideR/Vaccination contre <strong>la</strong> fièvre catarrhaleovine (bluetongue)La fièvre catarrhale ovine (FCO oubluetongue) est une ma<strong>la</strong>die viraledes ovins, des bovins, des caprins etd’autres ruminants, notamment sauvages,transmise par des insectes vecteursappartenant au genre Culicoides(moucherons piqueurs). Il s’agit d’unema<strong>la</strong>die saisonnière. Les symptômeschez les bovins sont souvent moinsgraves que chez les ovins. Chez cesderniers, <strong>la</strong> mortalité est élevée. En2007, plus de 10% des moutons atteintsde <strong>la</strong> ma<strong>la</strong>die seraient morts. En2006, <strong>la</strong> mortalité était de 1 %. Aprèsles campagnes de vaccination obligatoirescontre le virus de <strong>la</strong> fièvrecatarrhale ovine de type 8 en 2009 eten 2010, financées par <strong>la</strong> Commissioneuropéenne, l’Agence Fédérale pour <strong>la</strong>Sécurité de <strong>la</strong> Chaîne Alimentaire et leFonds Sanitaire, aucun cas clinique defièvre catarrhale ovine n’a été constatéen Belgique. La Belgique ainsi queles Pays-Bas, l’Allemagne et le GrandDuché de Luxembourg ont été déc<strong>la</strong>résofficiellement indemnes de <strong>la</strong> FCOdepuis le 15 février 2012. Les bovins,les ovins et les caprins peuvent doncà nouveau être exportés vers d’autrespays indemnes, sans contrainte devaccination ou d’analyse. La fièvre catarrhaleovine est une ma<strong>la</strong>die à déc<strong>la</strong>rationobligatoire.VaccinationLes animaux des espèces sensiblespeuvent être vaccinés avec des vaccinsinactivés autorisés contre lessérotypes 1 et 8 de <strong>la</strong> fièvre catarrhale<strong>du</strong> mouton sur tout le territoire national(AR <strong>du</strong> 2/10/2012 modifiant l’arrêtéroyal <strong>du</strong> 7/05/2008 re<strong>la</strong>tif à <strong>la</strong> lutte et àl’éradication de <strong>la</strong> fièvre catarrhale <strong>du</strong>mouton et AM <strong>du</strong> 28/9/2012 re<strong>la</strong>tif à <strong>la</strong>vaccination contre <strong>la</strong> fièvre catarrhale<strong>du</strong> mouton). Voir aussi www.afsca.be.ProtectionLe vaccin doit être spécifique <strong>du</strong> sérotype.Celui qui a émergé en Belgique etdans une grande partie de l’Europe <strong>du</strong>Nord est le sérotype 8. La vaccinationde 80 % des animaux devrait assurerune immunité suffisante dans <strong>la</strong> popu<strong>la</strong>tionpour obtenir le contrôle desinfections et ré<strong>du</strong>ire considérablementles signes cliniques et <strong>la</strong> mortalité. Lavaccination de base des bovins comprenddeux doses, celle des ovins uneseule dose. Les animaux sont revaccinésavec une seule dose.(Voir aussi Folia Veterinaria 2007 n°3 ,2009 n°3 et Folia Veterinaria 2011 n°1)BTVPUR AlSap 8 (Merial)antigènes <strong>du</strong> BTV sérotype 8:min 7,1 DICC50/doseadjuv: hydroxyde d’aluminium, saponinevaccin injectable scPosologie:Bo, Ov sans imm mat: vac à partir de l’âgede 1 mBo, Ov avec imm mat: vac à partir de l’âgede 2,5 mBo: 2 x 1 dose (1 ml)/animal à 3 - 4 semd’intervalleOv: 1 dose (1 ml)/animalOOI: Bo, Ov: 3 sem après primovacDOI: Ov: min 6 mTemps d’attente: 0 jf<strong>la</strong>con 50 dosesR/ZULVAC 8 Bovis (Pfizer A.H.)virus Bluetongue, sérotype 8 souche BTV-8/BEL2006/02: min 10exp6,7 TCID50/2 mlAdjuv: hydroxide d’aluminium, saponinevaccin injectable imPosologie:Bo (âge > 2,5 m): 2 x 1 dose (2 ml) à 3 semd’intervalleOOI: 25 j après 2e vac, DOI: min 12 m aprèsvac de baseTemps d’attente: 0 jf<strong>la</strong>con 10 doses (20 ml)R/
13 VACCINS POUR LES RUMINANTS 23113.1.2.2 Vaccins bactériens pourruminants (bovins et ovins)Vaccins colibacil<strong>la</strong>iresVaccinLes vaccins contenant une ou plusieursvalences des souches entérotoxinogènesd’Escherichia coli (K99 ou F5,F41, F17, CS31A) sont destinés à protégerles veaux contre les diarrhées <strong>du</strong>nouveau-né (24 à 48 heures) causéespar ces souches ETEC. Les valencesE. coli sont presque toujours combinéesà des valences virales (rotavirus,coronavirus) qui permettent d’étendrele spectre d’agents infectieux couvertpar ces vaccins. La vaccination estfaite chez <strong>la</strong> mère en période de gestationselon les instructions <strong>du</strong> RCP etl’immunité est transférée au veau parle colostrum.ProtectionLa protection conférée par ces vaccinsest excellente, à condition que l’agentétiologique des diarrhées soit bien uncolibacille ETEC, un rotavirus et/ouun coronavirus, et sous réserve d’unebonne administration <strong>du</strong> colostrum.Particu<strong>la</strong>ritésLa protection contre les diarrhées néonatalesdoit prendre en considérationtrois éléments qui sont tous très critiquespour une efficacité maximale:<strong>la</strong> vaccination appropriée des mères,l’ingestion d’une quantité suffisante decolostrum de bonne qualité, suffisammenttôt dans <strong>la</strong> vie <strong>du</strong> veau (un demilitreà <strong>la</strong> naissance et deux litres dansles deux premières heures de <strong>la</strong> vie),et l’hygiène de l’élevage des veauxnouveau-nés. Il n’existe pas de vaccinscontre les souches septicémiquesd’E. coli. Cependant, même sansvaccination de <strong>la</strong> mère, <strong>la</strong> distribution<strong>du</strong> colostrum est indispensable pourprotéger le veau contre les souchessepticémiques d’E. coli. Rappelonsque l’intestin <strong>du</strong> veau n’est totalementperméable aux immunoglobulines quependant les 12 premières heures de <strong>la</strong>vie, et qu’il ne faut que 2 à 3 heures àun colibacille pour envahir le systèmecircu<strong>la</strong>toire. Vaccins contre E. coli combinésavec rotavirus et coronavirusBOVILIS LACTOVAC (Pfizer A.H.)rotavirus bovin inact (1005/78):10exp 7,4 DICT50/doserotavirus bovin inact (Hol<strong>la</strong>nd):10exp 7,0 DICT50/dosecoronavirus bovin inact (800):10exp 5,8 DICT50/doseE. coli inact F5/F41: min 250 UHA/doseadjuv: hydroxyde d’aluminium, saponinevaccin injectable scPosologie:Primovac:Bo: 2 x 1 dose (5 ml) à 4 - 5 sem d’intervalle(1ère à 6 - 8 sem et 2e à 1 - 3 sem avant <strong>la</strong>mise bas)Revac:Bo: 1 dose 2 - 6 sem avant <strong>la</strong> mise basImmunisation passive <strong>du</strong> veau: donner lecolostrum de <strong>la</strong> vache vaccinée dans lespremières 12 h après <strong>la</strong> naissanceOOI-DOI: pas d’infoViande, Lait: 0 jf<strong>la</strong>con 25 ml (5 doses)R/ROTAVEC CORONA (MSD A.H.)par dose de 2 ml:- 1/4 de dose <strong>du</strong> vaccin:rotavirus bovin inact (souche UK-Compton,sérotype G6 P5): min 7,7 log2/ml d’Ac neutralisantle virus (cobaye)- 1/20 de dose <strong>du</strong> vaccin:coronavirus bovin inact (souche Mebus): min3,41 log10/ml d’Ac ELISA (cobaye)adhésine E. coli F5 (K99): min 0,64 d’Ac ELISA(OD492) (cobaye)adjuv: huile minérale, hydroxyde d’aluminiumvaccin injectable imPosologie:Bo (gestant): 1 x 1 dose (2 ml) entre 12 - 3sem avant <strong>la</strong> mise basOOI: dès le début de <strong>la</strong> prise de colostrumDOI: veau artificiellement nourri: jusqu’à <strong>la</strong> finde l’administration de colostrum, veau al<strong>la</strong>ité:rotavirus: 7 j, coronavirus: 14 jTemps d’attente: 0 jf<strong>la</strong>con 10 ml, 40 mlR/
23213 VACCINS POUR LES RUMINANTSSCOURGUARD 3 (Pfizer A.H.)- fraction lyophilisée:rotavirus bovin att (Lincoln, groupe A sérotypeG6): 10exp 7 - 10exp8 DICC50/2 mlcoronavirus bovin att (Hansen):10exp 5 - 10 exp 7,5 DICC50/2 ml- fraction liquide:E. coli F5 (K99): 10exp 10 - 2 x 10exp 10germes/2 mlvaccin lyophilisé et solvant injectable imPosologie:Primovac:Bo: 1 x 1 dose 6 - 8 sem sem avant <strong>la</strong> misebas2e dose 3 sem avant <strong>la</strong> mise basRevac:Bo: 1 dose/an 3 sem avant chaque mise basImmunisation passive <strong>du</strong> veau par lecolostrum de <strong>la</strong> vache vaccinée, dans lespremières 6 h après <strong>la</strong> naissance et pendantles 2 premières sem par le <strong>la</strong>it de <strong>la</strong> vachevaccinéeOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 x 1 dose de fraction lyophilisée et25 x 1 dose de fraction liquideR/Vaccins anti-clostridiensVaccinPlusieurs vaccins sont commercialisésactuellement. Les vaccins contenantune ou plusieurs valences dedifférentes espèces de clostridies(anatoxines et/ou anacultures) sontdestinés à protéger les bovins et lesovins contre les différentes affectionscausées par ces bactéries :tétanos, entérotoxémies, ma<strong>la</strong>die <strong>du</strong>rein pulpeux, abomasite, myositesnécro-hémorragiques (charbon bactérien),hépatites nécrosantes et gangrènegazeuse. Grâce à une mesured’exception, un vaccin a été autorisérécemment (Autorisation Temporaired’Utilisation pendant 1 an) pour <strong>la</strong> protectiondes bovins contre le botulisme.Les vaccins monovalents à base del’anatoxine tétanique ou les vaccinscombinant l’anatoxine tétanique auvirus de <strong>la</strong> grippe sont abordés dans lechapitre Vaccins pour le cheval.ProtectionL’efficacité des vaccins multivalentsest excellente chez les ovins (nouveaunés,jeunes et a<strong>du</strong>ltes), pour autantque l’on respecte bien les instructions<strong>du</strong> fabricant et que les pathologiesobservées soient bien causées par l’undes toxinotypes des espèces de clostridiesincluses dans le vaccin. Sousces conditions, les jeunes agneaux etveaux sont aussi protégés via l’immunitécolostrale après vaccination de<strong>la</strong> mère. L’efficacité de ces vaccinschez les bovins contre l’entérotoxémie(entre autres) est sujette à discussionpar manque de données sur l’étiologieexacte des pathologies simi<strong>la</strong>ires.Etant donné qu’il n’y a pas de protectioncroisée entre les différentstypes de neurotoxines botuliques(BotNT), <strong>la</strong> protection conférée parle vaccin sera limitée aux intoxicationspar BotNT C et D. En F<strong>la</strong>ndre, <strong>la</strong>grande majorité des intoxications est<strong>du</strong>e au type D, mais les types B et Cpeuvent également toucher les bovins.Il convient de tenir compte <strong>du</strong> fait quedes signes cliniques peuvent se manifestermalgré <strong>la</strong> vaccination, surtoutchez les jeunes animaux brusquementexposés à de grandes quantités detoxines. Il faut donc prendre les mesuresnécessaires pour éviter le risquede contamination de l’alimentation parles cadavres, et les pâturages des bovinsne doivent pas être fertilisés avecde l’engrais de poules.RemarqueLe vaccin contre le botulisme actuellementdisponible était initialement autorisédans les régions où le botulismeest endémique. Ceci explique les pluslongs intervalles entre deux revaccinations.En Belgique, on recommandeune revaccination annuelle.
13 VACCINS POUR LES RUMINANTS 233BRAVOXIN 10 (MSD A.H.)par ml:C. perfringens type A (a) anatoxine: min 0,5 UC. perfringens type B & C (b) anatoxine: min18,2 UIC. perfringens type D (e) anatoxine: min 5,3 UIC. chauvoei anaculture: min 90% de protectionC. novyi anatoxine: min 3,8 UIC. septicum anatoxine: min 4,6 UIC. tetani anatoxine: min 4,9 UIC. sordellii anatoxine: min 4,4 UC. haemolyticum anatoxine: min 17,4 Uadjuv: sulfate de potassium et d’aluminiumvaccin injectable scPosologie:Bo (âge > 2 sem): 1 dose = 2 mlOv (âge > 2 sem): 1 dose = 1 mlPrimovac: 2 x 1 dose/animal (à 4 - 6 semd’intervalle)Revac: 1 dose/6 - 12 mOOI: 2 sem après primovac- DOI imm active:Bo: C. tetani, C. perfringens type D: 12 m,C. perfringens type A, B, C: max 12 m, C. novyitype B, C. septicum, C. sordellii, C. haemolyticum,C. chauvoei: max 6 mOv: C. perfringens type A, B, C et D, C. novyitype B, C. sordellii, C. tetani: 12 mC. septicum, C. haemolyticum, C. chauvoei:max 6 m- DOI imm passive:veau: C. sordellii et C. haemolyticum: min 2sem, C. septicum et C. chauvoei: min 8 sem,C. perfringens type A, C. perfringens type B,C. perfringens type C, C. perfringens type D,C. novyi type B et C. tetani: min 12 semagneau: C. septicum et C. chauvoei: min 2 sem,C. perfringens type B et C. perfringens type C:min 8 sem, C. perfringens type A, C. perfringenstype D, C. novyi type B, C. tetani et C. sordellii:min 12 sem (pas d’imm passive contreC. haemolyticum)Viande: 0 jf<strong>la</strong>con 50 mlR/COVEXIN 10 (Pfizer A.H.)anatoxine C. perfringens type A: min 0,5 Uanatoxine C. perfringens type B & C: min 18,2 UIanatoxine C. perfringens type D: min 5,3 UIC. chauvoei culture inactanatoxine C. novyi: min 3,8 UIanatoxine C. septicum: min 4,6 UIanatoxine C. tetani: min 4,9 UIanatoxine C. sordellii: min 4,4 Uanatoxine C. haemolyticum: min 17,4 Uadjuv: alunvaccin injectable scPosologie:Primovac:Ov (âge min 2 sem): 2 x 1 dose (1 ml) à 4 - 6sem d’intervalleBo (âge min 2 sem): 2 x 1 dose (2 ml) à 4 - 6sem d’intervalleRevac:1 dose tous les 6 - 12 mPour protection passive <strong>du</strong> veau, agneau:revacciner mère (primovaccinée avantpériode de gestation) 8 - 2 sem avant <strong>la</strong>mise basOOI: 2 sem après primovacDOI: Ov: C. perfringens de type A, B, C et D,C. novyi de type B, C. sordellii, C. tetani: 12 m,C. septicum, C. haemolyticum, C. chauvoei:max 6 m, Bo: C. tetani, C. perfringens de typeD: 12 m, C. perfringens de type A, B et C: max12 m, C. novyi de type B, C. septicum, C. sordellii,C. haemolyticum, C. chauvoei: max 6 mTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/MILOXAN (Merial)anatoxines Clostridium/2 ml:Cl. perfringens B, C, D:min 10 UI d’anatoxine bêtaCl. perfringens B, C, D:min 5 UI d’anatoxine epsilonCl. septicum:min 2,5 UI d’anatoxine/ml de sérumCl. novyi: min 3,5 UI d’anatoxine/ml de sérumCl. tetani: min 2,5 UI d’anatoxine/ml de sérumCl. sordellii: 90 % de protectionCl. chauvoei: 90 % de protectionadjuv: hydroxyde d’aluminiumvaccin injectable scPosologie:Primovac:Bo: 4 ml/dosejeune Bo, Ov: 2 ml/dose2 x 1 vac avec 4 sem d’intervallejeunes animaux (imm mat): âge > 8 semjeunes animaux (sans imm mat):âge > 2 semRevac:1 dose/anBo et Ov gestants: 2e vac ou revac 1 - 2sem avant <strong>la</strong> mise basOOI: 1 - 2 sem après <strong>la</strong> primovacDOI: pas d’infoimm passive: jusque l’âge de 2 semTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/
23413 VACCINS POUR LES RUMINANTSULTRAVAC BOTULINUM (Pfizer A.H.)Clostridium botulinumtype C toxine: min 5 UI/mltype D toxine: min 1 UI/mlvaccin injectable scPosologie:Primovac: Bo: 2,5 ml, Ov: 1 mlRevac: 1 dose/anOOI: 4 sem après 1e vacDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 250 ml (Bo: 100 doses, Ov: 250 doses)R/iVaccin contre le piétinLe piétin est une ma<strong>la</strong>die infectieuseengendrée par deux germes anaérobiesFusobacterium necrophorum etDichelobacter nodosus. L’infection, quiapparaît surtout lors d’un climat re<strong>la</strong>tivementchaud et humide, entraîne uneérosion de l’hypoderme au niveau del’onglon et de l’espace interdigité. Unséjour prolongé dans <strong>la</strong> bergerie sur unsol humide peut également être à l’originede cette infection.VaccinVaccin inactivé avec Bacteroïdesnodosus.ProtectionAprès <strong>la</strong> primovaccination (deux injections),<strong>la</strong> vaccination sera répétée tousles six mois ou une fois par an en fonction<strong>du</strong> risque d’infection et des conditionsclimatiques. Selon <strong>la</strong> gravité dessignes cliniques, <strong>la</strong> vaccination peutparfois favoriser <strong>la</strong> guérison de l’anima<strong>la</strong>tteint.Particu<strong>la</strong>ritésLa vaccination constitue un desmoyens de lutte préventive. La préventionde cette infection se fait cependanten premier lieu grâce à de bonnesmesures d’hygiène : soins des pieds(onglon, corne), pédiluves au sulfatede zinc ou de cuivre ou désinfectionau formol.FOOTVAX (MSD A.H.)Bacteroïdes nodosus inact (Dichelobacternodosus)sérotypes: A, B1, B2, C, D, E, F, G, H:10 x 10 mcg pili-Ag/dosesérotype I: 5 x 10exp8 cells/minadjuv: paraffine liquide, oleate de mannidevaccin injectable scPosologie:Primovac:Ov (âge > 3 m): 2 x 1 dose (1 ml) à 4 - 6 semd’intervalleRevac:1 dose/4 - 6 mOOI: 2 sem, DOI: 6 mTemps d’attente: 0 jf<strong>la</strong>con 20 mlR/iVaccins contre les ma<strong>la</strong>dies respiratoiresd’origine bactérienne -Mannheimia haemolyticaOutre les pathogènes viraux,Mannheimia haemolytica peut être impliquéedans des troubles respiratoireschez les bovins.VaccinVaccin monovalent contre Mannheimiahaemolytica – Vaccins contreMannheimia haemolytica combinésavec des agents bactériens ou viraux.ProtectionL’efficacité de ces vaccins est liéeavant tout à l’étiologie exacte destroubles respiratoires constatés.Particu<strong>la</strong>ritésS’il est vrai que M. haemolytica intervientfréquemment dans des troublesrespiratoires graves, il est tout aussivrai que d’autres facteurs infectieux,parasitaires et d’environnement participentau développement <strong>du</strong> complexerespiratoire. En d’autres termes,<strong>la</strong> vaccination contre des infectionsrespiratoires ne permet jamais de prédireune protection parfaite contre cestroubles respiratoires ni d’ignorer lesmesures c<strong>la</strong>ssiques de prophy<strong>la</strong>xiehygiénique. Vaccin contre M. haemolyticaPASTOBOV (Merial)Ag de Mannheimia (Pasteurel<strong>la</strong>) haemolytica(type A1): min 68 U ELISA/mlvaccin injectable im, scPosologie:Primovac:Bo (âge > 15 j): 2 x 1 dose (2 ml) à21 - 28 j d’intervalleRevac:1 dose/anOOI: 14 j après 2e vac de <strong>la</strong> primovacDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 10 doses (20 ml)R/
13 VACCINS POUR LES RUMINANTS 235 Vaccin contre M. haemolyticacombiné avec les virus RSB etPI-3BOVILIS BOVIPAST RSP (MSD A.H.)BRSV inact (souche EV 908): min 10exp 5,5 -max 10exp 6,4 DICT50/5 mlvirus PI-3 inact (souche SF-4 Reisinger): min10exp 7,3 - max 10exp 8,3 DICT50/5 mlMannheimia (Pasteurel<strong>la</strong>) haemolytica inact (A1,souche M4/1): 9 x 10exp 9 cellulesadjuv: hydroxyde d’aluminium, Quil A (saponine)vaccin injectable scPosologie:Primovac:Bo (âge > 2 sem): 2 x 1 dose (5 ml) à 4 semd’intervalleRevac:Bo: 1 dose 2 sem avant période à risqueOOI: 2 sem après vac de base, l’imm humoraleest maxDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/Vaccin contre les mammites causéespar E. coli et S. aureusVaccinLe vaccin contient des souchesinactivées d’Escherichia coli etStaphylococcus aureus et ne doit êtreadministré qu’aux animaux sains.ProtectionLe vaccin est destiné à améliorerl’immunité des troupeaux de bovins<strong>la</strong>itiers présentant des problèmesrécurrents de mammites causées parE. coli et S. aureus. Il in<strong>du</strong>it une ré<strong>du</strong>ctionde l’incidence des mammitessubcliniques, ainsi que de l’incidenceet de <strong>la</strong> sévérité des symptômes associésaux mammites cliniques. Le programmecomplet de vaccination serarépété pour chaque gestation.STARTVAC (Hipra Lab)E.coli, souche J5 inact: min 50 DEL60Staphylococcus aureus (PC8), souche inact SP140, complexe antigénique associé à <strong>la</strong> pro<strong>du</strong>ctionde slime (CAAS): min 50 DEL80adjuv: paraffine liquidevaccin injectable imPosologie:Bo: 3 x 1 dose (2 ml): 1e inject 45 j avant<strong>la</strong> date prévue de mise bas, 2e inject 35 japrès, 3e inject 62 j après <strong>la</strong> 2eRevac: répéter à chaque gestationOOI: 13 j après <strong>la</strong> 1e injectDOI: 78 j après 3e inject (=130 j après mise bas)Temps d’attente: 0 jf<strong>la</strong>con 20 x 1 dose, 1 x 5 doses, 1 x 25 dosesR/Vaccination contre <strong>la</strong> fièvre Q(Coxiel<strong>la</strong> burnetii)La coxiellose ou fièvre Q est une ma<strong>la</strong>diebactérienne provoquée par Coxiel<strong>la</strong>burnetii. Les ruminants représententle réservoir principal. L’affection estgénéralement asymptomatique chezles ruminants. Chez les caprins et lesovins, on peut observer des avortementsen fin de gestation, des misesbasprématurées, et des nouveau-néschétifs. Chez les bovins en gestation,une métrite, de l’infertilité et desavortements peuvent être observés.L’homme peut également être infecté.Parmi les personnes infectées, uneminorité développera un syndromepseudo-grippal. La ma<strong>la</strong>die est surtoutdangereuse chez les patients à risque(femmes enceintes, patients cardiaques)qui risquent de développer<strong>la</strong> forme chronique de <strong>la</strong> ma<strong>la</strong>die. Voiraussi le Folia Veterinaria 2011, n° 1.VaccinVaccin inactivé contenant l’antigènephase I pour bovins et caprins.BovinsImmunisation active des bovins visantà ré<strong>du</strong>ire le risque chez les animauxvaccinés non-infectés et non-gestantsde devenir excréteurs et à diminuerl’excrétion de Coxiel<strong>la</strong> burnetii chezces animaux par le <strong>la</strong>it et le mucusvaginal.OOI : non établie, DOI : 280 jours aprèsachèvement de <strong>la</strong> primo-vaccination.CaprinsImmunisation active des caprins visantà ré<strong>du</strong>ire les avortements causés parCoxiel<strong>la</strong> burnetii et l’excrétion de cetagent causal de l’organisme par le<strong>la</strong>it, le mucus vaginal, les fèces et lep<strong>la</strong>centa.OOI : non établie, DOI : non établie.Une protection a été démontrée parépreuve virulente 8 semaines aprèsprimo-vaccination.Particu<strong>la</strong>ritésSuite à l’importante épidémie defièvre Q aux Pays-Bas, l’EMA a décidéd’octroyer une autorisation temporairesous conditions au vaccin ci-dessous.L’utilisation de ce vaccin en Belgiquese fait dans le cadre <strong>du</strong> programme desurveil<strong>la</strong>nce de l’AFSCA concernant <strong>la</strong>fièvre Q dans les exploitations <strong>la</strong>itièresovines et caprines. Voir aussi www.afsca.be.
23613 VACCINS POUR LES RUMINANTSCOXEVAC (Ceva Santé Animale)Coxiel<strong>la</strong> burnetii (Nine Mile stam), inact:72 QF Unit/mlvaccin injectable scPosologie:Bo (âge > 3 m): 2 x 1 dose (4 ml) avec 3 semd’intervalleBo revac: 1 dose/9 mCapr (âge > 3 m): 2 x 1 dose (2 ml) avec 3sem d’intervalleCapr revac: pas d’info<strong>la</strong> primovac doit être finalisée 3 sem avantl’accouplement ou l’insémination artificielleOOI: Bo: pas d’info, Capr: pas d’info primovacDOI: Bo: 208 j après primovac, Capr: pas d’infoViande, Lait: 0 jf<strong>la</strong>con 40 mlR/13.1.2.3 Vaccins antiparasitairespour ruminantsPar rapport aux vaccins antiviraux etantimicrobiens, le nombre des vaccinsantiparasitaires est limité surle marché vétérinaire en Belgiqueaussi bien que dans les autres Etatsmembres de l’Union européenne, etce pour plusieurs raisons : 1) les organismescibles sont des eucaryotescaractérisés par un cycle parasitairecomplexe associé à des modificationsantigéniques marquées et à desmécanismes d’échappement efficacesvis-à-vis de <strong>la</strong> réponse immunitairedéveloppée par leur hôte ; 2) un grandnombre de médicaments hautementactifs et peu toxiques existent sur lemarché vétérinaire pour le contrôledes affections <strong>du</strong>es aux protozoaires,aux helminthes, aux arthropodes etaux champignons, ce qui fait quel’approche vaccinale a été quelquepeu négligée ; 3) de nombreux parasites,en particulier les helminthes, lesarthropodes et certains champignonspathogènes, parasitent le revêtementcutané et les muqueuses de leur hôtece qui peut présenter un obstacle audéveloppement de vaccins efficaceset sûrs d’emploi ; 4) <strong>la</strong> pro<strong>du</strong>ction defractions antigéniques bien définies àun prix compétitif est limitée par <strong>la</strong> difficultéqu’il y a à maintenir in vitro ungrand nombre d’espèces parasitaires.Vaccin contre <strong>la</strong> bronchite vermineuse(Dictyocaulus viviparus)Le cycle biologique de D. viviparus estdirect et comprend une phase exogènesur <strong>la</strong> pâture et une phase endogèneparasitaire qui con<strong>du</strong>it le ver depuisl’intestin (stade L3) jusqu’à <strong>la</strong> trachéeet les grosses bronches (stade a<strong>du</strong>lte).La réponse immunitaire protectriceest essentiellement dirigée contre <strong>la</strong>L4 au niveau de l’alvéole pulmonaire.C<strong>la</strong>ssiquement, <strong>la</strong> ma<strong>la</strong>die apparaîtchez les animaux dépourvus d’immunitéet soumis à une forte infestationsur peu de temps. Ce sont donc lesveaux en première ou en deuxièmesaison de pâture qui sont concernésau premier chef. Néanmoins, au coursdes dernières années, l’épidémiologiede l’affection a évolué et il n’est pasrare d’observer des atteintes graves,voire mortelles, chez le bétail a<strong>du</strong>lte.Ceci est généralement dû à un excèsde protection contre le parasite, obtenugrâce à <strong>la</strong> chimioprophy<strong>la</strong>xie au coursdes deux premières années de vie del’animal, ou à l’intro<strong>du</strong>ction dans uneferme infestée d’animaux élevés ailleurs,hors sol, ou provenant de régionsd’Europe où <strong>la</strong> ma<strong>la</strong>die est absente.VaccinCe vaccin a comme seule indication<strong>la</strong> prophy<strong>la</strong>xie des infestationspar Dictyocaulus viviparus chez lesbovins et <strong>la</strong> bronchite vermineuse quien découle. Le vaccin contre <strong>la</strong> bronchitevermineuse est atténué par irradiationde <strong>la</strong>rves de troisième stade(L3). Ceci permet d’exposer l’animal àl’entièreté <strong>du</strong> cycle parasitaire depuisl’intestin jusqu’au tractus respiratoire.Les <strong>la</strong>rves sont conditionnées dans del’eau distillée stérile. Une dose (25 ml)contient 1000 <strong>la</strong>rves de D. viviparus.Il est important de noter que chez lesanimaux vaccinés, les <strong>la</strong>rves atténuéespeuvent néanmoins effectuer le cycleendogène complet et par conséquentêtre à l’origine de l’excrétion de <strong>la</strong>rvesL1 via les matières fécales. Cettesource d’infestation est d’ailleurs nécessairechez les animaux vaccinéspour assurer le développement d’uneimmunité solide car elle sera à l’originede petites infestations ultérieures lors<strong>du</strong> pâturage.ProtectionLe vaccin s’administre en principe auxveaux avant leur première saison depâture. Du fait de l’excrétion de <strong>la</strong>rvesL1 par les veaux vaccinés, tous lesanimaux <strong>du</strong> groupe concernés doiventêtre vaccinés avant <strong>la</strong> mise à l’herbe.C<strong>la</strong>ssiquement, les veaux reçoiventpar voie orale deux doses de 1000<strong>la</strong>rves, 6 et 2 semaines avant <strong>la</strong> sortie.Il est impératif <strong>du</strong>rant cette périodede maintenir les animaux à l’intérieur.De même, une fois <strong>la</strong> vaccinationaccomplie, les veaux doivent aller au
13 VACCINS POUR LES RUMINANTS 237pâturage, à défaut de quoi l’immunitéatteinte va décroître pour disparaîtreaprès 100 jours environ.Particu<strong>la</strong>ritésLes conditions de conservation <strong>du</strong>vaccin doivent être particulièrementrespectées. Les échecs observés suiteà l’emploi <strong>du</strong> vaccin contre <strong>la</strong> bronchitevermineuse sont presque toujours liésau non respect de ces précautions ouà l’exposition de veaux vaccinés à unepâture massivement infestée. Le vaccinatténué doit être conservé de + 2à + 4 °C et <strong>la</strong> <strong>du</strong>rée de conservationse limite à 90 jours après <strong>la</strong> pro<strong>du</strong>ction.Comme les <strong>la</strong>rves atténuées quiconstituent le vaccin doivent effectuerle cycle endogène au moins jusqu’auxpoumons, il faut éviter de tuer les <strong>la</strong>rvesen migration par l’usage d’anthelminthiquesà activité systémique. En cequi concerne les anthelminthiques peuou moyennement rémanents commeles imidazothiazolés (lévamisole) ou lesbenzimidazolés (par exemple le fenbendazole,l’oxfendazole et l’albendazole),il faut éviter toute vermifugation aumoins <strong>du</strong> 7e jour avant <strong>la</strong> première au10e jour après <strong>la</strong> deuxième dose vaccinale.Dans le cas des endectocidesrémanents tels que les avermectines(ivermectine, doramectine, éprinomectine)et milbémycines (moxidectine) eten fonction de <strong>la</strong> préparation choisie,il faudra éviter toute administrationdepuis 3 à 6 semaines avant applicationde <strong>la</strong> première dose et jusqu’à unminimum de 10 jours après applicationde <strong>la</strong> deuxième dose vaccinale.BOVILIS LUNGWORM (MSD A.H.)<strong>la</strong>rves de Dictyocaulus viviparus viv:min 1000/dosevaccin poPosologie:veau (âge > 2 sem): 2 x 1 dose à 4 semd’intervalleOOI: 2 semDOI: l’immunité se maintient d’une saison àl’autre grâce à l’exposition aux stades <strong>la</strong>rvairesTemps d’attente: 0 jf<strong>la</strong>con 1 dose (25 ml)R/Tableau récapitu<strong>la</strong>tif des vaccins pour bovinsRSBIBRBVD – MDrotavirus et coronavirusPI - 3virus de <strong>la</strong> fièvre catarrhale ovineE. coliClostridium spp.Clostridium tetaniCoxiel<strong>la</strong> burnetiiM. haemolyticaDictyocaulus viviparusS.aureusrageBOVILIS BOVIPAST RSPMSD A.H.BOVILIS BVDMSD A.H.BOVILIS IBR MARKER INACMSD A.H.BOVILIS IBR MARKER LIVEMSD A.H.BOVILIS LACTOVACMSD A.H.BOVILIS LUNGWORMMSD A.H.BRAVOXIN 10Schering-PloughBTVPUR AlSap 8MerialX X XXXXX XX XXX
23813 VACCINS POUR LES RUMINANTSRSBIBRBVD – MDrotavirus et coronavirusPI - 3virus de <strong>la</strong> fièvre catarrhale ovineE. coliClostridium spp.Clostridium tetaniCoxiel<strong>la</strong> burnetiiM. haemolyticaDictyocaulus viviparusS.aureusrageCOVEXIN 10Schering-PloughXXCOXEVACCeva S.A.XHIPRABOVIS IBR MARKERLIVEHipra LabXIBRAXIONMerialXMILOXANMerialXXNOBIVAC RABIESMSD A.H.XPASTOBOVMerialXRABDOMUNPfizer A.H.XRABISINMerialXRISPOVAL 3 BRSV-PI3-BVDPfizer A.H.X X XRISPOVAL IBR-MARKERINACTIVATUMPfizer A.H.XRISPOVAL IBR-MARKERVIVUMPfizer A.H.XRISPOVAL RS + PI3IntranasalPfizer A.H.XXROTAVEC CORONASchering-PloughXXSCOURGUARD 3Pfizer A.H.XXSTARTVACHipra LabXXULTRAVAC BOTULINUMPfizer A.H.XZULVAC 8 BovisPfizer A.H.X
13 VACCINS POUR LE PORC 239Tableau récapitu<strong>la</strong>tif des vaccins pour ovins et/ou chèvresvirus de <strong>la</strong> fièvre catarrhaleovineDichelobacter (Bacteroïdes)nodosusClostridia spp.virus de <strong>la</strong> rageCoxiel<strong>la</strong> burnetiiClostridium tetaniBRAVOXIN 10Schering-PloughBTVPUR Alsap 8MerialCOVEXIN 10Schering-PloughCOXEVACCeva S.A.FOOTVAXSchering-PloughMILOXANMerialNOBIVAC RABIESMSD A.H.RABISINMerialXXXXXXXXXXX13.1.3 Vaccins pour le porc13.1.3.1 Vaccination contre lesma<strong>la</strong>dies virales <strong>du</strong> porcLes vaccins contre les infections viraleschez le porc sont en premier lieu destinésà in<strong>du</strong>ire une protection de l’animallui-même contre des signes cliniques ;mais parfois ils sont également destinésà fournir une protection virologiquecomplète ou partielle afin d’éviter ouré<strong>du</strong>ire <strong>la</strong> pro<strong>du</strong>ction d’un virus sauvage.Dans ce cas, les recommandationsd’usage sont souvent formuléesde <strong>la</strong> manière suivante : “obtenir uneré<strong>du</strong>ction significative de <strong>la</strong> multiplicationd’un virus sauvage”. Lors d’unevaccination de <strong>la</strong> popu<strong>la</strong>tion ou lorsd’un programme de vaccination obligatoire,cette vaccination peut être lepremier pas non négligeable vers l’élimination<strong>du</strong> virus sauvage. Les vaccinspeuvent également servir à vacciner lestruies ou cochettes et donc in<strong>du</strong>ire uneprotection contre <strong>la</strong> transmission transp<strong>la</strong>centaire<strong>du</strong> virus sauvage ou encoreprotéger les nouveau-nés par immunitématernelle. Dans certains cas, lesvaccins peuvent également être utiliséspour immuniser une popu<strong>la</strong>tion à uncertain âge dans l’intention de réprimerl’infection par le virus sauvage lors depériodes cruciales où le risque d’infectiondevient plus grand (par exempleaffection multifactorielle, lors <strong>du</strong> rassemblementaprès le sevrage ou dans<strong>la</strong> porcherie). La plupart des vaccinsviraux chez le porc sont destinés àplusieurs groupes d’âge (par exemple,virus <strong>du</strong> SDRP, grippe porcine). A l’inverse,parfois, seul un âge ou un étatphysiologique est indiqué, soit pour desraisons d’innocuité, soit parce qu’unseul groupe cible doit être protégé(par exemple parvovirose). Des programmesde vaccination généralisésmis à jour annuellement et courammentappliqués au niveau de l’exploitation ne
24013 VACCINS POUR LE PORCsont cependant pas disponibles pour leporc.ParvoviroseLe parvovirus porcin est responsable,après infection chez <strong>la</strong> truie gestanteséronégative, d’une transmission transp<strong>la</strong>centairevers les fœtus et de mortalitéfœtale; <strong>la</strong> truie elle-même n’est pasma<strong>la</strong>de. Une infection qui débute chezun ou plusieurs fœtus se dissémine demanière intra-utérine et touche ainsi <strong>la</strong>majeure partie de <strong>la</strong> portée. A côté defœtus momifiés (de différentes tailles),des porcelets vivants peuvent égalementnaître, vu que <strong>la</strong> gestation n’estpas interrompue. L’avortement n’adonc pas lieu.VaccinLes vaccins contre le parvovirus sontsouvent combinés à d’autres vaccins,par exemple en vue de combattre lerouget <strong>du</strong> porc (Erysipelothrix rhusiopathiae).Tous deux sont utilisés pour luttercontre les troubles de repro<strong>du</strong>ction,mais on administre également le vaccincontre le rouget <strong>du</strong> porc afin d’in<strong>du</strong>irepar le colostrum une immunité maternellechez le porcelet. Tous les vaccinscontre <strong>la</strong> parvovirose porcine sont inactivéset destinés à vacciner <strong>la</strong> mère etentraver <strong>la</strong> transmission transp<strong>la</strong>centairelors d’un contact ultérieur avec levirus sauvage.ProtectionLes vaccins sont administrés dès <strong>la</strong>puberté de façon à garantir une protectionlors de <strong>la</strong> gestation. On notera quede très bas titres en anticorps dans lesang peuvent prévenir <strong>la</strong> transmissiontransp<strong>la</strong>centaire <strong>du</strong> virus de <strong>la</strong> truie versle fœtus. Il est recommandé de revaccinerles animaux étant donné que l’on neconnaît pas <strong>la</strong> <strong>du</strong>rée exacte de l’immunitéaprès <strong>la</strong> vaccination. Vaccin monovalent contre <strong>la</strong>parvovirosePORCILIS PARVO (MSD A.H.)parvovirus porcin inact (souche PPV 014):min 9 log2 HI/dose (2 ml)adjuv: dl-alpha-tocophéro<strong>la</strong>cétatevaccin injectable imPosologie:Primovac:cochette: 1 dose (2 ml) entre 8 - 2 semavant <strong>la</strong> saillietruie: 1 dose 2 sem min avant <strong>la</strong> saillieRevac: annuellementOOI-DOI: 1 seule vac au moins 2 sem avant <strong>la</strong>saillie protège contre une infection transp<strong>la</strong>centairepar le PPVTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/ Vaccins bivalents contre <strong>la</strong>parvovirosePARVORUVAX (Merial)parvovirus porcin inact: 2 U.HAI/2 mlErysipelothrix rhusiopathiae inact (sérotype 2):min 1 U Elisa/2 m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:Primovac:Su (sans imm mat): 2 x 1 dose (2 ml) à 3 - 4sem d’intervalle (2e vac min 2 sem avant1e saillie)Revac:1 dose/6 m (périodes d’al<strong>la</strong>itement)rouget:OOI: 3 sem après 2e inject de <strong>la</strong> primovacDOI: pas d’infoparvo:OOI: primovac complète min 14 j avantrepro<strong>du</strong>ction, protège contre une infectiontransp<strong>la</strong>centaireDOI: 9 mTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/PARVOSUIN-MR (Hipra Lab)parvovirus porcin inact (NADL-2): min 2048HAE/2 mlErysipelothrix rhusiopathiae (R32E11) inact:min 50 UI/2 m<strong>la</strong>djuv: huilevaccin injectable imPosologie:Primovac:cochette, verrat (âge > 6 m):2 x 1 dose (2 ml) à 3 - 4 sem d’intervalle(min 1 sem avant <strong>la</strong> saillie)Revac:truie: 1 dose 10 - 15 j après <strong>la</strong> mise basverrat: 1 dose/anParvo:primovac min 1 sem avant <strong>la</strong> repro<strong>du</strong>ction protègecontre une infection transp<strong>la</strong>centaireRouget:OOI: pas d’info, DOI: 3 mViande: 0 jf<strong>la</strong>con 10 x 25 doses10 x 50 dosesR/PORCILIS ERY-PARVO (MSD A.H.)Erysipelothrix rhusiopathiae inact (M2 sérotype2): min 50 UI/dose (2 ml)parvovirus porcin inact (PPV 014): min 9 log2HI/dose (2 ml)adjuv: alpha-tocophérol acétatevaccin injectable imPosologie:Primovac:cochette (âge > 20 sem):Parvovirose: 1 dose (2 ml) 2 sem avant <strong>la</strong>saillieRouget <strong>du</strong> porc: 2 x 1 dose à 4 semd’intervalleRevac:truie: 1 dose pendant chaque période de<strong>la</strong>ctation, au moins 2 sem avant saillieParvo:1 vac min 2 sem avant <strong>la</strong> repro<strong>du</strong>ction protègecontre une infection transp<strong>la</strong>centaire par le PPVRouget:OOI: 3 sem, DOI: 6 mViande: 0 jf<strong>la</strong>con 25 dosesR/
13 VACCINS POUR LE PORC 241SUVAXYN PARVO/E (Pfizer A.H.)chaque dose (2 ml) contient:parvovirus porcin (souche S-80), inact: min titreIHA 160 chez le <strong>la</strong>pinErysipelothrix rhusiopathiae (souche B-7, sérotype2), inact: potency selon Ph EurAdjuv: marcol 52 (huile minérale), montanide888 (émulsifiant), simulsol 5100 (émulsifiant)vaccin injectable imPosologie:Primovac:cochette (âge > 5 m) et truie: 2 x 1 dose à3 - 4 sem d’intervalle, 2e dose min 4 semavant <strong>la</strong> saillieRevac:1 dose pendant <strong>la</strong> <strong>la</strong>ctation, 3 - 4 sem avant<strong>la</strong> saillieTemps d’attente: 0 jf<strong>la</strong>con 2 x 25 dosesR/Grippe porcine (Influenza)La grippe chez le porc est causée pardeux types de virus n’in<strong>du</strong>isant pasd’immunité croisée, à savoir H1N1et H3N2. Ces deux types viraux sontcontenus dans les vaccins depuisenviron 15 à 20 ans. En général, lesvaccins sont composés d’un sérotypeH1N1 (New Jersey ou souche locale)et d’un ou deux sérotypes H3N2 (PortChalmers-humain et/ou une soucheisolée chez le porc). Un troisièmesous-type de virus, H1N2, a récemmentété signalé dans <strong>la</strong> popu<strong>la</strong>tionporcine belge. Un vaccin trivalent,contenant les trois valences H1N1,H3N2 et H1N2, permet de pallier cettenouvelle situation.VaccinTous les vaccins sont inactivés etcontiennent un adjuvant.ProtectionIls sont administrés aux truies afin deles protéger elles-mêmes et en vue desusciter une immunité maternelle chezleur progéniture. Ils sont égalementrecommandés pour les porcelets audébut de <strong>la</strong> période d’engraissementafin de ré<strong>du</strong>ire les pertes <strong>du</strong>es auxtroubles respiratoires.GRIPOVAC 3 (Merial)souches <strong>du</strong> virus inact de <strong>la</strong> grippe porcine A:Bakum/IDT1769/2003 (H3N2):min 10.53 log2 MGUN/2 mlHaselünne/IDT2617/2003 (H1N1):min 10.22 log2 MGUN/2 mlBakum/1832/2000 (H1N2):min 12.34 log2MGUN/2 m<strong>la</strong>djuv:carbomère 971 P NFvaccin injectable imPosologie:porcelet (âge en fonction de <strong>la</strong> DOI),cochette, truie: 2 x 1 dose (2 ml) à 3 semd’intervalleun rappel est possible à tout stade de <strong>la</strong>gestation ou de <strong>la</strong> <strong>la</strong>ctationOOI: 7 j après vac de baseDOI:4 m si vac entre l’âge de 56 et 96 j, 6 m si 1evac à partir de l’âge de 96 jimm mat <strong>du</strong> porcelet si truie vaccinée 14 j avantmise bas: 33 j après mise basTemps d’attente: 0 jf<strong>la</strong>con 100 ml (50 doses)R/Syndrome dysgénésique et respiratoireporcin (SDRP)Ce syndrome est provoqué par unvirus découvert assez récemment, responsablede troubles respiratoires etde <strong>la</strong> repro<strong>du</strong>ction. Cette affection aété décrite aux Etats-Unis dans <strong>la</strong> deuxièmemoitié des années quatre-vingtet est apparue en Europe dès 1990.Le virus, appelé SDRP, a été isolé enpemier lieu en Europe puis s’est rapidementéten<strong>du</strong> à toute l’Europe continentalepuis à l’échelle mondiale. On lerencontre maintenant fréquemment ausein <strong>du</strong> cheptel porcin.VaccinDes vaccins, aussi bien vivantsqu’inactivés, ont été mis au point pourune utilisation chez les truies et lesporcelets.ProtectionLes vaccins inactivés sont exclusivementdestinés à <strong>la</strong> vaccination destruies. La vaccination des porceletscharcutiers est destinée à prévenir lestroubles respiratoires, <strong>la</strong> vaccinationdes truies à prévenir les troubles de <strong>la</strong>repro<strong>du</strong>ction. Il existe des variants antigéniques<strong>du</strong> virus. La souche SDRPaméricaine présente ainsi des différencesgénétiques et antigéniques parrapport à <strong>la</strong> souche européenne. Lessouches in<strong>du</strong>isent une immunité pluscomplète face à <strong>la</strong> souche homologueque face à <strong>la</strong> souche hétérologue ; lessituations hétérologues engendrentcependant aussi une immunité croisée.
24213 VACCINS POUR LE PORCParticu<strong>la</strong>ritésCertains vaccins vivants se multiplientlongtemps dans les poumons desporcelets vaccinés, ce qui explique <strong>la</strong>discussion ayant cours à propos deleur innocuité. De même, certainessouches de vaccins vivants pourraientengendrer une infection transp<strong>la</strong>centaire.Aussi, on comprend le danger devacciner des truies gestantes n’ayantjamais été en contact auparavant avecle virus SDRP. Il n’est pas rare cependantqu’on utilise des vaccins vivantspour susciter une infection avec unvirus atténué, afin d’in<strong>du</strong>ire une immunitécollective en bas-âge (porceletsâgés de 3 - 4 semaines) et/ou d’homogénéiserle statut immunitaire destruies non gestantes. Vaccins monovalents contre leSDRPVaccins vivantsINGELVAC PRRS Modified Live Virus (BoehringerIngelheim)virus SDRP att: min 10exp 4,9 CCID50/2 mlvaccin lyophilisé et solvant injectable imPosologie:porcelet (âge > 3 sem): 1 x 1 dose de 2 mltruie, cochette: 1 dose (2 ml) 3 - 4 semavant <strong>la</strong> prochaine saillieRevac: après <strong>la</strong> mise bas, 3 - 4 sem avant<strong>la</strong> prochaine saillieOOI: porcelet: 7 j (souche hétérologue: 43 japrès vac), truie et cochette: 40 j après vacDOI: porcelet: min 110 j, truie et cochette: min154 jTemps d’attente: 0 jf<strong>la</strong>con 1 x 10 doses + 1 x 20 ml de solvant1 x 50 doses + 1 x 100 ml de solvantR/iPORCILIS PRRS (MSD A.H.)virus SDRP att (DV): min 10exp 4 DICT50/dose(2 ml)adjuv solvant: alpha-tocophérol acétatevaccin lyophilisé et solvant pour suspensioninjectable im, idermPosologie:Su (âge > 2 sem): 1 dose/animal (im: 2 ml,iderm: 0,2 ml)Revac:cochette: 2 - 4 sem avant <strong>la</strong> saillietruie: avant chaque gestation ou tous les4 m - truies gestantes: uniquement aprèscontact avec virus SDRP européenOOI: 28 j après vacDOI: min 24 semTemps d’attente: 0 jf<strong>la</strong>con 10, 50, 100 doses de vaccin et 20, 100,200 ml de solvantR/iVaccins inactivésINGELVAC PRRS KV (Boehringer Ingelheim)virus SDRP inact, souche P120:min 2,5 log 10 U IF/2 m<strong>la</strong>djuv: excipient huileux o/wvaccin injectable imPosologie:Su:Primovac:cochette, truie: 2 x 1 dose (2 ml) à 3 - 4sem d’intervalle (cochette: 3 sem min avant<strong>la</strong> saillie)Revac:1 dose à 60 - 70 j de chaque gestationOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/iPROGRESSIS (Merial)virus SDRP inact, souche P120:min 2,5 log10 U IFadjuv: excipient huileuxvaccin injectable imPosologie:Primovac:cochette, truie: 2 x 1 dose (2 ml) à 3 - 4sem d’intervalle (cochette: 3 sem min avantsaillie)Revac: 1 x 1 dose à 60 à 70 j de chaquegestationOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/iCircovirus porcinL’infection de jeunes porcelets par lecircovirus porcin 2 (PCV 2) est associéeà l’apparition d’un syndromeappelé « Syndrome de DépérissementPostSevrage » (SDPS) ou encorePorcine Multisystemic WastingSyndrome (PMWS), une ma<strong>la</strong>diegagnant de l’importance en Europe,en Asie et en Amérique <strong>du</strong> Nord. LePMWS pourrait aussi impliquer, outrele PCV2, d’autres facteurs tels qued’autres agents infectieux, des facteursgénétiques ou encore des facteursliés à <strong>la</strong> gestion de l’exploitation.Après l’infection initiale par le PCV 2,et <strong>la</strong> virémie, le virus diffuse vers différentsorganes où apparaissent deslésions. Le PMWS touche surtout lesanimaux à l’âge <strong>du</strong> sevrage et sonévolution est lente et progressive. Lessymptômes sont peu typiques : pertede poids, <strong>du</strong>reté <strong>du</strong> poil, faiblesse,ictère, lymphadénopathie, diarrhée etessoufflement. Des infections granulomateusespeuvent apparaître dansdivers organes (poumons, foie, reins,ganglions lymphatiques, rate, thymuset p<strong>la</strong>ques de Peyer). Si <strong>la</strong> ma<strong>la</strong>diese déc<strong>la</strong>re, <strong>la</strong> mortalité peut atteindre10% et plus. Les foetus peuvent être
13 VACCINS POUR LE PORC 243infectés par voie transp<strong>la</strong>centaire viale sang de <strong>la</strong> mère non immunisée, cequi peut entraîner une momification oudes porcelets morts-nés ou faibles à <strong>la</strong>naissance. Il semble que le virus joueaussi un rôle important dans le complexerespiratoire <strong>du</strong> porc, et peut-êtreégalement dans le syndrome dermatite-néphropathieporcin (PDNS).VaccinLes vaccins contiennent un circovirusporcin inactivé de type 2 (PCV 2) oudes sous-unités. Les vaccins visentà stimuler l’immunité active chez lescochettes et les truies afin d’obtenirune immunité passive chez les porceletsvia l’ingestion <strong>du</strong> colostrum, ouà stimuler l’immunité active chez lesporcelets.ProtectionImmunisation passive des porceletsvia le colostrum, après immunisationactive des truies et des cochettes, afinde ré<strong>du</strong>ire les lésions dans les tissuslymphoïdes associées à l’infectionpar le PCV 2 et ainsi contribuer à <strong>la</strong>ré<strong>du</strong>ction de <strong>la</strong> mortalité liée au PCV 2.La <strong>du</strong>rée de cette immunité s’étendjusqu’à 5 semaines après l’ingestion<strong>du</strong> colostrum. Dans une étude de terrain,une ré<strong>du</strong>ction de <strong>la</strong> mortalité de3,6 à 10 % chez les porcelets ayantreçu <strong>du</strong> colostrum de mères vaccinées,a été constatée. Après vaccination, lesporcelets sont protégés pendant 17 ou22 semaines selon le vaccin.CIRCOVAC (Merial)circovirus porcin de type 2 (CVP2) inact:min 1.8 log10 U ELISA/2 mlémulsion et suspension pour vaccin injectableimPosologie:Primovac:cochette: 2 x 1 dose (2 ml) à 3 - 4 semd’intervalle (2e vac min 2 sem avant <strong>la</strong>saillie), suivi d’1 dose min 2 sem avant <strong>la</strong>mise bastruie: 2 x 1 dose (2 ml) à 3 - 4 sem d’intervalle(2e vac min 2 sem avant <strong>la</strong> mise bas)Revac: 1 dose à chaque gestation (min 2 - 4sem avant <strong>la</strong> mise bas)porcelet (âge> 3 sem): 1 dose (0,5 ml)imm passive porcelet DOI: 5 sem après l’ingestion<strong>du</strong> colostrumimm active porcelet OOI: 2 sem, DOI: 14 semaprès vacTemps d’attente: 0 jf<strong>la</strong>con 5 ou 25 dosesR/INGELVAC CIRCOFLEX (Boehringer Ingelheim)circovirus porcin inact type 2 (protéine ORF2):min 1,0 - max 3,75 RPadjuv: carbomèrevaccin injectable imPosologie:Su (âge > 2 sem): 1 x 1 dose (1 ml) paranimalOOI: 2 sem après <strong>la</strong> vacDOI: min 17 semTemps d’attente: 0 jf<strong>la</strong>con 50 ml (50 doses), 100 ml (100 doses),250 ml (250 doses)R/PORCILIS PCV (MSD A.H.)antigène sous-unitaire type 2 ORF2 <strong>du</strong> circovirusporcin: min 4.5 log2 U ELISAadjuv: acétate de dl-alpha-tocophérol, paraffineliquidevaccin injectable imPosologie:Su:- taux d’Ac mat moyen/faible:1 x 1 dose (2 ml) dès l’âge de 3 sem- taux d’Ac mat élevé ou en cas de doute:2 x 1 dose, 1e vac dès l’âge de 3 - 5 j,2e vac 2 - 3 sem plus tardOOI: 2 sem, DOI: 22 semTemps d’attente: 0 jf<strong>la</strong>con 100 mllR/SUVAXYN PCV (Pfizer A.H.)circovirus porcin de type 1 recombinant inactexprimant <strong>la</strong> protéine encodée par ORF2 <strong>du</strong> circovirusporcin de type 2: AR min 1,6 et max 5,3vaccin injectable imPosologie:Su (dès l’âge de 21 j): 1 dose (2 ml)OOI: dès 3 sem après vacDOI: 19 sem après vacTemps d’attente: 0 jf<strong>la</strong>con 50 doses (100 ml), 125 doses (250 ml)R/13.1.3.2 Vaccination contre lesma<strong>la</strong>dies bactérienneschez le porcPleuropneumonie contagieuse(infections par Actinobacilluspleuropneumoniae)La pleuropneumonie contagieuse estcaractérisée par une pneumonie hémorragiqueet nécrotique aiguë et unepleurésie, ou encore par une affectionpulmonaire chronique avec des foyersnécrotiques localisés et une pleurésiefibrineuse. La bactérie Actinobacilluspleuropneumonia est à l’origine del’affection. On connaît deux biotypeset 15 sérotypes de ce germe.La pathogénie de <strong>la</strong> pleuropneumonieest fort complexe. Plusieurs facteursde virulence ont été décrits dont lestoxines Apx, <strong>la</strong> capside, des protéinases,des lipopolysaccharides, del’uréase, des adhésines et des protéinesde <strong>la</strong> membrane extérieure
24413 VACCINS POUR LE PORCtelles que des protéines de fixationde <strong>la</strong> transferrine et de l’hémoglobine.A. pleuropneumoniae est inhalé etpeut coloniser les muqueuses nasaleset les amygdales. Aucun signe cliniquen’apparaît tant que l’infection se ré<strong>du</strong>itaux voies respiratoires supérieures; lesanimaux peuvent, dans ce cas, resterlongtemps porteurs <strong>du</strong> germe. Dessignes cliniques peuvent apparaîtrelorsque ce dernier atteint les bronchioleset les alvéoles. Cette situationest favorisée par une pression d’infectionélevée, un environnement néfaste,une infection virale et une infectionpar <strong>la</strong> bactérie Mycop<strong>la</strong>sma hyopneumoniae.A. pleuropneumoniae se fixesur l’épithélium des bronchioles et desalvéoles terminales. Les lésions sontprincipalement causées par <strong>la</strong> pro<strong>du</strong>ctionde ce qu’on appelle les toxinesApx. Il s’agit d’exotoxines qui peuventformer des pores dans <strong>la</strong> membranedes cellules de l’animal infecté. Ondécrit quatre toxines Apx. L’Apx IV estdécelée chez tous les sérotypes maisson rôle dans <strong>la</strong> pathogénie n’est pasc<strong>la</strong>ir. Cette toxine est exprimée exclusivementin vivo. Les autres toxinesApx (I, II, III) sont aussi exprimées invitro. Il n’existe pas de neutralisationcroisée entre ces toxines Apx. Chaquesérotype pro<strong>du</strong>it une ou deux de cestoxines. Elles peuvent entre autresdétruire les phagocytes, les cellules del’endothélium et les cellules alvéo<strong>la</strong>iresde l’épithélium ; et jouent un rôle importantdans l’apparition des lésions.Apx I et II ont également une activitéhémolytique.VaccinLe vaccin inactivé à base de toxinesApx est en mesure d’in<strong>du</strong>ire uneprotection clinique partielle par rapportaux différents sérotypes deA. pleuropneumoniae.ProtectionLes animaux doivent être vaccinésà deux reprises avec un intervalle dequatre semaines. Le vaccin ne peutêtre administré avant l’âge de six semainesen raison d’une interférencepossible avec l’immunité maternelle.Particu<strong>la</strong>ritésLa vaccination des porcelets peut serévéler judicieuse dans les exploitationsà problèmes et en combinaisonavec d’autres mesures de protection.PORCILIS APP (MSD A.H.)Ag d’A. pleuropneumoniae pur 50 U (OMP,ApxI, ApxII, ApxIII): 600 mg/dose (2 ml)adjuv: dl-a-tocophérol acetatevaccin injectable imPosologie:porcelet: 2 x 1 dose (2 ml) à l’âge de 6 et10 semFaire jeûner les porcelets avant <strong>la</strong> vacOOI: 2 sem après 2e vacDOI: min 11 sem après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 50 doses (100 ml)R/Pneumonie enzootique (infections àMycop<strong>la</strong>sma hyopneumoniae)La pneumonie enzootique est uneaffection multifactorielle des voiesrespiratoires et dont <strong>la</strong> bactérieMycop<strong>la</strong>sma hyopneumoniae constituele principal agent pathogène. Lesigne clinique le plus marquant estune toux chronique non pro<strong>du</strong>ctivequi se révèle surtout lorsque les porcssont ren<strong>du</strong>s nerveux. Les signes cliniquessont lents à apparaître, mais <strong>la</strong>toux peut per<strong>du</strong>rer pendant plusieurssemaines voire même plusieurs mois.La température corporelle est susceptibled’augmenter légèrement. Dans lecas d’infections bactériennes secondaires,de graves troubles respiratoirespeuvent apparaître et parfois mêmeengendrer de <strong>la</strong> mortalité. La touxdevient pro<strong>du</strong>ctive et peuvent alors semanifester une respiration saccadée etde <strong>la</strong> fièvre. Les animaux gravementtouchés subissent un retard de croissancevisible par rapport aux autresanimaux de <strong>la</strong> loge. Après une phasede guérison clinique, <strong>la</strong> ma<strong>la</strong>die estsusceptible de resurgir. Au niveau del’exploitation, <strong>la</strong> toux est souvent plusimportante chez les porcelets sevrés etles porcs d’engraissement. L’évolutionde <strong>la</strong> ma<strong>la</strong>die est fortement influencéepar <strong>la</strong> gestion de l’exploitation et lesfacteurs environnementaux.VaccinOn peut vacciner contre <strong>la</strong> pneumonieenzootique avec des vaccins inactivés.Un vaccin combiné protégeant contre<strong>la</strong> pneumonie enzootique et <strong>la</strong> ma<strong>la</strong>diede Glässer est également disponible.ProtectionLes porcelets sont en général vaccinéspendant <strong>la</strong> période d’al<strong>la</strong>itement. Selonle vaccin, <strong>la</strong> vaccination aura lieu dèsl’âge de 1 ou 3 semaines. Certainesétudes ont montré qu’une vaccinationlors de <strong>la</strong> période de post-sevrage etd’engraissement peut s’avérer fruc-
13 VACCINS POUR LE PORC 245tueuse. Ceci dépend <strong>du</strong> moment oùles porcs ont été contaminés au seinde l’exploitation. Les animaux doiventêtre vaccinés avant d’être infectés.Tous les porcelets de l’exploitationdoivent être vaccinés. Les porceletsnon vaccinés peuvent constituer unesource d’infection pour les animauxvaccinés et peuvent retarder ou limiter<strong>la</strong> ré<strong>du</strong>ction de <strong>la</strong> pression d’infectiondans l’exploitation. Les principaux résultatsde <strong>la</strong> prévention vaccinale sontune utilisation moindre des antibiotiquesà visée curative et de meilleuresprestations zootechniques: améliorationde <strong>la</strong> croissance quotidienneet <strong>du</strong> rendement alimentaire, périoded’engraissement raccourcie, signescliniques ré<strong>du</strong>its, pourcentage diminuéd’animaux souffrant de lésions pulmonaireset lésions pulmonaires moinséten<strong>du</strong>es.Particu<strong>la</strong>ritésLa vaccination en elle-même ne suffitpas comme mesure de lutte contreles infections à M. hyopneumoniae:d’autres mesures complémentairesdoivent être prises simultanément. Vaccin monovalent contre <strong>la</strong>pneumonie enzootiqueHYORESP (Merial)Mycop<strong>la</strong>sma hyopneumoniae inact:min 3 U ELISA/2 m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:porcelet (âge > 5 j): 2 x 1 dose (2 ml) à 3 - 4sem d’intervalleSu, porcelet (âge > 10 sem): 1 doseOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 50 dosesR/INGELVAC MYCOFLEX (Boehringer Ingelheim)Mycop<strong>la</strong>sma hyopneumoniae inact (souche J,iso<strong>la</strong>t B-3745): min 1,0 RP/m<strong>la</strong>djuv: carbomèrevaccin injectable imPosologie:Su (âge > 3 sem): 1 x 1 dose (1 ml)OOI: 2 sem après vacDOI: min 26 semTemps d’attente: 0 jf<strong>la</strong>con 50 ml (50 doses), 100 ml (100 doses),250 ml (250 doses)R/M+PAC (MSD A.H.)Mycop<strong>la</strong>sma hyopneumoniae inact:min 1,47 RPU/m<strong>la</strong>djuv: huile minérale, sorbitan oleate, polysorbate,hydroxyde d’aluminiumvaccin injectable imPosologie:porc de chair (âge > 7 j):2 x 1 dose (1 ml) à 14 - 28 j d’intervalleporc de chair (âge > 21 j):1 x 2 ml ou 2 x 1 ml à 14 - 28 j d’intervalleschéma à base de 2 vac (2 x 1 ml):- OOI: 35 j après 1e vac- DOI: min 6 mschéma à base d’une seule vac (1 x 2 ml):- OOI: 24 j après vac- DOI: min 6 mTemps d’attente: 0 jf<strong>la</strong>con 100 mlR/MYPRAVAC SUIS (Hipra Lab)Mycop<strong>la</strong>sma hyopneumoniae inact, souche J:min 1,0 DE80 caviaadjuv: lévamisole, carbomèrevaccin injectable imPosologie:porc de chair (âge 7 - 10 j):2 x 1 dose (2 ml)/animal à 21 j d’intervalleOOI: pas d’infoDOI: min 70 jViande: 2 jNe pas administrer <strong>du</strong>rant <strong>la</strong> gestation, <strong>la</strong> <strong>la</strong>ctationni aux porcs de repro<strong>du</strong>ctionf<strong>la</strong>con 50 dosesR/PORCILIS M. HYO (MSD A.H.)Mycop<strong>la</strong>sma hyopneumoniae inact, souche 11:min 7 log2 Ab titeradjuv: dl-alpha-tocophérol acétatevaccin injectable imPosologie:Su (dès l’âge de 1 sem):2 x 1 dose (2 ml)/animal à 3 sem d’intervalleOOI: 2 sem après 2e vacDOI: min 20 sem après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 200 mlR/STELLAMUNE MYCOPLASMA (Eli Lilly)Mycop<strong>la</strong>sma hyopneumoniae inact: min 6000RU/dose (2 ml)vaccin injectable imPosologie:- vac néonatale:porcelet (âge > 3 j et < 14 j): 1 dose (2 ml),2e dose au moment <strong>du</strong> sevrage (âge > 3sem et < 5 sem)- vac après <strong>la</strong> 2e sem d’âge:2 x 1 dose à 2 - 4 sem d’intervalleOOI-DOI: pas d’infoViande: 0 jf<strong>la</strong>con 50 doses (100 ml)R/
24613 VACCINS POUR LE PORCSTELLAMUNE ONE (Eli Lilly)Mycop<strong>la</strong>sma hyopneumoniae inact (souche NL1042): 4,5 à 5,2 log10 UR/doseadjuv: amphigène base drakeol 5 (huileminérale)vaccin injectable imPosologie:Su: 1 x 1 dose (2 ml)OOI: 2 sem après vac (vac à l’âge de 1 sem)DOI: min 25 sem (vac à l’âge de 1 sem)Temps d’attente: 0 jf<strong>la</strong>con 50 doses (100 ml), 125 doses (250 ml)R/SUVAXYN M.HYO (Pfizer A.H.)Mycop<strong>la</strong>sma hyopneumoniae, inact: RP =1adjuv: carbopolvaccin injectable imPosologie:porcelet (âge > 1 sem et < 10 sem): 2 x 1dose (2 ml) à 2 sem d’intervalleOOI: 1 sem après 2e vacDOI: 4,5 mTemps d’attente: 3 semf<strong>la</strong>con 10 x 50 doses10 x 125 dosesR/SUVAXYN MH-ONE (Pfizer A.H.)Mycop<strong>la</strong>sma hyopneumoniae inact (soucheP-5722-3): min 1,00 RP/dose (2 ml)adjuv: carbopol, squa<strong>la</strong>nvaccin injectable imPosologie:Su (âge > 7 j): 1 dose/animalOOI: 2 sem après vacDOI: 6 mTemps d’attente: 0 jf<strong>la</strong>con 50 doses (100 ml), 1250 doses (250 ml)R/ Vaccin combiné contre <strong>la</strong>pneumonie enzootique et <strong>la</strong>ma<strong>la</strong>die de GlässerSUVAXYN M.HYO - PARASUIS (Pfizer A.H.)Mycop<strong>la</strong>sma hyopneumoniae inact, soucheP-5722-3: AR 1 - 1,9/doseHaemophilus parasuis inact, sérotype 4, souche2170B: AR 1 - 8,1/doseHaemophilus parasuis inact, sérotype 5, soucheIA84-29755: AR 1 - 3,4/doseadjuv: Carbopol 941vaccin injectable imPosologie:porc d’engraissement (âge min 7 j): 2 x 1dose (2 ml) à 14 - 21 j d’intervalleOOI: Myc. hyopneum: 1 sem après 2e vac,Haem. parasuis: 3,5 sem après 2e vacDOI: 6 m après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 120 ml (50 doses)R/Ma<strong>la</strong>die de Glässer (infections àHaemophilus parasuis)La ma<strong>la</strong>die de Glässer, engendrée parHaemophilus parasuis, a été décrite àl’origine comme une affection survenantchez les jeunes animaux (âgésde 2 à 4 semaines) et caractériséepar une polysérosite fibrineuse, unepolyarthrite, une méningite et danscertains cas, de <strong>la</strong> mortalité. Peuventapparaître également : une septicémie(sans polysérosite), une myosite aiguë(muscle masseter) et des troubles respiratoires.Des facteurs de stress telsque le sevrage ou le transport prédisposentà ce type d’affection. Lama<strong>la</strong>die est généralement bénigne etprésente un taux faible de morbidité.Ce sont aujourd’hui surtout les exploitationsà niveau sanitaire très élevéqui peuvent souffrir de grandes perteséconomiques, plus particulièrementdans les cas où des animaux d’originesdifférentes y sont rassemblés.Les taux de morbidité et de mortalitédans ce type d’entreprises sont élevés,quel que soit l’âge ou le stadede pro<strong>du</strong>ction dans lequel se trouventles porcs. Haemophilus parasuis estfréquemment présent au niveau de <strong>la</strong>muqueuse nasale des animaux sainset même immunisés, et peut aussi êtreisolé des amygdales et de <strong>la</strong> trachée.Quinze sérotypes sont connus pour cegerme. Les souches non sérotypablessont régulièrement isolées. Toutesles souches de H. parasuis ne sontpas aussi virulentes. La virulence dépendplus ou moins <strong>du</strong> sérotype. Lessouches des sérotypes 1, 5, 10, 12,13 et 14 ont été c<strong>la</strong>ssées comme hautementvirulentes, et les souches dessérotypes 2, 4 et 15 comme moyennementvirulentes. Dans un même sérotype,des souches peuvent être aussibien plus et moins virulentes et mêmeles souches non sérotypables peuventêtre virulentes. Il reste donc à déterminersi <strong>la</strong> variation dans <strong>la</strong> virulenceest dépendante de souche ou de sérotype.Le traitement ou <strong>la</strong> prévention àbase d’antibiotiques n’est pas toujoursefficace et ne doit avoir lieu en aucuncas à un stade avancé. On peut éviterque <strong>la</strong> ma<strong>la</strong>die ne se déc<strong>la</strong>re en ré<strong>du</strong>isantle stress et en ne rassemb<strong>la</strong>nt queles animaux présentant une immunitéprotectrice, obtenue naturellement oupar le biais de vaccinations.VaccinLe vaccin monovalent commercialiséen Belgique contient une souche inactivéede sérotype 5. Un vaccin combinéprotégeant contre <strong>la</strong> pneumonieenzootique et <strong>la</strong> ma<strong>la</strong>die de Glässer(types 4 et 5) est également disponible.ProtectionCes vaccins stimulent, selon <strong>la</strong> spécialité,le développement d’une immunitéactive contre le sérotype 5 ou contreles types 4 et 5 de Haemophilus pa-
13 VACCINS POUR LE PORC 247rasuis. Les animaux doivent être vaccinésà deux reprises. Les animauxsont protégés après <strong>la</strong> deuxièmesemaine suivant <strong>la</strong> deuxième vaccination,et ce pour une <strong>du</strong>rée d’aumoins quatorze semaines. Le vaccincombiné déclenche une immunitécontre Mycop<strong>la</strong>sma hyopneumoniae1 semaine après <strong>la</strong> seconde vaccinationet contre Haemophilus parasuis3,5 semaines après <strong>la</strong> seconde vaccination.Le vaccin protège pendant6 mois après <strong>la</strong> seconde vaccinationcontre Mycop<strong>la</strong>sma hyopneumoniaeet les sérotypes 4 et 5 d’Haemophilusparasuis. Vaccin contre <strong>la</strong> ma<strong>la</strong>die deGlässerPORCILIS GLÄSSER (MSD A.H.)Haemophilus parasuis inact, sérotype 5, souche4800: min 9,1 U Elisa/dose (2 ml)adjuv: dl-alpha-tocophérol acétatevaccin injectable imPosologie:Su (âge min 5 sem): 2 x 1 dose (2 ml) à 2sem d’intervalletruie:Primovac: 2 x 1 dose à 4 sem d’intervalle, 8à 6 sem avant <strong>la</strong> mise basRevac: 1 dose 4 à 2 sem avant <strong>la</strong> mise basSu: OOI: 2 sem après 2e vac, DOI: 14 semaprès 2e vacImm mat porcelet: OOI: après ingestion decolostrum, DOI: sérotype 4: 4 sem, sérotype 5:6 semTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/ Vaccin combiné contre <strong>la</strong>pneumonie enzootique et <strong>la</strong>ma<strong>la</strong>die de GlässerSUVAXYN M.HYO - PARASUIS (Pfizer A.H.)Mycop<strong>la</strong>sma hyopneumoniae inact, soucheP-5722-3: AR 1 - 1,9/doseHaemophilus parasuis inact, sérotype 4, souche2170B: AR 1 - 8,1/doseHaemophilus parasuis inact, sérotype 5, soucheIA84-29755: AR 1 - 3,4/doseadjuv: Carbopol 941vaccin injectable imPosologie:porc d’engraissement (âge min 7 j): 2 x 1dose (2 ml) à 14 - 21 j d’intervalleOOI: Myc. hyopneum: 1 sem après 2e vac,Haem. parasuis: 3,5 sem après 2e vacDOI: 6 m après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 120 ml (50 doses)R/Rhinite atrophiqueLa rhinite atrophique est une affectionmultifactorielle caractérisée par uneatrophie des cornets. Lorsque l’affectionest sérieuse, elle s’accompagnede différents degrés de distorsionfaciale tels que <strong>la</strong> brachygnatie supérieureet une déviation <strong>la</strong>térale <strong>du</strong> groinet <strong>du</strong> septum nasal. On distingue <strong>la</strong>rhinite atrophique non progressive etprogressive. La première est engendréepar des souches toxigènes deBordetel<strong>la</strong> bronchiseptica et <strong>la</strong> secondepar des souches toxigènes dePasteurel<strong>la</strong> multocida ou par une combinaisonde souches B. bronchisepticaet P. multocida toxigènes. Les toxinesdermonécrotiques de B. bronchisepticaet P. multocida peuvent endommagerles cornets mais leur mécanismed’action est différent. L’hypop<strong>la</strong>siedes cornets in<strong>du</strong>ite par les souchesde B. bronchiseptica est en généralmoins grave que celle engendrée parles souches de P. multocida toxigènes.VaccinLes vaccins contre <strong>la</strong> rhinite atrophiqueprogressive doivent au minimumcontenir <strong>la</strong> toxine dermonécrotique deP. multocida. Elles peuvent en outrecomporter <strong>la</strong> toxine dermonécrotiquede B. bronchiseptica et les germesinactivés.ProtectionLa vaccination des truies avec desvaccins inactivés peut favoriser <strong>la</strong>régression de <strong>la</strong> rhinite atrophique.L’objectif de cette vaccination est <strong>la</strong>transmission de l’immunité colostraleaux porcelets.PORCILIS AR-T DF susp inj (MSD A.H.)par dose (2 ml):dO protéine (Pasteurel<strong>la</strong> multocida):min 6,2 log2 titre TNBordetel<strong>la</strong> bronchiseptica inact:min 4,2 log2 titre aggl.adjuv: acétate de dl-alpha-tocophérolvaccin injectable imPosologie:- primovac:truie, cochette (âge min 18 sem): 2 x 1 dose(2 ml) à 4 sem d’intervalle, 1ère vac 6 semavant <strong>la</strong> mise bas- revac:1 x 1 dose 2 - 4 sem avant chaque mise basOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/
24813 VACCINS POUR LE PORCRHINIFFA T (Merial)Bordetel<strong>la</strong> bronchiseptica (souche toxinogène)inact: min 0,9 SA.U/2 mlPasteurel<strong>la</strong> multocida type D (souche toxinogène)inact: min 0,9 ELISA.U/2 m<strong>la</strong>natoxine de Pasteurel<strong>la</strong> multocida:min 1,0 ELISA.U/2m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:Primovac:Su: 2 x 1 dose (2 ml) à 4 - 6 sem d’intervalle,2e dose 2 sem avant <strong>la</strong> mise basRevac:1 dose 2 sem avant chaque mise basOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/RHINISENG (Hipra Lab)Bordetel<strong>la</strong> bronchiseptica inact, souche833CER: 9,8 CBbtoxine recombinante de Pasteurel<strong>la</strong> multocida,type D (PMTr): min 1 DEM63adjuv: hydroxyde d’aluminiumvaccin injectable imPosologie:truie, cochette:primovac: 2 x 2 ml à 3 - 4 sem d’intervalle(1e inject 6 - 8 sem avant <strong>la</strong> mise bas)revac: 1 x 2 ml, 3 à 4 sem avant chaquemise bas suivanteOOI-DOI: pas d’infoimm passive porcelet jusqu’à l’âge de 6 semTemps d’attente: 0 jf<strong>la</strong>con 50 dosesR/Diarrhée néonatale causée par lessouches E. coli entérotoxigènesLes souches entérotoxinogènesd’Escherichia coli (ETEC) peuvent engendrerune diarrhée aqueuse. Celle-cipeut être à l’origine d’une importantemortalité chez les porcelets nouveaunés.Cette forme dite entérotoxinogènede <strong>la</strong> colibacillose se rencontreégalement chez les porcelets plusâgés, qu’ils soient sevrés ou non.Les souches ETEC possèdent deuxfacteurs importants de virulence. Lesfimbriae leur permettent de se fixersur les entérocytes de l’intestin grêle.Les principaux facteurs d’adhésiondes souches ETEC qui engendrent <strong>la</strong>diarrhée néonatale sont les fimbriae F4(K88), F5 (K99), F6 (987P) et F41. Lessouches ETEC F4+ peuvent égalementjouer un rôle dans <strong>la</strong> diarrhée de porceletsà un âge plus avancé. En ce quiconcerne <strong>la</strong> diarrhée survenant aprèsle sevrage, ce sont les ETEC F4+ etF18+ qui sont les plus impliquées. Lessouches ETEC forment également desentérotoxines qui sont à l’origine de <strong>la</strong>diarrhée aqueuse, les thermo<strong>la</strong>biles(LT) et les thermostables (STa et STb).L’entérotoxine LT est une protéine depoids molécu<strong>la</strong>ire élevé, fortementantigénique. Les entérotoxines STa etSTb sont des peptides de faible poidsmolécu<strong>la</strong>ire, peu immunogènes, sauf sielles sont conjuguées avec une autreentérotoxine, LT par exemple. La vaccinationdes truies gestantes peut serévéler efficace dans <strong>la</strong> lutte contre <strong>la</strong>diarrhée néonatale à E. coli.VaccinOn administrera à cet effet des vaccinsinactivés contenant des facteurs d’adhésionpurifiés ou un nombre ré<strong>du</strong>itde sérotypes E. coli avec les facteursd’adhésion et éventuellement l’entérotoxineLT.ProtectionUne primovaccination avec de telsvaccins suit en général le schéma suivant: deux injections à 3-6 semainesd’intervalle, <strong>la</strong> deuxième dose étantadministrée 2 à 6 semaines avant <strong>la</strong>mise bas. Ces vaccins ont principalementcomme résultat une augmentationde <strong>la</strong> teneur en IgG dans lecolostrum.Particu<strong>la</strong>ritésEn combinaison avec d’autres mesuresvisant à ré<strong>du</strong>ire le risque d’infectionet augmenter l’immunité générale,ils s’avèrent dans <strong>la</strong> plupart des casfructueux dans le traitement de <strong>la</strong>diarrhée néonatale. Ils sont cependantbeaucoup moins efficaces contre <strong>la</strong>diarrhée chez les porcelets plus âgéset non sevrés et n’offrent aucuneprotection contre <strong>la</strong> diarrhée après lesevrage.NEOCOLIPOR (Merial)E. Coli inact:adhésines F4 (F4ab, F4 ac, F4ad): min 2,1 U.SAadhésine F5: min 1,7 U.SAadhésine F6: min 1,4 U.SAadhésine F41: min 1,7 U.SAadjuv: AL3+, thiomersalvaccin injectable imPosologie:Primovac:Su: 2 x 1 dose (2 ml) , 1e vac 5 - 7 semavant <strong>la</strong> mise bas, 2e vac 2 sem avant <strong>la</strong>mise basRevac:1 dose 2 sem avant chaque mise basOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/
13 VACCINS POUR LE PORC 249PORCILIS PORCOLI DF (MSD A.H.)adhésines d’E. coli:F4ab (K88ab): min 9,0 log2 titre AcF4ac (K88ac): min 5,4 log2 titre AcF5 (K99): min 6,8 log2 titre AcF6 (987 P): min 7,1 log2 titre Acanatoxine LT = 6,8 log2 titre Acadjuv: acétate de dl-alpha-tocophérolvaccin injectable imPosologie:Primovac:truie, cochette: 2 x 1 dose (2 ml), 6 à 8 semavant <strong>la</strong> mise bas, suivi d’une 2e vac 4 semplus tardRevac:1 dose <strong>du</strong>rant <strong>la</strong> 2e moitié de chaque gestation,2 - 4 sem avant <strong>la</strong> mise basOOI: pas d’infoDOI: 1ers j de vieTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/Vaccin combiné: souches entérotoxigenesd’Escherichia coli,Clostridium perfringens etClostridium novyiClostridium novyi peut provoquer uneinfection aiguë chez les truies, accompagnéeentre autres d’une nécrosehépatique et de mort soudaine. Lessouches entérotoxigènes d’E. colipeuvent engendrer de <strong>la</strong> diarrhéechez les porcelets (Voir aussi chapitreDiarrhée néonatale). Clostridium perfringenstype C provoque l’entéritenécrotique chez les porcelets.VaccinCe vaccin inactivé stimule <strong>la</strong> synthèsed’anticorps, dans le sérum des animauxvaccinés, contre les adhésineset l’entérotoxine <strong>la</strong>bile à <strong>la</strong> chaleur(LT) des souches entérotoxigènesd’Escherichia coli, <strong>la</strong> bêta-toxine deClostridium perfrigens de type C etl’alpha-toxine de Clostridium novyi.ProtectionPar l’immunisation active des truies etdes cochettes repro<strong>du</strong>ctrices, les porceletsnouveaux-nés sont protégés,après ingestion suffisante de colostrum,contre <strong>la</strong> diarrhée néonatalecausée par les Escherichia coli entérotoxinogènesexprimant les adhésinesF4ab (K88ab), F4ac (K88ac), F5 (K99)ou F6 (987P) et contre l’entérite nécrotiquecausée par Clostridium perfringensde type C. Cette protection semanifeste par une ré<strong>du</strong>ction de <strong>la</strong> mortalitéet des signes cliniques. La vaccinationdes truies et des cochettesin<strong>du</strong>it également des anticorps séroneutralisantscontre l’alpha-toxine deClostridium novyi.SUISENG (Hipra Lab)adhésine fimbriale F4ab d’E. coli:min 65% ER60adhésine fimbriale F4ac d’E. coli:min 78% ER70adhésine fimbriale F5 d’E. coli: min 79% ER50adhésine fimbriale F6 d’E. coli: min 80% ER25anatoxine entérique LT d’E. coli: min 55% ER70anatoxine de Clostridium perfringens, type C:min 35% ER25anatoxine de Clostridium novyi: min 50% ER120adjuv: hydroxyde d’aluminium, extrait deginsengvaccin injectable imPosologie:PrimovacSu: 2 x 1 dose (2 ml) 6 sem et 3 sem avant<strong>la</strong> mise basRevac:Su: 1 dose (2 ml)/gestation, 3 sem avant <strong>la</strong>mise basOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 50 dosesR/Entéropathie proliférative porcine(EPP) (infections à Lawsoniaintracellu<strong>la</strong>ris)L’entéropathie proliférative porcine(EPP) est causée par <strong>la</strong> bactérieLawsonia intracellu<strong>la</strong>ris et peut êtreaiguë (entéropathie proliférative hémorragique),chronique (adénomatoseintestinale porcine) ou subclinique. Laforme aiguë de l’entéropathie proliférativehémorragique est le plus souventobservée chez des porcs de chair oude repro<strong>du</strong>ction plus âgés (> 70 kgpoids vif) et peut entraîner une mortalitéaiguë sans signes cliniques préa<strong>la</strong>bles.Dans certains cas, des fèces decouleur rougeâtre voire goudronneusepeuvent être constatées avant que<strong>la</strong> mort ne s’ensuive. En cas de progressionplus lente de <strong>la</strong> ma<strong>la</strong>die, lesporcs deviennent d’abord anémiques,anorexiques puis moins mobiles. Desvomissements de matières goudronneusessont possibles. L’apparencedes fèces peut varier considérablement: profuses, plus ou moinsaqueuses, goudronneuses, rouge vifou sang<strong>la</strong>ntes. La mortalité peut semanifester dans les 48 h. Certains animauxse rétablissent complètement,mais en général, on constate un retardde croissance <strong>du</strong>rable. La mortalitépeut atteindre jusqu’à 50 % des animauxtouchés. L’adénomatose intestinaleporcine peut apparaître chezdes porcs dès l’âge de 7 semaines etse manifeste par une diarrhée chronique,une peau pâle et, tout commedans le cas d’une entéropathie subclinique,un manque d’uniformité dans <strong>la</strong>
25013 VACCINS POUR LE PORCcroissance. En général, les signes cliniquessont cependant peu typiques.Lawsonia intracellu<strong>la</strong>ris est identifiéedans <strong>la</strong> plupart des exploitations etpeut causer des dégâts économiquesimportants. La forte capacité de surviedans le fumier (2 à 3 semaines) etl’excrétion prolongée par les animauxinfectés exigent une stricte applicationdes mesures d’hygiène c<strong>la</strong>ssiquesdans l’exploitation (all in all out, désinfectionde <strong>la</strong> porcherie et <strong>du</strong> matérielutilisé) afin d’entraver <strong>la</strong> ma<strong>la</strong>die et delimiter les pertes économiques.VaccinLe vaccin actuellement commercialisécontient une souche atténuée deLawsonia intracellu<strong>la</strong>ris.ProtectionLe vaccin est destiné à immuniser activementles porcelets (dès l’âge de 3semaines) afin de ré<strong>du</strong>ire les lésionsintestinales causées par Lawsonia intracellu<strong>la</strong>riset éviter ainsi les pertesde poids. La protection débute 3 semainesaprès <strong>la</strong> vaccination et <strong>du</strong>re aumoins 17 semaines.Particu<strong>la</strong>ritésLa vaccination se faisant avec desgermes atténués, on n’administrerapas de médicaments antimicrobiens<strong>du</strong>rant les trois jours précédant et suivant<strong>la</strong> vaccination. Si <strong>la</strong> vaccination sefait par l’eau de boisson, l’instal<strong>la</strong>tiond’eau de boisson doit également êtreexempte de toute substance antimicrobienne,désinfectant ou détergent.Du <strong>la</strong>it en poudre écrémé ou <strong>du</strong> thiosulfatede sodium peuvent fonctionnercomme stabilisateurs <strong>du</strong> vaccindans l’eau de boisson. De l’ADN deLawsonia intracellu<strong>la</strong>ris peut être présentdans les excréments des porcsvaccinés jusqu’à trois jours après <strong>la</strong>vaccination. Même si le risque de propagation<strong>du</strong> germe après vaccinationest moindre, on n’excluera pas <strong>la</strong> possibilitéde transmission aux animauxde <strong>la</strong> même porcherie.ENTERISOL ILEITIS (Boehringer Ingelheim)Lawsonia intracellu<strong>la</strong>ris (MS B3903) att: min 10exp4,9 TCID50 et max 10 exp6,1 TCID50/2 mlvaccin lyophilisé et solvant pour solution po(gavage ou eau de boisson)Posologie:Su (âge > 3 sem): 1 dose (2 ml)OOI: 3 semDOI: min 17 semTemps d’attente: 0 jf<strong>la</strong>con 20 ml (10 doses), 100 ml (50 doses)R/Rouget <strong>du</strong> porcLe rouget <strong>du</strong> porc est engendré par <strong>la</strong>bactérie Erysipelothrix rhusiopathiae.Cette affection sous sa forme aiguës’accompagne de graves signes cliniquesgénéraux dont parfois desaltérations dermatologiques typiques.La fièvre est susceptible d’engendrerl’avortement chez <strong>la</strong> truie gestante.Les verrats peuvent, quant à eux,souffrir de troubles de fécondité. Soussa forme chronique, l’affection estcaractérisée par de <strong>la</strong> polyarthrite etde l’endocardite. On connaît un grandnombre de sérotypes de ce germe. Laplupart des souches isolées chez leporc appartiennent toutefois aux sérotypes1 ou 2.VaccinIl existe des vaccins monovalents etbivalents. En Belgique, seuls des vaccinsinactivés ont été enregistrés. Lesvaccins à base de souches <strong>du</strong> sérotype2 bien déterminées n’in<strong>du</strong>isentpas seulement une protection contrece sérotype mais également contreles souches de sérotype 1 et <strong>la</strong> plupartdes autres sérotypes. De tels vaccinsse composent de germes inactivés etd’un antigène soluble pro<strong>du</strong>it lors de <strong>la</strong>croissance <strong>du</strong> germe dans des milieuxliquides.ProtectionLa <strong>du</strong>rée de <strong>la</strong> protection après unedouble vaccination à 3 - 6 semainesd’intervalle est d’environ six mois.L’immunité maternelle peut interféreravec <strong>la</strong> vaccination jusqu’à l’âge detrois mois environ. La vaccination estsurtout préconisée chez les animauxde repro<strong>du</strong>ction. Dans les exploitationsà problèmes, les porcs de chairpeuvent également être vaccinés. Il aété démontré que, pour certains vaccins,une seule vaccination dès l’âgede trois mois in<strong>du</strong>it une protection<strong>du</strong>rant <strong>la</strong> période d’engraissement.Les vaccins contre le rouget <strong>du</strong> porcne peuvent cependant in<strong>du</strong>ire qu’unefaible (voire aucune) protection contre<strong>la</strong> forme chronique de cette affection.
13 VACCINS POUR LE PORC 251 Vaccins monovalents contre lerouget <strong>du</strong> porcPORCILIS ERY (MSD A.H.)Erysipelothrix rhusiopathiae (M2 sérotype 2)inact: min 50 UI/dose (2 ml)vaccin injectable imPosologie:Primovac:Su (âge > 12 sem): 2 x 1 dose (2 ml) à 4 semd’intervalleRevac:truie: 1 dose pendant chaque période de<strong>la</strong>ctationverrat: 2 x 1 dose/ancochette, verrat: ne pas vac les 2 dernièressem avant <strong>la</strong> saillieOOI: 3 sem, DOI: 6 mTemps d’attente: 0 jf<strong>la</strong>con 50 mlR/RUVAX VET (Merial)Erysilopethrix rhusiopathiae (sérotype 2):1 Elisa U/2 m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:Primovac:cochette, verrat (âge > 3 m):2 x 1 dose (2 ml) à 3 - 4 sem d’intervalleRevac:truie: 1 dose au moment <strong>du</strong> sevrageverrat: pas dans les 3 sem qui précèdent<strong>la</strong> saillieporc de chair (âge > 3 m): 2 x 1 dose (2 ml) à3 - 4 sem d’intervalleOOI: 3 sem après 1e vacDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/ Vaccins bivalents :rouget <strong>du</strong> porc - parvovirosePARVORUVAX (Merial)parvovirus porcin inact: 2 U.HAI/2 mlErysipelothrix rhusiopathiae inact (sérotype 2):min 1 U Elisa/2 m<strong>la</strong>djuv: hydroxyde d’aluminiumvaccin injectable imPosologie:Primovac:Su (sans imm mat): 2 x 1 dose (2 ml) à 3 - 4sem d’intervalle (2e vac min 2 sem avant1e saillie)Revac:1 dose/6 m (périodes d’al<strong>la</strong>itement)rouget:OOI: 3 sem après 2e inject de <strong>la</strong> primovacDOI: pas d’infoparvo:OOI: primovac complète min 14 j avantrepro<strong>du</strong>ction, protège contre une infectiontransp<strong>la</strong>centaireDOI: 9 mTemps d’attente: 0 jf<strong>la</strong>con 25 doses (50 ml)R/PARVOSUIN-MR (Hipra Lab)parvovirus porcin inact (NADL-2):min 2048 HAE/2 mlErysipelothrix rhusiopathiae (R32E11) inact:min 50 UI/2 m<strong>la</strong>djuv: huilevaccin injectable imPosologie:Primovac:cochette, verrat (âge > 6 m):2 x 1 dose (2 ml) à 3 - 4 sem d’intervalle(min 1 sem avant <strong>la</strong> saillie)Revac:truie: 1 dose 10 - 15 j après <strong>la</strong> mise basverrat: 1 dose/anParvo:primovac min 1 sem avant <strong>la</strong> repro<strong>du</strong>ction protègecontre une infection transp<strong>la</strong>centaireRouget:OOI: pas d’info, DOI: 3 mViande: 0 jf<strong>la</strong>con 10 x 25 doses10 x 50 dosesR/PORCILIS ERY-PARVO (MSD A.H.)Erysipelothrix rhusiopathiae inact (M2 sérotype2): min 50 UI/dose (2 ml)parvovirus porcin inact (PPV 014):min 9 log2 HI/dose (2 ml)adjuv: alpha-tocophérol acétatevaccin injectable imPosologie:Primovac:cochette (âge > 20 sem):Parvovirose: 1 dose (2 ml) 2 sem avant <strong>la</strong>saillieRouget <strong>du</strong> porc: 2 x 1 dose à 4 semd’intervalleRevac:truie: 1 dose pendant chaque période de<strong>la</strong>ctation, au moins 2 sem avant saillieParvo:1 vac min 2 sem avant <strong>la</strong> repro<strong>du</strong>ction protègecontre une infection transp<strong>la</strong>centaire par le PPVRouget:OOI: 3 sem, DOI: 6 mViande: 0 jf<strong>la</strong>con 25 dosesR/SUVAXYN PARVO/E (Pfizer A.H.)chaque dose (2 ml) contient:parvovirus porcin (souche S-80), inact: min titreIHA 160 chez le <strong>la</strong>pinErysipelothrix rhusiopathiae (souche B-7, sérotype2), inact: potency selon Ph EurAdjuv: marcol 52 (huile minérale), montanide888 (émulsifiant), simulsol 5100 (émulsifiant)vaccin injectable imPosologie:Primovac:cochette (âge > 5 m) et truie: 2 x 1 dose à3 - 4 sem d’intervalle, 2e dose min 4 semavant <strong>la</strong> saillieRevac:1 dose pendant <strong>la</strong> <strong>la</strong>ctation, 3 - 4 sem avant<strong>la</strong> saillieOOI : 3 sem après vacDOI : 6 mTemps d’attente: 0 jf<strong>la</strong>con 2 x 25 dosesR/
25213 VACCINS POUR LE PORCTableau récapitu<strong>la</strong>tif des vaccins pour le porcparvovirus porcinvirus influenzavirus SDRPcircovirus porcinA. pleuropneumonieM. hyopneumoniaeB. bronchiseptica etP. multocidaE. coliClostridium spp.E. rhusiopathiaeHaemophilus parasuisLawsonia intracellu<strong>la</strong>risCIRCOVACMerialXENTERISOL ILEITISBoehringer IngelheimXGRIPOVAC 3MerialXHYORESPMerialXINGELVAC CIRCOFLEXBoehringer IngelheimXINGELVAC MYCOFLEXBoehringer IngelheimXINGELVAC PRRS KVBoehringer IngelheimXINGELVAC PRRS Modified LiveVirusBoehringer IngelheimXM+PACSchering-PloughXMYPRAVAC SUISHipra LabXNEOCOLIPORMerialXPARVORUVAXMerialXXPARVOSUIN-MRHipra LabXXPORCILIS APPMSD A.H.XPORCILIS AR-T DF susp injMSD A.H.XPORCILIS ERYMSD A.H.XPORCILIS ERY-PARVOMSD A.H.XXPORCILIS GlässerMSD A.H.XPORCILIS M. HYOMSD A.H.X
13 VACCINS POUR LE PORC 253parvovirus porcinvirus influenzavirus SDRPcircovirus porcinA. pleuropneumonieM. hyopneumoniaeB. bronchiseptica etP. multocidaE. coliClostridium spp.E. rhusiopathiaeHaemophilus parasuisLawsonia intracellu<strong>la</strong>risPORCILIS PARVOMSD A.H.XPORCILIS PCVMSD A.H.XPORCILIS PORCOLI DFMSD A.H.XPORCILIS PRRSMSD A.H.XPROGRESSISMerialXRHINIFFA TMerialXRHINISENGHipra LabXRUVAX VETMerialXSTELLAMUNE MYCOPLASMAPfizer A.H.XSTELLAMUNE ONEPfizer A.H.XSUISENGHipra LabXXSUVAXYN M.HYOPfizer A.H.XSUVAXYN M.HYO – PARASUISPfizer A.H.XXSUVAXYN MH ONEPfizer A.H.XSUVAXYN PARVO/EPfizer A.H.XXSUVAXYN PCVPfizer A.H.X
25413 VACCINATION DES LAPINS13.1.4 Vaccination des <strong>la</strong>pins13.1.4.1 Vaccin combiné contre <strong>la</strong>myxomatose et <strong>la</strong> ma<strong>la</strong>diehémorragique viraleLa myxomatose est une ma<strong>la</strong>die provoquéepar le virus myxomateux appartenantà <strong>la</strong> famille des Poxviridaeet atteignant les <strong>la</strong>pins européens. Elletouche les animaux à tout âge. On distinguedeux formes cliniques:1) <strong>la</strong> forme c<strong>la</strong>ssique est principalementobservée chez les <strong>la</strong>pins domestiqueset les <strong>la</strong>pins sauvages quiconstituent le réservoir <strong>du</strong> virus. Levirus se transmet ici principalementpar des morsures d’insectes, mais <strong>la</strong>promiscuité entre les <strong>la</strong>pins peut égalementconstituer un facteur de contagion.La ma<strong>la</strong>die a une courte périoded’incubation et est caractérisée parune mortalité élevée. Elle est diagnostiquéeà partir des signes cliniquestypiques.2) Au cours de ces dernières décennies,une myxomatose à symptômesrespiratoires est apparue dans l’élevagein<strong>du</strong>striel. Cette forme respiratoireest présente en élevage toutel’année. Elle est provoquée par dessouches virales moins pathogènes.Elle peut être subclinique et n’est pastoujours facile à diagnostiquer.La ma<strong>la</strong>die hémorragique virale <strong>du</strong><strong>la</strong>pin (rabbit haemorrhagic disease ouRHD) atteint les <strong>la</strong>pins européens etest provoquée par un virus appartenantà <strong>la</strong> famille des Caliciviridae. LaRHD se propage rapidement, l’infectionse contractant par voie nasale,conjonctivale et orale. La ma<strong>la</strong>die peutse transmettre directement ou indirectementpar le contact avec les cages,les humains, les oiseaux ou les insectes.Elle se caractérise par un tauxde mortalité élevé chez le <strong>la</strong>pin a<strong>du</strong>lte,<strong>la</strong> mort étant précédée par peu desymptômes, voire aucun. Les symptômescliniques ne se manifestent quechez les animaux âgés de plus de 8 à10 semaines. Le mécanisme de résistancechez les animaux plus jeunesn’est pas encore bien connu.VaccinLa souche vaccinale est un virus de<strong>la</strong> myxomatose qui exprime le gènecodant pour <strong>la</strong> protéine de capside <strong>du</strong>RHDV. Ainsi les <strong>la</strong>pins sont immunisésà <strong>la</strong> fois contre le virus de <strong>la</strong> myxomatoseet contre le RHDV.ProtectionLe vaccin est utilisé pour l’immunisationactive des <strong>la</strong>pins, dès l’âge de 5semaines, afin de ré<strong>du</strong>ire <strong>la</strong> mortalitéet les signes cliniques <strong>du</strong>s à <strong>la</strong> myxomatoseet de prévenir <strong>la</strong> mortalité <strong>du</strong>eà <strong>la</strong> RHD. Les animaux vaccinés sontprotégés à partir de 3 semaines après<strong>la</strong> vaccination. La protection <strong>du</strong>re 1an. Une augmentation transitoire de<strong>la</strong> température de l’ordre de 1 à 2°Cpeut survenir. Dans les deux premièressemaines après <strong>la</strong> vaccination,un œdème non douloureux de petitetaille peut être observé au niveau <strong>du</strong>site d’injection. Cet œdème disparaîtcomplètement à <strong>la</strong> fin de <strong>la</strong> troisièmesemaine. Après une infection avecle virus sauvage de <strong>la</strong> myxomatose,certains animaux vaccinés peuventdévelopper quelques vésicules detrès petite taille, particulièrement auxendroits dépourvus de poils, formantrapidement des croûtes. Les croûtesdisparaissent généralement dans les2 semaines après l’observation despetites vésicules. Ces croûtes sont observéesuniquement chez les animauxavec une immunité active et n’ont pasd’influence sur l’état de santé général,l’appétit ou le comportement <strong>du</strong> <strong>la</strong>pin.Particu<strong>la</strong>ritésIl se peut que les <strong>la</strong>pins ayant été précédemmentvaccinés avec un autrevaccin contre <strong>la</strong> myxomatose ou ayantcontracté une myxomatose naturellesur le terrain ne développent pas deréponse immunitaire appropriée contre<strong>la</strong> RHD après <strong>la</strong> vaccination.La vaccination n’est pas recommandéedans les 14 premiers jours de <strong>la</strong>gestation. Aucun essai n’ayant étéréalisé sur l’effet de <strong>la</strong> vaccinationchez les <strong>la</strong>pins mâles repro<strong>du</strong>cteurs,<strong>la</strong> vaccination de ces <strong>la</strong>pins n’est pasrecommandée.La myxomatose et <strong>la</strong> RHD sont soumisesà déc<strong>la</strong>ration obligatoire.NOBIVAC MYXO-RHD (MSD A.H.)virus viv de <strong>la</strong> myxomatose exprimant uneglycoprotéine <strong>du</strong> virus de <strong>la</strong> MHL (souche 009):min 103.0 et max 106.1 FFU/dosevaccin lyophilisé injectable scPosologie:<strong>la</strong>pin (dès l’âge de 5 sem): 1 dose/animalrevac: 1 x/anOOI: 3 sem après vac, DOI: 1 anTemps d’attente: 0 jf<strong>la</strong>con 5 x 1 dose + 5 x 1 ml de solvantR/i
13 VACCINATION DES POULES 255Tableau récapitu<strong>la</strong>tif des vaccins pour le <strong>la</strong>pinNOBIVAC MYXO-RHDMSD A.H.13.1.5 Vaccination des poulesmyxomatoseXma<strong>la</strong>die hémorragiquevirale <strong>du</strong> <strong>la</strong>pinX13.1.5.1 Vaccins contre <strong>la</strong> ma<strong>la</strong>diede MarekLes poules pondeuses et repro<strong>du</strong>ctricessont vaccinées en période d’élevage.Etant donné <strong>la</strong> <strong>du</strong>rée d’élevageplus longue des poulets à <strong>la</strong>bel, il estrecommandé de vacciner les poussinsà l’âge d’un jour, au couvoir, contre <strong>la</strong>ma<strong>la</strong>die de Marek.VaccinLes vaccins contre <strong>la</strong> ma<strong>la</strong>die deMarek sont administrés par injection,au couvoir, à des poussins d’un jourou à des embryons âgés de 18 jours.Ils contiennent soit l’herpèsvirus de <strong>la</strong>dinde (souche HVT FC126) sous formelyophilisée, soit <strong>la</strong> souche Rispens <strong>du</strong>virus de <strong>la</strong> ma<strong>la</strong>die de Marek atténuée(CVI988) sous forme cellu<strong>la</strong>ireconservée en azote liquide. Certainsvaccins combinent l’herpèsvirus de <strong>la</strong>dinde et <strong>la</strong> souche homologue, tousdeux sous forme cellu<strong>la</strong>ire et doncconservés en azote liquide. Une spécialitécontient comme souche vaccinaleun herpèsvirus de <strong>la</strong> dinde (HVT)recombinant, exprimant l’antigèneprotecteur (VP2) <strong>du</strong> virus de <strong>la</strong> bursiteinfectieuse aviaire (IBDV ou ma<strong>la</strong>die deGumboro), souche Faragher 52/70. Cevaccin in<strong>du</strong>it une immunisation activeet une réponse sérologique vis-à-visde <strong>la</strong> ma<strong>la</strong>die de Gumboro (InfectiousBursal Disease ou IBD) et de <strong>la</strong> ma<strong>la</strong>diede Marek chez le poussin.ProtectionLa vaccination empêche <strong>la</strong> formationdes tumeurs et des lésions nerveuses<strong>du</strong>es au virus pathogène de <strong>la</strong> ma<strong>la</strong>diede Marek. Elle ne prévient cependantpas l’infection des vo<strong>la</strong>illes par cevirus. Les résultats de <strong>la</strong> vaccinationdépendent <strong>la</strong>rgement <strong>du</strong> respect de <strong>la</strong>technique de vaccination.La vaccination doit obligatoirementêtre pratiquée à l’âge d’un jour, aucouvoir, afin de protéger les poussins<strong>du</strong>rant les quatre premières semainesde vie, période critique <strong>du</strong>rant <strong>la</strong>quelleune infection par le virus de <strong>la</strong> ma<strong>la</strong>diede Marek engendre <strong>la</strong> formation ultérieurede tumeurs spécifiques.Particu<strong>la</strong>ritésCette ma<strong>la</strong>die est à déc<strong>la</strong>ration obligatoire.La vaccination doit toujours êtreeffectuée en présence <strong>du</strong> vétérinaireresponsable <strong>du</strong> couvoir.13.1.5.2 Vaccins contre <strong>la</strong> ma<strong>la</strong>diede NewcastleLa vaccination contre <strong>la</strong> ma<strong>la</strong>die deNewcastle (ND) est obligatoire pourtoutes les exploitations de vo<strong>la</strong>illes deplus de 100 animaux. Le responsablede l’exploitation doit faire appel à unvétérinaire agréé pour <strong>la</strong> faire exécuter.Toutes les vo<strong>la</strong>illes (y compris lespigeons, voir chapitre Vaccinationdes pigeons) présentées lors de rassemblements(les expositions, lesconcours et les marchés sont à considérercomme des rassemblements)doivent être vaccinées contre <strong>la</strong> ND.Les vo<strong>la</strong>illes achetées sur les marchésdoivent légalement être ven<strong>du</strong>es avecun certificat de vaccination.La loi prévoit que <strong>la</strong> vaccination doitêtre pratiquée à un âge compris entre10 et 18 jours avec un vaccin de typeLa Sota ou avec un vaccin contenantun clone viral dérivé de cette souche.Cette seule vaccination suffit pour lespoulets de chair alors que les poulespondeuses et repro<strong>du</strong>ctrices sontrevaccinées contre <strong>la</strong> ND <strong>du</strong>rant <strong>la</strong>période d’élevage.VaccinLes vaccins à virus vivants contenantdes souches lentogènes (Hitchner, LaSota et Ulster) sont administrés <strong>du</strong>rant<strong>la</strong> période d’élevage. L’utilisation desvaccins à base de <strong>la</strong> souche La Sotaest exclusivement réservée aux immunisationsde rappel.ProtectionLa <strong>du</strong>rée d’immunité des vaccins à virusvivant est de 6 à 12 semaines. Desvaccinations de rappel sont donc nécessaires<strong>du</strong>rant <strong>la</strong> période d’élevage
25613 VACCINATION DES POULESdes poules destinées à <strong>la</strong> ponte ou à <strong>la</strong>repro<strong>du</strong>ction.Les vaccins à virus inactivés enémulsion huileuse sont utilisés principalementpour <strong>la</strong> revaccination despondeuses et repro<strong>du</strong>ctrices. Cesvaccins sont administrés avant letransfert des poules pondeuses et repro<strong>du</strong>ctricesdans les unités de ponteou de repro<strong>du</strong>ction. Le but de cesvaccinations est double : a) protégerles vo<strong>la</strong>illes <strong>du</strong>rant toute <strong>la</strong> période deponte b) protéger de façon passive lespoussins provenant de vo<strong>la</strong>illes vaccinées<strong>du</strong>rant les premières semaines deleur vie.Les vo<strong>la</strong>illes d’agrément peuventêtre vaccinées au printemps ou enautomne avec un vaccin inactivé, <strong>la</strong><strong>du</strong>rée de protection étant de l’ordred’une année.Particu<strong>la</strong>ritésLa ND est une ma<strong>la</strong>die à déc<strong>la</strong>rationobligatoire assortie d’une politiqued’abattage pour raison sanitaire. Si <strong>la</strong>ND est constatée dans une exploitationavicole, <strong>la</strong> réalisation de <strong>la</strong> vaccinationpréventive obligatoire est l’unedes conditions pour le remboursementdes animaux mis à mort.Depuis le début des vaccinations obligatoires,<strong>la</strong> Belgique n’a plus connu decas de ND chez les vo<strong>la</strong>illes détenuesdans des exploitations avicoles professionnelles.Le dernier cas de NDchez des vo<strong>la</strong>illes détenues par desparticuliers date de 1998. Par contre,les cas de souches spécifiques aupigeon de ND (paramyxovirose) sontfréquents (voir chapitre Vaccinationdes pigeons).13.1.5.3 Vaccins contre <strong>la</strong> bronchiteinfectieuseLa bronchite infectieuse aviaire estcausée par un coronavirus dont il existeplusieurs sérotypes en Belgique :Massachusetts, D274, B1648 et793/B. Le sérotype Massachusetts estle plus répan<strong>du</strong>, justifiant l’immunisationde toutes les vo<strong>la</strong>illes contre cesérotype.VaccinDes vaccins à virus vivants atténuésde <strong>la</strong> bronchite infectieuse sont administrés<strong>du</strong>rant <strong>la</strong> période d’élevage.Ces virus vaccinaux sont atténuéspar passages en série sur des œufsembryonnés. Les vaccins de typeMassachusetts les plus atténués(H120, MA 5) servent à <strong>la</strong> primovaccination,dès l’âge d’un jour, alors queles vaccins moins atténués (H 52) sontréservés à <strong>la</strong> revaccination des poulespondeuses et repro<strong>du</strong>ctrices avantleur transfert dans les unités de ponteou de repro<strong>du</strong>ction.En général, les poulets de chair nesont vaccinés qu’à l’âge d’un jour,mais en cas de nécessité, un rappel devaccination peut éventuellement êtrepratiqué au moyen d’un virus variantde type 4/91 ou de type CR88121 dèsl’âge de 14 jours.Des vaccins inactivés combinéscontenant les valences IB et ND oules valences IB, ND, EDS et rhinotrachéiteaviaire, sont destinés à <strong>la</strong>revaccination des poules pondeuseset repro<strong>du</strong>ctrices. Ils sont administrés4 semaines avant le début de <strong>la</strong> ponteet protègent les vo<strong>la</strong>illes <strong>du</strong>rant toute<strong>la</strong> période de ponte.13.1.5.4 Vaccins contre <strong>la</strong> ma<strong>la</strong>diede GumboroVaccinDes vaccins à virus vivants atténuéscontenant des souches intermédiaires<strong>du</strong> virus de <strong>la</strong> ma<strong>la</strong>die de Gumboro (infectiousbursal disease virus ou IBDV)sont administrés <strong>du</strong>rant <strong>la</strong> périoded’élevage des poules pondeuses etrepro<strong>du</strong>ctrices et des poulets de chair,entre le 10e et le 18e jour d’élevage.Deux vaccins disponibles sur le marchébelge peuvent être utilisés pourvacciner les poulets de chair dès l’âged’un jour, à condition que le taux enanticorps maternels soit suffisammentbas (titre en ELISA < 500).Un vaccin à virus recombinant destinéprincipalement à <strong>la</strong> vaccination despoussins de ponte ou de repro<strong>du</strong>ctionest soit injecté aux poussins à l’âged’un jour, soit inoculé aux embryonsà l’âge de 18 jours. Il contient commesouche vaccinale un herpèsvirus de <strong>la</strong>dinde (HVT) recombinant, exprimantl’antigène protecteur (VP2) <strong>du</strong> virusde <strong>la</strong> bursite infectieuse aviaire (IBDVou ma<strong>la</strong>die de Gumboro), soucheFaragher 52/70. Ce vaccin protègeles vo<strong>la</strong>illes simultanément contre <strong>la</strong>ma<strong>la</strong>die de Gumboro et <strong>la</strong> ma<strong>la</strong>die deMarek.ProtectionLes vaccins contre <strong>la</strong> ma<strong>la</strong>die deGumboro n’in<strong>du</strong>isent aucune immunosuppression;ils causent cependant
13 VACCINATION DES POULES 257une légère atrophie de <strong>la</strong> bourse deFabricius.Particu<strong>la</strong>ritésLe succès de <strong>la</strong> vaccination contre<strong>la</strong> ma<strong>la</strong>die de Gumboro dépend <strong>la</strong>rgement<strong>du</strong> respect des mesuresd’hygiène en matière d’élevage, notammenten ce qui concerne <strong>la</strong> désinfectiondes locaux.13.1.5.5 Vaccins contrel’encéphalomyélite aviaireVaccinLes vaccins doivent nécessairementêtre administrés au moins 4 semainesavant l’entrée en ponte. Seuls des vaccinsà virus vivant atténué sont utilisés.ProtectionLa vaccination des poules-mèresconfère une protection passive auxpoussins.13.1.5.6 Vaccins contre l’arthrite<strong>du</strong>e aux réovirusCes vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.VaccinUn vaccin inactivé en émulsion huileuseest utilisé chez les poulesrepro<strong>du</strong>ctrices.ProtectionLes vaccins protègent passivement lespoussins contre l’arthrite virale.13.1.5.7 Vaccins contre l’anémieinfectieuse viraleVaccinUn vaccin vivant atténué est administréaux poules repro<strong>du</strong>ctrices afind’augmenter leurs taux en anticorpsspécifiques <strong>du</strong> virus CAV et de protégerpassivement les poussins qui ensont issus. Le vaccin est administrépar injection sous-cutanée au moins 6semaines avant l’entrée en ponte.ProtectionLa vaccination confère une protectionpassive aux poussins contre les signescliniques et <strong>la</strong> mortalité <strong>du</strong>s au virus del’anémie infectieuse aviaire.13.1.5.8 Vaccins contre le syndromede <strong>la</strong> chute de ponte (eggdrop syndrome)Ces vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.VaccinCes vaccins à adénovirus inactivéssont associés au vaccin contre <strong>la</strong>ma<strong>la</strong>die de Newcastle, éventuellementen association avec <strong>la</strong> valencecontre <strong>la</strong> bronchite infectieuse et <strong>la</strong>rhinotrachéite.ProtectionIls procurent une immunité d’une <strong>du</strong>réed’un an au moins.13.1.5.9 Vaccins contre <strong>la</strong><strong>la</strong>ryngotrachéite infectieuseCes vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.VaccinCette ma<strong>la</strong>die est à déc<strong>la</strong>ration obligatoire.Les vaccins sont administrés auxpoules pondeuses et repro<strong>du</strong>ctricespar instil<strong>la</strong>tion ocu<strong>la</strong>ire.13.1.5.10 Vaccin contre <strong>la</strong> varioleaviaireCe vaccin est utilisé en fonction de <strong>la</strong>situation épidémiologique.VaccinVaccin pour l’immunisation des pouleset autres vo<strong>la</strong>illes contre <strong>la</strong> varioleaviaire.ProtectionAprès <strong>la</strong> vaccination selon <strong>la</strong> méthodewing-web apparaît un no<strong>du</strong>le dont<strong>la</strong> taille varie d’un grain de riz à celled’un pois. Cette réaction vaccinaleprouve que <strong>la</strong> vaccination est réussie.Les animaux vaccinés à l’âge d’unjour doivent être revaccinés après 12semaines. Lorsque <strong>la</strong> première vaccinations’effectue à l’âge de 7-10semaines, elle entraîne une immunité<strong>du</strong>rable, suffisante pour toute <strong>la</strong> périodede ponte.13.1.5.11 Vaccin contre <strong>la</strong>rhinotrachéiteCes vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.VaccinUn vaccin à virus vivant atténué estrecommandé pour <strong>la</strong> primovaccinationdes futures poules pondeuses etrepro<strong>du</strong>ctrices qui sont revaccinéesavec un vaccin rhinotrachéite inactivéafin de prévenir les symptômes respiratoires,<strong>la</strong> chute de ponte et <strong>la</strong> diminutionde qualité de <strong>la</strong> coquille d’œuf,provoqués par le virus de <strong>la</strong> rhinotrachéiteaviaire (sous-types A et B).Durée de l’immunité après le schémade vaccination complet: 1 période deponte.
25813 VACCINATION DES DINDES, PINTADES, FAISANS, PERDREAUX ET CAILLES13.1.5.12 Vaccins utilisés dans <strong>la</strong>prévention de <strong>la</strong> coccidioseCes vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.VaccinDes vaccins anticoccidiens atténuéssont disponibles. Lors de leur utilisation,ni l’aliment ni l’eau de boissonne pourront contenir de substancesà effet coccidiostatique. Le recyc<strong>la</strong>gedes oocystes vaccinaux est indispensableafin d’assurer le maintien et lerenforcement de l’immunité in<strong>du</strong>ite.Par ailleurs, l’index thérapeutique deces vaccins est re<strong>la</strong>tivement faible. Encas de surdosage accidentel (10 fois<strong>la</strong> dose et plus), on pourra administrerdans l’aliment ou l’eau de boisson uncoccidiostatique pour éviter l’apparitionde coccidiose clinique. La vaccinationcontre <strong>la</strong> ma<strong>la</strong>die de Gumboro,<strong>la</strong> ma<strong>la</strong>die de Newcastle et <strong>la</strong> bronchiteinfectieuse peut être réaliséesimultanément. Cependant, l’activitéantivirale des excipients n’ayant pasété vérifiée, il faut éviter d’administrerces vaccins ensemble dans l’eau deboisson.Particu<strong>la</strong>ritésPour éviter l’exposition des nouveauxanimaux à une infection sévère (d’originenaturelle), les locaux d’élevageseront vidés, nettoyés et désinfectésentre chaque lot de poussins.13.1.5.13 Vaccins contre <strong>la</strong>salmonelloseLa vaccination des poules pondeusesest une obligation légale (voir aussi l’AR<strong>du</strong> 27 avril 2007 re<strong>la</strong>tif à <strong>la</strong> lutte contreles Salmonelles chez les vo<strong>la</strong>illes).13.1.5.14 Vaccins contre d’autresinfections bactériennesCes vaccins sont utilisés en fonctionde <strong>la</strong> situation épidémiologique.Ils peuvent être utilisés pour prévenirles ma<strong>la</strong>dies <strong>du</strong>es aux infectionsà E. coli ou Mycop<strong>la</strong>sma gallisepticum.Les poules-mères de poulets dechair peuvent être vaccinées contreOrnithobacterium rhinotracheale sérotypeA afin de protéger les poulets dechair.Tableau: schéma c<strong>la</strong>ssique de vaccination des vo<strong>la</strong>illesAgeVoied’administrationPondeusesPoulets dechairPoulets dechair <strong>la</strong>bel1 jour IM Marek Marek MarekSpray NewcastleBronchiteNewcastleBronchiteNewcastleBronchiteNewcastleBronchite2 à 4sem7 à 12sem14 à 18semEau de boissonou aérosolEau de boissonou aérosolEau de boissonou aérosolRepro<strong>du</strong>ctricesNewcastleGumboroNewcastleBronchiteEncéphalomyéliteNewcastleNewcastleGumboroNewcastleBronchiteEncéphalomyéliteNewcastleIM Newcastle NewcastleNewcastleGumboro13.1.6 Vaccination des dindes, pintades, faisans, perdreaux et caillesNewcastleGumboro13.1.6.1 Vaccination contre <strong>la</strong>ma<strong>la</strong>die de NewcastleToutes les vo<strong>la</strong>illes (y compris lespigeons, voir chapitre Vaccinationdes pigeons) présentées lors de rassemblements(les expositions, lesconcours et les marchés sont à considérercomme des rassemblements)doivent être vaccinées contre <strong>la</strong> ma<strong>la</strong>diede Newcastle. La vaccination doitêtre exécutée par un vétérinaire agréé.La vaccination doit être pratiquée à unâge compris entre 10 et 18 jours avecun vaccin de type La Sota ou avec unvaccin contenant un clone viral dérivéde cette souche. Les vo<strong>la</strong>illes achetéessur les marchés doivent légalementêtre ven<strong>du</strong>es avec un certificatde vaccination.Voir aussi 13.1.5.2 Vaccins contre <strong>la</strong>ma<strong>la</strong>die de Newcastle
13 VACCINATION DES DINDES, PINTADES, FAISANS, PERDREAUX ET CAILLES 259Dindes destinées à <strong>la</strong>consommationLa primovaccination est effectuée àl’âge d’un jour avec un vaccin vivantde type La Sota, administré par nébulisationà raison de 2 doses vaccinalespar animal. Des rappels de vaccinationsont effectués à l’âge de 3 et 10semaines avec les mêmes vaccins,administrés soit par nébulisation, soitdans l’eau de boisson.Dindes de chair et de repro<strong>du</strong>ctionLa primovaccination est effectuée àl’âge de 10 à 18 jours avec un vaccinvivant de type La Sota, administré parnébulisation ou dans l’eau de boissonà raison de 2 doses vaccinales par animal.Des rappels de vaccination sonteffectués à l’âge de 8 à 10 semaineset à 17 semaines avec les mêmes vaccinsadministrés soit par nébulisationsoit dans l’eau de boisson. Avant l’entréeen ponte, à l’âge de 27 semaines,les vo<strong>la</strong>illes sont revaccinées avec unvaccin inactivé administré par voiesous-cutanée.Pintades destinées à <strong>la</strong>consommationLa primovaccination est effectuée àl’âge de 14 à 21 jours avec un vaccinvivant de type La Sota, administré parnébulisation ou dans l’eau de boisson.Un rappel de vaccination est effectuéà l’âge de 7 à 9 semaines avecles mêmes vaccins administrés soitpar nébulisation, soit dans l’eau deboisson.Pintades de chair et derepro<strong>du</strong>ctionLa primovaccination est effectuée àl’âge de 14 à 21 jours avec un vaccinvivant de type La Sota, administrésoit par nébulisation soit dans l’eaude boisson. Des rappels de vaccinationsont effectués à l’âge de 10 à12 semaines et de 17 à 18 semainesavec les mêmes vaccins, administréssoit par nébulisation soit dans l’eaude boisson. Avant l’entrée en ponte, àl’âge de 28 semaines, les vo<strong>la</strong>illes sontrevaccinées avec un vaccin inactivéadministré par voie sous-cutanée.Remarque : les vaccinations par nébulisationdoivent obligatoirementêtre effectuées en maintenant le locald’élevage dans l’obscurité afin d’éviterles mouvements de panique générateursde mortalité par étouffement.Faisans et perdreaux destinés à <strong>la</strong>consommationLa primovaccination est effectuée àl’âge de 14 à 21 jours avec un vaccinvivant de type La Sota, administrédans l’eau de boisson. Un rappel devaccination est effectué à l’âge de 8 à10 semaines avec les mêmes vaccins,administrés dans l’eau de boisson.Faisans et perdreaux de chair et derepro<strong>du</strong>ctionLa primovaccination est effectuée àl’âge de 14 à 21 jours avec un vaccinvivant de type La Sota, administrédans l’eau de boisson. Un rappel devaccination est effectué à l’âge de 8 à10 semaines avec les mêmes vaccins,administrés dans l’eau de boisson.Un dernier rappel de vaccination esteffectué à l’âge de 18 à 20 semainespar voie sous-cutanée avec un vaccininactivé.Attention, les faisans et les perdreauxsont particulièrement sensibles à <strong>la</strong>souche Hitchner <strong>du</strong> virus de <strong>la</strong> ma<strong>la</strong>diede Newcastle. Les vaccins contenantce virus ne doivent jamais être utiliséspour ces espèces.Cailles de chair et de repro<strong>du</strong>ctionLa vaccination est effectuée à l’âge de5 à 6 semaines avec un vaccin inactivéinjecté par voie intramuscu<strong>la</strong>ire àraison de 0,25 ml (aiguille de 0,6 mmde diamètre) dans les muscles <strong>du</strong>bréchet.Remarque : l’utilisation de vaccins àvirus vivants n’est pas indiquée.13.1.6.2 Vaccin contre <strong>la</strong>rhinotrachéite aviaireinfectieuseDindes de chair et de repro<strong>du</strong>ctionLa rhinotrachéite infectieuse de <strong>la</strong>dinde est causée par un pneumovirusaviaire. Il existe des vaccins à virus vivantatténué destinés à prévenir cetteaffection. Ces vaccins sont administréspar nébulisation.
26013 VACCINATION DES PIGEONS13.1.7 Vaccination des pigeons13.1.7.1 Vaccins contre <strong>la</strong>ma<strong>la</strong>die de Newcastle(Paramyxovirose)Voir aussi 13.1.5.2 Vaccins contre <strong>la</strong>ma<strong>la</strong>die de NewcastleLa vaccination de pigeons qui participentà des concours et expositionsest obligatoire (AR <strong>du</strong> 28/11/1994). Leschéma recommandé est le suivant:- Vaccination de début d’année,avant <strong>la</strong> saison des concours: tousles pigeons de plus de 5 semaines, ycompris les pigeons a<strong>du</strong>ltes vaccinésl’année précédente, sont vaccinésavec un vaccin inactivé en émulsionaqueuse ou huileuse.- Vaccination <strong>du</strong>rant <strong>la</strong> saison desconcours: tous les pigeons nés <strong>du</strong>rant<strong>la</strong> période des concours seront vaccinésdès l’âge de 5 semaines avec unvaccin inactivé en émulsion aqueuseou huileuse.Remarque : il est essentiel que <strong>la</strong> quantitéde vaccin injectée soit correcte.L’injection doit être pratiquée par voiesous-cutanée dans <strong>la</strong> région <strong>du</strong> cou,l’aiguille étant intro<strong>du</strong>ite parallèlementà <strong>la</strong> colonne cervicale en direction <strong>du</strong>dos et pas trop près de <strong>la</strong> nuque.En Belgique, les cas de Newcastle disease(paramyxovirose) sont fréquentschez les pigeons. Le médecin vétérinaire(agréé) qui se charge des vaccinationsdoit veiller à ce que tous lesoiseaux <strong>du</strong> pigeonnier soient vaccinéset revaccinés de manière adéquate.13.1.8 Vaccination des canaris et des pinsons13.1.8.1 Vaccin contre <strong>la</strong> variole <strong>du</strong>canariVacciner au mois de juin tous les oiseauxde plus de 4 semaines avec unvaccin vivant atténué injecté dans <strong>la</strong>membrane de l’aile. Vacciner chaqueoiseau tous les ans, au moment où lesplus jeunes sont âgés de 4 semaines,mais au plus tard à <strong>la</strong> mi-juillet.13.1.9 Liste des spécialités disponiblesVaccins antiviraux pour vo<strong>la</strong>ille Vaccins contre <strong>la</strong> ma<strong>la</strong>die deMarekNOBILIS RISMAVAC (MSD A.H.)virus de <strong>la</strong> ma<strong>la</strong>die de Marek cellu<strong>la</strong>ire (CVI988): min 1000 DICT50/dosevaccin injectable imPosologie:poussin d’un jour: 1 dose (0,2 ml)/animalOOI: 9 jDOI: pas d’infoTemps d’attente: 0 jampoule 1000 dosesR/iNOBILIS RISMAVAC + CA 126 (MSD A.H.)par dose:virus de <strong>la</strong> ma<strong>la</strong>die de Marek att (souche CVI988): min 3,0 log10 pfuherpèsvirus de <strong>la</strong> dinde att (souche FC 126):min 3,0 log10 pfususpension cellu<strong>la</strong>ire congelée et solvant pourvaccin injectable sc, im, in ovoPosologie:poussin d’un jour, embryons (âge 18 j):1 dose par animalOOI: 5 jDOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 12000 doses et 400 ml de solvantR/i
13 VACCINS POUR VOLAILLE261POULVAC MAREK H.V.T. (Pfizer A.H.)virus de <strong>la</strong> ma<strong>la</strong>die de Marek (HVT, FC 126):1000 UFP/dosevaccin lyophilisé injectable im, scPosologie:poussin d’un jour:1 dose (0,2 ml)/animalOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 doses + 200 ml de solvantR/i Vaccins contre <strong>la</strong> ma<strong>la</strong>die deNewcastleAVINEW (Merial)par dose:virus viv de <strong>la</strong> ma<strong>la</strong>die de Newcastle (soucheVG/GA): min 5,5 log10 DIO50vaccin lyophilisé voie ocu<strong>la</strong>ire ou oculo-nasale,poPosologie:Primovac:- poule de chair (dès l’âge d’1 j): 1 dose/animal (voie ocu<strong>la</strong>ire ou oculo-nas)Revac:âge: 2 - 3 sem (po) (min 2 sem entre les2 vac)- poule future pondeuse et future reprod:2 x 1 dose/animal à l’âge de 4 sem et 8 sem(voie ocu<strong>la</strong>ire, oculo-nas ou po)Revac avec vac inact avant début de ponteOOI: 14 après vac de base, DOI: jusqu’à 6 semd’âgeTemps d’attente: 0 jf<strong>la</strong>con 2000 dosesR/iAVIPRO ND C131 (Lohmann A.H.)virus viv de <strong>la</strong> ma<strong>la</strong>die de Newcastle (Clone131): min 10 exp6 - max 10 exp7,2 DIE50/dosevaccin lyophilisé po (via l’eau de boisson), intraocu<strong>la</strong>ire,sprayPosologie:dès l’âge de 14 jpoulet de chair: 1 dose/animalpoule pondeuse, poulet de repro<strong>du</strong>ction:2 x 1 dose/animal à 4 sem d’intervallepoulet de chairOOI:3 sem après vac (7 j chez les pouletsséronégatifs) - DOI: 4 sem après vacpoule pondeuse/repro<strong>du</strong>ct:OOI: 3 sem après 1e vacDOI: 9 sem après schéma de vac completTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000, 10 x 2500, 10 x 5000 dosesR/iHIPRAVIAR-NDV CLON (Hipra Lab)virus viv de <strong>la</strong> ma<strong>la</strong>die de Newcastle (CloneCL/79): min 10exp 6,5 EID50/dosevaccin lyophilisé po, nébulisation, instill.oculo-nasalePosologie:poulet (de chair) (âge > 1 j):2 x 1 dose, 2e après l’âge de 14 jOOI: pas d’info, DOI: 6 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosissen, 10 x 5000 dosesR/iNOBILIS ND C2 (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Newcastle (C2):min 5,7 - max 7,5 log10 EID50/dosevaccin lyophilisé instill nasale et ocu<strong>la</strong>ire,vaporisationPosologie:poule (âge 1 j): 1 dose/anima<strong>la</strong>près 2 - 3 sem vac avec souche Clone 30animaux séronégatifs:OOI: 2 semDOI: 5 semanimaux avec imm mat:OOI: 2 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 2500 ou 1 x 10.000 dosesR/iNOBILIS ND CLONE 30 (MSD A.H.)virus viv de <strong>la</strong> ma<strong>la</strong>die de Newcastle (clone 30):10exp 6 EID50/dosevaccin lyophilisé dans l’eau de boisson, parvoie oculo-nasale ou sprayPosologie:poulette de chair:(âge > 1 j): 1 dose/animal méthode spray,intranas ou intraocul(âge > ou = 7 j): 1 dose/animal dans l’eaude boissonRevac: après 2-3 sem méthode avec l’eaude boisson, spray, intranas ou intraoculpoules pondeuses, anim d’élevage, pouletsdestinés à <strong>la</strong> reprod: 1 dose/animal méthodespray, intranas ou intraoculRevac: après 5-6 sem méthode avec l’eaude boisson, spray, intranas ou intraoculOOI: 3 sem, DOI: 6 semViande: 0 j, Oeuf: 0 jf<strong>la</strong>con 10 x 1000 doses10 x 2500 dosesR/iNOBILIS NEWCAVAC (MSD A.H.)virus inact de <strong>la</strong> ma<strong>la</strong>die de Newcastle (Clone30): min 50 PD50/mlAdjuv: paraffine liquidevaccin injectable im (pas chez les poulets dechair), scPosologie:poule: 0,5 ml/animalpoules pondeuses: ne pas vac le jour de <strong>la</strong>vac Marek ou <strong>du</strong> sexageOOI: 3 sem après vacDOI: 1 période de ponteViande: 0 jNe pas utiliser pendant <strong>la</strong> ponte ou pendant les4 sem avant le début de <strong>la</strong> pontef<strong>la</strong>con 12 x 1000 doses (500 ml)R/iPOULVAC ND HITCHNER B1 (Pfizer A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Newcastle (soucheHitchner B1): 10exp 5,5 EID50/dosevaccin lyophilisé po dans l’eau de boisson, nébulisationou pulvérisation, instill. oculo-nasalePosologie:poule: 1 dose/animalen cas d’imm mat: 2e vac avec Poulvac NDLasota®OOI: 21 j après vacDOI: min 6 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 5000 dosesR/i
262 13 VACCINS POUR VOLAILLEPOULVAC ND LA SOTA (Pfizer A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Newcastle (souche LaSota): 10exp 5,5 EID50/dosevaccin lyophilisé po dans l’eau de boisson, nébulisationou pulvérisation, instill oculo-nasalePosologie:Primovac: avec Poulvac ND Hitchner B1®poule pondeuse: avant <strong>la</strong> ponte, vac avecPoulvac ND Lasota®OOI: 21 j, DOI: min 6 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 2500 dosesR/i Vaccins contre <strong>la</strong> bronchiteinfectieuseSérotype MassachusettsNOBILIS IB MA 5 (MSD A.H.)virus att de <strong>la</strong> bronchite infectieuse (Ma 5):min 10exp 3 log EID50/dosevaccin lyophilisé méthode de vaporisation, inas,intra-ocu<strong>la</strong>ire et eau de boissonPosologie:poule: 1 dose/animalnébulisation, voie oculo-nasale: dès l’âged’1 jeau de boisson: âge > 14 jIn<strong>du</strong>it une protection partielle contre lesérotype D274OOI: 3 sem, DOI: 6 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 2500 doses, 1 x 10 000 dosesR/POULVAC IB H 120 (Pfizer A.H.)virus de <strong>la</strong> bronchite infectieuse, soucheMassachusetts: min 10exp 3 EID50/dosevaccin lyophilisé eau de boisson, nébulisation,instill. oculo-nasalePosologie:poulette de chair (âge 1 j), poule pondeuse(âge 1 j ou 4 sem): 1 dose/animalpoule pondeuse: 2e vac à l’âge de 12 - 16semOOI: 25 j, DOI: 16 semtemps d’attente: 0 jf<strong>la</strong>con 10 x 5000 dosesR/POULVAC IB PRIMER (Pfizer A.H.)virus att de <strong>la</strong> bronchite infectieusesouche Massachusetts H 120:min 10exp 3 EID50/dosesouche D274 clone: min 10exp 3 EID50/dosevaccin lyophilisé sprayPosologie:poule de chair (âge 1 j):1/2 dosepoule pondeuse ou reprod:(âge 1 j ou 4 sem): 1/2 dose (âge 1 j) ou1 dose (âge > 1 j)(âge 15 - 16 sem): 2e vac avec vac inactOOI: 21 j, DOI: 16 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 5000 dosesR/Sérotype Massachusetts +ArkansasPOULVAC IBMM + ARK (Pfizer A.H.)virus de <strong>la</strong> bronchite infectieuse, soucheMassachusetts 1263 et Arkansas 3168:min 10 exp3,3 EID50/dosevaccin lyophilisé sprayPosologie:poussin (dès l’âge d’1 j):1 dose (0,5 ml)/animalOOI: 3 sem après vac, DOI: 6 sem après vacTemps d’attente: 0 jf<strong>la</strong>con 10 x 5000 dosesR/Sérotype CR88121GALLIVAC IB 88 (Merial)virus att de <strong>la</strong> bronchite infectieuse (CR88121):min 4 log10 DIO50/dosevaccin lyophilisé pour nébulisationPosologie:poussin (âge > 14 j): 1 dose/animalOOI: 3 sem après vacDOI: min 5 sem après vacTemps d’attente: 0 jf<strong>la</strong>con 2000 dosesR/Sérotype 4 – 91NOBILIS IB 4 - 91 (MSD A.H.)virus att de <strong>la</strong> bronchite infectieuse (4-91):min 3,6 log10 EID50/dosevaccin lyophilisé méthode de pulvérisation,instill. oculo-nasale, eau de boissonPosologie:Primovac:1 dose/animalpoulet de chairâge > 1 j: pulvérisation ou instil<strong>la</strong>tionâge > 7 j: eau de boissonfutures pondeuses et repro<strong>du</strong>ctrices (âge> 3 sem) : pulvérisation, instil<strong>la</strong>tion ou eaude boissonRevac: 1 dose/6 semOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 ou 10 x 5000 dosesR/ Vaccin contre l’encéphalomyéliteaviairePOULVAC AE (Pfizer A.H.)virus de l’encéphalomyélite aviaire (AE-67):min 10exp 3,1 EID50/dosevaccin lyophilisé po dans l’eau de boissonPosologie:Primovac:poule (âge > 10 sem): 1 dose/animal 4 semmin avant <strong>la</strong> période de ponteOOI: pas d’infoDOI: transmet l’immunité jusque 12 m après<strong>la</strong> vacTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosesR/
13 VACCINS POUR VOLAILLE263 Vaccin contre <strong>la</strong> ma<strong>la</strong>die deMarek – ma<strong>la</strong>die de GumboroVAXXITEK HVT + IBD (Merial)virus viv recombinant vHVT013-69:3,6 log10 UFP/dosevaccin injectable sc, in ovoPosologie:poussin âge 1 j: 1 x 0,2 ml (sc)/animaloeuf embryonné âge 18 j:1 x 0,05 (in ovo)/œufGumboro: OOI: 2 sem après vac, DOI: jusqu’à9 semMarek: OOI: dès le 4e j, DOI: vac protège enpériode de risqueTemps d’attente: 0 jampoule 5 x 1000 dosesR/ Vaccin bivalent : ma<strong>la</strong>die deNewcastle – bronchite infectieuseNOBILIS IB MULTI + ND (MSD A.H.)virus inact de <strong>la</strong> bronchite infectieuse:M41: min 5,5 log2 VN U/doseD274: min 4 log2 VN U/dosevirus inact de <strong>la</strong> ma<strong>la</strong>die de Newcastle clone 30:min 50 PD50/doseadjuv: eau dans l’huilevaccin injectable sc, imPosologie:poule pondeuse, reprod (âge 14 - 18 sem):0,5 ml/animal (min 3 sem avant <strong>la</strong> ponte)Ce vac est administré min 4 sem après unevac avec un vaccin BI viv. attOOI: 4 sem après vacDOI: 1 période de ponteViande: 0 jf<strong>la</strong>con 1000 doses (500 ml)R/i Vaccin bivalent : ma<strong>la</strong>die deNewcastle – syndrome de <strong>la</strong>chute de ponteNOBILIS ND + EDS (MSD A.H.)virus inact de <strong>la</strong> ma<strong>la</strong>die de Newcastle (soucheClone 30): min 50 PD50/dosevirus inact <strong>du</strong> Egg Drop Syndrome (soucheBC14): min 6,5 log2 U-HI/doseadjuv: eau dans l’huilevaccin injectable im, scPosologie:poule pondeuse, reprod (âge 16 - 20 sem):1 dose (0,5 ml)/animal, 4 sem min avant<strong>la</strong> ponteIl est indispensable de prévac avec un vacND attOOI: non déterminéDOI: 1 période de ponteViande: 0 j, Oeuf: 0 jf<strong>la</strong>con 12 x 1000 doses (500 ml)R/i Vaccin associant <strong>la</strong> ma<strong>la</strong>die deNewcastle, le syndrome de <strong>la</strong>chute de ponte, <strong>la</strong> rhinotrachéiteinfectieuse aviaire et <strong>la</strong> bronchiteinfectieuseNOBILIS RT+ IBmulti + ND + EDS (MSD A.H.)par dose (0,5 ml) antigènes inact <strong>du</strong>:virus de <strong>la</strong> bronchite infectieuse, souche M41:min 5,5 log exp2 VN Uvirus de <strong>la</strong> bronchite infectieuse, souche 249g:min 4 log exp2 VN Uvirus de <strong>la</strong> rhinotrachéite aviaire, soucheBut1#8544: min 9,5 log exp2 U Elisavirus Egg Drop Syndrome ‘76, souche BC14:min 6,5 log exp2 U HIvirus de <strong>la</strong> ma<strong>la</strong>die de Newcastle, souche Clone30: 50 PD50Adjuv: paraffine liquidevaccin injectable imPosologie:poule reprod, poule pondeuse: âge 14 - 20sem: 0,5 ml/animalne pas admin pendant <strong>la</strong> ponte ni dans les 4sem avant le début de <strong>la</strong> ponteOOI: 4 sem après vacDOI: 1 période de ponteTemps d’attente: 0 jf<strong>la</strong>con 500 ml (1000 doses)R/ Vaccins contre <strong>la</strong> ma<strong>la</strong>die deGumboroAVIPRO GUMBORO VAC (Lohmann A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Gumboro (Cu-1M):min 2 log10, max 3,7 log10 EID50/dosevaccin lyophilisé dans l’eau de boissonPosologie:poulette de chair: 1 dose/animalimm mat basse: âge > 7 jimm mat élevée: âge > 14 jpoule pondeuse ou reprod: (âge 3 - 4 sem):1 dose/animal, de préférence 2e vac après3 - 7 jLes vaccins contre ND et BI peuvent êtreadministrés simultanémentAucun autre vac ne sera administré dans les14 j avant et après l’admin de ce vacOOI: 3 semDOI: min 14 sem après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000, 10 x 5000 ou 10 x 10 000dosesR/AVIPRO PRECISE (Lohmann A.H.)virus viv de <strong>la</strong> ma<strong>la</strong>die Gumboro (souche LC75): min 10 exp3 - max 10 exp4,5 EID50/dosevaccin lyophilisé po avec l’eau de boissonPosologie:poule: 1 dose/animalpoulets de chair:sans anticorps mat: âge > 7 j,avec anticorps mat: 14 jpoules pondeuses et poulets repro<strong>du</strong>cteurs:sans anticorps mat: âge > 7 j,avec anticorps: âge 3-4 semOOI: 14 jDOI: 28 jTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000, 5000 ou 10 000 dosesR/
264 13 VACCINS POUR VOLAILLEHIPRAGUMBORO CW (Hipra Lab)virus viv de <strong>la</strong> bursite infectieuse, soucheCH/80: 10exp3,5 - 10exp5,5 CCID50vaccin lyophilisé pour suspension po avec l’eaude boissonPosologie:calculer le moment approprié pour <strong>la</strong> vac(cf RCP)poulets de chair: 1 dose/animal avec l’eaude boissonOOI: 14 j après vac, DOI: 30 j après vacTemps d’attente: 0 jf<strong>la</strong>con 1000 doses, 10 x 5000 doses, 10 x10000 dosesR/HIPRAGUMBORO-GM97 (Hipra Lab)virus viv de <strong>la</strong> ma<strong>la</strong>die Gumboro (soucheGM97): min 10 exp2 - 10 exp3 EID50/dosevaccin lyophilisé pour suspension po avec l’eaude boissonPosologie:poule de chair (âge > 1 j): 1 dose/animall’âge de <strong>la</strong> vac dépend <strong>du</strong> titre d’Ac à l’âgede 1 j (titre ELISA de 500 ou moins)OOI: 14 j après vacDOI: 43 j après vacTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 doses, 10 x 5000 dosesR/NOBILIS GUMBORO D 78 (MSD A.H.)virus de <strong>la</strong> ma<strong>la</strong>die de Gumboro (D78):min 10exp 4 DICT50/dosevaccin lyophilisé méthode de pulvérisation,instill. oculo-nasale, eau de boissonPosologie:poussin (âge 14 - 21 j): 1 dose/animal(poussin sans imm mat âge: 8 j)au plus tard 4 sem avant <strong>la</strong> période deponteOOI: 6-7 j, DOI: 31 jTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 doses, 10 x 2500 doses, 10 x10.000 dosesR/POULVAC BURSA PLUS (Pfizer A.H.)virus viv de <strong>la</strong> bursite infectieuse (souche V877):10exp2,2 - 10exp3,4 EID50/dosevaccin lyophilisé po dans l’eau de boissonPosologie:poussin (âge > 10 j): 1dose/animalOOI: 14 j après vac, DOI: 32 jTemps d’attente: 0 jf<strong>la</strong>con 10 x 2000 doses, 10 x 5000 dosesR/POULVAC BURSINE 2 (Pfizer A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Gumboro (Lukert):min 10exp 4,3 DICT50/dosevaccin lyophilisé eau de boissonPosologie:imm mat basse:poussin (âge > 14 j): 1 dose/animalimm mat élevée:poussin: 2 x 1 dose (à l’âge de 14 j et à l’âgede 21 - 28 j)OOI-DOI: pas d’infoViande, Oeuf: 0 jf<strong>la</strong>con 10 x 1000, 10 x 5000 dosesR/ Vaccins contre l’arthrite <strong>du</strong>e auréovirusNOBILIS REO ERS INAC (MSD A.H.)antigène ERS <strong>du</strong> réovirus inact: min 6,7 log2 etmax 10,0 log2 U ELISAadjuv: paraffine liquidevaccin injectable imPosologie:poule (âge > 7 sem, max 4 sem avant entréeen ponte): 2 x 1 dose (0,5 ml)/animal à 11sem d’intervalleOOI: 4 sem après 2 vacDOI: 47 sem après 2 vacTemps d’attente: 0 jf<strong>la</strong>con 500 mlR/NOBILIS REO INAC (MSD A.H.)réovirus (1733 + 2408) inact: min 7,4 log2 UELISA/doseadjuv: paraffine liquidevaccin injectable sc, imPosologie:vo<strong>la</strong>ille (âge 16 - 20 sem): 1 dose (0,5 ml)/animal (4 sem min avant <strong>la</strong> ponte)Prévacciner avec Nobilis Reo 1133, 4-6 semavant <strong>la</strong> vaccination-booster avec le vaccininactivéOOI-DOI: pas d’infoTemps d’attente: 0 jf<strong>la</strong>con 1000 doses (500 ml)R/ Vaccins contre l’anémieinfectieuse virale aviaireAVIPRO THYMOVAC (Lohmann A.H.)anémie infectieuse virale (CAV), souche Cux-1,att: min 10exp 4,5 - max 10exp 5,5 TCID50/dosevaccin lyophilisé po dans l’eau de boissonPosologie:poulet reprod (âge > 8 sem): 1 dose (min 6sem avant début de ponte)OOI imm active: 4 semDOI: imm active: 43 semOOI imm passive: à partir de l’âge d’1 jTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosesR/NOBILIS CAV P4 (MSD A.H.)chicken anaemia virus (26P4) att:min 10exp 3 DICT50/dosevaccin lyophilisé et solvant injectable im, sc(solvant di<strong>la</strong>via), méthode “wing web” (solvantunisolve)Posologie:poule de reprod (âge > 6 sem): 1 x 1 dosevac jusqu’à au plus tard 6 sem avant <strong>la</strong>ponteOOI-DOI: pas d’infoViande: 0 j, Oeuf: 0 jf<strong>la</strong>con 10 x 1000 dosesR/
13 VACCINS POUR VOLAILLE265 Vaccins contre <strong>la</strong><strong>la</strong>ryngotrachéite infectieuseaviaireNOBILIS ILT (MSD A.H.)virus att de <strong>la</strong> <strong>la</strong>ryngo-trachéite infectieuse(souche Serva): min 10exp 2,5 EID50/dosevaccin lyophilisé instill ocu<strong>la</strong>irePosologie:poule (âge 6 sem): 1 goutte/animalOOI: 3 sem, DOI: pas d’infoViande: 0 jf<strong>la</strong>con 1000 doses, 2500 dosesR/iPOULVAC ILT (Pfizer A.H.)virus att de <strong>la</strong> <strong>la</strong>ryngo-trachéite infectieuse(Salsbury 146): 10exp 2,5 EID50/dosevaccin lyophilisé instill ocu<strong>la</strong>irePosologie:poule (âge > 4 sem): 1 goutte/animalOOI: 14 j, DOI: non connuTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosesR/i Vaccin contre <strong>la</strong> variole aviairePOULVAC CHICK-N-POX TC (Pfizer A.H.)virus att de <strong>la</strong> variole aviaire (souche 946):min 10exp 3 EID50/dosevaccin lyophilisé injectable méthode “wing web”Posologie:poule, vo<strong>la</strong>ille: 1 dose/animalpoussin (1 j): 1 dose/animal, repéter après12 semOOI: 1 j après vac, DOI: 12 sem (vac à l’ âge 1 j),toute <strong>la</strong> période de ponte (vac à l’ âge 7-10 sem)Temps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosesR/ Vaccins contre le virus de <strong>la</strong>rhinotrachéiteNOBILIS RHINO CV (MSD A.H.)virus att de <strong>la</strong> rhinotrachéite aviaire, souche TRT11/94: min 10exp1.5 DICT50 et max 10exp3.7DICT50/dosevaccin lyophilisé à usage oculo-nasal ou sprayPosologie:Av (âge > 1 j): 1 dose/animalOOI: 3 sem après vac, DOI: 16 sem après vacTemps d’attente: 0 jNe pas utiliser chez des animaux en cours deponte ou dans les 4 sem précédant le débutde <strong>la</strong> pontef<strong>la</strong>con 10 x 1000 doses, 10 x 5000 dosesR/NOBILIS RTV 8544 (MSD A.H.)virus att de <strong>la</strong> rhinotrachéite de <strong>la</strong> dinde (BUT#8544): min 10exp 3 CCID50/dosevaccin lyophilisé spray, instill oculo-nasalePosologie:poule: 1 dose/animalOOI: pas d’infoDOI: 1 période de ponteTemps d’attente: 0 jf<strong>la</strong>con 10 x 1000 dosesR/POULVAC TRT (Pfizer A.H.)virus att de <strong>la</strong> rhinotrachéite de <strong>la</strong> dinde (cloneK): min 10exp 3,2 CCID50 et max 10exp 4,5CCID50/dosevaccin lyophilisé pour solution pour instill oculonasaleou sprayPosologie:dinde (âge 1 j): 1 dose/animalOOI: 3 sem après vacDOI: 14 semTemps d’attente: 0 jf<strong>la</strong>con 10 x 2000 dosesR/Vaccins antiparasitaires pourvo<strong>la</strong>ille Vaccins contre <strong>la</strong> coccidioseHIPRACOX (Hipra Lab)Eimeria acervulina, souche 003:300 - 390 oocystes/doseEimeria maxima, souche 013:200 - 260 oocystes/doseEimeria mitis, souche 006:300 - 390 oocystes/doseEimeria praecox, souche 007:300 - 390 oocystes/doseEimeria tenel<strong>la</strong>, souche 004:250 - 325 oocystes/dosevaccin po, par pulvérisationPosologie:poulet de chair (âge 1 j):1 dose (0,007 ml)/animalOOI: 14 j après vac, DOI: min 28 jTemps d’attente: 0 jf<strong>la</strong>con 1000 doses + 20 ml de colorant ou5000 doses + 100 ml de colorantR/PARACOX (MSD A.H.)E. acervulina HP: 500 oocystes/dose (0,1 ml)E. brunetti HP: 100 oocystes/doseE. maxima CP: 200 oocystes/doseE. maxima MFP: 100 oocystes/doseE. mitis: 1000 oocystes/doseE. necatrix HP: 500 oocystes/doseE. praecox HP: 100 oocystes/doseE. tenel<strong>la</strong> HP: 500 oocystes/dosevaccin po dans l’eau de boissonPosologie:poussin (âge 5 - 9 j): 1 dose (0,1 ml)OOI: 10 jDOI: min 36 sem si élevés sur une litièreTemps d’attente: 0 jsachets 1000 doses, 5000 dosesR/PARACOX-5 (MSD A.H.)E. acervulina HP: 500 - 650 oocystes/doseE. maxima CP: 200 - 260 oocystes/doseE. maxima MFP: 100 - 130 oocystes/doseE. mitis HP: 1000 - 1300 oocystes/doseE. tenel<strong>la</strong> HP: 500 - 650 oocystes/dosevaccin po avec l’alimentation ou en spray(poussin 1 j), dans l’eau de boisson (poussin 3 j)Posologie:poussin (âge 1 - 3 j): 1 dose/animalOOI: 14 j, DOI: 40 jTemps d’attente: 0 jf<strong>la</strong>con 5 x 1000 doses (4 ml)R/
266 13 VACCINS POUR VOLAILLEVaccins antibactériens pour vo<strong>la</strong>ille Vaccin contre E. coliNOBILIS E. COLI (MSD A.H.)par dose, Ag d’E. coli:F11: 68,3 mgFT: 68,3 mgadjuv: paraffine liquidevaccin injectable sc, imPosologie:poule (âge 6 - 12 sem): 2 x 1 dose (0,5 ml)/animal, à 6 sem d’intervalle minDOI: Imm passive partielle pendant les 7premières sem de <strong>la</strong> vieViande: 35 j, Oeuf: 0 jf<strong>la</strong>con 1000 doses (500 ml)R/POULVAC E. COLI (Pfizer A.H.)Escherichia coli viv type O78, délété <strong>du</strong> gènearoA (souche EC34195):5,2 x 10 exp6 à 9,1 x 10 exp8 UFCvaccin lyophilisé pour suspension pournébulisationPosologie:poule: 1 dose dès l’âge de 1 jOOI: ré<strong>du</strong>ction lésions: 2 sem après vac,ré<strong>du</strong>ction mortalité: pas d’infoDOI: ré<strong>du</strong>ction lésions: 8 sem après vac,ré<strong>du</strong>ction mortalité: 12 sem après vacTemps d’attente: 0 jf<strong>la</strong>con 10 x 2500 doses, 10 x 5000 dosesR/ Vaccins contre Salmonel<strong>la</strong>AVIPRO SALMONELLA DUO (Lohmann A.H.)Salmonel<strong>la</strong> enteritidis (souche Sm24/Rif12/Ssq),att: min 1 x 10exp 6 x 108 KVESalmonel<strong>la</strong> typhimurium (souche Nal2/Rif9/Rtt),att: min 1 x 10exp 6 x 108 KVEvaccin lyophilisé po avec l’eau de boissonPosologie:poule (âge 1 j): 1 dose/animal, 2e dose à 6-8sem, 3e dose à 16 sem (min 3 sem avant<strong>la</strong> ponte)canard (âge 1 j): 1 dose/animalOOI: 15 j, DOI: âge 68 sem (S. enteritidis), âge62 sem (S. typhimurium)canard: OOI: 22 j, DOI: 43 jViande et abats: 21 j, Oeuf: 21 jf<strong>la</strong>con 10 x 2000 dosesR/AVIPRO SALMONELLA VAC E (Lohmann A.H.)Salmonel<strong>la</strong> enteritidis (souche Sm24/Rif12/Ssq),att : min 1, max 6 x 10exp 8 kvevaccin lyophilisé po dans l’eau de boissonPosologie:poule pondeuse et reprod: 1 dose dès l’âgede 1 j, 2e dose à 6 - 8 sem, 3e dose à 16 -18 sem (min 3 sem avant <strong>la</strong> ponte)OOI: dans les 14 j après <strong>la</strong> 1e vacDOI: jusqu’à l’âge de 52 semViande: 21 jNe pas administrer aux poules pondeuses oudans les 3 sem avant <strong>la</strong> pontef<strong>la</strong>con 10 x 1000, 2000 ou 5000 dosesR/AVIPRO SALMONELLA VAC T (Lohmann A.H.)Salmonel<strong>la</strong> typhimurium (Nal 2/Rif 9/Rtt) att:min 1 - max 6 x 10exp8 kve/dosevaccin lyophilisé po dans l’eau de boissonPosologie:poussin de chair: 1 dose dès l’âge de 1 jpoule pondeuse et reprod: 1 dose dès l’âgede 1 j, 2e dose à l’âge de 7 sem, 3e doseà l’âge de 16 sem, au moins 3 sem avant<strong>la</strong> ponteOOI: dans les 15 j après vacDOI: 50 sem après programme à 3 doses ou 6sem après vac uniqueViande: 21 jf<strong>la</strong>con 10 x 2000 dosesR/NOBILIS SALMONELLA ET (MSD A.H.)Salmonel<strong>la</strong> enteritidis inact (PT4 souche 109):1 x 10exp 9 cellules/doseSalmonel<strong>la</strong> typhimurium (DT104):1 x 10exp 9 cellules/doseAdjuv: gel d’hydroxyde d’aluminiumvaccin injectable imPosologie:poule: mère, poule pondeuse (à l’âge de 12et 16 sem):2 x 1 dose (0,5 ml) à 4 sem d’intervallevac d’urgence poussins d’1 j:0,1 ml/animal suivi de 0,5 ml 4 sem plus tardOOI: 4 sem après 2e vacDOI: pas d’infoTemps d’attente: 0 jNe pas utiliser chez les poules en pontef<strong>la</strong>con 500 mlR/ Vaccin contre Mycop<strong>la</strong>smagallisepticumPOULVAC MG (Pfizer A.H.)Mycop<strong>la</strong>sma gallisepticum (980) inact:min 1000 CFU/doseadjuv: huilevaccin injectable im, scPosologie:milieu sain (jusqu’à l’âge de 20 sem):poule pondeuse (âge 12 - 16 sem): 1 dose(0,5 ml)/animal, 4 sem min avant <strong>la</strong> pontemilieu contaminé (jusqu’à l’âge de 20 sem):poule pondeuse: vac à l’âge de 7 j (poussinsans imm mat), revac 4 sem min avant <strong>la</strong>ponteOOI: pas d’info, DOI: 6 mViande: 12 semf<strong>la</strong>con 1000 doses (500 ml)R/ Vaccins contre OrnithobacteriumrhinotrachealeNOBILIS OR INAC (MSD A.H.)suspension cellu<strong>la</strong>ire d’Ornithobacterium rhinotracheale,sérotype A (souche B3263/91):1 x 10exp 7 cellules/doseadjuv: paraffine liquidevaccin injectable sc, imPosologie:poule: 2 x 1 dose (0,25 ml), 1ère dose àl’âge de 6 - 12 sem, 2de dose min 6 semplus tardTemps d’attente: 0 jf<strong>la</strong>con 1 x 1000 dosesR/
13 VACCINS POUR VOLAILLE267Vaccins pour pigeons Vaccins contre <strong>la</strong> ma<strong>la</strong>die deNewcastle (paramyxovirose)COLUMBA (Pharmagal Bio)paramyxovirus type 1 columbae inact (souche988M-ca): min 5,8 log2 HIAdjuv: huile non-minéralevaccin injectable scPosologie:Co (âge > 4 sem):2 x 1 dose (0,3 ml) à 21 - 28 j d’intervalleRevac: 1 dose/an (min 21 j avant début desaison des vols et concours)OOI: 14 j après dernière vacDOI: 1 anTemps d’attente: 0 jf<strong>la</strong>con 30 ml (100 doses)R/iVaccin pour canaris et pinsonsPOULVAC P CANARY (Pfizer A.H.)virus de <strong>la</strong> variole <strong>du</strong> canari (KP1):min 10 exp4 EID50/dosevaccin lyophilisé méthode “wing web”Posologie:canaris, pinsons (âge > 4 sem):1 dose/animalRevac: 1 x/anOOI-DOI: pas d’infof<strong>la</strong>con 50 dosesR/Tableau récapitu<strong>la</strong>tif des vaccins pour <strong>la</strong> vo<strong>la</strong>illevirus de <strong>la</strong> ma<strong>la</strong>die de Marekvirus de <strong>la</strong> ma<strong>la</strong>die de Newcastlevirus de <strong>la</strong> bronchite infectieuseEgg Drop Syndrome virusvirus de <strong>la</strong> ma<strong>la</strong>die de Gumbororéovirusanémie infectieuse viralevirus de <strong>la</strong> variole aviairevirus de <strong>la</strong> <strong>la</strong>ryngotrachéite infectieusevirus de <strong>la</strong> rhinotrachéite infectieusevirus de l’encéphalite aviairecoccidiesMycop<strong>la</strong>sma gallisepticumSalmonel<strong>la</strong> spp.E. coliOrnithobacterium rhinotrachealeAVINEWMerialXAVIPRO GUMBOROVACLohmann A.H.XAVIPRO ND C131Lohmann A.H.XAVIPRO PRECISELohmann A.H.XAVIPROSALMONELLA Vac ELohmann A.H.XAVIPROSALMONELLA DUOLohmann A.H.XAVIPROSALMONELLA Vac TLohmann A.H.XAVIPRO THYMOVACLohmann A.H.X
268 13 VACCINS POUR VOLAILLEvirus de <strong>la</strong> ma<strong>la</strong>die de Marekvirus de <strong>la</strong> ma<strong>la</strong>die de Newcastlevirus de <strong>la</strong> bronchite infectieuseEgg Drop Syndrome virusvirus de <strong>la</strong> ma<strong>la</strong>die de Gumbororéovirusanémie infectieuse viralevirus de <strong>la</strong> variole aviairevirus de <strong>la</strong> <strong>la</strong>ryngotrachéite infectieusevirus de <strong>la</strong> rhinotrachéite infectieusevirus de l’encéphalite aviairecoccidiesMycop<strong>la</strong>sma gallisepticumSalmonel<strong>la</strong> spp.E. coliOrnithobacterium rhinotrachealeGALLIVAC IB 88MerialXHIPRACOXHipra LabXHIPRAGUMBORO CWHipra LabXHIPRAGUMBORO-GM97Hipra LabXHIPRAVIAR-NDVCLONHipra LabXNOBILIS CAV P4MSD A.H.XNOBILIS E. COLIMSD A.H.XNOBILIS GUMBOROD 78MSD A.H.XNOBILIS IB 4 - 91MSD A.H.XNOBILIS IB MA 5MSD A.H.XNOBILIS IB MULTI + NDMSD A.H.XXNOBILIS ILTMSD A.H.XNOBILIS ND + EDSMSD A.H.XXNOBILIS ND C2MSD A.H.XNOBILIS ND CLONE 30MSD A.H.XNOBILIS NEWCAVACMSD A.H.XNOBILIS OR INACMSD A.H.X
13 VACCINS POUR VOLAILLE269virus de <strong>la</strong> ma<strong>la</strong>die de Marekvirus de <strong>la</strong> ma<strong>la</strong>die de Newcastlevirus de <strong>la</strong> bronchite infectieuseEgg Drop Syndrome virusvirus de <strong>la</strong> ma<strong>la</strong>die de Gumbororéovirusanémie infectieuse viralevirus de <strong>la</strong> variole aviairevirus de <strong>la</strong> <strong>la</strong>ryngotrachéite infectieusevirus de <strong>la</strong> rhinotrachéite infectieusevirus de l’encéphalite aviairecoccidiesMycop<strong>la</strong>sma gallisepticumSalmonel<strong>la</strong> spp.E. coliOrnithobacterium rhinotrachealeNOBILIS REO ERSINACMSD A.H.XNOBILIS REO INACMSD A.H.XNOBILIS RHINO CVMSD A.H.XNOBILIS RISMAVACMSD A.H.XNOBILIS RISMAVAC+ CA 126MSD A.H.XNOBILISRT+IBmulti+ND+EDSMSD A.H.X X X XNOBILIS RTV 8544MSD A.H.XNOBILISSALMONELLA ETMSD A.H.XPARACOXSchering-PloughXPARACOX-5Schering-PloughXPOULVAC AEPfizer A.H.XPOULVAC BURSAPLUSPfizer A.H.XPOULVAC BURSINE 2Pfizer A.H.XPOULVAC CHICK-N-POX TCPfizer A.H.XPOULVAC E. COLIPfizer A.H.X
270 13 VACCINS POUR VOLAILLEvirus de <strong>la</strong> ma<strong>la</strong>die de Marekvirus de <strong>la</strong> ma<strong>la</strong>die de Newcastlevirus de <strong>la</strong> bronchite infectieuseEgg Drop Syndrome virusvirus de <strong>la</strong> ma<strong>la</strong>die de Gumbororéovirusanémie infectieuse viralevirus de <strong>la</strong> variole aviairevirus de <strong>la</strong> <strong>la</strong>ryngotrachéite infectieusevirus de <strong>la</strong> rhinotrachéite infectieusevirus de l’encéphalite aviairecoccidiesMycop<strong>la</strong>sma gallisepticumSalmonel<strong>la</strong> spp.E. coliOrnithobacterium rhinotrachealePOULVAC IB H 120Pfizer A.H.XPOULVAC IB PRIMERPfizer A.H.XPOULVAC IBMM +ARKPfizer A.H.XPOULVAC ILTPfizer A.H.XPOULVAC MAREKH.V.T.Pfizer A.H.XPOULVAC MGPfizer A.H.XPOULVAC NDHITCHNER B1Pfizer A.H.XPOULVAC ND LASOTAPfizer A.H.XPOULVAC TRTPfizer A.H.XVAXXITEK HVT + IBDMerialXXTableau récapitu<strong>la</strong>tif des vaccins pour pigeonsvirus de <strong>la</strong> ma<strong>la</strong>die de NewcastleCOLUMBAXPharmagal BioTableau récapitu<strong>la</strong>tif des vaccins pour canaris et pinsonsvirus de <strong>la</strong> variole <strong>du</strong> canariPOULVAC P CANARYPfizer A.H.X
13 VACCINS POUR LE CHIEN27113.1.10 Vaccins pour le chien13.1.10.1 Vaccins contre lesma<strong>la</strong>dies virales <strong>du</strong> chienChez le chien, il existe trois catégoriesprincipales de vaccins : les vaccinsmultivalents, utilisés chez les chiots enprimovaccination et chez les a<strong>du</strong>ltescomme rappel, qui confèrent une protectionéten<strong>du</strong>e contre les virosescanines les plus graves ; ensuite les vaccinsmono- ou bivalents destinés à uneprotection plus spécifique envers <strong>la</strong> touxde chenil ; enfin, les vaccins contre <strong>la</strong>rage. Quel que soit le vaccin envisagé, <strong>la</strong>consultation de <strong>la</strong> notice renseignera sur<strong>la</strong> <strong>du</strong>rée d’immunité de <strong>la</strong> vaccination etdonc sur <strong>la</strong> fréquence des rappels devaccination, qui sont généralement annuels.Cependant, de nouvelles étudesétendent les <strong>du</strong>rées d’immunité de certainsvaccins à trois ans au moins, pourles valences parvovirose, ma<strong>la</strong>die deCarré et hépatite infectieuse. Ces <strong>du</strong>réesd’immunité doivent être spécifiquementindiquées dans les notices vaccinales.(Voir Folia Veterinaria 2007 n°3 et FoliaVeterinaria 2010 n°1)Hépatite infectieuse canineL’hépatite infectieuse canine, connueaussi sous le nom de ma<strong>la</strong>die deRubarth, a pour agent pathogènel’adénovirus canin 1 (CAV-1). Chezle chiot, l’infection peut pro<strong>du</strong>ire unema<strong>la</strong>die aiguë ou suraiguë et mortelle;chez l’a<strong>du</strong>lte, elle est responsable designes cliniques de gravité variable. Lavaccination est systématiquement appliquée,car <strong>la</strong> valence vaccinale protégeantcontre l’hépatite infectieusecanine est présente dans tous les vaccinsmultivalents destinés à <strong>la</strong> primovaccination<strong>du</strong> chiot. L’épidémiologiede cette infection reste encore inconnuedans notre pays, en outre <strong>la</strong> ma<strong>la</strong>dieest rarement rencontrée en Europe.VaccinLa valence vaccinale est composée del’adénovirus canin 2 (CAV-2) vivant atténué,car les deux adénovirus caninspossèdent des parentés antigéniquesétroites. La valence CAV-2 protège à <strong>la</strong>fois contre l’hépatite infectieuse canineprovoquée par le CAV-1 et <strong>la</strong> <strong>la</strong>ryngotrachéiteinfectieuse canine causéepar le CAV-2, un des agents de <strong>la</strong> touxde chenil. Elle présente également unetrès bonne innocuité et cette propriétéa motivé le remp<strong>la</strong>cement <strong>du</strong> CAV-1par le CAV-2 comme valence vaccinale.En effet des réactions secondairesavaient été rencontrées chezdes chiens après vaccination avec unevalence CAV-1 : de l’œdème cornéenavait été observé et imputé à ce virus.ProtectionUne injection vaccinale est protectriceà l’âge de 12 semaines. Une vaccinationantérieure à cet âge peut êtrecontrecarrée par l’immunité maternelleet doit être complétée par une revaccinationà partir de 12 semaines.CANIGEN CHP (Virbac)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 3 DICT50/m<strong>la</strong>dénovirus canin type 2 att: min 300 DICT50/mlparvovirus canin att: min 10exp 4 DICT50/mlvaccin lyophilisé et solvant injectable sc, imPosologie:Primovac:Ca (âge > 14 - 16 sem): 2 x 1 dose à 15 jd’intervalleRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/EURICAN CHPPI2 (Merial)adénovirus canin att: min 10exp 2,5 DICC50parvovirus canin att: min 10exp 4,9 DICC50virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 4 DICC50virus parainfluenza att: min 10exp 4,7 DICC50vaccin lyophilisé injectable scPosologie:Primovac:Ca (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, 2e vac à partir de l’âge de12 semRevac:1 dose/anOOI: CAV1: 21 j, CPV: 21 jDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/NOBIVAC DHP (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort):min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICTD50/mlvaccin lyophilisé injectable scPosologie:Primovac- Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 sem- Ca (âge > 12 sem): 1 dose/animalSi nécessaire Ca (âge 6 sem):1 dose/animal et ensuite 1 dose à l’âge de9 sem et à 12 semRevac: Carré, hépatite, parvo: tous les 3 ansOOI: 3 sem (CAV1) - 2 sem (CAV2) - 1 sem(CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV)f<strong>la</strong>con 10 x 1 doseR/
27213 VACCINS POUR LE CHIENNOBIVAC DHPPI (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort):min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvirus parainfluenza att (souche Cornell):min 10exp 5,5 DICT/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 semCa (âge > 12 sem): 1 dose/animalSi nécessaire, vac Ca à l’âge de 6 sem:1 dose/animal et ensuite à l’âge de 9 sem età l’âge de 12 semRevac:- Carré, hépatite, Parvo: tous les 3 ans- Para-influenza: annuellementOOI: 4 sem (CPI), 3 sem (CAV1) - 2 sem (CAV2),1 sem (CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV) - 1 an (CPI)f<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/VANGUARD DA2PI-CPV-LEPTO (Pfizer A.H.)- fraction liquide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/mlL. Canico<strong>la</strong> inact: min 40 HPU/mlL. Icterohaemorrhagiae inact: min 40 HPU/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 att (NL CPI 5):min 10exp 6 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose, revac avecVanguard Lepto® après 2 - 3 semCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, PI: 12 m, CPV: 12 m, CDV,CAV: non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/TRIVIROVAX (Merial)virus de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien, att:min 10exp 3 DICC50adénovirus canin type 2, att:min 10exp 2,5 DICC50parvovirus canin, att: min 10exp 3 DECP50vaccin lyophilisé injectable sc, im, ivPosologie:PrimovacCa (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, dernière vac après âge de12 semRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/VANGUARD DA2PI-CPV (Pfizer A.H.)- fraction fluide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 (NL-CPI-5) att:min 10exp 6 DICC50/mlvaccin lyophilisé et solvant avec vaccin injectablescPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 doseCa (âge 6 -12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j après vac, CAV, PI, CDV: 3 semaprès vacDOI: PI: min 12 m, CPV: min 12 m, CDV, CAV:non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/
13 VACCINS POUR LE CHIEN 273ParvoviroseLa parvovirose canine est pro<strong>du</strong>ite parle parvovirus canin de type 2 (CPV)dont il existe trois sous-types : a, b et c.Les souches virales présentes dansles vaccins protègent contre ces troissous-types. Le virus est responsabled’une gastro-entérite hémorragiquemortelle chez le chiot. Il est donc indispensablede protéger le chiot desconséquences de cette infection.VaccinLes vaccins contiennent une souchede parvovirus atténué. La résistanceélevée de cet agent pathogène permetde le conserver dans le solvant utilisépour reconstituer <strong>la</strong> partie lyophiliséed’un vaccin multivalent.ProtectionLes chiots possèdent presque tousune immunité maternelle envers le parvovirus.Celle-ci joue un rôle paradoxalqui est à l’origine <strong>du</strong> concept <strong>du</strong> « trouimmunitaire », défini comme étant <strong>la</strong>période au cours de <strong>la</strong>quelle le chiotn’est plus protégé contre l’infectionpar l’immunité maternelle, alors quecelle-ci interfère encore avec <strong>la</strong> vaccination.Certains vaccins c<strong>la</strong>ssiquesne peuvent pas tout à fait contournerce phénomène et doivent donc êtreré-administrés à l’âge de 16 semaines,outre <strong>la</strong> vaccination à l’âge de 12semaines.Des virus vaccinaux surtitrés sontprésents dans <strong>la</strong> plupart des vaccinsqui surmontent ainsi plus facilementl’immunité maternelle, même dès l’âgede six semaines chez certains chiots.Avec ces vaccins surtitrés, <strong>la</strong> vaccinationprotège plus de 90 % des chiotsdès l’âge de 12 semaines. Certainschiots, moins de 10 %, nés de mèresfortement immunisées peuvent doncne pas être va<strong>la</strong>blement immunisés à12 semaines. Ils sont repérés par desdonnées épidémiologiques ou par undiagnostic sérologique et ils sont revaccinésà l’âge de 15 semaines. Vaccins monovalentsCANIGEN PUPPY 2b (Virbac)parvovirus canin att (type 2 b) (souche CPV39):min 10exp 5,6 TCID50 /mlvaccin injectable scPosologie:Ca/chiot (âge > 5 sem): 2 x 1 dose (1 ml) à 2sem d’intervallePour une protection à long terme, vaccineravec un parvovirus selon schéma de vacc<strong>la</strong>ssique (commencer avant l’âge de 11sem)OOI: 2 sem après vacDOI: jusqu’à l’âge de 11 semf<strong>la</strong>con 10 x 1 doseR/NOBIVAC PARVO-C (MSD A.H.)parvovirus canin att (souche 154):10exp 7 DICT50/dosevaccin lyophilisé injectable scPosologie:Primovac- Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 sem- Ca (âge > 12 sem): 1 dose/animalSi nécessaire Ca (âge 6 sem):1 dose/animal et ensuite 1 dose à l’âge de 9sem et à 12 semRevac: parvo: tous les 3 ansOOI: 1 sem après primovac (CPV)DOI: 3 ans (CPV)f<strong>la</strong>con 10 x 1 doseR/PARVODOG (Merial)parvovirus canin viv (souche C-780916,Cornell): min 10exp 3 DECP50vaccin injectable im, sc, ivPosologie:Primovac:Ca (âge < 3 m): 2 x 1 dose (1 ml), 1e à l’âgede 6 - 8 sem, 2e après l’âge de 12 semCa (âge > 3 m): 1 doseRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/PRIMODOG (Merial)parvovirus canin att (CPV 115-780916, Cornell):min 10exp 5,5 DICC50/mlvaccin injectable scPosologie:Primovac:Ca (âge min 4 sem):2 x 1 dose (1 ml) (2 - 4 sem d’intervalle)peut être associé à Istolept® à partir del’âge de 7 semsuivi par le schéma de vaccination conventionne<strong>la</strong>près l’âge de 12 semRevac: 1 an après <strong>la</strong> 1e primovac avec unesouche <strong>du</strong> parvovirusOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dose (1 dose = 1 ml)R/
27413 VACCINS POUR LE CHIENVANGUARD CPV (Pfizer A.H.)parvovirus canin att (NL-35-D):min 10exp 7 CCID50vaccin injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 doseCa (âge 6 -12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: 7 j après vacDOI: min 12 mf<strong>la</strong>con 25 x 1 doseR/ Vaccins multivalentsCANIGEN CHP (Virbac)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 3 DICT50/m<strong>la</strong>dénovirus canin type 2 att: min 300 DICT50/mlparvovirus canin att: min 10exp 4 DICT50/mlvaccin lyophilisé et solvant injectable sc, imPosologie:Primovac:Ca (âge > 14 - 16 sem): 2 x 1 dose à 15 jd’intervalleRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/EURICAN CHPPI2 (Merial)adénovirus canin att: min 10exp 2,5 DICC50parvovirus canin att: min 10exp 4,9 DICC50virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 4 DICC50virus parainfluenza att: min 10exp 4,7 DICC50vaccin lyophilisé injectable scPosologie:Primovac:Ca (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, 2e vac à partir de l’âge de12 semRevac:1 dose/anOOI: CAV1: 21 j, CPV: 21 jDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/NOBIVAC DHP (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort):min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICTD50/mlvaccin lyophilisé injectable scPosologie:Primovac- Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 sem- Ca (âge > 12 sem): 1 dose/animalSi nécessaire Ca (âge 6 sem):1 dose/animal et ensuite 1 dose à l’âge de 9sem et à 12 semRevac: Carré, hépatite, parvo: tous les 3 ansOOI: 3 sem (CAV1) - 2 sem (CAV2) - 1 sem(CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV)f<strong>la</strong>con 10 x 1 doseR/NOBIVAC DHPPI (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort):min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvirus parainfluenza att (souche Cornell):min 10exp 5,5 DICT/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 semCa (âge > 12 sem): 1 dose/animalSi nécessaire, vac Ca à l’âge de 6 sem:1 dose/animal et ensuite à l’âge de 9 sem età l’âge de 12 semRevac:- Carré, hépatite, Parvo: tous les 3 ans- Para-influenza: annuellementOOI: 4 sem (CPI), 3 sem (CAV1) - 2 sem (CAV2),1 sem (CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV) - 1 an (CPI)f<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/NOBIVAC PUPPY DP (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderste Poort):min 10exp 5 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 6 sem): 1 dose (1 ml)Ca (âge 9 - 12 sem): vacciner avec un vacappropriévac âge 12 sem OOI: 1 sem (CDV, CPV)DOI: non connuf<strong>la</strong>con 5 x 1 dose + 5 x 1 ml de solvantR/TRIVIROVAX (Merial)virus de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien, att:min 10exp 3 DICC50adénovirus canin type 2, att:min 10exp 2,5 DICC50parvovirus canin, att: min 10exp 3 DECP50vaccin lyophilisé injectable sc, im, ivPosologie:PrimovacCa (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, dernière vac après âge de12 semRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/
13 VACCINS POUR LE CHIEN 275VANGUARD CPV-LEPTO (Pfizer A.H.)parvovirus canin att (NL-35-D):min 10exp 7 CCID50/mlL. Canico<strong>la</strong> inact (C-51): min 40 UPH/mlL. Icterohaemorrhagiae inact (NADL):min 40 UPH/mlvaccin injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose (1 ml), 1 dose deVanguard Lepto® après 14 jCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, CPV: 12 mf<strong>la</strong>con 25 x 1 doseR/VANGUARD DA2PI-CPV (Pfizer A.H.)- fraction fluide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 (NL-CPI-5) att:min 10exp 6 DICC50/mlvaccin lyophilisé et solvant avec vaccin injectablescPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 doseCa (âge 6 -12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j après vac, CAV, PI, CDV: 3 semaprès vacDOI: PI: min 12 m, CPV: min 12 m, CDV, CAV:non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/VANGUARD DA2PI-CPV-LEPTO (Pfizer A.H.)- fraction liquide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/mlL. Canico<strong>la</strong> inact: min 40 HPU/mlL. Icterohaemorrhagiae inact: min 40 HPU/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 att (NL CPI 5):min 10exp 6 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose, revac avecVanguard Lepto® après 2 - 3 semCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, PI: 12 m, CPV: 12 m, CDV,CAV: non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/Ma<strong>la</strong>die de CarréL’agent pathogène de <strong>la</strong> ma<strong>la</strong>die deCarré (distemper) est un morbillivirus(CDV). La ma<strong>la</strong>die se présente sousdes formes cliniques variées, avecfréquemment des signes nerveux, quipeuvent être mortelles. Une immunodépressionpeut être in<strong>du</strong>ite au coursde <strong>la</strong> phase aiguë. La vaccination estdonc indispensable chez le chiot.VaccinLa valence «ma<strong>la</strong>die de Carré» estincorporée dans des vaccins multivalents.Le vaccin contre <strong>la</strong> ma<strong>la</strong>die deCarré est constitué d’un virus vivantatténué.ProtectionUne seule injection de vaccin est protectricesi elle est effectuée à l’âge de12 semaines ou plus quand l’immunitématernelle n’interfère plus avec <strong>la</strong>vaccination.RemarqueLa notice des vaccins permet parfoisson utilisation chez le jeune chiot, àpartir de 6 semaines. Toute vaccinationpratiquée avant 12 semaines doitcependant être répétée après cet âge.CANIGEN CHP (Virbac)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 3 DICT50/m<strong>la</strong>dénovirus canin type 2 att: min 300 DICT50/mlparvovirus canin att: min 10exp 4 DICT50/mlvaccin lyophilisé et solvant injectable sc, imPosologie:Primovac:Ca (âge > 14 - 16 sem): 2 x 1 dose à 15 jd’intervalleRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/EURICAN CHPPI2 (Merial)adénovirus canin att: min 10exp 2,5 DICC50parvovirus canin att: min 10exp 4,9 DICC50virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 4 DICC50virus parainfluenza att: min 10exp 4,7 DICC50vaccin lyophilisé injectable scPosologie:Primovac:Ca (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, 2e vac à partir de l’âge de12 semRevac:1 dose/anOOI: CAV1: 21 j, CPV: 21 jDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/
27613 VACCINS POUR LE CHIENNOBIVAC DHP (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort):min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICTD50/mlvaccin lyophilisé injectable scPosologie:Primovac- Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 sem- Ca (âge > 12 sem): 1 dose/animalSi nécessaire Ca (âge 6 sem):1 dose/animal et ensuite 1 dose à l’âgede 9 sem et à 12 semRevac: Carré, hépatite, parvo: tous les 3 ansOOI: 3 sem (CAV1) - 2 sem (CAV2) - 1 sem(CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV)f<strong>la</strong>con 10 x 1 doseR/NOBIVAC DHPPI (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort): min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvirus parainfluenza att (souche Cornell):min 10exp 5,5 DICT/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 semCa (âge > 12 sem): 1 dose/animalSi nécessaire, vac Ca à l’âge de 6 sem:1 dose/animal et ensuite à l’âge de 9 sem età l’âge de 12 semRevac:- Carré, hépatite, Parvo: tous les 3 ans- Para-influenza: annuellementOOI: 4 sem (CPI), 3 sem (CAV1) - 2 sem (CAV2),1 sem (CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV) - 1 an (CPI)f<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/NOBIVAC PUPPY DP (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderste Poort):min 10exp 5 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 6 sem): 1 dose (1 ml)Ca (âge 9 - 12 sem): vacciner avec un vacappropriévac âge 12 sem OOI: 1 sem (CDV, CPV)DOI: non connuf<strong>la</strong>con 5 x 1 dose + 5 x 1 ml de solvantR/TRIVIROVAX (Merial)virus de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien, att:min 10exp 3 DICC50adénovirus canin type 2, att:min 10exp 2,5 DICC50parvovirus canin, att: min 10exp 3 DECP50vaccin lyophilisé injectable sc, im, ivPosologie:PrimovacCa (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, dernière vac après âge de12 semRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/VANGUARD DA2PI-CPV (Pfizer A.H.)- fraction fluide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 (NL-CPI-5) att:min 10exp 6 DICC50/mlvaccin lyophilisé et solvant avec vaccin injectablescPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 doseCa (âge 6 -12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j après vac, CAV, PI, CDV: 3 semaprès vacDOI: PI: min 12 m, CPV: min 12 m, CDV, CAV:non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/VANGUARD DA2PI-CPV-LEPTO (Pfizer A.H.)- fraction liquide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/mlL. Canico<strong>la</strong> inact: min 40 HPU/mlL. Icterohaemorrhagiae inact: min 40 HPU/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 att (NL CPI 5):min 10exp 6 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose, revac avecVanguard Lepto® après 2 - 3 semCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, PI: 12 m, CPV: 12 m, CDV,CAV: non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/
13 VACCINS POUR LE CHIEN 277Herpèsvirose canineL’infection par l’herpèsvirus canin esttrès fréquente en Belgique, à <strong>la</strong> fois chezles chiens de particuliers et dans les élevageset les chenils. Le virus se transmetaisément par <strong>la</strong> voie respiratoireet de nombreux chiens sont infectésde manière asymptomatique et <strong>du</strong>ranttoute leur vie à cause de <strong>la</strong> persistance<strong>du</strong> virus à l’état <strong>la</strong>tent. Le virus se transmetégalement par <strong>la</strong> voie vénérienne.Les chiens montrent donc des épisodesd’excrétion et de réexcrétion virales auniveau nasal et génital. L’herpèsviruscanin est principalement associé à <strong>la</strong>ma<strong>la</strong>die hémorragique <strong>du</strong> chiot, uneaffection généralisée, hémorragiqueet rapidement mortelle, qui atteint leschiots âgés de moins de 4 semaines.Les chiots s’infectent au moment de <strong>la</strong>naissance, par contact avec <strong>la</strong> mère oudes congénères qui excrètent le virus.Le chiot infecté devient anorexique, apathiqueet présente de l’hypothermie, uneextrême faiblesse et des troubles nerveux.La mortalité survient dans les 10 à14 jours après <strong>la</strong> naissance. Des cas demorts subites sont également observés.En général, c’est l’ensemble de <strong>la</strong> portéequi est atteinte sans signes cliniquesparticuliers chez <strong>la</strong> mère. Parmi lesautres affections provoquées par l’herpèsviruscanin, des résorptions fœtales,des momifications, des avortements, de<strong>la</strong> mortalité néonatale et <strong>la</strong> naissance dechiots normaux porteurs <strong>la</strong>tents <strong>du</strong> virussont rapportés. La présence <strong>du</strong> virus auniveau respiratoire l’associe à certainesformes de toux de chenil.ProtectionLe vaccin sous-unitaire actuellement surle marché est donc destiné à l’immunisationactive des chiennes gravides,afin d’assurer l’immunisation passivedes chiots. Cependant, <strong>la</strong> faible persistancedes anticorps après vaccinationou infection naturelle recommande unrappel de vaccination à <strong>la</strong> fin de chaquegestation.EURICAN HERPES 205 (Merial)Ag de l’herpèsvirus canin (souche F205):0,3 à 1,75 mcg/dose (1 ml)poudre et solvant pour vaccin injectable scPosologie:Ca (chienne gestante): 2 x 1 dose (1 ml) à6 sem d’intervalle (1e dose 7 - 10 j après<strong>la</strong> saillie)Revac: même schéma lors de chaquegestationOOI-DOI: pas d’infof<strong>la</strong>con 1 dose de poudre + 1 ml de solvantR/Infections virales associées à <strong>la</strong>toux de chenilLa toux de chenil est une affection respiratoireépidémique multifactorielle.Ce caractère rend sa prévention difficile.Comme l’adénovirus canin 2, levirus para-influenza canin (CPIV) et levirus de <strong>la</strong> ma<strong>la</strong>die de Carré sont impliquéscomme agents étiologiques partielsde cette entité.VaccinDeux catégories de vaccins existent :inactivé et atténué.ProtectionLes vaccins multivalents utilisés enprimovaccination et en rappel chezle chien apportent un premier niveaude protection. Celle-ci est complétéepar les vaccins bivalents possédantdes valences spécifiques : Bordetel<strong>la</strong>bronchiseptica et virus para-influenzacanin. Les vaccins par voie sous-cutanéenécessitent deux injections enprimovaccination, alors que le vaccinintranasal est injecté une seule fois etin<strong>du</strong>it une protection dans les jours quisuivent <strong>la</strong> vaccination. Le vaccin intranasalpeut être administré chez le chiotà partir de l’âge de 3 semaines, ce quipeut être favorable dans un milieucontaminé. L’administration d’antibiotiquesjuste avant ou 1 semaine après<strong>la</strong> vaccination a un effet négatif surl’efficacité <strong>du</strong> vaccin, <strong>la</strong> vaccinationdevant alors être répétée. Les animauxvaccinés par voie intranasalepeuvent excréter <strong>la</strong> souche vaccinalede Bordetel<strong>la</strong> bronchiseptica pendant6 semaines après <strong>la</strong> vaccination, et<strong>la</strong> souche vaccinale de parainfluenzacanin pendant quelques jours après <strong>la</strong>vaccination.RemarqueLa vaccination est à conseiller dansun chenil à problèmes et chez les animauxdestinés à être en contact avecd’autres lors d’expositions, soit enrefuge, en élevage ou en pension. Ilest donc indispensable, avant l’entrée<strong>du</strong> chien en ces lieux, de réaliser l’ensemble<strong>du</strong> protocole de vaccination etde respecter le dé<strong>la</strong>i nécessaire à l’établissementde <strong>la</strong> protection.
27813 VACCINS POUR LE CHIEN Vaccin monovalent contre le viruspara-influenzaNOBIVAC Pi (MSD A.H.)parainfluenza canin att (Cornell):min 10 exp5,5 - max 10exp7,3 TCID50/mlvaccin lyophilisé et solvant injectable scPosologie:Ca:Primovac:- âge < 12 sem: 2 x 1 dose, 1ère dose dèsl’âge de 8 sem, 2de dose 2 - 4 sem plustard- âge min 12 sem: 1 dose/animalRevac: 1 dose/anOOI: 4 sem après vacDOI: pas d’info (une réponse anamnéstique apu être constatée chez les Ca ayant reçu unerévac 1 an après <strong>la</strong> primovac)f<strong>la</strong>con 10 x 1 dose (1 ml)R/ Vaccins contre le viruspara-influenza incluantB. bronchisepticaNOBIVAC BbPi (MSD A.H.)Bordetel<strong>la</strong> bronchiseptica (B-C2), att:min 10exp 8 et max 10 exp 9,7 CFU/dosevirus parainfluenza canin (Cornell), att:min 10exp 3 et max 10exp 5,8 DICT50/dosevaccin et solvant inasPosologie:Ca (âge > 3 sem): 1 dose/animal, min 3 semavant période de risque, B. bronchiseptica:min 72 h avant période de risqueRevac: 1 x/anOOI: 72 h (B. bronchiseptica) - 3 sem (CPI)DOI: 1 anf<strong>la</strong>con 5 x 1 doseR/PNEUMODOG (Merial)Bordetel<strong>la</strong> bronchiseptica, inact:min 10exp 9 germes/mlvirus parainfluenza inact: min 32 UHA/mlvaccin injectable scPosologie:Primovac:Ca: 2 x 1 dose (2 ml) à 2 - 3 sem d’intervallechiot (imm mat): 1ère vac dès l’âge de 6semchiot (sans imm mat): 1ère vac dès l’âgede 4 semRevac:1 dose/an avant période de repro<strong>du</strong>ctionet 7 j avant tout contact avec collectivitécaninepeut être administré (site d’injection distinct)avec Istolept®, Parvodog® ou Trivirovax®OOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/ Vaccins contre le virus parainfluenzaet autres valencesviralesEURICAN CHPPI2 (Merial)adénovirus canin att: min 10exp 2,5 DICC50parvovirus canin att: min 10exp 4,9 DICC50virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien:min 10exp 4 DICC50virus parainfluenza att: min 10exp 4,7 DICC50vaccin lyophilisé injectable scPosologie:Primovac:Ca (âge > 7 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalle, 2e vac à partir de l’âge de12 semRevac:1 dose/anOOI: CAV1: 21 j, CPV: 21 jDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/NOBIVAC DHPPI (MSD A.H.)virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(souche Onderstepoort): min 10exp 4 DICT50/m<strong>la</strong>dénovirus canin type 2 att (souche ManhattanLPV3): min 10exp 4 DICT50/mlparvovirus canin att (souche 154):min 10exp 7 DICT50/mlvirus parainfluenza att (souche Cornell):min 10exp 5,5 DICT/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge < 12 sem): 1 dose/animal à 9 semet à 12 semCa (âge > 12 sem): 1 dose/animalSi nécessaire, vac Ca à l’âge de 6 sem:1 dose/animal et ensuite à l’âge de 9 sem età l’âge de 12 semRevac:- Carré, hépatite, Parvo: tous les 3 ans- Para-influenza: annuellementOOI: 4 sem (CPI), 3 sem (CAV1) - 2 sem (CAV2),1 sem (CDV, CPV)DOI: 3 ans (CDV, CAV2, CPV) - 1 an (CPI)f<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/VANGUARD DA2PI-CPV (Pfizer A.H.)- fraction fluide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 (NL-CPI-5) att:min 10exp 6 DICC50/mlvaccin lyophilisé et solvant avec vaccin injectablescPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 doseCa (âge 6 -12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j après vac, CAV, PI, CDV: 3 semaprès vacDOI: PI: min 12 m, CPV: min 12 m, CDV, CAV:non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/
13 VACCINS POUR LE CHIEN 279VANGUARD DA2PI-CPV-LEPTO (Pfizer A.H.)- fraction liquide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/mlL. Canico<strong>la</strong> inact: min 40 HPU/mlL. Icterohaemorrhagiae inact: min 40 HPU/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 att (NL CPI 5):min 10exp 6 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose, revac avecVanguard Lepto® après 2 - 3 semCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, PI: 12 m, CPV: 12 m, CDV,CAV: non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/Vaccination <strong>du</strong> chiot avec lesvaccins multivalentsLa primovaccination <strong>du</strong> chiot s’effectuepar l’injection de vaccins multivalentscomposés au minimum <strong>du</strong>parvovirus canin, <strong>du</strong> virus de <strong>la</strong> ma<strong>la</strong>diede Carré et de l’adénovirus canin 2,ce dernier protégeant essentiellementcontre l’hépatite infectieuse canine.Les valences «leptospirose» et «parainfluenzacanin» peuvent également yêtre associées. La primovaccinationest couramment effectuée à un âge inférieurà 12 semaines, par exemple à 9semaines, au moment où les anticorpsmaternels peuvent toujours jouer unrôle d’interférence. La vaccinationdoit alors être répétée à 12 semainespour toutes les valences. Si <strong>la</strong> valence«rage» fait partie de <strong>la</strong> multivaccination<strong>du</strong> chiot, il faut être attentif à <strong>la</strong> réglementationqui ne confère qu’une <strong>du</strong>réede validité de 3 mois au certificat devaccination antirabique lorsque cettevaccination a été effectuée avant l’âgede trois mois.13.1.10.2 Vaccins bactériens pourle chienBordetel<strong>la</strong> bronchisepticaBordetel<strong>la</strong> bronchiseptica joue un rôleimportant dans <strong>la</strong> trachéobronchiteinfectieuse <strong>du</strong> chien, encore appeléetoux de chenil. Il s’agit d’une affectionqui se caractérise principalement parune toux sèche.Chez les jeunes animaux, on peutaussi observer des signes cliniquestels qu’anorexie, fièvre et somnolence.La toux de chenil, comme son noml’indique, apparaît surtout lors des rassemblementscanins, elle peut cependantse rencontrer chez des indivi<strong>du</strong>sisolés. Dans les élevages, les signescliniques surgissent en général chezles indivi<strong>du</strong>s âgés de 6 à 7 semaines,même s’ils peuvent parfois apparaîtredès l’âge de 3 semaines.VaccinVaccin monovalent à usage intranasalet vaccins multivalents contenant levirus para-influenza canin.ProtectionAprès administration parentérale, lesvaccins inactivés peuvent au moinsin<strong>du</strong>ire une protection partielle. Laprimovaccination nécessite deuxinjections, à 2 ou 3 semaines d’intervalle.La revaccination doit avoir lieutous les ans. On tiendra compte de<strong>la</strong> possibilité d’une interférence avecl’immunité maternelle. Pour les chiotsissus de mères vaccinées, <strong>la</strong> 1e injectionpeut être administrée à partir de<strong>la</strong> 6ème semaine; quant à ceux issusde mères non vaccinées, ils peuventrecevoir leur première injection dèsleur 4ème semaine. D’autres vaccinssont atténués et sont administrés parvoie intranasale dès l’âge de 3 semaines,quelque soit le statut immunitairematernel. Une seule injection estnécessaire.RemarqueLa vaccination est à conseiller dansun chenil à problèmes et chez les animauxdestinés à être en contact avecd’autres lors d’expositions, soit enrefuge, en élevage ou en pension. Ilest donc indispensable, avant l’entrée<strong>du</strong> chien en ces lieux, de réaliser l’ensemble<strong>du</strong> protocole de vaccination etde respecter le dé<strong>la</strong>i nécessaire à l’établissementde <strong>la</strong> protection. Vaccin monovalentBRONCHI-SHIELD (Pfizer A.H.)Bordetel<strong>la</strong> bronchiseptica att, souche 92B:2,1 x 10 exp6 CFU - 5,5 x 10 exp8 CFU/dosevaccin lyophilisé et solvant pour suspensioninasPosologie:Ca (âge > 8 sem): 1 dose (1 ml)/animalRevac: annuelleOOI: 5 j après vacDOI: 1 anf<strong>la</strong>con 10 x 1 dose de vaccin lyophilisé + 1 dosede solvantR/
28013 VACCINS POUR LE CHIEN Vaccins contre Bordetel<strong>la</strong>bronchiseptica combinés avec levirus para-influenza caninNOBIVAC BbPi (MSD A.H.)Bordetel<strong>la</strong> bronchiseptica (B-C2), att:min 10exp 8 et max 10 exp 9,7 CFU/dosevirus parainfluenza canin (Cornell), att:min 10exp 3 et max 10exp 5,8 DICT50/dosevaccin et solvant inasPosologie:Ca (âge > 3 sem): 1 dose/animal, min 3 semavant période de risque, B. bronchiseptica:min 72 h avant période de risqueRevac: 1 x/anOOI: 72 h (B. bronchiseptica) - 3 sem (CPI)DOI: 1 anf<strong>la</strong>con 5 x 1 doseR/PNEUMODOG (Merial)Bordetel<strong>la</strong> bronchiseptica, inact:min 10exp 9 germes/mlvirus parainfluenza inact: min 32 UHA/mlvaccin injectable scPosologie:Primovac:Ca: 2 x 1 dose (2 ml) à 2 - 3 sem d’intervallechiot (imm mat):1ère vac dès l’âge de 6 semchiot (sans imm mat):1ère vac dès l’âge de 4 semRevac:1 dose/an avant période de repro<strong>du</strong>ctionet 7 j avant tout contact avec collectivitécaninepeut être administré (site d’injection distinct)avec Istolept®, Parvodog® ou Trivirovax®OOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 doseR/Leptospira Canico<strong>la</strong>/IcterohaemorrhagiaeLa leptospirose canine est une ma<strong>la</strong>dieinfectieuse aiguë, subaiguë ou chroniqueet parfois à évolution subclinique,au cours de <strong>la</strong>quelle <strong>la</strong> septicémieéventuellement présente peut aboutirà une néphrite et une hépatite s’accompagnantd’urémie voire d’ictère.Les chiens peuvent être infectés pardifférents sérotypes. La leptospiroseclinique est principalement engendréepar des germes appartenant aux sérogroupeIcterohaemorrhagiae et sérotypesgrippotyphosa et canico<strong>la</strong>. Cesont les rats qui tiennent lieu de réservoirpour le sérotype icterohaemorrhagiae,tandis que les rats musqués et lescampagnols sont le réservoir <strong>du</strong> sérotypegrippotyphosa. Ces hôtes jouantle rôle de réservoir peuvent excréter lesgermes via l’urine pendant une <strong>du</strong>réetrès longue. Au sein d’un milieu humideà pH neutre ou légèrement alcalin, lesleptospires sont en mesure de survivretrès longtemps. Ceci explique que <strong>la</strong>ma<strong>la</strong>die apparaît surtout chez les chiensse promenant dans les fossés ou prèsdes cours d’eau où l’on retrouve précisémentce type de rongeurs. Le chientient lieu de réservoir pour LeptospiraCanico<strong>la</strong>. Ce dernier sérotype n’a plusété isolé en Belgique depuis 1975.VaccinPour <strong>la</strong> prévention de cette ma<strong>la</strong>die,des vaccins inactivés sont disponiblessur le marché. Ils contiennent les sérogroupesIcterohaemorrhagiae et lesérotype canico<strong>la</strong>.ProtectionLa primovaccination consiste en deuxinjections à 2 – 5 semaines d’intervalleselon le vaccin utilisé. On n’oublierapas de prendre en considération l’interférencede l’immunité maternelle avec<strong>la</strong> vaccination chez les chiots issusde mères vaccinées, et ce jusqu’àl’âge de 7 à 16 semaines. Une revaccinationsemestrielle ou annuelle estindispensable.Particu<strong>la</strong>ritésIl est également important de tenircompte <strong>du</strong> fait qu’il n’y a pas d’immunitécroisée entre les différentssérogroupes de leptospires. Ainsi, unvaccin à base de Icterohaemorrhagiae/Canico<strong>la</strong> ne protège pas contreGrippotyphosa. (Voir aussi FoliaVeterinaria 2008 n° 2) Vaccins contre LeptospiraCanico<strong>la</strong>/IcterohaemorrhagiaeCANIGEN L (Virbac)L. Canico<strong>la</strong>: 800 - 1200 10exp 6 de germes/mlL. Icterohaemorrhagiae:800 - 1200 10exp 6 de germes/mlvaccin injectable sc, imPosologie:Primovac:Ca (âge > 8 sem): 2 x 1 dose (1 ml) à 3 - 4sem d’intervalleRevac:Ca: 1 dose/anOOI: L. Canico<strong>la</strong>: 5 sem après primovac,L. Icterohaem: 2 sem après primovacDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/ISTOLEPT (Merial)L. Canico<strong>la</strong> inact: min 10exp 8 germes/mlL. Icterohaemorrhagiae inact:min 10exp 8 germes/mlvaccin injectable sc, imPosologie:Primovac:Ca (âge > 7 sem): 2 x 1 dose (1 ml),2e 3 - 5 sem plus tard dès l’âge de 12 semRevac:1 dose/an (ou 1 dose/6 m)Peut servir de solvant aux vac Parvodog®et Trivirovax®OOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dosisR/
13 VACCINS POUR LE CHIEN 281NOBIVAC LEPTO (MSD A.H.)L. Canico<strong>la</strong> inact, sérovar port<strong>la</strong>nd-vere, s. Ca-12-000: min 1300 U/mlL. Icterohaemorrhagiae inact, sérovar copenhageni,s. 820K: min 750 U/mlsuspension injectable scPosologie:Primovac:Ca (âge > 8 sem): 2 x 1 dose à 2 - 4 semd’intervalleRevac:1 dose tous les 6 - 12 m (tous les 6 m pourle sérovar icterohaemorrhagiae)OOI: 4 semDOI: serovar Canico<strong>la</strong>: 1 an, serovarIcterohaemorrhagiae: 6 mf<strong>la</strong>con 10 x 1 dose (1 ml)R/VANGUARD LEPTO (Pfizer A.H.)L. Canico<strong>la</strong> (C-51), inact: min 40 HPU/mlL. Icterohaemorrhagiae (NADL): min 40 HPU/mlvaccin injectable scPosologie:Ca (âge > 7sem, < 12 sem): 2 x 1 dose à 14 jd’intervalle (2e vac à l’âge de min 12 sem)Ca (âge > 12 sem): 2 x 1 dose à 14 jd’intervalleRevac:1 dose/anOOI: 3 sem après <strong>la</strong> dernière vac de baseDOI: 12 mf<strong>la</strong>con 25 x 1 mlR/ Vaccins contre <strong>la</strong> leptospirose etautres valencesLEPTORABISIN (Merial)L. Canico<strong>la</strong> inact: min 10exp 8 germes/doseL. Icterohaemorrhagiae inact:min 10exp 8 germes/doseAg de <strong>la</strong> rage inact: min 1 UI/dosevaccin injectable sc, imPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 dose (1 ml), aubesoin 2e vac après 4 semRevac:1 dose/anPeut être administré simultanément àParvodog® ou Trivirovax®OOI-DOI : pas d’informationf<strong>la</strong>con 10 x 1 doseR/iVANGUARD CPV-LEPTO (Pfizer A.H.)parvovirus canin att (NL-35-D):min 10exp 7 CCID50/mlL. Canico<strong>la</strong> inact (C-51): min 40 UPH/mlL. Icterohaemorrhagiae inact (NADL):min 40 UPH/mlvaccin injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose (1 ml), 1 dose deVanguard Lepto® après 14 jCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, CPV: 12 mf<strong>la</strong>con 25 x 1 doseR/VANGUARD DA2PI-CPV-LEPTO (Pfizer A.H.)- fraction liquide:parvovirus canin att (NL-35-D):min 10exp 7 DICC50/mlL. Canico<strong>la</strong> inact: min 40 HPU/mlL. Icterohaemorrhagiae inact: min 40 HPU/ml- fraction lyophilisée:virus att de <strong>la</strong> ma<strong>la</strong>die de Carré <strong>du</strong> chien(N-CDV): min 10exp 3 DICC50/m<strong>la</strong>dénovirus canin type 2 att (Manhattan):min 10exp 3,2 DICC50/mlvirus parainfluenza canin type 5 att (NL CPI 5):min 10exp 6 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Ca (âge > 12 sem): 1 dose, revac avecVanguard Lepto® après 2 - 3 semCa (âge 6 - 12 sem): 2 x 1 dose avec aumoins 14 j d’intervalle, 2e dose après l’âgede 12 semRevac:1 dose/anOOI: CPV: 7 j, autres: 3 sem après vacDOI: Leptosp: 12 m, PI: 12 m, CPV: 12 m, CDV,CAV: non démontréf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/13.1.10.3 Vaccins antiparasitairespour le chienLeishmania infantumLa leishmaniose est une zoonose provoquéepar Leishmania infantum, unparasite protozoaire transmis par desphlébotomes. Ce parasite est endémiquedans le bassin méditerranéen,en Asie et en Amérique centrale etAmérique <strong>du</strong> Sud. Sans vecteur dansnos régions, <strong>la</strong> leishmaniose reste pourl’instant une ma<strong>la</strong>die importée. Le réservoirprincipal de L. infantum est lechien. L’évolution de l’infection est trèsvariable. Certains chiens développent<strong>la</strong> ma<strong>la</strong>die tandis que d’autres restentdes porteurs sains ou guérissent spontanément.L’émergence de <strong>la</strong> ma<strong>la</strong>diedépend de l’immunité indivi<strong>du</strong>elle del’animal. Le tableau clinique varie selonles organes atteints. L’évolution de <strong>la</strong>ma<strong>la</strong>die est lente. Il s’agit d’une ma<strong>la</strong>diechronique à manifestation cutanée et/ou viscérale. Chez l’homme, L. infantumprovoque <strong>la</strong> leishmaniose viscérale, touchantplus particulièrement les enfants.VaccinCe vaccin contient des protéines excrétéessécrétées de Leishmania infantum.Ces protéines interviennent dansle cycle de vie <strong>du</strong> parasite et in<strong>du</strong>isentune immunité cellu<strong>la</strong>ire chez les chiensvaccinés. Les protéines se présententsous forme de lyophilisat à reconstituerdans une solution isotonique de chlorurede sodium. La primovaccination
13 VACCINS POUR LE CHIEN 283parvovirus caninadénovirus canin 2virus de <strong>la</strong> ma<strong>la</strong>die de Carrévirus para-influenzaherpèsvirus caninBordetel<strong>la</strong> bronchisepticavirus de <strong>la</strong> rageLeptospira IctérohaemorrhagiaeLeptospira Canico<strong>la</strong>Leishmania infantumEURICAN CHP/PI2MerialEURICAN HERPES 205MerialISTOLEPTMerialLEPTORABISINMerialNOBIVAC BbPiMSD A.H.NOBIVAC DHPMSD A.H.NOBI-VAC DHPPIMSD A.H.NOBIVAC LEPTOMSD A.H.NOBIVAC PARVO-CMSD A.H.NOBIVAC PiMSD A.H.NOBIVAC PUPPY DPMSD A.H.NOBIVAC RABIESMSD A.H.PARVODOGMerialPNEUMODOGMerialPRIMODOGMerialRABDOMUNPfizer A.H.RABISINMerialTRIVIROVAXMerialVANGUARD CPVPfizer A.H.VANGUARD CPV-LEPTOPfizer A.H.x x x xxx xx x xx xx x xx x x xx xxxx xxxx xxxxx x xxx x x
28413 VACCINS POUR LE CHATparvovirus caninadénovirus canin 2virus de <strong>la</strong> ma<strong>la</strong>die de Carrévirus para-influenzaherpèsvirus caninBordetel<strong>la</strong> bronchisepticavirus de <strong>la</strong> rageLeptospira IctérohaemorrhagiaeLeptospira Canico<strong>la</strong>Leishmania infantumVANGUARD DA2PI-CPVPfizer A.H.VANGUARD DA2PI-CPV-LEPTOPfizer A.H.VANGUARD LEPTOPfizer A.H.x x x xx x x x x xx x13.1.11 Vaccins pour le chat13.1.11.1 Vaccination contre lesma<strong>la</strong>dies virales <strong>du</strong> chatLa vaccination des chats avec desvaccins viraux a non seulement pourbut de prévenir <strong>la</strong> ma<strong>la</strong>die (protectionclinique) mais assure également uneprotection virologique. Cette protectionvirologique con<strong>du</strong>it à une excrétionré<strong>du</strong>ite <strong>du</strong> virus lors d’une infection parun virus sauvage, un risque d’infectionplus faible et une transmission viralemoins importante. La vaccination viseà protéger l’indivi<strong>du</strong> vacciné ainsi qu’àassurer une protection temporaire desnouveau-nés par le biais d’anticorpsdans le colostrum (immunité passive).Le degré de protection obtenupar <strong>la</strong> vaccination dépend de l’immunitéengendrée. L’immunité maternelle,l’immunosuppression, <strong>la</strong> ma<strong>la</strong>die etles situations de stress sont autant defacteurs qui peuvent compromettrel’édification de l’immunité après <strong>la</strong>vaccination. C’est en fonction desconditions d’environnement telles quele risque d’infection, <strong>la</strong> voie d’infectionet l’âge de l’animal que l’immunitéengendrée par <strong>la</strong> vaccination sera enmesure ou non d’arrêter <strong>la</strong> ma<strong>la</strong>die.Outre <strong>la</strong> vaccination, d’autres mesuresdoivent impérativement être prises afinde ré<strong>du</strong>ire le risque d’infection : nettoyageet désinfection des locaux et<strong>du</strong> matériel, amélioration de l’aérationet séparation des animaux sensiblesdes animaux excréteurs de virus. Enraison de toutes ces circonstancesinfluentes, il est important de mettreau point une stratégie de vaccinationadaptée à chaque propriétaire et àchaque animal et, si nécessaire, deprendre des mesures sanitaires supplémentaires.(voir Folia Veterinaria2007 n° 3 et Folia Veterinaria 2010n°1 ; Folia Veterinaria 2012 n° 3)Panleucopénie félineLa panleucopénie féline est engendréepar le parvovirus félin et se caractérisepar de <strong>la</strong> fièvre, de <strong>la</strong> léthargie, de l’anorexie,des vomissements, de <strong>la</strong> diarrhéeet de <strong>la</strong> déshydratation. Une leucopénieprononcée est observée <strong>du</strong> pointde vue hématologique. La mortalité serencontre surtout chez les chatons. Levirus est transmis de manière orofécalemais également transp<strong>la</strong>centaire.L’infection précoce d’embryons et defœtus entraîne <strong>la</strong> mortalité suivie d’unerésorption ou d’un avortement. Lorsquel’infection des fœtus a lieu alors que <strong>la</strong>gestation est déjà plus avancée, elleengendre une hypop<strong>la</strong>sie cérébelleuse.Le virus étant très résistant, il reste infectieux<strong>du</strong>rant des mois. Il se transmetfacilement par le biais de matériel ou depersonnel contaminés.VaccinDes vaccins à parvovirus atténuéset inactivés sont disponibles sur le
13 VACCINS POUR LE CHAT 285marché, et sont en général combinés(parvovirus félin et virus de <strong>la</strong>rhinotrachéite virale féline / calicivirusfélin / Ch<strong>la</strong>mydophi<strong>la</strong> felis / virusde <strong>la</strong> leucose féline) afin de ré<strong>du</strong>ire lenombre d’injections.ProtectionL’immunité colostrale assure une protection<strong>du</strong>rant les premières semainesde <strong>la</strong> vie <strong>du</strong> chat, cette période étantcelle où sa sensibilité est <strong>la</strong> plusgrande. Des revaccinations sont doncconseillées chez les chattes repro<strong>du</strong>ctrices.L’immunité maternelle interférantavec l’édification de l’immunitéactive, <strong>la</strong> primovaccination se fera depréférence après disparition des anticorpsd’origine maternelle.Particu<strong>la</strong>ritésVu <strong>la</strong> résistance <strong>du</strong> parvovirus, un nettoyageet une désinfection insuffisantsdes locaux et <strong>du</strong> matériel contaminéspeuvent contribuer à augmenter sérieusementle risque d’infection. Cecipourrait avoir comme conséquencele franchissement de <strong>la</strong> barrière del’immunité maternelle par le virus sauvageavant même <strong>la</strong> première vaccination.Les résultats de <strong>la</strong> vaccinationseule pourraient alors se révéler décevants.C’est pour cette raison qu’ilest conseillé d’assurer <strong>la</strong> séparationdes chats sensibles et des excréteurspotentiels, et le nettoyage et <strong>la</strong> désinfectionde l’environnement. Vaccins combinés à parvovirusatténuéFELIGEN CRP (Virbac)virus att de <strong>la</strong> panleucopénie féline (LR 72):min 10exp 3,7 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (F2):min 10exp 5,0 DICT50/mlcalicivirus félin (F9) att: min 10exp 4,6 DICT50/mlvaccin lyophilisé et solvant injectable sc, imPosologie:Primovac:Fe (âge 9 sem): 2 x 1 dose à 3 semd’intervalleRevac:1 dose/an ou 1 dose/6 m si risque d’infect.élevéOOI: 3 sem après FPV, 4 sem après FCV et FRVDOI: 1 anf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvant50 x 1 dose + 50 x 1 ml de solvantR/FELOCELL CVR (Eli Lilly)virus att de <strong>la</strong> panleucopénie féline (SnowLeopard): min 10exp 3 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin att (F-9): min 10exp 5,5 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose (1 ml) à3 - 4 sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 mf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/FELOCELL CVR-C (Eli Lilly)virus att de <strong>la</strong> panleucopénie féline (SnowLeopard): min 10exp 3 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin att (F-9): min 10exp 5,5 DICT50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) att:min 10exp 3,2 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose (1 ml) à 3 - 4sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 m, FCp: pas d’infof<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/LEUCOFELIGEN FeLV/RCP (Virbac)- lyophilisat:calicivirus félin viv (souche F9):10 exp4,6 -10 exp6,1 DICC50/mlvirus viv de <strong>la</strong> rhinotrachéite virale féline (soucheF2): 10 exp5,0 -10 exp6,6 DICC50/mlvirus viv de <strong>la</strong> panleucopénie féline (souche LR72): 10 exp3,7 -10 exp4,5 DICC50/ml- solvant: antigène purifié p45 de l’enveloppe<strong>du</strong> FeLV: min 102 µgAdjuv: hydroxyde d’aluminium, saponinevaccin lyophilise et solvant injectable scPosologie:Fe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleFe avec imm mat: 3e dose dès l’âge de15 semRevac: 1 x/anOOI: 3 sem après 1e vac (FPV, FeLV), 4 semaprès 1e vac (FCV, FRV)DOI: 1 an après 1e vac10 f<strong>la</strong>cons de lyophilisat + 10 f<strong>la</strong>cons de solvant50 f<strong>la</strong>cons de lyophilisat + 50 f<strong>la</strong>cons de solvantR/
28613 VACCINS POUR LE CHATNOBIVAC TRICAT TRIO (MSD A.H.)par dose (1 ml):calicivirus félin att (souche F9):min 4,6 log10 pfuherpèsvirus att de <strong>la</strong> rhinotrachéite féline type 1(souche G2620A): min 5,2 log10 pfuvirus att de <strong>la</strong> panleucopénie féline (soucheMW-1): min. 4,3 log10 CCID50vaccin lyophilisé injectable scPosologie:Primovac:Fe (âge > 8 - 9 sem) 2 x 1 dose à 3 - 4 semd’intervalle (2e dose après l’âge de 12 sem)Revac:1 dose/an contre le calicivirus félin, l’herpèsvirusde <strong>la</strong> rhinotrachéite féline (BR),1 dose/3 ans contre <strong>la</strong> panleucopénie féline(souche MW-1)OOI: FCV et FHV: 4 sem, FPV: 3 semDOI: FCV, FHV: 1 an, FPV: 3 ansf<strong>la</strong>con 10 x 1 doseR/PUREVAX RCP (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose ettous les 3 ans pour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après vac de base FPV, FRV et FCVDOI: FRV et FCV: 1 an, FPV: 3 ansf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCPCh (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ ch<strong>la</strong>mydiose, et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après vac de base FPV, C. felis,FRV, FCVDOI: FRV, FCV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCPCh FeLV (Merial)- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/ml- solvant: virus canarypox recombiné FeLV(vCP97): min 10 exp7.2 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose +ch<strong>la</strong>mydiose + leucose, et tous les 3 anspour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV, C. felis: 1 sem après vacde base, FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCP FeLV (Merial)- solvant:virus canarypox, recombinant FeLV (vCP97):min 10 exp7.2 DICC50/ml- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4,9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3,5 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe imm mat (âge > 12 sem):2 x 1 dose (1 ml) à 3 - 4 sem d’intervalle- Fe pas d’imm mat (âge > 8 sem):2 x 1 dose (1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ leucémie féline et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV: 1 sem après vac de base,FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV: 1 an après revac, FPV:3 ans après revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/
13 VACCINS POUR LE CHAT 287 Vaccins combinés à parvovirusinactivéFEVAXYN i-CHP (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): min 5,69/0,2 ml puissance re<strong>la</strong>tivecalicivirus félin inact (souche 255):min 1,50/0,5 ml puissance re<strong>la</strong>tivevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): min 1,39/0,1 ml puissance re<strong>la</strong>tiveadjuv: copolymère éthylène-anhydride maléiquenéocryl XK 62, émulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac: 1 dose/anOOI: 2 sem après primovacDOI: 1 anseringue 10 x 1 dose (1 ml)R/FEVAXYN i-CHP Ch<strong>la</strong>m (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): min 5,69/0,2 ml puissance re<strong>la</strong>tivecalicivirus inact (souche 255):min 1,50/0,5 ml puissance re<strong>la</strong>tivevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): min 1,39/0,1 ml puissance re<strong>la</strong>tiveCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) inact(Cello): min 1,69/0,01 ml puissance re<strong>la</strong>tiveadjuv: copolymère éthylène-anhydride maléique,néocryl XK, emulsigen SAvaccin injectable scPosologie:PrimovacFe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac: 1 dose/anOOI: 2 sem après primovacDOI: 1 anseringue 10 x 1 dose (1 ml)R/FEVAXYN PENTOFEL (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): R.P 9.5-12.25/dosecalicivirus félin inact (souche 225):R.P 1.65-2.15/dosevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): R.P 1.60-2.10/doseCh<strong>la</strong>mydophi<strong>la</strong> felis inact (Ch<strong>la</strong>mydia psittaci)(Cello): R.P 2.00-2.30 /dosevirus inact de <strong>la</strong> leucémie féline (souche 61E):R.P 1.45-2.0/doseadjuv: EMA, néocryl A640, emulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac:1 dose/anOOI-DOI: pas d’infoseringues 10 x 1 dose, 25 x 1 doseR/Vaccins contre le coryza félinLe coryza félin est un complexe respiratoireimpliquant principalement deuxvirus : le virus de <strong>la</strong> rhinotrachéite féline(herpèsvirus félin 1) et le calicivirusfélin. Tous deux sont présents de manièreenzootique au sein de <strong>la</strong> popu<strong>la</strong>tionféline. Les infections apparaissentsurtout après disparition de l’immunitématernelle. La résistance de l’herpèsvirusétant faible, il perd rapidementson caractère infectieux après excrétion.Il se transmet principalement parcontact direct et aérogène avec defines gouttes de sécrétion nasale éternuéespar des chats contaminés ouoralement par ingestion de sécrétionscontaminées (salive, sécrétion nasaleou liquide <strong>la</strong>crymal). Le calicivirus setransmet de manière analogue. Cevirus étant plus stable que l’herpèsvirus,il demeure plus longtemps infectieuxet peut également être transmisde manière mécanique. D’un pointde vue épidémiologique, les chatssouffrant d’une infection aiguë constituentles principales sources virales.Ils excrètent le virus en très grandesquantités. L’herpèsvirus ainsi que lecalicivirus peuvent cependant égalementrester présents chez l’hôte.L’herpèsvirus est présent de manière<strong>la</strong>tente dans le ganglion trijumeauet peut être réactivé et de nouveauexcrété lors de situations de stress.Le calicivirus peut persister après uneinfection aiguë au niveau de <strong>la</strong> gorge.Il est alors excrété de manière continueen quantités minimes. L’excrétionde virus par des chats immuniséscontribue à maintenir les calicivirus etles herpèsvirus au sein de <strong>la</strong> popu<strong>la</strong>tionféline <strong>du</strong>rant l’absence temporaired’infections aiguës. Les signescliniques dépendent <strong>du</strong> virus, de <strong>la</strong>souche virale (surtout importante pourle calicivirus), de <strong>la</strong> dose d’infection,de l’âge, de <strong>la</strong> réponse immunitaire <strong>du</strong>chat et de <strong>la</strong> présence ou non d’uneimmunité maternelle. Les infectionsobservées chez le chat a<strong>du</strong>lte sont enmajeure partie subcliniques. Chez lesjeunes chatons sans immunité maternelle,les signes cliniques observéssont graves : fièvre, anorexie, éternuements,sécrétions mucopurulentesnasales et ocu<strong>la</strong>ires, ulcérations et déglutitiondifficile. Il existe quelques différencesdans les syndromes causéspar les deux virus respiratoires. Dansle cas d’une infection avec l’herpèsvirus,le chat présente des signes générauxet les yeux sont plus gravementatteints. Dans le cas d’une infectionpar le calicivirus, on observe fréquemmentdes ulcérations dans <strong>la</strong> cavitébuccale et des boiteries.
28813 VACCINS POUR LE CHATVaccinLes vaccins contre le coryza félin sontconstitués des deux composantesvirales, et sont disponibles sous formeinactivée et sous forme atténuée. Labactérie Ch<strong>la</strong>mydophi<strong>la</strong> felis pouvantêtre impliquée dans le coryza félin, lesvaccins sont parfois complétés parcette composante bactérienne. Afind’éviter le nombre de vaccinations,d’autres composantes virales sont parfoisajoutées (virus de <strong>la</strong> panleucopénieet de <strong>la</strong> leucose féline, par exemple).ProtectionIl est conseillé de revacciner régulièrementles chattes afin d’augmenter aumaximum <strong>la</strong> concentration d’anticorpsdans le colostrum. De cette façon, leschatons bénéficient d’une protectionavant <strong>la</strong> primovaccination. La vaccinationcontre le coryza félin est effectuéeaprès disparition de l’immunité maternellecar celle-ci peut interférer avecl’édification d’une immunité active.Particu<strong>la</strong>ritésLorsque le risque d’infection est élevé,des infections à virus sauvage peuventapparaître avant <strong>la</strong> vaccination, ce quioblige alors de prendre des mesuressupplémentaires telles que le nettoyage,<strong>la</strong> désinfection des lieux et<strong>la</strong> séparation des chats qui n’ont pasencore été vaccinés des excréteursde virus potentiels (infections aiguës,<strong>la</strong>tentes ou chroniques). Cette dernièremesure peut être prise en iso<strong>la</strong>nt <strong>la</strong>mère et ses chatons dans un lieu biendésinfecté et de séparer <strong>la</strong> mère, quipeut être un excréteur potentiel <strong>du</strong>virus, des chatons avant <strong>la</strong> disparitionde <strong>la</strong> protection assurée par l’immunitématernelle (à l’âge de 5 semaines). Vaccins combinés contre lecoryza félin à herpèsvirus atténuéet calicivirus atténuéFELIGEN CRP (Virbac)virus att de <strong>la</strong> panleucopénie féline (LR 72):min 10exp 3,7 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (F2):min 10exp 5,0 DICT50/mlcalicivirus félin (F9) att: min 10exp 4,6 DICT50/mlvaccin lyophilisé et solvant injectable sc, imPosologie:Primovac:Fe (âge 9 sem): 2 x 1 dose à 3 semd’intervalleRevac:1 dose/an ou 1 dose/6 m si risque d’infect.élevéOOI: 3 sem après FPV, 4 sem après FCV et FRVDOI: 1 anf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvant50 x 1 dose + 50 x 1 ml de solvantR/FELOCELL CVR (Eli Lilly)virus att de <strong>la</strong> panleucopénie féline (SnowLeopard): min 10exp 3 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin att (F-9): min 10exp 5,5 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose (1 ml) à 3 - 4sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 mf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/FELOCELL CVR-C (Eli Lilly)virus att de <strong>la</strong> panleucopénie féline (SnowLeopard): min 10exp 3 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin att (F-9): min 10exp 5,5 DICT50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) att:min 10exp 3,2 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose (1 ml) à 3 - 4sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 m, FCp: pas d’infof<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/FELOCELL RC (Eli Lilly)virus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin (F9) att: min 10exp 5,5 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac: Fe (âge > 9 sem):2 x 1 dose à 3 - 4 sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 mf<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/LEUCOFELIGEN FeLV/RCP (Virbac)- lyophilisat:calicivirus félin viv (souche F9):10 exp4,6 -10 exp6,1 DICC50/mlvirus viv de <strong>la</strong> rhinotrachéite virale féline (soucheF2): 10 exp5,0 -10 exp6,6 DICC50/mlvirus viv de <strong>la</strong> panleucopénie féline (souche LR72): 10 exp3,7 -10 exp4,5 DICC50/ml- solvant: antigène purifié p45 de l’enveloppe<strong>du</strong> FeLV: min 102 µgAdjuv: hydroxyde d’aluminium, saponinevaccin lyophilise et solvant injectable scPosologie:Fe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleFe avec imm mat: 3e dose dès l’âge de15 semRevac: 1 x/anOOI: 3 sem après 1e vac (FPV, FeLV), 4 semaprès 1e vac (FCV, FRV)DOI: 1 an après 1e vac10 f<strong>la</strong>cons de lyophilisat + 10 f<strong>la</strong>cons de solvant50 f<strong>la</strong>cons de lyophilisat + 50 f<strong>la</strong>cons de solvantR/
13 VACCINS POUR LE CHAT 289NOBIVAC DUCAT (MSD A.H.)virus att de <strong>la</strong> rhinotrachéite féline, soucheG2620A: min 4,8 log10 TCID50/dosecalicivirus félin att, souche F9:min 4,6 log10 PFU/dosevaccin lyophilisé et solvant pour suspensioninjectable scPosologie:Primovac:Fe (âge min 8 sem): 2 x 1 ml à 3 - 4 semd’intervalleRevac: annuellementOOI: 4 semDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/NOBIVAC TRICAT TRIO (MSD A.H.)par dose (1 ml):calicivirus félin att (souche F9): min 4,6 log10 pfuherpèsvirus att de <strong>la</strong> rhinotrachéite féline type 1(souche G2620A): min 5,2 log10 pfuvirus att de <strong>la</strong> panleucopénie féline (soucheMW-1): min. 4,3 log10 CCID50vaccin lyophilisé injectable scPosologie:Primovac:Fe (âge > 8 - 9 sem) 2 x 1 dose à 3 - 4 semd’intervalle (2e dose après l’âge de 12 sem)Revac:1 dose/an contre le calicivirus félin, l’herpèsvirusde <strong>la</strong> rhinotrachéite féline (BR),1 dose/3 ans contre <strong>la</strong> panleucopénie féline(souche MW-1)OOI: FCV et FHV: 4 sem, FPV: 3 semDOI: FCV, FHV: 1 an, FPV: 3 ansf<strong>la</strong>con 10 x 1 doseR/ Vaccins combinés contre lecoryza félin à herpèsvirus atténuéet calicivirus inactivésPUREVAX RC (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: annuellementNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après primovac rhinotrachéite etcalicivirusDOI: 1 anf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCP (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose ettous les 3 ans pour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après vac de base FPV, FRV et FCVDOI: FRV et FCV: 1 an, FPV: 3 ansf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCP FeLV (Merial)- solvant:virus canarypox, recombinant FeLV (vCP97):min 10 exp7.2 DICC50/ml- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4,9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3,5 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe imm mat (âge > 12 sem):2 x 1 dose (1 ml) à 3 - 4 sem d’intervalle- Fe pas d’imm mat (âge > 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ leucémie féline et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV: 1 sem après vac de base,FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV: 1 an après revac, FPV:3 ans après revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/
29013 VACCINS POUR LE CHATPUREVAX RCPCh (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ ch<strong>la</strong>mydiose, et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après vac de base FPV, C. felis,FRV, FCVDOI: FRV, FCV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCPCh FeLV (Merial)- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/ml- solvant: virus canarypox recombiné FeLV(vCP97): min 10 exp7.2 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose +ch<strong>la</strong>mydiose + leucose, et tous les 3 anspour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV, C. felis: 1 sem après vacde base, FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/ Vaccins combinés contre lecoryza félin à herpèsvirusinactivé et calicivirus inactivéFEVAXYN i-CHP (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): min 5,69/0,2 ml puissance re<strong>la</strong>tivecalicivirus félin inact (souche 255):min 1,50/0,5 ml puissance re<strong>la</strong>tivevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): min 1,39/0,1 ml puissance re<strong>la</strong>tiveadjuv: copolymère éthylène-anhydride maléiquenéocryl XK 62, émulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac: 1 dose/anOOI: 2 sem après primovacDOI: 1 anseringue 10 x 1 dose (1 ml)R/FEVAXYN i-CHP Ch<strong>la</strong>m (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): min 5,69/0,2 ml puissance re<strong>la</strong>tivecalicivirus inact (souche 255):min 1,50/0,5 ml puissance re<strong>la</strong>tivevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): min 1,39/0,1 ml puissance re<strong>la</strong>tiveCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) inact(Cello): min 1,69/0,01 ml puissance re<strong>la</strong>tiveadjuv: copolymère éthylène-anhydride maléique,néocryl XK, emulsigen SAvaccin injectable scPosologie:PrimovacFe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac: 1 dose/anOOI: 2 sem après primovacDOI: 1 anseringue 10 x 1 dose (1 ml)R/FEVAXYN PENTOFEL (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): R.P 9.5-12.25/dosecalicivirus félin inact (souche 225):R.P 1.65-2.15/dosevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): R.P 1.60-2.10/doseCh<strong>la</strong>mydophi<strong>la</strong> felis inact (Ch<strong>la</strong>mydia psittaci)(Cello): R.P 2.00-2.30 /dosevirus inact de <strong>la</strong> leucémie féline (souche 61E):R.P 1.45-2.0/doseadjuv: EMA, néocryl A640, emulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac:1 dose/anOOI-DOI: pas d’infoseringues 10 x 1 dose, 25 x 1 doseR/Virus de <strong>la</strong> leucose félineLe virus de <strong>la</strong> leucose féline n’est pastrès répan<strong>du</strong>. Il apparaît principalementchez les chats errants et les chatsvivant à l’extérieur, dans certainesrégions. Ce virus étant très instable en
13 VACCINS POUR LE CHAT 291milieu extérieur, sa transmission n’estpossible que par contact très direct. Levirus est excrété par <strong>la</strong> salive d’excréteurspersistants et transmis lors debatailles ou de léchages. La transmission<strong>du</strong> virus peut également se fairelors de l’accouplement, par voie transp<strong>la</strong>centaire,pendant <strong>la</strong> mise bas et lorsde l’ingestion <strong>du</strong> colostrum ou de <strong>la</strong>it.Il existe trois types de virus de leucoseféline: A, B et C. C’est principalementle type A qui engendre des infections,tandis que les types B et C sont formésau moyen d’une recombinaison <strong>du</strong> typeA avec <strong>du</strong> matériel génétique endogènede virus de <strong>la</strong> leucose féline qui a étéintégré au cours de l’évolution dans legénome <strong>du</strong> chat et qui sont transmisà <strong>la</strong> descendance par le biais des gamètes.Si l’animal a été en contact avecle virus de <strong>la</strong> leucose féline, il s’ensuitune multiplication dans les cellules enmitose au niveau de l’organisme entier.Cette phase de l’infection se déroule demanière subclinique. Par l’édificationd’une immunité adéquate, le chat peutempêcher l’instal<strong>la</strong>tion d’une virémiepersistante ou repousser le virus dansun état <strong>la</strong>tent dans <strong>la</strong> moelle osseuse.Le virus persiste cependant chez certainschats. Ils sont alors virémiqueset excrètent de manière continue levirus par le biais de chaque sécrétionet excrétion. De ce fait, ils constituentun danger permanent pour les chatssensibles. Les signes cliniques, quisont l’immunosuppression, l’anémie,l’apparition de tumeurs, <strong>la</strong> diarrhée etdes troubles de <strong>la</strong> repro<strong>du</strong>ction, ne sontobservés que chez les chats virémiquespersistants.VaccinIl existe, outre des vaccins inactivésou à sous-unités, un vaccin recombinantformé <strong>du</strong> virus de <strong>la</strong> variole decanari. Le génome viral recombinant aintégré les gènes codant les antigènes<strong>du</strong> FeLV qui sont exprimés lors de <strong>la</strong>vaccination.ProtectionIl est nécessaire de déterminer l’étatvirologique <strong>du</strong> chat avant <strong>la</strong> vaccination.Il est en effet déconseillé devacciner des chats virémiques car ilspeuvent développer <strong>la</strong> ma<strong>la</strong>die malgré<strong>la</strong> vaccination. Ceci pourrait porter àcroire, à tort, que le vaccin est inefficace.La vaccination des chats contre<strong>la</strong> leucose féline a pour but de limiterau maximum <strong>la</strong> multiplication <strong>du</strong> virusen cas de contact avec un virus sauvage,afin d’éviter <strong>la</strong> persistance etl’excrétion <strong>du</strong> virus ainsi que les signescliniques.Particu<strong>la</strong>ritésLa vaccination est à conseiller dansles régions où le nombre de chats virémiquesest important et dans le casoù le chat pourrait entrer en contactavec des chats errants. Les éleveursde chats ont tout intérêt à s’assurer,outre <strong>la</strong> vaccination, à l’absence d’infectionpar le virus de <strong>la</strong> leucose féline.Pour y parvenir, il faut analyser le sangdes chats présents afin d’y déceler <strong>la</strong>présence ou non d’antigènes viraux,puis exclure les chats virémiques persistants.De cette manière, on éliminetoute source virale. Vaccins monovalents à FeLVinactivé ou sous-unitaireLEUCOGEN (Virbac)virus de <strong>la</strong> leucémie féline, recombinant purif.p45: min 102 mcgAdjuv: hydroxyde d’aluminium, saponinevaccin injectable sc, imPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 15 - 21 jd’intervalleRevac:1 dose/anOOI-DOI: pas d’infof<strong>la</strong>con 10 x 1 dose50 x 1 doseR/LEUKOCELL 2 doses (Pfizer A.H.)protéines virales <strong>du</strong> virus de <strong>la</strong> leucémie félinegp 70: min 1334 ng Ag/mlvaccin injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac:1 dose/anOOI: 3 sem après 2e injDOI: pas d’infof<strong>la</strong>con 10 x 1 dose25 x 1 doseR/ Vaccin recombinant <strong>du</strong> virus de<strong>la</strong> variole de canari exprimant lesantigènes <strong>du</strong> FeLVPUREVAX FeLV (Merial)FeLV, recombinant virus de <strong>la</strong> variole <strong>du</strong> canari(vCP97): 10exp 7,2 CCID50vaccin injectable scPosologie:Primovac:Fe (âge > 8 sem): 2 x 1 dose (1 ml) à 3 - 5sem d’intervalleRevac:1 dose/anOOI: 2 sem après primovacDOI: 1 anf<strong>la</strong>con 10 x 1 doseR/
29213 VACCINS POUR LE CHAT Vaccins combinés avec unvirus vaccinal FeLV inactivé ourecombinant <strong>du</strong> virus de <strong>la</strong> variolede canariFEVAXYN PENTOFEL (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): R.P 9.5-12.25/dosecalicivirus félin inact (souche 225): R.P1.65-2.15/dosevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): R.P 1.60-2.10/doseCh<strong>la</strong>mydophi<strong>la</strong> felis inact (Ch<strong>la</strong>mydia psittaci)(Cello): R.P 2.00-2.30 /dosevirus inact de <strong>la</strong> leucémie féline (souche 61E):R.P 1.45-2.0/doseadjuv: EMA, néocryl A640, emulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac:1 dose/anOOI-DOI: pas d’infoseringues 10 x 1 dose, 25 x 1 doseR/LEUCOFELIGEN FeLV/RCP (Virbac)- lyophilisat:calicivirus félin viv (souche F9):10 exp4,6 -10 exp6,1 DICC50/mlvirus viv de <strong>la</strong> rhinotrachéite virale féline (soucheF2): 10 exp5,0 -10 exp6,6 DICC50/mlvirus viv de <strong>la</strong> panleucopénie féline (souche LR72): 10 exp3,7 -10 exp4,5 DICC50/ml- solvant: antigène purifié p45 de l’enveloppe<strong>du</strong> FeLV: min 102 µgAdjuv: hydroxyde d’aluminium, saponinevaccin lyophilise et solvant injectable scPosologie:Fe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleFe avec imm mat: 3e dose dès l’âge de15 semRevac: 1 x/anOOI: 3 sem après 1e vac (FPV, FeLV), 4 semaprès 1e vac (FCV, FRV)DOI: 1 an après 1e vac10 f<strong>la</strong>cons de lyophilisat + 10 f<strong>la</strong>cons de solvant50 f<strong>la</strong>cons de lyophilisat + 50 f<strong>la</strong>cons de solvantR/PUREVAX RCP FeLV (Merial)- solvant:virus canarypox, recombinant FeLV (vCP97):min 10 exp7.2 DICC50/ml- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4,9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3,5 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe imm mat (âge > 12 sem):2 x 1 dose (1 ml) à 3 - 4 sem d’intervalle- Fe pas d’imm mat (âge > 8 sem):2 x 1 dose (1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ leucémie féline et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV: 1 sem après vac de base,FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV: 1 an après revac, FPV:3 ans après revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCPCh FeLV (Merial)- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/ml- solvant: virus canarypox recombiné FeLV(vCP97): min 10 exp7.2 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose +ch<strong>la</strong>mydiose + leucose, et tous les 3 anspour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV, C. felis: 1 sem après vacde base, FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/Vaccin contre <strong>la</strong> péritonite infectieusefélineLes coronavirus félins peuvent êtrec<strong>la</strong>ssés selon deux biotypes: lescoronavirus félins entériques qui necausent qu’une diarrhée momentanéeet les virus de <strong>la</strong> péritonite infectieuseféline qui engendrent une pleurésie/péritonite/péricardite chroniques etexsudatives, et dont l’issue est fatale.On a c<strong>la</strong>irement pu observer que c’estle biotype entérique qui engendre le
13 VACCINS POUR LE CHAT 293biotype de <strong>la</strong> péritonite par mutation.Cette mutation aide le coronavirus àéchapper à l’immunité, et de ce fait, àpersister au sein de l’organisme hôte.Le biotype entérique est présent demanière enzootique dans <strong>la</strong> plupartdes élevages de chats. Il infecte lesjeunes chatons de manière généraliséeaprès le sevrage. Le risque demutation étant corrélé à <strong>la</strong> quantité devirus pro<strong>du</strong>it, <strong>la</strong> plupart des cas de péritoniteinfectieuse féline apparaissentlorsque le risque d’infection par descoronavirus entériques félins est élevé.VaccinUn seul vaccin est disponible, et contientun virus mutant thermosensible.ProtectionLes chats séronégatifs sont vaccinés.Le vaccin est administré par voie intranasale,et stimule une réaction immunitairelocale (IgA et réaction immunitaireà médiation cellu<strong>la</strong>ire).Particu<strong>la</strong>ritésOn peut prévenir <strong>la</strong> péritonite infectieuseféline: (a) par <strong>la</strong> protection deschatons contre une infection par levirus sauvage avant <strong>la</strong> vaccination, enséparant <strong>la</strong> mère et ses chatons desexcréteurs de virus potentiels (chatonsinfectés et excréteurs persistants) eten anticipant le sevrage (<strong>la</strong> mère peutêtre un excréteur potentiel); (b) puispar <strong>la</strong> vaccination des chatons séronégatifset, (c) par <strong>la</strong> ré<strong>du</strong>ction <strong>du</strong> risqued’infection au moyen de mesuressanitaires.PRIMUCELL FIP (Pfizer A.H.)virus att de <strong>la</strong> péritonite infectieuse féline(Norden DF2): min 10exp 4,8 DICT50/dosevaccin lyophilisé et solvant inasPosologie:Primovac:Fe (âge > 16 sem): 2 x 1 dose à 3 semd’intervalleRevac:1 dose/anCe vac peut être administré simultanémentà Felocell CVR-C®, Felocell CVR® etFelocell RC®OOI: 3 sem après 2ième dos primovacDOI: 12 mf<strong>la</strong>con 10 x 1 dose + solvant25 x 1 dose + solvantR/13.1.11.2 Vaccins bactériens pourle chatCh<strong>la</strong>mydophi<strong>la</strong> felisLa ma<strong>la</strong>die engendrée par Ch<strong>la</strong>mydophi<strong>la</strong>felis apparaît surtout chez leschats vivant en groupe, comme, parexemple, dans les magasins d’animaux,les refuges et les élevages.Les animaux sont généralementinfectés par C. felis en bas âge. Unetelle affection engendre au départ unécoulement ocu<strong>la</strong>ire séreux, un blépharospasme,<strong>du</strong> chemosis et unehyperémie conjonctivale. La conjonctivitepeut être uni<strong>la</strong>térale au début,puis affecter l’autre oeil, en général1 à 3 semaines plus tard. Dans unstade plus avancé de <strong>la</strong> ma<strong>la</strong>die, desinfections bactériennes secondairesapparaissent et l’écoulement devientmucopurulent. Une rhinite accompagnéed’écoulement nasal et d’éternuementspeut également faire partie dessignes cliniques observés. La conjonctivitedisparaît spontanément, sanstraitement, après 3 à 4 semaines. Ellepeut cependant persister dans certainscas pendant 8 semaines voire plus. Laplupart des chats se rétablissent enfin de compte, mais <strong>la</strong> ma<strong>la</strong>die peutrécidiver. On a par ailleurs démontréque l’agent pathogène est toujourssusceptible d’être isolé un an et demiaprès l’infection.VaccinOn peut administrer des vaccins inactivésou atténués. Les vaccins disponiblessont combinés à des valencesvirales.ProtectionPour <strong>la</strong> primovaccination des animauxâgés de 8 – 9 semaines ou plus, onadministrera deux doses, à 3 ou 4 semainesd’intervalle. On tiendra comptede l’interférence des anticorps d’originematernelle jusqu’à l’âge d’environneuf semaines. La revaccination doitavoir lieu annuellement. La protectionn’est pas totale après <strong>la</strong> vaccination,mais les signes cliniques sont toutefoisnettement moins marqués et de pluscourte <strong>du</strong>rée chez les animaux vaccinés,et l’agent pathogène est excrétépendant moins longtemps.Particu<strong>la</strong>ritésLa vaccination contre C. felis est surtoutconseillée dans le cas où l’animalentre fréquemment en contact avecd’autres chats, et au sein des élevagesde chats où l’affection est endémique.
29413 VACCINS POUR LE CHATFELOCELL CVR-C (Eli Lilly)virus att de <strong>la</strong> panleucopénie féline (SnowLeopard): min 10exp 3 DICT50/mlvirus att de <strong>la</strong> rhinotrachéite féline (FVRm):min 10exp 5 DICT50/mlcalicivirus félin att (F-9):min 10exp 5,5 DICT50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) att: min10exp 3,2 DICT50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose (1 ml) à 3 - 4sem d’intervalleRevac:1 dose/anOOI: 3 sem après 2e primovacDOI: 12 m, FCp: pas d’infof<strong>la</strong>con 25 x 1 dose + 25 x 1 ml de solvantR/FEVAXYN i-CHP Ch<strong>la</strong>m (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): min 5,69/0,2 ml puissance re<strong>la</strong>tivecalicivirus inact (souche 255):min 1,50/0,5 ml puissance re<strong>la</strong>tivevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): min 1,39/0,1 ml puissance re<strong>la</strong>tiveCh<strong>la</strong>mydophi<strong>la</strong> felis (Ch<strong>la</strong>mydia psittaci) inact(Cello): min 1,69/0,01 ml puissance re<strong>la</strong>tiveadjuv: copolymère éthylène-anhydride maléique,néocryl XK, emulsigen SAvaccin injectable scPosologie:PrimovacFe (âge > 8 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac: 1 dose/anOOI: 2 sem après primovacDOI: 1 anseringue 10 x 1 dose (1 ml)R/FEVAXYN PENTOFEL (Pfizer A.H.)virus inact de <strong>la</strong> panleucopénie féline (soucheCU4): R.P 9.5-12.25/dosecalicivirus félin inact (souche 225):R.P 1.65-2.15/dosevirus inact de <strong>la</strong> rhinotrachéite féline (souche605): R.P 1.60-2.10/doseCh<strong>la</strong>mydophi<strong>la</strong> felis inact (Ch<strong>la</strong>mydia psittaci)(Cello): R.P 2.00-2.30 /dosevirus inact de <strong>la</strong> leucémie féline (souche 61E):R.P 1.45-2.0/doseadjuv: EMA, néocryl A640, emulsigen SAvaccin injectable scPosologie:Primovac:Fe (âge > 9 sem): 2 x 1 dose à 3 - 4 semd’intervalleRevac:1 dose/anOOI-DOI: pas d’infoseringues 10 x 1 dose, 25 x 1 doseR/PUREVAX RCPCh (Merial)lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose+ ch<strong>la</strong>mydiose, et tous les 3 ans pourpanleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: 1 sem après vac de base FPV, C. felis,FRV, FCVDOI: FRV, FCV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/PUREVAX RCPCh FeLV (Merial)- lyophilisat:herpèsvirus att de <strong>la</strong> rhinotrachéite féline(souche FHV F2): min 10 exp4.9 DICC50/m<strong>la</strong>ntigènes inact de <strong>la</strong> calicivirose féline (souchesFCV 431 et G1): min 2.0 U. ELISA/mlvirus att de <strong>la</strong> panleucopénie féline (PLI IV):min 10 exp3.5 DICC50/mlCh<strong>la</strong>mydophi<strong>la</strong> felis att (souche 905):min 10 exp3.0 DIO50/ml- solvant: virus canarypox recombiné FeLV(vCP97): min 10 exp7.2 DICC50/mlvaccin lyophilisé et solvant injectable scPosologie:Primovac:- Fe pas d’imm mat (âge min 8 sem): 2 x 1dose (1 ml) à 3 - 4 sem d’intervalle- Fe imm mat (âge min 12 sem): 2 x 1 dose(1 ml) à 3 - 4 sem d’intervalleRevac: 1 an après <strong>la</strong> Primovac, puis annuellementpour rhinotrachéite + calicivirose +ch<strong>la</strong>mydiose + leucose, et tous les 3 anspour panleucopénieNe pas utiliser chez les femelles gestantesou en <strong>la</strong>ctationOOI: FRV, FCV, FPV, C. felis: 1 sem après vacde base, FLV: 2 sem après vac de baseDOI: FRV, FCV, FLV, C. felis: 1 an après dernièrerevac, FPV: 3 ans après dernière revacf<strong>la</strong>con 10 x 1 dose + 10 x 1 ml de solvantR/
13 VACCINS POUR LE CHAT 295Tableau récapitu<strong>la</strong>tif des vaccins pour le chatvirus de <strong>la</strong>panleucopénievirus de <strong>la</strong> rhinotrachéiteet calicivirusvirus de <strong>la</strong> leucémievirus de <strong>la</strong> péritoniteinfectieuseCh<strong>la</strong>mydophi<strong>la</strong> felisrageFELIGEN CRPVirbacFELOCELL CVRPfizer A.H.FELOCELL CVR-CPfizer A.H.FELOCELL RCPfizer A.H.FEVAXYN i-CHPPfizer A.H.FEVAXYN i-CHP Ch<strong>la</strong>mPfizer A.H.FEVAXYN PENTOFELPfizer A.H.LEUCOFELIGEN FeLV/RCPVirbacLEUCOGENVirbacLEUKOCELL 2 dosesPfizer A.H.NOBIVAC DUCATMSD A.H.NOBIVAC RABIESMSD A.H.NOBIVAC TRICAT TRIOMSD A.H.PRIMUCELL FIPPfizer A.H.PUREVAX FeLVMerialPUREVAX RABIESMerialPUREVAX RCMerialPUREVAX RCPMerialPUREVAX RCP FeLVMerialPUREVAX RCPChMerialPUREVAX RCPCh FeLVMerialX XX XX X XXX XX X XX X X XX X XXXXX XXXXX XX X XX X XX X X XXX
29613 VACCINS ANTIRABIQUESvirus de <strong>la</strong>panleucopénievirus de <strong>la</strong> rhinotrachéiteet calicivirusvirus de <strong>la</strong> leucémievirus de <strong>la</strong> péritoniteinfectieuseCh<strong>la</strong>mydophi<strong>la</strong> felisrageRABDOMUNPfizer A.H.RABISINMerialXX13.1.12 Vaccins antirabiquesLa rage demeure une ma<strong>la</strong>die <strong>la</strong>rgementrépan<strong>du</strong>e dans le monde etparticipe de plusieurs cycles épidémiologiquesgénéralement distincts, <strong>la</strong> rageurbaine, <strong>la</strong> rage sylvatique terrestre et <strong>la</strong>rage aérienne liée aux chauves-sourisinsectivores ou hématophages.VaccinUne des particu<strong>la</strong>rités des vaccins antirabiquesest donc qu’ils sont destinés,contrairement à <strong>la</strong> majorité des autresvaccins, à de très nombreuses espèces.Des vaccins sont disponibles pour lescarnivores et les herbivores domestiques.Actuellement, seule l’utilisationde vaccins inactivés est autorisée. Ceciélimine tout risque spécifique, d’autantque certains sont préparés au départde souches préa<strong>la</strong>blement atténuéesce qui leur confère un double volet d’innocuité.La rage est en effet une anthropozoonosemajeure ce qui explique sonappartenance aux ma<strong>la</strong>dies légalementcontagieuses et qu’elle fasse donc l’objetd’une réglementation internationale(O.M.S., O.I.E.: Organisation mondialede santé animale) et nationale. Du faitde sa portée épidémiologique, <strong>la</strong> vaccinationantirabique est pratiquée dansun cadre légal strict qu’il convient derespecter. De même, il faut respecter leprotocole de vaccination: le vétérinaireporte une responsabilité toute particulièreen <strong>la</strong> matière. Une autre particu<strong>la</strong>ritédes vaccins antirabiques est depouvoir être utilisés pour le traitementaprès exposition ; ce type de traitementest systématiquement appliqué chezl’homme conformément aux règles primitivementdéfinies par Louis Pasteur.Le traitement de l’infection après risqued’exposition n’est pas autorisé chezles animaux domestiques ; dans certainspays une dérogation peut êtreobtenue pour peu que le propriétaire del’animal puisse dûment faire état d’unevaccination antérieure, encore valide, àl’aide d’un certificat. Actuellement deuxvaccins antirabiques destinés au renardsont autorisés dans <strong>la</strong> plupart des paysmembres de l’Union Européenne aprèsévaluation européenne. Il s’agit d’unvaccin recombinant vaccine-rage, etd’un virus rabique mutant atténué parsélection. Seul le vaccin recombinantvaccine-rage a été utilisé en Belgique.Ces vaccins sont distribués par voieaérienne sur prescription des autoritéssanitaires nationales et ne sont doncpas disponibles à d’autres fins. Lescampagnes de vaccination antirabique<strong>du</strong> renard ont permis l’élimination de<strong>la</strong> ma<strong>la</strong>die dans notre pays puisque <strong>la</strong>Belgique est actuellement reconnueofficiellement indemne de rage terrestreurbaine et sylvatique.Légis<strong>la</strong>tionLa légis<strong>la</strong>tion re<strong>la</strong>tive à <strong>la</strong> vaccinationantirabique évolue cependant enfonction de l’évolution de <strong>la</strong> situationde l’infection sur le terrain. La vaccinationcontre <strong>la</strong> rage est obligatoirechez les chiens, les chats et les furetslors de voyages dans d’autres pays del’UE. Les animaux doivent être préa<strong>la</strong>blementidentifiés et <strong>la</strong> vaccinationnotée dans le passeport de l’animal.La <strong>du</strong>rée de validité de <strong>la</strong> vaccinationest indiquée par le titu<strong>la</strong>ire d’enregistrement<strong>du</strong> vaccin et correspond à <strong>la</strong><strong>du</strong>rée d’immunité <strong>du</strong> vaccin (RèglementCE/998/2003 concernant les conditionsde police sanitaire applicablesaux mouvements non commerciauxd’animaux de compagnie). La primovaccinationn’est va<strong>la</strong>ble qu’après 21
13 VACCINS ANTIRABIQUES 297jours, tandis qu’une revaccination estva<strong>la</strong>ble dès le moment de <strong>la</strong> vaccinationpour autant que celle-ci ait eu lieu<strong>du</strong>rant <strong>la</strong> période de validité de <strong>la</strong> vaccinationprécédente (Décision 2005/91/CE établissant <strong>la</strong> période après <strong>la</strong>quellele vaccin antirabique est considéré encours de validité). Pour voyager vers<strong>la</strong> Suède, le Royaume-Uni, l’Ir<strong>la</strong>nde, <strong>la</strong>Fin<strong>la</strong>nde ou Malte, il ne faut plus effectuerde prise de sang pour prouver quel’animal est immunisé contre <strong>la</strong> rage.Une identification préa<strong>la</strong>ble lors d’unevaccination contre <strong>la</strong> rage n’est pasobligatoire pour les (chiens), les furetset les chats ne voyageant pas à l’étranger.Lorsque l’animal n’est pas identifié,le vétérinaire agréé qui a procédéà <strong>la</strong> vaccination délivre un certificatconforme au modèle annexé à l’AR <strong>du</strong>21 septembre 2004 (Arrêté royal modifiantl’arrêté royal <strong>du</strong> 10 février 1967portant règlement de police sanitairede <strong>la</strong> rage). Si l’animal est déjà identifiéou que l’identification est en cours aumoment de <strong>la</strong> vaccination, le médecinvétérinaire agréé complète le passeportavec les informations nécessairesre<strong>la</strong>tives à <strong>la</strong> vaccination effectuée. EnBelgique, <strong>la</strong> vaccination contre <strong>la</strong> rageest encore obligatoire chez les chiensau sud <strong>du</strong> sillon Sambre-et-Meuse etles chiens qui voyagent en campingcaravaningavec leurs propriétairesdans toute <strong>la</strong> Belgique.13.1.12.1 Vaccins antirabiquesmonovalentsNOBIVAC RABIES (MSD A.H.)virus rabique inact souche Pasteur RIV:min 2,0 IUAdjuv: phosphate d’aluminiumvaccin injectable im (Eq, Bo, Ov), im, sc (Ca, Fe)Posologie:Primovac:Eq, Bo, Ov (âge > 6 m): 1 dose (im)Eq, Bo, Ov (âge < 6 m): 2e dose après l’âgede 6 m (im)Ca, Fe (âge > 3 m): 1 dose (im, sc)Ca, Fe (âge < 3 m): 2e dose après l’âge de3 m (im, sc)Revac:Eq, Bo: 1 dose/2 ansOv: 1 dose/anCa, Fe: 1 dose/3 ansNobivac Rabies® peut être utilisé commesolvant pour Nobivac DHPPi®, NobivacDHP®, Nobivac Parvo-c®, Nobivac PuppyDP®, Nobivac Pi®, Nobivac Ppi® etNobivac Ducat®OOI:3-4 sem après vacDOI: Ca, Fe: 3 ans, Bo, Eq: 2 ans, Ov: 1 anViande: 0 j, Lait: 0 jf<strong>la</strong>con 10 x 1 doseR/iPUREVAX RABIES (Merial)virus rabique recombinant canarypox virus(vCP65): min 10 exp6.8 FAID50vaccin injectable scPosologie:Primovac:Fe (âge > 12 sem): 1 dose (1 ml)Revac:1 dose après 1 an, ensuite min 1 dose/3 ansOOI: 4 sem après vac de baseDOI: 1 an après vac de base, ensuite 3 ansf<strong>la</strong>con 2 x 1 doseR/iRABDOMUN (Pfizer A.H.)virus rabique inact (Flury LEP): min 1,0 UI/mlvaccin injectable scPosologie:Primovac:Bo, Ca, Fe (âge > 7 sem): 1 dose/animalsi primovac à un âge < 12 sem: rappel àl’âge de 12 semRevac:tous les 3 ans (Bo, Ca), tous les 4 ans (Fe)OOI: 14 j après vacDOI Ca, Bo: 3 ans, Fe: 4 ansViande, Lait: 0 j10 x 1 dose (1 ml)R/iRABISIN (Merial)virus rabique inact: 10exp 7 DL50/mlAdjuv: hydroxide d’aluminiumvaccin injectable im, scPosologie:- Eq, Bo, Ov:Primovac:(sans imm mat): vac à l’âge de 2 m min1ère revac après 1 an(imm mat): vac à l’âge de 4 - 6 m min1ère revac après 1 an (Eq, Bo), 3 ans (Ov)Revac:tous les ans (Eq), tous les 2 ans (Bo), tousles 3 ans (Ov)- Ca, Fe:(sans imm mat): vac à l’âge de 4 sem min1ère revac après 6 m(imm mat): vac à l’âge de 3 m min1ère revac après 3 ansRevac:tous les 3 ansPeut être administré simultanément avecParvodog® ou Trivirovax® (inj en 2 pointsdifférents) chez le chien- Mustélidés (âge> 3 m): 1 dose (1 ml)Revac: tous les ansOOI, DOI: pas d’infof<strong>la</strong>con 10 x 1 dose (1 ml)R/i13.1.12.2 Vaccin antirabique multivalentLEPTORABISIN (Merial)L. Canico<strong>la</strong> inact: min 10exp 8 germes/doseL. Icterohaemorrhagiae inact:min 10exp 8 germes/doseAg de <strong>la</strong> rage inact: min 1 UI/dosevaccin injectable sc, imPosologie:Primovac:Ca (âge > 12 sem): 1 x 1 dose (1 ml),au besoin 2e vac après 4 semRevac:1 dose/anPeut être administré simultanément àParvodog® ou Trivirovax®OOI-DOI : pas d’informationf<strong>la</strong>con 10 x 1 doseR/i
29813 IMMUNOCASTRATION13.2 Immunocastration13.2.1 Vaccin anti-GnRFIndicationsCe vaccin est proposé pour <strong>la</strong> castration immunologique, pour <strong>la</strong> ré<strong>du</strong>ction del’odeur de verrat in<strong>du</strong>ite par l’androsténone et le scatole chez les porcs mâlesentiers après <strong>la</strong> puberté. L’administration peut se faire à partir de l’age de 8 semaines.L’immunité (in<strong>du</strong>ction d’anticorps anti-GnRF) se met généralement enp<strong>la</strong>ce 1 semaine après <strong>la</strong> seconde vaccination.VaccinLe vaccin contient comme principe actif un analogue hormonalement inactif <strong>du</strong>facteur de libération de <strong>la</strong> gonadotrophine (GnRF), conjugué à une protéine detransport (Diphteria toxoïd, utilisé dans des vaccins à usage humain). Une premièrevaccination amorce le système immunitaire sans conséquences physiologiques.Après <strong>la</strong> deuxième dose, des anticorps sont pro<strong>du</strong>its qui neutralisent leGnRF endogène, d’où une diminution de <strong>la</strong> sécrétion de <strong>la</strong> LH et de <strong>la</strong> FSH, entraînantune diminution temporaire de <strong>la</strong> pro<strong>du</strong>ction de stéroïdes dans les testicules.Le vaccin diminue ainsi <strong>la</strong> pro<strong>du</strong>ction de testostérone et d’autres stéroïdes telsque l’androsténone, qui est principalement à l’origine de l’odeur de verrat. Uneautre composante importante de l’odeur de verrat est le scatole qui est inhibéindirectement.Effets secondairesDes gonflements au niveau <strong>du</strong> site d’injection sont observés surtout chez lesjeunes animaux. Les réactions locales disparaissent progressivement, maispeuvent persister longtemps (42 j) chez certains animaux. Une légère augmentationde <strong>la</strong> température corporelle (0,5 °C) peut être observée <strong>du</strong>rant les premières24 heures suivant <strong>la</strong> vaccination. Chez un nombre limité d’animaux, des réactionsde type anaphy<strong>la</strong>ctoïde apparaissent immédiatement après l’injection. Dans derares cas, l’issue est fatale, mais en général, l’animal se rétablit spontanément.Les réactions ne surviennent plus lors des injections suivantes.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser chez les femelles ou les mâles destinés à <strong>la</strong> repro<strong>du</strong>ction.Risques pour l’hommeUne injection chez l’homme peut provoquer une diminution temporaire des hormonessexuelles et des fonctions repro<strong>du</strong>ctives aussi bien chez les hommes quechez les femmes, ainsi que des effets indésirables sur <strong>la</strong> grossesse. Ce risqueaugmente après une seconde (ou plus) injection. Le pro<strong>du</strong>it doit donc être administréavec <strong>la</strong> plus grande prudence, au moyen d’un injecteur de sécurité spécialementprévu à cet effet. Le pro<strong>du</strong>it ne doit pas être manipulé ni administré pardes femmes enceintes ou susceptibles de l’être. En cas de contact avec les yeuxou <strong>la</strong> peau ou en cas d’(auto-)injection, rincer immédiatement et abondamment àl’eau. En cas d’(auto-)injection, consulter un médecin. On conseille aux personnesayant été victimes d’une (auto-)injection de ne plus manipuler ce pro<strong>du</strong>it ou despro<strong>du</strong>its simi<strong>la</strong>ires dans le futur.IMPROVAC (Pfizer A.H.)peptide synthétique analogue au GnRF, conjuguéà une toxine diphtérique: min 300 mcgadjuv: DEAE-dextranvaccin injectable scPosologie:Su (âge > 8 sem): 2 x 1 dose (2 ml) à 4 semd’intervalle, dernière vac min 4 - 6 semavant l’abattageOOI: 1 sem après 2e vacTemps d’attente: 0 jf<strong>la</strong>con 12 x 10 doses (20 ml), 10 x 50 doses(100 ml), 4 x 125 doses (250 ml)R/
13 IMMUNOGLOBULINES ET SÉRUMS 29913.3 Immunoglobulines et sérumsL’immunisation passive est basée sur l’administration d’anticorps à un animal àrisque afin d’instaurer une protection immédiate. La protection conférée par lesimmunoglobulines est toujours limitée à quelques semaines voire quelques mois.13.3.1 Immunoglobulines et sérums utilisés chez le bovinLes spécialités répertoriées ci-dessous sont utilisées en prophy<strong>la</strong>xie ou en traitementcontre les colibacilloses <strong>du</strong> veau. Comme <strong>la</strong> protection conférée par lesimmunsérums ne dépasse pas celle conférée par un bon colostrum, l’utilisationde ces pro<strong>du</strong>its ne devrait jamais se substituer à l’administration <strong>du</strong> colostrum.Les spécialités à usage oral doivent être administrées pendant les 12 premièresheures de <strong>la</strong> vie, période pendant <strong>la</strong>quelle l’intestin <strong>du</strong> veau est perméable auximmunoglobulines.LOCATIM (Biokema Anstalt)IgG anti -Coli F5 (K99): min 2,8 log10/mlimmunosérocolostrum poPosologie:veau (âge < 4 h, max 12 h):60 ml/animalViande: 0 jf<strong>la</strong>con 60 mlR/LOCATIM PLUS (Fendigo)IgG1, IgG2, IgM, IgA (dont Ac ctre E. coli):10 g/100 mlgamma-globulines spécifiques homologuesanti-coli: titre agglutinant078/0115/015 1/5000086/0117 1/3000solution injectable im, sc, ivPosologie:Préventif:- veau: 50 - 100 mg/kgCuratif:- veau: 100 - 200 mg/kgTemps d’attente: 0 jf<strong>la</strong>con 100 mlR/13.3.2 Sérum antitétaniqueL’immunisation passive contre le tétanos est indiquée en cas de p<strong>la</strong>ies suspecteschez les animaux dont l’immunisation est nulle ou douteuse. Une immunisationactive doit être entreprise simultanément. Des doses massives seront utiliséesune fois que des signes cliniques apparaissent.SERUM ANTITETANIQUE (MSD A.H.)Ac tétanos: 1.160 UI/mlsolution injectable sc, im, iv, épidPosologie:- prophy<strong>la</strong>xie, pas de blessure (sc, im):Eq, Bo: 7 500 UIpou<strong>la</strong>in, veau (< 100 kg PV): 3 000 UISu: 1 500 - 3 000 UIOv: 3 000 UICa: 500 - 1000 UI, selon PV- prophy<strong>la</strong>xie, blessure (sc, im):Eq, Bo: 15 000 UIpou<strong>la</strong>in, veau (< 100 kg PV): 6 000 UISu: 3 000 - 6 000 UIOv: 6 000 UICa: 1 000 – 2 000 UI selon PVSi <strong>la</strong> blessure n’est pas guérie après 10 - 14 j,répéter l’admin- thérapie:quotidiennement jusqu’à rétablissementEq, Bo: 30 000 UI (épid, iv) + 15 000 (sc, im)Ca: 3 000 - 5 000 UI (iv, im) selon PVViande Eq, Bo, Su, Ov: 0 j, Lait Bo, Ov: 0 jf<strong>la</strong>con 50 mlR/
30013 IMMUNOMODULATEURS13.4 Immunomo<strong>du</strong><strong>la</strong>teurs13.4.1 InterféronLes interférons appartiennent au groupe des cytokines et ont des propriétés antiviraleset immunomo<strong>du</strong><strong>la</strong>trices.IndicationsUn seul interféron possède actuellement une autorisation de mise sur le marchéen médecine vétérinaire : l’interféron oméga recombinant d’origine féline qui estindiqué pour ré<strong>du</strong>ire <strong>la</strong> mortalité et les signes cliniques de <strong>la</strong> parvovirose (formeentérique) chez les chiens de plus de 1 mois. Les chats infectés par le virus de <strong>la</strong>leucose féline (FeLV) et/ou le virus de l’immunodéficience féline (FIV), à un stadeclinique non terminal, peuvent être traités à partir de l’âge de 9 semaines. Uneré<strong>du</strong>ction des signes cliniques pendant <strong>la</strong> phase symptomatique ainsi qu’uneré<strong>du</strong>ction de <strong>la</strong> mortalité ont également été observées.PharmacodynamieLe mécanisme d’action est mal connu, mais pourrait impliquer l’augmentation desdéfenses non spécifiques de l’organisme. L’interféron oméga félin n’a pas d’effetdirect sur le virus pathogène.PharmacocinétiqueL’interféron oméga félin (rFeIFN) diffuse principalement vers les reins et le foie. LerFeIFN est très rapidement métabolisé dans les reins et excrété par les urines. Defortes concentrations se retrouvent dans les reins, le foie, <strong>la</strong> g<strong>la</strong>nde thyroïde et <strong>la</strong>rate. Le rFeIFN ne traverse pas <strong>la</strong> barrière hémato-méningée. De faibles concentrationsont été relevées dans les tissus muscu<strong>la</strong>ires et adipeux. L’activité pharmacologique<strong>du</strong> rFeIFN <strong>du</strong>re plus longtemps que sa détection dans le p<strong>la</strong>sma.Contre-indicationsVoir Repro<strong>du</strong>ction et <strong>la</strong>ctation.Effets indésirablesDe l’hyperthermie, des vomissements, de <strong>la</strong> leucopénie, de <strong>la</strong> thrombocytopénieet de l’anémie peuvent être constatés <strong>du</strong>rant le traitement. Aucune donnéen’est connue concernant les effets indésirables apparaissant chez le chien et lechat après un usage prolongé (chez l’homme, des ma<strong>la</strong>dies auto-immunes apparaissentsuite à un usage prolongé).Précautions particulièresLa vaccination de l’animal doit être reportée jusqu’à <strong>la</strong> guérison complète del’animal.Repro<strong>du</strong>ction et <strong>la</strong>ctationL’innocuité de l’utilisation de ce pro<strong>du</strong>it chez les chiens et chats en gestation ouen <strong>la</strong>ctation n’a pas été démontrée.VIRBAGEN OMEGA 10 ME (Virbac)interféron oméga félin recombinant:10 x 10exp 6 Ulyophilisat pour solution injectable iv (Ca), sc(Fe)Posologie:Ca: 1 x pj 2,5 x 10exp 6 U/kg (3 j)Fe: 1 x pj 1 x 10exp 6 U/kg (5 j)Répéter le traitement chez le chat 14 puis60 j après le 1erf<strong>la</strong>con 1 of 5 x lyophilisat + solvantR/
14 MÉDICAMENTS ANTITUMORAUX 30114 MÉDICAMENTS ANTITUMORAUX14.1 Inhibiteurs des tyrosine kinasesIndicationsTraitement des tumeurs à mastocytes non résécables ou récidivantes chez lechien (grade 2 ou 3). Les animaux traités doivent faire l’objet d’un suivi intensifet, si nécessaire, le traitement doit être ajusté ou arrêté. La spécialité à base demasitinib ne doit être utilisée que chez les chiens présentant une tumeur à mastocytesnon résécable et exprimant le récepteur tyrosine kinase c-kit muté. (Voiraussi Folia Veterinaria 2010 n° 3)PharmacodynamieLe mécanisme d’action de ces substances à bas poids molécu<strong>la</strong>ire (small moleculeou “-nib”) repose sur l’inhibition compétitive d’enzymes intracellu<strong>la</strong>ires. Lemasitinib inhibe puissamment et de manière sélective, in vitro, <strong>la</strong> forme mutée<strong>du</strong> récepteur tyrosine kinase c-kit. Il inhibe également le récepteur au facteur decroissance derivé des p<strong>la</strong>quettes (PDGF) et le récepteur <strong>du</strong> facteur fibrob<strong>la</strong>stiquede croissance (FGFR3). Le traitement par masitinib ne doit être envisagé que chezles chiens présentant une tumeur à mastocytes non résécable, exprimant le récepteurtyrosine kinase c-kit muté.Le tocéranib exerce à <strong>la</strong> fois une activité directe antitumorale et une activité antiangiogène.Le tocéranib inhibe de façon sélective l’activité tyrosine kinase deplusieurs membres de <strong>la</strong> famille des split kinases (récepteurs à activité tyrosinekinase : RTK) dont certains sont impliqués dans <strong>la</strong> croissance tumorale, l’angiogenèsepathologique et dans <strong>la</strong> progression métastatique <strong>du</strong> cancer.Lors d’essais biochimiques et cellu<strong>la</strong>ires, le tocéranib inhibe l’activité de <strong>la</strong> tyrosinekinase Flk-1/KDR (récepteur des facteurs de croissance de l’endothéliumvascu<strong>la</strong>ire, VEGFR2), des récepteurs des facteurs de croissance dérivés des p<strong>la</strong>quettes(PDGFR) et des récepteurs Stem Cell Factor (c-Kit).PharmacocinétiqueAprès administration orale chez le chien (11,2 mg/kg PV), le masitinib est rapidementabsorbé et le temps nécessaire pour atteindre <strong>la</strong> concentration maximale(Tmax) est d’environ 2 heures. La demi-vie d’élimination (t½) est d’environ 3-6heures. Le masitinib se lie à environ 93 % aux protéines p<strong>la</strong>smatiques. Le masitinibest principalement métabolisé par N-désalky<strong>la</strong>tion. L’excrétion se fait dans <strong>la</strong>bile.La demi-vie d’élimination (t1/2) <strong>du</strong> tocéranib est d’environ 17 heures, le tempspour atteindre <strong>la</strong> concentration p<strong>la</strong>smatique maximale (Tmax) d’environ 6 heures.Le tocéranib a un taux de liaison important aux protéines, entre 91% et 93%.Après administration orale <strong>du</strong> phosphate de tocéranib, environ 92% <strong>du</strong> pro<strong>du</strong>itest excrété dans les fèces et 7% dans l’urine.Contre-indicationsNe pas utiliser : chez les chiennes gravides ou al<strong>la</strong>itantes, chez les chiens demoins de 6 mois ou de moins de 4 kg. L’utilisation de masitinib est égalementdéconseillée chez les chiens souffrant de troubles hépatiques ou de <strong>la</strong> fonctionrénale, chez les chiens souffrant d’anémie ou présentant une neutropénie, ou encas d’hypersensibilité au principe actif ou à l’un des excipients.Effets indésirablesLes effets indésirables suivants surviennent assez fréquemment et ont une évolutionbénigne: effets gastro-intestinaux (diarrhée, vomissements, anorexie), alopécie(masitinib). Des cas d’hépatotoxicité, d’anémie, de toxicité rénale et desyndrome néphrotique peuvent également survenir. Pour <strong>la</strong> liste détaillée deseffets indésirables, nous renvoyons aux RCP des spécialités.InteractionsIl convient de tenir compte des interactions possibles avec d’autres substanceséliminées par le foie ou inhibant les enzymes hépatiques. L’utilisation concomitanted’autres substances présentant un degré élevé de liaison protéique peutentraîner une compétition au niveau de <strong>la</strong> liaison <strong>du</strong> masitinib et provoquer ainsi
30214 MÉDICAMENTS ANTITUMORAUXdes effets indésirables. L’efficacité de masitinib peut être diminuée chez leschiens précédemment traités par chimiothérapie et/ou radiothérapie. Il n’y a pasdonnées concernant une éventuelle résistance croisée avec d’autres pro<strong>du</strong>itscytostatiques.Etant donné que le tocéranib augmente le risque d’ulcération ou de perforationgastro-intestinale, l’utilisation concomitante d’anti-inf<strong>la</strong>mmatoires non stéroïdiensdoit se faire avec prudence.Précautions particulières/ Risques pour l’hommeLes comprimés doivent être administrés entiers, sans être coupés, cassés oubroyés.Un contact cutané répété avec le masitinib peut provoquer des troubles de <strong>la</strong>fertilité féminine et nuire au développement fœtal, provoquer une sensibilisationcutanée, ou une irritation ocu<strong>la</strong>ire sévère et de graves lésions de l’oeil. Éviter toutcontact cutané avec les selles, l’urine et le vomi des chiens traités. En cas decontact cutané ou avec les yeux, rincer abondamment à l’eau. Les enfants nedoivent pas avoir de contact rapproché avec les chiens traités, leurs selles ouleur vomi.Repro<strong>du</strong>ction et <strong>la</strong>ctationNe pas utiliser chez les chiennes gravides ou al<strong>la</strong>itantes. Ne pas utiliser chez leschiens destinés à <strong>la</strong> repro<strong>du</strong>ction.14.1.1 MasitinibLMR masitinib: MASIVET 50 mg, 150 mg (AB Science)masitinib (mésy<strong>la</strong>te): 50 mg ou 150 mgcomprimés poPosologie:Ca (âge > 6 m, PV > 4 kg): 1 x 12,5 mg/kg pjcompr 30R/14.1.2 TocéranibLMR tocéranib: PALLADIA 10 mg, 15 mg, 50 mg compr pelliculéspour chiens (Pfizer A.H.)tocéranib (phosphate):10 mg, 15 mg ou 50 mg/comprcomprimé pelliculé poPosologie:Ca (âge > 2 ans, PV > 3 kg):3,25 mg/kg tous les 2 jcompr 4 x 5R/
LISTE DES PREMELANGES MEDICAMENTEUX 303LISTE DES PRÉMÉLANGES MÉDICAMENTEUXAIVLOSIN 42,5 mg/g prém méd porcs (Eco A.H.)APRALAN 100 Vet Premix (Eli Lilly)AUROFAC 250 mg/g premix (Pfizer A.H.)DOKAMOX 100 mg/g premix (Sogeval Lab)DOXYPREX 100 mg/g premix (In<strong>du</strong>strial Veterinaria)DOXYRAL 10% premix (Emdoka)ECOMECTIN 6 mg/g premix (Eco A.H.)ECONOR 10 % (Novartis)FEEDMIX OXY 10% (Dopharma Research)FLUBENOL 5 % prém méd (Eli Lilly)LINCO-SPECTIN 22 + 22 premix (Pfizer A.H.)NOROMECTIN premix (Norbrook Lab)PANACUR 4% premix (MSD A.H.)PHARMASIN 250 mg/g premix (Huvepharma)PROMYCINE 400 IU/mg prém méd (VMD)PULMOTIL 200 Vet Premix (Eli Lilly)RHEMOX premix (In<strong>du</strong>strial Veterinaria)SURAMOX 5% premix (Virbac)TIAMUTIN 10% prém méd (VMD)TILMOVET 200 g/kg premix (Huvepharma)TUCOPRIM poudre (Pfizer A.H.)TYLAN 250 Vet Premix (Eli Lilly)VETMULIN 100 g/kg premix (Huvepharma)
305INDEXIndex des spécialités et des substances activesLes spécialités sont imprimées en majuscules.
INDEX 307Ac anti-coli, voir E.coliACEPE 172acépromazine 171-172acétylisovaléryltylosine,voir tylvalosineacide acétylsalicylique 101acide borique 135acide citrique 129acide c<strong>la</strong>vu<strong>la</strong>nique 8-10acide hyaluronique 137acide <strong>la</strong>ctique 193-194acide pantothènique, voir vitamine Bacide propionique 130acide tolfénamique 102-103ACTICAM 108Actinobacillus pleuropneumoniae243-244ACTIVYL 203-204ACTIVYL TICK PLUS 207-208adénovirus canin 271-272, 274, 277,279, 282-284adrénaline 169-170ADVANTAGE 201ADVANTIX 204-205ADVOCATE 60-61ADVOCIN 33aglépristone 85-86AIVLOSIN 24, 303albendazole 43ALBIPEN LA 6ALCIDE UDDERGOLD PM VET 194alfaprostol 83alfaxalone 163-164ALFAXAN 164ALIZIN 86alpha-tocophérol, voir vitamine Ealtrénogest 69-72ALTRESYN 71aluminium 191-192ALUSPRAY 192ALZANE 180amitraz 202-203, 206-208amoxicilline 5-10, 40AMOXICLAV-VMD 8AMOXICURE 6AMOXIVAL VET 6AMOXYCILLINE 70 % Ke<strong>la</strong> 6AMOXY-kel 15 6ampicilline 5-6, 215, 217AMPICLOX Q.R. 215AMPI-DRY 6amprolium 50ANARTHRON 138anatoxine tétanique, voir Clostridiumtetanianémie infectieuse virale (virus de l’ -)257, 264, 267-270ANESKETIN 161ANTHELMEX FORTE 54ANTIROBE 25-26ANTISEDAN 180APRALAN 127, 303apramycine 14, 127ARISTAL 106ASPI-KEL 101ATIPAM 180atipamézole 179-180ATOPICA 190ATUSSIN 142AURIZON 212AUROFAC 18, 303AVICAS 43AVINEW 261, 267, 267-270AVIPRO GUMBORO VAC263, 267, 267-270AVIPRO ND C131 261, 267, 267-270AVIPRO PRECISE 263, 267, 267-270AVIPRO SALMONELLA DUO266, 267, 267-270AVIPRO SALMONELLA VAC E266, 267, 267-270AVIPRO SALMONELLA VAC T266, 267, 267-270AVIPRO THYMOVAC264, 267, 267-270azapérone 172-173B.BRAUN VET CARE hypertoniqueNaCl sol 130B.BRAUN VET CARE Ringer LactateHartmann sol 130bacitracine 29BACIVET S 29Bacteroides nodosus, voirDichelobacter nodosusBANACEP VET 144BAXYL LA 20BAYCOX 50-51BAYTICOL 198BAYTRIL 33-34BENAKOR F 144BENAZECARE FLAVOUR 144bénazépril 144BENEFORTIN FLAVOUR 144benzylpénicilline 3-5, 39, 215, 217bétamethasone 212BEXEPRIL 144bicarbonate 129bismuth subnitrate 217BLOCKADE 193Bluetongue Virus, voir fièvre catarrhaleovine (virus de <strong>la</strong> -)BOLFO 196Bordetel<strong>la</strong> bronchisepticachien 279-280, 282-284porc 247-248, 252-253BORGAL 30BOVIDIP 193BOVILIS BOVIPAST RSP226, 235, 237BOVILIS BVD 228, 237BOVILIS IBR MARKER INAC 227, 237BOVILIS IBR MARKER LIVE 227, 237BOVILIS LACTOVAC 229, 231, 237BOVILIS LUNGWORM 237BOVIMEC B 62BRAVOXIN 10 233, 237, 239bromure de potassium 186-187BRONCHI-SHIELD 279, 282
308INDEXbronchite infectieuse (virus de <strong>la</strong> -)256, 262-263, 267-270BTVPUR AlSap 8 230, 237, 239buprénorphine 113-115bursite infectieuse (virus de <strong>la</strong> -), voirGumboroBUSCOPAN 112, 123buséréline 74, 77-78butafosfan 135-136BUTOMIDOR 117butorphanol 115-117BUTOX PROTECT 197BVD (virus -) 228-229BYEMITE 196cabergoline 84CALCII BOROGLUCONAS 135calcium 134-135CALCIUMBORO-kel 135calicivirus felin 287-290, 295-296CALPHONE 135CANAURAL 212CANIGEN CHP 271, 274-275, 282CANIGEN L 280, 282CANIGEN PUPPY 2b 273, 282CANILEISH 282CANINSULIN 97CANIQUANTEL PLUS 53carbétocine, voir oxytocineCARDALIS 148CARDISURE APPETENT 149carnidazole 52CARPRODYL F 105carprofène 104-106Carré (virus de <strong>la</strong> ma<strong>la</strong>die de -)275-276CATMINTH 48CATOSAL 136CAZITEL PLUS 54céfalexine 10-12, 214-216CEFALEXINE Ke<strong>la</strong> 11céfapirine 213CEFASEPTIN Forte 11CEFASEPTIN Mite 11céfazoline 214-216CEFENIL 12CEFFECT 12céfopérazone 215céfovécine 10-13CEFOVET <strong>la</strong>ctation 215CEFOVET DC 216cefquinome 10-13, 215-216CEFTIOCYL 12ceftiofur 10-13CEFTIOSAN 12CENTIDOX 18CEPHACARE FLAVOUR 11CEPOREX 11CEPRAVIN DRY COW 216CERENIA 124CERTIFECT 207CESTEM 54CEVAXEL 12CEVAXEL RTU 12CEVAZURIL 51Ch<strong>la</strong>mydophi<strong>la</strong> felis 293-294chlorhexidine 191-192chlorite de sodium 194chlorphénamine 142chlortétracycline 18, 194, 213cholécalciférol, voir vitamine DCHORULON 77CHRONOPIL 71chute de ponte (virus <strong>du</strong>syndrome de <strong>la</strong> -) 257, 263, 267-270ciclosporine 189-190, 211CIDR 71CIMALGEX 111cimicoxib 110-111CIRCOVAC 243, 252circovirus 242-243, 252-253CITROXY 20CLAMOXYL 6CLAVASEPTIN 8CLAVOBAY 8-9CLAVUBACTIN 9clenbutérol 79, 141CLINAGEL-VET 211CLINDABUC 26clindamycine 24-26CLINDAMYCINE Ke<strong>la</strong> 26CLOMICALM 182clomipramine 181-182cloprosténol 83clorsulon 63-64CLOSAMECTIN 61, 64closantel 49, 61, 64Clostridium spp.vaccin bovin 232-234, 237-238vaccin porc 249, 252-253Clostridium tetanisérum antitétanique 299vaccin cheval 222-224clotrimazole 212cloxacilline 214-217COBACTAN 12-13, 215COCCIBAL 50Coccidia spp., voir Eimeria spp.CODITANE 192CODIVERM 47COLFEN 16COLIPLUS 127COLISTIMAX 127colistine 28-29, 40, 127-128COLISTINE EUROVET 127COLISTINE SULFATE 28COLISTINEMIX 127COLIVET 127COLIVET “S” 29COLIVET “S” FORTE 29COLLIER PROPOXUR 196COLMYC 34COLUMBA 267, 270COMFORTAN 120COMFORTIS 66-67CONTRALAC 85CONVENIA 13coronavirusbovins 229-231, 237-238vo<strong>la</strong>ille 256, 267-270chat 292-293, 295-296
INDEX 309CORTAVANCE 209COSUMIX PLUS 30COVEXIN 233, 238, 239COXEVAC 236, 238-239COXI PLUS 51Coxiel<strong>la</strong> burnetii 235-236, 239COXOFEN 106CRONYXIN 103cyano-coba<strong>la</strong>mine, voir vitamine BCYCLIX 83CYCLOSOL 200 LA 20CYCLOSPRAY 194CYDECTIN 60, 63CYDECTIN TRICLAMOX BOVINS 56CYDECTIN TRICLAMOX OVINS 53DALMAZIN 83danofloxacine 31-33DECTOMAX 59, 61-62DEFENDOG 198delmadinone acétate 71, 73deltaméthrine 197DELVOSTERON 71DEPO-PROMONE 71DEPOSIL 5desloréline 74-78DETOGESIC 177détomidine 175-177DETONERVIN 177DEXA 89DEXAFORT 89DEXA-JECT 89dexaméthasone 89DEXAMETHASONE Ke<strong>la</strong> 89DEXDOMITOR 177dexmédétomidine 177dexpanthénol, voir vitamine Bdextrométhorphane 142dextrose, voir glucoseDiarrhée Virale Bovine (virus de <strong>la</strong> -),voir BVDdibotermine alpha 139Dichelobacter nodosus 234, 239dic<strong>la</strong>zuril 50Dictyocaulus viviparus 236-238DICURAL 33diéthano<strong>la</strong>mine fusidate 212difloxacine 33dihydrostreptomycine 217DIMAZON 151dimpy<strong>la</strong>te 195-196DINOLYTIC 83dinoprost 83DIPAL 193dirlotapide 125-126DOFATRIM-JECT 31DOG ECZEMA 210DOGMINTH 48DOKAMOX 7, 303DOLAGIS 105DOLETHAL 166DOLOREX 117DOLPAC 55DOLTHENE 45DOMIDINE 177DOMITOR 177DOMOSEDAN 177DORAFLOX 34-35doramectine 58-59, 61-62DORBENE VET 177DOVENIX 49doxycycline 17-19DOXYCYCLINE 19DOXYLIN 50% WSP 19DOXYPREX 19DOXYRAL 19DOXYVETO 19DOZURIL 51DRAXXIN 23DRONTAL CAT 53DRONTAL DOG FLAVOUR 54DRONTAL LARGE DOG FLAVOUR 54DRONTAL PUP 55DRYCLOXA-kel 216DUPHACYCLINE 20DUPHAFRAL AD3E 133DUPHAFRAL D3 1000 132DUPHAMOX LA 7DUPHAPEN 5DUPHATROXIM 31DUVAXYN IE PLUS T 220, 223-224E. coliimmunoglobulines 299vaccin vo<strong>la</strong>ille 258, 266-270vaccin bovin 231-232, 237-238vaccin porc 248-249, 252-253EASOTIC 212eCG 74-78ECOMECTIN 59, 62, 303ECONOR 28, 303ECUTAN 192EFFIPRO 198-199EFFYDRAL 129EFICUR 13Egg Drop Syndrome Virus,voir chute de ponte(virus <strong>du</strong> syndrome de <strong>la</strong> -)EHV-1, -4, voir herpèsvirusEimeria spp. 265, 267-270EIMERYL 50ELIMINALL 199embutramide 166-167EMDACTILIN 39EMDOCAM 108EMDOCOLIN 128EMDOFLUXIN 103EMDOTRIM 31EMEPRID 125emodepside 55-57ENACARD 145ena<strong>la</strong>pril 145encéphalite aviaire (virus de l’ -)262, 267-270ENDOGARD 54ENGEMYCIN 20, 194enilconazole 209enrofloxacine 31-36
310INDEXENRO-K 35ENROSHORT 35ENROVETO 35ENROX FLAVOUR 35ENROXIL MAX 35ENTERFLUME 36ENTERISOL ILEITIS 250, 252ENURACE 156ENZAPROST 83éphédrine 142, 155-156épinéphrine, voir adrénalineEPRINEX 59éprinomectine 58-59EQUEST 63-64EQUIBACTIN 31EQUILIS PREQUENZA 220, 224EQUILIS PREQUENZA TE220, 223-224EQUIMAX 65Equine Chorionic Gonadotropin,voir eCGEQUIOXX 111-112EQUIP EHV 1,4 221, 224EQUIP WNV 222, 224EQVALAN 62EQVALAN DUO 65ERAQUELL 62Erysipelothrix rhusiopathiae 250-253ESB 3 51Escherichia coli, voir E. coliestriol, voir oestriolESTRUMATE 83ETOSOL-SE 136EURICAN CHPPI2271, 274-275, 278, 283EURICAN HERPES 205 277, 283EUROLECTROL 129EXCENEL 13EXCENEL RTU 13EXSPOT 198FATROX 217FCO, voir fièvre catarrhale ovinefébantel 43-44, 54-55FEEDMIX OXY 20, 303FELIGEN CRP 285, 288, 295FELIMAZOLE 96FELOCELL CVR 285, 288, 295FELOCELL CVR-C 285, 288, 294-295FELOCELL RC 288, 295fenbendazole 42-44, 53FENDOV 45FENFLOR 16FENOFLOX 35FENTADON 118fentanyl 117-118FENYLBUTAZON 102fer 133-134FERRAJECT-200 134FERROHIPRA 134FERTIPIG 78FEVAXYN i-CHP 287, 290, 295FEVAXYN i-CHP Ch<strong>la</strong>m287, 290, 294-295FEVAXYN PENTOFEL 287, 290, 292,294-295fièvre catarrhale ovine (virus de <strong>la</strong> -)230, 239fièvre <strong>du</strong> Nil occidental (virus de <strong>la</strong> -),voir West Nile VirusFINADYNE 103-104fipronil 198-200, 205-207FIPROSPOT 199firocoxib 110-112FLEVOX 199florfénicol 16-17, 40, 112FLORFENIKEL 16FLORGANE 16FLORKEM 17FLOXABACTIN 35FLOXADIL 36FLOXAMAX 36flubendazole 45FLUBENOL 45, 303FLUKIVER 49, 64fluméquine 36fluméthrine 198, 204-205FLUMIQUIL 36FLUNIVETO 104flunixine 40, 102-104, 112fluoxétine 182-183FLURAZIN 104FLUVEX 104FOLLIGON 77follitropine, voir FSHFOOTVAX 234, 239FORCYL 37FORTEKOR 145FORTHYRON 94framycétine 212, 217FRONTLINE 199-200FRONTLINE COMBO 206FSH 74-78FUREXEL IVERMECTINE 62furosémide 150-151GABBROSTIM 83GABBROVET 15, 127GALASTOP 84GALLIVAC IB 88 262, 268gamithromycine 21-22GASTROGARD 121GENTA-kel 15gentamicine 14-15, 211-212GENTAVETO-5 15GESTAVET 78glucose 130-131GLUCOSE 131GLUCOSE B. BRAUN VET CARE 131GLUCOSE Ke<strong>la</strong> 131glycine 129GnRF-analogue 298gonadoréline 74-77gonadotrophine chorionique, voir hCGgonadotrophine sérique, voir eCGGRIPOVAC 3 241, 252grippe équine (virus de <strong>la</strong> -),voir influenzagrippe, voir influenzaguaïfénésine 142, 180-181Gumboro (virus de <strong>la</strong> ma<strong>la</strong>die de -)256-257, 263-264, 267-270
INDEX 311Haemophilus parasuis 246-247,252-253HALOCUR 52halofuginone 51-52hCG 74-78hépatite infectieuse canine, voiradénovirus caninherpès (virus -)bovin, voir IBRchat 287-289, 295-296cheval 221, 224chien 277, 282-284vo<strong>la</strong>ille, voir MarekHIPRABOVIS IBR MARKER LIVE 227,238HIPRACOX 265, 268HIPRAGUMBORO CW 264, 268HIPRAGUMBORO-GM97 264, 268HIPRAVIAR-NDV CLON 261, 268HORSEMINTH 48Human Chorionic Gonadotropin,voir hCGhydrocortisone 209, 212HYDRODOXX 19HYMATIL 22HYONATE 137HYORESP 245, 252hyoscine 112, 122-123IBAFLIN 37ibafloxacine 31-33, 37IBR (virus -) 224-227, 237-238IBRAXION 227, 238IMAVEROL 209imidaclopride 60-61, 201, 204-205imidapril 143-144, 146immunoglobine 299IMPROVAC 298INCURIN 154indoxacarbe 203-204, 207-208INFLACAM 108influenza (virus -)cheval 219-221, 224porc 241, 252-253INGELVAC CIRCOFLEX 243, 252INGELVAC MYCOFLEX 245, 252INGELVAC PRRS KV 242, 252INGELVAC PRRSModified Live Virus 242, 252insuline 96-97interféron 300iode (composés) 191-193ISOBA 165ISOFLO 165isoflurane 164-166ISO-VET 166ISTOLEPT 280, 283itraconazole 40-41ITRAFUNGOL 41IVERMAX 62ivermectine 58-60, 61, 62-65IVOMEC 59, 62, 64KALMIVET 172kanamycine 14-15, 215KARSIVAN 150KEFAVET VET 11KEFLORIL 17KELACTIN 84KELAPROFEN 106KENOCIDIN 192KENOSTART 193KESIUM 9kétamine 159-161KETAMINE 1000 CEVA 161kétanserine 210kétoconazole 41-42KETOFEN 106-107KETOFUNGOL 42kétoprofène 104-107KETOPROPIG 107KILTIX 204KLOXERATE 216, 217LACTETROL 130LACTOLYTE 130<strong>la</strong>ctose 129-130<strong>la</strong>ryngotrachéite infectieuse(virus de <strong>la</strong> -) 257, 265, 267-270LAURABOLIN 74Lawsonia intracellu<strong>la</strong>ris 249-250,252-253Leishmania infantum 281-282,282-284LEPTORABISIN 281, 283, 297Leptospira spp. 280-281, 282-284leucémie féline (virus de <strong>la</strong> -) 290-292,295-296LEUCOFELIGEN FeLV/RCP285, 288, 292, 295LEUCOGEN 291, 295LEUKOCELL 2 doses 291, 295lévamisole 46-47, 56LEVAMISOLE 7,5 % 47LEVAMISOLE HCl Ke<strong>la</strong> 47LEVATUM SUPER 64LEVAVETO 47LEVENTA 94lévothyroxine 94LH 74-78LIBROMIDE 187lidocaine 167-169LIDOPRIM S 31LIGNOCAINE HCL 2 % +ADRENALINE TARTRATE 169LINCOCIN 26LINCOCIN intramammaire 215lincomycine 24-25, 26, 38-39, 215LINCOMYCINE 40 %-VMD pulvis 26LINCOMYCINE-SPECTINOMYCINE-VMD 39LINCOMYCINE-VMD 26LINCO-SPECTIN 39, 303LOCATIM 299LOCATIM PLUS 299LONGACTON 81LONGAMOX 7LOXICOM 108lufénurone 65-66lutropine, voir LHM+Pac 245, 252
312INDEXmagnésium 130, 134-135ma<strong>la</strong>die de Carré, voir Carréma<strong>la</strong>die de Gumboro (virus de <strong>la</strong> -),voir Gumboroma<strong>la</strong>die de Gumboro, voir Gumboroma<strong>la</strong>die de <strong>la</strong> <strong>la</strong>ngue bleue (virus de <strong>la</strong>-), voir fièvre catarrhale ovinema<strong>la</strong>die de Marek, voir Marekma<strong>la</strong>die hémorragique virale(virus de <strong>la</strong> -), voir RHD virusMAMMYZINE 5Mannheimia haemolytica 234, 237-238MAPRELIN 77MARBIFLOX 37MARBOCYL 37marbofloxacine 31-32, 37-38, 212MARBOX 37Marek (virus de -) 255, 258, 260-261,263, 267-270MARFLOQUIN 37-38maropitant 123-124masitinib 301-302MASIVET 302MASTI-kel 215mavacoxib 110-112MAXIMEC 63MD, voir BVDmébendazole 42-43, 45, 64mébézonium (io<strong>du</strong>re de -) 167MEDESEDAN 177médétomidine 175-178MEDETOR 178médroxyprog 69-71MEFLOSYL 104MEGECAT 71mégéstrol acétate 69-71MELOVEM 108méloxicam 107-110MELOXIDYL 109MELOXIVET 109MELOXORAL 109METACAM 109-110métaflumizone 201-202, 208métamizole 101-102, 112, 122-123métergoline 83-85méthadone 119-120méthimazole 95-96méthoprène (S) 205-207METHOXASOL 31méthylprednisolone 86-88, 90métoclopramide 124-125METRICURE 213METRICYCLIN 213métronidazole 38, 40miconazole nitrate 191-192, 210, 212MICOTIL 22MILBEMAX 53milbémycine 53, 58-59MILOXAN 233, 238, 239MODERIN 90mométasone furoate 213monépantel 47-48MORPHASOL 117MOXAJECT 7MOXAPULVIS 7moxidectine 52-53, 56, 58-61, 63-64Mucosal Disease Virus, voir BVDMycop<strong>la</strong>sma gallisepticum 258,266-270Mycop<strong>la</strong>sma hyopneumoniae244-246, 252-253MYOGASTER-E 136MYORELAX 181MYPRAVAC SUIS 245, 252myxomatose (virus de <strong>la</strong> -) 254-255nafcilline 217NAFPENZAL DC 217nandrolone 73-74NARCOSTART 178NARCOSTOP 180NATRIUM PENTOBARBITAL 166NAXCEL 13NELIO 145NEMBUTAL 159NEOCOLIPOR 248, 252néomycine 14-15, 39, 210, 212, 215NEOPEN 39Newcastle Disease (virus -)vaccin pigeon 260, 267, 270vaccin vo<strong>la</strong>ille 255-256, 258-259,261-263, 267-270nicotinamide, voir vitamine BNIGLUMINE 104nitroxinil 49NIXAL spray 194NOBILIS CAV P4 264, 268NOBILIS E. COLI 266, 268NOBILIS GUMBORO D 78 264, 268NOBILIS IB 4 - 91 262, 268NOBILIS IB MA 5 262, 268NOBILIS IB MULTI + ND 263, 268NOBILIS ILT 265, 268NOBILIS ND + EDS 263, 268NOBILIS ND C2 261, 268NOBILIS ND CLONE 30 261, 268NOBILIS NEWCAVAC 261, 268NOBILIS OR INAC 266, 268NOBILIS REO ERS INAC 264, 269NOBILIS REO INAC 264, 269NOBILIS RHINO CV 265, 269NOBILIS RISMAVAC 260, 269NOBILIS RISMAVAC + CA 126260, 269NOBILIS RT+ IBmulti + ND + EDS263, 269NOBILIS RTV 8544 265, 269NOBILIS SALMONELLA ET 266, 269NOBIVAC BbPi 278, 280, 283NOBIVAC DHP 271, 274, 276, 283NOBIVAC DHPPI 272, 274,276, 278, 283NOBIVAC DUCAT 289, 295NOBIVAC LEPTO 281, 283NOBIVAC MYXO-RHD 254, 255NOBIVAC PARVO-C 273, 283NOBIVAC Pi 278, 283NOBIVAC PUPPY DP 274, 276, 283NOBIVAC RABIES224, 238, 239, 283, 295, 297
INDEX 313NOBIVAC TRICAT TRIO 286, 289, 295NOROCARP 105-106NOROCLAV 9NOROMECTIN 60, 63, 303NUFLOR 17nystatine 212OBLETS GYNECOLOGIQUES 213OCTACILLIN 7oestriol 154oméprazole 121ONSIOR 112OPTIMMUNE-CANIS 211ORBENIN E.D.C. 216ORBENIN LA 214ORBESEAL 217orbifloxacine 213ORIGIN 7ORNICURE 19Ornithobacterium rhinotracheale258, 266, 267-270osatérone 72-73OTOMAX 212OTOSPECTRINE 212OVARELIN 77oxantel 48, 55oxfendazole 42-43, 45oxyclozanide 49-50OXY-kel 20OXYTEM 194oxytétracycline 17-18, 20, 194OXYTETRACYCLINE Ke<strong>la</strong> 20oxytocine 79-81OXYTOCINE 81PALLADIA 302PANACUR 44, 303panleucopénie féline (virus de <strong>la</strong> -),voir parvovirusparacétamol 113PARACOX 265, 269PARACOX-5 265, 269para-influenza (virus -)bovin 224-226, 237-238chien 277-279, 282-284paramyxovirose (virus de <strong>la</strong> -), voirNewcastle DiseasePARAZAN 53paromomycine 14-15, 127PARPUMAG 135PARVODOG 273, 283PARVORUVAX 240, 251, 252PARVOSUIN-MR 240, 251, 252parvoviruschat 284-287, 295-296chien 273-275, 282-284porc 240-241, 252-253Pasteurel<strong>la</strong> multocida 247-248,252-253PASTOBOV 234, 238PATHOZONE 215péforéline 74-77pénéthamate 3-5, 217PENI-kel 5pentobarbital 157-159pergolide 92-93péritonite infectieuse féline(virus de <strong>la</strong> -) 292-293, 295-296perméthrine 196-198, 204-205,207-208PG-600 78PHARMASIN 23, 303phénobarbital 184-186PHENOLEPTIL 186phénoxyméthylpénicilline 3-5PHENOXYPEN WSP 5phénylbutazone 101-102phénylpropano<strong>la</strong>mine 153-154phosphate 130phoxime 195-196PI-3 (virus -), voir para-influenzapimobendan 148-149pirlimycine 215PIRSUE 215PLACIVET 172PLANATE 83PLANIPART 79PLUSET 78PMSG, voir eCGPNEUMODOG 278, 280, 283polymyxine B 210, 212polysulfate de pentosane 138PORCILIS APP 244, 252PORCILIS AR-T DF 247, 252PORCILIS ERY 251-252PORCILIS ERY-PARVO 240, 251, 252PORCILIS GLÄSSER 247, 252PORCILIS M. HYO 245, 252PORCILIS PARVO 240, 253PORCILIS PCV 243, 253PORCILIS PORCOLI DF 249, 253PORCILIS PRRS 242, 253PORCIMEC P 63posaconazole 213POSATEX 213potassium 129-130POTENCIL 40POULVAC AE 262, 269POULVAC BURSA PLUS 264, 269POULVAC BURSINE 264, 269POULVAC CHICK-N-POX TC 265, 269POULVAC E. COLI 266, 269POULVAC IB H 120 262, 270POULVAC IB PRIMER 262, 270POULVAC IBMM + ARK 262, 270POULVAC ILT 265, 270POULVAC MAREK H.V.T. 261, 270POULVAC MG 266, 270POULVAC ND HITCHNER B1 261, 270POULVAC ND LA SOTA 262, 270POULVAC P CANARY 267, 270POULVAC TRT 265, 270POVIDERM 192povidone iodée, voir iode (composés)PRACETAM 113PRAC-TIC 200-201pradofloxacine 31-33, 38PRASCEND 93praziquantel 48-49, 53-57, 64-65PRAZITEL PLUS 54prednisolone 86-88, 90-91
314INDEXPREDNISOLONE 90, 91Pregnant Mare Serum Gonadotropin,voir eCGPREVENTEF 196PREVICOX 112PRID DELTA 71PRILACTONE 147-148PRILBEN VET 145PRILENAL 145-146PRILIUM 146PRIMODOG 273, 283PRIMUCELL FIP 293, 295PROACTIVE 193PROACTIVE PLUS 193procaïne 169-170PROCAINE HCl 4 % 169PROCAINE HCL 4 % + ADRENALINE169, 170PROCOX 56PROFENDER 56,57progestérone 69-71PROGRAM 65-66PROGRESSIS 242, 253proligestone 69-71PROMERIS 202PROMERIS DUO 208PROMYCINE 128, 303PROPALIN 154propentofylline 149-150propofol 162-163PROPOVET MULTIDOSE 163propoxur 195-196, 204PROTEQ WEST NILE 222, 224PROTEQFLU 220, 224PROTEQFLU-TE 221, 223, 224PROXYLAZ 178PULMOTIL 22, 23, 303PUREVAX FeLV 291, 295PUREVAX RABIES 295, 297PUREVAX RC 289, 295PUREVAX RCP 286, 289, 295PUREVAX RCP FeLV 286, 289,292, 295PUREVAX RCPCh 286, 290, 294, 295PUREVAX RCPCh FeLV 286, 290, 292,294, 295pyrantel 48, 53-55pyridoxine, voir vitamine Bpyriprole 200-201QUADROSOL 10 % 47QUADROSOL pour-on 56rabbit haemorrhagic disease, voirRHD virusRABDOMUN 238, 283, 296, 297RABISIN 224, 238, 239, 283, 296, 297rage (virus de <strong>la</strong> -) 296-297ramipril 143-144, 146RAPIDEXON 89READYCEF 13RECEPTAL 77RECONCILE 183REGUMATE 72REGUMATE EQUINE 72RELEASE 166réovirus 257, 264, 267-270RESFLOR 40, 112RETARDOXI 20rétinol, voir vitamine A 20REVERTOR 180RHD virus 254, 255RHEMOX 7, 303RHEUMOCAM 110RHINIFFA T 248, 253RHINISENG 248, 253rhinopneumonie (virus de <strong>la</strong> -),voir herpèsvirusrhinotrachéite infectieuse bovine,voir IBRrhinotrachéite de <strong>la</strong> dinde(virus de <strong>la</strong> -) 257, 259,263, 265, 267-270rhinotrachéite féline (virus de <strong>la</strong> -), voirherpèsvirusribof<strong>la</strong>vine, voir vitamine Brifaximine 216-217RILEXINE 11, 215, 216RIMADYL 106RIMIFIN 106RINTAL 43-44RISPOVAL 3 BRSV-PI3-BVD226, 229, 238RISPOVAL IBR-MARKERINACTIVATUM 227, 238RISPOVAL IBR-MARKER VIVUM228, 238RISPOVAL RS + PI3 intranasal225, 238robénacoxib 110-112romifidine 175-176, 178ROMPUN 178RONAXAN 19ronidazole 51-52ROTAVEC CORONA 229, 231, 238rotavirus 229-230, 237-238RSB (virus -) 224-226, 237-238RUVAX VET 251, 253salicy<strong>la</strong>te 100-101Salmonel<strong>la</strong> spp. 258, 266, 267-270SARNACURAN 196SCALIBOR PROTECTORBAND 197SCOURGUARD 3 230, 232, 238SDRP (virus -) 241-242, 252-253SEDATOR 178SEDAXYL 178SEDAXYLAN 179SEDEDORM 178SEDIVET 178sé<strong>la</strong>mectine 58-60SELECTAN 17sélégiline 183-184SELENATE LA 134sélénium 134-136SELGIAN 184SERESTO 205SERUM ANTITETANIQUE 299SHOTAFLOR 17SLENTROL 126sodium 129-130
INDEX 315SODIUM SALICYL 80% WSP 101SOLACYL 101SOLIGENTAL 211SOLUBENOL 45SOLU-DELTA-CORTEF 90SOLUDOX 19SOLUTION PHYSIOLOGIQUE 130soufre 210SPARTRIX 52SPECTAM SCOUR-HALT 15, 127spectinomycine 14-15, 38-39, 127SPECTOLIPHEN 39SPECTRON 36spinosad 66-67spiramycine 21-22, 40spirono<strong>la</strong>ctone 146-148Staphylococcus aureus 235, 237-238STARTVAC 235, 238STELLAMUNE MYCOPLASMA245, 253STELLAMUNE ONE 246, 253STIMUFOL 78STOMORGYL 40STRESNIL 173STRONGHOLD 60SUISENG 249, 253sulfachlorpyridazine 29-30sulfaclozine 51sulfadiazine 29-31sulfadiméthoxine 51sulfadoxine 29-31sulfaméthoxazole 29-31sulfiram 212SUPPRESTRAL 71SUPRELORIN 77, 78SURAMOX 7, 303SUROLAN 210, 212SUVAXYN M.HYO 246, 253SUVAXYN M.HYO - PARASUIS246, 247, 253SUVAXYN MH-ONE 246, 253SUVAXYN PARVO/E 241, 251, 253SUVAXYN PCV 243, 253SYNCROSTIM 500 IU 77syndrome de chute de ponte (virus -),voir GumboroSyndrome Dysgénésique etRespiratoire Porcin (virus <strong>du</strong> -), voirSDRPSYNULOX 9-10T 61 167TAKTIC 203TARDAK 71, 73TELMIN KH 45TELMIN pâte 45TENASAN LA 20TERRAMYCINE 20tétanos, voir Clostridium tetaniTETAPUR 223, 224tétracaïne 166-167THERAPRIM 30THERIOS 12thiamazole, voir méthamizolethiamine, voir vitamine Bthymol 208-209THYMOVAR 209tiamuline 26-27TIAMUTIN 27, 303tildipirosine 21-22tilétamine 159-162tilmicosine 21-23TILMI-KEL 23TILMODIL 23TILMOVET 23, 303tocéranib 301-302tocophérol, voir vitamine ETOLFEDINE 103TOLFINE 103TOLTAROX 51TOLTRANIL 51toltrazuril 50-51TOPIMEC 60TRANQUILINE 172TRATOL 51TRICHO PLUS 52TRICHOCURE 52tric<strong>la</strong>bendazole 45-46, 53, 56trilostane 91-92TRIMAZIN 31triméthoprime 29-31TRIVIROVAX 272, 274, 276, 283TROCOXIL 112TRULEVA RTU 13TRUSCIENT 139TUCOPRIM 31, 303tu<strong>la</strong>thromycine 21-23TYLAN 24, 303TYLO-kel 24tylosine 21-24TYLOSINE Ke<strong>la</strong> 24TYLOVETO-20 24tylvalosine 21-22, 24UBIFLOX 38UBROLEXIN 215UBROSTAR DRY COW 217ULTRAVAC BOTULINUM 234, 238UNIFERON 134UNISOL 36VALBAZEN 43valnémuline 26-27, 28VANGUARD CPV 274, 283VANGUARD CPV-LEPTO275, 281, 283VANGUARD DA2PI-CPV272, 275, 276, 278, 284VANGUARD DA2PI-CPV-LEPTO272, 275, 276, 279, 281, 284VANGUARD LEPTO 281, 284variole (virus de <strong>la</strong> -)canari 260, 267, 270vo<strong>la</strong>ille 257, 265, 267-270VASOTOP P 146VAXXITEK HVT + IBD 263, 270VECOXAN 50VENTIPULMIN 141VEPRAFEN 53VERAFLOX 38VETALGIN 102
316INDEXVET-CLEAN 192VETERELIN 78VETERGESIC MULTIDOSIS 115VETFLURANE 166VETMEDIN 149VETMULIN 27, 303VETODEXIN 89VETORYL 92VETRIMOXIN 7-8VEXYLAN 179VIRBACTAN 216VIRBAGEN OMEGA 300VIRBAGEST 72VIRBAMEC 60Virus Respiratoire Syncytial Bovin,voir RSBvitamine A 132-133VITAMINE A + D3 + E inj 133VITAMINE A + D3 + E sol buvable 133vitamine B 131-132VITAMINE B COMPLEX Ke<strong>la</strong> 132vitamine D 132-133vitamine E 132-133VITAMINE E + SELENIUM 136VITOFYLLIN 150VOMEND ANTI-EMETICUM 125VOREN 89VULKETAN 210West Nile Virus, voir fièvre<strong>du</strong> Nil occidental (virus de <strong>la</strong> -)XEDEN 36xy<strong>la</strong>zine 175-176, 178-179XYL-M 179YPOZANE 73ZACTRAN 22ZANIL 50ZANTEL 53ZEROFEN 44zinc 210zo<strong>la</strong>zépam 159-162ZOLETIL 162ZOLVIX 48ZULVAC 8 Bovis 230, 238ZUPREVO 22DRUK GOEKINT GRAPHICS OOSTENDE