La reproduction des algues Diatomées
La reproduction des algues Diatomées
La reproduction des algues Diatomées
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>La</strong> <strong>reproduction</strong> <strong>des</strong> <strong>algues</strong><br />
I. <strong>La</strong> multiplication végétative<br />
I. <strong>La</strong> multiplication végétative<br />
1.1 Multiplication végétative par mitose<br />
1.2 Multiplication végétative par fragmentation du thalle<br />
1.3 Reproduction asexuée par spores directes<br />
II. <strong>La</strong> <strong>reproduction</strong> sexuée avec recombinaison génétique<br />
2.1 Cycle monogénétique haplophasique : Clamydomonas, Spirogyre<br />
2.2 Cycle monogénétique diplophasique : Fucus<br />
2.3 Cycle digénétique diplohaplophasique hétéromorphe : <strong>La</strong>minaires<br />
2.4 Cycle digénétique haplodiplophasique isomorphe : Ulve<br />
2.5 Cycle trigénétique : Antithamniom, Polysiphonia<br />
• 1.1. Multiplication végétative par division<br />
mitotique (cas <strong>des</strong> espèces unicellulaires)<br />
•1.2 Multiplication végétative par<br />
fragmentation de thalles, chaque fragment<br />
régénère un thalle complet<br />
•1.3 Multiplication végétative par<br />
production de spores directes<br />
I. <strong>La</strong> multiplication végétative<br />
1.1. Multiplication végétative par division<br />
mitotique<br />
Cas du Chlamydomonas<br />
I. <strong>La</strong> multiplication végétative<br />
1.1. Multiplication végétative par division<br />
mitotique<br />
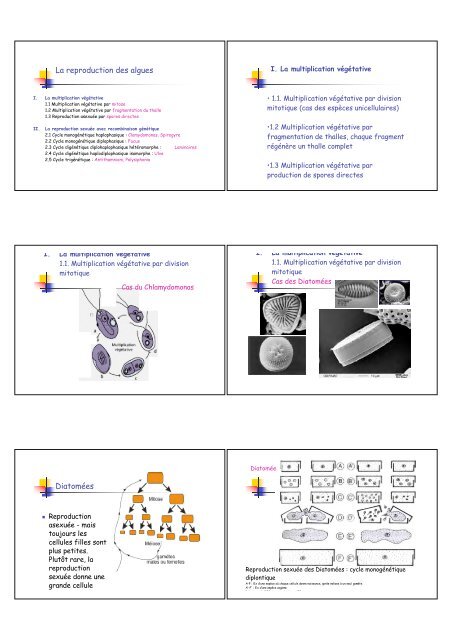
Cas <strong>des</strong> <strong>Diatomées</strong><br />
Diatomée<br />
<strong>Diatomées</strong><br />
! Reproduction<br />
asexuée - mais<br />
toujours les<br />
cellules filles sont<br />
plus petites.<br />
Plutôt rare, la<br />
<strong>reproduction</strong><br />
sexuée donne une<br />
grande cellule<br />
Reproduction sexuée <strong>des</strong> <strong>Diatomées</strong> : cycle monogénétique<br />
diplontique<br />
A-F : Ex d’une espèce où chaque cellule donne naissance, après méiose à un seul gamète<br />
A’-F’ : Ex d’une espèce oogame<br />
Robert et al. 1998, <strong>La</strong> <strong>reproduction</strong> p.100
I. <strong>La</strong> multiplication végétative<br />
1.2 Multiplication végétative par fragmentation<br />
de thalles<br />
Les marées vertes : pullulation d’Ulves<br />
Marée verte en baie de <strong>La</strong>nion<br />
Marée vert en baie de <strong>La</strong>nion
Stock d'ulves diffus dans le<br />
proche littoral.<br />
Rideau d'ulves se déplaçant avec la<br />
marée. C'est le siège de la<br />
multiplication <strong>des</strong> <strong>algues</strong>.<br />
Dépôt d'<strong>algues</strong> sur la zone<br />
découverte par la marée. Elles<br />
seront repoussées par la marée<br />
sur le haut de la plage.<br />
Dépôts en haut de plage<br />
Rivière<br />
Vue aérienne d’une marée verte<br />
En baie de <strong>La</strong>nnion et Saint Brieuc : Ulva armorica<br />
espèce opportuniste<br />
sciaphile<br />
optimum de croissance 17-23°C<br />
En rade de Brest : Ulva rotundata<br />
Venise : Ulva laetevirens (95%) Enteromorpha et<br />
Cladophora. <strong>La</strong> dégradation <strong>des</strong> <strong>algues</strong> génère de<br />
l’anoxie, seules les larves de Chironomes survivent<br />
..<br />
Les marées vertes<br />
Les problèmes :<br />
aspect, contact et odeur désagréables<br />
DMSP<br />
mais recyclages <strong>des</strong> nutriments et pullulation inoffensive<br />
Aspects économiques :<br />
Impact négatif sur le tourisme<br />
Coût élevé de l’enlèvement (collecte, transport stockage)<br />
Prévention :<br />
récolte en hiver Pb développement d’autres <strong>algues</strong><br />
régulation <strong>des</strong> intrants Financement <br />
I. <strong>La</strong> multiplication végétative<br />
1.2 Multiplication végétative par production de<br />
spores directes<br />
Porphyra<br />
II. <strong>La</strong> <strong>reproduction</strong> sexuée avec<br />
recombinaison génétique<br />
Rappels et définitions<br />
Sporophyte, Gamétophyte<br />
Spores : meïospores, zoospores (avec flagelle)<br />
Gamètes : zoogamètes, isogamie, anisogamie,<br />
oogamie.<br />
Cystes : organes reproducteurs<br />
Cycles monogénétique, digénétique, trigénétique<br />
Haplontique, diplontique, haplodiplontique,<br />
diplohaplontique, hétéromorphe , isomorphe)
II.<br />
<strong>La</strong> <strong>reproduction</strong> sexuée avec recombinaison génétique<br />
2.1 Cycle monogénétique haplophasique<br />
a. 1 er exemple : Cas du Chlamydomonas<br />
Rappels<br />
2.1 Cycle monogénétique haplophasique<br />
b. 2 ème exemple : Cas de la Spirogyre<br />
Cycle monogénétique haplophasique de Clamydomonas moewusii<br />
d'après B. de Riviers – Biologie et phylogénie <strong>des</strong> <strong>algues</strong>, 2002, Ed Belin – Tome 1 p.199<br />
Cystogamie<br />
chez la Spirogyre<br />
Le cytoplasme passe<br />
d’une cellule à l’autre<br />
par un tube de<br />
conjugaison<br />
Cycle monogénétique haplophasique de la Spirogyre<br />
d'après J.-C. Roland et B.Vian - Atlas de Biologie Végétale, 1985, Ed MASSON - fig 1.70
2.1 Cycle monogénétique haplophasique<br />
c. 3 ème exemple : Chara<br />
d. 4 ème exemple : Acetabularia<br />
Depuis le Silurien (-420 MA) : le Gyrogonite équivalent de Chara<br />
Cycle monogénétique haplophasique de l’Acétabulaire<br />
d'après de Riviers<br />
2.2 Cycle monogénétique diplophasique<br />
Cas du Fucus vesiculosus<br />
Fucus mâle<br />
Coupe Transversale d'un conceptacle d’un pied<br />
mâle<br />
(espèce dioïque)<br />
Photographie Vincent Tandart, 1997<br />
Fucus femelle<br />
Coupe Transversale d'un conceptacle d’un pied<br />
femelle<br />
Cycle monogénétique diplophasique du Fucus vésiculeux<br />
d'après J.-C. Roland et B.Vian - Atlas de Biologie Végétale, 1985, Ed MASSON - fig 1.57
Ascophyllum nodosum<br />
Réceptacles femelles d’Ascophyllum nodosum<br />
! Fucus spiralis<br />
! Fucus vesiculosus<br />
! Ascophyllum nodosum<br />
! Fucus serratus<br />
monoïque<br />
dioïques<br />
2.3 Cycle<br />
digénétique<br />
diplohaplophasique<br />
hétéromorphe :<br />
<strong>La</strong>minaria digitata<br />
Conceptacles orangés = pied mâle<br />
Conceptacles verdâtres = pied femelle<br />
2.3 Cycle digénétique diplohaplophasique hétéromorphe :<br />
Sporophyte de <strong>La</strong>minaria digitata<br />
Gamétophyte
Découverte <strong>des</strong> phéromones <strong>des</strong> <strong>algues</strong><br />
brunes.<br />
Les phéromones <strong>des</strong> Algues brunes<br />
1854 : Thuret observe sur Fucus, gamètes mâles attirés par<br />
oosphère<br />
1947 : Cook montre que certaines substances ont un effet<br />
attracteur sur les gamètes.<br />
1967 : Müller, sur Ectocarpus, montre qu’une substance est<br />
secrétée par le gamète femelle.<br />
1971 : le composé est isolé, purifié, son activité démontrée.<br />
Sur plus de 60 <strong>algues</strong> brunes 11 composés de ce type ont<br />
été mis en évidence.<br />
Structure chimique <strong>des</strong> phéromones isolées de diverses <strong>algues</strong> brunes<br />
d'après B. de Riviers – Biologie et phylogénie <strong>des</strong> <strong>algues</strong>, 2002, Ed Belin – Tome 1 p.267<br />
Les phéromones <strong>des</strong> Algues brunes<br />
2.4. Cycle digénétique haplodiplophasique<br />
Cas de la <strong>La</strong>itue de mer<br />
Ces composés provoquent la libération <strong>des</strong> gamètes mâles et<br />
leur attraction vers les gamètes femelles.<br />
Spécificité :<br />
Solvant organique aussi attracteurs mais l’attractant<br />
spécifique agit à <strong>des</strong> concentrations très faibles 10 -7 ou 10 -10<br />
M.<br />
Ulva lactuca<br />
Rôle dans la compétition.<br />
2.5 Cycle trigénétique <strong>des</strong> <strong>algues</strong> rouges<br />
a. Cas d’Antithamnion<br />
Antithamnion plumula<br />
Cycle digénétique haplodiplophasique de la <strong>La</strong>itue de mer<br />
d'après J.-C. Roland et B.Vian - Atlas de Biologie Végétale, 1985, Ed MASSON - fig 1.71
Carposporophyte<br />
(2n)<br />
Trichogyne<br />
Pyrémoïde<br />
Oosphère<br />
Cycle trigénétique d'Antithamnion<br />
d'après J.-C. Roland et B.Vian - Atlas de Biologie Végétale, 1985, Ed MASSON<br />
Spermatocystes<br />
Carpogone<br />
Organes reproducteurs <strong>des</strong> <strong>algues</strong> rouges<br />
d'après B. de Riviers – Biologie et phylogénie <strong>des</strong> <strong>algues</strong>, 2002, Ed Belin – Tome 1 p.196<br />
Thalle porteur de tétraspores<br />
Carpogone<br />
D’après P. Gayral et J. Cosson - Les Algues du littoral 1997 Ed. Ouest France p. 28<br />
A gauche : micrographie par interférence différentielle (tr:trichogyne, s:spermatie)<br />
A droite : radiographie par marquage à l'alpha-D-mannosylated-FITC-albumine<br />
2.5. Cycle trigénétique <strong>des</strong> <strong>algues</strong> rouges<br />
b. Cas de Polysiphonia elongata<br />
Cycle trigénétique haplophasique de Polysiphonia elongata<br />
d'après B. de Riviers – Biologie et phylogénie <strong>des</strong> <strong>algues</strong>, 2002, Ed Belin – Tome 1 p.225
Polysiphonia<br />
elongata<br />
Gamétophyte mâle portant <strong>des</strong> amas de spermatocystes<br />
Gamétophyte femelle portant un carposporophyte<br />
Tétrasporophyte contenant les tétraspores en cours de formation (meïose)<br />
Chondrus crispus<br />
Gamétophyte femelle portant <strong>des</strong> cystocarpes (emplacement marqué par<br />
une saillie d’un coté du thalle)<br />
Gamétophyte femelle portant <strong>des</strong> cystocarpes<br />
Mastocarpus stellatus
Mastocarpus stellatus<br />
Chara<br />
Petrocellis cruenta<br />
Tétrasporophyte encroutant<br />
Mastocarpus stellatus<br />
Gamétophyte femelle<br />
Depuis le Silurien (-420 MA) : le Gyrogonite équivalent de Chara<br />
Coleochaete<br />
Coleochaete<br />
Exemple de nématothalle de type rampant : les filaments<br />
rampants se soudent pour former un disque aplati sur le support.<br />
Evolution du cycle de <strong>reproduction</strong> <strong>des</strong> Streptophyta<br />
De Reviers p. 219<br />
Contrôle du cycle de <strong>reproduction</strong><br />
Il s'opère lors du passage à la <strong>reproduction</strong> sexuée. Ce passage peut être sous<br />
le contrôle de :<br />
! facteurs externes<br />
! les ressources du milieu. Chlamydomonas ou <strong>des</strong> spirogyres, et de<br />
nombreuses autres espèces <strong>des</strong> eaux temporaires. Le zygote est alors<br />
une forme de résistance.<br />
! le rythme lunaire (<strong>des</strong> marées). Ulve dont la libération <strong>des</strong> spores est<br />
liée aux marées de mortes-eaux. Contrôle par la photopériode.<br />
! période d'obscurité. Chez Pelvetia ou les laminaires, la libération <strong>des</strong><br />
gamètes.<br />
! Les radiations bleues, Chez Acetabularia, <strong>La</strong>minaria, Macrocystis, la<br />
formation <strong>des</strong> gamètes. le cryptochrome est responsable de la détection<br />
<strong>des</strong> radiations.<br />
! facteurs endogènes<br />
! la taille. <strong>Diatomées</strong>. Volvox lorsque la taille de la colonie est suffisante<br />
certaines colonies produisent <strong>des</strong> gamètes mâles, sécrètent alors une<br />
phéromone peptidique dans le milieu qui induit la production de gamètes<br />
mâles et femelles chez les autres colonies. Ici le Volvox anticipe les<br />
mauvaises conditions en provoquant la <strong>reproduction</strong> sexuée et la<br />
formation de zygote de résistance au moment où la croissance de la<br />
colonie est maximale.
Conclusion<br />
Pas d’unité dans les cycles de <strong>reproduction</strong>, même au<br />
sein de chaque lignée<br />
<strong>La</strong> <strong>reproduction</strong> <strong>des</strong> <strong>algues</strong> est <strong>des</strong> plus diversifiée.<br />
Le rythme et le régime de <strong>reproduction</strong> sont influencés<br />
par les facteurs du milieu, notamment la lumière, la<br />
température et la teneur en éléments nutritifs.