desc pp - desc orthopedie
desc pp - desc orthopedie
desc pp - desc orthopedie
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
UNIVERSITE PAUL SABATIER – TOULOUSE III<br />
FACULTES DE MEDECINE<br />
Reconstruction osseuse après reprise de<br />
prothèse totale de hanche par la tige PP<br />
Au recul minimal de 12 ans<br />
Mémoire présenté le 5 Septembre 2009 en vue de l’obtention du<br />
Diplôme d’Etude Spécialisée de Chirurgie<br />
orthopédique et traumatologique<br />
Dr DAO Charles
I INTRODUCTION<br />
II GENERALITES<br />
A/ LES CAUSES DU DESCELLEMENT ASEPTIQUE<br />
B/ CLASSIFICATION DE LA PERTE DE SUBSTANCE OSSEUSE FEMORALE<br />
C/ LES DIFFERENTS MOYEN DE REPRISE<br />
D/ STRATEGIE THERAPEUTIQUE<br />
E/ ANALYSE DE LA RECONSTRUCTION OSSEUSE<br />
F/ TECHNIQUE CHIRURGICALE<br />
III NOTRE ETUDE<br />
A/ MATERIEL ET METHODE<br />
B/ RESULTATS<br />
C/ DISCUSSION<br />
IV CONCLUSION<br />
BIBLIOGRAPHIE<br />
1
I INTRODUCTION<br />
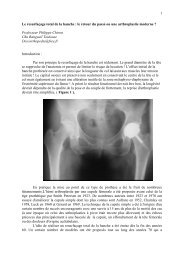
L’arthroplastie totale de hanche est devenue, comme le présageait Charnley, une<br />
intervention orthopédique de routine. Il est posé a<strong>pp</strong>roximativement 120 000 prothèses totales<br />
de hanche en France par an dont plus de 12 000 révisions avec un taux de progression annuel<br />
de 10% environ.<br />
Les implantations primaires sont en constante progression, devant une demande<br />
croissante dans une population vieillissante en age et en nombre, mais aussi de plus en plus<br />
exigeante, élargissant le champ des indications vers des patients plus jeunes.<br />
L’essor de l’arthroplastie totale de hanche dans les années 80 se répercute aujourd’hui<br />
en terme de rescellement. D’autre part, l’implantation sur des patients de plus en plus jeunes<br />
accroît le risque de reprises itératives.<br />
La reprise d’arthroplastie totale de hanche devient donc de plus en plus fréquente et<br />
répandue devant le vieillissement de la population et une demande fonctionnelle accrue.<br />
Elle pose essentiellement le problème de la perte du capital osseux fémoral et<br />
cotyloïdien. Elle doit donc permettre une reconstruction osseuse et une stabilité mécanique de<br />
l’implant.<br />
La planification pré-opératoire est donc primordiale dans le choix de la technique<br />
chirurgicale et le choix des implants.<br />
Nous présentons ici une série de reprises de prothèse totale de hanche pour <strong>desc</strong>ellement<br />
aseptique utilisant la prothèse de reconstruction « PP »avec un erccul minimal de 12 ans.<br />
B/ LES CAUSES DU DESCELLEMENT ASEPTIQUE<br />
Le <strong>desc</strong>ellement aseptique peut être considéré comme une véritable maladie iatrogène<br />
liée à l’implantation d’une prothèse totale de hanche. Il correspond au facteur limitant<br />
essentiel de la longévité des arthroplasties totales de hanche.<br />
LES FACTEURS DU DESCELLEMENT<br />
Le patient<br />
Le très jeune age 9,23 , l’obésité 8,66 , l’activité physique intense 67 sont des facteurs<br />
favorisants ainsi que l’implantation d’une prothèse sur une hanche non vierge 14 .<br />
2
Le scellement<br />
Le scellement prothétique entraîne une nécrose osseuse au niveau du site<br />
d’implantation. Cette nécrose est due à la dévascularisation osseuse par le passage des râpes, à<br />
la toxicité locale du monomère, à la réaction thermique et l’hyper pression qui accompagnent<br />
la polymérisation du ciment 3 .<br />
Le ciment<br />
Soumis à la fréquence importante des contraintes notamment en torsion 54,65 , il se<br />
fragilise progressivement à l’interface implant-ciment et entraîne la libération de débris<br />
d’usure, responsables d’une réaction à corps étranger, source d’une ostéolyse progressive 68,69 .<br />
Il s’y associe également une dégradation des propriétés mécaniques avec le temps 47 .<br />
L’implant<br />
Un dessin inadapté de l’implant fémoral peut entraîner un excès de contraintes sur le<br />
ciment aboutissant à une fragmentation du ciment ou une mauvaise transmission des<br />
contraintes sur le su<strong>pp</strong>ort osseux cortical, source d’ostéolyse progressive par « stressschielding<br />
». L’ostéolyse peut également être due à l’usure du couple de frottement utilisé<br />
avec libération de débris de polyéthylène et formation d’un granulome.<br />
Le chirurgien<br />
Le positionnement a<strong>pp</strong>roximatif des implants, en varus notamment 49 , ainsi que la<br />
technique de scellement et de cimentage influent naturellement sur la longévité de<br />
l’arthroplastie 24 .<br />
Ces différents facteurs aboutissent à une perte osseuse péri-prothétique responsable du<br />
<strong>desc</strong>ellement des implants.<br />
C/ CLASSIFICATION DE LA PERTE DE SUBSTANCE OSSEUSE<br />
FEMORALE<br />
Il existe de nombreuses classifications de la perte de substance osseuse périprothétique.<br />
Il s’agit pour la plupart de classifications radiologiques <strong>desc</strong>riptives.<br />
SOFCOT 88<br />
C’est la classification de Vives définie pour le symposium de 1988 que nous avons<br />
a<strong>pp</strong>elé SO.F.C.O.T. 88<br />
3
Stade I : les corticales sont amincies mais correctes avec une lyse plus ou moins<br />
importante du Merckel<br />
Stade II : la corticale latérale est très amincie, mais la corticale médiale amincie reste<br />
correcte<br />
Stade III : la corticale latérale est très amincie et la corticale médiale en partie détruite<br />
sous le petit trochanter,<br />
Stade IV : le fémur est pellucide ou disparu.<br />
AAOS<br />
Pour la classification AAOS 11 , trois niveaux sont évalués :<br />
Le niveau I situé au-dessus du petit trochanter,<br />
Le niveau II situé sur la diaphyse 10 cm au-dessous du petit trochanter<br />
Le niveau III au-delà.<br />
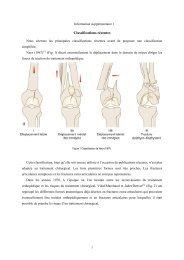
Il s'agit d'une classification mixte, qui évalue à la fois les dégâts osseux selon une<br />
graduation croissante pour les stades IIa, IIb, IIc et III, mais qui en même temps décrit des<br />
anomalies morphologiques localisées comme les cals vicieux, les fractures, les sténoses, mais<br />
aussi des pertes de substance localisées comme les types 1A1 ou 1A2 ou 1C.<br />
4
Type IVA /IVB Type V Type VI<br />
Classification de Paprosky 56<br />
Stade I : Métaphyse proximale intacte. Merckel partiellement détruit. Perte de substance<br />
antérieure et postérieure peu importante. Diaphyse intacte.<br />
Stades II (II A, IIB, IIC) : la métaphyse est altérée, il n'y a plus de Merckel, la perte de<br />
substance antérieure et postérieure est majeure, la diaphyse est intacte.<br />
Stade II A : Merckel disparu mais la perte de substance osseuse n'atteint pas la région<br />
sous-trochantérienne.<br />
Stade IIB : Disparition de la face antéro-latérale de la métaphyse (région soustrochantérienne).<br />
Stade IIC : Absence d'a<strong>pp</strong>ui métaphysaire (corticale médiale absente ou non<br />
fonctionnelle).<br />
Stade III : La métaphyse ne peut plus assurer de soutien. Il n'y a plus de Merckel. Perte<br />
de substance antérieure et postérieure majeure. La diaphyse est intéressée par la destruction<br />
osseuse.<br />
5
SOFCOT 99<br />
Le symposium de la SOFCOT en 1999 nous a montré certaines insuffisances de la<br />
classification SO.F.C.O.T. 88, et il est a<strong>pp</strong>aru utile de la faire évoluer en l'intitulant<br />
SO.F.C.O.T. 99. Cette évolution se traduit par des modifications mineures, la trame de la<br />
classification SO.F.C.O.T. 88 ayant été maintenue. Les modifications portent sur l'ajout de<br />
suffixes aux stades précédemment décrits et sur la création d'un stade « zéro ». Ainsi on peut<br />
simplement ajouter aux stades habituels des lettres suffixes identifiant respectivement l'état du<br />
grand trochanter par la lettre T, l'atteinte diaphysaire distale à plus de 10 cm sous le petit<br />
trochanter par la lettre D, la lettre F permet d'identifier une fracture, et V un cal vicieux ou<br />
une déformation. Cette évolution était indispensable car il semblerait qu'une atteinte distale<br />
doive être considérée même dans un stade III, qu'il s'agisse d'une destruction ou d'une<br />
déformation fémorale.<br />
Il faut signaler que ces différentes classifications évaluent la perte de substance osseuse<br />
au travers d’un bilan radiologique. Elles sous-estiment fréquemment l’importance des dégâts<br />
et la situation doit être réévaluée systématiquement en per-opératoire après extraction de<br />
l’implant fémoral et nettoyage des débris de ciment.<br />
D/ LES DIFFERENTS MOYENS DE REPRISE<br />
LES TIGES DE REVISION CIMENTEES<br />
Bien que les tiges de révision cimentées aient l’avantage de faciliter la fixation primaire<br />
en permettant une mobilisation immédiate, la surface endostée, souvent lisse et sclérotique,<br />
empêche une fixation optimale de l’implant du type de celle obtenue en chirurgie primaire.<br />
Dohmae et al 12 ont montré que les forces de cisaillement nécessaires pour mobiliser le<br />
ciment diminuent de 20% après la première reprise et chutent encore de 6% en cas de<br />
deuxième révision. En plus de l’absence d’interdigitation du ciment dans l’os lors d’une<br />
reprise avec une tige cimentée, il semble également que la pressurisation du ciment autour<br />
d’une longue tige de reprise soit moins bonne.<br />
Les résultats obtenus dans différentes séries publiées ne sont pas satisfaisants avec un<br />
taux de <strong>desc</strong>ellement entraînant une révision, allant de 3 à 38%, pour un recul allant jusqu’à<br />
6
15 ans. Le taux global de <strong>desc</strong>ellement radiographique atteint même 53% si l’on inclue les<br />
patients n’ayant pas subi de nouvelle révision 22,39,48,51,64 .<br />
L’amélioration des techniques de cimentage (préparation minutieuse du canal,<br />
pressurisation optimale du ciment) a permis d’améliorer les résultats de ces reprises. Ce taux<br />
de <strong>desc</strong>ellement reste néanmoins élevé, il est de l’ordre de 10% à 9 ans de recul moyen 19,30,58 .<br />
Il est également possible, dans des situations particulières, de recimenter un implant<br />
fémoral à l’intérieur du fourreau cimenté pré-existant. Cette technique est néanmoins à<br />
réserver par exemple à des patients dont l’état général ne permet pas un nettoyage minutieux<br />
de l’ensemble du manteau de ciment .Cette technique à fait l’objet de publications plus ou<br />
moins récentes. Lieberman et al 36 n’ont pas retrouvé de re-révision ni <strong>desc</strong>ellement des<br />
implants dans une série de 19 patients, à 59 mois de recul. Cependant, Li et al 11 ont constaté<br />
dans une étude biomécanique que les forces de cohésion étaient significativement diminuées<br />
entre les deux envelo<strong>pp</strong>es de ciment, surtout s’il persistait des débris ou du sang à l’intérieur<br />
du manteau de ciment initial.<br />
LES TIGES DE REVISION NON CIMENTEES<br />
Afin de tenter d’abaisser le taux de <strong>desc</strong>ellement des séries de révision cimentées, il a<br />
été dévelo<strong>pp</strong>é des tiges de révision non cimentées.<br />
Les résultats de ces révisions non cimentées ont été publiés et semblent meilleurs dans<br />
l’ensemble à ceux des reprises non cimentées. Il faut néanmoins différencier les tiges à<br />
traitement de surface total et celles qui sont à traitement de surface uniquement proximal.<br />
En effet, dans les séries utilisant des tiges à revêtement proximal le taux de re-révision<br />
est selon les séries de 3% à 10% à 3 ou 4 ans de recul 37,50 , mais il s’élève à 18 à 42% si le<br />
recul atteint 7 à 8ans 2,17 .<br />
Le traitement de surface total permet d’obtenir des résultats plus favorables en<br />
permettant d’optimiser l’ancrage distal. Dans les séries utilisant ce type d’implant, pour un<br />
recul compris entre 4 et 8 ans, le taux de re-révision oscille entre 0 et 6%.<br />
Signalons la série d’Essig, utilisant la prothèse modulaire « PP »à traitement de surface<br />
total, dans laquelle le taux de ré-intervention est de 7% pour un recul moyen de 6 ans 18 .<br />
LES REPRISES AVEC GREFFE IMPACTEE<br />
Le principe est de cimenter un implant fémoral à l’intérieur d’un lit de greffe morcelée<br />
impactée 15,16,43 .<br />
7
Elle permet dans ces situations, de reconstituer un nouveau canal médullaire grâce à<br />
l’impaction d’os à l’intérieur du fût fémoral préexistant. Une tige fémorale peut alors être<br />
cimentée dans le nouveau canal médullaire, rendant possible une éventuelle désescalade.<br />
Cette technique permet une restauration du stock osseux, comme le montrent les études<br />
histologiques effectuées après l’ablation des tiges post mortem 27 , ou sur des biopsies 1,53 .<br />
Les résultats de cette technique semblent satisfaisants avec un recul atteignant 5 ans. En<br />
effet, le taux de re-révision dans ces séries ne dépasse 4% 5,15,33,43 .Cette technique, malgré le<br />
risque de fracture fémorale et d’infection, parait donc adaptée aux <strong>desc</strong>ellements conservant<br />
un fémur plus ou moins continent. Le taux d’enfoncement de l’implant fémoral est néanmoins<br />
important mais sans répercussion clinique dans la majorité des cas. Le risque de fracture<br />
fémorale serait quant à lui corrélé à la longueur du bras de levier distal 15,16,40,43 . Il est donc<br />
recommandé, si la prothèse est en regard d’une corticale amincie, de la renforcer par une<br />
allogreffe a<strong>pp</strong>osée 26,55 .<br />
LES ALLOGREFFES SEGMENTAIRES MASSIVES<br />
Il s’agit d’une technique essentiellement utilisée en France par l’équipe de l’hôpital<br />
Cochin (Pr Kerboull, Pr Courpied). Elle est proposée dans les reprises comportant une perte<br />
de substance segmentaire étendue, afin de reconstruire l’extrémité supérieure du fémur. Elle<br />
est en général associée à une longue tige cimentée. Celle-ci est scellée à la greffe corticale en<br />
proximal et au fémur hôte en distal.<br />
Courpied 10 a présenté une série de 20 reprises fémorales utilisant cette technique. A un<br />
recul moyen de 5 ans, il ra<strong>pp</strong>orte 3 cas de <strong>desc</strong>ellement radiologique et un cas de migration de<br />
la tige. Il existait 7 cas de résorption partielle de l’allogreffe et 2 cas de résorption majeure.<br />
LES PROTHESES NON CIMENTEES MODULAIRES<br />
Cette technique a été ra<strong>pp</strong>ortée à partir du système PP en France et par Chandler en<br />
Amérique du Nord. Cette technique est fondée sur l’idée de s’adapter aux modifications de<br />
l’extrémité supérieure du fémur, qu’il s’agisse de déformations de la métaphyse ou de perte<br />
de substance.<br />
Le système PP recherche un a<strong>pp</strong>ui le plus proximal possible, mais en zone suffisamment<br />
solide pour stabiliser la tige. La partie prothétique métaphysaire a pour objectif de combler la<br />
perte de substance osseuse métaphysaire. La stabilité est assurée par la collerette et surtout par<br />
l’a<strong>pp</strong>ui de la tige quadrangulaire dans le fût fémoral. La tige fémorale possède également un<br />
8
traitement de surface total. Dans une série de 46 reprises, Essig 18 a retrouvé un taux de<br />
<strong>desc</strong>ellement de 10%.<br />
Chandler, lui, cherche à remplir la métaphyse et à résoudre l’incongruence métaphysodiaphysaire.<br />
Il ra<strong>pp</strong>orte dans une série de 52 prothèses avec un recul moyen de 3 ans, un taux<br />
de <strong>desc</strong>ellement de 10%.<br />
Mc Carthy 6 a publié une série de révision utilisant la prothèse modulaire S-ROM® , un<br />
taux de ré-intervention de 1,5 % à 5 ans de recul.<br />
Chao et Sim 7 ont présenté une série de méga-prothèses modulaires, suivant la<br />
reconstruction de l’extrémité supérieure du fémur après exérèse tumorale mais également<br />
dans des reprises fémorales stade IV 38 . La technique chirurgicale est fondée sur le cimentage<br />
d’une tige fémorale associée à des greffes corticales devant induire la reconstruction osseuse.<br />
LES PROTHESES NON CIMENTEES VEROUILLEES<br />
Le concept de prothèses de reprise de hanche verrouillées a été introduit en France par<br />
Vives, et par Stossel en Grande-Bretagne 63 . Vives associait initialement à cette tige<br />
verrouillée, une allogreffe impactée morcelée. Actuellement, il a abandonné cette allogreffe et<br />
préfère effectuer une fémorotomie en a<strong>pp</strong>liquant le concept de consolidation osseuse après<br />
traitement d’une fracture par enclouage verrouillé. Cependant, la transmission des contraintes<br />
vers l’extrémité distale de la prothèse, peut entraîner un stress-schielding accru et<br />
inhomogène, pouvant aboutir à une faillite de l’implant.<br />
E/ STRATEGIE THERAPEUTIQUE<br />
La réalisation d’une reprise de prothèse totale de hanche doit tenir compte de multiples<br />
paramètres qui ne concernent pas tous l’acte chirurgical. Dans ce contexte, la planification<br />
pré-opératoire est essentielle.<br />
Etat général du patient.<br />
L’âge de ces patients est en général supérieur à celui des prothèses de première<br />
intention. Les comorbidités sont également plus fréquentes, ainsi que les portes d’entrée<br />
infectieuse. Le score ASA est le plus souvent égal à 2 ou 3.<br />
La présence d’une boiterie et d’une éventuelle inégalité de longueur des membres<br />
inférieurs doit également être noté, car cela peut orienter le choix des implants.<br />
9
Tous ces éléments sont alors pris en considération dans l’analyse bénéfice-risque de<br />
l’intervention.<br />
Arthroplastie initiale<br />
Le type de prothèse initiale, le diamètre de la tête fémorale et le mode de fixation<br />
doivent être documentés à l’aide des compte-rendus opératoires ou des registres.<br />
Le type de <strong>desc</strong>ellement<br />
Un <strong>desc</strong>ellement global de la tige fémorale n’entraînera que des lésions osseuses<br />
minimes lors de l’extraction endo-médullaire de l’implant fémoral. À l’inverse, un<br />
<strong>desc</strong>ellement n’intéressant que l’interface implant-ciment augure d’une extraction difficile et<br />
donc des lésions osseuses secondaires non négligeables qu’il faut savoir anticiper.<br />
L’évaluation du stock osseux reste un des facteurs les plus importants dans le choix de<br />
la technique chirurgicale. Les classifications les plus fréquemment utilisées sont celles de<br />
Paprosky, SoFCOT, AAOS.<br />
Puget propose de regrouper les différentes situations chirurgicales en trois niveaux<br />
lésionnels pratiques 59 .<br />
Niveau I : Pas de perte de substance osseuse significative<br />
Ce stade peut être considéré comme une prothèse de première intention. Des techniques<br />
diverses, comme une tige non cimentée à traitement de surface proximal ou total, une tige<br />
cimentée ou même une technique d’impaction de greffe peuvent être utilisées avec des<br />
résultats similaires. Cependant, une atteinte importante du calcar peut rendre nécessaire<br />
l’utilisation d’un implant modulaire de type PP avec a<strong>pp</strong>ui transversal trochantérodiaphysaire.<br />
Niveau II : Perte de substance osseuse avec métaphyse non continente mais<br />
diaphyse continente<br />
L’utilisation de tiges de révision non scellées à press-fit diaphysaire paraît être<br />
aujourd’hui la solution de choix. Si l’on souhaite reconstruire la métaphyse dans les cas peu<br />
détruits, une technique associant prothèse cimentée et allogreffes morcelées impactées peut<br />
être utilisée.<br />
Niveau III : Métaphyse et diaphyse incontinente<br />
Les tiges verrouillées sans ciment a<strong>pp</strong>ortent une sécurité immédiate, mais il existe un<br />
risque d’enfoncement à l’ablation des vis ou une rupture de celles-ci par excès de contraintes.<br />
10
On peut également rechercher un blocage fémoral diaphysaire distal autour d’une tige non<br />
scellée et non verrouillée. La reconstruction métaphysaire et diaphysaire est alors de bonne<br />
qualité et durable. Le risque d’enfoncement est important pour ce type d’implant.<br />
L’allogreffe massive structurelle avec scellement d’une longue tige type Kerboull fait<br />
partie des options possibles si l’on dispose d’une banque d’os 21 .<br />
F/ ANALYSE DE LA RECONSTRUCTION OSSEUSE<br />
Les modifications osseuses péri-prothétiques et donc la reconstruction osseuse peuvent<br />
être analysées selon deux moyens techniques distincts : la radiographie conventionnelle et la<br />
densitométrie biphotonique à rayons X.<br />
RADIOGRAPHIE CONVENTIONNELLE<br />
Des clichés radiographiques standards de face et de profil, de bonne qualité, permettent<br />
tout d’abord d’évaluer la stabilité mécanique de l’implant fémoral avec notamment la qualité<br />
de l’interface corticale-implant, la stabilité de l’implant dans le plan axial (enfoncement),<br />
frontal et sagittal (index de varisation).<br />
La reconstruction osseuse proprement dite est, elle, analysée grâce à la mesure des<br />
épaisseurs corticales et de l’index cortical. Les épaisseurs corticales sont mesurées sur le<br />
cliché de face (rotule au zénith) du post-opératoire immédiat et à la révision et ceci à trois<br />
niveaux : petit trochanter, 5cm et 10 cm en dessous de la collerette d’a<strong>pp</strong>ui de la tige fémorale<br />
sur un axe perpendiculaire à l’axe anatomique du fémur.<br />
L’index cortical de Hoffman peut être calculé selon la formule :<br />
IC = (Epaisseur corticale interne + Epaisseur corticale externe) X 100<br />
Largeur du canal médullaire<br />
Les zones de liseré et d’ostéolyse sont également déterminées selon les 7 zones<br />
périprothétiques de Gruen 56 .<br />
11
Zones de Gruen de face et de profil<br />
DENSITOMETRIE BIPHOTONIQUE A RAYONS X (DPX)<br />
Il s’agit d’une technique performante qui permet, in vivo de déterminer de façon précise<br />
la densité osseuse péri-prothétique. Elle a été jugée suffisamment précise et reproductible<br />
pour être utilisée dans des publications récentes afin d’évaluer la reconstruction osseuse 32,34 .<br />
Cette technique peut également être adaptée aux 7 zones de Gruen comme cela a été fait<br />
dans la série de reprises par prothèse de Puget de Nehme 52 .<br />
12
G/ TECHNIQUE CHIRURGICALE<br />
Le Système PP 60<br />
Il s’agit d’un implant initialement imaginé en 1981 pour le traitement chirurgical des<br />
fractures trochantériennes comminutives du sujet âgé. Il permettait grâce à son a<strong>pp</strong>ui<br />
diaphysaire transversal et son faible volume, la reconstruction du massif trochantérien autour<br />
de l’embase prothétique ainsi qu’un lever précoce diminuant la morbidité de ce type de<br />
pathologie.<br />
Il trouve alors progressivement une indication préférentielle dans les reprises<br />
d’arthroplastie totale de hanche associées à une perte de substance osseuse de l’extrémité<br />
supérieure du fémur. Le système PP permet une reprise de l’ostéogenèse et une restitution du<br />
capital osseux péri-prothétique.<br />
L’a<strong>pp</strong>ui diaphysaire de cet implant est un a<strong>pp</strong>ui cortical le plus proximal possible. Cet<br />
a<strong>pp</strong>ui est de niveau variable, ce qui explique le dévelo<strong>pp</strong>ement d’un système modulaire<br />
s’adaptant aux différentes situations rencontrées.<br />
Le matériel 60<br />
Le kit « PP » comprend une tige fémorale et une embase solidarisée par une vis d’union,<br />
dont l’a<strong>pp</strong>ui diaphysaire peut être augmenté par une rondelle. Chaque élément du kit est<br />
disponible dans des tailles variables et c’est en jouant sur les différentes associations possibles<br />
que l’on s’adapte aux différentes situations chirurgicales.<br />
13
En dehors des têtes prothétiques qui sont en chrome cobalt, l’ensemble des pièces est<br />
réalisé en alliage de Titane de faible densité, d’Aluminium et de Vanadium connu sous la<br />
désignation de TA 6V. Ce matériel permet une bonne biocompatibilité, une résistance élevée<br />
à la rupture avec un module d’élasticité situé entre ceux de l’acier ou du chrome cobalt et de<br />
l’os cortical.<br />
La tige diaphysaire est longue, de section quadrangulaire, décroissante de proximal en<br />
distal. Elle possède également une courbure à concavité postérieure correspondant à la<br />
morphologie anatomique du fémur. Ce dessin permet à la tige d’avoir un effet autobloquant<br />
dans deux plans. L’extrémité en sifflet diminue, quant à elle, les contraintes au niveau de la<br />
corticale.<br />
L’ostéo-intégration est assurée par un traitement de surface total avec trois rangées de<br />
rainurages et d’écailles orientées de façon à faciliter l’ablation éventuelle de la tige.<br />
La tige est surmontée d’une collerette d’a<strong>pp</strong>ui augmentant la stabilité primaire au niveau<br />
de l’ostéotomie transversale. Elle est percée à sa face supérieure de plusieurs orifices<br />
permettant de régler l’antéversion du col fémoral. L’antéversion physiologique est repérée par<br />
un marquage laser au niveau de la collerette et de l’embase.<br />
Cette tige est disponible en 3 longueurs (126/180/270) et initialement, en sept tailles (9 à<br />
21mm). La taille 9 a été ensuite retirée du catalogue.<br />
Si l’a<strong>pp</strong>ui osseux de la collerette s’avère insuffisant, des rondelles d’a<strong>pp</strong>ui de tailles<br />
différentes peuvent, en théorie, être ajoutées.<br />
L’embase possède à sa partie inférieure une cavité tronconique qui reçoit la tige<br />
fémorale avec laquelle elle est vissée. Un téton d’antéversion s’adapte aux orifices de la partie<br />
supérieure de la tige fémorale. L’embase est perforée de multiples orifices le long de ses<br />
bords médial et latéral permettant la réinsertion des éléments ostéo-musculaires de l’extrémité<br />
supérieure du fémur (le digastrique fessier-vaste externe en dehors, le psoas en dedans inséré<br />
sur le petit trochanter).<br />
Cette embase est disponible en tailles de longueur croissante de 20 à 160 mm.<br />
La tête prothétique réalisée en alliage de chrome cobalt s’adapte sur le cône morse du<br />
col de l’embase métaphysaire. Quatre diamètres de tête sont possibles (22/26/28/32) ainsi que<br />
4 longueurs de col (court, moyen, long et extra-long sur demande).<br />
Voie d’abord et technique chirurgicale 60<br />
Nous utilisons dans le service un abord postéro-latéral de l’articulation coxo-fémorale.<br />
14
Le patient est installé en décubitus latéral strict, la hanche à opérer étant en légère<br />
flexion et adduction. Le relief du grand trochanter est alors aisément palpé.<br />
L’incision cutanée selon Gibson est rectiligne, légèrement incurvée vers l’arrière et doit<br />
être centrée en proximo-distal et en antéro-postérieur sur le relief du grand trochanter. Dans la<br />
voie de Moore, la ligne de réflexion se situe deux doigts au-dessous du sommet du grand<br />
trochanter.<br />
On incise ensuite, après avoir franchi le tissu sous-cutané, la portion aponévrotique du<br />
Fascia-Lata. Le muscle Gluteus Maximus (Grand Fessier) est alors discisé dans le sens de ses<br />
fibres (Moore) ou désinséré de son insertion sur la bandelette de Maissiat (Gibson). Ensuite,<br />
après avoir placé un écarteur de type Charnley, on a le jour sur le digastrique Gluteus Medius-<br />
Grand Trochanter-Vastus Lateralis. Le positionnement de la jambe en rotation interne fait<br />
alors a<strong>pp</strong>araître en arrière un espace cellulo-graisseux au fond duquel chemine le nerf<br />
Sciatique. Cette rotation interne du membre inférieur met en tension les muscles pelvitrochantériens<br />
rotateurs externes qui se dirigent vers la fossette digitale et la ligne intertrochantérienne<br />
postérieure.<br />
On peut décider à ce temps de l’intervention de pratiquer une trochantérotomie en<br />
digastrique dérivée de la technique d’Osborne et modifiée par Bourgeon et Vidal 61 . On<br />
pratique longitudinalement et dans un plan frontal, d’arrière en avant, une première<br />
ostéotomie à la scie oscillante qui permet d’obtenir une baguette osseuse pédiculée par tous<br />
les rotateurs externes. Celle-ci est mobilisée et maintenue en arrière à l’aide d’un écarteur de<br />
type Homann. Elle emporte assez souvent le petit trochanter qui est fréquemment très fragilisé<br />
par les destructions osseuses de la région. En augmentant encore la rotation interne, après<br />
avoir ruginé le vaste externe sur le fémur sans le désinsérer de la crête trochantérienne, le<br />
grand trochanter est ostéotomisé dans un plan sagittal. Cette deuxième ostéotomie est<br />
perpendiculaire à la première.<br />
15
Ainsi, on libère un ensemble digastrique composé du Gluteus-Medius-Grand trochantervastus<br />
Lateralis qui peut être mobilisé et maintenu par un deuxième Homann. On obtient alors<br />
un bon jour sur la partie supérieure de la prothèse qui peut être nettoyée des débris habituels.<br />
On peut élargir l’abord en sectionnant l’insertion fémorale du grand fessier sur la ligne âpre,<br />
tout en laissant environ 1 cm pour la réinsertion en fin d’intervention. L’abord est ainsi<br />
facilité pour pratiquer l’ablation de la prothèse et du ciment ce qui diminue le risque de fausse<br />
route. Les deux fragments ostéotomisés qui sont restés pédiculés (grand trochanter et baguette<br />
des rotateurs externes) seront le point de départ de la reconstruction osseuse.<br />
Le dernier temps de l’abord consiste, après l’ablation de la prothèse primitive, en la<br />
recoupe de la diaphyse fémorale dans la zone qui a<strong>pp</strong>araîtra suffisamment solide pour<br />
recevoir la collerette de la prothèse.<br />
Cet abord peut être susceptible de variations. La trochantérotomie n’est pas toujours<br />
nécessaire en cas d’extraction aisée de l’implant fémoral <strong>desc</strong>ellé. A l’inverse, la<br />
trochantérotomie peut évoluer vers une ostéotomie plus étendue ou être associée à une<br />
fémorotomie en fonction des difficultés opératoires rencontrées.<br />
III NOTRE ETUDE<br />
A/ MATERIEL ET METHODE<br />
Présentation de la série<br />
Nous avons revu 31 patients ayant bénéficié d’une reprise de prothèse totale de hanche<br />
entre 1990 et 1997 et dont le recul était d’au minimum 12 ans. Il s’agissait de patients opérés<br />
pour des <strong>desc</strong>ellements aseptiques d’arthroplastie totale de hanche utilisant le système PP.<br />
Méthodologie statistique<br />
Le recueil des données a été effectué sur le logiciel Microsoft Excel®. L’analyse<br />
statistique a été réalisée sur Microsoft Excel® et sur le logiciel de statistique SPSS®.<br />
1 / Epidémiologie de la série<br />
Il existait une nette prédominance féminine avec 22 femmes (71%) et 9 hommes (30%).<br />
On retrouve quasiment autant de côtés droits (15) que de cotés gauches (16).<br />
Le poids moyen était de 71 kg, la taille moyenne de 164 cm, et l’index de masse<br />
corporel moyen de 26,75 (18-40) :<br />
16
- Il existait une surcharge pondérale (24
3 / Arthroplastie initiale<br />
Il s’agissait dans la majorité des cas d’implants fémoraux cimentés de type Muller ou<br />
Charnley (80%).<br />
4 / Type de <strong>desc</strong>ellement<br />
Ce <strong>desc</strong>ellement était bipolaire dans 23 cas (74%) et uni-polaire dans 8 cas (26%).<br />
Il s’agissait dans tous les cas d’un <strong>desc</strong>ellement aseptique confirmé par la négativité des<br />
prélèvements réalisés systématiquement en per-opératoire.<br />
Selon la classification de Vives (SOFCOT 88), l’atteinte fémorale était répartie de la<br />
façon suivante :<br />
Pour le fémur<br />
Stade 1 : 9 cas (29%)<br />
Stade 2 : 15 cas (48%)<br />
Stade 3 : 7 cas (23%)<br />
Pour le trochanter<br />
Stade 1 : 18 cas (57%)<br />
Stade 2 : 1 cas (3%)<br />
Grand trochanter non altéré : 12 cas (39%)<br />
18
5 / Intervention et technique chirurgicale<br />
Les interventions ont été effectuées dans le même centre, par 3 opérateurs différents.<br />
L’intervention consistait donc en un changement en un temps d’une prothèse totale de hanche<br />
<strong>desc</strong>ellée par un implant de reprise de type PP. Cet implant est caractérisé par la modularité<br />
des différents composants (tige et embase essentiellement). La tige est non cimentée, à<br />
traitement de surface total, possédant un a<strong>pp</strong>ui diaphysaire proximal.<br />
L’âge moyen lors de l’intervention était de 57 ans les extrêmes allant de 38 ans à 73 ans.<br />
L’évaluation de l’état général retrouvait un score de l’American Society of<br />
Anesthesiology (ASA) égal à 2 en moyenne.<br />
Les interventions ont été réalisées dans la majorité des cas sous anesthésie générale<br />
La durée opératoire était en moyenne de 166 minutes.<br />
Voie d’abord<br />
La voie d’abord était dans la totalité des interventions un abord postéro-latéral.<br />
L’incision cutanée était variable : elle était soit rectiligne selon Gibson, soit incurvée vers<br />
l’arrière selon Moore.<br />
Une trochantérotomie en digastrique selon la technique précédemment décrite a été<br />
réalisée dans 24 cas (77%).<br />
La fémorotomie selon la technique de Wagner a, quant à elle, été nécessaire dans 6 cas<br />
(23%) afin de réaliser soit l’extraction de l’implant fémoral, soit l’ablation du bouchon de<br />
ciment.<br />
Ces différents artifices ont imposé l’utilisation de cerclages de fil d’acier<br />
(trochantérotomie et fémorotomie) ou de cerclages de type Partridge® (fémorotomie).<br />
Au total, chez 5 patients, ni la trochanterotomie ni la fémorotomie n’ont été nécessaires.<br />
Réimplantation du cotyle<br />
Le changement de prothèse a été bipolaire dans 23 cas (74%).<br />
Une greffe osseuse de type allogreffe cortico-spongieuse, autogreffe cortico-spongieuse<br />
ou spongieuse à été nécessaire au niveau du cotyle dans 10 cas (33%), afin de combler la<br />
perte du capital osseux péri-cotyloidien.<br />
L’utilisation d’un anneau de soutient (Kerboul, Ganz ou Muller), afin de compléter la<br />
greffe osseuse et de faciliter le recentrage, a été nécessaire dans 15 cas (48%). Un cotyle<br />
standard était alors scellé dans cet anneau de soutient.<br />
19
Réimplantation au niveau du fémur<br />
La tige<br />
Dans toutes les interventions, nous avons impacté la tige à frottement dur, de façon à<br />
obtenir une bonne stabilité primaire.<br />
La longueur des implants fémoraux la plus utilisée était 180 mm. L’implant « long »<br />
mesurant 270mm a été utilisé 3 fois, et la tige de 126 mm n’a été quant à elle implantée que 2<br />
fois. Celle-ci est actuellement retirée du catalogue.<br />
On peut noter que 24 tiges soit 76% des implants étaient des tailles 15,17 et 19.<br />
La rondelle permettant d’optimiser l’assise horizontale a été utilisée à 4 reprises .<br />
Le concepteur conseille aujourd’hui de ne pas utiliser cette rondelle. La stabilité<br />
primaire de la tige doit provenir de calage diaphysaire proximal. La présence de cette rondelle<br />
peut entraîner une fausse impression de stabilité primaire et aboutir à un <strong>desc</strong>ellement précoce<br />
de l’implant fémoral.<br />
L’embase<br />
Les tailles d’embase les plus utilisées étaient les embases 20, 30 et 40.<br />
L’embase 50 a été utilisée 4 fois, l’embase 70 à 2 reprises.<br />
Chez les 5 patients n’ayant pas nécessité de trochantérotomie ni de fémorotomie, les<br />
embases utilisées étaient des tailles 20 et 30.<br />
Taille du col et de la tête fémorale<br />
Le col moyen a été utilisé 20 fois et le col long 9 fois. Le col extra-long et le col court<br />
ont été utilisés chacun une fois.<br />
La tête fémorale 32 mm a été implantée 9 fois, la tête 28 mm 22 fois.<br />
Il n’existait pas de différence significative en terme de luxation, <strong>desc</strong>ellement<br />
cotyloïdien ou de l’implant fémoral entre le groupe utilisant une tête 32 mm par ra<strong>pp</strong>ort à<br />
celui avec des têtes 28 mm.<br />
6 / Complications per-opératoires<br />
La complication per-opératoire la plus fréquente a été la fracture diaphysaire du fémur<br />
lors du passage des râpes d’essai ou de l’implantation de la tige définitive. Elle est survenue à<br />
4 reprises dans notre série soit 13%. Elles ont nécessité dans 2 cas un cerclage immédiat du<br />
fémur à l’aide de fil d’acier ou de cerclages de type Partridge®. Il s’agissait dans les 2 autre<br />
cas de traits de fracture non déplacés, découverts sur la radiographie post-opératoire. L’a<strong>pp</strong>ui<br />
a été différé avec mise en décharge pendant 4 à 6 semaines.<br />
Nous avons également relevé 2 fractures du petit trochanter.<br />
20
Lors de l’ablation du bouchon de ciment, du passage des râpes d’essai ou de<br />
l’implantation de la tige définitive, le risque de « fausse route » est également important. Un<br />
contrôle radiographique per-opératoire était donc réalisé au moindre doute. Il a permis de<br />
diagnostiquer 1 cas de fausse route (3%) dans cette série.<br />
Pour ce patient, il n’avait pas été réalisé de trochantérotomie.<br />
Au total, dans cette série, nous avons rencontré 6 complications per-opératoires de type<br />
fracture ce qui représente 19 % des interventions.<br />
La présence d’une fracture per-opératoire ne modifie pas statistiquement les résultats<br />
fonctionnels au recul, que ce soit les scores totaux PMA et HHS ainsi que les sous-scores de<br />
douleur.<br />
7 / Suites opératoires immédiates<br />
Luxations post-opératoires précoces<br />
Nous avons observé 2 cas de luxations post-opératoires précoces, c’est-à-dire dans des<br />
délais allant de 2 semaines à 2 mois post-opératoires. Ces épisodes de luxation n’ont pas<br />
récidivé et n’ont pas nécessité de reprise chirurgicale.<br />
Le nombre de prothèses ayant précédé la reprise étudiée est lui statistiquement lié à la<br />
survenue d’épisodes de luxations post-opératoires (p=0,004).<br />
Complications infectieuses précoces<br />
Il n’y a pas eu d’infection post-opératoire précoce dans notre série.<br />
Durée d’hospitalisation et sortie<br />
La durée d’hospitalisation dans le service était en moyenne de 18 jours (9-31).<br />
Les patients ont été transférés en centre de rééducation et en établissement de moyen<br />
séjour.<br />
8 / Révision<br />
Tous les patients de la série ont été revus en consultation pour ce travail avec un<br />
interrogatoire et un examen clinique. Cela nous a permis de calculer pour chacun :<br />
21
- le score fonctionnel Harris Hip Score 25 (HHS) fondé sur l’évaluation de la<br />
douleur, la fonction, les mobilités de hanche ainsi que les attitudes vicieuses. Il est coté sur un<br />
total de 100 points.<br />
- Inférieur à 70 : mauvais<br />
- Entre 70 et 79 : correct<br />
- Entre 80 et 90 : bon<br />
- Entre 90 et 100 : excellent<br />
- le score fonctionnel de Postel et Merle d’Aubigné 44 (PMA) qui évalue la douleur,<br />
la mobilité de la hanche avec ou sans attitude vicieuse et la marche (cotation sur 18).<br />
- un indice subjectif de satisfaction allant de 1 (insatisfait) à 5 (très satisfait).<br />
La présence d’une douleur située au niveau de la cuisse a également été notée. L’étude<br />
de la station debout et de la marche a permis de déceler une boiterie de type Trendelenburg.<br />
Un bilan radiographique complet a été réalisé comprenant :<br />
- un cliché de bassin de face en charge<br />
- les radiographies de hanche face et profil incluant la totalité de la prothèse<br />
- un cliché pangonométrique réalisé en charge<br />
9 / Analyse radiologique<br />
Pré-opératoire<br />
Détermination sur la radiographie pré-opératoire du stade de <strong>desc</strong>ellement de l’implant<br />
fémoral selon les classifications de la SOFCOT 88 modifiée<br />
Post-opératoire immédiat<br />
- Mesure de la distance entre le sommet du grand trochanter et la pointe de la tige<br />
fémorale.<br />
22
- Détermination de la position de la tige par ra<strong>pp</strong>ort à l’axe fémoral dans le plan frontal,<br />
sur le cliché de face (Normale, Varus ou Valgus supérieur à 5°).<br />
- Mesure des épaisseurs corticales interne et externe ainsi que de la largeur du canal<br />
médullaire à différents niveaux :<br />
- petit trochanter<br />
- 5 cm sous le petit trochanter<br />
- 10 cm sous le petit trochanter<br />
- Mesure de la tête fémorale afin d’établir un facteur de correction pour pouvoir calculer<br />
les valeurs réelles d’épaisseur corticale et de distance entre grand trochanter et pointe de la<br />
tige.<br />
- Calcul de l’index cortical selon Hoffman 28 pour chaque niveau (petit trochanter, 5 cm<br />
et 10 cm sous le petit trochanter).<br />
Nous n’avons pas calculé le taux de remplissage à 10 cm en dessous du petit trochanter<br />
en raison de l’impossibilité de mesurer de façon fiable la largeur de l’extrémité distale de la<br />
tige PP. Le dessin quadrangulaire, l’affinement distal de la tige associés à des incidences<br />
radiographiques variables rendaient difficile cette mesure.<br />
Bilan radiographique à la révision<br />
- Mesure de la distance entre le sommet du grand trochanter et la pointe de la tige<br />
fémorale.<br />
- Détermination de la position de la tige par ra<strong>pp</strong>ort à l’axe fémoral dans le plan frontal,<br />
sur le cliché de face (Normale, Varus ou Valgus supérieur à 5°).<br />
- Détermination de la consolidation ou non, des éventuels artifices comme les<br />
fémorotomies ou trochantérotomies.<br />
- Mesure des épaisseurs corticales interne et externe ainsi que de la largeur du canal<br />
médullaire à différents niveaux :<br />
- petit trochanter<br />
- 5 cm sous le petit trochanter<br />
- 10 cm sous le petit trochanter<br />
- Mesure de la tête fémorale afin d’établir un facteur de correction pour pouvoir calculer<br />
les valeurs réelles d’épaisseur cortical et de distance entre grand trochanter et la pointe de la<br />
tige.<br />
- Calcul de l’index cortical de Hoffman et du taux de remplissage du canal fémoral.<br />
23
B/ RESULTATS<br />
Le recul moyen dans cette série était de 163 mois soit 13 ans et 7 mois.<br />
L’âge moyen au recul était de 71ans, les extrêmes allant de 57 à 86 ans.<br />
1 / Reprises chirurgicales<br />
Au recul, il y a eu au total 15 reprises chirurgicales (45%):<br />
- 6 reprises n’intéressant que le cotyle en raison d’un <strong>desc</strong>ellement associé ou non à<br />
une usure excessive du polyéthylène. Quatre cas correspondaient initialement à des<br />
changements unipolaires intéressant uniquement l’implant fémoral.<br />
- 3 reprises bipolaires pour un nouveau <strong>desc</strong>ellement bipolaire aseptique des implants<br />
fémoraux et cotyloïdiens.<br />
- 1 reprise isolée d’une tige fémorale pour une fracture et un <strong>desc</strong>ellement associé de<br />
l’implant fémoral.<br />
- 1 réintervention pour changement de taille d’embase et de longueur de col pour des<br />
épisodes de luxation tardive.<br />
- 2 réintervention afin de traiter une pseudarthrose du grand trochanter symptomatique,<br />
par une décortication et de nouveaux cerclages.<br />
- 1 lavage chirurgical pour un sepsis tardif.<br />
- 1 changement de prothèse en deux temps pour un sepsis avéré.<br />
Complications infectieuses tardives<br />
Nous avons dénombré 2 sepsis sur prothèse (6%) pour lesquels un changement de<br />
prothèse en 2 temps a été réalisé dans 1 cas. Il était effectué dans un premier temps la dépose<br />
de la prothèse puis la mise en place d’une Spacer en ciment et d’une antibiothérapie adaptée<br />
pendant au moins 3 mois et enfin une réimplantation d’une nouvelle prothèse. Dans 1 cas, le<br />
traitement retenu a été un lavage chirurgical soigneux de la prothèse et une antibiothérapie<br />
adaptée et prolongée.<br />
Luxation tardive<br />
Nous avons observé 1 cas luxations tardives dans cette série. Dans ce cas, il s’agissait<br />
d’une authentique instabilité prothétique à distance de l’intervention et elle a bénéficié d’une<br />
réintervention.<br />
24
Survie de l’implant fémoral<br />
Bien qu’il y ait eu 15 reprises chirurgicales, il n’y a eu que 5 reprises de l’implant<br />
fémoral. Il s’agissait dans 1 cas d’un changement en 2 temps pour une complication septique.<br />
Dans 3 cas, il s’agissait d’un nouveau <strong>desc</strong>ellement bipolaire aseptique. Dans 1 cas, la tige<br />
fémorale était fracturée et <strong>desc</strong>ellée nécessitant le changement de l’implant fémoral<br />
uniquement.<br />
Fracture de l’implant<br />
Nous avons constaté un cas de fracture de l’implant fémoral. La fracture de l’implant<br />
s’était produite à la jonction entre la tige proprement dite et la collerette d’a<strong>pp</strong>ui. Il s’agissait<br />
d’une tige de petit diamètre (taille 9). Cette taille qui a été retirée du catalogue par la suite.<br />
Récidive du <strong>desc</strong>ellement<br />
Un nouveau <strong>desc</strong>ellement non septique de la prothèse totale de hanche s’est produit à 10<br />
reprises. Il était bipolaire dans 3 cas, unipolaire intéressant uniquement le cotyle dans 6 cas.<br />
Autres complications<br />
Nous signalons dans 1 cas, un dévissage de la vis unissant l’embase et la tige. Celle-ci<br />
était dévissée et complètement désadaptée de l’embase. Il n’existait néanmoins pas de<br />
démontage de l’implant fémoral. Cette complication radiologique était néanmoins sans<br />
répercussion clinique.<br />
2 / Résultats cliniques<br />
Scores fonctionnels<br />
* HHS (Harris Hip Score)<br />
Au recul, le score de Harris moyen était de 72 points. Les valeurs minimales et<br />
maximales étaient respectivement de 34 et 91 points. Le score maximal possible étant de 100<br />
points.<br />
Le Score total de Harris était supérieur ou égal à 70 (résultat correct) dans 24 cas soit<br />
77% de la série<br />
25
* PMA (Score de Postel et Merle d’Aubigné)<br />
Le score fonctionnel PMA évaluant la douleur, la mobilité de la hanche avec ou sans<br />
attitude vicieuse et la qualité de la marche, était en moyenne 13 points (8-17)<br />
Indice de Satisfaction<br />
Cet indice subjectif est coté de 1 à 5 selon la satisfaction ressentie par le patient<br />
(insatisfait, pas très satisfait, moyennement satisfait, satisfait, très satisfait).<br />
L’indice moyen de satisfaction dans la série était de 4 (satisfait).<br />
Le nombre de patients dont l’indice était supérieur à 3, c'est-à-dire satisfait ou très<br />
satisfait était de 25 soit 80 % des patients.<br />
1 patients était coté 2 (peu satisfait).<br />
Douleurs de cuisse<br />
Lors de la révision, nous avons retrouvé 9 douleurs localisées à la cuisse (29%).<br />
Dans 1 cas, la tige implantée était une tige longue mesurant 270 mm. Les autres cas<br />
correspondaient à des implants fémoraux de longueur standard (180mm) et à une tige de<br />
longueur 126mm.<br />
Dans 3 cas, l’implant fémoral était varisé de plus de 5 degrés par ra<strong>pp</strong>ort à l’axe du<br />
fémur sur la radiographie de face lors de la révision.<br />
Boiterie<br />
L’insuffisance du moyen fessier à l’origine de la boiterie de Trendelenburg a été évaluée<br />
en consultation lors de la marche et de la position debout en a<strong>pp</strong>ui monopodal.<br />
Chez les patients déambulants, nous avons retrouvé 17 cas soit 55% d’insuffisance du<br />
moyen fessier entraînant une boiterie de Trendelenburg.<br />
3 / Résultats radiologiques<br />
Positionnement de l’implant fémoral<br />
Le positionnement de l’implant fémoral dans le plan frontal par ra<strong>pp</strong>ort à l’axe du fémur<br />
a été analysé sur les clichés post-opératoires immédiats et à la révision.<br />
Nous avons retrouvé en post-opératoire immédiat, 4 cas de tiges fémorales varisées de<br />
plus de 5 degrés (10%).<br />
26
A la révision, 3 tiges étaient varisées et 1 tige valgisée.<br />
La tige valgisée correspondait au changement d’une tige initialement varisée ayant<br />
entraîné une fausse route.<br />
Migration et enfoncement de la tige<br />
La migration de l’implant fémoral et notamment son enfoncement dans le fut<br />
diaphysaire a été évaluée par la mesure de la distance entre le sommet du grand trochanter et<br />
la pointe de la tige.<br />
Nous avons exclu de cette mesure, les cas où la tige a été reprise et les cas présentant<br />
une pseudarthrose associée à une migration du grand trochanter.<br />
L’enfoncement moyen de la tige était en moyenne de 5 mm (0-16mm).<br />
Chez 3 patients (9%), l’enfoncement était supérieur à 7 mm.<br />
Consolidation trochantérienne<br />
Nous ra<strong>pp</strong>elons que la trochantérotomie en digastrique a été réalisée à 24 reprises<br />
(77%).<br />
Sur ces 24 trochantérotomies, 16 ont consolidé.<br />
Dans 4 cas, l’évolution s’est faite vers une non continuité osseuse du grand trochanter<br />
(13% de la série) mais avec une continuité fonctionnelle.<br />
4 patients présentaient une véritable pseudarthrose avec ascension du grand trochanter.<br />
Deux patients ont bénéficié d’une reprise chirurgicale (décortication et nouveaux<br />
cerclages).<br />
Dans ce groupe de patients, le score HHS moyen (66,08) était inférieur au score HHS de<br />
la série (71 points).<br />
Chez un patient, il existait une lyse quasi-complète du grand trochanter. Il s’agissait<br />
d’un patient étant à 1 an d’une reprise en 2 temps pour sepsis sur prothèse.<br />
Epaisseur corticale et reconstruction osseuse<br />
Les épaisseurs corticales et les index corticaux ont été mesurés et calculés en postopératoire<br />
immédiat et à la révision à 3 niveaux différents (petit trochanter, 5 cm et 10 cm).<br />
27
Post-opératoire immédiat<br />
* Petit trochanter<br />
Les épaisseurs moyennes des corticales interne et externe étaient respectivement<br />
de 4 mm (0,85-11,38, DS=2,65) et 4,3mm (0-12, DS=2,9).<br />
La largeur du canal médullaire était en moyenne de 29,8mm(12,5-50, DS=9,1).<br />
L’index cortical de Hoffman au petit trochanter en post-opératoire immédiat a été<br />
calculé à 33,6 (4,7-119, DS=25,7).<br />
* à 5 cm en dessous du petit trochanter<br />
La corticale interne mesurait en moyenne de 5,4mm (0,9-12,8 et DS=2,4).<br />
La corticale externe mesurait en moyenne 5,5mm (0,82-10,26, DS= 1,91).<br />
La largeur du fût diaphysaire était de 17,3mm (9,8-24,3 et DS=4).<br />
L’index cortical a été calculé à 63,4(15-157 et DS=29,8).<br />
* à 10 cm en dessous du petit trochanter<br />
Les mesures moyennes étaient pour la corticale interne de 5,8mm (0,9-15,1 et<br />
DS=2,6) et pour la corticale externe de 5,5mm (0-9,9 et DS=2,2).<br />
La largeur du canal fémoral était de 14,6mm (8,8-22,8, DS=3).<br />
L’index cortical était calculé à 83,2 (17-182, DS=37,9).<br />
Révision<br />
*petit trochanter<br />
Les mesures réalisées sur les clichés à la révision étaient :<br />
- Corticale interne : 5,8mm (0-12,7 et DS=3,4).<br />
- Corticale externe : 5,4mm (0-13,1 et DS=3,2).<br />
- Largeur du canal médullaire : 27,8mm (13,9-47,7 et DS=8,2)<br />
- Index Cortical : 46,3 (0-130 et DS=30,7)<br />
* à 5 cm au-dessous du petit trochanter<br />
- Corticale interne : 6mm (0,9-10,7 et DS=2,1).<br />
- Corticale externe : 6,5mm (1,6-14,4 et DS=2,8).<br />
- Largeur du canal médullaire : 17mm (8,5-24,6 et DS=3,8).<br />
28
- Index Cortical : 76,2 (20-200, DS=36,9).<br />
* à 10 cm au-dessous du petit trochanter<br />
- Corticale interne : 6,2mm (0,8-12,2 et DS=2,35).<br />
- Corticale externe : 6mm (1,4-11,9 et DS=2,4).<br />
- Largeur du canal médullaire : 15,6mm (5,9-25,2 et DS=4,2).<br />
- Index Cortical : 87,4 (12,5-243 et DS=43,3).<br />
Comparaison post-opératoire immédiat et à la révision<br />
* petit trochanter<br />
- L’épaisseur de la corticale interne est passée de 4 mm à 5,8mm. Ce gain<br />
d’épaisseur de 1,8 mm est statistiquement significatif avec t=3,2 et p=0,002<br />
- L’épaisseur de la corticale externe est passée de 4,3mm à 5,4mm soit un gain de 1,1<br />
mm. Cette différence est significative avec t=2,536 et p=0,014<br />
- La largeur du canal médullaire est passée de 29,8mm à 27,8 mm. La variation est<br />
significative, t=2,225 et p=0,031<br />
- L’Index Cortical est passé de 33,6 à 46,3 ce qui représente une augmentation de<br />
12,7 points. Cette différence est très significative, t=3,203 et p=0,002.<br />
* à 5cm en dessous du petit trochanter<br />
- L’épaisseur moyenne de la corticale interne est passée de 5,4mm à 6 mm. Elle a<br />
donc augmenté de 0,54 mm et cette différence est significative avec t=2,357 et p=0,022<br />
- L’épaisseur moyenne de la corticale externe est passée de 5,5mm à 6,5mm soit un<br />
gain de 10 mm. La variation est significative, t=2,66 et p=0,01<br />
- La largeur moyenne du canal médullaire est passée de 17,3mm à 17 mm. Ici la<br />
variation n’est pas significative, t=0,299 et p=0,766<br />
- L’Index Cortical est passé de 63,4 à 76,2 soit une augmentation de 11,8 points. La<br />
différence est significative avec t=2,436 et p=0,018.<br />
* à 10cm en dessous du petit trochanter<br />
- L’épaisseur moyenne de la corticale interne est passée de 5,8mm à 6,2mm. La<br />
différence est non significative avec t=1,213 et p=0,231<br />
29
- L’épaisseur moyenne de la corticale externe est passée de 5,5mm à 6mm. Cette<br />
variation de 0,58 mm est ici juste significative, t=2,007 et p=0,05<br />
- La largeur moyenne du canal médullaire est passée de 14,6mm à 15,6mm. La<br />
différence est statistiquement significative, t=2,379 et p=0,021.<br />
- L’Index Cortical est passé de 83,2 à 87,4 soit un gain de 2,58 points. La différence<br />
est par contre non significative avec t=0,473 et p=0,638.<br />
Il existe donc dans notre série, une augmentation statistiquement significative de<br />
l’épaisseur des corticales interne et externe au niveau du petit trochanter et à 5 cm en<br />
dessous du petit trochanter. Ce résultat est confirmé par l’augmentation significative de<br />
l’index cortical de Hoffman à ces 2 niveaux.<br />
Au niveau 10 cm sous le petit trochanter, les résultats ne sont pas homogènes.<br />
L’augmentation d’épaisseur de la corticale externe est juste significative alors que les<br />
variations d’épaisseur de la corticale interne de d’index cortical ne sont pas<br />
statistiquement significatives.<br />
Il existait une augmentation significative de gain d’épaisseur de la corticale<br />
interne au niveau du petit trochanter entre le groupe ayant un stade « fémur » 1 et le<br />
groupe présentant un stade « fémur » 2 ou 3 de la classification SOFCOT (p=0 ,012).<br />
Ce n’était pas le cas pour les autres mesures d’épaisseur corticale.<br />
Gain d’épaisseur et d’index cortical<br />
Moyenne Ecart-type<br />
Corticale médiale-petit trochanter 1,8 mm 3,38<br />
Corticale latérale-petit trochanter 1,1 mm 3,00<br />
Corticale médiale-5cm 0,54 mm 1,67<br />
Corticale latérale-5cm 0,99 mm 2,7<br />
Corticale médiale-10cm 0,35 mm 2,13<br />
Corticale latérale-10cm 0,58 mm 2,08<br />
Index de Hoffman- petit trochanter 12,7 26,7<br />
Index de Hoffman-5cm 11,79 34,56<br />
Index de Hoffman-10cm 2,58 39,11<br />
30
D/ DISCUSSION<br />
Méthodologie<br />
Il s’agissait ici d’une étude rétrospective sur dossiers, elle est donc soumise à certaines<br />
critiques méthodologiques.<br />
Il existe ainsi un biais de recrutement en raison de la multiplicité des étiologies, de<br />
stades de <strong>desc</strong>ellement variable ou encore du nombre d’interventions antérieures. En effet,<br />
Kavanagh a montré que la qualité du résultat final était dépendante du nombre d’interventions<br />
ayant précédé la reprise chirurgicale étudiée 31 .<br />
Ce travail correspond à une série multi-opérateur mais mono-centrique, ce qui peut<br />
influencer la qualité du résultat. Cela représente un biais de performance.<br />
Le biais de susceptibilité est lui bien contrôlé par la mise en place d’un implant unique<br />
chez tous les patients de la série.<br />
La taille de l’échantillon étudiée est supérieure à 30 permettant l’adoption de<br />
l’hypothèse d’une distribution normale et donc d’utiliser les tests statistiques classiques.<br />
L’examinateur ayant recueilli les données était différent des opérateurs et n’était ni<br />
promoteur ni concepteur de matériel implanté. Ceci doit en principe augmenter l’objectivité<br />
de l’étude.<br />
Nous avons décidé de comparer ce travail à différentes séries récentes de reprises<br />
d’arthroplastie de hanche utilisant des techniques différentes, mais dans lesquelles il existait<br />
une homogénéité des implants :<br />
-Les reprises cimentées (Katz 30 ) utilisant les dernières techniques de cimentage.<br />
-Les reprises cimentées associées à une greffe osseuse impactée (Gie 20 ) selon la<br />
technique d’Exeter.<br />
-Les reprises cimentées avec greffe osseuse selon la technique d’Exeter modifiée<br />
(Migaud 46 ) avec mise en place d’un treillis métallique endofémoral.<br />
-Les reprises non cimentées avec tiges verrouillées comme la tige Ultime® (May 41 )<br />
-Les reprises non cimentées utilisant différents implants<br />
*Wagner® (Boisgard 4 / implant fémoral non scellé à ancrage distal)<br />
*S-Rom® (Chandler 6 , McCarthy 42 / implant modulaire non cimenté)<br />
*PP® (Essig 18 / Tige modulaire à traitement de surface total)<br />
*JRI® (Raman 62 / implant à revêtement d’hydroxyapatite proximal)<br />
*PFMR® (Le Béguec 35 / implant modulaire et concept Press-fit)<br />
31
Age<br />
L’âge moyen lors de la révision était dans notre série de 57 ans. Dans les différentes<br />
séries que nous avons citées, l’age moyen était le plus souvent supérieur ou égal à 60 ans.<br />
Seule la série de Migaud 46 présentait un age moyen au recul de moins de 60 ans (58 ans).<br />
On peut expliquer cet age précoce dans notre série par le fait que dans 55% des cas,<br />
l’étiologie initiale ayant motive la mise en place de la première arthroplastie totale de hanche<br />
était une maladie luxante de la hanche. Il s’agissait donc de jeunes patients.<br />
Année Technique et Implants Effectif Recul Age moyen<br />
Katz 1997 Tige Cimentée 83 11,9 ans 64 ans<br />
Gie 1993 Allogreffe impactée et tige Cimentée 68 2,5 ans 68,8 ans<br />
Migaud 1997<br />
Allogreffe morcelée, impactée et tige<br />
Cimentée avec treillis<br />
19 6,9 ans 58 ans<br />
May 2006 Tige Verrouillée (Ultime®) 101 6 ans 72,3 ans<br />
Boisgard 2001 Tige non Cimentée (Wagner®) 52 3,6 ans 70 ans<br />
Chandler 1995 Non Cimentée, modulaire (S-Rom®) 52 3 ans 60 ans<br />
McCarthy 2007 Non Cimentée, modulaire (S-Rom®) 67 14 ans -<br />
Essig 1993 Non Cimentée, modulaire (PP®) 42 4 ans 65 ans<br />
Le Béguec 2002 Non cimentée, modulaire (PFM-R®) 152 3 ans 75 ans<br />
Raman 2005 Non cimentée (JRI®) 86 8 ans 71 ans<br />
Notre Série 2009 Non Cimentée, modulaire (PP®) 31 13ans 57 ans<br />
Recul<br />
D’un point de vue clinique, un recul moyen de 2 ans est un minimum à la fois nécessaire<br />
et suffisant pour a<strong>pp</strong>récier un résultat dans sa forme définitive. En effet, l’état clinique d’un<br />
patient n’évolue guère après un an (en l’absence de complications) et tout au plus, on peut<br />
noter une légère diminution de la boiterie ou une amélioration de quelques degrés de la<br />
flexion, si le patient n’est pas handicapé par sa hanche controlatérale. En ce qui concerne les<br />
douleurs, celles-ci sont en règle générale absentes après un an d’évolution. Si elles persistent<br />
après ce délai, il faut rechercher un <strong>desc</strong>ellement de la tige ou du cotyle. Si ce n’est pas le cas,<br />
on peut alors évoquer des fémoralgies liées à la mise en place d’un implant sans ciment.<br />
32
Sur le plan radiologique, un recul moyen de 2 ans est nécessaire pour a<strong>pp</strong>récier les<br />
premiers résultats, en sachant que, s’il est possible dans cet intervalle, d’évaluer la<br />
reconstruction du stock osseux et la qualité de l’ostéo-intégration, il faut un recul plus<br />
important pour évaluer le remodelage osseux adaptatif et les autres complications inhérentes à<br />
toute arthroplastie (usure, etc).<br />
Migaud 46 et Boisgard 4 n’ont pas retrouvé de modifications radiologiques au delà de 18<br />
mois après l’intervention. Boisgard 4 a également signalé la stabilité des signes cliniques<br />
comme la boiterie ou la douleur après 12 mois d’évolution.<br />
Le recul moyen dans notre série était de 13 ans et 7 mois avec un recul minimal de 12<br />
ans et un maximum de 19 ans. Ce recul est donc suffisant pour évaluer les résultats à moyen<br />
et surtout à long terme de cette technique chirurgicale tant sur le plan clinique que<br />
radiologique. Dans les séries auxquelles nous avons décidé de comparer notre travail, le recul<br />
varie en moyenne de 2,5 ans à 14 ans pour la série de McCarthy 42 .<br />
Étiologie primitive<br />
Il existait dans notre série un taux important de pathologie dysplasique de hanche<br />
(55%), ce qui n’est pas le cas des autres séries étudiées ou l’étiologie arthrosique prédominait.<br />
La mise en place d’une prothèse totale de hanche sur dysplasie semble techniquement plus<br />
délicate avec des difficultés spécifiques. La reprise de prothèse sur ce terrain paraît<br />
naturellement plus difficile avec un retentissement probable sur le résultat fonctionnel final.<br />
Type de <strong>desc</strong>ellement<br />
L’interprétation des clichés radiographiques pré-opératoires était soumise aux<br />
variabilités inter-individuelles des classifications a<strong>pp</strong>liquées. Dans le symposium de la<br />
SoFCOT 1999, Migaud et al 45 a souligné qu’aucune classification n’était reproductible,<br />
néanmoins, les plus reproductibles étaient celles décrites par Vivès pour le symposium de la<br />
SoFCOT 1988 et la classification AAOS au moins pour les 10 cm au dessous du petit<br />
trochanter.<br />
Nous avons donc utilisé la classifications de Vivès modifiée SoFCOT dans cette étude.<br />
Dans notre série, 29% des défects osseux étaient de stade 1, 48 % étaient cotés stade 2 et<br />
23 % stade 3 selon la classification de la SoFCOT et 60% des patients présentaient une<br />
atteinte trochantérienne.<br />
Ce sont les séries de Katz (80% de stade A de Harris), Essig (52% de stade SOFCOT I<br />
et IIa) et Le Béguec (43% des stade Sofcot I) qui se ra<strong>pp</strong>rochent le plus de notre travail en<br />
33
terme d’évaluation préopératoire des dégâts osseux. Les séries d’Essig 18 et de Le Béguec 35 ont<br />
en plus l’avantage d’utiliser la classification de la SOFCOT.<br />
Dans les autres études, les altérations osseuses sont plus évoluées et la comparaison des<br />
résultats cliniques et radiologiques est donc plus délicate.<br />
Il faut préciser que ces différentes classifications sont des évaluations radiographiques<br />
pré-opératoires. Elles ne tiennent donc pas des dégâts qui peuvent se surajouter lors de<br />
l’extraction de la prothèse et le nettoyage des débris de ciment. Ces classifications devraient<br />
être réévaluée systématiquement en per-opératoire.<br />
Type de classification<br />
Répartition des dégâts osseux<br />
Katz Harris A=80% ; B=18% ; C=2%<br />
Gie EndoKlinik I=5% ; II=71% ; III=23% ; IV=0%<br />
Migaud SOFCOT/Vives I=0% ; II=10% ; III=74% ; IV=16%<br />
May SOFCOT/Vives I=28% ; II=20% ; III=25% ; IV=26%<br />
Boisgard SOFCOT/Vives I=0% ; II=10% ; III=46% ; IV=44%<br />
Chandler<br />
44% de défects osseux importants<br />
McCarthy Paprosky I=0% ; II=46% ; IIIa=25% ; IIIb=13% ; IV=15%<br />
Essig Paprosky I=6% ; IIa=46% ; IIb=19% ; IIc=11% ; III=17%<br />
Le Béguec SOFCOT I=43% ; II=22% ; III=25% ; IV=10%<br />
Raman Paprosky I=33% ; II=50% : IIIa=11% ; IIIb=5% ; IV=0<br />
Notre série<br />
SOFCOT/Vives<br />
I=29% ; II=48% ; III=23%<br />
T (1ou2)=60% ; D=11%<br />
Classifications des dégâts osseux selon les séries.<br />
34
Complications<br />
Fractures per-opératoires<br />
Dans notre série, le nombre de fractures per-opératoires était de 6 cas dont 4 cas<br />
concernaient la diaphyse fémorale (13%). Les 2 autres fractures per-opératoires intéressaient<br />
le petit trochanter (2 cas).<br />
Cette complication peut survenir soit pendant la préparation endo-fémorale (ablation de<br />
l’implant et des débris de ciment), soit lors du passage des râpes ou de la mise en place de<br />
l’implant définitif pour les implants non cimentés. Cela explique la présence de cette<br />
complication dans les séries de reprises cimentées de Gie 20 (3%) et Migaud 46 (15%).<br />
Dans les séries utilisant les techniques de reprise non cimentées, ce taux varie de 3%<br />
pour Le Béguec 35 à 28% pour Chandler 6 . Notre série avec 13% de fractures, se situe ici, de<br />
façon intermédiaire. Nous signalons que dans la série de Le Béguec, qui présente le taux le<br />
plus faible (3%), le taux de volet fémoral pédiculé était lui très important (84%) et selon<br />
l’auteur lui-même excessif.<br />
La survenue d’une complication fracturaire ne modifie pas en principe le résultat final<br />
de l’intervention. C’est le cas dans notre étude ou l’analyse statistique des 2 groupes<br />
« fracture » et « pas de fracture » ne montre pas de différence significative en terme de scores<br />
fonctionnels au recul final.<br />
Fracture de l’implant<br />
Nous avons constaté un cas de fracture de l’implant. La faillite de l’implant s’est<br />
produite au niveau de la jonction tige-collerette à 5 ans de l’intervention initiale. L’union<br />
entre l’embase et la tige, qui était en théorie une zone de faiblesse, n’a pas présenté de<br />
complication importante. Nous avons juste dénombré 1 dévissage de la vis d’union, sans<br />
aucun démontage et totalement asymptomatique.<br />
Fausse route<br />
Nous avons dénombré 1 cas de fausse route dans notre série soit 3% des interventions.<br />
Le taux de notre série est ici dans la moyenne des différentes séries citées. Ce taux, quand il<br />
est noté, varie de 1,5% à 25% (5 cas dans la série de reprises cimentées de Migaud 46 ).<br />
Complications vasculo-nerveuses<br />
Nous n’avons pas noté de lésion de structure vasculo-nerveuse dans notre travail.<br />
Raman 62 a signalé une lésion du nerf sciatique, la série de Le Béguec en comptait deux et<br />
35
Essig dans sa série de reprises par le système PP avait retrouvé une lésion sciatique et une<br />
lésion vasculaire (paquet obturateur) 18 .<br />
Luxation<br />
L’augmentation du taux de luxation dans les reprises est évoquée par de nombreux<br />
auteurs. Les facteurs de ces luxations sont multiples (Huten 29 ) : outre les défauts liés au<br />
positionnement des implants, les paramètres de la population étudiée comme l’âge élevé ou la<br />
chirurgie itérative sont des facteurs péjoratifs. Les taux retrouvés dans les différentes séries<br />
que nous avons retenues allaient de 4,4% à 26%. Dans notre série, ce taux est de 6% pour les<br />
luxations précoces et 9% en y ajoutant les luxations tardives à l’origine d’une reprise<br />
chirurgicale. Nous avions trouvé une relation significative entre épisodes de luxation et<br />
nombre d’intervention précédant la reprise.<br />
Sepsis<br />
Nous avons dénombré dans notre série 2 cas d’infection tardive (6%) ayant motivé dans<br />
1 cas une reprise chirurgicale et un changement de prothèse en 2 temps. Ce taux d’infection<br />
profonde était indépendant, dans notre travail, des caractéristiques de la population étudiée.<br />
Ce taux est comparable à celui retrouvé dans la série à long terme de McCarthy, mais il<br />
est plus élevé que ceux retrouvés dans les autres séries de la littérature.<br />
Fracture per-opératoire Luxation Sepsis<br />
Katz 26% 2,4%<br />
Gie 3% 4,4% 0%<br />
Migaud 15% 5%<br />
May 17,2% 9% 1,3%<br />
Boisgard 4% 8% 0%<br />
Chandler 28% 23% 6%<br />
McCarthy - - 10%<br />
Le Béguec 3% 5% 2,6%<br />
Essig 12% 10% 4%<br />
Raman 6% 5% 2%<br />
SOFCOT 1999 4,7% 1%<br />
Notre série 13% 6% 6%<br />
36
Taux de complications dans les différentes séries<br />
Résultats fonctionnels<br />
Nous avons utilisé dans ce travail les scores fonctionnels de Harris 25 et de Postel et<br />
Merle d’Aubigné 44 . Bien que le score PMA ne prenne que peu en compte l’activité globale du<br />
patient, cette cotation reste néanmoins simple et reproductible. Nous l’avons donc associé à la<br />
cotation de Harris (Harris Hip Score) afin d’optimiser l’évaluation fonctionnelle. Ces<br />
cotations ont enfin l’avantage d’être largement utilisées dans la littérature. Ces deux cotations<br />
ont été complétées par un indice subjectif de satisfaction divisé en 5 stades.<br />
Les résultats fonctionnels de notre série semblent légèrement inférieurs à ceux retrouvés<br />
dans les différentes études que nous avons citées en ce qui concerne les cotations de Harris et<br />
Postel et Merle d’Aubigné. En ce qui concerne l’indice de satisfaction, 80% des patients<br />
considéraient le résultat satisfaisant ou très satisfaisant ce qui est comparable au chiffre<br />
retrouvé dans la série de May. On peut expliquer ces résultats par le taux élevé de boiterie de<br />
Trendelenburg (55%). On peut su<strong>pp</strong>oser que la médialisation induite par l’implant « PP »<br />
entraînant une diminution du bras de levier des muscles stabilisateurs de la hanche, de même<br />
que le taux non négligeable de pseudarthrose du grand trochanter peut être à l’origine de ces<br />
boiteries. La comparaison avec les autres séries reste délicate dans la mesure où les<br />
caractéristiques de chaque étude sont différentes en terme d’age, de stade Charnley, de dégâts<br />
osseux et aussi de recul.<br />
Le taux important de patients présentant une pathologie dysplasique dans notre série,<br />
avec une arthroplastie initiale difficile et une reprise également plus délicate, peut influer sur<br />
le résultat fonctionnel final. Cela peut également expliquer les résultats fonctionnels<br />
légèrement inférieurs de notre série.<br />
37
Série Implant Recul HHS PMA Satisfaction<br />
Katz Tige Cimentée 11,9 ans 49% de satisfaction<br />
Gie<br />
Allogreffe impactée et tige<br />
Cimentée<br />
2,5 ans 15,84<br />
Migaud<br />
Allogreffe morcelée,<br />
impactée et tige Cimentée 6,9 ans 16,3<br />
avec treillis<br />
May Tige Verrouillée (Ultime) 6 ans 13,4 (0-18)<br />
Satisfait/très satisfait=67,8%<br />
Insatisfait=11,1%<br />
Boisgard<br />
Tige non Cimentée<br />
(Wagner)<br />
3,6 ans 14,6<br />
Chandler<br />
Non Cimentée, modulaire<br />
(S-Rom)<br />
3 ans 82 (36-100) 84% de satisfaction<br />
Essig<br />
Non Cimentée, modulaire<br />
(PP)<br />
4 ans 14,3<br />
Lebeguec<br />
Non cimentée, modulaire<br />
(PFM-R)<br />
3 ans 81,4 14,70<br />
Raman Non cimentée (JRI) 8 ans 82 (59-96) 14,5<br />
Notre Non Cimentée, modulaire<br />
Satisfait/très satisfait=80%<br />
13 ans 72 13<br />
Série<br />
(PP)<br />
Insatisfait=3%<br />
Résultats fonctionnels (HHS, PMA et satisfaction).<br />
Survie de l’implant et reprise chirurgicale<br />
Notre taux de reprise chirurgicale de l’implant fémoral pour <strong>desc</strong>ellement aseptique était<br />
de 9% (3 cas). Il est sensiblement identique au taux retrouvé dans l’étude d’Essig 18 (10%). Il<br />
est plus élevé que dans les séries de Boisgard 4 (4%), Chandler 6 (4%), le Béguec 35 (3%),<br />
Migaud 46 (0%), Raman 62 (0%), Gie 20 (0%). On peut remarquer que, mis à part la série de<br />
Raman et de Migaud, ces études possèdent un recul limité allant de 2,5 à 3,6 ans. Cela peut<br />
expliquer l’absence ou le faible taux de reprise chirurgicale dans ces séries. Katz, dans sa série<br />
de reprise à un recul moyen de 11,9 ans, signale un taux de re-révision de l’implant fémoral<br />
aseptique de 16%. Il semble logique que plus on s’avance dans le long terme, plus le nombre<br />
de reprise des implants augmente.<br />
38
Reconstruction osseuse<br />
La restauration du stock osseux est un élément fondamental de la survie des<br />
rescellements des prothèses totales de hanche comme le montre Dujardin 13 dans le<br />
symposium de la SOFCOT 1999. Dans cette optique, deux techniques semblent se<br />
démarquer : les tiges à ancrage distal et les greffes morcelées impactées. Dans le premier cas,<br />
la régénération osseuse sera jugée sur le gain d’épaisseur corticale et dans le deuxième cas,<br />
sur l’intégration des greffons selon la classification de Pierchon 57 par exemple.<br />
L’indice de Hoffman 28 semble être également un bon indice de reconstruction osseuse<br />
global puisqu’il prend en compte les trois variables susceptibles d’évoluer à savoir la largeur<br />
du canal et les deux épaisseurs corticales.<br />
La tige PP non cimentée fait partie de ces tiges à ancrage distal. La régénération<br />
osseuse corticale diaphysaire autour de cet implant en Titane, même en l’absence de surface<br />
ostéo-inductrice, a été démontrée par Essig 18 et Nehme 52 sur des travaux portant sur des<br />
reprises par le système « PP ». Ils ont noté, au recul, de façon significative une augmentation<br />
des épaisseurs corticales à différents niveaux. L’analyse de la série de la SOFCOT 1999 a<br />
même montré que la régénération osseuse diaphysaire avec le système PP était l’une des<br />
meilleures.<br />
Ces résultats sont confirmés à long terme dans notre série de 31 reprises utilisant<br />
l’implant PP. Nous avons effectivement retrouvé cette qualité de régénération osseuse avec<br />
des augmentations significatives des épaisseurs de corticales médiales et latérales au niveau<br />
du petit trochanter et 5 cm en dessous de celui-ci. Au niveau 10 cm en dessous du petit<br />
trochanter, l’augmentation n’était significative qu’au niveau de la corticale médiale.<br />
Certains auteurs ont retrouvé une relation entre la régénération osseuse et le stade<br />
d’altérations osseuses pré-opératoire. C’était également le cas ici, mais nous n’avons retrouvé<br />
de relation statistique qu’entre gain d’épaisseur corticale médiale au petit trochanter et stade<br />
SOFCOT.<br />
Cette régénération osseuse est conditionnée par l’a<strong>pp</strong>lication d’une technique<br />
chirurgicale rigoureuse d’extraction et de réimplantation épargnant le manchon<br />
musculopériosté diaphysaire associée à un abord limité par des ostéotomies pédiculées<br />
(trochantérotomie en digastrique par exemple) conservant la vascularisation régionale.<br />
La reconstruction osseuse semble être dans notre travail, maximale dans la région du<br />
petit trochanter avec une baisse progressive quand on se dirige vers la partie distale de la<br />
prothèse. Ceci a été noté par Nehme 52 et peut être expliqué par le dessin spécifique de<br />
l’implant. L’a<strong>pp</strong>ui diaphysaire cortical exercé par la collerette induit probablement une mise<br />
39
en contrainte à ce niveau avec un gradient de force qui diminue en s’éloignant de cette<br />
collerette.<br />
Dans les séries que nous avions retenues à titre comparatif, plusieurs auteurs n’ont pas<br />
précisé leur protocole d’évaluation de la reconstruction osseuse (Katz, Gie, Chandler,<br />
Raman). Boisgard utilise une classification en 3 stades fondée sur la présence d’une<br />
reconstruction avec ou sans trabéculation. Le Béguec utilise lui sur une cotation en 4 stades<br />
basée sur le caractère complet ou incomplet de la régénération osseuse et sur la présence ou<br />
non de stress-schielding.<br />
Essig et May ont utilisé la mesure des épaisseurs corticales .May avait retrouvé une<br />
augmentation significative des épaisseurs corticales dans sa série de tiges verrouillées avec<br />
un gain maximal à 10 cm du petit trochanter. Il avait attribué ce résultat au processus de<br />
consolidation des volets fémoraux réalisés dans sa série. Nous n’avons pas retrouvé ce<br />
phénomène dans notre série.<br />
Gain Index Hoffman petit<br />
trochanter<br />
Gain index Hoffman<br />
5cm<br />
Gain Index Hoffman<br />
10cm<br />
May +9 +15 +25<br />
Notre série +12,7 +11,7 +2,6<br />
Variation de l’Index de Hoffman à différents niveaux<br />
40
IV CONCLUSION<br />
Ce travail réalisé sur 31 reprises, à long terme, de prothèses totales de hanche par le<br />
système « PP » confirme les bons résultats déjà observés avec cette technique de reprise.<br />
Cette technique est fondée sur l’utilisation d’un implant modulaire, en titane, non cimenté, à<br />
traitement de surface total sans revêtement d’hydroxy-apatite recherchant un blocage<br />
diaphysaire, associée à un abord chirurgical permettant de préserver la vascularisation<br />
régionale. Elle permet de traiter les pertes osseuses modérées mais également sévères (Stade<br />
III), en induisant une régénération osseuse métaphysaire et diaphysaire traduisant la qualité<br />
de la reconstruction osseuse péri-prothétique..<br />
avec un taux de complications sensiblement identique aux autres séries. Ce travail avait<br />
l’avantage d’évaluer cette technique avec un recul moyen de 13 ans, ce que l’on peut<br />
considérer comme du long terme en matière de reprise d’arthroplastie de hanche. Ceci<br />
Le système « PP » reste donc une réponse toujours adaptée pour le traitement des<br />
<strong>desc</strong>ellements aseptiques d’arthroplastie totale de hanche asssociés à une perte osseuse périprothétique.<br />
41
BIBLIOGRAPHIE<br />
1. Anthony, P. P.; Gie, G. A.; Howie, C. R.; and Ling, R. S.: Localised endosteal bone<br />
lysis in relation to the femoral components of cemented total hip arthroplasties. J Bone<br />
Joint Surg Br, 72(6): 971-9, 1990.<br />
2. Berry, D. J.; Harmsen, W. S.; Ilstrup, D.; Lewallen, D. G.; and Cabanela, M. E.:<br />
Survivorship of uncemented proximally porous-coated femoral components. Clin<br />
Orthop Relat Res, (319): 168-77, 1995.<br />
3. Blacker, G. J., and Charnley, J.: Changes in the u<strong>pp</strong>er femur after low friction<br />
arthroplasty. Clin Orthop Relat Res, (137): 15-23, 1978.<br />
4. Boisgard, S.; Moreau, P. E.; Tixier, H.; and Levai, J. P.: [Bone reconstruction, leg<br />
length discrepancy, and dislocation rate in 52 Wagner revision total hip arthroplasties<br />
at 44-month follow-up]. Rev Chir Orthop Reparatrice A<strong>pp</strong>ar Mot, 87(2): 147-54,<br />
2001.<br />
5. Boldt, J. G.; Dilawari, P.; Agarwal, S.; and Drabu, K. J.: Revision total hip<br />
arthroplasty using impaction bone grafting with cemented nonpolished stems and<br />
charnley cups. J Arthroplasty, 16(8): 943-52, 2001.<br />
6. Chandler, H. P.; Ayres, D. K.; Tan, R. C.; Anderson, L. C.; and Varma, A. K.:<br />
Revision total hip replacement using the S-ROM femoral component. Clin Orthop<br />
Relat Res, (319): 130-40, 1995.<br />
7. Chao, E. Y., and Sim, F. H.: Composite fixation of salvage prostheses for the hip and<br />
knee. Clin Orthop Relat Res, (276): 91-101, 1992.<br />
8. Charnley, J., and Cupic, Z.: The nine and ten year results of the low-friction<br />
arthroplasty of the hip. Clin Orthop Relat Res, (95): 9-25, 1973.<br />
9. Collis, D. K.: Cemented total hip replacement in patients who are less than fifty years<br />
old. J Bone Joint Surg Am, 66(3): 353-9, 1984.<br />
10. Courpied, J.: Femoral revisions in iterative total hip arthroplasties. Reconstruction<br />
with segmental allograft. Hip 99 Congress proceedings. Toulouse France, 295-8,<br />
1999.<br />
11. D'Antonio, J.; McCarthy, J. C.; Bargar, W. L.; Borden, L. S.; Ca<strong>pp</strong>elo, W. N.;<br />
Collis, D. K.; Steinberg, M. E.; and Wedge, J. H.: Classification of femoral<br />
abnormalities in total hip arthroplasty. Clin Orthop Relat Res, (296): 133-9, 1993.<br />
12. Dohmae, Y.; Bechtold, J. E.; Sherman, R. E.; Puno, R. M.; and Gustilo, R. B.:<br />
Reduction in cement-bone interface shear strength between primary and revision<br />
arthroplasty. Clin Orthop Relat Res, (236): 214-20, 1988.<br />
13. Dujardin, F., and Mazirt, N.: Régénération osseuse spontanée. Symposium<br />
SO.F.C.O.T, 1999.<br />
14. Echeverri, A.; Shelley, P.; and Wroblewski, B. M.: Long-term results of hip<br />
arthroplasty for failure of previous surgery. J Bone Joint Surg Br, 70(1): 49-51, 1988.<br />
15. Eldridge, J. D.; Smith, E. J.; Hubble, M. J.; Whitehouse, S. L.; and Learmonth, I.<br />
D.: Massive early subsidence following femoral impaction grafting. J Arthroplasty,<br />
12(5): 535-40, 1997.<br />
16. Elting, J. J.; Mikhail, W. E.; Zicat, B. A.; Hubbell, J. C.; Lane, L. E.; and House,<br />
B.: Preliminary report of impaction grafting for exchange femoral arthroplasty. Clin<br />
Orthop Relat Res, (319): 159-67, 1995.<br />
17. Emerson, R. H., Jr.; Malinin, T. I.; Cuellar, A. D.; Head, W. C.; and Peters, P.<br />
C.: Cortical strut allografts in the reconstruction of the femur in revision total hip<br />
arthroplasty. A basic science and clinical study. Clin Orthop Relat Res, (285): 35-44,<br />
1992.<br />
42
18. Essig, J., and Puget, J.: La reprise d'arthroplastie totale de hanche par la prothèse de<br />
reconstruction du système PP. Thèse, Université Toulouse III, 1993.<br />
19. Estok, D. M., 2nd, and Harris, W. H.: Long-term results of cemented femoral<br />
revision surgery using second-generation techniques. An average 11.7-year follow-up<br />
evaluation. Clin Orthop Relat Res, (299): 190-202, 1994.<br />
20. Gie, G. A.; Linder, L.; Ling, R. S.; Simon, J. P.; Slooff, T. J.; and Timperley, A.<br />
J.: Impacted cancellous allografts and cement for revision total hip arthroplasty. J<br />
Bone Joint Surg Br, 75(1): 14-21, 1993.<br />
21. Gross, A. E., and Hutchison, C. R.: Proximal femoral allografts for reconstruction of<br />
bone stock in revision arthroplasty of the hip. Orthop Clin North Am, 29(2): 313-7,<br />
1998.<br />
22. Gruen, T. A.; McNeice, G. M.; and Amstutz, H. C.: "Modes of failure" of cemented<br />
stem-type femoral components: a radiographic analysis of loosening. Clin Orthop<br />
Relat Res, (141): 17-27, 1979.<br />
23. Halley, D. K., and Wroblewski, B. M.: Long-term results of low-friction arthroplasty<br />
in patients 30 years of age or younger. Clin Orthop Relat Res, (211): 43-50, 1986.<br />
24. Harris, W. H.: The first 32 years of total hip arthroplasty. One surgeon's perspective.<br />
Clin Orthop Relat Res, (274): 6-11, 1992.<br />
25. Harris, W. H.: Traumatic arthritis of the hip after dislocation and acetabular<br />
fractures: treatment by mold arthroplasty. An end-result study using a new method of<br />
result evaluation. J Bone Joint Surg Am, 51(4): 737-55, 1969.<br />
26. Head, W. C.; Bauk, D. J.; and Emerson, R. H., Jr.: Titanium as the material of<br />
choice for cementless femoral components in total hip arthroplasty. Clin Orthop Relat<br />
Res, (311): 85-90, 1995.<br />
27. Heekin, R. D.; Engh, C. A.; and Vinh, T.: Morselized allograft in acetabular<br />
reconstruction. A postmortem retrieval analysis. Clin Orthop Relat Res, (319): 184-90,<br />
1995.<br />
28. Hofmann, A. A.; Wyatt, R. W.; France, E. P.; Bigler, G. T.; Daniels, A. U.; and<br />
Hess, W. E.: Endosteal bone loss after total hip arthroplasty. Clin Orthop Relat Res,<br />
(245): 138-44, 1989.<br />
29. Huten, D.: Luxation et subluxation des prothèses totales e hanches. Cahiers<br />
d'enseignement de la SOFCOT, 55, 1996.<br />
30. Katz, R. P.; Callaghan, J. J.; Sullivan, P. M.; and Johnston, R. C.: Long-term<br />
results of revision total hip arthroplasty with improved cementing technique. J Bone<br />
Joint Surg Br, 79(2): 322-6, 1997.<br />
31. Kavanagh, B. F., and Fitzgerald, R. H., Jr.: Multiple revisions for failed total hip<br />
arthroplasty not associated with infection. J Bone Joint Surg Am, 69(8): 1144-9, 1987.<br />
32. Kilgus, D. J.; Shimaoka, E. E.; Tipton, J. S.; and Eberle, R. W.: Dual-energy X-<br />
ray absorptiometry measurement of bone mineral density around porous-coated<br />
cementless femoral implants. Methods and preliminary results. J Bone Joint Surg Br,<br />
75(2): 279-87, 1993.<br />
33. Kim, Y. H.: Cemented revision hip arthroplasty using strut and impacted cancellous<br />
allografts. J Arthroplasty, 19(6): 726-32, 2004.<br />
34. Kiratli, B. J.; Heiner, J. P.; McBeath, A. A.; and Wilson, M. A.: Determination of<br />
bone mineral density by dual x-ray absorptiometry in patients with uncemented total<br />
hip arthroplasty. J Orthop Res, 10(6): 836-44, 1992.<br />
35. LeBéguec, P.: Reprise des prothèses fémorales <strong>desc</strong>ellées avec tiges fémorales pressfit.<br />
Maitrise orthopédique, 2002.<br />
43
36. Lieberman, J. R.; Moeckel, B. H.; Evans, B. G.; Salvati, E. A.; and Ranawat, C.<br />
S.: Cement-within-cement revision hip arthroplasty. J Bone Joint Surg Br, 75(6): 869-<br />
71, 1993.<br />
37. Malkani, A. L.; Lewallen, D. G.; Cabanela, M. E.; and Wallrichs, S. L.: Femoral<br />
component revision using an uncemented, proximally coated, long-stem prosthesis. J<br />
Arthroplasty, 11(4): 411-8, 1996.<br />
38. Mallory, T. H.; Lombardi, A. V., Jr.; Leith, J. R.; Fujita, H.; Hartman, J. F.;<br />
Ca<strong>pp</strong>s, S. G.; Kefauver, C. A.; Adams, J. B.; and Vorys, G. C.: Minimal 10-year<br />
results of a tapered cementless femoral component in total hip arthroplasty. J<br />
Arthroplasty, 16(8 Su<strong>pp</strong>l 1): 49-54, 2001.<br />
39. Martin: Les prothèses de charnley-Kerboul. Rev Chir Orthop Reparatrice A<strong>pp</strong>ar Mot<br />
Symposium Sofcot, 1989.<br />
40. Masterson, E. L.; Masri, B. A.; Duncan, C. P.; Rosenberg, A.; Cabanela, M.; and<br />
Gross, M.: The cement mantle in femoral impaction allografting. A comparison of<br />
three systems from four centres. J Bone Joint Surg Br, 79(6): 908-13, 1997.<br />
41. May, O.: Implant fémoral de reprise à verrouillage distal. A propos de 101 cas, au<br />
recul minimum de 5 ans. Thèse, Université Lille II, 2006.<br />
42. McCarthy, J. C., and Lee, J.: Complex Revision Total Hip Arthroplasty with<br />
Modular Stems at a Mean of 14 Years. Clin Orthop Relat Res, 2007.<br />
43. Meding, J. B.; Ritter, M. A.; Keating, E. M.; and Faris, P. M.: Impaction bonegrafting<br />
before insertion of a femoral stem with cement in revision total hip<br />
arthroplasty. A minimum two-year follow-up study. J Bone Joint Surg Am, 79(12):<br />
1834-41, 1997.<br />
44. Merle d'Aubigné, R.: Cotation chiffrée de la fonction de la hanche. Rev Chir Orthop<br />
Reparatrice A<strong>pp</strong>ar Mot, 56: 481-486, 1970.<br />
45. Migaud, H.; Eddine., A.; Demondion, X.; Jardin, C.; Laffargue, P.; and<br />
Dujardin, F.: Classification des pertes de substances: reproductilbilité des<br />
classifications et groupements lésionnels. Symposium SO.F.C.O.T.1999, 1999.<br />
46. Migaud, H.; Jardin, C.; Fontaine, C.; Pierchon, F.; d'Herbomez, O.; and<br />
Duquennoy, A.: [Femoral reconstruction with endosteal bone allografts protected by<br />
a metallic mesh in reoperation of total hip prosthesis. 19 cases with an average followup<br />
of 83 months]. Rev Chir Orthop Reparatrice A<strong>pp</strong>ar Mot, 83(4): 360-7, 1997.<br />
47. Mittelmeier, H., and Heisel, J.: Sixteen-years' experience with ceramic hip<br />
prostheses. Clin Orthop Relat Res, (282): 64-72, 1992.<br />
48. Morrey, B. F., and Kavanagh, B. F.: Complications with revision of the femoral<br />
component of total hip arthroplasty. Comparison between cemented and uncemented<br />
techniques. J Arthroplasty, 7(1): 71-9, 1992.<br />
49. Muller, M. E.: Lessons of 30 years of total hip arthroplasty. Clin Orthop Relat Res,<br />
(274): 12-21, 1992.<br />
50. Mulliken, B. D.; Rorabeck, C. H.; and Bourne, R. B.: Uncemented revision total<br />
hip arthroplasty: a 4-to-6-year review. Clin Orthop Relat Res, (325): 156-62, 1996.<br />
51. Mulroy, R. D., Jr., and Harris, W. H.: The effect of improved cementing techniques<br />
on component loosening in total hip replacement. An 11-year radiographic review. J<br />
Bone Joint Surg Br, 72(5): 757-60, 1990.<br />
52. Nehme, A., and Puget, J.: Le système PP dans les reprises de PTH. Thèse, Université<br />
Toulouse III, 2000.<br />
53. Nelissen, R. G.; Bauer, T. W.; Weidenhielm, L. R.; LeGolvan, D. P.; and Mikhail,<br />
W. E.: Revision hip arthroplasty with the use of cement and impaction grafting.<br />
Histological analysis of four cases. J Bone Joint Surg Am, 77(3): 412-22, 1995.<br />
44
54. Nunn, D.; Freeman, M. A.; Tanner, K. E.; and Bonfield, W.: Torsional stability of<br />
the femoral component of hip arthroplasty. Response to an anteriorly a<strong>pp</strong>lied load. J<br />
Bone Joint Surg Br, 71(3): 452-5, 1989.<br />
55. Pak, J. H.; Paprosky, W. G.; Jablonsky, W. S.; and Lawrence, J. M.: Femoral<br />
strut allografts in cementless revision total hip arthroplasty. Clin Orthop Relat Res,<br />
(295): 172-8, 1993.<br />
56. Paprosky, W. G.; Bradford, M. S.; and Younger, T. I.: Classification of bone<br />
defects in failed prostheses. Chir Organi Mov, 79(4): 285-91, 1994.<br />
57. Pierchon, F.; Migaud, H.; and Duquennoy, A.: [Reconstitution of femoral bone<br />
stock in loosening of total hip prosthesis]. Acta Orthop Belg, 59(3): 278-86, 1993.<br />
58. Pierson, J. L., and Harris, W. H.: Effect of improved cementing techniques on the<br />
longevity of fixation in revision cemented femoral arthroplasties. Average 8.8-year<br />
follow-up period. J Arthroplasty, 10(5): 581-91, 1995.<br />
59. Puget: Stratégies dans les reprises de prothèse totale de hanche. Conférences<br />
d'enseignement de la SOFCOT 2006.<br />
60. Puget J, T. J.: Reprise de prothèse totale de hanche par système PP. Reconstruction<br />
prothétique de l'extrémité supérieure du fémur, 14-16 Octobre 1993: 60-70, 1993.<br />
61. Puget, J.; Tricoire, J. L.; Chiron, P.; and Uthéza, G.: Système PP : Matériel et<br />
technique. Le <strong>desc</strong>ellement fémoral des prothèses totales de hanche, 204, 1992.<br />
62. Raman, R.; Kamath, R. P.; Parikh, A.; and Angus, P. D.: Revision of cemented<br />
hip arthroplasty using a hydroxyapatite-ceramic-coated femoral component. J Bone<br />
Joint Surg Br, 87(8): 1061-7, 2005.<br />
63. Sabo, D.; Reiter, A.; Simank, H. G.; Thomsen, M.; Lukoschek, M.; and<br />
Ewerbeck, V.: Periprosthetic mineralization around cementless total hip<br />
endoprosthesis: longitudinal study and cross-sectional study on titanium threaded<br />
acetabular cup and cementless Spotorno stem with DEXA. Calcif Tissue Int, 62(2):<br />
177-82, 1998.<br />
64. Stromberg, C. N.; Herberts, P.; and Palmertz, B.: Cemented revision hip<br />
arthroplasty. A multicenter 5-9-year study of 204 first revisions for loosening. Acta<br />
Orthop Scand, 63(2): 111-9, 1992.<br />
65. Sugiyama, H.; Whiteside, L. A.; and Kaiser, A. D.: Examination of rotational<br />
fixation of the femoral component in total hip arthroplasty. A mechanical study of<br />
micromovement and acoustic emission. Clin Orthop Relat Res, (249): 122-8, 1989.<br />
66. Sutherland, C. J.; Wilde, A. H.; Borden, L. S.; and Marks, K. E.: A ten-year<br />
follow-up of one hundred consecutive Muller curved-stem total hip-replacement<br />
arthroplasties. J Bone Joint Surg Am, 64(7): 970-82, 1982.<br />
67. Weaver, J. K.: Activity expectations and limitations following total joint<br />
replacement. Clin Orthop Relat Res, (137): 55-61, 1978.<br />
68. Willert, H. G.; Bertram, H.; and Buchhorn, G. H.: Osteolysis in alloarthroplasty of<br />
the hip. The role of ultra-high molecular weight polyethylene wear particles. Clin<br />
Orthop Relat Res, (258): 95-107, 1990.<br />
69. Willert, H. G.; Ludwig, J.; and Semlitsch, M.: Reaction of bone to methacrylate<br />
after hip arthroplasty: a long-term gross, light microscopic, and scanning electron<br />
microscopic study. J Bone Joint Surg Am, 56(7): 1368-82, 1974.<br />
45
Mme D. 72 ans<br />
Descellement Bipolaire d’une PTH cimentée<br />
datant de 1983<br />
(Stade Sofcot 3 avec atteinte du grand<br />
trochanter)<br />
1993 : Reprise par tige PP,<br />
trochantérotomie et Anneau de<br />
soutient<br />
Résultats à 17 ans de Recul<br />
46