You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Page 1/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
ASPECTS CINÉTIQUES DES RÉACTIONS D’OXYDO-RÉDUCTION :<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
I : Cinétique des réactions électrochimiques.<br />
1°) Lien entre vitesse et <strong>intensité</strong>.<br />
Terminologie et conventions :<br />
Une réaction électrochimique correspond à un transfert d’électrons entre un oxydant et<br />
un réducteur, se faisant au contact d’une électrode métallique, suivant le schéma :<br />
− réduction<br />
α Ox + n e ←⎯⎯ ⎯⎯⎯⎯→ ⎯ β Red<br />
.<br />
1 1 1<br />
oxydation<br />
1 1<br />
Anode l’électrode sur laquelle se produit une réaction<br />
d’oxydAtion et<br />
Cathode celle sur laquelle se produit une réaction de<br />
réduCtion.<br />
L’anode est l’électrode par laquelle entre le courant depuis<br />
l’extérieur dans la cellule électrochimique.<br />
I > 0<br />
Anode Cathode<br />
pile ou<br />
électrolyseur.<br />
Intensité et vitesse de réaction.<br />
oxydation<br />
−<br />
Soit la réaction électrochimique à une électrode : β Re d←⎯⎯ ⎯⎯⎯⎯→ ⎯ αOx+<br />
ze<br />
réduction<br />
On note υ Ox la vitesse de la réaction directe et υ Red celle de la réaction inverse. On a :<br />
⎛ 1 dnOx ⎞<br />
υOx<br />
= ⎜<br />
α dt<br />
⎟<br />
⎝ ⎠Ox ⎛ 1 dnRed<br />
⎞<br />
= ⎜− ⎟<br />
⎝ β dt ⎠Ox<br />
et<br />
⎛ 1 dnOx ⎞<br />
υred<br />
= ⎜− α dt<br />
⎟<br />
⎝ ⎠Red ⎛ 1 dnRed<br />
⎞<br />
= ⎜ ⎟<br />
⎝β dt ⎠red<br />
Si pendant la durée dt, l’avancement de la réaction électrochimique<br />
varie de dξ, la charge électrique échangée traversant formellement<br />
l’interface électrode <strong>–</strong> solution dans le sens électrode solution est<br />
dξ<br />
dq dξ<br />
dq = z F correspondant à l’<strong>intensité</strong> i = = zF<br />
.<br />
dt<br />
dt dt<br />
Or d<br />
I<br />
e<br />
ξ<br />
est la vitesse de la réaction électrochimique : υ = υOx − υRed<br />
.<br />
dt<br />
On retient :<br />
La vitesse de la réaction électrochimique au contact d’une électrode est pro-<br />
i = zF υ −υ<br />
- Ox<br />
Red<br />
portionnelle à l’<strong>intensité</strong> du courant traversant l’électrode : ( )<br />
Rappel : F désigne le faraday : Ae = F N soit<br />
96485 Cmol .<br />
−<br />
=<br />
1<br />
F .<br />
On retrouve bien les conventions d’algébrisation précédentes :<br />
Ox Red<br />
I est positive si la réaction à l’électrode est une oxydation (l’électrode est une anode),<br />
I est négative si la réaction à l’électrode est une réduction (l’électrode est une cathode).<br />
Les facteurs cinétiques.<br />
Facteurs cinétiques communs à toute réaction hétérogène : température T, aire S de l’interface<br />
électrode <strong>–</strong> solution, concentrations des espèces dissoutes ci .<br />
Facteurs cinétiques propres aux réactions électrochimiques : nature et <strong>potentiel</strong> de l’électrode<br />
(ou plutôt d.d.p. V entre l’électrode et la solution).<br />
On retient :
Page 2/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
On peut en général mettre l’<strong>intensité</strong> I sous la forme : I = kTSV ( , , ). f( c)<br />
.<br />
Les <strong>courbes</strong> représentant, à T, S, et c i bloqués, les variations de I en fonction<br />
de E sont appelées <strong>courbes</strong> <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong> (en abrégé I(E)) du<br />
couple Ox/Red pour l’électrode considérée.<br />
Remarque :<br />
Les vitesses de réaction υ Ox et υ Red sont des grandeurs extensives, de même que l’aire S de<br />
l’interface électrode <strong>–</strong> solution. On définit alors une vitesse de réaction « intensive » par la vitesse<br />
surfacique, obtenue en divisant la vitesse par S.<br />
I<br />
On déduit des équations précédentes la relation entre la densité de courant j = et les vi-<br />
S<br />
tesses surfaciques v Ox et v Red : j = zF ( vOx − vRed ) = jOx + jRed<br />
.<br />
Pour décrire les phénomènes sur une seule électrode, on pourra indifféremment utiliser les<br />
<strong>courbes</strong> I(V) ou j(V).<br />
L’étude d’un système réel (à deux électrodes) doit être menée à l’aide des <strong>courbes</strong><br />
I(V) pour traduire la conservation de la charge électrique !<br />
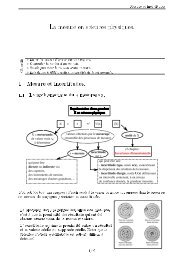
2°) Les différentes étapes de réactions à une électrode.<br />
La réaction électrochimique se produit au sein d’un milieu réactionnel hétérogène au voisinage<br />
de l’interface électrode <strong>–</strong> solution, qu’on peut schématiser par le modèle dit à double couche<br />
(proposé par Helmholtz) et mettant en jeu les trois processus suivants :<br />
1. Approche de l’électrode par les réactifs : transfert de matière , assuré au sein de la solution<br />
par trois phénomènes principaux :<br />
- la diffusion : déplacement des molécules ou des ions sou l’effet d’un gradient de concentration,<br />
qui satisfait en général à la loi de Fick.<br />
- la migration : déplacement des ions sous l’effet du champ électrique créé dans<br />
l’électrolyte<br />
- la convection : déplacement des molécules ou des ions sous l’effet d’une agitation mécanique<br />
de la solution<br />
<br />
2. Transformations chimiques dans une zone entourant l’électrode baptisée « double<br />
couche », où règne un gradient de <strong>potentiel</strong> qui modifie la structure électronique des espèces<br />
(transferts de protons ou de ligands, réactions de surface et transferts d’électrons).<br />
C’est la zone d’activation au sens cinétique du terme<br />
<br />
3. Transfert de charge qui se produit à la surface de l’électrode puis éloignement des (ou<br />
de certains) produits de la réaction de l’électrode.<br />
électrode<br />
métallique<br />
double couche (≈ qqs μm)<br />
espèces activées ou désactivées notées ≠ espèces usuelles<br />
transfert de<br />
trasnfert<br />
ze<br />
de charges matière<br />
− réactions<br />
≠<br />
X Ox <br />
1<br />
1 Ox<br />
chimiques<br />
1<br />
<br />
≠<br />
Red Red<br />
≠ <br />
réactions<br />
Y ≠ réactions<br />
X '1<br />
desurface<br />
<br />
≠ <br />
réactions<br />
Y '<br />
≠ <br />
1<br />
desurface<br />
1<br />
chimiques<br />
solution<br />
1 1<br />
i
3°) Courbes <strong>intensité</strong> <strong>–</strong><strong>potentiel</strong>.<br />
Principe.<br />
Page 3/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Le relevé d’une courbe <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong> d’un couple rédox donné sur une électrode de<br />
travail fixée nécessite de mesurer simultanément d’une part la d.d.p. d’interface électrode <strong>–</strong> solution,<br />
ce qui suppose la construction d’une cellule galvanique et d’autre part de mesurer<br />
l’<strong>intensité</strong> du courant en précisant si l’électrode reçoit ou fournit des électrons.<br />
Le montage satisfaisant à ces deux contraintes est un montage à trois électrodes dont le schéma<br />
de principe est donné sur la figure ci-dessous :<br />
La d.d.p. nécessaire est fournie par un générateur extérieur de f.e.m. variable U.<br />
L’<strong>intensité</strong> du courant d’électrolyse est mesurée grâce à l’ampèremètre .<br />
La cellule d’électrolyse contient la solution électrolytique dans laquelle plongent trois<br />
électrodes : l’électrode de travail E T dont on mesure le <strong>potentiel</strong> E par rapport à une<br />
électrode de référence (E.C.S. par exemple) à l’aide d’un voltmètre .<br />
Le courant circule entre l’électrode de travail et la contre électrode .<br />
Les trois électrodes sont rapprochées au maximum pour éviter les chutes ohmiques.<br />
Relevé expérimental.<br />
Les <strong>courbes</strong> obtenues sont dites <strong>courbes</strong> <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong>, bien qu’en fait :<br />
o L’<strong>intensité</strong> mesurée I soit rapidement convertie en densité de courant j pour<br />
s’affranchir des autres paramètres électriques, comme la taille des électrodes.<br />
o Le « <strong>potentiel</strong> » E soit en fait une f.e.m. algébrisée, convertie en d.d.p. par rapport<br />
à l’électrode standard à hydrogène.<br />
L’électrode peut être : La réaction est L’<strong>intensité</strong> est comptée<br />
anode une oxydation positivement i a > 0<br />
cathode une réduction négativement i c < 0<br />
Dans la réalité, le montage de principe montre vite ses limites :<br />
chaque fois que l’on fait varier la d.d.p. V , il faut s’assurer que le<br />
courant est bien nul dans la cellule galvanique E T / ECS, ce qui ne<br />
permet pas des enregistrements continus et précis. Il faut donc faire<br />
appel à un montage électrique particulier : le potentiostat.<br />
Dans ce montage, l’<strong>intensité</strong> dans la cellule galvanique auxiliaire<br />
E T / ECS est relevée à chaque modification de la tension appliquée<br />
entre E T et la contre électrode, et automatiquement annulée. Le<br />
temps de réaction étant très faible, on lit instantanément l’<strong>intensité</strong><br />
du courant I dans le circuit principal E T / CE en fonction du <strong>potentiel</strong><br />
E.<br />
mA<br />
C.E.<br />
potentiostat<br />
auxiliaire commande consigne<br />
V<br />
E.C.S.<br />
V consigne<br />
E T<br />
E
II : Les <strong>courbes</strong> I(E) obtenues : allures et interprétations.<br />
Page 4/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Considérons le relevé expérimental suivant réalisé à 298 K, obtenu en plaçant dans un bécher<br />
jouant le rôle de la cellule :<br />
- 50 mL d’une solution d’hexacyanoferrate III de potassium K 3Fe(CN) 6 à 0,05 mol.L -1 ,<br />
- 50 mL d’une solution d’hexacyanoferrate II de potassium K 4Fe(CN) 6 à 0,05 mol.L -1 .<br />
On utilise deux électrodes de platine comme électrode de travail et contre électrode, en opérant<br />
avec une agitation modérée.<br />
On donne :<br />
( )<br />
Relevé point par point<br />
de la courbe I(U)<br />
Analyse des résultats<br />
obtenus<br />
3−<br />
⎛Fe CN<br />
⎞<br />
E° 6 ⎜ 4−<br />
= 0, 40 V<br />
⎜<br />
⎟<br />
Fe( CN ) ⎟<br />
⎝ 6 ⎠<br />
et E° ( EC . . S.) = 0,25V<br />
.<br />
Phase 1 :<br />
1. L’état d’équilibre électrochimique tel que : i = 0 est obtenu pour un<br />
<strong>potentiel</strong> égal au <strong>potentiel</strong> rédox thermodynamique E eq calculable par<br />
la relation de Nernst.<br />
2. Dès qu’on diminue la tension appliquée, le système réagit par une réaction<br />
de réduction, correspondant à la transformation :<br />
−<br />
( ) + → ( )<br />
3−4− 6 6<br />
Fe CN e Fe CN<br />
Le courant devient plus important et tend rapidement vers une valeur<br />
sensiblement constante : un palier.<br />
3. Dans un large domaine de <strong>potentiel</strong>, le courant ne varie pratiquement<br />
plus : on observe une saturation.<br />
4. Pour des <strong>potentiel</strong>s très négatifs, on constate l’apparition de petites<br />
bulles gazeuses à la surface de l’électrode de travail : il s’agit de la réduc-<br />
− −<br />
tion du solvant (ici l’eau) selon : 2HO+ 2e → H 2 2 + 2OH<br />
Phase 2 :<br />
5. Dans le domaine des <strong>potentiel</strong>s croissants, on obtient des résultats analogues<br />
: nette augmentation du courant dans la phase d’oxydation selon :<br />
4− 3−<br />
−<br />
Fe CN → Fe CN + e<br />
( ) ( )<br />
6 6<br />
6. puis palier de saturation,<br />
− +<br />
7. enfin oxydation du solvant selon : 2HO→ O 2 2 + 4e+ 4Haq Cet exemple permet de dégager les caractéristiques principales des <strong>courbes</strong> I(E) en analysant<br />
l’étape cinétiquement limitante.
Page 5/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
1°) Cas où le transfert de charge est l’étape cinétiquement limitante.<br />
On distingue les systèmes électrochimiques rapides et lents :<br />
Système rapide. Système lent.<br />
• Pour un système rapide, l’<strong>intensité</strong> croît (i a ><br />
0 et i c < 0) rapidement dès que l’on s’écarte<br />
du <strong>potentiel</strong> d’équilibre E eq donné par la formule<br />
de Nernst.<br />
• On parle de vague d’oxydation pour i > 0<br />
et de vague de réduction pour i < 0.<br />
• On peut considérer la courbe de polarisation<br />
comme la somme des <strong>intensité</strong>s dues à deux<br />
phénomènes opposés : ox red et red ox.<br />
• On peut considérer E c,éq comme le <strong>potentiel</strong><br />
à courant nul lorsque la solution ne contient<br />
que l’oxydant.<br />
• On peut considérer E a,éq comme le <strong>potentiel</strong><br />
à courant nul lorsque la solution ne contient<br />
que le réducteur.<br />
• Les systèmes rapides correspondent à un<br />
faible changement de structure entre<br />
l’oxydant et le réducteur.<br />
3+<br />
• Exemples : Fe<br />
2+<br />
sur platine,<br />
Fe<br />
Ag +<br />
Ag<br />
H<br />
+<br />
aq<br />
H<br />
2<br />
sur argent,<br />
2+<br />
Zn<br />
Zn<br />
sur platine platiné.<br />
sur zinc,<br />
• L’<strong>intensité</strong> ne s’annule pas pour une valeur<br />
bien définie du <strong>potentiel</strong> E.<br />
di<br />
• ≈ 0 pour une grande plage de E (d’où<br />
dE<br />
l’appellation de système lent).<br />
Il en résulte qu’il n’est pas possible de retrouver<br />
l’expression du <strong>potentiel</strong> d’équilibre ni du<br />
<strong>potentiel</strong> standard du couple étudié à l’aide des<br />
résultats cinétiques.<br />
• On obtient un courant d’oxydation anodique<br />
détectable i 1 si E <strong>–</strong> E eq > η A, où η A est appelée<br />
surtension anodique avec η A > 0.<br />
• On obtient un courant de réduction cathodique<br />
détectable i 2 si E <strong>–</strong> E eq < η C, où η C est<br />
appelée surtension cathodique, η C < 0.<br />
• Les zones de <strong>potentiel</strong> où se produisent les<br />
réactions d’oxydation et de réduction sont disjointes.<br />
• Les systèmes lents correspondent à une<br />
profonde modification de structure entre<br />
l’oxydant et le réducteur, mais aussi à des couples<br />
à faible changement de structure sur<br />
certaines électrodes.<br />
+<br />
H aq<br />
• Exemples : sur fer ou sur mercure.<br />
H<br />
O<br />
2<br />
HO<br />
2<br />
2<br />
sur toute électrode !<br />
Remarque : Les surtensions varient essentiellement avec la nature de l’électrode. Prenons<br />
+<br />
H aq<br />
l’exemple du couple à pH = 0 pour j = 1,0 mA.cm<br />
H 2<br />
-2 .<br />
métal Pt platiné Pt poli Fe C Zn Hg<br />
ηC (V) - 0,01 - 0,10 - 0,40 - 0,50 - 0,75 - 1,40<br />
type rapide ←⎯⎯⎯⎯⎯⎯⎯⎯⎯ lent ⎯⎯⎯⎯⎯⎯⎯⎯→ très lent
2°) Cas où la vitesse de la réaction est limitée par la diffusion.<br />
Page 6/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Cherchons maintenant à analyser l’existence d’un palier pour le courant avec un phénomène<br />
de saturation (cf l’étude expérimentale précédente).<br />
En revenant aux trois phases des réactions aux électrodes, on conçoit qu’à partir du moment<br />
où le transfert des charges est rapide, le processus cinétiquement limitant correspond au<br />
déplacement de matière jusqu’à la zone voisine de l’électrode. Très généralement, ce déplacement<br />
est réalisé par diffusion.<br />
En effet, la réaction à l’électrode appauvrit la solution à son voisinage en la forme réagissante<br />
Ox ou Red.<br />
Tant que les densités de courant sont faibles, la vitesse de diffusion est suffisante et ne limite<br />
donc pas la réaction.<br />
Pour des densités de courant plus élevées, la concentration de l’espèce réagissante<br />
au niveau de l’électrode finit par quasiment s’annuler et la réaction<br />
est alors limitée par la diffusion :<br />
Le courant atteint une <strong>intensité</strong> limite, dite de diffusion. D’où l’existence<br />
d’un palier horizontal.<br />
Présence d’un seul couple rédox.<br />
−<br />
Supposons que l’électrode soit une anode. Il se produit : β Re d → αOx+<br />
ze<br />
Le courant de diffusion anodique iDa est proportionnel au coefficient de diffusion du réducteur<br />
et au gradient de concentration du réducteur entre la solution et l’électrode :<br />
i k Re d Re d i ≈ k d .<br />
= (Re ) ( [ ] − [ ] ) ⇒ (Re ) [ ] Re<br />
Da D d sol él<br />
Da D d sol<br />
Le coefficient de diffusion k D dépend de la mobilité du corps, du nombre<br />
d’électrons mis en jeu ainsi que de la géométrie de l’appareillage.<br />
De même, si l’électrode est une cathode, on aurait : i k [ Ox]<br />
≈ .<br />
Dc D( Ox) sol<br />
Les <strong>courbes</strong> <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong> complètes ont alors l’allure suivante :<br />
Cas d’un système rapide. Cas d’un système lent.<br />
Présence de plusieurs couples rédox à l’électrode.<br />
Si la solution contient plusieurs espèces susceptibles d’être oxydées ou réduites, et que le <strong>potentiel</strong><br />
imposé à l’électrode permette leur transformation, le courant qui traverse<br />
l’électrode est la somme des courants correspondants à chacune des réactions.<br />
Lorsque l’écart entre les <strong>courbes</strong> est suffisant pour que la première courbe ait atteint son palier<br />
de diffusion, on observe des sauts de courants successifs, la hauteur de chaque palier<br />
étant proportionnelle au nombre d’électrons échangés.
Les <strong>courbes</strong> I(E) ci-dessous illustrent les résultats précédents :<br />
Cas d’un système rapide.<br />
Influence des concentrations initiales où :<br />
( ) = 2 ( )<br />
⎡Fe CN ⎤ ⎡Fe CN ⎤<br />
⎣ ⎦ ⎣ ⎦<br />
4− 3−<br />
6<br />
0<br />
6<br />
0<br />
Page 7/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Cas d’un système lent.<br />
Influence du nombre d’électrons échangés.<br />
On notera par ailleurs l’absence de paliers de diffusion :<br />
• pour les couples du solvant, toujours en grand excès,<br />
• pour l’oxydation des espèces solides, seules dans leurs phases (en particulier les métaux)<br />
3°) Limitation par le solvant.<br />
Le montage à trois électrodes permet de tracer la courbe I = f(E) relative à l’eau solvant.<br />
L’eau, amphotère rédox, peut être réduite ou oxydée suivant deux couples différents:<br />
Couple et <strong>potentiel</strong> d’équilibre à<br />
pH = 7<br />
O<br />
HO 2<br />
H ou<br />
H<br />
2<br />
2<br />
2<br />
Réaction subie par<br />
l’eau :<br />
HO (E a = 0,81 V) Oxydation anodique 2 2( )<br />
+<br />
aq<br />
H<br />
2<br />
Bilan de la réaction :<br />
<br />
2HO→ O + 4H+ 4e<br />
+ −<br />
g aq<br />
2HO+ 2e→ H + 2OH<br />
− <br />
−<br />
(Ec = -0,42 V) Réduction cathodique 2 2( g )<br />
L’oxydation de l’eau est régulièrement lente. La surtension anodique observée η a est<br />
de l’ordre de 0,6 V.<br />
La surtension anodique élargit fortement le domaine du solvant, du côté<br />
des <strong>potentiel</strong>s élevés. Ainsi, de nombreuses solutions oxydantes sont apparemment<br />
stables dans l’eau.<br />
La réduction de l’eau dépend fortement de la nature du métal utilisé comme<br />
électrode. Il n’y a pas de loi générale. Il convient donc de déterminer expérimentalement<br />
la comportement d’une électrode vis-à-vis de cette réaction avant toute application.<br />
On peut différencier dans ce cas la réduction des ions oxonium de celle de l’eau :<br />
o la réduction des ions est rapide et présente de ce fait l’habituel palier de diffusion.<br />
o l’eau est toujours en grand excès et ne présente jamais ce phénomène de saturation.
Le domaine dans lequel les<br />
réactions rédox se déroulent<br />
sans que le solvant « eau »<br />
n’intervienne est appelé domaine<br />
d’électro-activité de<br />
l’eau, typiquement de largeur<br />
2 V.<br />
Ce domaine est limité par<br />
les « murs du solvant »<br />
Le graphique ci-contre montre<br />
les domaines d’électro-activité<br />
de l’eau pour différentes électrodes<br />
(ici construit à pH = 0).<br />
Page 8/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Les ions 3 HO+ jouent des rôles multiples dans les réactions d’oxydo-réduction :<br />
- ils sont consommés par la réaction chimique : ce sont des réactifs.<br />
- ils sont souvent nécessaires pour que l’affinité chimique de la réaction soit positive (ils<br />
créent donc les conditions nécessaires à la réaction d’un point de vue thermodynamique).<br />
- ils augmentent la vitesse de la réaction : c’est leur rôle du point de vue cinétique.<br />
Remarquons enfin que les réactions sont plus rapides en milieu ionisé qu’en milieu non<br />
chargé : le domaine d’électroactivité de l’eau est donc particulièrement large en<br />
milieu neutre.<br />
III : Réactions rédox spontanées (en solution ou dans une pile).<br />
1°) Réaction spontanée en solution : <strong>potentiel</strong> mixte.<br />
Notion de <strong>potentiel</strong> mixte.<br />
Les <strong>courbes</strong> de dosage par oxydo-réduction ne présentent généralement pas les formes que<br />
prévoit l’analyse et l’application des relations de Nernst, à cause de l’importance de l’aspect<br />
cinétique, en particulier au voisinage et au-delà du point équivalent.<br />
Il faut prendre en compte les <strong>courbes</strong> <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong> de deux systèmes électrochimiques<br />
pour interpréter les phénomènes.<br />
Soit deux couples rédox, l’un noté (1) subissant une réduction, l’autre, noté<br />
(2) subissant une oxydation..<br />
La vitesse des échanges électroniques entre ces deux couples rédox se visualise<br />
à partir des <strong>courbes</strong> I = f(E), en écrivant (principe de conservation<br />
de la charge) : Ianode2 =− Icathode1.<br />
Le <strong>potentiel</strong> qui assure cette relation entre les courants est appelé <strong>potentiel</strong><br />
mixte, noté Em car il met en jeu les deux couples rédox.<br />
Les figures a), b), c) et d) ci-dessous présentent les différents cas qui peuvent se présenter lorsqu’on<br />
met en présence un oxydant Ox 1 et un réducteur Red 2. Ces <strong>courbes</strong> décrivent la situation<br />
instantanée du système : elles se modifient au fur et à mesure que le système évolue.
Page 9/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
• Pour les cas a), b) et c), on a E 1 > E 2 : oxydation spontanée du réducteur 2 par l’oxydant 1.<br />
La réaction est : rapide pour a),<br />
lente pour b)<br />
infiniment lente pour c).<br />
• Pour le cas d), on a E 1 < E 2 : réaction non spontanée et I ne peut être que nulle.<br />
2°) Action d’un cation métallique sur un métal : cémentation.<br />
En, hydrométallurgie, la réduction d’un cation métallique par un métal<br />
est appelée cémentation.<br />
Remarque :<br />
La cémentation est un des plus anciens procédés électrochimiques mis en jeu en métallurgie. Elle<br />
consiste à introduire le métal en poudre très fine, pour augmenter la vitesse de réaction. Il y a dépôt des<br />
métaux réduits sur la poudre introduite, ce qui donne des céments, que l’on sépare par filtration afin de<br />
récupérer les métaux qu’ils contiennent.<br />
La cémentation est utilisée pour la récupération des métaux précieux, pour celle du cuivre, dans les<br />
solutions de lessivage des minerais pauvres ou pour la purification de solutions avant l’électrolyse (par<br />
exemple pour la préparation du zinc par voie électrochimique).<br />
Pour que la cémentation soit thermodynamiquement<br />
possible, le métal utilisé comme réducteur doit avoir un <strong>potentiel</strong><br />
standard inférieur à celui des cations métalliques.<br />
Pour que la cémentation soit cinétiquement favorable,<br />
il doit exister un <strong>potentiel</strong> mixte sur les <strong>courbes</strong> I(E) relatives<br />
aux systèmes électrochimiques en présence.<br />
Les <strong>courbes</strong> ci-contre montrent que la réaction entre Cu et<br />
les ions Ag + est rapide (elle est de plus quantitative).
3°) Action des acides sur les métaux.<br />
Action d’un acide à anion non oxydant sur le magnésium.<br />
+<br />
H<br />
2+<br />
aq<br />
Les couples rédox en présence sont : et<br />
Mg<br />
.<br />
H 2 Mg<br />
La réaction est thermodynamiquement possible (cf la règle du « γ ») :<br />
Action d’un acide à anion non oxydant sur le plomb.<br />
+<br />
H aq<br />
Les couples en présence<br />
H<br />
thermodynamiquement possible.<br />
Page 10/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
L’analyse des <strong>courbes</strong> <strong>intensité</strong> <strong>–</strong> <strong>potentiel</strong> montre qu’il existe<br />
une zone commune de <strong>potentiel</strong> où les deux demi-réactions rédox<br />
peuvent se produire simultanément.<br />
On observe une attaque du magnésium avec dégagement ga-<br />
+ 2+<br />
zeux de dihydrogène selon : Mg+ 2Haq → Mg + H<br />
.<br />
2<br />
et<br />
2+<br />
Pb<br />
Pb<br />
Action des ions oxonium sur le métal zinc.<br />
Bien que la constante d’équilibre K° de la réaction :<br />
montrent que la réaction est<br />
Mais il ne se passe rien, même avec de l’acide chlorhydrique<br />
concentré, ce qui prouve l’existence d’un<br />
blocage cinétique, dû à une forte surtension du cou-<br />
+<br />
H aq ple sur plomb et à l’absence de <strong>potentiel</strong><br />
H 2<br />
mixte comme le montre la courbe ci-contre.<br />
Si en revanche, on touche le plomb, immergé dans<br />
l’acide avec un fil de platine, on observe un dégagement<br />
gazeux de H2 sur le platine, et le plomb est attaqué.<br />
Les deux réactions sont alors :<br />
2+<br />
−<br />
Sur le plomb : Pb → Pb + 2e<br />
+ −<br />
<br />
2H + 2e<br />
→H<br />
Sur le platine : aq 2( g )<br />
de l’ordre de 10 25 , le dégagement de H 2 observé est très variable.<br />
Il est abondant avec un métal<br />
impur, il devient très faible avec<br />
du zinc pur et pratiquement nul<br />
avec du zinc amalgamé (alliage<br />
zinc <strong>–</strong> mercure).<br />
Cet exemple met en évidence<br />
le rôle des surtensions pour<br />
l’existence ou non d’un <strong>potentiel</strong><br />
mixte et le blocage cinétique qui<br />
en découle.<br />
H Zn H Zn<br />
+ 2+<br />
2 aq + → 2( g ) +<br />
H aq<br />
+ 2 H<br />
2<br />
Mg + Mg<br />
2<br />
E° (V)<br />
0<br />
E° (V)<br />
-2,4<br />
0<br />
H aq<br />
+ 2 H<br />
2<br />
Pb + Pb<br />
-0,13<br />
soit à 298 K
IV : Réactions rédox forcées : électrolyses.<br />
1°) Généralités.<br />
Prévision thermodynamique de la polarité d’une pile électrochimique.<br />
En mode de fonctionnement « générateur », l’anode constitue<br />
le pôle de la pile et la cathode le pôle ⊕, ce qui suppose<br />
d’avoir : Ecathode > Eanode. Un transfert « naturel » des charges est<br />
donc possible à condition que la « règle du<br />
gamma » soit satisfaite :<br />
Page 11/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
Dans une pile électrochimique, il y a transformation d’énergie chimique en<br />
énergie électrique. Le pôle ⊕ d’une pile est du côté du <strong>potentiel</strong> rédox le<br />
plus fort, et l’électrode correspondante constitue la cathode.<br />
L’électrolyse.<br />
C’est l’opération inverse de l’étude précédente. Un électrolyseur<br />
est constitué de deux électrodes plongeant dans une solution<br />
conductrice, reliées à un générateur électrique extérieur<br />
permettant d’imposer le sens du passage du courant.<br />
Dans une électrolyse, il y a transformation<br />
d’énergie électrique en énergie chimique. Elle<br />
n’est possible que grâce à l’énergie fournie par<br />
le générateur.<br />
En considérant que les réactions se font à température et pression constantes, l’enthalpie libre<br />
du système « électrolyseur » s’écrit : dGTP , = − A dξ .<br />
∗<br />
∗<br />
Or on a dG ≤ δWreçu<br />
, où δWreçu<br />
désigne le travail élémentaire reçu par le système, autre que<br />
∗<br />
celui des forces de pression. Dans le cas d’un électrolyseur, δW<br />
= U dq = U Idt > 0 .<br />
reçu AC AC<br />
On en déduit le signe de l’affinité de la réaction d’électrolyse : A < 0 .<br />
L’électrolyse est une transformation non naturelle.<br />
Le générateur extérieur joue le rôle de « pompe à électrons » et permet de réaliser des réactions<br />
électrochimiques aux électrodes, non naturelles compte tenu des <strong>potentiel</strong>s rédox des<br />
couples mis en présence.<br />
Les définitions de l’anode et de la cathode et les réactions qui s’y déroulent<br />
sont les mêmes que précédemment (le courant entre dans l’électrolyseur par<br />
l’anode), mais les rôles des électrodes sont inversées lors d’une électrolyse par<br />
rapport au fonctionnement en mode générateur.<br />
En mode générateur comme lors d’une électrolyse, les cations se dirigent vers la cathode<br />
tandis que les anions migrent vers l’anode.<br />
2°) Aspect thermodynamique des réactions électrochimiques.<br />
Tension seuil.<br />
Du seul point de vue thermodynamique, il existe une d.d.p. minimale U AC pour que la réaction<br />
d’électrolyse puisse se produire.<br />
Soit z la quantité de moles d’électrons mis en jeu dans la réaction d’électrolyse.<br />
Ox C<br />
Ox A<br />
E<br />
E C<br />
E A<br />
Red C<br />
Red A<br />
anode<br />
I<br />
⊕<br />
e -<br />
<br />
e -<br />
I I<br />
U AC<br />
cathode<br />
Anode A Cathode C<br />
I<br />
Cuve à<br />
électrolyse
Page 12/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
⎛∂G⎞ On a dq = z F dξ . Ainsi : dG = ⎜ ⎟dξ≤UAC<br />
z F dξ<br />
, qui conduit à U AC<br />
⎝ ∂ξ<br />
⎠<br />
ΔrG<br />
≥ .<br />
z F<br />
Pour fixer les idées, considérons que la réaction d’électrolyse a pour bilan :<br />
• à l’anode : Red2 Ox2 ze −<br />
→ + Δ rga =+ zF E2<br />
• à la cathode :<br />
−<br />
Ox1+ ze → Re d1<br />
Δ g =−zF E1<br />
On a alors Δ G =+ z ( E −E<br />
)<br />
r<br />
2 1<br />
r c<br />
F , qui conduit à : U ≥( E − E ) .<br />
AC<br />
2 1<br />
Pour qu’il y ait électrolyse, il faut que la d.d.p. U AC appliquée entre les<br />
électrodes soit supérieure ou égale à une tension seuil telle qu’une réaction<br />
électrochimique soit thermodynamiquement possible sur chacune des<br />
électrodes :<br />
V A > <strong>potentiel</strong> d’équilibre du couple dont le réducteur est oxydé à l’anode,<br />
V C < <strong>potentiel</strong> d’équilibre du couple dont l’oxydant est réduit à la cathode.<br />
Les réactions envisageables aux électrodes :<br />
1. A l’anode : 3 réactions peuvent avoir lieu :<br />
- l’oxydation des anions contenus dans la solution,<br />
- l’oxydation des molécules d’eau (H2O → O2), - l’oxydation du matériau constituant l’électrode.<br />
Le réducteur le plus facile à oxyder est celui du couple de plus bas <strong>potentiel</strong><br />
rédox.<br />
2. A la cathode : 2 réactions peuvent avoir lieu :<br />
- la réduction des cations contenus dans la solution,<br />
- la réduction des molécules d’eau (H 2O → H 2).<br />
L’oxydant le plus facile à réduire est celui du couple de plus haut <strong>potentiel</strong><br />
rédox.<br />
Ces prévisions qui s’appuient uniquement sur des considérations thermodynamiques<br />
peuvent être infirmées par l’expérience si les vitesses des réactions concurrentes sont très différentes.<br />
On observe alors des surtensions qui augmentent la tension à appliquer aux électrodes<br />
pour observer l’électrolyse.<br />
3°) Loi quantitative de Faraday.<br />
La loi de Faraday permet d’établir les bilans molaires, massiques ou énergétiques pour une<br />
électrolyse. elle découle du bilan de matière associé à la réaction d’oxydo-réduction mise en jeu.<br />
En fait, cette loi permet de calculer la quantité maximale de produits formés aux électrodes<br />
(la quantité réellement obtenue est plus faible).<br />
Supposons qu’un courant continu d’<strong>intensité</strong> constante I circule dans l’électrolyseur pendant<br />
la durée Δt. Il a été donc transféré entre l’anode et la cathode la charge Q = I.Δt, correspondant<br />
au passage de Q<br />
moles d’électrons.<br />
F<br />
Si la formation d’une mole d’un corps donné de masse molaire A à l’une des électrodes nécessite<br />
l’échange de z moles d’électrons, on pourra alors obtenir au plus N moles de ce corps avec :<br />
Q<br />
I. Δt<br />
N = , soit encore une masse formée : m= . A (c’est la loi quantitative de Faraday).<br />
z.<br />
F z.<br />
F<br />
Attention aux différentes unités employées lors des applications numériques !
Page 13/13<br />
COURBES INTENSITÉ <strong>–</strong> POTENTIEL.<br />
4°) Aspect cinétique : utilisation des <strong>courbes</strong> <strong>intensité</strong> <strong>potentiel</strong>.<br />
Les <strong>courbes</strong> <strong>intensité</strong> <strong>potentiel</strong> permettent de bien visualiser les facteurs cinétiques et thermodynamiques<br />
qui interviennent lors d’une électrolyse. Ces facteurs interviennent dans la relation<br />
entre la tension U AC et l’<strong>intensité</strong> I d’une part, et dans le choix des réactions se produisant<br />
aux électrodes d’autre part.<br />
Il convient d’avoir toujours à l’esprit que les réactions anodique et cathodique<br />
sont sous contrôle cinétique : les réactions observées ne sont pas les<br />
plus faciles thermodynamiquement, mais les plus rapides.<br />
La ddp à appliquer.<br />
La tension à appliquer aux bornes de l’électrolyseur est la somme d’un certain nombre de<br />
anode cathode<br />
UAC = Eéq − Eéq+ ηA− ηC+<br />
Rcircuit + Rcellule) . i<br />
où E anode<br />
éq et E cathode<br />
éq sont les <strong>potentiel</strong>s rédox d’équilibre des couples envisagés à l’anode et à<br />
la cathode,<br />
ηA et ηC sont les surtensions à l’anode et à la cathode,<br />
Rcircuit est la résistance totale du circuit extérieur à l’électrolyseur (fils + générateur),<br />
Rcellule est la résistance de l’électrolyseur (encore appelé cellule électrolytique).<br />
termes : ( )<br />
Ce sont les termes de surtension et de chute ohmique qui coûtent cher à la production. On<br />
<br />
cherche à obtenir une valeur de Rcellule la plus faible possible. Or, R = ρ . Il faut donc trouver<br />
S<br />
des électrolytes dont la résistivité est faible, des électrodes de grande surface et de faible écart.<br />
5°) Applications industrielles de l’électrolyse.<br />
Production de l’aluminium, préparé par réduction cathodique d’un mélange d’alumine<br />
(A2O3) et de cryolite fondue.<br />
Production du zinc (par hydrométallurgie à partir de solutions aqueuses d’ions Zn 2+ ).<br />
Raffinage électrolytique des métaux (pour obtenir des puretés > 99,90 %).<br />
Placage de métaux (argenture, chromage, électrozingage, nickelage, …<br />
Préparation du dichlore par électrolyse d’une solution aqueuse de NaC,<br />
Préparation du sodium par électrolyse du chlorure de sodium fondu.