A) = B) =
A) = B) =
A) = B) =
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Avogadron laki: Samassa lämpötilassa ja paineessa yhtä suurettilavuudet eri kaasua sisältävät yhtä monta molekyyliä ja siis yhtämonta moolia kaasua.1 mooli kaasua:- sisältää Avogadron vakion verran kaasun molekyylejä(tai atomeja) 6,0221367 ∙ 10 1/. (MAOL s. 70 (71)).- on molekyylipainon (atomipainon) osoittamagrammamäärä ainetta- vie tilavuuden V m = 22,41410∙10 -3 m 3 /mol (Ideaalikaasunmoolitilavuus NTP-tilassa), V m ≈ 22,414 dm 3 /mol.(MAOL s. 70 (71)).Ainemäärä n voidaan laskea eri tavoin:1) 2) 3) n = ainemäärä (mol) n = ainemäärä (mol) n = ainemäärä (mol)m = massa (g) V = tilavuus (dm 3 ) N = hiukkasmääräM = moolimassa (g/mol) Vm = ideaalikaasun NA = Avogadron vakiomoolitilavuus 6,0221367 ∙ 10 1/Vm = 22,41410∙10 -3 m 3 /mol (MAOL s. 70 (71))(MAOL s. 70 (71))Kaasun tiheys: = (NTP) [ks. MAOL s. 70 (71), 138-139 (130-131)]¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤¤Kineettisen kaasuteorian perusoletukset ideaalikaasulleKineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka onmatemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasukäyttäytyy ideaalikaasun tavoin, kun lämpötila on korkea ja paine alhainen.Huoneenlämpötilassa ja –paineessa useimmat reaalikaasuja (esim. ilma) voidaantarkastella ideaalikaasuina.
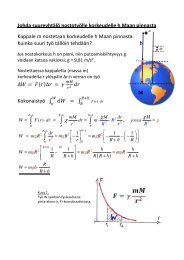
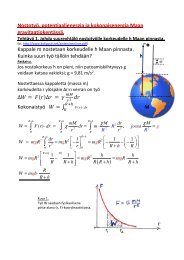
Tehtävien ratkaisut:1) 2,0 1,0 3,0 8,0 273,15 281,15 ? 35 273,15 308,15 Oletus: renkaan tilavuus V ei muutu: V 1 = V 2 = V on vakio ∣: V ∣∙ T2 , ∙ , , 3,29 3,3 absoluuttinen paineMittari näyttää ylipainetta ilmanpaineeseen nähden, jotenpainemittarin lukema on 3,3 bar – 1,0 bar 2,3 bar.Vastaus: Renkaan paine on 3,3 bar ja mittarin lukema on 2,3 bar.2) Veden tiheys on 1000 kg/m 3 .Olosuhteet 25 metrin syvyydellä ovat: 6,0 273,15 279,15 5,0 101325 1000 ∙ 9,81 ∙ 25 346 575 . Olosuhteet pinnassa ovat: 13 273,15 286,15 101325 . ?Ideaalikaasun tilanyhtälön mukaan josta saadaan kuplan tilavuus 17,53 18 . ∣∙ ∙ , ∙. ∙ , Vastaus: Kaasukuplan tilavuus veden pinnalla on 18 mm 3 .
3) Pullossa olevan heliumin massa m = 3,0 gTilavuus V = 14 dm 3Lämpötila 15 + 273,15 = 288,15 .Helium on yksiatominen jalokaasu, jonka suhteellinen atomimassaon 4,00.Heliumin moolimassa = 4,0 /Pallossa olevan heliumkaasun ainemäärä = = , = 0,75 =?,Ideaalikaasun tilanyhtälön mukaan = , josta saadaanpaineelle lauseke = =, ∙ , ∙ ∙ ∙, ≈ 1,283 = 1,3 = 1,3 ∙ 10 = 0,13 Vastaus: Vappupallon sisällä oleva paine on 0,13 MPa.4) a) Ilma noudattaa kaasujen tilanyhtälöä .Ilman ainemäärä on ja molekyylien lukumäärä on ∙ = ∙ = ∙ = ∙ = ,∙ ∙ ,∙ ∙ ,∙ ,∙ ∙ ,≈ 2,6867626 ∙ 10 .Vastaus: 2,68∙1019 molekyyliä.