- Page 1 and 2:
MANUAL DE ENSAYO DE MATERIALES Edic
- Page 3 and 4:
SECCION N° 2 AGREGADOS ...........
- Page 5 and 6:
MTC E 606 TIEMPO DE FRAGUADO DEL CE
- Page 7 and 8:
MTC E 1235 DETERMINACION DE LA RESI
- Page 9 and 10:
GENERALIDADES 1 Organización del M
- Page 11 and 12:
1.4 GLOSARIO DE TERMINOS La definic
- Page 13 and 14:
SECADOR: Aparato que seca los agreg
- Page 15 and 16:
MTC E 101 MUESTREO DE SUELOS Y ROCA
- Page 17 and 18:
· Módulo Resiliente sobre muestra
- Page 19 and 20:
esistividad eléctrica, pueden resu
- Page 21 and 22:
MTC E 102 MUESTREO POR PERFORACION
- Page 23 and 24:
Alíviese el “muestreador” carg
- Page 25 and 26:
Tamaño Máximo de Muestra 4.2 METO
- Page 27 and 28:
6.0 PROCEDIMIENTO 6.1 METODO A: CUA
- Page 29 and 30:
MTC E 104 CONSERVACION Y TRANSPORTE
- Page 31 and 32:
Tabla 1 Diámetro nominal de las pa
- Page 33 and 34:
6.5 Grupo D · Deberán cumplir los
- Page 35 and 36:
Figura 3. Barriles metálicos para
- Page 37 and 38:
MTC E 105 OBTENCION EN LABORATORIO
- Page 39 and 40:
APENDICE A CUARTEADORES O DIVISORES
- Page 41 and 42:
Figura 3: Cuarteo sobre lona. Manua
- Page 43 and 44:
5.2.2 Determinación de las constan
- Page 45 and 46:
MTC E 107 ANALISIS GRANULOMETRICO D
- Page 47 and 48:
TAMICES ABERTURA (mm) 3” 75,000 2
- Page 49 and 50:
Las pequeñas diferencias resultant
- Page 51 and 52:
5.0 MUESTRA 5.1 Las muestras serán
- Page 53 and 54:
Nota 7. En la mayoría de los casos
- Page 55 and 56:
MTC E 109 ANALISIS GRANULOMETRICO P
- Page 57 and 58:
temperatura. La temperatura normal
- Page 59 and 60:
Lectura del hidrómetro * R’ + Cm
- Page 61 and 62:
6.0 PROCEDIMIENTO El procedimiento
- Page 63 and 64:
Tabla 2 Valores de Ct para la corre
- Page 65 and 66:
Porcentaje más fino = Gs Gs - 1 10
- Page 67 and 68:
Tabla 4 Valores del coeficiente de
- Page 69 and 70:
4.1.5 Calibrador. Ya sea incorporad
- Page 71 and 72:
la misma forma. Si una burbuja hubi
- Page 73 and 74:
MTC E 111 DETERMINACION DEL LIMITE
- Page 75 and 76:
8.0 PRECISION Y DISPERSION 8.1 PREC
- Page 77 and 78:
4.2.4 Placa de vidrio, con tres pat
- Page 79 and 80:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 81 and 82:
MTC E 113 METODO DE ENSAYO ESTENDAR
- Page 83 and 84:
4.1.6 Contenedor aislado - Un refri
- Page 85 and 86:
V P ( M - M ) pw, c p = (1) r w, c
- Page 87 and 88:
Nota 5. Para algunos suelos conteni
- Page 89 and 90:
partículas, calcule un peso espec
- Page 91 and 92:
TABLA 4 Sumario de los resultados d
- Page 93 and 94:
2.7.3 Después de remojar, permita
- Page 95 and 96:
. Desmenuzar cualquier grumo de mat
- Page 97 and 98:
6.2.8.2 Método del agitador manual
- Page 99 and 100:
ocho resultados de pruebas pareadas
- Page 101 and 102:
Figura 1A - Dispositivo de pie pesa
- Page 103 and 104:
Figura 5 - Transferencia de muestra
- Page 105 and 106:
º Figura 9 - Lectura de arena Manu
- Page 107 and 108:
2.3.2.6 Otros Usos: Si el método n
- Page 109 and 110:
(¾ ± 1 / 16 pulg) y espaciados a
- Page 111 and 112:
Mezclar el suelo continuamente dura
- Page 113 and 114:
Nota 9. La curva de 100% de saturac
- Page 115 and 116:
ANEXO (INFORMACION OBLIGATORIA) A1.
- Page 117 and 118:
Tabla 2 Equivalencia métricas para
- Page 119 and 120:
Figura 3. Ejemplo de Gráfico de Cu
- Page 121 and 122:
2.3.2.5 Usos: Cuando más del 20% d
- Page 123 and 124:
4.2.2 Pisón Mecánico Circular.- E
- Page 125 and 126:
especificado en 6.1.2.3 de este ens
- Page 127 and 128:
error en la gravedad específica, e
- Page 129 and 130:
ANEXO A (INFORMACION OBLIGATORIA) A
- Page 131 and 132:
Tabla 2 Equivalencia métricas para
- Page 133 and 134:
Figura 3: Ejemplo de Gráfico de Cu
- Page 135 and 136:
humedad. Cualquier prueba de densid
- Page 137 and 138:
6.1.3 Coloque el plato de base sobr
- Page 139 and 140:
E 116, ASTM D 4253 ó ASTM D 4254.
- Page 141 and 142:
A1.2.4.2 A1.2.4.3 Determine la masa
- Page 143 and 144:
Figura 1. Aparato de densidad Manua
- Page 145 and 146:
6.2 Escoger una muestra de peso apr
- Page 147 and 148:
Figura 1: Definiciones del número
- Page 149 and 150:
6.1.2.1 Método de perforación por
- Page 151 and 152:
ecipiente para prevenir la evaporac
- Page 153 and 154:
Figura 1. Tubo de pared delgada par
- Page 155 and 156:
ANEXO 1 Tabla 1 Tubos de acero de p
- Page 157 and 158:
4.1.6 Balanzas que den el peso de l
- Page 159 and 160:
En muchos casos, puede ser convenie
- Page 161 and 162:
deformación, el que ocurra primero
- Page 163 and 164:
MTC E 122 CORTE EN SUELOS COHESIVOS
- Page 165 and 166:
6.0 PROCEDIMIENTO 6.1 En el caso do
- Page 167 and 168:
Donde: d = diámetro de la varilla,
- Page 169 and 170:
· Liberación de los marcos que so
- Page 171 and 172:
El equipo con control de deformacio
- Page 173 and 174:
en estudio. Para muestras inalterad
- Page 175 and 176:
Figura 3: Definición de la resiste
- Page 177 and 178:
libra dentro de una sola norma. Est
- Page 179 and 180:
6.0 PROCEDIMIENTO 6.1 PROCEDIMIENTO
- Page 181 and 182:
7.1.1.2 Si el contenido de humedad
- Page 183 and 184:
MTC E 125 HUMEDAD DEL SUELO EN EL T
- Page 185 and 186:
4.1.1 Fuente de neutrones rápidos.
- Page 187 and 188:
e) Establézcase uno nuevo Nº calc
- Page 189 and 190:
MTC E 126 CONTENIDO DE HUMEDAD EN S
- Page 191 and 192:
6.2 Con el vaso de presión en una
- Page 193 and 194:
MTC E 127 MUESTREO DE SUELOS INALTE
- Page 195 and 196:
6.3.5 Tanto la superficie superior
- Page 197 and 198:
MUESTRAS CILINDRICAS En suelos blan
- Page 199 and 200:
1. Se taladran agujeros en el fondo
- Page 201 and 202:
7.0 CALCULOS E INFORME 7.1 INFORME
- Page 203 and 204:
2.3 Los valores del módulo resilie
- Page 205 and 206:
abrazaderas. Las abrazaderas y los
- Page 207 and 208:
egulador de burbujas, dilatador de
- Page 209 and 210:
· Determínese la humedad w1, seca
- Page 211 and 212:
Figura 7. Módulo resiliente para s
- Page 213 and 214:
3. Úsense los datos así obtenidos
- Page 215 and 216:
14. Determínese el peso del espéc
- Page 217 and 218:
laboratorio, éstos se pueden compa
- Page 219 and 220:
haya obtenido un registro del puent
- Page 221 and 222:
9. Con el esfuerzo desviador en 14
- Page 223 and 224:
· Observaciones: anótense condici
- Page 225 and 226:
5.0 MUESTRA 5.1 Dejar la muestra se
- Page 227 and 228:
Figura 1: Piezómetro abierto tipo
- Page 229 and 230:
6.1.1.1 Piezómetros de pozo abiert
- Page 231 and 232:
empleado para la limpieza deberá p
- Page 233 and 234:
6.1.2.4 Fórmese una capa de 25,4 m
- Page 235 and 236:
c) Alargamiento de las guías horiz
- Page 237 and 238:
electrónica para medir las cargas
- Page 239 and 240:
deberá ser igual al de la probeta.
- Page 241 and 242:
6.2 METODO DEL ESFUERZO TOTAL NO CO
- Page 243 and 244:
Figura 3A. Aparato para el ensayo t
- Page 245 and 246:
7.1.2 Calcúlese la deformación ax
- Page 247 and 248:
7.3.5 Utilícese el valor de (s 1 -
- Page 249 and 250:
MTC E 132 CBR DE SUELOS (LABORATORI
- Page 251 and 252:
4.1.5 Aparato medidor de expansión
- Page 253 and 254:
se ensaya, la aproximación quedar
- Page 255 and 256:
Penetración Milímetros Pulgadas 0
- Page 257 and 258:
Figura 3: Curva para cálculo de í
- Page 259 and 260:
· También se pueden usar otros ga
- Page 261 and 262:
espesor de 3 a 6 mm (0,12 a 0,24"),
- Page 263 and 264:
MTC E 134 DETERMINACION DE MATERIA
- Page 265 and 266:
7.1.3 Es ampliamente aceptado que l
- Page 267 and 268:
4.1.3 Diámetro mínimo del espéci
- Page 269 and 270:
5.3 DETERMINACION DE LAS PROPIEDADE
- Page 271 and 272:
M Tf = la masa seca total del espé
- Page 273 and 274:
7.2.2.3 La deformación al 100% de
- Page 275 and 276:
7.4.4.2 Graficar la curva de relaci
- Page 277 and 278:
Figura 2: Curva Tiempo-Deformación
- Page 279 and 280:
MTC E 136 DETERMINACION DEL VALOR D
- Page 281 and 282:
Figura 3: Molde 4.1.5 Guía metáli
- Page 283 and 284:
Figura 6: Dispositivo para presión
- Page 285 and 286:
de modo que el papel de filtro qued
- Page 287 and 288:
6.2.2.5 Determínese la resistencia
- Page 289 and 290:
los apartados aplicables de este en
- Page 291 and 292:
Tabla 2 Resumen de resultados de la
- Page 293 and 294:
MTC E 201 MUESTREO PARA MATERIALES
- Page 295 and 296:
Nota 4. Una guía para determinar e
- Page 297 and 298:
se describe en los apartados aplica
- Page 299 and 300:
MTC E 203 PESO UNITARIO Y VACIOS DE
- Page 301 and 302:
Donde: M = Peso unitario del agrega
- Page 303 and 304:
Tabla 3 Densidad del agua Temperatu
- Page 305 and 306:
Tabla 1 Cantidad mínima de muestra
- Page 307 and 308:
7.1.2 Cuando sea requerido, calcula
- Page 309 and 310:
Tabla 3 Precisión para muestras de
- Page 311 and 312:
5.2 Colocar el agregado fino obteni
- Page 313 and 314:
MTC E 206 PESO ESPECIFICO Y ABSORCI
- Page 315 and 316:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 317 and 318:
Nota 2. Es preferible el uso de una
- Page 319 and 320:
Figura 1. Máquina de ensayo de abr
- Page 321 and 322:
ANEXO B (INFORMATIVO) B.1 La pesta
- Page 323 and 324:
Tabla 1 Gradación de las muestras
- Page 325 and 326:
Figura 1. Molde cilíndrico 4.1.4 C
- Page 327 and 328:
aplicando 10 golpes de varilla por
- Page 329 and 330:
Figura 2: Nomograma para determinar
- Page 331 and 332:
4.1.4 Balanzas. Se usará una balan
- Page 333 and 334:
5.4.2 Agregado grueso. Se lava y se
- Page 335 and 336:
7.2.1.6 Clase de solución (Sulfato
- Page 338 and 339:
ANEXO A ENSAYO DE INALTERABILIDAD D
- Page 340 and 341:
5.0 MUESTRA 5.1 Muestrear el agrega
- Page 342 and 343:
Donde: P = F = N = porcentaje de pa
- Page 344 and 345:
Figura: 7 Partículas no Fracturada
- Page 346 and 347:
(preferentemente del tipo tiro desc
- Page 348 and 349:
MTC E 212. ARCILLA EN TERRONES Y PA
- Page 350 and 351:
P = [(M - R) / M] x 100 Donde: P M
- Page 352 and 353:
6.1.2 Adicione la solución de hidr
- Page 354 and 355:
Figura: 1 Vaso Mecánico de lavado
- Page 356 and 357:
las partículas. Los métodos de se
- Page 358 and 359:
a) Si cada uno de los tamaños de a
- Page 360 and 361:
lavado caiga en el mismo recipiente
- Page 362 and 363:
Altura de Altura de Altura de Altur
- Page 364 and 365:
TABLA 1 Tamaño de la muestra de ag
- Page 366 and 367:
MTC E 216. ANALISIS GRANULOMETRICO
- Page 368 and 369:
MTC E 217. DETERMINACION DE LA REAC
- Page 370 and 371:
progresivamente, hasta que todo el
- Page 372 and 373:
agua hasta el aforo y mezclar compl
- Page 374 and 375:
MTC E 218 DETERMINACION CUANTITATIV
- Page 376 and 377:
Si el tamaño máximo es de: mm Tab
- Page 378 and 379:
y a distancia para prevenir cualqui
- Page 380 and 381:
MTC E 219 SALES SOLUBLES EN AGREGAD
- Page 382 and 383:
MTC E 220 ADHESIVIDAD DE LOS LIGANT
- Page 384 and 385:
Nota 2. Es la viscosidad del ligant
- Page 386 and 387:
MTC E 221 INDICE DE APLANAMIENTO Y
- Page 388 and 389:
Tabla 1 Dimensiones de los calibrad
- Page 390 and 391:
7.2.1 Los resultados obtenidos medi
- Page 392 and 393:
7.1.1 Determinando el peso del agre
- Page 394 and 395:
Tamaño máximo nominal malla cuadr
- Page 396 and 397:
Figura 2: Uso de calibrador proporc
- Page 398 and 399:
MTC E 301 MUESTREO DE MATERIALES BI
- Page 400 and 401:
Figura 1. Válvula tomamuestras ·
- Page 402 and 403:
por cualquiera de los procedimiento
- Page 404 and 405:
Número de envases del cargamento N
- Page 406 and 407:
MTC E 302 SOLUBILIDAD DE MATERIALES
- Page 408 and 409:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 410 and 411:
pequeña esfera metálica sobre la
- Page 412 and 413:
Milímetros Pulgadas A 100 4 Nomina
- Page 414 and 415:
la parte exterior del aparato, vac
- Page 416 and 417:
MTC E 304 PENETRACION DE LOS MATERI
- Page 418 and 419:
con el método E-77. Un dispositivo
- Page 420 and 421:
8.1.1 Repetibilidad. Los ensayos po
- Page 422 and 423:
adecuados. Un parante ú otro apoyo
- Page 424 and 425:
MTC E 306 DUCTILIDAD DE LOS MATERIA
- Page 426 and 427:
5.3 Prueba - Ajuste los anillos de
- Page 428 and 429:
MTC E 307 PUNTO DE ABLANDAMIENTO DE
- Page 430 and 431:
alrededor de ellos, pero sin tocar
- Page 432 and 433:
7.1.4 Para convertir puntos de abla
- Page 434 and 435:
Figura 1. Viscosímetro de vacío c
- Page 436 and 437:
todas las uniones de vidrio deben s
- Page 438 and 439:
7.2 INFORME 7.2.1 Reportar la visco
- Page 440 and 441:
4.1.3 Un tubo en forma de pipeta, d
- Page 442 and 443:
Figura 3. Tubo en forma de pipeta p
- Page 444 and 445:
4.2.6 Llénese el baño hasta una c
- Page 446 and 447:
temperatura del baño debe ajustars
- Page 448 and 449:
ecomendable la práctica de sumergi
- Page 450 and 451:
Donde: 7.2 INFORME C = Constante de
- Page 452 and 453:
Figura 1. Viscosímetro de flujo in
- Page 454 and 455:
Figura 3. Viscosímetro BS/IP/RF de
- Page 456 and 457:
· Colocar el viscosímetro Zeitfuc
- Page 458 and 459:
é F = ê4 × V × êë ( r ) ù f
- Page 460 and 461:
Figura 1. Mecanismo de Flexión 4.1
- Page 462 and 463:
Figura 2. Conjunto del Aparato Nota
- Page 464 and 465:
MTC E 312 PUNTO DE INFLAMACION MEDI
- Page 466 and 467:
8.0 PRECISION Y DISPERSION 8.1 PREC
- Page 468 and 469:
Figura 1. Equipo para ensayo de Pun
- Page 470 and 471:
MTC E 313 DESTILACION DE ASFALTOS L
- Page 472 and 473:
Figura 3. Montaje del aparato de de
- Page 474 and 475:
6.2.6 Si el exceso de espuma persis
- Page 476 and 477:
MTC E 314 ENSAYO DE LA MANCHA (OLIE
- Page 478 and 479:
estar ejecutada solamente en el res
- Page 480 and 481:
MTC E 315 EFECTO DEL CALOR Y AIRE E
- Page 482 and 483:
pesar con aproximación de 0,001 g
- Page 484 and 485:
MTC E 316 EFECTO DEL CALOR Y AIRE E
- Page 486 and 487:
Nota 1. El Sílica Gel activo trata
- Page 488 and 489:
6.1.1 Ponga el orificio por donde s
- Page 490 and 491:
7.0 CALCULOS E INFORME 7.1 Reportar
- Page 492 and 493:
interferirse el movimiento de la ba
- Page 494 and 495:
4.1.3 Termómetros, Calibrados, de
- Page 496 and 497:
7.2 INFORME 7.2.1 Reportar la densi
- Page 498 and 499:
Figura 1. Esquema del recipiente pa
- Page 500 and 501:
MTC E 320 RECUPERACION ELASTICA POR
- Page 502 and 503:
Figura 2. Esquema del dispositivo p
- Page 504 and 505:
MTC E 401 DESTILACION DE EMULSIONES
- Page 506 and 507:
5.0 MUESTRA Antes de realizar las p
- Page 508 and 509:
MTC E 402 AGUA EN EMULSIONES ASFALT
- Page 510 and 511:
5.0 MUESTRA La muestra de laborator
- Page 512 and 513:
MTC E 403 VISCOSIDAD SAYBOLT DE EMU
- Page 514 and 515:
6.1.4 Se agita la muestra con un te
- Page 516 and 517:
6.2 Ensayo a 50 ºC. 6.2.1 Se agita
- Page 518 and 519:
6.2 Después de sacar las muestras
- Page 520 and 521:
5.3 Los asfaltos emulsionados con r
- Page 522 and 523:
MTC E 406 DEMULSIBILIDAD DE LAS EMU
- Page 524 and 525:
MTC E 407 CARGA DE LAS PARTICULAS D
- Page 526 and 527:
MTC E 408 Ph DE LAS EMULSIONES ASFA
- Page 528 and 529:
MTC E 409 CUBRIMIENTO Y RESISTENCIA
- Page 530 and 531:
Figura 2. 4.3 INSUMOS 4.3.1 Agregad
- Page 532 and 533:
MTC E 410 ESTABILIDAD DE LAS EMULSI
- Page 534 and 535:
MTC E 411 RESIDUO POR EVAPORACION D
- Page 536 and 537:
Residuo por evaporación % en peso
- Page 538 and 539:
6.0 PROCEDIMIENTO 6.1 Se pesan 465
- Page 540 and 541:
aunque no afecta de manera importan
- Page 542 and 543:
MTC E 414 ADHESIVIDAD Y COHESIVIDAD
- Page 544 and 545:
6.2 Preparación de las placas para
- Page 546 and 547:
Figura 2. Dispositivo para el ensay
- Page 548 and 549:
MTC E 415 COEFICIENTE DE EMULSIBILI
- Page 550 and 551:
MTC E 416 CONSISTENCIA CON EL CONO
- Page 552 and 553:
Figura 2. Representación gráfica
- Page 554 and 555:
5.0 MUESTRA 5.1 La proporción adec
- Page 556 and 557:
Figura (04) Figura (05) Manual de E
- Page 558 and 559:
ser también empleado como una supe
- Page 560 and 561:
· Espátula o cuchara. Espátula o
- Page 562 and 563:
iqueta a la rueda y el desprendimie
- Page 564 and 565:
Figura 1: Cohesiómetro de ensayo (
- Page 566 and 567:
Nota 1. En ciertas ocasiones la pru
- Page 568 and 569:
SECCION N° 5 MEZCLAS BITUMINOSAS M
- Page 570 and 571:
6.0 PROCEDIMIENTO 6.1 TOMA DE MUEST
- Page 572 and 573:
MTC E 502 EXTRACCION CUANTITATIVA D
- Page 574 and 575:
5.3.1 Determine el contenido de hum
- Page 576 and 577:
solución carbonato de amonio satur
- Page 578 and 579:
Figura 2. Equipo extractor (método
- Page 580 and 581:
Nota 8. Esta declaración de precis
- Page 582 and 583:
MTC E 503 ANALISIS MECANICO DE LOS
- Page 584 and 585:
Porcentaje total de material pasant
- Page 586 and 587:
planta y la efectuada en laboratori
- Page 588 and 589:
4.2.5 Baño de Agua (precisión de
- Page 590 and 591:
Figura 4. Máquina de Carga a Compr
- Page 592 and 593:
precalculada de 50% en peso del sol
- Page 594 and 595:
7.2.5 Tipo de martillo (sostenido m
- Page 596 and 597:
MTC E 505 PORCENTAJE DE VACIOS DE A
- Page 598 and 599:
MTC E 506 GRAVEDAD ESPECIFICA APARE
- Page 600 and 601:
6.3.5.1 Determine la gravedad espec
- Page 602 and 603:
MTC E 507 ESPESOR O ALTURA DE ESPEC
- Page 604 and 605:
7.2 INFORME 7.2.1 Informar el espes
- Page 606 and 607:
mientras se halla bajo vacío y par
- Page 608 and 609:
Permítase que algo del agua rebose
- Page 610 and 611:
establecerse promediando al menos 5
- Page 612 and 613:
A = Peso de la muestra seca al aire
- Page 614 and 615:
9.0 PRECISION Y DISPERSION 9.1 PREC
- Page 616 and 617:
MTC E 509 DETERMINACION DEL GRADO D
- Page 618 and 619:
APENDICE A OBTENCION DE UNA MUESTRA
- Page 620 and 621:
MTC E 510 DENSIDAD DEL HORMIGON BIT
- Page 622 and 623:
- Cuando se mide la densidad de una
- Page 624 and 625:
utilizando la hipótesis de que σ
- Page 626 and 627:
que se encuentra en la muestra (seg
- Page 628 and 629:
ANEXOS (Información no obligatoria
- Page 630 and 631:
MTC E 512 HUMEDAD O DESTILADOS VOLA
- Page 632 and 633:
Figura 2. Trampa (Tipo B) Figura 3.
- Page 634 and 635:
Figura 6. Ensamblaje típico con al
- Page 636 and 637:
7.2 INFORME 7.2.1 Reportar el conte
- Page 638 and 639:
2,5 mm por lo menos (0,1 pulg)/min
- Page 640 and 641:
es 3 a 5 ºC sobre la temperatura c
- Page 642 and 643:
hallado esta 372 kPa (ver Nota 3).
- Page 644 and 645:
5.7 Si se desea, los especímenes p
- Page 646 and 647:
MTC E 515 CARACTERIZACION DE LAS ME
- Page 648 and 649:
MTC E 516 PERMEABILIDAD IN SITU DE
- Page 650 and 651:
Tamaño máximo, mm 10 - 12 % pasa
- Page 652 and 653:
como lo descrito en el método para
- Page 654 and 655:
Nota 7. En caso que el bitumen este
- Page 656 and 657:
usado con mezclas diseñadas por ot
- Page 658 and 659:
MTC E 519 GRADO ESTIMADO DE CUBRIMI
- Page 660 and 661:
MTC E 520 ADHERENCIA EN BANDEJA 1.0
- Page 662 and 663:
es expuesto a un suministro de calo
- Page 664 and 665:
4.1.10 Segmentos de carga de acero
- Page 666 and 667:
V a P × E = a 100 Donde: V a P a E
- Page 668 and 669:
Razón del Esfuerzo a Tensión (TSR
- Page 670 and 671:
MTC E 601 MUESTREO Y ACEPTACION DEL
- Page 672 and 673:
· Número de lote y/o orden de tom
- Page 674 and 675:
4.1.2 Horno Mufla con temperatura m
- Page 676 and 677:
6.2 DIOXIDO DE SILICIO 6.2.1 Cement
- Page 678 and 679:
ojo a naranja, añadir 1 ó 2 gotas
- Page 680 and 681:
valorada de NaOH 1N, usando fenolta
- Page 682 and 683:
Buffer (pH 4,7) - 68 g de NaC 2H 3O
- Page 684 and 685:
Procedimiento: 6.8.1 Acidificar los
- Page 686 and 687:
Nota 16. Extremo cuidado debe ser e
- Page 688 and 689:
contenido del frasco a temperatura
- Page 690 and 691:
0,658 = proporción molecular de Na
- Page 692 and 693:
N = 0,25 / V Donde: N = normalidad
- Page 694 and 695:
inmediatamente añadir 185 mL de HC
- Page 696 and 697:
6.16.2 Transferir el precipitado y
- Page 698 and 699:
Tabla 1: (66 de 89 de la NTP). Cont
- Page 700 and 701:
4.1.4 Comparador de longitudes. El
- Page 702 and 703:
alrededor de los topes de medida. L
- Page 704 and 705:
MTC E 605 CONSISTENCIA NORMAL DEL C
- Page 706 and 707:
Figura 1: Equipo de Vicat El Equipo
- Page 708 and 709:
5.4 Encender la mezcladora y mezcla
- Page 710 and 711:
MTC E 607 FRAGUA DEL CEMENTO HIDRÁ
- Page 712 and 713:
7.0 CALCULOS E INFORME 7.1 INFORME
- Page 714 and 715:
Largo 50,0 mm ± 0,8 mm (2” ± 0,
- Page 716 and 717:
iguales a los valores h dados en la
- Page 718 and 719:
Tabla 1 Valores de h, d y h/d 2 emp
- Page 720 and 721:
cuidado en usar solamente kerosene
- Page 722 and 723:
= Porcentaje corregido en peso que
- Page 724 and 725:
APENDICE 1.0 INDICACIONES COMPLEMEN
- Page 726 and 727:
Tabla 1 Variaciones permisibles de
- Page 728 and 729:
5.0 MUESTRA 5.1 Preparación de los
- Page 730 and 731:
MTC E 610 DENSIDAD DEL CEMENTO PORT
- Page 732 and 733:
Figura 1: Frasco de Le Chatelier Ma
- Page 734 and 735:
Figura1: Paleta mezcladora Figura 2
- Page 736 and 737:
MTC E 612 CONTENIDO DE AIRE EN MORT
- Page 738 and 739:
Utilizando la cuchara, depositar su
- Page 740 and 741:
MTC E 613 FINURA DEL CEMENTO PORTLA
- Page 742 and 743:
4.2 MATERIALES 4.2.1 Papel de filtr
- Page 744 and 745:
llegue a la segunda marca la que si
- Page 746 and 747:
7.1.2 Para calcular los valores de
- Page 748 and 749:
4.0 EQUIPOS, MATERIALES E INSUMOS 4
- Page 750 and 751:
MTC E 615 RESISTENCIA A LA TENSIÓN
- Page 752 and 753:
Figura 3: Muestras para ensayo El p
- Page 754 and 755:
Si es necesario demorar la prueba,
- Page 756 and 757:
La leva y el árbol (figuras 2b y 2
- Page 758 and 759:
4.2.3 Guantes de jebe. 4.3 INSUMOS
- Page 760 and 761:
MTC E 617 RESISTENCIA A LA FLEXIÓN
- Page 762 and 763:
Figura 2: Guía del compactador 5.0
- Page 764 and 765:
Figura 3: Dispositivos especiales p
- Page 766 and 767:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 768 and 769:
MTC E 701 TOMA DE MUESTRAS DE CONCR
- Page 770 and 771:
Se debe tener especial cuidado de n
- Page 772 and 773:
MTC E 702 ELABORACION Y CURADO DE E
- Page 774 and 775:
4.1.6.2 Vibradores externos - Puede
- Page 776 and 777:
Los aditivos que son incompatibles
- Page 778 and 779:
Se adicionan el agua y el aditivo s
- Page 780 and 781:
muestra. Para moldes de ancho mayor
- Page 782 and 783:
MTC E 703 REFRENTADO DE CILINDROS D
- Page 784 and 785:
4.2.1.2 La desviación normal de la
- Page 786 and 787:
Nota 3. Las pastas frescas tienden
- Page 788 and 789:
la placa de refrentado, golpeando s
- Page 790 and 791:
6.2.4.1 Precaución: Se pueden prod
- Page 792 and 793:
4.1.1.2 Diseño - La máquina debe
- Page 794 and 795:
) El centro de la rótula debe coin
- Page 796 and 797:
Cuando no se requiera determinar la
- Page 798 and 799:
Donde: W = masa de la muestra, kg (
- Page 800 and 801:
Los cilindros que no cumplan con es
- Page 802 and 803:
esistencia. A opción del fabricant
- Page 804 and 805:
Un tercio del volumen del molde cor
- Page 806 and 807:
MTC E 706 CONTENIDO DE AIRE EN EL C
- Page 808 and 809:
La cubierta debe tener un dispositi
- Page 810 and 811:
Donde: P 1 = presión inferior de e
- Page 812 and 813:
APÉNDICE: CALIBRACIÓN DE APARATOS
- Page 814 and 815: cuidadosamente la tapa. Después co
- Page 816 and 817: MTC E 707 TOMA DE NUCLEOS Y VIGAS E
- Page 818 and 819: a las alcanzadas por inmersión por
- Page 820 and 821: Nota 4. En muchos casos, particular
- Page 822 and 823: Los núcleos deberán cumplir con e
- Page 824 and 825: 7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 826 and 827: o con el centro de la esfera en el
- Page 828 and 829: d = altura promedio de la muestra m
- Page 830 and 831: MTC E 711 RESISTENCIA A LA FLEXION
- Page 832 and 833: = 2Sbd² 3L Donde: r = rata de carg
- Page 834 and 835: MTC E 712 MEDIDA DE LA LONGITUD DE
- Page 836 and 837: MTC E 713 EXUDACION DEL CONCRETO 1.
- Page 838 and 839: Figura 2. Detalles del equipo del e
- Page 840 and 841: 6.7 Para determinar la masa del agu
- Page 842 and 843: MTC E 714 PESO UNITARIO DE PRODUCCI
- Page 844 and 845: 4.1.6 Equipo de calibración - Se r
- Page 846 and 847: 7.1.1.3 Contenido de cemento - Se c
- Page 848 and 849: 4.0 EQUIPOS Y MATERIALES 4.1 EQUIPO
- Page 850 and 851: instrumentado cuyo diámetro sea ig
- Page 852 and 853: E = módulo elástico instantáneo
- Page 854 and 855: 13.2.1 El total de residuo sólido
- Page 856 and 857: diluyen a 1 litro. Esta solución d
- Page 858 and 859: 4.3.1 Se emplearán como reactivos
- Page 860 and 861: MTC E 719 CONCENTRACION DEL ION SUL
- Page 862 and 863: La constancia de masa se determina
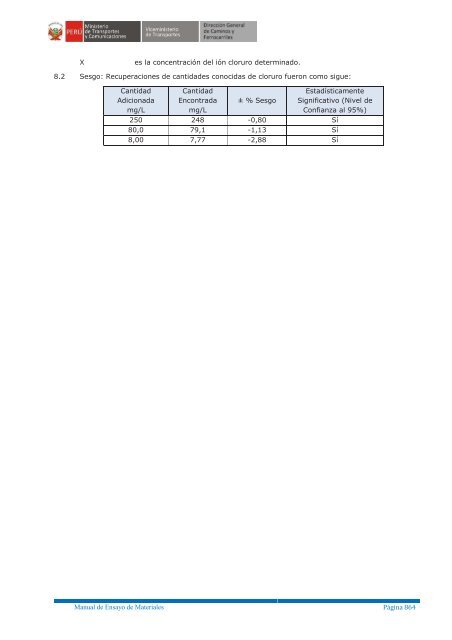
- Page 866 and 867: X es la concentración del ión clo
- Page 868 and 869: A.5 MUESTRA · Solución del indica
- Page 870 and 871: Cantidad Adicionada mg/L Cantidad E
- Page 872 and 873: (ver Nota 8). Agitar bien. Diluir c
- Page 874 and 875: Figura 2. Precisión interlaborator
- Page 876 and 877: MTC E 722 CONTENIDO DE CEMENTO PORT
- Page 878 and 879: Nota 2. Observar la presencia de ef
- Page 880 and 881: 7.1.3.4 Calcular la densidad D 1 en
- Page 882 and 883: 5.0.2 Cuando el volumen de material
- Page 884 and 885: MTC E 724 METODO DE ENSAYO NORMALIZ
- Page 886 and 887: MTC E 725 METODO DE ENSAYO PARA DET
- Page 888 and 889: área de ensayo. Los ensayos de imp
- Page 890 and 891: La tolerancia de la dureza del dur
- Page 892 and 893: TABLA 1 Requisitos para el uso de l
- Page 894 and 895: esistencias están en el rango de 7
- Page 896 and 897: ANEXO A (INFORMATIVO) A1 REPORTE DE
- Page 898 and 899: van a ser ensayados sin el refrenta
- Page 900 and 901: c) El contenedor tiene un termómet
- Page 902 and 903: 6.2.3 Método D 6.2.3.1 Verificar l
- Page 904 and 905: d) Almacenar el contenedor del cura
- Page 906 and 907: 7.2.7 Defectos en el espécimen o e
- Page 908 and 909: FIGURA 2. Contenedor de curado aut
- Page 910 and 911: ANEXO A2 (Informativo) A2. ESTIMACI
- Page 912 and 913: TABLA 2 Valores usados en la muestr
- Page 914 and 915:
A2.3.1 Supongamos que la resistenci
- Page 916 and 917:
4.1.1.1 Agua de la tanda (agua pesa
- Page 918 and 919:
ANEXO A (NORMATIVO) TABLA 1 Requisi
- Page 920 and 921:
ANEXO C (NORMATIVO) C.1 Guía para
- Page 922 and 923:
SECCION N° 8 METALICOS Manual de E
- Page 924 and 925:
ajo carga debe ajustarse, para que
- Page 926 and 927:
5.13 Marcas del espécimen. Los esp
- Page 928 and 929:
6.5 Determinación del límite conv
- Page 930 and 931:
· Reducción en porcentaje, del á
- Page 932 and 933:
5.0 MUESTRA 5.1 Para evitar los pro
- Page 934 and 935:
Figura 2. Matriz de doblamiento Cua
- Page 936 and 937:
a) Indicaciones relativas a la form
- Page 938 and 939:
6.5 Magnitud de la carga de ensayo.
- Page 940 and 941:
MTC E 901 RESISTENCIA A LA ROTURA D
- Page 942 and 943:
Tabla 1 Alturas recomendadas de vig
- Page 944 and 945:
MTC E 902 ENSAYO DE ABSORCION PARA
- Page 946 and 947:
MTC E 903 ENSAYO DE INFILTRACION EN
- Page 948 and 949:
Internal Designated Diameter. TABLE
- Page 950 and 951:
6.2.3 Si fue encontrada la línea d
- Page 952 and 953:
Figura 1. Equipo para determinar el
- Page 954 and 955:
6.2.2 Efectúense las siguientes me
- Page 956 and 957:
el tubo de admisión con agua prove
- Page 958 and 959:
SECCION N° 10 MISCELANEOS Manual d
- Page 960 and 961:
uedas extremas, preferiblemente la
- Page 962 and 963:
h) distancias a referencias fijas i
- Page 964 and 965:
MTC E 1002 MEDIDA DE LA DEFLEXION D
- Page 966 and 967:
4.1.6 Manómetro, que disponga de u
- Page 968 and 969:
5.6.2 Tampoco deberá efectuarse el
- Page 970 and 971:
Remolque. La configuración del rem
- Page 972 and 973:
consecutivos deberán concordar con
- Page 974 and 975:
APARATO PARA MEDIR LA FUERZA DE FRI
- Page 976 and 977:
A.5 PRESENTACION Las llantas deber
- Page 978 and 979:
0,98 N sobre la superficie de ensay
- Page 980 and 981:
tornillo (H). Seguidamente se fija
- Page 982 and 983:
5.3.3 La superficie de pavimento a
- Page 984 and 985:
Figura 1: Péndulo del TRRL Manual
- Page 986 and 987:
Figura 3: Detalle de la disposició
- Page 988 and 989:
Figura 5: Detalle del dispositivo d
- Page 990 and 991:
Figura 7: Regla graduada para ajust
- Page 992 and 993:
4.3 Disco para esparcir, plano y r
- Page 994 and 995:
APARATO PARA MEDIR PROFUNDIDAD DE M
- Page 996 and 997:
MTC E 1101 PREPARACION EN EL LABORA
- Page 998 and 999:
exceda de los 60 ºC. Desháganse c
- Page 1000 and 1001:
6.20 El refrentado puede hacerse co
- Page 1002 and 1003:
· Cara del pisón. Deberá emplear
- Page 1004 and 1005:
5.5 Escójanse y manténganse separ
- Page 1006 and 1007:
W = Peso seco en el horno en kg/m 3
- Page 1008 and 1009:
La parte movible de este bloque deb
- Page 1010 and 1011:
Figura 1. Distribución de la varia
- Page 1012 and 1013:
4.1.8 Bandejas y soportes adecuados
- Page 1014 and 1015:
diseño. Fórmese, tan rápidamente
- Page 1016 and 1017:
MTC E 1105 DETERMINACION POR TITULA
- Page 1018:
Manual de Ensayo de Materiales Pág
- Page 1021 and 1022:
subsecuentemente cuantas adiciones
- Page 1023 and 1024:
6.0 PROCEDIMIENTO Figura N 2 Curva
- Page 1025 and 1026:
MTC E 1106 PREPARACION EN EL LABORA
- Page 1027 and 1028:
MTC E 1107 CONTENIDO DE CAL DE MEZC
- Page 1029 and 1030:
que muestre ml de solución EDTA ve
- Page 1031 and 1032:
MTC E 1108 RESISTENCIA DE MEZCLAS D
- Page 1033 and 1034:
5.1.6 Sobre la base de porcentajes
- Page 1035 and 1036:
N° de Golpes/capa Clase de martill
- Page 1037 and 1038:
6.4 Capilaridad de los especímenes
- Page 1039 and 1040:
Séquese el material hasta peso con
- Page 1041 and 1042:
MTC Ministerio de Transportes, y Co
- Page 1043 and 1044:
MTC E 1109 ESTABILIZACION QUIMICA D
- Page 1045 and 1046:
3.1.2 MTC E 108 Mecánica de suelos
- Page 1047 and 1048:
h) condiciones y forma de utilizaci
- Page 1049 and 1050:
Tabla 4 Estabilidad bajo agua - Mé
- Page 1051 and 1052:
SECCION N° 12 PINTURAS Manual de E
- Page 1053 and 1054:
Figura 2. Rotor Tipo paleta para Us
- Page 1055 and 1056:
a) Resultado, expresado en gramos o
- Page 1058 and 1059:
MTC E 1203 DETERMINACION DE LA DENS
- Page 1060 and 1061:
7.1.2 Calcular la densidad en libra
- Page 1062 and 1063:
5.0 MUESTRA 5.1 Pinturas y producto
- Page 1064 and 1065:
MTC E 1206 DETERMINACION DE LA FLEX
- Page 1066 and 1067:
MTC E 1207 DETERMINACION DEL CONTEN
- Page 1068 and 1069:
d) El resultado del ensayo, como se
- Page 1070 and 1071:
6.1.2 Realizar los ensayos en ambie
- Page 1072 and 1073:
Figura 1 Modelo dual de rueda y ram
- Page 1074 and 1075:
MTC E 1210 DETERMINACION DE LA DURE
- Page 1076 and 1077:
MTC E 1211 DETERMINACION DE LA RESI
- Page 1078 and 1079:
MTC E 1213 DETERMINACION DE LA ADHE
- Page 1080 and 1081:
6.3.4 Examinar el borde de la herra
- Page 1082 and 1083:
MTC E 1214 DETERMINACION DE LA RELA
- Page 1084 and 1085:
MTC E 1215 DETERMINACION DE LA RESI
- Page 1086 and 1087:
8.0 PRECISION Y DISPERSION 8.1 Si l
- Page 1088 and 1089:
6.1 PREPARACIÓN DEL ENSAYO 6.1.1 M
- Page 1090 and 1091:
MTC E 1217 TOMA DE MUESTRAS PINTURA
- Page 1092 and 1093:
Tubo para toma de muestras con vál
- Page 1094 and 1095:
A excepción de los productos no ho
- Page 1096 and 1097:
h) Todos los símbolos de advertenc
- Page 1098 and 1099:
6.1.1 Mezclar cuidadosamente la mue
- Page 1100 and 1101:
MTC E 1228 DETERMINACION DE LA ADHE
- Page 1102 and 1103:
6.1.3 Siguiendo los requisitos de 6
- Page 1104 and 1105:
7.1.5 No considerar el ensayo en el
- Page 1106 and 1107:
ANEXO A1 PROBADOR DE ADHERENCIA DE
- Page 1108 and 1109:
A2.2.4 Mantener firmemente el instr
- Page 1110 and 1111:
A4.1 APARATOS ANEXO A4 PROBADOR DE
- Page 1112 and 1113:
A5.1 APARATOS ANEXO A5 PROBADOR DE
- Page 1114 and 1115:
MTC E 1230 DETERMINACIN DE LA RESIS
- Page 1116 and 1117:
4.2 MATERIALES 4.2.1 Abrasivo Está
- Page 1118 and 1119:
MTC E 1231 DETERMINACION DEL TIEMPO
- Page 1120 and 1121:
de sección transversal. La pelícu
- Page 1122 and 1123:
MTC E 1232 DETERMINACION DE LA ADHE
- Page 1124 and 1125:
6.3.8 Repetir el ensayo en otros do
- Page 1126 and 1127:
6.1.1 Mezclar cuidadosamente la mue
- Page 1128 and 1129:
MTC E 1235 DETERMINACION DE LA RESI
- Page 1130 and 1131:
MTC E 1236 DETERMINACION DE LA MATE
- Page 1132 and 1133:
MTC E 1237 DETERMINACION DEL CONTEN
- Page 1134 and 1135:
MTC E 1238 DETERMINACION DEL COLOR
- Page 1136 and 1137:
4.1.6 Patrón de reflectancia secun
- Page 1138 and 1139:
6.2.1 Los paneles de aluminio se pr
- Page 1140 and 1141:
MTC E 1239 DETERMINACION DEL CONTEN
- Page 1142 and 1143:
TABLA 1 Resumen de Métodos Tipo de
- Page 1144 and 1145:
SECCION N° 13 ESFERAS Y MICROESFER
- Page 1146 and 1147:
) Pesar 50 g de muestra seca con ap
- Page 1148 and 1149:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 1150 and 1151:
Figura 1. Embudo b) La muestra se d
- Page 1152 and 1153:
MTC E 1305 DETERMINACION DE LA DENS
- Page 1154 and 1155:
MTC E 1306 DETERMINACION DE LA APAR
- Page 1156 and 1157:
8.0 PRECISION Y DISPERSION 8.1 Si l
- Page 1158 and 1159:
7.0 CALCULOS E INFORME 7.1 CALCULOS
- Page 1160 and 1161:
7.1.1 Comparar en el microscopio la
- Page 1162 and 1163:
6.2.2 Cubrir totalmente la muestra
- Page 1164 and 1165:
“GW”, grava bien graduada; “G
- Page 1166 and 1167:
ANEXO Nº 2 INTRODUCCIÓN CONTROL D
- Page 1168 and 1169:
la obra. Será responsabilidad del
- Page 1170 and 1171:
CONTROLES DE OBRA Descripción Gene
- Page 1172 and 1173:
Mensualmente y acorde a lo establec
- Page 1174 and 1175:
Porcentaje estimado por fuera de l
- Page 1177:
Aceptabilidad I Categoría II n=5 n
- Page 1180 and 1181:
CEMENTO ASFÁLTICO Descripción El
- Page 1182 and 1183:
DISPOSICIONES GENERALIDADES Descrip
- Page 1184:
Tabla D Especificaciones del cement
- Page 1187 and 1188:
Equipo Todos los equipos empleados
- Page 1190:
Tabla F-1 Especificaciones para emu
- Page 1194:
Tabla H Requisitos de material bitu
- Page 1197 and 1198:
por los resultados de los ensayos d
- Page 1199 and 1200:
· Ejecutar ensayos de control de m
- Page 1201 and 1202:
Pavimento de concreto hidráulico D
- Page 1203 and 1204:
Su gradación se deberá ajustar a
- Page 1205 and 1206:
El acero de refuerzo de las losas e
- Page 1207 and 1208:
Si se emplean tolvas de pesada inde
- Page 1209 and 1210:
La pavimentadora compactará adecua
- Page 1211 and 1212:
Los procedimientos y equipos de exp
- Page 1213 and 1214:
e. Mezcla de los componentes La mez
- Page 1215 and 1216:
· La temperatura de la masa de con
- Page 1217 and 1218:
No se permite el empleo de producto
- Page 1219 and 1220:
Aceptación de los trabajos Criteri
- Page 1221 and 1222:
mayores de 7 m entre sí y de 0,5 m
- Page 1223 and 1224:
la resistencia a compresión, segú
- Page 1225 and 1226:
Todas las labores requeridas para l
- Page 1227 and 1228:
Los equipos de corte y doblado de l
- Page 1229 and 1230:
. Calidad del acero Las barras y ma
- Page 1231 and 1232:
Requerimientos de construcción Pre
- Page 1233 and 1234:
Para determinar la sanidad del tubo
- Page 1235 and 1236:
Equipo Básicamente, se requieren l
- Page 1237 and 1238:
Tabla N° 4 Diámetro interno de di
- Page 1239 and 1240:
CONTROLES DE CALIDAD PARA LA RECEPC
- Page 1241 and 1242:
- Baches Como en el caso anterior,
- Page 1243 and 1244:
En la última fila de cada 10 km se
- Page 1245 and 1246:
En el FORMATO A se reflejará, el j
- Page 1248 and 1249:
PROCEDIMIENTO Nº 2 EVALUACION DE P
- Page 1250 and 1251:
· Aclaraciones sobre cualquier asp
- Page 1252 and 1253:
d) En los casos de presentarse ahue
- Page 1254 and 1255:
CONDICION N° 3 Muy Bueno CONDICION
- Page 1256 and 1257:
CONDICION N° 7 Moderado (--) CONDI
- Page 1258 and 1259:
FOTOGRAFIAS DE LAS FALLAS DEL PAVIM
- Page 1260 and 1261:
FOTO N° 5 Parchado mal conformado
- Page 1262:
Región: Ruta: Región: Tramo: De k
- Page 1265 and 1266:
13. A través de un análisis de re
- Page 1267 and 1268:
ENSAYO DE DEFLEXION RECUPERABLE Y D
- Page 1269 and 1270:
carga del camión afecte las patas
- Page 1271 and 1272:
PARA LA DETERMINACIÓN DEL RADIO DE
- Page 1273 and 1274:
VOLUMEN CAPACIDAD 1 m 3 1,30795 yda
- Page 1275 and 1276:
TEMPERATURA Kelvin (K) ( tf + 459,6
- Page 1277 and 1278:
NORMA GENERAL MTC E 001 - 2013 1.0
- Page 1279 and 1280:
INFORME DE ENSAYO N° ………….
- Page 1281:
Nombre del Analista : Cargo : Cumpl