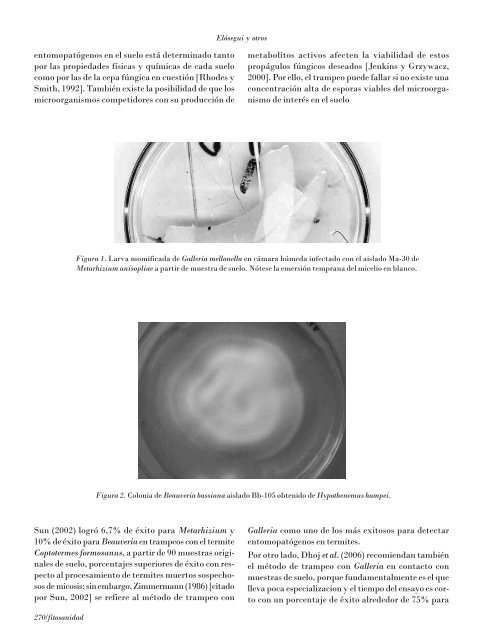
Elósegui y otrosentomopatógenos en el suelo está <strong>de</strong>terminado tantopor las propieda<strong>de</strong>s físicas y químicas <strong>de</strong> cada suelocomo por las <strong>de</strong> la cepa fúngica en cuestión [Rho<strong>de</strong>s ySmith, 1992]. También existe la posibilidad <strong>de</strong> que losmicroorganismos competidores con su producción <strong>de</strong>metabolitos activos afecten la viabilidad <strong>de</strong> estospropágulos fúngicos <strong>de</strong>seados [Jenkins y Grzywacz,2000]. Por ello, el trampeo pue<strong>de</strong> fallar si no existe unaconcentración alta <strong>de</strong> esporas viables <strong>de</strong>l microorganismo<strong>de</strong> interés en el sueloFigura 1. Larva momificada <strong>de</strong> Galleria mellonella en cámara húmeda infectado con el aislado Ma-30 <strong>de</strong>Metarhizium anisopliae a partir <strong>de</strong> muestra <strong>de</strong> suelo. Nótese la emersión temprana <strong>de</strong>l micelio en blanco.Figura 2. Colonia <strong>de</strong> Beauveria bassiana aislado Bb-105 obtenido <strong>de</strong> Hypothenemus hampei.Sun (2002) logró 6,7% <strong>de</strong> éxito para Metarhizium y10% <strong>de</strong> éxito para Beauveria en trampeos con el termiteCoptotermes formosanus, a partir <strong>de</strong> 90 muestras originales<strong>de</strong> suelo, porcentajes superiores <strong>de</strong> éxito con respectoal procesamiento <strong>de</strong> termites muertos sospechosos<strong>de</strong> micosis; sin embargo, Zimmermann (1986) [citadopor Sun, 2002] se refiere al método <strong>de</strong> trampeo conGalleria como uno <strong>de</strong> los más exitosos para <strong>de</strong>tectarentomopatógenos en termites.Por otro lado, Dhoj et al. (2006) recomiendan tambiénel método <strong>de</strong> trampeo con Galleria en contacto conmuestras <strong>de</strong> suelo, porque fundamentalmente es el quelleva poca especializacion y el tiempo <strong>de</strong>l ensayo es cortocon un porcentaje <strong>de</strong> éxito alre<strong>de</strong>dor <strong>de</strong> 75% para270/fitosanidad
Aislamiento, i<strong>de</strong>ntificación y caracterización...aislar Beavuveria y Metarhizium. Estos mismos autoresusaron 15 g <strong>de</strong> suelo aproximadamente por cadaindividuo <strong>de</strong> Galleria y pusieron en contacto con el sueloal insecto trampeador hasta 18 días; sin embargo, eneste trabajo se obtuvo una sola muestra <strong>de</strong> suelo útilpor trampeo con Galleria, lo que representó 7% <strong>de</strong> éxito.Este comportamiento pue<strong>de</strong> <strong>de</strong>berse a que la cantidad<strong>de</strong> suelo por individuo fue <strong>de</strong> 6-10 g, y el tiempo encontacto con este solo fue <strong>de</strong> nueve días, a<strong>de</strong>más <strong>de</strong> quela cantidad <strong>de</strong> propágulos <strong>de</strong>l hongo <strong>de</strong> interés presenteen el suelo es muy variable y <strong>de</strong>pen<strong>de</strong> <strong>de</strong> condicionesespecíficas <strong>de</strong> cada ecosistema (Tabla 1 y Fig. 1).Un método más efectivo para obtener nuevos aislados<strong>de</strong> hongos es el aislamiento <strong>de</strong> colonias fúngicas únicas(ufc) a partir <strong>de</strong> muestras <strong>de</strong> suelo por dilucionesseriadas, según procedimiento <strong>de</strong>tallado por Lecuona(1996). No obstante, es ampliamente aceptado que estemétodo es muy caro y se prefiere usar en el aislamientoy selección <strong>de</strong> especies bacterianas, como por ejemploBacillus thuringiensis [Johnson y Bishop, 1996], <strong>de</strong> ahíque se <strong>de</strong>cidiera no emplearlo para enriquecer el número<strong>de</strong> aislados <strong>de</strong> la Colección <strong>de</strong> Hongos Entomopatógenos<strong>de</strong>l INISAV.El porcentaje <strong>de</strong> éxito obtenido en este trabajo paralas muestras <strong>de</strong> insectos sospechosos <strong>de</strong> micosis o conuna evi<strong>de</strong>nte fue <strong>de</strong> 42%. Jackson et al. (2000) planteanque aunque este método <strong>de</strong> aislamiento directoconlleva mucho tiempo <strong>de</strong> muestreo en campo y experiencia,la realidad es que entre los más exitosos agentes<strong>de</strong> control con microorganismos se encuentranaquellos aislados obtenidos directamente <strong>de</strong> los insectoshospe<strong>de</strong>ros, y no <strong>de</strong> las colecciones <strong>de</strong> cultivos o <strong>de</strong>métodos indirectos a través <strong>de</strong> medios <strong>de</strong> cultivo selectivos.La frecuencia alta <strong>de</strong> aparición <strong>de</strong> Beauveria bassianase <strong>de</strong>bió al amplio rango <strong>de</strong> hospedantes <strong>de</strong> este patógeno,a<strong>de</strong>más <strong>de</strong> que la mayoría <strong>de</strong> los aislamientos sehicieron a partir <strong>de</strong> Hypothenemus hampei (broca <strong>de</strong>lcafé), y se conoce que esta especie fúngica regularmentese ha encontrado que atacan las poblaciones <strong>de</strong>l insecto<strong>de</strong> forma natural en los cafetales. De hecho, esesta la razón <strong>de</strong> que sea uno <strong>de</strong> los entomopatógenosmás estudiados para el control <strong>de</strong> esta plaga [Bustilloet al., 1999].Beauveria bassiana (Bals.) Vuill. así como Metarhiziumanisopliae (Metsch.) Sorok. y Metarhizium flavoviri<strong>de</strong>Gams and Rozsypal están entre los hongos entomopatógenosmás usualmente encontrados en la naturaleza.Por ello, colecciones <strong>de</strong> cultivo internacionalmentereconocidas cuentan con varios cientos <strong>de</strong> aislados <strong>de</strong>estas tres especies como la Colección <strong>de</strong> HongosEntomopatógenos para <strong>Investigaciones</strong> Agrícolas <strong>de</strong>lDepartamento <strong>de</strong> Agricultura <strong>de</strong> Estados Unidos(ARCEF), la ATCC (American Type Culture Collection)y la Colección <strong>de</strong>l IMI (International MycologicalInstitute) en el Reino Unido [Humber, 1992; Batemanet al., 1996]. En Cuba más <strong>de</strong>l 85% <strong>de</strong> la Colección <strong>de</strong>Hongos Entomopatógenos <strong>de</strong>l INISAV está representadapor aislados <strong>de</strong> Beauveria y Metarhizium.En relación con el aislamiento <strong>de</strong> Paecilomyces lilacinusobtenido <strong>de</strong> Hypothenemus hampei se sabe que estehongo se encuentra comúnmente en las crías <strong>de</strong> brocaen laboratorio, don<strong>de</strong> es posible que las condiciones <strong>de</strong>hacinamiento, la alta humedad relativa y la falta <strong>de</strong><strong>de</strong>sinfección <strong>de</strong> las cerezas favorezcan la invasión <strong>de</strong> estaespecie para atacar a la broca, si bien en la planta <strong>de</strong>café en el campo no se ha encontrado [Posada et al.,1998]. También es cierto que P. lilacinus está catalogadocomo hongo entomopatógeno oportunista y se hausado exitosamente en el control <strong>de</strong> nematodosfitopatógenos [López, 1995]. Por esta razón se <strong>de</strong>cidióincorporarlo a la Colección <strong>de</strong> Hongos Entomopatógenos<strong>de</strong>l INISAV para futuras investigaciones.Los productos exitosos a base <strong>de</strong> hongos <strong>de</strong>sarrolladosen el mercado han surgido a partir <strong>de</strong> un monitoreo <strong>de</strong>aislados obtenidos <strong>de</strong> las regiones geográficas yagroecosistemas, don<strong>de</strong> está el organismo plaga porcontrolar, así como <strong>de</strong> las colecciones <strong>de</strong> cultivos.Bateman et al. (1996) reportaron la selección <strong>de</strong> unasola cepa <strong>de</strong> M. anisopliae, <strong>de</strong>spués <strong>de</strong> haber ensayado159 aislados <strong>de</strong> Beauveria y Metarhizium contraSchistocerca gregaria (langosta <strong>de</strong>l <strong>de</strong>sierto). Esto confirmala necesidad <strong>de</strong> contar con abundante cantidad<strong>de</strong> aislados <strong>de</strong> los más diversos orígenes cuando se precisaobtener agentes microbianos efectivos comobiocontroladores <strong>de</strong> plagas [Bateman et al., 1996;Jenkins y Grzywacz, 2003].Como se pue<strong>de</strong> apreciar, <strong>de</strong> acuerdo con las característicasmacro y microculturales, para los aislados <strong>de</strong>Beauveria existió una alta similitud, por lo que unaseparación entre estos por los métodos tradicionalesmorfométricos no es factible (Tabla 1). Para lograr ladistinción entre aislados hay que recurrir a métodos <strong>de</strong>biología molecular como RFLP y PCR-RAPDS [Bridgeet al., 1993; Bridge y Arora, 1998; Bielikova et al.,2002]. Estos métodos moleculares también se usan comouna forma altamente reproducible <strong>de</strong> reconocer cadafitosanidad/271
- Page 1 and 2: ContenidoDiagnóstico fitosanitario
- Page 3 and 4: FITOSANIDAD vol. 10, no. 4, diciemb
- Page 5: Detección de β-exotoxina en cepas
- Page 9: FITOSANIDAD vol. 10, no. 4, diciemb
- Page 12 and 13: Hernández y otrosTabla 2. Fauna de
- Page 15 and 16: Aislamiento, identificación y cara
- Page 17: Aislamiento, identificación y cara
- Page 21 and 22: FITOSANIDAD vol. 10, no. 4, diciemb
- Page 24 and 25: 276/fitosanidadJiménez y otrosTabl
- Page 26 and 27: Jiménez y otrosDe Ávila, A. C.; L
- Page 28 and 29: Estrada y PiñónTabla 1. Relación
- Page 30 and 31: Estrada y PiñónFigura 2. Análisi
- Page 32 and 33: 284/fitosanidadEstrada y Piñón
- Page 34 and 35: Cabrera y otrosbrera et al., 2002a]
- Page 36 and 37: 288/fitosanidad
- Page 38 and 39: Reinoso y otroslos. Las enfermedade
- Page 40 and 41: Reinoso y otrosantagonista preparad
- Page 42 and 43: Fitosanidad tiene como objetivo div
- Page 44 and 45: García y otrosagitados, aunque má
- Page 46 and 47: García y otrosCONCLUSIONES• La p
- Page 48 and 49: Tejeda Gómezmado por estudios del
- Page 50 and 51: Tejeda Gómeznocido como ribotyping
- Page 52 and 53: Tgxkuvc"FitosanidadKPKUCX""""""""""
- Page 54 and 55: Veitía y otrosEn más del 50% de l
- Page 56 and 57: Vázquez y otrosFigura 1. Corte de
- Page 58: FITOSANIDAD vol. 10, no. 4, diciemb