Portada Simposios - Supplements - Haematologica
Portada Simposios - Supplements - Haematologica Portada Simposios - Supplements - Haematologica
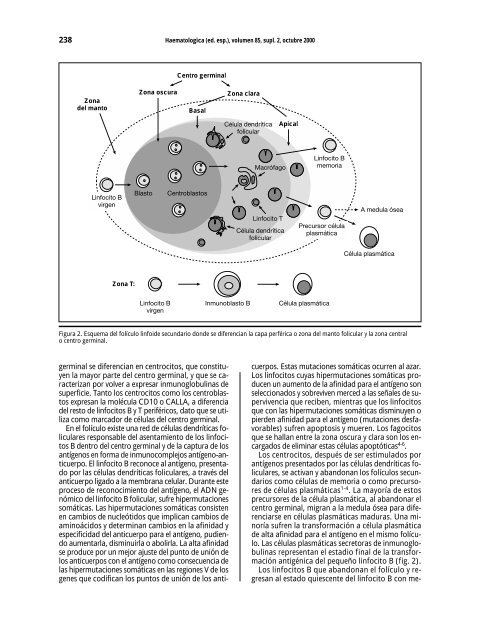
238 Haematologica (ed. esp.), volumen 85, supl. 2, octubre 2000 Centro germinal Zona del manto Zona oscura Basal Zona clara Célula dendrítica folicular Apical Macrófago Linfocito B memoria Linfocito B virgen Blasto Centroblastos Linfocito T Célula dendrítica folicular Precursor célula plasmática A medula ósea Célula plasmática Zona T: Linfocito B virgen Inmunoblasto B Célula plasmática Figura 2. Esquema del folículo linfoide secundario donde se diferencian la capa perférica o zona del manto folicular y la zona central o centro germinal. germinal se diferencian en centrocitos, que constituyen la mayor parte del centro germinal, y que se caracterizan por volver a expresar inmunoglobulinas de superficie. Tanto los centrocitos como los centroblastos expresan la molécula CD10 o CALLA, a diferencia del resto de linfocitos B y T periféricos, dato que se utiliza como marcador de células del centro germinal. En el folículo existe una red de células dendríticas foliculares responsable del asentamiento de los linfocitos B dentro del centro germinal y de la captura de los antígenos en forma de inmunocomplejos antígeno-anticuerpo. El linfocito B reconoce al antígeno, presentado por las células dendríticas foliculares, a través del anticuerpo ligado a la membrana celular. Durante este proceso de reconocimiento del antígeno, el ADN genómico del linfocito B folicular, sufre hipermutaciones somáticas. Las hipermutaciones somáticas consisten en cambios de nucleótidos que implican cambios de aminoácidos y determinan cambios en la afinidad y especificidad del anticuerpo para el antígeno, pudiendo aumentarla, disminuirla o abolirla. La alta afinidad se produce por un mejor ajuste del punto de unión de los anticuerpos con el antígeno como consecuencia de las hipermutaciones somáticas en las regiones V de los genes que codifican los puntos de unión de los anticuerpos. Estas mutaciones somáticas ocurren al azar. Los linfocitos cuyas hipermutaciones somáticas producen un aumento de la afinidad para el antígeno son seleccionados y sobreviven merced a las señales de supervivencia que reciben, mientras que los linfocitos que con las hipermutaciones somáticas disminuyen o pierden afinidad para el antígeno (mutaciones desfavorables) sufren apoptosis y mueren. Los fagocitos que se hallan entre la zona oscura y clara son los encargados de eliminar estas células apoptóticas 4-6 . Los centrocitos, después de ser estimulados por antígenos presentados por las células dendríticas foliculares, se activan y abandonan los folículos secundarios como células de memoria o como precursores de células plasmáticas 1-4 . La mayoría de estos precursores de la célula plasmática, al abandonar el centro germinal, migran a la medula ósea para diferenciarse en células plasmáticas maduras. Una minoría sufren la transformación a célula plasmática de alta afinidad para el antígeno en el mismo folículo. Las células plasmáticas secretoras de inmunoglobulinas representan el estadio final de la transformación antigénica del pequeño linfocito B (fig. 2). Los linfocitos B que abandonan el folículo y regresan al estado quiescente del linfocito B con me-
XLII Reunión Nacional de la AEHH y XVI Congreso de la SETH. Simposios 239 A D B Figura 3. Diversos aspectos morfológicos del centrocito del centro folicular (May-Grünwald-Giemsa, ×1.000). moria inmunológica presentan características morfológicas indistinguibles del linfocito B maduro virgen. A diferencia de éste, el linfocito B con memoria es CD25+ y en su membrana ya no expresa IgD sino IgG, o IgM e IgG, o IgA y posee actividad de ATPasa y de 5’-nucleotidasa. Para algunos autores la positividad para el antígeno CD27 permite diferenciar el linfocito B con memoria (CD27+) del linfocito B virgen (CD27-) 5 . Los linfocitos con memoria pasan a formar parte de los linfocitos B recirculantes del manto o corona. Algunos de los linfocitos B vírgenes se sitúan en las zonas T del ganglio donde pueden ser estimulados por antígenos y transformarse en inmunoblastos, también denominados grandes células pironinófilas. Estos inmunoblastos pueden seguir el proceso de estimulación hasta células plasmáticas secretoras de anticuerpos de baja afinidad (fig. 2). Morfología Los centrocitos pueden ser grandes o pequeños y se caracterizan por poseer un citoplasma muy escaso e hialino en la variedad pequeña y algo más extenso, con discreta basofilia, en la variedad grande siempre son agranulares. El núcleo tiene una cromatina condensada, sin nucleolos visibles ópticamente en la variedad pequeña y con nucleolos visibles en la forma grande, semejando una célula blástica (centrocito blástico). Ambas subvariedades ofrecen como rasgo característico una hendidura, única o múltipe, que puede insinuarse o llegar a ser tan profunda que segmente el núcleo (fig. 1 y 3). A veces, esta hendidura es doble y simétrica, hecho que proporciona al núcleo un aspecto “riederiforme” 7-10 . Citoquímicamente, las células hendidas se caracterizan por ser negativas o sólo débilmente positivas a la fosfatasa ácida y a la -glucuronidasa 7 . En su superficie expresan los antígenos CD10, CD20, CD79a y, al igual que los centroblastos, no expresan CD5, CD21, CD23, ni cadenas ligeras de inmunoglobulina, ni proteína bcl 2 1-5 . Las células del linfoma del manto se caracterizan por su heterogeneidad. La mayoría son de mediano E C tamaño (fig. 1) pero se observan células del tamaño de un linfocito y otras grandes con descompensación N/C (gran núcleo/escaso citoplasma). El núcleo tiene el contorno irregular con varias hendiduras y la cromatina es de aspecto maduro excepto en la variante blástica, en la que la cromatina es más fina y pueden observarse nucleolos. Fenotípicamente se caracterizan por la expresión de CD5 y CD22 en ausencia de CD23, y son más frecuentemente Lambda que Kappa 11-15 positivos. Los centrocitos de la leucemia linfática crónica son morfologicamente indistinguibles de los observados en el centro folicular. El inmunofenotipo y la histología ganglionar serán fundamentales para su correcta filiación (fig. 1). Bibliografía 1. Stein H. Lymphocyte diferentiation. En: Masson DY, Harris NL, eds. Human Lymphoma: Clinical implications of the REAL classification. Londres: Springer-Verlag, 1999; 2: 2-4. 2. Roitt I, Brostoff J, Male D. Immunology. Londres: Mosby, 1997. 3. Fanboin L, Satz L. En Introducción a la inmunología humana. Barcelona: Mosby/Doyma, 1994. 4. Harris NL. Anatomy and biology of lymphocyte differentiation. Tutorial on neoplastic hematopathology. Miami, Florida. 1999; 1-20. 5. Klein U, Rajewski K, Küppers R. Human immunoglobulin IgM + IgD + peripheral blood B-cells expressing the CD27 cell surface antigen carry somatically mutated variable region genes: CD27 as a general marker for somatically mutated (memory) B-cells. J Exp Med 1998; 188: 1679-1689. 6. Küppers R, Klein U, Hansmann ML, Rajewski K. Cellular origin of human B-cell lymphomas. N Engl J Med 1999; 341: 1520-1529. 7. Woessner S, Florensa L. La citología óptica en el diagnóstico hematológico, 4.ª ed. Madrid: Ediciones Acción Médica, 2000 (en prensa). 8. Lennert K, Feller AC. Histopathology of non Hodgkin’s lymphomas. Berlin: Springer Verlag, 1992; 28-39. 9. Lukes KJ, Collins PD. A functional approach to the classification of malignant lymphoma. En: Musshoff K, ed. Diagnosis and therapy of malignant lymphoma. Berlin: Springer Verlag, 1974; 18: 1-8. 10. Lennert K. Follicular lymphoma. A tumor of germinal centers. En: Malignant diseases of the hematopoietic system. Gann Monograph Japanesse Cancer Association, University of Tokyo Press 1975; 217. 11. Harris NL, Jaffe E, Stein H et al. A revised European-American classification of lymphoid neoplasm: a proposal from the International Lymphoma Study Group. Blood 1994; 84: 1361-1392. 12. Matutes E. Immunophenotype of the chronic lymphoproliferative disorders. Haematologica 1998; 83 (Supl. 1): 393-398. 13. San Miguel JF, Orfao A, López-Borrasca A. Síndromes linfoproliferativos crónicos con expresión hemoperiférica no LLC. En: Sans Sabrafen J, ed. Hematología Clínica, 4.ª ed. Barcelona: 1999 (en prensa). 14. Weisenburger D, Armitage JO. Mantle cell lymphoma: an entity comes of age. Blood 1996; 87: 4483-4494. 15. Jaffe ES, Bookman MA, Longo DL. Lymphocytic lymphoma of intermediate differentation. Mantle zone lymphoma: a distinct subtype of B-cell lymphoma. Hum Pathol 1987; 18: 877-880. THE SECONDARY LYMPHOID FOLLICLE. MOLECULAR AND PHENOTYPICAL ANALYSIS M.S. MATEO, M. MOLLEJO, R. VILLUENDAS, P. ALGARA, M. SÁNCHEZ-BEATO, P. MARTÍNEZ AND M.A. PIRIS Centro Nacional de Investigaciones Oncológicas. Carretera de Majadahonda a Pozuelo, Km 2, Madrid 28220. The investigation of B-cell lineage and differentiation has been enormously facilitated by the discovery that B-cells in the germinal centre suffer somatic hypermutation of the immunoglobulin heavy chain
- Page 185 and 186: XLII Reunión Nacional de la AEHH y
- Page 187 and 188: XLII Reunión Nacional de la AEHH y
- Page 189 and 190: XLII Reunión Nacional de la AEHH y
- Page 191 and 192: XLII Reunión Nacional de la AEHH y
- Page 193 and 194: XLII Reunión Nacional de la AEHH y
- Page 195 and 196: XLII Reunión Nacional de la AEHH y
- Page 197 and 198: XLII Reunión Nacional de la AEHH y
- Page 199 and 200: XLII Reunión Nacional de la AEHH y
- Page 201 and 202: XLII Reunión Nacional de la AEHH y
- Page 203 and 204: XLII Reunión Nacional de la AEHH y
- Page 205 and 206: XLII Reunión Nacional de la AEHH y
- Page 207 and 208: XLII Reunión Nacional de la AEHH y
- Page 209 and 210: XLII Reunión Nacional de la AEHH y
- Page 211 and 212: XLII Reunión Nacional de la AEHH y
- Page 213 and 214: XLII Reunión Nacional de la AEHH y
- Page 215 and 216: XLII Reunión Nacional de la AEHH y
- Page 217 and 218: XLII Reunión Nacional de la AEHH y
- Page 219 and 220: XLII Reunión Nacional de la AEHH y
- Page 221 and 222: XLII Reunión Nacional de la AEHH y
- Page 223 and 224: XLII Reunión Nacional de la AEHH y
- Page 225 and 226: XLII Reunión Nacional de la AEHH y
- Page 227 and 228: XLII Reunión Nacional de la AEHH y
- Page 229 and 230: XLII Reunión Nacional de la AEHH y
- Page 231 and 232: XLII Reunión Nacional de la AEHH y
- Page 233 and 234: XLII Reunión Nacional de la AEHH y
- Page 235: CLUB ESPAÑOL DE CITOLOGÍA HEMATOL
- Page 239 and 240: XLII Reunión Nacional de la AEHH y
- Page 241 and 242: XLII Reunión Nacional de la AEHH y
- Page 243 and 244: XLII Reunión Nacional de la AEHH y
- Page 245 and 246: XLII Reunión Nacional de la AEHH y
- Page 247 and 248: XLII Reunión Nacional de la AEHH y
- Page 249 and 250: XLII Reunión Nacional de la AEHH y
- Page 251 and 252: XLII Reunión Nacional de la AEHH y
- Page 253 and 254: XLII Reunión Nacional de la AEHH y
- Page 255 and 256: XLII Reunión Nacional de la AEHH y
- Page 257 and 258: XLII Reunión Nacional de la AEHH y
- Page 259 and 260: XLII Reunión Nacional de la AEHH y
- Page 261 and 262: XLII Reunión Nacional de la AEHH y
- Page 263 and 264: XLII Reunión Nacional de la AEHH y
- Page 265 and 266: XLII Reunión Nacional de la AEHH y
- Page 267 and 268: XLII Reunión Nacional de la AEHH y
- Page 269 and 270: XLII Reunión Nacional de la AEHH y
- Page 271 and 272: XLII Reunión Nacional de la AEHH y
- Page 273 and 274: XLII Reunión Nacional de la AEHH y
- Page 275 and 276: XLII Reunión Nacional de la AEHH y
- Page 277 and 278: XLII Reunión Nacional de la AEHH y
- Page 279 and 280: XLII Reunión Nacional de la AEHH y
- Page 281 and 282: XLII Reunión Nacional de la AEHH y
- Page 283 and 284: CASOS CLÍNICO-CITOLÓGICOS CLUB ES
- Page 285 and 286: XLII Reunión Nacional de la AEHH y
238 <strong>Haematologica</strong> (ed. esp.), volumen 85, supl. 2, octubre 2000<br />
Centro germinal<br />
Zona<br />
del manto<br />
Zona oscura<br />
Basal<br />
Zona clara<br />
Célula dendrítica<br />
folicular<br />
Apical<br />
Macrófago<br />
Linfocito B<br />
memoria<br />
Linfocito B<br />
virgen<br />
Blasto<br />
Centroblastos<br />
Linfocito T<br />
Célula dendrítica<br />
folicular<br />
Precursor célula<br />
plasmática<br />
A medula ósea<br />
Célula plasmática<br />
Zona T:<br />
Linfocito B<br />
virgen<br />
Inmunoblasto B<br />
Célula plasmática<br />
Figura 2. Esquema del folículo linfoide secundario donde se diferencian la capa perférica o zona del manto folicular y la zona central<br />
o centro germinal.<br />
germinal se diferencian en centrocitos, que constituyen<br />
la mayor parte del centro germinal, y que se caracterizan<br />
por volver a expresar inmunoglobulinas de<br />
superficie. Tanto los centrocitos como los centroblastos<br />
expresan la molécula CD10 o CALLA, a diferencia<br />
del resto de linfocitos B y T periféricos, dato que se utiliza<br />
como marcador de células del centro germinal.<br />
En el folículo existe una red de células dendríticas foliculares<br />
responsable del asentamiento de los linfocitos<br />
B dentro del centro germinal y de la captura de los<br />
antígenos en forma de inmunocomplejos antígeno-anticuerpo.<br />
El linfocito B reconoce al antígeno, presentado<br />
por las células dendríticas foliculares, a través del<br />
anticuerpo ligado a la membrana celular. Durante este<br />
proceso de reconocimiento del antígeno, el ADN genómico<br />
del linfocito B folicular, sufre hipermutaciones<br />
somáticas. Las hipermutaciones somáticas consisten<br />
en cambios de nucleótidos que implican cambios de<br />
aminoácidos y determinan cambios en la afinidad y<br />
especificidad del anticuerpo para el antígeno, pudiendo<br />
aumentarla, disminuirla o abolirla. La alta afinidad<br />
se produce por un mejor ajuste del punto de unión de<br />
los anticuerpos con el antígeno como consecuencia de<br />
las hipermutaciones somáticas en las regiones V de los<br />
genes que codifican los puntos de unión de los anticuerpos.<br />
Estas mutaciones somáticas ocurren al azar.<br />
Los linfocitos cuyas hipermutaciones somáticas producen<br />
un aumento de la afinidad para el antígeno son<br />
seleccionados y sobreviven merced a las señales de supervivencia<br />
que reciben, mientras que los linfocitos<br />
que con las hipermutaciones somáticas disminuyen o<br />
pierden afinidad para el antígeno (mutaciones desfavorables)<br />
sufren apoptosis y mueren. Los fagocitos<br />
que se hallan entre la zona oscura y clara son los encargados<br />
de eliminar estas células apoptóticas 4-6 .<br />
Los centrocitos, después de ser estimulados por<br />
antígenos presentados por las células dendríticas foliculares,<br />
se activan y abandonan los folículos secundarios<br />
como células de memoria o como precursores<br />
de células plasmáticas 1-4 . La mayoría de estos<br />
precursores de la célula plasmática, al abandonar el<br />
centro germinal, migran a la medula ósea para diferenciarse<br />
en células plasmáticas maduras. Una minoría<br />
sufren la transformación a célula plasmática<br />
de alta afinidad para el antígeno en el mismo folículo.<br />
Las células plasmáticas secretoras de inmunoglobulinas<br />
representan el estadio final de la transformación<br />
antigénica del pequeño linfocito B (fig. 2).<br />
Los linfocitos B que abandonan el folículo y regresan<br />
al estado quiescente del linfocito B con me-