Clase 4 2da parte - Pedeciba
Clase 4 2da parte - Pedeciba Clase 4 2da parte - Pedeciba
Factores que influyen en el G de hidrólisis del ATP 1. Repulsión electrostática 2. Estabilización por resonancia del Pi saliente 3. Ionización del ADP 4. Mayor solvatación de ADP + Pi que ATP G = G o ’ + RT ln [ADP][Pi] [ATP] [ADP] = 0,25 x 10 -3 M [Pi] = 1,65 x 10 -3 M [ATP] = 2,25 x 10 -3 M G = -51,8 KJ/mol
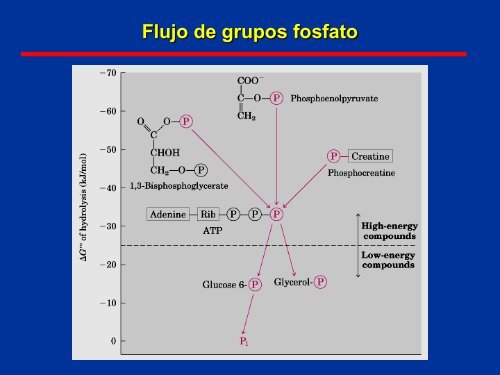
Flujo de grupos fosfato
- Page 1 and 2: Bioquímica y Biología Molecular M
- Page 4 and 5: Bioenergética: es el estudio cuant
- Page 6 and 7: Algunas definiciones: Entalpía H o
- Page 8 and 9: G = H - T S H S G - + entalpía neg
- Page 10 and 11: Dependencia de G con la concentraci
- Page 12 and 13: ¿Qué sucede cuando se alcanza el
- Page 14 and 15: Reacciones acopladas Una cantidad t
- Page 16 and 17: Reacciones acopladas
- Page 18 and 19: Glucosa Glucosa-6-P Fructosa-6-P Pi
- Page 20 and 21: Características del Metabolismo 1.
- Page 23: Ciclo del ATP
- Page 30 and 31: Molécula que participa en las reac
- Page 32 and 33: ¿Quién se lleva los electrones? A
- Page 35 and 36: Enzimas A. Propiedades generales de
- Page 37 and 38: Propiedades generales de las enzima
- Page 40 and 41: Enzimas A. Propiedades generales de
- Page 42 and 43: Las enzimas alteran las velocidades
- Page 44 and 45: Las interacciones débiles entre en
- Page 46 and 47: El modelo de Michaelis-Menten (1913
- Page 48 and 49: Cinética del estado estacionario
- Page 50 and 51: E + S ↔ ES → E + P Formación d
- Page 52 and 53: Relación entre concentración de s
- Page 54 and 55: [E T ] [S] = [ES] (K M +[S]) [ES] =
- Page 56 and 57: K m y V max son característicos pa
- Page 58 and 59: Si k 2 es la constante del paso lim
- Page 60 and 61: Inhibición competitiva K M aparent
- Page 62 and 63: Inhibición acompetitiva
- Page 64 and 65: Enzimas A. Propiedades generales de
- Page 66: Enzimas reguladoras 2. Modulación
Flujo de grupos fosfato