to get the file - OCW CEU
to get the file - OCW CEU
to get the file - OCW CEU
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Tema 3<br />
SÍNTESIS DE FÁRMACOS.<br />
DERIVADOS ARÓMATICOS<br />
SUSTITUIDOS<br />
1
1. Introducción<br />
2. Funcionalización de hidrocarburos arómaticos<br />
3. Compues<strong>to</strong>s aromáticos monocíclicos sustituidos<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. Compues<strong>to</strong>s aromáticos policíclicos condensados<br />
4.1. Derivados de naftaleno<br />
2
1. INTRODUCCIÓN<br />
Objetivo de la química farmacéutica<br />
Conocer estrategias de síntesis de fármacos<br />
representativos agrupados según su estructura<br />
Se necesita tener en cuenta la reactividad de los<br />
compues<strong>to</strong>s orgánicos<br />
Para:<br />
Su utilización como reactivos<br />
Desconexiones posibles en la estructura obje<strong>to</strong> de<br />
síntesis<br />
3
• Compues<strong>to</strong>s alifáticos: importancia menor como agentes<br />
terapéuticos<br />
La mayoría de los fármacos:<br />
• Compues<strong>to</strong>s aromáticos monocíclicos y policíclicos<br />
Antiparkinsoniano<br />
HO<br />
HO<br />
N<br />
Dopamina<br />
Antihistamínico<br />
N CH2 Cl<br />
CH 2CH 2N(CH 3) 2<br />
Clopiramina<br />
CH 2CH 2NH 2<br />
Antiinflama<strong>to</strong>rio<br />
i-Bu<br />
CH3 C<br />
H<br />
COOH<br />
Ibuprofeno<br />
Sulfonamidas antibacterianas<br />
H 2N SO 2NH<br />
sulfatiazol<br />
N<br />
S<br />
4
2. FUNCIONALIZACIÓN DE HIDROCARBUROS<br />
ARÓMATICOS<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO: AROMATICIDAD<br />
2. REACTIVIDAD<br />
Reacciones de sustitución electrofílica aromática (SEAr)<br />
Mecanismo<br />
Reacciones<br />
Efec<strong>to</strong> de los sustituyentes<br />
Activación y desactivación del anillo aromático<br />
Efec<strong>to</strong> sobre la orientación<br />
Reacciones de oxidación y reducción del benceno<br />
Reacciones de reducción<br />
Reacciones de oxidación de las cadenas laterales<br />
3. SALES DE ARENODIAZONIO COMO INTERMEDIOS<br />
SINTÉTICOS<br />
5
6<br />
5<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO:<br />
AROMATICIDAD<br />
1<br />
4<br />
benceno<br />
- Compues<strong>to</strong> aromático<br />
-Cíclico<br />
- Plano<br />
2<br />
3<br />
- Conjugado<br />
- Regla de Hückel<br />
Hibridación sp2<br />
Experimentalmente<br />
Resonancia<br />
Enlaces de igual longitud<br />
Estabilidad 1,3,5-ciclohexatrieno<br />
NO reacciones de adición<br />
anillos conjugados<br />
planos<br />
nº de electrones = 4n+2, n = 0, 1, 2…<br />
6
Clasificación<br />
de los<br />
compues<strong>to</strong>s<br />
aromáticos<br />
• Compues<strong>to</strong> aromático bencenoide<br />
Anillos de benceno fusionados o no<br />
benceno naftaleno antraceno<br />
CH 3 NH 2 OH<br />
<strong>to</strong>lueno anilina fenol<br />
• Compues<strong>to</strong> aromático heterocíclico<br />
Anillos aromáticos que contienen heteroá<strong>to</strong>mos<br />
N<br />
piridina<br />
N<br />
H<br />
pirrol<br />
O<br />
furano<br />
S<br />
tiofeno<br />
7
2. FUNCIONALIZACIÓN DE HIDROCARBUROS<br />
ARÓMATICOS<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO: AROMATICIDAD<br />
2. REACTIVIDAD<br />
Reacciones de sustitución electrofílica aromática (SEAr)<br />
Mecanismo<br />
Reacciones<br />
Efec<strong>to</strong> de los sustituyentes<br />
Activación y desactivación del anillo aromático<br />
Efec<strong>to</strong> sobre la orientación<br />
Reacciones de oxidación y reducción del benceno<br />
Reacciones de reducción<br />
Reacciones de oxidación de las cadenas laterales<br />
3. SALES DE ARENODIAZONIO COMO INTERMEDIOS<br />
SINTÉTICOS<br />
8
2. REACTIVIDAD<br />
Reacciones del benceno<br />
Sustitución electrofílica aromática<br />
(SEar)<br />
Oxidación<br />
Reducción<br />
9
SUSTITUCIÓN ELECTROFÍLICA AROMÁTICA<br />
(SEAR)<br />
H<br />
+ E +<br />
E + = Br +, NO 2 + , SO3, CH 3CH 2 + , CH3CO +<br />
• Benceno: rico en electrones<br />
Diferencia con alquenos y alquinos<br />
Mecanismo de la SEAr<br />
E +<br />
+<br />
+<br />
H E H E H E<br />
+<br />
E<br />
+ H +<br />
- Sustitución de uno de los hidrógenos del anillo por E +<br />
- NO adición electrófila<br />
Puede ser atacado por electrófilos<br />
-H +<br />
E<br />
10
Reacciones de SEAr más importantes<br />
1. Halogenación<br />
2. Nitración<br />
3. Sulfonación<br />
HNO 3<br />
H 2SO 4<br />
X 2<br />
AlX 3<br />
SO 3<br />
H 2SO 4<br />
NO 2<br />
X<br />
Nitrobenceno<br />
Halobenceno<br />
SO 3H<br />
A. bencenosulfónico<br />
<br />
X X AlX3 HO NO2 H<br />
+ H H O NO2 H<br />
O<br />
NO 2<br />
11<br />
H<br />
NO 2
4. Alquilación<br />
de Friedel-<br />
Crafts<br />
R-X<br />
AlX 3<br />
5. Acilación de<br />
O<br />
Friedel-Crafts R-C<br />
AlX 3<br />
X<br />
<br />
RC X AlX3 O<br />
R<br />
Alquilbenceno<br />
O<br />
C<br />
R<br />
Acilbenceno<br />
<br />
R X AlX3 12
2. FUNCIONALIZACIÓN DE HIDROCARBUROS<br />
ARÓMATICOS<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO: AROMATICIDAD<br />
2. REACTIVIDAD<br />
Reacciones de sustitución electrofílica aromática (SEAr)<br />
Mecanismo<br />
Reacciones<br />
Efec<strong>to</strong> de los sustituyentes<br />
Activación y desactivación del anillo aromático<br />
Efec<strong>to</strong> sobre la orientación<br />
Reacciones de oxidación y reducción del benceno<br />
Reacciones de reducción<br />
Reacciones de oxidación de las cadenas laterales<br />
3. SALES DE ARENODIAZONIO COMO INTERMEDIOS<br />
SINTÉTICOS<br />
13
• Efec<strong>to</strong> de los sustituyentes en la SEAr<br />
Se estudian:<br />
Benceno<br />
E +<br />
- Activación-desactivación del anillo<br />
- Regioselectividad<br />
¿El E + entrará con la misma facilidad y en la misma<br />
posición en el benceno, nitrobenceno o anilina?<br />
NO 2<br />
Nitrobenceno<br />
NH 2<br />
Anilina<br />
E + E +<br />
14
■ Activación y desactivación del anillo aromático<br />
- Sustituyentes o grupos activantes<br />
Aumentan la reactividad del anillo por cesión electrónica<br />
ACTIVAN EL ANILLO facilitan la introducción de un<br />
- Sustituyentes o grupos desactivantes<br />
nuevo sustituyente<br />
Disminuyen la reactividad del benceno atrayendo electrones<br />
DESACTIVAN EL ANILLO dificultan la introducción<br />
de un nuevo sustituyente<br />
Mecanismos de cesión y atracción: inducción o resonancia<br />
15
■ Clasificación de los sustituyentes<br />
Activantes Desactivantes<br />
Fuertemente activantes<br />
- NH 2 , -NHR, -NR 2<br />
-OH<br />
Moderadamente activantes<br />
-NHCOR<br />
-OCOR<br />
-OR<br />
Débilmente activantes<br />
-R<br />
-Ph<br />
Fuertemente desactivantes<br />
-NO 2<br />
-NR 3 +<br />
-CF 3 , -CCl 3<br />
Moderadamente desactivantes<br />
-CN<br />
-SO 3 H<br />
-COOH, -COOR, -CONHR<br />
-CHO, -COR<br />
Débilmente desactivantes<br />
-X<br />
16
Ejercicio<br />
Ordena los siguientes compues<strong>to</strong>s en orden decreciente<br />
de reactividad frente a la nitración<br />
Br<br />
NO 2<br />
NO 2<br />
CH 3<br />
OCH 3<br />
NO 2<br />
CH 3<br />
1 2<br />
Br<br />
3 4 5 6<br />
Respuesta: 2 4 6 5 3 1<br />
Br<br />
17
• Efec<strong>to</strong> de los sustituyentes en la SEAr<br />
Se estudian:<br />
Benceno<br />
E +<br />
- Activación-desactivación del anillo<br />
- Regioselectividad<br />
¿El E + entrará en la misma posición en el benceno,<br />
nitrobenceno o anilina?<br />
NO 2<br />
Nitrobenceno<br />
NH 2<br />
Anilina<br />
E + E +<br />
18
Efec<strong>to</strong> de los sustituyentes sobre la orientación<br />
Direc<strong>to</strong>res ORTO-PARA Direc<strong>to</strong>res META<br />
Fuertemente activantes<br />
- NH 2 , -NHR, -NR 2<br />
-OH<br />
Moderadamente activantes<br />
-NHCOR<br />
-OCOR<br />
-OR<br />
Débilmente activantes<br />
-R<br />
-Ph<br />
Débilmente desactivantes<br />
-X<br />
Fuertemente desactivantes<br />
-NO 2<br />
-NR 3 +<br />
-CF 3 , -CCl 3<br />
Moderadamente desactivantes<br />
-CN<br />
-SO 3 H<br />
-COOH, -COOR, CONHR<br />
-CHO, -COR<br />
19
Predice la posición favorecida en una sustitución electrofílica aromática de los<br />
siguientes compues<strong>to</strong>s.<br />
CN NH 2 CF 3 NO 2<br />
+<br />
PPh 3<br />
C OCH3<br />
O<br />
O<br />
O C<br />
O<br />
CH3<br />
+<br />
NMe3<br />
20
Solución<br />
CN NH2<br />
CF3 NO2<br />
PPh 3<br />
COOCH 3<br />
O<br />
OCOCH 3<br />
NMe 3<br />
21
Regioselectividad con varios sustituyentes<br />
Varios sustituyentes<br />
- Todos activantes<br />
- Todos desactivantes<br />
- Activantes y desactivantes<br />
La sustitución está controlada por el carácter activante<br />
El activante más fuerte (o el desactivante más débil)<br />
controla la regioselectividad<br />
22
Ejercicio<br />
¿En qué posición entrará el electrófilo en los compues<strong>to</strong>s<br />
que se muestran a continuación<br />
NH 2<br />
CH 3<br />
Respuesta<br />
NH 2<br />
E +<br />
NH 2<br />
E<br />
CH 3<br />
CH 3<br />
NH 2<br />
NH 2<br />
NH 2<br />
E<br />
E +<br />
NO 2<br />
NO 2<br />
NO 2<br />
NH 2<br />
NH 2<br />
E<br />
E +<br />
NH 2<br />
NO 2<br />
NO 2<br />
NO 2<br />
23
2. FUNCIONALIZACIÓN DE HIDROCARBUROS<br />
ARÓMATICOS<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO: AROMATICIDAD<br />
2. REACTIVIDAD<br />
Reacciones de sustitución electrofílica aromática (SEAr)<br />
Mecanismo<br />
Reacciones<br />
Efec<strong>to</strong> de los sustituyentes<br />
Activación y desactivación del anillo aromático<br />
Efec<strong>to</strong> sobre la orientación<br />
Reacciones de oxidación y reducción del benceno<br />
Reacciones de reducción<br />
Reacciones de oxidación de las cadenas laterales<br />
3. SALES DE ARENODIAZONIO COMO INTERMEDIOS<br />
SINTÉTICOS<br />
24
REACCIONES DE OXIDACIÓN Y REDUCCIÓN<br />
A. REDUCCIÓN DEL BENCENO<br />
1. Hidrogenación<br />
2. Reducción de Birch<br />
3. Hidrogenólisis bencílica<br />
B. REACCIONES DE OXIDACIÓN DE LAS<br />
CADENAS LATERALES<br />
25
A. REDUCCIÓN DEL BENCENO<br />
1. Hidrogenación<br />
2. Reducción de Birch<br />
3. Hidrogenólisis bencílica<br />
CH 2OR<br />
+ 3 H 2<br />
Na<br />
NH 3(l)<br />
H 2<br />
Pd/C<br />
Ni<br />
100 at<br />
CH 3<br />
+ ROH<br />
26
B. REACCIONES DE OXIDACIÓN DE LAS CADENAS<br />
LATERALES<br />
CHR 2<br />
KMnO4<br />
COOH<br />
27
2. FUNCIONALIZACIÓN DE HIDROCARBUROS<br />
ARÓMATICOS<br />
1. DEFINICIÓN. ESTRUCTURA DEL BENCENO: AROMATICIDAD<br />
2. REACTIVIDAD<br />
Reacciones de sustitución electrofílica aromática (SEAr)<br />
Mecanismo<br />
Reacciones<br />
Efec<strong>to</strong> de los sustituyentes<br />
Activación y desactivación del anillo aromático<br />
Efec<strong>to</strong> sobre la orientación<br />
Reacciones de oxidación y reducción del benceno<br />
Reacciones de reducción<br />
Reacciones de oxidación de las cadenas laterales<br />
3. SALES DE ARENODIAZONIO COMO INTERMEDIOS<br />
SINTÉTICOS<br />
28
SALES DE ARENODIAZONIO (SALES DE DIAZONIO AROMÁTICAS)<br />
1. SÍNTESIS<br />
2. REACCIONES<br />
NH2 N N<br />
HNO 2<br />
- Reacciones de Sandmeyer<br />
- Sustitución por -I<br />
N<br />
N<br />
sal de diazonio<br />
CuCl<br />
N N<br />
I<br />
KI<br />
CuBr<br />
CuCN<br />
Cl<br />
Br<br />
CN<br />
29
4. Sustitución por -OH<br />
N<br />
N<br />
H 2O<br />
calor<br />
5. Sustitución por -H. Desaminación por diazotación<br />
N<br />
N<br />
H 3PO 2<br />
6. Reacciones de acoplamien<strong>to</strong> de las sales de diazonio<br />
N<br />
N<br />
OH<br />
OH<br />
SEar<br />
+ N<br />
N OH<br />
H<br />
30
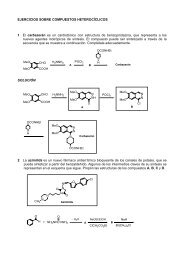
Ejercicio:<br />
Se dispone de nitrobenceno marcado con el isó<strong>to</strong>po 14C en la posición del anillo<br />
bencénico. Diseña cuatro síntesis A)-D) que a partir de dicho compues<strong>to</strong> permita<br />
obtener los clorobencenos marcados que se señalan<br />
Cl<br />
Cl Cl<br />
Cl Cl<br />
A)<br />
D)<br />
NO 2<br />
B)<br />
C)<br />
Cl Cl<br />
Cl<br />
Cl<br />
31
1. Introducción<br />
2. Funcionalización de hidrocarburos arómaticos<br />
3. Compues<strong>to</strong>s aromáticos monocíclicos sustituidos<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. Compues<strong>to</strong>s aromáticos policíclicos condensados<br />
4.1. Derivados de naftaleno<br />
32
3.1. Arilalquilaminas Ar(C) nN<br />
Estructura de muchos fármacos<br />
Síntesis: distancia entre el núcleo aromático y el grupo amino<br />
bencilaminas<br />
fenetilaminas<br />
3-arilpropilaminas<br />
4-fenilbutilaminas<br />
C N<br />
C C N<br />
3<br />
1<br />
C C C N<br />
4<br />
1<br />
C C C C N<br />
33
Bencilaminas<br />
Estructura de bencilamina<br />
N<br />
N CH2 Cl<br />
CH 2CH 2N(CH 3) 2<br />
Cloropiramina<br />
C N<br />
Se puede encontrar en antihistamínicos H1<br />
y a un arilo<br />
uno de los grupos amino está unido a un bencilo<br />
34
SÍNTESIS:<br />
A) ESTRATEGIA GENERAL<br />
alquilaciones sucesivas de una amina aromática<br />
Ar NH2<br />
1. XCH 2Ar<br />
2. XCH 2CH 2 N R1<br />
R2<br />
Ar N CH 2Ar<br />
CH2CH2N<br />
B) Alternativamente: reducción de una base de Schiff<br />
N CH<br />
Imina o base de Schiff<br />
[H]<br />
NH CH 2<br />
35<br />
R 1<br />
R 2
A) SÍNTESIS: ESTRATEGIA GENERAL<br />
Alquilaciones sucesivas de una amina aromática<br />
Ar NH2<br />
1. XCH 2Ar<br />
2. XCH 2CH 2 N R1<br />
R2<br />
NH2 N CH 2<br />
CH2CH2<br />
Fenbenzamina<br />
N CH2<br />
CH2CH2<br />
Histapirrodina<br />
Ar N CH 2Ar<br />
CH2CH2N<br />
CH3<br />
N<br />
CH3<br />
N<br />
R 1<br />
R 2<br />
1942. Uno de<br />
los primeros<br />
antiH1<br />
36
B) reducción de una base de Schiff<br />
Síntesis de la cloropiramina<br />
[H]<br />
N<br />
N<br />
NH 2<br />
N<br />
O<br />
H<br />
Cl<br />
NH CH2 Cl<br />
N CH2 Cl<br />
CH 2CH 2N(CH 3) 2<br />
Cloropiramina<br />
N<br />
N CH Cl<br />
Imina o base de Schiff<br />
ClCH 2CH 2N(CH 3) 2<br />
37
3.1. Arilalquilaminas Ar(C) nN<br />
bencilaminas<br />
fenetilaminas<br />
3-arilpropilaminas<br />
4-fenilbutilaminas<br />
C N<br />
C C N<br />
3<br />
1<br />
C C C N<br />
4<br />
1<br />
C C C C N<br />
38
Estructura de fenetilamina<br />
Presente en<br />
Agonistas<br />
adrenérgicos<br />
- Fenilisopropilaminas:<br />
anfetaminas<br />
- Ariletanolaminas:<br />
Ar CHO HNu Ar CH Nu<br />
Neurotransmisores adrenérgicos y<br />
fármacos relacionados<br />
OH<br />
C C N<br />
Ar CH CH<br />
R 1 NHR 3<br />
R 2<br />
R 1 = OH ariletanolaminas<br />
R 1 = H fenilisopropilaminas<br />
39
SÍNTESIS de FENETILAMINAS<br />
1. A partir de aldehídos aromáticos<br />
2. A partir de ce<strong>to</strong>nas aromáticas<br />
3. Clorometilación<br />
40
1. aldehído aromático<br />
Ejemplo: síntesis de hidroxianfetamina<br />
adición de nitroalcano y manipulación de grupos<br />
funcionales<br />
CH 3O<br />
- H 2O<br />
Fe/HCl<br />
CH 3O<br />
O<br />
C<br />
H<br />
CH 3O<br />
CH 3O<br />
NO 2CH 2CH 3 / base<br />
NO 2CHCH 3<br />
C<br />
H<br />
C<br />
H<br />
C CH 3<br />
NH 2<br />
Enamina<br />
H<br />
C<br />
H<br />
C CH 3<br />
NO 2<br />
C CH 3<br />
O<br />
CH 3O<br />
CH 3O<br />
H 2NOH<br />
- H 2O<br />
OH<br />
C<br />
H<br />
H<br />
C<br />
H<br />
CH CH 3<br />
NO 2<br />
C CH 3<br />
NH<br />
Imina<br />
41
CH 3O<br />
HBr<br />
H<br />
C<br />
H<br />
Oxima<br />
C CH 3<br />
N OH<br />
HO<br />
[H]<br />
H<br />
C<br />
H<br />
Hidroxianfetamina<br />
Midríatico:<br />
Dilatación pupilar<br />
antes de una<br />
oftalmoscopia<br />
CH 3O<br />
H<br />
C CH 3<br />
NH 2<br />
H<br />
C<br />
H<br />
H<br />
C CH 3<br />
NH 2<br />
Fenilisopropilamina<br />
42
2. Ce<strong>to</strong>nas aromáticas<br />
HO<br />
Ejemplo: Sinefrina (adrenérgico)<br />
C 6H 5CO<br />
H 2, cat<br />
O<br />
O<br />
C<br />
HO<br />
CH 3<br />
ClCOC6H5 (protección)<br />
O<br />
CCH 2Br<br />
CH<br />
OH<br />
Sinefrina (racémica)<br />
C 6H 5CO<br />
CH 3NH 2<br />
CH 2 NH<br />
O<br />
HO<br />
O<br />
CCH 3<br />
O<br />
Br 2<br />
CCH 2NHCH 3<br />
CH 3 Ariletanolamina<br />
43
HO<br />
Sinefrina<br />
CH<br />
OH<br />
Sinefrina (racémica)<br />
- Ariletanolamina<br />
CH 2 NH CH 3<br />
- Se extrae del citrus aurantium<br />
- Extrac<strong>to</strong>: Induce pérdida del peso graso<br />
Mejora el rendimien<strong>to</strong><br />
Capaz de mantener la proporción de masa<br />
magra aún en condiciones de déficit calórico<br />
44
3. clorometilación y sustitución nucleofílica<br />
Dopamina (neurotransmisor): antiparkinsoniano<br />
R<br />
NaCN<br />
R<br />
H<br />
+ H<br />
O<br />
HCl<br />
H CH2Cl SEar<br />
R<br />
CH 2CN<br />
Manipulación de<br />
grupos funcionales<br />
45
H 3CO<br />
H3CO O<br />
H3CO H 3CO<br />
DOPAMINA<br />
KCN<br />
SN2<br />
H 3CO<br />
+ H<br />
H 3CO<br />
H 3CO<br />
CH 2CH 2NH 2<br />
HCl<br />
H H3CO CH2Cl SEar<br />
HBr<br />
CH 2CN<br />
HO<br />
H 2, cat<br />
HO<br />
Dopamina<br />
CH 2CH 2NH 2<br />
46
H<br />
O<br />
Clorometilación: Mecanismo<br />
H<br />
H<br />
Cl<br />
CH 2OH<br />
H<br />
H Cl<br />
O<br />
H<br />
H<br />
SEar<br />
CH 2Cl<br />
47
labetalol<br />
H 2N<br />
HO<br />
O<br />
C<br />
HN(CH 2Ph) 2<br />
ClCOCH 2Br/<br />
antianginoso y vasodilatador<br />
AlCl 3<br />
Acilación de Friedel-Crafts<br />
H 2N<br />
HO<br />
O<br />
C<br />
H 2N<br />
HO<br />
O<br />
C<br />
H 2, cat<br />
COCH 2Br<br />
COCH 2N(CH 2Ph) 2 hidrogenolisis<br />
bencílica<br />
48
H 2N<br />
HO<br />
[H]<br />
O<br />
C<br />
COCH 2NH 2<br />
H 2N<br />
HO<br />
O<br />
C<br />
O C<br />
CH3 (CH2) 2 Ph<br />
OH<br />
CH 3<br />
CHCH2N CH<br />
H (CH2) 2Ph<br />
bloqueante -adrenérgico<br />
- vasodilatador<br />
- antiarrítmico<br />
- angina de pecho<br />
H 2N<br />
HO<br />
O<br />
C<br />
Labetalol<br />
COCH 2N C<br />
CH 3<br />
(CH 2) 2Ph<br />
49
3.1. Arilalquilaminas Ar(C) nN<br />
bencilaminas<br />
fenetilaminas<br />
3-arilpropilaminas<br />
4-fenilbutilaminas<br />
C N<br />
C C N<br />
C C C N<br />
C C C C N<br />
50
- H 2O<br />
3-arilpropilaminas<br />
Prenilamina<br />
O<br />
C<br />
H + NC CH2 COOEt<br />
NC<br />
CH COOEt<br />
<br />
C<br />
H<br />
C CN<br />
CO 2Et<br />
Bloquea los canales de Ca<br />
Antianginoso<br />
Vasodilatador coronario<br />
base<br />
MgBr<br />
Adición de Michael<br />
OH<br />
C<br />
H<br />
CH CN<br />
CO 2Et<br />
C<br />
H<br />
H<br />
C CN<br />
CO 2Et<br />
51
1. NaOH<br />
2. HCl<br />
3. calor<br />
PhCH 2<br />
CH 3<br />
O<br />
CH CH 2 CN H 2/cat<br />
CH CH 2 CH 2 N<br />
H<br />
CH CH2 CH2 N C CH2Ph CH3 H<br />
C<br />
CH 3<br />
CH 2Ph Prenilamina<br />
CH CH 2 CH 2 NH 2<br />
H 2<br />
Pd<br />
52
3.1. Arilalquilaminas Ar(C) nN<br />
bencilaminas<br />
fenetilaminas<br />
3-arilpropilaminas<br />
4-fenilbutilaminas<br />
C N<br />
C C N<br />
C C C N<br />
C C C C N<br />
53
H 3CO<br />
4-fenilbutilaminas: verapamilo, propoxifeno<br />
H 3CO H 3CO<br />
H 3CO<br />
CH 2 CN<br />
NaNH 2<br />
H3CO CH<br />
CN<br />
CH(CH3) 2<br />
H 3CO<br />
H 3CO<br />
CH(CH 3) 2<br />
C<br />
CN<br />
CH 2CH 2CH 2<br />
Verapamilo<br />
H 3CO<br />
1. NaNH2 2. Cl(CH2) 3<br />
N<br />
CH 3<br />
(CH 2) 2<br />
CH<br />
CH3 N (CH2) 2<br />
OCH 3<br />
CN<br />
OCH 3<br />
ClCH(CH 3) 2<br />
OCH 3<br />
OCH 3<br />
Bloqueo de los<br />
canales de Ca<br />
Antianginoso<br />
Antiarrítmico<br />
54
Propoxifeno: análogo de la metadona (analgésico<br />
opiaceo)<br />
Ph<br />
O<br />
CH 3<br />
BrMgCH 2Ph<br />
Ph<br />
H 3O<br />
Ph<br />
H<br />
O<br />
O<br />
CH 3<br />
H<br />
O<br />
H HN(CH 3) 2 HCl<br />
1. reacción de Mannich<br />
2. resolución<br />
Ph<br />
Ph<br />
N(CH 3) 2<br />
H<br />
OH<br />
CH 3<br />
N(CH 3) 2<br />
(d)-propoxifeno<br />
Ph<br />
O<br />
H<br />
O<br />
CH 3<br />
O O<br />
N(CH 3) 2<br />
anhídrido propiónico<br />
(d)-propoxifeno:<br />
hipnoanalgésico<br />
(l)-propoxifeno:<br />
antitusígeno<br />
55
Reacción de Mannich: mecanismo<br />
1. Formación del ion imonio<br />
H<br />
O<br />
H<br />
2. Enolización<br />
Ph<br />
O<br />
H<br />
CH 3<br />
H<br />
O<br />
H<br />
H<br />
HN(CH 3) 2<br />
Ph<br />
H<br />
OH<br />
H<br />
(H 3C) 2N H<br />
OH<br />
CH 3<br />
H H<br />
O<br />
H<br />
H<br />
N(CH 3) 2<br />
3. Formación del enlace C-C y pérdida de protón<br />
Ph<br />
OH<br />
CH 3<br />
H 2C N(CH 3) 2<br />
Ph<br />
O<br />
H<br />
CH 3<br />
N(CH 3) 2<br />
-H<br />
Ph<br />
O<br />
- H 2O H H<br />
CH 3<br />
N(CH 3) 2<br />
Ion imonio<br />
N(CH 3) 2<br />
56
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
57
3.2. Ácidos arilalcanoicos y derivados<br />
Estructura de ácidos arilacéticos o 2-arilpropiónicos<br />
antiinflama<strong>to</strong>rios no esteróidicos:<br />
i-Bu<br />
CH3 C<br />
H<br />
COOH<br />
Ibuprofeno<br />
C<br />
H<br />
C O<br />
OH<br />
Ácidos fenilacéticos: modificaciones<br />
R<br />
artritis reuma<strong>to</strong>ide y analgésicos<br />
H 3CO<br />
anillo bencénico<br />
función carboxílica<br />
grupo metileno<br />
Naproxeno<br />
CH3 CHCOOH<br />
58
Síntesis de ácidos arilacéticos sustituidos<br />
A) Alquilación en de carbaniones<br />
estabilizados<br />
- Ibuprofeno: arilace<strong>to</strong>nitrilos<br />
- Naproxeno: arilaceta<strong>to</strong>s<br />
B) A partir de fenonas<br />
- Fenoprofeno<br />
59
Síntesis de ácidos arilacéticos -sustituidos<br />
i-Bu<br />
A) alquilación en de carbaniones estabilizados<br />
- Ibuprofeno: arilace<strong>to</strong>nitrilos<br />
- Naproxeno: arilaceta<strong>to</strong>s<br />
HCl<br />
CH 2O<br />
i-Bu CH2 CN i-Bu<br />
NaNH2 o HNa<br />
CH 3<br />
i-Bu C<br />
H<br />
CN<br />
i-Bu CH 2 Cl<br />
NaOH,H 2O<br />
HCl, H 2O<br />
KCN<br />
CH<br />
CN<br />
ICH 3<br />
i-Bu<br />
CH3 C<br />
H<br />
COOH<br />
Ibuprofeno<br />
60
A) alquilación de carbaniones estabilizados<br />
H 3CO<br />
H 3CO<br />
H 3CO<br />
CH 2COOCH 3<br />
CH 3<br />
CHCOOCH 3<br />
CH3 CHCOOH<br />
1. HNa<br />
2. CH 3I<br />
Naproxeno<br />
hidrólisis<br />
61
Síntesis de ácidos arilacéticos -sustituidos<br />
B) a partir de fenonas: Fenoprofeno<br />
O<br />
PBr 3 O<br />
hidrólisis<br />
C<br />
O<br />
CH 3<br />
O<br />
NaBH 4<br />
CH3 CH<br />
Br<br />
CH3 CH<br />
NaCN<br />
COOH<br />
O<br />
Fenoprofeno<br />
O<br />
CH3 HC<br />
OH<br />
CH3 CH<br />
CN<br />
62
Derivados de ácidos arilacéticos: amidas y ésteres<br />
- Amidas: Diisopiramida (antiarrítmico, bloqueo de los<br />
canales de sodio)<br />
1. NaNH 2<br />
CH2 CN NaNH2 o HNa<br />
2. Cl(CH 2) 2N(CH(CH 3) 2<br />
N<br />
C CONH 2<br />
(CH 2) 2N(CH(CH 3) 2<br />
CH<br />
Cl<br />
N<br />
CN C CN<br />
N<br />
C CN<br />
(CH 2) 2N(CH(CH 3) 2<br />
Diisopiramida<br />
H 2SO 4<br />
H<br />
N<br />
63
- Ésteres: -fenilbutira<strong>to</strong> de etilo (hipocolesterolémico)<br />
calor<br />
(-CO 2)<br />
COOEt<br />
C COOEt<br />
Et<br />
H 3O<br />
H<br />
C COOH<br />
Et<br />
H<br />
C COOEt<br />
Et<br />
EtOH, H 2SO 4<br />
-fenilbutira<strong>to</strong> de etilo<br />
COOH<br />
C COOH<br />
Et<br />
64
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
65
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
N<br />
O<br />
OH<br />
Ciclizina<br />
Cinarizina<br />
Difenhidramina<br />
Difenilpiralina<br />
Clorfenoxamina<br />
Clemastina<br />
Difenidol<br />
Pirindol<br />
Ar<br />
Ar C<br />
H<br />
Haluro<br />
diaril<br />
metílico<br />
X<br />
A<br />
Alcohol B<br />
diarilmetílico<br />
Ce<strong>to</strong>na,éster<br />
magnesiano<br />
66<br />
C
A) A PARTIR DE HALUROS DE DIARILAMETILO<br />
N-ALQUILACIÓN<br />
Ciclizina<br />
Cinarizina<br />
O-ALQUILACIÓN<br />
Difenilpiralina<br />
Difenhidramina<br />
Ar<br />
Ar C N<br />
Ar<br />
Ar C O<br />
67
A) A PARTIR DE HALUROS DE DIARILAMETILO<br />
Preparación de los haluros de diarilmetilo<br />
O<br />
C OH<br />
H<br />
H<br />
HCl<br />
MgBr<br />
C Cl<br />
H<br />
C OMgBr<br />
H<br />
cloruro de difenilmetilo<br />
H 3O<br />
68
Ciclizina<br />
Cinarizina<br />
Ar<br />
Ar C N<br />
AntiH1, antiemético<br />
Bloquea los canales de Ca<br />
Vasodilatador<br />
N-alquilación<br />
C N<br />
H<br />
C N<br />
H<br />
Ciclizina<br />
N C<br />
H 2<br />
CH=CH<br />
NCH 3<br />
69
Estrategia<br />
Estrategia<br />
C Cl<br />
H<br />
haluro de diarilmetilo<br />
C N<br />
H<br />
HN<br />
NCH 3<br />
K 2 CO 3<br />
HN<br />
K 2 CO 3<br />
BrCH 2 CH=CH Ph<br />
K 2CO 3<br />
N C<br />
H 2<br />
CH=CH<br />
NH<br />
Cinarizina<br />
C N<br />
H<br />
Ciclizina<br />
CH N NH<br />
ClCO<br />
O<br />
CH N N C<br />
HC<br />
NCH 3<br />
C<br />
H<br />
CH=CH<br />
LiAlH 4<br />
70
Ar<br />
Ar C O<br />
DIFENILPIRALINA<br />
DIFENHIDRAMINA<br />
Antihistamínicos H1<br />
O-alquilación<br />
C<br />
H<br />
O<br />
Difenilpiralina<br />
NCH 3<br />
CH O (CH 2) 2N(CH 3) 2<br />
Difenhidramina<br />
71
Difenilpiralina y difenhidramina<br />
(Antihistamínicos H1)<br />
C Br<br />
H<br />
Na 2 CO 3<br />
HO<br />
Na 2 CO 3<br />
HO(CH 2) 2N(CH 3) 2<br />
NCH 3<br />
CH O<br />
Ar<br />
Ar C O<br />
C<br />
H<br />
Difenilpiralina<br />
(CH 2) 2N(CH 3) 2<br />
Difenhidramina<br />
O<br />
Oalquilación<br />
NCH 3<br />
Preparación del 2-dimetilaminoetanol O Me2NH HO(CH2) 2NMe2 72
3.3. Compues<strong>to</strong>s diarilmetánicos Ar C<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
N<br />
O<br />
OH<br />
Ciclizina<br />
Cinarizina<br />
Difenhidramina<br />
Difenilpiralina<br />
Clorfenoxamina<br />
Clemastina<br />
Difenidol<br />
Pirindol<br />
Ar<br />
H<br />
Haluro<br />
diaril<br />
metílico<br />
X<br />
A<br />
Alcohol B<br />
diarilmetílico<br />
Ce<strong>to</strong>na,éster<br />
magnesiano<br />
73<br />
C
B) A PARTIR DE ALCOHOL DIARILAMETÍLICO<br />
Via A<br />
Cl<br />
Cl<br />
Cl<br />
O<br />
ClCOCH 3/ AlCl 3<br />
CH 3<br />
O<br />
Preparación del alcohol diarilmetílico<br />
magnesianos<br />
MgBr<br />
CH 3MgBr<br />
AlCl 3<br />
COCl<br />
Cl<br />
Cl Cl<br />
C OMgBr<br />
CH 3<br />
Via B<br />
H 3O<br />
C OH<br />
CH 3<br />
74
clorfenoxamina<br />
clemastina<br />
(antiH1)<br />
OH<br />
Cl C<br />
CH 3<br />
Alcohol diarilmetílico<br />
NaNH 2<br />
clemastina<br />
Cl C<br />
O<br />
Cl C<br />
Cl C<br />
O(CH 2) 2N(CH 3) 2<br />
CH 3<br />
Cl(CH 2) 2N(CH 3) 2<br />
CH 3<br />
Cl(CH 2) 2<br />
O(CH 2) 2<br />
CH 3<br />
clorfenoxamina<br />
CH 3<br />
N<br />
CH 3<br />
N<br />
75
3.3. Compues<strong>to</strong>s diarilmetánicos Ar C<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
Ar<br />
Ar C<br />
H<br />
N<br />
O<br />
OH<br />
Ciclizina<br />
Cinarizina<br />
Difenhidramina<br />
Difenilpiralina<br />
Clorfenoxamina<br />
Clemastina<br />
Difenidol<br />
Pirindol<br />
Ar<br />
H<br />
Haluro<br />
diaril<br />
metílico<br />
X<br />
A<br />
Alcohol B<br />
diarilmetílico<br />
Ce<strong>to</strong>na,éster<br />
magnesiano<br />
76<br />
C
C) REACCIÓN DE GRIGNARD: difenidol y pirindol<br />
O<br />
Benzofenona<br />
(CETONA)<br />
NH<br />
CH 2=CH COOEt<br />
(Michael)<br />
N (CH 2) 2 COOEt<br />
(ÉSTER)<br />
N (CH 2) 3 Cl<br />
Mg<br />
N (CH 2) 3 MgCl<br />
MgBr<br />
OH<br />
C<br />
(CH 2) 3 N<br />
Difenidol<br />
ANTIEMÉTICO<br />
N (CH 2) 2 C<br />
OH<br />
Pirindol<br />
RELAJANTE MUSCULAR<br />
ANTIPARKINSONIANO<br />
77
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
78
3.4. Compues<strong>to</strong>s diariletilenicos Ar<br />
Tamoxifeno: antitumoral<br />
H O<br />
C C<br />
Et<br />
HCl C C<br />
Et<br />
OH<br />
H 3CO MgBr<br />
H 3O<br />
EtONa<br />
Cl(CH 2) 2N(CH 3) 2<br />
H OH<br />
C C<br />
Et<br />
H<br />
C C<br />
H<br />
OCH 3<br />
C C<br />
Et<br />
Tamoxifeno<br />
Ar<br />
O(CH 2) 2N(CH 3) 2<br />
79
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
80
3.5. Éteres arilalquílicos Ar O R<br />
- Ariloxialcanoles<br />
PRACTOLOL<br />
- Ariloxialquilaminas:<br />
-<br />
FENITOLOXAMINA<br />
Acidos ariloxialcanoicos:<br />
ÁCIDO ETACRÍNICO<br />
Ar O C C<br />
OH<br />
Ar O C C<br />
ESTRATEGIA: ALQUILACIÓN DE FENOLES<br />
N<br />
Ar O C COOH<br />
81
- Ariloxialcanoles: PRACTOLOL (bloqueante -adrenérgico)<br />
H3C O<br />
CHN<br />
OH + CH2 CH<br />
Ar O C C<br />
OH<br />
O<br />
CH2Cl H3C O<br />
CHN<br />
O CH2 CH<br />
OH<br />
CH2Cl NH 2 CH CH 3<br />
CH 3<br />
H3C O<br />
CHN<br />
O CH2 CH<br />
OH<br />
CH2NH Prac<strong>to</strong>lol<br />
O<br />
OH<br />
H3C CHN<br />
O CH2 CH CH2 CH<br />
CH 3<br />
NH 2 CH CH 3<br />
CH 3<br />
CH 3<br />
82<br />
O
- Ariloxialquilaminas:<br />
Feni<strong>to</strong>loxamina (antihistamínico)<br />
CH 2<br />
OH<br />
Cl(CH 2) 2N(CH 3) 2<br />
EtONa<br />
CH 2<br />
O<br />
Feni<strong>to</strong>loxamina<br />
Ar O C C<br />
CH 2<br />
O<br />
(CH 2) 2N(CH 3) 2<br />
N<br />
83
Cl<br />
- Ácidos ariloxialcanoicos: ácido etacrínico (diurético)<br />
Cl<br />
OH<br />
CH 3(CH 2) 2COCl<br />
AlCl 3<br />
acilación de F-C<br />
CH 3CH 2CH<br />
(H 3C) 2NCH 2<br />
EtONa<br />
ClCH 2CO 2Et<br />
Cl<br />
O<br />
C<br />
Cl<br />
CH 3CH 2CH 2<br />
Cl<br />
Cl<br />
Cl<br />
O<br />
C<br />
OCH 2CO 2H<br />
OCH 2CO 2Et<br />
calor<br />
Cl<br />
HCl<br />
H 2O<br />
Cl<br />
OCH 2CO 2H<br />
CH 3CH 2C<br />
Cl<br />
O<br />
C<br />
Cl<br />
OCH 2CO 2H<br />
CH 2O, NH(CH 3) 2<br />
HCl (Mannich)<br />
Cl<br />
CH 2 A. etacrínico<br />
OCH 2CO 2H<br />
84
Mecanismo eliminación<br />
H 3C<br />
H<br />
N CH 3<br />
CH 3<br />
calor<br />
H 3C<br />
CH 2<br />
+ NH(CH 3) 2<br />
85
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
86
3.6. Ácidos arenocarboxílicos y derivados<br />
Ar COOH<br />
A) Derivados del ácido salicílico<br />
(ácido or<strong>to</strong>-hidroxibenzoico)<br />
B) Derivados del ácido p-aminobenzoico<br />
OH<br />
COOH<br />
NH 2<br />
COOH<br />
87
■ A) DERIVADOS DEL ÁCIDO SALICÍLICO<br />
O<br />
O<br />
CH 3<br />
COOH<br />
Aspirina<br />
OH<br />
NH 2<br />
C O<br />
salicilamida<br />
88
■ A) Derivados del ácido salicílico<br />
Síntesis del ÁCIDO SALICÍLICO: síntesis de Kolbe<br />
Na<br />
OH OH<br />
O<br />
NaOH<br />
1. NaOH<br />
2. CO 2<br />
3. H 3O<br />
O O O<br />
C<br />
O<br />
COOH<br />
A. salicílico<br />
COO<br />
H 3O<br />
OH<br />
COO<br />
89
OH 1. NaOH<br />
Fenol<br />
ASPIRINA<br />
2.CO 2<br />
3. H 3O<br />
OH<br />
COOH<br />
A. salicílico<br />
analgésico<br />
antipirético<br />
antiinflama<strong>to</strong>rio<br />
H 3C<br />
O<br />
O<br />
O<br />
- CH 3COOH<br />
CH 3<br />
O<br />
O<br />
CH 3<br />
COOH<br />
Aspirina<br />
90
■ A) Derivados del ácido salicílico<br />
SALICILAMIDA analgésico<br />
OH<br />
Fenol<br />
OH<br />
1. NaOH<br />
2.CO 2<br />
C<br />
3. H 3O<br />
OCH 3<br />
O<br />
NH 3<br />
OH<br />
COOH<br />
A. salicílico<br />
(aminolisis)<br />
antipirético<br />
OH<br />
CH 3OH<br />
H<br />
(Esterificación)<br />
NH 2<br />
C O<br />
salicilamida<br />
91
OH<br />
OH<br />
OH<br />
O<br />
C<br />
O<br />
Salsala<strong>to</strong><br />
O<br />
C<br />
NH 2<br />
C O<br />
salicilamida<br />
O<br />
Benorila<strong>to</strong><br />
Carece de propiedades antiinflama<strong>to</strong>rias<br />
Necesidad de un grupo carboxílico libre<br />
COOH<br />
NH<br />
O<br />
CH 3<br />
Formas biorreversibles<br />
a nivel del grupo<br />
carboxila<strong>to</strong><br />
92
■ B) Derivados del ácido p-aminobenzoico<br />
HO<br />
O<br />
C<br />
● PROCAÍNA: bloqueo de los canales de Na +<br />
anestésico local<br />
NH 2<br />
● METOCLOPRAMIDA: antagonista de los<br />
recep<strong>to</strong>res dopaminérgicos<br />
antiemético, coadyuvante en la<br />
quimioterapia del cáncer: vómi<strong>to</strong>s por<br />
radiación y fármacos ci<strong>to</strong>tóxicos<br />
93
■ B) Derivados del ácido p-aminobenzoico<br />
● Procaína: anestésico local<br />
SOCl 2<br />
HN(Et) 2<br />
CH 3<br />
O 2N<br />
HNO 3<br />
O 2N<br />
O 2N<br />
COCl<br />
CH 3<br />
HOCH 2CH 2Cl<br />
CO 2CH 2CH 2N(Et) 2<br />
KMnO 4<br />
H2N CO2CH2CH2N(Et) 2 Procaína<br />
O 2N<br />
Fe<br />
HCl<br />
O 2N<br />
COOH<br />
CO 2CH 2CH 2Cl<br />
94
■ B) Derivados del ácido p-aminobenzoico<br />
● Me<strong>to</strong>clopramida: antiemético<br />
H 2N<br />
H 3C<br />
H 3C<br />
Cl<br />
O<br />
C<br />
O<br />
C<br />
HN<br />
HN<br />
OCH 3<br />
Cl<br />
Cl<br />
CO 2H<br />
OCH 3<br />
COCl<br />
OCH 3<br />
Ac 2O<br />
H 3C<br />
O<br />
C<br />
CONHCH 2CH 2N(Et) 2<br />
HN<br />
Cl<br />
H 2NCH 2CH 2N(Et) 2<br />
OCH 3<br />
H 3O +<br />
COOH<br />
SOCl 2<br />
95
H 3C<br />
O<br />
C<br />
H 2O/<br />
HN<br />
más reactivo<br />
H<br />
Cl<br />
OCH 3<br />
Hidrólisis quimioselectiva<br />
OCH 3<br />
CONHCH 2CH 2N(Et) 2<br />
H2N CONHCH2CH2N(Et) 2 Me<strong>to</strong>clopramida<br />
Cl<br />
96
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
97
3.7. Anilinas y anilidas<br />
Ar N<br />
O<br />
Ar NH C<br />
● Anilinas: Clorambucilo<br />
anilinas<br />
anilidas<br />
Antitumoral, inhibidor de la síntesis del ADN<br />
● Anilidas: Lidocaína y Bupivacaína<br />
Anestésicos locales<br />
98
● Anilinas: clorambucilo (antineoplásico)<br />
CH 3OH, HCl<br />
esterificación<br />
(CH 2) 3CO 2CH 3<br />
O 2N<br />
HNO 3, H 2SO 4<br />
nitración<br />
e hidrólisis<br />
(CH 2) 3CO 2CH 3<br />
H 2O/<br />
O 2N<br />
1 H 2/Pd<br />
O<br />
2 HOCH2CH2 N<br />
(CH2) 3CO2CH3 HOCH2CH2 ClCH 2CH 2<br />
ClCH 2CH 2<br />
N<br />
(CH 2) 3CO 2CH 3<br />
H<br />
Hidrólisis<br />
H 2N<br />
ClCH 2CH 2<br />
ClCH 2CH 2<br />
(CH 2) 3CO 2H<br />
SOCl 2<br />
N<br />
Ar N<br />
Clorambucilo<br />
(CH 2) 3CO 2CH 3<br />
(CH 2) 3CO 2H<br />
99
● Anilidas: lidocaína y bupivacaína<br />
Anestésicos locales<br />
CH 3<br />
CH 3<br />
NH(Et) 2<br />
NH 2<br />
alquilación<br />
Cl<br />
O<br />
C CH 2Cl<br />
acilación<br />
CH 3<br />
N<br />
H<br />
CH 3<br />
O<br />
C<br />
CH 2N(Et) 2<br />
Lidocaína<br />
CH 3<br />
N<br />
H<br />
CH 3<br />
O<br />
C<br />
O<br />
Ar NH C<br />
CH 2Cl<br />
100
● Anilidas: lidocaína y bupivacaína<br />
CH 3<br />
CH 3<br />
NH 2<br />
ICH 2(CH 2) 2CH 3<br />
alquilación<br />
CH 3<br />
N<br />
H<br />
CH 3<br />
O<br />
C<br />
ó<br />
N<br />
Cl<br />
O<br />
C<br />
N<br />
O<br />
O<br />
C O C OEt<br />
N<br />
anhídrido mix<strong>to</strong><br />
CH 3<br />
N<br />
H<br />
CH 3<br />
CH 2(CH 2) 2CH 3<br />
O<br />
C<br />
N<br />
bupivacaína<br />
CH 3<br />
N<br />
H<br />
CH 3<br />
CH 2(CH 2) 2CH 3<br />
H 2, Pt<br />
O<br />
C<br />
reducción<br />
N<br />
101
N<br />
ácido<br />
Síntesis del anhídrido mix<strong>to</strong><br />
O<br />
C OH<br />
Cl<br />
O<br />
COEt<br />
Más reactivo que un anhídrido<br />
+<br />
O<br />
Anhídrido<br />
O<br />
O<br />
C O C OEt<br />
N<br />
anhídrido mix<strong>to</strong><br />
C O C R<br />
O<br />
O<br />
O<br />
C O C O<br />
Ester<br />
102
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
103
3.8. Sulfonamidas y sulfonilureas<br />
●Sulfonamidas<br />
●Sulfonilureas<br />
O<br />
Ar S<br />
O<br />
NH<br />
sulfonilo<br />
O<br />
O<br />
Ar S NH C<br />
O Urea<br />
N<br />
104
●Sulfonamidas Ar S NH<br />
- Diuréticas<br />
- Antibacterianas<br />
Estrategia sintética<br />
1. Clorosulfonación de anillos bencénicos<br />
2. Aminolisis<br />
O<br />
O<br />
105
● Sulfonamidas diuréticas: DICLORFENAMIDA<br />
Mecanismo de acción: inhibición de la anhidrasa<br />
carbónica<br />
HO<br />
Cl<br />
PCl 5<br />
O<br />
Cl S<br />
O<br />
SEar<br />
Cl<br />
O<br />
S<br />
O<br />
O<br />
Cl S Cl<br />
Cl<br />
OH (á. clorosulfónico)<br />
O<br />
NH 3<br />
H 2N<br />
O<br />
Cl<br />
O<br />
S<br />
O<br />
O<br />
HO S Cl<br />
S<br />
O<br />
Cl<br />
O<br />
O<br />
Cl S<br />
O<br />
NH2 Cl<br />
Diclorfenamida<br />
106
● SULFONAMIDAS ANTIBACTERIANAS<br />
Característica estructural: derivadas del<br />
á. p-aminobencenosulfónico<br />
Antagonistas competitivas del á. paminobenzoico<br />
(PABA)<br />
Estrategia sintética a partir de la anilina<br />
(H 2N-Ar)<br />
1. Protección del grupo amino<br />
2. Clorosulfonación del anillo bencénico<br />
3. Aminolisis<br />
4. Desprotección<br />
O<br />
NH 2<br />
NH 2<br />
S O<br />
NHR<br />
COOH<br />
A. p-aminobenzoico<br />
(PABA)<br />
107
●Sulfonamidas antibacterianas<br />
- Estrategia sintética a partir de anilina<br />
H 2N<br />
Anilina<br />
H3C C HN<br />
amida<br />
Cl S<br />
O<br />
O<br />
EtO<br />
H3C C<br />
O<br />
C<br />
HN<br />
HN<br />
SO2Cl NH2R aminolisis<br />
EtO<br />
H3C C<br />
O<br />
C<br />
HN<br />
HN<br />
SO2NHR NaOH<br />
desprotección<br />
O<br />
Cl C<br />
o<br />
OEt<br />
Ac2O O<br />
EtO C HN<br />
carbama<strong>to</strong><br />
O<br />
H 2N SO 2NHR<br />
sulfonamida<br />
O<br />
O<br />
OH<br />
clorosulfonación<br />
108
●Sulfonamidas antibacterianas<br />
SULFATIAZOL: infecciones urinarias<br />
H 2N<br />
Anilina<br />
NaOH<br />
Ac 2O<br />
O<br />
H3C C HN<br />
amida<br />
O<br />
Cl S<br />
O<br />
OH<br />
clorosulfonación<br />
O<br />
H2N S O<br />
H3C C HN<br />
SO2Cl aminolisis<br />
H3C C HN<br />
SO2NH desprotección<br />
sulfatiazol<br />
N<br />
H 2N SO 2NH<br />
N<br />
S<br />
109<br />
N<br />
S
3.8. Sulfonamidas y sulfonilureas<br />
sulfonilo<br />
O<br />
● SULFONILUREAS<br />
O<br />
Ar S NH C<br />
ESTRATEGIA SINTÉTICA:<br />
O Urea<br />
A) Arilsulfonamida + cloroformia<strong>to</strong> de alquilo<br />
+ amina<br />
B) Arilsulfonamida + isociana<strong>to</strong><br />
N<br />
110
● Sulfonilureas: TOLBUTAMIDA<br />
antidiabético oral estimulación de la liberación de insulina<br />
Estrategia A<br />
H 3C<br />
O<br />
S<br />
Arilsulfonamida<br />
H 3C<br />
O<br />
O<br />
S<br />
O<br />
NH 2<br />
Éster N-arilsulfonilcarbámico<br />
O<br />
H 3C S<br />
O<br />
NH<br />
NH<br />
O<br />
O<br />
C<br />
C<br />
O<br />
+ Cl C<br />
OEt<br />
OEt<br />
cloroformia<strong>to</strong> de etilo<br />
NH(CH 2) 3CH 3<br />
Na 2CO 3<br />
NH 2 (CH 2) 3CH 3<br />
111
●Sulfonilureas: Tolbutamida<br />
H 3C<br />
O<br />
S<br />
O<br />
Arilsulfonamida<br />
O<br />
H 3C S<br />
O<br />
H<br />
N<br />
H<br />
NH 2<br />
O<br />
C<br />
O<br />
H 3C S<br />
O<br />
+ O C N<br />
N<br />
NH<br />
isociana<strong>to</strong> de butilo<br />
O<br />
C<br />
Bu<br />
Bu H 3C S<br />
NH(CH 2) 3CH 3<br />
Estrategia B<br />
O<br />
O<br />
H<br />
N<br />
H<br />
O<br />
C<br />
N Bu<br />
112
3. COMPUESTOS AROMATICOS MONOCÍCLICOS<br />
3.1. Arilalquilaminas<br />
3.2. Ácidos arilalcanoicos y derivados<br />
3.3. Compues<strong>to</strong>s diarilmetánicos<br />
3.4. Compues<strong>to</strong>s diariletilénicos<br />
3.5. Éteres arilalquílicos<br />
3.6. Ácidos arenocarboxílicos y sus derivados<br />
3.7. Anilinas y anilidas<br />
3.8. Sulfonamidas y sulfonilureas<br />
4. COMPUESTOS AROMATICOS POLICÍCLICOS<br />
4.1. Derivados del naftaleno<br />
113
• Naftidofurilo: vasodilatador<br />
CO 2Et<br />
CH 2<br />
CO 2Et<br />
H 2/ Pt<br />
CH 2Cl<br />
NaOEt<br />
EtO2C CH<br />
EtO2C CO 2Et<br />
CH<br />
CO 2Et<br />
CH 2<br />
CO2Et EtO2C C CH2 CH 2<br />
Cl<br />
CH 2<br />
O NaOEt<br />
O<br />
1. KOH<br />
2. HCl<br />
3. calor<br />
O<br />
CO 2Et<br />
C<br />
CO 2Et<br />
EtO2C CH<br />
EtO2C CH 2<br />
O<br />
HO2C CH CH2 H 2C<br />
Naftidofurilo<br />
CH 2<br />
O<br />
O<br />
114