to get the file - OCW CEU
to get the file - OCW CEU
to get the file - OCW CEU
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
EJERCICIOS SOBRE COMPUESTOS HETEROCÍCLICOS<br />
1 El carbazerán es un cardiotónico con estructura de benzopiridazina, que representa a los<br />
nuevos agentes inotrópicos de síntesis. El compues<strong>to</strong> puede ser sintetizado a través de la<br />
secuencia que se muestra a continuación. Complétala adecuadamente.<br />
MeO<br />
MeO<br />
SOLUCIÓN<br />
MeO<br />
MeO<br />
OCONHEt<br />
N<br />
H<br />
CHO<br />
COOH<br />
CHO<br />
COOH<br />
H 2NNH 2<br />
H 2NNH 2<br />
MeO<br />
MeO<br />
A<br />
MeO<br />
MeO<br />
N<br />
N<br />
N<br />
POCl 3<br />
A<br />
OCONHEt<br />
B<br />
O<br />
N<br />
NH<br />
Carbazerán<br />
OCONHEt<br />
N<br />
H<br />
POCl 3<br />
Carbazerán<br />
2 La azimilida es un nuevo fármaco antiarrítmico bloqueante de los canales de potasio, que se<br />
puede sintetizar a partir del benzaldehído. Algunos de los intermedios claves de su síntesis se<br />
representan en el esquema que sigue. Propón las estructuras de los compues<strong>to</strong>s A, B, C y D.<br />
CH 3<br />
N<br />
N<br />
O<br />
O<br />
H + NH2NHC N<br />
O N<br />
N<br />
O<br />
Azimilida<br />
NH 2<br />
O<br />
− H2O<br />
A<br />
Cl<br />
NaOEt/EtOH<br />
ClCH 2CO 2Et<br />
B<br />
MeO<br />
MeO<br />
NaH<br />
Br(CH 2) 4Cl<br />
B<br />
Cl<br />
N<br />
N
C<br />
SOLUCIÓN<br />
I<br />
O<br />
O<br />
H<br />
O<br />
NaI<br />
CH 3COCH 3<br />
H<br />
N<br />
N<br />
N<br />
N<br />
N<br />
N<br />
D<br />
+ NH2NH O<br />
C<br />
O<br />
O<br />
B<br />
D<br />
HN N CH3 NH 2<br />
NaH<br />
Br(CH 2) 4Cl<br />
HN N CH3 H 2O<br />
CH 3<br />
Cl<br />
N<br />
H 3C<br />
N<br />
N<br />
N<br />
O<br />
O<br />
N<br />
N<br />
N<br />
O<br />
O<br />
NNH C<br />
N<br />
N<br />
N<br />
O<br />
O<br />
N<br />
N<br />
N<br />
O<br />
C<br />
NH 2<br />
A<br />
NaOEt/EtOH<br />
ClCH 2CO 2Et<br />
NaI<br />
CH 3COCH 3<br />
3 Uno de los representantes más característicos de los derivados de 2,4-diamino-quinazolina<br />
empleados como antihipertensivos es el antagonista α-adrenérgico prazosina. Escribe los<br />
reactivos A y B necesarios para completar la siguiente síntesis de la prazosina, así como la<br />
estructura de los produc<strong>to</strong>s que se obtienen en cada etapa.<br />
CH 3O<br />
CH 3O CHO<br />
SOLUCIÓN<br />
CH 3O<br />
CH 3O CHO<br />
1. A<br />
2. [Ox]<br />
3. SOCl 2<br />
4. NH3<br />
5. H 2/cat<br />
CH 3O<br />
CH3O C<br />
O<br />
NH 2<br />
Prazosina<br />
NH 2<br />
5. urea<br />
6. B<br />
7. NH 3<br />
8.<br />
HN<br />
HNO3 CH3O NO2 [Ox] CH3O<br />
A<br />
CH 3O CHO<br />
N<br />
CH 3O<br />
CH 3O<br />
O<br />
O<br />
NO 2<br />
CH 3O COOH<br />
N Cl<br />
Cl<br />
N<br />
1. SOCl 2<br />
2. NH 3
CH 3O<br />
CH3O C<br />
O<br />
POCl 3<br />
PCl 5<br />
B<br />
CH 3O<br />
CH 3O<br />
NO 2<br />
NH 2 cat<br />
CH 3O<br />
CH 3O<br />
N<br />
NH<br />
NH 2<br />
H 2<br />
N<br />
N<br />
CH 3O<br />
CH 3O C<br />
O<br />
N<br />
Cl<br />
NH<br />
O<br />
Cl<br />
Prazosina<br />
NH 2<br />
O<br />
NH 3<br />
NH 2<br />
O<br />
CH 3O<br />
CH 3O<br />
4 Completa la síntesis del antihipertensivo losulazina.<br />
F 3C<br />
1. KOH<br />
2. H 3O +<br />
POCl 3<br />
NH 2<br />
+<br />
EtO 2C<br />
3<br />
6<br />
F 3C<br />
CO 2Et<br />
OEt<br />
calor<br />
NH<br />
N<br />
1<br />
NH 2<br />
O<br />
N<br />
NH 2<br />
Losulazina<br />
N<br />
N SO2<br />
calor<br />
F<br />
CH 3O<br />
CH 3O<br />
NH<br />
NH 2<br />
Cl<br />
4 5<br />
2<br />
HN<br />
H<br />
N<br />
O<br />
N<br />
O<br />
NH<br />
O<br />
O
HN<br />
SOLUCIÓN<br />
H<br />
N<br />
N<br />
H<br />
F 3C<br />
O 2N<br />
NH<br />
F 3C<br />
+<br />
8<br />
O<br />
N<br />
H<br />
SO 2Cl<br />
F<br />
NH 2<br />
CO 2Et<br />
2<br />
H 2<br />
Pd-C<br />
+<br />
EtO 2C<br />
1. KOH<br />
2. H3O +<br />
SO2Cl O<br />
+ HN N S<br />
F<br />
O<br />
C<br />
N<br />
O<br />
N S<br />
O<br />
8<br />
F<br />
O<br />
7<br />
H 2<br />
Pd<br />
OEt<br />
9<br />
CO 2Et<br />
F 3C<br />
7<br />
F 3C<br />
F<br />
O<br />
N<br />
H<br />
O 2N<br />
6<br />
H 2N<br />
O 2N<br />
6<br />
COCl<br />
Losulazina<br />
EtO 2C<br />
CO 2Et<br />
F3C N<br />
H<br />
OEt<br />
1<br />
CO 2H<br />
Cl<br />
N<br />
3<br />
O<br />
C<br />
calor<br />
POCl 3<br />
COCl<br />
N<br />
O<br />
N S<br />
O<br />
F 3C<br />
F 3C<br />
9<br />
F<br />
calor<br />
O<br />
N<br />
H<br />
OH<br />
N<br />
4<br />
5
6<br />
F 3C<br />
Cl<br />
N<br />
F 3C<br />
HN<br />
N<br />
O<br />
N<br />
Losulazina<br />
N SO2<br />
5 La preparación del vasodilatador periférico y cerebral naftidrofurilo, utilizado para el<br />
tratamien<strong>to</strong> de la insuficiencia circula<strong>to</strong>ria cerebral y periférica, se indica a continuación.<br />
Completa la secuencia sintética.<br />
O<br />
SOLUCIÓN<br />
O<br />
HCHO<br />
HCl<br />
O CH 2 C<br />
HCHO<br />
HCl<br />
A<br />
CO 2Et<br />
CH 2<br />
CO 2Et<br />
O CH CO2Et 2CH CO2Et C<br />
1. KOH<br />
2. HCl<br />
3. calor<br />
O CH 2Cl<br />
NaOEt<br />
CH 2(CO 2Et) 2<br />
A<br />
1. KOH<br />
2. HCl<br />
3. calor<br />
1. NaOEt<br />
2.<br />
O CH CO2H 2 CH<br />
CH2 Naftidrofurilo<br />
B<br />
H2 Pt/C<br />
Naftidrofurilo<br />
F<br />
C<br />
1. NaOEt<br />
2. D<br />
NaOEt<br />
O<br />
CH2(CO2Et) 2 B<br />
CH CO2Et 2CH CO2Et CH 2Cl<br />
D<br />
O CH CO2Et 2 C CO2Et 6 El timolol es un fármaco β−bloqueante adrenérgico con estructura de ariloxipropanolamina, de<br />
aplicación terapéutica en el tratamien<strong>to</strong> del glaucoma. El timolol posee un carbono asimétrico,<br />
sin embargo, sólo se emplea el enantiómero (S)(−).<br />
CH 2<br />
H2 Pt/C
a) La síntesis enantioespecífica del (S)-timolol puede llevarse a cabo a partir de Dgliceraldehído<br />
con terc-butilamina y posterior hidrogenación del produc<strong>to</strong> formado.<br />
SOLUCIÓN<br />
Escribe la estructura de los compues<strong>to</strong>s E y F de la secuencia descrita:<br />
H OH<br />
C<br />
HOH2C CHO<br />
D-gliceraldehído<br />
t-Bu-NH2 H 2 / Pd-C<br />
E F<br />
b) La última etapa de la síntesis<br />
se muestra a continuación.<br />
Escribe la estructura del timolol<br />
con la estereoquímica adecuada.<br />
F +<br />
Cl<br />
N S<br />
N<br />
N<br />
O<br />
Timolol<br />
a) Los compues<strong>to</strong>s E y F han cambiado la notación esteroquímica de (R) a (S), no por<br />
reacción en el carbono quiral sino por cambio del orden de prioridad de los sustituyentes en<br />
dicho carbono.<br />
H<br />
HOH 2C<br />
C<br />
H<br />
HOH 2C<br />
OH<br />
CHO<br />
C<br />
OH<br />
CH 2<br />
t-Bu-NH 2<br />
NH t-Bu<br />
+<br />
Cl<br />
N S<br />
H OH<br />
C<br />
HOH2C CH N CMe3 E<br />
N<br />
N<br />
O<br />
O<br />
N<br />
H 2<br />
Pd-C<br />
N N<br />
S<br />
H<br />
HOH 2C<br />
C<br />
F<br />
OH<br />
CH 2<br />
H OH H<br />
O N<br />
t-Bu<br />
Timolol<br />
7 El sistema de 1,4-dihidropiridina presente en la nifedipina, cabeza de serie de una de las<br />
familias estructurales bloqueantes de los canales de calcio utilizadas terapéuticamente como<br />
vasodilatadores coronarios, es obtenido en la mayoría de los casos mediante la síntesis de<br />
Hantzsch. Sobre esta base, propón una síntesis para la nifedipina, 2,6-dimetil-4-(2-nitrofenil)-<br />
1,4-dihidropiridina-3,5-dicarboxila<strong>to</strong> de dimetilo.<br />
CH 3CO 2<br />
CH 3<br />
N<br />
H<br />
Nifedipina<br />
NO 2<br />
CO 2CH 3<br />
CH 3<br />
N<br />
H<br />
CMe 3
O H<br />
SOLUCIÓN<br />
NO2 base<br />
+ 1<br />
CH 3COCH 2COOCH 3<br />
NH 3 + CH 3COCH 2COOCH 3 2<br />
CH 3CO 2<br />
H 3C<br />
1<br />
O<br />
NO 2<br />
CO 2CH 3<br />
Adición de<br />
Michael<br />
CO 2CH 3<br />
HN CH3 H2N CH3 Imina 2 Enamina<br />
Nifedipina<br />
8 Los sistemas 1,4-dihidropiridina se encuentran presentes en compues<strong>to</strong>s utilizados<br />
terapéuticamente como bloqueantes de los canales de iones calcio. Completa el siguiente<br />
esquema correspondiente a la síntesis de la felodipina, dihidropiridina sustituida de forma no<br />
simétrica, teniendo en cuenta que la obtención se puede llevar a cabo a través de una<br />
modificación de las condiciones de la reacción de Hantzsch.<br />
O H<br />
SOLUCIÓN<br />
MeO 2C<br />
H 3C<br />
Cl<br />
Cl<br />
+ CH3COCH2COOMe 1<br />
base<br />
NH 3 + CH 3COCH 2COOEt 2<br />
1<br />
O<br />
Cl<br />
Cl<br />
HN<br />
H 2N<br />
2<br />
CO 2Et<br />
CH 3<br />
CO 2Et<br />
CH 3<br />
MeO 2C<br />
Felodipina<br />
Cl<br />
H3C N CH3 H<br />
Felodipina<br />
Cl<br />
CO2Et 9 El minoxidilo es un agente activador selectivo de los canales de potasio, lo que produce un<br />
efec<strong>to</strong> vasodilatador, sin embargo, su empleo terapéutico principal se debe a sus efec<strong>to</strong>s<br />
secundarios como antialopécico.<br />
Una posible estrategia para la obtención del minoxidilo podría ser a partir del ácido barbitúrico<br />
como precursor. Cuando éste se trata con oxicloruro de fósforo, POCl3, se obtiene la 2,4,6-
tricloropirimidina.<br />
Sin embargo, los tres á<strong>to</strong>mos de cloro de la 2,4,6-tricloropirimidina no son igualmente reactivos<br />
y es más fácil sustituir los que se encuentran en las posiciones 2 y 4. Así pues, el tratamien<strong>to</strong><br />
de la 2,4,6-tricloropirimidina con amoniaco produce la sustitución de es<strong>to</strong>s dos á<strong>to</strong>mos de cloro<br />
por grupos amino, conduciendo a la 6-cloro-2,4-diaminopirimidina.<br />
Completa el siguiente esquema que continúa la síntesis del minoxidilo partiendo de la 6-cloro-<br />
2,4-diaminopirimidina.<br />
Cl<br />
N NH 2<br />
N<br />
NH 2<br />
SOLUCIÓN<br />
a<br />
X<br />
b<br />
Y<br />
c<br />
N<br />
Minoxidilo<br />
N NH 2<br />
Primero, sustituiremos el á<strong>to</strong>mo de cloro en posición 6 de la 6-cloro-2,4-diaminopirimidina por<br />
el nucleófilo, anión 2,4-diclorofenóxido.<br />
Cl<br />
N NH2<br />
N<br />
NH 2<br />
Cl<br />
Cl<br />
KOH<br />
a<br />
OH<br />
Cl<br />
Cl<br />
X<br />
O<br />
N<br />
N<br />
NH 2<br />
N NH 2<br />
El á<strong>to</strong>mo de nitrógeno de la posición 3 se transforma en N-óxido por tratamien<strong>to</strong> con MCPBA<br />
(ácido m-cloroperbenzoico). Por último, se sustituye nucleofílicamente la posición 6 por la<br />
piperidina.<br />
MCPBA<br />
b<br />
Cl<br />
Cl<br />
Y<br />
O<br />
N NH 2<br />
NH 2<br />
N<br />
O<br />
c<br />
NH<br />
NH 2<br />
N<br />
O<br />
N NH 2<br />
N<br />
O<br />
NH2 Minoxidilo<br />
10 En los últimos años han aparecido en terapéutica una serie de compues<strong>to</strong>s antibacterianos<br />
con estructura de 4-quinolonas, cuyo mecanismo de acción, aunque no <strong>to</strong>talmente elucidado,<br />
está relacionado la modificación de la estructura terciaria del ADN bacteriano. Uno de los<br />
primeros antibacterianos de esta familia fue el ácido nalidíxico, cuya síntesis se muestra a<br />
continuación. Complétala adecuadamente.
SOLUCIÓN<br />
Me N N<br />
H<br />
Me<br />
1. HNa<br />
+<br />
N NH2 EtO2C CO2Et OEt<br />
2. CH 3CH 2I<br />
EtO 2C CO 2Et<br />
C<br />
H 3O +<br />
O<br />
A. nalidixico<br />
CO 2Et<br />
A calor<br />
Me N N<br />
Me N N<br />
A<br />
H<br />
B<br />
Et<br />
C<br />
O<br />
Me N N<br />
Et<br />
A. nalidíxico<br />
CO 2H<br />
B<br />
O<br />
CO 2Et<br />
11 El ácido oxolínico es una quinolona antibacteriana que surgió poco después del ácido<br />
nalidíxico y, aunque presenta un perfil terapéutico interesante, la rápida aparición de resistencias y<br />
su espectro relativamente reducido han limitado su uso. Completa adecuadamente la secuencia<br />
sintética que conduce al ácido oxolínico.<br />
SOLUCIÓN<br />
O<br />
1. HNa<br />
EtO 2C CO 2Et<br />
O N<br />
H<br />
O<br />
O<br />
2. CH 3CH 2I<br />
O<br />
+<br />
NH2 C<br />
H 3O +<br />
O<br />
EtO 2C CO 2Et<br />
OEt<br />
A. oxolínico<br />
CO 2Et O<br />
A calor<br />
O N<br />
O N<br />
A<br />
H B Et<br />
C<br />
O<br />
CO 2Et<br />
B
O<br />
O<br />
O N<br />
Et<br />
A. oxolínico<br />
CO 2H<br />
12 Cefalosporinas con utilidad terapéutica, entre las cuales se encuentra la cefalotina, son<br />
preparadas fundamentalmente mediante reacciones de acilación del 7-ACA con diversos<br />
derivados de ácidos carboxílicos. Completa la siguiente secuencia sintética que conduce a la<br />
obtención de cefalotina partiendo de tiofeno y 7-ACA.<br />
H 2N<br />
S<br />
O<br />
SOCl 2<br />
H<br />
S<br />
N<br />
SOLUCIÓN<br />
S<br />
S<br />
7-ACA<br />
S<br />
CH2OCOCH3 CO2H O<br />
H H<br />
HCl<br />
O<br />
D 7-ACA<br />
H H<br />
HCl<br />
COOH<br />
C<br />
S<br />
A<br />
(C 6H 5SCl)<br />
S<br />
A<br />
SOCl 2<br />
CH 2CONH<br />
Cefalotina<br />
KCN<br />
Cefalotina<br />
O<br />
Cl<br />
H S<br />
N<br />
S<br />
B<br />
KCN<br />
S<br />
CH 2CONH<br />
O<br />
Cefalotina<br />
1. NaOH<br />
2. H3O +<br />
D<br />
S<br />
COCl<br />
CH2OCOCH3 CO2H C<br />
H S<br />
N<br />
CN<br />
B<br />
CH2OCOCH3 CO2H 7-ACA<br />
1. NaOH<br />
2. H 3O +
13 El grupo bencenosulfonamida se encuentra presente en muchos compues<strong>to</strong>s con diferentes<br />
actividades farmacológicas, como agentes antibacterianos, diuréticos, o antidiabéticos orales.<br />
Completa la secuencia sintética para la obtención de la sulfadime<strong>to</strong>xina (madribón®),<br />
sulfonamida antibacteriana de elevada vida media, utilizada en el tratamien<strong>to</strong> de infecciones<br />
sistémicas.<br />
CN<br />
COOEt<br />
SOLUCIÓN<br />
NH 2<br />
Anilina<br />
CN<br />
COOEt<br />
Anilina<br />
Ac 2O<br />
H2N + O<br />
H2N A + D E<br />
Ac 2O<br />
MeONa/MeOH<br />
MeO<br />
2 equiv<br />
N<br />
OMe<br />
H<br />
+<br />
2N<br />
O<br />
H2N N NH 2<br />
D<br />
+<br />
B<br />
NaOH<br />
NHCOCH 3<br />
H 2N<br />
MeO<br />
EtOH<br />
SO 2Cl<br />
N<br />
N<br />
NHCOCH 3<br />
A<br />
NHCOCH 3<br />
POCl 3<br />
HN<br />
O<br />
OMe<br />
D<br />
C<br />
Sulfadime<strong>to</strong>xina<br />
ClSO 3H<br />
NH<br />
O<br />
NH<br />
B<br />
MeO<br />
N<br />
A<br />
MeONa/MeOH<br />
ClSO 2<br />
POCl 3<br />
OMe<br />
N<br />
2 equiv<br />
NHSO 2<br />
E<br />
A<br />
H 2N<br />
Cl<br />
D<br />
NHCOCH 3<br />
N<br />
N<br />
C<br />
Cl<br />
NHCOCH 3
NaOH<br />
MeO<br />
N<br />
OMe<br />
N<br />
NHSO 2<br />
Sulfadime<strong>to</strong>xina<br />
14 Completa la siguiente secuencia sintética que conduce a la obtención de la<br />
sulfonamida antibacteriana de acción sistémica, sulfame<strong>to</strong>xipiridazina.<br />
NH 2<br />
ClCO 2Et<br />
ClSO3H A B<br />
O<br />
NH 2<br />
C + D<br />
NH<br />
NH<br />
POCl3 E<br />
NH3 (1 equiv)<br />
F (C4H4ClN3) O<br />
G<br />
H2N SO2NH N N<br />
OCH3 1. B<br />
2. NaOH<br />
H<br />
SOLUCIÓN<br />
NHCO 2Et<br />
A<br />
Cl<br />
N<br />
N<br />
Cl<br />
Sulfame<strong>to</strong>xipiridazina<br />
NHCO 2Et<br />
SO 2Cl<br />
B<br />
NH 2<br />
Cl<br />
E F<br />
N<br />
N<br />
G<br />
O<br />
O<br />
CH 3ONa<br />
OEt<br />
OEt<br />
C<br />
H 2N<br />
D<br />
NH 2<br />
NH 2<br />
N<br />
N<br />
OCH3 H<br />
15 Las tetraciclinas constituyen una familia de antibióticos de amplio espectro. Aunque la mayoría<br />
de las tetraciclinas proceden de procesos de fermentación a partir de especies de<br />
Strep<strong>to</strong>myces, algunas transformaciones semisintéticas son especialmente interesantes por<br />
conducir a tetraciclinas más estables o con propiedades fisicoquímicas más adecuadas. Tal es<br />
el caso de la rolitetraciclina, profármaco de la tetraciclina que se prepara por reacción de la<br />
tetraciclina con formaldehído y pirrolidina.<br />
a) Escribe la estructura de la rolitetraciclina, explicando detalladamente la reacción que<br />
tiene lugar y justifica por qué, en este caso, la reacción ocurre en el á<strong>to</strong>mo de nitrógeno del<br />
grupo carboxamido.
) ¿Cuál es el objetivo de esta modificación sintética?<br />
OH O OH O<br />
OH<br />
Tetraciclina<br />
CONH 2<br />
H OH<br />
CH3 OH H N(CH3) 2<br />
SOLUCIÓN<br />
a)<br />
OH O OH O<br />
OH<br />
+<br />
CONH 2<br />
H<br />
OH<br />
CH3 OH H N(CH3) 2<br />
H<br />
O<br />
H + NH<br />
H<br />
O<br />
Rolitetraciclina<br />
Tetraciclina Rolitetraciclina<br />
H<br />
NH<br />
OH O OH O<br />
OH<br />
CH 3 OH<br />
H<br />
O<br />
N<br />
H<br />
OH<br />
H N(CH 3) 2<br />
La rolitetraciclina es resultado de una reacción de Mannich del grupo carboxamido de la<br />
tetraciclina con la sal de iminio resultante de la condensación entre el formaldehído y la<br />
pirrolidina.<br />
O<br />
H H<br />
+ NH H2C N<br />
OH O<br />
OH<br />
CONH 2<br />
H<br />
OH<br />
H N(CH3) 2<br />
Sal de iminio<br />
H 2C<br />
N<br />
Sal de iminio<br />
− H +<br />
OH O O<br />
OH<br />
N<br />
H<br />
H OH<br />
H N(CH3) 2<br />
Tetraciclina Rolitetraciclina<br />
La conjugación del carbonilo del grupo carboxamido con el sistema 1,3-dicetónico en el anillo<br />
de tetraciclina, le confiere al á<strong>to</strong>mo de nitrógeno de la amida una elevada nucleofilia, lo que<br />
hace que presente una reactividad inusual.<br />
b) La rolitetraciclina es un profármaco de la tetraciclina, que revierte por hidrólisis a la tetraciclina,<br />
diseñado con el obje<strong>to</strong> de aumentar la solubilidad en agua de la tetraciclina para su<br />
incorporación en formas farmacéutica acuosas<br />
16 La pefloxacina es un antibiótico perteneciente al grupo de las quinolonas antibacterianas,<br />
activo contra las infecciones producidas por Pseudomonas aeruginosa. Estructuralmente se<br />
caracteriza por la presencia en el anillo de quinolona de un á<strong>to</strong>mo de fluor en posición 6 y un<br />
res<strong>to</strong> de piperazina en posición 7, sustituyentes que favorecen que se retrase la aparición de<br />
N<br />
N
esistencias bacterianas, confiriéndole, por tan<strong>to</strong>, una mayor utilidad terapéutica. La<br />
pefloxacina puede ser sintetizada a través de la secuencia que se muestra a continuación.<br />
Dibuja la estructura de la pefloxacina y de los compues<strong>to</strong>s indicados con letras<br />
F<br />
+<br />
Cl NH2 SOLUCIÓN<br />
Pefloxacina<br />
F<br />
+<br />
Cl NH2 F<br />
O<br />
Cl N<br />
H<br />
F<br />
EtO 2C CO 2Et<br />
OEt<br />
HN NMe<br />
EtO 2C CO 2Et<br />
CO 2Et<br />
B<br />
O<br />
Cl N<br />
H<br />
OEt<br />
CO 2H<br />
D<br />
1. NaH<br />
2. EtBr<br />
D<br />
A calor<br />
HN NMe<br />
H 3O +<br />
F<br />
B<br />
C<br />
EtO 2C<br />
Cl N<br />
H<br />
F<br />
O<br />
Cl N<br />
1. NaH<br />
2. EtBr<br />
A<br />
Et<br />
Me<br />
N<br />
CO 2Et<br />
CO 2Et<br />
C<br />
F<br />
N N<br />
calor<br />
O<br />
Et<br />
H 3O +<br />
Pefloxacina<br />
CO 2H<br />
17 El compues<strong>to</strong> N es un intermedio utilizado en la preparación de cefalosporinas semisintéticas,<br />
como por ejemplo la cefotaxima.<br />
CH 3O<br />
N<br />
N<br />
COOEt<br />
S<br />
N<br />
NH 2<br />
H 2N<br />
S<br />
N<br />
N<br />
O<br />
O<br />
N<br />
N<br />
H H<br />
O CH3 Cefotaxima<br />
COOH<br />
S<br />
O<br />
O CH 3<br />
Diseña una síntesis que conduzca al compues<strong>to</strong> N partiendo del compues<strong>to</strong> P.
HO N<br />
P<br />
SOLUCIÓN<br />
HO N<br />
P<br />
CH 3O N<br />
COOEt<br />
COOEt<br />
O<br />
CH 3<br />
COOEt<br />
O<br />
CH 3O<br />
CH3 N S<br />
O<br />
CH 2 Br<br />
CH 3<br />
S C<br />
O<br />
O<br />
S<br />
O<br />
CH3 O<br />
K 2CO 3<br />
NH 2<br />
NH 2<br />
(tiourea)<br />
CH 3O<br />
N<br />
COOEt<br />
CH 3O N<br />
N<br />
COOEt<br />
N S<br />
N<br />
NH 2<br />
COOEt<br />
O<br />
18 El desarrollo de algunos cánceres de pecho está asociado a la hormona sexual femenina,<br />
estrógeno. Una posible terapia consiste en la administración de compues<strong>to</strong>s que inhiban la<br />
producción de estrógeno. A continuación se indica la síntesis de la aminoglutetimida,<br />
compues<strong>to</strong> que bloquea la biosíntesis de estrógeno del organismo, inhibiendo la aromatasa,<br />
enzima clave en la transformación de andrógenos a estrógenos. ¿Cuál es la estructura de los<br />
reactivos y los produc<strong>to</strong>s indicados con una letra?<br />
CN<br />
NaNH 2<br />
I<br />
Et<br />
CH3COOH O2N Et<br />
H2SO4 O<br />
N<br />
H<br />
O<br />
SOLUCIÓN<br />
CN<br />
NaNH 2<br />
Et I<br />
N<br />
CH 3<br />
NH 2<br />
A<br />
HNO3 B<br />
NaNH2 C<br />
H2SO4 H2C CH COOCH3 H<br />
CN<br />
Et<br />
A<br />
H 2<br />
Pd<br />
HNO 3<br />
H 2SO 4<br />
H<br />
Aminoglutetimida<br />
NO 2<br />
CN<br />
Et<br />
B<br />
Br 2
NaNH 2<br />
CH 3COOH<br />
H 2SO 4<br />
NO 2<br />
NC Et<br />
O 2N<br />
O<br />
Et<br />
O<br />
N<br />
H<br />
O<br />
OCH 3<br />
H 2<br />
Pd<br />
O 2N<br />
H 2N<br />
C<br />
Et<br />
CN<br />
COOCH 3<br />
Et<br />
O<br />
N<br />
H<br />
O<br />
Aminoglutetimida<br />
19 Propón un esquema sintético a partir de 2-fenilaceta<strong>to</strong> de etilo y los reactivos que consideres<br />
necesarios para la obtención del fenobarbital, barbitura<strong>to</strong> utilizado en terapéutica como<br />
antiepiléptico, que estructuralmente se caracteriza por la presencia de un fenilo en la posición<br />
5 del núcleo del ácido barbitúrico, sustituyente que le confiere una actividad hipnótica<br />
prolongada y propiedades anticonvulsivantes.<br />
SOLUCIÓN<br />
EtO<br />
Ph<br />
O<br />
ClCOOEt<br />
NaOEt<br />
Ph<br />
Fenobarbital<br />
OEt<br />
O<br />
O<br />
OEt<br />
BrEt<br />
NaOEt<br />
O<br />
Et<br />
Ph<br />
O<br />
Ph<br />
Et<br />
H<br />
N<br />
O<br />
N<br />
H<br />
OEt<br />
O<br />
O<br />
OEt<br />
H 2N<br />
O<br />
NH 2<br />
Et Ph<br />
O O<br />
HN NH<br />
O<br />
Fenobarbital<br />
20 Las benzodiazepinas constituyen uno de los grupos más importantes de fármacos ansiolíticos.<br />
Completa la siguiente secuencia sintética que conduce a la obtención del diazepam<br />
(Valium®), caracterizado estructuralmente por el sistema de 1,4-benzodiazepín-2-ona, y cuya<br />
alquilación en el á<strong>to</strong>mo de nitrógeno de la posición 1 permite mejorar su absorción.<br />
Cl<br />
NH 2<br />
O<br />
O + O<br />
H3C NH 2<br />
HCl<br />
CH3 O O<br />
S<br />
piridina O O CH3 A<br />
CH3ONa Diazepam
SOLUCIÓN<br />
Cl<br />
Cl<br />
NH 2<br />
O +<br />
O<br />
O<br />
NH2 CH3 HCl<br />
piridina<br />
Cl<br />
A<br />
H<br />
N O<br />
N<br />
(CH 3O) 2SO 2<br />
CH 3ONa<br />
Cl<br />
N O<br />
CH3 N<br />
Diazepam<br />
21 El clordiazepóxido (Librium®), fue la primera 1,4-benzodiazepina descubierta, siendo su<br />
hallazgo consecuencia de una serie de hechos fortui<strong>to</strong>s. El conocimien<strong>to</strong> de que la<br />
actividad ansiolítica del clordiazepóxido era debida a la 1,4-benzodiazepin-2-ona resultante<br />
de la hidrólisis metabólica, permitió que el clordiazepóxido se convirtiese en el cabeza de<br />
serie para el desarrollo de las benzodiazepinas ansiolíticas.<br />
N<br />
NHCH 3<br />
N O<br />
Clordiazepóxido<br />
metabolismo<br />
Cl<br />
H<br />
N O<br />
N O<br />
X<br />
N O<br />
R<br />
N<br />
Estructura general de<br />
las benzodiazepinas<br />
22 En una posible secuencia sintética para la obtención del clordiazepóxido se parte de la pcloroanilina,<br />
la cual se acila con cloruro de benzoilo en posición or<strong>to</strong> al grupo amino para<br />
formar un dímero que por hidrólisis conduce a la o-benzoil-p-cloroanilina. Las etapas<br />
siguientes se recogen en el esquema que se muestra a continuación:<br />
NH 2<br />
O<br />
Cl<br />
o-benzoil-p-cloroanilina<br />
X<br />
Cl<br />
NH 2OH<br />
N CH 2Cl<br />
N<br />
O<br />
Z<br />
Y<br />
O<br />
C<br />
CH2Cl NH N<br />
OH<br />
Cl<br />
N<br />
H2NCH3 Cl<br />
N<br />
O<br />
Clordiazepóxido<br />
Completa los reactivos y produc<strong>to</strong>s designados por las letras Z, Y, X.<br />
NHCH 3
SOLUCIÓN<br />
NH 2<br />
Cl<br />
O NH2 N<br />
NH2OH ClCH2COCl OH<br />
O CH<br />
C<br />
2Cl<br />
OH<br />
NH N<br />
Cl<br />
NaOH<br />
X<br />
Cl<br />
Z<br />
Cl<br />
N<br />
Y<br />
N CH 2Cl<br />
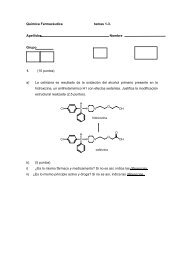
El produc<strong>to</strong> Z es la oxima que se forma al reaccionar el carbonilo de la ce<strong>to</strong>na con la<br />
hidroxilamina. El reactivo Y, ClCH2COCl, es el cloruro de cloroacetilo que transforma la amina<br />
primaria en una amida. El reactivo X es el hidróxido de sodio, medio básico, necesario para la<br />
ciclación.<br />
23 El mé<strong>to</strong>do más general para la obtención de 1,4-benzodiazepinas consiste en la acilación de<br />
o-aminobenzofenonas con cloruro de cloroacetilo seguida de amoníaco. Completa el esquema<br />
de síntesis del prazepam, fármaco perteneciente a las 1,4-benzodiazepinas ansiolíticas,<br />
depresoras selectivas del SNC.<br />
Cl<br />
Cl<br />
SOLUCIÓN<br />
Cl<br />
NH 2<br />
O<br />
NH 2<br />
O<br />
ClCOCH 2Cl<br />
Cl<br />
N O<br />
N<br />
ClCOCH 2Cl<br />
A NH3 - HCl<br />
- H2O Prazepam<br />
Cl<br />
B<br />
H<br />
N<br />
HNa<br />
O<br />
C<br />
CH2Cl O<br />
A<br />
O<br />
NH 3<br />
- HCl<br />
- H2O Cl<br />
B<br />
H<br />
N O<br />
N
HNa<br />
Cl<br />
Na<br />
N O<br />
N<br />
C<br />
Cl<br />
Cl<br />
Prazepam<br />
N O<br />
24 El alobarbital es un barbitúrico que se emplea como sedante. Partiendo del ácido barbitúrico<br />
propón una síntesis del alobarbital.<br />
O<br />
H<br />
N<br />
O<br />
N<br />
O<br />
H<br />
Ác. barbitúrico<br />
O<br />
N<br />
H<br />
N<br />
O<br />
N<br />
O<br />
Alobarbital<br />
SOLUCIÓN<br />
Una posible vía de síntesis sería una sustitución nucleofílica en posición alílica del bromuro de<br />
alilo con el anión barbitura<strong>to</strong> como nucleófilo<br />
bromuro<br />
de alilo<br />
Br +<br />
O<br />
H<br />
N<br />
O<br />
N<br />
O<br />
H<br />
NaOH<br />
H<br />
N<br />
Ác. barbitúrico Alobarbital<br />
En medio básico, el ácido barbitúrico pierde un protón y forma la sal sódica del anión<br />
barbitura<strong>to</strong>, que se comporta como un nucleófilo y ataca al bromuro de alilo.<br />
O<br />
H H<br />
H<br />
N<br />
O<br />
N<br />
O<br />
H<br />
+<br />
NaOH<br />
O<br />
O<br />
O<br />
N<br />
H<br />
N<br />
O<br />
H<br />
O<br />
N<br />
H<br />
O<br />
25 Los barbitura<strong>to</strong>s disustituidos en posición 5 presentan interés terapéutico como hipnóticosedantes,<br />
aunque en la actualidad debido a su <strong>to</strong>xicidad y dependencia han sido<br />
desplazados, casi <strong>to</strong>talmente, por las benzodiazepinas, limitándose su uso fundamentalmente<br />
al tratamien<strong>to</strong> epiléptico y la anestesia quirúrgica.<br />
Na<br />
La obtención de los barbitura<strong>to</strong>s se puede llevar a cabo por reacción de derivados del éster<br />
malónico con la urea o guanidina. Sobre esta base, propón dos síntesis alternativas del<br />
H<br />
H
u<strong>to</strong>barbital (ácido 5-butil-5-etilbarbitúrico).<br />
SOLUCIÓN<br />
EtO<br />
EtO<br />
O<br />
O<br />
CH 3<br />
BrEt<br />
O H<br />
Et N<br />
O<br />
N<br />
O<br />
H<br />
Bu<strong>to</strong>barbital<br />
NaOEt<br />
Et<br />
EtO<br />
EtO<br />
O<br />
O<br />
CH 3<br />
BrCH 2(CH 2) 2CH 3<br />
NaOEt<br />
Et<br />
Bu<strong>to</strong>barbital<br />
O<br />
O<br />
NH<br />
O<br />
NH<br />
CH 3<br />
H 2N<br />
O<br />
Et<br />
NH 2<br />
hidrólisis<br />
EtO<br />
EtO<br />
O<br />
O<br />
CH 3<br />
H 2N<br />
Et<br />
NH<br />
NH 2<br />
O<br />
O<br />
NH<br />
NH<br />
NH<br />
26 La obtención de los barbitura<strong>to</strong>s comienza, generalmente, con una síntesis malónica. El<br />
ácido malónico se transforma en el malona<strong>to</strong> disustituido, que se condensa con la urea,<br />
según un proceso químico que se representa por la reacción siguiente.<br />
O C<br />
NH 2<br />
NH 2<br />
HOOC R1 C<br />
HOOC<br />
R 2<br />
Urea Ácido dicarboxílico<br />
disustituido<br />
- 2 H 2O<br />
H O<br />
N C<br />
O<br />
N C<br />
H O<br />
R1 R2 Ácido bartitúrico<br />
disustituido<br />
Escribe <strong>to</strong>das las reacciones del proceso de síntesis del hipnótico sedante butalbital.<br />
SOLUCIÓN<br />
H O<br />
N C CH2CH O<br />
N C CH2CH H O<br />
CH 3<br />
CH 3<br />
CH2 Butalbital<br />
Comenzamos con una síntesis malónica para introducir el radical isobutilo.
COOEt<br />
H 2C<br />
COOEt<br />
MeO −<br />
MeOH<br />
COOEt<br />
CH<br />
COOEt<br />
Br<br />
CH 3<br />
CH 3<br />
Luego, condensamos el alquilmalona<strong>to</strong> de etilo con la urea.<br />
CH 3<br />
CH 3<br />
CH<br />
CH 2<br />
COOEt<br />
C H<br />
COOEt<br />
+<br />
O C<br />
NH 2<br />
NH 2<br />
NaEtO<br />
CH 3<br />
CH 3<br />
O<br />
CH 3<br />
CH 3<br />
CH<br />
H<br />
N O<br />
O<br />
N<br />
H<br />
CH 2<br />
COOEt<br />
C H<br />
COOEt<br />
Por último, el sustituyente alílico se introduce mediante una sustitución nucleofílica.<br />
CH 3<br />
CH 3<br />
O<br />
H<br />
N O<br />
N<br />
H<br />
O<br />
+<br />
Br<br />
NaOH<br />
CH 3<br />
CH 2<br />
CH 3<br />
O<br />
H<br />
N O<br />
O<br />
N<br />
Butalbital<br />
27 La obtención de los barbitura<strong>to</strong>s puede plantearse desde el pun<strong>to</strong> de vista sintético por la<br />
condensación entre un malona<strong>to</strong> adecuadamente disustituido en posición 2 y un derivado de<br />
la urea. La introducción de los radicales alquenilo en la síntesis de los derivados disustituidos<br />
del éster malónico no suele llevarse a cabo utilizando los correspondientes haluros de alquilo,<br />
sino ce<strong>to</strong>nas. Teniendo en cuenta este hecho, completa razonadamente la síntesis del<br />
ciclobarbital, barbitúrico de acción intermedia.<br />
SOLUCIÓN<br />
EtO<br />
EtO<br />
O<br />
O<br />
Malona<strong>to</strong><br />
de dietilo<br />
NaOEt<br />
O<br />
NaOEt<br />
O<br />
1<br />
EtO<br />
OH<br />
-H 2O<br />
O<br />
2<br />
-H 2O<br />
3<br />
BrEt<br />
NaOEt<br />
EtO<br />
O<br />
EtO<br />
EtO<br />
1 2<br />
4<br />
O<br />
O<br />
Urea<br />
H<br />
O<br />
O<br />
N<br />
N O<br />
H<br />
H<br />
Ciclobarbital
EtO<br />
EtO<br />
3<br />
O<br />
O<br />
BrEt<br />
NaOEt<br />
EtO<br />
Et<br />
EtO<br />
4<br />
O<br />
O<br />
H 2N<br />
O<br />
NH 2<br />
O<br />
O<br />
N<br />
N O<br />
H<br />
H<br />
Ciclobarbital<br />
28 a) Completa la síntesis del barbitúrico secobarbital<br />
(ácido 5-alil-5-secbutil-barbitúrico).<br />
b) ¿Por qué se utiliza para la introducción del radical alquilo secundario en el<br />
malona<strong>to</strong> de dietilo, la 2-butanona (una ce<strong>to</strong>na) en lugar del 2-bromobutano<br />
(un haluro de alquilo)?<br />
Malona<strong>to</strong><br />
de dietilo<br />
SOLUCIÓN<br />
a)<br />
EtO<br />
EtO<br />
H 2<br />
cat<br />
O<br />
O<br />
H 2N<br />
CH3COCH2CH3 1<br />
NaOEt<br />
O<br />
CH 3COCH 2CH 3<br />
NH 2<br />
NaOEt<br />
O<br />
OEt<br />
O OEt<br />
-H 2O<br />
2<br />
H 2<br />
cat<br />
BrCH2CH=CH2 Urea<br />
3 4<br />
NaOEt<br />
OHOEt<br />
O<br />
-H2O EtO<br />
O<br />
1<br />
O<br />
OEt<br />
EtO<br />
O<br />
2<br />
BrCH 2CH=CH 2<br />
NaOEt<br />
3 4<br />
N<br />
N O<br />
O H<br />
O H<br />
Secobarbital<br />
O<br />
O<br />
OEt<br />
OEt<br />
O<br />
O<br />
N<br />
N O<br />
H<br />
H<br />
Secobarbital<br />
b) Cuando se requiere la introducción en el malona<strong>to</strong> de dietilo de una cadena lateral<br />
ramificada, si ésta se lleva a cabo con el haluro de alquilo secundario correspondiente tiene<br />
lugar de forma preferente una reacción de eliminación, en lugar de la esperada reacción de<br />
sustitución.<br />
29 A continuación se indica la estructura del barbitura<strong>to</strong> amobarbital. Sugiere alguna síntesis<br />
<strong>to</strong>mando como materiales de partida urea, malona<strong>to</strong> de dietilo y cualquier otro compues<strong>to</strong><br />
que no contenga más de tres á<strong>to</strong>mos de carbono.
SOLUCIÓN<br />
CO 2Et<br />
CH 2<br />
CO 2Et<br />
Malona<strong>to</strong><br />
de dietilo<br />
O<br />
EtONa<br />
EtOH<br />
H<br />
N<br />
N<br />
H<br />
O<br />
CH<br />
O<br />
CH2CH3 CH2CH2CH CO 2Et<br />
CO 2Et<br />
O<br />
H<br />
N O<br />
N<br />
H<br />
O<br />
CH2CH3<br />
CH2CH2CH(CH3)2<br />
Amobarbital<br />
CH 3<br />
BrCH 2CH 3<br />
- Síntesis del bromuro de isopentilo<br />
BrCH(CH 3) 2<br />
Mg<br />
BrMgCH(CH 3) 2<br />
CH 3<br />
O<br />
CO 2Et<br />
H2N NH2 (urea)<br />
1.<br />
Amobarbital<br />
(Amital)<br />
CH CH2CH3 CO2Et O<br />
EtONa<br />
EtOH<br />
CO 2Et<br />
C CH2CH3 CO 2Et<br />
BrCH 2CH 2CH(CH 3) 2<br />
CO 2Et<br />
(CH3) 2CHCH2CH2 C CH2CH3 CO2Et 2. H 3O + HOCH 2CH 2CH(CH 3) 2<br />
PBr 3<br />
BrCH2CH2CH(CH3) 2<br />
bromuro de isopentilo<br />
30 Propón dos posibles vías de síntesis del nitrazepam, benzodiazepina utilizada<br />
terapéuticamente como hipnótico.<br />
SOLUCIÓN<br />
¬ Vía A<br />
O 2N<br />
H<br />
N O<br />
N<br />
Nitrazepam
O 2N<br />
O 2N<br />
HN<br />
NH 2<br />
O<br />
O<br />
NH<br />
O<br />
BrCOCH2Br HN Br<br />
NH3 O2N O<br />
Br<br />
- HBr<br />
O 2N<br />
H<br />
N O<br />
N<br />
Nitrazepam<br />
31 El derivado tricíclico del pirrol, cuya estructura aparece más abajo, es un fármaco que suele<br />
emplearse en el tratamien<strong>to</strong> de la esquizofrenia.<br />
CH 3<br />
N<br />
H<br />
H<br />
O<br />
N<br />
H<br />
CH 3<br />
CH 3<br />
Teniendo en cuenta que se puede preparar mediante la síntesis de Knorr de pirroles, en la que<br />
tiene lugar una condensación de una ce<strong>to</strong>na con una α-aminoce<strong>to</strong>na. ¿Cuáles son las<br />
estructuras de los dos materiales de partida y de la enamina intermedia?<br />
SOLUCIÓN<br />
La condensación de la dice<strong>to</strong>na A con la 2-amino-3-pentanona da lugar a la enamina, que no<br />
se aísla, porque inmediatamente se cicla formando el fármaco.<br />
CH3 N<br />
O<br />
H<br />
+<br />
O<br />
CH3 CH3 N<br />
O<br />
H<br />
O<br />
CH3 H<br />
A<br />
O H2N CH3 - H2O H<br />
N<br />
H<br />
CH3 CH 3<br />
N<br />
H<br />
H<br />
O<br />
O<br />
N<br />
H<br />
CH 3<br />
CH 3<br />
- H 2O<br />
CH 3<br />
32 El compues<strong>to</strong> M es un antidepresivo que puede sintetizarse en dos etapas: en la primera<br />
etapa se forma el triciclo mediante la síntesis de indoles de Fischer, a partir de fenilhidrazina<br />
y ciclooctanona; en la segunda reacción se alquila convenientemente el nitrógeno. Escribe la<br />
síntesis completa de M.<br />
N<br />
H<br />
H<br />
O<br />
N<br />
H<br />
CH 3<br />
CH 3
SOLUCIÓN<br />
NHNH 2 +<br />
Cl N CH 3<br />
NaH<br />
CH 3<br />
O<br />
N<br />
N<br />
NMe 2<br />
N<br />
H<br />
N CH 3<br />
CH 3<br />
33 La cloroquina es un derivado de la 4-aminoquinoleína utilizado para el tratamien<strong>to</strong> de la<br />
malaria, cuya introducción en terapéutica fue resultado del desarrollo de análogos de la<br />
quinina por simplificación del anillo de quinuclidina y que actúa por intercalación con los<br />
pares de bases del ADN del plasmodio. Completa la siguiente ruta sintética correspondiente<br />
a la cloroquina.<br />
SOLUCIÓN<br />
Cl<br />
NH 2<br />
F<br />
Cl NH 2<br />
O<br />
CO 2Et<br />
CO 2Et<br />
- H 2O<br />
+<br />
O<br />
CO 2Et<br />
CO 2Et<br />
M<br />
- H 2O - EtOH<br />
Cloroquina<br />
A<br />
CO 2Et<br />
calor<br />
- CO 2<br />
calor<br />
B<br />
C<br />
1. NaOH<br />
2. H 3O +<br />
Cl N CO2Et Cl<br />
N<br />
H<br />
A<br />
CO 2Et<br />
CO 2Et
- EtOH<br />
calor<br />
- CO 2<br />
calor<br />
Cl<br />
Cl<br />
B<br />
O<br />
N<br />
H<br />
OH<br />
N<br />
Cloroquina<br />
CO 2Et<br />
1. NaOH<br />
2. H 3O +<br />
Cl<br />
Cl<br />
O<br />
N<br />
H<br />
OH<br />
C<br />
N<br />
CO 2H<br />
CO 2H<br />
34 La bromocumarina es un compues<strong>to</strong> que exhibe actividad biológica contra los trema<strong>to</strong>dos<br />
parási<strong>to</strong>s que causan la esquis<strong>to</strong>somiasis, una enfermedad muy común en los trópicos.<br />
Br<br />
O<br />
COOCH 3CH 3<br />
a) Realiza el análisis retrosintético de esta lac<strong>to</strong>na.<br />
O<br />
Bromocumarina<br />
b) Propón una síntesis de la bromocumarina, utilizando malona<strong>to</strong> de dietilo como<br />
compues<strong>to</strong> de partida.<br />
SOLUCIÓN<br />
a) Análisis retrosintético.<br />
Br<br />
O<br />
COOEt<br />
b) Condensación de Knoevenagel.<br />
Br<br />
O<br />
CHO<br />
+<br />
OH<br />
COOEt<br />
CH2 COOEt<br />
Br<br />
NaEtO<br />
COOEt<br />
OH COOEt<br />
Br<br />
OH<br />
OH COOEt<br />
Br<br />
COOEt<br />
CH 2<br />
COOEt<br />
COOEt<br />
CHO<br />
OH<br />
Sin<strong>to</strong>nes<br />
- H 2O
- H 2O<br />
Br<br />
COOEt<br />
OH COOEt<br />
- EtOH<br />
Br<br />
O<br />
COOEt<br />
35 Completa el siguiente esquema sintético que conduce a la obtención del intermedio B,<br />
utilizado en la preparación del antihelmíntico activo frente a Enterobius vermicularis y<br />
Strongyloides stercularis pamoa<strong>to</strong> de pirvinio.<br />
SOLUCIÓN<br />
CH 3<br />
Anilina<br />
O<br />
O<br />
COOH<br />
OH<br />
CH 2OH<br />
+<br />
Hexano-2,5-diona<br />
NH 2<br />
Anilina<br />
COOH 1/2<br />
CH 3<br />
Hexano-2,5-diona<br />
H<br />
CH 3<br />
- 2 H 2O<br />
Síntesis de<br />
Paal-Knorr<br />
O<br />
N<br />
B<br />
CH 3<br />
CH 3<br />
H3C N<br />
OH<br />
Pamoa<strong>to</strong> de pirvinio<br />
CH 3<br />
O<br />
N<br />
CH3 H3C N<br />
Síntesis de Paal-Knorr<br />
N<br />
A<br />
CH 3<br />
H<br />
O<br />
A<br />
H<br />
CH 3<br />
O<br />
N CH 3<br />
CH 3<br />
POCl 3<br />
N CH 3<br />
CH 3<br />
POCl 3<br />
36 El cardiotónico y broncodilatador proxifilina es una base xántica que puede obtenerse por<br />
dos mé<strong>to</strong>dos diferentes.<br />
En ambas síntesis se parte del produc<strong>to</strong> natural teofilina. En una de las estrategias<br />
B
sintéticas la teofilina reacciona con un derivado clorado, según se recoge en el siguiente<br />
esquema.<br />
CH 3<br />
O<br />
N<br />
O<br />
N<br />
CH 3<br />
Teofilina<br />
H<br />
N<br />
N<br />
+ Cl<br />
OH<br />
CH 3<br />
NaOH<br />
CH 3<br />
O<br />
N<br />
O<br />
N<br />
CH 3<br />
CH 2<br />
N<br />
N<br />
OH<br />
CH<br />
Proxifilina<br />
Propón un sustra<strong>to</strong>, para la otra estrategia sintética, que al reaccionar con la teofilina produzca<br />
también la proxifilina.<br />
SOLUCIÓN<br />
El segundo mé<strong>to</strong>do de síntesis se basa en la apertura de un epóxido, el metiloxaciclopropano.<br />
La teofilina en medio fuertemente básico forma una sal, cuyo anión se comporta como un<br />
nucleófilo atacando el epóxido por el lado menos impedido y produciendo su apertura. La<br />
hidrólisis posterior conducirá a la proxifilina.<br />
CH 3<br />
O<br />
CH 3<br />
O<br />
N<br />
N<br />
O<br />
N<br />
CH 3<br />
O<br />
N<br />
CH 3<br />
H<br />
N<br />
N<br />
Na<br />
N<br />
N<br />
+ NaOH<br />
+<br />
O<br />
CH 3<br />
H 2O<br />
CH 3<br />
O<br />
N<br />
O<br />
N<br />
CH 3<br />
CH 3<br />
O<br />
N<br />
N<br />
O<br />
N<br />
N<br />
Proxifilina<br />
37 La almitrina es un fármaco estimulante respira<strong>to</strong>rio, utilizado para el tratamien<strong>to</strong> de la<br />
depresión respira<strong>to</strong>ria por in<strong>to</strong>xicación con depresores del SNC (alcohol, anestésicos, etc).<br />
En su estructura molecular tiene un anillo de triazina trisustituido.<br />
F<br />
F<br />
CH<br />
N N<br />
N<br />
N<br />
CH 3<br />
NH<br />
N<br />
NH<br />
Na<br />
CH 2<br />
N<br />
N<br />
OH<br />
CH<br />
CH 3<br />
Almitrina<br />
CH 3
a) Aplicando el análisis retrosintético, dibuja sobre la molécula las desconexiones que consideres<br />
más adecuadas.<br />
b) Escribe la síntesis completa de la almitrina.<br />
SOLUCIÓN<br />
a) Análisis retrosintético:<br />
1ª desconexión<br />
F<br />
F<br />
2ª desconexión<br />
F<br />
F<br />
3ª desconexión<br />
F<br />
CH<br />
N N<br />
CH N N<br />
CH<br />
F<br />
N<br />
NH<br />
N<br />
N<br />
N<br />
N<br />
NH<br />
N<br />
NH<br />
Cl<br />
N<br />
Cl<br />
F<br />
F<br />
F<br />
F<br />
Almitrina<br />
CH<br />
F<br />
F<br />
F<br />
F<br />
3<br />
CH<br />
N N<br />
2<br />
Cl<br />
CH<br />
2<br />
N<br />
N<br />
N N<br />
NH<br />
N<br />
1<br />
1<br />
NH<br />
NH 2<br />
CH N NH<br />
NH NH<br />
b) Síntesis de la almitrina. En la primera etapa partimos de piperazina y de un derivado<br />
halogenado del difenilmetano.<br />
+<br />
N<br />
N<br />
+<br />
Cl<br />
N<br />
Cl<br />
Cl<br />
N<br />
N<br />
Cl<br />
N<br />
Cl
H<br />
N N H<br />
+<br />
Cl<br />
CH<br />
F<br />
F<br />
H<br />
N<br />
N CH<br />
La reacción con la triclorotriazina del sintón formado, completa la estructura del sistema anular<br />
de esta molécula.<br />
H N<br />
N<br />
CH<br />
F<br />
F<br />
Cl<br />
N Cl<br />
N N<br />
Cl<br />
F<br />
F<br />
F<br />
F<br />
CH N N<br />
N Cl<br />
Por último, la sustitución nucleofílica de los dos á<strong>to</strong>mos de cloro restantes en el anillo de<br />
triazina por alilamina conduce a la formación del fármaco.<br />
F<br />
F<br />
CH<br />
N N<br />
N Cl<br />
N<br />
N<br />
Cl<br />
NH 2<br />
F<br />
F<br />
N<br />
Almitrina<br />
CH N N<br />
N<br />
Cl<br />
N<br />
N<br />
NH<br />
N<br />
NH