BASES MOLECULARES DEL DOLOR NEUROPÁTICO: UNA ...
BASES MOLECULARES DEL DOLOR NEUROPÁTICO: UNA ... BASES MOLECULARES DEL DOLOR NEUROPÁTICO: UNA ...
Figura 1. Estructuras moleculares de los enantiómeros de los diasterómeros cis VU0155041 (rac-2) y trans VU0155040 (rac-3) del compuesto padre VU0003423. La síntesis se describe en el esquema 1. Esquema 1. Síntesis de los enantiómeros de VU0155041. Los detalles de la síntesis pueden encontrarse en Christov et al., Chem Med Chem, 2011, 6, 131-40. Cuando se ensayaron en el receptor mGluR4 por el equipo 1, el enantiómero (1R, 2S)-2 demostró ser más activo que el (1S, 2R)-2, que en nuestro ensayo fue prácticamente inactivo en la figura 2 (Christov et al., 6
Chem Med Chem, 2011, 6, 131-40). El enantiómero activo es un PAM de este receptor. El compuesto racémico cis (rac-2) es también un PAM, aunque menos potente que el enantiómero activo, de acuerdo con la actividad medida para los enantiómeros individuales. El compuesto trans racémico (rac-3) muestra un efecto débil como PAM. La actividad diferente de los enantiómeros está en conflicto con un estudio anterior que describía una actividad similar para ambos enantiómeros (Niswender et al., Mol. Pharmacol, 2008, 74, 1345-1358). No tenemos una explicación definitiva para esta discrepancia, pero parece que la racemización en estos sistemas es factible bajo las condiciones del ensayo. Figura 2. Resultados de las pruebas de actividad sobre el receptor mGluR4 de cis VU0155041 (rac-2), trans VU0155040 (rac-3) y los enantiómeros (1R, 2S)-2 y (1S, 2R)-2 del diasterómero cis. Para definir un farmacóforo PAM mGluR4 a partir de los datos anteriores de estructura-actividad, el equipo 4 caracterizó un conjunto de conformaciones de los diasterómeros cis y trans. En particular, para el enantiómero activo (1R, 2S)-2 se obtuvieron dos conformaciones [(1Ra, 2Se)-2 y (1Ra, 2Se)- 2]. Sin embargo, debido a que la diferencia de energía fue muy pequeña (0.8 kcal/mol), no se pudo elucidar la conformación activa (Christov et al., Chem Med Chem, 2011, 6, 131-40). A tal fin, decidimos restringir la libertad conformacional del ciclohexano insertando un enlace C=C en posiciones particulares del anillo. 7
- Page 1 and 2: BASES MOLECULARES DEL DOLOR NEUROP
- Page 3 and 4: 2. Resultados Subproyecto I. Farmac
- Page 5: mGluR4. Es importan señalar que la
- Page 9 and 10: Sin embargo, la falta de éxito par
- Page 11 and 12: 3. Relevancia y posibles implicacio
- Page 13: 6. Rovira X, Pin JP, Giraldo J. The
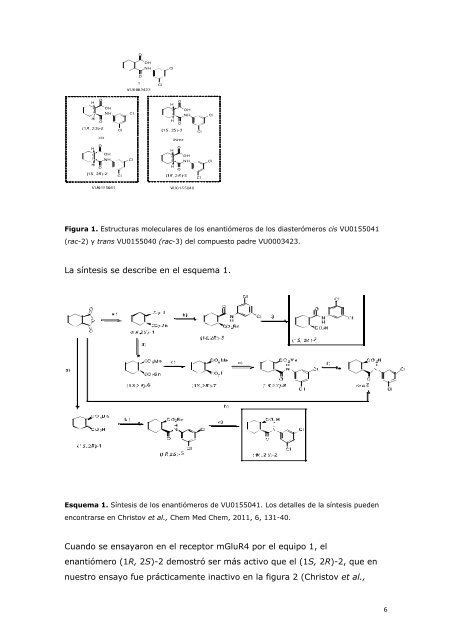
Figura 1. Estructuras moleculares de los enantiómeros de los diasterómeros cis VU0155041<br />
(rac-2) y trans VU0155040 (rac-3) del compuesto padre VU0003423.<br />
La síntesis se describe en el esquema 1.<br />
Esquema 1. Síntesis de los enantiómeros de VU0155041. Los detalles de la síntesis pueden<br />
encontrarse en Christov et al., Chem Med Chem, 2011, 6, 131-40.<br />
Cuando se ensayaron en el receptor mGluR4 por el equipo 1, el<br />
enantiómero (1R, 2S)-2 demostró ser más activo que el (1S, 2R)-2, que en<br />
nuestro ensayo fue prácticamente inactivo en la figura 2 (Christov et al.,<br />
6