Tema 11 ESTRATEGIAS DE FARMACOMODULACIÓN - OCW CEU
Tema 11 ESTRATEGIAS DE FARMACOMODULACIÓN - OCW CEU
Tema 11 ESTRATEGIAS DE FARMACOMODULACIÓN - OCW CEU
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Tema</strong> <strong>11</strong><br />
<strong>ESTRATEGIAS</strong> <strong>DE</strong><br />
<strong>FARMACOMODULACIÓN</strong><br />
1
<strong>ESTRATEGIAS</strong> <strong>DE</strong> <strong>FARMACOMODULACIÓN</strong><br />
1. Introducción<br />
2. Finalidad de la farmacomodulación<br />
3. Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
4. Ejemplo de aplicación de la estrategia<br />
2
1. Introducción<br />
3
<strong>DE</strong>SARROLLO <strong>DE</strong> NUEVOS FÁRMACOS<br />
Búsqueda de CABEZAS <strong>DE</strong> SERIE o<br />
prototipos<br />
Moléculas que presentan una actividad<br />
interesante<br />
Optimización del prototipo<br />
Modificación química para mejorar un cabeza<br />
de serie<br />
Uno de los métodos más<br />
utilizados<br />
4
1) CABEZA <strong>DE</strong> SERIE<br />
2) DISEÑO <strong>DE</strong> ANÁLOGOS<br />
Exploración sistemática del cabeza de<br />
serie<br />
<strong>FARMACOMODULACIÓN</strong><br />
(MODIFICACIÓN MOLECULAR)<br />
5
<strong>FARMACOMODULACIÓN</strong><br />
Modificaciones estructurales sobre un prototipo<br />
Inconveniente<br />
Ventajas<br />
• Mayor probabilidad de mejorar<br />
las propiedades farmacológicas<br />
• Compuestos más simples<br />
• Mismo método de valoración<br />
farmacológica o bioquímica<br />
Método empírico<br />
Estrecha relación<br />
estructural entre<br />
los compuestos<br />
• rutas sintéticas comunes<br />
• ahorro: tiempo y dinero<br />
Interés económico y científico<br />
mejor comparación de las actividades<br />
relaciones estructura-actividad más fiables<br />
6
<strong>ESTRATEGIAS</strong> <strong>DE</strong> <strong>FARMACOMODULACIÓN</strong><br />
1. Introducción<br />
2. Finalidad de la farmacomodulación<br />
3. Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
4. Ejemplo de aplicación de la estrategia<br />
7
2. Finalidad de la<br />
farmacomodulación<br />
8
<strong>FARMACOMODULACIÓN</strong><br />
FINALIDAD<br />
Explorar las propiedades de un cabeza<br />
de serie en relación a los siguientes<br />
aspectos:<br />
a) Estudio preliminar de las relaciones<br />
estructura-actividad (REA)<br />
b) Modificación del espectro de acción<br />
c) Modificación de la farmacocinética<br />
d) Aumento de la estabilidad química<br />
9
A) Estudio preliminar de las relaciones<br />
estructura-actividad (REA)<br />
Modificaciones estructurales del prototipo<br />
SERIES <strong>DE</strong> FÁRMACOS<br />
Gradación de propiedades farmacológicas<br />
Características estructurales más idóneas<br />
10
Ejemplo<br />
Farmacomodulación de<br />
antihistamínicos H 1<br />
<strong>11</strong>
<strong>FARMACOMODULACIÓN</strong><br />
FINALIDAD<br />
a) Estudio preliminar de las relaciones<br />
estructura-actividad (REA)<br />
b) Modificación del espectro de acción<br />
c) Modificación de la farmacocinética<br />
d) Aumento de la estabilidad química<br />
12
B) Modificación del espectro de acción<br />
“Espectro de acción”<br />
Conjunto de acciones, con sus respectivas potencias,<br />
que presenta un determinado compuesto<br />
Farmacomodulación<br />
potenciar efectos secundarios<br />
enmascarar efectos secundarios<br />
búsqueda de propiedades antagonistas<br />
Histamina<br />
Agonista natural<br />
de receptores H 2<br />
Cimetidina<br />
anti H 2<br />
Antiulceroso<br />
13
<strong>FARMACOMODULACIÓN</strong><br />
FINALIDAD<br />
a) Estudio preliminar de las relaciones<br />
estructura-actividad (REA)<br />
b) Modificación del espectro de acción<br />
c) Modificación de la farmacocinética<br />
d) Aumento de la estabilidad química<br />
14
Modificación de la farmacocinética<br />
Modificación del ADME<br />
Ejemplo<br />
Modificación de la<br />
concentración<br />
plasmática de un<br />
fármaco sin afectar<br />
su espectro de<br />
acción<br />
Absorción<br />
Distribución<br />
Metabolismo<br />
Excreción<br />
Tolbutamida Clorpropamida<br />
15
Modificación de la Farmacocinética<br />
Modulación de la distribución del fármaco entre los<br />
tejidos y órganos<br />
• Ejemplo<br />
Atropina Bromuro de ipratropio<br />
Anticolinérgico<br />
central y periférico<br />
CH3 N<br />
O<br />
H<br />
OH<br />
O<br />
Atropina<br />
(Alcaloide de las solanaceas)<br />
Anticolinérgico<br />
exclusivamente periférico<br />
Br<br />
H 3C<br />
CH(CH3) 2<br />
N<br />
O<br />
H<br />
OH<br />
O<br />
Bromuro de ipratropio<br />
Broncodilatador por inhalación<br />
16
<strong>FARMACOMODULACIÓN</strong><br />
FINALIDAD<br />
a) Estudio preliminar de las relaciones<br />
estructura-actividad (REA)<br />
b) Modificación del espectro de acción<br />
c) Modificación de la farmacocinética<br />
d) Aumento de la estabilidad química<br />
17
D) Aumento de la estabilidad química<br />
Ejemplo: Penicilinas lábiles en medio ácido<br />
Ph<br />
O<br />
H<br />
N<br />
H<br />
H<br />
N<br />
O H<br />
S CH3<br />
CH 3<br />
COOH<br />
Apertura del<br />
anillo de<br />
-lactama O<br />
Pérdida de la<br />
actividad<br />
antibacteriana<br />
Modificaciones en la cadena lateral:<br />
grupos atrayentes de electrones<br />
R<br />
NH 2<br />
H<br />
O N<br />
O<br />
R = H Ampicilina<br />
R = OH Amoxicilina<br />
Grupo atrayente de electrones<br />
H<br />
N<br />
H<br />
H<br />
S CH 3<br />
CH 3<br />
COOH<br />
Ph<br />
nucleofilia del<br />
oxígeno<br />
del CO de la<br />
cadena<br />
lateral<br />
O<br />
N<br />
HN<br />
S CH 3<br />
CH 3<br />
COOH<br />
estabilidad del<br />
sistema -lactama<br />
frente a los ácidos<br />
Administración<br />
oral<br />
18
<strong>ESTRATEGIAS</strong> <strong>DE</strong> <strong>FARMACOMODULACIÓN</strong><br />
1. Introducción<br />
2. Finalidad de la farmacomodulación<br />
3. Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
4. Ejemplo de aplicación de la estrategia<br />
19
3. Técnicas de<br />
Farmacomodulación<br />
20
Las técnicas de farmacomodulación dependen de:<br />
Tamaño<br />
Complejidad estructural<br />
CABEZA <strong>DE</strong><br />
SERIE<br />
Simplificación: aproximación disyuntiva<br />
Complejidad semejante: aproximación<br />
modulativa<br />
Introducción de elementos estructurales<br />
adicionales: aproximación conjuntiva<br />
21
3.Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
22
3.1. APROXIMACIÓN DISYUNTIVA<br />
• Reducción de la estructura del modelo conservación<br />
del fragmento esencial para la actividad o<br />
farmacóforo<br />
• Utilizada en modelos de estructura compleja<br />
(productos naturales de núcleo policíclico)<br />
Ejemplo de<br />
aproximación<br />
disyuntiva<br />
CH 3O<br />
HO<br />
H<br />
R<br />
N<br />
Quinina<br />
S<br />
Alcaloide de la<br />
quina<br />
N<br />
R<br />
R<br />
H<br />
Cl<br />
ANTIPALÚDICO <strong>DE</strong> SÍNTESIS<br />
HN<br />
N<br />
N<br />
Cloroquina<br />
23
Otro ejemplo de aproximación disyuntiva<br />
Cocaína: efectos<br />
estimulantes centrales<br />
H3C N<br />
H<br />
Cocaína<br />
COOCH 3<br />
O<br />
O<br />
H 3C<br />
H 3C<br />
H 2N<br />
H 3C<br />
HN<br />
Farmacóforo para la<br />
acción anestésica<br />
local<br />
N<br />
O<br />
O<br />
O<br />
C<br />
O<br />
Procaína<br />
O<br />
C<br />
O<br />
Tetracaína<br />
N CH 3<br />
CH 3<br />
N CH 3<br />
CH 3<br />
24
3.Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
25
3.2. APROXIMACIONES MODULATIVAS<br />
Modificaciones moleculares<br />
Se caracterizan por<br />
Ser transformaciones limitadas<br />
Conservar aspectos esenciales del modelo<br />
Pueden incidir en propiedades físicoquímicas<br />
de la molécula<br />
26
APROXIMACIONES<br />
MODULATIVAS<br />
RECURSOS<br />
MÁS<br />
EMPLEADOS<br />
Apertura de anillos<br />
Formación de anillos<br />
Variación del tamaño de anillo<br />
Reorganización de anillos<br />
Homología<br />
Vinilogía<br />
Isomerización<br />
Ramificación, alquilación desalquilación<br />
Saturación de dobles enlaces<br />
Bioisostería<br />
ANILLOS<br />
27
A) Apertura de anillos<br />
Mayoría de los ejemplos descritos menos<br />
potentes que el prototipo<br />
Excepción:<br />
Dietilestilbestrol y otros análogos de elevada<br />
potencia estrogénica<br />
28
B) Formación de anillos<br />
Formación de anillos a partir de estructuras lineales<br />
Fusión de anillos<br />
Inverso a la apertura de anillos (en cierto modo)<br />
H 3C<br />
HN<br />
O<br />
S<br />
O<br />
Sumatriptán<br />
N<br />
CH 3<br />
O<br />
Ondansetron<br />
N<br />
N<br />
H<br />
CH 3<br />
N<br />
N<br />
CH 3<br />
CH 3<br />
N<br />
S<br />
O<br />
O<br />
Almotriptán<br />
N<br />
Cilansetron<br />
O<br />
N<br />
H<br />
N<br />
N<br />
CH 3<br />
N<br />
CH 3<br />
CH 3<br />
29
Ejemplo de compuestos con diferente perfil<br />
farmacológico por formación de ciclos<br />
Difenhidramina<br />
( Antihistamínico H1)<br />
ciclación<br />
Nefopam<br />
(relajante muscular<br />
a nivel central)<br />
30
C) Variación del tamaño de anillo<br />
Una de las técnicas más utilizadas<br />
Pocas alteraciones terapéuticas<br />
Ejemplo<br />
Metilfenobarbital y mefenitoína<br />
(fármacos antiepilépticos)<br />
31
D) Reorganización de anillos<br />
Lipofilia semejante a la del prototipo<br />
Guanetidina: antihipertensivo, graves efectos 2ºs<br />
Espiros<br />
Sistemas<br />
con puente<br />
32
Homólogo<br />
Análogo que resulta de la adición o sustracción de un<br />
grupo metileno<br />
Derivados monoalquilados<br />
E) Homología<br />
R X R CH 2 X R CH 2 CH 2 X etc<br />
Derivados cíclicos<br />
X (CH2) n<br />
X (CH2) n+1<br />
Derivados difuncionales<br />
X (CH 2) n Y X (CH 2) n+1 Y<br />
33
Ejemplo<br />
Aproximación<br />
disyuntiva<br />
Homología<br />
Antihipertensivos (desuso)<br />
Herramientas farmacológicas<br />
Cloruro de<br />
tubocurarina<br />
Antagonista de<br />
los receptores<br />
nicotínicos<br />
34
Comportamientos frecuentes en series homólogas<br />
a) Actividad del compuesto ligada a la lipofilia (función<br />
del coeficiente de reparto)<br />
Introducción de grupos metileno<br />
Aumenta la actividad hasta un máximo, a partir del<br />
cual comienza a decrecer<br />
35
) Fármacos que se unen a una diana específica: la<br />
homologación no afecta si la distancia entre grupos<br />
esenciales para la unión con el receptor no se ve afectada<br />
Ph CO 2Et<br />
N<br />
CH 3<br />
Meperidina<br />
(hipnoanalgésico)<br />
N<br />
CH 3<br />
Ph<br />
CO 2Et<br />
Etoheptazina<br />
(hipnoanalgésico)<br />
c) Nueva actividad resultado de la homologación<br />
S<br />
N<br />
N(CH 3) 2<br />
Dietazina<br />
(antihistamínico H1)<br />
S<br />
N<br />
N(CH 3) 2<br />
Clorpromazina<br />
(neuroléptico)<br />
36
F) Vinilogía<br />
Dos sustituyentes X e Y unidos por una cadena<br />
vinílica o polivinílica se comportan como si estuvieran<br />
unidos directamente<br />
El grupo vinilo se comporta como conductor de<br />
propiedades electrónicas (resonancia)<br />
X Y X CH=CH Y X (CH=CH) n Y<br />
La actividad del prototipo puede mantenerse en los<br />
vinílogos si la densidad electrónica en una determinada<br />
zona de la molécula es importante en la unión con el<br />
receptor<br />
37
Descubrimiento: Claisen (1926)<br />
Formilacetona<br />
Propiedades ácidas semejantes al ácido acético<br />
Extensión del principio de vinilogía<br />
38
Inconvenientes de la vinilogía<br />
- Posibles metabolitos tóxicos<br />
- Cambios geométricos<br />
Ejemplos<br />
Analgésico<br />
Antiinflamatorio<br />
Antipirético<br />
Uricosúrico<br />
Bloqueante<br />
de los<br />
receptores adrenérgicos<br />
39
G) Isomerización<br />
Isomería de doble enlace (Z y E ) Isomería de posición<br />
Antidepresivo Mantenimiento en adictos<br />
a opiáceos<br />
40
Isomería de función<br />
Analgésicos<br />
opiáceos<br />
G) Isomerización<br />
Más activo<br />
41
H) Ramificación, alquilación y desalquilación<br />
• Alquilación y desalquilación<br />
Cambios en la polaridad de la molécula<br />
Importante en grupos hidroxilo o amino<br />
• Ramificación<br />
Disminución de la lipofilia<br />
Cambios conformacionales o estéreos<br />
Alteración sustancial de la actividad del modelo<br />
42
Ejemplo de<br />
Farmacomodulación<br />
por Ramificación<br />
HS<br />
O<br />
N<br />
Ejemplo de un cambio de la actividad por ramificación<br />
Profármaco de la dopamina<br />
Antiparkinsoniano<br />
COOH<br />
Mercaptoalcanoilprolina<br />
Ramificación<br />
HS<br />
H 3C H<br />
O<br />
N<br />
Captopril<br />
COOH<br />
Inhibidor de la ECA<br />
Antihipertensivo<br />
43
i) Saturación de dobles enlaces<br />
Puede modificar la conformación del fármaco<br />
Alteración de la capacidad para formar enlaces con la<br />
biofase<br />
Oxitócico potente Carece de acción sobre la<br />
Alcaloide aislado del<br />
Claviceps purpurea<br />
hongo parásito del<br />
cornezuelo del<br />
centeno<br />
musculatura lisa uterina<br />
Uso: migrañas y arterioesclerosis<br />
cerebral leve<br />
44
J) Bioisostería<br />
• Uno de los métodos más frecuentes de<br />
farmacomodulación<br />
• Equivalencia entre átomos o grupos de átomos<br />
Criterios<br />
Tamaño<br />
Distribución electrónica<br />
Propiedades físico-químicas de la molécula<br />
• Origen: Isostería química (Langmuir, 1919)<br />
ISÓSTEROS: moléculas con mismo número de átomos y<br />
distribución electrónica<br />
C O<br />
N N<br />
O<br />
O<br />
C O<br />
N O<br />
N<br />
N<br />
N N<br />
C O<br />
45
Ley del desplazamiento del hidruro (Grimm, 1925)<br />
Extiende el concepto a especies con distinto número de<br />
átomos<br />
La adición de un átomo de hidrógeno a un átomo de número<br />
atómico “n” proporciona una especie con las propiedades del<br />
átomo de número atómico superior n+1<br />
Ejemplo:<br />
Isostería F y OH<br />
C N O F Ne<br />
CH NH OH FH<br />
CH 2 NH 2 OH 2<br />
CH 3<br />
NH 3<br />
CH 4<br />
46
Erlenmeyer<br />
Isósteros:<br />
- Átomos idénticos en su capa electrónica externa<br />
Ejemplo: N, P y As; O, S, y Se, etc<br />
-Grupos diferentes con propiedades semejantes<br />
Ejemplo: pseudohalógenos (Cl, CN, SCN)<br />
-Grupo CH=CH y S<br />
-Equivalencias de anillo<br />
Ampliaciones posteriores<br />
Isosterismo CH-N Isosterismo O-N Isosterismo O-NH Isosterismo vinilo-S<br />
y<br />
y<br />
N O S<br />
y<br />
O N<br />
H<br />
y<br />
S<br />
47
“BIOISÓSTEROS”<br />
Principios 1950 (Friedman)<br />
Grupos o moléculas similares en algunas de sus<br />
propiedades físicas o químicas y con el mismo tipo de<br />
actividad biológica<br />
Compuestos bioisósteros (o bioequivalentes)<br />
Máxima analogía en cuanto a las características<br />
físicas y químicas<br />
Interacción fármaco-receptor acción biológica<br />
Agonistas y Antagonistas interacción con el<br />
mismo tipo de receptor pueden ser bioisósteros<br />
48
Parámetros<br />
a) Tamaño o volumen de los grupos: Br/iso-propilo y I/terc-butilo<br />
b) Ángulos de hibridación: RCH=R´ /RN=R´<br />
c) Distribución electrónica, polarizabilidad, efectos inductivos,<br />
cargas, dipolos efectos electrónicos<br />
d) Solubilidad en lípidos (lipofilia): grupos –CH2- y –S-<br />
–CH3 y Cl<br />
e) Acidez<br />
- benceno/ tiofeno<br />
f) Capacidad de formar enlaces de hidrógeno:<br />
–OH (fenol)<br />
CH 3SO 2NH-<br />
RNHCONH-<br />
49
Bioisosterismo<br />
Clásico<br />
No clásico<br />
Distribución electrónica<br />
Geometría (hibridación, ángulos de<br />
enlace, tamaño molecular)<br />
Solubilidad<br />
Acidez<br />
Capacidad para formar puentes de<br />
hidrógeno<br />
Polaridad<br />
50
“Bioisósteros” propiedades comparables<br />
Ejemplo:–OH y –Cl<br />
Bioisósteros: volumen<br />
No biosósteros: lipofilia<br />
Mayor número de propiedades equivalentes entre bioisósteros <br />
mayores probabilidades de que se conserven las propiedades<br />
esenciales de la molécula original<br />
benceno tiofeno<br />
Tamaño, forma, lipofilia y propiedades electrónica semejantes<br />
Intercambiables en prácticamente en todos los tipos<br />
de fármacos sustitución bioisóstera frecuente<br />
–CH 3 y – OH: muy pocas propiedades en común<br />
S<br />
51
Aplicación del concepto de bioisostería<br />
Ejemplos<br />
Niketamida y la dietilamida del ácido meta-nitrobenzoico<br />
Distribución electrónica análoga en los anillos aromáticos<br />
propiedades analépticas similares<br />
N<br />
O<br />
N Et<br />
Et<br />
NO 2<br />
O<br />
N Et<br />
Niketamida N,N-dietil-meta-nitrobenzamida<br />
Oxofenarsina y su análogo piridínico<br />
Et<br />
Semejanza en el carácter básico actividad tripanocida<br />
NH 2<br />
As<br />
Oxofenarsina<br />
O<br />
HO HO<br />
N<br />
As<br />
O<br />
52
3.Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
54
3.3 Aproximaciones conjuntivas<br />
Reunión de elementos estructurales de varios<br />
modelos<br />
Nuevo compuesto: propiedades farmacológicas<br />
Enlaces covalentes<br />
comunes<br />
Ventajas galénicas o farmacocinéticas<br />
55
Duplicación molecular<br />
Combinación de dos moléculas idénticas<br />
HO O<br />
O<br />
O<br />
CH 3<br />
+<br />
H 3C<br />
O<br />
HO O<br />
Combinación o hibridación molecular<br />
Combinación dos moléculas diferentes<br />
HO O<br />
Ácido acetilsalicílico<br />
OH<br />
Ácido salicílico<br />
+<br />
HO<br />
O<br />
N<br />
H<br />
Paracetamol<br />
O<br />
CH 3<br />
HO O<br />
O<br />
O<br />
Diaspirina<br />
HO<br />
O<br />
O<br />
Benorilato<br />
O<br />
O<br />
HO<br />
N<br />
H<br />
O<br />
O<br />
CH 3<br />
56
HÍBRIDO BIORREVERSIBLE<br />
Componentes precursores: regeneración mediante un<br />
proceso metabólico profármacos<br />
HO O<br />
OH<br />
Ácido salicílico<br />
+<br />
HO<br />
Perfil terapéutico comparable al ácido salicílico<br />
Menos efectos gastrointestinales que el AAS<br />
Administración cada 8-12 horas<br />
N<br />
H<br />
Paracetamol<br />
O<br />
CH 3<br />
HO<br />
O<br />
O<br />
Benorilato<br />
N<br />
H<br />
O<br />
CH 3<br />
57
HÍBRIDO NO REVERSIBLE METABÓLICAMENTE<br />
Unión en una misma molécula dos fragmentos cuyas<br />
acciones sean complementarias<br />
Ventaja respecto a la administración por separado:<br />
farmacocinética propia<br />
Híbridos del pindolol<br />
diseño de nuevos<br />
antihipertensivos<br />
58
<strong>ESTRATEGIAS</strong> <strong>DE</strong> <strong>FARMACOMODULACIÓN</strong><br />
1. Introducción<br />
2. Finalidad de la farmacomodulación<br />
3. Técnicas de farmacomodulación<br />
3.1. Aproximaciones disyuntivas<br />
3.2. Aproximaciones modulativas<br />
3.3. Aproximaciones conjuntivas<br />
4. Ejemplo de aplicación de la estrategia<br />
59
4. Ejemplo de<br />
aplicación de la<br />
estrategia<br />
60
Diseño racional para el descubrimiento de<br />
nuevos fármacos<br />
Farmacomodulación de la histamina<br />
Antihistamínicos H 2 de 2ª generación<br />
Antagonistas selectivos H 2<br />
HN<br />
N<br />
histamina<br />
NH 2<br />
Agonista H 1 y H 2<br />
H 3C<br />
Fármacos<br />
Antiulcerosos<br />
S<br />
H<br />
N<br />
H<br />
N<br />
CH 3<br />
HN<br />
N<br />
N<br />
CN<br />
cimetidina<br />
(primer anti H2 con utilidad terapéutica)<br />
61
HN<br />
Diseño racional para el descubrimiento de<br />
nuevos fármacos<br />
N<br />
histamina<br />
NH 2<br />
Ensayo de más<br />
de 200<br />
compuestos<br />
HN<br />
N<br />
H<br />
N<br />
NH<br />
Guanilhistamina<br />
NH 2<br />
Primer agonista parcial<br />
Bioisostería<br />
HN N<br />
tiourea<br />
S<br />
62<br />
NH<br />
NH 2<br />
agonista parcial<br />
mayor carácter<br />
antagonista
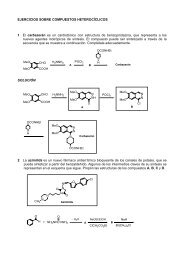
Farmacomodulación de la guanilhistamina: análogos A, B y C<br />
Estudio de los análogos A, B y C<br />
Modelo de interacción de la guanilhistamina y el análogo de tiourea<br />
sobre el receptor H 2<br />
Grupo guanidina y tiourea<br />
interaccionan con el carboxilato de<br />
una zona accesoria del receptor<br />
mediante un enlace iónico<br />
Cambio conformacional del<br />
receptor H 2 a un estado inactivo<br />
63
Farmacomodulación de la guanilhistamina<br />
Necesidad de dos grupos amino<br />
64
Búsqueda de grupos funcionales capaces de bloquear el receptor H 2<br />
HN<br />
N<br />
H<br />
N<br />
NH<br />
guanilhistamina<br />
H 3C<br />
NH 2<br />
N NH<br />
SFK 91581<br />
H<br />
N<br />
H<br />
N<br />
CH 3<br />
HN S<br />
N<br />
metiamida<br />
S<br />
agranulocitosis y daño renal agudo<br />
N<br />
H<br />
S<br />
NH 2<br />
H 3C<br />
N NH<br />
S<br />
H<br />
N<br />
burimamida<br />
H<br />
N<br />
H<br />
N<br />
S<br />
H<br />
N<br />
Primer antagonista<br />
Antagonista puro<br />
Introducción de elementos en la cadena lateral para aproximar el pH al de<br />
la histamina<br />
CH 3<br />
HN<br />
N<br />
N<br />
CN<br />
cimetidina<br />
(primer anti H2 con utilidad terapéutica)<br />
CH 3<br />
65
Antihistamínicos H 2 de segunda generación:<br />
naturaleza no imidazólica<br />
H 3C<br />
CH 3<br />
N<br />
O<br />
Ranitidina<br />
S<br />
S<br />
N<br />
H<br />
N<br />
N<br />
CH 3<br />
NO 2<br />
N<br />
H<br />
S<br />
CH 3<br />
CH 3<br />
H<br />
N<br />
N<br />
N<br />
S<br />
H 2N NH 2<br />
H<br />
N<br />
N<br />
NO2<br />
Nizatidina<br />
CH 3<br />
S<br />
Famotidina<br />
H<br />
N NH 2<br />
N SO2NH 2<br />
66