BỘ ĐỀ THI+HƯỚNG DẪN CHẤM CHÍNH THỨC CÁC SỞ GIÁO DỤC KÌ THI CHỌN HỌC SINH GIỎI CẤP TỈNH LỚP 9 THCS NĂM HỌC 2011-2012 MÔN HÓA HỌC
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/0B_NNtKpVZTUYSGNvaGlNdVl0LXM/view?usp=sharing
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/0B_NNtKpVZTUYSGNvaGlNdVl0LXM/view?usp=sharing
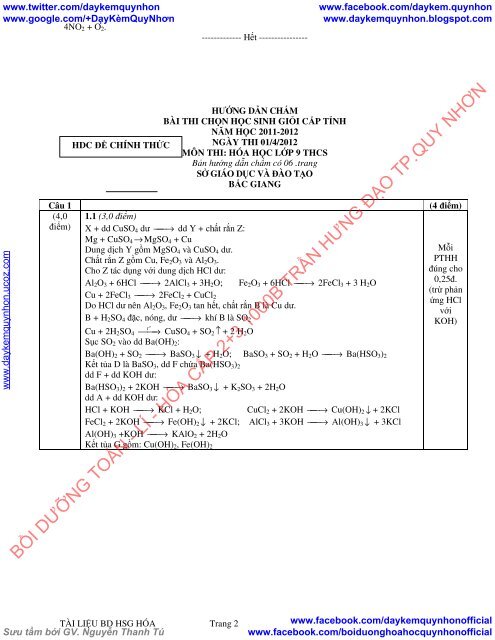
www.twitter.com/daykemquynhon www.google.com/+DạyKèmQuyNhơn 4NO 2 + O 2 . ------------- Hết ---------------- www.facebook.com/daykem.quynhon www.daykemquynhon.blogspot.com www.daykemquynhon.ucoz.com Câu 1 (4,0 điểm) HƯỚNG DẪN CHẤM BÀI THI CHỌN HỌC SINH GIỎI CẤP TỈNH NĂM HỌC 2011-2012 HDC ĐỀ CHÍNH THỨC NGÀY THI 01/4/2012 MÔN THI: HÓA HỌC LỚP 9 THCS Bản hướng dẫn chấm có 06 .trang SỞ GIÁO DỤC VÀ ĐÀO TẠO BẮC GIANG 1.1 (3,0 điểm) X + dd CuSO 4 dư ⎯ ⎯→ dd Y + chất rắn Z: Mg + CuSO 4 →MgSO 4 + Cu Dung dịch Y gồm MgSO 4 và CuSO 4 dư. Chất rắn Z gồm Cu, Fe 2 O 3 và Al 2 O 3 . Cho Z tác dụng với dung dịch HCl dư: Al 2 O 3 + 6HCl ⎯ ⎯→ 2AlCl 3 + 3H 2 O; Fe 2 O 3 + 6HCl ⎯ ⎯→ 2FeCl 3 + 3 H 2 O Cu + 2FeCl 3 ⎯ ⎯→ 2FeCl 2 + CuCl 2 Do HCl dư nên Al 2 O 3 , Fe 2 O 3 tan hết, chất rắn B là Cu dư. B + H 2 SO 4 đặc, nóng, dư ⎯ ⎯→ khí B là SO 2 o t Cu + 2H 2 SO 4 ⎯⎯→ CuSO 4 + SO 2 ↑ + 2 H 2 O Sục SO 2 vào dd Ba(OH) 2 : Ba(OH) 2 + SO 2 ⎯ ⎯→ BaSO 3↓ + H 2 O; BaSO 3 + SO 2 + H 2 O ⎯ ⎯→ Ba(HSO 3 ) 2 Kết tủa D là BaSO 3 , dd F chứa Ba(HSO 3 ) 2 dd F + dd KOH dư: Ba(HSO 3 ) 2 + 2KOH ⎯ ⎯→ BaSO 3↓ + K 2 SO 3 + 2H 2 O dd A + dd KOH dư: HCl + KOH ⎯ ⎯→ KCl + H 2 O; CuCl 2 + 2KOH ⎯ ⎯→ Cu(OH) 2↓ + 2KCl FeCl 2 + 2KOH ⎯ ⎯→ Fe(OH) 2↓ + 2KCl; AlCl 3 + 3KOH ⎯ ⎯→ Al(OH) 3↓ + 3KCl Al(OH) 3 +KOH ⎯ ⎯→ KAlO 2 + 2H 2 O Kết tủa G gồm: Cu(OH) 2 , Fe(OH) 2 (4 điểm) Mỗi PTHH đúng cho 0,25đ. (trừ phản ứng HCl với KOH) BỒI DƯỠNG TOÁN - LÍ - HÓA CẤP 2+3 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN TÀI LIỆU BD HSG HÓA Trang 2 Sưu tầm bởi GV. Nguyễn Thanh Tú www.facebook.com/daykemquynhonofficial www.facebook.com/boiduonghoahocquynhonofficial
www.twitter.com/daykemquynhon www.facebook.com/daykem.quynhon www.google.com/+DạyKèmQuyNhơn 1.2 www.daykemquynhon.blogspot.com Gọi số mol của A, B lần lượt là x, y mol. ⇒ (14n+16)x + (14n + 18)y = 13,2 ⇒ 14nx+16x + 14ny + 18y = 13,2 (*) 29,7 Bảo toàn nguyên tố cacbon: n CO 2 = nx + ny = = 0,675mol (**) 44 Từ (*) và (**) ⇒ 16x + 18y = 13,2 - 14 x 0,675 = 3,75 ⇒ 16(x+y) m 2 Fe = 0,1 . 56 = 5,6(g) 11,6 → mFe 17, 2 5, 6 11, 6( ) xO = − = g → n ( mol ) y Fe x O y 56 x + 16 y n = (*) Từ (1): n HCl = 2 H2 = 2.0,1= 0,2 (mol) m ddA = 200 + 17,2 − 0,2 = 217( g) m ddB = 217 + 33 = 250 (g) 250.2,92 n HCl dư = = 0,2( mol) 100.36,5 n HCl ở (2) = 0,8 - 0,2 - 0,2 = 0,4(mol) n Fe x O y 1 = . n 2 y HCl 1 = .0,4 = 2 y 0,2 ( mol ) y (**) Mỗi PTHH đúng cho 0,25đ. BỒI DƯỠNG TOÁN - LÍ - HÓA CẤP 2+3 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN 0,25đ 0,25đ www.facebook.com/daykemquynhonofficial www.facebook.com/boiduonghoahocquynhonofficial
- Page 1: www.twitter.com/daykemquynhon www.g
- Page 5 and 6: www.twitter.com/daykemquynhon www.f
- Page 7 and 8: www.twitter.com/daykemquynhon www.f
- Page 9 and 10: www.twitter.com/daykemquynhon www.g
- Page 11 and 12: www.twitter.com/daykemquynhon www.f
- Page 13 and 14: www.twitter.com/daykemquynhon www.f
- Page 15 and 16: www.twitter.com/daykemquynhon www.g
- Page 17 and 18: www.twitter.com/daykemquynhon www.f
- Page 19 and 20: www.twitter.com/daykemquynhon www.g
- Page 21 and 22: www.twitter.com/daykemquynhon www.g
- Page 23 and 24: www.twitter.com/daykemquynhon www.g
- Page 25 and 26: www.twitter.com/daykemquynhon www.f
- Page 27 and 28: www.twitter.com/daykemquynhon www.f
- Page 29 and 30: www.twitter.com/daykemquynhon www.g
- Page 31 and 32: www.twitter.com/daykemquynhon www.g
- Page 33 and 34: www.twitter.com/daykemquynhon www.g
- Page 35 and 36: www.twitter.com/daykemquynhon www.g
- Page 37 and 38: www.twitter.com/daykemquynhon www.f
- Page 39 and 40: www.twitter.com/daykemquynhon www.g
- Page 41 and 42: www.twitter.com/daykemquynhon www.g
- Page 43 and 44: www.twitter.com/daykemquynhon www.f
- Page 45 and 46: www.twitter.com/daykemquynhon www.g
- Page 47 and 48: www.twitter.com/daykemquynhon www.f
- Page 49 and 50: www.twitter.com/daykemquynhon www.f
- Page 51 and 52: www.twitter.com/daykemquynhon www.g
www.twitter.com/daykemquynhon<br />
www.google.com/+DạyKèmQuyNhơn<br />
4NO 2 + O 2 .<br />
------------- Hết ----------------<br />
www.facebook.com/daykem.quynhon<br />
www.daykemquynhon.blogspot.com<br />
www.daykemquynhon.ucoz.com<br />
Câu 1<br />
(4,0<br />
điểm)<br />
HƯỚNG <strong>DẪN</strong> <strong>CHẤM</strong><br />
BÀI <strong>THI</strong> <strong>CHỌN</strong> <strong>HỌC</strong> <strong>SINH</strong> <strong>GIỎI</strong> <strong>CẤP</strong> <strong>TỈNH</strong><br />
<strong>NĂM</strong> <strong>HỌC</strong> <strong>2011</strong>-<strong>2012</strong><br />
HDC <strong>ĐỀ</strong> <strong>CHÍNH</strong> <strong>THỨC</strong> NGÀY <strong>THI</strong> 01/4/<strong>2012</strong><br />
<strong>MÔN</strong> <strong>THI</strong>: <strong>HÓA</strong> <strong>HỌC</strong> <strong>LỚP</strong> 9 <strong>THCS</strong><br />
Bản hướng dẫn chấm có 06 .trang<br />
<strong>SỞ</strong> <strong>GIÁO</strong> <strong>DỤC</strong> VÀ ĐÀO TẠO<br />
BẮC GIANG<br />
1.1 (3,0 điểm)<br />
X + dd CuSO 4 dư ⎯ ⎯→ dd Y + chất rắn Z:<br />
Mg + CuSO 4 →MgSO 4 + Cu<br />
Dung dịch Y gồm MgSO 4 và CuSO 4 dư.<br />
Chất rắn Z gồm Cu, Fe 2 O 3 và Al 2 O 3 .<br />
Cho Z tác dụng với dung dịch HCl dư:<br />
Al 2 O 3 + 6HCl ⎯ ⎯→ 2AlCl 3 + 3H 2 O; Fe 2 O 3 + 6HCl ⎯ ⎯→ 2FeCl 3 + 3 H 2 O<br />
Cu + 2FeCl 3 ⎯ ⎯→ 2FeCl 2 + CuCl 2<br />
Do HCl dư nên Al 2 O 3 , Fe 2 O 3 tan hết, chất rắn B là Cu dư.<br />
B + H 2 SO 4 đặc, nóng, dư ⎯ ⎯→ khí B là SO 2<br />
o<br />
t<br />
Cu + 2H 2 SO 4 ⎯⎯→ CuSO 4 + SO 2 ↑ + 2 H 2 O<br />
Sục SO 2 vào dd Ba(OH) 2 :<br />
Ba(OH) 2 + SO 2 ⎯ ⎯→ BaSO 3↓ + H 2 O; BaSO 3 + SO 2 + H 2 O ⎯ ⎯→ Ba(HSO 3 ) 2<br />
Kết tủa D là BaSO 3 , dd F chứa Ba(HSO 3 ) 2<br />
dd F + dd KOH dư:<br />
Ba(HSO 3 ) 2 + 2KOH ⎯ ⎯→ BaSO 3↓ + K 2 SO 3 + 2H 2 O<br />
dd A + dd KOH dư:<br />
HCl + KOH ⎯ ⎯→ KCl + H 2 O; CuCl 2 + 2KOH ⎯ ⎯→ Cu(OH) 2↓ + 2KCl<br />
FeCl 2 + 2KOH ⎯ ⎯→ Fe(OH) 2↓ + 2KCl; AlCl 3 + 3KOH ⎯ ⎯→ Al(OH) 3↓ + 3KCl<br />
Al(OH) 3 +KOH ⎯ ⎯→ KAlO 2 + 2H 2 O<br />
Kết tủa G gồm: Cu(OH) 2 , Fe(OH) 2<br />
(4 điểm)<br />
Mỗi<br />
PTHH<br />
đúng cho<br />
0,25đ.<br />
(trừ phản<br />
ứng HCl<br />
với<br />
KOH)<br />
BỒI DƯỠNG TOÁN - LÍ - <strong>HÓA</strong> <strong>CẤP</strong> 2+3 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
TÀI LIỆU BD HSG <strong>HÓA</strong> Trang 2<br />
Sưu tầm bởi GV. Nguyễn Thanh Tú<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial