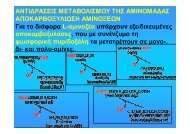
Δυσλιπιδαιμία, φλεγμονή, αθηρογένεση - ρόλος του PAF97τελεί μία από τις κυριότερες οδούς μεταγωγής σήματος πουενεργοποιείται ως απόκριση σε προφλεγμονώδεις κυτταροκίνεςόπως ο νεκρωτικός παράγοντας όγκων-α (TumorNecrosis Factor-alpha, TNF-a), οι ιντερλευκίνες-1 και -8(IL-1 and IL-8), καθώς και μέσω της ενεργοποίησης τωνTL υποδοχέων 8 .ΑθηροσκλήρωσηΣτα μέσα της δεκαετίας του 1970, η θεωρία των λιποειδών(Lipid theory) για την αθηρογένεση έδωσε τη θέσητης στη θεωρία της απόκρισης στον τραυματισμό (responseto injury hypothesis) που αναπτύχθηκε από τον Russel Ross.Η θεωρία αυτή δεχόταν ως αξίωμα ότι οι αθηροσκληρωτικέςβλάβες αναπτύσσονται ως αποτέλεσμα τοπικού τραυματισμούστο αρτηριακό ενδοθήλιο, που ακολουθείται απόπροσκόλληση και συσσώρευση αμοπεταλίων 9 .Αργότερα διαπιστώθηκε ότι και η ενεργοποίηση του ενδοθηλίουαρκούσε ώστε να λάβουν χώρα οι ανοσοφλεγμονώδειςαποκρίσεις που διέπουν την αθηροσκληρωτικήδιαδικασία. Η παρατήρηση από τους Poole και Florey ότι ηχορήγηση χοληστερόλης στην τροφή κουνελιών 10 οδηγείσε προσκόλληση μονοκυττάρων στο ενδοθήλιο τα οποίαστη συνέχεια μεταναστεύουν, μέσω του μορφολογικά άθικτουενδοθηλίου, στον υποενδοθηλιακό χώρο, οδήγησετον Michael Gimbrone να προτείνει ότι κατά την αθηροσκλήρωσησυμβαίνει μία τροποποίηση του φυσιολογικούενδοθηλίου σε ένα δυσλειτουργικό ενδοθήλιο, με αποτέλεσματην απώλεια της προστατευτικής επίδρασής του 11 .Σήμερα είναι αποδεκτό ότι η αθηροσκλήρωση είναι μίαχρόνια φλεγμονώδης ασθένεια κατά την έναρξη της οποίαςπαρατηρείται προσκόλληση μονοκυττάρων/λεμφοκυττάρωνστο ενεργοποιημένο ενδοθήλιο 12 .Ο ρόλος του Παράγοντα ΕνεργοποίησηςΑιμοπεταλίωνΈνας αριθμός βιοδραστικών λιποειδικών μεσολαβητώνέχουν χαρακτηριστεί ως πρωταρχικοί ενεργοποιητές τηςαθηρογένεσης. Ανάμεσα σε αυτούς ο Παράγοντας ΕνεργοποίησηςΑιμοπεταλίων (Platelet Activating Factor, PAF)και τα ανάλογά του αποτελούν τους ισχυρότερους λιποειδικούςφλεγμονώδεις μεσολαβητές. Ο PAF είναι σε θέσηνα επάγει την παραγωγή TNF-α από τα μονοκύτταρα μεμηχανισμό ίδιο με των Ox-LDLs 13 . Επιπλέον, μετά την ανίχνευσηαπό την ερευνητική μας ομάδα παραγόμενου PAFστα σωματίδια των ox-LDLs 14 η δραστικότητα των σωματιδίωναυτών αποδόθηκε στα μόρια του PAF 15 . Μία απότις σημαντικότερες δράσεις του PAF κατά την έναρξη τηςαθηρογένεσης είναι η μεσολάβησή του για προσκόλλησητων μονοκυττάρων στο ενδοθήλιο σε συνέργεια με τηνP-σελεκτίνη 16 . Ο PAF ενισχύει τη μεταφορά του πυρηνικούπαράγοντα κΒ (NF-κB) στον πυρήνα των ανθρώπινων μονοκυττάρωνπου είναι προσδεμένα στην P-σελεκτίνη καικατά τον τρόπο αυτό αυξάνεται δραματικά η βιοσύνθεσητης MCP-1, της IL-8, του παράγοντα νέκρωσης όγκων-α(TNF-α), και άλλων προϊόντων γονιδίων που σχετίζονταιμε τη φλεγμονή 17 .Η οξειδωμένη μορφή της 1-παλμιτοϋλο-2-αραχιδονοϋλο-s n-γλυκερο-3-φωσφορυλοχολίνης (Oxidized1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine,OxPAPC), αποτελεί ένα από τα ανάλογα του PAF που έχειανιχνευθεί στις τροποποιημένες LDL αλλά και στις αθηρωματικέςβλάβες. Η OxPAPC ενεργοποιεί τα ενδοθηλιακάκύτταρα και προωθεί την προσκόλληση μονοκυττάρων καιτην έκκριση της MCP-1, και της IL-8 18 . Ενδιαφέρον παρουσιάζειτο γεγονός ότι η OxPAPC αναστέλλει τη δέσμευσητων LPS στις πρωτεΐνες δέσμευσής τους (LPS-binding protein)που απαιτείται ώστε να εκθέσουν τους LPS για ναγίνει η σύνδεσή τους στους TLR-4. Αυτό υποδεικνύει ένανδιπλό ρόλο για τη δράση του PAF και των αναλόγων τουκαθώς φαίνεται ότι σε καταστάσεις οξείας φλεγμονής απόβακτηριακούς παράγοντες δρουν ως αντιφλεγμονώδειςπαράγοντες αναστέλλοντας την οδό του NF-κβ 19 , ενώ σεκαταστάσεις χρόνιας φλεγμονής, η δραστικότητά τους καθίσταταιυπεύθυνη για ανάπτυξη παθολογικών καταστάσεων18 .Η παραγωγή του PAFΤόσο οι ενδογενείς όσο και οι τροποποιημένες, μέσωοξείδωσης ή γλυκοζυλίωσης, λιποπρωτεΐνες του αίματοςαποτελούν συστατικά των αθηρωματικών πλακών και τωναφρωδών κυττάρων. Οι τροποποιημένες λιποπρωτεΐνεςείναι σε θέση να προκαλέσουν οξειδωτικό στρες με αποτέλεσματόσο την παραγωγή ελευθέρων ριζών όσο καιτου Παράγοντα Ενεργοποίησης των Αιμοπεταλίων (PAF)και των αναλογών του (PAF-like) (Σχήμα 1) 14,20-22 . Συγχρόνωςο PAF δεσμεύεται στους υποδοχείς σε κύτταρατου αίματος σηματοδοτώντας την εκ νέου παραγωγή τόσοελευθέρων ριζών όσο και νέας ποσότητας PAF 23,24 .Πολλές μελέτες in vitro και ex vivo σε πειραματόζωα καιανθρώπους αποδεικνύουν τα παραπάνω επιμέρους μηχανιστικάστάδια 25 . Επιπλέον, in vivo μελέτες που διενήργησεη ερευνητική μας ομάδα σε πειραματόζωα που τράφηκανμε τροφή πλούσια σε χοληστερόλη (αθηρογόνο δίαιτα,ΟΜΑΔΑ Γ) δείχνουν αύξηση των επιπέδων του PAF στοαίμα των πειραματόζωων (Σχήμα 2). Η αύξηση αυτή τωνεπιπέδων του PAF αφορά τόσο τον PAF που κυκλοφορείσυνδεδεμένος με λιποπρωτεΐνες (free PAF) όσο και τονPAF που είναι δεσμευμένος στα έμμορφα συστατικά τουαίματος (bound PAF) 26,27 .Τα αποτελέσματα αυτά επιβεβαιώνονται και ενισχύονταιαπό μελέτες που αφορούν τη δραστικότητα των μεταβολικώνενζύμων του PAF στο αίμα. Οι μελέτες αυτές αφορούντο ένζυμο της φωσφο-χολινο-τρανσφεράσης του PAF(PAF-cholinephosphotransferase; PAF-CPT, EC 2.7.8.16)που αποτελεί ρυθμιστικό ένζυμο της de novo βιοσυνθετικής
98 Χ.X. Καραντώνης και συν.Σχήμα 1. Σχηματική υπεραπλοποιημένη απόδοση της συσχέτισης της δυσλιπιδαιμίας με τη φλεγμονή και την αθηρογένεση.Η φλεγμονή, για την πρόκληση της αθηρογένεσης, μπορεί να προέλθει όχι μόνο από την χοληστερόλη αλλά και από άλλες αιτίες, όπωςπροϊόντα οξείδωσης (οξειδωτικό στρες), φλεγμονώδεις καταστάσεις και μολυσματικούς παράγοντες και μικροοργανισμούς. Η προστασίαμπορεί να ασκείται από τον περιορισμό της οξείδωσης (μείωση οξειδωτικού στρες), αναστολή επιπέδων χοληστερόλης, παρεμπόδισηενεργοποίησης υποδοχέων φλεγμονωδών ενώσεων, αναστολή βιολογικών δράσεων φλεγμονωδών ενώσεων, καθώςεπίσης και παρέμβαση στο μεταβολισμό των φλεγμονωδών ενώσεων, με αναστολή της βιοσύνθεσής τους. Η προστασία αυτή ασκείταιείτε από φάρμακα είτε από τρόφιμα.του οδού, το ένζυμο της ακετυλο-τρανσφεράσης του lyso-PAF (Lyso-PAF-acetyltransferase; Lyso-PAFAT, EC2.3.1.67), που αποτελεί το ρυθμιστικό ένζυμο της βιοσυνθετικήςτου οδού αναδιαμόρφωσης, (Σχήμα 3) καθώς καιτο ένζυμο της PAF ακετυλο-υδρολάσης (PAF-AH, EC3.1.1.47), όπου ανήκει και η ισομορφή που υπάρχει στοπλάσμα του αίματος, γνωστή ως λιποπρωτεϊνική φωσφολιπάσηΑ 2 (Lp-PLA 2 ), που αποτελεί το ρυθμιστικό ένζυμοτης οδού αποικοδόμησης του PAF 28 .Στις παραπάνω μελέτες μας η δραστικότητα των βιοσυνθετικώνενζύμων (PAF-CPT και lyso-PAF-AT) αυξάνεται σεέμμορφα συστατικά του αίματος, όπως τα λευκοκύτταρακαι τα αιμοπετάλια. Η αύξηση αυτή συνοδεύεται με μείωσητης δραστικότητας του αποικοδομητικού ενζύμου (PAF-AH)στα ίδια κύτταρα, ενώ η δραστικότητα της Lp-PLA 2 μετάαπό παροδική αύξηση στο πλάσμα των πειραματόζωων,επανέρχεται στα αρχικά της επίπεδα 28 .Τα παραπάνω αποτελέσματα επιβεβαιώνουν την αύξησητων επιπέδων του PAF στο αίμα των πειραματόζωων, σταοποία προκλήθηκε δυσλιπιδαιμία μέσω διατροφικής παρέμβασηςμε παροχή χοληστερόλης και συγχρόνως φανερώνουνως κύρια πηγή προέλευσης του PAF τα λευκοκύτταρατου αίματος 28 . Αξίζει δε να σημειωθεί ότι ο PAF που υπάρχειστο αίμα μπορεί - ανάλογα με την κατάσταση των οργανισμών- να προέρχεται και από άλλες πηγές, καθώς παράγεταιαπό πληθώρα κυττάρων και ιστών.Η πρόκληση της φλεγμονήςΟ PAF και τα ανάλογά του που παράγονται κατά το οξειδωτικόστρες απαντώνται είτε στις Ox-LDL, είτε σε κύτταρατου αίματος και του ενδοθηλίου είτε ελευθερώνονται στηνκυκλοφορία του αίματος. Μετά την παραγωγή τους προσδένονταιστους υποδοχείς του PAF, που υπάρχουν στα κύτταρατου αίματος και του ενδοθηλίου σηματοδοτώντας τηνπρόκληση φλεγμονής 21,24 .Καταστάσεις στις οποίες δεν μπορεί να ρυθμιστεί η διαδικασίατης φλεγμονής από τον οργανισμό, λόγω ανεξέλεγκτηςκαι παρατεταμένης σηματοδότησης, οδηγεί σε χρόνιαφλεγμονή προκαλώντας την έναρξη της αθηρογένεσης.Σύμφωνα με την «νέα θεωρία της αθηρογένεσης με εμπλοκήτου PAF» προτείνουμε συγκεκριμένο μηχανισμό, σύμφωνα