7. Substitution am Aromaten - Institut für Organische Chemie
7. Substitution am Aromaten - Institut für Organische Chemie
7. Substitution am Aromaten - Institut für Organische Chemie
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong><br />
Versuche im Praktikum (Nummerierung wie dort) (S E Ar), Teil 1:<br />
4.1 Bromierung von Arenen<br />
4-Brom-tert.-butylbenzol, Brommesitylen, 1-Brom-2-methylnaphthalen<br />
4.2 Nitrierung von unterschiedlichen aktivierten Arenen<br />
(4-Nitrophenyl)acetonitril, 3-Nitrobenzoesäuremethylester, 4-Bromnitrobenzol, 4-Nitroveratrol<br />
4.3 Vilsmeier-Formylierung<br />
Thiophen-2-carbaldehyd, Zimtaldehyd, 4-Dimethyl<strong>am</strong>inobenzaldehyd, 4-Diethyl<strong>am</strong>inobenzaldehyd, 3,4-<br />
Dimethoxybenzaldehyd<br />
4.4 Friedel-Crafts-Alkylierung<br />
4-iso-Propyltoluen, 4-tert.-Butyltoluen, 4-Propyltoluen<br />
4.5 Friedel-Crafts-Acylierung<br />
TU BS, Lindel<br />
4-Methylacetophenon, Methyl-α-naphthylketon, 3,4-Dimethoxyacetophenon, 4-Chloracetophenon, 4-<br />
Bromacetophenon, 2,4-Dimethylacetophenon<br />
4.6 Acylierung aromatischer Kohlenwasserstoffe mit Anhydriden<br />
4-Methoxyacetophenon, β-(4-Methylbenzoyl)-propionsäure<br />
4.7 Acylierung aromatischer Kohlenwasserstoffen mit Phthalsäureanhydrid<br />
4-Ethyl-benzoylbenzoesäure, Methyl-benzoylbenzoesäure, Phenyl-benzoylbenzoesäure<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong><br />
Versuche im Praktikum (Nummerierung wie dort) (S E Ar), Teil 2:<br />
11 Farbstoffsynthese<br />
11.1 Azokupplung<br />
1-(Phenylazo)-2-naphthol, β-Naphtholorange, Pararot, 4-Hydroxy-4'-nitro-azobenzol-3-carbonsäure,<br />
Methylorange, Methylrot, 1-Benzolazo-2-naphthol (Sudangelb), 4-Benzolazo-1-naphthol<br />
11.2 Indigo<br />
11.3 Triphenylmethanfarbstoffe: Fluorescein, Eosin<br />
11.4 Kupferphthalocyanin<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>1. S E Ar-Mechanismus<br />
<strong>7.</strong>1. S E Ar-Mechanismus<br />
Gemeins<strong>am</strong>er Reaktionsmechanismus (X=H, tBu, SO 3 H):<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>2. Wichtige S E Ar-Reaktionen<br />
<strong>7.</strong>2. Wichtige S E Ar-Reaktionen - <strong>7.</strong>2.1. Kurzübersicht<br />
ArH +<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>2. Wichtige S E Ar-Reaktionen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>2. Wichtige S E Ar-Reaktionen<br />
<strong>7.</strong>2.2. Friedel-Crafts-Alkylierung<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>2. Wichtige S E Ar-Reaktionen<br />
<strong>7.</strong>2.3. Vilsmeier-Haack-Formylierung (1925)<br />
Iminiumsalz<br />
TU BS, Lindel<br />
N,N-Dimethylchloriminium<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>2. Wichtige S E Ar-Reaktionen<br />
<strong>7.</strong>2.4. De-tert.-butylierung<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
<strong>7.</strong>3. S E Ar-Reaktionen: Zweitsubstitution<br />
<strong>7.</strong>3.1. Mechanismen<br />
a)<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
b)<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
c) regiodirigierende Erstsubstituenten<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
<strong>7.</strong>3.2. Beispiele<br />
a)<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
b)<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
c)<br />
σ-Komplex<br />
mit 2 aromatischen Grenzformen<br />
an Naphthalin<br />
σ-Komplex<br />
mit 1 aromatischen Grenzform<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
d) Farbstoffsynthese durch Azokupplung<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>3. S E Ar-Zweitsubstitution<br />
vorher: Diazotierung<br />
NH 2 NaNO 2<br />
HCl<br />
NO<br />
0-5°C<br />
O<br />
N<br />
N<br />
H<br />
H<br />
H<br />
O<br />
N<br />
N<br />
+<br />
H<br />
N 2<br />
Cl<br />
OH<br />
N<br />
N<br />
-H 2O<br />
HCl<br />
Cl<br />
H H<br />
O<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
N<br />
N
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>4. S R Ar-Reaktion<br />
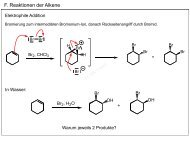
<strong>7.</strong>4. Radikalische <strong>Substitution</strong><br />
z. B.<br />
Sandmeyer-Reaktionen<br />
TU BS, Lindel<br />
Mech.:<br />
Bei X=I muss kein CuI<br />
zugesetzt werden. Warum?<br />
verwandt: Schiemann-<br />
Reaktion zu Fluorarenen:<br />
Zusatz von HBF 4 (-BF 3 ).<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>5. S N Ar-Reaktion<br />
<strong>7.</strong>5. S N Ar-Reaktion<br />
<strong>7.</strong>5.1. Additions-Eliminierungs-Mech.<br />
Im Detail:<br />
Angriff d. Nukleophils in o- und p-<br />
Stellung, da bei m-Angriff die negative<br />
Ladung nicht auf den elektronenziehenden<br />
Substituenten delokalisierbar ist.<br />
Meisenheimer-Salze, isolierbar<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>5. S N Ar-Reaktion<br />
Best. d. N-terminalen A.-s. mit Sangers Reagenz:<br />
H 2N<br />
O 2N<br />
O 2N<br />
R 1<br />
O<br />
N<br />
H<br />
NO 2<br />
NO 2<br />
R 2<br />
H<br />
N<br />
H<br />
N<br />
O<br />
R 1<br />
R 1<br />
H<br />
N<br />
O<br />
O<br />
R 3<br />
N<br />
H<br />
OH<br />
zur Vergleichsanalyse<br />
O<br />
R 2<br />
OH<br />
O<br />
H<br />
N<br />
R 3<br />
O 2N<br />
O<br />
R 2<br />
NO 2<br />
TU BS, Lindel<br />
OH<br />
F<br />
Sangers Reagenz<br />
+<br />
H2N OH +<br />
O<br />
6 M HCl, ∆<br />
H 2N<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
R 3<br />
O<br />
OH<br />
Sir Frederick Sanger<br />
(*1918)<br />
2 Nobelpreise <strong>für</strong> <strong>Chemie</strong><br />
1958 und 1980!
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>5. S N Ar-Reaktion<br />
<strong>7.</strong>5.2. Eliminierungs-Additions-Mech.<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>6. Halogen-Metall-Austausch<br />
<strong>7.</strong>6. Halogen-Metall-Austausch<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
<strong>7.</strong> <strong>Substitution</strong> <strong>am</strong> <strong>Aromaten</strong> - <strong>7.</strong>6. Halogen-Metall-Austausch<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
8. Oxidation<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
5.1 Oxidation von Alkylaromaten zu aromatischen Carbonsäuren mit KMnO 4<br />
Benzoesäure, Phthalsäure, Terephthalsäure<br />
5.2 Oxidation von prim. Alkoholen und Olefinen unter Phasentransferkatalyse<br />
Hexansäure, Oktansäure, Heptansäure<br />
5.3 Carbonsäuren aus Methylketonen durch Haloformreaktion<br />
Benzoesäure, Veratrumsäure, 4-Chlorbenzoesäure, 4-Brombenzoesäure, α-Naphthoesäure<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
8. Oxidation - 8.1. zu Aldehyden und Ketonen<br />
Oxidation v. Alkenen s. Kap. 6.<br />
8.1. Alkohole zu Aldehyden und Ketonen<br />
prim. Alkohol<br />
sek. Alkohol<br />
gem. Diol<br />
Halbacetal<br />
Y Ox n<br />
H<br />
H<br />
O<br />
O<br />
Ox<br />
R<br />
H<br />
X<br />
R<br />
H<br />
X<br />
+n<br />
m<br />
Y<br />
O<br />
m+2<br />
R X<br />
H 2 O<br />
charge<br />
In Anwesenheit von Wasser:<br />
TU BS, Lindel<br />
Aldehyd<br />
Keton<br />
Carbonsäure<br />
Carbonsäureester<br />
Weiteroxidation im Ggew. befindlicher Halbacetale zu Carbonsäuren.<br />
m, n: Oxidationsstufen.<br />
Wenn Y einfach an das<br />
Oxidationsmittel Ox gebunden,<br />
dann Freisetzung von HY.<br />
Ox n-2<br />
+ Y<br />
+ H +<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
H<br />
charge-1
8. Oxidation - 8.1. zu Aldehyden und Ketonen<br />
8.1.1. Chrom(VI)-Reagenzien:<br />
CrO 3 -verd. H 2 SO 4 od. HOAc in Aceton (Jones-Oxidation, ungeeignet, wenn es interessant wird,<br />
"sledge h<strong>am</strong>mer method");<br />
CrO 3 ·2 Pyr in DCM (wasserfr. => Ox. nur zum Aldehyd, "Collins-Reag.").<br />
Pyridiniumchlorochromat (PCC, schwach sauer),<br />
Pyridiniumdichromat (PDC, neutral)<br />
8.1.2. Ley-Oxidation:<br />
kat. nPr4N RuVIIO4 (Tetra-N-propyl<strong>am</strong>moniumperruthenat, TPAP), stöch. NMO.<br />
R 1<br />
R 2<br />
H<br />
O<br />
H<br />
n Pr4N + RuO 4 - (5 mol-%),<br />
NMO (1.5 Äquiv.),<br />
DCM-MeCN (9:1), 4 A, rt<br />
TU BS, Lindel<br />
R 1<br />
- f. prim. od. sek. Alkohole;<br />
-milder als Ru VIII O 4 , löslich in org. LM;<br />
- auch andere Oxidationstufen von Ru sind beteiligt.<br />
O<br />
R 2<br />
CrO 3 Cl –<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
N<br />
O<br />
N-Methylmorpholin-N-oxid
8. Oxidation - 8.1. zu Aldehyden und Ketonen<br />
8.1.3. Swern-Oxidation; Agens "aktiviertes DMSO":<br />
O<br />
S<br />
DMSO<br />
OH<br />
R 1 R 2<br />
Edukt<br />
Cl<br />
O<br />
O<br />
Cl<br />
Oxalylchlorid<br />
R 2<br />
R<br />
O<br />
S<br />
1 H<br />
H<br />
O<br />
S<br />
NEt 3<br />
Cl<br />
O<br />
O<br />
Cl<br />
R 2<br />
TU BS, Lindel<br />
R<br />
O<br />
S<br />
CH2<br />
1 H<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
S<br />
Cl<br />
O<br />
O<br />
Cl<br />
R 2<br />
R 1 +<br />
O<br />
Produkt<br />
+<br />
+<br />
Cl<br />
S<br />
O C O<br />
C O ,+Cl<br />
Reaktion bei -78 °C; zuerst Bildung von CO 2 und CO abwarten, dann Zugabe des Edukts und<br />
nach ca. 30 min Zugabe von NEt 3 .<br />
S
8. Oxidation - 8.1. zu Aldehyden und Ketonen<br />
8.1.4. Dess-Martin-Oxidation<br />
CO 2 H<br />
I<br />
KBrO 3<br />
HO<br />
o-Iodbenzoesäure IBX<br />
I<br />
O<br />
O<br />
O<br />
Ac 2 O<br />
TU BS, Lindel<br />
AcO<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
I<br />
O<br />
O<br />
OAc<br />
OAc<br />
Dess-Martin-<br />
Periodinan (DMP)<br />
Formulieren Sie den Mech. der Oxidation vom Alkohol zum Aldehyd mit DMP!
8. Oxidation - 8.1. zu Aldehyden und Ketonen<br />
8.1.5. Transfer-Dehydrierung<br />
Oppenauer-Oxidation<br />
z. B.:<br />
HO<br />
via<br />
OH<br />
OH<br />
H<br />
H H<br />
O<br />
(i) Übersch.<br />
iPrO OiPr<br />
Al<br />
O O<br />
H<br />
TU BS, Lindel<br />
O<br />
1)<br />
-<br />
, Al(OiPr) 3,<br />
PhMe, Rückfluss<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
OH<br />
(ii) Alkoholyse<br />
- häufig stöchiom. Mengen Al(OiPr) 3<br />
(i) Al(OiPr) 3, PhMe,<br />
Rückfl., 5 h<br />
N O<br />
(ii) 1% HCl, 0 °C<br />
2) TsOH, Et 2O, rt, 18 h<br />
HO<br />
H<br />
H H<br />
O<br />
O
8. Oxidation - 8.2. zu Carboxylverbindungen<br />
8.2. zu Carboxylverbindungen<br />
8.2.1. KMnO4 a) Alkohole zu Carbonsäuren unter Phasentransfer-Katalyse. Gefahr v. C-C-Spaltungen (wie?).<br />
O<br />
KMnO4, CH2Cl2, H2O Cl<br />
N<br />
Hauptbest. v. "Aliquat 336"<br />
OH "Aliquat 336"<br />
OH<br />
TU BS, Lindel<br />
b) Oxidation zu Arylcarbonsäuren gut mögl., da im Produkt kein α-H mehr.<br />
H<br />
H H H<br />
H<br />
O<br />
H<br />
-e -H -e<br />
-H<br />
Elektronenakzeptor: Oxidationsmittel KMnO 4 .<br />
Phasentransferkatalysator: in DCM (aber n. in Wasser)<br />
lösl. Tetraalkyl<strong>am</strong>monium-Ion schleppt MnO 4 − in die<br />
org. Phase.<br />
Weiteroxidation des Benzylalkohols zur Dihydroxyverbindung, dann oxidative Spaltung des Enols<br />
zu Benzoesäure.<br />
H OH<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
8. Oxidation - 8.2. zu Carboxylverbindungen<br />
8.2.2. Aldehyd zur Carbonsäure mit Natriumchlorit (NaClO 2 ), Pinnick-Oxidation (1981):<br />
R<br />
O<br />
H<br />
Na<br />
O Cl<br />
O<br />
R<br />
O<br />
Na<br />
H<br />
O Cl<br />
O<br />
TU BS, Lindel<br />
alternativer HOCl-Fänger (Zusatz v. z. B. 10 Äquiv.):<br />
HOCl<br />
HO<br />
Cl<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
OH<br />
R + NaOCl<br />
O<br />
stark oxidierend, kann durch H 2 O 2<br />
zu Chlorit reoxidiert werden<br />
(Reaktion?)
8. Oxidation - 8.2. zu Carboxylverbindungen<br />
8.2.3. Iodoformprobe auf Methylketone (Haloform-Reaktion)<br />
R<br />
O<br />
KI 3<br />
Na<br />
R<br />
O<br />
I<br />
O H<br />
I<br />
I<br />
HO<br />
CI 3<br />
R O<br />
Auch mit Cl 2 , Br 2 ausführbar; Erweiterung:<br />
Trichlormethylketone als aktivierte Carbonsäure.<br />
Na<br />
TU BS, Lindel<br />
R O<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
O<br />
R OH<br />
Na<br />
Na<br />
+<br />
+<br />
H<br />
I<br />
I<br />
I<br />
I<br />
I<br />
I<br />
gelb, fest
8. Oxidation - 8.2. zu Carboxylverbindungen<br />
8.2.4. Baeyer-Villiger-Oxidation:<br />
Menthon<br />
Es wandert der höher substituierte Rest unter Retention<br />
der Stereochemie aus antiperiplanarer Position.<br />
TU BS, Lindel<br />
Nebenreaktion b. d. Epoxidierung von Alkenen!<br />
Ozonolyse/reduktive Aufarbeitung des Silylenolethers (unten) zum regioisomeren Lacton<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
5.4 Reduktion von Ketonen zu Alkoholen mit NaBH4 5-Nonanol, 3-Octanol, 2-Octanol, 4-tert.-Butylcyclohexanol<br />
5.5 Reduktion einer Ketocarbonsäure zur Hydroxysäure mit NaBH 4<br />
4-(p-Tolyl)-4-hydroxybutansäure<br />
5.6 Reduktion mit LiAlH4 1-(p-Tolyl)-butan-1,4-diol, 4-tert.-Butylcyclohexanol, 2-Hydroxybenzylalkohol, rac-α-Phenylethanol<br />
5.7 Reduktion aromatischer Nitroverbindungen<br />
3,4-Dimethoxyanilin, Anilin, 4-Bromanilin<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
9.1. Hydrid-Übertragung<br />
Hydroborierung s. Kap. 6 .<br />
9.1.1. Transfer-Hydrierung<br />
a) mit Alkoholen: Meerwein-Ponndorf-Verley-Reduktion (Rückreaktion der Oppenauer-Oxidation)<br />
z. B.:<br />
O<br />
O<br />
N<br />
O<br />
(i) wasserfr. iPrOH,<br />
20 Äquiv. Al(OiPr) 3 ,<br />
Rückfl., 24 h<br />
(ii) 5% HCl<br />
O<br />
dr 4:1<br />
HO<br />
H<br />
1. MeI, Et 4NBr,<br />
KOH, THF, rt, 18 h<br />
2. Übersch. AlH 3 ,<br />
THF, rt, 2 h<br />
TU BS, Lindel<br />
O<br />
O<br />
H<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
N<br />
N<br />
O
9. Reduktion - 9.1. Hydrid-Übertragung<br />
b) mit Aldehyden: Cannizzaro-Disproportionierung<br />
z. B.: O O O<br />
TU BS, Lindel<br />
c) mit Ameisensäure: Reduktive Aminierung nach Leuckart-Wallach<br />
R 1<br />
O<br />
2<br />
über<br />
R 2<br />
+<br />
R N<br />
H<br />
R<br />
KOH<br />
100 °C, 5 min<br />
HCO 2H<br />
160 °C<br />
-CO 2<br />
R<br />
R 1<br />
N<br />
R<br />
R 2<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
K<br />
+<br />
via<br />
O<br />
O<br />
HO<br />
41 % 38 %<br />
H NR2<br />
H<br />
R 2<br />
R 1
9. Reduktion - 9.1. Hydrid-Übertragung<br />
9.1.2. Reduktion mit B- und Al-Hydriden<br />
a) NaBH 4<br />
Carbonyl-Kohlenstoff von<br />
Aldehyden ist reaktiver als<br />
der von Ketonen.<br />
TU BS, Lindel<br />
Luche-Reduktion:<br />
Carbonyl-Sauerstoff von<br />
Ketonen basischer als der<br />
von Aldehyden (wg. des<br />
doppelten +I-Effekts der<br />
flankierenden<br />
Alkylgruppen).<br />
auch: 1,2-Reduktion von<br />
α,β-unges. Ketonen.<br />
NaBH 4 wird in Wasser nur langs<strong>am</strong> zersetzt und eignet sich <strong>für</strong> nur wasserlösliche Substrate.<br />
NaB(OMe) 3 H bildet sich aus NaBH 4 /MeOH und ist aktiver.<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
b) LiAlH 4<br />
Amid-Reduktion:<br />
ebenso von<br />
Hydroxyl<strong>am</strong>inen,<br />
Oximen, Nitroverb.,<br />
Aziden<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
Reduktion von Epoxiden<br />
regioselektiver Angriff von<br />
Hydrid an der sterisch weniger<br />
gehinderten Epoxid-Seite<br />
LiBEt 3 H: "Superhydrid", sicherer als LiAlH 4 .<br />
TU BS, Lindel<br />
komplexe Hydride desto nukleophiler, je größer der +(I/M)-Effekt der Subst. an B bzw. Al;<br />
andere Richtung: NaB(CN)H 3 .<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
c) DIBAL-H<br />
aus: Brückner, Reaktionsmechanismen<br />
LM THF beschleunigt.<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
d) L-Selectrid<br />
Sperriger Hydrid-<br />
Donor L-Selectrid<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Sperrige Lewis-<br />
Säure<br />
Aluminoxan<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
9.1.3. Diastereoselektivität<br />
a) konvex > konkav<br />
aus: Brückner, Reaktionsmechanismen<br />
endo-Alkohol<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.1. Hydrid-Übertragung<br />
Nur L-Selectrid führt, aus sterischem Grund, zur Bildung des axialen Alkohols:<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Bei sterisch anspruchslosen Reagenzien Angriff von Hydrid aus axialer Richtung:<br />
Überlappung des entstehenden σ-MOs der C-H-Bindung mit dem σ*-MO der trans-ständigen<br />
C-H-Bindung(en) in α-Stellung (analog Felkin-Anh).<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.2. Hydrierung<br />
9.2.1. von Alkinen<br />
a) Lindlar-Hydrierung<br />
(cis-selektiv)<br />
b) trans-selektiv<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.2. Hydrierung<br />
9.2.2. Heterogene <strong>Aromaten</strong>-Hydrierung<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.2. Hydrierung<br />
9.2.3. Reduktion von Benzylethern<br />
Abspaltung einer Z- (=Cbz)-<br />
Schutzgruppe in der Peptidsynthese:<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.3. Einelektronen-Reduktion mit Metallen<br />
9.3. Einelektronen-Reduktionen mit Metallen<br />
a) von Ketonen<br />
ein Test auf Wasser in<br />
Lösungsmitteln!<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.3. Einelektronen-Reduktion mit Metallen<br />
Diastereoselektive Reduktion eines Cyclohexanons mit sich auflösendem Natrium:<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.3. Einelektronen-Reduktion mit Metallen<br />
b) Pinakol-Kupplung:<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Auch z. B. mit SmI 2 .<br />
"Pinakol"<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.3. Einelektronen-Reduktion mit Metallen<br />
c) von Estern<br />
Bouveault-Blanc-Reduktion in<br />
An- (oben) und Abwesenheit<br />
(unten) von Protonen<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Protonierung<br />
Reduktion<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
9. Reduktion - 9.3. Einelektronen-Reduktion mit Metallen<br />
d) Birch-Reduktion zu 1,4-Cyclohexadienen<br />
TU BS, Lindel<br />
aus: Brückner, Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
10. <strong>Substitution</strong> an der Carboxylgruppe<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
6.1 Hydrolyse von Nitrilen zur Carbonsäure<br />
(4-Nitrophenyl)-essigsäure, Bernsteinsäure, Phenylessigsäure<br />
6.2 Veresterung von Carbonsäuren<br />
(4-Nitrophenyl)-essigsäuremethylester, Diethylsuccinat, Diethylphthalat, Ethyloctanoat,<br />
Methylbenzoat, Ethylbenzoat<br />
6.3 Darstellung von Essigsäureestern aus Acetanhydrid<br />
Acetylsalicylsäure, Essigsäureheptylester, L-Menthylacetat, Essigsäurebutylester,<br />
Essigsäurehexylester<br />
TU BS, Lindel<br />
6.4 Darstellung von Carbonsäureestern durch Alkoholyse von Säurechloriden<br />
Ethyl-3,5-dinitrobenzoat, Isopropyl-3,5-dinitrobenzoat<br />
6.5 Darstellung von Carbonsäurechloriden und Aminolyse zum Carbonsäure<strong>am</strong>id<br />
4-Chlorbenz<strong>am</strong>id, Essigsäure<strong>am</strong>id, Acetylsalicylsäure<strong>am</strong>id, Bernsteinsäure<strong>am</strong>id,<br />
Phthalsäure<strong>am</strong>id, Terephthalsäure<strong>am</strong>id<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.1. Mechanismus<br />
10.1. Mechanismus<br />
E<br />
O<br />
R X<br />
Nu H<br />
E<br />
O NuH<br />
R X<br />
-H<br />
Säurekatalyse: Je stärker basisch X, desto eher der untere Weg. Gleichgewichtsreaktion => das<br />
stabilere beider Carbonsäurederivate wird gebildet.<br />
TU BS, Lindel<br />
R X<br />
Basenkatalyse: NuH wird vorher deprotoniert. Warum lassen sich Carbonsäuren so nicht verestern<br />
(aber verseifen)?<br />
Bei reaktiven Carbonsäurederivaten (z. B. X=Cl) auch unkatalysierte Reaktion möglich.<br />
Abnehmende Reaktivität mit steigenden +M und +I-Effekten:<br />
E O Nu -E ,-X<br />
E<br />
-HX O<br />
-E<br />
R Nu<br />
R Nu<br />
X = Cl (C.-s.-chlorid) > O 2 CR (C.-s.-anhydrid) > H (Aldehyd) > R (Keton) > OR (C.-s.-ester) > OH<br />
(C.-s.) > NHR (C.-s.-Amid) > O − (Carboxylat)<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.2. Beispiele<br />
10.2. Beispiele<br />
a) Veresterung v. C.-s.<br />
Cl<br />
O<br />
OH<br />
+5EtOH<br />
0.2<br />
konz. H 2SO 4<br />
5hRückfluß<br />
Cl<br />
O<br />
OEt<br />
TU BS, Lindel<br />
+H 2O<br />
+4EtOH<br />
alternativ: Verwendung von Ionenaustauschern <strong>am</strong> Wasserabscheider (azeotrope Veresterung)<br />
b) Verseifung von Säurechloriden<br />
Benzoylchlorid + Alkohol (oder Amin) + tropfenweise 5 N Kalilauge mit pH-Überprüfung in<br />
Aceton (Schotten-Baumann-R.); Aroylchlorid + Alkohol in Pyridin: Einhorn-Variante<br />
(nukleophile Katalyse durch Pyridin, s. 10.1.3.!).<br />
c) Verseifung von Estern<br />
Reaktivitätsreihen:<br />
α) MeCO 2 R > EtCO 2 R > iPrCO 2 R > tBuCO 2 R<br />
β) RCO 2 Me > RCO 2 Et > RCO 2 iPr > RCO 2 tBu R O<br />
H<br />
tBu-Ester: Spaltung der C q -O-Bindung<br />
(vgl. Boc-S.-gr.)!<br />
O<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
OH<br />
O +<br />
OH
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.2. Beispiele<br />
d) Verseifung von β-Oxocarbonsäureestern<br />
R 1<br />
O O<br />
OR 2<br />
KOH<br />
R 1<br />
H<br />
O O<br />
O<br />
150 °C<br />
-CO2<br />
R 1 = OR: Malonsäureester Decarboxylierung<br />
e) Synthese von C.-s.-chloriden<br />
R<br />
O<br />
Cl S<br />
Cl<br />
O<br />
OH<br />
R<br />
Cl<br />
Cl<br />
O<br />
O H<br />
S O<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
R 1<br />
OH<br />
(R 1 = Alk: "Ketonspaltung")<br />
O<br />
R<br />
-HCl Cl<br />
O<br />
S<br />
O<br />
-SO2 - auch mit 1 PCl 5 (-> POCl 3 + HCl) und 1/3 PCl 3 (-> H 3 PO 3 ).<br />
- C.-s.-anhydride aus C.-s.-chloriden<br />
R 1<br />
Keto-Enol-Tautomerie<br />
O<br />
Cl<br />
O
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.3. Katalysierte Varianten<br />
f) Hydrolyse von Nitrilen<br />
über das Iso<strong>am</strong>id zum Amid.<br />
Zwischenfrage: Was passiert bei der Umsetzung von Nitrilen mit LiAlH 4 ?<br />
10.3. Katalysierte Varianten:<br />
a) 4-Dimethyl<strong>am</strong>inopyridin<br />
("Steglichs<br />
Reagenz",<br />
10000-fach<br />
schneller als<br />
Pyridin)<br />
TU BS, Lindel<br />
DMAP: W. Steglich, G. Höfle, Angew. Chem. 1969, 1001; Angew. Chem. 2003, 4975.<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.3. Katalysierte Varianten<br />
TU BS, Lindel<br />
Zyklus der DMAPkatalysierten<br />
Alkohol-<br />
Veresterung<br />
aus:<br />
Angew. Chem. 2004, 5552.<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
10. <strong>Substitution</strong> an der Carboxylgruppe - 10.3. Katalysierte Varianten<br />
b) Aktivierung durch Carbodiimide<br />
HO<br />
N<br />
O<br />
R<br />
N N O<br />
NHFmoc<br />
O<br />
R<br />
N<br />
C N<br />
DCC: Dicyclohexylcarbodiimid<br />
NHFmoc<br />
R' NH 2<br />
-HOBt<br />
OH<br />
TU BS, Lindel<br />
N<br />
N<br />
N<br />
Katalysator<br />
schneller<br />
Festphasensynthese von Peptiden!<br />
Cy<br />
HN<br />
Cy<br />
ein O-Acylisoharnstoff<br />
R'<br />
N<br />
H<br />
N<br />
O<br />
O<br />
O<br />
R<br />
R' NH 2<br />
R<br />
NHFmoc<br />
O<br />
-<br />
CyHN NHCy<br />
NHFmoc<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
<strong>7.</strong>1 Darstellung von Ethylenacetalen (Dioxolanen)<br />
Cyclopentanon-ethylenacetal, Acetessigsäureethylester-ethylenacetal, Ethylmethylketon-ethylenacetal<br />
<strong>7.</strong>2 Darstellung von Schiffschen Basen<br />
Benzylidenmethyl<strong>am</strong>in<br />
<strong>7.</strong>3 Darstellung von En<strong>am</strong>inen<br />
1-Pyrrolidino-cyclopent-1-en, 1-Morpholinocyclopent-1-en, 1-Morpholino-cyclohex-1-en, α-Methyl<strong>am</strong>inocrotonsäureethylester,<br />
α-Dimethyl<strong>am</strong>ino-crotonsäureethylester, α-Benzyl<strong>am</strong>ino-crotonsäureethylester<br />
<strong>7.</strong>4 Acyloinkondensation von aromatischen Aldehyden<br />
Benzoin, 4,4'-Dimethylbenzoin, 4-Anisoin<br />
<strong>7.</strong>5 Wittig-Reaktion<br />
1,4-Diphenyl-1,3-butadien, α-Phenylstyren<br />
<strong>7.</strong>6 Wittig-Horner-Emmons-Reaktion<br />
TU BS, Lindel<br />
1,4-Diphenyl-1,3-butadien, Stilben, 4-Methylstilben, 4-Chlorstilben, 4-Methoxystilben<br />
<strong>7.</strong>7 Alkohole durch Cannizzaro-Reaktion<br />
Benzylalkohol<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
9.1 Aldol-Reaktion<br />
Benzalaceton, 3-Hydroxy-2-methylpentanal, 2-Ethyl-3-hydroxyhexanal, 4-Methoxybenzylidenaceton,<br />
Dibenzylidenaceton<br />
9.2 Variante nach Cope<br />
Butyliden-malonsäurediethylester, Isobutyliden-malonsäurediethylester, Benzyliden-malonsäurediethylester<br />
9.3 Variante nach Knoevenagel und Doebner: Zimtsäure, 4-Methoxyzimtsäure<br />
9.4 Nitroaldol-Reaktion: 3,4-Dimethoxy-ω-nitrostyrol<br />
9.5 Claisen-Kondensation: Acetessigsäureethylester<br />
9.6 Orthoessigsäurekondensation: α-Ethoxymethylen-acetessigsäureethylester<br />
9.7 Acylierung von β-Dicarbonylverbindungen<br />
TU BS, Lindel<br />
2-Benzoyl-3-oxo-butansäureethylester, Benzoylmalonsäurediethylester<br />
9.8 Alkylierung von β-Dicarbonylverbindungen<br />
Propylmalonsäurediethylester, Isobutylmalonsäurediethylester, Butylmalonsäurediethylester, 2-Acetylhexansäureethylester,<br />
2-Acetyl-4-methyl-pentansäureethylester<br />
9.9 Michael-Addition: 2-Oxo-6-phenylcyclohex-3-en-1-carbonsäureethylester<br />
9.10 Mannich-Reaktion: 1-Phenyl-3-piperidino-propan-1-on, 3-Dimethyl<strong>am</strong>ino-1-phenyl-propan-1-on, 3-<br />
Dimethyl<strong>am</strong>ino-1-(4-mehoxyphenyl)-propan-1-on, 3-Dimethyl<strong>am</strong>ino-2-methyl-1-phenyl-propan-1-on, 1-<br />
Phenyl-5-piperidino-pent-1-en-3-on<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.1. O-Nukleophile<br />
Reduktion zum Alkohol s. Kap. 9.<br />
11.1. Addition von O-Nukleophilen<br />
R 1<br />
O<br />
R 2 O<br />
R R 1<br />
OR 3<br />
R<br />
R=H:<br />
R 2 =R 3 =H: geminales Diol<br />
R 2 =H, R 3 ungleich H: Halbacetal<br />
R 2 ,R 3 ungleich H: Vollacetal<br />
Carbonylform gegenüber den Diolen bevorzugt, außer z. B. bei Ninhydrin:<br />
Was ist ein 1,3-Dioxolan, was ein 1,3-Dioxan? Darstellung?<br />
O<br />
Erinnern Sie sich der Halbacetalformen von Glucose und der Hemiketalformen von Fructose!<br />
TU BS, Lindel<br />
Struktur von Diethylcarbonat? Was ist ein Orthoester? Was ist ein Carb<strong>am</strong>at?<br />
RungleichH:<br />
R 2 =R 3 =H: geminales Diol<br />
R 2 =H, R 3 ungleich H: Hemiketal<br />
R 2 , R 3 ungleich H: Ketal<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
OH<br />
OH
11. Addition an die Carbonylgruppe - 11.2. N-Nukleophile<br />
11.2. N-Nukleophile<br />
Imin-En<strong>am</strong>in-Tautomerie<br />
Ausgehend von Aldehyden/Ketonen und sekundären Aminen nur En<strong>am</strong>ine möglich.<br />
En<strong>am</strong>in-Tautomer auch bevorzugt nach der Umsetzung β-Ketocarbonylverbindungen.<br />
Was ist ein Harnstoff: Darstellung ausgehend von Isocyanaten, Phosgen. Was ist ein Isoharnstoff?<br />
Anwendung von En<strong>am</strong>inen als C-Nukleophile:<br />
Cl<br />
R O<br />
+<br />
O<br />
N<br />
Cl<br />
R<br />
TU BS, Lindel<br />
O<br />
O N<br />
H 3O +<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
R<br />
O<br />
O<br />
+<br />
O<br />
N<br />
H H
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
11.3. C-Nukleophile<br />
a) Knoevenagel-Kondensation von Malonsäureestern und Aldehyden<br />
b) Claisen-Kondensation<br />
c) Aldoladdition und -kondensation<br />
d) Mannich-Reaktion<br />
Enol-Nukleophil, z. B. Acetondicarbonsäure, + CH 2 NMe 2 +<br />
auch: Synthese von Gr<strong>am</strong>in ausgehend von Indol.<br />
TU BS, Lindel<br />
e) Acyloinkondensation: Cyanid-katalysiert ("Organokatalyse"), Umpolungsreaktion<br />
O<br />
Ar H<br />
CN O CN HO CN Ar H<br />
Ar H<br />
Ar<br />
O<br />
O<br />
O<br />
O<br />
O<br />
HO CN<br />
Ar<br />
Na, EtOH<br />
40°C,12h,50%<br />
Knoevenagel-Michael-Kombination<br />
(Mechanismus?)<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
Ar<br />
-CN<br />
O<br />
O<br />
Ar<br />
O<br />
O<br />
OH<br />
Ar
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
f) Wittig-Reaktion<br />
Stereoselektivität der Wittig-Reaktion (I)<br />
"Z"<br />
TU BS, Lindel<br />
"E"<br />
Triebkraft: Bildung von Ph 3 PO<br />
Synthese der Phosphonium-Ylide?<br />
Stabilisiertes Phosphoran: Konjugation der P=C-Bindung zu einer weiteren Doppelbindung (meist<br />
C=C, C=O); nicht stab. Ylid: sonst.<br />
Varianten zur Stereoselektivität:<br />
E-Alken Z-Alken<br />
stab. Phosphoran<br />
Wittig-Horner-<br />
Emmons, Wittig<br />
Still-Gennari<br />
nicht stab. Ylid Schlosser-Wittig Wittig<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
Mechanismus der Wittig-Reaktion<br />
TU BS, Lindel<br />
aus: Brückner,<br />
Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
Diastereomere ÜZ der Oxaphosphetan-<br />
Bildung ausgehend von<br />
Triphenylphosphonium-Yliden,<br />
führend zu Z- bzw. E-Alkenen.<br />
Betaine spielen keine Rolle.<br />
Calculated potential energy surface (kcal/mol)<br />
for reaction 2, Ph 3 PCHMe + MeCHO, at the<br />
B3LYP/6-31G*(THF)//B3LYP/6-31G* level<br />
of theory.<br />
TU BS, Lindel<br />
aus: JACS 2006, 2394<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
Stereoselektivität der Wittig-Reaktion (II)<br />
Schlosser-Variante zur Synthese<br />
von (E)-Alkenen ausgehend von<br />
nicht stabilisierten Yliden<br />
Still-Gennari-Variante der<br />
Horner-Wadsworth-Emmons-<br />
Reaktion zur Synthese von (Z)-<br />
Alkenen ausgehend von<br />
stabilisierten Phosphoranen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
Wittig-Reaktion: Beispiele<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
Horner-Wadsworth-Emmons-Reaktion<br />
Zur Darstellung des Diethylphosphonats: Arbusov-Reaktion<br />
O<br />
OEt Br<br />
P<br />
EtO OEt<br />
OCH3 EtO<br />
P<br />
EtO<br />
O O<br />
Br<br />
O<br />
OCH 3<br />
TU BS, Lindel<br />
OCH 3<br />
H<br />
O<br />
-Li + (EtO) 2 PO 4<br />
-EtBr<br />
EtO<br />
P<br />
EtO<br />
O<br />
EtO<br />
P<br />
EtO<br />
O<br />
OCH 3<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
LDA, -HNiPr 2<br />
O<br />
Li +<br />
OCH 3
11. Addition an die Carbonylgruppe - 11.3. C-Nukleophile<br />
HWE-Olefinierung<br />
TU BS, Lindel<br />
Still-Gennari-Olefinierung<br />
aus: Brückner,<br />
Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.4. Metallorganyle<br />
11.4. Metallorganyle<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
8.1 Addition von Grignard-Verbindungen an Aldehyde, Ketone und Ester<br />
2-Methylpentan-3-ol, 3-Methyl-1-phenylbutan-2-ol, 2-Methylbutan-2-ol, 2,3-Dimethylbutan-2-ol,<br />
3-Ethylpentan-3-ol, 3-Methylpentan-3-ol, Triphenylmethanol<br />
11.4.1. Alkyllithium-Verbindungen<br />
TU BS, Lindel<br />
bei α,β-unges. Carbonylverb: bevorzugt 1,2-Addition direkt an die C=O-Bindung.<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.4. Metallorganyle<br />
Bildungsmechanismus einer Grignard-<br />
Verbindung (Oxidationsstufe des Kohlenstoffs<br />
in MeMgI?):<br />
Rieke-Mg: durch Reduktion einer Suspension von<br />
MgCl 2 in THF mit K:<br />
Heterogene Reduktion von Alkylhalogeniden<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.4. Metallorganyle<br />
11.4.2. Grignard-<br />
Reagenzien<br />
1,2-Addition<br />
TU BS, Lindel<br />
aus: Brückner,<br />
Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.4. Metallorganyle<br />
TU BS, Lindel<br />
aus: Brückner,<br />
Reaktionsmechanismen<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
11. Addition an die Carbonylgruppe - 11.4. Metallorganyle<br />
11.4.3. Cuprate<br />
1,4-Addition (best choice)<br />
aus: Brückner, Reaktionsmechanismen<br />
TU BS, Lindel<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
12. Reaktionen von Amiden<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
10.1 Hofmann-Abbau von Carbonsäure<strong>am</strong>iden<br />
Benzyl<strong>am</strong>in, Anthranilsäure<br />
10.2 N-Alkylformanilide über Chapman-Umlagerung<br />
N-Ethyl-3-methylformanilid<br />
10.3 Hydrolyse von N-Alkylformaniliden<br />
N-Ethyl-3-toluidin<br />
10.4 Darstellung von Harnstoffderivaten<br />
N-(4-Ethoxyphenyl)-harnstoff<br />
10.5 Diazotierung und anschließende Sandmeyer-Reaktion<br />
TU BS, Lindel<br />
2-Iodbenzoesäure, 2-Chlortoluen, 3-Bromtoluen, 2-Chlornitrobenzol, 3-Chlornitrobenzol, 2-Bromnitrobenzol,<br />
3-Bromnitrobenzol<br />
10.6 Darstellung von p-Toluensulfonsäurealkylestern<br />
Methyltosylat, Ethyltosylat, Propyltosylat<br />
10.7 Darstellung von Sulfonsäure<strong>am</strong>iden<br />
Benzolsulfon<strong>am</strong>id- oder Toluensulfon<strong>am</strong>id von Benzyl<strong>am</strong>in, Benzolsulfon<strong>am</strong>id- oder Toluensulfon<strong>am</strong>id von<br />
Anilin, Benzolsulfon<strong>am</strong>id- oder Toluensulfon<strong>am</strong>id von N-Methylanilin, Benzolsulfon<strong>am</strong>id- oder<br />
Toluensulfon<strong>am</strong>id von 4-Chloranilin, Benzolsulfon<strong>am</strong>id- oder Toluensulfon<strong>am</strong>id von 4-Bromanilin<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
12. Reaktionen von Amiden<br />
12.1. Umlagerungen<br />
Hofmann-Abbau<br />
Lossen-Abbau<br />
Curtius-Abbau<br />
Beckmann-Uml.<br />
Chapman-Uml.<br />
Iminoether zum Alkyl-<br />
/Aryl<strong>am</strong>id<br />
O<br />
R NH 2<br />
O<br />
R N H<br />
O<br />
R N<br />
N OH<br />
OH<br />
N N<br />
HOBr<br />
NaOH α-Eliminierung von HBr<br />
∆<br />
H 2SO 4, ∆<br />
O<br />
R N<br />
TU BS, Lindel<br />
[1,2]-Umlagerung<br />
O<br />
R N C O<br />
Isocyanat<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
NH<br />
Wanderung der<br />
Alkylgruppe vom<br />
Carbonyl-C zum N.<br />
Nylon-Vorstufe<br />
J. Chem. Soc. Perkin Trans. 2, 1987, 205
13. Radikalische Reaktionen<br />
Radikalische Defunktionalisierung<br />
a) Radikalische Dehalogenierung<br />
O<br />
O<br />
I<br />
Bu 3 SnH<br />
kat. AIBN<br />
∆ oder hν<br />
O<br />
O<br />
oder<br />
Aber: Alkohole lassen sich so nicht dehydroxylieren!<br />
b) Lösung: Barton-McCombie-Desoxygenierung<br />
Bsp.:<br />
HO<br />
H<br />
H H<br />
Ein wichtiges Molekül. Welches?<br />
TU BS, Lindel<br />
1) NaH; CS 2 ;MeI<br />
2) Bu 3SnH, kat. AIBN<br />
Br<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
(TMS) 3SiH<br />
kat. AIBN<br />
∆ oder hν<br />
H<br />
H H<br />
O
13. Radikalische Reaktionen<br />
Radikalische Defunktionalisierung (<strong>Substitution</strong> von X· durch H· („H-Punkt“))<br />
allgemein:<br />
Radikalstarter<br />
R X + L3M H L3M X + R H<br />
funktionalisiert defunktionalisiert<br />
Mechanismus:<br />
R X L3M + R H<br />
TU BS, Lindel<br />
St H<br />
Propagation Initiation<br />
L3M X + R L3M H St<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
13. Radikalische Reaktionen<br />
Mech. d. Barton-McCombie-Desoxygenierung<br />
Vorab: Bildung des Xanthogenats<br />
Desoxygenierung:<br />
S<br />
S<br />
S<br />
O<br />
R<br />
S<br />
S SnBu 3<br />
O<br />
thiophil<br />
S SnBu 3<br />
+<br />
O<br />
Bu 3Sn<br />
R<br />
+<br />
S<br />
TU BS, Lindel<br />
S<br />
R H<br />
Bu 3Sn H<br />
O<br />
Propagation Initiation<br />
R<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
N<br />
N<br />
H
13. Radikalische Reaktionen<br />
Mech. d. Wohl-Ziegler-Bromierung<br />
N<br />
O<br />
O<br />
N<br />
CN<br />
Initiation<br />
TU BS, Lindel<br />
reversibel !<br />
Br<br />
Propagation<br />
Br H +<br />
Br Br<br />
O<br />
O<br />
N<br />
Br<br />
Propagation<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
+<br />
ionischer Schritt<br />
Br<br />
Weiterreaktion zu 1,2-Dibromhexan nur bei<br />
großer Br 2 -Konz., die aber nicht vorliegt.<br />
Br<br />
+<br />
O<br />
O<br />
N<br />
H
Z. Anhang - Z.1. Naturstoff-Isolierung<br />
Versuche im Praktikum (Nummerierung wie dort):<br />
12. Naturstoffisolierung<br />
- Furfural (aus Kleie oder Leins<strong>am</strong>en)<br />
- Trimyristin (aus Muskatnuß)<br />
- Piperin (schwarzem Pfeffer)<br />
- Eugenol (aus Gewürznelken)<br />
- Hesperidin (aus Orangenschalen)<br />
- Sinalbin (aus weißem Senf)<br />
O<br />
O<br />
Welcher<br />
Naturstoff ist<br />
welcher?<br />
O<br />
O<br />
O O<br />
O O<br />
N<br />
HO<br />
O<br />
TU BS, Lindel<br />
HO<br />
HO<br />
HO<br />
O<br />
OH<br />
OH<br />
O<br />
O<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong><br />
O<br />
O<br />
O<br />
OH O<br />
HO<br />
HO<br />
MeO<br />
HO<br />
OH<br />
OH<br />
OH<br />
O<br />
OMe<br />
MeO<br />
HO<br />
OMe<br />
S N O SO 3<br />
O<br />
O<br />
OH<br />
NMe 3
Z. Anhang - Z.1. Naturstoff-Isolierung<br />
S-(+)-Carvon,<br />
Kümmelgeruch,<br />
aus Kümmelöl (85 %),<br />
Dillöl (60 %).<br />
O O<br />
Wichtigster Nebenbestandteil in Kümmelöl: R-(+)-Limonen.<br />
R-(+)-Limonen,<br />
Orangengeruch,<br />
aus Öl von Citrusfrüchten,<br />
industriell wichtigstes<br />
Monoterpen.<br />
Sdp. 230 °C<br />
TU BS, Lindel<br />
Sdp. 175 °C<br />
Racemat z. B. aus Zanthoxylum piperitum<br />
R-(–)-Carvon,<br />
Krauseminzegeruch,<br />
aus Krauseminzeöl (70 %).<br />
S-(–)-Limonen,<br />
Terpentingeruch,<br />
aus Tannenöl.<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>
Z. Anhang - Z.2. Aminosäuren<br />
20 proteinogene L-α-Aminosäuren (+ Selenocystein):<br />
C α<br />
H<br />
Glycin<br />
(G)<br />
HN<br />
C α<br />
H 3C<br />
Alanin<br />
(A)<br />
H 2N NH 2<br />
C α<br />
C α<br />
HO<br />
Phenylalanin (F)<br />
H 2N<br />
C α C α C α<br />
Valin<br />
(V)<br />
C α<br />
Arginin (R) Lysin (K)<br />
C α<br />
Tyrosin (Y)<br />
Isoleucin<br />
(I)<br />
Leucin (L)<br />
H 2N<br />
O<br />
HN<br />
C α<br />
TU BS, Lindel<br />
C α<br />
HN<br />
H2N α CO2H H<br />
N<br />
C α<br />
O NH 2<br />
N<br />
H<br />
Asparagin (N) Glut<strong>am</strong>in (Q)<br />
Tryptophan (W)<br />
R<br />
CO 2H<br />
C α<br />
Histidin (H)<br />
HO<br />
HO<br />
O<br />
HS<br />
C α<br />
C α<br />
Asparaginsäure<br />
(D)<br />
C α<br />
Cystein<br />
(C)<br />
HO<br />
C α<br />
Prolin (P) Serin (S) Threonin (T)<br />
C α<br />
O OH<br />
Glut<strong>am</strong>insäure<br />
(E)<br />
C α<br />
H3CS Methionin<br />
(M)<br />
Prof. Dr. Th. Lindel, TU Braunschweig: Seminar zum Grundpraktikum <strong>Organische</strong> <strong>Chemie</strong>