Dissertation Martin Krause.pdf - KLUEDO - Universität Kaiserslautern
Dissertation Martin Krause.pdf - KLUEDO - Universität Kaiserslautern
Dissertation Martin Krause.pdf - KLUEDO - Universität Kaiserslautern
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
6.5 ITC-Messungen mit Verbindungen 9a-f<br />
Es wurden 0.4 mM Lösungen der Bis(kronenether)-Derivate in den jeweiligen<br />
Lösungsmittelgemischen angesetzt und die auf 25 °C temperierte Messzelle damit befüllt. In diese<br />
Lösung wurde eine 8 mM Lösung Kaliumbromid in demselben Lösungsmittelgemisch in 30<br />
Injektionen zutitriert. Die erste Injektion betrug 2 µL und wurde bei der Auswertung ignoriert. Die<br />
folgenden 29 Injektionen betrugen 8 µL. Die Zugabegeschwindigkeit betrug 0.5 µL/s, der Abstand<br />
zwischen zwei Zugaben 180 s.<br />
Die Auswertung geschah mit dem Programm Data Analysis Origin V7.0, wobei das<br />
Bindungsmodell “one set of sites“ für die Analyse von 1:1 Komplexen zugrunde gelegt wurde. Die so<br />
für die Verbindungen 9a-f erhaltenen Ergebnisse sind in den nachfolgenden Tabellen<br />
zusammengefasst.<br />
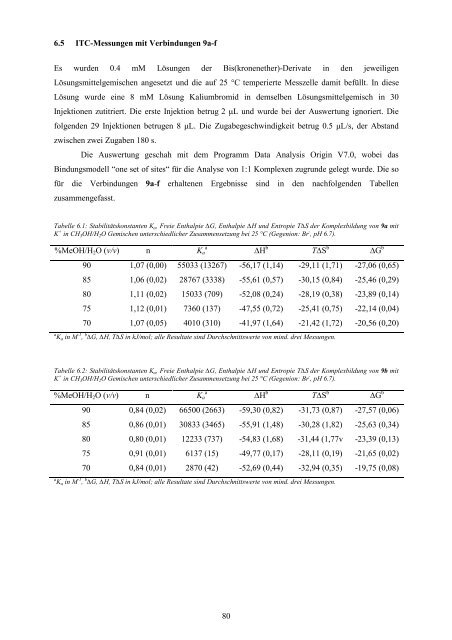
Tabelle 6.1: Stabilitätskonstanten K a, Freie Enthalpie ∆G, Enthalpie ∆H und Entropie T∆S der Komplexbildung von 9a mit<br />
K + in CH 3OH/H 2O Gemischen unterschiedlicher Zusammensetzung bei 25 °C (Gegenion: Br - , pH 6.7).<br />
%MeOH/H2O (v/v) n Ka a ∆H b T∆S b ∆G b<br />
90 1,07 (0,00) 55033 (13267) -56,17 (1,14) -29,11 (1,71) -27,06 (0,65)<br />
85 1,06 (0,02) 28767 (3338) -55,61 (0,57) -30,15 (0,84) -25,46 (0,29)<br />
80 1,11 (0,02) 15033 (709) -52,08 (0,24) -28,19 (0,38) -23,89 (0,14)<br />
75 1,12 (0,01) 7360 (137) -47,55 (0,72) -25,41 (0,75) -22,14 (0,04)<br />
70 1,07 (0,05) 4010 (310) -41,97 (1,64) -21,42 (1,72) -20,56 (0,20)<br />
a Ka in M -1 , b ∆G, ∆H, T∆S in kJ/mol; alle Resultate sind Durchschnittswerte von mind. drei Messungen.<br />
Tabelle 6.2: Stabilitätskonstanten K a, Freie Enthalpie ∆G, Enthalpie ∆H und Entropie T∆S der Komplexbildung von 9b mit<br />
K + in CH 3OH/H 2O Gemischen unterschiedlicher Zusammensetzung bei 25 °C (Gegenion: Br - , pH 6.7).<br />
%MeOH/H2O (v/v) n Ka a ∆H b T∆S b ∆G b<br />
90 0,84 (0,02) 66500 (2663) -59,30 (0,82) -31,73 (0,87) -27,57 (0,06)<br />
85 0,86 (0,01) 30833 (3465) -55,91 (1,48) -30,28 (1,82) -25,63 (0,34)<br />
80 0,80 (0,01) 12233 (737) -54,83 (1,68) -31,44 (1,77v -23,39 (0,13)<br />
75 0,91 (0,01) 6137 (15) -49,77 (0,17) -28,11 (0,19) -21,65 (0,02)<br />
70 0,84 (0,01) 2870 (42) -52,69 (0,44) -32,94 (0,35) -19,75 (0,08)<br />
a Ka in M -1 , b ∆G, ∆H, T∆S in kJ/mol; alle Resultate sind Durchschnittswerte von mind. drei Messungen.<br />
80