8-Stoffwechsel I_Gly
8-Stoffwechsel I_Gly
8-Stoffwechsel I_Gly
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
1. Einleitung: Die Chemie des Lebens<br />
2. Kohlenhydrate<br />
3. Lipide und Membranen<br />
4. Nukleinsäuren<br />
5. Aminosäuren und Proteine<br />
6. Enzyme und Katalyse<br />
7. Vitamine & Kofaktoren<br />
Inhaltsverzeichnis - Kapitel<br />
8. <strong>Stoffwechsel</strong> I: Kohlenhydratstoffwechsel<br />
9. <strong>Stoffwechsel</strong> II: Citratcyclus & oxidative Phosphorylierung<br />
10. <strong>Stoffwechsel</strong> III: β-Oxidation & Aminosäureabbau<br />
11. <strong>Stoffwechsel</strong>physiologie & Ernährungsbiochemie<br />
1<br />
2
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
Überblick über metabolische Prozesse<br />
Die Prinzipien des <strong>Stoffwechsel</strong>s sind in allen Organismen gleich<br />
( Evolution / Thermodynamische Gesetze ):<br />
-> Reaktionstypen – Regulation - speicherbare Energie<br />
� Organismen unterscheiden sich jedoch in ihrer trophischen Strategie<br />
(autotroph, heterotroph, etc.).<br />
- Autotrophe Organismen (fotosynthetisierende Organismen):<br />
bauen das anorganische Material durch Fotosynthese unter Produktion von O 2 in<br />
organische Substanz um, die den heterotrophen Organismen als Nahrung dienen<br />
- Heterotrophe Organismen:<br />
bauen die organische Substanz ab um aus ihr Energie zu gewinnen<br />
- unter sauerstoffarmen Bedingungen: anaerober Abbau oder Gärung<br />
- unter sauerstoffreichen Bedingungen: aerober Abbau oder Atmung<br />
Überblick über metabolische Prozesse<br />
� Anaerober Abbau von organischen Substanzen: 2 Wege<br />
1. GÄRUNG: O 2 fehlt; organisches Substrat dient als H-Akzeptor<br />
(z.B. Hefen)<br />
2. ANAEROBE ATMUNG: NO 3 oder SO 4 dienen als H-Akzeptoren<br />
Endprodukte sind auch v.a. CO 2 und H 2 O.<br />
3<br />
4
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong>wege<br />
Eine Abfolge spezifischer Reaktionen, die zu<br />
einem definierten Produkt führen wird als<br />
STOFFWECHSELWEG bezeichnet.<br />
Der Abbau verschiedener Substanzklassen<br />
führt zu einem zentralen <strong>Stoffwechsel</strong>produkt<br />
(Acetyl-CoA), das dann weiter abgebaut<br />
(oxidiert) wird. �<br />
Dabei werden reduzierte Coenzyme generiert<br />
(FADH 2 und NADPH), die im weiteren Verlauf<br />
durch Sauerstoff (re-)oxidert werden.<br />
(oxidative Phosphorylierung).<br />
Bei diesem Prozess entsteht ATP<br />
(Adenosintriphosphat), das universell als<br />
Energieträger eingesetzt werden kann.<br />
Katabole und anabole <strong>Stoffwechsel</strong>wege<br />
Katabolismus<br />
Reaktion des Körpers auf Belastung<br />
Abbau von <strong>Stoffwechsel</strong>produkten zu einfachen Molekülen<br />
Energiegewinnung für anabole Reaktionen (exergonisch)<br />
Kurzzeitiger Energiespeicher und<br />
Energieüberträger = ATP<br />
Katabolismus<br />
Katabole und anabole Reaktionen<br />
hängen voneinander ab, aber laufen<br />
in der Zelle nicht gleichzeitig ab.<br />
Anabolismus<br />
Aufbau von körpereigenen Bestandteilen<br />
Energie wird verbraucht (endergonisch)<br />
Energie stammt aus katabolen Reaktionen<br />
5<br />
Anabolismus<br />
6
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
Katabole und anabole <strong>Stoffwechsel</strong>wege<br />
Produkte des katabolen <strong>Stoffwechsel</strong>s werden in exergonischen Reaktionen gebildet und<br />
daher muss für die Umkehrung des Prozesses (anabole <strong>Stoffwechsel</strong>wege) ein<br />
energieliefernder Schritt eingeschaltet werden!<br />
� Daher unterscheiden sich katabole und anabole <strong>Stoffwechsel</strong>wege in mindestens<br />
einem Schritt!<br />
� Dies ist von Vorteil, da die Prozesse damit unabhängig voneinander reguliert werden<br />
können:<br />
<strong>Stoffwechsel</strong>weg A<br />
<strong>Stoffwechsel</strong>weg XY<br />
Katabole <strong>Stoffwechsel</strong>wege: E-Gewinnung<br />
Kataboler <strong>Stoffwechsel</strong>:<br />
7<br />
8
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
Allosterische Regulation:<br />
Regulation von <strong>Stoffwechsel</strong>wegen<br />
• Ein Endprodukt hemmt eine frühe Reaktion im <strong>Stoffwechsel</strong>weg (negative Rückkopplung)<br />
• Diese sogenannten Effektoren binden an allosterische Taschen (≠ aktives Zentrum) am<br />
Enzym<br />
Produkthemmung/negative Rückkopplung<br />
Allosterie: Veränderung der Konformation unter Beeinflussung des<br />
aktiven Zentrums / Bindungszentrums<br />
Energiereiche Verbindungen<br />
Die vollständige Oxidation von Kohlenhydraten<br />
und Fetten setzt Energie frei, die in Form von<br />
sog. „Energiereichen Verbindungen“<br />
gespeichert wird (vor allem ATP).<br />
Diese Verbindungen können<br />
dann dazu verwendet werden<br />
endergonische Reaktionen<br />
(„uphill“ -> Reaktion braucht<br />
Energie) anzutreiben.<br />
9<br />
10
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
Warum ist ATP ein energiereiches Molekül?<br />
• Im Anhydrid konkurrieren die beiden Sauerstoffatome um die Elektronen des<br />
Brückensauerstoffatoms.<br />
• Außerdem kommt es zur elektrostatische Abstoßung der negativen Ladungen im<br />
Anhydrid.<br />
• Die hydratisierten Produkte sind besser solvatisiert und daher energieärmer.<br />
Acylphosphate<br />
Spaltung einer Anhydrid-<br />
Bindung setzt > 30 kJ/<br />
mol an Energie frei!<br />
• In Acylphosphaten besteht eine noch größere Konkurrenz um die Elektronen des<br />
Brückensauerstoffs.<br />
• Daher besitzen diese Verbindungen ein höheres Phosphatgruppenübertragungspotential<br />
als ATP.<br />
Acylphosphate sind gemischte<br />
Phosphorsäure/Carbonsäure Anhydride<br />
11<br />
12
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
Verbindungen mit hohem<br />
Potential können die<br />
Phosphatgruppe auf<br />
Verbindungen mit<br />
niedrigem Potential<br />
übertragen.<br />
ATP steht dabei im<br />
Zentrum der<br />
Übertragungswege.<br />
Thioester<br />
Auch die Hydrolyse einer Thioesterbindung ist<br />
exergonisch<br />
und kann für die Synthese von ATP verwendet<br />
werden!<br />
Phosphatgruppenübertragungspotential<br />
13<br />
14
<strong>Stoffwechsel</strong> 1<br />
<strong>Stoffwechsel</strong> 1<br />
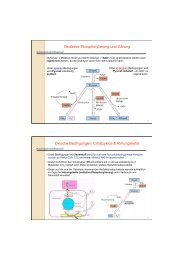
Kopplung von Reaktionen<br />
Wie kann eine exergonische Reaktion eine endergonische antreiben?<br />
Gibbs-Energie<br />
Chemische Reaktionen folgen den Gesetzen<br />
der Thermodynamik. Dabei ist die<br />
Veränderung der Gibbs-Energie ΔG das<br />
entscheidende Kriterium:<br />
ΔG < 0: exergone Reaktion<br />
läuft spontan ab<br />
ΔG = 0: Gleichgewicht<br />
keine Reaktion<br />
ΔG > 0: endergone Reaktion<br />
braucht Energie-Zufuhr<br />
+<br />
-<br />
Endergone Reaktion<br />
Exergone Reaktion<br />
Beispiele für gekoppelte Reaktionen<br />
15<br />
16
<strong>Stoffwechsel</strong> 1<br />
Kohlenhydratstoffwechsel<br />
Bildung von ATP im <strong>Stoffwechsel</strong><br />
ATP wird permanent im menschlichen Körper umgesetzt (ca. 1,5 kg/h !)<br />
und muss daher ständig generiert werden.<br />
Es gibt drei prinzipielle Wege ATP herzustellen:<br />
Abbau von Kohlenhydraten - <strong>Gly</strong>colyse<br />
Die <strong>Gly</strong>kolyse (gr.: glykys = süß; lysis =<br />
auflösen) ist der schrittweise Abbau von C 6 -<br />
Zuckern wie der Glucose zu 2 C 3 -Molekülen<br />
(Pyruvat) und besteht aus 10 enzymatischen<br />
Einzelschritten.<br />
Sie ist ein zentraler, katabolischer Prozess zur<br />
Energiegewinnung in den Zellen der meisten<br />
Lebewesen. Sie ist der einzige metabolische<br />
Weg, den fast alle Organismen gemeinsam<br />
haben, was auf eine sehr frühe Entstehung<br />
hinweist.<br />
Insgesamt werden 2 Moleküle ATP pro<br />
Molekül Glucose hergestellt. Weiters entstehen<br />
2 Moleküle NADH.<br />
Außerdem kann das Endprodukt Pyruvat zur<br />
weiteren Oxidation, d.h. Energieerzeugung<br />
verwendet werden.<br />
17<br />
18
Kohlenhydratstoffwechsel<br />
<strong>Gly</strong>colyse - Fakten<br />
Die <strong>Gly</strong>kolyse findet im Cytoplasma aller (differenzierten) Zelltypen statt<br />
Die <strong>Gly</strong>kolyse liefert Energie und bereitet Glucose für den oxidativen Abbau vor<br />
Sie liefert auch Vorläufer für die Biosynthese anderer Verbindungen:<br />
• Pyruvat: Fettsäuresynthese;<br />
Aminosäuren-Synthese (Alanin, Valin, Leucin)<br />
• Dihydroxyacetonphosphat (DHAP): Lipid-Synthese<br />
• Phosphoenolpyruvat (PEP): Biosynthese aromatischer Aminosäuren<br />
(Phenylalanin, Tryptophan, Tyrosin)<br />
• 3-Phosphoglycerat (3PG): Biosynthese von L-Serin<br />
Bei der <strong>Gly</strong>kolyse wird ATP 100x schneller bereitgestellt als über die vollständige<br />
oxidative Phosphorylierung in der Atmungskette.<br />
Manche spezialisierte Zellen beziehen ihre Energie ausschließlich aus der <strong>Gly</strong>kolyse:<br />
Gehirn, Nierenmark, Erythrozyten, Spermien, proliferierende Tumorzellen<br />
In der <strong>Gly</strong>kolyse werden neben ATP auch die Reduktionsäquivalente NADH erzeugt -><br />
werden in der Atmungskette für weiteren ATP-Gewinn reoxidiert, oder zum Zweck der<br />
NAD + -Regeneration als Reduktionsmittel für Synthese anderer Moleküle verwendet.<br />
Kohlenhydratstoffwechsel<br />
<strong>Gly</strong>colyse – auch ohne Sauerstoff<br />
Die <strong>Gly</strong>kolyse läuft auch unter sauerstoffarmen/freien Bedingungen ab:<br />
• Mikroorganismen können so in einem anoxischen Milieu Energie gewinnen<br />
• bei Wirbeltieren: bei starker Muskelbeanspruchung muss die Zelle Energie kurzfristig<br />
ausschließlich aus der <strong>Gly</strong>kolyse beziehen, da mehr O 2 verbraucht wird als vorhanden<br />
ist -> Glucose schnell durch <strong>Gly</strong>kolyse und Milchsäuregärung zu Lactat umgesetzt<br />
• Pflanzen betreiben die <strong>Gly</strong>kolyse auch zusätzlich in den Plastiden. Dadurch kann der<br />
<strong>Stoffwechsel</strong> bei Licht- oder O 2 -Armut aufrechterhalten werden.<br />
19<br />
20
Kohlenhydratstoffwechsel<br />
1<br />
3<br />
Kohlenhydratstoffwechsel<br />
<strong>Gly</strong>colyse - Reaktionen und Enzyme<br />
5<br />
2<br />
4<br />
6<br />
10<br />
<strong>Gly</strong>colyse – 2 PHASEN<br />
Die <strong>Gly</strong>colyse kann in zwei Abschnitte unterteilt werden:<br />
1. INVESTMENT-Phase: -> Energie investiert<br />
Im ersten Abschnitt wird Glucose 2x phosphoryliert und schlussendlich in 2 Moleküle<br />
<strong>Gly</strong>cerinaldehyd-3-phosphat zerlegt. Dieser Abschnitt verbraucht 2 Moleküle ATP<br />
pro Molekül Glucose.<br />
2. ERNTE-Phase: -> liefert Energie und Reduktionsäquivalente<br />
Im zweiten Abschnitt wird <strong>Gly</strong>cerinaldehyd-3-Phosphat (G3P) zu Pyruvat abgebaut.<br />
Bei diesem Abbau werden insgesamt 4 Moleküle ATP gebildet (2 pro G3P). Daraus<br />
ergibt sich eine Nettosynthese von 2 ATP.<br />
8<br />
9<br />
7<br />
21<br />
22
Kohlenhydratstoffwechsel<br />
2<br />
4<br />
Phosphoglucose-<br />
isomerase<br />
Aldolase<br />
Kohlenhydratstoffwechsel<br />
<strong>Gly</strong>colyse - die „Investment“phase<br />
1. Phosphorylierung der Glucose:<br />
1. Schritt: Hexokinase<br />
Übertragung einer Phosphatgruppe von ATP auf die<br />
C-6 Alkoholgruppe der Glucose -> Bildung des<br />
Phosphomonoesters Glucose-6-Phosphat<br />
1<br />
Hexokinase<br />
3<br />
Phosphofructokinase<br />
5<br />
Triosephosphatisomerase<br />
Hexokinase<br />
1 Molekül ATP wird investiert.<br />
Glucose-6-Phosphat reichert sich in der Zelle<br />
an, da die Zellmembran nur für Glucose<br />
durchlässig ist. Außerdem sinkt die<br />
intrazelluläre Glucose-Konzentration im<br />
Vergleich zur extrazellulären, wodurch die<br />
Aufnahme von Glucose begünstigt wird.<br />
23<br />
24
Kohlenhydratstoffwechsel<br />
8 Å<br />
Kohlenhydratstoffwechsel<br />
Substrat-induzierte Konformationsänderung<br />
Beispiel eines INDUCED FIT:<br />
• Glucose und ATP werden im aktiven Zentrum zusammengeführt<br />
• Wasser wird ausgeschlossen um Hydrolyse von ATP zu vermeiden<br />
Offene Konformation Geschlossene Konformation<br />
2. Schritt: Phosphoglucoisomerase (G6P-Isomerase)<br />
2. Isomerisierung (Aldohexose zu Ketohexose):<br />
Die Phosphoglucoisomerase oder Glucose-6-<br />
Phosphat-Isomerase katalysiert die Isomerisierung<br />
von G6P in Fructose-6-Phosphat (F6P).<br />
Unter Standardbedingungen liegt das Gleichgewicht<br />
auf der Seite von G6P. Das Produkt F6P reagiert aber<br />
schnell weiter, darum wird es dem Gleichgewicht<br />
entzogen und die Isomerisierung läuft zu Gunsten der<br />
Ketohexose ab.<br />
Phosphoglucoisomerase<br />
25<br />
26
Kohlenhydratstoffwechsel<br />
Kohlenhydratstoffwechsel<br />
3. Schritt: Phosphofructokinase<br />
Ein 2. Molekül ATP wird investiert.<br />
Phosphofructokinase<br />
Phosphofructokinase: 1. Kontrollpunkt der <strong>Gly</strong>colyse<br />
Warum Kontrollpunkt / Schlüsselenzym?<br />
Die Phosphofructokinase als Regulatorenzym katalysiert den Geschwindigkeitsbestimmenden<br />
Schritt („Flaschenhals“) im ersten Teil der <strong>Gly</strong>kolyse und bestimmt so<br />
entscheidend mit, wie viel verfügbare Energie die Zelle (ATP, Citrat, NADH/H + )<br />
beziehungsweise der Organismus (Blutglucose) besitzt. (-> siehe REGULATION)<br />
Dieser dieser Schritt macht – neben der Glucokinase sowie der Pyruvatkinase – die<br />
<strong>Gly</strong>kolyse unter physiologischen Bedingungen irreversibel.<br />
Weiters ermöglicht diese zweite Phosphorylierung im nächsten Schritt die Bildung von zwei<br />
phosphorylierten Triosen (DHAP und GAP) -> C1-C3 der F1,6bP finden sich dann in<br />
DHAP, C4-C6 in GAP.<br />
Zwei Enzymformen:<br />
• PFKI (Bildung von Fructose-1,6-bisphosphat (F-1,6-BP))<br />
• PFKII (Bildung des PFK-I-Effektors und Isomers Fructose-2,6-bisphosphat (F-2,6-BP))<br />
Beide Enzyme regulieren damit auch den Blutzucker durch Verarbeitung der Signale von<br />
Glucagon und Insulin.<br />
27<br />
28
Kohlenhydratstoffwechsel<br />
Kohlenhydratstoffwechsel<br />
Phosphofructokinase: Regulation<br />
Aktivität der PFK als Funktion von F6P -><br />
Regulation:<br />
Allosterische Inhibierung:<br />
• ATP �: Substrathemmung<br />
• NADH+H + , Citrat<br />
Allosterische Aktivierung:<br />
• ADP, AMP: Energiemangelsignale<br />
• F-2,6-bisP: Isomer von F-1,6,-bisP<br />
gebildet durch PFKII<br />
Allosterische Regulation der Phosphofructokinase<br />
29<br />
30
Kohlenhydratstoffwechsel<br />
Kohlenhydratstoffwechsel<br />
Allosterische Regulation der Phosphofructokinase<br />
Allosterische Bindung von ADP/ATP<br />
ATP hemmt und AMP aktiviert das Enzym<br />
4. Schritt: Aldolase<br />
4. Spaltung in 2 Triosen:<br />
Spaltung des C-6 Zuckers F-1,6-bisP in<br />
zwei C-3 Fragment:<br />
• Dihydroxyacetonphosphat (DHAP)<br />
• <strong>Gly</strong>cerinaldehyd-3-Phosphat (GAP)<br />
Aldolase<br />
31<br />
32
Kohlenhydratstoffwechsel<br />
5. Schritt: Triosephosphatisomerase<br />
5. Isomerisierung von DHAP in GAP:<br />
Da nur GAP weiterverwendet wird, muss DHAP in GAP umgewandelt (isomerisiert)<br />
werden:<br />
Die Isomerisierung in GAP wird dadurch begünstigt, dass GAP in der <strong>Gly</strong>kolyse<br />
weiter abgebaut wird -> Konzentration in der Zelle wird niedrig gehalten.<br />
Kohlenhydratstoffwechsel<br />
Zusammenfassung „Investment“phase<br />
In der ersten Phase der <strong>Gly</strong>colyse wird<br />
Glucose zu 2 <strong>Gly</strong>cerinaldehyd-3-Phosphat<br />
umgewandelt.<br />
Dabei wurde 2 Moleküle ATP verbraucht.<br />
In der zweiten Phase der <strong>Gly</strong>colyse findet<br />
eine Nettobiosynthese von ATP statt<br />
(Energiegewinn).<br />
Triosephosphatisomerase<br />
33<br />
34
Kohlenhydratstoffwechsel<br />
<strong>Gly</strong>colyse - die „Ernte“ / Amortisierungs-Phase<br />
<strong>Gly</strong>cerinaldehyd-3-phospat<br />
8<br />
6<br />
Phosphoglycerat-Mutase<br />
Pyruvatkinase<br />
Kohlenhydratstoffwechsel<br />
10<br />
Enolase<br />
7<br />
Phosphoglycerat-Kinase<br />
6. Schritt: <strong>Gly</strong>cerinaldehyd-3-Phosphat-Dehydrogenase<br />
6. Bildung einer Energiereiche Verbindung:<br />
In dieser Reaktion wird die Oxidation und<br />
Phosphorylierung von G3P mit der Synthese von<br />
NADH gekoppelt.<br />
Gleichzeitig entsteht ein energiereiches<br />
Acylphosphat (gemischtes Säureanhydrid):<br />
1,3-Bisphosphoglycerat (1,3-BPG).<br />
GAP-Dehydrogenase<br />
9<br />
35<br />
36
Kohlenhydratstoffwechsel<br />
Kohlenhydratstoffwechsel<br />
7. Schritt: Phosphoglycerat-Kinase<br />
7. Substratkettenphosphorylierung 1:<br />
Dies ist der erste Schritt, in dem durch eine<br />
Substratkettenphosphorylierung ATP hergestellt<br />
wird -> 1 Molekül ATP pro 1,3-BPG.<br />
Aus 1,3-BPG entsteht dabei 3-Phosphoglycerat<br />
(3PG).<br />
Feedbackregulation:<br />
Falls die Zelle bereits viel ATP hat, hält die<br />
Reaktion an dieser Stelle an, bis wieder<br />
genügend ADP zur Verfügung steht.<br />
Phosphoglycerat-Kinase<br />
8. Schritt: Phosphoglycerat-Mutase<br />
8. Umlagerung der Phosphatgruppe:<br />
D.h. diese Reaktion ist<br />
auch ATP/ADP-reguliert<br />
und damit die 2.<br />
irreversible Reaktion<br />
der <strong>Gly</strong>kolyse.<br />
Dieser Schritt ist notwendig, um in der nächsten Reaktion wieder eine energiereiche<br />
Verbindung herzustellen:<br />
Dabei wird 3-Phosphoglycerat in 2-Phosphoglycerat umgewandelt, wobei die<br />
Phosphatgruppe dabei zwischenzeitlich auf einen Aminosäurerest des Enzyms<br />
übertragen wird.<br />
Phosphoglycerat-Mutase<br />
37<br />
38
Kohlenhydratstoffwechsel<br />
9. Schritt: Enolase<br />
9. Bildung einer energiereichen Verbindung durch Dehydratisierung:<br />
Die Dehydratisierung von 2-Phosphglycerat generiert die energiereiche Verbindung<br />
Phosphoenolpyruvat (PEP). Dies besitzt ein hohes Phosphatgruppen-<br />
Übertragungspotential, was im letzten Schritt der <strong>Gly</strong>kolyse für die Generierung eines<br />
weiteren ATPs genutzt wird.<br />
Kohlenhydratstoffwechsel<br />
10. Schritt: Pyruvatkinase<br />
10. Substratkettenphosphorylierung 2:<br />
Enolase<br />
In der letzten glykolytischen Reaktion wird das zweite energiereiche Produkt PEP zur<br />
Synthese von ATP via Substratkettenphosphorylierung verwendet. Dabei entsteht aus<br />
PEP Pyruvat.<br />
Diese Reaktion ist ebenfalls ATP/ADPreguliert<br />
und damit die 3. irreversible<br />
Reaktion der <strong>Gly</strong>kolyse.<br />
Pyruvatkinase<br />
39<br />
40
Kohlenhydratstoffwechsel<br />
Zusammenfassung „Ernte“phase<br />
Aus jedem Molekül GAP werden in der Erntephase<br />
2 Moleküle ATP durch Substratkettenphosphorylierung<br />
gewonnen, d.h. ein Nettogewinn<br />
von 2 ATP pro 1 Molekül Glucose:<br />
1 Glucose<br />
- 2 ATP<br />
GAP Pyruvat<br />
+ 2 ATP<br />
GAP Pyruvat<br />
+ 2 ATP<br />
Außerdem werden 2 Moleküle NADH erzeugt,<br />
die ebenfalls zur ATP-Gewinnung<br />
herangezogen werden können (im Zuge der<br />
oxidativen Phosphorylierung).<br />
Pyruvat wird weiter abgebaut (Citratcyclus);<br />
dabei wird ebenfalls ATP generiert.<br />
41