03 Kardiale Unterstützungs- und Ersatzsysteme
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Leitthema<br />
MedKlinIntensivmedNotfmed2017 ·112:417–425<br />
DOI 10.1007/s00063-017-0295-8<br />
Eingegangen: 5. März 2017<br />
Angenommen: 24. März 2017<br />
Online publiziert: 2. Mai 2017<br />
© Springer Medizin Verlag GmbH 2017<br />
Redaktion<br />
S. Kluge, Hamburg<br />
T. Graf 1,2 ·H.Thiele 1,2<br />
1<br />
Universitäres Herzzentrum Lübeck Medizinische Klinik II (Kardiologie, Angiologie, Intensivmedizin),<br />
Universitätsklinikum Schleswig-Holstein, Campus Lübeck, Lübeck, Deutschland<br />
2<br />
Deutsches Zentrum für Herz-Kreislauf-Forschung (DZHK) Standort Hamburg/Kiel/Lübeck, Lübeck,<br />
Deutschland<br />
<strong>Kardiale</strong> <strong>Unterstützungs</strong>- <strong>und</strong><br />
<strong>Ersatzsysteme</strong><br />
Die Zahl der Therapien mit kardialen<br />
<strong>Unterstützungs</strong>- <strong>und</strong> <strong>Ersatzsysteme</strong>n<br />
hat in den letzten Jahren deutlich<br />
zugenommen. Immer noch stellt der<br />
therapierefraktäre kardiogene Schock<br />
hierfür die Hauptindikation auf Intensivstationen<br />
in der Erwachsenenmedizin<br />
dar. Neben der frühen Revaskularisation<br />
bei akutem Myokardinfarkt <strong>und</strong><br />
medikamentöser Unterstützung der Hämodynamik<br />
finden hier verschiedene<br />
Systeme zur Kreislaufunterstützung Anwendung.<br />
Die Mortalität des Krankheitsbilds<br />
bleibt trotz aller erwähnter<br />
therapeutischer Maßnahmen hoch <strong>und</strong><br />
liegt immer noch bei bis zu 50 % [1, 2].<br />
» Die Mortalität des<br />
kardiogenen Schocks liegt immer<br />
noch bei bis zu 50 %<br />
Es gibt inzwischen eine Vielzahl zugelassener<br />
Systeme zur mechanischen<br />
Kreislaufunterstützung im kardiogenen<br />
Schock. Das wohl immernocham weitesten<br />
verbreitete Verfahren seit 5 Dekaden<br />
ist die intraaortale Ballonpumpe (IABP)<br />
mit dem Prinzip der getriggerten Gegenpulsation.<br />
Weitere Möglichkeiten bieten<br />
Systeme mit axialem Fluss (Impella® 2.5,<br />
CP <strong>und</strong> 5.0; Abiomed Europe, Aachen,<br />
Germany), Systeme die einen kontinuierlichen<br />
Fluss zwischen linkem Vorhof<br />
<strong>und</strong> Femoralarterie (TandemHeart ; Cardiac<br />
Assist Inc., Pittsburgh, PA, USA)<br />
aufbauen, eine parakorporale pulsatile<br />
Pumpe (iVAC® 2L, Becton Dickinson,<br />
Kelberg, Deutschland), die Heart-<br />
Mate PHP® (Thoratec, Pleasanton, CA,<br />
USA) als transiente transaortale <strong>Unterstützungs</strong>pumpe<br />
sowie der komplett<br />
Extracorporeal Life Support (ECLS)<br />
mit extrakorporaler Membranoxygenierung<br />
(ECMO) als einziges echtes Herz-<br />
(/Lungen-)Ersatzverfahren.<br />
Intraaortale Gegenpulsation<br />
Die IABP war 5 Jahrzehnte als additive<br />
Option zur inotropen Katecholamingabe<br />
<strong>und</strong> Volumentherapie für Patienten im<br />
kardiogenen Schock im Einsatz [3]. In<br />
dieser Zeit kam es zu dramatischen Veränderungen<br />
der Infarkttherapie bis zur<br />
frühzeitigen perkutanen Koronarintervention<br />
(PCI) als derzeitige Standardtherapie<br />
des infarktbedingten kardiogenen<br />
Schocks. Die IABP war bis einschließlich<br />
2012 offizielle Empfehlung für die<br />
Therapie des kardiogenen Schocks mit<br />
einem sehr hohen Empfehlungsgrad (im<br />
Jahr 2012: USA: IC; Europa: IB).<br />
Die IABP ist ein Ballonkatheter, der<br />
perkutan durch die Arteria (A.) femoralis<br />
in die Aorta descendens platziert wird<br />
(distal des Abgangs derA. subclavia sinistra).<br />
Der Ballon füllt sich während der<br />
Diastole <strong>und</strong> deflatiert vor der systolischen<br />
Auswurfphase.<br />
» Die intraaortale Ballonpumpe<br />
wird perkutan durch die<br />
A. femoralis in die Aorta<br />
descendens platziert<br />
Mit der Unterstützung der IABP kann<br />
nach experimentellen Daten der koronare<br />
Blutfluss mittels Augmentation<br />
des Blutdrucks in der diastolischen<br />
Phase verstärkt <strong>und</strong> die Nachlast gesenkt<br />
werden. Das wiederum führt zu<br />
einer Reduktion des myokardialen Sauerstoffverbrauchs,<br />
einer Reduktion des<br />
systolischen Blutdrucks sowie einer Anhebung<br />
des diastolischen Blutdrucks<br />
ohne Veränderung des mittleren arteriellen<br />
Blutdrucks (MAP). Registerdaten<br />
ohne Kontrollgruppe zeigten zusätzlich<br />
die Verbesserung des „cardiac output“<br />
als Maß der Herzleistung sowie eine<br />
verbesserte hämodynamische Kreislaufsituation<br />
für die IABP-behandelten Patienten<br />
[4]. Eine randomisierte Singlecenter-Studie<br />
(n = 40) wies bei Patienten<br />
mit IABP bei infarktbedingtem<br />
kardiogenem Schock gegenüber einer<br />
konservativ geführten Kontrollgruppe<br />
interessanterweise keinen signifikanten<br />
Unterschied in wichtigen hämodynamischen<br />
Kennziffern, wie „cardiac output“,<br />
„cardiac power output“ sowie systemischer<br />
Gefäßwiderstand, nach [5]. Die<br />
Messung der sublingualen Mikrozirkulation<br />
(als nachgewiesen relevanter<br />
prognostischer Faktor im kardiogenen<br />
Schock) wurde unter IABP-Therapie<br />
ebenfalls nicht positiv beeinflusst [6–8].<br />
Eine große Metaanalyse aus dem Jahr<br />
2009, die nur Registerstudien im kardiogenen<br />
Schock auswerten konnte, ließ<br />
erste Zweifel an einer generellen Empfehlungslage<br />
für die IABP aufkommen<br />
[9]. Eine weitere Metaanalyse mit randomisierten<br />
Studien <strong>und</strong> unterschiedlichen<br />
Indikationen zum Einsatz der IABP<br />
zeigte keinen Mortalitätsbenefit [10]. In<br />
Zusammenschau der widersprüchlichen<br />
Datenlage kam es zu einer Abwertung<br />
der Empfehlung zum Einsatz der IABP<br />
im kardiogenen Schock durch die Euro-<br />
Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017 417
Leitthema<br />
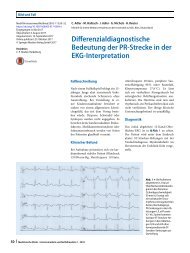
Abb. 1 8 Schematische Darstellung der aktuell verfügbaren kardialen <strong>Unterstützungs</strong>systeme. IABP<br />
intraaortale Ballonpumpe, ECLS Extracorporeal Life Support. (Adaptiert nach [48] mit fre<strong>und</strong>l. Genehmigung<br />
von © H. Thiele et al.)<br />
pean Society of Cardiology (ESC) <strong>und</strong><br />
die Amerikanischen Fachgesellschaften<br />
im Jahr 2013 [11].<br />
» Es kam zu einer Abwertung<br />
der Empfehlung zum Einsatz der<br />
IABP im kardiogenen Schock<br />
Um diese wichtige Datenlücke zu schließen,<br />
wurde schließlich die IABP-<br />
SHOCK-II-Studie durchgeführt [12].<br />
Ziel war es, eine Mortalitätsreduktion<br />
von 12 % unter IABP-Therapie nachzuweisen<br />
[9, 13]. Eingeschlossen wurden<br />
Patienten mit infarktbedingtem kardiogenem<br />
Schock, die einer frühen Revaskularisation<br />
zugeführt werden sollten<br />
(mittels PCI oder „coronary artery bypass<br />
surgery“, CABG). Insgesamt wurden<br />
600 Patienten 1:1 in einen Arm Standardtherapie<br />
mit IABP <strong>und</strong> in einen Arm<br />
Standardtherapie ohne IABP als Kontrollgruppe<br />
randomisiert (301 Patienten<br />
in der IABP-Gruppe, 299 in der Kontrollgruppe).<br />
Als wichtigstes Ergebnis zeigte<br />
sich kein signifikanter Unterschied im<br />
primären Endpunkt der Studie (30-<br />
Tages-Mortalität) zwischen IABP- <strong>und</strong><br />
Kontrollgruppe (. Abb. 1; [14]). In allen<br />
Subgruppenanalysen ließ sich kein signifikanter<br />
Unterschied feststellen [15]. In<br />
allensek<strong>und</strong>ärenEndpunktenzeigtesich<br />
ebenfalls kein signifikanter Unterschied<br />
zwischen den Gruppen. Die Ergebnisse<br />
blieben auch im 12-Monats-Follow-up<br />
der IABP-SHOCK-II-Studie konsistent<br />
[16].<br />
Zu den Sicherheitsendpunkten ist zu<br />
erwähnen, dass sich bei Blutung, peripherer<br />
Ischämie oder Inzidenz von katheterassoziierten<br />
Septitiden keine signifikanten<br />
Unterschiede zwischen den beiden<br />
Gruppen in der IABP-SHOCK-II-<br />
Studie zeigten.<br />
DieseStudieführtezueinemUmdenken<br />
im Einsatz der IABP <strong>und</strong> einer Neuorientierung<br />
in den Leitlinien. Die ESC<br />
stufteaufdemBodenvonIABP-SHOCK-<br />
II indenLeitlinienzurRevaskularisation,<br />
zum akuten Koronarsyndrom ohne ST-<br />
Strecken-Hebung <strong>und</strong> zur Herzinsuffizienz<br />
seit dem Jahr 2014 die Empfehlung<br />
für einen generellen Einsatz der IABP<br />
herab (Empfehlungslage III A; [17–19]).<br />
Perkutane mechanische Kreislaufunterstützungssysteme<br />
In den letzten Jahren kam es im Bereich<br />
der Left Ventricular Assist Devices<br />
(LVAD) <strong>und</strong> der ECLS zu einer Vielzahl<br />
technischer Innovationen <strong>und</strong> aufgr<strong>und</strong><br />
einer einfacheren Handhabung (auch in<br />
der Implantation durch Interventionalisten)<br />
haben diese Systeme auch außerhalb<br />
herzchirurgischer Eingriffe eine breitere<br />
Anwendung erfahren. Weitere Trigger<br />
für eine Zunahme des Einsatzes von<br />
aktiven mechanischen Kreislaufsystemen<br />
waren die negativen Ergebnisse<br />
<strong>und</strong> die Herabstufung der IABP in den<br />
Leitlinien. In einer US-amerikanischen<br />
Registerstudie zeigte sich eine Abnahme<br />
von IABP <strong>und</strong> eine leichte Zunahme<br />
von mechanischen Kreislaufunterstützungssystemen<br />
[20]. In einer weiteren<br />
nationalen US-amerikanischen Beobachtungsstudie<br />
in den Jahren 2007–2011<br />
wurde der Gebrauch von perkutanen<br />
mechanischen Kreislaufunterstützungssystemen<br />
untersucht. Hier zeigte sich ein<br />
deutlicher Anstieg der Implantationen<br />
<strong>und</strong> auch ein Abfall der Mortalitätsraten<br />
bei der Therapie von Patienten im kardiogenen<br />
Schock (51,6 % im Jahr 2007<br />
vs. 43,1 % im Jahr 2011, p = 0,012).<br />
Ein kausaler Zusammenhang zwischen<br />
Nutzung von aktiven <strong>Unterstützungs</strong>systemen<br />
<strong>und</strong> Mortalität lässt sich daraus<br />
aber nicht ableiten. Als wichtigste Mortalitätstrigger<br />
unter der Therapie mit<br />
perkutanen Systemen wurden Koagulopathien<br />
(Odds-Ratio, OR: 2,35; 95 %-<br />
Konfidenzintervall, 95%-KI: 1,88–2,94)<br />
<strong>und</strong> eine der Therapie vorangegangene<br />
kardiopulmonale Reanimation (OR:<br />
3,50; 95 %KI: 2,20–5,57) beobachtet [21].<br />
» Bei den perkutanen Systemen<br />
gehören Koagulopathien zu den<br />
wichtigsten Mortalitätstriggern<br />
Eine Übersicht der Conformité-Européenne(CE)-zertifizierten<br />
in Europa<br />
gebräuchlichen Systeme zeigt . Tab. 1.<br />
Dabei unterscheidet man Systeme, die<br />
nur als reine hämodynamische Unterstützung<br />
gelten (perkutane Assist<br />
Devices), <strong>und</strong> Verfahren mit der Möglichkeit<br />
der Oxygenierung <strong>und</strong> Dekarboxylierung<br />
als kombinierte Herz- <strong>und</strong><br />
Lungenersatzverfahren.<br />
Extrakorporeal-Life-Support-<br />
Systeme<br />
Die Systeme mit der Möglichkeit des<br />
Herz- <strong>und</strong> Lungenersatzverfahrens werden<br />
als ECLS-Systeme bezeichnet, früher<br />
war auch die Bezeichnung extrakorporale<br />
Membranoxygenierung (ECMO)gebräuchlich.DieImplantationerfolgtüblicherweise<br />
perkutan über femorale vaskuläre<br />
Zugangswege. Zugangsweg sind im<br />
Einzelnen eine lange 18–21 French (F)<br />
großevenöseKanüle(dievonderFemoralvene<br />
eingeführt wird <strong>und</strong> im rechten<br />
Atrium zum Liegen kommt) <strong>und</strong> eine<br />
16–18 F große arterielle Kanüle, die in<br />
der distalen Aorta descendens oder der<br />
Iliakalarterie platziert wird.<br />
418 Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017
Zusammenfassung · Abstract<br />
Im Betrieb wird das Blut über den venösenSchenkelinsSystemangesaugt<strong>und</strong><br />
über einen speziellen Membranoxygenator<br />
mit Sauerstoff beladen <strong>und</strong> decarboxyliert.Anschließend<br />
erfolgtdie Rückführung<br />
des sauerstoffreichen Bluts über<br />
die arterielle Kanüle. Dabei kann abhängig<br />
von der Kanülengröße ein Fluss<br />
bis zu 7 l/min aufgebaut <strong>und</strong> somit auch<br />
ein komplettes Herz- <strong>und</strong> Lungenersatzverfahren<br />
etabliert werden. Die periphere<br />
Anlage der Kanülen hat den Vorteil<br />
eines geringeren Blutungsrisikos gegenüber<br />
der zentralen Anlage <strong>und</strong> einer Anlage<br />
durch einen erfahrenen Interventionalisten<br />
unter Durchleuchtung. Die<br />
zentrale Anlage erfolgt venös über eine<br />
Kanülierung im rechten Atrium <strong>und</strong> arteriell<br />
in der Aorta ascendens als kardiopulmonaler<br />
Bypass. Diese Kanülierung<br />
kann nur herzchirurgisch erfolgen, hat<br />
aber den Vorteil einer geringeren Nachlast<br />
mit einem verbesserten „unloading“<br />
des linken Ventrikels.<br />
» Die ECLS-Implantation<br />
erfolgt perkutan über femorale<br />
vaskuläre Zugangswege<br />
Die Hauptkomplikationen des peripheren<br />
Verfahrens sind vaskulärer Art<br />
mit Blutungen <strong>und</strong> Gefäßverletzungen<br />
aufgr<strong>und</strong> des großen Kanülendurchmessers.<br />
Eine ischämische Komplikation des<br />
Beins lässt sich durch antegrade Punktion<br />
<strong>und</strong> Einbringen einer Schleuse in<br />
die A. femoralis mit adäquater Umgehungsperfusion<br />
vermeiden <strong>und</strong> sollte<br />
eine Standardmaßnahme sein.<br />
Randomisierte Daten für ECLS-Systeme<br />
im kardiogenen Schock liegen nicht<br />
vor. Es gibt Register, die einen möglichen<br />
Mortalitätsvorteil suggerieren. Im Register<br />
von Takayama et al. [22] zeigte sich bei<br />
Patienten im therapierefraktären kardiogenen<br />
Shock mit Kollaps der Spontanzirkulation<br />
immerhin eine Überlebensrate<br />
bis zurKrankenhausentlassung von49 %.<br />
Weitere Registerdaten von Combes et al.<br />
[23] wiesen eine ähnliche Überlebensrate<br />
bis zur Krankenhausentlassung (40 %)<br />
auf.<br />
Trotz dieser vielversprechenden Daten<br />
sollten immer die möglichen Komplikationen<br />
beim Einsatz eines ECLS<br />
Med Klin Intensivmed Notfmed 2017 · 112:417–425<br />
© Springer Medizin Verlag GmbH 2017<br />
T.Graf·H.Thiele<br />
<strong>Kardiale</strong> <strong>Unterstützungs</strong>- <strong>und</strong> <strong>Ersatzsysteme</strong><br />
Cardiac support and replacement systems<br />
Abstract<br />
In recent years, the widespread use of<br />
partial mechanical cardiac support and<br />
even temporary complete replacement of<br />
cardiac function has been established in<br />
many intensive care units in the treatment<br />
of refractory cardiogenic shock. There is<br />
a difference between partial left-ventricular<br />
assist devices (LVAD) and the possibility of<br />
complete heart (and lung) replacement<br />
by extra corporeal life support (ECLS).<br />
Despite the use of mechanical support<br />
devices, the mortality of cardiogenic shock<br />
remains high. The consideration of using<br />
percutaneous LVAD and ECLS in cardiogenic<br />
shock should be considered in refractory<br />
cardiogenic shock patients in addition<br />
to support by catecholamines and after<br />
early revascularization in acute coronary<br />
syndromes. However, there are no large<br />
randomized studies evaluating mechanical<br />
support systems with respect to outcome<br />
in cardiogenic shock patients. German and<br />
DOI 10.1007/s00063-017-0295-8<br />
Zusammenfassung<br />
In der Intensivmedizin des Erwachsenen<br />
haben in den letzten Jahren mechanische<br />
Herz-Kreislauf-<strong>Unterstützungs</strong>- (perkutane<br />
Assist Devices) <strong>und</strong> Ersatzverfahren der<br />
Herzfunktion vor allem zur Behandlung<br />
des therapierefraktären infarktbedingten<br />
kardiogenen Schocks Einzug gehalten.<br />
Dabei unterscheidet man partielle <strong>Unterstützungs</strong>systeme<br />
<strong>und</strong> die Möglichkeit eines<br />
kurzzeitigen kompletten Herz- <strong>und</strong> (Lungen)-<br />
Ersatzes mittels Extracorporeal Life Support<br />
(ECLS). Trotz Einsatz dieser Systeme bleibt der<br />
kardiogene Schock mit einer hohen Mortalität<br />
verb<strong>und</strong>en. Die Erwägung mechanischer<br />
Systeme, wie perkutaner linksventrikulärer<br />
<strong>Unterstützungs</strong>systeme <strong>und</strong> ECLS, sollte erst<br />
nach Ausschöpfung medikamentöser Therapien<br />
zur Stabilisation der hämodynamischen<br />
Zielparameter erfolgen. Die Datenlage zur<br />
Implantation perkutaner Left Ventricular<br />
Assist Devices (LVAD) oder des ECLS bei<br />
Patienten im kardiogenen Schock ist bisher<br />
noch deutlich begrenzt. Eine Empfehlung zur<br />
Implantation des ECLS gibt es in den deutschen<br />
<strong>und</strong> internationalen Leitlinien erst nach<br />
Ausschöpfung der medikamentösen Therapie<br />
im kardiogenen Schock. In anderen Fällen<br />
eines nichtinfarktbedingten kardiogenen<br />
Schocks (z. B. Intoxikation, Myokarditis) kann<br />
ein ECLS als Überbrückung genutzt werden.<br />
ECLS kann auch in Fällen der Reanimation als<br />
sogenannte E-CPR eingesetzt werden <strong>und</strong><br />
zeigte nach Register-Daten einen möglichen<br />
Mortalitätsbenefit bei ausgewählten<br />
Patienten.<br />
Eine weitere Sondersituation für den Einsatz<br />
von ECLS stellt die akzidentielle schwere<br />
Hypothermie mit Herzkreislaufstillstand<br />
dar, auch hier gibt es limitierte Daten für<br />
die Anwendung der Systeme. Bei fehlender<br />
Therapie-Alternative sollte aber in diesen<br />
Fällen frühzeitig über den Einsatz der<br />
Organersatzsysteme nachgedacht werden.<br />
Schlüsselwörter<br />
Herzinfarkt · Kardiogener Schock · Myokardiale<br />
Revaskularisation · Extrakorporale<br />
Membranoxygenierung · Hypothermie<br />
international guidelines do not recommend<br />
the routine use of mechanical support as<br />
a first-line treatment in cardiogenic shock<br />
patients and emphasize that their application<br />
should be restricted to patients with therapy<br />
refractory shock. In other cases of noninfarctrelated<br />
cardiogenic shock (e. g., poisoning,<br />
myocarditis), ECLS use should be considered<br />
as bridging therapy. ECLS may also be<br />
considered in cardiopulmonary resuscitation<br />
which is termed E-CPR. According to registry<br />
data, E-CPR may reduce mortality in selected<br />
patients. A possible application of ECLS is<br />
severe accidental hypothermia with cardiac<br />
arrest despite limited data. In these rare<br />
cases, early ECLS should be considered for<br />
rewarming and stabilization.<br />
Keywords<br />
Myocardial infarction · Cardiogenic shock ·<br />
Myocardial revascularization · Extracorporeal<br />
membrane oxygenation · Hypothermia<br />
Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017 419
Leitthema<br />
Tab. 1 Technische Daten der in der Europäischen Union zugelassenen perkutanen Left Ventricular Assist Devices (LVAD) <strong>und</strong> des Extracorporal Life<br />
Support System (ECLS)<br />
iVAC® 2L TandemHeart Impella®<br />
Impella® 2.5 Impella ® 5.0 Impella ® CP HeartMate ECLS<br />
5.0 PHP® (multiple<br />
Systeme)<br />
Kathetergröße 11 – 9 9 9 14 –<br />
Kanülengröße 17 21 venös<br />
12–19 arteriell<br />
21 12 14 13 17–21<br />
16–19<br />
Flussrate (l/min) Maximal 2,8 Maximal 4,0 Maximal 2,5 Maximal 5,0 3,7–4,0 Maximal 5,0 Maximal 7,0<br />
Pumpengeschwindigkeit Pulsatil 40 ml/ Maximal 7500 Maximal Maximal Maximal Maximal Maximal 5000<br />
Schlag<br />
33,000 51,000 51,000 20,500<br />
Zugangsweg<br />
Perkutan<br />
(A. femoralis)<br />
Perkutan (A. femoralis<br />
<strong>und</strong><br />
V. femoralis für<br />
transseptale<br />
Punktion)<br />
Perkutan<br />
(A. femoralis)<br />
Peripher chirurgisch<br />
(A. femoralis)<br />
Perkutan<br />
(A. femoralis)<br />
Perkutan<br />
(A. femoralis)<br />
Perkutan<br />
(A. femoralis<br />
<strong>und</strong> V. femoralis)<br />
LV-Entlastung + ++ ++ + + ++ –<br />
Antikoagulation + + + + + + +<br />
Empfohlene maximale 21 Tage 14 Tage 10 Tage 10 Tage 10 Tage 6h 7Tage<br />
Verweildauer<br />
CE-Zertifikat + + + + + + +<br />
Relative Kosten ++ +++++ +++ ++++ ++++ ++++ +(+)<br />
LV linker Ventrikel, CE Conformité Européenne<br />
bedacht werden. In einer Metaanalyse<br />
von vorwiegend chirurgisch implantierten<br />
Systemen wurde eine nicht unerhebliche<br />
Komplikationsrate mit ECLS<br />
gezeigt [24]. So traten bei insgesamt<br />
1452 Patienten, die in die Komplikationsanalyse<br />
eingingen, transfusions- oder<br />
interventionspflichtige Blutungen („major<br />
bleeding“ 40,8 %), ischämische <strong>und</strong><br />
hämorrhagische Schlaganfälle (5,9 %)<br />
bzw. neurologische Komplikationen<br />
(13,3 %) sowie ein akutes Nierenversagen<br />
(teilweise mit der Notwenigkeit<br />
einer Nierenersatztherapie 55,6 % bzw.<br />
46 %) auf, allerdings ohne Diskriminierung,<br />
ob diese Blutungen deviceassoziiert<br />
oder im Rahmen des chirurgischen<br />
Eingriffs bzw. der Gr<strong>und</strong>erkrankung<br />
zu werten waren. An ECLS-typischen<br />
Komplikationen wurden v. a. Patienten<br />
mit Beinischämie (16,9 %) bzw. der<br />
Notwendigkeit einer Fasziotomie der<br />
unteren Extremität bei Kompartmentsyndrom<br />
(10,3 %) <strong>und</strong> teilweise auch<br />
Amputationen (4,7 %) beobachtet. Die<br />
insgesamt hohe Komplikationsrate ist<br />
hier teilweise als Ausdruck der Schwere<br />
des kardiogenen Schocks <strong>und</strong> auch im<br />
Rahmen herzchirurgischer Eingriffe zu<br />
werten. Die ECLS-typischen Komplikationen<br />
an den unteren Extremitäten<br />
lassen sich durch den adäquaten Einsatz<br />
einer antegraden Beinperfusion bei der<br />
Anlage minimieren.<br />
» Als ECLS-typische<br />
Komplikation wurden Patienten<br />
mit Beinischämie beobachtet<br />
Nicht unerwähnt sollten auch mögliche<br />
hämodynamische Nachteile des ECLS<br />
im kardiogenen Schock bleiben. Durch<br />
den retrograden Fluss der arteriellen<br />
Kanüle bei der peripheren Implantation<br />
des ECLS kommt es zu einer deutlichen<br />
Nachlasterhöhung, was gerade<br />
im kardiogenen Schock bei akutem<br />
Myokardinfarkt zu einem Problem des<br />
erhöhten Sauerstoffbedarfs am Myokard<br />
führt. Hier kann das Problem des<br />
fehlenden „unloading“ des linken Ventrikels<br />
zum Tragen kommen, das zu<br />
einem zusätzlichen Lungenversagen bei<br />
Rückwärtsversagen <strong>und</strong> sogar zu einer<br />
Thrombosierung des linken Ventrikels<br />
beifehlendemintrinsischemAuswurfdes<br />
linken Ventrikels führt. Eine Möglichkeit<br />
zur Reduktion dieser Nachteile scheint<br />
das „venting“ des linken Ventrikels zu<br />
sein. Hierzu kann z. B. eine zusätzliche<br />
Impella® -Pumpe in den linken Ventrikel<br />
eingeführt werden, was den Auswurf aus<br />
dem linken Ventrikel verbessert [25]. In<br />
gewissen Notfallsituationen kann auch<br />
eine kardiopulmonale Reanimation den<br />
Auswurf aus dem linken Ventrikel kurzzeitig<br />
aufrecht halten. Andere Ansätze<br />
sind eine zentrale Kanülierung des linken<br />
Vorhofs, der A. axillaris oder auch<br />
des linken Ventrikels mit nachfolgender<br />
Verringerung einer pulmonalen Stauung.<br />
Kleinere Fallserien berichten hier<br />
gute Ergebnisse für das linksventrikuläre<br />
„venting“ als „Salvage-Prozedur“<br />
[26] bei inadäquatem Ansprechen auf<br />
ein peripheres ECLS-Verfahren. In einer<br />
Metaanalyse zeigte sich kein Vorteil<br />
einer zusätzlichen IABP bei ECLS-Verwendung,<br />
sodass diese Kombination<br />
für das „venting“ nicht sinnvoll zu sein<br />
scheint [27].<br />
Patientenselektion<br />
DiehoheKomplikations-<strong>und</strong>Nebenwirkungsrate<br />
nach Implantation eines<br />
ECLS-Systems wirft die Frage nach einer<br />
adäquaten Patientenselektion auf.<br />
Daten aus der IABP-SHOCK-II-Studie<br />
[14] zeigen, dass 50–60 % der Patienten<br />
einen kardiogenen Schock ohne mechanische<br />
<strong>Unterstützungs</strong>systeme überleben.<br />
Für diese Patienten sind hohe<br />
Komplikationsraten der ECLS-Implantation<br />
aber auch anderer Systeme eher<br />
ein Mortalitätsnachteil. Die Ergebnisse<br />
420 Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017
der IMPRESS-in-Severe-Shock-Studie<br />
[28] suggerieren zudem, dass unter mechanischer<br />
Kreislaufunterstützung im<br />
therapierefraktären kardiogenen Schock<br />
eher eine hämodynamische Stabilisierung<br />
der Patienten erfolgt, aber die<br />
neurologische Prognose nicht positiv<br />
beeinflusst wird.<br />
» Etwa 50–60 % der Patienten<br />
überleben einen kardiogenen<br />
Schock ohne mechanische<br />
<strong>Unterstützungs</strong>systeme<br />
Hier steht eine Anzeige.<br />
K<br />
Auch der optimale ImplantationszeitpunktderECLS-Systemeimkardiogenen<br />
Schock (in Relation zur Durchführung<br />
der perkutanen Koronarintervention)<br />
bleibt unklar. Einerseits kann ein frühzeitiger<br />
Einsatz von ECLS ein Multiorganversagen<br />
verhindern, andererseits<br />
könnte durch Komplikationen die Mortalität<br />
ansteigen [29]. Auch hier müssen<br />
die entscheidenden Fragen in weiteren<br />
Studien beantwortet werden.<br />
Dem Lebensalter der Patienten fällt<br />
in der Entscheidungsfindung zum ECLS<br />
wohl insgesamt eine besondere Rolle zu.<br />
Registerdaten von Beurtheret et al. haben<br />
im Jahr 2013 belegt, dass insbesondere<br />
bei älteren Patienten oder Patienten mit<br />
laufender Reanimation die Mortalität bis<br />
zu 100 % trotz Einsatz von ECLS liegt<br />
[30]. So konnten auch de Waha et al.<br />
im Jahr 2016 zeigen, dass in einem bizentrischen<br />
Register Patienten in einer<br />
dichotomen Untersuchung ab einem Lebensalter<br />
>60 Jahre eine deutlich geringere<br />
Überlebenschance unter ECLS <strong>und</strong><br />
in der Nachbeobachtung hatten als Patienten,<br />
die beim Implantationszeitpunkt<br />
60 Jahre oder jünger waren [31].<br />
Extrakorporale kardiopulmonale<br />
Reanimation<br />
Ein weiteres Einsatzfeld des ECLS ist<br />
die sog. extrakorporale kardiopulmonale<br />
Reanimation (E-CPR). Das bedeutet die<br />
frühzeitigeImplantationeinesECLS-Systems<br />
im Herz-Kreislauf-Stillstand unter<br />
mechanischer Reanimation. Es gibt einige<br />
Registerstudien, die einen möglichen<br />
Mortalitätsvorteil suggerieren [32]. Eine<br />
aktuelle Metaanalyse [33] zeigte, dass ge-
Leitthema<br />
poolte ECLS-Patienten im Herz-Kreislauf-Stillstand<br />
außerhalb <strong>und</strong> innerhalb<br />
des Krankenhauses sowie mit therapierefraktärem<br />
kardiogenem Schock nach<br />
akutem Myokardinfarkt eine verbesserte<br />
30-Tages-Mortalität <strong>und</strong> ein verbessertesneurologischesOutcomegegenüber<br />
Kontrollgruppen ohne ECLS aufwiesen.<br />
Auch bei der E-CPR spielt die Patientenselektion<br />
eine wichtige Rolle.<br />
Selektionskriterien sollten das Lebensalter,<br />
der beobachtete Herz-Kreislauf-<br />
Stillstand mit geringer „No-flow-“ <strong>und</strong><br />
„Low-flow-Zeit“, Bystander-Reanimation<br />
<strong>und</strong> die vermutete kardiale Ursache<br />
des Herz-Kreislauf-Stillstands mit zu<br />
erwartendem gutem neurologischem<br />
Outcome sein. Ebenso ist eine zeitnahe<br />
ECMO-Implantation elementar, da bei<br />
länger fortgeschrittener Reanimation die<br />
Überlebenschancen sehr gering sind.<br />
Zur Beurteilung des möglichen Überlebensvorteils<br />
für Patienten im therapierefraktären<br />
kardiogenen Schock, die mit<br />
ECLS behandelt sowie zur E-CPR selektioniert<br />
werden, sind allerdings weiterhin<br />
dringend randomisierte Studien notwendig.<br />
TandemHeart<br />
Das TandemHeart ist eine extrakorporale<br />
Kreislaufunterstützung, die keine<br />
Möglichkeit eines Lungenersatzverfahrens,<br />
sondern eine reine hämodynamische<br />
Unterstützung anbietet. Eine<br />
ableitende Kanüle entnimmt nach einer<br />
transseptalen Punktion oxygeniertes<br />
Blut aus dem linken Vorhof. Angetrieben<br />
durch eine extrakorporal gelegene<br />
Zentrifuge wird das Blut anschließend<br />
in einer über die A. femoralis liegende<br />
Kanüle retrograd zurückgegeben.<br />
Dabei erreicht das System einen unterstützenden<br />
Fluss von bis zu 4 l/min.<br />
Kleinere randomisierte Studien verglichen<br />
den Einsatz des TandemHeart mit<br />
der IABP im kardiogenen Schock [34,<br />
35]. Es zeigte sich eine Verbesserung<br />
der hämodynamischen Parameter bei<br />
den Patienten in der TandemHeart-<br />
Gruppe, aber auch eine Erhöhung der<br />
Komplikationsrate (Blutung, periphere<br />
Ischämie). Aufgr<strong>und</strong> der geringen<br />
Patientenzahlen lässt sich bisher kein<br />
Mortalitätsvorteil für die Behandlung<br />
mit dem TandemHeart nachweisen.<br />
Durch seine fehlende Möglichkeit der<br />
Oxygenierung <strong>und</strong> Decarboxylierung ist<br />
die Methode eher Patienten mit isoliertem<br />
linksventrikulärem Pumpversagen<br />
im kardiogenen Schock vorbehalten. Bei<br />
pulmonalen Problemen sollte über eine<br />
Alternative nachgedacht werden. Die<br />
transseptale Lage macht das Tandem-<br />
Heart-System anfällig für Dislokation<br />
bzw. größere Verletzungen oder Perforation<br />
der Vorhöfe bei Manipulation.<br />
In einer kürzlich publizierten Tierversuchsstudie<br />
zeigte sich eine bessere Herz-<br />
Kreislauf-Unterstützung mit dem TandemHeart<br />
im Vergleich zur Impella®<br />
[36].<br />
Impella®<br />
Die Impella® ist eine mikroaxiale Pumpe.<br />
Dabei stehen 3 Varianten zur Verfügung;<br />
als Flusssystem mit 2,5 l/min <strong>und</strong><br />
3,5 l/min (Impella® CP) perkutan über<br />
die Leiste implantierbar <strong>und</strong> mit maximalem<br />
Fluss von 5,0 l/min nach chirurgischer<br />
peripherer Freilegung der Leistengefäße<br />
implantierbar. Die katheterbasierte<br />
Version wird über die Leiste eingeführt<br />
<strong>und</strong> retrograd über die Aortenklappe in<br />
den linken Ventrikel platziert. Über eine<br />
mikroaxiale Pumpe wird das Blut vom<br />
linken Ventrikel in die Aorta ascendens<br />
gepumpt.<br />
» Das Blut wird über eine<br />
mikroaxiale Pumpe vom linken<br />
Ventrikel in die Aorta ascendens<br />
gepumpt<br />
Die Pumpe arbeitet mit einer Geschwindigkeit<br />
von bis zu 50.000 Umdrehungen<br />
pro Minute. Für die Impella® 2,5 l Pumpe<br />
konnte eine bessere Hämodynamik<br />
gegenüber der Unterstützung mit einer<br />
IABP in einer kleinen prospektiv-randomisierten<br />
Studie gezeigt werden [37]. Allerdings<br />
zeigte die IMPRESS-in-Severe-<br />
Shock-Studie, dass es nach Randomisation<br />
von Patienten mit kardiogenem<br />
Schock nach Myokardinfarkt in einen<br />
Arm mit Impella® 2.5 (n = 24) <strong>und</strong> einen<br />
Arm mit IABP-Unterstützung (n = 24)<br />
zu keinem statistisch signifikanten Unterschied<br />
im 30-Tages-Überleben kam.<br />
Ebenso zeigten sich unter der Impella®<br />
keine Vorteile bei sek<strong>und</strong>ären Endpunkten,<br />
wie Laktat, Katecholamindosen oder<br />
der Nierenfunktion.<br />
Es gibt weitere Registerdaten, die den<br />
Einsatz im therapierefraktären kardiogenen<br />
Schock beschreiben [38, 39]. Bei<br />
fehlender Kontrollgruppe sind weitere<br />
Rückschlüsse allerdings schwierig.<br />
Derzeit wird in Dänemark eine weitere<br />
randomisierte Studie im kardiogenen<br />
Schock (DanSHOCK) mit der<br />
Impella® CP durchgeführt.<br />
HeartMate PHP®<br />
Die HeartMate PHP® („percutaneous<br />
heart pump“) ist eine perkutan inserierte<br />
<strong>Unterstützungs</strong>pumpe ohne Oxygenierung.<br />
Über eine transfemorale arterielle<br />
14 F-Schleuse wird ein Impeller retrograd<br />
über die Aortenklappe in den<br />
linken Ventrikel eingebracht <strong>und</strong> dort<br />
verankert. Über den Impeller wird ein<br />
laminärer Fluss (bis zu 4 l/min) aus dem<br />
linken Ventrikel in die Aorta ascendens<br />
erzeugt. Das System entfaltet sich erst<br />
nach Insertion in die Aorta <strong>und</strong> kann<br />
somit im Gefäß bis zu 24 F Durchmesser<br />
erreichen. Das System ist derzeit<br />
nur für Hochrisikointerventionen im<br />
Katheterlabor zugelassen <strong>und</strong> kann bis<br />
zu 6 h genutzt werden. Randomisierte<br />
Outcomedaten gibt es für die HeartMate<br />
PHP® bis zum jetzigen Zeitpunkt nicht.<br />
Parakorporales pulsatiles LVAD<br />
Das parakorporale pulsatile LVAD<br />
(iVAC® 2L) ist ein perkutanes <strong>Unterstützungs</strong>system,<br />
das arteriell transfemoral<br />
oder subklavikulär eingebracht wird<br />
<strong>und</strong> über eine Membranpumpe einen<br />
<strong>Unterstützungs</strong>fluss von bis zu 2 l/min<br />
gewährleisten kann. Dabei wird mit pulsatiler<br />
Flussunterstützung Blut über die<br />
Spitze des Systems im linken Ventrikel<br />
angesaugt <strong>und</strong> anschließend in der Aorta<br />
ascendens mit 40 ml pro Herzschlag<br />
wieder in den Kreislauf abgegeben.<br />
In Fallberichten konnten Patienten<br />
im akuten Linksherzversagen mit dieser<br />
Therapie überbrückt <strong>und</strong> erfolgreich therapiert<br />
werden [40]. Endpunktstudien<br />
fehlen auch zu diesem Verfahren. Das<br />
422 Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017
System kann auch als Right-Ventricular-<br />
Assist-Device(RVAD)- oder sogar als<br />
Biventricular-Assist-Device(BiVAD)-<br />
Verfahren eingesetzt werden.<br />
Behandlungszeitpunkt im<br />
kardiogenen Schock<br />
Wie bereits mehrfach erwähnt gibt es<br />
keine randomisierten Studien mit einem<br />
Mortalitätsvorteil für Patienten,<br />
die mittels perkutaner LVAD-Unterstützung<br />
oder ECLS im kardiogenen<br />
Schock behandelt wurden. Es existiert<br />
eine Metaanalyse von Chen et al. [41]mit<br />
Zusammenfassung der randomisierten<br />
Studien, wobei eine Studie Impella® [35]<br />
<strong>und</strong> 2 weitere Studien TandemHeart<br />
mit der IABP-Therapie verglichen [34].<br />
In der Zusammenschau zeigten die perkutanen<br />
LVAD-Patienten verbesserte<br />
hämodynamische Parameter gegenüber<br />
den IABP-Patienten (erhöhter Herzindex,<br />
höherer MAP <strong>und</strong> erniedrigter<br />
pulmonal-kapillarer Okklusionsdruck).<br />
In den 30-Tages-Mortalitätsdaten gab<br />
es allerdings keine signifikante Differenz<br />
der verglichenen Gruppen bei einer<br />
höheren Anzahl von Blutungen in der<br />
TandemHeart-Gruppe. Auf dem Boden<br />
dieser Datenlage ist eine generelle<br />
Empfehlung der Anwendung perkutaner<br />
LVAD-Systeme bei kardiogenem Schock<br />
nicht sinnvoll. Europäische <strong>und</strong> amerikanische<br />
Leitlinien geben derzeit nur<br />
eine Empfehlung zum Einsatz bei therapierefraktärem<br />
kardiogenem Schock<br />
(Empfehlungsgrad Klasse IIb C; [12]).<br />
Die routinemäßige Anwendung von perkutanen<br />
LVAD-Systemen könnte einigen<br />
Patienten durch potenzielle Komplikationen<br />
der Therapie eher schaden, da<br />
sie oftmals auch ohne mechanische Unterstützung<br />
hämodynamische Stabilität<br />
<strong>und</strong> Überleben erreichen können.<br />
» Es fehlen genaue Kriterien<br />
für die Patientenselektion<br />
oder die Auswahl des<br />
Implantationszeitpunkts<br />
Durch den Mangel an randomisierten<br />
Studien gibt es keine genauen Kriterien<br />
für die Patientenselektion oder die Auswahl<br />
des Implantationszeitpunkts. Hier<br />
spielen sowohl die patientenindividuelle<br />
Situation, die Erfahrung des Intensivmediziners<br />
<strong>und</strong> des Implantationsteams als<br />
auch klinikinterne Standardabläufe eine<br />
wichtige Rolle.<br />
Derzeit scheint die Höhe des Serumlaktats<br />
<strong>und</strong> sein dynamischer Verlauf<br />
über die Zeit bei Patienten im kardiogenen<br />
Schock ein guter Indikator für die<br />
Mortalitätsprädiktion zu sein [42–44].<br />
Insofern kann sowohl die hämodynamische<br />
Situation als auch das initiale<br />
Laktat bzw. die ausbleibende Laktatclearance<br />
im Verlauf zusammen mit den<br />
Katecholamindosen eine mögliche Entscheidungshilfe<br />
für den Einsatz eines<br />
LVAD oder eines ECLS sein.<br />
Auswahl des <strong>Unterstützungs</strong>oder<br />
Ersatzverfahrens<br />
Es gibt bisher keine Direktvergleiche<br />
vons Studiendaten zwischen den einzelnen<br />
perkutanen <strong>Unterstützungs</strong>- <strong>und</strong><br />
<strong>Ersatzsysteme</strong>n. Deshalb sollte die Entscheidung<br />
zur Auswahl des Systems auf<br />
Gr<strong>und</strong>lage aller pathophysiologischen<br />
<strong>und</strong> klinischen Überlegungen <strong>und</strong> somit<br />
patientenindividuell erfolgen. Tierversuchsdaten<br />
zeigten einen möglichen<br />
Vorteil des TandemHeart im Vergleich<br />
zur Impella® , was derzeit aber nicht<br />
durch humane Daten gestützt werden<br />
kann [36].<br />
Die erste Überlegung sollte den Bedarf<br />
an Flussunterstützung betreffen. Die<br />
Impella® 2.5 kann hier nur einen maximalenFlussvon2,5l/minaufbringen.<br />
Vor Implantation sollte geklärt werden,<br />
ob der Patient nur ein linksventrikuläres<br />
infarktbedingtes Vorwärtsversagen<br />
hat, oder beide Ventrikel betroffen sind<br />
<strong>und</strong> möglicherweise auch ein pulmonales<br />
Problem hinzukommen könnte.<br />
Im Fall des isolierten linksventrikulären<br />
Vorwärtsversagens sind TandemHeart<br />
<strong>und</strong> Impella® (Wahl des Systems je nach<br />
vermutetem Herzzeitvolumenbedarf)<br />
eine mögliche Wahl. Im Fall eines kombinierten<br />
Herz-Lungen-Versagens oder<br />
auch bei Rechtsherzbeteiligung sollte<br />
eher über ein ECLS nachgedacht werden<br />
[45].<br />
Die Impella® <strong>und</strong> das HeartMate PHP<br />
sollten nicht bei mechanischen Komplikationen<br />
des akuten Myokardinfarkts<br />
eingesetzt werden. Weitere Kontraindikationen<br />
sind Kunstklappenersatz in<br />
Aortenposition, hochgradige Aortenklappenstenose<br />
oder -insuffizienz sowie<br />
ein linksventrikulärer intrakavitärer<br />
Thrombus. Die Vor- <strong>und</strong> Nachteile der<br />
einzelnen Systeme sind ohne randomisierte<br />
Daten aber eher theoretischer<br />
Natur<strong>und</strong>unterliegenv.a.pathophysiologischen<br />
Überlegungen. Zusammenfassend<br />
ist ein Teamansatz (Implanteur<br />
<strong>und</strong> Intensivmediziner) zum Erkennen<br />
des optimalen Implantationszeitpunktes<br />
zu empfehlen. Auch die Auswahl des<br />
Verfahrens sollte konsensuell im Team<br />
getroffen werden.<br />
» Die Auswahl des Verfahrens<br />
sollte konsensuell im Team<br />
getroffen werden<br />
Komplikationen sollten, wenn möglich,<br />
vermieden oder bei Auftreten durch<br />
Standardvorgehensweisen während der<br />
Implantation <strong>und</strong> der Betreuung der Patienten<br />
durch Ärzte <strong>und</strong> Pflegepersonal<br />
behoben werden können. Dabei sollten<br />
die theoretisch möglichen Komplikationen<br />
allen Behandelnden bekannt sein<br />
<strong>und</strong> somit erkannt werden können. Standardprotokolle<br />
<strong>und</strong> Checklisten in der<br />
täglichen Routine können hier hilfreich<br />
sein.<br />
Behandlungsoptionen <strong>und</strong><br />
Indikationen<br />
<strong>Kardiale</strong> <strong>Unterstützungs</strong>- <strong>und</strong> Ersatzverfahren<br />
können als „bridge to recovery“,<br />
„bridge to transplant“, „bridge to decision“<br />
oder „bridge to surgery“ benutzt<br />
werden. Wenn keine der genannten Optionen<br />
erreichbar scheint, sollte auf die<br />
Implantation eines <strong>Unterstützungs</strong>- oder<br />
Ersatzverfahrens verzichtet werden. Ausnahmefälle<br />
können Patienten mit einem<br />
unklaren neurologischen Status darstellen.<br />
Für diese Patienten kann die Anwendung<br />
eines <strong>Unterstützungs</strong>- oder Ersatzverfahrens<br />
als „bridge to decision“ eingesetzt<br />
werden, um Zeit für die endgültige<br />
Evaluation des neurologischen Status zu<br />
gewinnen.<br />
Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017 423
Leitthema<br />
Schwere akzidentielle<br />
Hypothermie<br />
Die schwere akzidentielle Hypothermie<br />
mit Herz-Kreislauf-Stillstand stellt eine<br />
seltenere Indikation für eine Organersatztherapie<br />
mit ECLS dar. Einzelfallberichte<br />
zeigen hier ein positives Outcome<br />
für Patienten [46]. Die Wahrscheinlichkeit,<br />
einen Herz-Kreislauf-Stillstand zu<br />
erleiden, steigt bei einer Körperkerntemperatur<br />
unter 28 °C deutlich an [46]. In<br />
den European-Research-Council(ERC)-<br />
Leitlinien aus dem Jahr 2015 findet<br />
die frühzeitige Transportentscheidung<br />
<strong>und</strong> Verlegung in ein ECLS-Zentrum<br />
(auch unter Reanimationsbedingungen)<br />
Erwähnung [47].<br />
Seltene Indikationen<br />
Zu den seltenen Indikationen für eine<br />
ECLS-Therapie in der Erwachsenenmedizin<br />
gehören Intoxikationen (v. a. bei<br />
transienten schweren Herzrhythmusstörungen)<br />
<strong>und</strong> nichtinfarktbedingtes<br />
kardiales Pumpversagen (z. B. dilatative<br />
Kardiomyopathie vor Herztransplantation<br />
oder LVAD-Implantation, fulminante<br />
Myokarditidenetc.).ZudiesenIndikationen<br />
existieren nur Einzelfallberichte <strong>und</strong><br />
keine randomisierten Studien. Die Implantationsentscheidung<br />
erfolgt hier am<br />
besten konsensuell im Team Implanteur/<br />
Intensivmediziner auf der Gr<strong>und</strong>lage<br />
der Pathophysiologie der zum kardialen<br />
Pumpversagen führenden Entität.<br />
Fazit für die Praxis<br />
4 Der Einsatz kardialer <strong>Unterstützungs</strong><strong>und</strong><br />
Ersatztherapien hat in den letzten<br />
Jahren stark zugenommen <strong>und</strong><br />
könnte bei kardiogenem Schock eine<br />
mögliche Behandlungsoption für<br />
ein vorselektioniertes Patientengut<br />
darstellen.<br />
4 Es gibt allerdings derzeit keine Mortalitätsverbesserung<br />
in randomisierten<br />
Outcomestudien. In den aktuellen<br />
Empfehlungen der großen Fachgesellschaften<br />
wird daher nahegelegt,<br />
die perkutane LVAD-Therapie nur<br />
bei therapierefraktären Patienten<br />
einzusetzen.<br />
4 Die Aspekte des Outcomes <strong>und</strong> der<br />
optimalen Patientenselektion sollten<br />
Gegenstand zukünftiger klinischer<br />
Studien werden.<br />
4 Eine seltene Indikation für ECLS<br />
stellt der Herz-Kreislauf-Stillstand bei<br />
schwerer Hypothermie dar, die Therapieoption<br />
sollte schon in die primäre<br />
Transportentscheidung einfließen.<br />
Seltenere ECLS-Indikationen (z. B.<br />
Intoxikationen, fulminante Myokarditis<br />
etc.) sollten in Abhängigkeit der<br />
Pathophysiologie <strong>und</strong> patientenindividuell<br />
abhängig von der klinischen<br />
Symptomatik <strong>und</strong> der Hämodynamik<br />
des Patienten getroffen werden.<br />
Korrespondenzadresse<br />
Prof. Dr. H. Thiele<br />
Universitäres Herzzentrum Lübeck<br />
Medizinische Klinik II (Kardiologie, Angiologie,<br />
Intensivmedizin), Universitätsklinikum<br />
Schleswig-Holstein, Campus Lübeck<br />
Ratzeburger Allee 160, 23538 Lübeck,<br />
Deutschland<br />
holger.thiele@uksh.de<br />
Einhaltung ethischer Richtlinien<br />
Interessenkonflikt. T. Graf <strong>und</strong> H. Thiele geben an,<br />
dass kein Interessenkonflikt besteht.<br />
Dieser Beitrag beinhaltet keine von den Autoren<br />
durchgeführten Studien an Menschen oder Tieren.<br />
Literatur<br />
1. Goldberg RJ, Spencer FA, Gore JM et al (2009)<br />
Thirty-yeartrends(1975to2005)inthemagnitude<br />
of, management of, and hospital death rates<br />
associated with cardiogenicshock in patients with<br />
acute myocardial infarction: a population-based<br />
perspective.Circulation119:1211–1219<br />
2. Thiele H, Schuler G (2009) Cardiogenic shock: to<br />
pumpornottopump?EurHeartJ30:389–390<br />
3. Werdan K, Buerke M, Engelmann L et al (2011)<br />
Deutsch-Österreichische S3-Leitlinie InfarktbedingterkardiogenerSchock.Diagnose,Monitoring<br />
<strong>und</strong>Therapie.Kardiologe5:166–224<br />
4. Kern MJ, Aguirre F, Bach R et al (1993) Augmentation<br />
of coronary blood flow by intra-aortic balloon<br />
pumping in patients after coronary angioplasty.<br />
Circulation87:500–511<br />
5. Prondzinsky R, Unverzagt S, Russ M et al (2013)<br />
Hemodynamic effects of intra-aortic balloon<br />
counterpulsationinpatientswithacutemyocardial<br />
infarction complicated by cardiogenic shock: the<br />
prospective, randomized IABP shock trial. Shock<br />
37:378–384<br />
6. denUilCA,LagrandWK,vanderEntMetal(2009)<br />
The effects of intra-aortic balloon pump support<br />
on macrocirculation and tissue microcirculation<br />
in patients with cardiogenic shock. Cardiology<br />
114:42–46<br />
7. denUilCA,LagrandWK,vanderEntMetal(2010)<br />
Impaired microcirculation predicts poor outcome<br />
of patients with acute myocardial infarction<br />
complicated by cardiogenic shock. Eur Heart J<br />
31:3<strong>03</strong>2–3<strong>03</strong>9<br />
8. Jung C, Lauten A, Ferrari M(2010)Microcirculation<br />
in cardiogenic shock: from scientific bystander to<br />
therapytarget.CritCare14:193<br />
9. Sjauw KD, Engstrom AE, Vis MM et al (2009) A<br />
systematicreviewandmeta-analysisofintra-aortic<br />
balloon pump therapy in ST-elevation myocardial<br />
infarction: should we change the guidelines? Eur<br />
HeartJ30:459–468<br />
10. Altayyar S, Rochwerg B, Alnasser S et al (2014)<br />
Intra-aortic balloon pump in patients with<br />
cardiogenic shock complicating myocardial<br />
infarction: a systematic review and meta-analysis<br />
ofrandomizedtrials.SystRev3:24<br />
11. Prondzinsky R, Lemm H, Swyter M et al (2010)<br />
Intra-aortic balloon counterpulsation in patients<br />
with acute myocardial infarction complicated by<br />
cardiogenic shock: the prospective, randomized<br />
IABP SHOCK Trial for attenuation of multiorgan<br />
dysfunctionsyndrome.CritCareMed38:152–160<br />
12. O’Gara PT, Kushner FG, Ascheim DD et al (2013)<br />
2013 ACCF/AHA guideline for the management<br />
of ST-elevation myocardial infarction: executive<br />
summary: a report of the American College of<br />
Cardiology Fo<strong>und</strong>ation/American HeartAssociation<br />
Task Force on Practice Guidelines. Circulation<br />
127:529–555<br />
13. Bengtson JR, Kaplan AJ, Pieper KS et al (1992)<br />
Prognosis in cardiogenic shock after acute<br />
myocardial infarction in the interventional era.<br />
JAmCollCardiol20:1482–1489<br />
14. Thiele H, Schuler G, Neumann FJ et al (2012)<br />
Intraaortic balloon counterpulsation in acute<br />
myocardial infarction complicated by cardiogenic<br />
shock: design and rationale of the Intraaortic<br />
BalloonPumpinCardiogenicShockII(IABP-SHOCK<br />
II)trial.AmHeartJ163:938–945<br />
15. Thiele H, Zeymer U, Neumann FJ et al (2012)<br />
Intraaortic balloon support for myocardial infarction<br />
with cardiogenic shock. N Engl J Med<br />
367:1287–1296<br />
16. Thiele H, Zeymer U, Neumann FJ et al (2013)<br />
Intra-aortic balloon counterpulsation in acute<br />
myocardial infarction complicated by cardiogenic<br />
shock (IABP-SHOCK II): final 12 month<br />
results of a randomised, open-label trial. Lancet<br />
382:1638–1645<br />
17. Kolh P, Windecker S, Alfonso F et al (2014) 2014<br />
ESC/EACTS Guidelines on myocardial revascularizationTask<br />
Force on Myocardial Revascularization<br />
of the European Society of Cardiology (ESC) and<br />
the European Association for Cardio-Thoracic<br />
Surgery (EACTS). Developed with the special<br />
contribution of the European Association of Percutaneous<br />
Cardiovascular Interventions (EAPCI). Eur<br />
JCardiothoracSurg46:517–592<br />
18. Ponikowski P, Voors AA, Anker SD et al (2016) 2016<br />
ESC Guidelines for the diagnosis and treatment of<br />
acute and chronic heart failure: The Task Force for<br />
the diagnosis and treatment of acute and chronic<br />
heartfailure of the European Society of Cardiology<br />
(ESC). Developed with the special contribution of<br />
theHeartFailureAssociation(HFA)oftheESC.Eur<br />
HeartJ14:2129–2200<br />
19. Roffi M, Patrono C, Collet JP et al (2015) 2015 ESC<br />
Guidelines for the management of acute coronary<br />
syndromes in patients presenting without<br />
424 Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017
persistent ST-segment elevation: Task Force for<br />
the Management of Acute Coronary Syndromes<br />
in Patients Presenting without Persistent ST-<br />
Segment Elevation of the European Society of<br />
Cardiology(ESC).EurHeartJ37:267–315<br />
20. Sandhu A, McCoy L, Smita IN et al (2015) Use<br />
of mechanical circulatory support in patients<br />
<strong>und</strong>ergoing percutaneous coronary intervention<br />
insights from the National Cardiovascular Data<br />
Registry.Circulation132:1243–1251<br />
21. Stretch R, Sauer CM, Yuh DD et al (2014)<br />
National trends in the utilization of short-term<br />
mechanical circulatory support. J Am Coll Cardiol<br />
14:1407–1415<br />
22. TakayamaH,TrubyL,KoekortMetal(2013)Clinical<br />
outcome of mechanical circulatory support for<br />
refractory cardiogenic shock in the current era.<br />
JHeartLungTransplant32:106–111<br />
23. CombesA,LeprinceP,LuytCE(2008)Outcomesand<br />
long-term quality-of-life of patients supported<br />
by extracorporeal membrane oxygenation for<br />
refractory cardiogenic shock. Crit Care Med<br />
36:1404–1411<br />
24. Cheng R, Hachamovitch R, Kittleson M et al (2014)<br />
Complications of extracorporeal membrane<br />
oxygenation for treatment of cardiogenic shock<br />
and cardiac arrest: a meta-analysis of 1,866 adult<br />
patients.AnnThoracSurg97:610–616<br />
25. Pappalardo F, Schulte C, Pieri M et al (2016) Concomitant<br />
implantation of Impella® on top of venoarterial<br />
extracorporeal membrane oxygenation<br />
may improve survival of patients with cardiogenic<br />
shock.EurJHeartFail.doi:10.1002/ejhf.668<br />
26. Weymann A, Schmack B, Sabashnikow S et al<br />
(2014) Central extracorporeal life support with<br />
left ventricular decompression for the treatment<br />
of refractory cardiogenic shock and lung failure.<br />
JCardiothoracSurg29:9–60<br />
27. Cheng R, Hachamovitch R, Makkar R et al<br />
(2015) Lack of survival benefit fo<strong>und</strong> with use<br />
of intraaortic balloon pump in extracorporeal<br />
membrane oxygenation. J Invasive Cardiol<br />
27:453–458<br />
28. Ouweneel DM, Eriksen E, Sjauw KD et al (2017)<br />
Percutaneous mechanical circulatory support<br />
versus intra-aortic balloon pump in cardiogenic<br />
shock after acute myocardial infarction. J Am Coll<br />
Cardiol69:278–287<br />
29. Zeymer U, Thiele H (2017) Mechanical support for<br />
cardiogenic shock: lost in translation? J Am Coll<br />
Cardiol69:288–290<br />
30. Beurtheret S, Mordant P, Paoletti X et al (2013)<br />
Emergency circulatory support in refractory<br />
cardiogenic shock patients in remote institutions:<br />
a pilot study (the cardiac-RESCUE program). Eur<br />
HeartJ34:112–120<br />
31. de Waha S, Graf T, Desch S et al (2017) Outcome<br />
of elderly <strong>und</strong>ergoing extracorporeal life support<br />
in refractory cardiogenic shock. Clin Res Cardiol.<br />
doi:10.1007/s0<strong>03</strong>92-016-1068-8<br />
32. ChenYS,LinJW,YuHYetal(2008)Cardiopulmonary<br />
resuscitation with assisted extracorporeal lifesupport<br />
versus conventional cardiopulmonary<br />
resuscitationinadultswithin-hospitalcardiac<br />
arrest: an observational study and propensity<br />
analysis.Lancet372:554–561<br />
33. Ouweneel D, Schotborgh JV, Limpens Jetal (2016)<br />
Extracorporeal life support during cardiac arrest<br />
and cardiogenic shock: a systematic review and<br />
meta-analysis.IntCareMed42:1922–1934<br />
34. Burkhoff D, Cohen H, Brunckhorst C et al (2006) A<br />
randomized multicenter clinical study to evaluate<br />
the safety and efficacy of the TandemHeart<br />
percutaneous ventricular assist device versus<br />
conventional therapy with intraaortic balloon<br />
pumping for treatment of cardiogenic shock. Am<br />
HeartJ152(469):e1–e8<br />
35. Thiele H, SickP, BoudriotEetal (2005)Randomized<br />
comparison of intra-aortic balloon support with<br />
a percutaneous left ventricular assist device in<br />
patients with revascularized acute myocardial<br />
infarction complicated by cardiogenic shock. Eur<br />
HeartJ26:1276–1283<br />
36. Weil BR, Konecny F, Suzuki G et al (2016) Comparative<br />
Hemodynamic effects of contemporary<br />
percutaneous mechanical circulatory support<br />
devices in a porcine model of acute myocardial<br />
infarction.JACCCardiovascInterv9:2292–23<strong>03</strong><br />
37. Arrigoni SC, Kuijpers M, Mecozzi G (2011) Use of<br />
a novel short-term mechanical circulatory support<br />
device for cardiac recovery. Interact Cardiovasc<br />
ThoracSurg12:891–894<br />
38. Engstrom AE, Cocchieri R, Driessen AH et al (2011)<br />
The Impella 2.5 and 5.0 devices for ST-elevation<br />
myocardial infarction patients presenting with<br />
severe and profo<strong>und</strong> cardiogenic shock: The<br />
Academic Medical Center intensive care unit<br />
experience.CritCareMed39:2072–2079<br />
39. Lamarche Y, Cheung A, Ignaszewski A et al (2011)<br />
Comparative outcomes in cardiogenic shock<br />
patients managed with Impella microaxial pump<br />
or extracorporeal life support. J Thorac Cardiovasc<br />
Surg42:60–65<br />
40. Anastasiadis K, Chalvatzoulis O, Antonitsis P et al<br />
(2011) Left ventricular decompression during<br />
peripheralextracorporealmembraneoxygenation<br />
support with the use of the novel iVAC pulsatile<br />
paracorporeal assist device. Ann Thorac Surg<br />
92:2257–2259<br />
41. Cheng JM, den Uil CA, Hoeks SE et al (2009)<br />
Percutaneous left ventricular assist devices vs.<br />
intra-aortic balloon pump counterpulsation for<br />
treatmentofcardiogenicshock: a meta-analysis of<br />
controlledtrials.EurHeartJ30:2102–2108<br />
42. Marty P, Roquilly A, Vallee F et al (2013) Lactate<br />
clearance for death prediction in severe sepsis<br />
or septic shock patients during the first 24 h in<br />
intensive care unit: an observational study. Ann<br />
IntensiveCare3:3<br />
43. Nguyen HB, Rivers EP, Knoblich BP et al (2004)<br />
Early lactate clearance is associated with improved<br />
outcome in severe sepsis and septic shock. Crit<br />
CareMed32:1637–1642<br />
44. Attana P, Lazzeri C, Chiostri M et al (2012) Lactate<br />
clearance in cardiogenic shock following ST<br />
elevation myocardial infarction: a pilot study.<br />
AcuteCardCare14:20–26<br />
45. Lamarche Y, Cheung A, Ignaszewski A et al (2011)<br />
Comparative outcomes in cardiogenic shock<br />
patients managed with Impella microaxial pump<br />
or extracorporeal life support. J Thorac Cardiovasc<br />
Surg142:60–65<br />
46. BrownDJ,BruggerH,BoydJetal(2012)Accidental<br />
hypothermia.NEnglJMed367:1930–1938<br />
47. Monsieurs KG, Nolan JP, Bossaert LL et al (2015)<br />
European Resuscitation Council Guidelines for<br />
Resuscitation.Resuscitation95:1–312<br />
48. Thiele H et al (2015) Management of cardiogenic<br />
shock.EurHeartJ36:1223–1230<br />
Fachnachrichten<br />
WeltweiteStudiezuPatienten<strong>und</strong><br />
Angehörigenbetreuung<br />
in der Intensivstation<br />
Teilnahme erwünscht!<br />
Die World Federation of Societies of<br />
Intensive and Critical Care Medicine<br />
(WFSICCM) bittet nationale wissenschaftliche<br />
Fachgesellschaften weltweit um<br />
Umsetzungsbeispiele für patienten- <strong>und</strong><br />
familienzentriete Betreuung. Immer mehr<br />
Studien attestieren, dass die patientenzentrierte<br />
Pflege <strong>und</strong> Strategien zur<br />
Einbeziehung der Familienangehörigen<br />
die Therapieresultate für schwerkranke<br />
Patienten fördern. Dennoch ist nicht<br />
bekannt, zu welchem Grad bestimmte<br />
Arten dieser Betreuungspraktiken weltweit<br />
umgesetzt werden.<br />
Die Studie „Patient and Family Centered<br />
Care in the ICU: Worldwide<br />
Exemplars“ soll nun eben diese Informationen<br />
sammeln. Zur Datenerhebung<br />
kommt bei dem Projekt eine sichere,<br />
web-basierte Anwendung zum Einsatz –<br />
die sogenannte Research Electronic Data<br />
Capture (REDCap).<br />
Die Informationen können einfach online<br />
hinterlegt werden:<br />
https://redcap.rush.edu/redcap/surveys/?s<br />
=JJ4RLREEXY<br />
Quelle: Deutsche Interdisziplinäre<br />
Vereinigung für Intensiv- <strong>und</strong><br />
Notfallmedizin (DIVI) 23.05.2017<br />
Medizinische Klinik - Intensivmedizin <strong>und</strong> Notfallmedizin 5 · 2017 425