Einfluss der ERM-Proteine auf die Protrusion- Ausbildung und Zell ...
Einfluss der ERM-Proteine auf die Protrusion- Ausbildung und Zell ...
Einfluss der ERM-Proteine auf die Protrusion- Ausbildung und Zell ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Phosphorylierung am<br />
konservierten C-terminalen<br />
Threonin<br />
L. monocytogenes<br />
an<strong>der</strong>e Aktivierungsmechanismen<br />
Membranligand z.B. CD44<br />
aktiviertes <strong>ERM</strong>-Molekül<br />
inaktives, maskiertes <strong>ERM</strong>-Molekül<br />
F-Aktin<br />
ActA<br />
4. Diskussion<br />
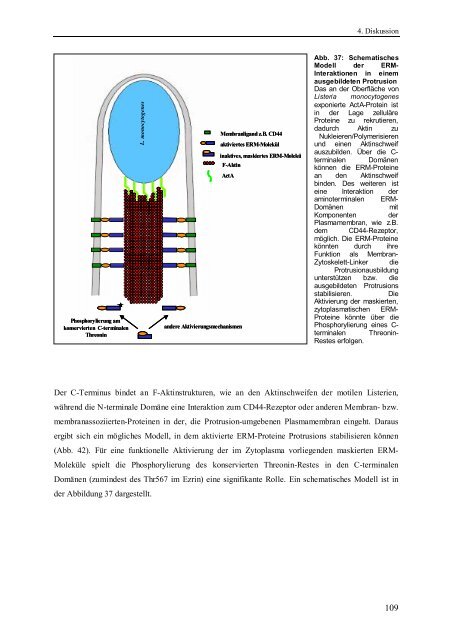
Abb. 37: Schematisches<br />
Modell <strong>der</strong> <strong>ERM</strong>-<br />
Interaktionen in einem<br />
ausgebildeten <strong>Protrusion</strong><br />
Das an <strong>der</strong> Oberfläche von<br />
Listeria monocytogenes<br />
exponierte ActA-Protein ist<br />
in <strong>der</strong> Lage zelluläre<br />
<strong>Proteine</strong> zu rekrutieren,<br />
dadurch Aktin zu<br />
Nukleieren/Polymerisieren<br />
<strong>und</strong> einen Aktinschweif<br />
auszubilden. Über <strong>die</strong> Cterminalen<br />
Domänen<br />
können <strong>die</strong> <strong>ERM</strong>-<strong>Proteine</strong><br />
an den Aktinschweif<br />
binden. Des weiteren ist<br />
eine Interaktion <strong>der</strong><br />
aminoterminalen <strong>ERM</strong>-<br />
Domänen mit<br />
Komponenten <strong>der</strong><br />
Plasmamembran, wie z.B.<br />
dem CD44-Rezeptor,<br />
möglich. Die <strong>ERM</strong>-<strong>Proteine</strong><br />
könnten durch ihre<br />
Funktion als Membran-<br />
Zytoskelett-Linker <strong>die</strong><br />
<strong>Protrusion</strong>ausbildung<br />
unterstützen bzw. <strong>die</strong><br />
ausgebildeten <strong>Protrusion</strong>s<br />
stabilisieren. Die<br />
Aktivierung <strong>der</strong> maskierten,<br />
zytoplasmatischen <strong>ERM</strong>-<br />
<strong>Proteine</strong> könnte über <strong>die</strong><br />
Phosphorylierung eines Cterminalen<br />
Threonin-<br />
Restes erfolgen.<br />
Der C-Terminus bindet an F-Aktinstrukturen, wie an den Aktinschweifen <strong>der</strong> motilen Listerien,<br />
während <strong>die</strong> N-terminale Domäne eine Interaktion zum CD44-Rezeptor o<strong>der</strong> an<strong>der</strong>en Membran- bzw.<br />
membranassoziierten-<strong>Proteine</strong>n in <strong>der</strong>, <strong>die</strong> <strong>Protrusion</strong>-umgebenen Plasmamembran eingeht. Daraus<br />
ergibt sich ein mögliches Modell, in dem aktivierte <strong>ERM</strong>-<strong>Proteine</strong> <strong>Protrusion</strong>s stabilisieren können<br />
(Abb. 42). Für eine funktionelle Aktivierung <strong>der</strong> im Zytoplasma vorliegenden maskierten <strong>ERM</strong>-<br />
Moleküle spielt <strong>die</strong> Phosphorylierung des konservierten Threonin-Restes in den C-terminalen<br />
Domänen (zumindest des Thr567 im Ezrin) eine signifikante Rolle. Ein schematisches Modell ist in<br />
<strong>der</strong> Abbildung 37 dargestellt.<br />
109